Медицинские аэрозольные препараты
Номер патента: 2381
Опубликовано: 25.04.2002
Авторы: Муллер Хельгерт, Фатаниа Кану М., Скотт Джон С., Оливер Мартин Дж.
Формула / Реферат
1. Фармацевтическая композиция, включающая терапевтически эффективное количество соединения формулы I
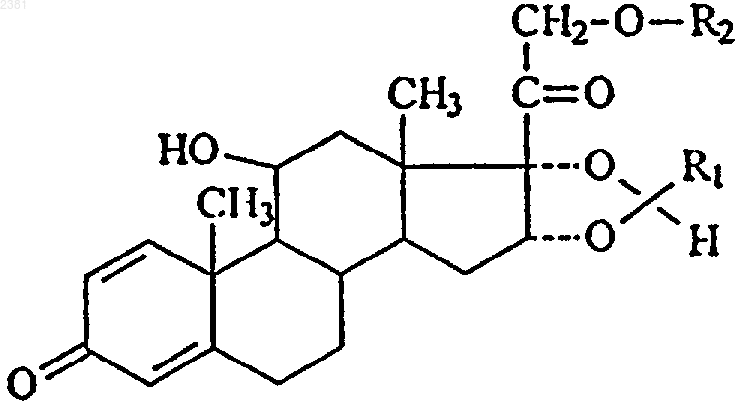
где R1 обозначает 1-бутил, 2-бутил, циклогексил или фенил и
R2 обозначает ацетил или изобутаноил, и пропеллент, выбранный из группы, включающей 1,1,1,2-тетрафторэтан, 1,1,1,2,3,3,3-гептафторпропан и их смесь, этанол в количестве, эффективном для растворения соединения формулы (I), а также необязательно поверхностно-активное вещество.
2. Фармацевтическая композиция по п.1, в которой соединение формулы (I) представляет собой циклесонид.
3. Фармацевтическая композиция по п.1, которая не содержит поверхностно-активного вещества.
4. Фармацевтическая композиция по п.1, которая включает от 3 до 25 мас.% этанола.
5. Фармацевтическая композиция по п.4, которая включает от 5 до 20 мас.% этанола.
6. Фармацевтическая композиция по п.5, которая включает от 7 до 12 мас.% этанола.
7. Фармацевтическая композиция по п.6, которая включает 8 мас.% этанола.
8. Фармацевтическая композиция по п.2, которая включает от 1 до 8 мг/мл циклесонида.
9. Фармацевтическая композиция по п.1, в которой пропеллент представляет собой 1,1,1,2-тетрафторэтан.
10. Фармацевтическая композиция по п.1, в которой пропеллент представляет собой 1,1,1,2,3,3,3-гептафторпропан.
11. Фармацевтическая композиция по п.9, включающая циклесонид в концентрации от 1 до 5 мг/мл в смеси этанол:1,1,1,2-тетрафторэтан в массовом соотношении 8:9.
12. Фармацевтический продукт в виде аэрозольного баллона, снабженного распылительным клапаном и заполненный композицией по п.1.
13. Фармацевтический продукт по п.12, в котором клапан представляет собой дозирующий распылительный клапан.
14. Фармацевтический продукт по п.13, в котором клапан имеет
обкладку с ободком и связанной с ним кольцевой прокладкой для присоединения к аэрозольному баллону и проходящий через него канал,
дозирующий резервуар, стенки которого образуют внутреннюю камеру, впускное отверстие, впускной конец и выпускное отверстие, и
удлиненный шток клапана, имеющий заполняющий канал, заполняющий конец, распылительный конец и распылительное отверстие, при этом
выпускной конец дозирующего резервуара герметично соединен с обкладкой клапана, выпускной конец штока клапана проходит через канал в обкладке клапана и выпускной конец дозирующего клапана и имеет скользящее герметичное соединение с обкладкой клапана,
заполняющий конец штока клапана проходит через впускное отверстие дозирующего резервуара и имеет с ним скользящее герметичное соединение, а опорожнитель баллона окружает дозирующий резервуар и заполняющий конец удлиненного штока клапана, образуя между дозирующим резервуаром и опорожнителем баллона канал, соединяющий впускное отверстие дозирующего резервуара с аэрозольным баллоном,
шток клапана имеет возможность перемещения между ненажатым закрытым положением, в котором заполняющий канал штока клапана открывает проход через входное отверстие между внутренней и внешней частями дозирующей камеры и в котором выпускной конец дозирующего резервуара закрыт, и нажатым открытым положением, в котором впускное отверстие дозирующего резервуара герметично соединено с заполняющим концом клапана, а распылительное отверстие штока открывает проход между внутренней и внешней частями дозирующей камеры.
15. Фармацевтический продукт по п.14, дополнительно имеющий переходник с корпусом для подсоединения к аэрозольному баллону, распылительным элементом, присоединяемым к распылительному концу штока клапана, и наконечником.
16. Фармацевтический продукт по п.15, в котором распылительный элемент имеет выпускное отверстие, направленное в наконечник, причем диаметр этого выпускного отверстия составляет от 0,20 до 0,33 мм.
17. Фармацевтический продукт по п.16, в котором диаметр выпускного отверстия составляет приблизительно 0,28 мм.
18. Фармацевтический продукт по п.17, в котором длина форсунки выпускного отверстия составляет от 0,30 до 0,60 мм.
19. Фармацевтический продукт по п.18, в котором длина форсунки выпускного отверстия составляет 0,50 мм.
20. Фармацевтическая аэрозольная композиция, которой заполнен аэрозольный баллон, снабженный распылительным клапаном, и которая включает соединение формулы I

где R1 обозначает 1-бутил, 2-бутил, циклогексил или фенил и
R2 обозначает ацетил или изобутаноил, и
гидрофторуглеводородный пропеллент, а также сорастворитель в количестве, эффективном для растворения соединения формулы (I).
Текст
1 Настоящее изобретение относится к медицинским аэрозольным препаратам, в частности к медицинским препаратам, содержащим 21 эфир прегна-1,4-диен-3,20-дион-16,17-ацеталя и пригодным для введения путем ингаляции. В GB 2247680 описаны 21-эфиры прегна 1,4-диен-3,20-дион-16,17-ацеталя и их применение при лечении воспалительных состояний. Соединения имеют строение, описываемое следующей общей формулойR2 обозначает ацетил или изобутаноил. Циклесонид представляет собой 21 изобутират циклического 16,17-ацеталя 11,16,17,21-тетрагидроксипрегна-1,4-диен 3,20-диона с циклогексанкарбоксальдегидом,имеющий структуру, охарактеризованную формулой (I), в которой отсутствуют атомы фтора и в которой R1 обозначает циклогексил, a R2 обозначает изобутаноил. Это соединение оценивали в качестве антиастматического средства и в результате исследования его фармакокинетических характеристик было установлено, что оно пригодно для приготовления композиций, предназначенных для ингаляции. Циклесонид при оральном введении поглощается лишь в ограниченной степени и обладает низкой системной активностью. Концентрация лекарства в легких является высокой, а метаболизм под действием оксидаз печени является очень интенсивным,что обусловливает малое время полужизни лекарства в плазме. Системная активность циклесонида в три раза ниже активности будесонида,однако, его противовоспалительная активность выше активности последнего. В GB 2247680 предложена специальная композиция, предназначенная для введения циклесонида в виде аэрозоля под давлением путем оральной и назальной ингаляции. Предложенная композиция включает циклесонид в виде суспензии тонкоизмельченных частиц, поверхностно-активного вещества, а именно, сорбитантриолеата, и смеси трех ХФУ-пропеллентов (хлорфторуглеводородных пропеллентов): трихлорфторметана, дихлортетрафторметана и дихлордифторметана. Однако считается,что эти ХФУ-пропелленты вызывают разложение озона в стратосфере, и поэтому существует необходимость в создании лекарственных средств в виде аэрозольных композиций, в которых используются так называемые "озонсберегающие" пропелленты. Класс пропеллентов, которые, как считается, оказывают минимальное разрушающее дей 002381 2 ствие на озон по сравнению с традиционными хлорфторуглеводородами, включая гидрофторуглеводороды, а разнообразные медицинские аэрозольные композиции с использованием таких пропеллентных систем описаны, например,в ЕР 0372777, WO 91/040011, WO 91/11173, WO 91/11495, WO 91/14422, WO 93/11743 и ЕР 0553298. Все эти публикации касаются получения предназначенных для введения лекарственных средств аэрозолей, находящихся под давлением, и направлены на решение проблем, связанных с этим новым классом пропеллентов, в частности, проблем, связанных со стабильностью получаемых фармацевтических композиций. В этих публикациях предлагается, например, добавлять один или несколько адъювантов,таких как спирты, алканы, диметиловый эфир,поверхностно-активные вещества (включая фторированные и нефторированные поверхностно-активные вещества, карбоновые кислоты,полиэтоксилаты и т.д.). Однако, несмотря на различные подходы,используемые при приготовлении лекарств,предназначенных для применения в виде аэрозоля для ингаляции, все еще часто приходится сталкиваться с различными трудностями и неопределенностями при попытке разработать обладающую физической и химической стабильностью композицию, не содержащую ХФУ,которая была бы пригодна для надежного введения точной дозы лекарства, размер частиц которого лежит в определенных пределах. В частности, существует необходимость в разработке не содержащего ХФУ медицинского аэрозольного препарата, который включал бы циклесонид (или сходные с ним молекулы) и который являлся бы химически и физически стабильным и был пригоден для введения в дыхательную систему пациента. При создании изобретения неожиданно было установлено, что в отличие от используемого в известных способах приготовления препарата на основе циклесонида в виде суспензии может оказаться наиболее предпочтительным приготавливать препарат на основе циклесонида в виде физически и химически стабильного раствора в композициях, включающих гидрофторуглеводородные пропелленты. В настоящем изобретении предложена фармацевтическая композиция, включающая терапевтически эффективное количество соединения формулы где R1 обозначает 1-бутил, 2-бутил, циклогексил или фенил иR2 обозначает ацетил или изобутаноил,и гидрофторуглеводородный пропеллент, предпочтительно пропеллент, выбранный из группы,включающей 1,1,1,2-тетрафторэтан, 1,1,1,2,3, 3 3,3-гептафторпропан и их смесь, а также сорастворитель, предпочтительно этанол, где этанол присутствует в количестве, эффективном для растворения соединения формулы (I), и необязательно поверхностно-активное вещество. Соединение формулы (I) предпочтительно представляет собой циклесонид и, как правило,присутствует в концентрации от 1 до 8 мг/мл,предпочтительно от 1 до 5 мг/мл. Композиция, как правило, включает от 3 до 25 мас.%, предпочтительно от 5 до 20 мас.%,наиболее предпочтительно от 7 до 12 мас.% этанола. Пропеллент предпочтительно представляет собой гидрофторалкан, в частности пропеллент 134 а, пропеллент 227 или их смесь, как правило,в массовом соотношении приблизительно 50:50. Более предпочтительно пропеллент представляет собой пропеллент 134 а. Композиции могут включать поверхностно-активное вещество, но предпочтительно не содержат поверхностно-активного вещества. Предпочтительно композиции не содержат других эксципиентов. Предпочтительно композиции содержат от 1 до 5 мг/мл циклесонида, 8 мас.% этанола и пропеллент 134 а. Композиции могут быть приготовлены путем заполнения аэрозольного баллона требуемым количеством лекарства, установки на флакон клапана путем обжатия для герметизации и введения через клапан предварительно приготовленной смеси пропеллента и этанола. Баллон помещают в ультразвуковую баню для растворения лекарства. В альтернативном варианте композиции могут быть получены путем приготовления концентрата лекарства с этанолом и добавления этого концентрата к предварительно охлажденному пропелленту в мерном сосуде. Полученной композицией заполняют баллоны. Полученными композициями можно заполнять пластиковые, металлические или стеклянные баллоны. Пригодным в этом отношении пластиком является полиэтилентерефталат, а предпочтительным металлом является алюминий. Баллоны снабжены дозирующим распылительным клапаном, например, выдающим 50 микролитровую порцию при каждом нажатии. Пригодный дозирующий распылительный клапан имеет обкладку с ободком и связанной с ним кольцевой прокладкой для присоединения к аэрозольному баллону и проходящий через него канал, дозирующий резервуар, стенки которого образуют внутреннюю камеру, впускное отверстие, впускной конец и выпускное отверстие, а также имеет удлиненный шток клапана, имеющий заполняющий канал, заполняющий конец,распылительный конец и распылительное отверстие, при этом выпускной конец дозирующего резервуара герметично соединен с обкладкой 4 клапана, выпускной конец штока клапана проходит через канал в обкладке клапана и выпускной конец дозирующего клапана и имеет скользящее герметичное соединение с обкладкой клапана, заполняющий конец штока клапана проходит через впускное отверстие дозирующего резервуара и имеет с ним скользящее герметичное соединение, а опорожнитель баллона окружает дозирующий резервуар и заполняющий конец удлиненного штока клапана, образуя между дозирующим резервуаром и опорожнителем баллона канал, соединяющий впускное отверстие дозирующего резервуара с аэрозольным баллоном, шток клапана имеет возможность перемещения между ненажатым закрытым положением, в котором заполняющий канал штока клапана открывает проход через входное отверстие между внутренней и внешней частями дозирующей камеры и в котором выпускной конец дозирующего резервуара закрыт, и нажатым открытым положением, в котором впускное отверстие дозирующего резервуара герметично соединено с заполняющим концом клапана, а распылительное отверстие штока открывает проход между внутренней и внешней частями дозирующей камеры. Пригодным клапаном является клапан, поступающий в продажу под торговым наименованием SPRAYMISER. Ниже изобретение описано на примере одного из вариантов его выполнения со ссылкой на прилагаемые чертежи, на которых показано на фиг. 1 - поперечное сечение дозирующего распылительного клапана, пригодного для применения согласно изобретению; на фиг. 2 - продольное сечение переходника для подсоединения к аэрозольному баллону,снабженному дозирующим распылительным клапаном, пригодным для применения согласно изобретению; на фиг. 3 - вид спереди переходника по фиг. 2; и на фиг. 4 - увеличенное изображение фрагмента Х по фиг. 2. Клапан, представленный на фиг. 1, имеет обкладку (2) и связанную с ней кольцевую прокладку (4) для присоединения к аэрозольному баллону. Кольцевая прокладка (4) предпочтительно может быть изготовлена из сополимера этилена и бутилена, например, сополимера, поставляемого фирмой Union Carbide под товарным знаком FLEXOMER GERS 1085NT. Дозирующий резервуар (6) имеет стенки,которые образуют дозирующую камеру (8),имеющую впускной конец, соединенный с затвором (10) резервуара, и выпускной конец, соединенный с диафрагмой (12). Удлиненный шток (14) клапана, имеющий заполняющий канал (16), распылительный конец (18) и распылительное отверстие (20), проходит через обкладку клапана и дозирующую камеру и герметично 5 уплотнен диафрагмой (12) и затвором (10) резервуара. Затвор резервуара и диафрагму предпочтительно изготавливают из сополимера бутадиена и акрилонитрила, например, типа DB-218, поставляемого фирмой American GasketRubberCompany. Дозирующий резервуар (6) и шток клапана окружены опорожнителем (22) баллона таким образом, что между дозирующим резервуаром и опорожнителем баллона образуется капиллярный канал (24), по которому аэрозольная композиция может проходить из аэрозольного баллона к впускному концу дозирующей камеры. Шток (14) клапана может перемещаться между ненажатым закрытым положением, в котором заполняющий канал (16) в штоке клапана открывает проход через впускное отверстие между внутренней и внешней частями дозирующей камеры и в котором выпускной конец дозирующего резервуара закрыт, и открытым нажатым положением, в котором впускное отверстие дозирующего резервуара герметично соединено с заполняющим концом штока клапана, а распылительное отверстие в штоке клапана открывает проход между внутренней и внешней частями дозирующей камеры. Шток(14) клапана возвращается в ненажатое закрытое положение пружиной (15). На фиг. 2-4 изображен переходник типа"нажми и дыши" для аэрозольного баллона,снабженный дозирующим клапаном, пригодным для применения согласно изобретению. Этот переходник имеет корпус (30) и наконечник(32). Внутри корпуса (30) имеется несколько ребер (34) для фиксации и удержания аэрозольного баллона (не показан) в требуемом положении. Распылительный конец удлиненного штока дозирующего распылительного клапана расположен внутри распылительного элемента (36). Переходник изготавливают из полипропилена или полиэтилена с большой плотностью. Однако для достижения хорошей герметичности между штоком (14) клапана и центральным каналом (38) предпочтительно использовать полиэтилен высокой плотности. Как показано на фиг. 4, распылительный элемент (36) имеет центральный канал (38) с конусообразным входным отверстием (40) под шток клапана. Шток клапана может входить в это отверстие до упора в выступ (42). При использовании для ингаляции пациент вставляет наконечник в рот и нажимает на основание аэрозольного баллона. При перемещении удлиненного штока клапана относительно дозирующего резервуара распылительное отверстие утапливается в дозирующий резервуар, содержимое которого под давлением проходит через распылительный конец удлиненного штока клапана во входную камеру (44) распылительного элемента (36) и выходит наружу через отверстие 6 для вдыхания, направляется из отверстия (46) в наконечник (32) для ингаляции пациенту. Было установлено, что размеры отверстия(46) могут оказывать существенное влияние на вдыхаемые фракции композиции, распыляемой из наконечника переходника. На параметры введения композиции в легкие влияют как длина "l" форсунки, так и диаметр "d" отверстия(46). Для оценки этих параметров часто используют тесты "in vitro", в которых применяют устройство типа Andersen Cascade Impactor, как описано в Фармакопее США. В соответствии с тестом по Андерсену вдыхаемая доза определяется как масса лекарства, попадающая на пластины с 3 по 7 и фильтр инерционного сепаратора частиц при однократном приведении в действие ингалятора. Оптимальные размеры также зависят от конкретной распыляемой композиции. Как правило, доставка лекарственного средства возрастает с увеличением диаметра отверстия "d" и с увеличением длины "l" форсунки. Однако вдыхаемые в соответствии с тестом по Андерсену дозы увеличиваются с уменьшением диаметра отверстия "d". Подбором конкретных размеров отверстия сопла можно достичь, чтобы вдыхаемая доза в соответствии с тестом по Андерсену с использованием устройства, распыляющего 200 мкг циклесонида при однократном нажатии на клапан, превышала 120 мкг без существенного отклонения от рекомендаций по доставке лекарства. Таким образом, пациент имеет возможность получить большую чем обычно дозу распыляемого лекарства, достигающую легких, без использования избыточного количества лекарства в устройстве или продукта, не удовлетворяющего соответствующим нормам. Было установлено, что для композиций,содержащих от 5 до 10 мас.% этанола, в частности 8 мас.% этанола, эффективные вдыхаемые дозы достигаются при диаметре отверстия "d" в пределах от 0,20 до 0,33 мм, предпочтительно приблизительно 0,28 мм, и при длине "l" форсунки в пределах от 0,30 до 0,60 мм, предпочтительно 0,50 мм. Ниже изобретение проиллюстрировано на примерах. Во всех этих примерах в скобках указано процентное содержание этанола в смеси этанол/пропеллент (сокращение П означает пропеллент). Пример 1. Циклесонид Этанол (5%) П 227 Пример 16. Циклесонид Олеиновая кислота Этанол П 134 а Все композиции из примеров 1-15 представляли собой прозрачные бесцветные растворы, в которых циклесонид находился в полностью растворенном состоянии. Композиции из примеров 13-15 тестировали в отношении стабильности в течение не 9 скольких месяцев, и они оказались физически и химически стабильными. Хотя выше изобретение описано на примерах предпочтительных композиций и ингредиентов, следует подчеркнуть, что эти примеры не ограничивают объем изобретения. Более того,для специалистов в данной области техники очевидно, что, не выходя за объем изобретения,в композицию необязательно могут быть включены различные ингредиенты, такие как корригенты, консерванты, дополнительные действующие вещества и т.п. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Фармацевтическая композиция, включающая терапевтически эффективное количество соединения формулы I где R1 обозначает 1-бутил, 2-бутил, циклогексил или фенил иR2 обозначает ацетил или изобутаноил, и пропеллент, выбранный из группы, включающей 1,1,1,2-тетрафторэтан, 1,1,1,2,3,3,3-гептафторпропан и их смесь, этанол в количестве,эффективном для растворения соединения формулы (I), а также необязательно поверхностноактивное вещество. 2. Фармацевтическая композиция по п.1, в которой соединение формулы (I) представляет собой циклесонид. 3. Фармацевтическая композиция по п.1,которая не содержит поверхностно-активного вещества. 4. Фармацевтическая композиция по п.1,которая включает от 3 до 25 мас.% этанола. 5. Фармацевтическая композиция по п.4,которая включает от 5 до 20 мас.% этанола. 6. Фармацевтическая композиция по п.5,которая включает от 7 до 12 мас.% этанола. 7. Фармацевтическая композиция по п.6,которая включает 8 мас.% этанола. 8. Фармацевтическая композиция по п.2,которая включает от 1 до 8 мг/мл циклесонида. 9. Фармацевтическая композиция по п.1, в которой пропеллент представляет собой 1,1,1,2 тетрафторэтан. 10. Фармацевтическая композиция по п.1,в которой пропеллент представляет собой 1,1,1,2,3,3,3-гептафторпропан. 11. Фармацевтическая композиция по п.9,включающая циклесонид в концентрации от 1 до 5 мг/мл в смеси этанол:1,1,1,2-тетрафторэтан в массовом соотношении 8:9. 12. Фармацевтический продукт в виде аэрозольного баллона, снабженного распылительным клапаном и заполненный композицией по п.1. 10 13. Фармацевтический продукт по п.12, в котором клапан представляет собой дозирующий распылительный клапан. 14. Фармацевтический продукт по п.13, в котором клапан имеет обкладку с ободком и связанной с ним кольцевой прокладкой для присоединения к аэрозольному баллону и проходящий через него канал,дозирующий резервуар, стенки которого образуют внутреннюю камеру, впускное отверстие, впускной конец и выпускное отверстие, и удлиненный шток клапана, имеющий заполняющий канал, заполняющий конец, распылительный конец и распылительное отверстие,при этом выпускной конец дозирующего резервуара герметично соединен с обкладкой клапана, выпускной конец штока клапана проходит через канал в обкладке клапана и выпускной конец дозирующего клапана и имеет скользящее герметичное соединение с обкладкой клапана,заполняющий конец штока клапана проходит через впускное отверстие дозирующего резервуара и имеет с ним скользящее герметичное соединение, а опорожнитель баллона окружает дозирующий резервуар и заполняющий конец удлиненного штока клапана, образуя между дозирующим резервуаром и опорожнителем баллона канал, соединяющий впускное отверстие дозирующего резервуара с аэрозольным баллоном,шток клапана имеет возможность перемещения между ненажатым закрытым положением, в котором заполняющий канал штока клапана открывает проход через входное отверстие между внутренней и внешней частями дозирующей камеры и в котором выпускной конец дозирующего резервуара закрыт, и нажатым открытым положением, в котором впускное отверстие дозирующего резервуара герметично соединено с заполняющим концом клапана, а распылительное отверстие штока открывает проход между внутренней и внешней частями дозирующей камеры. 15. Фармацевтический продукт по п.14,дополнительно имеющий переходник с корпусом для подсоединения к аэрозольному баллону,распылительным элементом, присоединяемым к распылительному концу штока клапана, и наконечником. 16. Фармацевтический продукт по п.15, в котором распылительный элемент имеет выпускное отверстие, направленное в наконечник,причем диаметр этого выпускного отверстия составляет от 0,20 до 0,33 мм. 17. Фармацевтический продукт по п.16, в котором диаметр выпускного отверстия составляет приблизительно 0,28 мм. 18. Фармацевтический продукт по п.17, в котором длина форсунки выпускного отверстия составляет от 0,30 до 0,60 мм. 19. Фармацевтический продукт по п.18, в котором длина форсунки выпускного отверстия составляет 0,50 мм. 20. Фармацевтическая аэрозольная композиция, которой заполнен аэрозольный баллон,снабженный распылительным клапаном, и которая включает соединение формулы I где R1 обозначает 1-бутил, 2-бутил, циклогексил или фенил иR2 обозначает ацетил или изобутаноил, и гидрофторуглеводородный пропеллент, а также сорастворитель в количестве, эффективном для растворения соединения формулы (I).
МПК / Метки
МПК: A61K 9/00
Метки: аэрозольные, медицинские, препараты
Код ссылки
<a href="https://eas.patents.su/7-2381-medicinskie-aerozolnye-preparaty.html" rel="bookmark" title="База патентов Евразийского Союза">Медицинские аэрозольные препараты</a>











