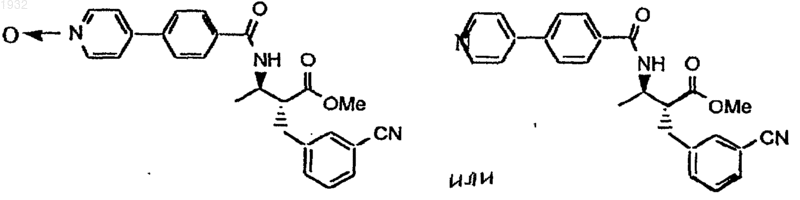
Замещенные n-[(аминоиминометил или аминометил)фенил] пропиламиды
Номер патента: 2358
Опубликовано: 25.04.2002
Авторы: Спада Альфред П., Макгарри Дэниел Г., Паулс Хейнц В., Гонг Енг, Гертин Кевин Р., Клейн Скотт И.
Формула / Реферат
1. Соединение формулы
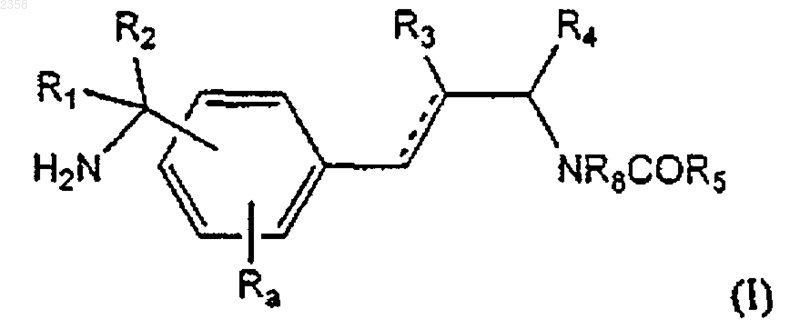
в которой ----- представляет одинарную или двойную связь;
Ra представляет водород, гидрокси или амино;
R1 и R2 представляют водород или, взятые вместе, представляют =NR9;
R3 представляет водород, -CO2R6, -C(O)R6, -CONR6R6, -CH2OR7 или -CH2SR7;
R4 представляет водород, C1-C15 алкил, Q-C1-C15 алкил или тиогетероциклил, где гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, причём, один или более атомов в кольце являются иными чем углерод, необязательно атомами азота, кислорода или серы, или группу формулы
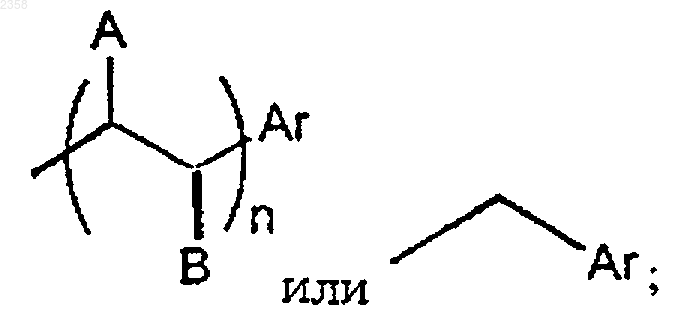
R5 представляет C1-C15 алкил; C2-C15 алкенил; C2-C15 алкинил; С3-С10 моно- или полициклический циклоалкил; С3-С10 моно- или полициклический циклоалкенил; моно- или полициклический гетероциклил с 3-10 кольцевыми атомами с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; моно- или полициклический гетероцикленил с 3-10 кольцевыми атомами с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; сконденсированный C6-C14 моно- или полициклический арил-С3-С10 моно- или полициклический циклоалкил; с 5-14 кольцевыми атомами сконденсированный моно- или полициклический гетероарил-С3-С10 моно- или полициклический циклоалкил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный C6-C14 моно- или полициклический арил-С3-С10 моно- или полициклический циклоалкенил; с 5-14 кольцевыми атомами сконденсированный моно- или полициклический гетероарил-С3-С10 моно- или полициклический циклоалкенил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный C6-C14 моно- или полициклический арил-гетероциклил, в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, причём один или более кольцевых атомов являются иными чем углерод, необязательно атомами азота, кислорода или серы; с 5-14 кольцевыми атомами сконденсированный моно- или полициклический гетероарил-гетероциклил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный C6-C14 моно- или полициклический арил-гетероцикленил, в котором гетероцикленил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, причём один или более атомов в кольце являются иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; сконденсированный, имеющий 5-14 кольцевых атомов моно- или полициклический гетероарил-гетероцикленил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и в котором гетероцикленил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, причём, один или более атомов в кольце являются иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; С6-С14 моно- или полициклический арил; сконденсированный С3-С10 моно- или полициклический циклоалкенил-С6-С14 моно- или полициклический арил; сконденсированный С3-С10 моно- или полициклический циклоалкил-С6-С14 моно- или полициклический арил; сконденсированный гетероциклил-С6-С14 моно- или полициклический арил, в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, причём, один или более атомов в кольце являются иными, чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный гетероцикленил-С6-C14 моно- или полициклический арил, в котором гетероцикленил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, причём, один или более атомов в кольце являются иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; моно- или полициклический с 5-14 кольцевыми атомами гетероарил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный С3-С10 моно- или полициклический циклоалкил моно- или полициклический с 5-14 кольцевыми атомами гетероарил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный С3-С10 моно- или полициклический циклоалкенил моно- или полициклический с 5-14 кольцевыми атомами гетероарил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный гетероцикленил моно- или полициклический с 5-14 кольцевыми атомами гетероарил, в котором гетероцикленил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, причём один или более атомов в кольце являются иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; сконденсированный гетероциклил моно- или полициклический гетероарил с 5-14 кольцевыми атомами с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, причём один или более атомов в кольце являются иными чем углерод, необязательно атомами азота, кислорода или серы; C6-C14 моно- или полициклический арил-C1-C15 алкил; с 5-14 кольцевыми атомами моно- или полициклический гетероарил-C1-C15 алкил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; C6-C14 моно- или полициклический арил-С2-С15 алкенил; с 5-14 кольцевыми атомами моно- или полициклический гетероарил-С2-С15 алкенил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; C6-C14 моно- или полициклический арил-С2-С15 алкинил; или с 5-14 кольцевыми атомами моно- или полициклический гетероарил-С2-С15 алкинил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы;
R6 представляет водород или C1-C6 алкил;
R7 представляет водород, C1-C6 алкил, C6-C14 моно- или полициклический Аr (C1-С6 низший алкил), C1-C6 ацил, ароиы ё C6-C14 моно- или полициклической арильной группой или гетероароил с моно- или полициклической гетероарильной группой с 5-14 кольцевыми атомами и с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы;
R8 представляет водород или C1-C6 алкил;
R9 представляет водород, R10O2C-, R10O-, НО-, циано, R10CO-, HCO-, C1-С6 алкил, нитро или Y1aY2aN-;
R10 представляет C1-C15 алкил, С6-С14 моно- или полициклический арил-C1-C15 алкил; или с 5-14 кольцевыми атомами моно- или полициклический гетероарил-С1-С15 алкил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы;
Y1a и Y2a представляют независимо водород или C1-C15 алкил;
А и В представляют водород или, взятые вместе, являются связью;
Q представляет R7O- или R7S-, или Y1Y2N-;
Y1 и Y2 представляют независимо водород, C1-C15 алкил, C6-C14 моно- или полициклический арил и C6-C14 моно- или полициклический арил-C1-C15 алкил или один из Y1 и Y2 представляет C1-C15 ацил или ароил с C6-C14 моно- или полициклической арильной группой, а другой из Y1 и Y2 представляет водород, C1-C15 алкил, C6-C14 моно- или полициклический арил, и C6-C14 моно- или полициклический арил-C1-C15 алкил;
Ar представляет C6-C14 моно- или полициклический арил или с 5-14 кольцевыми атомами моно- или полициклический гетероарил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атoмами азота, кислорода или серы; и
n равно 0, 1 или 2; или
его фармацевтически приемлемые соль, сольват или пролекарство.
2. Соединение по п.1, в котором - - - - - является одинарной связью, или его фармацевтически приемлемая соль, сольват или пролекарство.
3. Соединение по п.1, в котором ----- является двойной связью, или его фармацевтически приемлемая соль, сольват или пролекарство.
4. Соединение по п.1, в котором Ra представляет водород, или его фармацевтически приемлемая соль, сольват или пролекарство.
5. Соединение по п.1, в котором Ra представляет гидрокси или амино; более предпочтительно гидрокси, или его фармацевтически приемлемая соль, сольват или пролекарство.
6. Соединение по п.1, в котором R1 и R2, взятые вместе, представляют =NR9, или его фармацевтически приемлемая соль, сольват или пролекарство.
7. Соединение по п.1, в котором R1 и R2, взятые вместе, представляют =NH, или его фармацевтически приемлемая соль, сольват или пролекарство.
8. Соединение по п.1, в котором R3 представляет водород, или его фармацевтически приемлемая соль, сольват или пролекарство.
9. Соединение по п.1, в котором R3 представляет -СО2R6, -C(O)R6, -CH2OR7 или -СН2SR7, или его фармацевтически приемлемая соль, сольват или пролекарство.
10. Соединение по п.1, в котором R3 представляет -CO2R6, -CH2OR7 или -CH2SR7, или его фармацевтически приемлемая соль, сольват или пролекарство.
11. Соединение по п.1, в котором R3 представляет -СО2R6 или -CH2OR7, или его фармацевтически приемлемая соль, сольват или пролекарство.
12. Соединение по п.1, в котором R3 представляет -СO2R6 и R6 представляет C1-C6 алкил, или его фармацевтически приемлемая соль, сольват или пролекарство.
13. Соединение по п.1, в котором R3 представляет -CH2OR7 или -CH2SR7 и R7 представляет водород или C1-C6 алкил, или его фармацевтически приемлемая соль, сольват или пролекарство.
14. Соединение по п.1, в котором R4 представляет водород, C1-C15 алкил, Q-C1-C15 алкил или группу формулы

или его фармацевтически приемлемая соль, сольват или пролекарство.
15. Соединение по п.1, в котором R4 представляет C1-С6 алкил или группу формулы
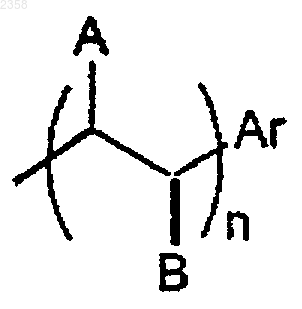
в которой А и В представляют водород и n равно 1, или его фармацевтически приемлемая соль, сольват или пролекарство.
16. Соединение по п.1, в котором R4 представляет Q-C1-C6 алкил, или его фармацевтически приемлемая соль, сольват или пролекарство.
17. Соединение по п.1, в котором R4 представляет R7O (C1-С6 алкил)-, или его фармацевтически приемлемая соль, сольват или пролекарство.
18. Соединение по п.1, в котором R4 представляет тиогетероциклил, в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, причём один или более атомов в кольце являются иными чем углерод, необязательно атомами азота, кислорода или серы, или его фармацевтически приемлемая соль, сольват или пролекарство.
19. Соединение по п.1, в котором R5 представляет C2-C15 алкинил, С3-С10 моно- или полициклический циклоалкил, С3-С10 моно- или полициклический циклоалкенил, с 3-10 кольцевыми атомами моно- или полициклический гетероциклил с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; с 3-10 кольцевыми атомами моно- или полициклический гетероцикленил с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; сконденсированный C6-C14 моно- или полициклический арил-С3-С10 моно- или полициклический циклоалкил; с 5-14 кольцевыми атомами сконденсированный моно- или полициклический гетероарил-С3-С10 моно- или полициклический циклоалкил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный C6-C14 моно- или полициклический арил-С3-С10 моно- или полициклический циклоалкенил; с 5-14 кольцевыми атомами сконденсированный моно- или полициклический гетероарил-С3-С10 моно- или полициклический циклоалкенил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный C6-C14 моно- или полициклический арил-гетероциклил, в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; с 5-14 кольцевыми атомами сконденсированный моно- или полициклический гетероарил-гетероциклил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольцх, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный C6-C14 моно- или полициклический арил-гетероцикленил, в котором гетероцикленил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; с 5-14 кольцевыми атомами сконденсированный гетероарил-гетероцикленил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и в котором гетероцикленил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, причём, один или более атомов в кольце являются иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; сконденсированный С3-С10 моно- или полициклический циклоалкенил-С6-С14 моно- или полициклический арил; сконденсированный С3-С10 моно- или полициклический циклоалкил-С6-С14 моно- или полициклический арил; сконденсированный гетероциклил-С6-С14 моно- или полициклический арил, в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированый гетероцикленил-С6-С14 моно- или полициклический арил, в котором гетероцикленил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; сконденсированный С3-С10 моно- или полициклический циклоалкил с 5-14 кольцевыми атомами моно- или полициклический гетероарил, причём один или более атомов в гетероарильном кольце являются иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный С3-С10 моно- или полициклический циклоалкенил с 5-14 кольцевыми атомами моно- или полициклический гетероарил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный гетероцикленил с 5-14 кольцевыми атомами моно- или полициклический гетероарил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и в котором гетероцикленил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; сконденсированный гетероциклил- с 5-14 кольцевыми атомами моно- или полициклический гетероарил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; C6-C14 моно- или полициклический арил-С1-С15 алкил; с 5-14 кольцевыми атомами моно- или полициклический гетероарил-C1-C15 алкил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; C6-C14 моно- или полициклический арил-С2-С15 алкенил; с 5-14 кольцевыми атомами моно- или полициклический гетероарил-алкенил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; С6-С14 моно- или полициклический арил-С2-С15 алкинил; или с 5-14 кольцевыми атомами моно- или полициклический гетероарил-С2-С15 алкинил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; более предпочтительно сконденсированный C6-C14 моно- или полициклический арил-С3-С10 моно- или полициклический циклоалкенил; с 5-14 кольцевыми атомами сконденсированный моно- или полициклический гетероарил-С3-С10 моно- или полициклический циклоалкил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированный C6-C14 моно- или полициклический арил-С3-С10 моно- или полициклический циклоалкил; сконденсированный C6-C14 моно- или полициклический арил-гетероциклил, в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; с 5-14 кольцевыми атомами сконденсированный моно- или полициклический гетероарил-гетероциклил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и в котором гетероциклил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; сконденсированый С6-С14 моно- или полициклический арил-гетероцикленил, в котором гетероцикленил обозначает моно- или полициклическую систему с 3-10 атомами в кольце с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; с 5-14 кольцевыми атомами сконденсированный моно- или полициклический гетероарил-гетероцикленил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и в котором гетероцикленил обозначает моно- или полициклическую систему с 3-10 атомами в кольце, с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, и который содержит, по крайней мере, одну углерод-углеродную или углерод-азотную двойную связь; или с 5-14 кольцевыми атомами сконденсированный моно- или полициклический гетероарил-С3-С10 моно- или полициклический циклоалкенил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы,
или его фармацевтически приемлемая соль, сольват или пролекарство.
20. Соединение по п.1, в котором R5 представляет С3-С10 моно- или полициклический циклоалкил; с 3-10 атомами моно- или полициклический гетероциклил с одним или более атомами в кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы; C6-C14 моно- или полициклический apил-C1-C15 алкил или С6-С14 моно- или полициклический арил-С2-С15 алкинил, или его фармацевтически приемлемая соль, сольват или пролекарство.
21. Соединение по п.1, в котором R5 представляет С6-C14 моно- или полициклический арил или с 5-14 кольцевыми атомами моно- или полициклический гетероарил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, или его фармацевтически приемлемая соль, сольват или пролекарство.
22. Соединение по п.1, в котором R5 представляет фенил, нафтил или с 5-14 кольцевыми атомами моно- или полицикличесъшщ гетероарилс одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, или его фармацевтически приемлемая соль, сольват или пролекарство.
23. Соединение по п.1, в котором R5 представляет фенилзамещенный фенил, с 5-14 кольцевыми атомами моно- или полициклический гетероарил-замещенный фенил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, фенил-замещенный с 5-14 кольцевыми атомами моно- или полициклический гетероарил с одним или более атомами в гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, или необязательно с 5-14 кольцевыми атомами моно- или полициклический гетероарил-замещенный с 5-14 кольцевыми атомами моно- или полициклический гетероарил с одним или более атомами в каждом гетероарильном кольце, являющимися иными чем углерод, необязательно атомами азота, кислорода или серы, или его фармацевтически приемлемая соль, сольват или пролекарство.
24. Соединение по п.1, в котором R6 представляет C1-С6 алкил, или его фармацевтически приемлемая соль, сольват или пролекарство.
25. Соединение по п.1, в котором Q представляет R7O-, или его фармацевтически приемлемая соль, сольват или пролекарство.
26. Соединение по п.1, в котором R7 представляет водород или C1-С6 алкил, или его фармацевтически приемлемая соль, сольват или пролекарство.
27. Соединение по п.1, в котором R7 представляет С6-C14 моно- или полициклический Аr (C1-С6 алкил) или гетероароил с моно- или полициклической гетероарильной группой с 5-14 кольцевыми атомами, или его фармацевтически приемлемая соль, сольват или пролекарство.
28. Соединение по п.1, в котором R8 представляет водород, или его фармацевтически приемлемая соль, сольват или пролекарство.
29. Соединение по п.1, в котором R9 представляет водород, или его фармацевтически приемлемая соль, сольват или пролекарство.
30. Соединение по п.1, в котором А, В, R8 и R9 представляют водород, или его фармацевтически приемлемая соль, сольват или пролекарство.
31. Соединение по п.1, в котором R10 представляет C1-C6 алкил, или его фармацевтически приемлемая соль, сольват или пролекарство.
32. Соединение по п.1, в котором n равно 1, или его фармацевтически приемлемая соль, сольват или пролекарство.
33. Соединение по п.1, в котором фрагмент

находится в мета-положении по отношению к положению присоединения фенильного фрагмента к фрагменту
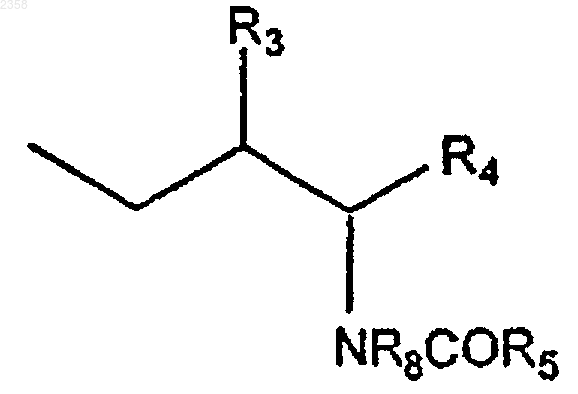
или его фармацевтически приемлемая соль, сольват или пролекарство.
34. Соединение по п.1, в котором Ra представляет гидрокси или амино, который находится в пара-положении по отношению к фрагменту
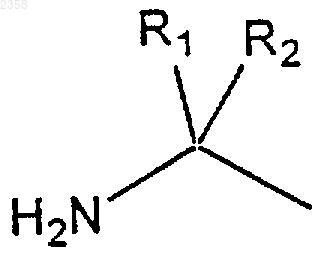
который находится в мета-положении по отношению к положению присоединения фенильного фрагмента к фрагменту
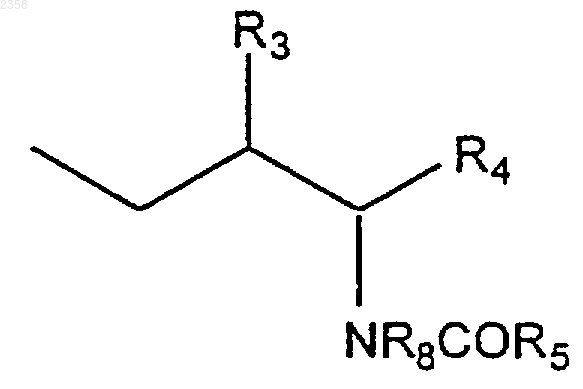
или его фармацевтически приемлемая соль, сольват или пролекарство.
35. Соединение по п.34, в котором Ra представляет гидрокси, или его фармацевтически приемлемая соль, сольват или пролекарство.
36. Соединение по п.1, в котором Аr представляет арил, или его фармацевтически приемлемая соль, сольват или пролекарство.
37. Соединение по п.1, в котором Аr представляет фенил, или его фармацевтически приемлемая соль, сольват или пролекарство.
38. Соединение по п.1, которое представляет собой
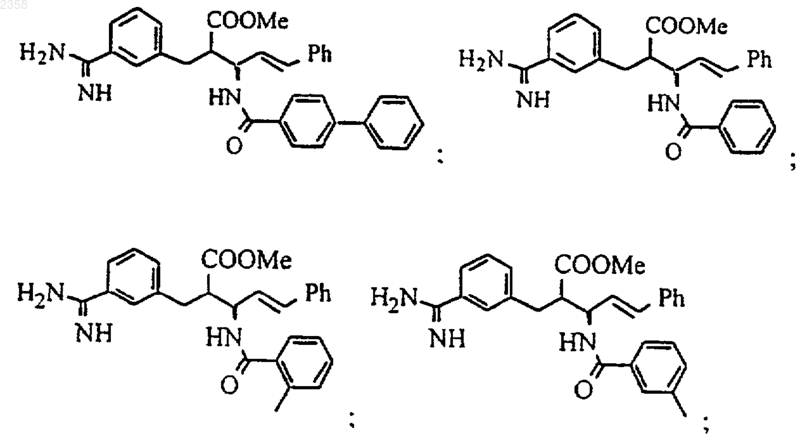
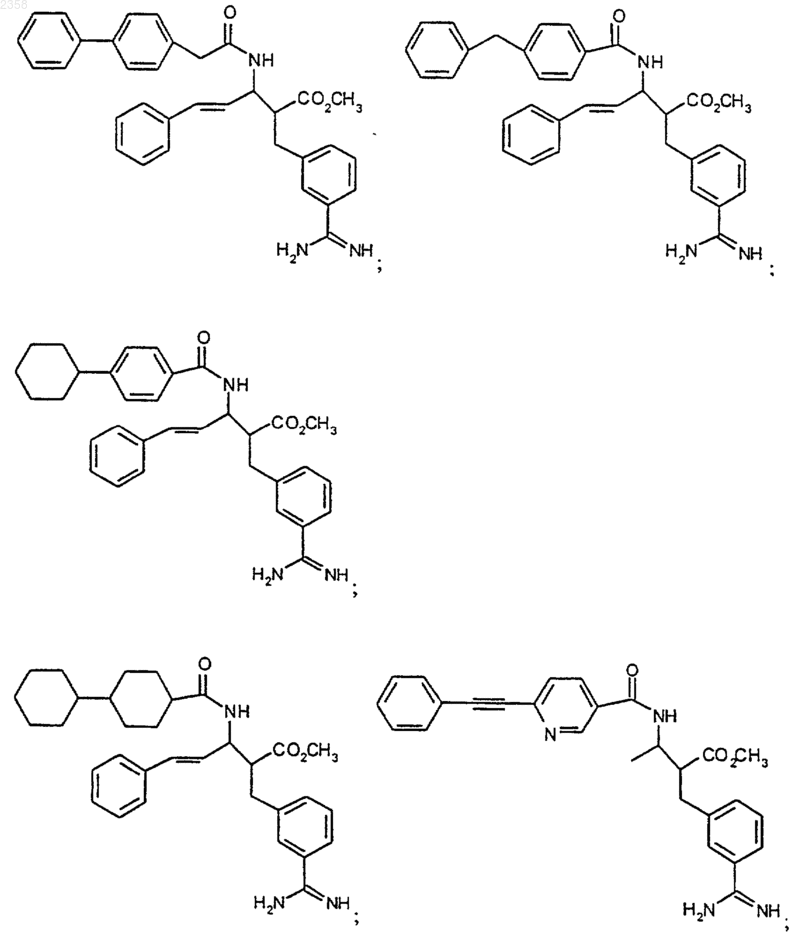
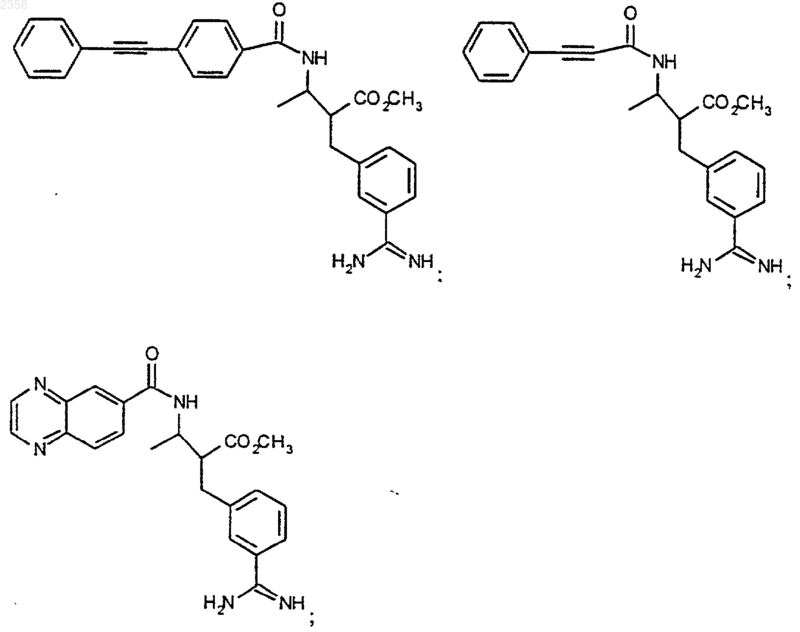
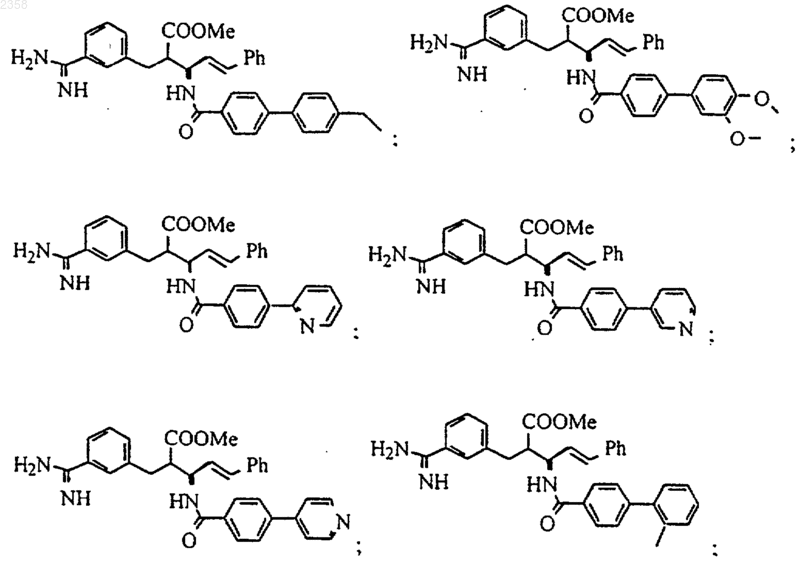
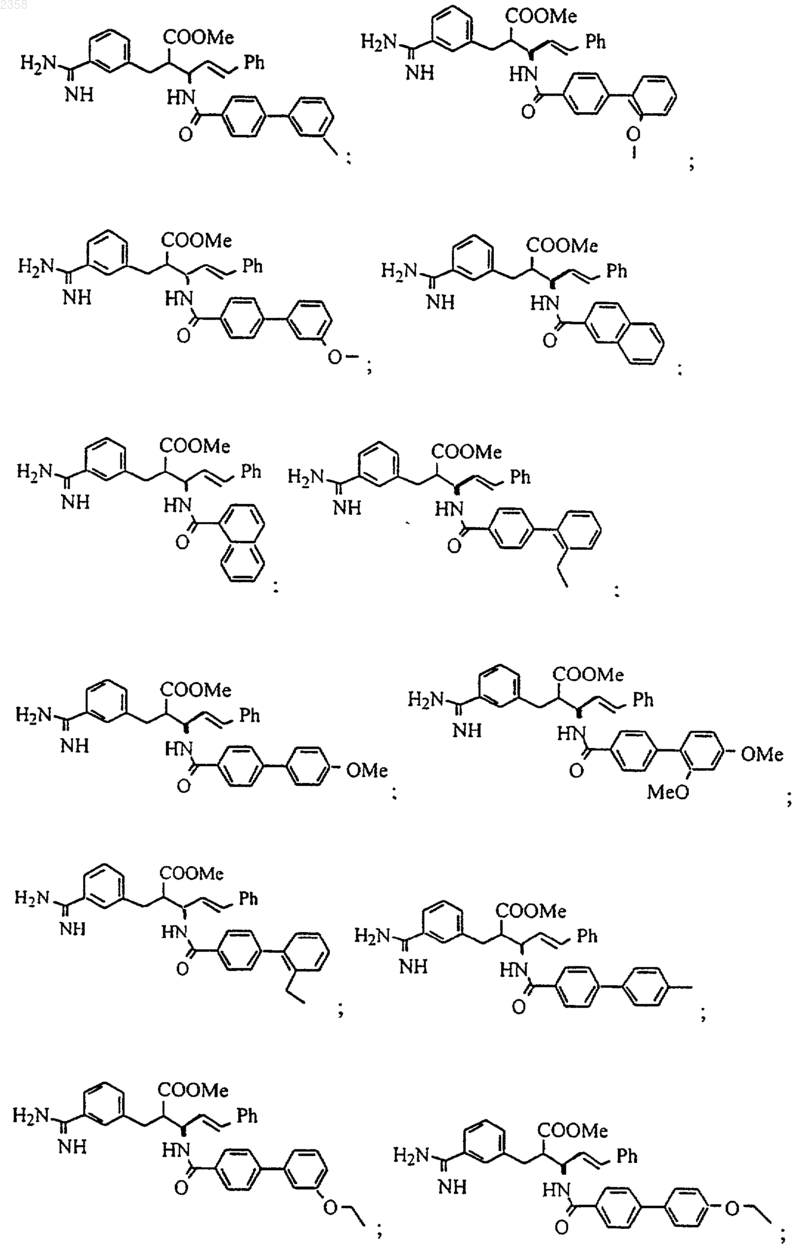

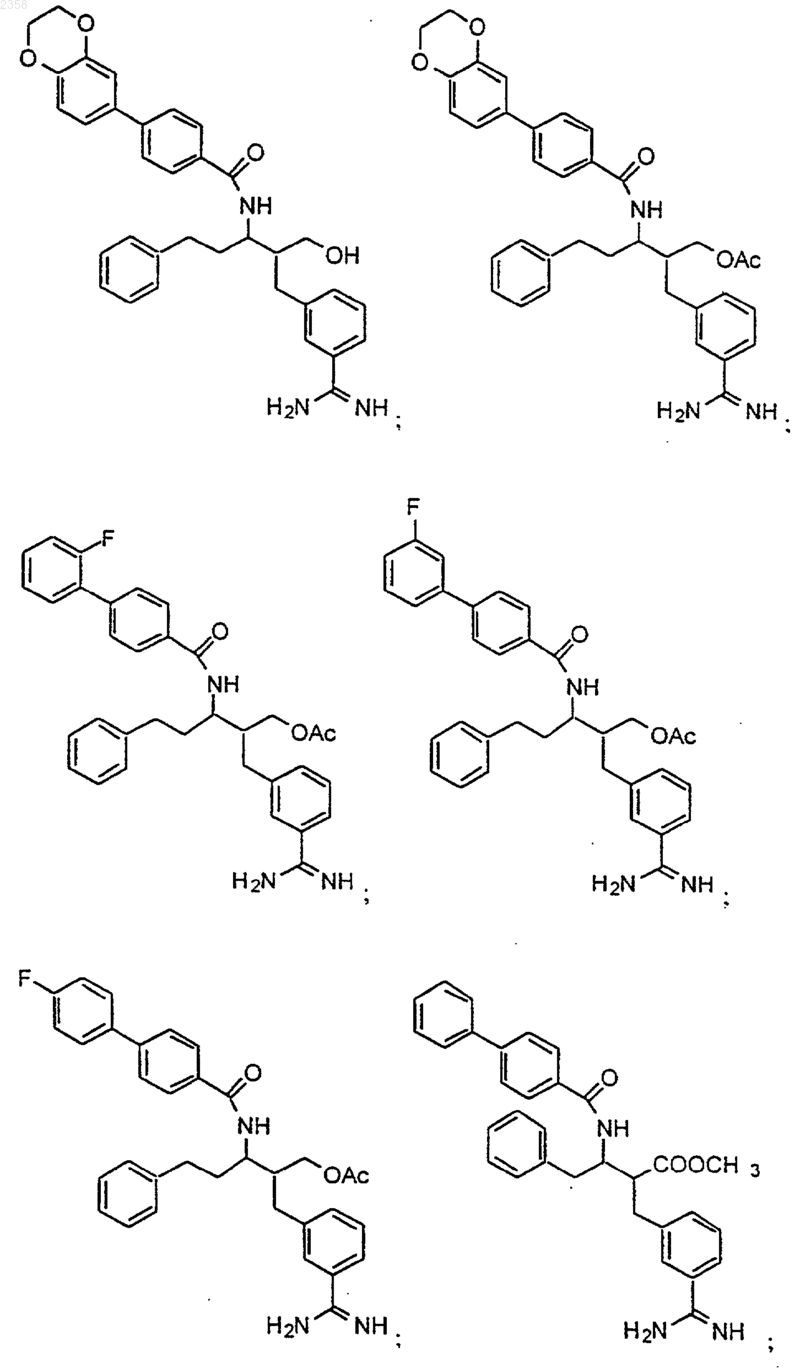
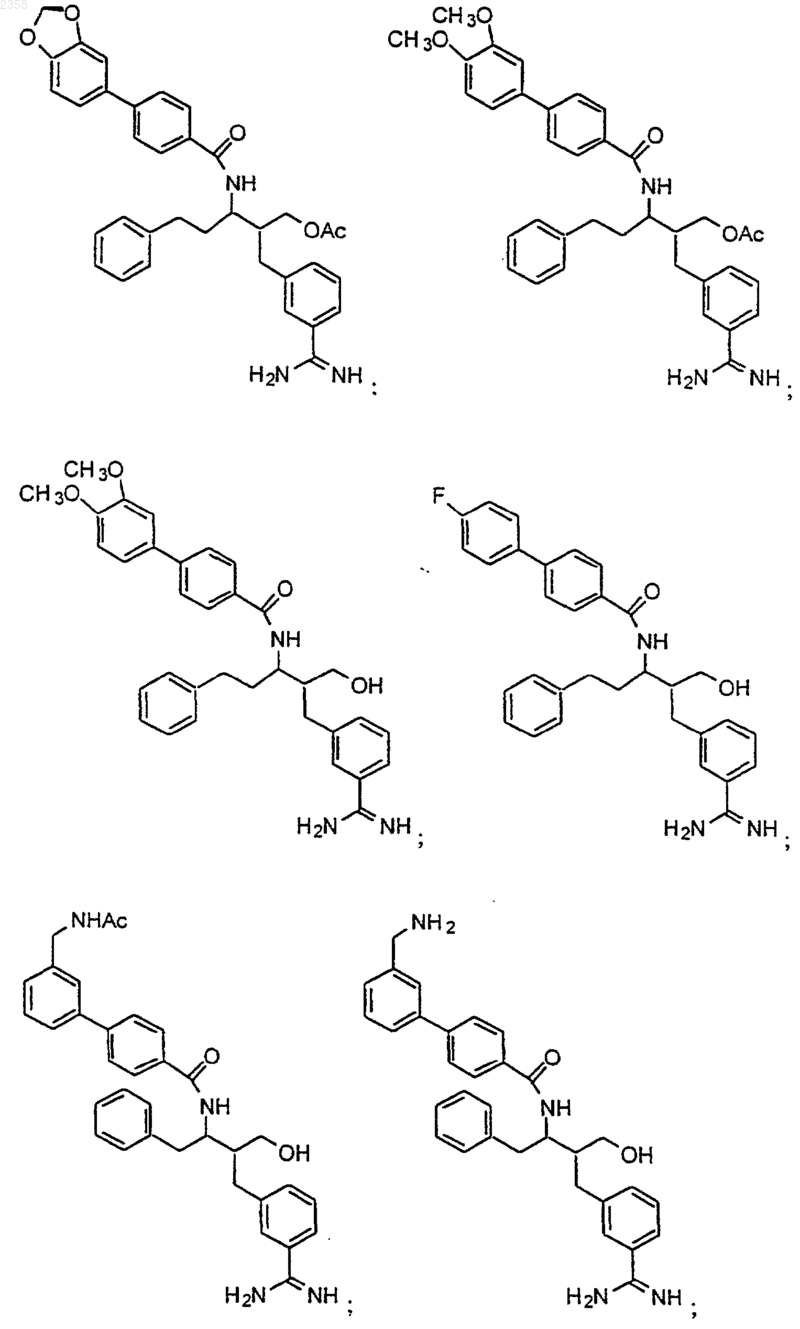
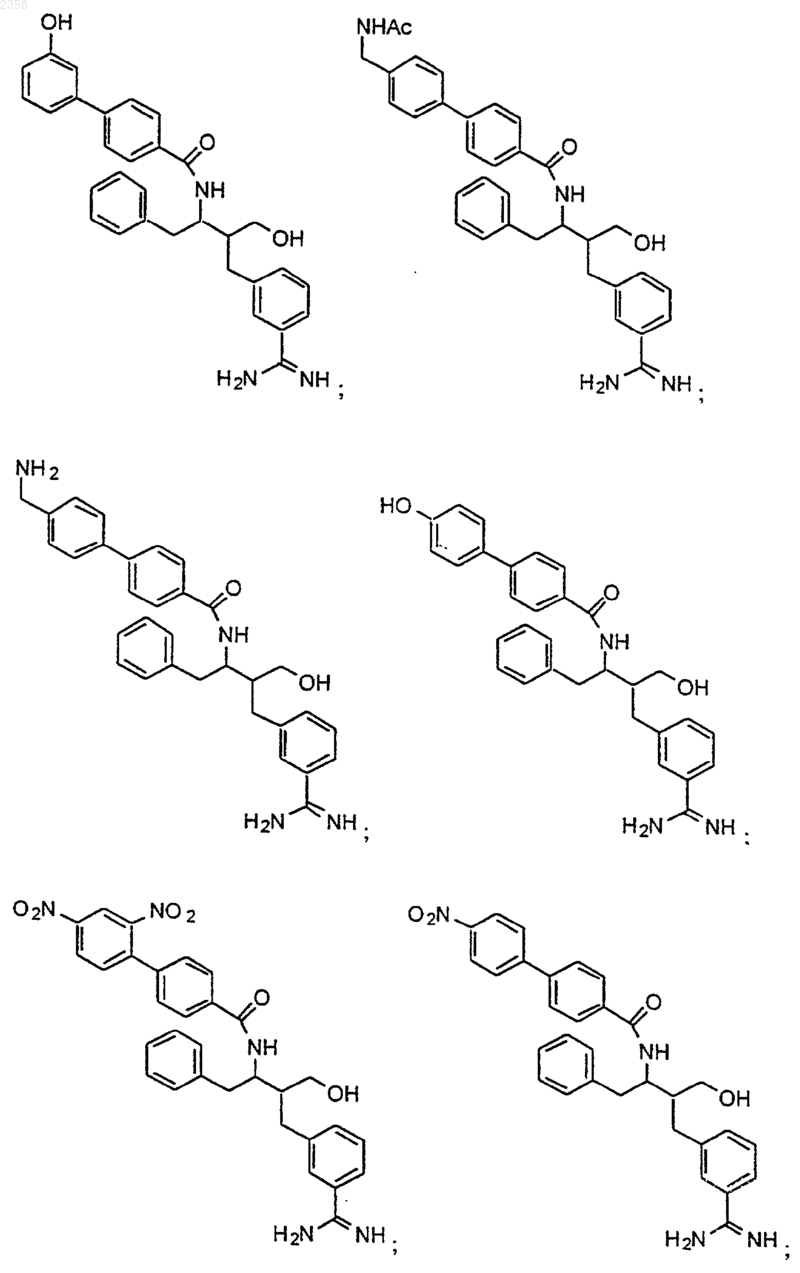
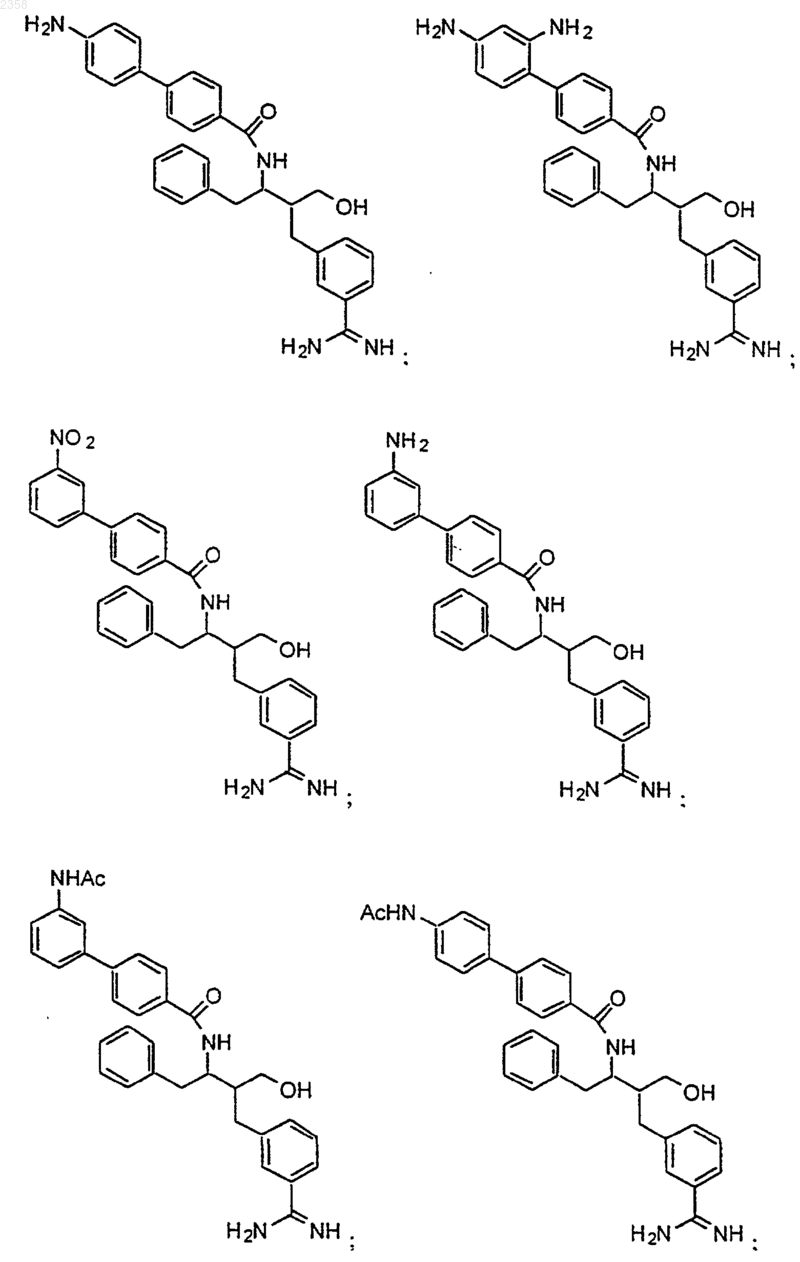
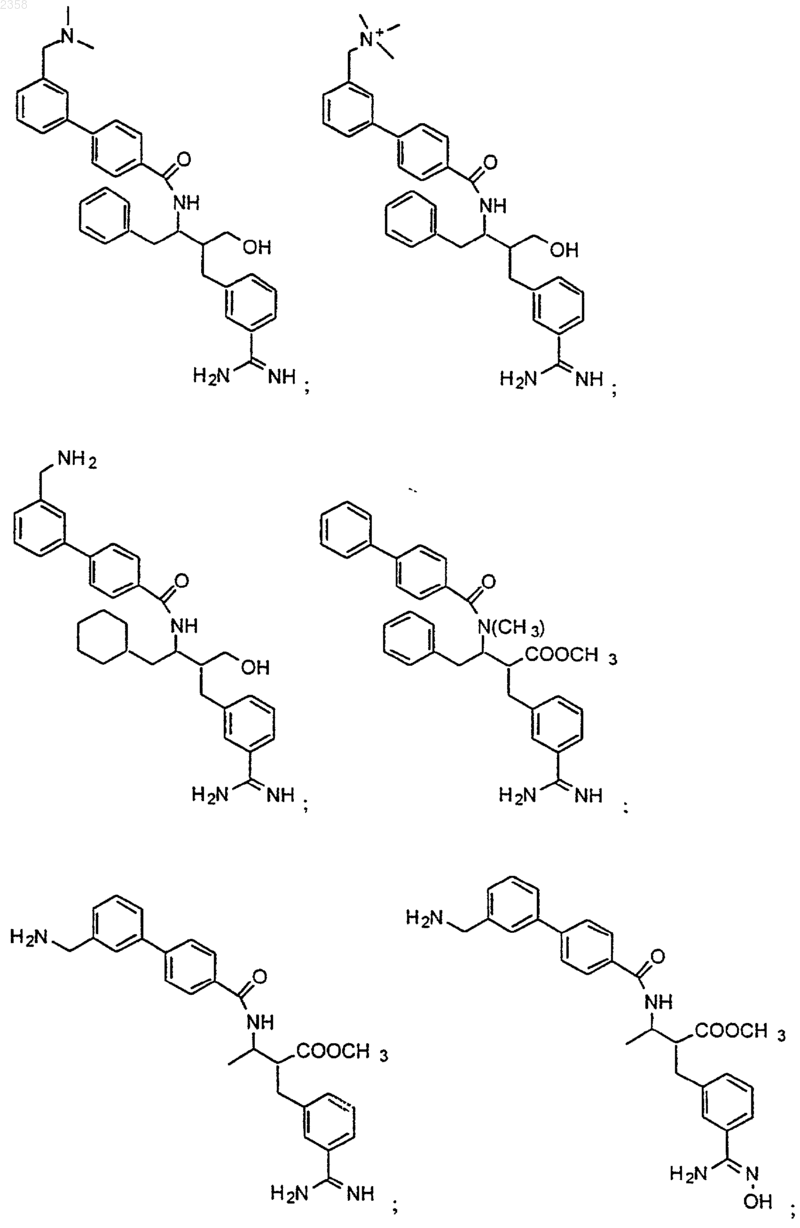
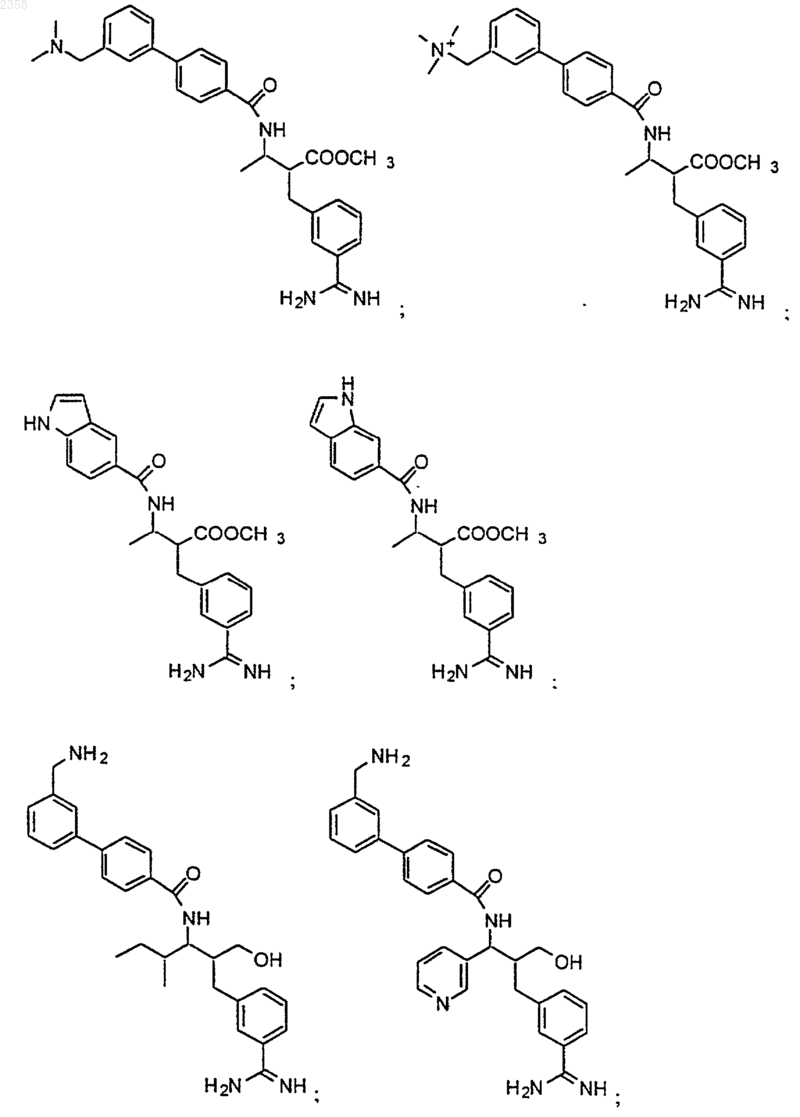
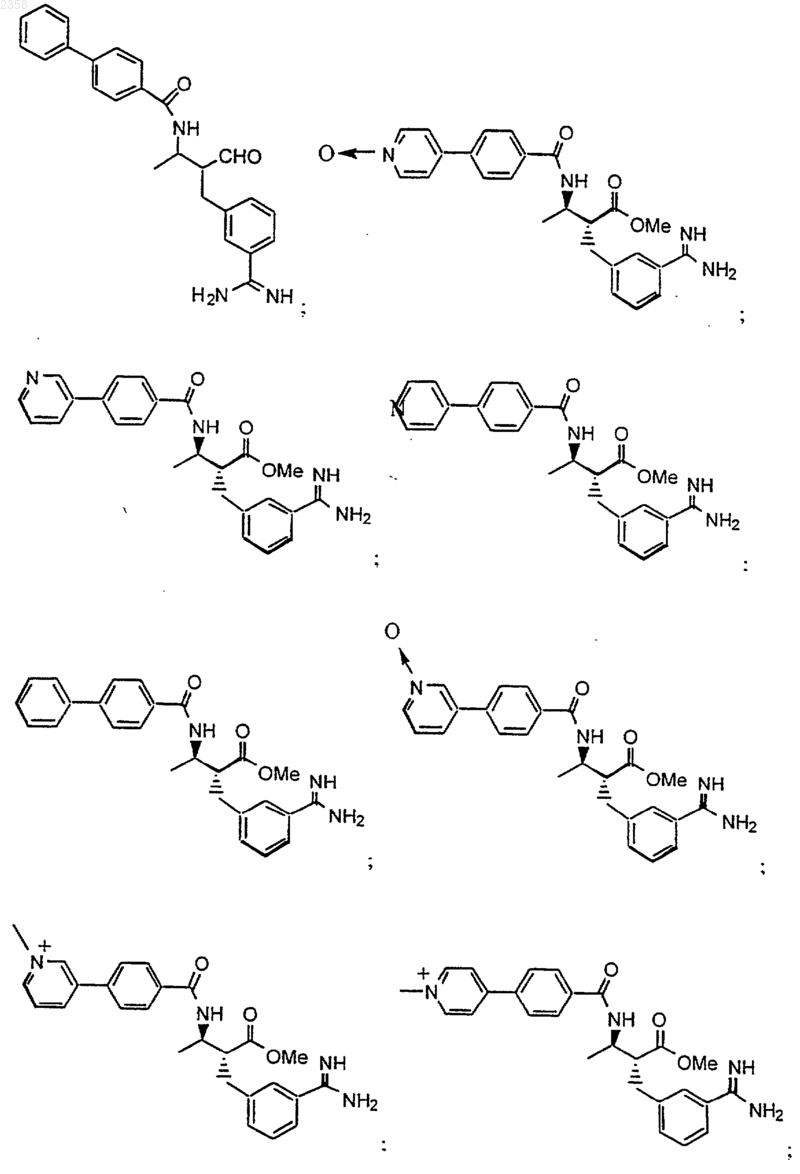
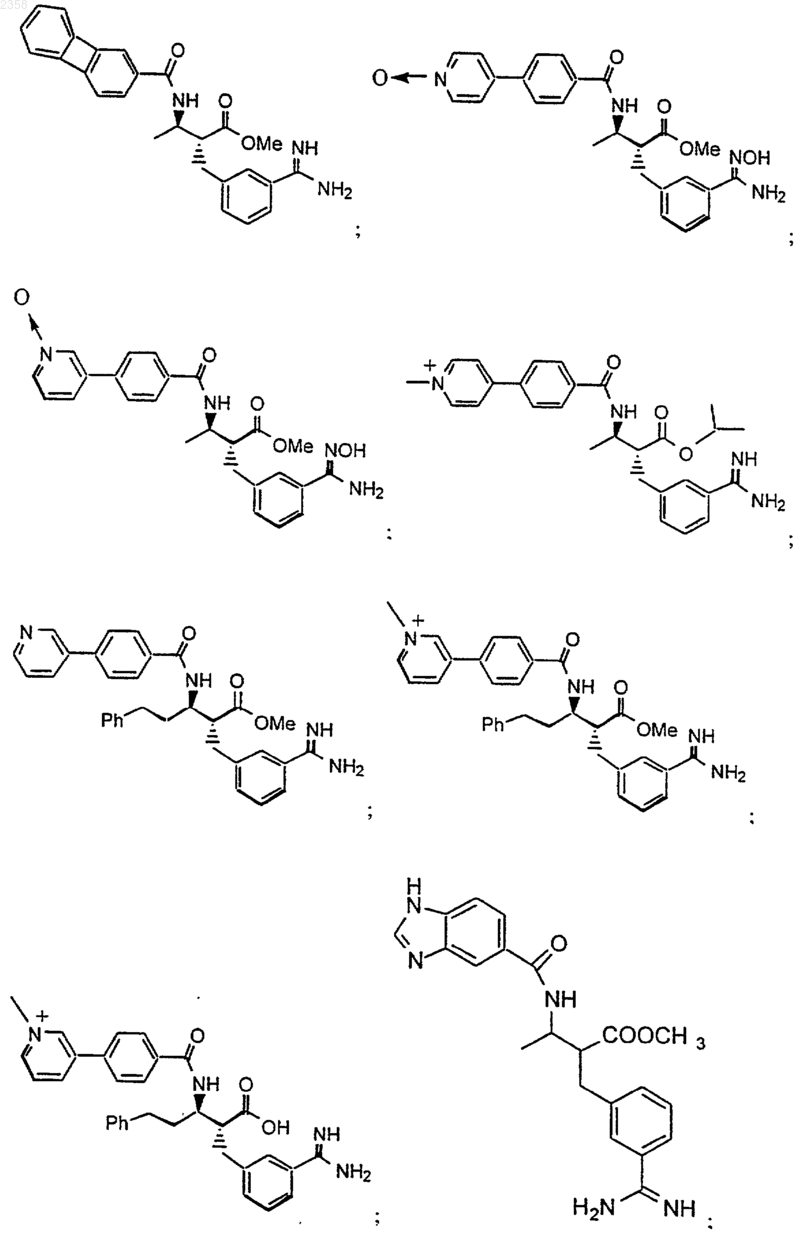
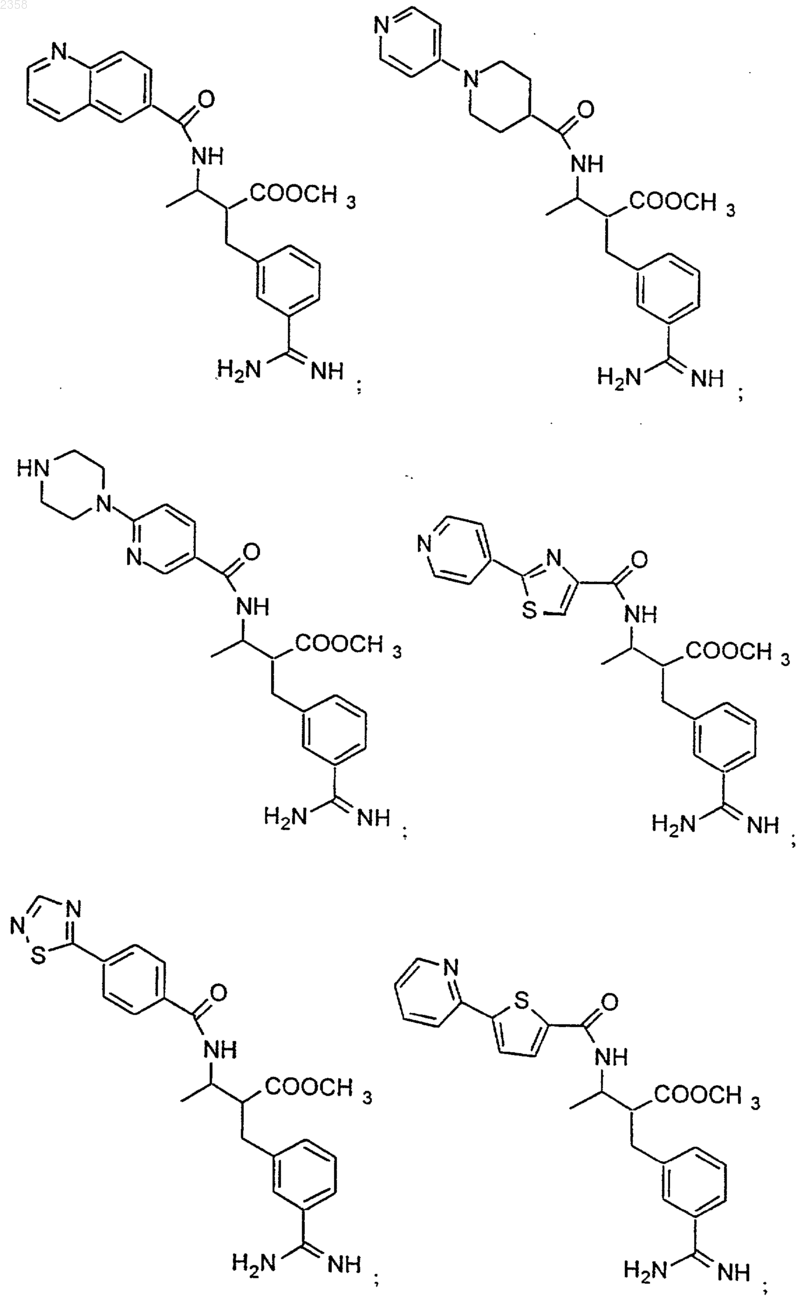
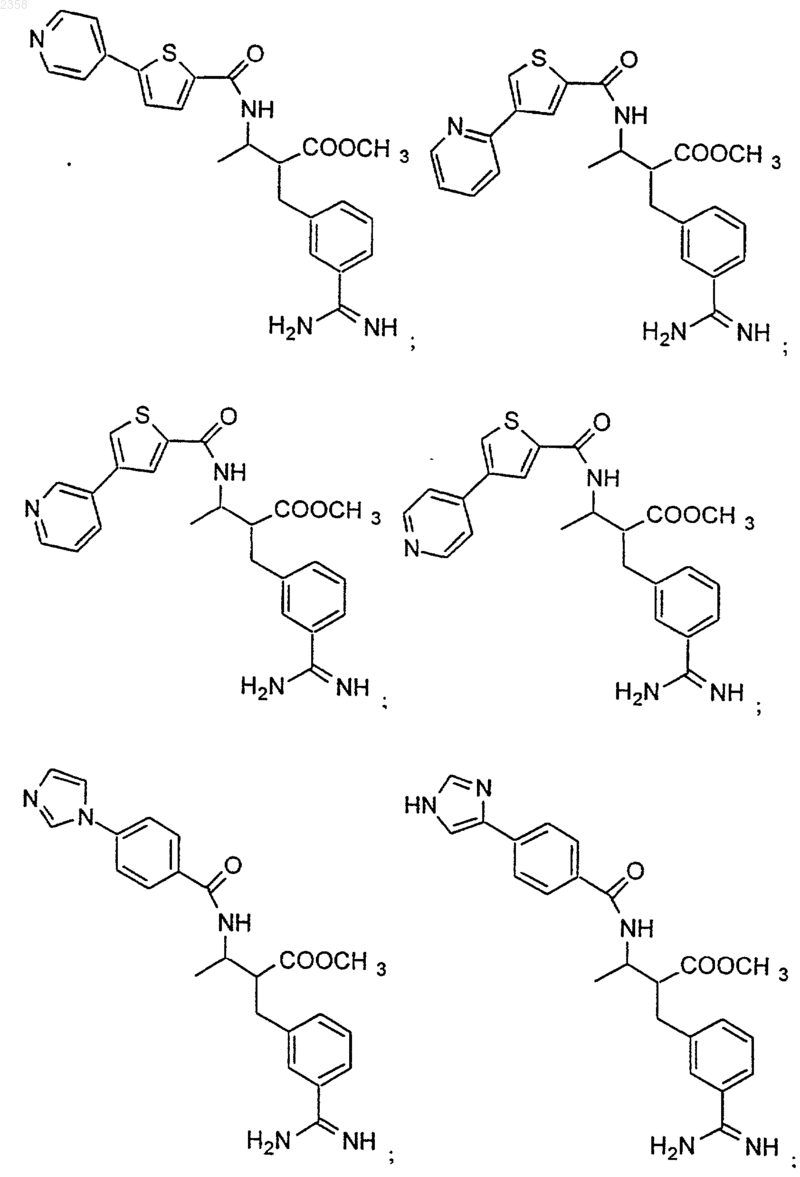
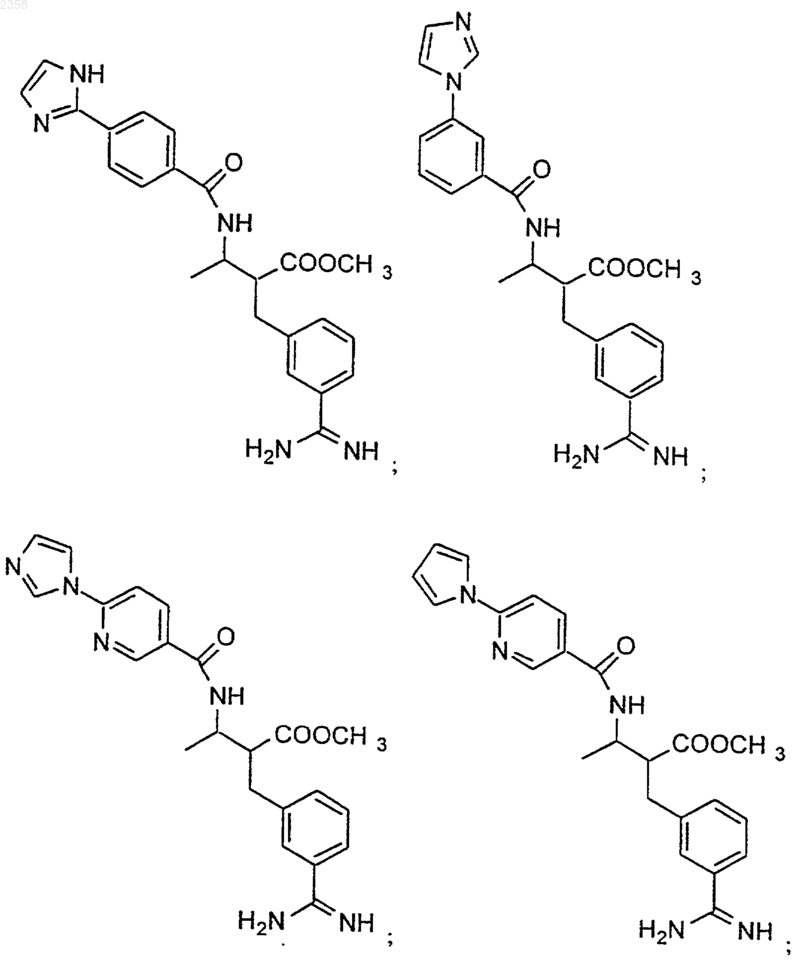
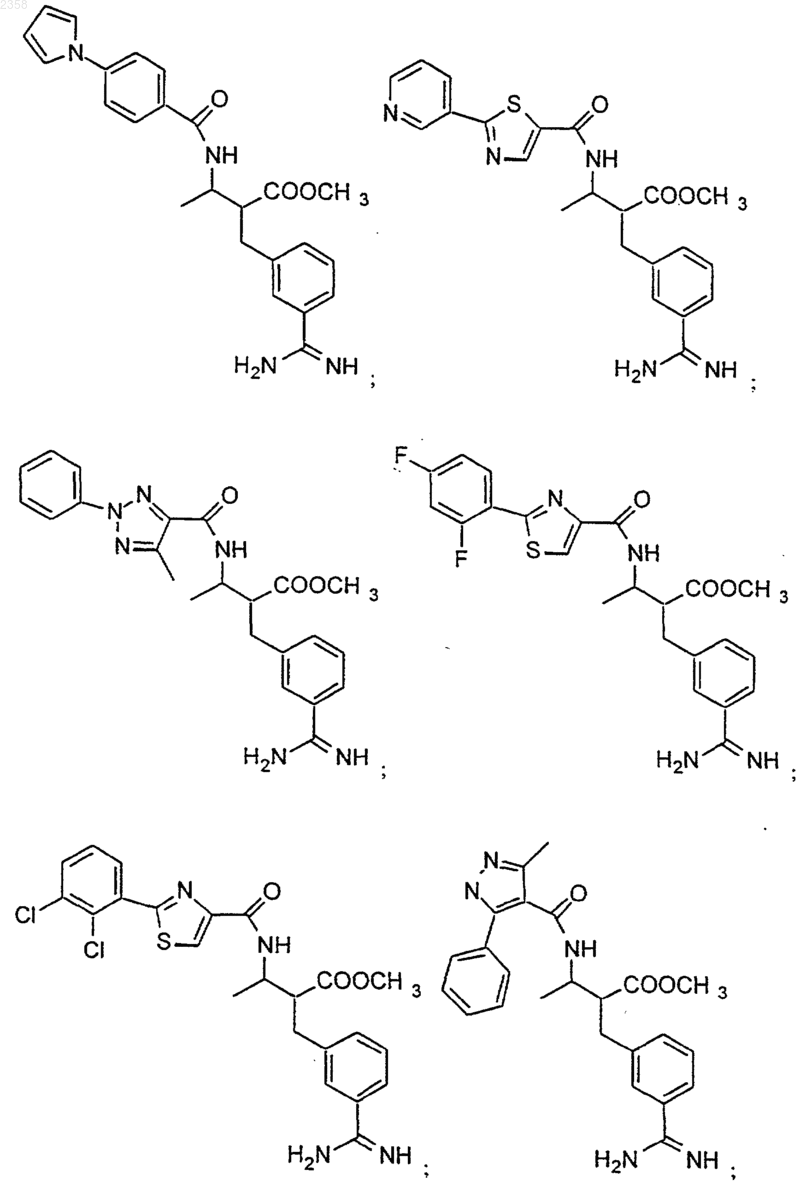
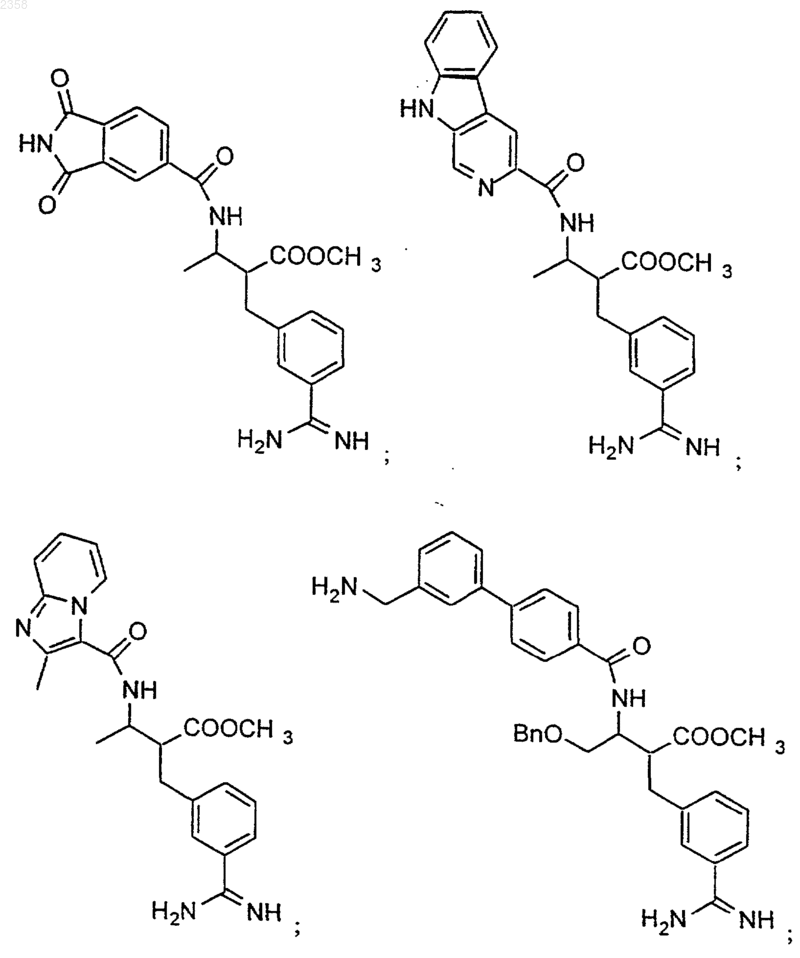
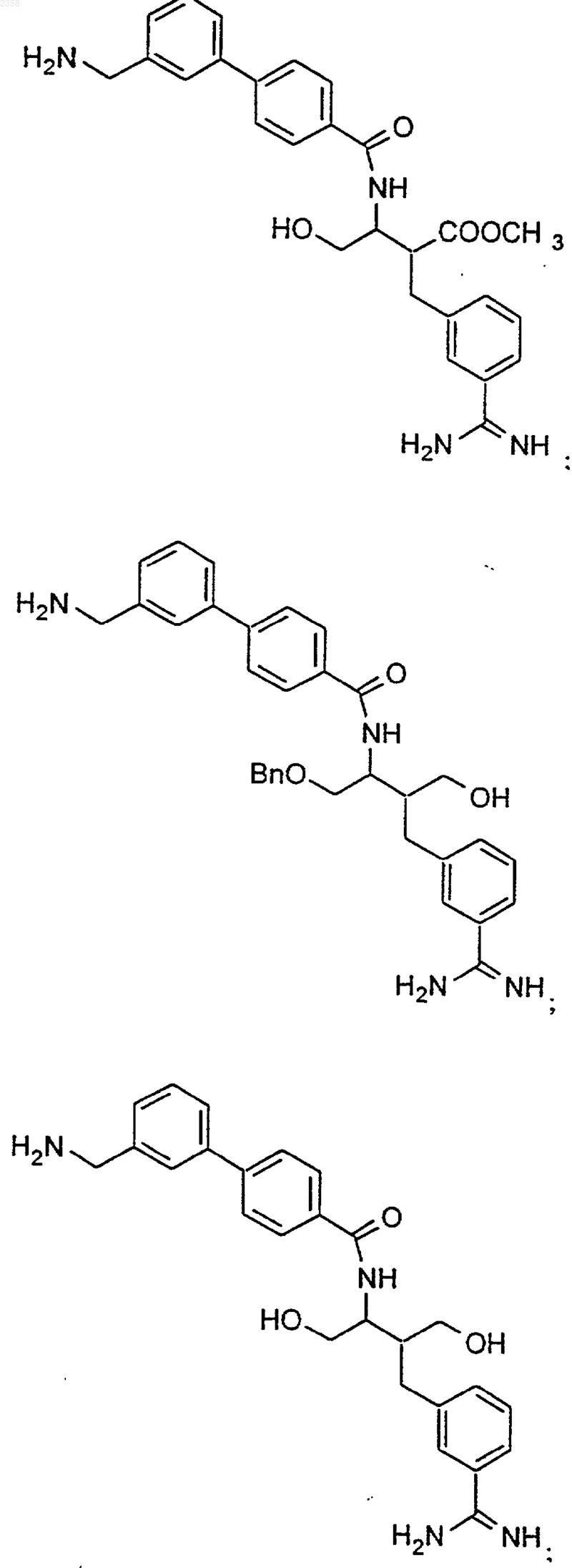
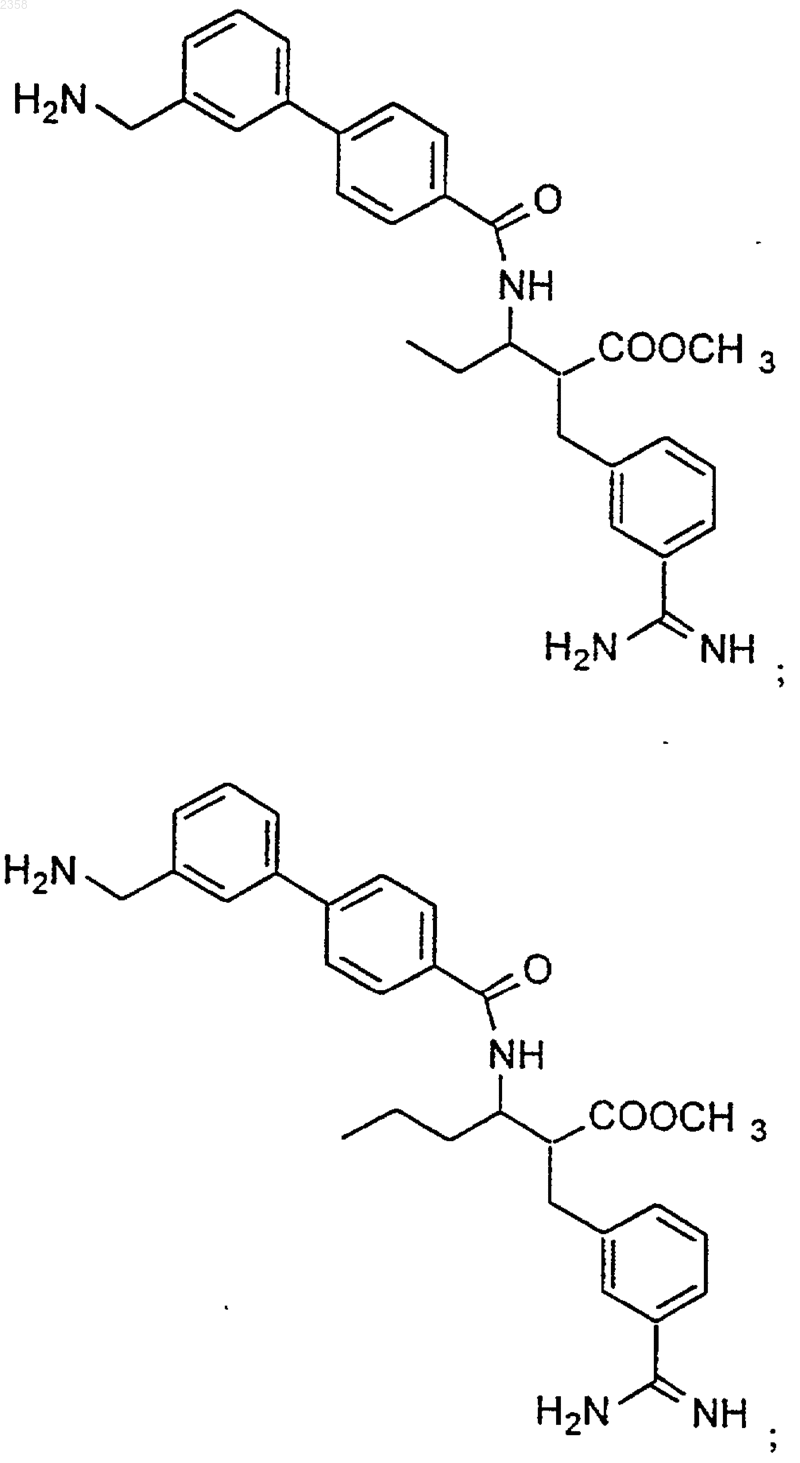
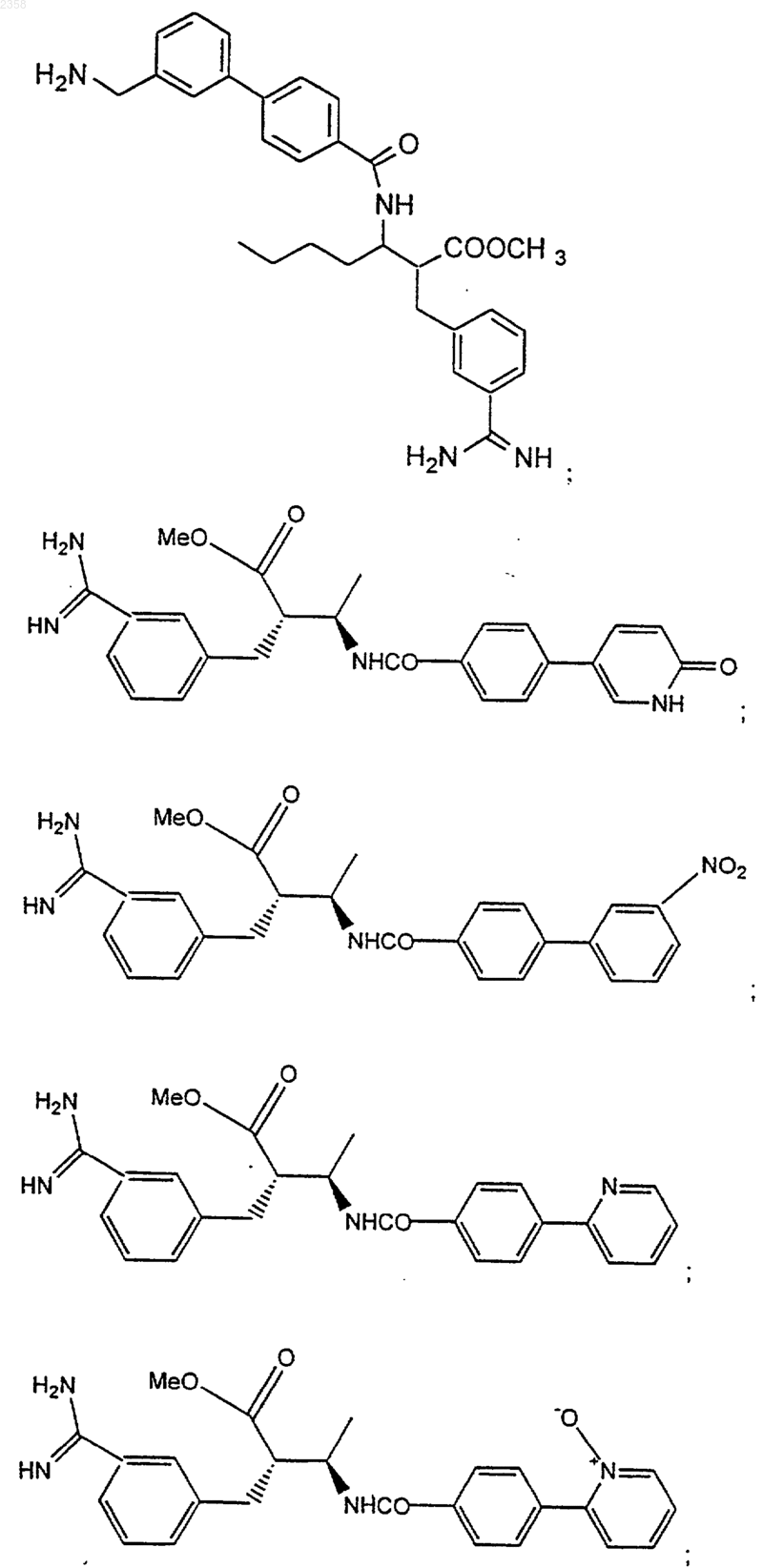
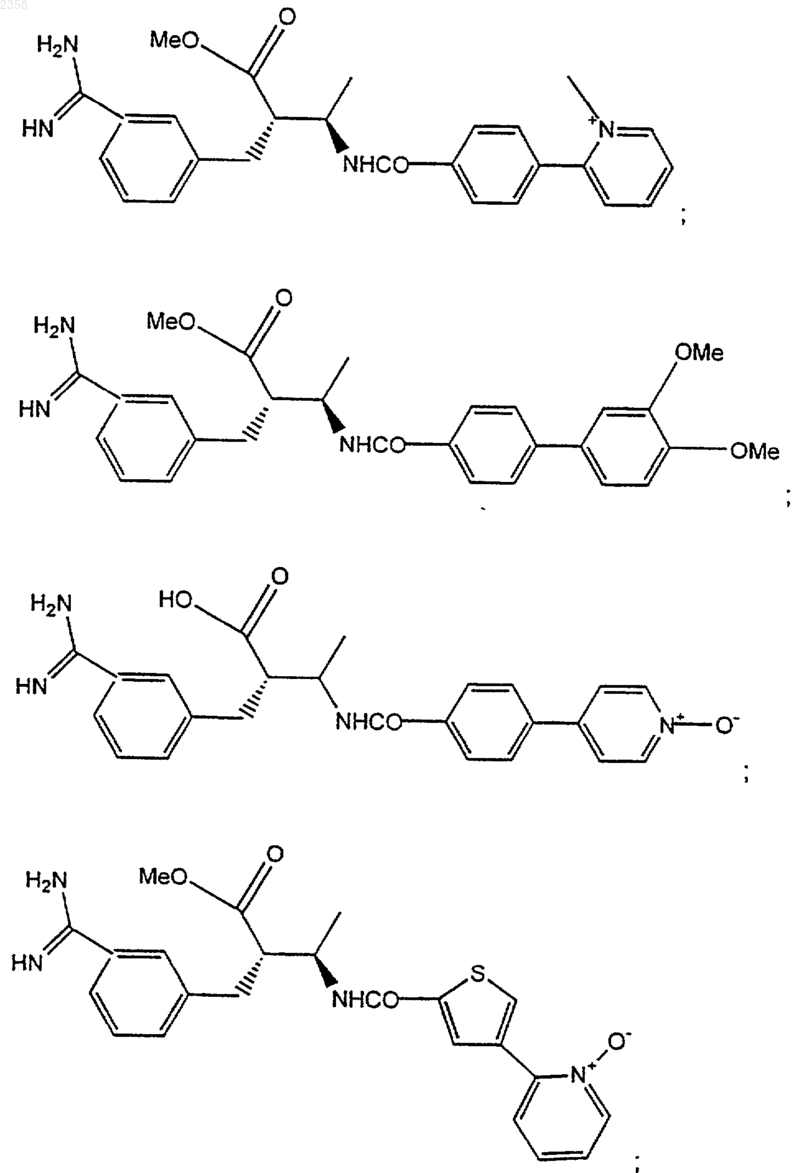
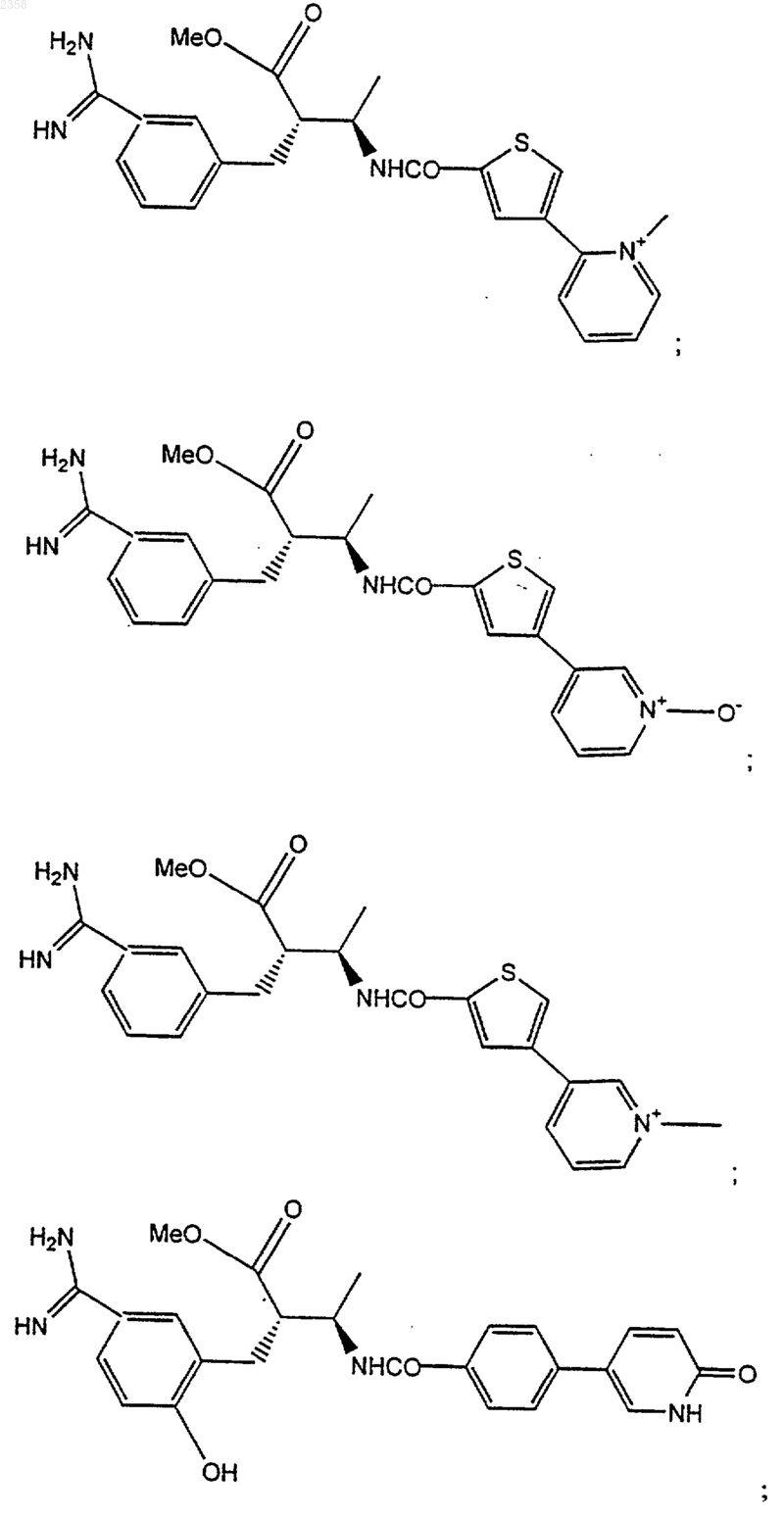
(Z)-N-[3-(5-карбамимидоил-2-гидроксифенил)аллил]-4-пиридин-3-илбензамид;
дитрифторацетат N-[3-(5-карбамимидоил-2-гидроксифенил)пропил]-(4-пиридин-3-ил)бензамида;
дитрифторацетат N-[3-(5-карбамимидоил-2-гидроксифенил)пропил]-4-(1-оксипиридин-4-ил)бензамида;
трифторацетат N-[3-(5-карбамимидоил-2-гидроксифенил)пропил]-4-(6-оксо-1,6-дигидропиридин-3-ил)бензамида;
дитрифторацетат N-[3-(5-карбамимидоил-2-гидроксифенил)пропил]-4-(пиридазин-4-ил)бензамида;
трифторацетат N-[3-(5-карбамимидоил-2-гидроксифенил)пропил]-7-хлорбензотиофен-2-карбоксамида;
трифторацетат (Е)-N-[3-(5-карбамимидоил-2-гидроксифенил)аллил]-4-(6-метоксипиридин-3-ил)бензамида;
трифторацетат (Е)-N-[3-(5-карбамимидоил-2-гидроксифенил)аллил]-4-(6-оксо-1,6-дигидропиридин-3-ил)бензамида;
трифторацетат [3-(5-карбамимидоил-2-гидроксифенил)аллил]амида (Е)-бифенил-4-карбоновой кислоты;
дитрифторацетат (Е)-N-[3-(5-карбамимидоил-2-гидроксифенил)аллил]-4-пиридин-3-илбензамида;
дитрифторацетат (Е)-N-[3-(5-карбамимидоил-2-гидроксифенил)аллил]-4-пиридин-4-илбензамида;
трифторацетат 4'-{[3-(5-карбамимидоил-2-гидроксифенил)аллил]амид}3-амида (Е)-бифенил-3,4'-дикарбоновой кислоты;
трифторацетат (Е)-4-трет-бутил-N-[3-(5-карбамимидоил-2-гидроксифенил)аллил]бензамида;
дитрифторацетат (Е)-N-[3-(5-карбамимидоил-2-гидроксифенил)аллил]-4-(3Н-имидазол-4-ил)бензамида;
трифторацетат 4-{[3-(5-карбамимидоил-2-гидроксифенил)аллил]амид}-4'-амида (Е)-бифенил-4,4'-дикарбоновой кислоты;
дитрифторацетат (Е)-N-[3-(5-карбамимидоил-2-гидроксифенил)аллил]-4-(1Н-имидазол-2-ил)бензамида;
трифторацетат [3-(5-карбамимидоил-2-гидроксифенил)аллил]амида (Е)-3-оксо-2,3-дигидротиено[3,2-с]пиридазин-6-карбоновой кислоты;
дитрифторацетат [3-(5-карбамимидоил-2-гидроксифенил)аллил]амида (Е)-5-пиридин-2-илтиофен-2-карбоновой кислоты;
трифторацетат [3-(5-карбамимидоил-2-гидроксифенил)пропил]амида бифенил-4-карбоновой кислоты;
трифторацетат N-[3-(5-карбамимидоил-2-гидроксифенил)пропил]-4-(6-метоксипиридин-3-ил)бензамида;
трифторацетат 4'-{[3-(5-карбамимидоил-2-гидроксифенил)пропил]амид}-3-амида бифенил-3,4-дикарбоновой кислоты;
трифторацетат 4-трет-бутил-N-[3-(5-карбамимидоил-2-гидроксифенил)пропил]бензамида;
дитрифторацетат [3-(5-карбамимидоил-2-гидроксифенил)пропил]-4-(3Н-имидазол-4-ил)бензамида;
дитрифторацетат N-[3-(5-карбамимидоил-2-гидроксифенил)пропил]-4-(1Н-имидазол-2-ил)бензамида;
дитрифторацетат [3-(5-карбамимидоил-2-гидроксифенил)аллил]амида-5-пиридин-2-илтиофен-2-карбоновой кислоты или
дитрифторацетат N-[3-(5-карбамимидоил-2-гидроксифенил)пропил]-4-пиперидин-4-илбензамида,
или его фармацевтически приемлемая соль, сольват или пролекарство.
39. Соединение по п.1, которое представляет
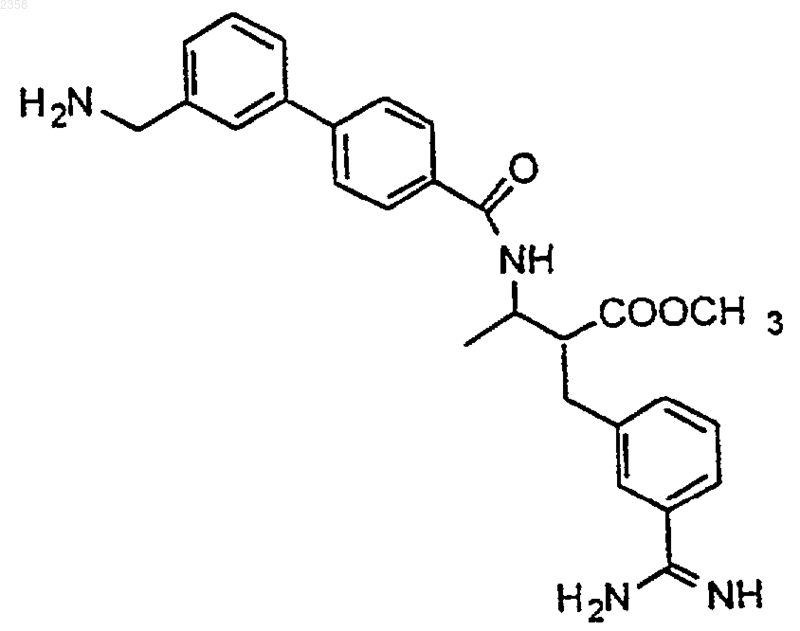
или его фармацевтически приемлемая соль, сольват или пролекарство.
40. Соединение по п.1, которое представляет
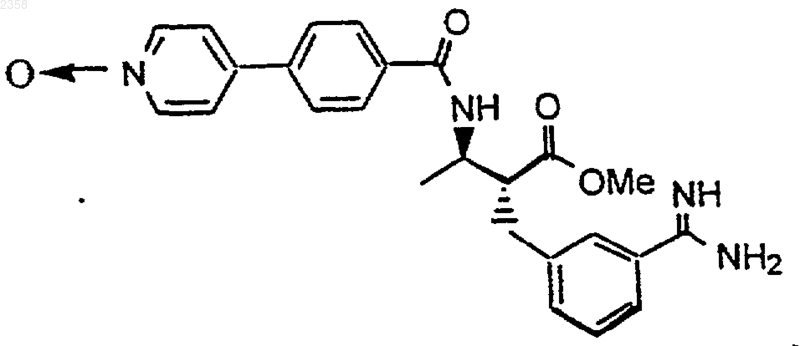
или его фармацевтически приемлемая соль, сольват или пролекарство.
41. Соединение по п.1, которое представляет
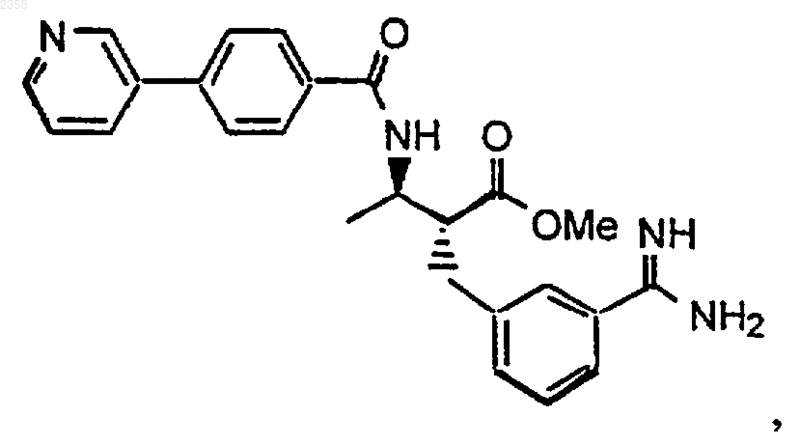
или его фармацевтически приемлемая соль, сольват или пролекарство.
42. Соединение по п.1, которое представляет
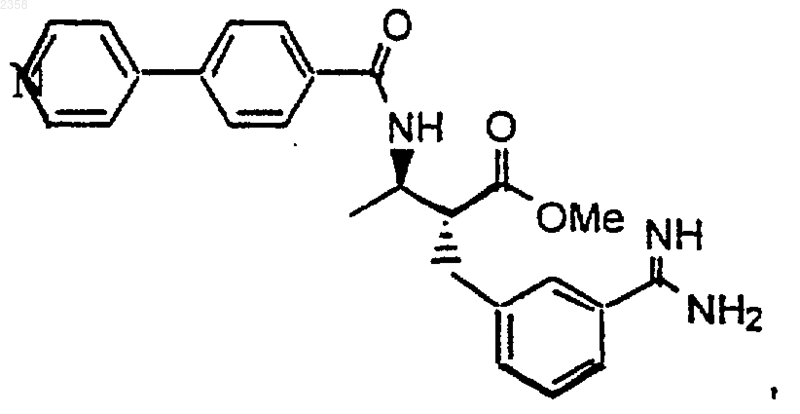
или его фармацевтически приемлемая соль, сольват или пролекарство.
43. Соединение по п.1, которое представляет
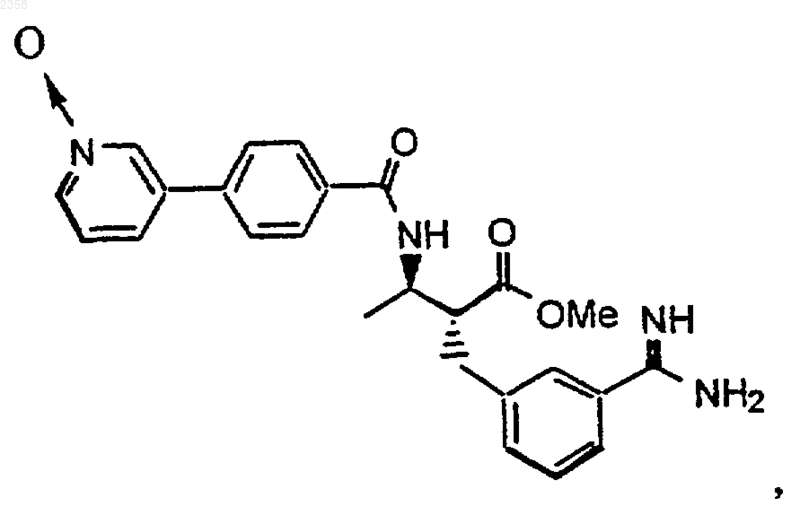
или его фармацевтически приемлемая соль, сольват или пролекарство.
44. Соединение по п.1, которое представляет
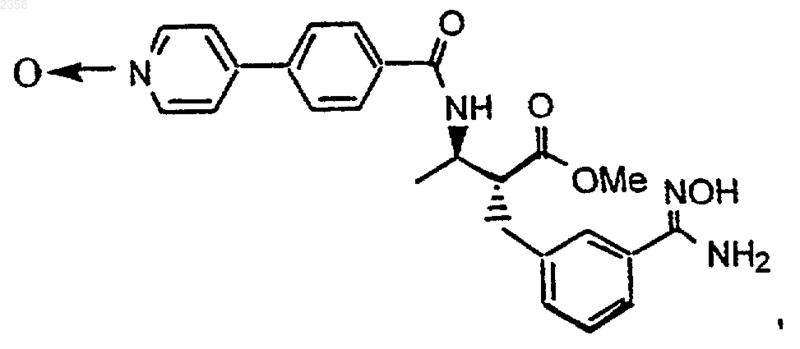
или его фармацевтически приемлемая соль, сольват или пролекарство.
45. Соединение по п.1, которое представляет
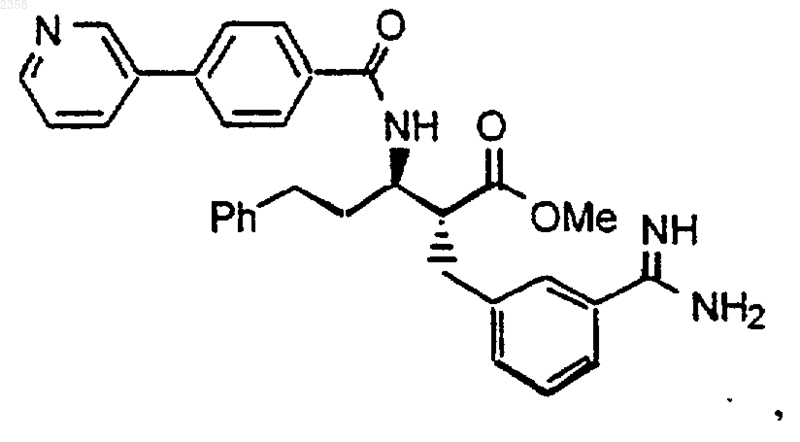
или его фармацевтически приемлемая соль, сольват или пролекарство.
46. Соединение по п.1, которое представляет
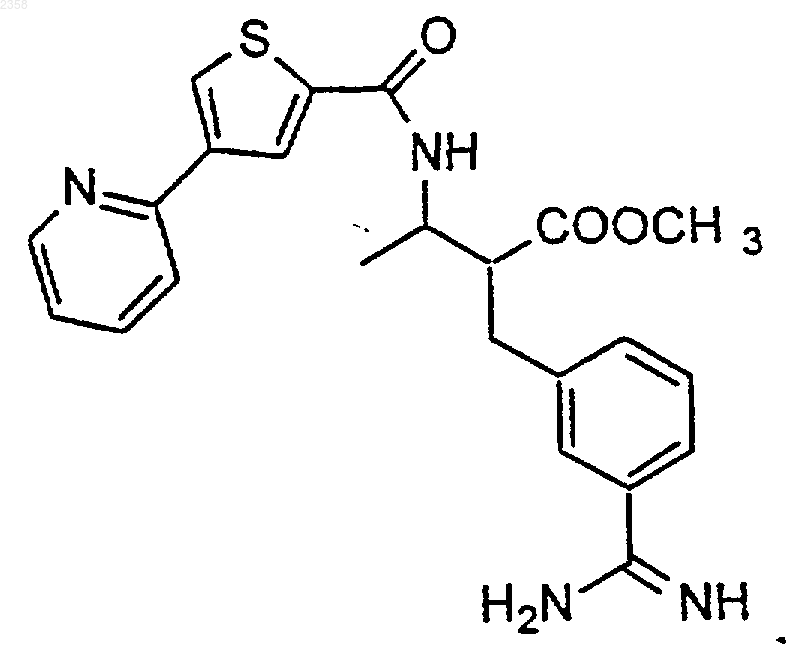
или его фармацевтически приемлемая соль, сольват или пролекарство.
47. Соединение по п.1, которое представляет
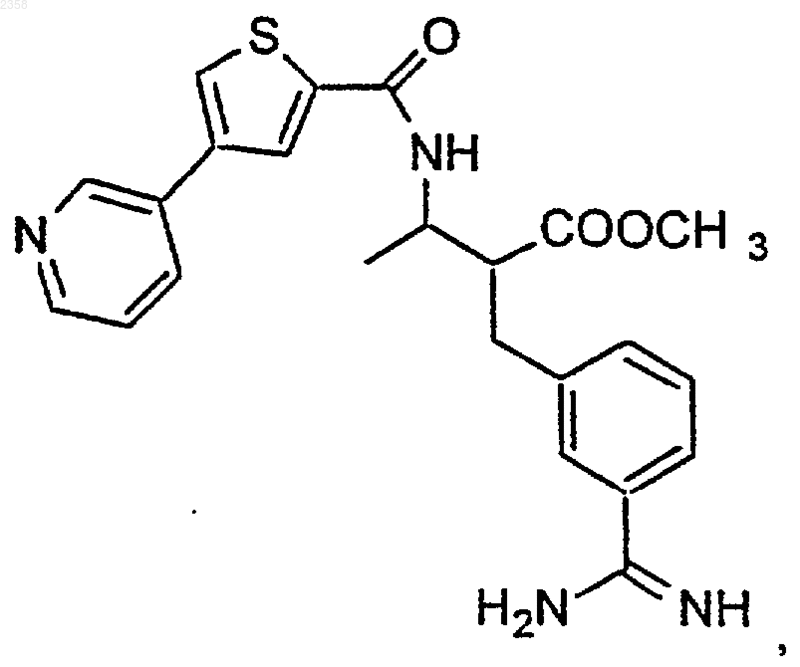
или его фармацевтически приемлемая соль, сольват или пролекарство.
48. Соединение по п.1, которое представляет
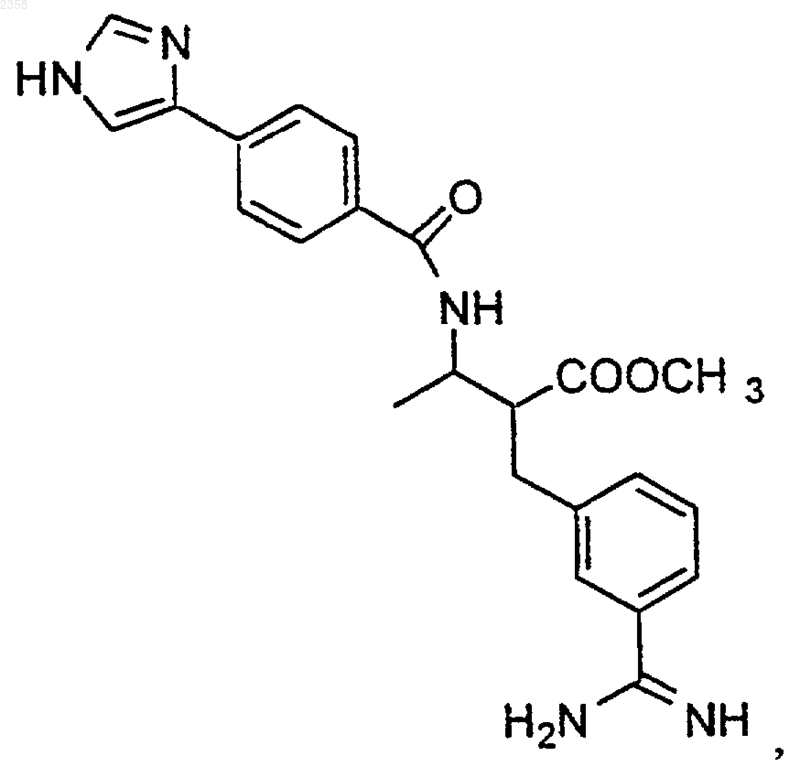
или его фармацевтически приемлемая соль, сольват или пролекарство.
49. Соединение по п.1, которое представляет
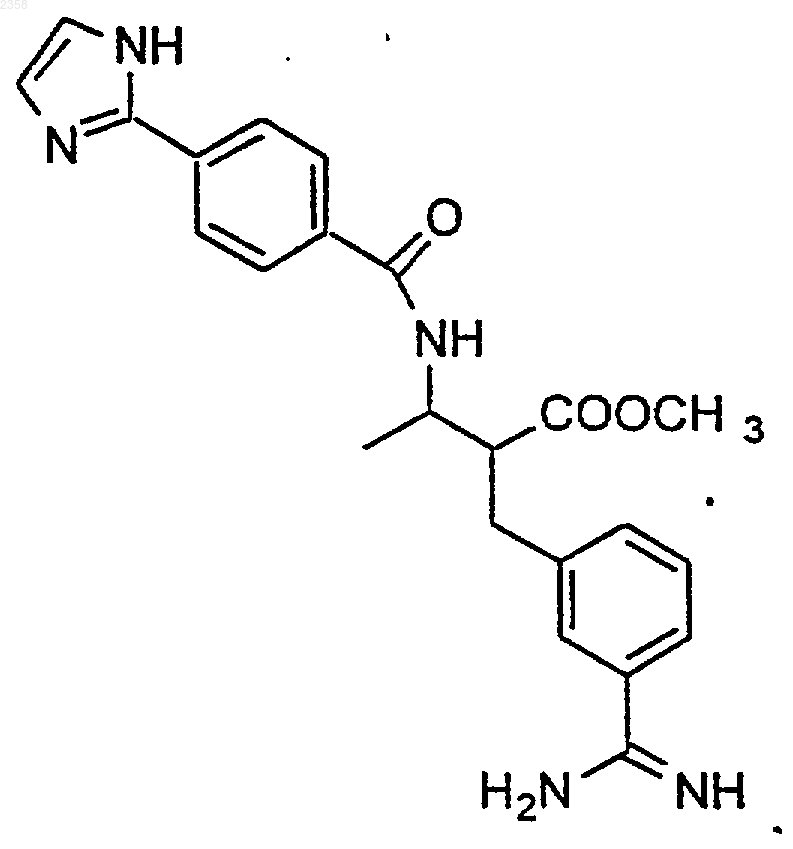
или его фармацевтически приемлемая соль, сольват или пролекарство.
50. Соединение по п.1, которое представляет
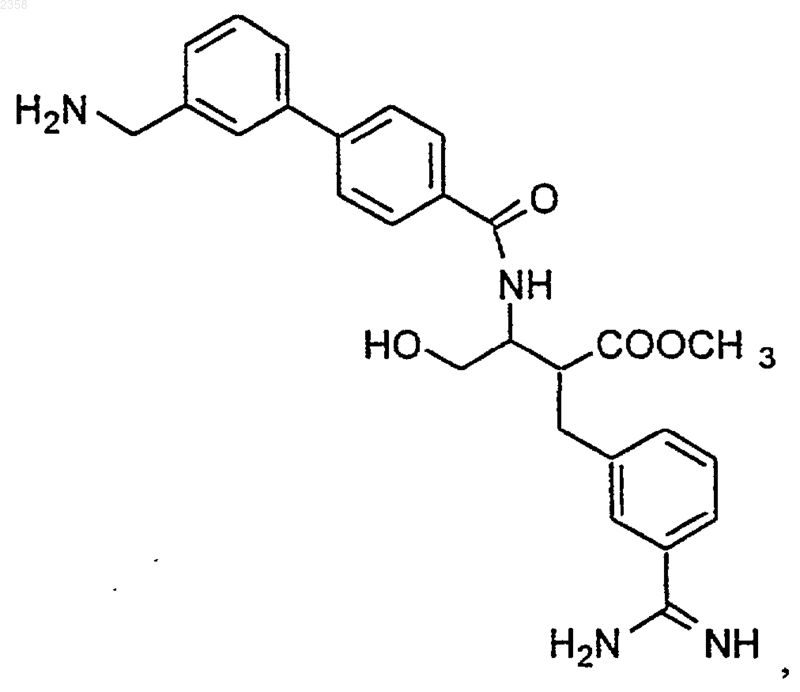
или его фармацевтически приемлемая соль, сольват или пролекарство.
51. Соединение по п.1, которое представляет
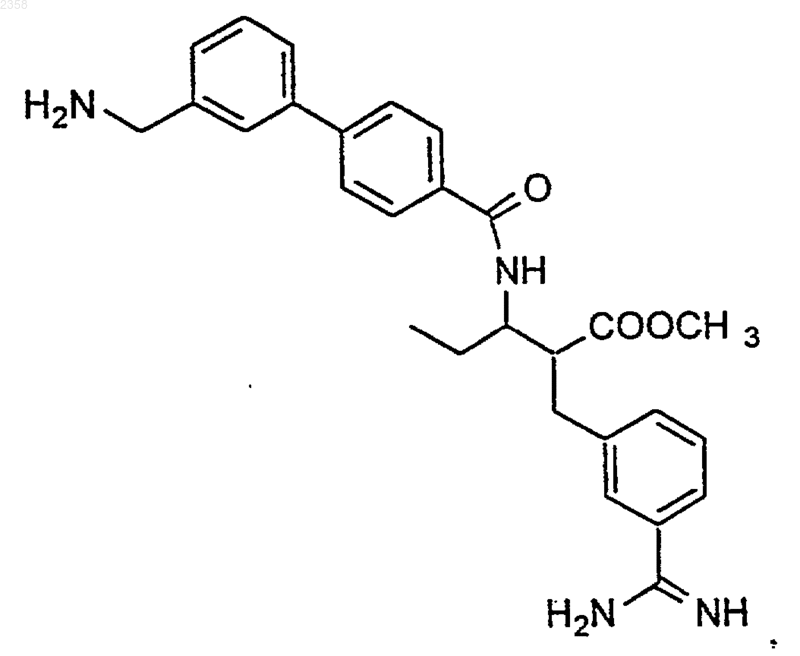
или его фармацевтически приемлемая соль, сольват или пролекарство.
52. Соединение по п.1, которое представляет
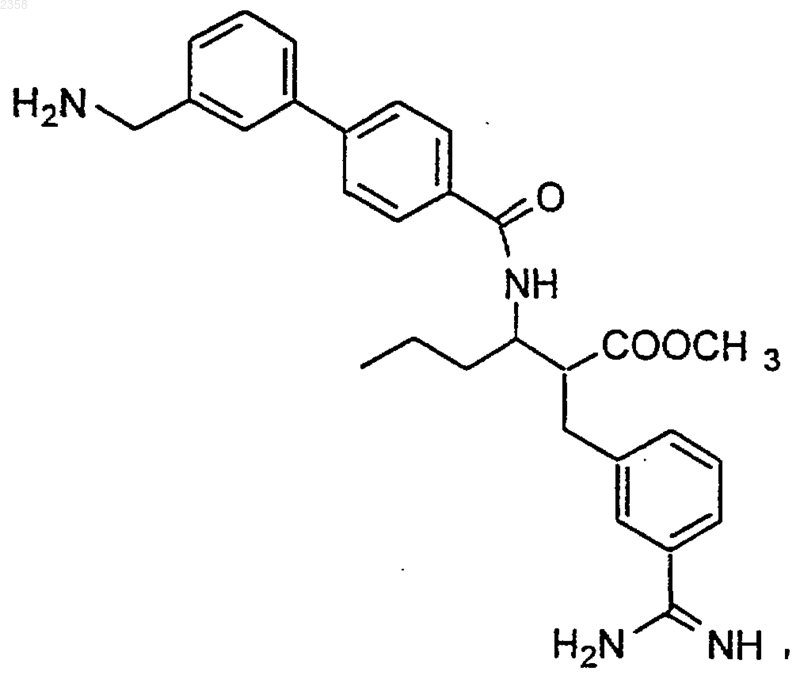
или его фармацевтически приемлемая соль, сольват или пролекарство.
53. Соединение по п.1, которое представляет собой трифторацетат метилового эфира 2(R)-(3-карбамимидоилбензил)-3(R)-[4-(6-оксо-1,6-дигидропиридин-3-ил)бензоиламино]масляной кислоты, или его фармацевтически приемлемая соль, сольват или пролекарство.
54. Соединение по п.1, которое представляет собой метиловый эфир 2(R)-(3-карбамимидоил-6-гидроксибензил)-3(R)-[4-(6-оксо-1,6-дигидропиридин-3-ил)бензоиламино]масляной кислоты, или его фармацевтически приемлемая соль, сольват или пролекарство.
55. Соединение по п.1, которое представляет собой трифторацетат N-[3-(5-карбамимидоил-2-гидроксифенил)пропил]-4-(6-оксо-1,6-дигидропиридин-3-ил)бензамида, или его фармацевтически приемлемая соль, сольват или пролекарство.
56. Соединение по п.1, которое представляет собой трифторацетат (Е)-N-[3-(5-карбамимидоил-2-гидроксифенил)аллил]-4-(6-оксо-1,6-дигидропиридин-3-ил)бензамида, или его фармацевтически приемлемая соль, сольват или пролекарство.
57. Соединение по п.1, которое представляет собой дитрифторацетат (Е)-N-[3-(5-карбамимидоил-2-гидроксифенил)аллил]-4-(1-оксипиридин-4-ил)бензамида, или его фармацевтически приемлемая соль, сольват или пролекарство.
58. Фармацевтическая композиция, включающая фармацевтически приемлемое количество соединения по п.1 и фармацевтически приемлемый носитель.
59. Способ лечения пациента, страдающего от болезненного состояния, которое можно модулировать путем ингибирования продуцирования фактора Ха, включающий введение указанному пациенту фармацевтически эффективного количества соединения по п.1.
60. Способ ингибирования фактора Ха, включающий контактирование ингибирующего фактор Ха количества соединения по п.1 с композицией, содержащей фактор Ха.
61. Способ ингибирования образования тромбина, включающий контактирование ингибирующего фактор Ха количества соединения по п.1 с композицией, содержащей фактор Ха.
Текст
1 Область изобретения Соединения формулы I проявляют полезную фармакологическую активность и соответственно включаются в фармацевтические композиции и используются при лечении пациентов, страдающих некоторыми заболеваниями. Более конкретно, они являются ингибиторами фактора Ха. Настоящее изобретение направлено на соединения формулы I, композиции, содержащие соединения формулы I, и их использование, которые предназначаются для лечения пациентов, страдающих от патологических состояний или подвергшихся состояниям, которые могут быть облегчены путем введения ингибитора фактора Ха. Фактор Ха является предпоследним ферментом в каскаде коагуляции. Как свободный фактор Ха, так и фактор Ха в составе протромбиназного комплекса (фактор Ха, фактор Va,кальций и фосфолипид) ингибируются соединениями формулы I. Ингибирование фактора Ха достигается в результате прямого образования комплекса между ингибитором и ферментом и поэтому не зависит от антитромбина III кофактора плазмы. Эффективное ингибирование фактора Ха достигается путем введения соединений или путем перорального введения, непрерывного внутривенного вливания, внутривенного введения болюса, или любым другим парентеральным путем, так чтобы достигался желаемый эффект предотвращения индуцируемого фактором Ха образования тромбина из протромбина. Терапия антикоагулянтами показана при лечении и профилактике ряда разнообразных тромботических патологических состояний как венозной, так и артериальной сосудистой системы. В артериальной системе аномальное образование тромбов ассоциируется прежде всего с артериями коронарной, церебральной и периферической сосудистой системы. Заболевания,связанные с тромботической окклюзией этих сосудов включают, главным образом, острый инфаркт миокарда (AMI), нестабильную стенокардию, тромбоэмболию, острую закупорку сосудов, связанную с тромболитической терапией и чрескожной транслюминальной коронарной ангиопластикой (РТСА), временные или транзиторные ишемические приступы, удар,перемежающуюся хромоту и обходное шунтирование коронарных (CABG) или периферических артерий. Хроническая антикоагулянтная терапия может быть также благоприятна при предотвращении или профилактике сужения просвета сосудов (рестеноза), которое часто происходит после РТСА и CABG, и при поддержании открытого состояния доступа к сосудам у пациентов при длительном гемодиализе. Что касается венозной сосудистой системы, патологическое образование тромбов часто происходит в венах нижних конечностей после хирургических вмешательств в брюшной полости, 002358DVT в дальнейшем предрасполагает пациента к более высокой степени риска легочной тромбоэмболии. Системная, диссеминированная внутрисосудистая коагулопатия (DIC) обычно происходит в обеих сосудистых системах во время септического шока, некоторых вирусных инфекций и при раке. Это состояние характеризуется быстрым расходом факторов коагуляции и их ингибиторов в плазме в результате образования угрожающих жизни сгустков по всей системе микрососудов некоторых систем органов. Показания для терапии, обсуждаемые выше,включают некоторые, но не все, из возможных клинических ситуаций, когда оправдана терапия антикоагулянтами. Опытные специалисты в данной области осведомлены об обстоятельствах, требующих или острой, или хронической профилактической терапии антикоагулянтами. Краткое изложение изобретения Данное изобретение направлено на соединение формулы I: представляет одинарную или двойную связь;R6 представляет водород или низший алкил;R8 представляет водород или низший алкил;Y1a и Y2a представляют независимо водород или алкил; А и В представляют водород или, взятые вместе, являются связью;Y1 и Y2 представляют независимо водород,алкил, арил или аралкил, или один из Y1 и Y2 представляет ацил или ароил, а другой из Y1 иY2 представляет водород, алкил, арил или аралкил; Аr представляет арил или гетероарил; иn равно 0, 1 или 2; или его фармацевтически приемлемые соль,сольват или пролекарство. Подробное описание изобретения Так как они использованы выше и по всему описанию изобретения, следующие термины,если не указано иное, должны пониматься как имеющие следующие значения. Определения"Алкил"' означает алифатическую углеводородную группу, которая может быть прямой или разветвленной, имеющей примерно от 1 до 15 атомов углерода в цепи. Предпочтительные алкильные группы имеют примерно от 1 до 12 атомов углерода в цепи. Термин "разветвленная"' означает, что одна или более низших алкильных групп, таких как метил, этил или пропил, присоединены к линейной алкильной цепи."Низший алкил" означает наличие примерно от 1 до 6 атомов углерода в цепи, которая может быть прямой или разветвленной. Aлкильная группа может быть замещена одним или более галогенами, циклоалкилами или циклоалкенилами. Примеры алкильных групп включают метил, фторметил, дифторметил, трифторметил,циклопропилметил, циклопентилметил, этил, нпропил, изопропил, н-бутил, трет-бутил, нпентил, 3-пентил, гептил, октил, нонил, децил и додецил."Алкенил" означает алифатическую углеводородную группу, содержащую двойную углерод-углеродную связь, которая может быть прямой или разветвленной, имеющей примерно от 2 до 15 атомов углерода в цепи. Предпочтительные алкенильные группы имеют примерно от 2 до 12 атомов углерода в цепи; и более предпочтительно, примерно от 2 до 6 атомов углерода в цепи."Разветвленная" означает, что одна или более низших алкильных групп, таких как метил, этил или пропил, связаны с линейной алкенильной цепью. "Низший алкенил" означает примерно от 2 до 4 атомов углерода в цепи, которая может быть прямой или разветвленной. Алкенильная группа может быть замещена одним или более атомами галогена. Примеры алкенильных групп включают этенил, пропенил,н-бутенил, изобутенил, 3-метилбут-2-енил, нпентенил, гептенил, октенил и деценил."Алкинил" означает алифатическую углеводородную группу, содержащую тройную углерод-углеродную связь, которая может быть прямой или разветвленной, имеющей примерно от 2 до 15 атомов углерода в цепи. Предпочтительные алкинильные группы имеют примерно от 2 до 12 атомов углерода в цепи; и более предпочтительно, примерно от 2 до 4 атомов углерода в цепи. "Разветвленная" означает, что одна или более низших алкильных групп, таких как метил, этил или пропил, связаны с линейной алкинильной цепью. "Низший алкинил" означает примерно от 2 до 4 атомов углерода в цепи,которая может быть прямой или разветвленной. Примеры алкинильных групп включают этинил,пропинил, н-бутинил, 2-бутинил, 3-метилбутинил, н-пентинил, гептинил, октинил и децинил."Циклоалкил"' означает неароматическую моно- или полициклическую кольцевую систему из примерно от 3 до 10 атомов углерода,предпочтительно из примерно от 5 до 10 атомов углерода. Предпочтительные циклоалкильные кольца содержат примерно от 5 до 6 атомов в кольце. Циклоалкил необязательно замещен одним или более "заместителями кольцевой системы", которые могут быть одинаковыми или различными, и являются такими, как они определены здесь. Примеры моноциклического циклоалкила включают циклопентил, циклогексил, циклогептил и аналогичные. Примеры полициклических циклоалкилов включают 1 декалин, норборнил, адамантил и аналогичные."Циклоалкенил" означает не ароматическую моно- или полициклическую кольцевую систему из примерно от 3 до 10 атомов углерода, предпочтительно из примерно от 5 до 10 атомов углерода, которая содержит, по меньшей мере, одну двойную углерод-углеродную связь. Предпочтительные циклоалкиленовые кольца содержат примерно от 5 до 6 атомов в кольце. Циклоалкенил необязательно замещен одним или более "заместителями кольцевой системы",которые могут быть одинаковыми или различными, и являются такими, как они определены здесь. Примеры моноциклических циклоалкенилов включают циклопентенил, циклогексенил, циклогептенил и аналогичные. Примером полициклического циклоалкенила является норборниленил."Гетероцикленил" означает неароматическую моноциклическую или полициклическую 5 кольцевую систему из примерно от 3 до 10 атомов в кольце, предпочтительно из примерно от 5 до 10 атомов в кольце, в котором один или более из атомов в кольцевой системе является(ются) иными, чем углерод, например, атомами азота, кислорода или серы, и которая содержит,по меньшей мере, одну двойную углеродуглеродную или двойную углерод-азотную связь. Предпочтительные гетероцикленильные кольца содержат примерно от 5 до 6 атомов в кольце. Приставка аза, окса или тиа перед названием "гетероцикленил" означает, что в кольце, соответственно в качестве кольцевого атома присутствует, по меньшей мере, один атом азота, кислорода или серы. Гетероцикленил необязательно замещен одним или более заместителями кольцевой системы, причем заместитель кольцевой системы является таким, как определено здесь. Атом азота или серы гетероцикленила необязательно окислен в соответствующийN-оксид, S-оксид или S,S-диоксид. Примеры моноциклических азагетероцикленильных групп включают 1,2,3,4-тетрагидропиридин, 1,2-дигидропиридил, 1,4-дигидропиридил, 1,2,3,6 тетрагидропиридин,1,4,5,6-тетрагидропиримидин,2-пирролинил,3-пирролинил,2 имидазолинил, 2-пиразолинил и аналогичные. Примеры оксагетероцикленильных групп включают 3,4-дигидро-2 Н-пиран, дигидрофуранил,фтордигидрофуранил и аналогичные. Примером полициклической оксагетероцикленильной группы является 7-оксабицикло[2.2.1]гептенил. Примеры моноциклических тиагетероцикленильных колец включают дигидротиофенил,дигидротиопиранил и аналогичные."Гетероциклил"' означает неароматическую насыщенную моноциклическую или полициклическую кольцевую систему из примерно от 3 до 10 атомов в кольце, предпочтительно из примерно от 5 до 10 атомов в кольце, в котором один или более атомов в кольцевой системе является(ются) иными, чем углерод, например,атомами азота, кислорода или серы. Предпочтительные гетероциклилы содержат примерно от 5 до 6 атомов в кольце. Приставка аза, окса или тиа перед названием гетероциклил означает, что в кольце в качестве кольцевого атома присутствует соответственно, по меньшей мере, один атом азота, кислорода или серы. Гетероциклил необязательно замещен одним или более "заместителями кольцевой системы", которые могут быть одинаковыми или различными, и являются такими, как определены здесь. Атом азота или серы гетероциклила необязательно окислен в соответствующий N-оксид, S-оксид или S,S-диоксид. Примеры моноциклических гетероциклильных колец включают пиперидил,пирролидинил, пиперазинил, морфолинил, тиоморфолинил, тиазолидинил, 1,3-диоксоланил,1,4-диоксанил, тетрагидрофуранил, тетрагидротиофенил, тетрагидротиопиранил и аналогичные."Арил" означает ароматическую моноциклическую или полициклическую кольцевую систему из примерно от 6 до 14 атомов углерода, предпочтительно из примерно от 6 до 10 атомов углерода. Арил необязательно замещен одним или более "заместителями кольцевой системы", которые могут быть одинаковыми или различными и являются такими, как они определены здесь. Примеры арильных групп включают фенил и нафтил."Гетероарил" означает ароматическую моноциклическую или полициклическую кольцевую систему из примерно от 5 до 14 атомов в кольце, предпочтительно из примерно от 5 до 10 атомов в кольце, в котором один или более атомов в кольцевой системе является(ются) атомами иных элементов, чем углерод, например,атомами азота, кислорода или серы. Предпочтительные гетероарилы содержат примерно от 5 до 6 атомов в кольце. "Гетероарил" необязательно замещен одним или более "заместителями кольцевой системы", которые могут быть одинаковыми или различными, и являются такими, как определены здесь. Приставка аза, окса или тиа перед названием "гетероарил" означает,что в кольце в качестве кольцевого атома присутствует соответственно, по меньшей мере,один атом азота, кислорода или серы. Атом азота гетероарила необязательно окислен в соответствующий N-оксид. Примеры гетероарилов включают пиразинил, фуранил, тиенил, пиридил, пиримидинил, изоксазолил, изотиазолил,оксазолил, тиазолил, пиразолил, фуразанил,пирролил,пиразолил,тиазолил,1,2,4 тиадиазолил, пиразинил, пиридазинил, хиноксалинил, фталазинил, имидазо[1,2-а]пиридин,имидазо[2,1-b]тиазолил, бензофуразанил, индолил, азаиндолил, бензимидазолил, бензотиенил,хинолинил, имидазолил, тиенопиридил, хиназолинил, тиенопиримидил, пирролопиридил, имидазопиридил, изохинолинил, бензоазаиндолил,1,2,4-триазинил, бензотиазолил и аналогичные."Сконденсированный арилциклоалкенил" означает радикал, происходящий из сконденсированного арила и циклоалкенила, которому дано определение здесь, получаемый путем удаления атома водорода из циклоалкенильной части. Предпочтительные сконденсированные арилциклоалкенилы представляют собой радикалы, в которых арил является фенилом, а циклоалкенил состоит из примерно 5-6 кольцевых атомов. Сконденсированный арилциклоалкенил необязательно замещен одним или более заместителями кольцевой системы, где "заместитель кольцевой системы" определен здесь. Примеры сконденсированного арилциклоалкенила включают 1,2-дигидронафтилен, инден и аналогичные, в которых связь с основной частью осуществлена через неароматический атом углерода."Сконденсированный циклоалкениларил" означает радикал, происходящий из сконденсированного арилциклоалкенила, определенного 7 здесь, получаемый путем удаления атома водорода из арильной части. Примерами сконденсированного циклоалкениларила являются такие,как описаны здесь для сконденсированного арилциклоалкенила, за исключением того, что связь с основной частью имеет место через ароматический атом углерода."Сконденсированный арилциклоалкил" означает радикал, происходящий из сконденсированного арила и циклоалкила, определенных здесь, путем удаления атома водорода из циклоалкильной части. Предпочтительными сконденсированными арилциклоалкилами являются такие, в которых арил является фенилом, а циклоалкил состоит примерно из 5-6 атомов в кольце. Сконденсированный арилциклоалкил необязательно замещен одним или более заместителями кольцевой системы, причем "заместители кольцевой системы" являются такими, как определены здесь. Пример сконденсированного арилциклоалкила включает 1,2,3,4-тетрагидронафтил и аналогичные, в которых связь с основной частью имеет место через неароматический атом углерода."Сконденсированный циклоалкиларил" означает радикал, происходящий из сконденсированного арилциклоалкила, определенного здесь,путем удаления атома водорода из арильной части. Примерами сконденсированных циклоалкиларилов являются такие, как описаны здесь для сконденсированного арилциклоалкильного радикала, за исключением того, что связь с основной частью имеет место через ароматический атом углерода."Сконденсированный арилгетероцикленил" означает радикал, получаемый из сконденсированного арила и гетероцикленила, определенных здесь, путем удаления атома водорода из гетероцикленильной части. Предпочтительные сконденсированные арилгетероцикленилы являются такими, в которых арил является фенилом, а гетероцикленил состоит из примерно 5-6 атомов в кольце. Приставка аза, окса или тиа перед названием гетероцикленильная часть сконденсированного арилгетероцикленила означает, что в качестве кольцевого атома в кольце присутствует соответственно, по меньшей мере, один атом азота, кислорода или серы. Сконденсированный арилгетероцикленил необязательно замещен одним или более "заместителями кольцевой системы", причем "заместители кольцевой системы" являются такими,как определены здесь. Атом азота или серы гетероцикленильной части сконденсированного арилгетероцикленила необязательно окислен в соответствующий N-оксид, S-оксид или S,Sдиоксид. Примеры сконденсированного арилгетероцикленила включают 3 Н-индолинил, 1 Н-2 оксохинолил,2 Н-1-оксоизохинолил,1,2 дигидрохинолинил, 3,4-дигидрохинолинил, 1,2 дигидроизохинолинил, 3,4-дигидроизохинолинил и аналогичные, в которых связь с основной 8 частью имеет место через не ароматический атом углерода."Сконденсированный гетероциклениларил" означает радикал, получаемый из сконденсированного арилгетероцикленила, определенного здесь, путем удаления атома водорода из арильной части. Примерами сконденсированного гетероциклениларила являются такие, как определены здесь для сконденсированного арилгетероцикленильного радикала, за исключением того, что связь с основной частью осуществлена через ароматический атом углерода."Сконденсированный арилгетероциклил" означает радикал, получаемый из сконденсированного арила и гетероциклила, определенных здесь, путем удаления атома водорода из гетероциклильной части. Предпочтительными сконденсированными арилгетероциклилами являются такие, в которых арил является фенилом, а гетероциклил состоит из примерно 5-6 атомов в кольце. Приставка аза, окса или тиа перед названием гетероциклил означает, что в кольце в качестве кольцевого атома присутствует соответственно, по меньшей мере, один атом азота,кислорода или серы. Сконденсированный арилгетероциклил необязательно замещен одним или более заместителями кольцевой системы,определенными здесь. Атом азота или серы гетероциклильной части сконденсированного арилгетероциклила необязательно окислен в соответствующий N-оксид, S-оксид или S,Sдиоксид. Примеры предпочтительных сконденсированных арилгетероциклильных кольцевых систем включают фталимид, 1,4-бензодиоксан,индолинил, 1,2,3,4-тетрагидроизохинолин, 1,2,3,4-тетрагидрохинолин, 1 Н-2,3-дигидроизоиндолил, 2,3-дигидробенз[f]изоиндолил, 1,2,3,4 тетрагидробенз[g]изохинолинил и аналогичные,в которых связь с основной частью осуществлена через неароматический атом углерода."Сконденсированный гетероциклиларил" означает радикал, получаемый из сконденсированного арилгетероциклила, определенного здесь, путем удаления атома водорода из гетероциклильной части. Примерами предпочтительных сконденсированных гетероциклиларильных кольцевых систем являются такие, как описаны для сконденсированного арилгетероциклила, за исключением того, что связь с основной частью осуществлена через ароматический атом углерода."Сконденсированный гетероарилциклоалкенил" означает радикал, получаемый из сконденсированного гетероарила и циклоалкенила,которые определены здесь, путем удаления атома водорода из циклоалкенильной части. Предпочтительными сконденсированными гетероарилциклоалкенилами являются такие, в которых гетероарил и циклоалкенил, каждый, содержит примерно 5-6 атомов в кольце. Приставка аза,окса или тиа перед названием гетероарил означает, что в качестве кольцевого атома присутст 9 вует соответственно, по меньшей мере, один атом азота, кислорода или серы. Сконденсированный гетероарилциклоалкенил необязательно замещен одним или более заместителями кольцевой системы такими, как определены здесь. Атом азота гетероарильной части сконденсированного гетероарилциклоалкенила необязательно окислен в соответствующий N-оксид. Примеры сконденсированного гетероарилциклоалкенила включают 5,6-дигидрохинолил, 5,6 дигидроизохинолил, 5,6-дигидрохиноксалинил,5,6-дигидрохиназолинил, 4,5-дигидро-1 Н-бензимидазолил, 4,5-дигидробензоксазолил и аналогичные, в которых связь с основной частью осуществлена через неароматический атом углерода."Сконденсированный циклоалкенилгетероарил" означает радикал, получаемый из сконденсированного гетероарилциклоалкенила, определенного здесь, путем удаления атома водорода из гетероарильной части. Примерами сконденсированных циклоалкенилгетероарилов являются такие, как описаны здесь для сконденсированных гетероарилциклоалкенилов, за исключением того, что связь с основной частью осуществлена через ароматический атом углерода."Сконденсированный гетероарилциклоалкил" означает радикал, получаемый из сконденсированного гетероарила и циклоалкила, определенного здесь, путем удаления атома водорода из циклоалкильной части. Предпочтительными сконденсированными гетероарилциклоалкилами являются те, в которых их гетероарил состоит примерно из 5-6 атомов в кольце, и циклоалкил состоит примерно из 5-6 атомов в кольце. Приставка аза, окса или тиа перед названием гетероарил означает, что в качестве кольцевого атома присутствует соответственно,по меньшей мере, один атом азота, кислорода или серы. Сконденсированный гетероарилциклоалкил необязательно замещен одним или более "заместителями кольцевой системы", в которых "заместитель кольцевой системы" является таким, как определен здесь. Атом азота гетероарильной части сконденсированного гетероарилциклоалкила необязательно окислен в соответствующий N-оксид. Примеры сконденсированных гетероарилциклоалкилов включают 5,6,7,8-тетрагидрохинолинил, 5,6,7,8-тетрагидроизохинолил, 5,6,7,8-тетрагидрохиноксалинил,5,6,7,8-тетрагидрохиназолил, 4,5,6,7-тетрагидро 1 Н-бензимидазолил,4,5,6,7-тетрагидробензоксазолил, 1 Н-4-окса-1,5-диазанафталин-2-онил,1,3-дигидроимидизол[4,5]пиридин-2-онил и аналогичные, в которых связь с основной частью осуществлена через неароматический атом углерода."Сконденсированный циклоалкилгетероарил"' означает радикал, получаемый из сконденсированного гетероарилциклоалкила, определенного здесь, путем удаления атома водорода 10 из гетероарильной части. Примерами сконденсированных циклоалкилгетероарилов являются такие, как описаны здесь для сконденсированных гетероарилциклоалкилов, за исключением того, что связь с основной частью осуществлена через ароматический атом углерода."Сконденсированный гетероарилгетероцикленил" означает радикал, получаемый из сконденсированного гетероарила и гетероцикленила, определенных здесь, путем удаления атома водорода из гетероцикленильной части. Предпочтительными сконденсированными гетероарилгетероцикленилами являются такие, в которых их гетероарил состоит примерно из 5-6 атомов в кольце, и гетероцикленил состоит примерно из 5-6 кольцевых атомов. Приставка аза, окса или тиа перед названием гетероарил означает, что в качестве кольцевого атома присутствует соответственно, по меньшей мере,один атом азота, кислорода или серы. Сконденсированный гетероарилгетероцикленил необязательно замещен одним или более "заместителями кольцевой системы", в которых "заместитель кольцевой системы" является таким, как определен здесь. Атом азота гетероарильной части сконденсированного гетероарилгетероцикленила необязательно окислен в соответствующий N-оксид. Атом азота или серы гетероцикленильной части сконденсированного гетероарилгетероцикленила необязательно окислен в соответствующий N-оксид, S-оксид или S,Sдиоксид. Примеры сконденсированных гетероарилгетероцикленилов включают 7,8-дигидро[1,7]нафтиридинил, 1,2-дигидро[2,7]нафтиридинил,6,7-дигидро-3 Н-имидазо[4,5-с]пиридил,1,2-дигидро-1,5-нафтиридинил, 1,2-дигидро-1,6 нафтиридинил, 1,2-дигидро-1,7-нафтиридинил,1,2-дигидро-1,8-нафтиридинил, 1,2-дигидро-2,6 нафтиридинил и аналогичные, в которых связь с основной частью осуществляется через неароматический атом углерода."Сконденсированный гетероцикленилгетероарил" означает радикал, получаемый из сконденсированного гетероарилгетероцикленила,определенного здесь, путем удаления атома водорода из гетероарильной части. Примерами сконденсированных гетероцикленилгетероарилов являются такие, как описаны здесь для сконденсированных гетероарилгетероцикленилов, за исключением того, что связь с основной частью осуществлена через ароматический атом углерода."Сконденсированный гетероарилгетероциклил" означает радикал, получаемый из сконденсированного гетероарила и гетероциклила,определенных здесь, путем удаления атома водорода из гетероциклильной части. Предпочтительными сконденсированными гетероарилгетероциклилами являются такие, в которых их гетероарил состоит примерно из 5-6 кольцевых атомов, и гетероциклил состоит примерно из 5-6 кольцевых атомов. Приставка аза, окса или тиа 11 перед названием гетероарильная или гетероциклильная часть сконденсированного гетероарилгетероциклила означает, что в качестве кольцевого атома присутствует соответственно, по меньшей мере, один атом азота, кислорода или серы. Сконденсированный гетероарилгетероциклил необязательно замещен одним или более"заместитель кольцевой системы" является таким, как определен здесь. Атом азота гетероарильной части сконденсированного гетероарилгетероциклила необязательно окислен в соответствующий N-оксид. Атом азота или серы гетероциклильной части сконденсированного гетероарилгетероциклила необязательно окислен в соответствующий N-оксид, S-оксид илиS,S-диоксид. Примеры сконденсированных гетероарилгетероциклилов включают 2,3-дигидро-1 Н-пиррол[3,4-b]хинолин-2-ил, 1,2,3,4-тетрагидробенз[b][1,7]нафтиридин-2-ил, 1,2,3,4-тетрагидробенз[b][1,6]нафтиридин-2-ил,1,2,3,4 тетрагидро-9 Н-пиридо[3,4-b]индол-2-ил, 1,2,3,4 тетрагидро-9 Н-пиридо[4,3-b]индол-2-ил,2,3 дигидро-1H-пирроло [3,4-b]индол-2-ил, 1 Н 2,3,4,5-тетрагидроазепино[3,4-b]индол-2-ил, 1H2,3,4,5-тетрагидроазепино[4,3-b]индол-3-ил, 1H2,3,4,5-тетрагидроазепино[4,5-b]индол-2-ил,5,6,7,8-тетрагидро[1,7]нафтиридинил,1,2,3,4 тетрагидро[2,7]нафтиридил,2,3-дигидро[1,4] диоксино[2,3-b]пиридил, 2,3-дигидро[1,4]диоксино[2,3-b]пиридил, 3,4-дигидро-2 Н-1-окса[4,6] диазанафталинил,4,5,6,7-тетрагидро-3 Н-имидазо[4,5-с]пиридил, 6,7-дигидро[5,8]диазанафталинил, 1,2,3,4-тетрагидро[1,5]нафтиридинил,1,2,3,4-тетрагидро[1,6]нафтиридинил,1,2,3,4 тетрагидро[1,7]нафтиридинил, 1,2,3,4-тетрагидро[1,8]нафтиридинил,1,2,3,4-тетрагидро[2,6] нафтиридинил и аналогичные, в которых связь с основной частью осуществляется через неароматический атом углерода."Сконденсированный гетероциклилгетероарил" означает радикал, получаемый из сконденсированного гетероарилгетероциклила, определенного здесь, путем удаления атома водорода из гетероарильной части. Примерами сконденсированных гетероциклилгетероарилов являются такие, как описанные здесь для сконденсированных гетероарилгетероциклилов, за исключением того, что связь с основной частью осуществляется через ароматический атом углерода."Аралкил" означает арилалкильную группу, в которой арил и алкил являются такими,как описаны ранее. Предпочтительные аралкилы содержат низшую алкильную часть. Примеры аралкильных групп включают бензил, 2 фенэтил и нафталинметил."Аралкенил" означает арилалкенильную группу, в которой арил и алкенил являются такими, как описаны ранее. Предпочтительные аралкенилы содержат низшую алкенильную 12 часть. Примеры аралкенильных групп включают 2-фенэтенил и 2-нафтилэтенил."Аралкинил" означает арилалкинильную группу, в которой арил и алкинил являются такими, как описаны ранее. Предпочтительные аралкинилы содержат низшую алкинильную часть. Примеры аралкинильных групп включают фенацетиленил и нафтилацетиленил.'"Гетероаралкил" означает гетероарилалкильную группу, в которой гетероарил и алкил являются такими, как описаны ранее. Предпочтительные гетероаралкилы содержат низшую алкильную часть. Примеры аралкильных групп включают пиридилметил, 2-(фуран-3-ил)этил и хинолин-3-илметил."Гетероаралкенил"' означает гетероарилалкенильную группу, в которой гетероарил и алкенил являются такими, как описаны ранее. Предпочтительные гетероаралкенилы содержат низшую алкенильную часть. Примеры гетероаралкенильных групп включают 2-(пирид-3 ил)этенил и 2-(хинолин-3-ил)этенил."Гетероаралкинил" означает гетероаралкинильную группу, в которой гетероарил и алкинил являются такими, как описаны ранее. Предпочтительные гетероалкинилы содержат низшую алкинильную часть. Примеры гетероаралкинильных групп включают пирид-3-илацетиленил и хинолин-3-илацетиленил."Гидроксиалкил" означает НО-алкильную группу, в которой алкил является таким, как описан ранее. Предпочтительные гидроксиалкилы содержат низший алкил. Примеры гидроксиалкильных групп включают гидроксиметил и 2-гидроксиэтил."Ацил" означает Н-СО- или алкил-СОгруппу, в которой алкильная группа является такой, как описана ранее. Предпочтительные ацилы содержат низший алкил. Примеры ацильных групп включают формил, ацетил,пропаноил, 2-метилпропаноил, бутаноил и пальмитоил."Ароил"' означает арил-СО-группу, в которой арильная группа является такой, как описана ранее. Примеры ароильных групп включают бензоил и 1- и 2-нафтоил."Гетероароил" означает гетероарил-СОгруппу, в которой гетероарильная группа является такой, как описана ранее. Примеры групп включают никотиноил и пиррол-2-илкарбонил и 1- и 2-нафтоил."Алкокси" означает алкил-O-группу, в которой алкильная группа является такой, как описана ранее. Примеры алкоксигрупп включают метокси, этокси, н-пропокси, изопропокси,н-бутокси и гептокси."Арилокси"' означает арил-О-группу, в которой арильная группа является такой, как описана ранее. Примеры арилоксигрупп включают фенокси и нафтокси."Аралкилокси"' означает аралкил-Oгруппу, в которой аралкильная группа является 13 такой, как описана ранее. Примеры аралкилоксигрупп включают бензилокси и 1- или 2 нафталинметокси."Алкилтио" означает алкил-S-группу, в которой алкильная группа является такой, как описана ранее. Примеры алкилтиогрупп включают метилтио, этилтио, изопропилтио и гептилтио."Арилтио" означает арил-S-группу, в которой арильная группа является такой, как описана ранее. Примеры арилтиогрупп включают фенилтио и нафтилтио."Аралкилтио" означает аралкил-S-группу,в которой алкильная группа является такой, как описана ранее. Примером аралкилтиогруппы является бензилтио."Y1Y2N-" означает замещенную или незамещенную аминогруппу, в которой Y1 и Y2 являются такими, как описаны ранее. Примеры групп включают амино (Н 2N-), метиламино,этилметиламино, диметиламино и диэтиламино."Алкоксикарбонил" означает алкил-O-СОгруппу. Примеры алкоксикарбонильных групп включают метокси- и этоксикарбонил."Арилоксикарбонил" означает арил-O-СОгруппу. Примеры арилоксикарбонильных групп включают фенокси- и нафтоксикарбонил."Аралкоксикарбонил" означает аралкил-OСО-группу. Примером аралкоксикарбонильной группы является бензилоксикарбонил."Y1Y2NCO-" означает замещенную или незамещенную карбамоильную группу, в которойY1 и Y2 являются такими, как описаны ранее. Примеры карбамоильных групп включают карбамоил (H2NCO-) и диметиламинокарбамоил"Y1Y2NSO2-" означает замещенную или незамещенную сульфамоильную группу, в которой Y1 и Y2 являются такими, как описаны ранее. Характерными группами являются сульфамоил (H2NSO2-) и диметилсульфамоил"Алкилсульфонил" означает алкил-SO2 группу. Предпочтительными группами являются те, в которых алкильная группа представляет низший алкил."Алкилсульфинил" означает алкил-SOгруппу. Предпочтительными группами являются те, в которых алкильная группа представляет низший алкил."Галоген" означает фтор, хлор, бром или иод. Предпочтительными являются фтор, хлор или бром, и более предпочтительными являются фтор или хлор."Заместитель кольцевой системы" означает присоединенный заместитель, который необязательно замещает водород в ароматической или неароматической кольцевой системе. Замести 002358 14 тели кольцевой системы выбираются из группы,состоящей из арила, гетероарила, аралкила,аралкенила, аралкинила, гетероаралкила, гетероаралкенила, гетероаралкинила, гидрокси, гидроксиалкила, алкокси, арилокси, аралкокси,ацила, ароила, галогена, нитро, циано, карбокси,алкоксикарбонила, арилоксикарбонила, аралкоксикарбонила, алкилсульфонила, арилсульфонила, гетероарилсульфонила, алкилсульфинила, арилсульфинила, гетероарилсульфинила,алкилтио, арилтио, гетероарилтио, аралкилтио,гетероаралкилтио, циклоалкила, циклоалкенила,гетероциклила, гетероцикленила, арилдиазо,гетероарилдиазо, амидино, Y1Y2N-, Y1Y2Nалкила, Y1Y2NCO- или Y1Y2NSO2-, где Y1 и Y2 представляют независимо водород, алкил, арил или аралкил, или когда заместитель представляет Y1Y2N- или Y1Y2N-алкил, тогда один из Y1 иY2 представляет ацил или ароил, а другой из Y1 и Y2 является водородом, алкилом, арилом или аралкилом. Когда кольцевая система является насыщенной или частично насыщенной, "заместитель кольцевой системы" дополнительно включает метилен (H2C=), оксо (O=), тиоксо"Сольват" означает физическую ассоциацию соединения данного изобретения с одной или более молекулами растворителя. Данная физическая ассоциация включает различные степени ионной и ковалентной связи, включая водородную связь. В некоторых случаях сольват можно будет выделить, например, когда одна или более молекул растворителей включаются в кристаллическую решетку твердого кристаллического вещества. "Сольват"' охватывает как фазу раствора, так и выделяемые сольваты. Примеры сольватов включают этаноляты, метаноляты и аналогичные. "Гидрат" является сольватом, в котором молекула(ы) растворителя является(ются) Н 2 О."Пролекарство" означает форму соединения формулы I, подходящую для введения пациенту (больному) без недопустимых токсичности, раздражения, аллергических реакций и аналогичных и эффективную для предназначенного его применения, включая кетальные, сложные эфирные и цвиттерионные формы. Пролекарство трансформируется in vivo, давая исходное соединение вышеприведенной формулы, например, путем гидролиза в крови. Полное обсуждение дано в работах Т. Higuchi и V. Stella,Prodrugs as Novel Delivery Systems. Vol. 14 of thePharmaceutical Association and Pergamon Press,1987, обе из которых включены сюда для сведения. Предпочтительные воплощения Предпочтительным воплощением данного изобретения является способ лечения болезненного состояния, способного к модулированию путем ингибирования продуцирования фактора 15 Ха, путем введения пациенту, страдающему от указанного заболевания, эффективного количества соединения формулы I. Предпочтительным аспектом соединения данного изобретения является соединение формулы I, в которой является одинарной связью. Предпочтительным аспектом соединения данного изобретения является соединение формулы I, в которой является двойной связью. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой Ra является водородом. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой Ra представляет гидрокси или амино; более предпочтительно гидрокси. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R1 и R2, взятые вместе, представляют=NR9. Еще одним предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R1 и R2, взятые вместе,представляют =NH. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R3 является водородом. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R3 представляет -СО 2R6, -С(О)R6,-СН 2 ОR7 или -CH2SR7; более предпочтительными являются-CH2SR7; еще более предпочтительны -CO2R6 или -CH2OR7. Еще одним предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R3 представляет -CO2R6 иR6 является низшим алкилом. Еще одним предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R3 представляет -CH2OR7 или -CH2SR7 и R7 является водородом или низшим алкилом. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R4 представляет водород, алкил или Qалкил, или группу формулы Другим предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R4 представляет низший алкил или группу формулы 16 Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R4 представляет Q-алкил. Еще одним предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R4 представляет R7O(низший алкил)-. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R4 представляет тиогетероциклил. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R5 представляет алкинил, циклоалкил,циклоалкенил, гетероциклил, гетероцикленил,сконденсированный арилциклоалкил, сконденсированный гетероарилциклоалкил, сконденсированный арилциклоалкенил, сконденсированный гетероарилциклоалкенил, сконденсированный арилгетероциклил, сконденсированный гетероарилгетероциклил,сконденсированный арилгетероцикленил, сконденсированный гетероарилгетероцикленил,сконденсированный циклоалкениларил, сконденсированный циклоалкиларил, сконденсированный гетероциклиларил, сконденсированный гетероциклениларил,сконденсированный циклоалкилгетероарил,сконденсированный циклоалкенилгетероарил,сконденсированный гетероцикленилгетероарил,сконденсированный гетероциклилгетероарил,аралкил, гетероаралкил, аралкенил, гетероаралкенил, аралкинил или гетероаралкинил; более предпочтительным является сконденсированный циклоалкениларил, сконденсированный циклоалкиларил, сконденсированный гетероциклиларил, сконденсированный гетероциклениларил, сконденсированный циклоалкилгетероарил, сконденсированный циклоалкенилгетероарил, сконденсированный гетероцикленилгетероарил или сконденсированный гетероциклилгетероарил. Еще одним предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R5 представляет циклоалкил, гетероциклил, аралкил или аралкинил. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R5 представляет арил или гетероарил. Другим предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R5 представляет фенил,нафтил или гетероарил. Еще одним предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R5 представляет фенилзамещенный фенил, гетероарил-замещенный фенил, фенил-замещенный гетероарил или гетероарил, необязательно замещенный гетероарилом. Другим предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R6 представляет низший алкил. 17 Еще одним предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R7 представляет водород или низший алкил. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R7 представляет Аr (низший алкил) или гетероароил. Другим предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R8 представляет водород. Следующим предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R9 представляет водород. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой А, В, R8 и R9 представляют водород. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой R10 представляет низший алкил. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой Q представляет R7O-. Предпочтительным аспектом соединения изобретения является соединение формулы I, в которой n равно 1. Другим предпочтительным аспектом соединения изобретения является соединение формулы I, в которой фрагмент находится в мета-положении по отношению к положению присоединения фенильного фрагмента к фрагменту Еще одним предпочтительным аспектом соединения изобретения является соединение формулы I, в которой Ra представляет гидрокси или амино, более предпочтительно, гидрокси,который находится в пара-положении по отношению к фрагменту который находится в мета-положении к положению присоединения фенильного фрагмента к фрагменту Другим предпочтительным аспектом соединения изобретения является соединение формулы I, в которой Аr представляет арил. Еще одним предпочтительным аспектом соединения изобретения является соединение формулы I, в которой Аr представляет фенил. В объем формулы I включены соединения,в которых R1 и R2, взятые вместе, представляют=NR9, где R9 представляет R10O2C-, R10O-, циано, R10CO-, необязательно замещенный низший алкил, нитро или Y1Y2N-. Такие производные сами по себе могут включать биологически активное соединение, полезное для лечения болезненного состояния, способного к модуляции путем ингибирования продуцирования фактора Ха, путем введения пациенту, страдающему от такого заболевания, или которые могут действовать как пролекарства таких биологически активных соединений, которые образуются из них в физиологических условиях. Виды соединений по данному изобретению выбираются из следующих: 30 дитрифторацетат N-[3-(5-карбамимидоил 2-гидроксифенил)пропил]-4-пиперидин-4 илбензамида. Более предпочтительными соединениями по данному изобретению являются соединения 188, 209-211, 213, 217, 231, 276-277, 280-281,297, 300-301, 306, 310, 321, 340 и 342. Должно быть понятно, что данное изобретение охватывает все соответствующие комбинации конкретных и предпочтительных группировок, названных здесь. Соединения формулы I могут быть получены путем применения или приспособления известных методов, под которыми понимаются методы, использованные в прошлом или описанные в литературе, или с помощью методов по данному изобретению. На схеме А приведен пример общего метода получения промежуточных соединений для использования при получении соединений формулы I согласно изобретению. Схема А Схема В дает пример общего способа превращения промежуточных соединений, полученных по схеме А, в соединения формулы I согласно изобретению. Схема С дает пример общего способа осуществления взаимопревращений соединений формулы I согласно изобретению. Схема С На схеме Е приведен пример дополнительного общего способа осуществления взаимопревращений соединений формулы I согласно изобретению. Схема Е Кроме того, соединения формулы I, в которой R3 - гидроксиметил, могут превращаться в соответствующие тиолметильные соединения путем обработки спирта алкил- или арилсульфонилгалогенидом и замещение алкил- или арилсульфоната NaSH, тиометильные соединения могут затем алкилироваться или ацилироваться, давая другие соединения, входящие в объем изобретения. Схема D дает пример общего способа превращения нитрильного промежуточного соединения в соединение формулы I и дополнительных общих способов осуществления взаимных превращений соединений формулы I согласно изобретению. На схеме F приведен пример общего способа получения соединений по данному изобретению, где R4 формулы I является необязательно замещенным фенэтилом. Схема F 33 На схеме G приведен пример общего способа получения соединений по данному изобретению, где R4 формулы I является метилом. На схеме Н приведен пример общего способа получения соединений по данному изобретению. Схема Н На схеме I приведен пример общего способа получения соединений по данному изобретению. Опытным специалистам очевидно ясно,что некоторые соединения формулы I могут проявлять изомерию, например геометрическую изомерию, например изомерию Е или Z, и оптическую изомерию, например иметь R или S конфигурации. Геометрические изомеры включают цис и транс-формы соединений изобретения, имеющих алкенильные заместители. Отдельные геометрические изомеры и стереоизомеры в пределах формулы I, и их смеси входят в объем изобретения. Такие изомеры могут быть выделены из их смесей путем применения или приспособления известных методов, например, хроматографических методик и методик перекристаллизации,или их можно получать отдельно из соответствующих изомеров их промежуточных соединений, например, путем применения или приспособления описанных здесь способов. Соединения данного изобретения полезны в форме свободного основания или кислоты,или в форме их фармацевтически приемлемых солей. Все формы входят в объем изобретения. Когда соединение данного изобретения замещено основным заместителем, образуются соли с присоединением кислоты (кислотноаддитивные соли), и они являются просто более удобной для применения формой; и на практике использование в форме соли по существу равносильно использованию их в форме свободного основания. Кислоты, которые могут использоваться для получения солей с присоединением кислоты, включают предпочтительно те, которые дают при соединении со свободным основанием фармацевтически приемлемые соли, то есть соли, анионы которых нетоксичны для пациента в фармацевтических дозах солей, так что благоприятные эффекты ингибирования или подавления фактора Ха, присущие свободному основанию, не снижаются за счет побочных эффектов, приписываемых анионам. Хотя фармацевтически приемлемые соли указанных основных соединений предпочтительны, все соли с присоединением кислоты полезны в качестве 35 источников формы свободного основания, даже если конкретная соль, сама по себе, желательна только как промежуточный продукт, как, например, когда соль образуется только в целях очистки и идентификации, или когда она используется как промежуточное соединение при получении фармацевтически приемлемой соли путем процедур ионообмена. Фармацевтически приемлемыми солями в объеме изобретения являются соли, которые образуются со следующими кислотами: минеральными кислотами,такими как соляная кислота, серная кислота,фосфорная кислота и сульфаминовая кислота; и органическими кислотами, такими как уксусная кислота, лимонная кислота, молочная кислота,винная кислота, малоновая кислота, метансульфоновая кислота, этансульфоновая кислота,бензолсульфоновая кислота, п-толуолсульфоновая кислота, циклогексилсульфаминовая кислота, хининовая кислота и аналогичные. Соответствующие соли с присоединением кислоты включают следующие: гидрогалогениды, например гидрохлорид и гидробромид, сульфат,фосфат, нитрат, сульфаминат, ацетат, цитрат,лактат, тартрат, малонат, оксалат, салицилат,пропионат, сукцинат, фумарат, малеат, метиленбис-В-гидроксинафтоаты, гентизаты, мезилаты,изотионаты и ди-п-толуоилтартрат, метансульфонат, этансульфонат, бензолсульфонат, птолуолсульфонат, циклогексилсульфаминат и хинат, соответственно. В соответствии с дополнительным признаком изобретения соли с присоединением кислот соединений изобретения получают путем взаимодействия свободного основания с соответствующей кислотой при использовании или приспособлении известных методов. Например,соли соединений изобретения с присоединением кислоты получают или путем растворения свободного основания в водном или водноспиртовом растворе, или в других подходящих растворителях, содержащих соответствующую кислоту, и выделения соли путем выпаривания раствора, или путем взаимодействия свободного основания и кислоты в органическом растворителе, причем в этом случае соль выделяется непосредственно и может быть получена путем концентрирования раствора. Соли соединений изобретения с присоединением кислоты могут быть регенерированы из солей путем применения или приспособления известных методов. Например, основные или исходные формы соединения изобретения могут регенерироваться из их солей с присоединением кислоты путем взаимодействия со щелочью,например, водным раствором бикарбоната натрия или водным раствором аммиака. Когда соединение изобретения замещено кислотным заместителем, могут быть образованы соли с присоединением основания, и они являются просто более удобной формой для использования; и на практике использование в 36 данной форме соли по существу равносильно использованию формы свободной кислоты. Основания, которые могут использоваться для получения солей с присоединением основания,предпочтительно включают основания, которые дают при соединении со свободной кислотой фармацевтически приемлемые соли, то есть соли, катионы которых нетоксичны для организма животного в фармацевтически приемлемых дозах солей, так что благоприятные подавляющие действия на фактор Ха, присущие свободной кислоте, не ослабляются побочным действием,относимым на счет катионов. Фармацевтически приемлемыми солями, включающими, например, соли щелочных и щелочно-земельных металлов, в объеме изобретения являются соли,которые получаются со следующими основаниями: гидридом натрия, гидроксидом натрия,гидроксидом калия, гидроксидом кальция, гидроксидом алюминия, гидроксидом лития, гидроксидом магния, гидроксидом цинка, аммиаком,этилендиамином,N-метилглюкамином, лизином, аргинином, орнитином, холином,N,N'-дибензилэтилендиамином, хлорпрокаином,диэтаноламином,прокаином,N-бензилфенэтиламином, диэтиламином, пиперазином,трис(гидроксиметил)аминометаном, гидроксидом тетраметиламмония и аналогичными. Соли с металлами соединений данного изобретения могут быть получены путем приведения в контакт гидрида, гидроксида, карбоната или подобного им реакционноспособного соединения выбранного металла в водном или органическом растворителе со свободной кислотной формой соединения. Используемый водный растворитель может быть водой или он может быть смесью воды с органическим растворителем, предпочтительно, спиртом, таким как метанол или этанол, кетоном, таким как ацетон, алифатическим простым эфиром, таким как тетрагидрофуран, или сложным эфиром,таким как этилацетат. Такие реакции обычно проводятся при температуре окружающей среды, но они могут проводиться, если желательно,при нагревании. Соли с аминами соединений данного изобретения могут быть получены путем приведения в контакт амина в водном или органическом растворителе со свободной кислотной формой соединения. Подходящие водные растворители включают воду и смеси воды со спиртами, такими как метанол или этанол, простыми эфирами, такими как тетрагидрофуран, нитрилами,такими как ацетонитрил, или кетонами, такими как ацетон. Соли с аминокислотами могут быть получены подобным образом. Соли соединений изобретения с присоединением основания могут регенерироваться из солей путем применения или приспособления известных методов. Например, основные соединения изобретения могут регенерироваться из их солей с присоединением основания путем 37 обработки кислотой, например соляной кислотой. Фармацевтически приемлемые соли также включают четвертичные соли низшего алкиламмония. В соответствии с изобретением четвертичные соли получают путем исчерпывающего алкилирования основных атомов азота в соединениях, включая неароматические и ароматические основные атомы азота, т.е. с помощью алкилирования несвязанной пары электронов азотных компонентов алкилирующим агентом, таким как метилгалогенид, особенно метилиодид или диметилсульфат. Кватернизация приводит к тому, что азотный фрагмент становится положительно заряженным и имеет отрицательный противоион, связанный с ним. Опытному специалисту, по-видимому,вполне очевидно, что некоторые соединения изобретения не образуют стабильных солей. Однако наиболее вероятно, что соли с присоединением кислоты образуются соединениями изобретения, имеющими содержащую азот гетероарильную группу, и/или соединениями, которые содержат в качестве заместителя аминогруппу. Предпочтительными солями с присоединением кислоты соединений изобретения являются соли, у которых нет кислотной лабильной группы. Соли соединений изобретения полезны сами по себе в качестве активных соединений,полезны также и в целях очистки соединений,например, путем использования различий в растворимости между солями и основными соединениями, побочными продуктами и/или исходными материалами с помощью методик, хорошо известных специалистам в данной области. Исходные материалы и промежуточные соединения получают путем применения или приспособления известных методов, например методов, которые описаны в "ссылочных примерах", или их очевидных химических эквивалентов, или с помощью методов по данному изобретению. Данное изобретение далее поясняется, но не ограничивается следующими иллюстративными примерами, в которых показано получение соединений по изобретению. В спектрах ядерного магнитного резонанса(ЯМР) химические сдвиги выражены в м. д. по отношению к тетраметилсилану. Аббревиатуры имеют следующие значения: с = синглет; д = дублет; т = триплет; м = мультиплет; дд = дублет дублетов; ддд = дублет дублетов дублетов; дт = дублет триплетов; ш = широкий. Пример 1. Соединение 1. 38 безводного ТГФ в атмосфере азота при комнатной температуре добавляют метил(трифенилфосфоранилиден)ацетат (61,2 г; 183 ммоль). Смесь оставляют перемешиваться в течение ночи при комнатной температуре и затем концентрируют в вакууме. Неочищенный остаток хроматографируют (40% ЕtOАС:гексан) с получением 27,3 г (96%) акрилата 1. 1 К перемешиваемому раствору соединения 1 (27,33 г) в 150 мл EtOH добавляют 2 г 10%Pd/СаСО 3. Полученную смесь гидрируют при 45 фунт/дюйм 2 (3,1.105 н/м 2, 3,07 атм) H2 в шейкере Парра в течение 8 ч при комнатной температуре. Смесь затем фильтруют через слой целита и концентрируют в вакууме с получением 26,93 г К перемешиваемому раствору соединения 2 (16,8 г; 89 ммоль) в 200 мл ТГФ:МеОН (2:1) по каплям при комнатной температуре добавляют 9 мл 10 N NaOH. Через 2 ч большую часть растворителя удаляют в вакууме и добавляют 30 мл 5 N НСl. Полученную смесь экстрагируют несколько раз EtOAC. Объединенные экстракты сушат (MgSO4), фильтруют и концентрируют с получением 9,8 г (63%) чистой кислоты 3 в виде белого твердого вещества. 1 К перемешиваемому раствору карбоновой кислоты 3 (8,2 г; 47 ммоль) и ДМФ (0,5 мл) в безводном CH2Cl2 в атмосфере азота при комнатной температуре по каплям добавляют оксалилхлорид (6,1 мл; 70 ммоль). Через 1 ч выделение газа прекращается и растворитель и избыток оксалилхлорида удаляют в вакууме. Остаток снова растворяют в 100 мл безводного CH2Cl2 и охлаждают до 0 С. Добавляют меркаптопиридин (5,6 г; 50 ммоль) с последующим добавлением триэтиламина (7,9 мл; 56 ммоль). Смеси дают нагреться до комнатной температуры и перемешивают в течение 1 ч. Смесь разбавляютCH2Cl2 и промывают 1 N NaOH. Органический слой сушат (MgSO4), фильтруют и концентрируют. Остаток хроматографируют (элюент = 50% EtOAc:гексан) с получением 5,12 г (84%) тиоэфира 4 в виде желтого масла. 1 Сульфат магния (19,55 г; 162 ммоль) добавляют к перемешиваемому раствору циннамальдегида (10,2 мл; 81 ммоль) и п-анизидина(10 г; 81 ммоль) в 200 мл CH2Cl2 в атмосфере азота при 0 С. Через 4 ч смесь фильтруют и фильтрат концентрируют с получением 18,87 г(98%) иминного соединения 5 в виде золотистокоричневого твердого вещества. 1 К перемешиваемому раствору тиоэфира 5(7 г; 26 ммоль) в безводном CH2Cl2 (120 мл) в атмосфере N2 при -78 С добавляют TiCl4 (26,1 мл, 1 М раствор в CH2CI2). Через 15 мин по каплям добавляют триэтиламин (3,6 мл; 26 ммоль). Полученную смесь оставляют перемешиваться на 1/2 ч при -78 С, а затем по каплям добавляют раствор имина 1 (4,42 г; 19 ммоль в 20 млCH2Cl2). Затем смесь нагревают до 0 С. Через 1,5 ч при этой температуре смесь гасят насыщенным раствором NаНСО 3 и распределяют водой. Органический слой промывают 1NNaOH, сушат (MgSO4) и концентрируют в вакууме. Неочищенный продукт хроматографируют (элюент = 40% EtOAc/гексан) с получением 2,42 г (32%) смеси транс-/цислактамов 6 а и 6b, 5:1, в виде смолы. Преобладающий транс-изомер 6 а: 1H ЯМР К перемешиваемому раствору 6 а, 6b (1,5 г; 3,8 ммоль) в 60 мл ТГФ/СН 3 СN (1/3) при -20 С добавляют раствор нитрата церий-аммония(CAN, 3,13 г; 5,7 ммоль в 10 мл воды). Через 15 мин добавляют еще 1,5 г CAN в 5 мл воды. Еще через 30 мин смесь гасят насыщенным раствором NаНСО 3 и позволяют ей достичь комнатной температуры. Полученную суспензию фильт 002358 40 руют через слой целита, промывают подушку целита несколько раз CH2Cl2 (в общем примерно 200 мл). Слои фильтрата разделяют и органический слой сушат (MgSO4), фильтруют и концентрируют в вакууме. Неочищенный продукт хроматографируют (элюент = 60% ЕtОАс:гексан) с получением 476 мг (43%) чистого транс-изомера 7 а вместе с 85 мг смеси цис 7b и транс-7 а изомеров. Преобладающий транс-изомер 7 а: 1 Н ЯМР К перемешиваемому раствору транс-лактама 7 а в безводном CH2Cl2 в атмосфере азота при комнатной температуре по каплям добавляют триэтиламин (4,04 мл; 29 ммоль). Затем добавляют бифенилкарбонилхлорид (5,05 г; 23,2 ммоль) с последующим добавлением DMAP (50 мг). Через 30 мин смесь разбавляют CH2Cl2 и промывают 1N НСl. Органический слой затем сушат (MgSO4), фильтруют и концентрируют. Неочищенный продукт хроматографируют(2,19 г; 4,7 ммоль) в 50 мл ТГФ при комнатной температуре добавляют по каплям 1N растворNaOH (13,6 мл). Через 2 ч большую часть ТГФ удаляют в вакууме и добавляют 20 мл 1N НСl. Полученную смесь экстрагируют EtOAc. Экстракт сушат (Na2SO4), фильтруют и концентрируют в вакууме. Сырой продукт очищают путем ВЭЖХ с обращенной фазой (СН 3 СN:вода, 0,1%TFA, градиент 40-100) и фракции, содержащие продукт, лиофилизуют с получением 1,1 г (50%) карбоновой кислоты 9 в виде белого твердого вещества. 1 К перемешиваемому раствору карбоновой кислоты 9 (105 мг; 0,22 ммоль) в 3 мл безводного МеОН при комнатной температуре добавляют молекулярное сито (примерно 50 мг). Затем в течение примерно 2 мин пропускают газообразный НСl. Смесь затем оставляют перемешиваться в течение ночи при комнатной температуре и затем концентрируют в потоке N2. Затем к остатку добавляют раствор NН 3 в МеОН (3 мл 7N раствора) и смесь нагревают до кипения с обратным холодильником в течение 1,5 ч, дают остыть и растворитель удаляют в вакууме. Остаток очищают путем ВЭЖХ с обращенной фазой (СН 3 СN:вода:0,1% TFA, градиент 40-100) и фракции, содержащие продукт, лиофилизуют с получением 73 мг (53%) продукта 10 в виде белого твердого вещества. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4, 4-бифенилкарбонилхлорид заменяется на м-толуоилхлорид на стадии лактамного ацилирования. Конечный продукт 13 очищают ВЭЖХ с обращенной фазой(м, 1 Н), 2,8-3 (м, 1 Н), 2,35 (с, 3 Н). Другие соединения, полученные таким же образом с использованием соответствующего исходного материала, включают следующие: Это соединение получают таким же образом, как и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют бензоилхлоридом на стадии лактамного ацилирования. Конечный продукт 11 очищают ВЭЖХ с обращенной фазой Это соединение получают таким же путем,что и соединение 10, выше, исходя из имина 5 и тиоэфира 4, 4-бифенилкарбонилхлорид заменяется на о-толуоилхлорид на стадии лактамного ацилирования. Конечный продукт 12 очищают ВЭЖХ с обращенной фазой Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на 4'-этил-4-бифенилкарбонилхлорид Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют 3',4'-диметокси-4-бифенилкарбонилхлоридом на стадии -лактамного ацилирования. Конечный продукт 15 очищают путем ВЭЖХ с обращенной фазой (СН 3 СN:Н 2O, 0,1% Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 4-(2'-пиpидил)бензоилхлорид. Конечный продукт 16 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2 О, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 4-(3'-пиридил)бензоилхлорид. Конечный продукт 17 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2 О, 0,1% TFA) и лиофилизуют. Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 4-(4'-пиридил) бензоилхлорид. Конечный продукт 18 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2O, 0,1% TFA) и лиофилизуют. 1 Н ЯМР (ДМСО-d6, ) : 9,5 (с, 1 Н), 9,3 (с,1 Н), 9 (д, J=7,6 Гц, 1 Н), 8,2 (с, 4 Н), 7,8 (с, 2 Н),7,5-7,8 (м, 11 Н), 7,4 (д, J=8 Гц, 1 Н), 6,9 (д, J=15 Гц, 1 Н), 6,6 (дд, J=15,6 Гц, 1 Н), 5,2 (дд, J=16,6 Гц, 1 Н), 3,7 (с, 3 Н), 3,4-3,5 (м, 1 Н), 3,2-3,4 (м,1 Н). Пример 19. Соединение 19. Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 2'-мeтил-4-бифeнилкapбoнилxлopид. Конечный продукт 19 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2O, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 3'-метил-4-бифенилкарбонилхлорид. Конечный продукт 20 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2 О, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 2'-метокси-4-бифенилкарбонилхлорид. Конечный продукт 21 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2 О, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 3'-метокси-4-бифенилкарбонилхлорид. Конечный продукт 22 очищают ВЭЖХ с обращенной фазой (CH3CN:H2O, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 2-нафтилкарбонилхлорид. Конечный продукт 23 очищают ВЭЖХ с обращенной фазой Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 1-нафтилкарбонилхлорид. Конечный продукт 24 очищают ВЭЖХ с обращенной фазой Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 3'-этил-4-бифенилкарбонилхлорид. Конечный продукт 25 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2O, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 4'-метокси-4-бифенилкарбонилхлорид. Конечный продукт 26 очищают путем ВЭЖХ с обращенной фазой (СН 3 СN:Н 2O, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 2',4'-димeтoкcи-4-бифeнилкapбoнилxлopид. Конечный продукт 27 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2O, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 2'-этил-4-бифенилкарбонилхлорид. Конечный продукт 28 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2 О, 0,1% TFA) и лиофилизуют. 1 Н ЯМР (ДМСО-d6, ): 9,25 (с, 1 Н), 8,92 (с,1 Н), 8,69 (д, J=8,7 Гц, 1 Н), 7,78 (д, J=9 Гц, 2 Н),7,68-7,08 (м, 15 Н), 6,65 (д, J=15,9 Гц, 1 Н), 6,38 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 4'-метил-4-бифенилкарбонилхлорид. Конечный продукт 29 очищают ВЭЖХ с обращенной фазой (CH3CN:H2O, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 3'-этокси-4-бифенилкарбонилхлорид. Конечный продукт 30 очищают ВЭЖХ с обращенной фазой (CH3CN:H2O, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 4'-этокси-4-бифенилкарбонилхлорид. Конечный продукт 31 очищают путем ВЭЖХ с обращенной фазой (СН 3 СN:Н 2O, 0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 5 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на 2'-этокси-4-бифенилкарбонилхлорид. Конечный продукт 32 очищают ВЭЖХ с обращенной фазой (CH3CN:H2O, 0,1% TFA) и лиофилизуют. 1 К перемешиваемому раствору 2-нафтальдегида (20 г; 0,13 моль) в 200 мл CH2Cl2 при комнатной температуре добавляют п-анизидин(15,8 г; 0,13 моль) с последующим добавлением безводного сульфата магния (16,9 г; 0,14 моль). Через 3,5 ч смесь фильтруют и фильтрат концентрируют в вакууме с получением 31,5 гH ЯМР (CDCl3, ): 8,64 (с, 1 Н), 8,19 (м,2 Н), 7,78-7,98 (м, 3 Н), 7,43-7,56 (м, 2 Н), 7,32 (м,2 Н), 6,96 (м, 2 Н), 3,83 (с, 3 Н). Пример 34. Соединение 34. Получено с использованием транс-3-(2'нафтил)акролеина, п-анизидина и безводного сульфата магния, как описано для соединения 33, выше. 1 Получено с использованием транс-3-(4'бифенил)акролеина, п-анизидина и безводного сульфата магния, как описано для соединения 33, выше. 1 Получено с использованием 4-бифенилкарбоксальдегида, п-анизидина и безводного сульфата магния, как описано для соединения 33, выше. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 33 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на бензоилхлорид. Конечный продукт 37 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2O,0,1% TFA) и лиофилизуют. ЯМР (MeOH-d4, ): 9,01 (д, J=9,4 Гц, 1 Н),7,77-7,98 (м, 6 Н), 7,43-7,67 (м, 9 Н), 5,53 (м, 1 Н), 002358 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 34 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на бензоилхлорид. Конечный продукт 38 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2 О,0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 35 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на бензоилхлорид. Конечный продукт 39 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2O,0,1% TFA) и лиофилизуют. 1 Это соединение получают таким же образом, что и соединение 10, выше, исходя из имина 36 и тиоэфира 4. 4-Бифенилкарбонилхлорид заменяют на стадии -лактамного ацилирования на бензоилхлорид. Конечный продукт 40 очищают ВЭЖХ с обращенной фазой (СН 3 СN:Н 2O,0,1% TFA) и лиофилизуют. 1 К перемешиваемому раствору карбоновой кислоты 9 (980 мг; 2 ммоль) и триэтиламина(0,44 мл; 3,2 ммоль) в безводном ТГФ в атмо 51 сфере N2 при 0 С по каплям добавляют изобутилхлорформиат (0,39 мл; 3 ммоль). Через 15 мин по каплям добавляют раствор боргидрида натрия (153 мг; 4 ммоль в 5 мл воды). Смеси дают подогреться до комнатной температуры. Через 1 ч большую часть ТГФ удаляют в вакууме. Затем добавляют воду и смесь экстрагируют этилацетатом. Объединенные экстракты сушат(МgSO4), фильтруют и концентрируют. Сырой продукт очищают хроматографией (элюент = 35% ЕtOАс:гексан) с получением 720 мг (76%) спирта 41. 1 К перемешиваемому раствору спирта 41(106 мг; 0,22 ммоль) в 3 мл безводного МеОН при комнатной температуре добавляют молекулярное сито (примерно 50 мг) . Затем примерно в течение 2 мин пропускают газообразный НСl. Смесь затем оставляют перемешиваться в течение ночи при комнатной температуре и затем концентрируют в потоке N2. К остатку затем добавляют раствор NH3 в МеОН (3 мл 7N раствора) и смесь нагревают до кипения с обратным холодильником в течение 1,5 ч, дают ей остыть и растворитель удаляют в вакууме. Остаток очищают ВЭЖХ с обращенной фазой К перемешиваемому раствору спиртового соединения (88 мг; 0,2 ммоль) в 2 мл ТГФ:ДМФ 2:1 в атмосфере N2 при 0 С добавляют NaH (15 мг 60% дисперсии; 0,4 ммоль). Через 15 мин добавляют метилиодид (0,02 мл; 0,3 ммоль) и смеси дают подогреться до комнатной температуры. Через 2 ч смесь гасят насыщенным раствором NaHCO3. Большую часть ТГФ удаляют в вакууме и остаток разбавляют водой и экстрагируют CH2Cl2. Объединенные экстракты сушат(Na2SO4), фильтруют и концентрируют. Неочищенный продукт хроматографируют (элюент = 35% ЕtOАс:гексан) с получением 21 мг (23%) продукта 43 вместе с 34 мг регенерированного спирта 41. Через перемешиваемый раствор соединения 43 (20 мг; 0,04 ммоль) в 1,5 мл смеси пиридин:Et3N 2:1 пропускают H2S в течение примерно 1 мин. Смесь оставляют перемешиваться в течение ночи при комнатной температуре и затем концентрируют в потоке N2, и потом собирают в 2 мл CH2Cl2. Добавляют метилиодид (1 мл) и смесь нагревают до кипения с обратным холодильником в течение 1 ч. Растворитель удаляют в вакууме, остаток собирают в 2 мл МеОН и добавляют NH4OAc (30 мг). Полученную смесь нагревают до кипения с обратным холодильником в течение 1 ч и затем дают ей остыть. Растворитель затем удаляют в вакууме и остаток очищают ВЭЖХ с обращенной фазой(0,12 мл; 1,2 ммоль) перемешивают в течение ночи при комнатной температуре. На следующий день добавляют 3 капли пиридина и уксусного ангидрида. На следующий день реакция не завершается и поэтому добавляют 4 мг DMAP. Через 1 ч реакция завершается по ТСХ. Смесь разбавляют CH2Cl2 и промывают 0,1N раствором НСl. Органический слой сушат (MgSO4),фильтруют и концентрируют с получением 520 мг соединения 45. 1H ЯМР (CDCl3, ): 7,98 (д,J=8 Гц, 2 Н), 7,73 (д, J=8 Гц, 2 Н), 7,67 (д, J=8 Гц,2 Н), 7,17-7,58 (м, 12 Н), 6,94 (д, 1 Н), 6,55 (д, J=18 Гц, 1 Н), 6,21 (дд, J=18, 5 Гц, 1 Н), 5,1 (м, 1 Н),4,38 (м, 1 Н), 4,08 (м, 1 Н), 2,68-2,97 (м, 2 Н), 2,51 Соединение 45 превращают в соответствующий амидин 46, используя последовательность сероводород/метилиодид : ацетат аммония, описанную для превращения 43 в 44. Продукт 46 очищают ВЭЖХ с обращенной фазой и выделяют в виде его трифторацетатной соли. 1 Карбоновую кислоту 9 превращают в ее соответствующий амидин 47, используя последовательность сероводород : метилиодид : ацетат аммония, описанную для превращения 43 в 44. Продукт 47 выделяют путем ВЭЖХ с обращенной фазой в виде его трифторацетатной соли. 1 Н ЯМР (MeOH-d4, ): 8 (д, J=9 Гц, 2 Н),7,82 (д, J=9 Гц, 2 Н), 7,22-7,77 (м, 14 Н), 6,73 (д,J=15,8 Гц, 1 Н), 6,4 (дд, J=15,8, 7,9 Гц, 1 Н), 4,95 К перемешиваемому раствору карбоновой кислоты 48 (120 мг; 0,29 ммоль) в 5 мл безводного СН 2 Сl2 в атмосфере N2 при комнатной температуре добавляют триэтиламин (0,05 мл; 0,38 ммоль). По каплям добавляют изопропилхлорформиат (0,38 мл 1 М раствора в толуоле). Через 30 мин добавляют DMAP (18 мг; 0,15 ммоль) и смесь оставляют дополнительно перемешиваться в течение 1,5 ч при комнатной температуре. Затем смесь разбавляют СН 2 Сl2 и промывают 1N НСl. Органический слой затем сушат (МgSO4), фильтруют и концентрируют. Неочищенный продукт хроматографируют(элюент = 40% ЕtOАс : гексан) с получением 44 мг (33%) соответствующего изопропилового эфира. Это соединение затем превращают в соответствующий амидин 49 с помощью процедуры сероводород : метилиодид : ацетат аммония,как описано для превращения 43 в 44. Продукт 49 очищают ВЭЖХ с обращенной фазой и выделяют в виде его трифторацетатной соли. Это соединение получают путем превращения соединения 48 в соответствующий амидин, используя последовательность сероводород:метилиодид:ацетат аммония, описанную для превращения 43 в 44. Продукт 50 очищают ВЭЖХ с обращенной фазой и выделяют в виде его трифторацетатной соли. 1 Н ЯМР (MeOH-d4,): 8,6 (д, J=7,9 Гц, 1 Н), 7,85 (д, J=8 Гц, 2 Н),7,16-7,7 (м, 12 Н), 6,69 (д, J=15,8 Гц, 1 Н), 6,32 Через перемешиваемый раствор карбоновой кислоты 50 (96 мг; 0,18 ммоль) в 3 мл EtOH при комнатной температуре пропускают НСl в течение примерно 3 мин. Смесь оставляют перемешиваться в течение 7 ч при комнатной температуре и затем хранят в холодильнике (0 С) в течение выходных дней. Затем растворитель удаляют в вакууме, а остаток очищают ВЭЖХ с обращенной фазой (ВЭЖХОФ). Продукт 51 выделяют в виде его трифторацетатной соли. 1EtOAC (2 мл) :EtOH (5 мл) гидрируют при 45 фунт/дюйм 2 (3,1 кг/см 2, 3,07 атм) Н 2 в течение 19 ч при комнатной температуре. Затем смесь фильтруют через слой целита и фильтрат концентрируют. Сырой продукт очищают ВЭЖХОФ (СН 3 СN : вода, 0,1% TFA, градиент 10100% CH3CN) и фракции, содержащие продукт,лиофилизуют с получением 21 мг 52.H ЯМР (MeOH-d4, ): 8,27 (д, J=9,3 Гц,1H), 7,83 (м, 2 Н), 7,43-7,65 (м, 7 Н), 7,09-7,27 (м,5 Н), 4,35 (м, 1H), 3,58 (с, 3 Н), 2,95-3,15 (м, 3 Н),2,54-2,75 (м, 2 Н), 1,93 (м, 2 Н). Разделение соединения 10. Рацемическое соединение 10 (примерно 650 мг обнаруженного единственного диастереоизомера с предполагаемым синстереохимическим строением) разделяют на два энантиомера 53 (позже элюируемый изомер) и 54(раньше элюируемый изомер), используя препаративную ВЭЖХ (колонка Chiralpak AD, 50 ммID x 500 мм, 15 микрон). Подвижная фаза представляет собой гептан (А) с 0,1% TFA и изопропанол (В) с 0,1% TFA, изократные 20% А, 80% В (поток = 200 мл/мин). Позже элюируемый изомер выделяется путем концентрирования в вакууме. Выход составляет 180 мг. Было найдено, что % ээ (% ее) энантиомера 53 составляет 100% по аналитической ВЭЖХ (Chiralpak AD). Спектры 1 Н ЯМР 53 и 54 идентичны. 1 Н ЯМР (ДМСО-d6, ): 8,7 (д, J=8,6 Гц,1 Н), 7,92 (д, J=9 Гц, 2 Н), 7,78 (д, J=9 Гц, 2 Н),7,75-7,21 (м, 14 Н), 6,67 (д, J=16,1 Гц, 1 Н), 6,4 Гидрогенизация соединения 53 (позже элюируемый энантиомер) проводится так же,как и для соединения 52, выше, за исключением того, что опускается этилацетат. Продукт очищают ВЭЖХОФ (СН 3 СN:вода, 0,1% TFA, 40100% СН 3 СN) и выделяют продукт 55 в виде трифторацетатной соли. 1 Н ЯМР (MeOH-d4, ) : 8,3 (д, J=9,3 Гц,1 Н), 7,84 (м, 2 Н), 7,07-7,8 (м, 16 Н), 4,37 (м, 1 Н),3,6 (с, 1 Н), 2,97-3,17 (м, 3 Н), 2,57-2,77 (м, 2 Н),1,95 (м, 2 Н). Пример 56. Соединение 56. К раствору NВос-D-фенилаланина (38 ммоль) в 80 мл безводного тетрагидрофурана добавляют N-метилморфолин (38 ммоль) одной порцией с последующим добавлением изобутилхлорформиата (38 ммоль) таким же образом при -20 С. Реакционную смесь перемешивают в течение 10 мин при -20 С и фильтруют в предварительно приготовленный эфирный раствор диазометана (70 ммоль) при 0 С. Полученному раствору дают постоять при 0 С в течение 20 мин. Избыток диазометана разлагают путем добавления по каплям ледяной уксусной кислоты и растворители удаляют в вакууме. Полученное масло растворяют в 150 мл безводного 56 метанола. При перемешивании при комнатной температуре медленно добавляют раствор бензоата серебра (8 ммоль) в 17 мл триэтиламина. Полученную черную реакционную смесь перемешивают в течение 45 мин при комнатной температуре. Метанол удаляют в вакууме и остаток собирают в 700 мл этилацетата. Смесь фильтруют через целит и последовательно промывают бикарбонатом натрия (3 х 150 мл), водой (1 х 150 мл), 1N бисульфатом калия (3 х 150 мл) и насыщенным раствором соли (1 х 150 мл). Органический слой сушат над сульфатом магния, фильтруют, концентрируют в вакууме и очищают флэш-хроматографией (3:1 гексаны : этилацетат). Пример 57. Соединение 57. Соединение 57 получают, применяя процедуру, описанную для соединения 56, делая замену на NBoc-D-аланин. Пример 58. Соединение 58. Соединение 58 получают, применяя процедуру, описанную для соединения 56, делая замену на NBoc-D-гомофенилаланин. Пример 59. Соединение 59. Соединение 59 получают, применяя процедуру, описанную для соединения 56, делая замену на NBoc-D-3-пиридилаланин. Пример 60. Соединение 60. Соединение 60 получают, применяя процедуру, описанную для соединения 56, делая замену на NBoc-D-изолейцин. Пример 61. Соединение 61. Соединение 61 получают, применяя процедуру, описанную для соединения 56, делая замену на NBoc-D-циклогексилаланин. Пример 62. Соединение 62. Раствор соединения 56 (11 ммоль) в 70 мл тетрагидрофурана охлаждают до -78 С и добавляют раствор гексаметилдисилазана лития в тетрагидрофуране (33 ммоль) с помощью шприца с такой скоростью, чтобы температура не повышалась выше -60 С. Реакционную смесь подогревают до -25 С в течение 40 мин и снова 57 охлаждают до -78 С. С помощью шприца добавляют раствор 3-цианобензилбромида (27 ммоль) в 20 мл тетрагидрофурана с такой скоростью, чтобы температура не превышала-60 С. Реакционной смеси позволяют достичь комнатной температуры и перемешивают при комнатной температуре в течение 1 ч. Добавляют 125 мл насыщенного раствора бикарбоната натрия и тетрагидрофуран удаляют в вакууме. Оставшийся материал распределяют между 500 мл этилацетата и 150 мл насыщенного раствора бикарбоната натрия, органическую фазу дополнительно промывают насыщенным раствором бикарбоната натрия (2 х 100 мл) и насыщенным раствором соли, органический слой сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Остаток растирают с 40 мл смеси гексан : этилацетат 4:1. Твердое вещество отфильтровывают и отбрасывают. Фильтрат, содержащий желаемый продукт, концентрируют в вакууме. Пример 63. Соединение 63. Соединение 63 получают по способу, описанному для соединения 62, делая замену на продукт, полученный в примере 57. Пример 64. Соединение 64. Соединение 64 получают по способу, описанному для соединения 62, делая замену на продукт, полученный в примере 58. Пример 65. Соединение 65. Соединение 65 получают по способу, описанному для соединения 62, делая замену на продукт, полученный в примере 59. Пример 66. Соединение 66. Соединение 66 получают по способу, описанному для соединения 62, делая замену на продукт, полученный в примере 60. Соединение 67 получают по способу, описанному для соединения 62, делая замену на продукт, полученный в примере 61. Пример 68. Соединение 68. К раствору соединения 62 (5 ммоль) в 60 ил метиленхлорида добавляют по каплям 20 мл трифторуксусной кислоты при 0 С. Полученный раствор перемешивают в течение 2 ч при 0 С. Растворители удаляют в вакууме и остаток очищают ВЭЖХ с обращенной фазой, используя градиент 30-70% ацетонитрила в воде, содержащей 0,1% трифторуксусной кислоты. Ацетонитрил удаляют в вакууме и оставшийся материал распределяют между насыщенным раствором бикарбоната натрия и этилацетатом. Водный слой экстрагируют дважды этилацетатом и объединенные органические слои сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Пример 69. Соединение 69. Соединение 69 получают по способу, описанному в примере 68, делая замену на продукт,полученный в примере 63. Пример 70. Соединение 70. Соединение 70 получают по способу, описанному в примере 68, делая замену на продукт, полученный в примере 64. Пример 71. Соединение 71. Соединение 71 получают по способу, описанному в примере 68, делая замену на продукт,полученный в примере 65. Соединение 72 получают по способу, описанному в примере 68, делая замену на продукт,полученный в примере 66. Пример 73. Соединение 73. Соединение 73 получают по способу, описанному в примере 68, делая замену на продукт,полученный в примере 67. Пример 74. Соединение 74. Раствор (А): К раствору 11,8 мл нбутиллития в гексанах (19 ммоль) в 13 мл тетрагидрофурана добавляют с помощью шприца по каплям раствор 1-бром-2-фторбензола (19 ммоль) в 2 мл тетрагидрофурана при -78 С. Перемешивание при -78 С продолжают в течение 1 ч. В течение 2 мин при -78 С добавляют раствор хлорида цинка (19 ммоль) в 38 мл тетрагидрофурана. Полученному раствору дают достичь комнатной температуры в течение 40 мин. Раствор (В): К раствору дихлорида бис(трифенилфосфин)палладия (1 ммоль) в 11 мл тетрагидрофурана добавляют диизобутилалюминийгидрид (1 ммоль) в виде раствора в гексане при комнатной температуре с последующим добавлением метилиодбензоата (16 ммоль) одной порцией при комнатной температуре. Раствор (А) добавляют к раствору (В) и реакционную смесь оставляют перемешиваться при комнатной температуре в течение ночи. Реакционную смесь разбавляют 300 мл диэтилового эфира и промывают 1N раствором соляной кислоты (3 х 75 мл) и насыщенным раствором соли. Органический слой сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Пример 75. Соединение 75. Соединение 75 получают по способу, описанному для соединения 74, делая замену на 1 бром-3-фторбензол при получении раствора (А). Пример 76. Соединение 76. 60 Соединение 76 получают по способу, описанному для соединения 74, делая замену на 1 бром-4-фторбензол при получении раствора (А). Пример 77. Соединение 77. Соединение 77 получают по способу, описанному в примере 74, делая замену на 3,4 этилендиоксибромбензол при получении раствора (А). Пример 78. Соединение 78. Соединение 78 получают по способу, описанному в примере 74, делая замену на 3,4 метилендиоксибромбензол при получении раствора (А). Пример 79. Соединение 79. Соединение 79 получают по способу, описанному в примере 74, делая замену на 3,4 диметоксибромбензол при получении раствора Соединение 80 получают по способу, описанному в примере 74, делая замену на 3 цианобромбензол при получении раствора (А). Пример 81. Соединение 81. Газообразный аммиак пропускают (барботируют) через суспензию соединения 80 (24 ммоль) в 200 мл метанола в течение пяти минут. К полученному раствору добавляют родий на двуокиси алюминия (5 г) и суспензию встряхивают при положительном давлении водорода в течение 36 ч. Катализатор отфильтровывают и метанол удаляют в вакууме с получением масла,которое растирают с эфиром и фильтруют. Пример 82. Соединение 82.(1,5 ммоль) в 60 мл диметилформамида перемешивают при комнатной температуре в течение ночи. Раствор разбавляют 800 мл этилацетата и промывают 1N соляной кислотой (3 х 150 мл) и насыщенным раствором соли. Органический слой сушат над сульфатом магния, фильтруют, концентрируют в вакууме и очищают флэш-хроматографией (гексаны:этилацетат 3:2).
МПК / Метки
МПК: A61P 7/02, C07D 213/58, C07C 257/18, A61K 31/216
Метки: замещенные, аминометил)фенил, пропиламиды, n-[(аминоиминометил
Код ссылки
<a href="https://eas.patents.su/30-2358-zameshhennye-n-aminoiminometil-ili-aminometilfenil-propilamidy.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные n-[(аминоиминометил или аминометил)фенил] пропиламиды</a>
Предыдущий патент: Производные бензимидазола.
Следующий патент: Производные эритромицина, способ их получения и их применение в качестве лекарственных средств
Случайный патент: Способ лечения инсульта