Замещенные (сульфиновой кислоты, сульфоновой кислоты, сульфониламино или сульфиниламино) n-[(аминоиминометил) фенилалкил] азагетероциклил-амидные производные
Номер патента: 700
Опубликовано: 28.02.2000
Авторы: Чои-Следески Енг Ми, Мэйсон Джонатан Стивен, Паулс Генри В., Бекер Майкл Р., Чини Дэниел Л., Евинг Вильям Р., Спада Альфред П.
Формула / Реферат
1. Соединение формулы (1)
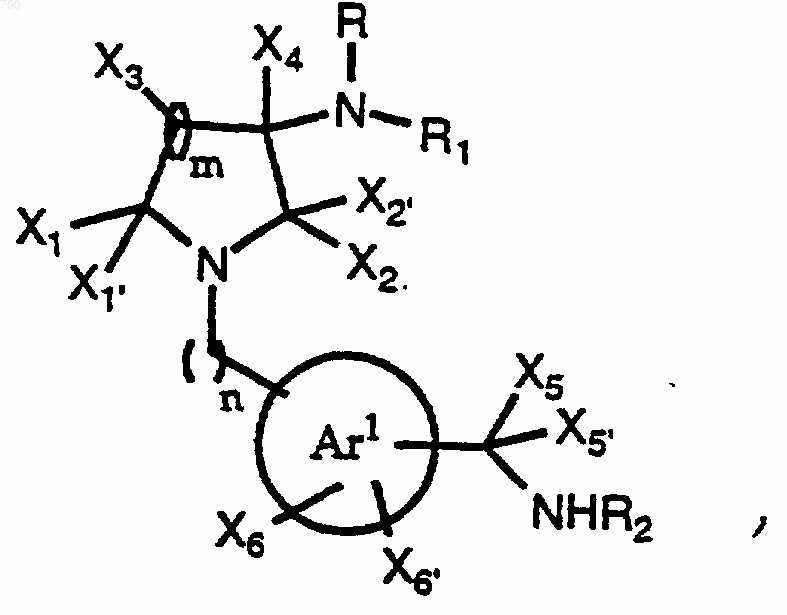

R представляет водород, необязательно замещенный алкил, необязательно замещенный аралкил, необязательно замещенный гетероаралкил или гидроксиалкил;
R1 представляет водород, R3S(O)p или R3R4NS(O)p-;
R2 представляет водород или, когда X5 и Х5', взятые вместе, представляют =NR5, R2 представляет водород, необязательно замещенный низший алкил, необязательно замещенный аралкил или необязательно замещенный гетероалкил;
R3 представляет необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный аралкил, необязательно замещенный гетероаралкил, необязательно замещенный аралкенил или необязательно замещенный гетероаралкенил, или R и R3, взятые вместе, образуют 5-7-членное кольцо; и
R4 представляет необязательно замещенный алкил, необязательно замещенный циклоалкил или необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный аралкил или необязательно замещенный гетероаралкил, или R3 и R4, взятые вместе с атомом азота, к которому R3 и R4 присоединены, образуют необязательно замещенный 4-7-членный гетероциклил;
X1 и Х1' независимо выбраны из водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного аралкила, необязательно замещенного гетероарила, необязательно замещенного гетероаралкила или гидроксиалкила, или X1 и Х1', взятые вместе, образуют оксо;
Х2 и Х2' представляют водород или, взятые вместе, образуют оксо;
Х3 представляет водород, гидрокси, необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный аралкил или необязательно замещенный гетероаралкил или Х3 и один из X1 и Х1', взятые вместе, образуют 4-7-членное кольцо;
Х4 представляет водород, необязательно замещенный алкил, необязательно замещенный аралкил или гидроксиалкил;
X5 и Х5' представляет водород или, взятые вместе, представляют =NR5;
R5 представляет водород, R6O2C-, R6O-, циано, R6CO-, необязательно замещенный низший алкил, нитро или Y1' Y2' N-;
Y1' и Y2' независимо представляют водород, алкил, аралкил или гетероаралкил;
Х6 и Х6' независимо представляют водород, R7R8N-, R9O-, R7R8NCO-, R7R8NSO2-, R9CO-, галоген, циано или нитро;
R6 представляет водород, необязательно замещенный низший алкил, или необязательно замещенный аралкил, или необязательно замещенный гетероаралкил;
R7 и R8 независимо представляют водород или необязательно низший алкил, или один R7 и R8 представляет водород, а другой из R7 и R8 представляет R10(O)CCH2- или низший ацил;
R9 представляет водород, необязательно замещенный низший алкил, низший ацил или R10(O)CCH2-;
R10 представляет водород, необязательно замещенный низший алкил, алкокси или гидрокси;
m представляет 0, 1, 2 или 3
n представляет 1, 2 или 3 или
р представляет 1 или 2,
его фармацевтически приемлемая соль, N-оксид, гидрат или сольват.
2. Соединение по п.1, отличающееся тем, что R3 представляет необязательно замещенный фенил, необязательно замещенный нафтил, необязательно замещенный тиенил или необязательно замещенный бензотиенил.
3. Соединение по п.1, отличающееся тем, что n=1 и m=1.
4. Соединение по п.1, отличающееся тем, что Х2 и Х2', взятые вместе, представляют оксо.
5. Соединение по п.1, отличающееся тем, что X1, Х1', Х3 и Х4 представляют водород.
6. Соединение по п.1, отличающееся тем, что X5 и Х5', взятые вместе, представляют =NH.
7. Соединение по п.1, отличающееся тем, что Х5 и Х5', взятые вместе, представляют =NH5, представляет R6O2C-.
8. Соединение по п.1, отличающееся тем, что

представляет фенил, и углерод, замещенный Х5, X5' и HR2N-, присоединен по положению 3 фенила.
9. Соединение по п.1, отличающееся тем, что

имеет формулу
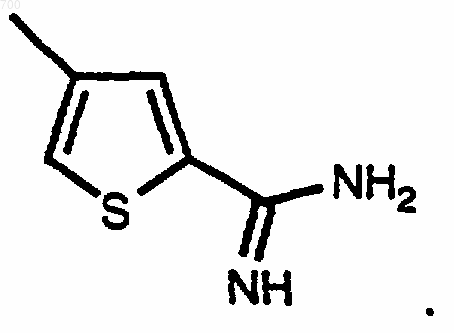
10. Соединение по п.1, отличающееся тем, что X1 представляют водород и Х1' представляет карбоксиалкил, алкоксикарбонилалкил или арил, или X1 и Х1', взятые вместе, образуют оксо.
11. Соединение по п.1, отличающееся тем, что R1 представляет R3SО2-.
12. Соединение по п.1, отличающееся тем, что R1 представляет R3R4NSO2-.
13. Соединение по п.1, отличающееся тем, что один из X6 и X6' представляет амино в параположении относительно радикала
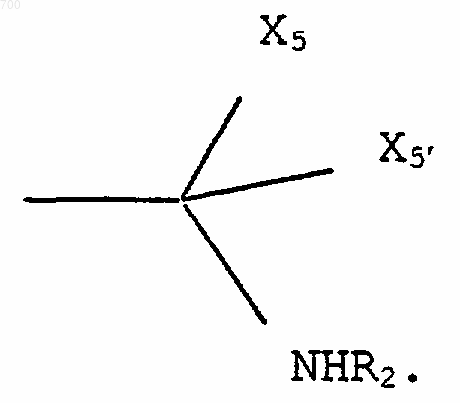
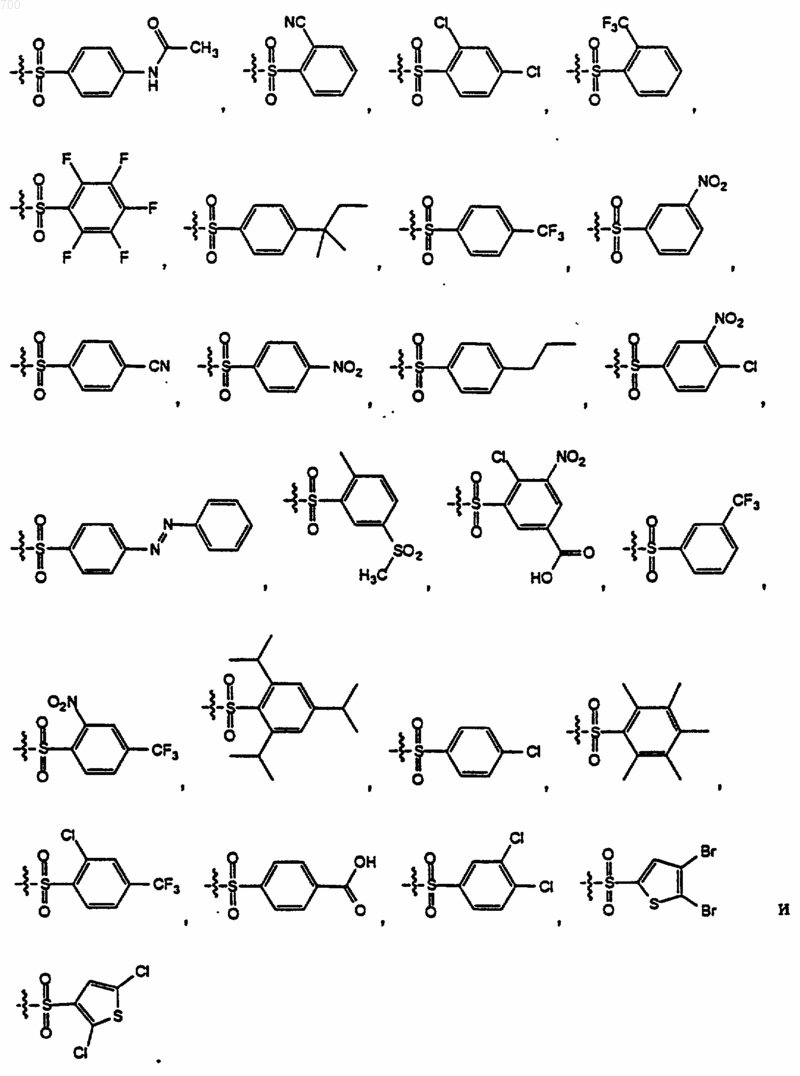
14. Соединение по п.1, отличающееся тем, что представляет собой:
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида нафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-аминоиминометил)бензил]-5-оксопирролидин-3-ил}амида дибензофуран-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида толуол-4-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 3,4-дигидро-1Н-изохинолин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 3'-метоксибифенил-4-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида нафталин-1-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 5-пирид-2-илтиофен-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида бифенил-4-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 7-этоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 5-хлор-6-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 5-хлор-6,7-диметоксинафталин-2-сульфоновой кислоты;
бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 7-аминонафталин-2-сульфоновой кислоты;
трифторацетат {1-[4-(аминоиминометил)бензил]-2-оксопиперидин-3-(S)-ил}амида нафталин-2-сульфоновой кислоты;
трифторацетат [1-(3-аминометилбензил)-2-оксопирролидин-3-(S)-ил]амида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат (1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}метиламида нафталин-2-сульфоновой кислоты;
бистрифторацетрт {1-[3-(аминоиминометил)бензил]пирролидин-3-(S)-ил}амида нафталин-2-сульфоновой кислоты;
трифторацетат{1-[3-(аминоиминометил)бензил]-2,5-диоксопирролидин-3-(S)-ил}амида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопиперидин-3-ил}амида нафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксоазепан-3-(S)-ил}амида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}метиламида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 6-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}метиламида 6-метоксинафталин-2-сульфоновой кислоты;
трифторацетат 2-[{1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил}-6-метоксинафталин-2-сульфониламино]-N-фенетилацетамида;
трифторацетат (1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 9,10-диоксо-8а,9,10, 10а-тетрагидроантрацен-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 8-хлор-7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[4-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 6,7-диметоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида нафто(2,3-d)-(1,3)диоксол-6-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 7-бензилоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 7-гидроксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 6-гидроксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 5-хлор-3-метилбензо[b]тиофен-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}метиламида 5-хлор-3-метилбензо[b]тиофен-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 7-метилнафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 7-этилнафталин-2-сульфоновой кислоты;
бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 5-хлор-6-аминонафталин-2-сульфоновой кислоты;
бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 7-метиламинонафталин-2-сульфоновой кислоты;
бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 2-метил-1,2,3,4-тетрагидроизохинолинил-7-сульфоновой кислоты;
дигидрохлорид {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}метиламида 1,2,3,4-тетрагидроизохинолинил-7-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-(4-нитробензил)амида 7-метоксинафталин-2-сульфоновой кислоты;
бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-(4-аминобензил)амида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-(3-аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил}-(3-нитробензил)амида 7-метоксинафталин-2-сульфоновой кислоты;
бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-(3-аминобензил) амида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-(2-нитробензил)амида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат 3-[2-оксо-3(S)-(2-фенилэтенсульфониламино)пирролидин-1-илметил]бензамидина;
трифторацетат 3-[2-оксо-3(S)-(2-фенилэтансульфониламино)пирролидин-1-илметил]бензамидина;
сложный этиловый эфир [имино-(3-{3-[7-метоксинафталин-2-сульфонилметиламино]-2-оксо-3(S)-пирролидин-1-илметил}фенил)метил]карбаминовой кислоты;
бистрифторацетат 3-[2-оксо-3(S-{2-(пиридин-4-иламино)этансульфониламино}пирролидин-1-илметил]бензамидина;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 2'-метоксибифенил-4-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил)амида 5,6,7,8-тетрагидрофенантрен-3-сульфоновой кислоты;
бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3 (S)-пирролидин-3-ил}амида изохинолинил-5-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}амида 5-хлортиофен-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}амида 2,4-диаминохиназолин-6-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}этиламида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(3-фторбензил) амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат (1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(4-метилбензил)амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(3-метилбензил)амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}нафталин-2-илметиламида 7-метокси-2-нафта-линсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(3-фенилаллил)амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(3-метилбензил)амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(2-фторбензил)амида 7-метокси-2-нафталин-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}метиламида 2-фторбифенил-4-сульфоновой кислоты;
трифторацетат 3-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}-(7-метоксинафталин-2-сульфонил)амино]пропионамида;
трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}нафталин-2-сульфониламино]-N-фенетилацетамида;
трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}бифенил-4-сульфониламино]-N-фенетилацетамида;
трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-фенетилацетамида;
трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-этилацетамида;
трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-7-мeтoкcинaфтaлин-2-cyльфoнилaминo]-N,N-диметилацетамида;
трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-бензилацетамида;
трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-(2-п-толуилэтил)ацетамида;
трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-(3-фенилпропил)ацетамида;
трифторацетат 2-[{1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-(4-метилбензил)ацетамида;
трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-[2-(3-фторфенил) этил]ацетамида;
трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-индан-2-илацетамида;
бистрифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-(2-пиридин-3-илэтил)ацетамида;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3-(S)-пирролидин-3-ил}амида 4,5-дихлортиофен-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3-(S)-пирролидин-3-ил}метиламида 4,5-дихлортиофен-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3-(S)-пирролидин-3-ил}бензиламида 4,5-дихлортиофен-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3-(S)-пирролидин-3-ил}-2-циклопропилфенетиламида 7-метокси-2-нафталин сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 3'-метилбифенил-4-сульфоновой кислоты;
трифторацетат 3-{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-3-ил)-(7-метоксинафталин-2-сульфонил)амино]ацетамида;
трифторацетат 3-{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-3-ил}-(7-метоксинафталин-2-сульфонил)амино]-2-метилацетамида;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксоазетидин-3-(S)-ил}амида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксоазетидин-3-(S)-ил}бензиламида 7-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида 5,6,7,8-тетрагидронафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3-(S)-пирролидин-3-ил}-(2-метоксибензил)амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3-(S)-ил}пирролидин-3-ил}-(3-метоксибензил)амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3-(S)-пирролидин-3-ил}-(4-метоксибензил)амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3-(S)-пирролидин-3-ил}-(пиридин-2-илметил) амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3-(S)-ил}пирролидин-3-ил}(пиридин-3-илметил)амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(пиридин-4-илметил) амида;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3-(S)-пирролидин-3-ил}-(1-бензил-1Н-имидазол-2-илметил) амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}амида(1-метил-1Н-имидазол-2-ил)бензол-4-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}-(3-гидроксибензил) амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(2-гидроксибензил) амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(пиразол-3-илметил) амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида хинолин-6-сульфоновой кислоты;
бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 4-пиридин-4-илбензолсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(тиофен-2-илметил)амида 7-метокси-2-нафталинсульфоновой кислоты;
бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 4-пиридин-3-илбензолсульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида N-метилпирид-4-илфенил-4-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 2-метоксихинолин-7-сульфоновой кислоты;
бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 4-(6-метоксипиридин-2-ил)бензол-4-сульфоновой кислоты;
трифторацетат {1-(3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 4-(3-хлорпиридин-2-илокси)бензол-4-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3(S)-ил}амида 4-(N-оксидопиридин-3-ил)бензол-4-сульфоновой кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 4-феноксибензол-4-сульфоновой кислоты;
трифторацетат (1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(тиофен-3-илметил)амида 7-метокси-2-нафталинсульфоновой кислоты;
трифторацетат {1-[3-(метоксиаминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}метиламида 6-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(цианаминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}метиламида 6-метоксинафталин-2-сульфоновой кислоты;
трифторацетат {1-[3-(гидроксиаминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил}метиламида 6-метоксинафталин-2-сульфоновой кислоты;
дигидрохлорид 4-амино-3-(3-(S)-(метоксинафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]бензамидина;
трифторацетат 4-амино-3-[3-(S)-(7-метоксинафталин-2-сульфонилметиламино)-2-оксопирролидин-1-илметил]бензамидина;
трифторацетат N-(4-карбамимидоил-2-{3-[(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-(S)-илметил}фенил)ацетамида;
трифторацетат 4-амино-3-[3-(S)-(4-трет-бутилбензолсульфониламино)-2-оксопирролидин-1-илметил]бензамидина;
бистрифторацетат 3-амино-5-[3-(S)-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]бензамидина;
трифторацетат сложного метилового эфира {4-(аминоиминометил)-2-[3-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]фенокси}уксусной кислоты;
трифторацетат {4-(аминоиминометил)-2-[3-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]фенокси}уксусной кислоты;
трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 2-хлор-6-нитрофеноксибензолсульфоновой кислоты;
трифторацетат 4-[3-(S)-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина;
трифторацетат 4-{3-(S)-[(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
трифторацетат 2-[[1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил](7-метоксинафталин-2-сульфонил) амино]-ацетамида;
трифторацетат 4-{3-(S)-[(7-метоксинафталин-2-сульфонил)бензиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
трифторацетат 4-{3-(S)-(5-хлор-3-метилбензо[b]тиофен-2-сульфониламино)-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина;
трифторацетат 5-{3-(S)-[(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}тиофен-3-карбоксамидина;
трифторацетат 4-{3-(S)-[(5-хлор-3-метилбензо[b]тиофен-2-сульфонил)бензиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
трифторацетат 4-{3-(S)-[(метансульфонил)-(3-фенилпропил)амино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
трифторацетат 4-{3-(S)-[(метансульфонил)(нафталин-2-ил)амино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
трифторацетат 4-{3-(S)-[(4,5-дихлортиофен-2-сульфонил)бензиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
трифторацетат 4-{3-(S)-[(5-хлор-3-метилбензо[b]тиофен-2-сульфонил)метиламино)-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина;
трифторацетат 2-[[1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил]-(7-метоксинафталин-2-сульфонил) aмино]-N-фенетилацетамида;
трифторацетат 2-[[1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил]-(4,5-дихлортиофен-2-сульфонил)амино]-N-бензилацетамида;
трифторацетат 2-[[1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил]-(7-метоксинафталин-2-сульфонил)амино]-N-бензилацетамида;
трифторацетат 2-[[-1-(4-карбамимидоилтиофен-2-илметил)-2-оксопирролидин-3-(S)-ил]-(7-метоксинафталин-2-сульфонил)амино]-ацетамида;
сложный метиловый эфир 2-[[1-(4-карбамимидоилтиофен-2-илметил)-2-оксопирролидин-3-(S)-ил]-(5-хлор-3-метилбензо[b]тиофен-2-сульфонил)амино] уксусной кислоты;
бистрифторацетат 4-{3-(S)-[(7-аминонафталин-2-сульфонил)бензиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
бистрифторацетат 4-{3-(S)-[(7-аминонафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
бистрифторацетрт 2-([1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил]-(7-аминонафталин-2-сульфонил)амино]-ацетамида;
трифторацетат 4-[3-(S)-(6-амино-5-хлор-2-сульфониламино]-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина;
трифторацетат 4-{3-(S)-[(6-амино-5-хлорнафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
трифторацетат 2-([1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил]-(6-амино-5-хлорнафталин-2-сульфонил) амино]ацетамида;
дигидрохлорид 4-[3-(S)-(6-аминонафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина;
трифторацетат 5-[3-(S)-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина;
трифторацетат 5-{3-(S)-[(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
трифторацетат 5-{3-(S)-[(7-метоксинафталин-2-сульфонил)бензиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
трифторацетат сложного метилового эфира [амино-(4-{3-(S)-(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}тиофен-2-ил) метилен карбаминовой кислоты;
трифторацетат 4-{3-(S)-[(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}тиофен-2-N-гидроксикарбоксамидина;
трифторацетат 4-[3-(S)-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]пиридин-2-карбоксамидина;
трифторацетат 4-{3-(S)-[(7-метоксинафталин-2-сульфонил)бензиламино]-2-оксопирролидин-1-илметил)пиридин-2-карбоксами-дина;
трифторацетат 4-{3-(S)-[(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}пиридин-2-карбоксамидина;
трифторацетат 4-[3-(S)-(5-хлор-3-метилбензо[b]тиофен-2-сульфониламино)-2-оксопирролидин-1-илметил]пиридин-2-карбоксамидина;
трифторацетат 4-{3-(S)-[(5-хлор-3-метилбензо[b]тиофен-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}пиридин-2-карбоксамидина;
трифторацетат 2-{[1-(2-карбамимидоилпиридин-4-илметил)-2-оксопирролидин-3-(S)-ил]-(7-метоксинафталин-2-сульфонил)амино} ацетамида;
трифторацетат 2-{[1-(2-карбамимидоилпиридин-4-илметил)-2-оксопирролидин-3-(S)-ил]-(7-метоксинафталин-2-сульфонил) амино}-N-фенетилацетамида;
трифторацетат 4-{3-(S)-[(7-метоксинафталин-2-сульфонил)тиофен-3-илметиламино]-2-оксопирролидин-1-илметил}пиридин-2-карбоксамидина;
трифторацетат 4-{3-(S)-[(7-метоксинафталин-2-сульфонил)тиофен-3-илметиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина;
трифторацетат 4-{3-(S)-[(4-(6-нитро-2-хлорфенокси) бензолсульфонил)амино]-2-оксопирролидин-1-илметил}тиофен-2-кар-боксамидина;
трифторацетат 5-{3-(S)-[(7-метоксинафталин-2-сульфониламино]-2-оксопирролидин-1-илметил}фуран-2-карбоксамидина; и
трифторацетат 4-[3-(S)-(5-хлор-3-метилбензо[b]тиофен-2-сульфониламино)-2-оксопирролидин-1-илметил]фуран-2-карбоксамидина.
15. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}метиламида 7-метоксинафталин-2-сульфоновой кислоты.
16. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат (1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 3'-метоксибифенилнафталин-4-сульфоновой кислоты.
17. Соединение по п.14, отличающееся тем, что представляет трифторацетат {1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3(S)-ил}амида 5-пирид-2-илтиофен-2-сульфоновой кислоты.
18. Соединение по п.14, отличающееся тем, что представляет трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-пирролидин-3(S)-ил}амида 7-метоксинафталин-2-сульфоновой кислоты.
19. Соединение по п.14, отличающееся тем, что представляет собой бистрифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 7-аминонафталин-2-сульфоновой кислоты.
20. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 5-хлор-3-метилбензо[b]тиофен-2-сульфоновой кислоты.
21. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 2-[{1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-фенетилацетамида.
22. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-бензилацетамида.
23. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 2-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}-7-метоксинафталин-2-сульфониламино]-N-(2-пиридин-3-илэтил)ацетамида.
24. Соединение по по.14, отличающееся тем, что представляет собой трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}амида 4,5-дихлортиофен-2-сульфоновой кислоты.
25. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида 3'-метоксибифенилнафталин-4-сульфоновой кислоты;
26. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 3-[{1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}-(7-метоксинафталин-2-сульфонил)-амино]ацетамида.
27. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксо-3(S)-пирролидин-3-ил}(пиридин-3-илметил)амида 7-метокси-2-нафталинсульфоновой кислоты.
28. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат {1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3(S)-ил}амида хинолин-6-сульфоновой кислоты.
29. Соединение по п.14, отличающееся тем, что представляет собой дигидрохлорид 4-амино-3-[3-(S)-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]-бензамидина.
30. Соединение по п. 14, отличающееся тем, что представляет собой трифторацетат 4-амино-3-[3-(S)-(7-метоксинафталин-2-сульфонилметиламино)-2-оксопирролидин-1-илметил]бензамидина.
31. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 4-амино-3-[3-(S)-(4-трет-бутилбензолсульфониламино) -2-оксопирролидин-1-илметил]-бензамидина.
32. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат сложного метилового эфира {4-(аминоиминометил)-2-[3-(7-метоксинафталин-2-сульфониламино)-оксопирролидин-1-илметил]фенокси}уксусной кислоты.
33. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 4-[3-(S)-(7-метоксинафталин-2-сульфониламино) -2-оксопирролидин-1-илметил]-тиофен-2-карбоксамидинана.
34. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 4-{3-(S)-[(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина.
35. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 2-[[1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил](7-метоксинафталин-2-сульфонил)амино] ацетамида.
36. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 4-[3-(S)-(5-хлор-3-метилбензо[b]тиофен-2-сульфониламино)-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина.
37. Соединение по п. 14, отличающееся тем, что представляет собой трифторацетат 4-{3-(S)-[(5-хлор-3-метилбензо[b]тиофен-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}-тиофен-2-карбоксамидина.
38. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 2-[[1-(5-карбамимидилтиофен-3-илметил)-2-оксопиролидин-3-(S)-ил]-(7-метоксинафталин-2-сульфонил)амино]-N-фенетилацетамида.
39. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат сложного метилового эфира [амино-(4-{3-(S)-(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}тиофен-2-ил)метилен]карбаминовой кислоты.
40. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 4-{3-(S)-[(6-амино-5-хлорнафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина.
41. Соединение по п.14, отличающееся тем, что представляет собой трифторацетрт 4-[3-(S)-(6-амино-5-хлор-2-сульфониламино]-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина.
42. Соединение по п.14, отличающееся тем, что представляет собой бистрифторацетат 4-{3-(S)-[(7-аминонафталин-2-сульфонил) бензиламино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина.
43. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 4-[3-(S)-(7-метоксинафталин-2-сульфониламино) -2-оксопирролидин-1-илметил]пиридин-2-карбоксамидина.
44. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 4-{3-(S)-[(7-метоксинафталин-2-сульфонил)бензиламино]-2-оксопирролидин-1-илметил}пиридин-2-карбоксамидина.
45. Соединение по п.14, отличающееся тем, что представляет собой трифторацетет 2-{[1-(2-карбамимидоилпиридин-4-илметил)-2-оксопирролидин-3-(S)-ил]-(7-метоксинафталин-2-сульфонил)амино}-N-фенетилацетамида.
46. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 4-{3-(S)-[(7-метоксинафталин-2-сульфонил)тиофен-3-илметиламино]-2-оксопирролидин-1-ил-метил}тиофен-2-карбоксамидина.
47. Соединение по п.14, отличающееся тем, что представляет собой трифторацетат 4-{3-(S)-[(4-(6-нитро-2-хлор-фенокси) бензолсульфонил) амино]-2-оксопирролидин-1-илметил}тиофен-2-карбоксамидина.
48. Соединение по п. 1, отличающееся тем, что оно имеет формулу
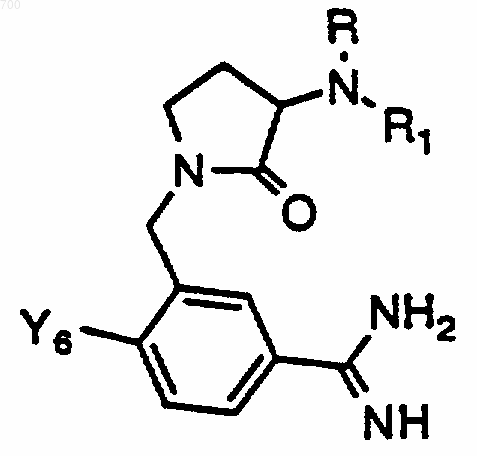
где R представляет водород, метил, аралкил, гетероаралкил, HO2CCH2-, НОС(O)СН2-, H2NC(O)CH2-, (аралкил) HNC(О)СН2- или (гетероаралкил) HNC(O)CH2; X6 представляет водород или амино и R1 выбран из группы формул
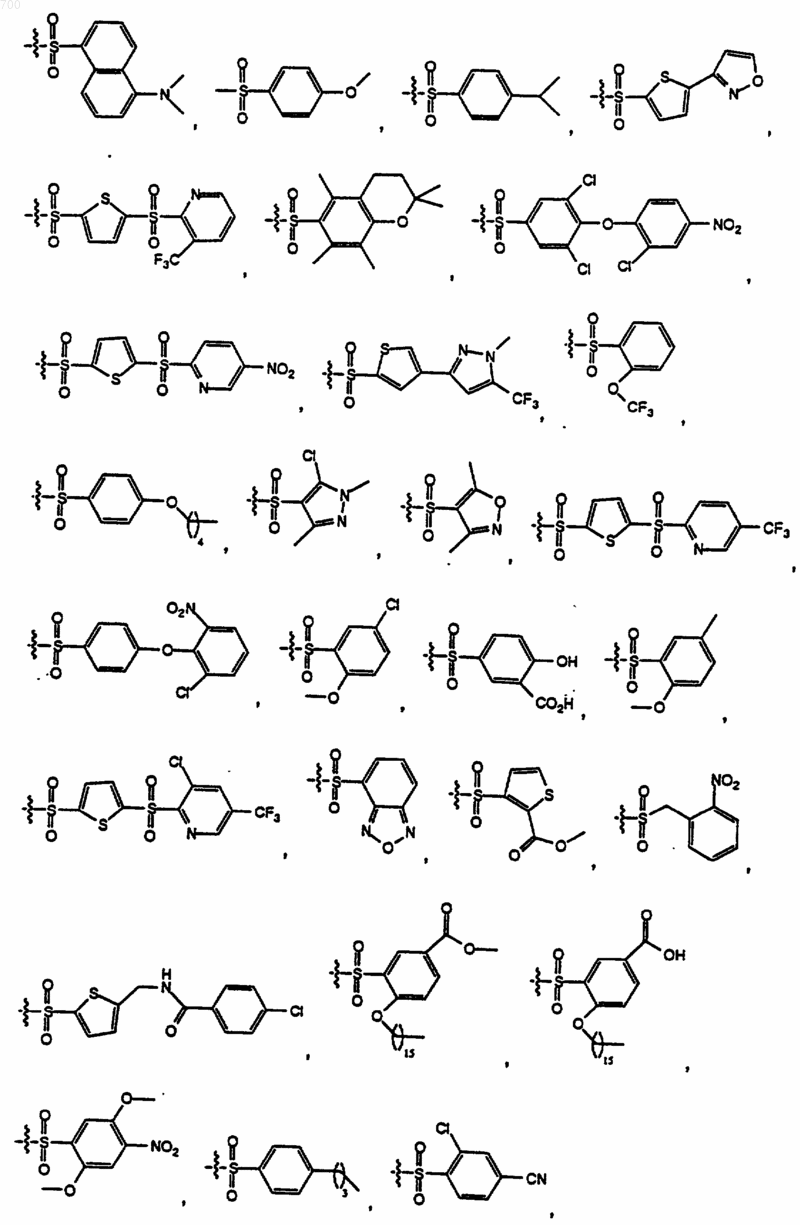
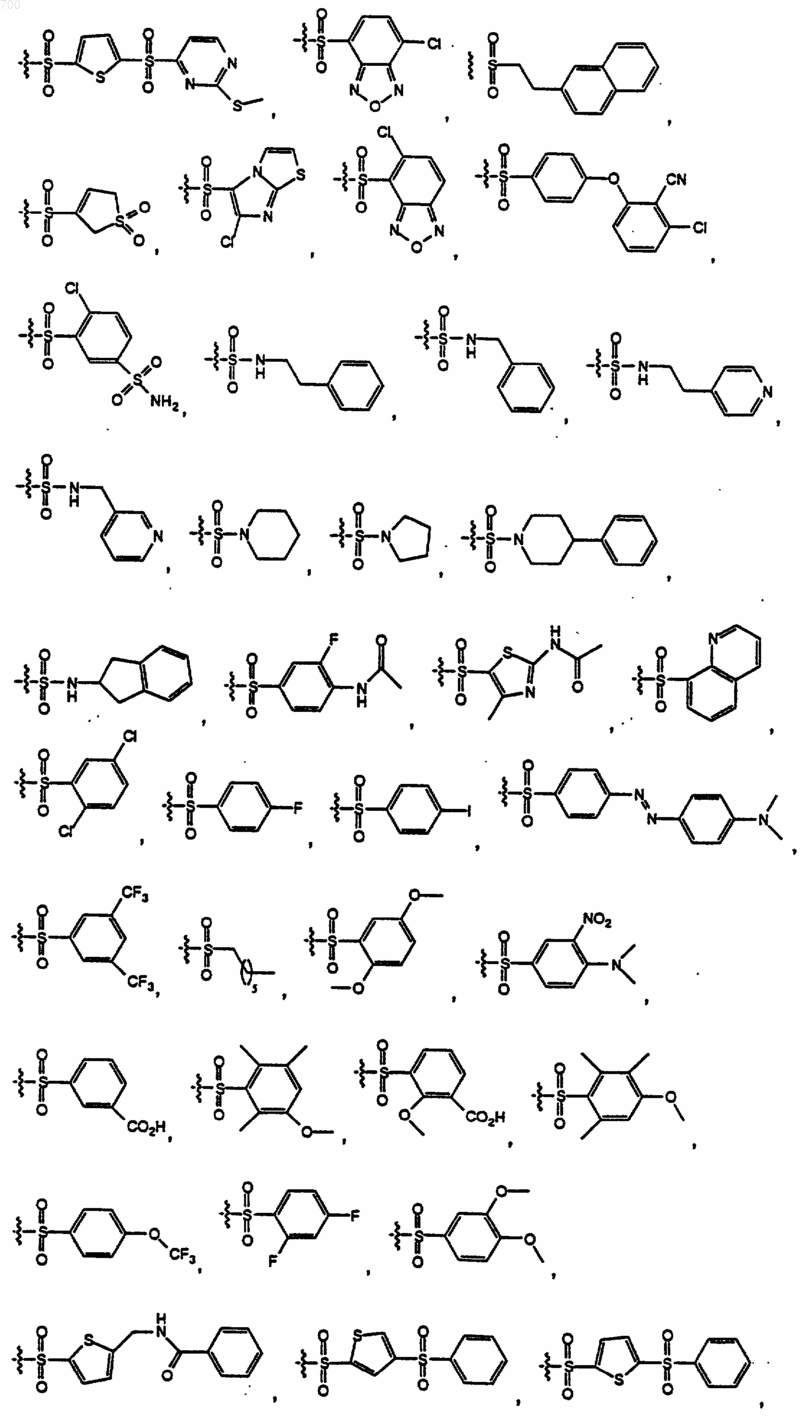
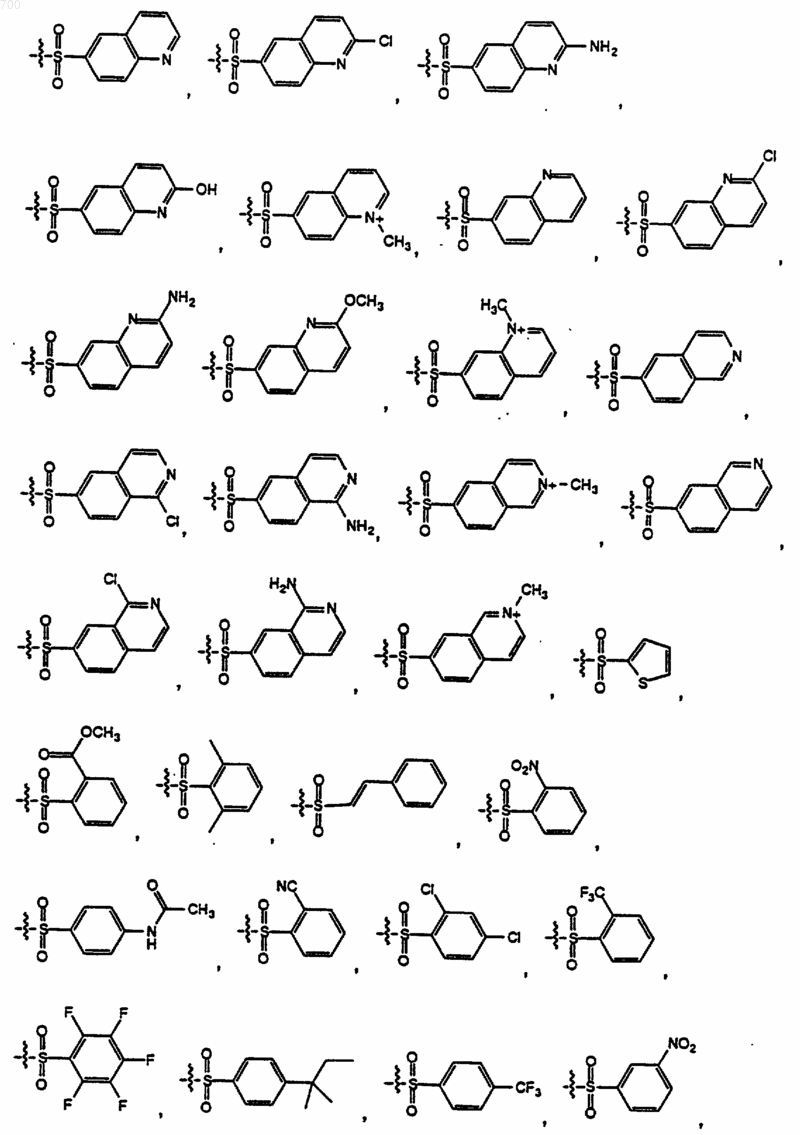
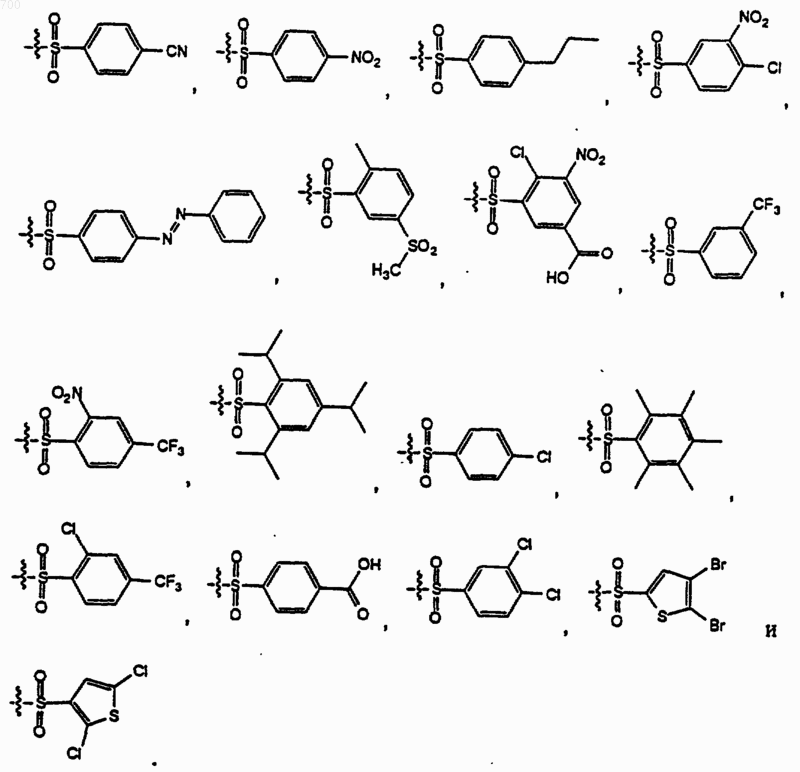
49. Соединение по п. 1 отличающееся тем, что оно имеет формулу
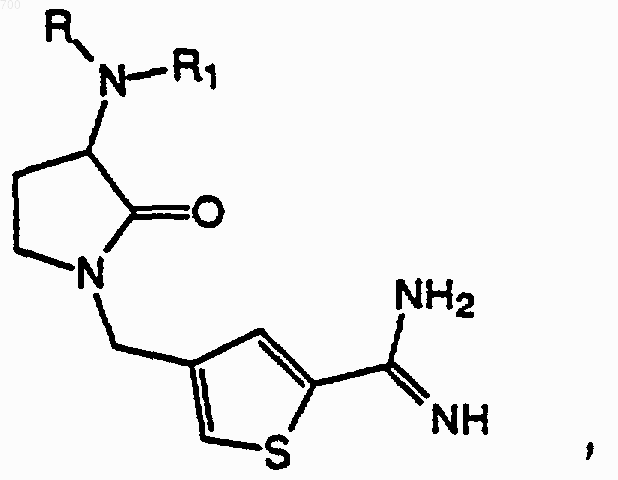
где R представляет водород, метил, аралкил, гетероаралкил, НО2ССН2-, НОС(O)СН2-, H2NC(O)CH2-, (аралкил) НNС(O)СН2- или (гетероаралкил) HNC(O)CH2; и R1 выбран из группы формул
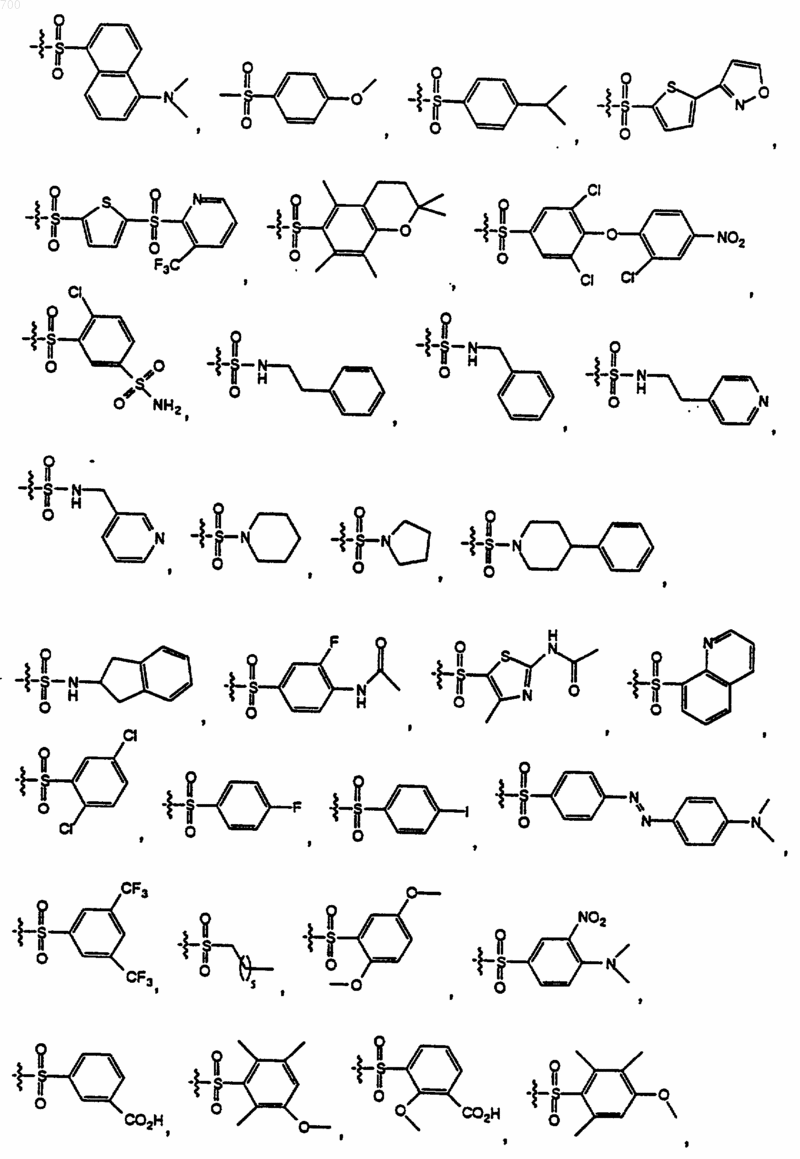
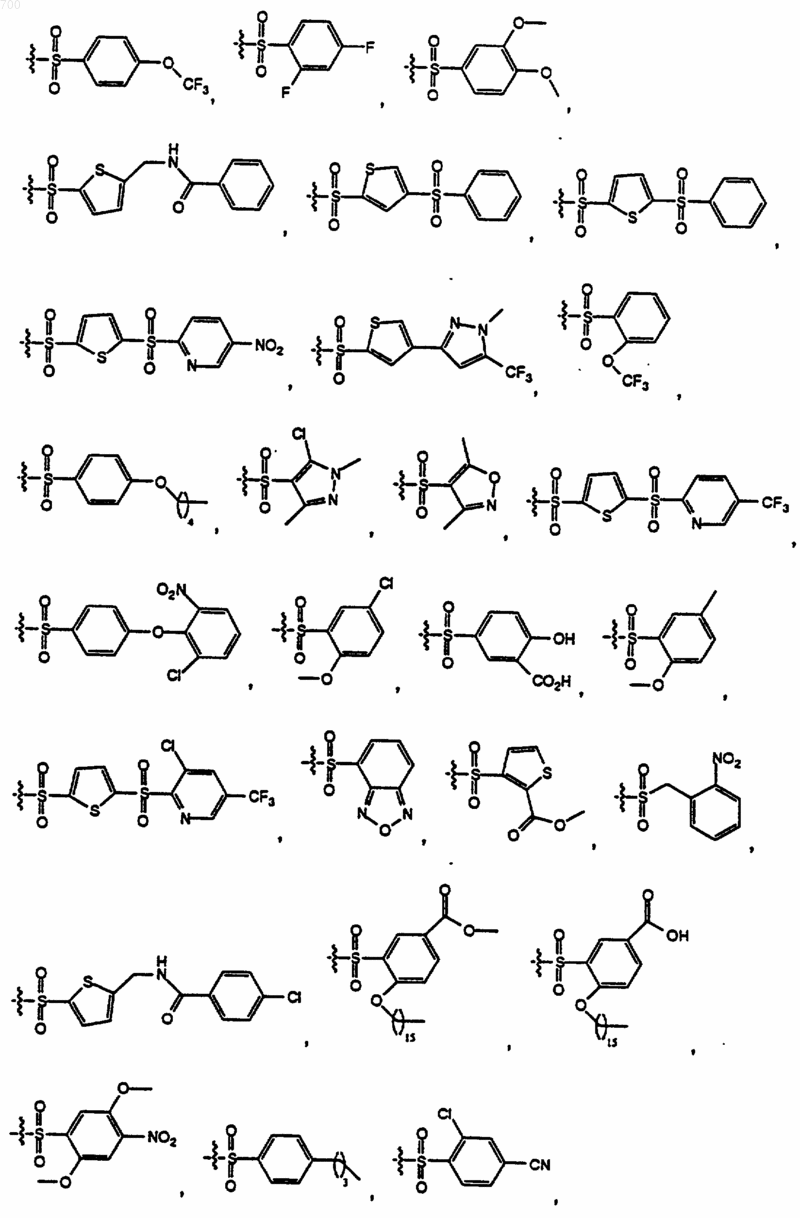
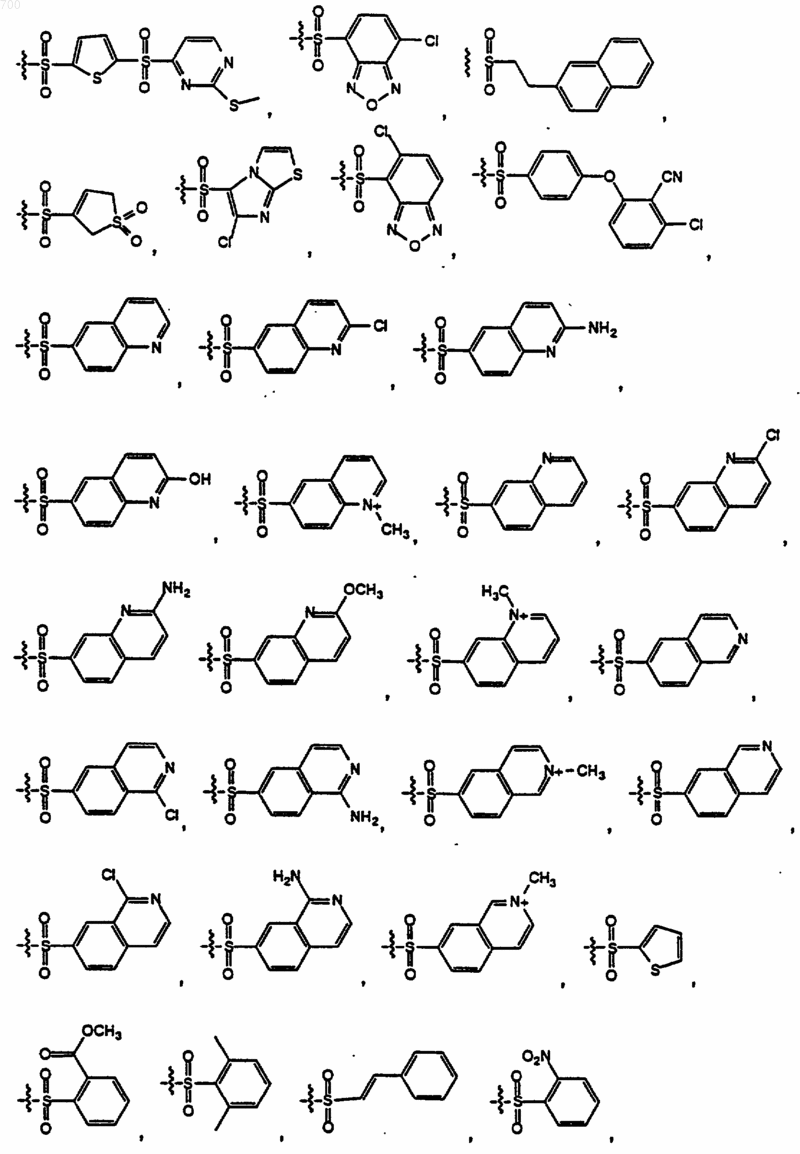
50. Соединение формулы II
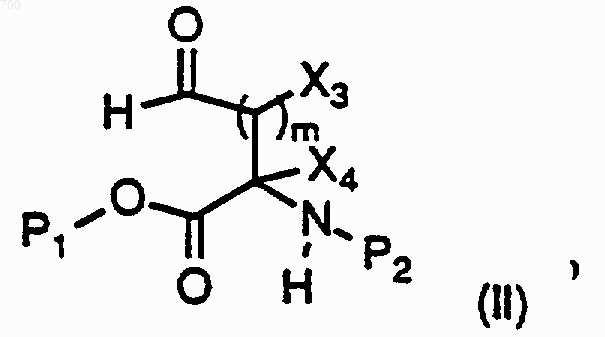
где Х3, Х4 и m такие, как определено в п.1, P1 представляет алкил, аралкил или арил и P2 представляет (алкил, аралкил или арил)карбамат.
51. Соединение формулы
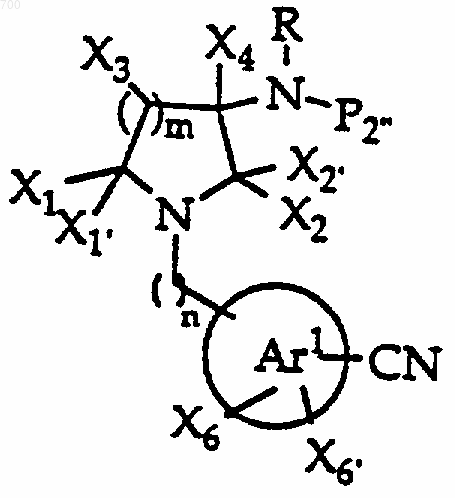
где Ar1, R, X1, X1', X2, X2', Х3, Х4, Х6, X6', m и n такие, как определено в п.1, и Р2 представляет (алкил, аралкил или арил) карбамат или R1 такой, как определенный в п.1.
52. Соединение формулы Х

где Ar1, X1, X1', X2, X2', Х3, Х4, X6, X6', m и n такие, как определено в п.1, и Р2 представляет водород или (алкил, аралкил или арил)карбамат.
53. Соединение формулы XII

где Ar1, X1, X1', X2, X2', Х3, X4, X6, Х6', m и n такие, как определено в п.1, и Р2 представляет (алкил, аралкил или арил)карбамат.
54. Фармацевтическая композиция, содержащая эффективное количество соединения по п.1 и фармацевтически приемлемый носитель.
55. Способ лечения пациента, страдающего от физиологического расстройства, которое можно регулировать ингибированием активности фактора Ха, путем введения терапевтически эффективного количества соединения по п.1.
56. Способ по п.55, в котором физиологическое расстройство представляет собой расстройство венозной сосудистой сети, расстройство артериальной сосудистой сети, патологическое тромбообразование, острый инфакрт миокарда, нестальную стенокардию, тромбоэмболию, острую закупорку сосуда, связанную с тромболитической терапией, чрезкожную внутрипросветную коронарную ангиопластику, преходящие нарушения мозгового кровообращения, удар, перемежающую хромоту или шунтирование коронарных или периферических артерий, сужение просвета сосудов, поддержание раскрытого состояния сосуда у пациентов, проходящих длительный гемодиализ, патологическое тромбообразование, происходящее в венах нижних конечностей после хирургии брюшной полости, колена и бедра, опасность возникновения легочной тромбоэмболии или системную диссеминированную внутрисосудистную коагулопатию, случающуюся в сосудистых системах при септическом шоке, некоторых вирусных инфекциях или раке.
Текст
1 Данная заявка является частичным продолжением заявки 08/481024 на патент США,поданной 7 июня 1995 г. Область техники, к которой относится изобретение Соединения формулы 1 проявляют полезную фармакологическую активность и потом входят в состав фармацевтических композиций и используются при лечении пациентов, страдающих от некоторых медицинских заболеваний. В частности, они являются ингибиторами фактора Ха. Настоящее изобретение относится к соединениям формулы 1, композициям, содержащим соединения формулы 1, и их применению для лечения пациента, страдающего от или подверженного воздействию состояний, которые могут быть улучшены путем введения ингибитора фактора Ха. Фактор Ха является предпоследним ферментом в каскаде свертывания крови. Соединения формулы 1 ингибируют как свободный фактор Ха, так и фактор Ха, входящий в протромбиназный комплекс (фактор Ха, фактор Va,кальций и фосфолипид). Ингибирование фактора Ха обеспечивается непосредственным образованием комплекса между ингибитором и ферментом и, следовательно, не зависит от плазменного кофактора антитромбина 111. Эффективное ингибирование фактора Ха обеспечивают путем введения соединенний перорально,путем непрерывного внутривенного вливания,способом внутривенного болюса или любым другим парентеральнм способом, обеспечивающим требуемый эффект предотвращения инициированного фактором Ха образования тромбина из протромбина. Противосвертывающая терапия показана для лечения и профилактики самых разнообразных тромботических состояний как венозной,так и артериальной сосудистой системы. В артериальной системе патологическое тромбообразование связано, главным образом, с артериями коронарной, церебральной и периферической сосудистых сетей. Заболевания, связанные с тромботической окклюзией этих сосудов, в основном включают острый инфаркт миокарда(AM1), нестабильную стенокардию, тромбоэмболию, острую закупорку сосуда, связанную с тромболитической терапией и чрескожной внутрипросветной коронарной ангиопластикой(РТСА), преходящие нарушения мозгового кровообращения, удар, перемежающуюся хромоту и шунтирование коронарных (САВС) или периферических артерий. Длительная антикоагулянтная терапия может быть также полезной для предотвращения сужения просвета сосудов (рестеноза), часто случающегося после РТСА и CABG, и для поддержания раскрытого состояния сосуда у пациентов, проходящих длительный гемодиализ. Что касается венозной сосудистой сети, то патологическое тромбообразование часто происходит в венах нижних ко 000700 2 нечностей после хирургии брюшной полости,колена и бедра (тромбоз глубоких вен, DVT). К тому же DVT вызывает предрасположенность больного к повышенной опасности возникновения лгочной тромбоэмболии. При септическом шоке, некоторых вирусных инфекциях и раке в обеих сосудистых системах обычно имеет место системная диссеминированная внутрисосудистая коагулопатия (DIC). Это состояние характеризуется быстрым потреблением свертывающих факторов и их плазменных ингибиторов,что приводит к образованию опасного для жизни тромбина по всей капиллярной сосудистой сети некоторых систем органов. Описанные выше показания охватывают некоторые, но не все, возможные клинические ситуации, где обоснована антикоагулянтная терапия. Специалисты в данной области хорошо знают случаи,когда требуется срочная или постоянная профилактическая антикоагулянтная терапия. КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ Настоящее изобретение касается фармацевтического применения соединения 1 для лечения пациента, страдающего от физиологического расстройства, которое может быть уменьшено путем ингибирования активности фактора Ха, где формула 1 является следующей представляет фенил или моноциклический гетероарил;R представляет водород, необязательно замещенный алкил, необязательно замещенный аралкил, необязательно замещенный гетероаралкил или гидроксиалкил;X5', взятые вместе, представляют =NR5, R2 представляет водород, необязательно замещенный алкил, необязательно замещенный аралкил или необязательно замещенный гетероаралкил;R3 представляет необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный аралкил, необязательно замещенный гетероаралкил, необязательно замещенный аралкенил или необязательно замещенный гетероаралкенил или R и R3, взятые вместе, образуют 5-7 членное кольцо; иR4 представляет необязательно замещенный алкил, необязательно замещенный циклоалкил или необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный аралкил или необязательно замещенный гетероаралкил, или R3 и R4, взятые вместе с атомом азота, к которому R3 и R4 присоединены, образуют необязательно замещенный 4-7 членный гетероциклил;X1 и Х 1' независимо выбраны из водорода,необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного аралкила, необязательно замещенного гетероарила, необязательно замещенного гетероаралкила или гидроксиалкила, или X1 и X1',взятые вместе, образуют оксо; Х 2 и Х 2' представляют водород или взятые вместе образуют оксо; Х 3 представляет водород, гидрокси, необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный аралкил или необязательно замещенный гетероаралкил,или Х 3 и один из X1 и Х 1', взятые вместе, образуют 4-7-членное кольцо; Х 4 представляет водород, необязательно замещенный алкил, необязательно замещенный аралкил или гидроксиалкил;X5 и Х 5' представляют водород, или взятые вместе представляют =NR5;R5 представляет водород, R6 О 2 С-, R6O-,циано, R6CO-, необязательно замещенный низший алкил, нитро или Y1'Y2'N-;R6 представляет водород, необязательно замещенный низший алкил или необязательно замещенный аралкил, или необязательно замещенный гетероаралкил;R7 и R8 независимо представляют водород или необязательно замещенный низший алкил или один из R7 и R8 представляет водород, а другой из R7 и R8 представляет R10(О)ССН 2- или низший ацил;R9 представляет водород, необязательно замещенный низший алкил, низший ацил илиR10 представляет водород, необязательно замещенный низший алкил, алкокси или гидрокси; 4 ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ Следует учесть, что при использовании выше, и во всем описании изобретения следующие термины имеют (если не указано иное) следующие значения. Определения Пациент включает как человека, так и других млекопитающих. Алкил означает алифатическую углеводородную группу, которая может быть неразветвленной или разветвленной и имеет от 1 до 20 углеродных атомов в цепи. Предпочтительные алкильные группы имеют от 1 до 12 углеродных атомов в цепи. Разветвленная означает, что к линейной алкильной цепи присоединены одна или несколько алкильных групп, таких как метил, этил или пропил. Низший алкил подразумевает от 1 до 4 углеродных атомов в цепи, которая может быть неразветвленной или разветвленной. Алкил может быть замещенный одним или несколькими заместителями алкильной группы, которые могут быть одинаковыми или разными и включают галоген, циклоалкил, алкокси, амино, ациламино, ароиламино,карбокси, алкоксикарбонил, аралкилоксикарбонил,гетероаралкилоксикарбонил илиY1'Y2'NCO-, где Y1' и Y2' независимо представляют водород, алкил, аралкил или гетероаралкил. Примеры алкильных групп включают метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изопропил, нбутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилэтил,бензилоксикарбонилметил, пиридилметилоксикарбонилметил. Циклоалкил означает неароматическую моно- или полициклическую кольцевую систему, имеющую от 3 до 10 углеродных атомов. Примеры моноциклических циклоалкильных колец включают циклопентил, фторциклопентил, циклогексил и циклогептил. Циклоалкильная группа является необязательно частично незамещенной или необязательно замещенной одной или несколькими группами, выбранными из галогена, метилена(Н 2 С=), алкила, конденсированного арила или конденсированного гетероарила. Примеры полициклических циклоалкильных колец включают 1-декалин, адамант-(1- или 2-) ил и норборнил. Гетероциклил означает неароматическую моноциклическую или полициклическую кольцевую систему, имеющую от 3 до 10 углеродных атомов. Предпочтительные кольца содержат от 5 до 6 кольцевых атомов, причем один из кольцевых атомов является кислородом,азотом или серой. Гетероциклил является необязательно частично незамещенным или необязательно замещенным одной или несколькими группами, выбранными из алкила, галогена,арила, гетероарила, конденсированного арила 5 или конденсированного гетероарила. Примеры моноциклических колец включают пирролидил,пиперидил,тетрагидрофуранил,тетрагидротиенил и тетрагидротиопиранил. Тио- или азотный фрагмент гетероциклила может быть также необязательно окисленным до соответствующего N-оксида, S-оксида или S,S-диоксида. Арил означает ароматический карбоциклический радикал, содержащий от 6 до 10 углеродных атомов. Примеры арила включают фенил или нафтил, или фенил или нафтил, замещенные одним или несколькими заместителями арильной группы, которые могут быть одинаковыми или разными, причем термин заместитель арильной группы включает водород,алкил, арил, гетероарил, аралкил, гетероаралкил, гидрокси, гидроксиалкил, алкокси, арилокси, аралкокси, ацил, ароил, галоген, нитро, циано, карбокси, алкоксикарбонил, арилоксикарбонил, аралкоксикарбонил, ациламино, ароиламино, алкилсульфонил, арилсульфонил, гетероарилсульфонил, алкилсульфинил, арилсульфинил, гетероарилсульфинил, алкилтио, арилтио,гетероарилтио, аралкилтио, гетероаралкилтио,конденсированный циклоалкил, конденсированный гетероциклил, арилазо, ге-тероарилазо,Y1Y2N-, Y1Y2NCO- или Y1Y2NSO2-, где Y1 и Y2 независимо представляют водород, алкил, арил,аралкил или гетероаралкил или Y1,Y2 и N вместе образуют гетероциклил. Заместители арильной группы такие, как определены в данном описании. Предпочтительными арильными группами являются необязательно замещенный фенил или необязательно замещенный нафтил. Предпочтительные заместители арильной группы включают водород, алкил, гидрокси, ацил,арил, ароил, арилокси, галоген, нитро, алкокси,циано, алкоксикарбонил, ациламино, алкилтио,Y1'Y2'N-, Y1'Y2' NCO- или Y1'Y2'NSO2-, где Y1' иY2' независимо представляют водород, алкил,аралкил или гетероаралкил, причем предпочтительными заместителями фенильной группы являются арилокси и арил, а предпочтительными заместителями нафтильной группы - нитро,алкокси и амино. Гетероарил означает 5-10-членную ароматическую моноциклическую или полициклическую углеводородную кольцевую систему, в которой один или несколько кольцевых углеродных атомов представляет(ют) собой элемент(ы), отличный(ые) от углерода, например азот, кислород или серу. Гетероарил может быть также замещенным одним или несколькими вышеупомянутыми заместителями арильной группы. Примеры гетероарильных групп включают пиразинил, фуранил, тиенил, пиридил, пиримидинил, изоксазолил, изотиазолил,оксазолил, тиазолил, пиразолил, фуразанил,пирролил, имидазо [2,1-b]тиазолил, бензофуразанил, индолил, азаиндолил, бензимидазолил, бензотиенил, хинолинил, имидазолил и изохинолинил. Предпочтительные гетероариль 000700 6 ные группы в R-заместителе включают бензотиенил, тиенил, имидазолил, пиридил и хинолинил, все из которых могут быть необязательно замещенными. Когда представляет моноциклический гетероарил, то предпочтительные гетероарилы включают тиенил, пиридил и фуранил. Аралкил означает арилалкильную группу, в которой арил и алкил такие, как описанные выше. Предпочтительные аралкилы содержат низшую алкильную часть. Примеры аралкильных групп включают бензил, 2-фенетил и нафталинметил. Гетероаралкил означает гетероарилалкильную группу, в которой гетероарил и алкил такие, как описанные выше. Предпочтительные гетероаралкилы содержат низшую алкильную часть. Примеры гетероаралкильных групп могут содержать тиенил, пиридил, имидазолил и пиразинил. Аралкенил означает арилалкенильную группу, в которой арил и алкенил такие, как описано выше. Предпочтительные аралкенилы содержат низшую алкенильную часть. Примером аралкенильной группы является 2 фенетенил. Гетероаралкенил означает гетероарилалкенильную группу, в которой гетероарил и алкенил такие, как описано выше. Предпочтительные гетероаралкенилы содержат низшую алкенильную часть. Примеры гетероаралкенильных групп могут содержать тиенил, пиридил, имидазолил и пиразинил. Гидроксиалкил означают НО-алкильную группу, в которой алкил такой, как описано выше. Предпочтительные гидроксиалкилы содержат низший алкил. Примеры гидроксиалкильных групп включают гидроксиметил и 2 гидроксиэтил. Ацил означает Н-СО- или алкил-СОгруппу, в которой алкильная группа такая, как описано выше. Предпочтительные ацилы содержат низший алкил. Примеры ацильных групп включают формил, ацетил, пропаноил, 2 метилпропаноил, бутаноил и пальмитоил. Ароил означает арил-СО-группу, в которой алкильная группа такая, как описано выше. Примеры ароильных групп включают бензоил и 1- и 2-нафтоил. Алкокси означает алкил-O-группу, в которой алкильная группа такая, как описано выше. Примеры алкоксигрупп включают метокси,этокси, н-пропокси, изопропокси, н-бутокси и гептокси. Арилокси означает арил-О-группу, в которой арильная группа такая, как описано выше. Примеры арилоксигрупп включают фенокси и нафтокси. Аралкилокси означает аралкил-Oгруппу, в которой аралкильные группы такие,как описано выше. Примеры аралкилоксигрупп 7 включают бензилокси и 1 или 2 нафталинметокси. Алкилтио означает алкил-S-группу, в которой алкильная группа такая, как описано выше. Примеры алкилтиогрупп включают метилтио, этилтио, изопропилтио и гептилтио. Арилтио означает арил-S-группу, в которой арильная группа такая, как описано выше. Примеры арилтиогрупп включают фенилтио и нафтилтио. Аралкилтио означает аралкил-S-группу,в которой аралкильная группа такая, как описано выше. Примером аралкилтиогруппы является бензилтио.Y3Y4N- - означает замещенную или незамещенную аминогруппу, где Y3 и Y4 такие,как описано выше. Примерные группы включают амино (H2N -), метиламино, этилметиламино,диметиламино и диэтиламино. Алкоксикарбонил означает алкил -OСО-группу. Примеры алкоксикарбонильных групп включают метокси- и этоксикарбонил. Арилоксикарбонил означает арил-O-СОгруппу. Примеры арилоксикарбонильных групп включают фенокси- и нафтоксикарбонил. Аралкоксикарбонил означает аралкил-OСО-группу. Примером аралкоксикарбонильной группы является бензилоксикарбонил.Y3Y4NCO- означает замещенную или незамещенную карбамоильную группу, где Y3 иY4 такие, как описано выше. Примерами групп являются карбамоил (H2NCO-) и диметиламинокарбамоил (Me2NCO-).Y3Y4NSO2- означает замещенную или незамещенную сульфамоильную группу, где Y3 и Y4 такие, как описанные выше. Примерами групп являются амино сульфамоил (H2NSO2 -) и диметиламиносульфамоил (Me2NSO2-). Ациламино является ацил- NH-группой,в которой ацил такой, как определено в данном описании. Ароиламино является ароил-NНгруппой, в которой ароил такой, как определено в данном описании. Алкилсульфонил означает алкил-SO2 группу. Предпочтительными группами являются те, в которых алкильная группа является низшим алкилом. Алкилсульфинил означает алкил-SOrpyппy. Предпочтительными группами являются те, в которых алкильная группа является низшим алкилом. Арилсульфонил означает арил-SO2 группу. Арилсульфинил означает арил-SOгруппу. Галоген означает фтор, хлор, бром или иод. Предпочтительными являются фтор, хлор или бром, а более предпочтительными фтор или хлор. 8 Предпочтительные варианты Предпочтительным вариантом осуществления настоящего изобретения является способ лечения пациента, страдающего от физиологического расстройства, которое можно уменьшить ингибированием активности фактора Ха путем введения терапевтически эффективного количества соединения формулы 1. Предпочтительным видом соединения по настоящему изобретению является соединение формулы I, где R3 представляет необязательно замещенный фенил, необязательно замещенный нафтил, необязательно замещенный тиенил или необязательно замещенный бензотиенил. Другим предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где n=1 и m=1. Следующим предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где Х 2 и Х 2', вместе представляют оксо. Еще одним предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где X1, Х 1', Х 3 и Х 4 представляют водород. Очередным предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где Х 5 и Х 5' вместе представляют =NH. Следующим предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где Х 5 и Х 5' вместе представляют =NR5, где R5 представляет R6O2C. Другим предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где представляет фенил и углерод, замещенный на X5, X5' и НR2N-, присоединен в положении 3 фенила. Следующим предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где Еще одним предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где R представляет водород,метил,аралкил,гетероаралкил,HO2CCH2-, НОС(O)СН 2-, H2NC(O)CH2-, (аралилиHNC(O)CH2HNC(O)CH2-. Следующим предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где X1 представляет водород и X1' представляет карбоксиалкил, алкоксикарбонилалкил или арил или X1 и X1' вместе образуют оксо. 9 Другим предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где R1 представляетR3SO2-. Еще одним предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где R1 представляетR3R4NSO2-. И еще одним предпочтительным видом соединения по настоящему изобретению является соединение формулы 1, где один из X6 и X6' представляет амино в параположении относительно фрагмента Конкретные соединения по настоящему изобретению выбирают из группы, включающей трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил-амида нафталин-2-сульфоновой кислоты; трифторацетат 1-[3-аминоиминометил) бензил]-5-оксопирролидин-3-иламида дибензофуран-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида толуол-4-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 3,4 дигидро-1 Н-изохинолин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 3'метоксибифенил-4-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида нафталин-1-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 5 пирид-2-илтиофен-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида бифенил-4-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7 метоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7 этоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 5 хлор-6-метоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 5 хлор-6,7-диметоксинафталин-2-сульфоновой кислоты; бистрифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7-аминонафталин-2-сульфоновой кислоты; 10 трифторацетат 1-[4-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида нафталин-2-сульфоновой кислоты; трифторацетат [1-(аминометилбензил)-2 оксопирролидин-3-(S)-ил]амида 7-метоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-илметиламида нафталин-2-сульфоновой кислоты; бистрифторацетат 1-[3-(аминоиминометил) бензил]пирролидин-3-(S)-иламида нафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2,5-диоксопирролидин-3-(S)-ил)амида 7-метоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопиперидин-3-иламида нафталин-2-сульфоновой кислоты; трифторацетат (1-[3-(аминоиминометил) бензил]-2-оксоазепан-3-(S)-иламида 7-метоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-илметиламида 7-метоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 6 метоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-илметиламида 6-метоксинафталин-2-сульфоновой кислоты; трифторацетат 2-[1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил-6 метоксинафталин-2-сульфониламино]-Nфенетилацетамида; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 9,10 диоксо-8 а,9,10,10 а-тетрагидроантрацен-2 сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 8 хлор-7-метоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[4-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7 метоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 6,7 диметоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида нафто (2,3-d)-(1,3) диоксол-6-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7 бензилоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7 гидроксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 6 гидроксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 5 11 хлор-3-метилбензо[b]тиофен-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-илметиламида 5-хлор-3-метилбензо[b]тиофен-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7 метилнафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7 этилнафталин-2-сульфоновой кислоты; бистрифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 5-хлор-6-аминонафталин-2-сульфоновой кислоты; бистрифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7-метиламинонафталин-2-сульфоновой кислоты; бистрифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 2-метил-1,2,3,4-тетрагидроизохинолинил-7 сульфоновой кислоты; дигидрохлорид 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-илметиламида 1,2,3,4-тетрагидроизохинолинил-7-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил-(4-нитробензил)амида 7-метоксинафталин-2-сульфоновой кислоты; бистрифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил-(4 аминобензил)амида 7-метоксинафталин-2 сульфоновой кислоты; трифторацетат 1-[3-аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил-(3-нитробензил) амида 7-метоксинафталин-2-сульфоновой кислоты; бистрифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил-(3 аминобензил)амида 7-метоксинафталин-2 сульфоновой кислоты; трифторацетат 1-[3-аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил-(2-нитробензил)амида 7-метоксинафталин-2 сульфоновой кислоты; трифторацетат 3-[2-оксо-3(S)-(2-фенилэтенсульфониламино) пирролидин-1-илметил] бензамидина; трифторацетат 3-[2-оксо-3(S)-(2 фенилэтансульфониламино) пирролидин-1 илметил]бензамидина; сложный этиловый эфир [имино (3-3-[7 метоксинафталин-2-сульфонил) метиламино]-2 оксо-3(S)-пирролидин-1-ил-метилфенил) метил] карбаминовой кислоты; бистрифторацетат 3-[2-оксо-3(S)-2(пиридин-4-иламино) этансульфониламино пирролидин-1 илметил]бензамидина; 16 трифторацетат 4-амино-3-[3-(S)-(7-метоксинафталин-2-сульфонилметиламино)-2-оксопирролидин-1-илметил]бензамидина; трифторацетат N-(4-карбамимидоил-2-3[(7-метоксинафталин-2-сульфонил) метиламино]-2-оксопирролидин-1-(S)-илметилфенил) ацетамида; трифторацетат 4-амино-3-[3-(S)-(4-третбутилбензолсульфониламино)-2-оксопирролидин-1-ил-метил]бензамидина; бистрифторацетат 3-амино-5-[3-(S)-(7 метоксинафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]бензамидина; трифторацетат сложного метилового эфира 4-(аминоиминометил)-2-[3-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1 илметил]феноксиуксусной кислоты; трифторацетат 4-(аминоиминометил)-2[3-(7-метоксинафталин-2-сульфониламино)-2 оксопирролидин-1-илметил]феноксиуксусной кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3(S)-иламида 2 хлор-6-нитрофеноксибензолсульфоновой кислоты; трифторацетат 4-[3-(S)-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1 илметил]тиофен-2-карбоксамидина; трифторацетат 4-3-(S)-[(7-метоксинафталин-2-сульфонил)метиламино)-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина; трифторацетат 2-1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)ил](7-метоксинафталин-2-сульфонил)амино] ацетамида; трифторацетат 4-3-(S)-[(7-метоксинафталин-2-сульфонил)бензиламино)-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина; трифторацетат 4-[3-(S)-(5-хлор-3-метилбензо[b]тиофен-2-сульфониламино)-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина; трифторацетат 5-3-(S)-[(7-метоксинафталин-2-сульфонил) метиламино]-2-оксопирролидин-1-илметил)тиофен-3-карбоксамидина; трифторацетат 4-3-(S)-[(5-хлор-3-метилбензо[b]тиофен-2-сульфонил) бензиламино]-2 оксопирролидин-1-илметилтиофен-2-карбоксамидина; трифторацетат 4-3-(S)-[(метансульфонил)-(3-фенилпропил)амино]-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина; трифторацетат 4-3-(S)-[(метансульфонил) 17 трифторацетат 2-1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил](7-метоксинафталин-2-сульфонил)амино]-Nфенетилацетамида; трифторацетат 2-1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил](4,5-дихлортиофен-2-сульфонил)амино]-Nбензилацетамида; трифторацетат 2-1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил](7-метоксинафталин-2-сульфонил)амино]-Nбензилацетамида; трифторацетат 2-1-(4-карбамимидоилтиофен-2-илметил)-2-оксопирролидин-3-(S)-ил](7-метоксинафталин-2-сульфонил)амино] ацетамида; сложный метиловый эфир 2-1-(4 карбамимидоилтиофен-2-илметил)-2-оксопирролидин-3-(S)-ил]-(5 хлор-3-метилбензо[b]тиофен-2-сульфонил)амино]уксусной кислоты; бистрифторацетат 4-3-(S)-[(7-аминонафталин-2-сульфонил) бензиламино]-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина; бистрифторацетат 4-3-(S)-[(7-аминонафталин-2-сульфонил) метиламино]-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина; бистрифторацетат 2-1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил](7-аминонафталин-2-сульфонил)амино]ацетамида; трифторацетат 4-[3-(S)-(6-амино-5-хлор-2 сульфониламино]-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина; трифторацетат 4-(3-(S)-[(6-амино-5-хлорнафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметил)тиофен-2-карбоксамидина ; трифторацетат 2-1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил](6-амино-5-хлорнафталин-2-сульфонил) амино] ацетамида; дигидрохлорид 4-[3-(S)-(6-аминонафталин 2-сульфониламино)-2-оксопирролидин-1-илметил] тиофен-2-карбоксамидина; трифторацетат 5-[3-(S)-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1 илметил]тиофен-2-карбоксамидина; трифторацетат 5-3-(S)-[(7-метоксинафталин-2-сульфонил]метил-амино]-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина; трифторацетат 5-3-(S)-[(7-метоксинафталин-2-сульфонил) бензиламино]-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина; трифторацетат сложного метилового эфира 18 трифторацетат 4-[3-(S)-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1 илметил]пиридин-2-карбоксамидина; трифторацетат 4-3-(S)-[(7-метоксинафталин-2-сульфонил) бензиламино]-2-оксопирролидин-1-илметилпиридин-2-карбоксамидина; трифторацетат 4-3-(S)-[(7-метоксинафталин-2-сульфонил) метиламино-2-оксопирролидин-1-илметилпиридин-2-карбоксамидина; трифторацетат 4-[3-(S)-(5-хлор-3-метилбензо[b]тиофен-2-сульфониламино)-2-оксопирролидин-1-илметил]пиридин-2-карбоксамидина; трифторацетат 4-3-(S)-[(5-хлор-3-метилбензо[b]тиофен-2-сульфонил) метиламино]-2 оксопирролидин-1-илметил)пиридин-2-карбоксамидина; трифторацетат 2-[1-(2-карбамимидоилпиридин-4-илметил)-2-оксопирролидин-3-(S)ил]-(7-метоксинафталин-2-сульфонил)амино ацетамида; трифторацетат 2-[1-(2-карбамимидоилпиридин-4-илметил)-2-оксопирролидин-3-(S)ил]-(7-метоксинафталин-2-сульфонил) аминоN-фенетилацетамида; трифторацетат 4-3-(S)-[(7-метоксинафталин-2-сульфонил)тиофен-3-илметиламино]-2 оксопирролидин-1-илметилпиридин-2-карбоксамидина; трифторацетат 4-3-(S)-[(7-метоксинафталин-2-сульфонил)тио-фен-3-илме-тиламино]-2 оксопирролидин-1-илметил тиофен-2-карбоксамидина; трифторацетат 4-3-(S)-[(4-(6-нитро-2 хлорфенокси)бензол-сульфонил)амино]-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина ; трифторацетат 5-3-(S)-[(7-метоксинафталин-2-сульфониламино]-2-оксопирролидин-1 илметилфуран-2-карбоксамидина; и трифторацетат 4-[3-(S)-(5-хлор-3-метилбензо[b]тиофен-2-сульфониламино)-2-оксопирролидин-1-илметил]фуран-2-карбоксамидина. Предпочтительными соединениями являются: трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-илметиламида 7-метоксинафталин-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 3'метоксибифенил-4-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил)амида 5 пирид-2-илтиофен-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7 метоксинафталин-2-сульфоновой кислоты; бистрифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 7-аминонафталин-2-сульфоно-вой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 5 19 хлор-3-метилбензо[b]тиофен-2-сульфоновой кислоты; трифторацетат 2-[(1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил-7 метоксинафталин-2-сульфониламино]-N-фенетилацетамида; трифторацетат 2-[(1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил-7 мeтoкcинaфтaлин-2-cyльфoнилaминo]-Nбензилацетамида; бистрифторацетат 2-[1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил-7 метоксинафталин-2-сульфониламино]-N-(2 пиридин-3-ил-этил)ацетамида; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксо-3(S)-пирролидин-3-иламида 4,5-дихлортиофен-2-сульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида 3'метилбифенил-4-сульфоновой кислоты; трифторацетат 3-[1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил-(7 метоксинафталин-2-сульфонил)амино] ацетамида; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксо-3-(S)-пирролидин-3-ил) (пиридин-3-илметил)амида 7-метокси-2-нафталинсульфоновой кислоты; трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида хинолин-6-сульфоновой кислоты; дигидрохлорид 4-амино-3-[3-(S)-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1-илметил]бензамидина; трифторацетат 4-амино-3-[3-(S)-(7 метоксинафталин-2-сульфонилметиламино)-2 оксопирролидин-1-илметил]бензамидина; трифторацетат 4-амино-3-[3-(S)-(4-третбутилбензолсульфониламино)-2-оксопирролидин-1-илметил]бензамидина; трифторацетат сложного метилового эфира 4-(аминоиминометил)-2-[3-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1 илметил]фенокси уксусной кислоты; трифторацетат 4-[3-(S)-метоксинафталин 2-сульфониламино)-2-оксопирролидин-1-илметил]тиофен-2-карбоксамидина; трифторацетат 4-3-(S)-[(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина; трифторацетат 2-1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил] 20 трифторацетат 2-1-(5-карбамимидоилтиофен-3-илметил)-2-оксопирролидин-3-(S)-ил](7-метоксинафталин-2-сульфонил)амино]-Nфенетилацетамида; трифторацетат сложного метилового эфира[амино-(4-3-(S)-(7-метоксинафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметилтиофен-2-ил)метилен]карбаминовой кислоты; трифторацетат 4-3-(S)-[(6-амино-5-хлорнафталин-2-сульфонил)метиламино]-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина; трифторацетат 4-[3-(S)-(6-амино-5-хлор-2 сульфониламино]-2-оксопирролидин-1-илметил] тиофен-2-каорбоксамидина; бистрифторацетат 4-3-(S)-[(7-аминонафталин-2-сульфонил) бензиламино]-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина; трифторацетат 4-[3-(S)-(7-метоксинафталин-2-сульфониламино)-2-оксопирролидин-1 илметил]пиридин-2-карбоксамидина; трифторацетат 4-3-(S)-[(7-метоксинафталин-2-сульфонил)бензиламино]-2-оксопирролидин-1-илметилпиридин-2-карбоксамидина; трифторацетат 2-[1-(2-карбамимидоилпиридин-4-илметил)-2-оксопирролидин-3-(S)ил]-(7-метоксинафталин-2-сульфонил)аминоN-фенетилацетамида; трифторацетат 4-3-(S)-[(7-метоксинафталин-2-сульфонил)тиофен-3-илметиламино]-2 оксопирролидин-1-илметилтиофен-2-карбоксамидина; и трифторацетат 4-3-(S)-[(4-(6-нитро-2-хлорфенокси)бензолсульфонил)амино]-2-оксопирролидин-1-илметилтиофен-2-карбоксамидина. Соединения формулы 1 можно получить путем применения или приспособления известных способов, т.е. способов, уже использованных ранее или описанных в литературе. В соответствии с вариантом по настоящему изобретению соединение формулы I где Ar1, R, R1, R2, Х 3, Х 4, Х 5, Х 5', Х 6, Х 6', m и n такие, как определено выше, и X1 и X1' представляют водород, а Х 2 и Х 2', взятые вместе,представляют оксо, может быть получено путем восстановительного аминирования соединения формулы II где Аr1, Х 6, Х 6' и n такие, как определено выше,в спиртовом растворителе, таком как метанол, и иминового восстановителя, такого как цианборогидрид натрия, триацетоксиборогидрид натрия, или каталитического гидрирования с использованием, например, палладия при температуре от около 0 до около 100 С с получением циклической структуры, представленной формулой IV где Аr1, Х 3, X4, Х 6, Х 6', m и n такие, как определено выше, и Х 1 и X1' представляют водород, Х 2 и Х 2', взятые вместе, представляют оксо, и P2 представляет (алкил, аралкил или арил) карбамат. Затем группу P2 удаляют подходящим методом снятия защиты, известным для карбаматов, таким как гидрирование сильной кислотой,гидрирование сильным основанием или каталитическое гидрирование, с получением соединений формулы V где Аr1, Х 3, X4, Х 6, Х 6', m и n такие, как определено выше, и X1 и Х 1' представляют водород, а Х 2 и X2', взятые вместе, представляют оксо. Затем амин соединения формулы V связывают с любой из групп, представленных формулами(VIb) где R3, R4 и р такие, как определено выше, и Hal представляет атом галогена, такого как хлор, с использованием основания, такого как триалкиламин, в инертном растворителе, таком как дихлорметан, тетрагидрофуран, эфир или ацетонитрил, при температуре от около 0 до около 100 С в присутствии или в отсутствии активи 000700 22 рующего агента,такого,как диметиламинопиридин (DMAP, ДМАП), с получением соединений формул VIIa или VIIbVIIa и VIIb, могут быть преобразованы в соответствующий сложный эфир имидат путем использования спиртового растворителя, такого как этанол, насыщенный хлороводородом (газ). Полученный продукт затем растворяют в спиртовом растворителе, таком как метанол, насыщенный аммиаком, с получением соединений формулы I, где Х 5 и Х 5', взятые вместе, представляют =NH. В соответствии с другим вариантом соединения формулы VII можно растворять в растворе пиридина, содержащем третичное аминовое основание, такое как триэтиламин, насыщенный сероводородом, при температуре от примерно 0 до примерно 60 С. Затем полученный продукт растворяют в органическом растворителе, таком как ацетон, и подвергают взаимодействию с алкилгалогенидом, таким как метилиодид, при температуре от 0 до примерно 80 С. Полученный продукт после этого растворяют в спиртовом растворителе, таком как метанол, и подвергают взаимодействию с ацетатом аммония с получением соединений формулы I, в которых Х 5 и Х 5', взятые вместе,представляют =NH. Когда X1 и X1' представляют О и Х 2 и Х 2' независимо выбраны из водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного аралкила, необязательно замещенного гетероарила, необязательно замещенного гетероаралкила или гидроксиалкила, соединения формулы I могут быть получены из соединения формулы где Х 3, Х 4 и m такие, как определено выше, Х 2,представляет водород, необязательно замещенный алкил, необязательно замещенный арил,необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил, карбоксиалкил,алкоксикарбонилалкил или гидроксиалкил и Р 1 представляет алкил, аралкил или арил, а Р 2 представляет (алкил, аралкил или арил) карба 23 мат, путем осуществления взаимодействия его с соединением приведенной выше формулы III аналогично взаимодействию соединения формулы II с соединением формулы III. Продуктом реакции между соединениями формул VIII и III является соединение формулы IV, где Аr1, Х 3,Х 4, Х 6, Х 6', m и n такие, как определено выше, и Х 1 и X1', взятые вместе, представляют оксо,один из Х 2 и X2' представляет водород, а другой из Х 2 и Х 2' представляет водород, необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил или гидроксиалкил, и Р 2 представляет (алкил, аралкил или арил)карбамат. Это соединение формулы IV может быть затем преобразовано в соединение формулы V и далее в соединения формул VIIa иVIIb, где Аr1, R3, R4, Х 3, Х 4, Х 6, Х 6', m, n и р такие, как определено выше, и X1 и X1' представляют оксо и один из Х 2 и Х 2' представляет водород, а другой из X2 и X2' представляет водород,необязательно замещенный алкил, необязательно замещенный арил, необязательно замещенный аралкил, необязательно замещенный гетероарил, необязательно замещенный гетероаралкил или гидроксиалкил, аналогично процедуре,предназначенной для преобразования соединения формулы IV в соединение формулы V, которое затем преобразуют в соединения формулVIIa или VIIb. В соответствии с другим вариантом соединения формулы V и формулы IV можно преобразовать в соединения формулы I следующим образом. Соединения формулы IV или V обрабатывают спиртовым растворителем, таким как насыщенный НСl этанол. Затем полученный продукт обрабатывают спиртовым растворителем, таким как насыщенный аммиаком метанол,с получением, соответственно, соединений формул IX или Х; где Аr1, X1, X1', Х 2, Х 2', Х 3, Х 4, Х 6, Х 6', Р 2, m, n такие, как определено выше. Соединение формулы IX может быть затем преобразовано в соединение формулы Х подходящим способом снятия защиты, описанным выше. После этого соединение формулы Х может быть растворено в органическом растворителе, таком как этанол или диметилформамид, с добавлением соединения формулы VIa или VIb при температуре от около 0 до около 100 С в присутствии или в отсутствии активирующего агента, такого как ДМАП, с сульфонилхлоридом, в результате чего представляет собой сочетание соединений формул (IX) и (X), где А', Х 1, X1', Х 2, Х 2', Х 3, Х 4, X6,X6' и указаны выше и Р 2 представляет водород или (алкил, аралкил или арил)карбамат. В соответствии со следующим вариантом соединение формулы I может быть получено из соединения формулы XI где X1, X1', X2, X2', , Х 3, Х 4, Х 6, Х 6', m и Р 2 такие,как определено выше. Соединение формулы XI растворяют в инертном органическом растворителе, таком как тетрагидрофуран, при температуре от около -78 до около 25 С. К полученному раствору добавляют сильное основание, такое как гидрид натрия, гексаметилдисилилазид лития или диизопропиламин лития, с последующим добавлением соединения формулы XIIHalo представляет атом галогена, такого, как хлор, бром или иод, в результате чего получают соединение формулы IV, которое затем преобразуют в соединение формулы I так, как описано выше. Соединение формулы I, в котором R иной,чем водород, может быть получено из соединений формул VIIa или VIIb. Соединения формулVIIa или VIIb могут быть растворены в инертном органическом растворителе, таком как тетрагидрофуран, диоксан или диметилформамид,при температуре от примерно 0 до примерно 100 С. К полученному раствору добавляют основание, такое как гидрид натрия или карбонат калия, и соединение формулы ХIIIR-Halo,XIII где R такой, как определенный выше, исключая водород, и Halo представляет галоген, такой как хлор или бром. Полученным продуктом является соединение формулы XIV где R1, X1, X1', Х 2, Х 2', Х 3, Х 4, Х 6, Х 6', m и n такие, как определено выше, и R представляет необязательно замещенный алкил, необязательно замещенный аралкил, необязательно замещенный гетероаралкил или гидроксиалкил. Соединение формулы XIV затем преобразуют, как описано выше, в соединение формулы I, содержащее радикал -C(=NH)NH2. В соответствии с еще одним вариантом соединение формулы XIV может быть обработано спиртовым растворителем, таким как насыщенный НСl этанол. Полученный продукт обрабатывают затем спиртовым растворителем, таким как насыщенный алкиламином метанол, гидразином или алкоаксиамином, с получением соединения формулы I, где R, R1, X2, X2', Х 3, X4,X6, Х 6', m и n такие, как определено выше, Х 5 иX5', взятые вместе, представляют =NR5; R2 и R5 независимо представляют водород или алкил,или, когда один из R2 или R5 представляет водород, R2 или R5 может представлять алкокси или амино. Соединение формулы I, в котором X5 и Х 5', взятые вместе, представляют =NR5 и R5 представляет нитро, может быть получено стандартным нитрованием соединения формулы I, в котором X5 и Х 5, взятые вместе, представляют=NR5 и R5 представляет водород. Соединения формулы I, в которых Х 5 и X5',взятые вместе, представляют =NR5 и R5 представляет R6 О 2 С, R6CO или циано, могут быть получены из соединений формулы I, в которыхR5 представляет водород. Например различные амидины обрабатывают алкилхлорформиатом в подходящем растворителе, таком как метиленхлорид или диметилформамид, в присутствии основания, такого как триалкиламин, с получением соединения формулы I, в котором R5 представляет R6O2C. Аналогичным образом амидин можно обрабатывать ацилирующим агентом,таким как ацилхлорид, в присутствии основания, такого как триалкиламин, с получением соединений формулы I, в которых R5 представляет R6OC. В соответствии с другим вариантом соединения, в которых R5 представляет циано,могут быть получены путем обработки амидина цианбромидом и триалкиламином в подходящем спиртовом растворителе. Соединение формулы I, в котором X5 и Х 5' представляют водород, может быть получено путем восстановления соединений формулы 26 вания в подходящем растворителе, таком как метанол, в присутствии катализатора, такого как родий на оксиде алюминия. Это преобразование можно также обеспечить, используя гидридный реагент, такой как диизобутилалюминий гидрид, с получением соединения формулы I, в котором Х 5 и Х 5' представляют водород. Соединения по настоящему изобретению пригодны в форме свободного основания или свободной кислоты или в форме их фармацевтически приемлемой соли. Все формы находятся в объеме изобретения. При замещении соединения по настоящему изобретению основной группой образуются кислотно-аддитивные соли, являющиеся более удобной формой для применения, использование которой практически равнозначно применению соединения в форме свободного основания. Кислоты, которые можно использовать для получения кислотно-аддитивных солей, включают предпочтительно те, которые вместе со свободным основанием дают фармацевтически приемлемые соли, то есть соли, анионы которых нетоксичны для пациента в фармацевтических дозах солей, благодаря чему полезные эффекты ингибирования активности фактора Ха, присущие свободному основанию, не ухудшаются побочными эффектами, приписываемыми анионам. Хотя предпочтительными являются фармацевтически приемлемые соли упомянутых оснований, все кислотно-аддитивные соли пригодны в качестве источников формы в виде свободного основания, даже если конкретная соль сама по себе нужна лишь как промежуточный продукт,например, при образовании соли лишь для целей очистки и идентификации или при использовании ее в качестве промежуточного продукта для получения фармацевтически приемлемой соли методом ионного обмена. Фармацевтически приемлемыми солями в объеме настоящего изобретения являются производные следующих кислот: минеральные кислоты, такие как хлороводородная кислота, серная кислота, фосфорная кислота и сульфаминовая кислота; и органические кислоты, такие как уксусная кислота, лимонная кислота, молочная кислота, винная кислота, малоновая кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота,циклогексилсульфаминовая кислота, хинная кислота и тому подобное. Соответствующими кислотно-аддитивными солями являются следующие: гидрогалогениды, например гидрохлорид и гидробромид, сульфат, фосфат, нитрат,сульфамат, ацетат, цитрат, лактат, тартрат, малонат, оксалат, салицилат, пропионат, сукцинат,фумарат,малеинат,метилен-бис-Вгидроксинафтоаты, гентизаты, мезилаты, изотионаты и ди-п-толуоилтартраты, метансульфонат, этансульфонат, бензолсульфонат, птолуолсульфонат, циклогексилсульфамат и хинат, соответственно. 27 В соответствии со следующим объектом настоящего изобретения кислотно-аддитивные соли соединений по настоящему изобретению получают путем взаимодействия свободного основания с подходящей кислотой с применением или приспособлением известных способов. Например, кислотно-аддитивные соли соединений по настоящему изобретению получают либо путем растворения свободного основания в водном или водно-спиртовом растворе или других подходящих растворителях, содержащих соответствующую кислоту, и выделения соли путем выпаривания раствора, либо путем взаимодействия свободного основания с кислотой в органическом растворителе, и в этом случае соль получают сразу или при концентрировании раствора. Соединения по настоящему изобретению могут быть регенерированы из кислотноаддитивных солей с применением или приспособлением известных способов. Например, исходные соединения по настоящему изобретению можно регенерировать из их кислотноаддитивных солей путем обработки щелочью,например водным раствором бикарбоната натрия или водным раствором аммиака. При замещении соединения по настоящему изобретению кислотной группой могут быть образованы основно-аддитивные соли, являющиеся более удобной формой для применения,использование которой практически равнозначно применению соединения в форме свободной кислоты. Основания, которые можно использовать для получения основно-аддитивных солей,включают предпочтительно те, которые вместе со свободной кислотой дают фармацевтически приемлемые соли, то есть соли, катионы которых не токсичны для организма животного в фармацевтических дозах солей, благодаря чему полезные эффекты ингибирования активности фактора Ха, присущие свободной кислоте, не ухудшаются побочными эффектами, приписываемыми катионам. Фармацевтически приемлемыми солями, включающими, например, соли щелочных и щелочно-земельных металлов, в объем настоящего изобретения входят производные следующих оснований: гидрида натрия,гидроксида натрия, гидроксида калия, гидроксида кальция, гидроксида алюминия, гидроксида лития, гидроксида магния, гидроксида цинка,аммиака,этилендиамина,N-метилглюкамина, лизина, аргинина, орнитина, холина, N,N'-дибензилэтилендиамина, хлорпрокаина,диэтаноламина,прокаина,Nбензилфенетиламина, диэтиламина, пиперазина,трис(гидроксиметил)аминометана, тетраметиламмонийгидроксида и тому подобное. Соли металлов соединений по настоящему изобретению могут быть получены путем контактирования гидрида, гидроксида, карбоната или подобного реакционно-способного соединения выбранного металла в водном или орга 000700 28 ническом растворителе с соединением в виде свободной кислоты. Используемым водным растворителем может служить вода или смесь воды с органическим растворителем, предпочтительно спиртом, таким как метанол или этанол, кетоном, таким как ацетон, алифатическим простым эфиром, таким как тетрагидрофуран, или сложным эфиром, таким как этилацетат. Такие реакции обычно проводят при температуре окружающей среды, но при необходимости их можно проводить при нагревании. Соли аминов соединений по настоящему изобретению можно получить путем контактирования амина в водном или органическом растворителе с соединением в виде свободной кислоты. Подходящие водные растворители включают воду и смеси воды со спиртами, такими как метанол или этанол, простыми эфирами,такими как тетрагидрофуран, нитрилами, такими как ацетонитрил, или кетонами, такими как ацетон. Аминокислотные соли могут быть получены аналогичным образом. Основно-аддитивные соли соединений по настоящему изобретению можно регенерировать из солей с применением или приспособлением известных способов. Например, исходные соединения по настоящему изобретению можно регенерировать из их основно-аддитивных солей путем обработки кислотой, например хлороводородной кислотой. Солевые формы по настоящему изобретению включают также соединения, содержащие кватернизованный азот. Кватернизованные соли получают такими способами, как алкилированиеsp3 или sp2 гибридизованного азота в соединениях. Как ясно специалистам в данной области,некоторые из соединений по настоящему изобретению не образуют устойчивых солей. Однако кислотно-аддитивные соли, наиболее вероятно, должны образовывать соединения по настоящему изобретению, имеющие азотсодержащую гетероарильную группу, и/или соединения, содержащие аминогруппу в качестве заместителя. Предпочтительными кислотноаддитивными солями соединений по настоящему изобретению являются те, в которых нет кислотно-подвижной группы. Кроме того, что соли соединений по настоящему изобретению полезны сами по себе в качестве активных соединений, они пригодны для целей очистки соединений, например, с использованием разницы в растворимости между солями и исходными соединениями, побочными продуктами и/или исходными материалами методами, хорошо известными специалистам в данной области химии. Соединения по настоящему изобретению могут содержать асимметрические центры. Эти асимметрические центры могут независимо находиться в R или S конфигурации. Специалистам в данной области химии понятно также, 29 что некоторые соединения формулы I могут проявлять геометрическую изомерию. Геометрические изомеры включают цис- и трансформы соединений по настоящему изобретению, имеющих алкенильные или диазенильные(азо) фрагменты. Настоящее изобретение включает отдельные геометрические изомеры и стереоизомеры и их смеси. Такие изомеры могут быть выделены из их смесей с применением или приспособлением известных способов, например хроматографии и перекристаллизации, или могут быть получены раздельно из соответствующих изомеров их промежуточных продуктов, например путем применения или приспособления, уже описанных здесь способов. Исходные материалы и промежуточные продукты получают путем применения или приспособления известных способов, например,таких, как описано в ссылочных примерах или их очевидные химические эквиваленты. Настоящее изобретение дополнительно пояснено на следующих неограничивающих примерах, которые иллюстрируют получение соединений по настоящему изобретению. В спектрах ядерного магнитного резонанса(ЯМР) химические сдвиги выражены в м. д.(миллионные доли) относительно тетраметилсилана. Сокращения имеют следующие значения: с=синглет; д=дублет; т=триплет; м=мультиплет; дд=дублет дублетов; ддд=дублет дублетов дублетов; дт=дублет триплетов; ш=широкий; шс=широкий синглет; кв=квартет; Ав=система АВ (линий или полос). Пример 1. Трифторацетат 1-[3(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида нафталин-2-сульфоновой кислоты.Bpc-L-Asp-Obn (15 г, 46,4 ммоль) растворяют в 50 мл ТГФ и охлаждают до -10 С. Раствор обрабатывают N-метилморфолином (4,9 г,48,7 ммоль) и перемешивают в течение 5 мин. К раствору добавляют по каплям изобутилхлорформиат (6,3 г, 46,4 ммоль). По окончании добавления раствор перемешивают 1 мин, после чего фильтруют через слой Целита. Собранный раствор охлаждают до -10 С. Добавляют в раствор борогидрид натрия (2,63 г, 70 ммоль),предварительно растворенный в 50 мл воды. Раствор перемешивают в течение 2 мин. Выливают раствор в делительную воронку и разбавляют его 800 мл EtOAc. Органический слой промывают водой и насыщенным растворомNaCl. Органический слой сушат над MgSO4,фильтруют и концентрируют. Полученные остаток добавляют к раствору оксалилхлорида (30 мл 2 М раствора в СН 2 Сl2, 60 ммоль) и метилсульфоксида (7,25 г, 92,8 ммоль) в 250 млCH2Cl2 при -78 С. Реакционную смесь перемешивают при -78 С в течение 40 мин, после чего добавляют триэтиламин (14 г, 140 ммоль). Реак 000700 30 ционную смесь перемешивают при -78 С в течение 1 ч и затем перемешивают при комнатной температуре в течение 30 мин. Раствор вливают в 200 мл 20% раствора лимонной кислоты в воде. Полученную смесь выливают в делительную воронку и разделяют слои. Органический слой промывают водой и насыщенным растворомNaCl, сушат над MgSO4, фильтруют и концентрируют. Остаток очищают путем колоночной хроматографии с элюированием градиентом от 10% EtOAc/гексаны до 30% EtOAc/гексаны. Получают продуктный альдегид (12 г, 39 ммоль) в виде масла. 1 Н ЯМР (CDCl3, 300 МГц)9,68 (С, 1 Н),7,32 (м, 4 Н), 5,42 (шс, 1 Н), 5,16 (с, 2 Н), 4,62 (м,2 Н), 3,05 (ддд, 2 Н), 1,40 (с, 9 Н). В. Сложный трет-бутиловый эфир [1-(3 цианбензил)-2-оксопирролидин-3-(S)-ил]карбаминовой кислоты. К раствору Boc-L-Asp(H)-Obn (13,5 г, 44 ммоль) в 75 мл метанола добавляют мцианбензиламингидрохлорид (7,4 г, 44 ммоль) и триэтиламин (4,7 г, 46 ммоль). Раствор перемешивают в течение 30 мин. По истечении этого времени добавляют раствор цианборогидрида натрия (3 г, 48,4 ммоль) и хлорида цинка (3,3 г,24,2 ммоль) в 30 мл МеОН. Смесь перемешивают еще 2 ч. По истечении этого времени добавляют 20 мл 1 н. NaOH и 100 мл воды и полученную смесь концентрируют. Остаток обрабатывают 100 мл воды и 800 мл ЕtOАс. Раствор фильтруют через слой Целита, выливают в делительную воронку и разделяют слои. Органический слой промывают 1 н НСl, 10% Na2CO3 и насыщенным раствором NaCl, сушат надMgSO4, фильтруют и концентрируют. Остаток очищают путем колоночной хроматографии с элюированием градиентом от 20%EtOAc/CH2Cl2 до 40% EtOAc/CH2Cl2 и в результате получают указанное в заголовке соединение (9,1 г, 29 ммоль) в виде белого твердого вещества. 1EtOAc при 0 С барботируют газообразный НСl в течение 10 мин. По истечении этого времени раствор перемешивают в течение 4 ч. Затем раствор концентрируют с получением указанного в заголовке соединения (7,3 г, 29 ммоль) в виде белого твердого вещества. 1D. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид нафталин-2-сульфоновой кислоты. Гидрохлорид 3-(3-(S)-амино-2-оксопирролидин-1-илметил)-бензонитрила (0,4 г, 1,6 ммоль) суспендируют в 10 мл СН 2 Сl2. К раствору добавляют триэтиламин (0,49 г, 4,8 ммоль), а затем 2-нафталинсульфонилхлорид (0,4 г, 1,8 ммоль). После перемешивания в течение 2 ч раствор разбавляют СН 2 Сl2. Раствор промывают в 1 н НСl, 10% Na2CO3 и насыщенным растворомNaCl. Органический слой сушат над MgSO4,фильтруют и концентрируют. Остаток растирают с эфиром и в результате получают указанное в заголовке соединение (0,46 г, 1,13 моль) в виде твердого вещества. 1[1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид нафталин-2-сульфоновой кислоты растворяют в 50 мл этанола. Раствор охлаждают до 0 С и барботируют через него газообразный НСl в течение 10 мин. Убирают ледяную баню и реакционную смесь перемешивают при комнатной температуре в течение 6 ч. По истечении этого времени раствор концентрируют. Остаток растворяют в 50 мл метанола. Охлаждают раствор до 0 С и в течение 10 мин барботируют через него газообразный аммиак. Реакционную смесь перемешивают в течение 24 ч. По истечении этого времени раствор концентрируют. Остаток очищают путем ОФ-ВЭЖХ (высокоэффективная жидкостная хроматография с обращенной фазой) с элюированием градиентом от 10% СН 3 СN/Н 2O (0,1% ТФУ) до 60%CH3CN/H2O (0,1% ТФУ). Соответствующие фракции лиофилизируют с получением указанного в заголовке соединения (0,33 г, 0,61 ммоль) в виде твердого вещества. 1A. Boc-Asp(Obn)-Н. Указанное в заголовке соединение получают как в примере 1, часть А, с использованием Boc-Asp(Obn)-ОН вместо Boc-L-Asp-Obn.(м, 1 Н), 3,94 (АВ, 1 Н), 3,72 (АВ, 1 Н), 1,41 (с,9 Н). В. Сложный трет-бутиловый эфир [1-(3 цианбензил)-5-оксопирролидин-3-ил] карбаминовой кислоты. Указанное в заголовке соединение получают как в примере 1, часть В, с использованием Boc-Asp-(Obn)-H вместо Вос-Asp(H)-Obn. 1H ЯМР (CDCl3, 300 МГц)7,65 (д, 1 Н),7,61 (с, 1 Н), 7,52 (м, 2 Н), 4,82 (шс, 1 Н), 4,51 (с,2 Н), 4,22 (м, 1 Н), 3,53 (кв, 1 Н), 3,16 (дд, 1H),2,83 (АВ, 1 Н), 2,33 (АВ, 1 Н), 1,40 (с, 9 Н). С. Гидрохлорид 3-(3-амино-5-оксопирролидин-1-илметил) бензонитрила. Указанное в заголовке соединение получают как в примере 1, часть С, с использованием трет-бутилового эфира [1-(3-цианбензил)-5 оксопирролидин-3-ил] карбаминовой кислоты вместо трет-бутилового эфираD. [1-(3-Цианбензил)-5-оксопирролидин-3 ил] амид дибензофуран-2-сульфоновой кислоты. Указанное в заголовке соединение получают из гидрохлорида 3-(3-амино-5 оксопирролидин-1-илметил)бензонитрила, как в примере 1, часть D, с использованием 2 дибензофурансульфонилхлорида вместо 2 нафталинсульфонилхлорида. Неочищенный продукт очищают путем колоночной хроматографии при градиенте от СН 2 Сl2 до 55[1-(3-цианбензил)-5 оксопирролидин-3-ил]амида дибензофуран-2 сульфоновой кислоты (0, 44 г, 0,99 ммоль) в 10 мл смеси (10:1) пиридин - триэтиламин барботируют газообразный сероводород. После перемешивания бледно-зеленого раствора в течение 18 ч реакционную смесь концентрируют в вакууме. Остаток растворяют в ЕtOАс и 0,5 н растворе НСl. Слои разделяют и органический слой промывают насыщенным раствором NaCl, сушат над безводным MgSO4, фильтруют и концентрируют с получением неочищенного тиоамида. К раствору тиоамида в 20 мл ацетона добавляют метилиодид (2 мл, 32 ммоль). Полученную смесь нагревают с обратным холодиль 33 ником в течение 1 ч, дают остыть до комнатной температуры и концентрируют в вакууме с получением неочищенного гидроиодида тиоимидата. К раствору гидроиодида тиоимидата в 20 мл МеОН добавляют ацетат аммония (0,3 г, 3,89 ммоль). Полученную смесь нагревают с обратным холодильником в течение 3,5 ч, дают остыть до комнатной температуры и концентрируют в вакууме с получением неочищенной соли амидина. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием градиентом от 10% СН 3 СN/Н 2 О (0,1% ТФУ) до 60% СН 3 СN/Н 2 О (0,1% ТФУ) и соответствующие продуктные фракции лиофилизируют с получением указанного в заголовке соединения (0,21 г,0,36 ммоль) в виде белого твердого вещества. 1FАВ МС, [М+H]+=463. Элементный анализ: вычислено с 2,3 моль Н 2 О: С=50,50%, Н=4,51%, N=9,06%; найдено С=50,1249%, Н=3,66%, N=8,61%. Пример 3. Трифторацетат (1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)ил]амида толуол-4-сульфоновой кислоты. А. [1-(3-Цианобензил)-2-оксопирролидин 3-(S-ил]амид толуол-4-сульфоновой кислоты. Указанное в заголовке соединение получают так, как в примере 1, часть D, с использованием толуолсульфонилхлорида вместо 2 нафталинсульфонилхлорида. 1(д, 2 Н), 4,40 (АВ, 2 Н), 4,05 (м, 1 Н), 3,05 (м, 2 Н),2,36 (с, 3 Н), 1,97 (м, 1 Н), 1,57 (м, 1 Н). В. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S) амида толуол-4-сульфоновой кислоты. Указанное в заголовке соединение получают так, как в примере 1, часть Е, с использованием [1-(3-цианбензил)-2-оксопирролидин-3(S)-ил]амида толуол-4-сульфоновой кислоты в качестве исходного материала. 1 34 А. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 3,4 дигидро-1 Н-изохинолин-2-сульфоновой кислоты. 1 М раствор сульфурилхлорида (14,1 мл,14,1 ммоль) в CH2Cl2 охлаждают до 0 С. К раствору добавляют по каплям триэтиламин (0,71 г,7,1 ммоль). Затем по каплям добавляют 1,2,3,4 тетрагидроизохинолин (0,94 г, 7,1 ммоль). Убирают ледяную баню и перемешивают раствор в течение 2 ч. Раствор разбавляют СН 2 Сl2 и выливают в ледяную баню. Разделяют слои. Органический слой промывают 1 н НСl и насыщенным раствором NaCl, сушат над MgSO4, фильтруют и концентрируют. К неочищенному остатку,растворенному в 10 мл CH2Cl2, добавляют гидрохлорид 3-(3-(S)-амино-2-оксопирролидин-1 илметил)бензонитрила (0,5 г, 2 ммоль). Добавляют триэтиламин (0,4 г, 4 ммоль) и смесь перемешивают в течение 16 ч. Реакционную смесь разбавляют EtOAc и промывают 1 н HCl, 10%Nа 2 СO3 и насыщенным раствором NaCl. Остаток очищают путем колоночной хроматографии с элюированием градиентом от 10%EtOAc/CH2Cl2 до 15% EtOAc/CH2Cl2 и в результате получают указанное в заголовке соединение (0,15 г, 0,36 ммоль) в виде твердого вещества. 1FAB MC, [M+H]+= 411. В. Трифторацетат 1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил амида 3,4-дигидро-1 Н-изохинолин-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как в примере 1, часть Е, с использованием [1-(3-цианбензил)-2-оксопирролидин-3(S)-ил] амида 3,4-дигидро-1 Н-изохинолин-2 сульфоновой кислоты в качестве исходного материала. 1H2O: C=47,83%, Н=5,24%, N=12,13%; найдено С=47,43%, Н=4,88%, N=11,63%. Пример 5. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)иламида 3'-метоксибифенил-4-сульфоновой кислоты. А. 3'-Метоксибифенил-4-бромид. 3-Броманизол (3,5 г, 18,7 ммоль) растворяют в 40 мл ТГФ и охлаждают до -78 С. К раствору добавляют по каплям 2,5 М раствор нбутиллития в гексанах (7,5 мл, 18,7 ммоль). Че 35 рез 10 мин добавляют раствор хлорида цинка(20 мл, 19,6 ммоль) в эфире и убирают охлаждающую баню. Реакционную смесь перемешивают при комнатной температуре в течение 2 ч. По истечении этого времени в реакционную колбу добавляют раствор 4-иодбромбензола (5,6 г, 19,6 ммоль) и Рd(Рh3 Р)4 (1,1 г, 1 ммоль) в 10 мл ТГФ. Раствор перемешивают 2 ч, вливают в 100 мл воды и экстрагируют EtOAc. Органический слой промывают водой и насыщенным раствором NaCl, сушат над MgSO4, фильтруют и концентрируют. Остаток очищают путем колоночной хроматографии с элюированием смесью от 10% СН 2 Сl2/гексаны и до 20% СН 2 Сl2/гексаны и в результате получают указанное в заголовке соединение (1,5 г, 5,7 ммоль) в виде твердого вещества. 1-78 С. К раствору добавляют 2,5 М раствор нбутиллития в ТГФ (2,3 мл, 5,7 ммоль). Реакционную смесь перемешивают в течение 15 мин и затем переносят посредством канюли в раствор конденсированного газа диоксида серы (10 мл) в 40 мл эфира при -78 С. Раствор перемешивают 30 мин, дают ему согреться до комнатной температуры и затем концентрируют в вакууме. Полученный остаток растирают с эфиром и в результате получают 1 г биарилсульфината лития в виде твердого вещества. Твердое вещество суспендируют в 15 мл гексанов и охлаждают до 0 С. К суспензии добавляют 1 М раствор сульфурилхлорида (4,2 мл, 4,2 ммоль) в СН 2 Сl2. После выдерживания в течение 1 ч при 0 С полученный раствор концентрируют. Остаток растирают с гексанами с получением указанного в заголовке соединения (0,6 г, 2,25 ммоль) в виде твердого вещества.FAB МС, [M+H]+ =267. С. [1-3-(Цианбензил)-2-оксопиролидин-3(S)-ил]амид 3'-метотоксибифенил-4-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в пример 1, часть D, с использованием 3'-метоксибифенил-4-сульфонилхлорида вместо 2-нафталинсульфонилхлорида. 1 Н ЯМР (CDCl3, 300 МГц)7,95 (д, 1 Н),7,72 (м, 2 Н), 7,52 (м, 1 Н), 7,40 (м, 5 Н), 7,16 (д,1 Н), 7,10 (д, 1 Н), 6,95 (д, 1 Н), 5,33 (шс, 1 Н), 4,43 36 Указанное в заголовке соединение получают так, как описано в примере 1, часть Е, с использованиемFAB MC, [M+H]+ =479. Элементный анализ: вычислено с 1 моль Н 2 О: С=53,11%, Н=4,79%, N=9,18%; найдено С=53,31%, Н=4,51%, N=9,15%. Пример 6. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)иламида нафталин-1-сульфоновой кислоты. А. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид нафталин-1-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть D, с использованием 1-нафталинсульфонилхлорида вместо 2-нафталинсульфонилхлорида. 1(шс, 1 Н), 4,37 (АВ, 2 Н), 3,75 (м, 1 Н), 3,14 (м,2 Н), 2,40 (м, 1 Н), 1,97 (м,1 Н). В. Трифторацетат 1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил амида нафталин-1-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть Е с использованием [1-(3-цианбензил)-2-оксопирролидин-3-(S)-ил]амида нафталин-1-сульфоновой кислоты в качестве исходного материала. 1 Н ЯМР (ДМСО-d6, 300 МГц)9,30 (шс,2 Н), 9,13 (шс, 2 Н), 8,65 (д, 1 Н), 8,51 (д, 1 Н), 8,32FAB МС, [М+Н]+ =423. Элементный анализ: вычислено с 1 моль Н 2 О: С=51,98%, Н=4,54%, N=10,10%; найдено С=52,20%, Н=4,17%, N=9,73%. Пример 7. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)иламида 5-пирид-2-илтиофен-2-сульфоновой кислоты. А. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 5-пирид-2-илтиофен-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть D, с использованием 5-пирид-2-илтиофен-2-сульфонилхлорида вместо 2-нафталинсульфонилхлорида. 1H ЯМР (СDСl3, 300 МГц)8,62 (м, 1 Н),7,78 (м, 1 Н), 7,69 (м, 1 Н), 7,58 (м, 2 Н), 7,50 (д,1 Н), 7,46 (м, 2 Н), 7,20 (м, 2 Н), 5,43 (шс, 1 Н), 37 4,42 (АВ, 2 Н), 3,98 (м, 1 Н), 3,26 (м, 2 Н), 2,68 (м,1 Н), 2,15 (м, 1 Н). В. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил амида 5-пирид-2-илтиофен-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть Е, с использованием [1-(3-цианбензил)-2-оксопирролидин-3-(S)-ил] амида 5-пирид-2-илтиофен-2 сульфоновой кислоты в качестве исходного материала. 1FAB МС, [М+Н]+ =456. Элементный анализ: вычислено: С=43,93%, Н=3,39%, N=10,24%; найдено С=44,04%, Н=3,43%, N=10,26%. Пример 8. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)ил)амида бифенил-4-сульфоновой кислоты. А. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид бифенил-А-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть D, с использованием бифенил-4-сульфонилхлорида вместо 2-нафталинсульфонилхлорида. 1H ЯМР (CDCl3, 300 МГц)8,14 (с, 1 Н),7,95 (д, 1 Н), 7,82 (д, 1 Н), 7,64 (м, 5 Н), 7,47 (м,6 Н), 5,42 (шс, 1 Н), 4,42 (АВ, 2 Н), 3,82 (м, 1 Н),3,22 (м, 1 Н), 2,62 (м, 1 Н), 2,13 (м, 1 Н). В. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида бифенил-4-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть Е, с использованием [1-(3-цианбензил)-2-оксопирролидин-3-(S)-ил]амида бифенил-4-сульфоновой кислоты в качестве исходного материала. 1FАВ МC, [M+H]+=449. Элементный анализ: вычислено с 0,25 моль Н 2 О: С=55,07%, Н=4,53%, N=9,88%; найдено С=55,12%, Н=4,41%, N=10,05%. Пример 9. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин 3-(S)иламида 7-метоксинафталин-2-сульфоновой кислоты. А. 7-Метоксинафталин-2-сульфонилхлорид. К суспензии натриевой соли 7 гидроксинафталин-2-сульфоновой кислоты (15 г, 60,9 ммоль) в 150 мл смеси (2:1) Н 2 О-этанол добавляют при комнатной температуре твердыйNaOH (2,68 г, 67 ммоль). Смесь перемешивают до образования гомогенного раствора и затем 38 добавляют диметилсульфат (6,34 мл, 67 ммоль). В результате образуется осадок, и смесь перемешивают в течение 16 ч. Неочищенную смесь концентрируют в вакууме и остаток перемешивают в 100 мл абсолютного ЕtOН в виде суспензии в течение 2 ч. Осадок отфильтровывают и высушивают. Твердое вещество нагревают с обратным холодильником в 100 мл 95% EtOH в течение 2 ч, дают остыть до комнатной температуры, фильтруют и сушат с получением 12,6 г неочищенной натриевой соли 7 метоксинафталин-2-сульфоновой кислоты. Смесь натриевой соли сульфоновой кислоты(12,6 г, 48,6 ммоль) в 20 мл оксихлорида фосфора и пентахлорида фосфора (13,2 г, 63,2 ммоль) медленно нагревают до 60 С, пока не образуется гомогенный раствор, и затем нагревают при 120 С в течение 4 ч. Полученную смесь охлаждают в ледяной бане и медленно добавляют к ней при перемешивании смесь льда и ледяной воды. Смесь разбавляют водой и экстрагируют посредством СHCl3 (2 х 100 мл). Объединенные органические слои промывают водой, насыщенным раствором NаНСO3 и насыщенным раствором NaCl. Органическую фазу сушат над безводным MgSO4, фильтруют и концентрируют с получением 10 г неочищенного масла. Неочищенный продукт очищают путем колоночной хроматографии с элюированием при градиенте от 5 % EtOAc/гексаны до 30% EtOAc/гексаны и в результате получают указанное в заголовке соединение (3,8 г, 14,8 ммоль) в виде кристаллического твердого вещества. 1 Н ЯМР (CDCl3, 300 МГц)8,49 (д, 1H),7,96 (д, 1H), 7,85 (д, 2 Н), 7,39 (дд, 1H), 7,29 (д,1H), 3,99 (с, 3 Н). Е 1 МС, [М]+ =256. В качестве второстепенного побочного продукта описанной выше процедуры выделяют также 8-хлор-7-метоксинафталин-2-сульфонилхлорид (1,49 г, 5,12 ммоль). 1(с,3 Н). Е 1 МС, [M]+=290. В. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 7-метоксинафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают из 3-(3-(S)-амино-2-оксопирролидин-1 илметил) бензонитрилгидрохлорида так, как описано в примере 1, часть D, с использованием 7-метоксинафталин-2-сульфонилхлорида. Неочищенный продукт растирают с раствором 50%EtOAc/гексаны с получением указанного в заголовке соединения в виде твердого вещества цвета беж. 1[1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 7-метоксинафталин-2-сульфоновой кислоты растворяют в 10 мл смеси (2:1) ЕtOН/СН 2 Сl2 и преобразуют в указанное в заголовке соединение так, как описано в примере 1,часть Е. В течение 18 ч при комнатной температуре образуется промежуточный продукт имидат. За 18 ч при комнатной температуре образуется амидин. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием при градиенте от 10% CH3CN/H2O (0,1% ТФУ) до 60% СН 3 СN/Н 2 О (0,1% ТФУ) и соответствующие продуктивные фракции лиофилизуют с получением указанного в заголовке соединения в виде белого твердого вещества. 1 Н ЯМР (ДМСО-d6, 300 МГц)9,41 (шс,2 Н), 9,29 (шс, 2 Н), 8,33 (д, 1 Н), 8,19 (д, 1 Н), 7,96FAB MC, [M+H]+ =453. Элементный анализ: вычислено с 1,7 моль Н 2O: С=50,28%, Н=4,79%, N=9,38%; найдено С=50,27%, Н=4,14%, N=9,07%. Аналогично описанному выше получают трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(R)-ил)амида 7 метоксинафталин-2-сульфоновой кислоты из [1(3-цианбензил)-2-оксопирролидин-(3R)-ил] амида 7-метоксинафталин-2-сульфоновой кислоты. Пример 10. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)иламида 7-этоксинафталин-2-сульфоновой кислоты. А. 7-Этоксинафталин-2-сульфонилхлорид. Дисперсию (60%) гидрида натрия (0,74 г,18,45 ммоль) в минеральном масле промывают гексанами два раза и суспендируют в 35 мл ДМФ (диметилформамид). К этой смеси медленно добавляют через капельную воронку натриевую соль 7-гидроксинафталин-2-сульфоновой кислоты (2,5 г, 10,1 ммоль) в 50 мл ДМФ при комнатной температуре. Реакционную смесь перемешивают 75 мин, в течение которых наблюдается умеренное выделение пузырьков (выделение Н 2). Смесь обрабатывают бромэтаном (2,42 мл, 32,5 ммоль) и перемешивают 16 ч при комнатной температуре. Добавляют немного льда, чтобы разложить избытокNaH, и полученную смесь концентрируют в вакууме. Остаток суспендируют в ацетоне и концентрируют в вакууме два раза и затем высушивают под высоким вакуумом. Твердое вещество суспендируют в ацетоне, отфильтровывают и высушивают с получением неочищенной на 000700 40 триевой соли 7-этоксинафталин-2-сульфоновой кислоты в виде бежевого твердого вещества. Смесь натриевой соли сульфокислоты (3,77 г) в 10 мл тионилхлорида нагревают при 80 С в течение 2 ч. Дают смеси остыть до комнатной температуры и концентрируют ее в вакууме. Остаток разводят в EtOAc и промывают последовательно водой (2 раза), насыщенным раствором NaHCO3 и насыщенным раствором NaCl. Органический слой сушат над безводнымMgSO4, фильтруют и концентрируют с получением 2,65 г неочищенного коричневого масла. Неочищенный продукт очищают путем колоночной хроматографии с элюированием при градиенте от 10% ЕtOАс/гексаны до 20% ЕtOАс/гексаны и в результате получают указанное в заголовке соединение (1,67 г, 6,17 ммоль) в виде бледно-желтого твердого вещества. 1 Н ЯМР (CDCl3, 300 МГц)8,46 (с,1 Н),7,97 (д, 1 Н), 7,85 (д, 1 Н), 7,84(д, 1 Н), 7,38 (дд,1 Н), 7,28 (с, 1 Н), 4,19 (кв,2 Н), 1,50 (т, 3 Н). В. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид-7-этоксинафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают из 3-(3-(S)-амино-2-оксопирролидин-1 илметил)бензонитрилгидрохлорида так, как описано в примере 1, часть D, с использованием 7-этоксинафталин-2-сульфонилхлорида. Неочищенный продукт растирают с раствором 50% ЕtOАс/гексаны с получением указанного в заголовке соединения в виде твердого вещества цвета беж. 1[1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 7-этоксинафталин-2-сульфоновой кислоты растворяют в 10 мл смеси (2:1) ЕtOН/CH2Cl2 и преобразуют в указанное в заголовке соединение так, как описано в примере 1,часть Е. В течение 18 ч при комнатной температуре образуется промежуточный продукт имидат. За 48 ч при комнатной температуре образуется амидин. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием при градиенте от 10% СН 3 СN/Н 2 О (0,1% ТФУ) до 60% СН 3 СN/Н 2 О (0,1% ТФУ) и соответствующие продуктивные фракции лиофилизуют с получением указанного в заголовке соединения в виде белого твердого вещества. 1FAB МС, [М+Н]+=467. Элементный анализ: вычислено с 1,9 моль Н 2 О: С=50,91%, H=5,04%, N=9,13%; найдено С=50,92%, Н=4,44%, Т=8,57%. Пример 11. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)иламида 5-хлор-6-метоксинафталин-2-сульфоновой кислоты. А. 5-Хлор-6-метоксинафталин-2-сульфонилхлорид. Указанное в заголовке соединение получают из натриевой соли 6-гидроксинафталин-2 сульфоновой кислоты так, как описано в примере 9, часть А. Неочищенную продуктную смесь очищают путем колоночной хроматографии с элюированием при градиенте от 5%EtOAc/гексаны до 10% ЕtOАс/гексаны и в результате получают указанное в заголовке соединение как второстепенный побочный продукт. 1H ЯМР (CDCl3, 300 МГц)8,57 (д, 1 Н),8,42 (Д, 1 Н), 8,05 (дд, 1 Н), 8,00 (д, 1 Н), 7,50 (д,1 Н), 4,10 (с, 3 Н). В. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 5-хлор-6-метоксинафталин-2 сульфоновой кислоты. Указанное в заголовке соединение получают из 3-(3-(S)-амино-2-оксопирролидин-1 илметил) бензонитрилгидрохлорида так, как описано в примере 1, часть D, с использованием 5-хлор-6-метоксинафталин-2-сульфонилхлорида. Неочищенный продукт растирают с ЕtOАс с получением указанного в заголовке соединения в виде твердого вещества цвета беж. 1(2:1) EtOH/CH2Cl2 и преобразуют в указанное в заголовке соединение так, как описано в примере 1, часть Е. В течение 16 ч при комнатной температуре образуется промежуточный продукт имидат. За 24 ч при комнатной температуре образуется амидин. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием при градиенте от 10% СН 3 СN/Н 2 О (0,1% ТФУ) до 60% СН 3 СN/Н 2O (0,1% ТФУ) и соответствующие продуктные фракции лиофилизуют с получением указанного в заголовке соединения в виде белого твердого вещества. 1H2O: C=47,88%, Н=4,32%, N=8,93%; найдено С=47,88%, Н=3, 88%, Т=8,48%. Пример 12. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)амида 5-хлор-6,7-диметоксинафталин-2-сульфоновой кислоты. А. 5-Хлор-6,7-диметоксинафталин-2-сульфонилхлорид. Указанное в заголовке соединение получают из полигидрата натриевой соли 6,7 дигидроксинафталин-2-сульфоновой кислоты так, как описано в примере 9, часть А. Неочищенную продуктную смесь очищают путем колоночной хроматографии с элюированием при градиенте от 5% EtOAc/гексаны до 30%EtOAc/гексаны и в результате получают указанное в заголовке соединение как второстепенный побочных продукт. 1H ЯМР (CDCl3, 300 МГц)8,48 (д, 1 Н),8,38 (д, 1 Н), 7,45 (дд, 1 Н), 7,30 (с, 1 Н), 4,05 (с,3 Н), 4,00 (с, 3 Н). В. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 5-хлор-6,7-диметоксинафталин-2 сульфоновой кислоты. Указанное в заголовке соединение получают из 3-(3-(S)-амино-2-оксопирролидин-1 илметил) бензонитрилгидрохлорида так, как описано в примере 1, часть D, с использованием 5-хлор-6,7-диметоксинафталин-2-сульфонилхлорида. Неочищенный продукт растирают с ЕtOАс с получением указанного в заголовке соединения в вид твердого вещества цвета беж. 1 Н ЯМР (СDСl3, 300 МГц)8,49 (д, 1H),8,25 (д, 1H), 7,86 (дд, 1H) 7,55 (м, 1H), 7,40 (м,3 Н), 7,20 (с, 1H), 5,89 (м, 1H), 4,44 (АВ, 2 Н),4,03 (с, 3 Н) , 4,00 (с, 3 Н), 3,86 (м, 1H), 3,20 (м,2 Н), 2,59 (м, 1H), 2,07 (м, 1H). С. Трифторацетат 1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-ил) амида 5-хлор-6,7-диметоксинафталин-2-сульфоновой кислоты.[1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 5-хлор-6,7-диметоксинафталин-2 сульфоновой кислоты растворяют в 10 мл смеси(2:1) EtOH/CH2Cl2 и преобразуют в указанное в заголовке соединение так, как описано в примере 1, часть Е. В течение 24 ч при комнатной температуре образуется промежуточный продукт имидат. За 24 ч при комнатной температуре образуется амидин. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием при градиенте от 10% СН 3 СN/Н 2 О (0,1% ТФУ) до 60% CH3CN/H2O (0,1% ТФУ) и соответствующие продуктные фракции лиофилизуют с полу 43 чением указанного в заголовке соединения в виде белого твердого вещества. 1ISP MC, [М+Н]+=517. Элементный анализ: вычислено с 1,5 моль Н 2 О: С=47,05%, Н=3,91%, N=8,22%; найдено С=47,40%, Н=4,05%, N=8,22%. Пример 13. Трифторацетат 1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)иламида дибензофуран-2-сульфоновой кислоты. А. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид дибензофуран-2-сульфоновой кислоты. Указанное в заголовке соединение получают из 3-(3-(S)-амино-2-оксопирролидин-1 илметил) бензонитрилгидрохлорида так, как описано в примере 1, часть D, с использованием 2-дибензофурансульфонилхлорида. Неочищенный продукт растирают с EtOAc с получением указанного в заголовке соединения в виде твердого вещества цвета беж. 1EtOH/CH2Cl2 и преобразуют в указанное в заголовке соединение так, как описано в примере 1,часть Е. В течение 24 ч при комнатной температуре образуется промежуточный продукт имидат. За 40 ч при комнатной температуре образуется амидин. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием при градиенте от 10% СН 3 СN/Н 2 О (0,1% TFA) до 60% СН 3 СN/Н 2 О (0,1% ТФУ) и соответствующие продуктные фракции лиофилизуют с получением указанного в заголовке соединения в виде белого твердого вещества. 1 44 Пример 14. Бистрифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3(S)-иламида 7-аминонафталин-2-сульфоновой кислоты. А. N-Сbz-7-аминонафталин-2-сульфонилхлорид. К суспензии натриевой соли 7 аминонафталин-2-сульфоновой кислоты (3 г,12,2 ммоль) в 70 мл воды добавляют твердыйNaOH (0,98 г, 24 ммоль) при комнатной температуре. Смесь перемешивают в течение 30 мин и затем добавляют бензилхлорформиат (3,43 мл 24 ммоль). Полученную смесь перемешивают 16 ч. Неочищенный продукт обрабатывают так, как описано в примере 9, часть А, и в результате получают 4,18 г неочищенной натриевой солиN-СDz-7-аминонафталин-2-сульфоновой кислоты. Смесь натриевой соли сульфоновой кислоты(4,18 г, 11 ммоль) в 12 мл тионилхлорида нагревают при 80 С в течение 3 ч. Дают смеси остыть до комнатной температуры и концентрируют в вакууме. Остаток разбавляют посредствомEtOAc и промывают последовательно водой (2 раза), насыщенным раствором NаНСO3 и насыщенным раствором NaCl. Органический слой сушат над безводным МgSO4 фильтруют продукт и концентрируют с получением коричневого масла. Неочищенный продукт очищают путем колоночной хроматографии с элюированием при градиенте от 10% EtOAc/гексаны до 30%EtOAc/гексаны и в результате получают указанное в заголовке соединение (1,76 г, 4,68 ммоль) в виде бежевого твердого вещества. 1(дд,1 Н), 7,34 (м, 5 Н), 7,27 (с, 1H), 5,21 (с, 2 Н). В. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид N-Cbz-7-аминонафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают из 3-(3-(S)-амино-2-оксопирролидин-1 илметил)бензонитрилгидрохлорида так, как описано в примере 1, часть D, с использованиемN-Сbz-7-аминонафталин-2-сульфонилхлорида вместо 7-метоксинафталин-2-сульфонилхлорида. Неочищенный продукт очищают путем колоночной хроматографии с использованием градиента от 10% EtOAc/CH2Cl2 до 25%EtOH/CH2Cl2 и преобразуют в указанное в заголовке соединение так, как описано в примере 1,часть Е. В течение 18 ч при комнатной температуре образуется промежуточный продукт имидат. За 18 ч при комнатной температуре образуется амидин. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием при градиенте от 10% СН 3 СN/H2 О (0,1% - ТФУ) до 6%CH3CN/H2O (0,1% ТФУ) и соответствующие продуктные фракции лиофилизуют с получением указанного в заголовке соединения в виде белого твердого вещества. 1FAB MC, [М+Н]+=438. Элементный анализ: вычислено с 0,8 моль Н 2 О: С=45,96%, Н=3,94%, N=10,31%; найдено С=45,97%, Н=4,02%, N=10,41%. Пример 15. Трифторацетат 1-[4(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-иламида нафталин-2-сульфоновой кислоты. А. Сложный трет-бутиловый эфир [1-(4 цианбензил)-2-оксопирролидин-3-(S)-ил] карбаминовой кислоты. Указанное в заголовке соединение получают из Boc-L-Asp(H)-OBn так, как описано в примере 1, часть В, с использованием пцианбензиламингидрохлорида вместо м-цианбензиламингдирохлорида. Неочищенный остаток очищают путем колоночной хроматографии с элюированием градиентом от 20%EtOAc/CH2Cl2 до 40% EtOAc/-CH2Cl2 с получением указанного в заголовке соединения в виде белого твердого вещества. 1 Н ЯМР (СDСl3, 300 МГц)7,62 (д, 2 Н),7,31 (д, 2 Н), 5,15 (шс, 1 Н), 4,53 (АВ, 2 Н), 4,21(м, 1 Н), 3,24 (м, 2 Н), 2,61 (м, 1 Н), 1,90 (м, 1 Н),1,46 (с, 9 Н). В. 4-(3-(S)-Амино-2-оксопирролидин-1 илметил) бензонитрил-гидрохлорид. Указанное в заголовке соединение получают в виде белого твердого вещества из третбутилового эфира [l-(4-цианбензил)-2-оксопирролидин-3-(S)-ил]карбаминовой кислоты так,как в примере 1, часть С. 1(м, 1 Н), 3,30 (м, 2 Н), 2,40 (м, 1 Н), 2,01 (м, 1 Н). С. [1-(4-Цианбензил)-2-оксопирролидин-3(S)-ил]амид нафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают из 4-(3-(S)-амино-2-оксопирролидин-1 илметил) бензонитрилгидрохлорида так, как описано в примере 1, часть D. Неочищенный продукт растирают с EtOAc с получением ука 000700 46 занного в заголовке соединения в виде белого твердого вещества. 1[1-(4-Цианбензил)-2-оксопирролидин-3(S)-ил]амид нафталин-2-сульфоновой кислоты растворяют в 10 мл смеси (2:1) EtOH/CH2Cl2 и преобразуют в указанное в заголовке соединение так, как описано в примере 1, часть Е. В течение 18 ч при комнатной температуре образуется промежуточный продукт имидат. За 48 ч при комнатной температуре образуется амидин. Неочищенный продукт очищают путем ОФВЭЖХ с элюированием при градиенте от 10% СН 3 СN/Н 2 О (0,1% ТФУ) до 60% СН 2 СN/Н 2 О(0,1% ТФУ) и соответствующие продуктные фракции лиофилизуют с получением указанного в заголовке соединения в виде белого твердого вещества. 1C=51,32%, H=4,36%, N=9,78%. Пример 16. Трифторацетат [1-(аминометилбензил)-2-оксопирролидин-3-(S)-ил]амида 7 метоксинафталин-2-сульфоновой кислоты. К раствору [1-(3-цианбензил)-2-оксопирролидин-3-(S)-ил]амида 7-метоксинафталин-2 сульфоновой кислоты (0,12 г, 0,27 ммоль) в 10 мл 7 н. NH3/MeOH добавляют каталитическое количество 5% родия на порошкообразном оксиде алюминия. Полученную смесь гидрируют при комнатной температуре в аппарате Паара при 50 фунтах на квадратный дюйм (3,5 кг/см 2) в течение 3 ч. Неочищенную смесь фильтруют через слой Целита, промывают МеОН (2 х 10 мл) и концентрируют в вакууме. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием при градиенте от 10% СН 3 СN/Н 2O (0,1% ТФУ) до 60% СН 3 СN/Н 2 О (0,1% ТФА) и соответствующие продуктные фракции лиофилизуют с получением указанного в заголовке соединения в виде белого твердого вещества. 1(0,3 г, 0,74 ммоль) растворяют в 9 мл смеси (8:1) ТГФ/ДМФ и охлаждают до 0 С. Добавляют гидрид натрия (30 мг 60% дисперсии в минеральном масле, 0,75 ммоль) и перемешивают раствор в течение 15 мин. К смеси добавляют метилиодид (0,33 г, 2,34 ммоль). Убирают охлаждающую баню и раствор перемешивают при комнатной температуре в течение 2 ч. Выливают раствор в делительную воронку и разбавляют его 100 мл EtOAc. Органический слой промывают 1 н HCl, сушат над МgSO4 и концентрируют. Остаток очищают путем колоночной хроматографии с элюированием смесью 10%EtOAc/CH2Cl2 и в результате получают указанное в заголовке соединение (0,23 г, 0,52 ммоль) в виде твердого вещества. 1FAB МС, [М+Н]+=420. В. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил)метиламида нафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть Е, с использованиемN-Boc-3-аминопирролидин (1,09 г, 5,83 ммоль) растворяют в 30 мл CH2Cl2. К раствору добавляют триэтиламин (0,61 г, 6,02 ммоль), а затем 2-нафталинсульфонилхлорид (1,32 г, 5,83 ммоль). Реакционную смесь перемешивают 4 ч. Неочищенную смесь разбавляют 150 мл EtOAc и промывают 1 н HCl, 10% Na2CO3 и насыщенным раствором NaCl. Органический слой сушатN-Boc-3-(S)-аминопирролидин нафталин 2-сульфоновой кислоты (1,8 г, 4,78 ммоль) растворяют в 50 мл CH2Cl2. Добавляют по каплям трифторуксусную кислоту (8 мл). Реакционную смесь перемешивают 16 ч. Раствор концентрируют в вакууме и затем вновь концентрируют из толуола с получением указанного в заголовке соединения (1,8 г, 4,64 ммоль). 1[1-(3-Цианбензил)-пирролидин-3-(S)ил]амид нафталин-2-сульфоновой кислоты. Трифторацетат пирролидин-3-(S)-иламида нафталин-2-сульфоновой кислоты (0,52 г, 1,34 ммоль) растворяют в 7 мл ДМФ. Добавляют триэтиламин (0,16 г, 1,6 ммоль) и реакционную смесь охлаждают до 0 С. Добавляют -бром-мтолуилнитрил (0,25 г, 1,27 ммоль) и смесь нагревают до комнатной температуры и перемешивают в течение 2 ч. Реакционную смесь разбавляют 150 мл EtOAc и промывают 1 н 10%Na2 СO3 и насыщенным раствором NaСl. Органический слой сушат над МgSO4, фильтруют и концентрируют. Остаток очищают путем колоночной хроматографии с элюированием смесью 50% EtOAc/CH2Cl2 и в результате получают указанное в заголовке соединение (0,2 г, 0,51 ммоль) в виде масла. 1D. Бистрифторацетат 1-[3-(аминоиминометил) бензил]пирролидин-3-(S)-иламида нафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть Е, с использованием [1-(3-цианбензил)-пирролидин 3-(S)-ил]амида нафталин-2-сульфоновой кислоты в качестве исходного материала. 1Boc-Asp-OBn (3,23 г, 10 ммоль) растворяют в 100 мл ТГФ. Добавляют триэтиламин (2,53 г, 25 ммоль), а затем м-цианбензиламингидрохлорид (1,75 г, 10,4 ммоль). Реакционную смесь охлаждают до -10 С и добавляют реагент ВОР (4,42 г, 10 ммоль). Смесь перемешивают 16 ч. Неочищенную смесь разбавляют 200 млEtOAc и промывают 1 н HCl, 10% Nа 2 СO3 и насыщенным раствором NaСL. Органический слой сушат над MgSO4, фильтруют и концентрируют. Остаток очищают путем колоночной хроматографии с элюированием смесью 20%N-Boc-Asp-(м-цианбензиламин)- Овn (1 г,2,08 ммоль) растворяют в 20 мл ТГФ и охлаждают до -78 С. Добавляют по каплям 1 М раствор гексаметилдисилилазида лития (4,8 мл, 4,8 ммоль) в ТГФ. Смесь перемешивают 20 мин и добавляют к ней 20 мл насыщенного NH4Cl. Раствор экстрагируют посредством EtOAc и затем промывают 1 н HCl, 10% Nа 2 СO3 и насыщенным раствором NaСl. Органический слой сушат над MgSO4, фильтруют и концентрируют. Остаток очищают путем колоночной хроматографии с элюированием смесью 20%EtOAc/CH2Cl2 с получением указанного в заголовке соединения (0,65 г, 1,8 ммоль) в виде твердого вещества. 1 Н ЯМР (CDСL3, 300 МГц)7,71 (с, 1 Н),7,58 м, 2 Н), 7,41 (м,1 Н), 5,12 (шс, 1 Н), 4,75 (АВ,2 Н), 4,20 (м, 1 Н), 3,10 (дд, 1 Н), 2,89 (дд, 1 Н),1,45 (с, 9 Н). С. 3-(3-(S)-Амино-2,5-диоксопирролидин 1-илметил)бензонитрилгидрохлорид. Указанное в заголовке соединение получают так, как описано в примере 1, часть С, с использованием трет-бутилового эфира [1-(3 цианбензил)-2,5-диоксопирролидин-3-(S)-ил] карбаминовой кислоты в качестве исходного материала. 1 50 Указанное в заголовке соединение получают так, как описано в примере 1, часть D, с использованием 3-(3-(S)-амино-2,5-диоксопирролидин-1-илметил)бензонитрилгидрохлорида и 7-метоксинафталин-2-сульфонилхлорида. 1(АВ, 2 Н), 4,12 (м, 1 Н), 3,92 (с, 3 Н), 3,15 (дд, 1 Н),2,90 (дд, 1 Н). Е. Трифторацетат 1-[3-(аминоиминометил) бензил]-2,5-диоксопирролидин-3-(S)-ил амида 7-метоксинафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть Е, с использованием [1-(3-цианбензил)-2,5-диоксопирролидин-3-(S)-ил]амида 7-метоксинафталин-2-сульфоновой кислоты в качестве исходного материала. 1 Н ЯМР ( ДМСО-d6, 300 МГц)9,29 (шс,2 Н), 9,18 (шс, 2 Н), 8,42 (д, 1 Н), 8,39 (с, 1 Н), 8,05FAB MC, [M+H]+=467. Элементный анализ: вычислено с 1,75 моль Н 2 О: С=49,06%, Н=4,36%, N=9,15%; найдено С=48,99%, Н=4,17%, N=8,98%. Пример 20. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопиперидин-2-ил амида нафталин-2-сульфоновой кислоты. А. 3-[(N-Boc)-3-амино-2-оксопиперидин-1 илметил]бензонитрил. Смесь NBoc-L-орнитина (1,5 г, 6,45 ммоль) и 3-цианбензальдегида (0,42 г, 3,23 ммоль) суспендируют в 20 мл МеОН. Добавляют раствор безводного хлорида цинка (0,24 г,1,79 ммоль) и цианборогидрида натрия (0,22 г,3,5 ммоль) в 5 мл МеОН. Смесь перемешивают 16 ч при комнатной температуре. По истечении этого времени добавляют 20 мл 1 н. NaOH. Раствор концентрируют и остаток распределяют между EtOAc и водой. Органический слой промывают насыщенным раствором NaCl. Органический слой сушат над МgSO4, фильтруют и концентрируют с получением NBoc-N(3 цианбензил)-L-орнитина. Часть неочищенного остатка (0,75 г, 2,16 ммоль), реагент ВОР (1,05 г,2,38 ммоль) и гидрокарбонат калия (1,08 г, 10,8 ммоль) растворяют в 20 мл ДМФ. Реакционную смесь перемешивают в течение 16 ч и затем разбавляют 300 мл EtOAc. Органический слой промывают 1 н HCl, 10% Nа 2 СO3 и насыщенным раствором NaСl, сушат над MgSO4, фильтруют и концентрируют. Остаток очищают путем колоночной хроматографии с элюированием градиентом от 15% EtOAc/CH2Cl2 до 35%(с, 9 Н). В. [1-(3-Цианбензил)-2-оксопиперидин-3 ил]амид нафталин-2-сульфоновой кислоты. 3-[(N-Boc)-3-амино-2-оксопиперидин-1 илметил]бензонитрил (0,25 г, 0,76 ммоль) растворяют в 5 мл CH2Cl2. К раствору добавляют 1 мл трифторуксусной кислоты. Смесь перемешивают 3 ч при комнатной температуре и затем концентрируют. Остаток переконцентрируют из толуола с получением трифторацетат 3-(3 амино-2-оксопиперидин-1-илметил)бензонитрила (0,23 г, 0,76 ммоль) в виде твердого вещества. Затем неочищенный продукт обрабатывают так, как в примере 1, часть D, с получением указанного в заголовке соединения. 1(м, 3 Н). С. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопиперидин-3-иламида нафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть Е, с использованиемL-(-)Воскапролактам (5 г, 39 ммоль) и триэтиламин (4,9 г, 49 ммоль) растворяют в 100 мл СН 2 Сl2. К раствору добавляют Воc ангидрид (8,5 г, 39 ммоль) и диметиламинопиридин (0,1 г). Реакционную смесь перемешивают 16 ч при комнатной температуре. По истечении этого времени раствор промывают 1 нNaСl. Органический слой сушат над МgSO4,фильтруют и концентрируют с получением указанного в заголовке соединения (6,23 г, 27 ммоль) в виде твердого вещества. 1L-(-)Вос-аминокапролактам (1,07 г,4,7 ммоль) растворяют в 45 мл ТГФ и охлаждают до 0 С. К раствору добавляют 1 М раствор гексаметилдисилилазида лития (4,7 мл, 4,7 ммоль) в ТГФ. Смесь перемешивают 30 мин при 0 С. К полученному раствору добавляют бром-м-толуилнитрил (0,9 г, 4,7 ммоль). Реакционную смесь перемешивают в течение 4 ч. Раствор разбавляют 10 мл EtOAc и промывают 1 н HCl, 10% Nа 2 СO3 и насыщенным растворомNaСl. Органический слой сушат над МgSO4,фильтруют и концентрируют. Остаток очищают путем колоночной хроматографии и элюированием смесью 20% EtOAc/CH2Cl2 с получением указанного в заголовке соединения (1,05 г, 3,1 ммоль) в виде твердого вещества. 1(м, 1 Н), 3,48 (м, 1 Н), 3,15(дд, 1 Н), 2,05 (м, 1 Н),1,90 (м, 1 Н), 1,70 (м, 2 Н), 1,49 (м, 1 Н), 1,45 (с,9 Н), 1,20 (м, 1 Н). С. 3-(3-(S)-Амино-2-оксоазепан-1-илметил) бензонитрилгидрохлорид. Указанное в заголовке соединение получают так, как описано в примере 1, часть С, с использованием трет-бутилового эфира [1-(3 цианбензил)-2-оксоазепан-3-(S)-ил]карбаминовой кислоты в качестве исходного материала.D. [1-(3-Цианбензил)-2-оксоазепан-3-(S)ил]амид 7-метоксинафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть D, с использованием 3-(3-(S)-амино-2-оксоазепан-1 илметил)бензонитрилгидрохлорида и 7-метоксинафталин-2-сульфонилхлорида в качестве исходных материалов. 1(м, 2 Н), 1,18 (м, 3 Н). Е. Трифторацетат 1-[3-(аминоиминометил)бензил]-2-оксоазепан-3-(S)-иламида 7 метоксинафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть Е, с использованиемH2O: C=53,73%, H=5,01%, N=9,28%; найдено С=53,77%, Н=4,86%, N=9,26%. Пример 22. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)илметиламида 7-метоксинафталин-2 сульфоновой кислоты. А. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]метиламид 7-метоксинафталин-2 сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 17, часть А, с использованием [1-(3-цианбензил)-2-оксопирролидин-3-(S)-ил]амида 7-метоксинафталин-2 сульфоновой кислоты в качестве исходного материала. 1H ЯМР (CDСl3, 300 МГц)8,44 (д, 1 Н),7,92 (д, 1 Н), 7,82 (м, 2 Н), 7,61 (м, 1 Н), 7,47 (м,3 Н), 7,28 (м, 2 Н), 4,97 (м, 1 Н), 4,53 (АВ, 1 Н),4,39 (АВ, 1 Н) , 3,96 (с, 3 Н), 3,13 (м, 2 Н), 2,83 (с,3 Н), 2,36 (м, 1 Н), 2,37 (м, 1 Н), 2,06 (м, 1 Н). В. Трифторацетат 1-[3-(аминоиминометил)бензил]-2-оксопирролидин-3-(S)-илметиламида 7-метоксинафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 1, часть Е, с использованием [1-(3-цианбензил-2-оксопирролидин-3-(S)-ил]метиламида 7-метоксинафталин 2-сульфоновой кислоты в качестве исходного материала. 1FAB MC, [M+H]+=467. Элементный анализ: вычислено с 2,5 моль Н 2 О: С=49,92%, Н=5,16%, N=8,98%; найдено С=50,03%, Н=4,56%, N=8,70. Пример 23. 3-(3-(S)-Амино-2-оксопирролидин-1-илметил)бензонитрилгидрохлорид. А. Сложный трет-бутиловый эфир (2 оксопирролидин-3-(S)-ил)карбаминовой кислоты. К раствору (S)-Вос-диаминомасляной кислоты (25 г, 115 ммоль), триэтиламина (35 г, 344 ммоль) и гидроксибензотриазола (19,3 г, 143 ммоль) в 0,5 л ТГФ добавляют 1-(3 диметиламинопропил)-3-этилкарбодиимидгидрохлорид (27,4 г, 143 ммоль). Раствор нагревают до 60 С в течение 15 мин, в результате чего образуется белый осадок. Температуру раствора поддерживают на уровне 60 С в течение 4 ч. По истечении этого времени раствор фильтруют и собранную жидкость концентрируют. Неочищенный продукт очищают путем колоночной хроматографии с элюированием при градиенте 1% МеОН/СН 2 Сl2 до 3% MeOH/CH2Cl2 и в результате получают указанное в заголовке соеди 000700 54 нение (19,6 г, 98 ммоль) в виде белого твердого вещества. 1(9,3 г, 47 ммоль) в 225 мл смеси (10:1) ТГФ/ДМФ при 0 С добавляют 60% дисперсию в минеральном масле гидрида натрия (1,8 г, 46 ммоль). Реакционную смесь перемешивают при 0 С в течение 0,5 ч и затем дают ей согреться до температуры окружающей среды. Через 3 ч реакционную смесь резко охлаждают добавлением насыщенного NH4Cl и разбавляют EtOAc. Разделяют слои. Органический слой промывают 1 нHCl, Н 2 О и насыщенным раствором NaСl сушат над MgSO4, фильтруют и концентрируют. Неочищенный продукт очищают путем колоночной хроматографии с элюированием градиентом от 20% EtOAc/гексаны до 40% EtOAc/гексаны с получением указанного в заголовке соединения(12,7 г, 40 ммоль) в виде белого твердого вещества. 1 ЯMP (CDСl3, 300 МГц)7,55 (м, 4 Н), 5,18EtOAc при 0 С барботируют газообразный HCl в течение 10 мин. По истечении этого времени раствор перемешивают 4 ч. Затем раствор концентрируют с получением указанного в заголовке соединения (7,3 г, 29 ммоль) в виде белого твердого вещества. 1 ЯМР (DMCO-d6, 300 МГц)8,71 (шс, 3 Н),7,85 (м, 2 Н), 7,70 (м, 2 Н), 4,58 (АВ, 2 Н), 4,13 (м,1 Н), 3,32 (м, 2 Н), 2,44 (м, 1 Н), 2,18 (м, 1 Н). Пример 24. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)иламида 6-метоксинафталин-2-сульфоновой кислоты. А. 6-Метоксинафталин-2-сульфонилхлорид. К суспензии натриевой соли 6 гидроксинафталин-2-сульфоновой кислоты (5 г,20,3 ммоль) в 40 мл смеси (2:1) Н 2O/этанол добавляют твердый NaOH (0,89 г, 22,3 ммоль) при комнатной температуре. Полученную темную смесь перемешивают до образования однородного раствора и затем добавляют диметилсульфат (2,11 мл, 22,3 ммоль). Смесь перемешивают в течение 16 ч, и в результате чего образуется осадок. Неочищенную смесь концен 55 трируют в вакууме и остаток перемешивают в 70 мл абсолютного EtOH как суспензию. Осадок отфильтровывают и высушивают. Твердое вещество нагревают с обратным холодильником в 100 мл 95% EtOH в течение 2,5 ч, дают остыть до комнатной температуры, отфильтровывают и высушивают с получением 3,31 г неочищенной натриевой соли 6-метоксинафталин-2 сульфоновой кислоты. Смесь натриевой соли сульфоновой кислоты (3,31 г, 12,7 ммоль) в 5,3 мл оксихлорида фосфора и пентахлорида фосфора (3,44 г, 16,5 ммоль) медленно нагревают до 60 С, пока не образуется однородный раствор, и затем нагревают при 120 С в течение 4 ч. Полученной смеси дают постоять при комнатной температуре в течение ночи и затем медленно добавляют к ней смесь ледяной воды со льдом. Смесь разбавляют водой и экстрагируют СHCl3. Объединенные органические слои промывают последовательно водой и насыщенным раствором NаНСO3. Органическую фазу сушат над безводным MgSO4, фильтруют и концентрируют с получением 4 г неочищенного продукта. Неочищенный продукт очищают путем колоночной хроматографии с элюированием градиентом от 10% EtOAc/гексаны до 20%EtOAc/гексаны с получением указанного в заголовке соединения (1,51 г, 5,88 ммоль) в виде кристаллического твердого вещества. 1 ЯМР (СDСl3, 300 МГц)8,50 (д, 1 Н), 7,91(м, 3 Н), 7,31 (д, 1 Н), 7,21 (д, 1 Н), 3,99 (с, 3 Н). Е 1 МС [М]+=256. В. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 6-метоксинафталин-2-сульфоновой кислоты. 3-(3-(S)-Амино-2-оксопирролидин-1 илметил)бензонитрилгидрохлорид (0,20 г, 0,79 ммоль) суспендируют в 10 мл CH2Cl2. К раствору добавляют триэтиламин (0,24 г, 2,37 ммоль),а затем 6-метоксинафталин-2-сульфонилхлорид(0,25 г, 0,99 ммоль). После перемешивания в течение 1,5 ч раствор разбавляют EtOAc и промывают 1 н водным раствором HCl, водой, насыщенным раствором NаНСO3 и насыщенным раствором NaСl. Органический слой сушат над МgSO4, фильтруют и концентрируют с получением неочищенного материала, который очищают путем колоночной хроматографии при градиенте от 20% EtOAc/CH2Cl2 до 50%[1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 6-метоксинафталин-2-сульфоновой кислоты (0,18 г, 0,41 ммоль) растворяют в 10 мл смеси (2:1) EtOH/CH2Cl2. Раствор охлаждают до 0 С и в течение 10 мин барботируют через него газообразный HCl. Убирают ледяную баню и перемешивают реакционную смесь при комнатной температуре в течение 18 ч. По истечении этого времени раствор концентрируют под высоким вакуумом досуха. Остаток растворяют в 10 мл метанола, охлаждают до 0 С и в течение 10 мин через раствор барботируют газообразный аммиак. Реакционную смесь перемешивают при комнатной температуре в течение 42 ч. По истечении этого времени раствор концентрируют и остаток очищают путем ОФ-ВЭЖХ с элюированием градиентом от 10% СН 3 СN/Н 2 О(0,1% ТФУ) до 60% СН 3 СN/Н 2 О (0,1% ТФУ) в течение 30 мин. Соответствующие фракции лиофилизуют с получением указанного в заголовке соединения (0,11 г, 0,19 ммоль) в виде аморфного белого твердого вещества. 1 ЯMP (ДМСО-d2, 300 МГц)9,30 (шс, 2 Н),9,10 (шс, 2 Н), 8,40 (с, 1 Н), 8,19 (д, 1 Н), 8,04 (д,1 Н), 8,00 (д, 1 Н), 7,82 (дд, 1 Н), 7,68 (м, 1 Н), 7,55[1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 6-метоксинафталин-2-сульфоновой кислоты (0,24 г, 0,55 ммоль) растворяют в 5 мл смеси (8:1) ТГФ/ДМФ и охлаждают до 0 С. Добавляют гидрид натрия (24 мг 60% дисперсии в минеральном масле, 0,61 ммоль) и перемешивают раствор в течение 15 мин. К смеси добавляют метилиодид (0,15 г, 1,10 ммоль). Убирают охлаждающую баню и раствор перемешивают при комнатной температуре в течение 2 ч. Выливают раствор в делительную воронку и разбавляют его 100 мл EtOAc. Органический слой промывают 1 н HCl, насыщенным растворомNаНСO3 и насыщенным раствором NaСl, после чего сушат над МgSO4, фильтруют и концентрируют. Неочищенный остаток очищают путем колоночной хроматографии с элюированием смесью 25% EtOac/CH2Cl2 и в результате получают указанное в заголовке соединение (0, 23 г,0,51 ммоль) в виде твердого вещества. 1 ЯМP (СDСl3, 300 МГц)8,45 (с, 1 Н), 7,87(м, 3 Н), 7,59 (м, 4 Н), 7,20 (м, 2 Н), 4,95 (м, 1 Н), 57 4,44 (АВ, 2 Н), 3,95 (с, 3 Н), 3,21 (м, 2 Н), 2,80 (с,3 Н), 2,40 (м, 1 Н), 2,09 (м, 1 Н). В. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-илметиламида 6-метоксинафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают так, как описано в примере 24, часть С, с использованием [1-(3-цианбензил)-2-оксопирролидин-3-(S)-ил]метиламида 6-метоксинафталин-2-сульфоновой кислоты в качестве исходного материала. В течение 18 ч при комнатной температуре образуется промежуточный продукт имидат. За 18 ч при комнатной температуре образуется амидин. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием при градиенте от 10% CH3CN/H2O (0,1% ТФА) до 60% СН 3 СN/Н 2 О (0,15 ТФА) и соответствующие продуктные фракции лиофилизуют с получением указанного в заголовке соединения в виде белого твердого вещества. 1 ЯМР (DMCO-d6, 300 МГц)9,30 (шс,2 Н), 9,17 (шс, 2 Н), 8,43 (д, 1 Н), 8,06 (д, 1 Н), 7,99H2O: С=50,91%, Н=5,04%, N=9,13%; найдено С=50,92%, Н=4,55%, N=8,83%. Пример 26. Трифторацетат 2-[1-[3(аминоиминометил) бензил]-2-оксопирролдин 3-(S)-ил)-6-метоксинафталин-2-сульфониламино]-N-фенетилацетамида. А. Сложный трет-бутиловый эфир 2-[1(3-цианбензил)-2-оксопирролидин-3-(S)-ил-6 метоксинафталин-2-сульфониламино-N-уксусной кислоты. К раствору [1-(3-цианбензил)-2-оксопирролидин-3-(S)-ил]амида 6-метоксинафталин-2 сульфоновой кислоты (0,33 г, 0,76 ммоль), полученного так, как описано в примере 24, часть В, и трет-бутилбромацетата (0,15 г, 0,77 ммоль) в ДМФ (6 мл) добавляют К 2 СO3 (0,21 г, 1,5 ммоль). Реакционную смесь перемешивают 3 ч. По истечении этого времени реакционную смесь разбавляют EtOAc и H2O. Разделяют слои. Органический слой промывают H2O и насыщенным раствором NaСl. Неочищенный продукт очищают путем колоночной хроматографии при градиенте от 10% EtOAc/CH2Cl2 до 20% EtOAc/CH2Cl2 с получением указанного в заголовке соединения (0,42 г, 0,76 ммоль) в виде белого пенообразного вещества. В. 2-[1-(3-Цианбензил)-2-оксопирролидин-3-(S)-ил-6-метоксинафталин-2-сульфониламино]-N-уксусная кислота. Трет-бутиловый эфир 2-[1-(3-цианбензил)-2-оксопирролидин-3-(S)-ил-6-метоксинафталин-2-сульфониламино]-N-уксусной кислоты растворяют в 25 мл смеси (5:1)CH2Cl2/трифторуксусная кислота. Через 3 ч раствор концентрируют с получением указанного в заголовке соединения в виде белого пенообразного вещества. 1 ЯМР (СDСl3, 300 МГц)8,39 (с, 1 Н), 7,85(м, 1 Н). С. 2-[1-(3-Цианбензил)-2-оксопирролидин-3-(S)-ил)-6-метоксинафталин-2-сульфониламино]-N-фенетилацетамид. К раствору 2-[1-(3-цианбензил)-2 оксопирролидин-3-(S)-ил-6-метоксинафталин 2-сульфониламино]-N-уксусной кислоты (0,41 г,0,83 ммоль), триэтиламина (0,28 г, 2,8 ммоль) и фенетиламина (0, 28 г, 2,8 ммоль) в 8 мл ДМФ добавляют гексафторфосфат бензотриазол-1 илокси-трис(диметиламино)фосфония (0,37 г,0,83 ммоль). Раствор перемешивают 16 ч. По истечении этого времени раствор разбавляютEtOAc. Органический слой промывают 1 н HCl,10% Nа 2 СO3 и насыщенным раствором NaСl,сушат над MgSO4, фильтруют и концентрируют. Неочищенный продукт очищают путем колоночной хроматографии при градиенте от 10%EtOAc/CH2Cl2 до 20% EtOAc/CH2Cl2 с получением указанного в заголовке соединения (0,40 г,0,70 ммоль) в виде белого твердого вещества. 1D. Трифторацетат 2-[1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)-ил 6-метоксинафталин-2-сульфониламино]-Nфенетилацетамида. Указанное в заголовке соединение получают так, как описано в примере 24, часть С, с использованием 2-[1-(3-цианбензил)-2 оксопирролидин-3-(S)-ил-6-метоксинафталин 2-сульфониламино]-N-фенетилацетамида в качестве исходного материала. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием при градиенте от 10% СН 3 СN/H2O (0,1% ТФУ) до 60% СН 3 СN/H2O (0,1% ТФУ) и соответствующие продуктные фракции лиофилизуют с получением указанного в заголовке соединения в виде белого твердого вещества. 1FAB МС, [М+Н]+=614. Элементный анализ: вычислено с 2,25 моль Н 2O: С=54,90%, Н=4,79%, N=9,01%; найдено С=54,72%, Н=5,31%, N=9,12%. Пример 27. Трифторацетат 1-[3(аминоиминометил)бензил]-2-оксопирролидин 59 3-(S)-иламида 9,10-диоксо-8 а,9,10,10 а-тетрагидроантрацен-2-сульфоновой кислоты. А. Антрахинон-2-сульфонилхлорид. Смесь натриевой соли антрахинон-2 сульфоновой кислоты (5 г, 15,2 ммоль) в 6,4 мл оксихлорида фосфора и пентахлорида фосфора(4,12 г, 19,8 ммоль) медленно нагревают до 60 С, пока не образуется гомогенный раствор, и затем нагревают при 120 С в течение 4 ч. Полученную смесь охлаждают в ледяной бане и медленно добавляют с перемешиванием смесь ледяной воды со льдом. Смесь разбавляют водой и экстрагируют два раза посредством СHCl3. Объединенные органические слои промывают последовательно насыщенным раствором NаНСO3 и насыщенным раствором NaСl. Органическую фазу сушат над безводным МgSO4, фильтруют и концентрируют с получением 4,50 г неочищенного продуктного сульфонилхлорида, имеющего чистоту, достаточную для использования в последующих реакциях. 1E1 MC, [М]+ =306. В. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 9,10-диоксо-8 а,9,10,10 а-тетрагидроантрацен-2-сульфоновой кислоты. Указанное в заголовке соединение получают из 3-(3-(S)-амино-2-оксопирролидин-1 илметил) бензонитрилгидрохлорида так, как в примере 24, часть В, с использованием антрахинон-2-сульфонилхлорида вместо 6-метоксинафталин-2-сульфонилхлорида. Неочищенный продукт очищают путем колоночной хроматографии при градиенте от 20% EtOAc/CH2Cl2 до 40% EtOAc/CH2Cl2 с получением указанного в заголовке соединения в виде твердого вещества. 1[1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 9,10-диоксо-8 а,9,10,10 а-тетрагидроантрацен-2-сульфоновой кислоты преобразуют в указанное в заголовке соединение так, как описано в примере 24, часть С. В течение 18 ч при комнатной температуре образуется промежуточный продукт имидат. 3 а 18 ч при комнатной температуре образуется амидин. Неочищенный продукт очищают путем ОФ-ВЭЖХ с элюированием при градиенте от 10% СН 3 СN/H2 О (0,1% ТФУ) до 60% СН 3 СN/H2 О(0,1% ТФУ) и соответствующие продуктные фракции лиофилизуют с получением указанного 60 в заголовке соединения в виде белого твердого вещества. 1 Н ЯМР (ДМСО-d6, 300 МГц)9,28 (шс,2 Н), 9,05 (шс, 2 Н), 8,63 (д, 1 Н), 8,59 (д, 1 Н), 8,32FAB МС, [М+Н]+=503. Элементный анализ: вычислено с 1,08 моль H2O: С=51,78%, Н=4,14%, N=8,63%; найдено С=51,79%, Н=3,82%, N=8,28%. Пример 28. Трифторацетат 1-[3-(аминоиминометил) бензил]-2-оксопирролидин-3-(S)иламида 8-хлор-7-метоксинафталин-2-сульфоновой кислоты. А. 8-Хлор-7-метоксинафталин-2-сульфонилхлорид. Указанное в заголовке соединение получают так, как описано в примере 24, часть А, с использованием натриевой соли 7-гидроксинафталин-2-сульфоновой кислоты (15 г, 60,9 ммоль) вместо натриевой соли 6-гидроксинафталин-2-сульфоновой кислоты. Полученную неочищенную натриевую соль 7-метоксинафталин-2-сульфоновой кислоты (12,6 г) аналогичным образом хлорируют в присутствии избыточного оксихлорида фосфора и пентахлорида фосфора. Сырой продукт (10 г) очищают путем колоночной хроматографии с элюированием градиентом от 5% EtOAc/гексаны до 30%H ЯМР (СDСl3, 300 МГц)8,95 (д, 1 Н),8,01 (д, 1 Н), 7,90 (д, 2 Н), 7,55 (д, 1 Н), 4,09 (с,3 Н). Е 1 МС, [M]+=290. В качестве основного компонента в результате описанной выше процедуры получен также 7-метоксинафталин-2-сульфонилхлорид(3,80 г, 14,8 ммоль) в виде белого кристаллического твердого вещества. 1 Н ЯМР (CDСl3, 300 МГц)8,49 (д, 1 Н),7,96 (д, 1 Н), 7,85 (д, 2 Н), 7,39 (дд, 1 Н), 7,29 (д,1 Н), 3,99 (с, 3 Н). Е 1 МС, [М]+=256. В. [1-(3-Цианбензил)-2-оксопирролидин-3(S)-ил]амид 8-хлор-7-метоксинафталин-2-сульфоновой кислоты. Указанное в заголовке соединение получают из 3-(3-(S)-амино-2-оксопирролидин-1 илметил)бензонитрилгидрохлорида так, как в примере 24, часть В, с использованием 8-хлор 7-метоксинафталин-2-сульфонилхлорида вместо 6-метоксинафталин-2-сульфонилхлорида. Неочищенный продукт растирают с раствором 50% EtOAc/гексаны с получением указанного в заголовке соединения в виде бежевого твердого вещества. 1
МПК / Метки
МПК: A61K 31/44, C07D 401/06
Метки: сульфиниламино, замещенные, n-[(аминоиминометил, сульфониламино, фенилалкил, сульфиновой, кислоты, сульфоновой, производные, азагетероциклил-амидные
Код ссылки
<a href="https://eas.patents.su/30-700-zameshhennye-sulfinovojj-kisloty-sulfonovojj-kisloty-sulfonilamino-ili-sulfinilamino-n-aminoiminometil-fenilalkil-azageterociklil-amidnye-proizvodnye.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные (сульфиновой кислоты, сульфоновой кислоты, сульфониламино или сульфиниламино) n-[(аминоиминометил) фенилалкил] азагетероциклил-амидные производные</a>
Предыдущий патент: Индазолкарбоксамиды, способ их получения, фармкомпозиция и способ ингибирования 5-нт4 рецептора.
Следующий патент: Пентациклическое соединение
Случайный патент: Бурение скважины












