Биосинтетический пирролинкарбоксилизин и сайт-специфичные модификации белка за счет химической модификации остатков пирролинкарбоксилизина и пирролизина
Номер патента: 21001
Опубликовано: 31.03.2015
Авторы: Уно Тетсуо, Кроссгроув Тиффани, Гайерштангер Бернхард, У Вэйцзя, Груневальд Ян, Чю Сяньпо, Челлитти Сьюсан Э., Хао Сюши
Формула / Реферат
1. Соединение формулы (I) или формулы (II)

где соединение формулы (I) получают биосинтетическим способом в клетке, и соединение формулы (II) получают из соединения формулы (I), и
где R1 обозначает Н;
R2 обозначает ОН;
n равен целому числу от 1 до 5000;
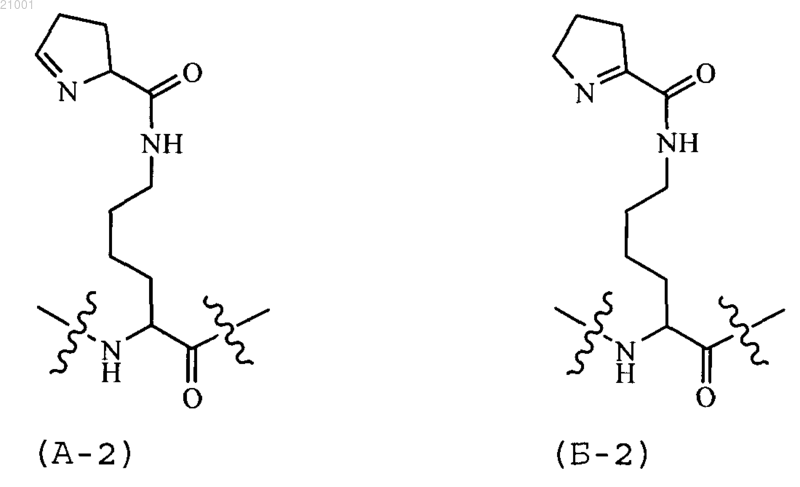
АА каждый независимо выбран из аминокислотного остатка, аминокислотного аналога-пирролизина формулы (А-2) и аминокислотного аналога-пирролизина формулы (Б-2), ВВ каждый независимо выбран из аминокислотного остатка, аминокислотного аналога-пирролизина формулы (А-2), аминокислотного аналога-пирролизина формулы (Б-2), аминокислотного аналога-пирролизина формулы (В-1), аминокислотного аналога-пирролизина формулы (Г-2), аминокислотного аналога-пирролизина формулы (Д-1), аминокислотного аналога-пирролизина формулы (Е-2), аминокислотного аналога-пирролизина формулы (Ж-1), аминокислотного аналога-пирролизина формулы (З-2), аминокислотного аналога-пирролизина формулы (И-1), аминокислотного аналога-пирролизина формулы (К-2), аминокислотного аналога-пирролизина формулы (Л-1) и аминокислотного аналога-пирролизина формулы (М-2),
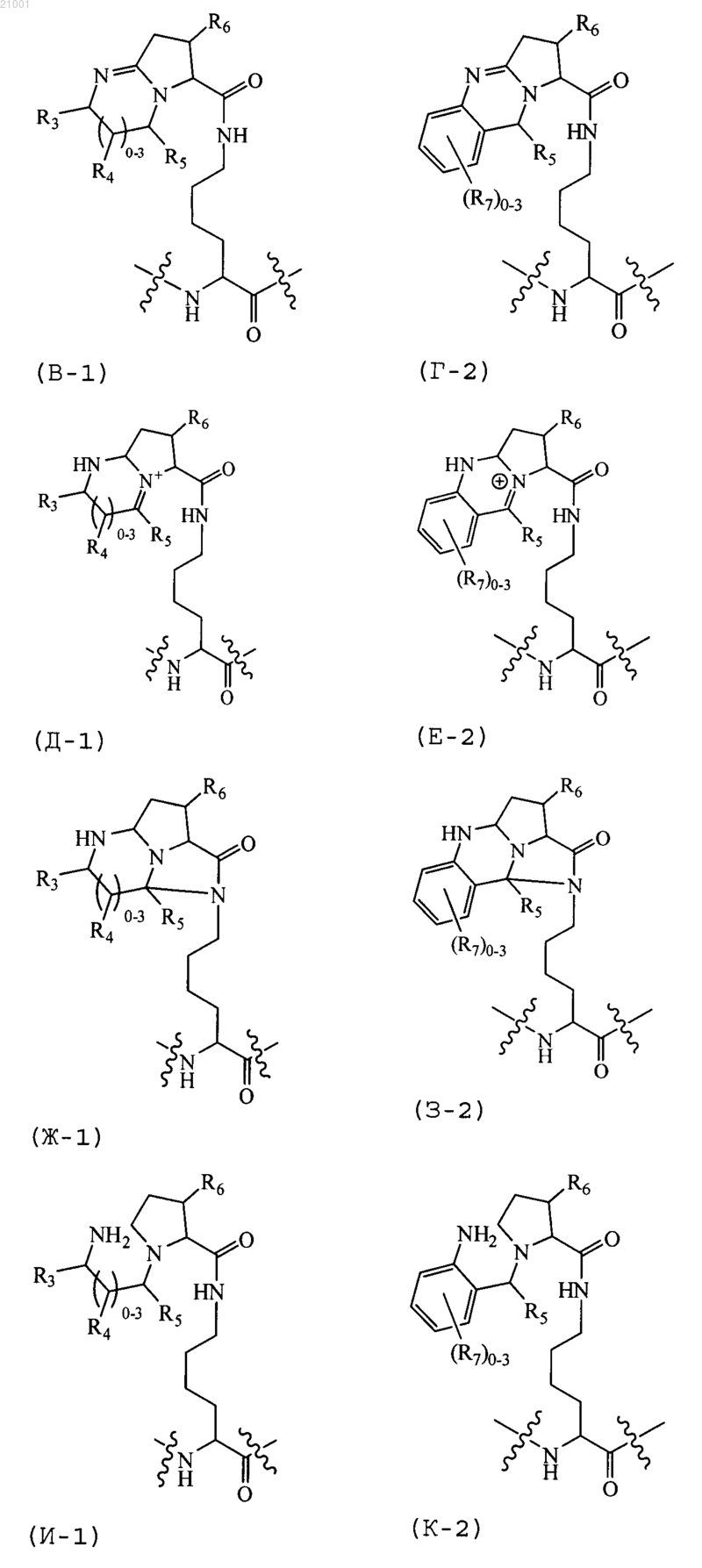
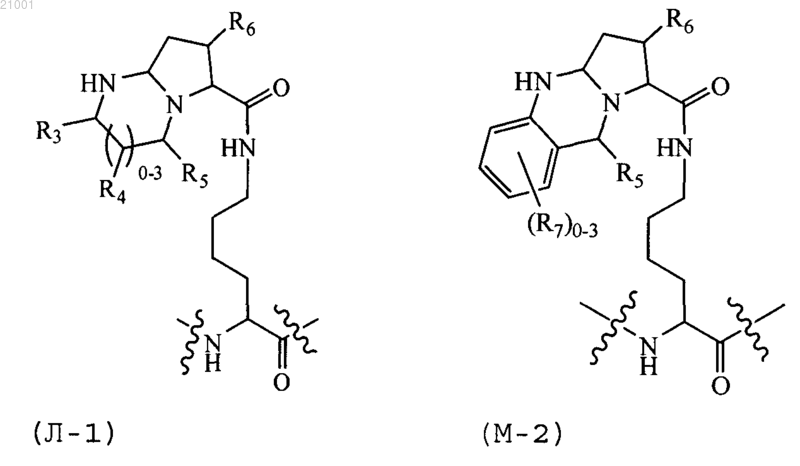
где R3, R5 и R4 каждый независимо выбран из Н, -ОН, -NO2, галогена, С1-С8алкила, замещенного галогеном С1-С8алкила, замещенного гидроксигруппой С1-С8алкила и -LX1;
R6 обозначает Н или С1алкил;
R7, если присутствует, каждый независимо выбран из -ОН, -NO2, галогена, С1-С8алкила, замещенного галогеном С1-8алкила, замещенного гидроксигруппой С1-С8алкила и -LX1;
L выбран из связи, С1-С8алкилена, замещенного галогеном С1-С8алкилена, замещенного гидроксигруппой С1-С8алкилена, С2-С8алкенилена, замещенного галогеном С2-С8алкенилена, замещенного гидроксигруппой С2-С8алкенилена,
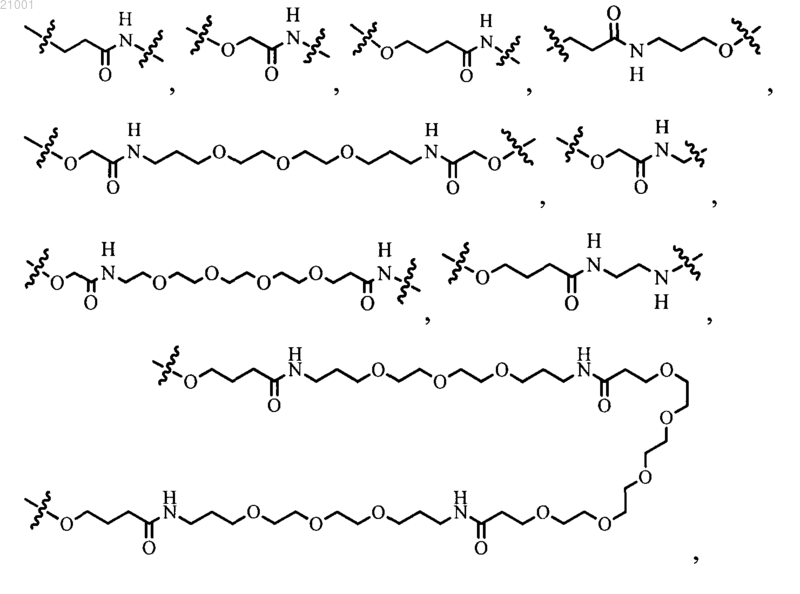
-OCCR11R12)k-, -S(CR11R12)k-, -S(O)k(CR11R12)k-, -O(CR11R12)k-NR11C(O)-, -O(CR11R12)kC(O)NR11-, -C(O)-,
-С(О)(CR11R12)k-, -C(S)-, -C(S)(CR11R12)k-, -C(O)NR11-, -NR11C(O)-, -NR11(CR11R12)k-, -CONR11(CR11R12)k-,
-N(R11)CO(CR11R12)k-, -C(O)NR11(CR11R12)k-, -NR11C(O)(CR11R12)k-, где R11 и R12, каждый независимо, обозначает Н, С1-С8алкил, замещенный галогеном С1-С8алкил или замещенный гидроксигруппой С1-С8алкил, а k равен целому числу от 1 до 12, и X1 выбран из водорастворимого полимера, полиалкиленгликоля, полиэтиленгликоля, сахара, липида, цитотоксического соединения, лекарственного средства, аффинной метки, реакционноспособного соединения, пептида, белка, антитела или фрагмента антитела, углевода, рибонуклеиновой кислоты (РНК), дезоксирибонуклеиновой кислоты (ДНК), модифицированной фосфоротиоатом ДНК, сахарида, дисахарида, олигосахарида, полисахарида, спиновой метки, флуорофора, фоточувствительного остатка, биотина, аналога биотина, агониста TLR7, фосфолипида, иммуногенного гаптена, иммуномодулятора, усилителя иммунного ответа, твердой подложки, -СН2СН2-(OCH2CH2O)р-ОХ2, -O-(CH2CH2O)рСН2СН2-Х2, а также любой комбинации указанных соединений, при этом р равен от 1 до 10000, а X2 обозначает Н или С1-С8алкил, и
где по крайней мере один АА обозначает остаток аминокислотного аналога-пирролизина формулы (А-2) или формулы (Б-2), и аминокислотный аналог-пирролизина формулы (А-2) означает аминокислотный остаток формулы (VII), и аминокислотный остаток формулы (Б-2) означает аминокислотный остаток формулы (VIII)
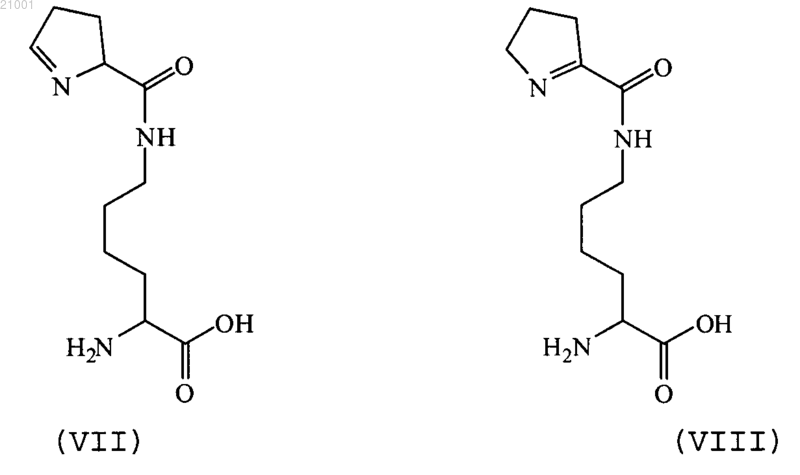
где аминокислотный остаток формулы (VII) или формулы (VIII) получают биосинтетическим способом в клетке, содержащей ген pylC и ген pylD, при этом клетку приводят в контакт с питательной средой, содержащей предшественник;
или по крайней мере один ВВ обозначает остаток аминокислотного аналога-пирролизина формулы (В-1), или формулы (Г-2), или формулы (Д-1), или формулы (Е-2), или формулы (Ж-1), или формулы (З-2), или формулы (И-1), или формулы (К-2), или формулы (Л-1), или формулы (М-2).
2. Соединение по п.1, где R6 обозначает Н.
3. Соединение по любому из пп.1-2, где R7 обозначает -LX1.
4. Соединение по любому из пп.1-3, где X1 обозначает сахар, полиэтиленгликоль, флуорофор, иммуномодулятор, рибонуклеиновую кислоту (РНК), дезоксирибонуклеиновую кислоту (ДНК), белок, пептид, биотин, фосфолипид, агонист TLR7, иммуногенный гаптен, липид, карбогидрат, модифицированную фосфоротиоатом ДНК, сахарид, дисахарид, олигосахарид, полисахарид, спиновую метку, усилитель иммунного ответа, цитотоксическое соединение или твердую подложку.
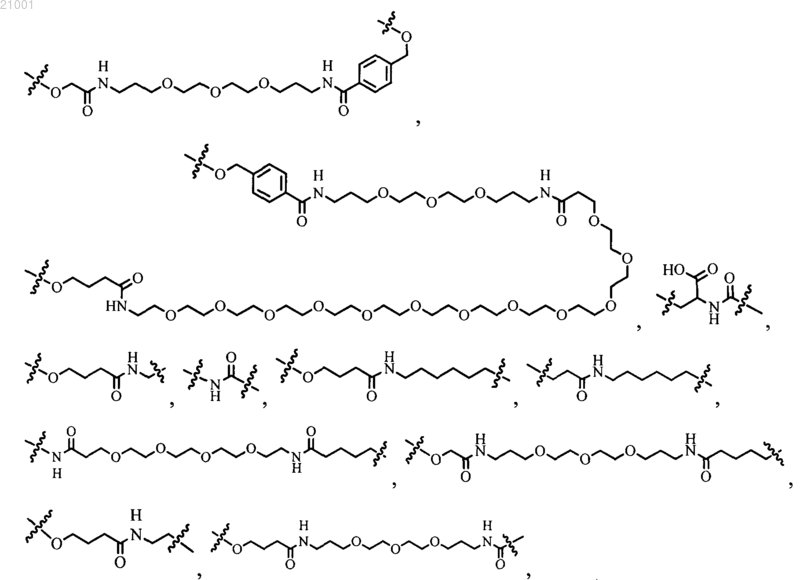
5. Соединение по любому из пп.1-4, где L обозначает связь, поли(алкиленгликоль), поли(этиленгликоль), С1-С8алкилен, замещенный галогеном С1-С8алкилен или замещенный гидроксигруппой С1-С8алкилен,
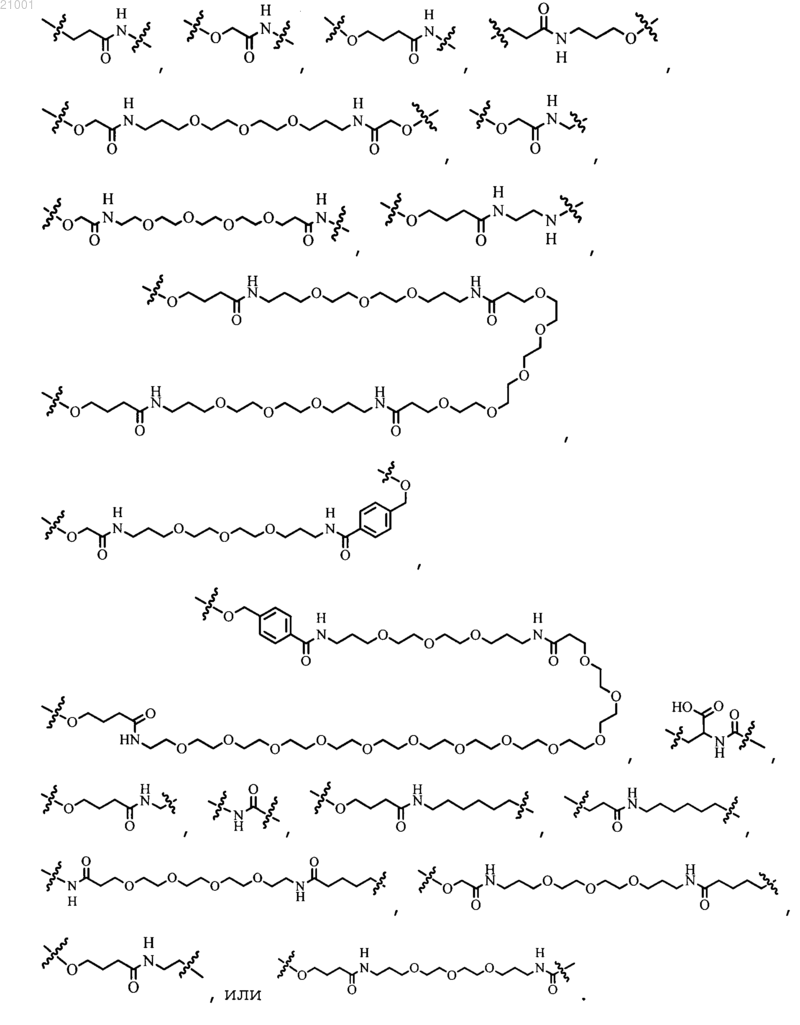
6. Соединение по п.1, где клетка содержит ген pylB, ген pylC и ген pylD.
7. Соединение по п.1 или 6, где предшественником является D-орнитин или D-аргинин, (2S)-2-амино-6-(2,5-диаминопентанамидо)гексановая кислота или (2S)-2-амино-6-((R)-2,5-диаминопентанамидо)гексановая кислота.
8. Соединение по п.1 или 6, где предшественником является D-орнитин или D-аргинин.
9. Соединение по любому из пп.1, 6, 7 или 8, где аминокислоту формулы (VII) или формулы (VIII) встраивают в белок в клетке с использованием ортогональной тРНК (О-тРНК) и ортогональной аминоацил-тРНК-синтетазы (О-РС), при этом О-РС аминоацилирует О-тРНК аминоксилотой формулы (VII) или формулы (VIII), и О-тРНК распознает кодон-селектор мРНК в клетке, и кодоном-селектором является янтарный кодон TAG.
10. Соединение по любому из пп.1, 6, 7, 8 или 9, где клетка дополнительно содержит ген pylS и ген pylT, и соединение формулы (VII) или формулы (VIII) встраивают в белок в клетке с использованием аминоацил-тРНК-синтетазы и тРНК, которая распознает по крайней мере один кодон-селектор мРНК в клетке, причем аминоацил-тРНК-синтетаза представляет собой генный продукт гена pylS, и тРНК является генным продуктом гена pylT, и кодоном-селектором является янтарный кодон TAG.
11. Соединение по любому из пп.1, 6, 7, 8, 9 или 10, где клеткой является клетка прокариотов или клетка эукариотов.
12. Соединение по п.11, где клеткой является клетка Escherichia coli, клетка млекопитающих, дрожжевая клетка, клетка насекомых, клетка СНО, клетка HeLa, клетка HEK293F или клетка sf9.
13. Способ модификации белка, где белок характеризуется формулой (I), причем указанный способ заключается в том, что белок контактирует с реагентом формулы (III) или формулы (IV); при этом формула (I) соответствует формуле
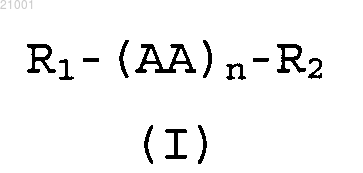
где R1 обозначает Н;
R2 обозначает ОН;
n равен целому числу от 1 до 5000;
АА, каждый независимо, выбран из аминокислотного остатка, аминокислотного остатка пирролизина, аминокислотного аналога-пирролизина формулы (А-1) и аминокислотного аналога-пирролизина формулы (Б-1);
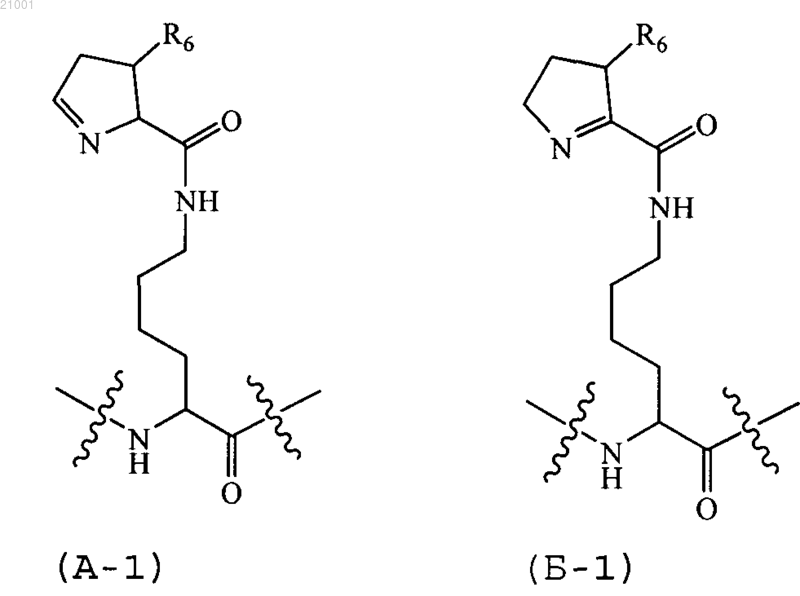
где R6 обозначает Н или С1алкил, и
по крайней мере один АА обозначает аминокислотный остаток пирролизина или аминокислотный аналог-пирролизин формулы (А-1) или формулы (Б-1), где аминокислотный остаток формулы (А-1) обозначает аминокислотный остаток формулы (V), и аминокислотный остаток формулы (Б-1) обозначает аминокислотный остаток формулы (VI)
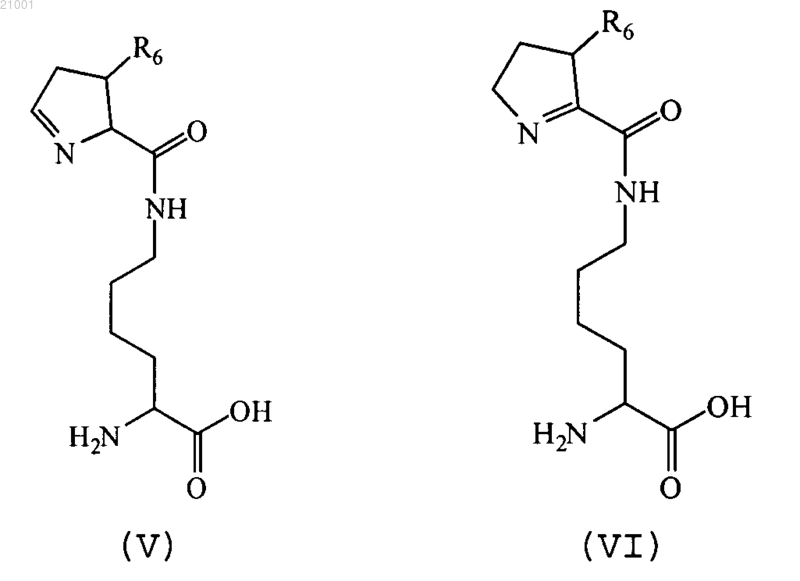
и аминокислоту формулы (V) или формулы (VI) получают биосинтетическим способом в клетке, содержащей ген pylC и ген pylD, при этом клетка контактирует с питательной средой, содержащей предшественник;
и где формула (III) и формула (IV) соответствуют формулам
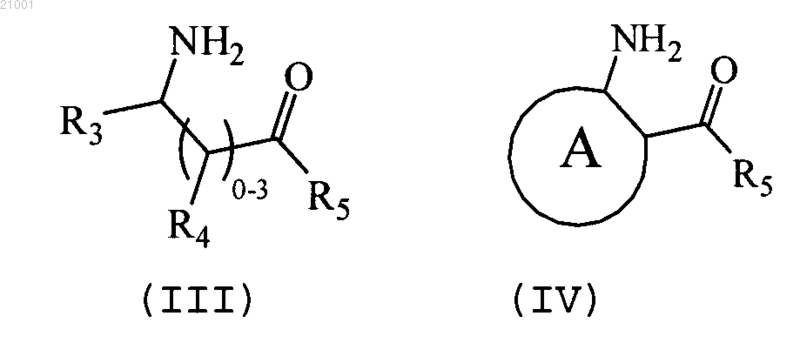
где R3, R5 и R4, каждый независимо, выбран из Н, -ОН, -NO2, галогена, С1-С8алкила, замещенного галогеном С1-8алкила, замещенного гидроксигруппой С1-С8алкила и -LX1;
А обозначает фенил, необязательно содержит от 1 до 5 заместителей, независимо выбранных из -ОН, -NO2, галогена, С1-С8алкила, замещенного галогеном С1-С8алкила, замещенного гидроксигруппой С1-С8алкила и
-LX1;
L выбран из связи, С1-С8алкилена, замещенного галогеном С1-С8алкилена, замещенного гидроксигруппой С1-С8алкилена, С2-С8алкенилена, замещенного галогеном С2-С8алкенилена, замещенного гидроксигруппой С2-С8алкенилена,
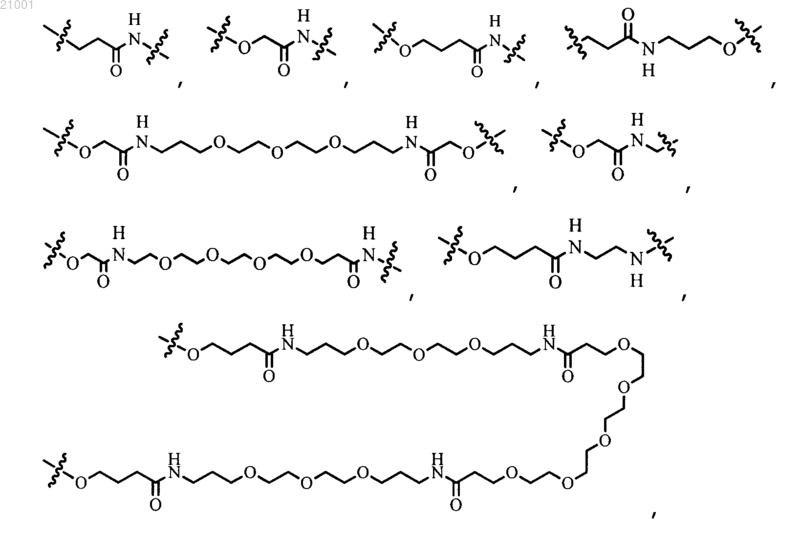
-O(CR11R12)k-, -S(CR11R12)k-, -S(O)k(CR11R12)k-, -O(CR11R12)k-NR11C(O)-, -O(CR11R12)kC(O)NR11-, -C(O)-,
-C(O)(CR11R12)k-, -C(S)-, C(S)(CR11R12)k-, -C(O)NR11-, -NR11C(O)-, -NR11(CR11R12)k-, -CONR11(CR11R12)k-,
-N(R11)CO(CR11R12)k-, -C(O)NR11(CR11R12)k-, -NR11C(O)(CR11R12)k-, где R11 и R12, каждый независимо, обозначает Н, С1-С8алкил, замещенный галогеном С1-С8алкил или замещенный гидроксигруппой С1-С8алкил, а k равен целому числу от 1 до 12, и
X1 выбран из водорастворимого полимера, полиалкиленгликоля, полиэтиленгликоля, сахара, липида, цитотоксического соединения, лекарственного средства, аффинной метки, реакционноспособного соединения, смолы, пептида, белка, антитела или фрагмента антитела, углевода, рибонуклеиновой кислоты (РНК), дезоксирибонуклеиновой кислоты (ДНК), модифицированной фосфоротиоатом ДНК, сахарида, дисахарида, олигосахарида, полисахарида, спиновой метки, флуорофора, фоточувствительного остатка, биотина, аналога биотина, агониста TLR7, фосфолипида, иммуногенного гаптена, иммуномодулятора, усилителя иммунного ответа, твердой подложки, -СН2СН2-(OCH2CH2O)P-OX2, -O-(CH2CH2O)рСН2СН2-Х2, а также любой комбинации указанных соединений, при этом р равен от 1 до 10000, а X2 обозначает Н или С1-С8алкил.
14. Способ по п.13, где аминокислоту формулы (V) или формулы (VI) получают биосинтетическим способом в клетке, содержащей ген pylB, ген pylC и ген pylD, при этом клетка контактирует с питательной средой, содержащей предшественник.
15. Способ по п.13 или 14, где аминокислотой формулы (V) является аминокислота формулы (VII) и аминокислота формулы (VI) является аминокислотой формулы (VIII)
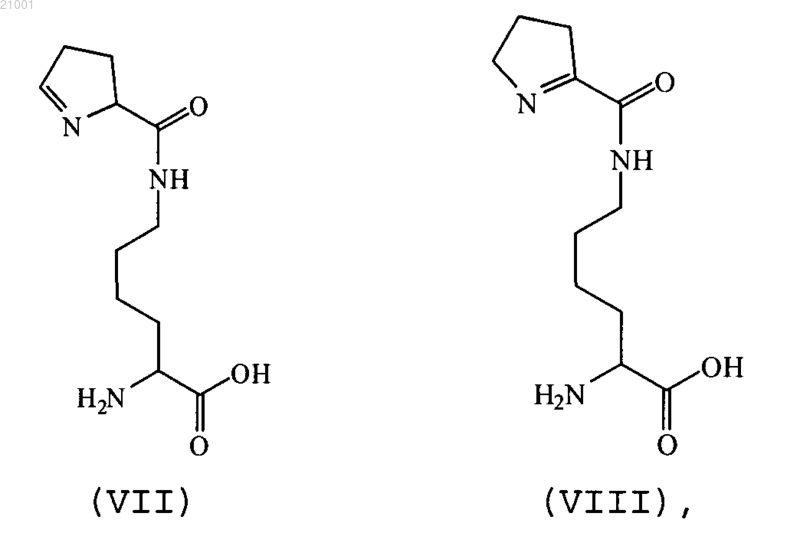
а предшественником является D-орнитин, D-аргинин, (2S)-2-амино-6-(2,5-диаминопентанамидо)гексановая кислота или (2S)-2-амино-6-((R)-2,5-диаминопентанамидо)гексановая кислота.
16. Способ по п.13 или 14, где аминокислотой формулы (V) является аминокислота формулы (IX)
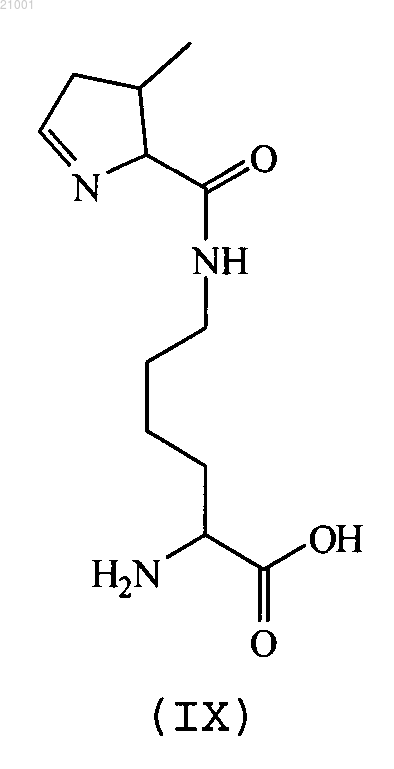
а предшественником является D-орнитин, D-аргинин, 2,5-диамино-3-метилпентановая кислота, (2S)-2-амино-6-(2,5-диаминопентанамидо)гексановая кислота или (2S)-2-амино-6-((R)-2,5-диаминопентанамидо)гексановая кислота и аминокислотой формулы (VI) является аминокислота формулы (X)
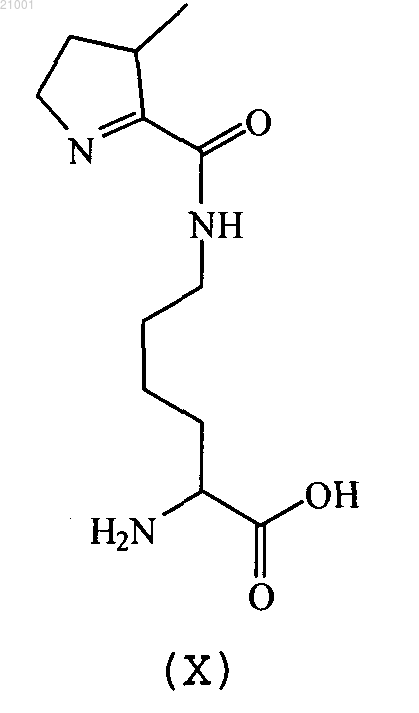
а предшественником является D-орнитин, D-аргинин, 2,5-диамино-3-метилпентановая кислота, (2R,3S)-2,5-диамино-3-метилпентановая кислота, (2R,3R)-2,5-диамино-3-метилпентановая кислота, (2S)-2-амино-6-(2,5-диаминопентанамидо)гексановая кислота или (2S)-2-амино-6-((R)-2,5-диаминопентанамидо)гексановая кислота.
17. Способ по любому из пп.13-16, где аминокислоту формулы (V), формулы (VI), формулы (VII), формулы (VIII), формулы (IX) или формулы (X) встраивают в белок в клетке с использованием ортогональной тРНК (О-тРНК) и ортогональной аминоацил-тРНК-синтетазы (О-PC), при этом О-PC аминоацилирует О-тРНК аминокислотой формулы (V) или формулы (VI), и О-тРНК распознает по крайней мере один кодон-селектор мРНК в клетке и кодоном-селектором является янтарный кодон TAG.
18. Способ по любому из пп.13-17, где клетка, кроме того, содержит ген pylS и ген pylT, и аминокислоту формулы (V), формулы (VI), формулы (VII), формулы (VIII), формулы (IX) или формулы (X) встраивают в белок в клетке с использованием аминоацил-тРНК-синтетазы и тРНК, которая распознает по крайней мере один кодон-селектор мРНК в клетке, причем аминоацил-тРНК-синтетаза представляет собой генный продукт гена pylS, а тРНК является генным продуктом гена pylT, и кодоном-селектором является янтарный кодон TAG.
19. Способ по любому из пп.13-18, где клеткой является клетка прокариотов или клетка эукариотов.
20. Способ по п.19, где клеткой является клетка Escherichia coli, клетка млекопитающих, дрожжевая клетка, клетка насекомых, клетка СНО, клетка HeLa, клетка HEK293F или клетка sf9.
21. Способ по любому из пп.13-20, где модифицированный белок характеризуется формулой (II)
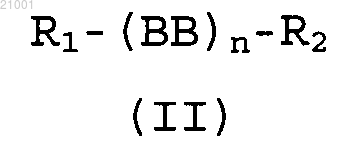
где R1 обозначает Н;
R2 обозначает ОН;
n равен целому числу от 1 до 5000;
ВВ, каждый независимо, выбран из аминокислотного остатка, аминокислотного аналога-пирролизина формулы (А-1), аминокислотного аналога-пирролизина формулы (Б-1), аминокислотного аналога-пирролизина формулы (В-1), аминокислотного аналога-пирролизина формулы (Г-2), аминокислотного аналога-пирролизина формулы (Д-1), аминокислотного аналога-пирролизина формулы (Е-2), аминокислотного аналога-пирролизина формулы (Ж-1), аминокислотного аналога-пирролизина формулы (З-2), аминокислотного аналога пирролизина формулы (И-1), аминокислотного аналога-пирролизина формулы (К-2), аминокислотного аналога-пирролизина формулы (Л-1) и аминокислотного аналога-пирролизина формулы (М-2),
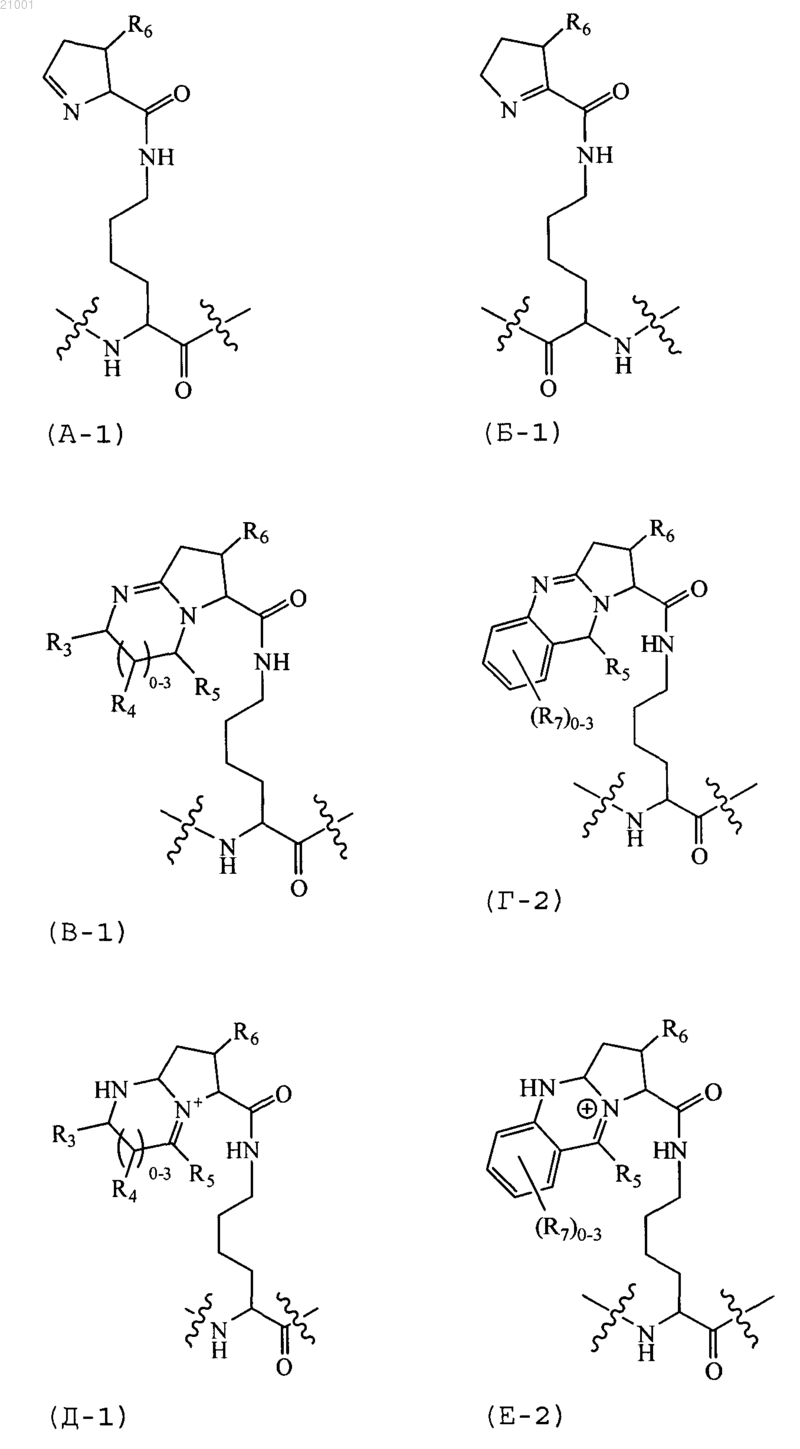
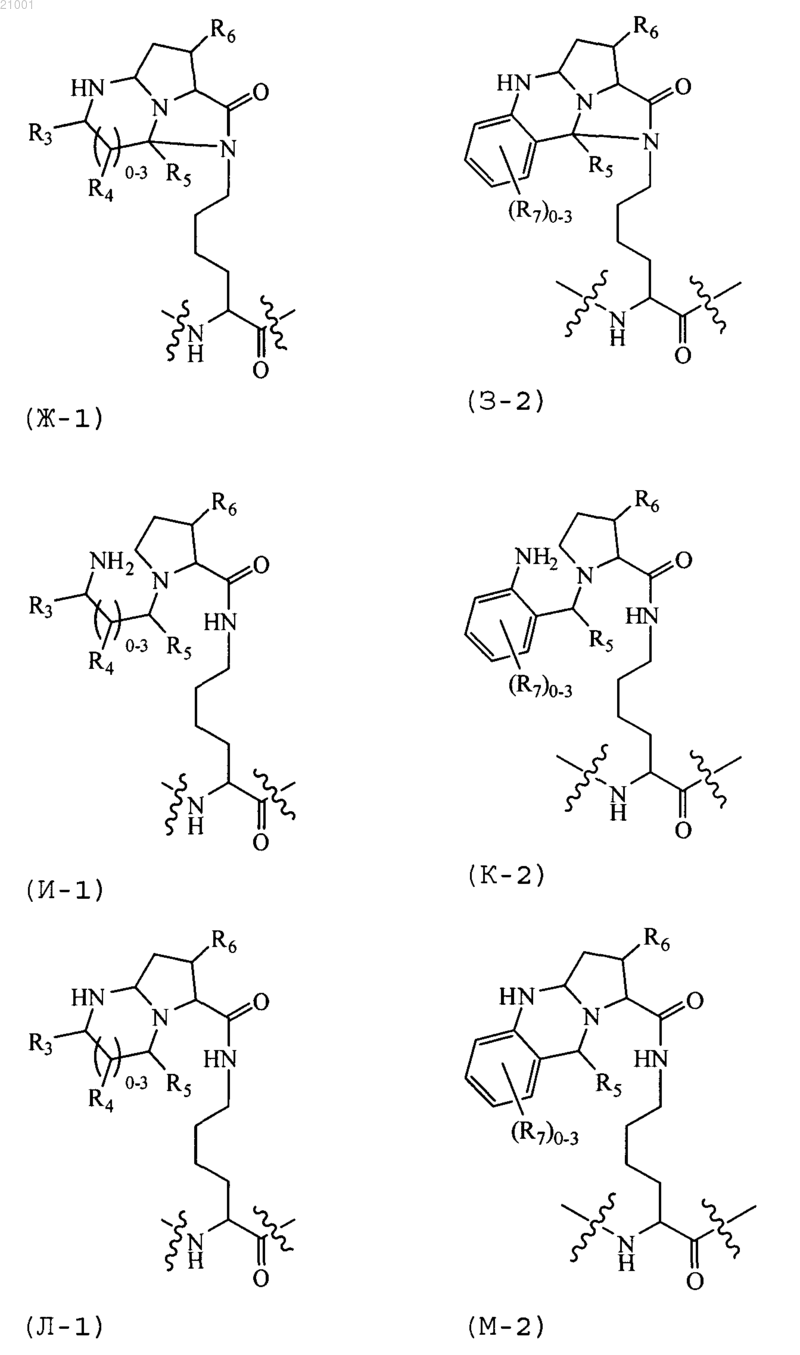
где по крайней мере один ВВ обозначает остаток аминокислотного аналога-пирролизина формулы (В-1), или формулы (Г-2), или формулы (Д-1), или формулы (Е-2), или формулы (Ж-1), или формулы (З-2), или формулы (И-1), или формулы (К-2), или формулы (Л-1), или формулы (М-2).
22. Способ по любому из пп.13-21, где R6 обозначает Н.
23. Способ по любому из пп.13-22, где R7 обозначает -LX1.
24. Способ по любому из пп.13-23, где X1 обозначает сахар, полиэтиленгликоль, флуорофор, иммуномодулятор, рибонуклеиновую кислоту (РНК), дезоксирибонуклеиновую кислоту (ДНК), белок, пептид, биотин, фосфолипид, агонист TLR7, иммуногенный гаптен, липид, карбогидрат, модифицированную фосфоротиоатом ДНК, сахарид, дисахарид, олигосахарид, полисахарид, спиновую метку, усилитель иммунного ответа, цитотоксическое соединение или твердую подложку.
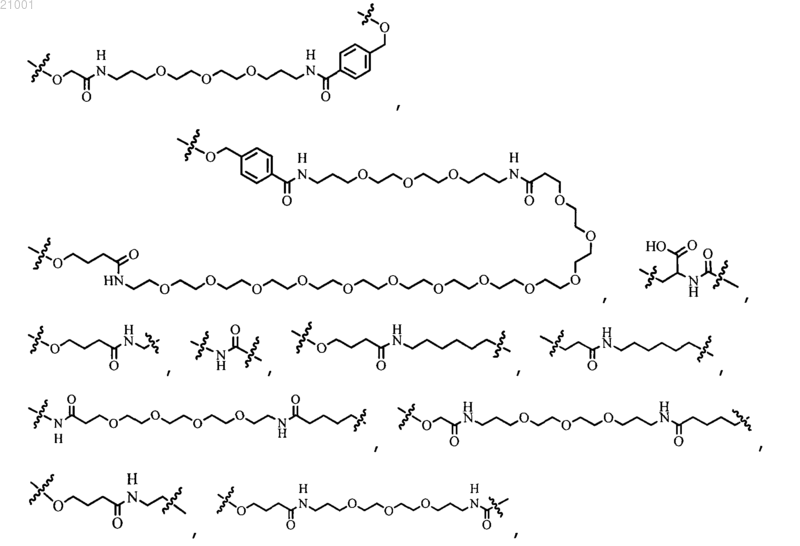
25. Способ по любому из пп.13-22, где реагент формулы (IV) характеризуется следующими структурами:
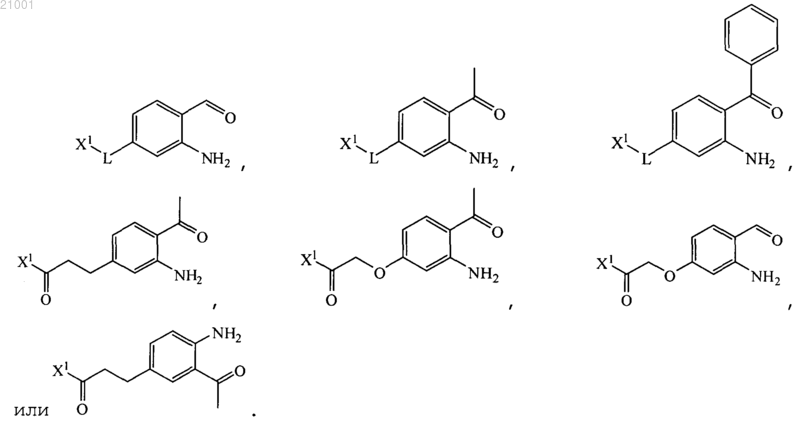
26. Способ по любому из пп.13-22, где реагент формулы (IV) выбран из следующих структур:
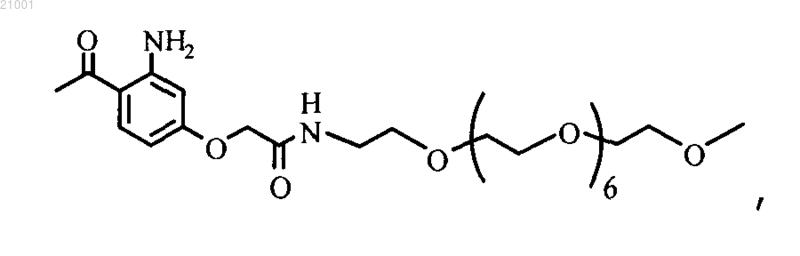
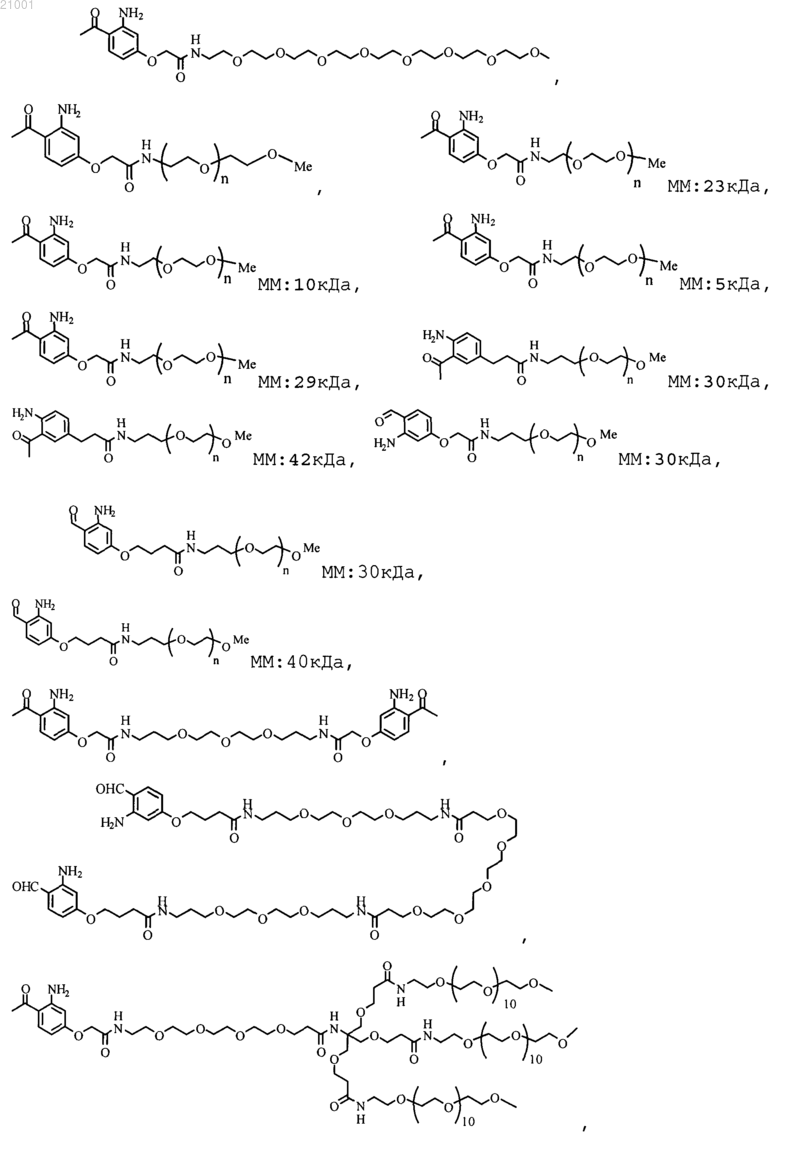
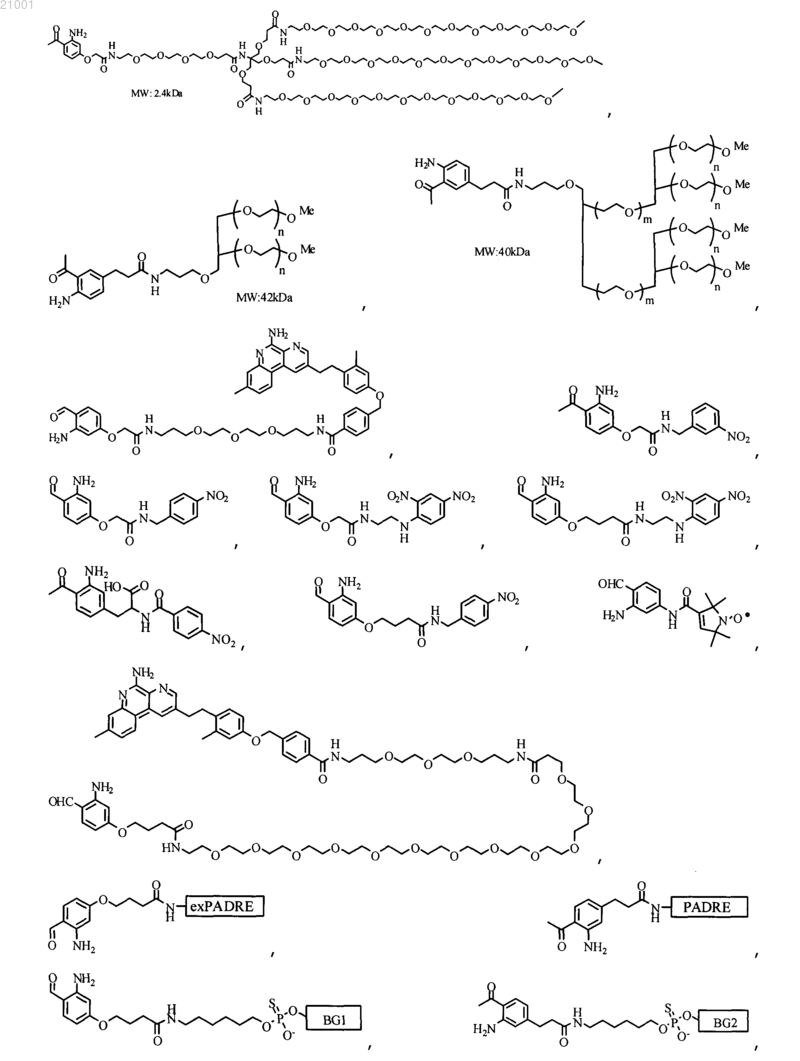

где exPADRE обозначает пептид, соответствующий SEQ ID NO:28,
PADRE обозначает пептид, соответствующий SEQ ID NO:29,
BG1 обозначает полинуклеотид, соответствующий SEQ ID NO:30,
BG2 обозначает полинуклеотид, соответствующий SEQ ID NO:31.
Текст
БИОСИНТЕТИЧЕСКИЙ ПИРРОЛИНКАРБОКСИЛИЗИН И САЙТ-СПЕЦИФИЧНЫЕ МОДИФИКАЦИИ БЕЛКА ЗА СЧЕТ ХИМИЧЕСКОЙ МОДИФИКАЦИИ ОСТАТКОВ ПИРРОЛИНКАРБОКСИЛИЗИНА И ПИРРОЛИЗИНА 61/108,434 2008.10.24 В заявке описан пирролинкарбоксилизин (PCL), аналог пиролизина, который представляет собой природную, полученную биосинтетическим способом аминокислоту, и способы биосинтеза PCL. В заявке также описаны белки, полипептиды и пептиды, которые содержат встроенный PCL, и способы встраивания PCL в указанные белки, полипептиды и пептиды. В заявке также описана сайт-специфичная модификация белков, полипептидов и пептидов, содержащих встроенный PCL или пирролизин. В заявке также описано сшивание белков, полипептидов и пептидов, содержащих встроенный PCL или пирролизин. Родственные заявки В настоящей заявке испрашивается приоритет согласно 35 U.S.С.119(е) в связи с предварительной заявкой US61/108434, поданной 24 октября 2008 г. Содержание предварительных заявок включено в полном объеме в настоящее описание в качестве ссылок. Область изобретения Настоящее изобретение относится к селективному встраиванию генетически кодируемых аминокислот в белки. Настоящее изобретение относится также к химической модификации указанных аминокислот. Предпосылки создания настоящего изобретения Природные метиламинметилтрансферазы метаногенных архей семейства Methanosarcina содержат пирролизин (PYL). Пирролизин представляет собой аналог лизина, который при совместной трансляции кодируется кодонами UAG внутри рамки считывания в соответствующих мРНК, и является 22-й природной аминокислотой. Краткое описание фигур Фиг. 1 - структуры пирролизина (PYL) и аналога пирролизина, пирролинкарбоксилизина (PCL:PCL-A или PCL-B). Фиг. 2 - сравнение возможных путей биосинтеза пирролизина (A) и PCL (В). Фиг. 3 - аминоацилирование тРНК pylT пирролизином (А) и PCL (B). Фиг. 4 А - плазмиды, содержащие pylT, pylS, pylB, pylC и pylD, для встраивания биосинтетическогоPCL или пирролизина в клетки млекопитающих, а также содержащие генный конструкт с одиночными мутантными сайтами TAG для модельного белка hRBP4. Фиг. 4 Б - генные конструкты с одиночными мутантными сайтами TAG для hRBP4, мЭПО (мышиный эритропоэтин), чЭПО и mIgG1. Одиночные сайты показаны стрелкой. Фиг. 5 - плазмида, содержащая pylT, pylS, pylB, pylC и pylD, для встраивания биосинтетическогоPCL или пирролизина в клетки Escherichia coli. Фиг. 6 А - экспрессия hRBP4 в клетках HEK293F. Мутантные TAG конструкты hRBP4 ( 1-9). Электрофорез в полиакриламидном геле с использованием додецилсульфата натрия (ДСН-ПААГ) с последующим вестерн-блоттингом в присутствии антитела против His. Стрелка, соответствующая 26 кДа,указывает на полноразмерный hRBP4. Фиг. 6 Б и 6 В - электрофорез в геле ДСН-ПААГ (А) и масс-спектр (Б) очищенного Phe62PCL hRBP4,продуцируемого в клетках HEK293F в присутствии D-орнитина. Фиг. 7 - масс-спектрометрический анализ триптического гидролизата Phe122PCL hRBP4 свидетельствует о встраивании PCL в требуемый сайт Phe122TAG. Соотнесенный МС/МС спектр YWGVASFLQK (F обозначает PCL) (SEQ ID NO:17). Фиг. 8 - масс-спектрометрический анализ (TIC и EIC для ионов 2+ YWGVASFLQK) (SEQ IDNO:17) триптического гидролизата Phe122PCL hRBP4 свидетельствует о встраивании PCL в требуемый сайт Phe122TAG. Фиг. 9 - масс-спектрометрический анализ триптического гидролизата Phe122PCL hRBP4. На массспектре присутствуют сигналы, соответствующие предшественникам 3+ и 2+ YWGVASFLQK (SEQ IDNO:17), что свидетельствует о встраивании PCL в требуемый сайт Phe122TAG. Фиг. 10 - детектирование PCL, биосинтезированного из D-орнитина, в лизате клеток HEK293F. Фиг. 11 - встраивание Nциклопентилоксикарбонил-L-лизина (CYC) в различные белки hRBP4 с мутантными сайтами TAG в клетках HEK293F. На фиг. 11 А показано встраивание CYC в различные сайты hRBP4, детектируемое методом электрофореза в геле ДСН-ПААГ и методом вестерн-блоттинга с использованием антител против His-tag и против RBP4. На фиг. 11 Б представлены результаты электрофореза в геле ДСН-ПААГ очищенного Phe62CYC hRBP4 (мутант 2). На фиг. 11 В представлен массспектр Phe62CYC hRBP4. Фиг. 12 - масс-спектрометрическое подтверждение встраивания CYC в сайт TAG белка hRBP4, мутантного по Phe62CYC. Фиг. 13 - встраивание PCL в зависимости от различных предшественников и прямое встраивание различных аналогов пирролизина (включая CYC) в мутантный по сайту TAG белок hRBP4 с использованием клеток HEK293F (фиг. 13 А и 13 Б), а также встраивание PCL с использованием различных комбинаций биосинтетических генов pylB, pylC и pylD (фиг. 13 В). На фиг. 13 А представлен вестерн-блоттинг неочищенных образцов с использованием антител против His-tag, а на фиг. 13 Б представлен электрофорез в геле ДСН-ПААГ белка, очищенного металл-хелатной хроматографией на колонке Ni-NTA. Фиг. 14 - потенциальные предшественники биосинтеза PCL (А) и различных аналогов пирролизина(Б). Фиг. 15 - оценка различных предшественников и генных комбинаций для встраивания PCL в FASTE в клетках НК 100. Фиг. 16 - предполагаемая схема биосинтеза PCL (PCL-A). Фиг. 17 А - сайт-специфичное встраивание биосинтетического PCL в одиночные кодируемые сайтыTAG (одиннадцать сайтов) в эритропоэтин (ЭПО), детектируемое методом электрофореза в геле ДСНПААГ. Фиг. 18 - сайт-специфичное встраивание биосинтетического PCL в одиночные кодируемые сайтыTAG (два сайта) в домен тиоэстеразы жирная кислота-синтетазы (FAS-TE) человека. На фиг. 18 представлены электрофорез в геле ДСН-ПААГ (А) и масс-спектр встраивания PCL (Б). Фиг. 19 - сайт-специфичное встраивание биосинтетического PCL в одиночный кодируемый сайтTAG (двадцать сайтов) в фактор роста фибропластов 21 (FGF21). Результаты электрофореза в геле ДСНПААГ свидетельствуют о встраивании PCL в FGF21 по множеству сайтов. Фиг. 21. На фиг. 21 А представлен анализ методом электрофореза в геле ДСН-ПААГ встраиванияPYL или PCL в мФНО-, содержащий глутамин Gln21 (САА), мутированный до стоп-кодона TAG, в присутствии и в отсутствие pylB. На фиг. 21 Б представлена оценка чистоты белка методом электрофореза в геле ДСН-ПААГ. На фиг. 21 В представлены интактные масс-спектры Tyr10TAG mEGF, экспрессированного в клетках Escherichia coli, свидетельствующие о присутствии смеси белков, содержащих встроенный PYL или PCL (фиг. 21 В, нижний МС) и предпочтительно PCL (фиг. 21 В, верхний МС). Фиг. 22 - предполагаемые схемы реакций для химической модификации PCL 2-аминобензальдегидом. Фиг. 23 - конъюгаты белков и изменение массы в результате модификации PCL 2-аминобензальдегидом, 2-аминоацетофеноном и 2-амино-5-нитробензофеноном. Фиг. 24 - масс-спектрометрический анализ Phe122PCL hRBP4, модифицированного 2-аминобензальдегидом (2-АБА). Фиг. 25 - масс-спектрометрический анализ триптического гидролизата белка Phe122PCL hRBP4,модифицированного 2-АБА, подтверждает модификацию остатка PCL, встроенного в сайт TAG. ПептидYWGVASFLQK (SEQ ID NO:17). Фиг. 26 - оценка зависимости модификации Phe122PCL hRBP4 в присутствии 2-АБА от рН. Фиг. 27 - оценка эффективности реакции в зависимости от соотношения концентраций реагента белка и реакционной способности в отношении 2-АБА, 2-АНБФ и 2-ААФ. Фиг. 28 - модификация при молярных соотношениях более 4700 (А: 4700-кратный избыток 2-АБА по сравнению с белком) и для hRBP4 со встроенным OMePhe (Б: 15400-кратный избыток). Фиг. 29 - модификация Tyr2454PCL FAS-TE 2-аминоацетофеноном (2-ААФ). Масс-спектры непрореагировавших образцов (А и В), а также образцов, модифицированных 2-ААФ при рН 5,0 (Б) и 7,4 (Г). Фиг. 30 - основная схема реакций для сайт-специфичной химической модификации белков по остаткам пирролизина и/или PCL 2-аминобензальдегидом или аналогами 2-аминобензальдегида. Фиг. 31 - иллюстрация варианта осуществления настоящего изобретения: модифицированный полимер ПЭГ, 2-аминоацетофенон-ПЭГ 8 (2-ААФ-ПЭГ 8, TU3205-044), конденсированный с белками через остаток PCL, встроенный в белок. Фиг. 32 - модификация Phe122PCL hRBP4 в присутствии 2-ААФ-ПЭГ 8. Масс-спектр hRBP4, содержащего PCL, встроенный в положении 122, после модификации реагентом 2-ААФ-ПЭГ 8 при рН 7,5(А) и 5,0 (Б) по сравнению с масс-спектрами непрореагировавшего белка Phe122PCL hRBP4 (В) и hRBP4 дикого типа в присутствии и в отсутствие (фиг. 32 Г и 32 Д соответственно) добавленного 2-ААФ-ПЭГ 8. Фиг. 33 - модификация Tyr2454PCL FAS-TE в присутствии 2-ААФ-ПЭГ 8. Масс-спектр непрореагировавшего белка (А) и белка Tyr2454PCL FAS-TE после реакции с 2-ААФ-ПЭГ 8 (TU3205-044) (Б). На фиг. 33 В и 33 Г показана модификация Tyr2454PCL FAS-TE в присутствии 2-ААФ-ПЭГ (TU3205-048),характеризующегося массой 2,4 кДа (на фиг. 33 В показана модификация при комнатной температуре, а на фиг. 33 Г показана модификация при 4 С). Фиг. 34 - ПЭГилирование Tyr2454PCL FAS-TE в присутствии 2-ААФ-ПЭГ (2-ААФ-ПЭГ 8), характеризующегося массой 0,5 кДа, в присутствии 2-ААФ-ПЭГ, характеризующегося массой 2,4 кДа, а также в присутствии 2-ААФ-ПЭГ, характеризующегося массой 23 кДа, при указанных молярных соотношениях. Фиг. 35 - модификация Lys81PCL FGF21 в присутствии 2-ААФ-ПЭГ 8. Масс-спектры непрореагировавшего Lys84PCL FGF21 (А) и Lys84PCL FGF21 после модификации 2-ААФ-ПЭГ 8 (Б). Фиг. 36 - ПЭГилирование белков FGF21. Результаты электрофореза в геле ДСН-ПААГ, полученные после модификации семи мутантных белков PCL FGF21 в присутствии 2-ААФ-ПЭГ, характеризующегося массой 23 кДа, свидетельствуют о присутствии ПЭГ-FGF21, полноразмерного (ПР) FGF21-PCL и укороченного (УК) FGF21-PCL до (А) и после частичной очистки (Б). Фиг. 37 - ПЭГилирование белков ЭПО. Результаты электрофореза в геле ДСН-ПААГ после модификации мутантных мышиных белков PCL ЭПО в присутствии 2-ААФ-ПЭГ, характеризующегося массой 23 кДа. Фиг. 38 - модификация PCL аминосахарами. Общая схема реакций, на которой D-маннозамин кон-2 021001PCL, встроенный в положении 122, после реакции с маннозамином. Фиг. 40 - модификация Leu2222PCL FAS-ТЕ D-маннозамином. Масс-спектры непрореагировавшей жирная кислота-синтетазы (FAS-ТЕ) человека, включающей PCL, встроенный в положении 2222 (FASTE Leu2222PCL/Leu2223Ile), (А) и белка, прореагировавшего с маннозамином (Б). Фиг. 41 - иллюстрация варианта сайт-специфичного присоединения олигосахарида к белку за счет взаимодействия остатка 2-АБА, связанного с олигосахаридом, с PCL, встроенным в белок. Фиг. 42 - иллюстрация некоторых вариантов конъюгата белок-белок (гетеродимеров, гетеротримеров, гомотримеров), образованных при сшивании белков, включающих встроенный PCL. Фиг. 43 - образование гомодимеров в присутствии специфичного в отношении PCL бифункционального сшивателя на примере белка Lys84PCL FGF21. На фиг. 43 А представлен типичный пример (но,не ограничиваясь только им) бифункционального сшивателя, используемого для образования гомодимера, а на фиг. 43 Б представлен масс-спектр реакционной смеси Lys84PCL FGF-21, сшитого с использованием указанного бифункционального сшивателя. Фиг. 44 - образование гомодимера мутантного белка PCL FGF-21 в присутствии бифункционального сшивателя. На фиг. 44 А представлен масс-спектр сшитого FGF-21, причем условия реакции отличаются от условий реакции, использованных на фиг. 43. Фиг. 45 - вариант сшивателя, используемого для образования тримеров. Фиг. 46 - иллюстрация различных вариантов сайт-специфичных меток и их включения с использованием способов по настоящему изобретению. Фиг. 47. На фиг. 47 А представлен МС (ESI) mEGF-Y10PCL, конъюгированного с биотином. На фиг. 47 Б представлен вестерн-блоттинг конъюгата mEGF-Y10PCL-АБА-биотин с использованием конъюгата пероксидазы хрена (HRP) и козьих антител против биотина. На фиг. 47 В представлен МС (ESI) mEGFY10PCL, конъюгированного с флуоресцеином. На фиг. 47 Г представлен МС (ESI) mEGF-Y10PCL, конъюгированного с дисахаридом. Фиг. 48. На фиг. 48 А представлен МС (ESI) мФНО-Q21PCL, конъюгированного с мононитрофенилгаптеном. На фиг. 48 Б показан МС (ESI) mEGF-Y10PCL, конъюгированного с мононитрофенилгаптеном. На фиг. 48 В представлен масс-спектрометрический анализ (ESI) мФНО-Q21PCL, конъюгированного с динитрофенилгаптеном. На фиг. 48 Г представлен МС (ESI) mEGF-Y10PCL, конъюгированного с динитрофенилгаптеном. Фиг. 49. На фиг. 49 А представлен МС (ESI) mEGF-Y10PCL, конъюгированного с агонистом TLR7,на фиг. 49 Б показан МС (ESI) mEGF-Y10PCL, конъюгированного с фосфолипидом. Фиг. 50. На фиг. 50 А и 50 Б показан МС (MALDI-TOF) конъюгата мФНО-Q21PCL и РХ 2-PADRE,полученного при двух различных значениях рН (фиг. 50 А: рН 5,0, фиг. 50 Б: рН 7,5). На фиг. 50 В показан МС (ESI) конъюгата мФНО-Q21PCL и BHA-exPADRE. На фиг. 51 представлен МС (ESI), иллюстрирующий конденсацию BHA-exPADRE и mEGFY10PCL. Фиг. 52. На фиг. 52 А представлен анализ изменения подвижности в геле при конденсации BHABG1 (7,4 кДа) и BHA-BG2 (7,4 кДа) с мФНО-Q21PCL (19,3 кДа). На фиг. 52 Б показан анализ изменения подвижности в геле при конденсации BHA-BG2 (7,4 кДа) с mEGF-Y10PCL (7,2 кДа). На фиг. 53 представлена иллюстрация варианта указанного сайт-специфичного ориентированного присоединения. Фиг. 54. На фиг. 54 А представлен МС (ESI) hFGF21-K150PCL, конъюгированного с 2-АБА и затем восстановленного в присутствии 20 мМ NaCNBH3 в течение 1 ч. На фиг. 54 Б представлен МС (ESI) восстановленного конъюгата hFGF21-K150PCL 2-АБА после диализа в 10 мМ фосфатном буферном растворе (рН 7,5) и инкубации при 50 С в течение 1 сут. Фиг. 55. На фиг. 55 показана стабильность связи PCL в пэгилированном FGF21 при восстановлении и без восстановления в присутствии NaCNBH3. На фиг. 55 А показан электрофорез в геле ДДС-ПААГ восстановленных образцов и невосстановленных образцов. Кроме того, на фиг. 55 Б представлен электрофорез в геле ДСН-ПААГ невосстановленных образцов, инкубированных в течение 60 ч при 4 С, при комнатной температуре, при 37 С, 50 С, а также при 95 С. Фиг. 56 - анализ методом ЯМР реакции PCL-A с 2-АБА. Фиг. 57. На фиг. 57 А представлена предполагаемая структура продукта реакции между PCL-A и 2 АБА. На фиг. 57 Б представлены равновесные структуры продукта реакции между PCL-A и 2-АБА. На фиг. 57 В представлена предполагаемая структура восстановленного продукта. Фиг. 58 - анализ методом ЯМР реакции PCL-B с 2-АБА. Фиг. 59 - модификация пирролизина (PYL) и PCL, встроенных в mEGF. Краткое описание сущности изобретения В настоящем изобретении предлагаются белки и/или полипептиды, содержащие один или более встроенных остатков PCL, при этом PCL получают биосинтетическим методом и встраивают в белки и/или полипептиды. В настоящем изобретении также предлагаются белки и/или полипептиды, содержащие один или более встроенных остатков пирролизина (PYL), причем PYL получают биосинтетическим методом и встраивают в белки и/или полипептиды. В настоящем изобретении предлагаются также белки и/или полипептиды, содержащие один или более встроенных остатков PCL, а также один или более встроенных остатков PYL, причем PCL и PYL получают биосинтетическим методом и встраивают в белки и/или полипептиды. В настоящем изобретении предлагаются также белки и/или полипептиды, содержащие один или более встроенных остатков PCL, при этом PCL получают биосинтетическим методом и встраивают в белки и/или полипептиды, причем один или более остатков PCL модифицируют при присоединении к белкам и/или полипептидам группы, выбранной из метки, красителя, полимера, водорастворимого полимера, полиалкиленгликоля, полиэтиленгликоля, производного полиэтиленгликоля, сахара, липида, фотосшивателя, цитотоксического соединения, лекарственного средства, аффинной метки, фотоаффинной метки, реакционноспособного соединения, смолы, пептида, второго белка или полипептида или аналога полипептида, антитела или фрагмента антитела, металлохелатного соединения, кофактора, жирной кислоты, углевода, полинуклеотида, ДНК, РНК, зонда ПЦР, антисмыслового полинуклеотида, рибоолигонуклеотида, дезоксирибоолигонуклеотида, модифицированной фосфоротиоатом ДНК, модифицированных ДНК и РНК, пептидонуклеиновой кислоты, сахарида, дисахарида, олигосахарида, полисахарида,водорастворимого дендримера, циклодекстрина, биоматериала, наночастицы, спиновой метки, флуорофора, металлсодержащего остатка, радиоактивного остатка, новой функциональной группы, группы, которая ковалентно или не ковалентно взаимодействует с другими молекулами, фоточувствительного остатка, остатка, который возбуждается при актиничном излучении, лиганда, фотоизомеризующегося остатка, биотина, аналога биотина, остатка, содержащего тяжелый атом, химически расщепляемой группы,фоторасщепляемой группы, остатка с удлиненной боковой цепью, связанного с атомом углерода сахара,восстановительно-окислительного агента, аминотиокислоты, токсичного остатка, изотопно-меченого остатка, биофизического зонда, фосфоресцентной группы, хромофорной группы, хемилюминесцентной группы, флуоресцентного остатка, группы с электронной плотностью, магнитной группы, интеркалирующей группы, хелатирующей группы, хромофора, энергопереносящего агента, биологически активного агента, детектируемой метки, низкомолекулярной молекулы, ингибирующей рибонуклеиновой кислоты, киРНК, радионуклеотида, нейтрон-захватывающего агента, производного биотина, квантовой точки(ек), наномедиатора, радиомедиатора, абзима, фермента, активированного комплексного активатора,вируса, токсина, адъюванта, агониста TLR2, агониста TLR4, агониста TLR7, агониста TLR9, агонистаTLR8, Т-клеточного эпитопа, фосфолипида, ЛПС-подобной молекулы, гемоцианина моллюска фисурелла, иммуногенного гаптена, агликана, аллергена, ангиостатина, антигормона, антиоксиданта, аптамера,гидовой РНК, сапонина, шаттл-вектора, макромолекулы, мимотопа, рецептора, обратной мицеллы, ПАВ,усилителей иммунного ответа, флуоресцентных красителей, реагентов FRET, зондов для радиовизуализации, другого спектроскопического зонда, пролекарств, токсинов для иммунотерапии, твердой подложки, -СН 2 СН 2-(OCH2CH2O)р-ОХ 2 и -О-(CH2CH2O)pCH2CH2-Х 2 (где р равен от 1 до 10000, а X2 обозначает Н, С 1-С 8 алкил, защитную группу или концевую функциональную группу). В некоторых вариантах указанные белки и/или полипептиды содержат один или более встроенных остатков PYL, где PYL получают биосинтетическим методом и встраивают в белки и/или полипептиды,причем пирролизин модифицируют при присоединении к белкам и/или полипептидам одной из упомянутых выше групп, приведенных для белков и/или полипептидов, содержащих один или более встроенных остатков PCL. В других вариантах указанные белки и/или полипептиды содержат один или более встроенных остатков PCL и один или более встроенных остатков PYL, при этом PCL и PYL получают биосинтетическим методом и встраивают в белки и/или полипептиды, причем PCL и пирролизин модифицируют при присоединении к белкам и/или полипептидам одной из упомянутых выше групп, приведенных для белков и/или полипептидов, содержащих один или более встроенных остатков PCL. В некоторых вариантах указанный упомянутый выше биосинтез проводят в клетках эукариотов,клетках млекопитающих, дрожжевых клетках или в клетках насекомых. В других вариантах клетками являются клетки Escherichia coli, в то время как в некоторых вариантах дрожжевыми клетками являются клетки Saccharomyces cerevisiae или Pichia pastoralis. В других вариантах клетками являются клетки СНО, клетки HeLa, клетки HEK293F или клетки sf9. В одном объекте настоящего изобретения предлагаются соединения формулы (I) или формулы (II) где R1 обозначает Н или N-концевую модифицирующую группу,R2 обозначает ОН или С-концевую модифицирующую группу,-4 021001n равен целому числу от 1 до 5000,АА каждый независимо выбирают из аминокислотного остатка, аминокислотного аналогапирролизина формулы (А-2) и аминокислотного аналога-пирролизина формулы (Б-2),ВВ каждый независимо выбирают из аминокислотного остатка, аминокислотного аналогапирролизина формулы (А-2), аминокислотного аналога-пирролизина формулы (Б-2), аминокислотного аналога-пирролизина формулы (В-1), аминокислотного аналога-пирролизина формулы (Г-1), аминокислотного аналога-пирролизина формулы (Д-1), аминокислотного аналога-пирролизина формулы (Е-1),аминокислотного аналога-пирролизина формулы (Ж-1), аминокислотного аналога-пирролизина формулы(З-1), аминокислотного аналога-пирролизина формулы (И-1), аминокислотного аналога-пирролизина формулы (К-1), аминокислотного аналога-пирролизина формулы (Л-1) и аминокислотного аналогапирролизина формулы (М-1) где R3, R5 и R4 каждый независимо выбирают из Н, -ОН, -NO2, галогена, С 1-С 8 алкила, замещенного галогеном С 1-С 8 алкила, замещенного гидроксигруппой С 1-С 8 алкила, арила, гетероарила, гетероциклоалкила или циклоалкила и -LX1,R6 обозначает Н или С 1 алкил,А обозначает С 3-С 8 циклоалкил, С 3-С 8 гетероциклоалкил, 5-6-членный моноциклический арил, 5-6 членный моноциклический гетероарил, 9-10-членное конденсированное бициклическое кольцо или 1314-членное конденсированное трициклическое кольцо, где А необязательно содержит от 1 до 5 заместителей, независимо выбранных из -ОН, -NO2, галогена, С 1-С 8 алкила, замещенного галогеном С 1-С 8 алкила,замещенного гидроксигруппой С 1-С 8 алкила, арила, гетероарила, гетероциклоалкила или циклоалкила и LX1,L выбирают из связи, С 1-С 8 алкилена, замещенного галогеном С 1-С 8 алкилена, замещенного гидроксигруппой С 1-С 8 алкилена, С 2-С 8 алкенилена, замещенного галогеном С 2-С 8 алкенилена, замещенного гидроксигруппой С 2-С 8 алкенилена, полиалкиленгликоля, полиэтиленгликоля, -О(CR11R12)k-, -S(CR11R12)k-5 021001,-S(O)k(CR11R12)k-, -O(CR11R12)k-NR11C(O)-, -O(CR11R12)kC(O)NR11-, -C(O)-, -C(O)(CR11R12)k-, -C(S)-,-C(S)(CR11R12)k-, -C(O)NR11-, -NR11C(O)-, -NR11(CR11R12)k-, -CONR11(CR11R12)k-, -N(R11)CO(CR11R12)k-,-C(O)NR11(CR11R12)k-, -NR11C(O)(CR11R12)k-, где R11 и R12 каждый независимо обозначает Н, С 1-С 8 алкил,замещенный галогеном С 1-С 8 алкил или замещенный гидроксигруппой С 1-С 8 алкил, а k равен целому числу от 1 до 12, иX1 выбирают из метки, красителя, полимера, водорастворимого полимера, полиалкиленгликоля, полиэтиленгликоля, производного полиэтиленгликоля, сахара, липида, фотосшивателя, цитотоксического соединения, лекарственного средства, аффинной метки, фотоаффинной метки, реакционноспособного соединения, смолы, пептида, второго белка или полипептида или аналога полипептида, антитела или фрагмента антитела, металлохелатного соединения, кофактора, жирной кислоты, углевода, полинуклеотида, ДНК, РНК, зонда ПЦР, антисмыслового полинуклеотида, рибоолигонуклеотида, дезоксирибоолигонуклеотида, модифицированной фосфоротиоатом ДНК, модифицированных ДНК и РНК, пептидонуклеиновой кислоты, сахарида, дисахарида, олигосахарида, полисахарида, водорастворимого дендримера,циклодекстрина, биоматериала, наночастицы, спиновой метки, флуорофора, металлсодержащего остатка,радиоактивного остатка, новой функциональной группы, группы, которая ковалентно или не ковалентно взаимодействует с другими молекулами, фоточувствительного остатка, остатка, который возбуждается при актиничном излучении, лиганда, фотоизомеризующегося остатка, биотина, аналога биотина, остатка,содержащего тяжелый атом, химически расщепляемой группы, фоторасщепляемой группы, остатка с удлиненной боковой цепью, связанного с атомом углерода сахара, восстановительно-окислительного агента, аминотиокислоты, токсичного остатка, изотопно-меченого остатка, биофизического зонда, фосфоресцентной группы, хромофорной группы, хемилюминесцентной группы, флуоресцентного остатка,группы с электронной плотностью, магнитной группы, интеркалирующей группы, хелатирующей группы, хромофора, энергопереносящего агента, биологически активного агента, детектируемой метки, низкомолекулярной молекулы, ингибирующей рибонуклеиновой кислоты, киРНК, радионуклеотида, нейтрон-захватывающего агента, производного биотина, квантовой точки(ек), наномедиатора, радиомедиатора, абзима, фермента, активированного комплексного активатора, вируса, токсина, адъюванта, агониста TLR2, агониста TLR4, агониста TLR7, агониста TLR9, агониста TLR8, Т-клеточного эпитопа, фосфолипида, ЛПС-подобной молекулы, гемоцианина моллюска фисурелла, иммуногенного гаптена, агликана,аллергена, ангиостатина, антигормона, антиоксиданта, аптамера, гидовой РНК, сапонина, шаттл-вектора,макромолекулы, мимотопа, рецептора, обратной мицеллы, ПАВ, усилителей иммунного ответа, флуоресцентных красителей, реагентов FRET, зондов для радиовизуализации, другого спектроскопического зонда, пролекарств, токсинов для иммунотерапии, твердой подложки, -СН 2 СН 2-(OCH2CH2O)р-ОХ 2, -O(CH2CH2O)рСН 2 СН 2-Х 2, а также любой комбинации указанных соединений, при этом р равен от 1 до 10000, а X2 обозначает Н, С 1-С 8 алкил, защитную группу или концевую функциональную группу, и где по крайней мере один АА обозначает аминокислотный аналог-пирролизин формулы (А-2) или формулы (Б-2), или по крайней мере один ВВ обозначает аминокислотный аналог-пирролизин формулы(В-1), или формулы (Г-1), или формулы (Д-1), или формулы (Е-1), или формулы (Ж-1), или формулы (З 1), или формулы (И-1), или формулы (К-1), или формулы (Л-1), или формулы (М-1). В некоторых вариантах указанных соединений цикл А выбирают из фурана, тиофена, пиррола, пирролина, пирролидина, диоксолана, оксазола, тиазола, имидазола, имидазолина, имидазолидина, пиразола,пиразолина, пиразолидина, изоксазола, изотиазола, оксадиазола, триазола, тиадиазола, пирана, пиридина,пиперидина, диоксана, морфолина, дитиана, тиоморфолина, пиридазина, пиримидина, пиразина, пиперазина, триазина, тритиана, индолизина, индола, изоиндола, индолина, бензофурана, бензотиофена, индазола, бензимидазола, бензотиазола, пурина, хинолизина, хинолина, изохинолина, циннолина, фталазина,хиназолина, хиноксалина, нафтиридина, птеридина, хинуклидина, карбазола, акридина, феназина, фентиазина, феноксазина, фенила, индена, нафталина, азулена, флуорена, антрацена, фенантрацена, норборана и адамантина. В других вариантах указанных соединений цикл А выбирают из фенила, фурана, тиофена, пиррола,пирролина, пирролидина, диоксолана, оксазола, тиазола, имидазола, имидазолина, имидазолидина, пиразола, пиразолина, пиразолидина, изоксазола, изотиазола, оксадиазола, триазола, тиадиазола, пирана, пиридина, пиперидина, диоксана, морфолина, дитиана, тиоморфолина, пиридазина, пиримидина, пиразина,пиперазина, триазина и тритиана. В еще одних вариантах указанных соединений цикл А выбирают из индолизина, индола, изоиндола,индолина, бензофурана, бензотиофена, индазола, бензимидазола, бензотиазола, пурина, хинолизина, хинолина, изохинолина, циннолина, фталазина, хиназолина, хиноксалина, нафтиридина, птеридина, хинуклидина, карбазола, акридина, феназина, фентиазина, феноксазина, индена, нафталина, азулена, флуорена,антрацена, фенантрацена, норборана и адамантина. В некоторых вариантах указанных соединений цикл А выбирают из фенила, нафталина и пиридина. В других вариантах указанных соединений ВВ каждый независимо выбирают из аминокислотного остатка, аминокислотного аналога-пирролизина формулы (А-2), аминокислотного аналога-пирролизина формулы (Б-2), аминокислотного аналога-пирролизина формулы (В-1), аминокислотного аналога-пирро-6 021001 лизина формулы (Г-2), аминокислотного аналога-пирролизина формулы (Д-1), аминокислотного аналогапирролизина формулы (Е-2), аминокислотного аналога-пирролизина формулы (Ж-1), аминокислотного аналога-пирролизина формулы (З-2), аминокислотного аналога-пирролизина формулы (И-1), аминокислотного аналога-пирролизина формулы (К-2), аминокислотного аналога-пирролизина формулы (Л-1) и аминокислотного аналога-пирролизина формулы (М-2) при этом по крайней мере один ВВ обозначает остаток аминокислотного аналога-пирролизина формулы (В-1), или формулы (Г-2), или формулы (Д-1), или формулы (Е-2), или формулы (Ж-1), или формулы (З-2), или формулы (И-1), или формулы (К-2), или формулы (Л-1), или формулы (М-2),где R3, R5 и R4 каждый независимо выбирают из Н, -ОН, -NO2, галогена, С 1-С 8 алкила, замещенного галогеном С 1-С 8 алкила, замещенного гидроксигруппой С 1-С 8 алкила и -LX1,R6 обозначает Н или С 1 алкил,R7, если присутствует, каждый независимо выбирают из -ОН, -NO2, галогена, С 1-С 8 алкила, замещенного галогеном С 1-8 алкила, замещенного гидроксигруппой С 1-С 8 алкила и -LX1,L выбирают из связи, С 1-С 8 алкилена, замещенного галогеном С 1-С 8 алкилена, замещенного гидроксигруппой С 1-С 8 алкилена, С 2-С 8 алкенилена, замещенного галогеном С 2-С 8 алкенилена, замещенного гидроксигруппой С 2-С 8 алкенилена,-O(CR11R12)k-, -S(CR11R12)k-, -S(O)k(CR11R12)k-, -O(CR11R12)k-NR11C(O)-, -O(CR11R12)kC(O)NR11-, -C(O)-,-C(O)(CR11R12)k-, -C(S)-, -C(S)(CR11R12)k-, -C(O)NR11-, -NR11C(O)-, -NR11(CR11R12)k-, CONR11(CR11R12)k-,-N(R11)CO(CR11R12)k-, -C(O)NR11(CR11R12)k-, NR11C(O)(CR11R12)k-, где R11 и R12 каждый независимо обозначает Н, C1-С 8 алкил, замещенный галогеном С 1-С 8 алкил или замещенный гидроксигруппой C1-С 8 алкил, а k равен целому числу от 1 до 12, иX1 выбирают из водорастворимого полимера, полиалкиленгликоля, полиэтиленгликоля, производного полиэтиленгликоля, сахара, липида, цитотоксического соединения, лекарственного средства, аффинной метки, реакционноспособного соединения, смолы, пептида, белка, антитела или фрагмента антитела, углевода, рибонуклеиновой кислоты (РНК), дезоксирибонуклеиновой кислоты (ДНК), карбогидрата, модифицированной фосфоротиоатом ДНК, сахарида, дисахарида, олигосахарида, полисахарида, спиновой метки, флуорофора, фоточувствительного остатка, биотина, аналога биотина, агониста TLR7,фосфолипида, иммуногенного гаптена, усилителей иммунного ответа, -СН 2 СН 2-(OCH2CH2O)P-OX2, -О(CH2CH2O)рСН 2 СН 2-Х 2, а также любой комбинации указанных соединений, при этом р равен от 1 до 10000, а X2 обозначает Н или С 1-С 8 алкил. По крайней мере один АА обозначает остаток аминокислотного аналога-пирролизина формулы (А 2) или формулы (Б-2), и аминокислотный аналог-пирролизина формулы (А-2) означает аминокислотный остаток формулы (VII), и аминокислотный остаток формулы (Б-2) означает аминокислотный остаток формулы (VIII) где аминокислотный остаток формулы (VII) или формулы (VIII) получают биосинтетическим способом в клетке, содержащей ген pylC и ген pylD, при этом клетку приводят в контакт с питательной средой, содержащей предшественник. По крайней мере один ВВ обозначает остаток аминокислотного аналога-пирролизина формулы (В 1), или формулы (Г-2), или формулы (Д-1), или формулы (Е-2), или формулы (Ж-1), или формулы (З-2),или формулы (И-1), или формулы (К-2), или формулы (Л-1), или формулы (М-2). В некоторых вариантах указанных соединений R6 обозначает Н, в то время как в других вариантах указанных соединений R6 обозначает С 1 алкил. В некоторых вариантах указанных соединений R5 обозначает -LX1. В других вариантах указанных соединений R7 обозначает -LX1. В некоторых вариантах указанных соединений X1 обозначает сахар, полиэтиленгликоль, флуоресцентный остаток, иммуномодулятор, рибонуклеиновую кислоту, дезоксирибонуклеиновую кислоту, белок, пептид, биотин, фосфолипид, агонист TLR7, иммуногенный гаптен или твердую подложку. В некоторых вариантах указанных соединений L обозначает полиалкиленгликоль,полиэтиленгликоль, С 1-С 8 алкилен, замещенный галогеном С 1-С 8 алкилен или замещенный гидроксигруппой C1-С 8 алкилен. В другом объекте настоящего изобретения предлагается способ модификации белка, где белок характеризуется формулой (I), причем указанный способ заключается в том, что белок контактирует с реагентом формулы (III) или формулы (IV), при этом формула (I) соответствует формулеR2 обозначает ОН,n равен целому числу от 1 до 5000,АА каждый независимо выбирают из аминокислотного остатка, аминокислотного остатка пирролизина, аминокислотного аналога-пирролизина формулы (А-1) и аминокислотного аналога-пирролизина формулы (Б-1) где R6 обозначает Н или С 1 алкил, и по крайней мере один АА обозначает аминокислотный остаток пирролизина или аминокислотный аналог-пирролизин формулы (А-1) или формулы (Б-1),и где формула (II) и формула (III) соответствуют формулам где R6 обозначает Н или С 1 алкил, и по крайней мере один АА обозначает аминокислотный остаток пирролизина или аминокислотный аналог-пирролизин формулы (А-1) или формулы (Б-1), где аминокислотный остаток формулы (А-1) обозначает аминокислотный остаток формулы (V), и аминокислотный остаток формулы (Б-1) обозначает аминокислотный остаток формулы (VI) и аминокислоту формулы (V) или формулы (VI) получают биосинтетическим способом в клетке,содержащей ген pylC и ген pylD, при этом клетка контактирует с питательной средой, содержащей предшественник; и где формула (III) и формула (IV) соответствуют формулам где R3, R5 и R4 каждый независимо выбран из Н, -ОН, -NO2, галогена, С 1-С 8 алкила, замещенного галогеном C1-8 алкила, замещенного гидроксигруппой С 1-С 8 алкила и -LX1; А обозначает фенил, необязательно содержит от 1 до 5 заместителей, независимо выбранных из-O(CR11R12)k-, -S(CR11R12)k-, -S(O)k(CR11R12)k-, -О(CR11R12)k-NR11C(O)-, -O(CR11R12)kC(O)NR11-, -С (О)-,-С(О)(CR11R12)k-, -C(S)-, C(S)(CR11R12)k-, -C(O)NR11-, -NR11C(O)-, -NR11(CR11R12)k-, CONR11(CR11R12)k-,-N(R11)CO(CR11R12)k-, -C(O)NR11(CR11R12)k-, NR11C(O)(CR11R12)k-, где R11 и R12 каждый независимо обозначает Н, С 1-С 8 алкил, замещенный галогеном С 1-С 8 алкил или замещенный гидроксигруппой C1-С 8 алкил, а k равен целому числу от 1 до 12, и X1 выбран из водорастворимого полимера, полиалкиленгликоля, полиэтиленгликоля, сахара, липида, цитотоксического соединения, лекарственного средства, аффинной метки, реакционноспособного соединения, смолы, пептида, белка, антитела или фрагмента антитела, углевода, рибонуклеиновой кислоты (РНК), дезоксирибонуклеиновой кислоты (ДНК), модифицированной фосфоротиоатом ДНК, сахарида, дисахарида, олигосахарида, полисахарида, спиновой метки, флуорофора, фоточувствительного остатка,биотина, аналога биотина, агониста TLR7, фосфолипида, иммуногенного гаптена, иммуномодулятора, усилителя иммунного ответа, твердой подложки, -CH2CH2-(OCH2CH2O)P-OX2, -O-(CH2CH2O)pCH2CH2-X2, а также любой комбинации указанных соединений, при этом р равен от 1 до 10000, а X2 обозначает Н или С 1-С 8 алкил. В некоторых вариантах упомянутого выше способа аминокислотный остаток формулы (А-1) обозначает аминокислотный остаток формулы (А-2) или формулы (А-3) В других вариантах упомянутого выше способа аминокислотный остаток формулы (Б-1) обозначает аминокислотный остаток формулы (Б-2) или формулы (Б-3) В некоторых вариантах упомянутого выше способа аминокислотный остаток формулы (А-1) обозначает аминокислотный остаток формулы (V), а аминокислотный остаток формулы (Б-1) обозначает аминокислотный остаток формулы (VI) где R6 обозначает Н или С 1 алкил. В одном варианте аминокислоту формулы (V) или формулы (VI) получают биосинтетическим способом в клетке, содержащей ген pylB, ген pylC и ген pylD, при этом клетка контактирует с питательной средой, содержащей предшественник. В других вариантах аминокислоту формулы (V) или формулы (VI) получают биосинтетическим способом в клетке, содержащей ген pylC и ген pylD, при этом клетка контактирует с питательной средой, содержащей предшественник. В некоторых вариантах аминокислотой формулы (V) является аминокислота формулы (VII) а предшественником является орнитин, аргинин, D-орнитин, D-аргинин, (2S)-2-амино-6-(2,5-диаминопентанамидо)гексановая кислота или (2S)-2-амино-6-R)-2,5-диаминопентанамидо)гексановая кислота. В других вариантах аминокислотой формулы (VI) является аминокислота формулы (VIII), а предшественником является орнитин или аргинин при этом предшественником является орнитин, аргинин, D-орнитин, D-аргинин, (2S)-2-амино-6(2,5-диаминопентанамидо)гексановая кислота или (2S)-2-амино-6-R)-2,5-диаминопентанамидо)гексановая кислота. В некоторых вариантах аминокислотой формулы (V) является аминокислота формулы (VII), а предшественником является D-орнитин или D-аргинин. В других вариантах аминокислотой формулы (VI) является аминокислота формулы (VIII), а предшественником является D-орнитин или D-аргинин. В некоторых вариантах аминокислотой формулы (V) является аминокислота формулы (VII), а предшественником является (2S)-2 амино-6-(2,5-диаминопентанамидо)гексановая кислота. В других вариантах аминокислотой формулы (V) является аминокислота формулы (VII), а предшественником является (2S)-2-амино-6-R)-2,5-диаминопентанамидо)гексановая кислота. В некоторых вариантах аминокислотой формулы (VI) является аминокислота формулы (VIII), а предшественником является (2S)-2-амино-6-(2,5-диаминопентанамидо)гексановая кислота. В других вариантах аминокислотой формулы (VI) является аминокислота формулы (VIII), а предшественником является (2S)-2-амино-6-R)-2,5-диаминопентанамидо)гексановая кислота. В некоторых вариантах аминокислотой формулы (V) является аминокислота формулы (IX), а предшественником является D-орнитин, D-аргинин, 2,5-диамино-3-метилпентановая кислота, (2S)-2-амино-6(2,5-диаминопентанамидо)гексановая кислота или (2S)-2-амино-6-R)-2,5-диаминопентанамидо)гексановая кислота В других вариантах аминокислотой формулы (VI) является аминокислота формулы (X), предшественником является D-орнитин, D-аргинин, 2,5-диамино-3-метилпентановая кислота, (2R,3S)-2,5 диамино-3-метилпентановая кислота, (2R,3R)-2,5-диамино-3-метилпентановая кислота, (2S)-2-амино-6(2,5-диаминопентанамидо)гексановая кислота или (2S)-2-амино-6-R)-2,5-диаминопентанамидо)гексановая кислота В некоторых вариантах аминокислотой формулы (V) является аминокислота формулы (IX), а предшественником является D-2,5-диамино-3-метилпентановая кислота. В других вариантах аминокислотой формулы (V) является аминокислота формулы (X), а предшественником является D-2,5-диамино-3 метилпентановая кислота. В некоторых вариантах аминокислотой формулы (V) является аминокислота формулы (IX), а предшественником является (2R,3S)-2,5-диамино-3-метилпентановая кислота. В других вариантах аминокислотой формулы (V) является аминокислота формулы (X), а предшественником является (2R,3S)-2,5 диамино-3-метилпентановая кислота. В некоторых вариантах аминокислотой формулы (V) является аминокислота формулы (IX), а предшественником является (2R,3R)-2,5-диамино-3-метилпентановая кислота. В других вариантах аминокислотой формулы (V) является аминокислота формулы (X), а предшественником является (2R,3R)-2,5 диамино-3-метилпентановая кислота. В некоторых вариантах аминокислотой формулы (V) является аминокислота формулы (IX), а предшественником является D-орнитин или D-аргинин или (2S)-2-амино 6-R)-2,5-диаминопентанамидо)гексановая кислота. В других вариантах аминокислотой формулы (V) является аминокислота формулы (X), а предшественником является D-орнитин или D-аргинин или (2S)2-амино-6-R)-2,5-диаминопентанамидо)гексановая кислота. В некоторых вариантах упомянутых выше способов аминокислоту формулы (V), формулы (VI),формулы (VII), формулы (VIII), формулы (IX) или формулы (X) встраивают в белок в клетке с использованием ортогональной тРНК (О-тРНК) и ортогональной аминоацил-тРНК-синтетазы (О-РС), при этом ОРС аминоацилирует О-тРНК аминокислотой формулы (V) или формулы (VI), и О-тРНК распознает по крайней мере один кодон-селектор мРНК в клетке. В других вариантах упомянутых выше способов клетка, кроме того, содержит ген pylS и ген pylT, и аминокислоту формулы (V), формулы (VI), формулы (VII), формулы (VIII), формулы (IX) или формулы (X) встраивают в белок в клетке с использованием аминоацил-тРНК-синтетазы и тРНК, которая распознает по крайней мере один кодон-селектор мРНК в клетке, причем аминоацил-тРНК-синтетаза представляет собой генный продукт гена pylS, а тРНК является генным продуктом гена pylT. В некоторых вариантах упомянутых выше кодоном-селектором является янтарный кодон (TAG). В некоторых вариантах упомянутых выше способов клеткой является клетка прокариотов, в то время как в других вариантах клеткой является клетка эукариотов. В некоторых вариантах клеткой является клеткаEscherichia coli, между тем в других вариантах клеткой является клетка млекопитающих, дрожжевая клетка или клетка насекомых. В некоторых вариантах дрожжевой клеткой является клетка Saccharomyces cerevisiae или клетка Pichia pastoralis. В других вариантах клеткой млекопитающих является клетка СНО, клетка HeLa или клетка HEK293F. В некоторых вариантах клеткой насекомых является клетка sf9. В другом объекте настоящего изобретения предлагаются модифицированные белки, полученные с использованием упомянутых выше способов, причем указанные модифицированные белки характеризуются формулой (II) где R1 обозначает Н или N-концевую модифицирующую группу,R2 обозначает ОН или С-концевую модифицирующую группу,n равен целому числу от 1 до 5000,ВВ каждый независимо выбирают из аминокислотного остатка, аминокислотного аналога-пирролизина формулы (А-1), аминокислотного аналога-пирролизина формулы (Б-1), аминокислотного аналогапирролизина формулы (В-1), аминокислотного аналога-пирролизина формулы (Г-1), аминокислотного аналога-пирролизина формулы (Д-1), аминокислотного аналога-пирролизина формулы (Е-1), аминокислотного аналога-пирролизина формулы (Ж-1), аминокислотного аналога-пирролизина формулы (З-1),аминокислотного аналога пирролизина формулы (И-1), аминокислотного аналога-пирролизина формулы при этом по крайней мере один ВВ обозначает аминокислотный аналог-пирролизин формулы (В-1),или формулы (Г-1), или формулы (Д-1), или формулы (Е-1), или формулы (Ж-1), или формулы (З-1), или формулы (И-1), или формулы (К-1), или формулы (Л-1), или формулы (М-1). В некоторых вариантах упомянутых выше способов и указанных модифицированных белков цикл А выбирают из фурана, тиофена, пиррола, пирролина, пирролидина, диоксолана, оксазола, тиазола, имидазола, имидазолина, имидазолидина, пиразола, пиразолина, пиразолидина, изоксазола, изотиазола, оксадиазола, триазола, тиадиазола, пирана, пиридина, пиперидина, диоксана, морфолина, дитиана, тиоморфолина, пиридазина, пиримидина, пиразина, пиперазина, триазина, тритиана, индолизина, индола, изоиндола, индолина, бензофурана, бензотиофена, индазола, бензимидазола, бензотиазола, пурина, хинолизина, хинолина, изохинолина, циннолина, фталазина, хиназолина, хиноксалина, нафтиридина, птеридина,хинуклидина, карбазола, акридина, феназина, фентиазина, феноксазина, фенила, индена, нафталина, азулена, флуорена, антрацена, фенантрацена, норборана и адамантина. В других вариантах упомянутых выше способов и указанных модифицированных белков цикл А выбирают из фенила, фурана, тиофена, пиррола, пирролина, пирролидина, диоксолана, оксазола, тиазола,имидазола, имидазолина, имидазолидина, пиразола, пиразолина, пиразолидина, изоксазола, изотиазола,оксадиазола, триазола, тиадиазола, пирана, пиридина, пиперидина, диоксана, морфолина, дитиана, тиоморфолина, пиридазина, пиримидина, пиразина, пиперазина, триазина и тритиана. В некоторых вариантах упомянутых выше способов и указанных модифицированных белков цикл А выбирают из индолизина, индола, изоиндола, индолина, бензофурана, бензотиофена, индазола, бензимидазола, бензотиазола, пурина, хинолизина, хинолина, изохинолина, циннолина, фталазина, хиназолина, хиноксалина, нафтиридина, птеридина, хинуклидина, карбазола, акридина, феназина, фентиазина,феноксазина, индена, нафталина, азулена, флуорена, антрацена, фенантрацена, норборана и адамантина. В других вариантах упомянутых выше способов и указанных модифицированных белков цикл А выбирают из фенила, нафталина и пиридина. В некоторых вариантах упомянутых выше способов ВВ каждый независимо выбирают из аминокислотного остатка, аминокислотного аналога-пирролизина формулы (А-2), аминокислотного аналога- 13021001(И-1), аминокислотного аналога пирролизина формулы (К-2), аминокислотного аналога пирролизина формулы (Л-1) и аминокислотного аналога-пирролизина формулы (М-2) при этом по крайней мере один ВВ обозначает остаток аминокислотного аналога-пирролизина формулы (В-1), или формулы (Г-2), или формулы (Д-1), или формулы (Е-2), или формулы (Ж-1), или формулы (З-2), или формулы (И-1), или формулы (К-2), или формулы (Л-1), или формулы (М-2),где R3, R5 и R4 каждый независимо выбран из Н, -ОН, -NO2, галогена, С 1-С 8 алкила, замещенного галогеном С 1-С 8 алкила, замещенного гидроксигруппой С 1-С 8 алкила и -LX1;R7, если присутствует, каждый независимо выбран из -ОН, -NO2, галогена, С 1-С 8 алкила, замещенного галогеном С 1-8 алкила, замещенного гидроксигруппой С 1-С 8 алкила и -LX1;(CR11R12)k-, -N(R11)CO(CR11R12)k-, -C(O)NR11(CR11R12)k-, NR11C(O)(CR11R12)k-, где R11 и R12 каждый независимо обозначает Н, С 1-С 8 алкил, замещенный галогеном C1-С 8 алкил или замещенный гидроксигруппойC1-С 8 алкил, а k равен целому числу от 1 до 12, иX1 выбран из водорастворимого полимера, полиалкиленгликоля, полиэтиленгликоля, сахара, липида, цитотоксического соединения, лекарственного средства, аффинной метки, реакционноспособного соединения, пептида, белка, антитела или фрагмента антитела, углевода, рибонуклеиновой кислоты(РНК), дезоксирибонуклеиновой кислоты (ДНК), модифицированной фосфоротиоатом ДНК, сахарида,дисахарида, олигосахарида, полисахарида, спиновой метки, флуорофора, фоточувствительного остатка,биотина, аналога биотина, агониста TLR7, фосфолипида, иммуногенного гаптена, иммуномодулятора,усилителя иммунного ответа, твердой подложки, -CH2CH2-(OCH2CH2O)p-OX2, -O-(CH2CH2O)pCH2CH2 Х 2, а также любой комбинации указанных соединений, при этом р равен от 1 до 10000, а X2 обозначает Н или С 1-С 8 алкил. В некоторых вариантах упомянутых выше способов и указанных модифицированных белков R6 обозначает Н, в то время как в других вариантах R6 обозначает С 1 алкил. В некоторых вариантах упомянутых выше способов и указанных модифицированных белков R5 обозначает -LX1. В других вариантах упомянутых выше способов и указанных модифицированных белков X1 обозначает сахар, полиэтиленгликоль, флуоресцентный фрагмент, иммуномодулятор, рибонуклеиновую кислоту, дезоксирибонуклеиновую кислоту, белок, пептид, биотин, фосфолипид, агонистTLR7, иммуногенный гаптен или твердую подложку. В некоторых вариантах L обозначает полиалкиленгликоль, полиэтиленгликоль, С 1-С 8 алкилен, замещенный галогеном С 1-С 8 алкилен или замещенный гидроксигруппой С 1-С 8 алкилен. В других вариантах упомянутых выше способов реагент формулы (IV) характеризуется следующими структурами:- 15021001 где L и X1 имеют значения, как описано в данном контексте. В некоторых вариантах указанных реагентов L обозначает связь, а X1 обозначает полиэтиленгликоль. В других вариантах реагент формулы (IV) характеризуется структурами где средняя молекулярная масса (ММ) соединений, содержащих один или более остатков полиэтиленгликоля (ПЭГ), составляет величину в диапазоне от 1000 Да до 50 кДа, а n равен от 20 до 1200, и гдеexPADRE обозначает пептид, соответствующий SEQ ID NO:28, PADRE обозначает пептид, соответствующий SEQ ID NO:29, BG1 обозначает полинуклеотид, соответствующий SEQ ID NO:30, а BG2 обозначает полинуклеотид, соответствующий SEQ ID NO:31. В некоторых вариантах реагентом формулы (IV) является соединение структуры при этом средняя молекулярная масса соединения составляет величину в диапазоне от 1000 Да до 30 кДа, а n равен от 20 до 679. В другом варианте реагентом формулы (IV) является соединение структуры при этом средняя молекулярная масса соединения составляет величину в диапазоне от 1000 Да до 45 кДа, а n равен от 20 до 1018. В другом объекте настоящего изобретения предлагаются соединения формулы (VII) или формулы при этом соединение формулы (VII) или формулы (VIII) получают биосинтетическим способом в клетке, содержащей ген pylC и ген pylD, причем клетка контактирует с питательной средой, содержащей предшественник. В некоторых вариантах указанных соединений клетка содержит ген pylB, ген pylC и ген pylD. В других вариантах указанных соединений предшественником является орнитин или аргинин, в то время как в некоторых вариантах предшественником является D-орнитин, или D-аргинин, или (2S)-2 амино-6-R)-2,5-диаминопентанамидо)гексановая кислота. В других вариантах указанных соединений соединение формулы (VII) или формулы (VIII) встраивают в белок в клетке с использованием ортогональной тРНК (О-тРНК) и ортогональной аминоацилтРНК-синтетазы (О-РС), при этом О-РС аминоацилирует О-тРНК соединением формулы (V) или формулы (VI), и О-тРНК распознает по крайней мере один кодон-селектор мРНК в клетке. В некоторых вариантах указанных соединений клетка, кроме того, содержит ген pylS и ген pylT, и соединение формулы (V) или формулы (VI) встраивают в белок в клетке с использованием аминоацилтРНК-синтетазы и тРНК, которая распознает по крайней мере один кодон-селектор мРНК в клетке, причем аминоацил-тРНК-синтетаза представляет собой генный продукт гена pylS, а тРНК является генным продуктом гена pylT. В других вариантах кодоном-селектором является янтарный стоп-кодон (TAG). В некоторых вариантах клеткой является клетка прокариотов, в то время как в других вариантах клеткой является клетка эукариотов. В некоторых вариантах клеткой является клетка Escherichia coli, между тем в других вариантах клеткой является клетка млекопитающих, дрожжевая клетка или клетка насекомых. В некоторых вариантах дрожжевой клеткой является клетка Saccharomyces cerevisiae или клетка Pichia pastoralis. В других вариантах клеткой млекопитающих является клетка СНО, клетка HeLa или клетка HEK293F. В некоторых вариантах клеткой насекомых является клетка sf9. В другом объекте настоящего изобретения предлагаются соединения формулы (VII) или формулы где соединение формулы (VII) или формулы (VIII) получают биосинтетическим способом, и оно секретируется первой клеткой при контактировании с питательной средой, содержащей предшественник и вторую клетку, и при этом первая клетка представляет собой питающую клетку, содержащую ген pylC и ген pylD. В некоторых вариантах указанных соединений первая клетка содержит ген pylB, ген pylC и генpylD. В других вариантах указанных соединений предшественником является орнитин или аргинин. В некоторых вариантах указанных соединений предшественником является D-орнитин или D-аргинин. В других вариантах указанных соединений предшественником является (2S)-2-амино-6-(2,5-диаминопентанамидо)гексановая кислота. В некоторых вариантах указанных соединений предшественником является (2S)-2-амино-6-R)-2,5-диаминопентанамидо)гексановая кислота. В других вариантах указанных соединений соединение формулы (VII) или формулы (VIII) встраивают в белок во второй клетке с использованием ортогональной тРНК (О-тРНК) и ортогональной аминоацил-тРНК-синтетазы (О-РС), при этом О-PC аминоацилирует О-тРНК соединением формулы (VII) или формулы (VIII), и О-тРНК распознает по крайней мере один кодон-селектор мРНК во второй клетке. В некоторых вариантах указанных соединений вторая клетка содержит ген pylS и ген pylT, при этом соединение формулы (VII) или формулы (VIII) встраивают в белок во второй клетке. В других вариантах указанных соединений соединение формулы (VII) или формулы (VIII) встраи- 18021001 вают в белок во второй клетке с использованием аминоацил-тРНК-синтетазы и тРНК, которая распознает по крайней мере один кодон-селектор мРНК в клетке, при этом аминоацил-тРНК-синтетаза является генным продуктом гена pylS, а тРНК является генным продуктом гена pylT. В некоторых вариантах указанных соединений кодоном-селектором является янтарный стоп-кодон(TAG). В других вариантах указанных соединений первой клеткой или второй клеткой является клетка прокариотов. В некоторых вариантах указанных соединений первой клеткой и второй клеткой является клетка прокариотов. В некоторых вариантах указанных соединений первой клеткой или второй клеткой является клетка эукариотов. В других вариантах указанных соединений первой клеткой и второй клеткой является клетка эукариотов. В других вариантах клеткой прокариотов является клетка Escherichia coli. В некоторых вариантах клеткой эукариотов является клетка млекопитающих, дрожжевая клетка или клетка насекомых. В некоторых вариантах дрожжевой клеткой является клетка Saccharomyces cerevisiae или клетка Pichiapastoralis. В некоторых вариантах клеткой млекопитающих является клетка СНО, клетка HeLa или клеткаHEK293F. В других вариантах клеткой насекомых является клетка sf9. В другом объекте настоящего изобретения предлагается соединение формулы (IX) где соединение формулы (IX) получают биосинтетическим способом в клетке, содержащей ген pylC и ген pylD, при этом клетка контактирует с питательной средой, содержащей 2,5-диамино-3 метилпентановую кислоту или D-2,5-диамино-3-метилпентановую кислоту. В некоторых вариантах указанного соединения 2,5-диамино-3-метилпентановой кислотой является(2R,3S)-2,5-диамино-3-метилпентановая кислота. В других вариантах указанного соединения 2,5-диамино-3-метилпентановой кислотой является(2R,3R)-2,5-диамино-3-метилпентановая кислота. В некоторых вариантах указанного соединения клетка содержит ген pylB, ген pylC и ген pylD, при этом клетка контактирует с питательной средой, содержащей орнитин, аргинин, D-орнитин, D-аргинин,(2S)-2-амино-6-(2,5-диаминопентанамидо)гексановую кислоту, 2,5-диамино-3-метилпентановую кислоту или D-2,5-диамино-3-метилпентановую кислоту. В других вариантах указанного соединения соединение формулы (IX) встраивают в белок в клетке с использованием ортогональной тРНК (О-тРНК) и ортогональной аминоацил-тРНК-синтетазы (О-РС),при этом О-РС аминоацилирует О-тРНК соединением формулы (IX), и О-тРНК распознает по крайней мере один кодон-селектор мРНК в клетке. В некоторых вариантах указанного соединения клетка кроме того содержит ген pylS и ген pylT, при этом соединение формулы (IX) встраивают в белок в клетке с использованием аминоацил-тРНКсинтетазы и тРНК, которая распознает по крайней мере один кодон-селектор мРНК в клетке, причем аминоацил-тРНК-синтетаза представляет собой генный продукт гена pylS, а тРНК является генным продуктом гена pylT. В других вариантах кодоном-селектором является янтарный стоп-кодон (TAG). В некоторых вариантах клеткой является клетка прокариотов, в то время как в других вариантах клеткой является клетка эукариотов. В некоторых вариантах клеткой прокариотов является клетка Escherichia coli. В других вариантах клеткой эукариотов является клетка млекопитающих, дрожжевая клетка или клетка насекомых. В некоторых вариантах дрожжевой клеткой является клетка Saccharomyces cerevisiae или клетка Pichia pastoralis. В других вариантах клеткой млекопитающих является клетка СНО, клетка HeLa или клеткаHEK293F. В некоторых вариантах клеткой насекомых является клетка sf9. В другом объекте настоящего изобретения предлагается соединение формулы (IX) где соединение формулы (IX) получают биосинтетическим способом, и оно секретируется первой клеткой, контактирующей с питательной средой, содержащей 2,5-диамино-3-метилпентановую кислоту или D-2,5-диамино-3-метилпентановую кислоту и вторую клетку, причем первая клетка представляет собой питающую клетку, содержащую ген pylC и ген pylD. В некоторых вариантах указанного соединения 2,5-диамино-3-метилпентановой кислотой является(2R,3S)-2,5-диамино-3-метилпентановая кислота. В других вариантах указанного соединения 2,5-диамино-3-метилпентановой кислотой является(2R,3R)-2,5-диамино-3-метилпентановая кислота. В некоторых вариантах указанного соединения клетка содержит ген pylB, ген pylC и ген pylD, при этом клетка контактирует с питательной средой, содержащей орнитин, аргинин, D-орнитин, D-аргинин,(2S)-2-амино-6-(2,5-диаминопентанамидо)гексановую кислоту, 2,5-диамино-3-метилпентановую кислоту или D-2,5-диамино-3-метилпентановую кислоту. В других вариантах указанного соединения соединение формулы (IX) встраивают в белок во второй клетке с использованием ортогональной тРНК (О-тРНК) и ортогональной аминоацил-тРНК-синтетазы(О-РС), при этом О-РС аминоацилирует О-тРНК соединением формулы (IX), и О-тРНК распознает по крайней мере один кодон-селектор мРНК во второй клетке. В некоторых вариантах указанного соединения вторая клетка содержит ген pylS и ген pylT, и соединение формулы (IX) встраивают в белок во второй клетке. В других вариантах указанного соединения соединение формулы (IX) встраивают в белок во второй клетке с использованием аминоацил-тРНК-синтетазы и тРНК, которая распознает по крайней мере один кодон-селектор мРНК в клетке, причем аминоацил-тРНК-синтетаза представляет собой генный продукт гена pylS, а тРНК является генным продуктом гена pylT. В некоторых вариантах кодоном-селектором является янтарный кодон (TAG). В других вариантах первой клеткой или второй клеткой является клетка прокариотов. В некоторых вариантах первой клеткой и второй клеткой является клетка прокариотов. В других вариантах первой клеткой или второй клеткой является клетка эукариотов. В некоторых вариантах первой клеткой и второй клеткой является клетка эукариотов. В других вариантах клеткой прокариотов является клетка Escherichia coli. В некоторых вариантах клеткой эукариотов является клетка млекопитающих, дрожжевая клетка или клетка насекомых. В других вариантах дрожжевой клеткой является клетка Saccharomycescerevisiae или клетка Pichia pastoralis. В некоторых вариантах клеткой млекопитающих является клетка СНО, клетка HeLa или клетка HEK293F. В других вариантах клеткой насекомых является клетка sf9. В другом объекте настоящего изобретения предлагаются следующие соединения формулы (IV): где средняя молекулярная масса (ММ) соединений, содержащих один или более остатков полиэтиленгликоля (ПЭГ), составляет величину в диапазоне от 1000 Да до 50 кДа, а n равен от 20 до 1200, и где гдеобозначает фосфотиоатное связующее звено. Подробное описание изобретения В настоящем изобретении предлагаются способы и композиции, используемые для сайтспецифичной модификации белков, полипептидов и/или пептидов, причем указанные способы заключаются том, что проводят сайт-специфичную модификацию генетически кодируемых остатков пирролизина или пирролинкарбоксилизина (PCL), причем аминокислоты, пирролизин и PCL, получают биосинтетическим способом. В настоящем изобретении предлагаются различные типы молекул, которые конденсируют сайт-специфичным методом с белками, полипептидами и/или пептидами, содержащими один или более биосинтетически встроенных остатков PCL или пирролизина. В некоторых вариантах указанные сайт-специфичные модификации используют для сайт-специфичного маркирования белков, полипептидов и/или пептидов. В других вариантах меткой является флуоресцентный остаток, фосфоресцентный остаток, хемилюминесцентный остаток, хелатирующий остаток, интеркалирующий остаток, радиоактивный остаток, хромофорный остаток, спин-меченый остаток, ЯМР-активный остаток, реагенты для ПЭТ или МРТ (позитронно-эмиссионной или магнитно-резонансной томографии). В некоторых вариантах указанные сайт-специфичные модификации используют для присоединения иммуномодуляторов к белкам, полипептидам и/или пептидам. В других вариантах указанные сайт-специфичные модификации используют для присоединения полиэтиленгликоля (ПЭГ) к белкам, полипептидам и/или пептидам. В некоторых вариантах указанные сайт-специфичные модификации используют для присоединения сахаров(гликозилирования) к белкам, полипептидам и/или пептидам. В других вариантах указанные сайт-специфичные модификации используют для сайт-специфичного сшивания белков, полипептидов и/или пептидов, при этом получают гетероолигомеры, включая, но не ограничиваясь только ими, гетеродимеры и гетеротримеры. В некоторых вариантах указанные сайт-специфичные модификации используют для сайт-специфичного сшивания белков, полипептидов и/или пептидов антителами. В других вариантах указанные сайт-специфичные модификации используют для сайт-специфичного сшивания белков, полипептидов и/или пептидов, при этом образуются конъюгаты белок-белок, конъюгаты белок-полипептид, конъюгаты белок-пептид, конъюгаты полипептидполипептид, конъюгаты полипептид-пептид или конъюгаты пептид-пептид. В некоторых вариантах указанные сайт-специфичные модификации используют для сайтспецифичного присоединения антител к белкам, причем белком является токсичный белок по настоящему изобретению, при этом образуются конъюгаты антител и лекарственных средств. В других вариантах указанные сайт-специфичные модификации используют для сайт-специфичного присоединения антител к белкам, причем антитела конденсируют с низкомолекулярными лекарственными средствами, при этом образуются конъюгаты антител и лекарственных средств. В некоторых вариантах указанные сайт-специфичные модификации используют для сайтспецифичного присоединения комплексов типа рецептор-лиганд к белкам, причем белком является токсичный белок по настоящему изобретению, при этом образуются конъюгаты рецептор-лигандлекарственное средство. В других вариантах указанные сайт-специфичные модификации используют для сайт-специфичного присоединения комплексов типа рецептор-лиганд к белкам, причем комплекс типа рецептор-лиганд конденсируют с низкомолекулярными лекарственными средствами, при этом образуются конъюгаты рецептор-лиганд-лекарственное средство. В настоящем изобретении предлагаются белки, полипептиды и/или пептиды, содержащие пирролизин и/или PCL, встроенные с использованием способов по настоящему изобретению. Указанные белки включают, но не ограничиваясь только ими, эритропоэтин (ЭПО), фактор роста фибропластов 21(FGF21), интерферон(ИФ-), интерлейкин 2 (ИЛ-2), интерлейкин 4 (ИЛ-4), интерлейкин 6 (ИЛ-6), интерлейкин 10 (ИЛ-10), интерлейкин 17 (ИЛ-17), инсулиноподобный фактор роста 1 (IGF-1) и интерферон(ИФ-). В настоящем изобретении предлагаются белки, полипептиды и/или пептиды, содержащие пирролизин и/или PCL, встроенные с использованием способов по настоящему изобретению и, кроме того, модифицированные с использованием способов по настоящему изобретению. Указанная модификация включает, но не ограничиваясь только им, ПЭГилирование. Указанные белки включают, но не ограничиваясь только ими, эритропоэтин (ЭПО), фактор роста фибропластов 21 (FGF21), интерферон(ИФ-),интерлейкин 2 (ИЛ-2), интерлейкин 4 (ИЛ-4), интерлейкин 6 (ИЛ-6), интерлейкин 10 (ИЛ-10), интерлейкин 17 (ИЛ-17), инсулиноподобный фактор роста 1 (IGF-1) и интерферон(ИФ-). Кроме того, в настоящем изобретении предлагаются белки, полипептиды и/или пептиды, содержащие встроенный пирролизин и/или PCL, при этом указанные белки, полипептиды и/или пептиды сшивают с использованием способов по настоящему изобретению. Указанные белки включают, но не ограничиваясь только ими, эритропоэтин (ЭПО), фактор роста фибропластов 21 (FGF21), интерферон(ИФ-) и интерферон(ИФ-). В других вариантах указанные сайт-специфичные модификации используют для получения белков,полипептидов и/или пептидов, в которых положение сайт-специфичного встраивания пирролизина илиPCL обеспечивает контролируемую ориентацию и присоединение указанных белков, полипептидов и/или пептидов к поверхности твердой подложки. В некоторых вариантах указанной твердой подложкой является пластиковый микротитрационный планшет, предметное стекло, поверхность диоксида кремния,полимерная гранула, золотые частицы или наночастицы с покрытием или без него. В других вариантах указанную контролируемую ориентацию и присоединение используют для анализа белков, полипептидов и/или пептидов методом ИФА или другими методами анализа с использованием антител. В некоторых вариантах указанную контролируемую ориентацию и присоединение используют для очистки и/или идентификации лигандов иммобилизованных белков, полипептидов и/или пептидов. В других вариантах указанную контролируемую ориентацию и присоединение используют для анализа белков, полипептидов и/или пептидов и их взаимодействий методом спектроскопии проникающей волны, включая, но не ограничиваясь только им, безмаркерный анализ с использованием поверхностного плазмонного резонанса. В некоторых вариантах указанную контролируемую ориентацию и присоединение к поверхностям используют для анализа белков, полипептидов и/или пептидов и их взаимодействия с использованием микровесов (электрических, оптических и/или механических), инфракрасной спектроскопии, рамановской спектроскопии, включая поверхностно-усиленную рамановскую спектроскопию, затухания резонанса, флуоресценции, интерферометрии, масс-спектроскопии и других спектроскопических методов. Указанные методы анализа используют для исследования взаимодействий иммобилизованных белков,полипептидов и/или пептидов с другими белками, полипептидами, пептидами, нуклеиновыми кислотами, ДНК, РНК, низкомолекулярными соединениями, лекарственными средствами, метаболитами, сахарами, углеводами, олигосахаридами, полисахаридами и/или другими молекулами, включая конформационные изменения, вызванные указанными взаимодействиями. Указанные методы анализа используют также для исследования взаимодействий иммобилизованных белков, полипептидов и/или пептидов с мультимерными комплексами белковых субъединиц, для изучения природных, рекомбинантных, синтетических или меченных рекомбинантных молекул, для поиска новых компонентов реакций в жидкостях организма, супернатантах клеточных культур или неочищенных экстрактах, для изучения взаимодействия низкомолекулярных соединений, таких как потенциальные лекарственные средства с их мишенями,для биохимического анализа мембран или взаимодействий с мембранносвязанными рецепторами с использованием природных мембран, искусственных мембран или везикул, для исследования репликации,транскрипции и трансляции, определения молекулярных взаимосвязей при формировании белковых комплексов и их взаимодействии с ДНК, для изучения гибридизации ДНК и РНК, изучения взаимодействий, в которых принимают участие интактные клетки или вирусы, изучения влияния гликозилирования на молекулярные взаимодействия, а также для определения специфичных свойств распознавания углеводов на клеточной поверхности. В других вариантах указанные сайт-специфичные модификации используют для сайт- 23021001 специфичного присоединения нуклеиновых кислот к белкам. В некоторых вариантах указанные сайтспецифичные модификации используют для сайт-специфичного присоединения нуклеиновых кислот к антителам или фрагментам антител. В других вариантах нуклеиновую кислоту, присоединенную к белку или антителу, используют для иммобилизации белка или антитела в определенных участках набора фрагментов ДНК за счет гибридизации. В некоторых вариантах нуклеиновую кислоту, присоединенную к белку или антителу, используют для детектирования связывания белка или антитела методом ПЦР,амплификацией замещением цепи (АЗЦ), лигазной цепной реакцией (ЛЦР), иммуно-ПЦР лигирования соседних фрагментов, амплификацией по типу катящегося кольца, транскрипционно опосредованной амплификацией, сигнальной амплификацией тирамид NEN или другими методами сигнальной амплификации. В некоторых вариантах указанное сайт-специфичное присоединение зонда ПЦР к антителу используют для получения реагента для иммуно-ПЦР (см. статью Adler М., Wacker R., Niemeyer Ch. M.,Sensitivity by combination: Immuno-PCR and related technologies, Analyst, 133, cc. 702-718 (2008. В других вариантах нуклеиновая кислота, присоединенная к белку или антителу, позволяет параллельно проводить анализ множества исследуемых соединений методом иммуно-ПЦР или другими методами иммуноанализа (мультиплексная иммуно-ПЦР или мультиплексные иммуно-анализы). В некоторых вариантах нуклеиновая кислота, присоединенная к белку или антителу, опосредует образование гомо- и гетеродимеров. Определения Использованный в данном контексте термин "алкил" обозначает насыщенный углеводород с разветвленной или прямой цепью. Использованные в данном контексте термины "C1-С 3 алкил", "С 1 С 4 алкил", "С 1-С 5 алкил", "С 1-С 6 алкил", "С 1-С 7 алкил" и "С 1-С 8 алкил" обозначают алкильную группу, содержащую по крайней мере 1 и не более 3, 4, 5, 6, 7 или 8 атомов углерода соответственно. Примеры алкильных групп, использованных в данном контексте, включают, но не ограничиваясь только ими, метил,этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, гексил, гептил, октил, нонил, децил и т.п. Использованный в данном контексте термин "алкилен" обозначает насыщенный двухвалентный углеводородный радикал с разветвленной или прямой цепью, причем радикал образуется при удалении одного атома водорода от каждого второго атома углерода. Использованные в данном контексте термины "C1-С 3 алкилен", "С 1-С 4 алкилен", "С 1-С 5 алкилен" и "С 1-С 6 алкилен" обозначают алкиленовую группу,содержащую по крайней мере 1 и не более 3, 4, 5 или 6 атомов углерода, соответственно. Примеры алкиленовых групп, использованных в данном контексте, включают, но не ограничиваясь только ими, метилен, этилен, н-пропилен, изопропилен, н-бутилен, изобутилен, втор-бутилен, трет-бутилен, н-пентилен,изопентилен, гексилен и т.п. Использованный в данном контексте термин "алкоксигруппа" обозначает группу -ORa, где Ra обозначает алкил, как определено в данном контексте. Использованные в данном контексте термины "C1 С 3 алкокси", "С 1-С 4 алкокси", "С 1-С 5 алкокси", "С 1-С 6 алкокси", "С 1-С 7 алкокси" и "С 1-С 8 алкокси" обозначают алкоксигруппу, в которой алкильный фрагмент содержит по крайней мере 1 и не более 3, 4, 5, 6, 7 или 8 атомов углерода. Примеры алкоксигрупп, использованных в данном контексте, включают, но не ограничиваясь только ими, метокси, этокси, н-пропокси, изопропокси, н-бутокси, трет-бутокси, пентокси,гексокси, гептокси и т.п. Использованный в данном контексте термин "N-концевая модифицирующая группа" обозначает любую молекулу, которая образует связь с концевой аминогруппой. Примеры указанных концевых аминогрупп включают, но не ограничиваясь только ими, аминозащитные группы, концевой фрагмент полимерных молекул, где указанные полимерные молекулы включают, но не ограничиваясь только ими, полипептиды, полинуклеотиды и полисахариды. N-концевые модифицирующие группы также включают,но не ограничиваясь только ими, различные водорастворимые полимеры, пептиды или белки. Примеры концевых модифицирующих групп включают полиэтиленгликоль или сывороточный альбумин. Некоторые N-концевые модифицирующие группы используют для модификации терапевтических свойств белков, включая, но не ограничиваясь только им, увеличение периода полураспада в сыворотке. Использованный в данном контексте термин "арил" обозначает моноциклическую, бициклическую и трициклическую кольцевые системы, содержащие в целом от пяти до четырнадцати атомов в цикле, где по крайней мере один цикл в системе является ароматическим и где каждый цикл в системе содержит от 3 до 7 атомов в цикле. Арил является "необязательно замещенным", при этом указанный арил содержит один или более заместителей. Если в данном контексте не указано иное, пригодные заместители обычно выбирают из галогена, -R, -OR, -SR, -NO2, -CN, -N(R)2, -NRC(O)R, -NRC(S)R, -NRC(O)N(R)2, -NRC(S)N(R)2, -NRCO2R,NRNRC(O)R, -NRNRC(O)N(R)2, -NRNRCO2R, -C(O)C(O)R, -С(O)CH2C(O)R, -CO2R, -C(O)R, -C(S)R,-C(O)N(R)2, -C(S)N(R)2, -OC(O)N(R)2, -OC(O)R, -C(O)N(OR)R, -C(NOR)R, -S(O)2R, -S(O)3R, -SO2N(R)2,-S(O)R, -NRSO2N(R)2, -NRSO2R, -N(OR)R, -C(=NH)-N(R)2, -P(O)2R, -PO(R)2, -OPO(R)2, - (CH2)0-2NHC(O)R,фенила (Ph), необязательно замещенного группой R, -O(Ph), необязательно замещенного группой R, - (СН 2)1-2(Ph), необязательно замещенного группой R, или -CH=CH(Ph), необязательно замещенного группой R, где в каждом случае R независимо выбирают из водорода, необязательно замещенного С 1-С 6 алкила, необязательно замещенной С 1-С 6 алкоксигруппы, незамещенного 5-6-членного гетероарила, фенила, -O(Ph) или -CH2(Ph),- 24021001 или два независимых R, расположенных у одного и того же заместителя или у различных заместителей,образуют вместе с атомом(ами), к которому присоединен каждый R, необязательно замещенный 3-12 членный насыщенный, частично ненасыщенный или полностью ненасыщенный моноциклический или бициклический цикл, содержащий 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы. Примеры использованных в данном контексте арилов включают, но не ограничиваясь только ими,фенил, нафтил, флуоренил, инденил, азуленил, антраценил, фенантраценил и т.п. Использованный в данном контексте термин "арилен" обозначает двухвалентный радикал, образующийся из арила. Использованный в данном контексте термин "бифункциональный сшиватель", также "бифункциональный полимер", обозначает линкер, содержащий две функциональные группы, которые способны специфически взаимодействовать с другими фрагментами, при этом образуются ковалентные или нековалентные связующие звенья. Указанные фрагменты включают, но не ограничиваясь только ими, группы боковых цепей аминокислот. Например, бифункциональный сшиватель содержит функциональную группу, вступающую в реакцию с группой в составе первого пептида, и другую функциональную группу,которая вступает в реакцию с группой в составе второго пептида, при этом образуется конъюгат, который включает первый пептид, бифункциональный линкер и второй пептид. Бифункциональный сшиватель характеризуется любой требуемой длиной или молекулярной массой, и его выбирают, чтобы обеспечить конкретное требуемое расположение в пространстве или конформацию. Использованный в данном контексте термин "многофункциональный сшиватель", также "многофункциональный полимер", обозначает линкер, содержащий две или более функциональных групп, которые способны взаимодействовать с другими фрагментами, при этом образуются ковалентные или нековалентные связующие звенья. Указанные фрагменты включают, но не ограничиваясь только ими,группы боковых цепей аминокислот. Многофункциональный сшиватель характеризуется любой требуемой длиной или молекулярной массой, и его выбирают, чтобы обеспечить конкретное требуемое расположение в пространстве или конформацию. Использованный в данном контексте термин "циано" обозначает группу -CN. Использованный в данном контексте термин "циклоалкил" обозначает насыщенную или частично ненасыщенную моноциклическую, конденсированную бициклическую, конденсированную трициклическую или мостиковую полициклическую систему. Использованные в данном контексте термины "С 3 С 5 циклоалкил", "С 3-С 6 циклоалкил", "С 3-С 7 циклоалкил", "С 3-С 8 циклоалкил", "С 3-С 9 циклоалкил" и "С 3 С 10 циклоалкил" обозначают циклоалкил, где насыщенная или частично ненасыщенная моноциклическая,конденсированная бициклическая или мостиковая полициклическая система содержит по крайней мере 3 и не более 5, 6, 7, 8, 9 или 10 атомов углерода. Примеры использованных в данном контексте групп циклоалкил включают, но не ограничиваясь только ими, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононил, циклодецил, циклопентенил, циклогексенил, декагидронафталенил, 2,3,4,5,6,7-гексагидро-1 Н-инденил и т.п. Использованный в данном контексте термин "циклодекстрин" обозначает циклические углеводы,содержащие по крайней мере от шести до восьми молекул глюкозы в циклической системе. Внешняя часть цикла содержит водорастворимые группы, в центре цикла расположена относительно неполярная полость, способная удерживать низкомолекулярные соединения. Использованный в данном контексте термин "галоген" обозначает фтор (F), хлор (Cl), бром (Br) или иод (I). Использованный в данном контексте термин "галоген" обозначает также радикалы галогенов: фтор(-F), хлор (-Cl), бром (-Br) и иод (-I). Использованный в данном контексте термин "галогенацил" обозначает ацил, который содержит атомы галогенов, включая, но не ограничиваясь только ими, -C(O)CH3, -C(O)CF3, -C(O)CH2OCH3 и т.п. Использованный в данном контексте термин "галогеналкил" или "замещенный галогеном алкил" обозначает алкил, как определено в данном контексте, замещенный по крайней мере одним атомом галогена или их комбинациями. Примеры указанных замещенных галогеном алкилов с разветвленной или прямой цепью, использованных в данном контексте, включают, но не ограничиваясь только ими, метил,этил, пропил, изопропил, изобутил и н-бутил, замещенные одним или более атомов галогенов или их комбинациями, включая, но не ограничиваясь только ими, трифторметил, пентафторэтил и т.п. Использованный в данном контексте термин "замещенная галогеном алкоксигруппа" обозначает алкоксигруппу, как определено выше, замещенную одним или более атомов галогенов или их комбинациями. Примеры указанных замещенных галогеном алкоксигрупп с разветвленной или прямой цепью,использованных в данном контексте, включают, но не ограничиваясь только ими, метокси, этокси, нпропокси, изопропокси, н-бутокси, трет-бутокси, пентокси, гексокси, гептокси и т.п., замещенные одним или более атомов галогенов или их комбинациями. Использованный в данном контексте термин "гетероалкил" обозначает алкил, как определено в данном контексте, в котором один или более атомов углерода независимо заменены на один или более атомов кислорода, серы, азота или их комбинации. Использованный в данном контексте термин "гетероалкилен" обозначает двухвалентный радикал,образующийся из гетероалкила. Использованный в данном контексте термин "гетероарил" обозначает моноциклическую, бициклическую и трициклическую кольцевые системы, содержащие в целом от пяти до четырнадцати атомов в цикле, где по крайней мере один цикл в системе является ароматическим, по крайней мере один цикл в системе содержит один или более гетероатомов, выбранных из азота, кислорода и серы, и где каждый цикл в системе содержит от трех до семи атомов. Если в данном контексте не определено иное, пригодные заместители ненасыщенного атома углерода в составе гетероарила обычно выбирают из галогена,-R, -OR, -SR, -NO2, -CN, -N(R)2, -NRC(O)R, -NRC(S)R, -NRC(O)N(R)2, -NRC(S)N(R)2, -NRCO2R,-NRNRC(O)R, -NRNRC(O)N(R)2, -NRNRCO2R, -C(O)C(O)R, -C(O)CH2C(O)R, -CO2R, -C(O)R, -C(S)R,-C(O)N(R)2, -C(S)N(R)2, -OC(O)N(R)2, -OC(O)R, -C(O)N(OR)R, -C(NOR)R, -S(O)2R, -S(O)3R, -SO2N(R)2,-S(O)R, -NRSO2N(R)2, -NRSO2R, -N(OR)R, -C(=NH)-N (R)2, -P(O)2R, -PO(R)2, -OPO(R)2,-(CH2)0-2NHC(O)R, фенила (Ph), необязательно замещенного группой R, -O(Ph), необязательно замещенного группой R, - (СН 2)1-2 (Ph), необязательно замещенного группой R, или -CH=CH(Ph), необязательно замещенного группой R, где в каждом случае R независимо выбирают из водорода, необязательно замещенного С 1-С 6 алкила, необязательно замещенной С 1-С 6 алкоксигруппы, незамещенного 5-6-членного гетероарила, фенила, -O(Ph) или -СН 2(Ph), или два независимых R, расположенных у одного и того же заместителя или у различных заместителей, вместе с атом(ами), к которому каждый R присоединен, образуют необязательно замещенный 3-12-членный насыщенный, частично ненасыщенный или полностью ненасыщенный моноциклический или бициклический цикл, содержащий 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы. Примеры использованных в данном контексте гетероарилов включают, но не ограничиваясь только ими, бензофуранил, бензофуразанил, бензоксазолил, бензопиранил, бензотиазолил, бензотиенил, бензазепинил, бензимидазолил, бензотиопиранил, бензо[1,3]диоксол,бензо[b]фурил, бензо[b]тиенил, циннолинил, фуразанил, фурил, фуропиридинил, имидазолил, индолил,индолизинил, индолин-2-он, индазолил, изоиндолил, изохинолинил, изоксазолил, изотиазолил, 1,8 нафтиридинил, оксазолил, оксаиндолил, оксадиазолил, пиразолил, пирролил, фталазинил, птеридинил,пуринил, пиридил, пиридазинил, пиразинил, пиримидил, пиримидинил, хиноксалинил, хинолинил, хиназолинил, 4 Н-хинолизинил, тиазолил, тиадиазолил, тиенил, триазинил, триазолил и тетразолил. Использованный в данном контексте термин "гетероциклоалкил" обозначает циклоалкил, как определено в данном контексте, где один или более атомов углерода в цикле заменены на остаток, выбранный из -О-,-N=, -NR-, -С(О)-, -S-, -S(O) - или -S(O)2-, при этом R обозначает водород, С 1-С 4 алкил или азотзащитную группу, при условии, что цикл, включающий указанную группу, не содержит два соседних атома О или S. Примеры использованных в данном контексте гетероциклоалкилов включают, но не ограничиваясь только ими, морфолино, пирролидинил, пирролидинил-2-он, пиперазинил, пиперидинил, пиперидинилон, 1,4 диокса-8-азаспиро[4.5]дец-8-ил, 2 Н-пирролил, 2-пирролинил, 3-пирролинил, 1,3-диоксоланил, 2-имидазолинил, имидазолидинил, 2-пиразолинил, пиразолидинил, 1,4-диоксанил, 1,4-дитианил, тиоморфолинил,азепанил, гексагидро-1,4-диазепинил, тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, тетрагидропиранил, дигидропиранил, тетрагидротиопиранил, тиоксанил, азетидинил, оксетанил, тиетанил, оксепанил,тиепанил, 1,2,3,6-тетрагидропиридинил, 2 Н-пиранил, 4 Н-пиранил, диоксанил, 1,3-диоксоланил, дитианил,дитиоланил, дигидропиранил, дигидротиенил, дигидрофуранил, имидазолинил, имидазолидинил, 3 азабицикло[3.1.0]гексанил и 3-азабицикло[4.1.0]гептанил. Использованный в данном контексте термин "гетероатом" обозначает один или более атомов кислорода, серы, азота, фосфора или кремния. Использованный в данном контексте термин "гидроксил" обозначает группу -ОН. Использованный в данном контексте термин "гидроксиалкил" обозначает алкил, как определено в данном контексте, замещенный по крайней мере одним гидроксилом, при этом гидроксил имеет значение, как определено в данном контексте. Примеры "C1-С 6 гидроксиалкилов" с разветвленной или прямой цепью включают, но не ограничиваясь только ими, метил, этил, пропил, изопропил, изобутил и н-бутил,независимо замещенные одной или более гидроксильных групп. Использованный в данном контексте термин "необязательно замещенный" обозначает, что указанная группа замещена или не замещена одной или более дополнительной группой(ами), в отдельности и независимо выбранной из алкила, алкенила, алкинила, циклоалкила, арила, гетероарила, гетероциклоалкила, гидроксила, алкоксигруппы, меркаптила, цианогруппы, галогена, карбонила, тиокарбонила, изоцианатогруппы, тиоцианатогруппы, изотиоцианатогруппы, нитрогруппы, пергалогеналкила, перфторалкила и аминогруппы,включая моно- и дизамещенные аминогруппы и защищенные производные указанных групп. Примеры необязательных заместителей включают, но не ограничиваясь только ими, галоген, -CN, -OR, -C(O)R, -OC(O)R,-С(О)OR, -OC(O)NHR, -C(O)N(R)2, -SR-, -S(=O)R, -S(=O)2R, -NHR, -N(R)2,-NHC(O)-, NHC(O)O-, -C(O)NH-,S(=O)2NHR, -S(O)2N(R)2, -NHS(=O)2, -NHS(O)2R, С 1-С 6 алкил, С 1-С 6 алкоксигруппу, арил, гетероарил, циклоалкил, гетероциклоалкил, замещенный галогеном С 1-С 6 алкил, замещенную галогеном С 1-С 6 алкоксигруппу, гдеR каждый независимо выбирают из Н, галогена, С 1-С 6 алкила, С 1-С 6 алкоксигруппы, арила, гетероарила, циклоалкила, гетероциклоалкила, замещенного галогеном С 1-С 6 алкила, замещенной галогеном С 1 С 6 алкоксигруппы. Использованный в данном контексте термин "аффинная метка" обозначает метку, которая обратимо или необратимо связывается с другой молекулой. Использованный в данном контексте термин "янтарный кодон" относится к встраиванию остатков пирролизина, PCL и других аналогов PCL и соответствует UAG, нуклеотидному триплету в составе матричной РНК. Нуклеотидная последовательность TAG закодирована в ДНК и транскрибируется в UAG в РНК, которая транслируется в белок. В данном контексте кодоны TAG и UAG используются взаимозаменяемо для обозначения встраивания остатка пирролизина, PCL и других аналогов пирролизина. Использованный в данном контексте термин "аминокислота" обозначает природные аминокислоты, не природные аминокислоты, аналоги аминокислот и миметики аминокислот, действие которых аналогично действию природных аминокислот, а также все D и L стереоизомеры указанных аминокислот, если их структура допускает существование таких стереоизомерных форм. В данном контексте используют стандартные названия аминокислот, известный трехбуквенный код или однобуквенный код, рекомендованные комиссией по биохимической номенклатуре IUPAC-IUB. Природные аминокислоты представляют собой аминокислоты,которые кодируются генетическим кодом и которые затем модифицируют. Природные аминокислоты включают, но не ограничиваясь только ими, аланин (Ala), аргинин (Arg), аспарагин (Asn), аспарагиновую кислоту(PCL). Модифицированные кодированные аминокислоты включают, но не ограничиваясь только ими, гидроксипролин, -карбоксиглутамат, O-фосфосерин, азетидинкарбоновую кислоту, 2-аминоадипиновую кислоту,3-аминоадипиновую кислоту, -аланин, аминопропионовую кислоту, 2-аминомасляную кислоту, 4 аминомасляную кислоту, 6-аминокапроновую кислоту, 2-аминогептановую кислоту, 2-аминоизомасляную кислоту, 3-аминоизомасляную кислоту, 2-аминопимелиновую кислоту, трет-бутилглицин, 2,4-диаминоизомасляную кислоту, десмозин, 2,2'-диаминопимелиновую кислоту, 2,3-диаминопропионовую кислоту, Nэтилглицин, N-метилглицин, N-этиласпарагин, гомопролин, гидроксилизин, аллогидроксилизин, 3 гидроксипролин, 4-гидроксипролин, изодесмозин, аллоизолейцин, N-метилаланин, N-метилглицин, Nметилизолейцин, N-метилпентилглицин, N-метилвалин, нафталанин, норвалин, норлейцин, орнитин, пентилглицин, пипеколиновую кислоту и тиопролин. Термин "аминокислота" также включает природные аминокислоты, которые являются метаболитами некоторых организмов, но не кодируются генетическим кодом для включения в состав белков. Указанные аминокислоты включают, но не ограничиваясь только ими, орнитин,D-орнитин и D-аргинин. Использованный в данном контексте термин "аналог аминокислоты" обозначает соединения, которые характеризуются той же основной химической структурой, что и природная аминокислота, но при этом содержат, например, атом -углерода, который связан с атомом водорода, карбоксильную группу,аминогруппу и группу R. Аналоги аминокислот включают природные и не природные аминокислоты,которые обратимо или необратимо блокированы, или входящая в их состав С-концевая карбоксильная группа, N-концевая аминогруппа и/или функциональные группы боковых цепей модифицированы химическим методом. Указанные аналоги включают, но не ограничиваясь только ими, метионинсульфоксид,метионинсульфон, S-(карбоксиметил)цистеин, S-(карбоксиметил)цистеинсульфоксид, S-(карбоксиметил)цистеинсульфон, -метиловый эфир аспарагиновой кислоты, N-этилглицин, аланинкарбоксамид, гомосерин, норлейцин и метилметионинсульфоний. Примеры блокирующих групп включают, но не ограничиваясь только ими, трет-бутилоксикарбонил (Boc) и 9-флуоренилметилоксикарбонил (Fmoc). Использованный в данном контексте термин "миметики аминокислот" обозначает химические соединения, структура которых отличается от основной химической структуры аминокислот, но действие которых аналогично действию природной аминокислоты. Использованный в данном контексте термин "не природная аминокислота" обозначает структуры аминокислот, которые не образуются биосинтетическим способом в любом организме с использованием не модифицированных или модифицированных генов из любого организма, одинаковых или различных. Кроме того, следует понимать, что для встраивания указанных "не природных аминокислот" в белок требуется модифицированная тРНК и модифицированная тРНК-синтетаза (PC). Указанные "выбранные" пары ортогональных тРНК/РС являются специфичными для не природной аминокислоты и их получают в процессе отбора (см. статью Schultz и др., или с использованием аналогичной методики). Например,пирролинкарбоксилизин представляет собой "природную аминокислоту", т.к. его получают биосинтетическим методом с использованием генов, перенесенных из одного организма в клетки-хозяина, и т.к. его встраивают в белки с использованием генов природной тРНК и тРНК-синтетазы, в то время как парааминофенилаланин (см. статью Mehl R. А., Anderson J. С., Santoro S. W., Wang L., Martin А. В., King D.S., Horn D. M., Schultz P. G., Generation of a bacterium with a 21 amino acid genetic code, J. Am. Chem. Soc.,125 (4), cc. 935-939 (29 января 2003 г. представляет собой "не природную аминокислоту", так как, несмотря на то, что его получают биосинтетическим методом, в белки его встраивают с использованием"выбранной" пары ортогональных тРНК/тРНК-синтетаза. Использованный в данном контексте термин "аминокислотный остаток" обозначает фрагменты где указанные фрагменты образуются из аминокислот, и группа R представляет собой боковую цепь любой аминокислоты, описанной в данном контексте. Указанные аминокислотные остатки включают, но не ограничиваясь только ими, аланинил, аргининил, аспарагинил, аспартил, цистеинил, глутаминил, глутамил, глицинил, гистидинил, изолейцинил, лейцинил, лизинил, метионинил, фенилаланинил,пролинил, серинил, треонинил, триптофанил, тирозинил, валинил, пироглутамат, формилметионин, пирроглицинил и селеноцистеинил. Использованный в данном контексте термин "N-концевая модифицирующая группа" обозначает любую молекулу, которую можно присоединить к концевой аминогруппе. Указанные N-концевые модифицирующие группы включают, но не ограничиваясь только ими, аминозащитные группы, концевой фрагмент полимерных молекул, причем указанные полимерные молекулы включают, но не ограничиваясь только ими, полипептиды, полинуклеотиды и полисахариды. Концевые модифицирующие группы также включают, но не ограничиваясь только ими, различные водорастворимые полимеры, пептиды или белки. Например, N-концевые модифицирующие группы включают полиэтиленгликоль или сывороточный альбумин. Некоторые N-концевые модифицирующие группы используют для модификации терапевтических свойств белка, полипептида или пептида, включая, но не ограничиваясь только им, увеличение периода полураспада указанных белков, полипептидов или пептидов в сыворотке. Использованный в данном контексте термин "фрагмент антитела" обозначает любую форму антитела, отличную от полноразмерной формы. В данном контексте фрагменты антител включают антитела,которые являются более короткими компонентами полноразмерных антител, и антитела, сконструированные генноинженерными методами. Фрагменты антител включают, но не ограничиваясь только ими,Fv, Fc, Fab и (Fab')2, одноцепочечный Fv (oцFv), диатела, триотела, тетратела, бифункциональные гибридные антитела, CDR1, CDR2, CDR3, комбинации CDR, вариабельные области, каркасные области,консервативные области, тяжелые цепи, легкие цепи, а также другие молекулы клеточного каркаса, не относящиеся к антителам, биспецифические антитела и т.п. Другой функциональной субструктурой является одноцепочечный Fv (oцFv), состоящий из вариабельных областей тяжелой и легкой цепей иммуноглобулина, ковалентно связанных пептидным линкером. Указанные низкомолекулярные (ММ 25000 Да) белки обычно сохраняют специфичность и аффинность в отношении антигена в одном полипептиде,и их можно использовать для конструирования более крупных антиген-специфичных молекул. Если не указано иное, при использовании в настоящем описании и в пунктах формулы изобретения термин "антитело" или "антитела" также включает "фрагмент антитела" и "фрагменты антител". Использованный в данном контексте термин "биодоступность" обозначает скорость и степень, с которой соединение или его активный фрагмент доставляется из фармацевтической лекарственной формы и становится доступным в участке действия или в основном кровотоке. Повышение биодоступности обозначает повышение скорости и степени, с которой соединение или его активный фрагмент доставляется из фармацевтической лекарственной формы и становится доступным в участке действия или в основном кровотоке. Например, о повышении биодоступности можно судить по увеличению концентрации соединения или его активного фрагмента в крови по сравнению с другими соединениями или активными фрагментами. Использованные в данном контексте термины "биологически активная молекула", "биологически активный фрагмент" или "биологически активный агент" обозначают любое соединение, которое влияет на любые физические или биохимические свойства биологической системы, пути передачи сигнала, на молекулы или взаимодействие, связанное с организмом, включая, но не ограничиваясь только ими, вирусы, бактерии, бактериофаг, транспозон, прион, насекомых, грибы, растения, животных и человека. Использованные в данном контексте биологически активные молекулы, прежде всего, включают, но не ограничиваясь только ими, любое соединение, предназначенное для диагностики, лечения, снижения интенсивности симптомов, лечения или профилактики заболевания у человека или других животных, или для другого улучшения физического или психического состояния человека или животных. Примеры биологически активных молекул включают, но не ограничиваясь толькоими, пептиды, белки, ферменты,ДНК, РНК, низкомолекулярные лекарственные средства, сильнодействующие наркотики, слабые наркотики, полисахариды, олигосахариды, дисахариды, углеводы, неорганические атомы или молекулы, красители, липиды, нуклеозиды, радионуклиды, олигонуклеотиды, токсины, клетки, вирусы, липосомы,микрочастицы и мицеллы. Классы биологически активных агентов, которые пригодны для использования в способах и композициях, описанных в данном контексте, включают, но не ограничиваясь только ими, лекарственные средства, пролекарства, радионуклиды, визуализирующие агенты, полимеры, антибиотики, фунгициды, противовирусные агенты, противовоспалительные агенты, противоопухолевые агенты, сердечно-сосудистые агенты, седативные агенты, гормоны, факторы роста, стероидные агенты,токсины бактериального происхождения и т.п. Использованный в данном контексте термин "модуляция биологической активности" обозначает повышение или снижение концентрации или реакционной способности белка, полипептида, пептида,ДНК, РНК, сахаридов, сахаров, метаболитов, предшественников, кофакторов или других биологически активных химических соединений или объектов, изменение селективности белка, полипептида, пептида,ДНК, РНК, сахаридов, сахаров, метаболитов, предшественников, кофакторов или других биологически активных химических соединений или объектов, или повышение или снижение субстратной селективности белка, полипептида, пептида, ДНК, РНК, сахаридов, сахаров, метаболитов, предшественников, кофакторов или других биологически активных химических соединений или объектов. Использованный в данном контексте термин "биоматерил" обозначает материал биологического происхождения, включая, но не ограничиваясь только ими, материал, полученный с использованием биореакторов и/или рекомбинантных методов и методик. Использованный в данном контексте термин "биофизический зонд" обозначает зонды, которые обеспечивают детекцию или контроль структурных изменений в молекулах физическими методами детектирования. Указанные молекулы включают, но не ограничиваясь только ими, белки, полипептиды,пептиды, ДНК или РНК. Указанный "биофизический зонд" также используют для детектирования или контроля взаимодействия белков, полипептидов, пептидов, ДНК или РНК с другими молекулами, включая, но не ограничиваясь только ими, макромолекулы. Примеры биофизических зондов включают, но не ограничиваясь только ими, молекулярную массу, ядерные спины, поглощение УФ, флуоресценцию, круговой дихроизм, теплоемкость, температуру плавления или другие характеристические молекулярные свойства. Примеры биофизических зондов включают также метки, которые включают в молекулу. Указанные зонды включают, но не ограничиваясь только ими, спиновые метки, флуорофоры, изотопные метки и фотоактивируемые группы. Использованный в данном контексте термин "полученный биосинтетическим способом" обозначает любой способ использования клетки или ферментов для получения аминокислоты. Указанные способы включают применение по крайней мере одного из следующих компонентов: предшественника и фермента. В некоторых вариантах указанные аминокислоты затем встраивают в белок. В других вариантах биосинтез и встраивание аминокислот осуществляют в одной и той же клетке, в то время как в некоторых вариантах аминокислоту получают биосинтетическим методом в отдельной клетке ("питающей клетке"),или в отдельной клеточной культуре, а в белок аминокислоту встраивают в другой клетке. В последнем случае аминокислоту необязательно очищают от отдельной клеточной культуры, и затем очищенную аминокислоту добавляют в среду другой клеточной культуры, где происходит встраивание аминокислоты в белок. Использованный в данном контексте термин "аналог" биотина", или также "миметик биотина", обозначает любую молекулу, отличную от биотина, которая с высокой аффинностью связывается с авидином и/или стрептавидином. Использованный в данном контексте термин "С-концевая модифицирующая группа" обозначает любую молекулу, которую можно присоединить к концевой карбоксигруппе. Указанные концевые карбоксигруппы включают, но не ограничиваясь только ими, карбоксилатзащитные группы, концевой фрагмент полимерных молекул, причем указанные полимерные молекулы включают, но не ограничиваясь только ими, полипептиды, полинуклеотиды и полисахариды. Концевые модифицирующие группы также включают, но не ограничиваясь только ими, различные водорастворимые полимеры, пептиды или белки. Например, концевые модифицирующие группы включают полиэтиленгликоль или сывороточный альбумин. Некоторые С-концевые модифицирующие группы используют для модификации терапевтических свойств белка, полипептида или пептида, включая, но не ограничиваясь только им, увеличение периода полураспада в сыворотке. Использованный в данном контексте термин "химически расщепляемая группа", а также "химически лабильная группа" обозначает группу, которая распадается или расщепляется в присутствии кислоты, основания, окислительных агентов, восстанавливающих агентов, химических инициаторов или радикальных инициаторов. Использованный в данном контексте термин "хемилюминесцентная группа" обозначает группу, которая испускает свет в результате химической реакции без нагревания. Например, люминал (5-амино-2,3 дигидро-1,4-фталазиндион) взаимодействует с окислителями, такими как пероксид водорода (H2O2), в присутствии основания и металлического катализатора, при этом образуется продукт в возбужденном состоянии, 3-аминофталат (3-АФА), что затем приводит к испусканию детектируемого света. Использованный в данном контексте термин "хромофор" обозначает молекулу, которая поглощает свет при длине волны в видимой области, длине волны в УФ-области или при длине волны в инфракрасной области. Использованный в данном контексте термин "кофактор" обозначает атом или молекулу, которые необходимы для действия макромолекулы. Кофакторы включают, но не ограничиваясь только ими, неорганические ионы, коферменты, белки или некоторые другие факторы, требующиеся для активности ферментов. Использованный в данном контексте термин "кофолдинг" обозначает процессы, реакции или спо- 29
МПК / Метки
МПК: C07K 2/00, C07D 209/00, C12P 13/04, C07D 207/20, C07K 1/107, C12P 21/00
Метки: счет, пирролинкарбоксилизин, пирролинкарбоксилизина, модификации, белка, биосинтетический, сайт-специфичные, химической, пирролизина, остатков
Код ссылки
<a href="https://eas.patents.su/30-21001-biosinteticheskijj-pirrolinkarboksilizin-i-sajjt-specifichnye-modifikacii-belka-za-schet-himicheskojj-modifikacii-ostatkov-pirrolinkarboksilizina-i-pirrolizina.html" rel="bookmark" title="База патентов Евразийского Союза">Биосинтетический пирролинкарбоксилизин и сайт-специфичные модификации белка за счет химической модификации остатков пирролинкарбоксилизина и пирролизина</a>
Предыдущий патент: Трансформаторная подстанция
Следующий патент: Стенд для проведения лабораторных работ по электротехнике, электронике и программированию
Случайный патент: Терапевтические композиции












