Соединения индола
Номер патента: 18724
Опубликовано: 30.10.2013
Авторы: Лундриган Реджина, Барден Тимоти, Скэйрер Уэйн, Милн Дж.Тодд, Спротт Кевин, Мермериан Ара, Пирсон Джеймс Филип, Ким Чарльз, Ян Джейн, Толли Джон Джефри, Карри Марк Дж.
Формула / Реферат
1. Соединение, имеющее формулу A, или его фармацевтически приемлемая соль
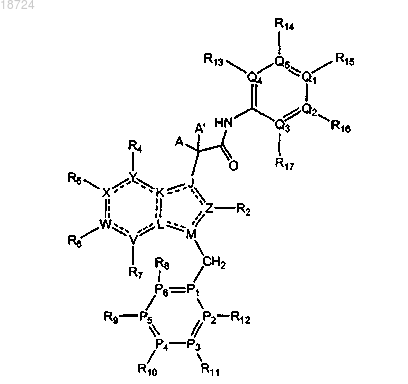
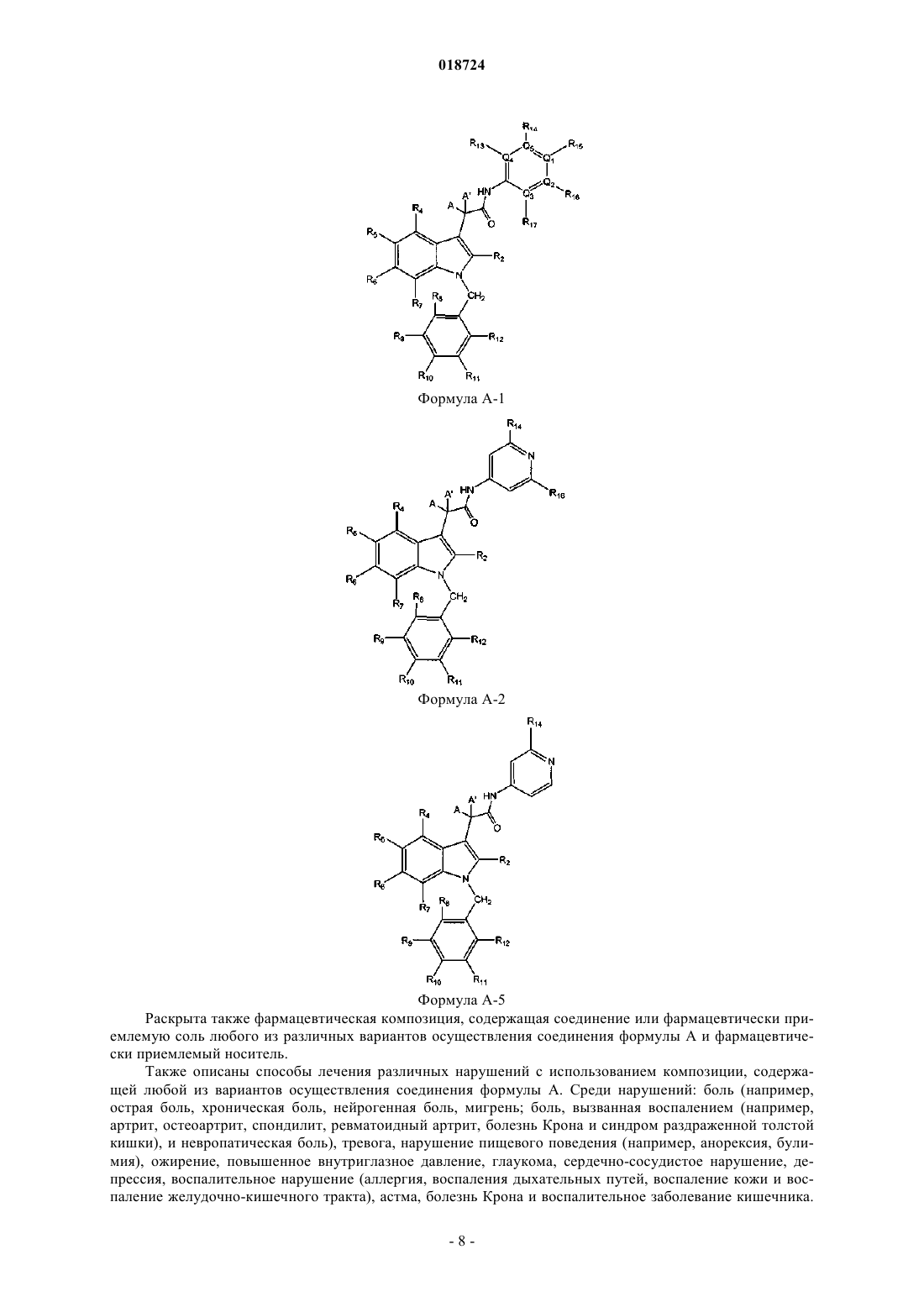
Формула A
где V, W, X, Y, Z, J, K, L представляют собой C;
M представляет собой N;
Q1 представляет собой N;
Q2, Q3, Q4 и Q5 представляют собой C;
a) P1, P2, P3, P4, P5 и P6 представляют собой C или
b) один из P1, P2, P3, P4, P5 и P6 представляет собой N, а остальные представляют собой C;
A и A', взятые вместе, представляют собой =O;
R2 представляет собой необязательно независимо замещенный C1-C3-алкил или циклопропил, где необязательные заместители выбирают из 1-3 атомов фтора;
каждый из R4, R6 и R7 независимо представляет собой H, галоген, гидрокси, необязательно независимо замещенный C1-C5-алкил или необязательно независимо замещенный C1-C5-алкокси;
где для каждого указанного C1-C5-алкила или C1-C5-алкокси необязательные заместители независимо выбирают из 1-3 атомов фтора и где вплоть до двух из R4, R6 и R7 являются одновременно замещенными;
R5 представляет собой H, галоген, -NO2, -CN, -C(O)OH, гидрокси, необязательно независимо замещенный C1-C5-алкил, необязательно независимо замещенный C2-C5-алкенил, необязательно независимо замещенный C2-C5-алкинил, необязательно независимо замещенный C1-C5-алкокси, -C(O)NRaRb или -NRaRb, где Ra и Rb независимо представляют собой H, необязательно независимо замещенный C1-C6-алкил или необязательно независимо замещенный C3-C6-циклоалкил;
где для каждого C1-C5-алкила, C2-C5-алкенила или C2-C5-алкинила необязательные заместители независимо выбирают из 1 или 2 оксо, гидрокси, C1-C3-ацилокси, C1-C3-алкокси и NH2 групп или 1-3 атомов галогена;
каждый из R8, R9, R11 и R12, когда связан с С, независимо представляет собой H, галоген или гидрокси;
R12, когда связан с C, представляет собой H, галоген, -NO2, гидрокси, необязательно независимо замещенный C1-C5-алкил или необязательно независимо замещенный C1-C5-алкокси, где необязательный заместитель для указанного C1-C5-алкила или С1-С5-алкокси выбирают из 1-3 атомов галогена;
каждый из R8, R9, R10 R11 и R12, когда связан с N, отсутствует;
R14 выбирают из H, галогена, -CN, гидрокси, необязательно независимо замещенного C1-C5-алкила или необязательно независимо замещенного C1-C5-алкокси;
R16 выбирают из H, галогена, гидрокси, необязательно независимо замещенного C1-C5-алкила или необязательно независимо замещенного C1-C5-алкокси;
где для R14 и R16 необязательные заместители в каждом указанном C1-C5-алкиле или C1-C5-алкокси выбирают из 1-3 атомов фтора;
R15 отсутствует;
R13 выбирают из H или галогена;
R17 выбирают из H или галогена.
2. Соединение по п.1, где один из Р1, Р2, P3, Р4, P5 и Р6 представляет собой N и остальные представляют собой C.
3. Соединение по п.1, где P1, Р2, P3, P4, P5 и P6 представляют собой C.
4. Соединение по п.1, где R2 представляет собой C1-C3-алкил или циклопропил.
5. Соединение по п.4, где R2 представляет собой метил.
6. Соединение по п.1, где один или два из R8, R9, R10, R11 и R12 представляют собой галоген и остальные представляют собой H.
7. Соединение по п.6, где один или два из R8, R9, R10, R11 и R12 представляют собой Cl или F и остальные представляют собой H.
8. Соединение по п.7, где R10 представляет собой галоген.
9. Соединение по п.8, где один из R8 и R12 представляет собой галоген и другой представляет собой H.
10. Соединение по п.9, где R10 представляет собой Cl или F и R8, R9, R11 и R12 представляют собой Н.
11. Соединение по п.10, где R10 представляет собой Cl или F; R8 представляет собой Cl или F и R9, R11 и R12 представляют собой H.
12. Соединение по п.1, где R4 и R7 представляют собой H.
13. Соединение по п.1, где R6 представляет собой H.
14. Соединение по п.12 и 13, где R5 выбирают из этокси, метокси, этила, метила, галогена и Н.
15. Соединение по п.14, где R5 выбирают из метокси, метила и Н.
16. Соединение по п.15, где R5 представляет собой метокси.
17. Соединение по п.15, где R5 представляет собой метил.
18. Соединение по п.1, где R14 представляет собой галоген или необязательно независимо замещенный метокси и R13 и R17 представляют собой H.
19. Соединение по п.18, где R14 представляет собой -OCH3.
20. Соединение по п.1, выбранное из следующего списка соединений:
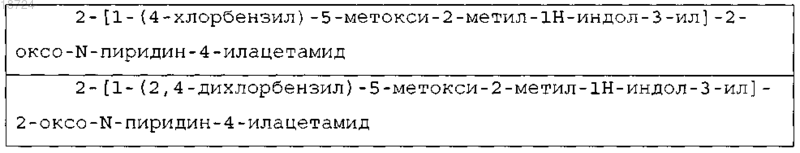



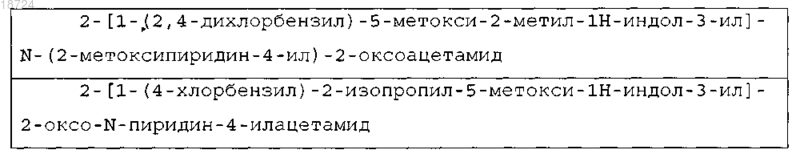
Текст
Изобретение относится к производным индола формулы A Формула А или их фармацевтически приемлемым солям, где V, W, X, Y, Z, J, K, L представляют собой C;M представляет собой N; Q1 представляет собой N; Q2, Q3, Q4 и Q5 представляют собой C; а) P1, P2,P3, P4, P5 и P6 представляют собой C или b) один из P1, P2, P3, P4, P5 и P6 представляет собой N, а остальные представляют собой C; A и A', взятые вместе, представляют собой =O; которые могут быть использованы для лечения боли, воспаления и других состояний. Предшествующий уровень техники Ингибиторы COX. Циклооксигеназы играют существенную роль в синтезе простагландина. Циклооксигеназа-1(COX-1) является конститутивной и относительно долго живущей, в то время как циклогеназа-2 (COX-2) индуцируема и сравнительно недолговечна. Предполагается, что COX-1 поддерживает базальный уровень продуцирования простагландина, который важен для нормального желудочно-кишечного и почечного функционирования. COX-2 стимулируется некоторыми возбудителями воспаления, гормонами,факторами роста, цитокинами, а также другими агентами. COX-2 играет существенную роль в синтезе простагландина в клетках воспаления, таких как макрофаги и моноциты, причем продуцирование простагландина путем индукции COX-2 может вызывать разрушительные эффекты в человеческом организме. Таким образом, для уменьшения нежелательного воспаления и для лечения определенных состояний желательно ингибировать активность COX-2 без существенного ингибирования COX-1. Многие нестероидные противовоспалительные лекарственные средства (NSAID) ингибируют какCOX-1, так и COX-2. Примером таких неселективных ингибиторов является индометацин (Shen et al.,1963, J. Am. Chem. Soc. 85:4881; 4-хлорбензоил-5-метокси-2-метил-1H-индоло-3-уксусная кислота). Актуальна проблема идентификации таких NSAID, которые существенно ингибируют COX-2 на физиологических уровнях, но в то же время только в незначительной степени блокируют COX-1. Ожидается, что такие селективные ингибиторы будут обладать желательными противовоспалительными, жаропонижающими и обезболивающими свойствами NSAID, имея при этом пониженную желудочно-кишечную и почечную токсичность или ее полное отсутствие. После введения индометацина в плазме в значительных количествах могут быть обнаружены не изменившиеся исходные соединения: десметил-метаболит [О-десметилиндометацин; (1-(4-хлорбензоил)-5-гидрокси-2-метил-1H-индолил-3 уксусная кислота)]; десбензоил-метаболит [N-десхлоробензоилиндометацин; (5-метокси-2-метил-1H-индолил-3-уксусная кислота)]; десметил-десбензоил-метаболит [O-десметил-N-десхлорбензоилиндометацин; (5-гидрокси-2-метил 1H-индолил-3-уксусная кислота)](Strachman et al. 1964, J. Am. Chem. Soc. 8:799; Helleberg. 1981, Clin. Pharmacokinet. 6:245),причем все в несвязанной форме (Harman et al. 1964, J. Pharmocol. Exp. Therap. 143:215). Известно, что все три метаболита не обладают противовоспалительной активностью (Helleberg 1981 Clin.Pharmacokine. 6:245 и Duggan et al. 1972, Pharmacol.Exp. Ther. 181:562), хотя и существуют данные,указывающие на некоторую способность десметил-метаболита ингибировать синтез простагландина(Shen et al. 1977, Adv. Drug. Res. 12:90). Производные индометацина, в которых бензоильная группа заменена 4-бромбензильной или удлинена боковая цепь во фрагменте уксусной кислоты, демонстрируют более выраженную селективность в ингибировании COX-2 по сравнению с COX-1 (Black et al. 1996, BioorganicMedicinal. Chem. Lett. 6:725 и Black et al. 1997, Advances in Experimental MedicineBiology. 407:73). В дополнение, разработана методика синтеза, позволившая получить ряд аналогов индометацина, некоторые из которых не ингибируют циклооксигеназы (Touhey et al. 2002, Eur. J. Cancer. 38:1661). Ингибиторы FAAH. Известно, что многие амиды жирных кислот обладают аналгезирующей активностью. Некоторые амиды жирных кислот (например, арахидонил-замещенные аминокислоты и анандамид) индуцируют анальгезию на болевых моделях животных (описанные в данном изобретении, Walker et al. 1999, Proc.Natl. Acad. Sci. 96:12198, FrideMechoulam 1993, Eur. J. Pharmacol. 231:313). Анандамид и некоторые другие амиды жирных кислот (например, N-пальмитоилэтаноламин, N-олеоилэтаноламид, олеамид,2-арахидоноилглицерол) расщепляются и дезактивируются гидролазой амидов жирных кислот (FAAH),интегральным мембранным белком (Deutsch et al. 2003, Prostaglandins Leukot Essent Fatty Acids. 66:201 иCravatt и Lichtman 2003, Current Opinion in Chemical Biology. 7:469). Недавно был идентифицирован паралог человеческой FAAH, названный FAAH-2 (Wei et al. 2006, J.Biol. Chem. 281:36569). FAAH-2 была идентифицирована у сложных приматов, сумчатых и у более эволюционно далеких позвоночных, но не обнаружена у нескольких видов низкоразвитых плацентарных млекопитающих, включая мышей и крыс. Два человеческих энзима FAAH, совпадая на 20% по идентичности последовательности, гидролизуют субстраты амидов первичных жирных кислот (например, олеамид) примерно с одинаковой скоростью, однако FAAH (иногда называемая FAAH-1) более активна в отношении N-ацилэтаноламинов (например, анандамида) и N-ацилтауринов. Согласно Wei et al., какFAAH, так и FAAH-2 чувствительны ко всем основным классам ингибиторов FAAH, которые известны на сегодняшний день, включая O-арилкарбаматы и -кетогетероциклы. Ожидается, что ингибирование FAAH приведет к увеличению уровня анандамида и амидов других жирных кислот. Такое увеличение в концентрации амидов жирных кислот может повысить порог болевой чувствительности. Следовательно, ингибиторы FAAH могут быть использованы в терапии боли. Подобные ингибиторы могут быть использованы также при лечении нарушений, для лечения которых при-1 018724 меняются амиды жирных кислот или модуляторы каннабиноидных рецепторов (например, при состоянии страха, нарушениях пищевого поведения и сердечно-сосудистых заболеваний). N-PAA (ангидролаза(PEA), амид жирной кислоты. PEA является природным субстратом каннабиноидного рецептора 2N-PAA могут быть использованы для снятия воспалительных и ноцицептивных болей. Моноацилглицерол-липаза (MAGL, MGL) является гидролазой, расщепляющей эндоканнабиноидный лиганд, 2-арахидоноидглицерин (2-AG). Несмотря на то что FAAH тоже расщепляет 2-AG, MAGL считается основным ферментом, ответственным за мозговой метаболизм 2-AG. Таким образом, ингибиторы 2-AG могут быть использованы для лечения заболеваний, ассоциированных с каннабиноидными рецепторами, включая тревогу, нарушение режима питания, а также сердечно-сосудистые заболевания. Ингибиторы MAGL и FAAH могут иметь различные терапевтические применения (Bahr et al. Expert.Opin. Investig Drugs, 2006, vol. 15 p. 351-65). Кроме того, существуют данные (описанные в данном изобретении, Weber et al. 2004, J. Lipid Res. 45:757), которые демонстрируют, что при условии подавления или полного блокирования активностиFAAH один из ее субстратов - анандамид - работает в качестве субстрата COX-2 с последующим преобразованием в простамид. Таким образом, возможно повышение уровня некоторых простамидов в присутствии ингибитора FAAH. Принимая во внимание, что определенные простамиды ассоциированы с пониженным внутриглазным давлением и глазной гипотензивностью, ингибиторы FAAH могут быть использованы при лечении глаукомы. Модуляторы CRTH2.CRTH2 является рецептором, связанным с Gi белком и участвующим в регулировании как хемоаттрактации, вызванной PGD2, так и активации определенных типов клеток при аллергическом воспалении. Известно, что CRTH2 экспрессирован Th2 клетками, эозинофилами и базофилами, а не клеткамиPGD2 продуцируется аллерген-активированными мастоцитами и вовлекается в различные аллергические заболевания в качестве провоспалительного медиатора, хотя в некоторых случаях может иметь место и противовоспалительная активность (Ajuebor et al. 2000, Am. J. Physiol Gastrointest Liver Physiol. 279:G238-44). CRTH2 рецептор, а также DP-1 рецептор, связанный с Gs белком, обладают высокой аффинностью в отношении PGD2.CRTH2 вызывает временный приток эозинофилов из костного мозга в кровь (Shichijo 2003, J. Pharmacol.Exp. Ther. 307:518-525). Генетические исследования в африкано-американской и китайской когортах обнаружили, что полиморфизмы CRTH2 тесно ассоциированы с восприимчивостью к астме (Huang et al. 2004, Hum. Mol. Genet. 2791). Было предположено, что модуляторы CRTH2 могут быть использованы при профилактике и/или лечении аллергической астмы и других аллергических нарушений(US 2002/0022218 A1 и WO 03/066047). Феномен рекрутмента и/или активации эозинофилов, базофилов и Th2 клеток представляет собой исключительно важные изменения, происходящие в астматическом легком. Аналогичная активация клеток такого типа или, точнее, их субпопуляций может играть важную роль в этиологии других заболеваний, включая эозинофильный эзофагит и атопический дерматит (Arora и Yamakazi 2004, Clin. Gastroenterol. Hepatol. 2:523-30; Kiehl et al. 2001, Br. J. Dermatol. 145:720-729). Этот факт, а также то, что CRTH2 опосредует индуцированный PGD2 хемотаксис, предполагает, что соединения, изменяющие хемотаксис путем модулирования активности CRTH2, могут быть использованы в контроле хронического воспаления дыхательных путей, атопического дерматита, хронического обструктивного заболевания легких (COPD) и/или эозинофильного эзофагита. Соединения, изменяющие хемотаксис модулированием активности CRTH2, также могут быть способны контролировать аллергический ринит. Аллергический ринит подразделяется на сезонный (CAP) и многолетний (MAP), в зависимости от типа триггера и продолжительности симптомов. Симптомы CAP проявляются весной, летом и/или ранней осенью и вызываются наружными аллергенами, такими как присутствующая в воздухе пыльца деревьев, травы и сорняков, в то время как MAP обычно является постоянным и хроническим, с круглогодичными симптомами и обычно вызывается внутренними аллергенами, такими как пылевые клещи,перхоть животных и/или споры плесени. Симптомы аллергического ринита могут включать насморк,носовой зуд, чихание, слезящиеся глаза и заложенный нос. Модуляторы CRTH2 могут быть использованы для лечения CAP и/или MAP. Антагонисты CRTH2, уменьшающие способность клеток Th2 и эозинофилов реагировать на произведенные из PGD2 мастоциты, могут быть использованы для предотвращения или лечения аллергических расстройств, таких как аллергический ринит и астма. Часто оказывается, что агонисты вызывают десенсибилизацию клеточной системы путем поддержки интернационализации и даун-регуляции клеточной поверхности рецептора (Int. Immunol. 15:29-38,-2 018724 2003). Таким образом, некоторые агонисты CRTH2 благодаря способности вызывать десенсибилизациюPGD2-чувствительных клеток могут быть использованы в терапии. На примерах некоторых агонистовCRTH2 было показано, что десенсибилизация PGD2-чувствительных клеток действительно происходит после активации агонистом CRTH2 (описанные в данном изобретении, Yoshimura-Uchiyama et al. 2004,Clin. Exp. Allergy. 34:1283-1290). Важно отметить, что агонисты CRTH2 могут также вызывать перекрестную десенсибилизацию. Перекрестная десенсибилизация может происходить во многих сигнализационных системах клетки и представляет собой уменьшение или полное подавление сигнальной чувствительности клетки, за исключением одной сигнальной системы агонист/рецептор. Например, известно,что агонист CRTH2 индометацин уменьшает экспрессию CCR3, являющегося рецептором для хемоаттрактанта эотаксина (Stubbs et al. 2002, J. Biol. Chem. 277:26012-26020). Ингибиторы DAO. Было предположено, что некоторые ингибиторы оксидазы D-аминокислот (DAO), включая определенные гетероциклы с фрагментом карбоновой кислоты в положении 2, могут быть использованы для улучшения памяти, обучения и познавательной способности у пациентов, страдающих нейродегенеративными нарушениями (US 20030162825). Показано, что индометацин также ингибирует DAO (Chen etal., 1994, Drug Metabol Drug Interact. 11:153-60). DAO расщепляет D-серин и другие D-аминокислоты. Считается, что D-глутамат и D-серин являются агонистами глутаматных рецепторовN-метил-D-аспартата (NMDA), которые регулируют обширный набор активностей мозга, включая синаптическую пластичность, ассоциируемую с определенными видами памяти и обучения(US 20030162825). Таким образом, предполагается, что ингибирование DAO приведет к увеличению уровня D-серина и улучшению функций памяти. Хемерин-R. Хемерин-R представляет собой связанный с G белком рецептор, который структурно и эволюционно связан с CRTH2. В WO 2005/000875 раскрыты способы тестирования способности соединений модулировать активность хемерин-R. Соединения, которые модулируют (например, противодействуют или ингибируют) активность хемерин-R, могут быть использованы при профилактике и/или лечении COPD,псориаза, вирусных или бактериальных инфекций, клеточной миграции, рака, роста опухолей и опухолевого метастаза, воспалительных и неопластических процессов, заживлении ран и срастании переломов, а также при нарушении функций, регулирующих рост, диабете, ожирении, анорексии, булимии, острой сердечной недостаточности, гипотонии, гипертензии, недержании мочи, остеопорозе, стенокардии, инфаркте миокарда, рестенозе, атеросклерозе, заболеваний, сопровождающихся избыточной пролиферацией гладкомышечных клеток, аневризмов, заболеваний, сопровождающихся потерей гладкомышечных клеток или ослабленной пролиферацией гладкомышечных клеток, удара, ишемии, язвы, аллергий, доброкачественной гипертрофии предстательной железы, мигрени, рвоты, психотических и неврологических заболеваний, включая состояние страха, шизофрению, маниакальную депрессию, делирий, слабоумие и тяжелую умственную отсталость, дегенеративных заболеваний, нейродегенеративных заболеваний, таких как болезни Альцгеймера и Паркинсона, и дискинезии, такой как болезни Гентингтона, синдром Жилль де ла Туретта, и других подобных заболеваний. Сущность изобретения В настоящем изобретении описано соединение, имеющее структурную формулу A, или его фармацевтически приемлемая соль:b) один из Р 1, Р 2, P3, Р 4, P5 и P6 представляет собой N, а остальные представляют собой C;-3 018724 А и А', взятые вместе, представляют собой =O; означает двойную или одинарную связь;R2 представляет собой необязательно независимо замещенный C1-C3-алкил или циклопропил, где необязательные заместители выбирают из 1-3 атомов фтора; каждый из R4, R6 и R7 независимо представляет собой H, галоген, гидрокси, необязательно независимо замещенный C1-C5-алкил или необязательно независимо замещенный C1-C5-алкокси; где для каждого указанного C1-C5-алкила или C1-C5-алкокси необязательные заместители независимо выбирают из 1-3 атомов фтора и где вплоть до двух из R4, R6 и R7 являются одновременно замещенными;R5 представляет собой H, галоген, -NO2, -CN, -C(O)OH, гидрокси, необязательно независимо замещенный C1-C5-алкил, необязательно независимо замещенный C2-C5-алкенил, необязательно независимо замещенный C2-C5-алкинил, необязательно независимо замещенный C1-C5-алкокси, -C(O)NRaRb или-NRaRb, где Ra и Rb независимо представляют собой H, необязательно независимо замещенный С 1-С 6-алкил или необязательно независимо замещенный C3-C6-циклоалкил,где для каждого C1-C5-алкила, C2-C5-алкенила или C2-C5-алкинила необязательные заместители независимо выбирают из 1 или 2 оксо, гидрокси, C1-C3-ацилокси, C1-C3-алкокси и NH2 групп или 1-3 атомов галогена; каждый из R8, R9, R11 и R12, когда связан с С, независимо представляет собой Н, галоген или гидрокси;R12, когда связан с С, представляет собой H, галоген, -NO2, гидрокси, необязательно независимо замещенный C1-C5-алкил или необязательно независимо замещенный C1-C5-алкокси, где необязательный заместитель для указанного C1-C5-алкила или C1-C5-алкокси выбирают из 1-3 атомов галогена; каждый из R8, R9, R10, R11 и R12, когда связан с N, отсутствует;R14 выбирают из Н, галогена, -CN, гидрокси, необязательно независимо замещенного C1-C5-алкила или необязательно независимо замещенного C1-C5-алкокси;R16 выбирают из Н, галогена, гидрокси, необязательно независимо замещенного C1-C5-алкила или необязательно независимо замещенного C1-C5-алкокси; где для R14 и R16 необязательные заместители в каждом указанном C1-C5-алкиле или C1-C5-алкокси выбирают из 1-3 атомов фтора;R17 выбирают из H или галогена. В одном варианте осуществления один из Р 1, Р 2, P3, P4, P5 и Р 6 представляет собой N и остальные представляют собой С. В другом варианте осуществления Р 1, Р 2, Р 3, Р 4, P5 и Р 6 представляют собой С. Предпочтительно R2 представляет собой C1-C3-алкил или циклопропил. Наиболее предпочтительно R2 представляет собой метил. В одном из вариантов осуществления один или два из R8, R9, R10, R11 и R12 представляют собой галоген и остальные представляют собой H. В другом из вариантов осуществления один или два из R8, R9, R10, R11 и R12 представляют собой Cl или F и остальные представляют собой H. Предпочтительно R10 представляет собой галоген. Предпочтительно один из R8 и R12 представляет собой галоген и другой представляет собой H. В одном из вариантов осуществления R10 представляет собой Cl или F и R8, R9, R11 и R12 представляют собой H. В другом из вариантов осуществления R10 представляет собой Cl или F; R8 представляет собой Cl или F и R9, R11 и R12 представляют собой H. В одном из вариантов осуществления R4 и R7 представляют собой H. В другом из вариантов осуществления R6 представляет собой H. Предпочтительно R5 выбирают из этокси, метокси, этила, метила, галогена и H. Наиболее предпочтительно R5 выбирают из метокси, метила и H. Еще более предпочтительно R5 представляет собой метокси. В другом варианте осуществления предпочтительно R5 представляет собой метил. В одном из вариантов осуществления R14 представляет собой галоген или необязательно независимо замещенный метокси и R13 и R17 представляют собой H. Предпочтительно R14 представляет собой -OCH3. Наиболее предпочтительными соединениями формулы А являются соединения, выбранные из следующего списка соединений. В различных случаях соединение формулы А имеет одну из следующих формул: Формула А-5 Раскрыта также фармацевтическая композиция, содержащая соединение или фармацевтически приемлемую соль любого из различных вариантов осуществления соединения формулы A и фармацевтически приемлемый носитель. Также описаны способы лечения различных нарушений с использованием композиции, содержащей любой из вариантов осуществления соединения формулы А. Среди нарушений: боль (например,острая боль, хроническая боль, нейрогенная боль, мигрень; боль, вызванная воспалением (например,артрит, остеоартрит, спондилит, ревматоидный артрит, болезнь Крона и синдром раздраженной толстой кишки), и невропатическая боль), тревога, нарушение пищевого поведения (например, анорексия, булимия), ожирение, повышенное внутриглазное давление, глаукома, сердечно-сосудистое нарушение, депрессия, воспалительное нарушение (аллергия, воспаления дыхательных путей, воспаление кожи и воспаление желудочно-кишечного тракта), астма, болезнь Крона и воспалительное заболевание кишечника.-8 018724 К другим нарушениям, которые можно лечить, относятся пищевая аллергия, астма, воспаление кожи,рвота, аллодиния, гипералгезия, головная боль, висцеральная боль, зубная боль, боль, связанная с ожогами, менструальная боль, дисменорея, первичная дисменорея, ревматоидный артрит, ювенильный ревматоидный артрит, остеоартрит, послеоперационная боль (например, связанная с ортопедической операцией, гинекологической операцией, брюшной операцией, разрезами, челюстно-лицевой операцией) и боль в спине. Также описан способ лечения боли (например, острая боль, хроническая боль, нейрогенная боль,мигрень; боль, вызванная воспалением (например, артрит, остеоартрит, спондилит, ревматоидный артрит, болезнь Крона и синдром раздраженной толстой кишки) и невропатическая боль), тревоги, нарушения пищевого поведения (например, анорексия, булимия), ожирения, повышенного внутриглазного давления, глаукомы, сердечно-сосудистого нарушения, депрессии, воспалительного нарушения (аллергия,воспаления дыхательных путей, воспаление кожи и воспаление желудочно-кишечного тракта), астмы,болезни Крона и воспалительного заболевания кишечника, рвоты, аллодинии, гипералгезии, головной боли, висцеральной боли, зубной боли, боли, связанной с ожогами, менструальной боли, дисменореи,первичной дисменореи, ревматоидного артрита, ювенильного ревматоидного артрита, остеоартрита, послеоперационной боли (например, связанной с ортопедической операцией, гинекологической операцией,брюшной операцией, разрезами, челюстно-лицевой операцией) и боли в спине с использованием композиции, содержащей соединение формулы А. Термин "гало" или "галоген" означает фтор, хлор, бром и йод. Термин "алкил" означает углеводородную цепь, прямую или разветвленную, содержащую указанное число атомов углерода. Например, C1-C12-алкил означает, что группа может иметь 1-12 (включительно) атомов углерода (т.е. 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12). Термин "галогеналкил" означает алкил, в котором один или несколько атомов водорода заменены группой галогена, и включает алкильные фрагменты, в которых все атомы водорода заменены группой галогена (например, перфторалкил). Термины "алкиламино" и "диалкиламино" означают радикалы -NH(алкил) и -N(алкил)2 соответственно. Термин "алкокси" означает радикал -O-алкил. Таким образом, например, алкокси или алкоксил могут означать линейные, разветвленные, циклические группы, содержащие 1, 2, 3, 4, 5, 6, 7 или 8 атомов углерода, или их комбинации, присоединенные к исходной структуре через атом кислорода. Неограничивающими примерами являются метокси, этокси, пропокси, изопропокси, циклопропилокси, циклогексилокси и подобные. Низший алкокси означает группу с 1-4 атомами углерода. Термин "меркапто" означает радикал SH. Термин "тиоалкокси" означает радикал -S-алкил. Используемый в данном описании термин "циклоалкил" включает насыщенные моноциклические,бициклические, трициклические или полициклические углеводородные группы, содержащие от 3 до 12 атомов углерода, в которых любой кольцевой атом, способный к замещению, может быть замещен заместителем. Неограничивающими примерами циклоалкильных фрагментов являются циклопентил, норборнил, циклопропил, циклогексил и адамантил. Термин "ацил" означает алкилкарбонильный заместитель, любой из которых может быть дополнительно замещен заместителями. Термин "оксо" означает атом кислорода, который образует карбонил, когда присоединен к атому углерода, N-оксид, когда присоединен к атому азота, и сульфоксид или сульфон, когда присоединен к атому серы. Термин "заместители" означает группу, которая "замещает" алкильную, циклоалкильную, алкенильную, алкинильную, арильную или гетероарильную группу, или другую группу по любому атому указанной группы. Группа может быть моно- или полизамещенной. В случае полизамещенной группы заместители являются независимыми. Подходящие заместители включают, но без ограничения, F, Cl, Br,I, алкил, алкенил, алкинил, алкокси, ацилокси, галоген, гидрокси, циано, нитро, амино, перфторалкил,перфторалкокси, карбоксил, оксо. В одном аспекте заместители в группе независимо представляют собой любой один или любую подгруппу указанных заместителей. В некоторых случаях заместители выбирают из F, Cl, Br и I. В других случаях заместители выбирают из галогена, необязательно замещенного галогеном C1-C3-алкила, необязательно независимо замещенного галогеном C1-C3-алкокси, гидрокси,циано, нитро и амино. В некоторых случаях заместители выбирают из галогена, гидрокси и C1-C3-алкила. В некоторых случаях заместители выбирают из галогена, гидрокси,C1-C3-алкила и C1-C3-алкоксила. Раскрыты соли, в частности физиологически приемлемые соли и сольваты соединений. Сольваты представляют собой формы соединений, в которых соединение образует комплекс с молекулами растворителя путем координации в твердом или жидком состоянии. Гидраты являются особенной формой сольвата, в которой соединение координируют с водой. Фармакологически приемлемые аддитивные соли, как указано выше, предназначены для получения форм терапевтически активных нетоксичных кислотно-аддитивной и основно-аддитивной соли, которые соединения способны образовывать. Фармацевтически приемлемые кислотно-аддитивные соли основных соединений можно получить путем обработки-9 018724 основного соединения соответствующей кислотой. Представителями кислот являются неорганические кислоты, такие как хлористо-водородная, бромисто-водородная, йодисто-водородная, серная, фосфорная кислоты; и органические кислоты, такие как уксусная, пропановая, гидроксиуксусная, молочная, пировиноградная, гликолевая, малеиновая, малоновая, щавелевая, бензолсульфоновая, толуолсульфоновая,метансульфоновая, трифторуксусная, фумаровая, янтарная, яблочная, винная, лимонная, салициловая, паминосалициловая, памовая, бензойная, аскорбиновая кислоты и подобные. Представителями основноаддитивных солей являются натриевая, калиевая и кальциевая соли и соли с фармацевтически приемлемыми аминами, такими как, например, аммиак, алкиламины, бензатин, и аминокислотами, такими как,например, аргинин и лизин. Используемый в данном описании термин "аддитивная соль" также включает сольваты, которые могут образовывать соединения и их соли, такие как, например, гидраты, алкоголяты и подобные. Некоторые соединения могут находиться в стереоизомерных формах, таких как энантиомеры, диастереомеры и их смеси. Смеси можно разделять с получением чистых стереоизомерных компонентов. Некоторые соединения могут существовать в виде таутомеров. Могут быть использованы различные таутомерные смеси. Описаны также фармацевтическая композиция, содержащая соединение настоящего изобретения, и способ получения фармацевтической композиции, включающий смешивание соединения настоящего изобретения с фармацевтически приемлемым носителем. Описаны также способы лечения состояния страха, депрессии, биполярного расстройства, ожирения, боли или нарушения сна у пациента, включающие введение эффективного количества соединения настоящего изобретения. Описаны фармацевтическая композиция, содержащая одно или несколько соединений, например соединение, которое ингибирует FAAH, настоящего изобретения и фармацевтически приемлемый носитель; способ лечения боли (например невропатической боли) и/или воспаления, включающий введение соединения настоящего изобретения или фармацевтической композиции, содержащей соединение настоящего изобретения; способ лечения состояния страха, включающий введение соединения настоящего изобретения или фармацевтической композиции, содержащей соединение настоящего изобретения; способ лечения депрессии, включающий введение соединения настоящего изобретения или фармацевтической композиции, содержащей соединение настоящего изобретения; способ лечения нарушения сна,включающий введение соединения настоящего изобретения или фармацевтической композиции, содержащей соединение настоящего изобретения; способ лечения гипертензии, включающий введение соединения настоящего изобретения или фармацевтической композиции, содержащей соединение настоящего изобретения; способ лечения желудочно-кишечного расстройства (например, диарея и воспалительное заболевание кишечника), включающий введение соединения настоящего изобретения или фармацевтической композиции, содержащей соединение настоящего изобретения; и способ лечения ожирения,включающий введение соединения настоящего изобретения или фармацевтической композиции, содержащей соединение настоящего изобретения. Пригодным для использования согласно изобретению является пролекарство соединения настоящего изобретения, имеющее гидроксильную группу, где гидроксильные группы пролекарственной формы выбирают из (а) сложного эфира, содержащего C1-C6-алкильную группу с разветвленной или прямой цепью, (b) сложного эфира фосфорной кислоты, содержащего C1-C6-алкильную группу с разветвленной или прямой цепью, (с) карбамата, содержащего C1-C6-алкильную группу с разветвленной или прямой цепью, и (d) карбонатной группы, содержащей C1-C6-алкильную группу с разветвленной или прямой цепью. Некоторые описанные в данном описании соединения ингибируют активность человеческой FAAH(иногда называемая FAAH-1) без существенного ингибирования активности человеческой FAAH-2. Таким образом, некоторые соединения демонстрируют значение IC50 в отношении FAAH-2, которое в 10,15, 20, 50, 100, 500 или 1000 раз превышает IC50 в отношении FAAH-1. Ингибирование гена hERG, кодирующего калиевые каналы сердца, может вызвать аритмию сердца. Некоторые соединения настоящего изобретения ингибируют человеческую FAAH, но не ингибируютhERG in vitro (например, при исследовании от 3 до 30 мкм) и/или in vivo. Некоторые соединения настоящего изобретения могут проявлять активность в отношении других ферментов, отличных от FAAH. Например, некоторые ингибиторы FAAH могут ингибировать COX-1,COX-2, DAO, DP-1, TXA2, CB1/CB2, MAGL, cysLT2, хемерин-R и/или CRTH2. В некоторых случаях соединение настоящего изобретения не является ингибитором FAAH, но ингибирует один или несколько из COX-1, COX-2, DAO, DP-1, TXA2, CB1/CB2, MAGL, cysLT2, хемерин-R и CRTH2. В некоторых случаях указанное соединение активирует CRTH2. В некоторых вариантах осуществления соединения, которые ингибируют FAAH, являются селективными ингибиторами FAAH в отношении COX-1, COX-2, DAO, DP-1, TXA2, CB1/CB2, MAGL,cysLT2, хемерин-R и/или CRTH2. Таким образом, в некоторых случаях значение IC50 соединения в отношении COX-1 превышает по меньшей мере в 5, 10, 15, 20, 50, 100, 500 или 1000 раз значение IC50 соединения в отношении FAAH. В некоторых случаях IC50 соединения в отношении COX-2 превышает в 5, 10,- 10018724 15, 20, 50, 100, 500 или 1000 раз значение IC50 соединения в отношении FAAH. В некоторых случаях IC50 соединения в отношении DP-1 превышает по меньшей мере в 5, 10, 15, 20, 50, 100, 500 или 1000 раз IC50 соединения в отношении FAAH. В некоторых случаях IC50 соединения для DAO превышает по меньшей мере в 5, 10, 15, 20, 50, 100, 500 или 1000 раз IC50 соединения в отношении FAAH. Таким образом, в некоторых случаях IC50 соединения в отношении TXA2 превышает по меньшей мере в 5, 10, 15, 20, 50, 100,500 или 1000 раз IC50 соединения в отношении FAAH. В некоторых случаях IC50 соединения в отношении СВ 1/СВ 2 превышает по меньшей мере в 5, 10, 15, 20, 50, 100, 500 или 1000 раз IC50 соединения в отношении FAAH. В некоторых случаях IC50 соединения в отношении MAGL превышает по меньшей мере в 5, 10, 15, 20, 50, 100, 500 или 1000 раз IC50 соединения в отношении FAAH. В некоторых случаяхIC50 соединения в отношении cysLT2 превышает по меньшей мере в 5, 10, 15, 20, 50, 100, 500 или 1000 раз IC50 соединения в отношении FAAH. В некоторых случаях IC50 соединения в отношении хемерин-R превышает по меньшей мере в 5, 10, 15, 20, 50, 100, 500 или 1000 раз IC50 соединения в отношенииFAAH. В некоторых случаях IC50 соединения в отношении CRTH2 превышает по меньшей мере в 5, 10,15, 20, 50, 100, 500 или 1000 раз IC50 соединения в отношении FAAH. Некоторые соединения, которые ингибируют FAAH, являются селективными и ингибируют в незначительной степени один или более из тубулина, PDE4 и PLA2. Селективные соединения демонстрируют значение IC50 в отношении одного или более из тубулина, PDE4 и PLA2, которое превышает по меньшей мере в 500, 1000 или 10000 раз значение IC50 соединения в отношении FAAH. В некоторых вариантах осуществления композицию вводят пациенту, которого не подвергают лечению с помощью неселективного нестероидного противовоспалительного препарата, например пациенту, которого не подвергают лечению с помощью индометацина. В некоторых вариантах осуществления соединения вводят в комбинации со вторым соединением,пригодным для уменьшения воспаления или боли. Субъектом может быть млекопитающее, предпочтительно человек. Работник здравоохранения может определить субъекта, нуждающегося в таком лечении, и это решение может быть субъективным (например, мнение) или объективным (например, по результатам исследования или диагностического метода). Термин "лечение" или "подвергать лечению" означает введение соединения настоящего изобретения субъекту с целью терапии, излечивания, ослабления, уменьшения, изменения, устранения, ослабления, улучшения или влияния на заболевание, симптомы заболевания или предрасположенности к заболеванию."Эффективное количество" означает количество соединения, которое обеспечивает терапевтический эффект у субъекта, которого подвергают лечению. Терапевтический эффект может оцениваться объективно (т.е. измеряться в ходе некоторого исследования или критерием) или субъективно (т.е. субъект указывает симптомы или чувствует эффект). Эффективное количество соединения настоящего изобретения может составлять приблизительно от 0,05 до приблизительно 500 мг/кг, альтернативно, приблизительно от 1 до приблизительно 50 мг/кг. Эффективные дозы также будут зависеть от способа введения, а также возможности совместного введения с другими агентами. Термин "млекопитающее" включает, например, мышей, хомяков, крыс, коров, овец, свиней, коз,лошадей, обезьян, собак (например, Canis familiaris), кошек, кроликов, морских свинок и приматов,включая человека. Термин "пролекарство" означает соединения, которые являются предшественниками лекарственного средства, которые после введения пациенту и последующей абсорбции высвобождают лекарственное средство in vivo посредством метаболического процесса. Примерами пролекарств являются ациламиды аминосоединений настоящего изобретения, таких как амиды алифатических (C1-C6)карбоновых кислот,амиды ариловых кислот (например, бензойная кислота) и алкан (C1-C6)дикислот. Описаны также пролекарства, которые преобразуются in vivo таким образом, что R5 становится гидроксильной группой. Таким образом, в пролекарственной форме соединений формулы I или формулыII R5 представляет собой группу, которая преобразуется в гидроксильную группу. Например, в пролекарственной форме соединений формулы I или формулы II R5 может являться карбонатом, сложным эфиром, сложным эфиром фосфорной кислоты или подобной группой. Ниже подробно изложены один или несколько вариантов осуществления данного изобретения. Другие признаки, характеристики и преимущества настоящего изобретения станут более понятными из следующего описания, чертежей и формулы изобретения. Все патенты, патентные заявки и публикации,приведенные в настоящем описании, полностью включены в него во всей их полноте путем ссылки.(анализ очищенного фермента) для ряда соединений. Все числовые значения выражены в микронах(мкм). В табл. 2 А приведены данные по активности CRTH2 для ряда соединений, являющихся агонистамиCRTH2. Соединения исследовали на предмет агонистической активности в отношении CRTH2 при 10 и 1 мкМ. В табл. 2 В приведены данные по активности CRTH2 для ряда соединений, некоторые из которых являются антагонистами CRTH2. Соединения исследовали на предмет антагонистической активности в отношении CRTH2 при 10 мкМ. В табл. 3A-3D приведены данные по активности COX, CRTH2, FAAH, DAO и DP-1 для ряда соединений. В табл. 4 приведены данные по активности DAO для ряда соединений. В табл. 5 приведены данные по активности DAO, FAAH и COX для ряда соединений. В табл. 6 приведены данные по активности COX для ряда соединений. В табл. 7 приведены данные по активности CRTH2 для ряда соединений. В табл. 8 А и 8 В приведены данные по активности DAO и DP-1 для ряда соединений. В табл. 9 А-9D приведены данные по активности FAAH для ряда соединений. Значения в данных таблицах основаны на результатах от 1 до 6 или более экспериментов. В табл. 10 приведены данные по активности TXA2 для ряда соединений. Подробное описание Некоторые соединения настоящего изобретения могут обладать активностью в отношении ферментов/белков, отличных от FAAH. Например, некоторые ингибиторы FAAH могут ингибировать COX-1,COX-2, DAO, DP-1, TXA2, CB1/CB2, MAGL, cysLT2, хемерин-R и/или CRTH2. В некоторых случаях соединение настоящего изобретения не является ингибитором FAAH, но ингибирует один или более изCOX-1, COX-2, DAO, DP-1, TXA2, CB1/CB2, MAGL, cysLT2, хемерин-R и/или CRTH2. Ожидается, что некоторые соединения будут иметь увеличенный период полужизни in vivo в организме человека по сравнению с некоторыми структурно родственными соединениями. Ожидается, что некоторые соединения будут обладать пониженной почечной и/или желудочной токсичностью по сравнению с некоторыми структурно родственными соединениями. Примеры Ниже описаны некоторые пригодные соединения. 2-[1-(4-Хлорбензил)-5-метокси-2-метил-1H-индол-3-ил]-2-оксо-N-пиридин-2-илацетамид. 1- 12018724 Другими пригодными соединениями являются следующие.FAAH. Пригодные соединения (например, ингибиторы FAAH) включают приведенные ниже соединения: Дополнительные пригодные соединения описаны ниже в разделе под заголовком "Другие пригодные соединения (например, ингибиторы FAAH)" и их производные, имеющие формулу A, где группа в положении 5 индола замещена H, галогеном, -OCH3, OCH2CH3, -CH3, -CH2CH3 и -OH (где любой атом углерода может быть необязательно один или несколько раз замещен галогеном), и бензильная группа является паразамещенной, например, Br, метокси или -OH или является 2-, 4-замещенной, например, Cl. Другие пригодные соединения (например, ингибиторы FAAH). 2-[1-(4-хлорбензил)-5-метокси-2-метил-1H-индол-3-ил]-2-оксо-N-пиридин-4-илацетамид; 2-[1-(4-хлорбензил)-5-метокси-1H-индол-3-ил]-2-оксо-N-пиридин-4-илацетамид; 2-[1-(4-хлорбензил)-5-метокси-2-метил-1H-индол-3-ил]-2-оксо-N-пиримидин-4-илацетамид; 2-[1-(4-хлорбензил)-5-метокси-1H-индол-3-ил]-2-оксо-N-пиридин-4-илацетамид. Способы синтеза. Общие способы синтеза для получения соединений согласно настоящему изобретению. Раздел 1. Общие способы синтеза с целью получения соединений, описанных выше. Схема 1Demuynck, M.; DeClercq, P.; Vanderwalle, M. J. Org. Chem. 1979, 44. 4863-4866. Grieco, P.A.; Nishizawa, M.; Oguri, Т.; Burke, S.D.; Marinovic, N. J. Am. Chem. Soc. 1977, 99, 5773-5780. Раздел 2. Получение 1-[(5-хлортиен-2-ил)карбонил]-6-фтор-5-гидрокси-2-метил-1H-индол-3 илуксусной кислоты. Указанное соединение может быть получено следующим образом. Стадия 1. Получение (3-фтор-4-метоксифенил)гидразина (2, R1 означает H, R2 означает CH3, R3 означает F). 3-Фтор-4-метоксианилин (1, R1 означает H, R2 означает CH3, R3 означает F) (95 г, 0,67 моль) добавляли в концентрированную хлористо-водородную кислоту (250 мл), суспензию перемешивали при температуре окружающей среды в течение 18 ч, затем охлаждали до 0C и раствор нитрита натрия (53,7 г,0,78 моль) в воде (200 мл) добавляли по каплям при 0-5C. После завершения добавления полученный раствор перемешивали при 0C в течение 1 ч и затем его добавляли по каплям при 0-5C в перемешиваемый раствор дигидрата хлорида олова (II) (638,9 г, 2,83 моль) в концентрированной хлористоводородной кислоте (500 мл). Смеси давали нагреться до температуры окружающей среды и затем выдерживали при 4C в течение 18 ч. Полученный осадок отделяли фильтрованием, промывали водой(400 мл) и эфиром (1000 мл) и сушили в вакууме. Твердую гидрохлоридную соль подщелачивали добавлением 10% водного раствора гидроксида натрия (800 мл), свободное основание экстрагировали простым эфиром (2400 мл) и объединенные экстракты сушили (MgSO4), растворитель удаляли в вакууме с получением (3-фтор-4-метоксифенил)гидразина (2, R1 означает H, R2 означает СН 3, R3 означает F) (51,9 г,50%) в виде желтого твердого вещества, т.п. 46-50C. 1H, R2 означает СН 3, R3 означает F, R4 означает В и H) и (4-фтор-5-метокси-2-метил-1H-индол-3 ил)уксусной кислоты (4, R1 означает F, R2 означает СН 3, R3 означает H, R4 означает B и H). Левулиновую кислоту (3, R4 означает B и H) (38 мл, 354 ммоль) и гидрохлорид 3-фтор-6 метоксифенилгидразина (2, R1 означает H, R2 означает СН 3, R3 означает F) (67,5 г, 350 ммоль) объединяли и добавляли 150 мл ледяной уксусной кислоты, суспензию перемешивали при 80C в течение 4 ч. Реакционную смесь охлаждали до комнатной температуры и добавляли в ледяную воду (500 мл). Полученный водный раствор экстрагировали дихлорметаном (3500 мл), органические экстракты сушили(MgSO4) и концентрировали с получением плотного полутвердого вещества. Добавляли воду(450-500 мл) и суспензию активно перемешивали в течение ночи, вручную разбивая крупные твердые части шпателем. Полученное мелкодисперсное желто-коричневое твердое вещество отделяли фильтрованием и сушили с получением смеси индолов 56,3 г, 67% выход, приблизительно 93% чистоты согласно ВЭЖХ (отношение 7/1 (6-фтор-5-метокси-2-метил-1H-индол-3-ил)уксусной кислоты (4, R1 означает H,R2 означает СН 3, R3 означает F, R4 означает В и H) и (4-фтор-5-метокси-2-метил-1H-индол-3-ил)уксусной кислоты (4, R1 означает F, R2 означает СН 3, R3 означает H, R4 означает В и H) согласно ЯМР).- 26018724 Основной изомер 1 Н ЯМР (CDCl3/300 МГц) 2,27 (с, 3H), 3,82 (с, 2H), 3,84 (с, 3H), 6,92-6,97 (м, 2H,ArH). Стадия 2 В. Получение 2-триметилсилилэтил(6-фтор-5-метокси-2-метил-1H-индол-3-ил)ацетата (4,R1 означает B и H, R2 означает СН 3, R3 означает F, R4 означает CH2CH2Si(СН 3)3). Индолы со стадии 2 А (56,3 г, 238 ммоль) объединяли с 2-триметилсилилэтанолом (41 мл, 1,25 экв.) и 4-(диметиламино)пиридином (DMAP) (4 г) в дихлорметане (600 мл) и охлаждали до 0C. Гидрохлорид 1-[3-(диметиламино)пропил)]-3-этилкарбодиимида (EDCI) (50,2 г, 1,1 экв.) добавляли частями и реакционную смесь перемешивали в течение 30 мин при 0C, затем давали нагреться до комнатной температуры и перемешивали в течение ночи. Реакционную смесь разбавляли дихлорметаном (600 мл) и промывали водой (2200 мл), сушили и концентрировали с получением густого оранжевого сиропа, который после растирания в гексанах вызывал образование твердого вещества, твердое вещество перекристаллизовывали из смеси гексан-этилацетат с получением желто-коричневых игл 2-триметилсилилэтил(6-фтор-5 метокси-2-метил-1H-индол-3-ил)ацетата (4, R1 означает Н и B, R2 означает СН 3, R3 означает F, R4 означает CH2CH2Si(СН 3)3), 52 г, 65% выход: более 98% чистота; 1H ЯМР (CDCl3/300 МГц) 0,16 (с, 9H), 0,98 (м, 2H), 2,37 (с, 3H), 3,61 (с, 2H), 3,93 (с, 3H), 4,12 (м,2H), 7,00-7,05 (м, 2H, ArH). Другой региоизомер - 2-триметилсилилэтил(4-фтор-5-метокси-2-метил-1H-индол-3-ил)ацетат (4, R1 означает F, R3 означает B и H, R2 означает СН 3, R4 означает CH2CH2Si(CH3)3) - может быть выделен путем концентрирования фильтрата и очистки хроматографией на силикагеле. Стадия 3. Получение 2-триметилсилилэтил 1-[(5-хлортиен-2-ил)карбонил]-6-фтор-5-метокси-2 метил-1H-индол-3-илацетата (5, R1 означает Н и B, R2 означает СН 3, R3 означает F, R4 означаетCH2CH2Si(CH3)3, А означает 5-хлортиофен). В сухой колбе 2-триметилсилилэтил(6-фтор-5-метокси-2-метил-1H-индол-3-ил)ацетат (4, R1 означает Н и B, R2 означает СН 3, R3 означает F, R4 означает CH2CH2Si(CH3)3) (1,0 г, 2,96 ммоль) растворяли в тетрагидрофуране (ТГФ) (10 мл) и гексаметилфосфорамиде (НМРА) (1 мл) и охлаждали до -78C. Добавляли бис-(триметилсилил)амид 0,5 М в толуоле (6,52 мл) и реакционную смесь перемешивали в течение 30 мин. 5-Хлортиофен-2-карбонилхлорид (562 мг, 3,1 ммоль) в 3 мл ТГФ добавляли и реакционную смесь перемешивали в течение 0,5 ч при -78C и 0,5 ч при 0C, затем обрабатывали насыщенным хлористым аммонием (20 мл) и реакционную смесь экстрагировали этилацетатом (330 мл), сушили над(CDCl3/300 МГц) согласно определенной структуре. Стадия 4. Получение 1-[(5-хлортиен-2-ил)карбонил]-6-фтор-5-метокси-2-метил-1H-индол-3 илуксусной кислоты (6, R1 означает H, R2 означает СН 3, R3 означает F, R4 означает H, А означает 5-хлортиофен). Раствор продукта со стадии 3, 2-триметилсилилэтил 1-[(5-хлортиен-2-ил)карбонил]-6-фтор-5 метокси-2-метил-1H-индол-3-илацетат 5 (R1 означает Н и B, R2 означает СН 3, R3 означает F, R4 означаетCH2CH2Si(CH3)3, А означает 5-хлортиофен), (600 мг, 1,24 ммоль) растворяли в 8 мл ТГФ, обрабатывали раствором тетрабутиламмонийфторида (1 М, 3,1 мл, 3,1 ммоль) в ТГФ. Раствор перемешивали при комнатной температуре до разложения сложного эфира (около 1 ч) и затем раствор разбавляли насыщенным водным аммонийхлоридом и экстрагировали этилацетатом. Объединенные экстракты промывали насыщенным раствором соли, сушили над MgSO4 и концентрировали с получением твердого вещества, которое очищали хроматографией при элюировании гексанами и этилацетатом, получая 280 мг, 59% чистой 1-[(5-хлортиен-2-ил)карбонил]-6-фтор-5-метокси-2-метил-1H-индол-3-илуксусной кислоты (6, R1 означает H, R2 означает СН 3, R3 означает F, R4 означает H, А означает 5-хлортиофен), т.п. 169C. 1(д, 1H, J=4,0 Гц), 3,93 (с, 3H), 3,70 (с, 2H), 2,42 (с, 3H). Стадия 5. Получение 1-[(5-хлортиен-2-ил)карбонил]-6-фтор-5-гидрокси-2-метил-1H-индол-3 илуксусной кислоты (6, R1 означает Н и B, R2 означает H, R3 означает F, А означает 5-хлортиофен). Продукт со стадии 3, 2-триметилсилилэтил 1-[(5-хлортиен-2-ил)карбонил]-6-фтор-5-метокси-2 метил-1H-индол-3-илацетат (5, R1 означает Н и B, R2 означает СН 3, R3 означает F, R4 означаетCH2CH2Si(CH3)3, А означает 5-хлортиофен), (400 мг, 0,83 ммоль) растворяли в 10 мл сухого дихлорметана и охлаждали до -78C. Затем раствор обрабатывали трибромидом бора (1 М, 4,9 мл, 4,9 ммоль) в дихлорметане, раствору давали нагреться до комнатной температуры и перемешивали при этой температуре еще 2 ч. Затем раствор выливали в воду, фазы разделяли и водную фазу экстрагировали дихлорметаном. Объединенные экстракты промывали насыщенным раствором соли, сушили над MgSO4 и концентрировали с получением твердого вещества, которое очищали хроматографией при элюировании метанолом и дихлорметаном, получая 150 мг, 49% чистоты 1-[(5-хлортиен-2-ил)карбонил]-6-фтор-5 гидрокси-2-метил-1H-индол-3-илуксусной кислоты (6, R1 означает Н и B, R2 означает H, R3 означает F,- 27018724 А означает 5-хлортиофен), т.п. 174C. 1H ЯМР (CDCl3/300 МГц) 7,34 (д, 1H, J=3,9 Гц), 7,13 (д, 1H, J=11,l Гц), 7,07 (д, 1H, J=8,4 Гц), 6,98 (д,1H, J=3,9 Гц), 3,66 (с, 2H), 2,39 (с, 3H). Раздел 3. Общая схема синтеза 1. Некоторые соединения по изобретению могут быть получены общим способом, описанным ниже.(3-фтор-4 Получение производных фенилгидразина (2) начинают с обработки коммерчески доступных анилинов (1) азотистой кислотой, полученной из нитрита натрия, и хлористо-водородной кислотой с получением соответствующей диазониевой соли. В том же реакционном сосуде диазониевую соль обрабатывают сульфитом натрия и хлористо-водородной кислотой с получением требуемого гидрохлорида гидразина (2) с 90% выходом. Альтернативно, диазониевую соль можно восстановить дихлоридом олова в хлористо-водородной кислоте. Стадия 2. Получение индолов путем синтеза индолов Фишера, репрезентативный пример: (6-фтор 5-метокси-2-метил-1H-индол-3-ил)уксусная кислота (5). Конденсация гидрохлорида гидразина (2) левулиновой кислотой (3) в уксусной кислоте приводит к образованию двух региоизомерных индольных производных 4 и 5 в соотношении 1:7. Основной региоизомер 5 может быть выделен в чистом виде путем кристаллизации реакционной смеси. Альтернативно, индольную смесь можно этерифицировать спиртом, таким как 2-триметилсилилэтанол, с получением соответствующих сложных эфиров, которые затем могут быть выделены различными способами,например хроматографией. Обработка сложного эфира индола 5b гидридом натрия в диметилформамиде (ДМФА) с последующей обработкой хлорангидридом кислоты, таким как 5-хлортиофен-2-карбонилхлорид, дает ацилированную производную индола 6b с 82% выходом. Затем сложный эфир может быть удален обработкой кислотой, такой как трифторуксусная кислота, с получением соответствующей кислоты, в данном случае кислоты 6 а. Стадия 4. Получение 5-гидроксипроизводных индола: получение 1-[(5-хлортиен-2-ил)карбонил]-6 фтор-5-метокси-2-метил-1H-индол-3-илуксусной кислоты (7). Сложные эфиры, такие как 6b, после обработки избытком трибромида бора в дихлорметане могут быть преобразованы в соответствующие кислые фенолы, такие как 7, с хорошим выходом. В таких условиях реакции сложноэфирные и 5-метоксигруппы деалкилируются до кислоты и фенола соответственно. При необходимости карбоновые кислоты могут быть преобразованы в их солевые производные обработкой основанием, таким как гидроксид натрия. Общая схема синтеза 2. Некоторые соединения могут быть получены согласно общей схеме синтеза 2 следующим образом. На первой стадии гидразин (2) конденсируют со сложным эфиром левулиновой кислоты в уксусной кислоте с получением смеси региоизомерных сложных эфиров индола 4 и 5 (например, при использовании этиллевулината (3, R означает Et, продукты (4 и 5) которого будут сложными этиловыми эфирами, R означает Et). Сложные эфиры могут быть выделены и затем ацилированы согласно схеме 1 с получением соответствующих ацильных производных, таких как соединение 6, где R означает Et в данном примере. Гидролиз сложного эфира дает соответствующую кислоту 6 а. При желании, сложноэфирные и 5-метоксигруппы могут быть удалены в ходе единственной операции обработки трибромидом бора в дихлорметане с получением фенолов, таких как 7. Общая схема синтеза 3. Некоторые соединения могут быть получены согласно приведенной ниже общей схеме синтеза.
МПК / Метки
МПК: C07D 401/12
Метки: соединения, индола
Код ссылки
<a href="https://eas.patents.su/30-18724-soedineniya-indola.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения индола</a>
Предыдущий патент: Полипептиды, вариабельные домены антител и антагонисты
Следующий патент: Курительное изделие с регулируемым выделением аромата
Случайный патент: Фармацевтические композиции для предотвращения передозировки или неправильного употребления лекарственных средств