Применение бензоконденсированных гетероциклических сульфамидных производных для лечения и профилактики эпилептогенеза
Формула / Реферат
1. Способ лечения, профилактики, замедления, прекращения или инвертирования эпилептогенеза, включающий введение пациенту терапевтически эффективного количества соединения формулы (I)
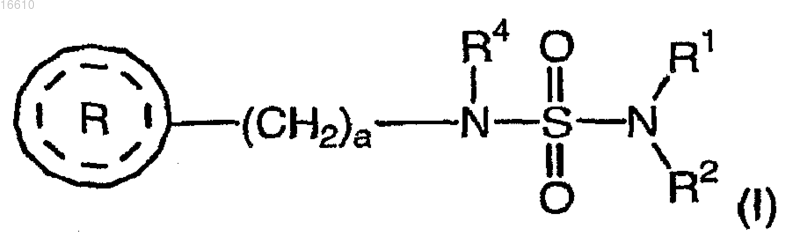
где R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и С1-4алкил;
R4 выбран из группы, включающей атом водорода и С1-4алкил;
а равно целому числу 1 или 2;
 представляет собой группу
представляет собой группу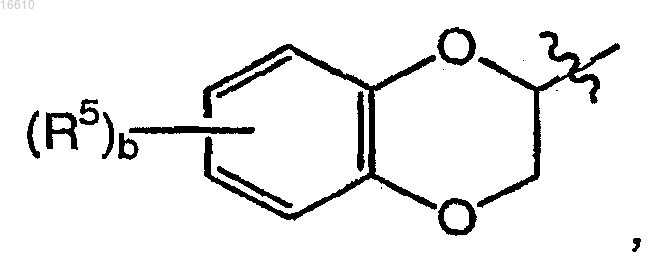
где b равно целому числу от 0 до 4;
каждый R5 независимо выбран из группы, включающей галоген и С1-4алкил;
или его фармацевтически приемлемой соли,
где пациент представляет собой пациента, который находится в группе риска развития эпилепсии или аналогичного связанного с припадками расстройства вследствие повреждения головного мозга или другого поражения центральной нервной системы.
2. Способ по п.1, где в соединении формулы (I)
R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и С1-4алкил;
R4 выбран из группы, включающей атом водорода и С1-4алкил;
а равно целому числу 1 или 2;
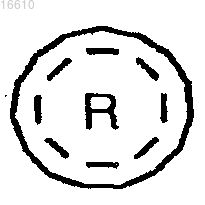 представляет собой группу
представляет собой группу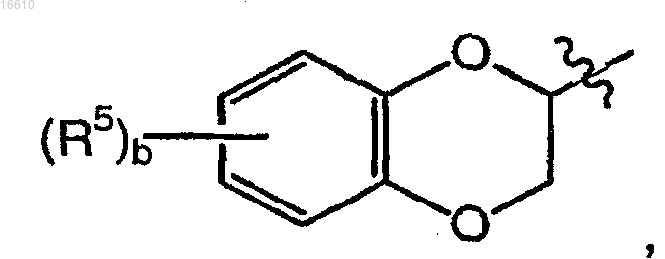
где b равно целому числу 1 или 2;
каждый R5 независимо выбран из группы, включающей галоген и С1-4алкил;
или это соединение формулы (I) вводят в виде фармацевтически приемлемой соли.
3. Способ по п.2, где в соединении формулы (I)
R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и С1-4алкил;
R4 выбран из группы, включающей атом водорода и метил;
а равно целому числу 1 или 2;
 выбран из группы, включающей
выбран из группы, включающей
2-(2,3-дигидробензо[1,4]диоксинил),
2-(6-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(6-фтор-2,3-дигидробензо[1,4]диоксинил),
2-(5-фтор-2,3-дигидробензо[1,4]диоксинил),
2-(7-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(6-хлорбензо[1,3]диоксолил),
2-(7-метил-2,3-дигидробензо[1,4]диоксинил),
2-(5-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(6-бром-2,3-дигидробензо[1,4]диоксинил),
2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил) и
2-(8-хлор-2,3-дигидробензо[1,4]диоксинил);
или это соединение формулы (I) вводят в виде фармацевтически приемлемой соли.
4. Способ по п.3, где в соединении формулы (I)
R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и метил;
R4 выбран из группы, включающей атом водорода и метил;
а равно целому числу 1 или 2;
 выбран из группы, включающей
выбран из группы, включающей
2-(2,3-дигидробензо[1,4]диоксинил),
2-(6-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(7-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(7-метил-2,3-дигидробензо[1,4]диоксинил),
2-(6-бром-2,3-дигидробензо[1,4]диоксинил) и
2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил);
или вводят фармацевтически приемлемую соль соединения.
5. Способ по п.1, где соединение формулы (I) представляет собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид и его фармацевтически приемлемую соль.
6. Способ по п.1, где повреждение головного мозга или другое поражение центральной нервной системы выбрано из группы, включающей повреждение или травму ЦНС любого типа; нейрохирургические операции; травму спинного мозга; инфекции ЦНС; аноксию; удар (CVA); историю болезни преходящих ишемических атак (TIA); стеноз сонной артерии; историю болезни атеросклеротического сосудистого заболевания; историю болезни легочной эмболии; периферическое сосудистое заболевание; аутоиммунные заболевания, затрагивающие ЦНС; перинатальную асфиксию; остановку сердечной деятельности; терапевтические или диагностические сосудистые хирургические операции; гипотензию; повреждение ЦНС от эмболии, гипер- или гипоперфузию; гипоксию; занимающие пространство поражения ЦНС; опухоли головного мозга; кровотечение или кровоизлияние в ЦНС или окружающие ткани; отек головного мозга; фебрильные судороги; гипертермию; воздействие токсических или ядовитых агентов; наркотическую интоксикацию и отмену наркотика.
7. Способ по п.6, где повреждение головного мозга или другое поражение центральной нервной системы выбрано из группы, включающей закрытую или проникающую травму головы; нейрохирургические операции, стеноз сонной артерии, удар или другой церебрально-сосудистый случай (CVA).
8. Способ по п.6, где повреждение головного мозга или другое поражение центральной нервной системы выбрано из закрытой травмы головы, или проникающей травмы головы, или нейрохирургической операции.
9. Способ по п.1, где повреждение головного мозга или другое поражение центральной нервной системы выбрано из удара, наличия стеноза сонной артерии или преходящей ишемической атаки.
10. Способ профилактики, замедления, прекращения или инвертирования эпилептогенеза, включающий введение пациенту терапевтически эффективного количества соединения, выбранного из группы, включающей (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид и его фармацевтически приемлемые соли; где пациент представляет собой пациента, который находится в группе риска развития эпилепсии или аналогичного связанного с припадками расстройства вследствие повреждения головного мозга или другого поражения центральной нервной системы.
11. Способ по п.10, где повреждение головного мозга или другое поражение центральной нервной системы выбрано из группы, включающей повреждение или травму ЦНС любого типа; нейрохирургические операции; травму спинного мозга; инфекции ЦНС; аноксию; удар (CVA); историю болезни преходящих ишемических атак (TIA); стеноз сонной артерии; историю болезни атеросклеротического сосудистого заболевания; историю болезни легочной эмболии; периферическое сосудистое заболевание; аутоиммунные заболевания, затрагивающие ЦНС; перинатальную асфиксию; остановку сердечной деятельности; терапевтические или диагностические сосудистые хирургические операции; гипотензию; повреждение ЦНС от эмболии, гипер- или гипоперфузию; гипоксию; занимающие пространство поражения ЦНС; опухоли головного мозга; кровотечение или кровоизлияние в ЦНС или окружающие ткани; отек головного мозга; фебрильные судороги; гипертермию; воздействие токсических или ядовитых агентов; наркотическую интоксикацию и отмену наркотика.
12. Способ по п.10, где повреждение головного мозга или другое поражение центральной нервной системы выбрано из группы, включающей закрытую или проникающую травму головы; нейрохирургические операции, стеноз сонной артерии, удар или другой церебрально-сосудистый случай (CVA).
13. Способ по п.11, где повреждение головного мозга или другое поражение центральной нервной системы выбрано из закрытой травмы головы, или проникающей травмы головы, или нейрохирургической операции.
14. Способ по п.11, где повреждение головного мозга или другое поражение центральной нервной системы выбрано из удара, наличия стеноза сонной артерии или преходящей ишемической атаки.
15. Способ профилактики, замедления, прекращения или инвертирования эпилептогенеза, включающий введение пациенту, профилактически или терапевтически эффективного количества соединения, выбранного из группы, включающей (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид и его фармацевтически приемлемые соли; где пациент находится в группе риска развития эпилепсии или аналогичного связанного с припадками расстройства вследствие повреждения головного мозга или другого поражения центральной нервной системы и где пациент не демонстрирует симптомы эпилепсии или аналогичных заболеваний, связанных с припадками до момента введения.
16. Способ по п.15, где повреждение головного мозга или другое поражение центральной нервной системы выбрано из группы, включающей закрытую или проникающую травму головы; нейрохирургические операции, стеноз сонной артерии, удар или другой церебрально-сосудистый случай (CVA).
17. Способ по п.16, где повреждение головного мозга или другое поражение центральной нервной системы выбрано из закрытой травмы головы или проникающей травмы головы.
18. Способ по п.17, где пациент, находящийся в группе риска развития эпилепсии или аналогичного связанного с припадками расстройства, имеет первую стадию развития эпилептогенеза вследствие повреждения, поражающего головной мозг.
19. Способ по п.18, где повреждение, поражающее головной мозг, является следствием травматического повреждения головного мозга, нейрохирургической операции, ЦНС-инфекции, удара, опухоли головного мозга, нейрохирургии, асфиксии плода и всасывания соединения, обладающего эпилептогенным действием.
Текст
ПРИМЕНЕНИЕ БЕНЗОКОНДЕНСИРОВАННЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СУЛЬФАМИДНЫХ ПРОИЗВОДНЫХ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЭПИЛЕПТОГЕНЕЗА Изобретение касается способа лечения, профилактики, замедления, прекращения или инвертирования эпилептогенеза, включающего введение пациенту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, где пациент находится в группе риска развития эпилепсии или аналогичного связанного с припадками расстройства вследствие повреждения головного мозга или другого поражения центральной нервной системы. 016610 Область изобретения Настоящее изобретение касается применения бензоконденсированных гетероциклических сульфамидных производных для лечения, предупреждения, инвертирования, задержки или ингибирования возникновения, развития и созревания припадков или заболеваний, связанных с припадками. Более конкретно, настоящее изобретение касается способов применения бензоконденсированных гетероциклических сульфамидных производных для терапевтического или профилактического лечения, предупреждения, инвертирования, задержки или ингибирования эпилептогенеза и эпилепсии. Предпосылки изобретения Повреждения или травмы различных типов центральной нервной системы (ЦНС) или периферической нервной систем (ПНС) могут вызывать сильные и длительные неврологические и психиатрические симптомы и расстройства. Одним общим механизмом возникновения этих эффектов является индуцирование припадочной активности или похожего на припадок явления в ЦНС или в нервах и нервных узлах ПНС. Полагают, что симптоматика пароксизмальных нарушений в электрической активности ЦНС или ПНС, припадки или похожие на припадки неврологические механизмы подвержены воздействию многих патологических явлений при широком многообразии неврологических и психиатрических расстройств. Одним серьезным неврологическим состоянием, характеризующимся припадками, является эпилепсия. Эпилепсия представляет собой общее разрушительное расстройство, затрагивающее более двух с половиной миллионов людей только в Соединенных Штатах. Эпилепсия описывает состояние, при котором человек испытывает повторяющиеся приступы вследствие хронического процесса, лежащего в основе. Эпилепсия относится скорее к клиническому явлению, чем к отдельной категории заболевания, так как существуют многие формы и причины эпилепсии. Используя определение эпилепсии как наличие двух или более неспровоцированных припадков, оценивают степень эпилепсии примерно от 0,3 до 0,5% в различных популяциях населения во всем мире с преобладанием оценки эпилепсии от 5 до 10 человек на 1000. На основании клинического и энцефалографического феномена различают четыре подраздела эпилепсии: тяжелый припадок эпилепсии (подгруппы: генерализованный, фокальный, джексоновский), легкий припадок эпилепсии, психомоторная или височная эпилепсия (подгруппы: психомоторная специфическая или тоническая с адверсивными или вращательными движениями или жевательными явлениями,автоматическая с амнезией или сенсорная с галлюцинациями или сонным состоянием) и автономная или диэнцефальная эпилепсия (с гиперемией, бледностью, тахикардией, гипертензией, потоотделением или другими висцеральными симптомами). При том что эпилепсия является одним из главных примеров расстройства, связанного с припадками, можно иметь широкое многообразие неврологических и психиатрических симптомов и расстройств по их этиологии, припадков или родственных неврологических явлений, подобных припадкам. Проще говоря, припадок или родственное подобное припадку неврологическое явление представляет собой отдельное дискретное клиническое событие, вызванное чрезмерным электрическим разрядом из совокупности нейронов или группы восприимчивых к припадкам нейронов способом, называемым "иктогенез". По существу, иктогенные припадки могут быть единственным симптомом болезни. Однако эпилепсия и другие аналогичные заболевания, связанные с припадками, являются динамическими и часто прогрессирующими заболеваниями с развитием процесса, характеризующимся сложной и плохо понятной последовательностью патологических трансформаций. Развитие и созревание таких изменений представляет собой процесс "эпилептогенеза", причем большая совокупность нейронов, которой является нормальный головной мозг, изменяется и впоследствии становится восприимчивой к аномальным, самопроизвольным, внезапным, повторяющимся, чрезмерным электрическим разрядам, то есть, припадкам. В результате развития эпилептогенного процесса происходит развитие "эпилептогенного очага", причем совокупности аномально разряжающихся нейронов или нейронов, восприимчивых к припадкам, образуют локализованные группы или "эпилептогенные зоны", разбросанные по корковой ткани. Эпилептогенные зоны биохимически взаимосвязаны, таким образом, что аномальный иктогенный разряд способен образовать каскад от зоны к зоне. С развитием эпилептогенеза вовлеченные области нервной системы становятся более восприимчивы к припадку, и припадок легче инициируется, результатом этого являются прогрессивно истощающие симптомы припадка или связанного с припадками расстройства. Тогда как иктогенез и эпилептогенез могут иметь общее происхождение при определенном биохимическом явлении и общие нейронные пути при различных заболеваниях, два процесса не являются идентичными. Иктогенез представляет собой стимуляцию и развитие припадков за дискретное время и в дискретном пространстве, быстрое и определенное электрическое/химическое событие, которое происходит за период времени от секунд до минут. По сравнению с этим эпилептогенез представляет собой постепенный биохимический или нейронный процесс реструктуризации, при котором нормальный головной мозг трансформируется посредством иктогенных событий в головной мозг с эпилептогенным очагом, имеющий нейронную схему, которая становится чувствительной и зависимой от иктогенных событий, делая человека все больше и больше-1 016610 восприимчивым к повторению самопроизвольных, эпизодических, ограниченных во времени припадков,результатом этого являются прогрессивно истощающие симптомы припадка или связанного с припадками расстройства и прогрессирующее отсутствие реакции на лечение. Развитие "эпилептогенного очага" является медленным биохимическим и/или структурным процессом, который обычно происходит за период от месяцев до лет. Эпилептогенез является двухфазным процессом: "фаза 1 эпилептогенеза" представляет собой стимуляцию эпилептогенного процесса до первого эпилептического припадка или симптома связанного с припадками аналогичного расстройства и часто является результатом некоторого типа поражения или травмы головного мозга, а именно, удара, заболевания (например, инфекции, такой как менингит), или травмы, такой как случайный удар по голове или хирургическая операция, проведенная на головном мозге. "Фаза 2 эпилептогенеза" относится к процессу, во время которого ткань головного мозга, которая уже восприимчива к эпилептическим припадкам или связанным с припадками явлениям, аналогичным связанным с припадками расстройствам, становится еще более восприимчивой к припадкам, происходящим с увеличивающейся частотой и/или тяжестью, и/или слабее откликается на лечение. Наряду с тем, что процессы, вовлеченные в эпилептогенез, определенно не идентифицированы, некоторые исследователи полагают, что в него вовлечена позитивная регуляция возбуждающего взаимодействия между нейронами, опосредованная рецепторами N-метил-D-аспартата (NMDA). Другие исследователи привлекают к рассмотрению отрицательную регуляцию ингибирующего взаимодействия между нейронами, опосредованную рецепторами гамма-аминомасляной кислоты (GABA). В этот процесс могут быть вовлечены многие другие факторы, касающиеся присутствия, концентрации или активности NO(оксида азота) или ионов железа, кальция или цинка. Хотя эпилептические припадки редко бывают смертельными, большое количество пациентов нуждаются в лечении, чтобы избежать разрушительных и потенциально опасных последствий припадков. Во многих случаях лечение, применяемое для погашения эпилептических припадков или симптомов аналогичного связанного с припадками расстройства, необходимо в течение продолжительных периодов времени и в некоторых случаях пациент должен продолжать принимать такое предписанное лечение на протяжении всей жизни. Кроме того, такие лекарства эффективны только для снятия симптомов и имеют побочные эффекты, связанные с хроническим длительным применением. Широкое разнообразие лекарств, доступных для усмирения эпилептических припадков, включают более старые агенты, такие как фенитоин, вальпроат и карбамазепин (блокаторы ионных каналов), а также более новые агенты, такие как фелбамат, габапентин, топирамат и тиагабин. Кроме того, сообщается,что, например, -аланин обладает противоприпадочной активностью, NMDA-ингибирующей активностью и GABA-эргической стимулирующей активностью, но не используется клинически для лечения эпилепсии. Общепринятыми лекарствами для лечения эпилепсии являются антиконвульсанты или, более правильно называемые, антиэпилептические лекарственные средства (AED), где выражение "антиэпилептический" является синонимом "антиприпадочный" или "антииктогенный". Эти лекарственные средства терапевтически подавляют припадки путем блокирования стимулирования отдельного иктогенного события. Но эти AED, теперь клинически доступные, не предупреждают процесс эпилептогенеза. Некоторые AED также могут быть терапевтически пригодны при лечении припадков или родственных симптомов аналогичного связанного с припадками расстройства, то есть, для лечения заболеваний и расстройств с неврологическими явлениями, подобными припадкам, которые, очевидно, могут относиться к припадочным расстройствам, таким как зацикливание настроения при биполярном расстройстве,импульсивное поведение у пациентов с расстройствами контроля над импульсами, или для лечения припадков, являющихся результатом повреждения головного мозга. Однако эти одобренные в настоящее время AED не способны предупреждать или терапевтически предотвращать начальное развитие или прогрессирующее развитие эпилептогенеза в эпилептогенный очаг, что также характеризует аналогичные заболевания, связанные с припадками. Трудно объяснимые патологические механизмы, которые лежат в основе эпилептогенеза, определенно играют некоторую роль в развитии эпилепсии и аналогичных заболеваний, связанных с припадками, под влиянием различных клинических обстоятельств, включая самопроизвольное развитие, или в результате многих типов повреждений или травм центральной или периферической нервной системы. Современное лечение эпилепсии сфокусировано на подавлении припадочной активности посредством введения AED после развития явной клинической эпилепсии. Хотя AED оказывают положительные эффекты при подавлении припадков, доступные в настоящее время соединения по общему признанию являются безрезультативными для предупреждения эпилептогенеза, то есть, начального развития или прогрессирования и ухудшения эпилепсии и других заболеваний, подобных припадкам. Даже предварительная AED-терапия не предотвращает развития эпилепсии после повреждения или травмы нервной системы. Более того, если AED-терапию прекращают, то припадки обычно возвращаются и в неблагоприятных случаях ухудшаются со временем. В настоящее время не существует клинически доступного способа лечения, предупреждения, инвертирования, задержки или ингибирования появления и/или прогрессирования эпилепсии или других припадочных заболеваний или многих аналогичных заболеваний,-2 016610 связанных с припадками. Кроме того, полагают также, что аналогичные неврологические механизмы, сответствующие эпилептогенезу, могут быть вовлечены в эволюцию и развитие многих связанных с припадками расстройств,клинически аналогичных эпилепсии, которые не являются явно "эпилептическими", таких как начальное развитие и прогрессирующее ухудшение, наблюдаемое при сформировавшемся болезненном состоянии в случае биполярного расстройства, расстройства контроля над импульсами, обсессивно-компульсивные расстройства, шизоаффективные расстройства, злоупотребление психоактивным веществом или аддикция и многие другие психиатрические и неврологические расстройства. Таким образом, несмотря на то что существует много лекарственных средств для лечения эпилепсии (а именно, подавления эпилептических припадков, то есть, конвульсий, связанных с эпилептическими припадками) и других аналогичных заболеваний, связанных с припадками, не имеется общепринятых лекарственных средств для лечения, предупреждения, инвертирования, задержки или ингибирования процесса, лежащего в основе эпилептогенеза, который может быть этиологическим при многих разрушительных неврологических и психиатрических расстройствах, таких как эпилепсия и аналогичные заболевания, связанные с припадками, включая биполярное расстройство. В настоящее время не известны способы ингибирования эпилептогенного процесса с целью предупреждения развития эпилепсии или других аналогичных заболеваний, связанных с припадками, у пациентов, которые пока не демонстрируют их симптомы клинически, но которые неосознанно имеют заболевание или находятся под риском развития заболевания. Кроме того, не известны способы предупреждения развития или инвертирования процесса эпилептогенеза, преобразующие совокупность нейронов в эпилептогенной зоне, которая является источником, или восприимчивы или способны участвовать в припадочной активности в нервной ткани, которая не демонстрирует аномальных, самопроизвольных,внезапных, повторяющихся или чрезмерных электрических разрядов или невосприимчива или не допускает такой припадочной активности. Кроме того, не имеется одобренных или неодобренных способов лечения, которые признаны как имеющие такие антиэпилептогенные свойства, то есть, действительно антиэпилептогенных лекарственных средств (AEGD) (см. Schmidt, D. и Rogawski, M. A., Epilepsy Research, 2002, 50; 71-78). Таким образом, имеется огромная потребность в разработке безопасных и эффективных лекарственных средств или AED и способов лечения, которые кроме подавления припадков или конвульсий или связанных с припадками симптомов у пациентов, которые уже обнаруживают симптомы таких типов,предпочтительно эффективно лечат, предупреждают, купируют, ингибируют и/или инвертируют эпилептогенез при связанных с припадками неврологических и/или психиатрических расстройствах. Краткое содержание изобретения Настоящее изобретение касается способа лечения, профилактики, замедления, прекращения или инвертирования эпилептогенеза, включающий введение пациенту терапевтически эффективного количества соединения формулы (I) где R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и С 1-4 алкил; R4 выбран из группы, включающей атом водорода и С 1-4 алкил; а равно целому числу 1 или 2; представляет собой группу где b равно целому числу от 0 до 4; каждый R5 независимо выбран из группы, включающей галоген и С 1-4 алкил; или его фармацевтически приемлемой соли, где пациент представляет собой пациента, который находится в группе риска развития эпилепсии или аналогичного связанного с припадками расстройства вследствие повреждения головного мозга или другого поражения центральной нервной системы. В предпочтительном варианте в соединении формулы (I) R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и С 1-4 алкил; R4 выбран из группы, включающей атом водорода иC1-4 алкил; а равно целому числу 1 или 2; представляет собой группу где b равно целому числу 1 или 2; каждый R5 независимо выбран из группы, включающей галоген и С 1-4 алкил; или это соединение формулы (I) вводят в виде фармацевтически приемлемой соли. Ещ более предпочтительно, когда R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и С 1-4 алкил, предпочтительно метил; R4 выбран из группы, включающей атом водорода и метил; а равно целому числу 1 или 2; выбран из группы, включающей 2-(2,3-дигидробензо[1,4]диоксинил),-3 016610 2-(6-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-фтор-2,3-дигидробензо[1,4]диоксинил),2-(5-фтор-2,3-дигидробензо[1,4]диоксинил),2-(7-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-хлорбензо[1,3]диоксолил),2-(7-метил-2,3-дигидробензо[1,4]диоксинил),2-(5-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-бром-2,3-дигидробензо[1,4]диоксинил),2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил) и 2-(8-хлор-2,3-дигидробензо[1,4]диоксинил); или это соединение формулы (I) вводят в виде фармацевтически приемлемой соли. Наиболее предпочтительно, когда соединение формулы (I) представляет собой (2S)-(-)-N-(6-хлор 2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид и его фармацевтически приемлемую соль. В вариантах настоящего изобретения повреждение головного мозга или другое поражение центральной нервной системы выбрано из группы, включающей повреждение или травму ЦНС любого типа; нейрохирургические операции; травму спинного мозга; инфекции ЦНС; аноксию; удар (CVA); историю болезни преходящих ишемических атак (TIA); стеноз сонной артерии; историю болезни атеросклеротического сосудистого заболевания; историю болезни легочной эмболии; периферическое сосудистое заболевание; аутоиммунные заболевания, затрагивающие ЦНС; перинатальную асфиксию; остановку сердечной деятельности; терапевтические или диагностические сосудистые хирургические операции; гипотензию; повреждение ЦНС от эмболии, гипер- или гипоперфузию; гипоксию; занимающие пространство поражения ЦНС; опухоли головного мозга; кровотечение или кровоизлияние в ЦНС или окружающие ткани; отек головного мозга; фебрильные судороги; гипертермию; воздействие токсических или ядовитых агентов; наркотическую интоксикацию и отмену наркотика. Настоящее изобретение также относится к способу профилактики, замедления, прекращения или инвертирования эпилептогенеза, включающему введение пациенту терапевтически эффективного количества соединения, выбранного из группы, включающей (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид и его фармацевтически приемлемые соли; где пациент представляет собой пациента, который находится в группе риска развития эпилепсии или аналогичного связанного с припадками расстройства вследствие повреждения головного мозга или другого поражения центральной нервной системы. Ещ одним вариантом предложенного изобретения является способ профилактики, замедления,прекращения или инвертирования эпилептогенеза, включающий введение пациенту профилактически или терапевтически эффективного количества соединения, выбранного из группы, включающей (2S)-(-)N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид и его фармацевтически приемлемые соли; где пациент находится в группе риска развития эпилепсии или аналогичного связанного с припадками расстройства вследствие повреждения головного мозга или другого поражения центральной нервной системы и где пациент не демонстрирует симптомы эпилепсии или аналогичных заболеваний, связанных с припадками до момента введения. Подробное описание изобретения Настоящее изобретение касается способа лечения и/или предупреждения эпилептогенеза, эпилепсии и родственных расстройств, включающего введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, где а, R1, R2 и R4 такие, как здесь определено. Соединения формулы (I) и формулы (II) являются антиконвульсантами и могут прекращать эпилептические припадки. Кроме того, соединения формулы (I) и формулы (II), как неожиданно обнаружено,являются сильнодействующими антиэпилептогенными соединениями, которые могут предупреждать начальное развитие и созревание патологических изменений в нервной системе, которые позволяют припадкам и родственным явлениям происходить и/или распространяться. Кроме того, соединения формулы(I) и формулы (II) могут обладать способностью устранять изменения, происходящие в результате эпилептогенеза. Таким образом, соединения формулы (I) и формулы (II) по настоящему изобретению, которые используются в способах данного изобретения, действительно являются антиэпилептогенными лекарственными средствами (AEGD) и обладают свойствами, которые заметно отличаются от свойств любых одобренных в настоящее время AED и которыми указанные препараты AED не обладают. Следовательно, настоящее изобретение касается способов лечения, предупреждения, инвертирования, задержки и/или ингибирования эпилептогенеза. В некоторых вариантах эти способы включают введение профилактически или терапевтически эффективного количества соединения формулы (I) или фор-4 016610 мулы (II) нуждающемуся в этом субъекту. Специалисту в данной области должно быть понятно, что перед профилактическим или терапевтическим введением любого из описанных здесь соединений с целью лечения, предупреждения, ингибирования, инвертирования или задержки эпилептогенеза определяют, страдает ли субъект от эпилепсии или аналогичного расстройства, связанного с припадками, или нет, или не предполагается ли, что субъект имеет высокий риск развития таких припадков или заболеваний, связанных с припадками. В одном из вариантов настоящего изобретения субъект или пациент, нуждающийся в лечении, может быть субъектом, который уже демонстрирует симптомы эпилепсии, то есть, припадки или конвульсии, или может быть субъектом, который демонстрирует симптомы аналогичного расстройства, связанного с припадками, до момента введения. В другом варианте настоящего изобретения субъект или пациент, нуждающийся в лечении лекарственным средством против эпилептогенеза (AEGD), может быть субъектом, который не демонстрирует симптомы эпилепсии или аналогичных заболеваний, связанных с припадками, то есть, припадки или конвульсии, до момента введения. В другом варианте настоящего изобретения определяют субъекта или пациента, нуждающегося в лечении, как пациента с риском развития эпилепсии или аналогичного связанного с припадками расстройства на момент введения, и на этом основании считают, что пациент нуждается в лечении с применением AEGD. В одном варианте настоящее изобретение касается способов лечения, предупреждения, ингибирования, задержки и/или инвертирования эпилептогенеза, независимо от стимулирования и/или основной причины. В другом варианте настоящее изобретение касается способов лечения, предупреждения, инвертирования, задержки и/или ингибирования эпилептогенеза, включающего введение терапевтически эффективного количества соединения формулы (I) или формулы (II), которые здесь описаны, пациенту, который не имеет развитой эпилепсии, или какого-либо типа припадочного расстройства, или аналогичного расстройства, связанного с припадками, но который может находиться в группе высокого риска развития припадков или аналогичного связанного с припадками расстройства вследствие повреждения или травмы нервной системы, которое произошло (включая, но не ограничиваясь этим, повреждение или удар головы) или может произойти в будущем (включая, но не ограничиваясь этим, запланированные нейрохирургические операции), или вследствие некоторой известной предрасположенности, биохимической или генетической, или обнаружения верифицированного биомаркера одного или нескольких таких расстройств. При лечении эпилептогенеза способы по изобретению могут предотвращать развитие припадков,особенно эпилептических припадков. Следовательно, такие способы можно применять для лечения и предупреждения эпилепсии и эпилептических припадков, снижения риска развития эпилепсии, задержки развития эпилепсии (особенно, развития совокупности нейронов, которые представляют собой источник или восприимчивы к иктогенным припадкам), ингибирования развития и созревания эпилепсии (особенно, развития эпилептогенных зон и эпилептогенного очага), снижения тяжести эпилепсии у субъекта и инвертирования процесса эпилептогенеза при эпилепсии. Кроме того, при лечении, предупреждении, ингибировании, задержке и/или инвертировании эпилептогенеза согласно способам по настоящему изобретению имеет место лечение, предупреждение, ингибирование, задержка и/или инвертирование развития или прогрессирования аналогичных неврологических и/или психиатрических расстройств, этиология которых частично или полностью основана на механизме действия, подобном механизму припадков. Используемое здесь выражение "эпилептогенез" обозначает биохимические, генетические, гистологические или другие структурные или фукциональные процессы или изменения, которые делают нервную ткань, включая центральную нервную систему (ЦНС), восприимчивой к повторяющимся, самопроизвольным припадкам. Кроме того, выражение "эпилептогенез" также используют здесь в более широком смысле для обозначения изменений и/или процессов, которые вносят вклад в клиническое прогрессирование, наблюдаемое у пациентов с эпилепсией, или другим припадочным расстройством, или аналогичными связанными с припадками расстройствами, включая, но не ограничиваясь этим, ухудшение или прогрессирование расстройства и его симптомов или развитие "фармакорезистентности", при которой расстройство труднее поддается лечению, в результате нейробиологических изменений, что ведет к снижению лекарственной восприимчивости или пополнению в процессе эпилептогенеза не склонной к припадкам нервной ткани. Кроме того, выражение "эпилептогенез" используют здесь в наиболее широком смысле для обозначения похожих явлений прогрессирующего во времени ухудшения признаков и симптомов явно неэпилептических расстройств, включая психиатрические расстройства, этиология которых, по-видимому,связана с припадками. Используемое здесь выражение "ингибирование эпилептогенеза" относится к профилактике, замедлению, прекращению и/или инвертированию процесса эпилептогенеза. Используемое здесь выражение "антиэпилептогенное средство или лекарственное средство" и аб-5 016610 бревиатура "AEGD" относятся к средству, которое способно ингибировать эпилептогенез, когда его вводят нуждающемуся в этом субъекту. Используемые здесь выражения "конвульсивное расстройство" и "припадочное расстройство" относятся к расстройству, при котором субъект страдает от конвульсий, например, конвульсий вследствие эпилептического припадка. Конвульсивные расстройства включают, но не ограничены этим, эпилепсию и неэпилептические конвульсии, например конвульсии в результате введения субъекту конвульсивного агента или токсина. Используемые здесь выражения "аналогичное расстройство(а), связанное с припадками" или "связанное с эпилепсией, подобное припадкам неврологическое явление" относятся к нейробиологическому расстройству или психиатрическому расстройству, которое может демонстрировать небольшую или неочевидную припадочную активность, но которое, как полагают, является полностью или частично результатом подобных припадков или родственных нервных механизмов и которое, как часто обнаруживается, поддается излечению при помощи AED. Используемое здесь выражение "субъект" относится к животному, предпочтительно к млекопитающему, наиболее предпочтительно к человеку, который является объектом лечения, наблюдения или эксперимента. Используемое здесь выражение "субъект" или "пациент" также включает субъект, предпочтительно человека, который пока не демонстрирует симптомы эпилепсии или аналогичного связанного с припадками расстройства, но который может находиться в группе высокого риска. Используемое здесь выражение "субъект, нуждающийся в лечении с использованием AEGD" включает любого индивидуума с историей болезни или того, кто в настоящее время имеет эпилепсию, припадочное расстройство, или аналогичное связанное с эпилепсией, подобное припадкам неврологическое явление, или расстройство, связанное с припадками, или любое расстройство, при котором настоящее клиническое состояние пациента или прогноз может получить пользу от подавления или ингибирования процесса эпилептогенеза, предупреждая распространение, прогрессирование, ухудшение или повышение резистентности к лечению любого неврологического или психиатрического расстройства. Выражение "субъект, нуждающийся в лечении с использованием AEGD" также включает любого индивидуума, который не имеет эпилепсии или и аналогичного связанного с припадками расстройства,но который может находиться в группе высокого риска развития припадков или связанного с припадками расстройства вследствие повреждения или травмы центральной (ЦНС) или периферической нервной системы (ПНС). Считают, что индивидуум или пациент находится под высоким риском развития таких припадков или заболеваний, связанных с припадками, в результате повреждения или травмы ЦНС или ПНС, из-за некоторой известной биохимической или генетической предрасположенности к эпилепсии или аналогичному связанному с припадками расстройству или из-за верифицированного биомаркера или обнаруженного суррогатного маркера одного или нескольких таких расстройств. Выражение "субъект, нуждающийся в лечении с применением AEGD" также включает любого индивидуума, чье клиническое состояние или прогноз могут получить пользу от лечения с применениемAEGD. Это понятие включает (но не ограничено этим) любого индивидуума, который, как определено,находится под повышенным риском развития эпилепсии, припадочного расстройства или аналогичного расстройства, связанного с припадками, или неврологического явления, связанного с эпилепсией, подобного припадкам, или связанного с припадками расстройства, которое определено выше, вследствие какого-либо предрасполагающего фактора. Предрасполагающие факторы включают (но не ограничены этим) повреждение или травму ЦНС или ПНС любого типа; инфекции ЦНС, например менингит или энцефалит; аноксию; удар, то есть церебро-сосудистые несчастные случаи (CVA); аутоиммунные заболевания,затрагивающие ЦНС, например волчанку; родовые травмы, например перинатальную асфиксию; остановку сердца; терапевтические или диагностические сосудистые хирургические операции, например эндартерэктомию сонной артерии или церебральную ангиографию; хирургическую операцию по шунтированию сердца; травму спинного мозга; гипотензию; повреждение ЦНС от эмболии, гипер- или гипоперфузию ЦНС; гипоксию, затрагивающую ЦНС; известную генетическую предрасположенность к расстройствам, которые, как известно, реагируют на AEGD; занимающие пространство поражения ЦНС; опухоли головного мозга, например глиобластомы; кровотечение или кровоизлияние в ЦНС или окружающие ткани, например интрацеребральные кровотечения или субдуральные гематомы; отек головного мозга; фебрильные судороги; гипертермию; воздействие токсических или ядовитых агентов; наркотическую интоксикацию, например кокаиновую; семейный анамнез припадочных расстройств или аналогичного связанного с припадками расстройства, историю болезни эпилептического состояния; текущее лечение лекарствами, которые снижают порог чувствительности припадков, например карбонатом лития,торазином или клозапином; показания от суррогатных маркеров или биомаркеров к тому, что пациент нуждается в лечении с применением антиэпилептогенного лекарственного средства, например МРИсканирование, показывающее гиппокампальный склероз или другую патологию ЦНС, повышенные уровни в сыворотке продуктов деградации нейронов. Используемый здесь (пока не указано иначе) термин "эпилепсия" обозначает некоторое расстройство, при котором субъект (предпочтительно взрослый человек, ребенок или младенец) претерпевает один или более припадков и/или случаев тремора. Подходящие примеры включают, но не ограничены-6 016610 этим, эпилепсию (включая, но не ограничиваясь этим, связанные с локализацией эпилептические припадки, генерализованные эпилептические припадки, эпилепсию с генерализованными и локальными припадками и подобное), припадки как осложнение при заболевании или состоянии (например, припадки,связанные с энцефалопатией, фенилкетонурией, юношеской болезнью Гоше, прогрессирующей миоклонической эпилепсией Лундборга, ударом, травмой головы, стрессом, гормональными изменениями, использованием или отменой лекарственного средства, приемом или прекращением приема алкоголя, потерей сна и подобным) и др. Этот термин предназначен для обозначения клинического расстройства,независимо от типа припадков, природы припадков, прогрессирования припадков или основной причины или этиологии. Выражение "антиэпилептическое лекарственное средство" и аббревиатура "AED" используются попеременно с термином "антиконвульсант" и, как здесь использовано, относится к средству, способному производить лечение, ингибирование или предупреждение припадочной активности или иктогенеза, когда данный агент вводят субъекту или пациенту. Используемое здесь выражение "субъект, нуждающийся в лечении с применением AED" включает любого индивидуума, который, как известно, страдает от эпилепсии, или который имеет повторяющиеся припадки или конвульсии или демонстрирует симптомы аналогичного связанного с припадками расстройства, независимо от этиологии этих симптомов. Используемые здесь термины "лечение" или "лечить" относятся к действиям, которые вызывают какой-либо признак успеха при предупреждении или облегчении травмы, патологии, симптомов или состояния, включая любые объективные или субъективные параметры, такие как ослабление, ремиссия,уменьшение симптомов или более легкая переносимость пациентом повреждения, патологии или состояния; замедление скорости дегенерации или ухудшения; менее истощающий конечный момент дегенерации или улучшение физического или ментального самочувствия субъекта. Таким образом, термины "лечение" или "лечить" включают любое действие, которое улучшает,предупреждает, инвертирует, купирует, и/или ингибирует патологический процесс эпилептогенеза, как этот термин здесь определяется и используется. Лечение или облегчение симптомов может основываться на объективных или субъективных параметрах; включая результаты физического исследования, неврологического исследования и/или психиатрических оценок. Таким образом, термин "лечить" или "лечение" включает введение соединений или средств по настоящему изобретению с целью лечения, предупреждения, инвертирования, задержки и/или ингибирования процесса эпилептогенеза. В некоторых случаях лечение соединениями по настоящему изобретению предупреждает, ингибирует и/или задерживает прогрессирование дисфункции головного мозга или гипервозбудимости головного мозга, связанной с эпилепсией. Используемое здесь выражение "терапевтический эффект" относится к лечению, ингибированию,ослаблению, инверсии и/или предупреждению эпилептогенеза, эффектов или симптомов эпилептогенеза или побочных эффектов эпилептогенеза у субъекта. Используемое здесь выражение "терапевтически эффективное количество" означает, что количество активного соединения или фармацевтического средства вызывает биологический или медицинский отклик в системе тканей, у животного или человека, подвергаемого вмешательству исследователя, ветеринара, врача или другого клинициста, который включает облегчение симптомов заболевания или расстройства, подлежащего лечению. Таким образом, выражения "терапевтически эффективное количество" или "терапевтически эффективная доза", которые используются здесь попеременно, обозначают количество или дозу одного или более соединений или композиций по изобретению, достаточную для продуцирования терапевтического эффекта, который определен выше, у субъекта или пациента, нуждающегося в таком лечении, ингибировании, ослаблении, инверсии и/или предупреждении эпилептогенеза, эффектов или симптомов эпилептогенеза или побочных эффектов эпилептогенеза. Диапазон доз, необходимых для этих различных терапевтических эффектов, различается согласно характеристикам субъекта или пациента и определенной природе подлежащего лечению состояния. Если настоящее изобретение касается совместной терапии или комбинационной терапии, включающей введение одного или более соединения(ий) формулы (I) или формулы (II) и одного или более"подходящих фармацевтических средств", то "терапевтически эффективное количество" обозначает такое количество комбинации средств, взятых вместе, что объединенный эффект вызывает требуемый биологический или медицинский отклик. Например, терапевтически эффективное количество при совместной терапии, включающей введение соединения формулы (I) или формулы (II), и по меньшей мере одного подходящего фармацевтического средства, равно такому количеству соединения формулы (I) или формулы (II) и количеству подходящего фармацевтического средства, которые, взятые вместе или последовательно, имеют объединенный эффект, который является терапевтически эффективным. Кроме того, специалисты в данной области признают, что в случае совместной терапии с использованием терапевтически эффективного количества, как в приведенном выше примере, индивидуальное количество соединения формулы (I) или формулы (II) и/или количество подходящего фармацевтического средства может быть или не быть терапевтически эффективным. Используемые здесь выражения "совместная терапия" и "комбинационная терапия" обозначают ле-7 016610 чение нуждающегося в этом субъекта посредством введения одного или более соединений формулы (I) или формулы (II) в комбинации с одним или несколькими подходящими фармацевтическими агентами,где соединение(я) формулы (I) или формулы (II) и подходящий фармацевтический агент(ы) вводят любыми подходящими способами: одновременно, последовательно, отдельно или в виде единого фармацевтического препарата. Если соединение(я) формулы (I) или формулы (II) и подходящий фармацевтический агент(ы) вводят в виде отдельных дозированных форм, количество доз, вводимых за день для каждого соединения может быть одинаковым или разным. Соединение(я) формулы (I) или формулы (II) и подходящий фармацевтический агент(ы) можно вводить одинаковыми или различными способами введения. Примеры подходящих способов введения включают, но не ограничены этим, пероральный, внутривенный (iv), внутримышечный (im), подкожный (sc), трансдермальный и ректальный. Соединения также можно вводить непосредственно в нервную систему, включая, но не ограничиваясь этим, интрацеребральный, интравентрикулярный, интрацеребровентрикулярный, интратекальный, интрацистернальный, интраспинальный и/или периспинальный способы введения, осуществляя доставку при помощи внутричерепных или внутрипозвоночных игл и/или катетеров, с или без применения компрессионных устройств. Соединение(я) формулы (I) или формулы (II) и подходящий фармацевтический агент(ы) можно вводить по схемам с одновременным или чередующимся приемом, в одно и то же или разное время в течение курса терапии, совместно, поделив на части или в виде единых форм. Используемое здесь (пока не указано по-другому) выражение "подходящее фармацевтическое средство" предполагается для обозначения любого фармацевтического средства, которое имеет одно или более из следующих свойств: антиокислительную активность; антагонистическую активность относительно NMDA-рецептора, увеличение эндогенного GABA-ингибирования; ингибирующую активность NO синтазы; способность связывать железо, например, хелатообразователь для железа; способность связывать кальций, например, Са(II)-хелатообразователь; способность связывать цинк, например, Zn(II)хелатообразователь; способность эффективно блокировать натриевые или кальциевые ионные каналы или открывать калиевые или хлоридные ионные каналы в ЦНС пациента; включая известные AED или терапевтические средства, пригодные для лечения злоупотребления и склонности к алкоголю или наркотикам, включающие, но не ограниченные этим, метадон, дисульфирам, бупропион, антипсихотические средства, антидепрессанты, бензодиазепины, буспирон, налоксон или налтрексон. Предпочтительно, если подходящее фармацевтическое средство проявляет антагонистические свойства относительно NMDA-рецепторов, присоединяясь к NMDA-рецепторам (например, присоединяясь к сайту связывания глицина NMDA-рецепторов), и/или агент усиливает GABA-ингибирование, снижая глиальное поглощение GABA. Кроме того, "подходящее фармацевтическое средство" может быть любым средством, для которого известно, что оно подавляет припадочную активность, даже если не известно, что это соединение ингибирует эпилептогенез. Такие средства включают, но не ограничены этим, любые эффективные AED или антиконвульсанты, известные специалистам в данной области или которые будут открыты в будущем,например, подходящие агенты включают, но не ограничены этим, карбамазепин, клобазам, клоназепам,этосукцимид, фелбамат, габапентин, ламотигин, левитирацетам, окскарбазепин, фенобарбитал, фенитоин, прегабалин; примидон, ретигабин, талампанел, тиагабин, топирамат, вальпроат, вигабатрин, зонизамид, бензодиазепины, барбитураты или седативные снотворные средства. Термин "эпилепсия" относится к расстройству функции головного мозга, характеризующемуся периодическим и непредсказуемым возникновением припадков (см., The Treatment of Epilepsy, PrinciplesPractice. Third Edition, Elaine Wyllie, M.D. Editor, Lippincott WilliaMCWilkins, 2001; GoodmanGilman's The Pharmacological Basis of Therapeutics, 9th edition, 1996) (обе работы включены здесь в виде ссылок). Припадки, которые происходят без очевидного стимула, классифицируют как эпилептические. Эпилепсия может быть идиопатической или может быть связана с некоторыми типами травм, пороков развития или повреждений центральной нервной системы на любой стадии жизни. Обычно считается,что субъект страдает от эпилепсии после двух или более случаев припадков, которые происходят с интервалом более 24 ч. Клинически эпилептический припадок случается в результате внезапного и аномального электрического разряда исходящего из совокупности взаимосвязанных нейронов в головном мозге или где-либо еще в нервной системе. В зависимости от типа вовлеченной эпилепсии результирующая активность нервных клеток может проявляться посредством широкого разнообразия клинических симптомов, таких как неконтролируемая двигательная активность, изменения уровня сознания пациента и подобные. Эпилепсию и эпилептические припадки и синдромы можно классифицировать различными способами (см.,The Treatment of Epilepsy, PrinciplesPractice, Third Edition, Elaine Wyllie, M.D. Editor, Lippincott WilliamsWilkins, 2001). Однако полагают, что используемые здесь выражения "эпилепсия", "эпилептические припадки" и "эпилептические синдромы" включают все известные типы эпилептических припадков и синдромов, в том числе частичные припадки, включая простые, смешанные и частичные припадки,развивающиеся в генерализованные тонические-клонические судороги, и генерализованные припадки,конвульсивные и неконвульсивные, и неклассифицированные эпилептические припадки."Эпилептогенез" "эпилептогенного процесса" обычно состоит из двух фаз. Предполагается, что-8 016610 способы по настоящему изобретению включают профилактическое и/или терапевтическое введение любого из описанных здесь соединений либо на первой, либо на второй эпилептогенной стадии, либо предваряя эти стадии, с целью лечения, ингибирования, предупреждения, задержки или инвертирования последующего развития эпилепсии или другого аналогичного связанного с припадками расстройства у нуждающегося в этом субъекта. Первая эпилептогенная стадия известна как стадия начального поражения или повреждения. Начальное поражение или повреждение, как правило, представляет собой повреждение, поражающее головной мозг, вызванное одним или несколькими из возможных факторов, включающих, например, травматическое повреждение головного мозга, включая повреждение тупым предметом и проникающую травму головы или нейрохирургическую операцию; ЦНС-инфекцию, такую как, например, бактериальный менингит, вирусный энцефалит, бактериальный церебральный абсцесс или нейроцистицеркоз); церебрососудистое заболевание (такое как удар или опухоль головного мозга, включая, например, злокачественные глиомы; нейрохирургию (например, трепанации черепа) и эпилептическое состояние. В некоторых случаях начальное поражение является результатом проблем развития до рождения (таких как асфиксия плода при рождении, внутричерепная травма при рождении, метаболические расстройства или врожденные пороки развития головного мозга, но не ограничиваясь этим) или результатом генетических детерминант. Вторая эпилептогенная стадия известна как "латентная стадия". Вторая эпилептогенная стадия включает процесс нейронной реструктуризации, который характеризуется повторяющимися припадками(например, симптоматическая эпилепсия) или симптомами, демонстрируемыми при аналогичных заболеваниях, связанных с припадками. Эпилептогенный процесс можно также наблюдать среди персон,фактически страдающих от эпилепсии или аналогичных заболеваний, связанных с припадками. Припадки, испытываемые персонами, страдающими от эпилепсии, сами по себе являются эпилептогенными, так как они имеют тенденцию делать возникновение последующих припадков более вероятным или расширять область нервной ткани, которая подвержена действию припадочной активности, или делать припадочное расстройство более резистентным к лечению. Последствия этого процесса для пациента, который имеет припадочное расстройство, заключаются в том, что припадки имеют тенденцию становиться более частыми и более тяжелыми и часто более резистентным к лечению традиционными AED. Аналогичным образом родственная подобная припадку реакция при неврологических или психиатрических расстройствах, аналогичных эпилепсии, может становиться со временем все более и более тяжелой или резистентной к лечению, как зрелые расстройства. Фаза 1 эпилептогенеза может быть инициирована факторами, отличными от перечисленных выше,такими как прием внутрь соединений с эпилептогенным потенциалом, например психотропных лекарств,таких как, например, трициклические антидепрессанты, клозапин, литий и подобные. Способы по настоящему изобретению также предназначены для лечения, предупреждения, задержки, ингибирования и/или инвертирования развития эпилептогенеза, стимулированного факторами, которые с повышеннием вероятности для субъекта имеют тенденцию становиться эпилептогенными. Соединения формулы (I) и формулы (II), которые здесь описаны, пригодны при лечении эпилепсии и аналогичных связанных с припадками расстройств. Кроме того, описанные здесь соединения формулы(I) и формулы (II) пригодны для подавления, регулирования и предупреждения процесса эпилептогенеза,результатом которого является ухудшение, клиническое прогрессирование или повышение резистентности к лечению эпилепсии и родственных припадочных расстройств, или новое стимулирование этих расстройств и их симптомов в результате некоторого вида повреждения или травмы нервной системы. Таким образом, в одном из вариантов настоящее изобретение касается способов, которые позволяют клиницисту лечить симптомы эпилепсии, других припадочных расстройств и/или симптомы аналогичных связанных с припадками расстройств при одновременном ингибировании эпилептогенного процесса, который отвечает за ухудшение, прогрессирование, распространение или повышение резистентности к лечению процесса, лежащего в основе заболевания. Способ включает профилактическое или терапевтическое введение нуждающемуся в этом субъекту эффективного против эпилептогенеза количества или дозы описанного здесь соединения формулы (I) и/или формулы (II), которое одновременно лечит и предупреждает припадки или другие симптомы расстройства и, кроме того, способно задерживать, ингибировать и инвертировать процесс эпилептогенеза у данного субъекта. В некоторых вариантах субъект или пациент, нуждающийся в лечении (предпочтительно субъект или пациент, нуждающийся в лечении с использованием AEGD), может быть субъектом, который уже демонстрирует симптомы эпилепсии, то есть, припадки или конвульсии, или субъектом или пациентом,который демонстрирует симптомы аналогичного связанного с припадками расстройства (например, зацикливание настроения, импульсивное поведение, поведение, вызывающее привыкание, и подобное) до или на момент введения. Следовательно, один аспект настоящего изобретения касается улучшенного способа лечения и предупреждения припадков и симптомов заболеваний, связанных с припадками, у нуждающегося в этом субъекта. Способ включает стадию профилактического или терапевтического введения нуждающемуся в этом субъекту терапевтически эффективного количества описанного здесь соединения формулы (I) и/или формулы (II), которое лечит и предупреждает возникновение припадков,-9 016610 конвульсий или заболеваний, связанных с припадками. В некоторых других вариантах субъект или пациент, нуждающийся в лечении (предпочтительно субъект или пациент, нуждающийся в лечении с применением AEGD), может быть субъектом, который не демонстрирует симптомы эпилепсии, то есть, припадки или конвульсии или симптомы аналогичного связанного с припадками расстройства до момента введения. В этом варианте субъект или пациент определяется как имеющий риск развития эпилепсии или аналогичного связанного с припадками расстройства на момент введения, и на этом основании считают, что пациент нуждается в лечении с применениемAEGD. В этом аспекте изобретение касается способа задержки, ингибирования и/или инвертирования эпилептогенеза. Способ включает стадию профилактического или терапевтического введения нуждающемуся в этом субъекту профилактически или терапевтически эффективного количества любого из описанных здесь соединений, которое лечит, предупреждает, задерживает, ингибирует и инвертирует эпилептогенез. Подавляя процесс эпилептогенеза, можно предупредить развитие припадочного расстройства или родственного расстройства у субъекта, который получил некоторый вид травмы или повреждения нервной системы или который находится под другим риском. Таким образом, настоящее изобретение касается способов лечения, предупреждения, задержки, ингибирования и/или инвертирования эпилептогенеза у нуждающегося в этом субъекта, включающих введение субъекту профилактически или терапевтически эффективного количества композиции, которая содержит по меньшей мере одно соединение формулы (I) и/или формулы (II). В варианте настоящего изобретения с пользой используют способ для лечения пациента, который не страдает, или для которого известно, что он страдает от состояния, которое, как известно в данной области, эффективно лечится известными в настоящее время антиконвульсантами или антиэпилептическими (AED) средствами. Эти состояния включают, но не ограничены этим, аналогичное связанное с припадками расстройство(а). В этих случаях решение использовать способы и соединения по настоящему изобретению принимается на основании определения, если пациент является "пациентом, нуждающимся в лечении с использованием антиэпилептогенного лекарственного средства (AEGD)", в том смысле как это выражение определено выше. В другом варианте настоящее изобретение касается способов, пригодных для лечения и/или предупреждения припадков у пациентов с эпилепсией или другими припадочными расстройствами и/или аналогичных симптомов при заболеваниях, связанных с припадками, при одновременном ингибировании процесса эпилептогенеза и, следовательно, профилактике распространения или ухудшения процесса,лежащего в основе заболевания, или привлечения в процессе эпилептогенеза не подверженной припадкам нервной ткани. Способы по настоящему изобретению касаются лечения эпилептогенеза у субъекта, который находится под риском развития эпилепсии, или связанного с припадками расстройства, или аналогичного связанного с припадками расстройства(расстройств), но не имеет эпилепсии или клинически очевидных припадков. Субъект, который находится под риском развития эпилепсии или аналогичного связанного с припадками расстройства(расстройств), но не имеет эпилепсии, или другого припадочного расстройства,или аналогичного связанного с припадками расстройства(расстройств), может быть субъектом, который не имеет пока диагноза эпилепсии или аналогичного связанного с припадками расстройства(расстройств), но который находится под большим, чем остальное население, риском развития эпилепсии или аналогичного связанного с припадками расстройства(расстройств). Этот "больший риск" можно определить при распознавании какого-либо фактора в медицинском анамнезе субъекта или его семьи посредством физического исследования или тестирования, показывающего риск больше среднего развития эпилепсии или аналогичного связанного с припадками расстройства(расстройств). Следовательно, это установленное любыми доступными средствами определение, что пациент находится под"большим риском", можно использовать для решения, следует ли лечить пациента способами по настоящему изобретению. Пациенты, которые находятся под большим риском, включают (но не ограничены этим) тех, кто не страдает от повреждения или травмы центральной нервной системы, но имеет высокую вероятность такого повреждения или травмы из-за своего медицинского состояния или окружения. Они включают (но не ограничены этим) пациентов с историей болезни преходящих ишемических атак (TIA), или известным стенозом сонной артерии, или просто известным значительным артериосклерозом, а также пациентов,готовящихся к нейрохирургической операции. Кроме того, индивидуумы, возможно, страдающие от неврологических повреждений вследствие войны или спортивных травм, могут профилактически принимать соединения по изобретению; они включают солдат в боевом походе или спортсменов, занимающихся силовым спортом, например боксом. Субъектов, которые могут получить пользу от лечения способами по настоящему изобретению,можно идентифицировать, применяя общепринятые методы отбора для определения факторов риска,связанных с эпилептогенезом, эпилепсией, или другими припадочными расстройствами, или аналогичным связанным с припадками расстройством. Определение, что субъект находится или может находиться под риском развития эпилепсии, другого припадочного расстройства или аналогичного связанного с- 10016610 припадками расстройства, также включает, например, медицинскую оценку, которая включает всестороннюю историю болезни, физическое исследование и ряд важных исследований крови. Оно также может включать электроэнцефалограмму (ЭЭГ), компьютерную томографию (КТ), магнито-резонансное изображение (МРИ) или позитронную эмиссионную томографию (ПЭТ). Определение повышенного риска развития эпилепсии или аналогичного связанного с припадками расстройства можно также выполнить посредством генетического тестирования, включающего профиль генной экспрессии или протеомические методики (см., Schmidt, D. Rogawski, M.A. Epilepsy Research 50; 71-78 (2002), и Loscher, W.,Schmidt D. Epilepsy Research 50; 3-16 (2002. Эти методы отбора включают, например, обычные медицинские действия для определения факторов риска, которые могут быть связаны с эпилептогенезом, включая, но не ограничиваясь этим, например, закрытую или проникающую травму головы, нейрохирургические операции, бактериальные или вирусные инфекции ЦНС, тригеминальную невралгию, церебрососудистое заболевание, включая, но не ограничиваясь этим, удар, или историю болезни TIA, опухоли головного мозга, отек головного мозга,цистицеркоз, порфирию, метаболическую энцефалопатию, отмену лекарственного средства, включая, но не ограничиваясь этим, отказ от седативного-снотворного средства или алкоголя, аномальную перинатальную историю, включая аноксию при рождении или родовое повреждение любого типа, церебральный паралич, необучаемость, гиперактивность, историю болезни фебрильных судорог, историю болезни эпилептического состояния, семейную историю болезни эпилепсии или любого связанного с припадками расстройства, воспалительное заболевание головного мозга или кровеносных сосудов, включая волчанку,наркотическую интоксикацию, непосредственную или при плацентарном переносе, включая, но не ограничиваясь этим, кокаиновую и метамфетаминовую токсичность, единокровие с родителями и лечение лекарствами, которые снижают порог чувствительности припадков, включая психотропные лекарства,такие как антидепрессанты или антипсихотические средства. Определение, по которому пациенты могут получить пользу от лечения с применением AEGD, у пациентов, не имеющих клинических признаков или симптомов эпилепсии, или другого припадочного расстройства, или аналогичного расстройства, связанного с припадками, может основываться на различных "суррогатных маркерах" или "биомаркерах". Такие биомаркеры включают, но не ограничены этим,профили экспрессии генов или белков в ткани, крови или спинномозговой жидкости (CSF) или присутствие генетических маркеров, таких как SNP. Используемые здесь выражения "суррогатный маркер" и "биомаркер" применяются попеременно и относятся к любому анатомическому, биохимическому, структурному, электрическому, генетическому или химическому индикатору или маркеру, который может достоверно коррелировать с настоящим существованием или будущим развитием эпилепсии, или припадочного расстройства, или аналогичного связанного с припадками расстройства. В некоторых случаях для определения, находится ли субъект под риском развития одного из указанных выше расстройств, можно применять методики с получением изображения головного мозга, такие как компьютерная томография (КТ), магнито-резонансное изображение(МРИ), позитронная эмиссионная томография (ПЭТ) или другие методики, дающие неврологическое изображение. Примеры биомаркеров, подходящих для способов по данному изобретению, включают, но не ограничены этим, определение методом МРИ, КТ или другими методиками, дающими изображение, склероза, атрофии или уменьшения объема гиппокампа или присутствия медиального височного склероза(MTS) или подобной важной анатомической патологии; выявление в крови, сыворотке или тканях пациента молекул таких видов, как белок или другой биохимический биомаркер, например, повышенные уровни цилиарного нейротрофического фактора (CNTF) или повышенные уровни в сыворотке продукта деградации нейронов; или другое подтверждение от суррогатных маркеров или биомаркеров, что пациент нуждается в лечении с применением антиэпилептогенного лекарственного средства, например, ЭЭГуказание на припадочное расстройство или связанное с припадками аналогичное расстройство(а), или связанное с эпилепсией подобное припадкам неврологическое явление, или связанное с припадками расстройство. Ожидается, что в будущем будет разработано гораздо больше таких биомаркеров, использующих широкое разнообразие методик детектирования. Предполагается, что любой такой маркер или индикатор существования или возможного будущего развития припадочного расстройства, эпилепсии или аналогичного связанного с припадками расстройства (в используемом здесь смысле) можно применять в способах по данному изобретению для определения необходимости лечения с использованием композиций и способов по данному изобретению. В варианте настоящего изобретения лечение касается пациентов, которые имеют эпилепсию, или связанное с эпилепсией подобное припадкам неврологическое явление, или аналогичное связанное с припадками расстройство, как определено выше, и, принимая во внимание преимущество в виде способности соединений по настоящему изобретению устранять эпилептогенез, допускает постепенное снижение доз поддерживающей лекарственной терапии или интенсивности лечения, требующихся для регулирования клинического проявления у пациента эпилепсии, или связанного с эпилепсией подобного припадкам неврологического явления, или аналогичного связанного с припадками расстройства, которые- 11016610 определены выше. Следовательно, так как лечение с применением способов по настоящему изобретению дает улучшение лежащего в основе расстройства, то пациенту можно отменить поддерживающую лекарственную терапию, включающую (но не ограниченную этим) сами соединения по настоящему изобретению, если они используются в качестве единственной терапии. Таким образом, пациенту с эпилепсией, принимающему поддерживающую терапию с использованием обычного AED, можно отменить AED после того,как лечение с использованием одного или более соединений по настоящему изобретению инвертирует лежащее в основе эпилептическое расстройство. Специалист в данной области может определить, как быстро проводить сокращение, на основании клинических признаков и симптомов, включающих ЭЭГ, прорывающиеся припадки или другие подходящие биомаркеры лежащего в основе расстройства. Настоящее изобретение касается способов лечения, предупреждения, подавления, задержки и/или ингибирования эпилептогенеза, включающих введение нуждающемуся в этом субъекту, предпочтительно, субъекту, нуждающемуся в лечении с применением AEGD, терапевтически и/или профилактически эффективного количества соединения формулы (I) и/или формулы (II), которые здесь описаны. В одном из вариантов настоящего изобретения R1 выбран из группы, включающей атом водорода и метил. В другом варианте настоящего изобретения R2 выбран из группы, включающей атом водорода и метил. Еще в одном варианте настоящего изобретения каждый R1 и R2 обозначает атом водорода, или каждый R1 и R2 обозначает метил. В одном из вариантов настоящего изобретения -(СН 2)а- выбран из группы, включающей -СН 2- и-СН 2 СН 2-. В другом варианте настоящего изобретения -(СН 2)а- представляет собой -СН 2-. В одном из вариантов настоящего изобретения R4 выбран из группы, включающей атом водорода и метил, предпочтительно R4 обозначает атом водорода. В одном из вариантов настоящего изобретения а равно 1. В одном из вариантов настоящего изобретения b равно целому числу от 0 до 2. В другом варианте настоящего изобретения с равно целому числу от 0 до 2. В другом варианте настоящего изобретения b равно целому числу от 0 до 1. В другом варианте настоящего изобретения с равно целому числу от 0 до 1. Еще в одном варианте настоящего изобретения сумма b и с равна целому числу от 0 до 2, предпочтительно целому числу от 0 до 1. Еще в одном варианте настоящего изобретения b равно целому числу от 0 до 2 и с равно 0. В варианте настоящего изобретения В другом варианте настоящего изобретения[1,4]диоксинил), 2-(бензо[1,3]диоксолил), 3-(3,4-дигидробензо[1,4]диоксепинил), 2-(6-хлор-2,3-дигидробензо[1,4]диоксинил), 2-(6-фтор-2,3-дигидробензо[1,4]диоксинил), 2-(хроманил), 2-(5-фтор-2,3-дигидробензо[1,4]диоксинил), 2-(7-хлор-2,3-дигидробензо[1,4]диоксинил), 2-(6-хлорбензо[1,3]диоксолил), 2-(7 нитро-2,3-дигидробензо[1,4]диоксинил), 2-(7-метил-2,3-дигидробензо[1,4]диоксинил), 2-(5-хлор-2,3 дигидробензо[1,4]диоксинил), 2-(6-бром-2,3-дигидробензо[1,4]диоксинил), 2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил), 2-(8-хлор-2,3-дигидробензо[1,4]диоксинил), 2-(2,3-дигидронафто[2,3-b][1,4] диоксинил) и 2-(4-метилбензо[1,3]диоксолил). В другом варианте настоящего изобретения[1,3]диоксолил), 2-(2,3-дигидробензо[1,4]диоксинил), 2-(6-хлор-2,3-дигидробензо[1,4]диоксинил), 2-(7 хлор-2,3-дигидробензо[1,4]диоксинил), 2-(7-метил-2,3-дигидробензо[1,4]диоксинил), 2-(6-бром-2,3 дигидробензо[1,4]диоксинил) и 2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил). В другом варианте настоящего изобретения выбран из группы, включающей 2-(2,3 дигидробензо[1,4]диоксинил), 2-(7-метил-2,3-дигидробензо[1,4]диоксинил) и 2-(6-бром-2,3-дигидробензо[1,4]диоксинил). В одном из вариантов настоящего изобретения R5 выбран из группы, включающей галоген и низший алкил. В другом варианте настоящего изобретения R5 выбран из хлора, фтора, брома и метила. В одном из вариантов настоящего изобретения стереоцентр на соединении формулы (I) находится вS-конфигурации. В другом варианте настоящего изобретения стереоцентр на соединении формулы (I) находится в R-конфигурации. В одном из вариантов настоящего изобретения соединение формулы (I) присутствует в виде энантиомерно обогащенной смеси, где % знантиомерного обогащения (% ее) составляет величину больше примерно 75%, предпочтительно больше примерно 90%, более предпочтительно больше примерно 95%,наиболее предпочтительно больше примерно 98%. Дополнительные варианты настоящего изобретения включают варианты, где заместители, выбранные для одной или более переменных, определенных здесь (то есть R1, R2, R3, R4, X-Y и А), выбраны независимо, представляя собой любые индивидуальные заместители или любое подмножество заместителей, выбранных из полного перечня, который определен здесь. Типичные соединения по настоящему изобретению перечислены ниже в таб.1. Дополнительные соединения по настоящему изобретению перечислены в таблице 3. В приведенных ниже табл.1 и 2 столбец,озаглавленный "стерео", определяет стереоконфигурацию на атоме углерода гетероцикла, присоединенном к отмеченной звездочкой связи. Если обозначение отсутствует, это значит, что соединение получают в виде смеси стереоконфигураций. Где приведено обозначение "R" или "S", там стереоконфигурация указана на основании энантиомерно обогащенного исходного материала. Таблица 1. Типичные соединения формулы (I) Таблица 2. Дополнительные соединения по настоящему изобретению Используемый здесь, пока не указано по-другому, термин "галоген" обозначает хлор, бром, фтор и йод. Используемый здесь, пока не указано по-другому, термин "алкил", сам по себе или как часть группы заместителя, включает линейные и разветвленные цепи. Например, алкильные радикалы включают метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил и подобные. Пока не указано по-другому, используемое с алкилом определение "низший" обозначает углеродную цепь, состоящую из 1-4 атомов углерода. Используемый здесь, пока не указано по-другому, термин "алкокси" обозначает радикал простого кислородного эфира с описанными выше линейными или разветвленными алкильными группами, например метокси, этокси, н-пропокси, втор-бутокси, трет-бутокси, н-гексилокси и подобными. Используемая здесь метка обозначает наличие стереогенного центра. Если конкретная группа является "замещенной" (например, алкильной, арильной и др.), то эта группа может иметь один или более заместителей, предпочтительно от одного до пяти заместителей, более предпочтительно от одного до трех заместителей, наиболее предпочтительно от одного до двух заместителей, независимо выбранных из перечня заместителей. Со ссылкой на заместители термин "независимо" означает, что если возможно присутствие более одного заместителя, то такие заместители могут быть одинаковыми или разными.- 14016610 По стандартной номенклатуре, используемой на протяжении всей этой заявки, сначала описывается конечная часть обозначенной боковой цепи, затем соседняя фукциональность по направлению к точке присоединения. Таким образом, например, заместитель "фенил-алкил-амино-карбонил-алкил" относится к группе формулы Далее приведены используемые в описании сокращения, в частности, на схемах и в примерах. Если соединения по этому изобретению имеют по меньшей мере один хиральный центр, то, соответственно, они могут существовать в виде энантиомеров. Если соединения обладают двумя или более хиральными центрами, то они могут дополнительно существовать в виде диастереомеров. Следует понимать, что все такие изомеры и их смеси включены в область настоящего изобретения. Кроме того, некоторые из кристаллических форм соединений могут существовать в виде полиморфов и, предполагается, что как таковые они включены в настоящее изобретение. Кроме того, некоторые соединения могут образовывать сольваты с водой (то есть, гидраты) или обычными органическими растворителями, и,предполагается также, что такие сольваты включены в область данного изобретения. Ввиду того, что соли соединений по данному изобретению используются в медицине, они относятся к нетоксическим "фармацевтически приемлемым солям". Однако другие соли могут быть пригодны при получении соединений по этому изобретению или их фармацевтически приемлемых солей. Подходящие фармацевтически приемлемые соли соединений включают аддитивные соли кислот, которые могут образовываться, например, при смешивании раствора соединения с раствором фармацевтически приемлемой кислоты, такой как соляная кислота, серная кислота, фумаровая кислота, малеиновая кислота,янтарная кислота, уксусная кислота, бензойная кислота, лимонная кислота, винная кислота, угольная кислота или фосфорная кислота. Кроме того, если соединения по изобретению несут кислотный фрагмент, то их подходящие фармацевтически приемлемые соли могут включать соли щелочных металлов,например соли натрия или калия; соли щелочно-земельных металлов, например соли кальция или магния; и соли, образованные с подходящими органическими лигандами, например четвертичные аммоний- 15016610 ные соли. Таким образом, типичные фармацевтически приемлемые соли включают следующие: ацетат,бензолсульфонат, бензоат, бикарбонат, бисульфат, битартрат, борат, бромид, эдетат кальция, камзилат,карбонат, хлорид, клавуланат, цитрат, дигидрохлорид, эдетат, эдизилат, эстолат, эзилат, фумарат, глюцептат, глюконат, глутамат, гликоллиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, йодид, изотионат, лактат, лактобионат, лаурат, малат, малеат, манделат, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напзилат, нитрат, соль N-метилглюкаминаммония,олеат, памоат (эмбонат), пальмитат, пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, сульфат, субацетат, сукцинат, таннат, тартрат, теоклат, тозилат, триэтиодид и валерат. Типичные кислоты и основания, которые можно использовать при получении фармацевтически приемлемых солей, включают следующие соединения. Кислоты: уксусная кислота, 2,2-дихлоруксусная кислота, ацилированные аминокислоты, адипиновая кислота, альгиновая кислота, аскорбиновая кислота, L-аспарагиновая кислота, бензолсульфоновая кислота, бензойная кислота, 4-ацетамидобензойная кислота, (+)-камфорная кислота, камфорсульфоновая кислота, (+)-(1S)-камфор-10-сульфоновая кислота, каприновая кислота, капроновая кислота, каприловая кислота, коричная кислота, лимонная кислота, цикламовая кислота, додецилсерная кислота, этан-1,2 дисульфоновая кислота, этансульфоновая кислота, 2-гидроксиэтансульфоновая кислота, муравьиная кислота, фумаровая кислота, галактаровая кислота, гентизиновая кислота, глюкогептоновая кислота, Dглюконовая кислота, D-глюкороновая кислота, L-глутаминовая кислота, -оксоглутаровая кислота, гликолевая кислота, гипуровая кислота, бромистоводородная кислота, соляная кислота, (+)-L-молочная кислота, -DL-молочная кислота, лактобионовая кислота, малеиновая кислота, (-)-L-яблочная кислота,малоновая кислота, (+)-DL-манделовая кислота, метансульфоновая кислота, нафталин-2-сульфоновая кислота, нафталин-1,5-дисульфоновая кислота, 1-гидрокси-2-нафтойная кислота, никотиновая кислота,азотная кислота, олеиновая кислота, оротовая кислота, щавелевая кислота, пальмитиновая кислота, памоевая кислота, фосфорная кислота, L-пироглутаминовая кислота, салициловая кислота, 4 аминосалициловая кислота, себациновая кислота, стеариновая кислота, янтарная кислота, серная кислота, дубильная кислота, (+)-L-винная кислота, тиоциановая кислота, паратолуолсульфоновая кислота и ундециленовая кислота; и основания: аммиак, L-аргинин, бенетамин, бензатин, гидроксид кальция, холин, деанол, диэтаноламин, диэтиламин, 2-(диэтиламино)этанол, этаноламин, этилендиамин, N-метилглюкамин, гидрабамин,1 Н-имидазол, L-лизин, гидроксид магния, 4-(2-гидроксиэтил)морфолин, пиперазин, гидроксид калия, 1(2-гидроксиэтил)пирролидин, вторичный амин, гидроксид натрия, триэтаноламин, трометамин и гидроксид цинка. Соединения формулы (I) можно получить согласно процессу, изображенному на схеме 1. Схема 1 Таким образом, проводят взаимодействие замещенного подходящим образом соединения формулы(X), известного соединения или соединения, полученного известными способами, с сульфамидом, известным соединением, где сульфамид предпочтительно присутствует в количестве примерно от 2 до 5 эквивалентов, в органическом растворителе, таком как ТГФ, диоксан и подобные, предпочтительно при повышенной температуре примерно от 50 до 100 С, более предпочтительно примерно при температуре кипения с обратным холодильником, получая соответствующее соединение формулы (Ia). Альтернативно, проводят взаимодействие замещенного подходящим образом соединения формулы(X), известного соединения или соединения, полученного известными способами, с замещенным подходящим образом соединением формулы (XI), известным соединением или соединением, полученным известными способами, в присутствии основания, такого как ТЭА, ДИПЭА, пиридин и подобные, в органическом растворителе таком как ДМФА, ДМСО и подобные, получая соответствующее соединение формулы (I). Соединения формулы (X), где представляет собой гласно способу, изображенному на схеме 2.- 16 можно получить со 016610 Схема 2 Таким образом, проводят взаимодействие замещенного подходящим образом соединения формулы(XII), известного соединения или соединения, полученного известным способом (например, как описано на схеме 2, выше), с NH4OH, известным соединением, необязательно в органическом растворителе, таком как ацетонитрил и подобные, получая соответствующее соединение формулы (XIII). Проводят взаимодействие соединения формулы (XIII) с выбранным подходящим образом восстановителем, таким как ЛАГ и подобные, в органическом растворителе, например ТГФ, диэтиловом эфире и подобном, получая соответствующее соединение формулы (Ха). Соединения формулы (X), где изображенному на схеме 3. можно получить согласно способу, Схема 3 Таким образом, проводят взаимодействие замещенного подходящим образом соединения формулы(XIV), известного соединения или соединения, полученного известными способами, с NH4OH в присутствии агента сочетания, такого как ДЦК и подобные, необязательно в органическом растворителе, например, ацетонитриле и подобном, получая соответствующее соединение формулы (XV). Проводят взаимодействие соединения формулы (XV) с выбранным подходящим образом восстановителем, таким как ЛАГ и подобные, в органическом растворителе, например, ТГФ, диэтиловом эфире и подобном, получая соответствующее соединение формулы (Xb). Соединения формулы (X), где выбран из согласно способу, изображенному на схеме 4. Схема 4 Таким образом, проводят взаимодействие замещенного подходящим образом соединения формулы(XVI), где J1 представляет собой подходящую уходящую группу, такую как Br, Cl, I, тозил, мезил, трифлил и подобные, известного соединения или соединения, полученного известными способами (например,активацией соответствующего соединения, где J1 представляет собой ОН), с цианидом, например цианидом калия, цианидом натрия и подобным в органическом растворителе, таком как ДМСО, ДМФА, ТГФ и подобные, получая соответствующее соединение формулы (XVII). Соединение формулы (XVII) восстанавливают согласно известным способам, например, посредством взаимодействия с подходящим восстановителем, таким как ЛАГ, боран и подобные, получая соответствующее соединение формулы (Хс). Соединения формулы (X) где выбран из согласно способу, изображенному на схеме 5. Таким образом, замещенное подходящим образом соединение формулы (XVIII), известное соединение или соединение, полученное известными способами, активируют согласно известному способу,получая соответствующее соединение формулы (XIX), где J2 представляет собой подходящую уходящую группу, например тозилат, Cl, Br, I, мезилат, трифлат и подобные. Проводят взаимодействие соединения формулы (XIX) с фталимидной солью, такой как фталимид калия, фталимид натрия и подобные, в органическом растворителе, например, ДМФА, ДМСО, ацетонитриле и подобном, предпочтительно при повышенной температуре в диапазоне от 50 примерно до 200 С,более предпочтительно около температуры кипения с обратным холодильником, получая соответствующее соединение формулы (XX). Проводят взаимодействие соединения формулы (XX) с N2H4, известным соединением, в органическом растворителе, таком как этанол, метанол и подобные, предпочтительно, при повышенной температуре в диапазоне примерно от 50 до 100 С, более предпочтительно, около температуры кипения с обратным холодильником, получая соответствующее соединение формулы (Xd). Специалист в данной области отдает себе отчет, что соединения формулы (X), где можно аналогично получить согласно известным способам или, например, согласно способам, изображенным выше на схемах 2-5, выбирая и производя соответствующую замену бензоконденсированных исходных материалов нафтилконденсированными соединениями. Кроме того, специалист в данной области понимает, что, если требуется отдельный энантиомер(или смесь энантиомеров, обогащенная одним энантиомером) соединения формулы (X), то можно применять способы, описанные выше на схемах 1-5, заменяя подходящий исходный материал соответствующим отдельным энантиомером (или смесью энантиомеров, обогащенной одним энантиомером). Специалист в данной области понимает, что, если реакционную стадию по настоящему изобретению можно проводить в различных растворителях или системах растворителей, то указанную реакционную стадию также можно проводить в смеси подходящих растворителей или систем растворителей. Если способы получения соединений по изобретению дают смесь стереоизомеров, эти изомеры можно разделить, используя обычные методики, например препаративную хроматографию. Соединения можно получить в рацемическом виде или в виде индивидуальных энантиомеров посредством энантиоспецифического синтеза или разделения. Например, можно разделить соединения на составные энантиомеры стандартными методиками, такими как образование диастереомерных пар при образовании соли с оптически активной кислотой, такой как (-)-ди-паратолуоил-D-винная кислота и/или (+)-ди-паратолуоилL-винная кислота, с последующей фракционированной кристаллизацией и регенерацией свободного основания. Соединения также можно разделить посредством образования диастереомерных сложных эфиров или амидов с последующим хроматографическим разделением и удалением хирального вспомогательного агента. По-другому, соединения можно разделить, используя хиральную ВДЖХ-колонку. В течение какого-либо из процессов получения соединений по настоящему изобретению может быть необходимо и/или желательно защитить чувствительные или реакционноспособные группы на ка- 18016610 ких-либо из рассматриваемых молекул. Этого можно достичь при помощи обычных защитных групп,таких как группы, описанные в работах Protective Groups in Organic Chemistry, ed. J.F.W. McOmie, PlenumPress, 1973; and T.W. GreeneP.G.M. Wuts, Protective Groups in Organic Synthesis, John WileySons,1991. Защитные группы можно удалить на последующей обычной стадии, используя способы, известные в данной области. Настоящее изобретение касается способов лечения эпилептогенеза, независимо от основной причины и стадии развития, включающих введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения формулы (I) или формулы (II), которые здесь описаны. Следовательно, способы по данному изобретению обеспечивают способность прекращать припадки, конвульсии или симптомы аналогичного связанного с припадками расстройства при одновременной профилактике процесса эпилептогенеза с целью предупреждения прогрессирования или ухудшения основного заболевания или пополнения количества нейронов в процессе эпилептогенеза не подверженной припадкам нервной ткани. Для достижения этой цели следует использовать соединения или композиции по данному изобретению в надлежащем терапевтически эффективном количестве или дозе, как описано ниже. Подлежащие введению оптимальные дозировки и схемы приема специалист в данной области может легко определить и варьировать в зависимости от конкретного используемого соединения, способа введения, силы препарата и прогрессирования болезненного состояния. Кроме того, факторы, касающиеся конкретного пациента, принимающего лечение, включая возраст, массу, питание пациента и время введения, обуславливают необходимость регулирования дозировки. В одном из вариантов настоящего изобретения схему лечения с использованием соединения формулы (I) и/или формулы (II) можно начинать у субъекта или пациента, который имеет припадки, достаточные для подтверждения диагноза эпилепсии. В этом варианте соединения по изобретению можно одновременно применять как AED для прекращения припадков у пациента с признанным припадочным расстройством или эпилепсией. Однако в этом контексте, согласно способам по изобретению, эти соединения применяют при дозах в надлежащих диапазонах, чтобы дополнительно обеспечить антиэпилептогенный эффект (AEGD-эффект) и предупредить развитие или распространение нервной ткани, подверженной припадочной активности, и, как следствие, ухудшение заболевания. В другом варианте лечение по схеме с использованием соединений по настоящему изобретению можно начинать, например, после повреждения головного мозга субъекта или другого начального поражения, но до того, как субъекту поставлен диагноз эпилепсии, например до первого или второго припадка у субъекта. В одном варианте субъект, принимающий лечение с использованием соединения, обладающего эпилептогенным потенциалом, например, психотропного лекарства, или субъект, имеющий заболевание, связанное с риском развития эпилепсии, например, аутизм, может начинать лечение по схеме с использованием соединения формулы (I) или формулы (II), которые здесь описаны. В другом варианте лечение по схеме с использованием соединений по настоящему изобретению можно начинать до повреждения или травмы нервной системы, но в момент, когда такое повреждение или травму можно ожидать или когда она является вероятной. Например, такое лечение по схеме можно начинать до проведения нейрохирургической операции или, например, при боевых действиях, в силовых видах спорта или автогонках, при повторяющихся ударах, TIA и др. В другом варианте соединения, которые здесь описаны, можно вводить ежедневно в течение установленного периода времени (недели, месяца, года) после возникновения повреждения или начального поражения головного мозга. Лечащий врач знает, как определить, что соединение формулы (I) или формулы (II), которое здесь описано, достигло терапевтически эффективного уровня, например, посредством клинического исследования пациента или измерения уровней лекарственного средства в крови или цереброспинальной жидкости. Специалист в данной области обладает способностью определения максимальной переносимой дозы посредством физического исследования с целью определения наличия и тяжести побочных эффектов, таких как нечеткая речь, летаргия или нарушение координации. Кроме того, настоящее изобретение включает фармацевтические композиции, содержащие одно или более соединений формулы (I) и/или формулы (II) с фармацевтически приемлемым носителем. Фармацевтические композиции, содержащие в качестве активного ингредиента одно или более из описанных здесь соединений по изобретению, можно приготовить путем тщательного перемешивания соединения или соединений с фармацевтическим носителем согласно обычным методикам получения фармацевтических препаратов. Носитель может иметь широко разнообразные формы в зависимости от требуемого способа введения (например, орального, парентерального). Таким образом, для жидких оральных препаратов, таких как суспензии, эликсиры и растворы, подходящие носители и добавки включают воду, гликоли, масла, спирты, вкусовые агенты, консерванты, стабилизаторы, красители и подобное; для твердых оральных препаратов, таких как порошки, капсулы и таблетки, подходящие носители и добавки включают крахмалы, сахара, разбавители, гранулирующие агенты, лубриканты, связующие, разрыхлители и подобное. Поверх твердых препаратов для орального приема можно также нанести такие вещества, как сахара или энтеросолюбильное покрытие с целью регулирования основного места абсорбции. Носители для препаратов парентерального введения обычно содержат стерильную воду, и можно добавлять другие ингредиенты для повышения растворимости или консервации. Вводимые путем инъекции суспензии или- 19016610 растворы можно также приготовить, используя водные носители вместе с подходящими добавками. Для получения фармацевтических композиций по данному изобретению одно или более соединений по настоящему изобретению в качестве активного ингредиента тщательно смешивают с фармацевтическим носителем согласно обычным методикам получения фармацевтических препаратов, указанный носитель может иметь разнообразные формы в зависимости от формы требуемого для введения препарата, например орального или парентерального, такого как внутримышечное. При получении композиций в виде дозированной формы для орального приема можно использовать любую из обычных фармацевтических сред. Таким образом, для жидких оральных препаратов, таких как, например, суспензии, эликсиры и растворы, подходящие носители и добавки включают воду, гликоли, масла, спирты, вкусовые агенты, консерванты, красители и подобное; для твердых оральных препаратов, таких как, например, порошки, капсулы, таблетки в виде капсул, желатиновые капсулы и таблетки, подходящие носители и добавки включают крахмалы, сахара, разбавители, гранулирующие агенты, лубриканты, связующие, разрыхлители и подобное. Из-за простоты введения таблетки и капсулы представляют наиболее полезные дозированные формы для орального приема, понятно, что в этом случае применяют твердые фармацевтические носители. Если требуется, на таблетки можно нанести покрытие из сахара или энтеросолюбильное покрытие по стандартным методикам. Носитель для парентеральных препаратов обычно содержит стерильную воду, хотя можно включать другие ингредиенты, например, для повышения растворимости или консервации. Можно также приготовить суспензии для инъекций, в этом случае можно использовать подходящие жидкие носители, суспендирующие агенты и подобное. Упоминаемые здесь фармацевтические композиции содержат некоторое количество активного ингредиента, необходимое для доставки эффективной дозы, которая описана выше, на стандартную дозу, например таблетку, капсулу, порошок,инъекцию, чайную ложку и подобное. Упоминаемые здесь фармацевтические композиции содержат примерно от 0,1 до 1000 мг на стандартную дозу, например таблетку, капсулу, порошок, инъекцию, суппозиторий, чайную ложку и подобное, и могут применяться при дозе примерно от 0,01 до 200,0 мг/кг/день, предпочтительно примерно от 0,1 до 100 мг/кг/день, более предпочтительно примерно от 0,5 до 50 мг/кг/день, более предпочтительно примерно от 1,0 до 25,0 мг/кг/день или в любом диапазоне внутри указанных. Однако дозировку можно варьировать в зависимости от потребностей пациентов, тяжести подлежащего лечению состояния и используемого соединения. Можно применять ежедневное введение или постпериодическое дозирование. Предпочтительно, если эти композиции находятся в виде стандартной дозированной формы, выбранной из таких форм, как таблетки, пилюли, капсулы, порошки, гранулы, стерильные растворы или суспензии для парентерального введения, дозированный аэрозоль или жидкие спреи, капли, ампулы, автоинжекторные устройства или суппозитории для орального, парентерального, внутриносового, подъязычного или ректального введения или для введения посредством ингаляции или инсуффляции. Альтернативно композицию можно представить в виде, подходящем для введения один раз в неделю или один раз в месяц; например, нерастворимую соль активного соединения, такую как соль деканоат, можно адаптировать для обеспечения запаса препарата для внутримышечной инъекции. Для приготовления твердых композиций, таких как таблетки, основной активный ингредиент смешивают с фармацевтическим носителем, например, обычными ингредиентами таблетирования, такими как кукурузный крахмал,лактоза, сахароза, сорбит, тальк, стеариновая кислота, стеарат магния, дикальцийфосфат или смолы, и другими фармацевтическими разбавителями, например, водой, с образованием твердой предварительной композиции, содержащей гомогенную смесь соединения по настоящему изобретению или его фармацевтически приемлемой соли. Называя эти предварительные композиции гомогенными, полагают, что активный ингредиент равномерно диспергирован по всей композиции, таким образом, что композицию можно легко поделить на равно эффективные дозированные формы, такие как таблетки, пилюли и капсулы. Эти твердые предварительные композиции затем делят на стандартные дозированные формы описанных выше типов, содержащие от 0,01 примерно до 1000 мг активного ингредиента по настоящему изобретению. На таблетки или пилюли из новой композиции можно нанести покрытие или, по-другому,скомбинировать их для получения дозированной формы, обеспечивающей преимущество длительного действия. Например, таблетка или пилюля может содержать внутренний и внешний дозированные компоненты, причем последний находится в виде оболочки поверх первого. Два компонента могут быть разделены энтеросолюбильным слоем, который служит для противодействия разрушению в желудке и позволяет внутреннему компоненту проходить нетронутым в двенадцатиперстную кишку или для задержки высвобождения. Для таких энтеросолюбильных слоев или покрытий можно использовать разнообразные материалы: материалы, включающие ряд полимерных кислот, с такими материалами как шеллак, цетиловый спирт и ацетат целлюлозы. Жидкие формы, в которые можно включать новые композиции по настоящему изобретению для орального введения или введения посредством инъекции, включают водные растворы, сиропы с подходящими вкусовыми агентами, водные или масляные суспензии и эмульсии, содержащие вкусовые агенты, с годными в пищу маслами, такими как хлопковое масло, кунжутное масло, кокосовое масло или арахисовое масло, а также эликсиры и подобные фармацевтические носители. Подходящие диспергирующие или суспендирующие агенты для водных суспензий включают синтетические и природные смо- 20016610 лы, такие как трагакант, гуммиарабик, альгинат, декстран, натрий-карбоксиметилцеллюлоза, метилцеллюлоза, поливинилпирролидон или желатин. Способ лечения депрессии, описанный в настоящем изобретении, также можно осуществить, используя фармацевтическую композицию, включающую любое из определенных здесь соединений и фармацевтически приемлемый носитель. Фармацевтическая композиция может содержать примерно от 0,1 мг до 1000 мг, предпочтительно от 50 до 500 мг, соединения, и может находиться в любой из форм, подходящих для выбранного способа введения. Носители включают необходимые и инертные фармацевтические наполнители, включая (но не ограничиваясь этим) связующие, суспендирующие агенты, лубриканты, вкусовые агенты, подсластители, консерванты, красители и покрытия. Композиции, подходящие для орального введения, включают твердые формы, такие как пилюли, таблетки, таблетки в виде капсул,капсулы (каждый вид включает препараты непосредственного высвобождения, синхронного высвобождения и длительного высвобождения), гранулы и порошки, и жидкие формы, такие как растворы, сиропы, эликсиры, эмульсии и суспензии. Формы, пригодные для парентерального введения, включают стерильные растворы, эмульсии и суспензии. Соединения по настоящему изобретению преимущественно можно вводить в виде единых дневных доз или можно вводить общую дневную дозу, поделив ее на две, три или четыре дозы в день. Кроме того,соединения по настоящему изобретению можно использовать как форму для внутриносового введения посредством подходящих внутриносовых носителей местного применения или как трансдермальные кожные пластыри, хорошо известные специалисту в данной области. Конечно, при трансдермальной системе доставки введение дозы будет скорее непрерывным, чем периодическим, на протяжении всей схемы приема. Например, для орального введения в виде таблетки или капсулы активный лекарственный компонент можно объединить с нетоксическим фармацевтически приемлемым инертным носителем для орального приема, таким как этанол, глицерин, вода и подобные. Более того, если желательно или необходимо, можно также включить в смесь подходящие связующие, лубриканты, разрыхлители и красители. Подходящие связующие включают (без ограничения) крахмал, желатин, природные сахара, такие как глюкоза или бета-лактоза, кукурузные подсластители, природные и синтетические смолы, такие как гуммиарабик, трагакант или олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия,хлорид натрия и подобные. Разрыхлители включают, без ограничения, крахмал, метилцеллюлозу, агар,бентонит, ксантановую смолу и подобные. Жидкие формы содержат подходящие ароматизирующие суспендирующие или диспергирующие агенты, такие как синтетические и природные камеди, например трагакант, гуммиарабик, метилцеллюлоза и подобные. Для парентерального введения требуются стерильные суспензии и растворы. Когда требуется внутривенное введение, применяют изотонические препараты, которые обычно содержат подходящие консерванты. Соединения по данному изобретению можно вводить в виде любой из описанных выше композиций и согласно схемам приема доз, установленным в данной области, когда бы ни потребовалось лечение депрессии. Дневную дозировку продуктов можно варьировать в широком диапазоне от 0,01 до 200 мг/кг для взрослого человека в день. Для перорального приема предпочтительно получают композиции в виде таблеток, содержащих 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200, 250, 500 и 1000 мг активного ингредиента для симптоматического регулирования введения дозы пациенту, принимающему лечение. Эффективное количество лекарства обычно доставляется при уровне доз примерно от 0,01 до 1500 мг/кг массы тела в день. Предпочтительный диапазон составляет примерно от 0,1 до 100,0 мг/кг массы тела в день, более предпочтительно примерно от 0,5 до 50 мг/кг, более предпочтительно примерно от 1,0 до 25,0 мг/кг массы тела в день. Соединения можно вводить по схеме от 1 до 4 раз в день. Специалисту в данной области понятно, что терапевтически эффективная дозировка соединений по настоящему изобретению может включать повторяемые дозы в течение длительной схемы лечения, которая дает клинически значимые результаты по профилактике, инвертированию, задержке или ингибированию эпилептогенеза. Специалисту в данной области понятно, что и in vivo, и in vitro испытания, использующие подходящие известные и общепринятые клеточные и/или животные модели, предсказывают способность исследуемого соединения лечить или предупреждать данное расстройство. Кроме того, специалисту в данной области понятно, что клинические испытания на людях, включающие первые исследования на людях диапазона доз и эффективности, можно выполнить на здоровых пациентах и/или пациентах, страдающих от данного расстройства, согласно способам, хорошо известным в клинической и медицинской практике. Определение эффективных доз обычно основано на исследованиях на животных моделях с последующими клиническими исследованиями на людях, при этом руководствуются определением эффективных доз и протоколами введения, которые значительно снижают возникновение или тяжесть симптомов,на которые нацелено воздействие, или состояний у субъекта. Подходящие в этом отношении модели включают, например, мышиные, крысиные, свиные, кошачьи модели, модели приматов (не человека) и другие общепринятые животные модели, известные в данной области. Альтернативно эффективные дозы- 21016610 можно определить, используя in vitro модели (например, иммунологические и гистопатологические исследования). При использовании таких моделей обычно требуются только обычные расчеты и регулировки для определения подходящей концентрации и дозы для введения терапевтически эффективного количества биологически активного агента(ов) (например, количества, которое при внутриносовом,трансдермальном, внутривенном или внутримышечном введении эффективно выявляет требуемый отклик). Следующие примеры приведены в помощь пониманию изобретения и никоим образом не предназначены и не должны толковаться как ограничение изобретения, изложенного в формуле изобретения,которая приведена далее. Пример 1. 3,4-Дигидро-2 Н-бензо[b][1,4]диоксепин-3-ил)метил)сульфамид (соединение 3). Катехин (5,09 г, 46,2 ммоль) и карбонат калия объединяют в ацетонитриле и нагревают при температуре рефлюкса в течение одного часа. Добавляют 2-хлорметил-3-хлор-1-пропен (5,78 г, 4 6,2 ммоль) и продолжают взаимодействие при температуре рефлюкса в течение 24 ч. Раствор охлаждают до комнатной температуры и фильтруют. Фильтрат выпаривают и остаток разбавляют водой и экстрагируют диэтиловым эфиром (3). Объединенный органический раствор сушат над MgSO4 и концентрируют. Хроматография (2% этиловый эфир в гексане) дает 3-метилен-3,4-дигидро-2 Н-бензо[b][1,4]диоксепин в виде бесцветного масла. МС (ESI): 163,2 (М+Н+). 1 Н ЯМР (300 МГц, CDCl3) : 6,94 (м, 4 Н), 5,07 (с, 2 Н), 4,76 (с, 4 Н). 3-Метилен-3,4-дигидро-2 Н-бензо[b][1,4]диоксепин (5,00 г, 30,8 ммоль) растворяют в сухом ТГФ(100 мл). Добавляют при 0 С боран-ТГФ (1,0 М в ТГФ, 10,3 мл). Реакционную смесь перемешивают при к.т. в течение 5 ч. Добавляют аминосульфоновую кислоту (6,97 г, 61,6 ммоль). Реакционную смесь нагревают при температуре рефлюкса в течение ночи. Охлаждают реакционную смесь до комнатной температуры и добавляют водный гидроксид натрия (3,0 М, 100 мл). Раствор экстрагируют этилацетатом(3100 мл). Объединенный органический раствор сушат над MgSO4. Раствор концентрируют в вакууме и очищают методом хроматографии (от 2 до 8% метанола в дихлорметане), получая 3,4-дигидро-2 Нбензо[b][1,4]диоксепин-3-ил)метил)амин в виде бесцветного масла. МС (ESI): 180,1 (М+Н+). 1 Н ЯМР (300 МГц, ДМСО) : 6,92 (м, 4 Н), 4,21 (м, 2 Н), 4,07 (м, 2 Н), 3,33(ушир., 2 Н), 3,16 (д, J=4 Гц, 1 Н), 2,72 (д, J=4 Гц, 1 Н), 2,30 (м, 1 Н). 3,4-Дигидро-2 Н-бензо[b][1,4]диоксепин-3-ил)метил)амин (2,90 г, 16,2 ммоль) и сульфамид (3,11 г,32,4 ммоль) объединяют в сухом диоксане (60 мл) и нагревают при температуре рефлюкса в течение ночи. Добавляют хлороформ и осадок удаляют фильтрованием. Фильтрат концентрируют в вакууме и очищают методом хроматографии (от 2 до 8% ацетона в дихлорметане), получая указанное в заголовке соединение в виде беловатого твердого вещества. МС (ESI): 258,8 (М+Н+). 1 Н ЯМР (300 МГц, ДМСО), : 6,92 (м, 4 Н), 6,71 (широкий, 1 Н), 6,59 Рацемический 2,3-дигидро-1,4-бенздиоксин-2-илметиламин (4,4 г, 26 ммоль) и сульфамид (5,1 г, 53 ммоль) объединяют в 1,4-диоксане (100 мл) и кипятят с обратным холодильником в течение 2 ч. Реакционную смесь охлаждают до комнатной температуры и небольшое количество твердого вещества отфильтровывают и отбрасывают. Фильтрат выпаривают в вакууме и остаток очищают, используя колонку для флэш-хроматографии (ДХМ:метанол = 10:1) и получая белое твердое вещество. Твердое вещество перекристаллизовывают из ДХМ, получая указанное в заголовке соединение в виде белого твердого вещества, т. пл.: 97,5-98,5 С. Элементный анализ: расчет: С 44,25; Н 4,95; N 11,47; S 13,13; найдено: С 44,28; Н 4,66; N 11,21; S 13,15. 1 Н ЯМР (ДМСО-d6) : 6,85 (м, 4 Н), 6,68 (ушир.с, 3 Н, NH), 4,28 (м, 2 Н), 3,97 (дд, J=6,9, 11,4 Гц, 1 Н); 3,20 (м, 1 Н), 3,10 (м, 1 Н). Пример 3. (Бензо[1,3]диоксол-2-илметил)сульфамид (соединение 2). Катехин (10,26 г, 93,2 ммоль), метилат натрия (25 мас.%, в метаноле, 40,3 г, 186 ммоль) и метилдихлорацетат (13,3 г, 93,2 ммоль) объединяют в сухом метаноле (100 мл). Раствор нагревают при температуре рефлюкса в течение ночи. Реакционную смесь охлаждают до комнатной температуры, подкисляют,- 22016610 добавляя концентрированную соляную кислоту, и затем уменьшают объем примерно до 50 мл в вакууме. Добавляют воду и смесь экстрагируют диэтиловым эфиром (3100 мл). Объединенный органический раствор сушат MgSO4, концентрируют до коричневого твердого вещества и хроматографируют (2% этилацетат в гексане), получая метиловый эфир бензо[1,3]диоксол-2-карбоновой кислоты в виде бесцветного масла. МС (ESI): 195,10 (М+Н+). 1 Н ЯМР (300 МГц, CDCl3) : 6,89 (ушир., 4 Н), 6,29 (с, 1 Н), 4,34 (кв, J=7 Гц, 2 Н), 1,33 (т, J=7 Гц, 3 Н). К метиловому эфиру бензо[1,3]диоксол-2-карбоновой кислоты (7,21 г, 40,0 ммоль) добавляют гидроксид аммония (29% в воде, 10 мл) и достаточно ацетонитрила, чтобы смесь была гомогенной (5 мл). Раствор перемешивают в течение часа при комнатной температуре и затем добавляют дистиллированную воду. Амид бензо[1,3]диоксол-2-карбоновой кислоты, выпавший в осадок в виде белого твердого вещества, собирают фильтрованием и используют без дополнительной очистки. МС (ESI): 160,00 (М+Н+). 1H ЯМР (300 МГц, ДМСО) : 7,99 (с, ушир., 1 Н), 7,72 (с, широкий, 1 Н),6,94 (м, 2 Н), 6,86 (м, 2 Н), 6,30 (с, 1 Н). Амид бензо [1,3] диоксол-2-карбоновой кислоты (5,44 г, 32,9 ммоль) растворяют в тетрагидрофуране (ТГФ, 100 мл). Медленно добавляют к раствору при комнатной температуре литийалюминийгидрид(ЛАГ, 1 М в ТТФ, 39,5 мл, 39,5 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 24 ч. Добавляют дистиллированную воду для разложения избытка ЛАГ. Добавляют водный гидроксид натрия (3,0 М, 100 мл) и раствор экстрагируют этилацетатом (3100 мл). Объединенный органический раствор промывают водой и сушат над MgSO4. Растворитель выпаривают, получая С-бензо[1,3] диоксол-2-илметиламин в виде бесцветного масла. МС (ESI): 152,1 (М+Н+). 1 Н ЯМР (300 МГц, CDCl3), : 6,87 (м, 4 Н), 6,09 (т, J=4 Гц, 1 Н), 3,13 (д, J=4 Гц, 2 Н). С-Бензо[1,3]диоксол-2-илметиламин (2,94 г, 19,4 ммоль) и сульфамид (3,74 г, 38,9 ммоль) объединяют в сухом диоксане (50 мл) и раствор нагревают при температуре рефлюкса в течение ночи. Реакционную смесь концентрируют и остаток хроматографируют (от 2 до 10% ацетона в дихлорметане), получая указанное в заголовке соединение в виде белого твердого вещества. МС (ESI): 230,0 (М+Н+). 1 Н ЯМР (300 МГц, CDCl3) : 6,87 (м, 4 Н), 6,25 (т, J=4 Гц, 1 Н), 4,79 (ушир.,1 Н), 4,62 (ушир., 1 Н), 3,64 (д, J=4 Гц, 2 Н). Пример 4. (2S)-(-)-N-(2,3-Дигидробензо[1,4]диоксин-2-илметил)сульфамид (соединение 4). Катехин (13,2 г, 0,12 моль) и карбонат калия (16,6 г, 0,12 моль) перемешивают в ДМФА (250 мл),добавляют (2R)-глицидилтозилат (22,8 г, 0,10 моль) и реакционную смесь перемешивают при 60 С в течение 24 ч. Охлаждают реакционную смесь до комнатной температуры, разбавляют ледяной водой (1 л) и экстрагируют диэтиловым эфиром (4 раза). Объединенный органический раствор промывают 3 раза 10% карбонатом калия, один раз водой, один раз насыщенным раствором соли и выпаривают в вакууме,получая белое твердое вещество, которое очищают методом колоночной флэш-хроматографии(ДХМ:метанол=50:1), получая 2S)-2,3-дигидробензо[1,4]диоксин-2-ил)метанол в виде твердого вещества. Твердое вещество (13,3 г, 68 ммоль) растворяют в пиридине (85 мл), охлажденном до 0 С, добавляют паратолуолсульфонилхлорид (13,0 г, 68 ммоль) и реакционную смесь перемешивают при комнатной температуре в течение 20 ч. Реакционную смесь разбавляют диэтиловым эфиром (1 л) и 1N HCl (1,2 л). Органический слой отделяют и промывают 2 раза 1N HCl (500 мл), 4 раза водой (150 мл), один раз насыщенным раствором соли, сушат (MgSO4) и выпаривают в вакууме, получая белое твердое вещество,которое очищают методом колоночной флэш-хроматографии (Hept:ЭА = 2:1), получая (2S)-2,3 дигидробензо[1,4]диоксин-2-илметиловый эфир толуол-4-сульфоновой кислоты в виде белого твердого вещества. Белое твердое вещество объединяют с фталимидом калия (14,4 г, 78 ммоль) в ДМФА (250 мл) и нагревают при температуре рефлюкса в течение 1 ч, охлаждают до комнатной температуры, выливают в энергично перемешиваемую воду (1,5 л) и перемешивают 30 мин. Белое твердое вещество отфильтровывают и твердое вещество промывают несколько раз водой, 2% NaOH и снова водой и сушат на воздухе,получая (2S)-2-(2,3-дигидробензо[1,4]диоксин-2-илметил)изоиндол-1,3-дион в виде белого порошкового твердого вещества. Порошкообразное белое твердое вещество объединяют с гидразином (2,75 г, 86 ммоль) в EtOH (225 мл) и нагревают при температуре рефлюкса в течение 2 ч, охлаждают до комнатной температуры, добавляют 1N HCl до рН 1,0 и перемешивают в течение 15 мин. Белое твердое вещество отфильтровывают и промывают свежим EtOH (твердое вещество отбрасывают), фильтрат выпаривают в вакууме до твердого вещества, которое распределяют между диэтиловым эфиром и разбавленным водным NaOH. Раствор в диэтиловом эфире сушат (Na2SO4) и выпаривают в вакууме, получая светло-желтое- 23016610 масло. Масло очищают методом колоночной флэш-хроматографии (ДХМ:МеОН = 10:1), получая масло. Часть масла (4,82 г, 2 9 ммоль) в 2-пропаноле (250 мл) обрабатывают 1N HCl (30 мл) и нагревают на паровой бане до гомогенности и затем дают охладиться до комнатной температуры. Через 3 ч смесь охлаждают на льду в течение 2 ч. Белое хлопьевидное твердое вещество (соответствующую HCl-соль (2S)-C(2,3-дигидробензо[1,4]диоксин-2-ил)метиламина) отфильтровывают и затем снова перекристаллизовывают из 2-пропанола, получая белое твердое вещество.[]D = -69,6 (с=1,06, EtOH). Белое твердое вещество распределяют между ДХМ и разбавленным NaOH, ДХМ-фракцию сушат[]D = -57,8 (с=1,40, CHCl3). Масло (2,1 г, 12,7 ммоль) и сульфамид (2,44 г, 25,4 ммоль) кипятят с обратным холодильником в диоксане (75 мл) в течение 2 ч и сырой продукт очищают методом колоночной флэш-хроматографии(ДХМ:МеОН = 10:1), получая белое твердое вещество, которое перекристаллизовывают из ДХМ, получая указанное в заголовке соединение в виде белого кристаллического твердого вещества. Т.пл. 102-103 С; Рацемический 2,3-дигидро-1,4-бенздиоксин-2-илметиламин (8,25 г, 5,0 ммоль) и триэтиламин (1,52 г, 15 ммоль) объединяют в ДМФА (10 мл) и охлаждают на бане со льдом, добавляют диметилсульфамоилхлорид (1,44 г, 10 ммоль). Затем реакционную смесь перемешивают в течение 3 ч при непрерывном охлаждении. Реакционную смесь распределяют между этилацетатом и водой и этилацетатный раствор промывают насыщенным раствором соли, сушат (MgSO4) и выпаривают в вакууме, получая масло. Масло очищают, используя колонку для флэш-хроматографии (этилацетат:гептан = 1:1) и получая белое твердое вещество, которое перекристаллизовывают (этилацетат/гексан), получая указанное в заголовке соединение в виде белого хлопьевидного твердого вещества. Т.пл. 76-78 С; МС 273 (МН+). Элементный анализ: расчет: С 48,52; Н 5,92; N 10,29; S 11,78; найдено: С 48,63; Н 5,62; N 10,20; S 11,90. 1 Н ЯМР (CDCl3) : 6,87 (м, 4 Н), 4,59 (ушир.м, 1 Н, NH), 4,35 (м, 1 Н), 4,27 (дд, J=2,3, 11,4 Гц, 1 Н),4,04 (дд, J=7,0, 11,4 Гц, 1 Н), 3,36 (м, 2 Н), 2,82 (с, 6 Н). Пример 6. N-(2,3-Дигидробензо[1,4]диоксин-2-илметил)-N-метилсульфамид (соединение 7). Рацемический 2,3-дигидро-1,4-бенздиоксин-2-илметиламин (825 мг, 5 ммоль) растворяют в этилформиате (15 мл), кипятят с обратным холодильником в течение 30 мин и выпаривают в вакууме, получая N-(2,3-дигидробензо[1,4]диоксин-2-илметил)формамид в виде масла. Масло в диэтиловом эфире (25 мл) обрабатывают 1 М ЛАГ в ТГФ (9,0 мл, 9,0 ммоль) при 0 С и перемешивают в течение 5 ч при комнатной температуре. Реакционную смесь охлаждают на бане со льдом и гасят водой (0,50 мл) с последующим добавлением 3N NaOH (0,50 мл) и воды (0,50 мл). Затем смесь перемешивают при комнатной температуре в течение 1 ч. Твердое вещество отфильтровывают и выпаривают фильтрат в вакууме, получая остаток, который распределяют между 1N HCl и диэтиловым эфиром. Водную фазу подщелачивают 1N NaOH и экстрагируют диэтиловым эфиром. Органическую фазу сушат(MgSO4) и выпаривают в вакууме, получая (2,3-дигидробензо[1,4]диоксин-2-илметил)метиламин в виде масла. МС 180 (МН+); 1 Н ЯМР (CDCl3) : 6,85 (м, 4 Н), 4,30 (м, 2 Н), 4,02 (дд, J=7,9, 11,6 Гц, 1 Н), 2,85 (м,2 Н), 2,50 (с, 3 Н). Масло (380 мг, 2,1 ммоль) и сульфамид (8 20 мг, 8,5 ммоль) объединяют в диоксане (15 мл), кипятят с обратным холодильником в течение 1,5 ч и выпаривают в вакууме, получая сырой остаток. Остаток очищают методом колоночной хроматографии (этилацетат/гептан = 1:1) и полученное твердое вещество перекристаллизовывают из смеси этилацетат/гексан, получая указанное в заголовке соединение в виде белого твердого вещества.[1,4]диоксин-2-ил)метиламина (соотношение изомеров 6-хлор: 7-хлор составляет примерно 3:1 по данным ОФ ВДЖХ). Смесь растворяют в 2-пропаноле (100 мл) и добавляют 1N HCl в диэтиловом эфире до достижения рН 1,0. Соль гидрохлорид, которая выпадает в осадок, отфильтровывают (2,65 г) и перекристаллизовывают из смеси метанол/IPA, получая белые кристаллы. Белые кристаллы распределяют между ДХМ и разбавленным NaOH. ДХМ-фазу сушат и выпаривают в вакууме, получая очищенный (2S)-С-(6-хлор-2,3 дигидробензо[1,4]диоксин-2-ил)метиламин в виде масла.[]D = -67,8 (с=1,51, CHCl3). Масло (7,75 ммоль) и сульфамид (1,50 г, 15,5 ммоль) объединяют в диоксане (50 мл) и кипятят с обратным холодильником в течение 2,0 ч, охлаждают до комнатной температуры и выпаривают в вакууме, получая твердое вещество. Продукт очищают методом колоночной флэш-хроматографии, используя смесь ДХМ/метанол = 20:1 и получая указанное в заголовке соединение в виде белого твердого вещества. МС 277 (М-1); []D = -59,9 (с=1,11 М). 1 Н ЯМР (CDCl3) : 6,90 (д, J=2,2 Гц, 1 Н), 6,81 (м, 2 Н), 4,76(м, 1 Н), 4,55 (с, 2 Н), 4,40 (м, 1 Н), 4,29 (дд, J=2,4, 11,5 Гц, 1 Н), 4,05 (дд, J=7,1, 11,5 Гц, 1 Н), 3,45 (м, 2 Н). Элементный анализ: расчет: С 38,78; Н 3,98; N 10,05; найдено: С 38,80; Н 3,67; N 9,99. Фильтраты образовавшейся в результате кристаллизации соли гидрохлорида (2S)-С-(6-хлор-2,3 дигидробензо[1,4]диоксин-2-ил)метиламина, полученной выше, выделяют (содержание изомеров 6-хлор: 7-хлор составляет примерно 1:1) и выпаривают в вакууме, получая твердое вещество, которое распределяют между ДХМ (200 мл) и разбавленным NaOH (0,5 М, 50 мл). ДХМ-раствор промывают один раз насыщенным раствором соли, сушат (Na2SO4) и выпаривают в вакууме, получая масло, которое очищают методом ВДЖХ с обращенной фазой (10-50% ACN с 0,16% ТФУ в воде с 0,20% ТФУ), получая в остатке(2S)-С-(7-хлор-2,3-дигидробензо[1,4]диоксин-2-ил)метиламин. Остаток объединяют с сульфамидом (0,90 г, 9,4 ммоль) в диоксане (25 мл) и кипятят с обратным холодильником в течение 2,5 ч, охлаждают до комнатной температуры и выпаривают в вакууме, получая масло. Масло очищают методом колоночной флэш-хроматографии, используя смесь ДХМ/метанол = 10:1 и получая (2S)-(-)-N-(7-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид в виде белого твердого вещества. МС 277 (M-1); 1 Н ЯМР (CDCl3/CD3OD) : 6,88 (д, J=0,7 Гц, 1 Н), 6,81 (м, 2 Н), 4,37 (м, 1 Н), 4,30 (дд,J=2,3, 11,6 Гц, 1 Н), 4,04 (дд, J=7,0, 11,6 Гц, 1 Н), 3,38 (м, 2 Н). Пример 8. Хроман-2-илметилсульфамид (соединение 10). Хроман-2-карбоновую кислоту (4,5 г, 25 ммоль) и ГОБТ (3,86 г, ммоль) объединяют в ДХМ (40 мл) и ДМФА (10 мл). Добавляют диметиламинопропилэтилкарбодиимид (EDC, 4,84 г, 25 ммоль) при комнатной температуре и реакционную смесь перемешивают в течение 30 мин. Добавляют гидроксид аммония (2,26 мл, 33,4 ммоль) и перемешивают реакционную смесь в течение 16 ч. Реакционную смесь разбавляют ДХМ (50 мл) и водой (50 мл) и доводят рН смеси примерно до рН 3,0 при помощи 1N HCl. ДХМ-фазу отделяют и водную фазу дважды экстрагируют ДХМ. Объединенную ДХМ-фазу сушат(Na2SO4) и выпаривают в вакууме, получая масло, которое очищают методом колоночной флэшхроматографии (этилацетат), получая масло. Масло (5,35 г, 30 ммоль) в ТГФ (90 мл) перемешивают, добавляют в это время 1 М ЛАГ в ТГФ (36 мл, 36 ммоль) и затем реакционную смесь перемешивают при комнатной температуре в течение 20 ч. Реакционную смесь гасят водой, перемешивают в течение 2 ч, раствор декантируют, сушат (Na2SO4) и выпаривают в вакууме, получая С-хроман-2-илметиламин в виде маслянистого амина. Маслянистый амин (1,63 г, 10 ммоль) и сульфамид (1,92 г, 20 ммоль) объединяют в диоксане (50 мл) и доводят до кипения с обратным холодильником в течение 2 ч. Раствор охлаждают и выпаривают в вакууме, получая масло, которое очищают методом колоночной хроматографии (ДХМ:метанол = 10:1),получая белое твердое вещество. Твердое вещество перекристаллизовывают из смеси этилацетат/гексан,- 25016610 получая хроман-2-илметилсульфамид в виде белого твердого вещества. Т.пл. 100-101 С; МС 241 (М-1). Элементный анализ: расчет: С 49,57; Н 5,82; N 11,56; S 13,23; найдено: С 49,57; Н 5,80; N 11,75; S 13,33. Пример 9. 2-(2,3-Дигидробензо[1,4]диоксин-2-ил)этилсульфамид (соединение 16). Добавляют цианид калия (2,05 г, 31,5 ммоль) к 2-бромметил-(2,3-дигидробензо[1,4]диоксину) (6,87 г, 30 ммоль) в ДМСО (90 мл) и перемешивают при температуре окружающей среды в течение 20 ч. Затем реакционную смесь разбавляют водой (250 мл) и дважды экстрагируют диэтиловым эфиром. Раствор в диэтиловом эфире промывают водой, затем дважды промывают насыщенным раствором соли, сушат(Na2SO4) и выпаривают в вакууме, получая 2-цианметил-(2,3-дигидробензо[1,4]диоксин) в виде белого твердого вещества. 1(80 мл, 80 ммоль) и реакционную смесь кипятят с обратным холодильником в течение 5 ч, затем перемешивают при температуре окружающей среды в течение 16 ч. При охлаждении на бане со льдом добавляют 2N HCl до достижения рН 1,0. Затем реакционную смесь перемешивают в течение 1 ч при комнатной температуре и выпаривают в вакууме, получая масло. Масло распределяют между 3N NaOH и диэтиловым эфиром и раствор в диэтиловом эфире промывают насыщенным раствором соли, сушатMS (M+H)+ 180. Сырой 2-(2,3-дигидробензо[1,4]диоксин-2-ил)этиламин в диоксане (100 мл) объединяют с сульфамидом (3,0 г, 31 ммоль) и нагревают при температуре рефлюкса в течение 2 ч. Раствор охлаждают и выпаривают в вакууме, получая оранжевое твердое вещество, которое очищают методом колоночной хроматографии (ДХМ:МеОН = 10:1), получая белое твердое вещество. Твердое вещество перекристаллизовывают из ДХМ, получая указанное в заголовке соединение в виде твердого вещества. МС (М-1) 257; Т.пл. 101-103 С (уточненная); 1 Н ЯМР (CDCl3) : 6,86 (м, 4 Н), 4,70 (м, 1 Н), 4,52 (с,2 Н), 4,30 (м, 2 Н), 3,94 (дд, J=7,4, 11,3 Гц, 1 Н), 3,43 (дд, J=6,4, 12,9 Гц, 2 Н), 1,94 (дд, J=6,5, 12,9 Гц, 2 Н). Элементный анализ: найдено: С 46,48; Н 5,60; N 10,81; S 12,41; расчет: С 46,50; Н 5,46; N 10,85; S 12,41. Пример 10. (2S)-(-)-N-(6,7-Дихлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид (соединение 29).(200 мл). Добавляют (2R)-глицидилтозилат (9,12 г, 40 ммоль) и реакционную смесь перемешивают при 60 С в течение 24 ч. Реакционную смесь охлаждают до комнатной температуры и затем разбавляют ледяной водой (600 мл) и экстрагируют диэтиловым эфиром (4 раза). Объединенный органический раствор промывают 3 раза 10% карбонатом калия, дважды насыщенным раствором соли, сушат (MgSO4) и выпаривают в вакууме, получая вязкое масло (2S)-2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксин)метанол. Масло (2S)-2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксин)метанол (6,4 г, 27 ммоль) растворяют в пиридине (50 мл) и охлаждают до 0 С. Затем добавляют пара-толуолсульфонилхлорид (5,2 г, 27 ммоль) и реакционную смесь перемешивают при комнатной температуре в течение 20 ч. Реакционную смесь разбавляют диэтиловым эфиром и 1N HCl (750 мл) и органический слой отделяют и промывают 2 раза 1NHCl (250 мл), один раз водой (150 мл), дважды насыщенным раствором соли, сушат (MgSO4) и выпаривают в вакууме, получая светло-желтое твердое вещество (2S)-6,7-дихлор-2,3-дигидробензо[1,4]диоксин 2-илметиловый эфир толуол-4-сульфоновой кислоты. 1 Н ЯМР (CDCl3) : 7,79 (д, J=8,3 Гц, 2 Н), 7,36 (д, J=8,0 Гц, 2 Н), 6,94 (с, 1 Н), 6,83 (с, 1 Н), 4,37 (м,1 Н), 4,2 (м, 3 Н), 4,03 (дд, J=6,3, 11,7 Гц, 1 Н), 2,47 (с, 3 Н).(2S)-6,7-Дихлор-2,3-дигидробензо[1,4]диоксин-2-илметиловый эфир толуол-4-сульфоновой кислоты (8,0 г, 20,5 ммоль) объединяют с фталимидом калия (6,1 г, 33 ммоль) в ДМФА (75 мл) и нагревают при температуре рефлюкса в течение 1 ч, охлаждают до комнатной температуры, выливают в энергично перемешиваемую воду (0,5 л) и затем перемешивают 30 мин. Белое твердое вещество отфильтровывают и промывают несколько раз водой, 2% NaOH и снова водой и затем сушат на воздухе, получая (2S)-2(6,7-дихлор-2,3-дигидробензо[1,4]диоксин-2-илметил)изоиндол-1,3-дион (6,0 г, 80%) в виде белого порошкообразного твердого вещества.- 26016610 Белое порошкообразное твердое вещество объединяют с гидразином (1,06 г, 33 ммоль) в EtOH (80 мл) и нагревают при температуре рефлюкса в течение 2 ч, затем охлаждают до комнатной температуры. Добавляют 1N HCl, доводя рН реакционной смеси до рН 1,0 и затем реакционную смесь перемешивают в течение 15 мин. Белое твердое вещество отфильтровывают и промывают свежим EtOH (твердое вещество отбрасывают), фильтрат выпаривают в вакууме, получая твердое вещество, которое распределяют между диэтиловым эфиром и разбавленным водным NaOH. Раствор в диэтиловом эфире сушат (Na2SO4) и выпаривают в вакууме, получая вязкое масло (2S)-2-аминометил-(6,7-дихлор-2,3-дигидробензо[1,4] диоксин). 1 Н ЯМР (CDCl3) : 6,98 (с, 1 Н), 6,96 (с, 1 Н), 4,25 (дд, J=2,0, 11,2 Гц, 1 Н), 4,15 (м, 1 Н), 4,0 (м, 1 Н),2,97 (д, J=5,5 Гц, 2 Н). Часть масла (3,8 г, 16 ммоль) и сульфамид (3,1 г, 32,4 ммоль) кипятят с обратным холодильником в диоксане (100 мл) в течение 2 ч и сырой продукт очищают методом колоночной флэш-хроматографии(ДХМ:МеОН = 20:1), получая указанное в заголовке соединение в виде белого твердого вещества, которое перекристаллизовывают из смеси этилацетат/гексан, получая указанное в заголовке соединение в виде белого кристаллического твердого вещества. МС [М-Н]- 311,0; Т.пл. 119-121 С; []D = -53,4 (с=1,17, М). 1 Н ЯМР (ДМСО-d6) : 7,22 (с, 1 Н), 7,20(2S)-(-)-N-(2,3-Дигидро-7-нитробензо[1,4]диоксин-2-илметил)сульфамид (1,2 г, 4,15 ммоль) получают из 4-нитрокатехола согласно способу, описанному в примере 4. Затем (2S)-(-)-N-(2,3-дигидро-7 нитробензо[1,4]диоксин-2-илметил)сульфамид объединяют с 10% Pd/C в метаноле (120 мл) и встряхивают в атмосфере водорода (2,7 кг/см 2 = 39 фунт/дюйм 2) при комнатной температуре в течение 3 ч. Твердые вещества отфильтровывают и промывают 10% М в ДХМ и фильтрат выпаривают в вакууме, получая сырой продукт. Сырой продукт растворяют в 0,2N HCl (25 мл), замораживают и лиофилизуют, получая указанное в заголовке соединение в виде белого хлопьевидного твердого вещества, соответствующей соли гидрохлорида. МС (М+Н)+ 260; 1H ЯМР (ДМСО-d6) : 10,2 (ушир.с, 3 Н), 6,86 (м, 1 Н), 6,85 (с, 1 Н), 6,74 (дд, J=2,5,8,4 Гц, 1 Н), 4,22 (м, 2 Н), 3,88 (дд, J=6,7, 11,4 Гц, 1 Н), 3,04 (м, 2 Н). Пример 12. (2S)-(-)-N-(7-Метил-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид (соединение 19). Указанное в заголовке соединение получают согласно методике, описанной выше в примере 4, исходя из 4-метилкатехола и получая белое твердое вещество, которое перекристаллизовывают из смеси этилацетат/гексан, получая указанное в заголовке соединение в виде белого твердого вещества.MS [M-H]- 257; 1H ЯМР (CDCl3) : 6,76 (м, 1 Н), 6,66 (м, 2 Н), 4,80 (м, 1 Н), 4,57 (ушир.с, 1 Н), 4,40 (м,1 Н), 4,28 (м, 1 Н), 4,03 (дд, J=6,9, 11,4 Гц, 1 Н), 3,45 (м, 2 Н), 2,25 (с, 3 Н). Элементный анализ: расчет: С 46,50; Н 5,46; N 10,85; S 12,41; найдено: С 46,65; Н 5,60; N 10,84; S 12,61. Пример 13. In vivo исследование киндлинга миндалины. Развитие киндлинга миндалины является принятой моделью эпилептогенеза. (Amano К., Hamada К.,Yagi К., Seino M. Antiepileptic effects of topiramate on amygdaloid kindling in rats. Epilepsy Res., 1998 Jul; 31(2): 123-8; Barton M.E., White H.S. The effect of CGX-1007 and CI-1041, novel NMDA receptor antagonists, on kindling acquisition and expression. Epilepsy Res. 2004 Mar; 59(1): 1-12; Loscher W., Honack D.,Rundfeldt С. Antiepileptogenic effects of the novel anticonvulsaht levetiracetam (ucb L059) in the kindlingModification of seizure activity by electrical stimulation. II. Motor seizure. Electroencephalogr. Clin. Neurophysiol. 32, 281-294). Киндлинг-модель частичной эпилепсии у крыс является общепринятой моделью эпилептогенеза (McNamara J.O. Analyses of molecular basis of kindling development. Psychiatry Clin. Neurosci. 1995 Jun.; 49(3): S175-8. Review). Кратко говоря, методика исследования состоит в следующем. Взрослых самцов крыс SpragueDawley массой 250-300 г получают от Charles River, Wilmington, MA. Всех животных размещают в клет- 27016610 ки с циклом свет:темнота 12:12 и свободным доступом к пище (Prolab RMH 3000) и воде, исключая время удаления из клетки для проведения экспериментальных процедур. За животными ухаживают согласно рекомендациям, подробно описанным в National Research. Council Publication, "Guide for the Care and Useof Laboratory Animals", используя оборудование с регулируемой температурой при отсутствии пестицидов. Киндлинг-стимуляцию обычно выполняют между 9 и 14 ч, избегая каких-либо циркадианных вариаций. Соединение 8 растирают с небольшим объемом 0,5% метилцеллюлозы, воздействуют ультразвуком в течение 10 мин и доводят до конечного объема 0,5% метилцеллюлозой. Соединение 8 вводят системно (внутрибрюшинно) при объеме 0,04 мл/10 г массы тела и все тесты проводят в предварительно определенное время пикового эффекта через 0,5 ч после внутрибрюшинного введения. Способность соединения 8 блокировать проявление судорог, вызванных киндлингом миндалин,определяют следующим образом. Крыс анестезируют коктейлем из кетамина (120 мг/кг внутрибрюшинно) и ксилазина (12 мг/кг внутрибрюшинно). В асептических условиях стереотаксически имплантируют биполярный электрод (пластиковый, Roanoke, VA) в правую базолатеральную часть миндалины (АР -2,2,ML -4,7, DV -8,7; Paxinos и Watson). Передне-задние и боковые определения производят от брегмы, тогда как дорсально-вентральное определение производят от поверхности черепа. Имплантируют стерильные черепные винты (3-4) для индифферентного электрода сравнения. Электроды фиксируют, используя зубной цемент и акриловый материал. Затем закрывают рану, используя стерильные хирургические зажимыMichel 18/8 (Roboz, Gaithersburg, MD). Накладывают на рану мазь на основе антибиотика неомицина и каждой крысе вводят разовую дозу пенициллина (60000 IU внутримышечно, AgriLabs) перед возвращением в чистую клетку на одну неделю для послеоперационного восстановления. Затем проводят киндлинг миндалины согласно следующему протоколу. После короткой акклиматизации (5 мин) в регистрационной камере получают записи базисных ЭЭГ (MP 100, Biopac Systems Inc.,Goleta, CA). Затем крыс делят случайным образом на группы, принимающие носитель (0,5% метилцеллюлозу) или соединение 8 (75 мг/кг внутрибрюшинно) (n = 10 крыс в группе). В день эксперимента вводят разовую дозу соединения 8 или 0,5% метилцеллюлозы за 30 мин до киндлинга миндалины (200 мкА в течение 2 с). Для каждой крысы в каждой лечебной группе регистрируют оценку поведенческого приступа и продолжительность AD. Оценку поведенческого приступа делают, используя шкалу Расина; то есть, 0 = нет отклика; стадия 1 = груминг/гиперактивность; стадия 2 = кивание головой/тремор; стадия 3 = односторонний клонус передних конечностей; стадия 4 = клонус с подъемом на задние лапы; и стадия 5 = генерализованный тонический-клонический приступ с подъемом на задние лапы и падением(Racine, 1972). Активность после разряда (AD) регистрируют в виде числовых оценок в течение 180 с после стимулирующего обучения и измеряют продолжительность первичной AD. Крыс считают полностью стимулированными, когда они демонстрируют пять последовательных генерализованных приступов стадии 4 или 5. Ежедневные стимуляции продолжают во всех трех группах в течение 13 последовательных дней до тех пор, пока крысы в группе с приемом носителя не будут полностью возбуждены (то есть, пять последовательных приступов стадии 4 или 5). В этот момент всем крысам дают однонедельный период без стимуляции и лекарственного средства; после которого их снова стимулируют в отсутствие лекарственного средства, применяя тот же раздражитель, что и на фазе накопления возбуждения (то есть, дни 1-13). Крыс, принимающих соединение 8, впоследствии стимулируют один раз в день до достижения ими полностью возбужденного состояния. Послеразрядовая (AD) продолжительность в обеих группах, принимающих носитель и соединение 8, демонстрирует прогрессирующее повышение на протяжении фазы накопления возбуждения. Статистической разницы между лечебными группами не наблюдается. Соединение 8 предупреждает накопление полного генерализованного стимулированного приступа. Этот вывод основан на обнаружении, что оценка приступа по завершении периода без лекарственного средства и без раздражителя для крыс в группе, принимавшей соединение 8, остается существенно меньшей, чем для крыс в группе, принимавшей носитель ("соединение 8" = 1,40,40 по сравнению с "носителем" = 4,60,24). Кроме того, при стимуляции в отсутствие лекарственного средства оценка приступа для крыс в группе, принимавшей соединение 8, повышается параллельно с оценкой, наблюдаемой для крыс, принимавших носитель-подкрепляя вывод, что соединение 8 замедляет накопление возбуждения на несколько дней. Результаты этого исследования демонстрируют, что соединение 8 обладает способностью модифицировать развитие киндлинга на модели частичной эпилепсии у крыс при киндлинге миндалины. Эти результаты согласуются с выводом, что соединение 8 обладает эффектами, модифицирующими заболевание. Этот вывод основан на обнаружении, что оценка приступа по завершении периода без лекарственного средства и без стимуляции крыс в группе, принимавшей соединение 8, остается существенно меньшей, чем для крыс в группе, принимавшей носитель. Кроме того, при подведении итога протокола стимуляции в отсутствие лекарственного средства оценка приступов прогрессирует параллельно с величиной для группы, принимающей носитель. Обнаружение, что оценка приступа, но не послеразрядовая продолжительность (ADD), в группе с приемом соединения через неделю отдыха без раздражителя и без лекарственного средства заметно ни- 28016610 же, чем оценка в группе с приемом носителя, предполагает, что соединение 8 предупреждает накопление вторично генерализованного приступа, но не фокального приступа. Пример 14. В специфическом варианте композиции для перорального приема 100 мг соединения 8, полученного как в примере 7, готовят в виде препарата с достаточно мелкодисперсной лактозой, обеспечивая общее количество от 580 до 590 мг для заполнения твердой желатиновой капсулы размера 0. При том что в предшествующем описании объясняются принципы настоящего изобретения вместе с примерами, приведенными для иллюстрации, понятно, что осуществление изобретения на практике охватывает все обычные вариации, адаптации и/или модификации, которые входят в область следующей далее формулы изобретения, и их эквиваленты. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ лечения, профилактики, замедления, прекращения или инвертирования эпилептогенеза,включающий введение пациенту терапевтически эффективного количества соединения формулы (I) где R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и С 1-4 алкил;R4 выбран из группы, включающей атом водорода и С 1-4 алкил; а равно целому числу 1 или 2; представляет собой группу где b равно целому числу от 0 до 4; каждый R5 независимо выбран из группы, включающей галоген и С 1-4 алкил; или его фармацевтически приемлемой соли,где пациент представляет собой пациента, который находится в группе риска развития эпилепсии или аналогичного связанного с припадками расстройства вследствие повреждения головного мозга или другого поражения центральной нервной системы. 2. Способ по п.1, где в соединении формулы (I)R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и С 1-4 алкил;R4 выбран из группы, включающей атом водорода и С 1-4 алкил; а равно целому числу 1 или 2; представляет собой группу где b равно целому числу 1 или 2; каждый R5 независимо выбран из группы, включающей галоген и С 1-4 алкил; или это соединение формулы (I) вводят в виде фармацевтически приемлемой соли. 3. Способ по п.2, где в соединении формулы (I)R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и С 1-4 алкил;R4 выбран из группы, включающей атом водорода и метил; а равно целому числу 1 или 2; выбран из группы, включающей 2-(2,3-дигидробензо[1,4]диоксинил),2-(6-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-фтор-2,3-дигидробензо[1,4]диоксинил),2-(5-фтор-2,3-дигидробензо[1,4]диоксинил),2-(7-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-хлорбензо[1,3]диоксолил),2-(7-метил-2,3-дигидробензо[1,4]диоксинил),2-(5-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-бром-2,3-дигидробензо[1,4]диоксинил),2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил) и 2-(8-хлор-2,3-дигидробензо[1,4]диоксинил); или это соединение формулы (I) вводят в виде фармацевтически приемлемой соли. 4. Способ по п.3, где в соединении формулы (I)R1 и R2, каждый независимо, выбраны из группы, включающей атом водорода и метил;R4 выбран из группы, включающей атом водорода и метил; а равно целому числу 1 или 2;
МПК / Метки
МПК: A61K 31/357, A61K 31/353, A61P 25/08
Метки: профилактики, применение, гетероциклических, лечения, бензоконденсированных, эпилептогенеза, производных, сульфамидных
Код ссылки
<a href="https://eas.patents.su/30-16610-primenenie-benzokondensirovannyh-geterociklicheskih-sulfamidnyh-proizvodnyh-dlya-lecheniya-i-profilaktiki-epileptogeneza.html" rel="bookmark" title="База патентов Евразийского Союза">Применение бензоконденсированных гетероциклических сульфамидных производных для лечения и профилактики эпилептогенеза</a>
Предыдущий патент: Рекомбинантные моновалентные антитела и способы их получения
Следующий патент: Способ лечения мастоцитоза
Случайный патент: Тиольные производные, обладающие ингибирующей активностью в отношении металлопептидаз.