Способ модуляции стресс-активированной протеинкиназной системы
Номер патента: 15252
Опубликовано: 30.06.2011
Авторы: Блатт Лоренс М., Сейверт Скотт Д., Бейгелман Леонид, Радхакришнан Рамачандран
Формула / Реферат
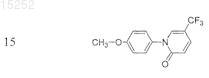
1. Соединение, имеющее формулу соединений класса VI
где Ar является пиридинилом или фенилом;
Z является О или S;
Х3 является Н, F, Cl, ОН, СН3 или ОСН3;
R2 означает фторметил, дифторметил или трифторметил; и
R4 означает Н или гидроксил;
при условии, что когда R2 означает трифторметил, Z является О, R4 является Н и Ar означает фенил, причем фенил замещен в 4'-положении не только Н, F или ОН;
где соединение имеет ЕС50в области приблизительно от 1 до 1000 мкМ для ингибирования MAPK р38,
или фармацевтически приемлемая соль, сложный эфир или сольват указанного соединения.
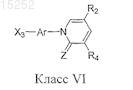
2. Соединение по п.1, где соединение выбрано из следующих соединений:
3. Соединение по п.2, имеющее EC50 в области приблизительно от 1 до 1000 мкМ для ингибирования по меньшей мере одной MAPK р38.
4. Соединение по п.3, где ЕС50составляет приблизительно от 50 до 650 мкМ.
5. Соединение по п.3, имеющее ЕС50в области приблизительно от 1 до 1000 мкМ для ингибирования секреции TNF-a в жидкости организма in vivo.
6. Соединение по п.3, имеющее ЕС50в области приблизительно от 1 до 1000 мкМ для ингибирования секреции TNF-a культивируемыми клетками in vitro.
7. Соединение, имеющее формулу соединений класса VII

где Х3 означает Н, галоген, C1-С10-алкокси или ОН;
Y1, Y2, Y3 и Y4независимо выбраны из группы, состоящей из Н, С1-С10-алкила, замещенного C1-С10-алкила, C1-С10-алкенила, C1-С10-галогеналкила, С1-С10-нитроалкила, C1-С10-тиоалкила, C1-С10-гидроксиалкила, С1-С10-алкокси, фенила, замещенного фенила, галогена, гидроксила, C1-С10-алкоксиалкила, C1-С10-карбокси, C1-С10-алкоксикарбонила, и
R4 означает Н, галоген или ОН, и
где соединение имеет ЕС50в области приблизительно от 1 до 1000 мкМ для ингибирования MAPK р38,
или фармацевтически приемлемая соль, сложный эфир или сольват указанного соединения.
8. Соединение по п.7, имеющее EC50 в области приблизительно от 1 до 1000 мкМ по меньшей мере для одной MAPK р38.
9. Соединение по п.7, где ЕС50составляет приблизительно от 50 до 650 мкМ.
10. Соединение по п.7, имеющее ЕС50 в области приблизительно от 1 до 1000 мкМ для ингибирования секреции TNF-a в жидкости организма in vivo.
11. Соединение по п.7, имеющее ЕС50 в области приблизительно от 1 до 1000 мкМ для ингибирования секреции TNF-a культивируемыми клетками in vitro.
12. Соединение по п.7, имеющее следующую формулу:
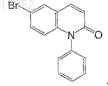
13. Соединение, выбранное из группы, состоящей из
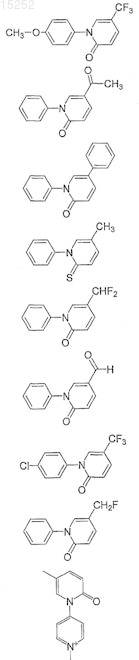
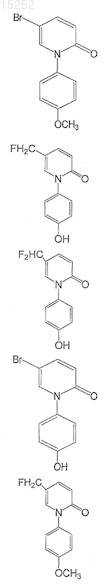
и
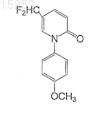
или их фармацевтически приемлемых солей, сольватов или эфиров.
14. Соединение по п.13, выбранное из группы, состоящей из
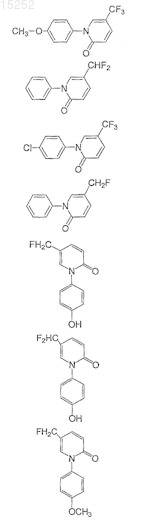
и
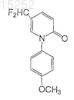
или их фармацевтически приемлемых солей, сольватов или эфиров.
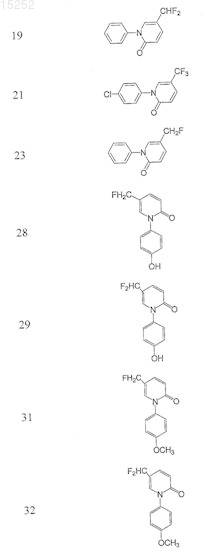
15. Соединение по п.13, выбранное из группы, состоящей из
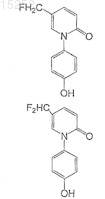
и
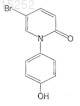
или их фармацевтически приемлемых солей, сольватов или эфиров.
16. Соединение по п.13, выбранное из группы, состоящей из
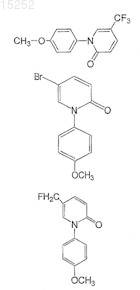
и
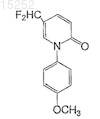
или их фармацевтически приемлемых солей, сольватов или эфиров.
17. Соединение по п.13, имеющее следующую формулу:
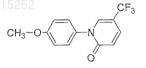
или его фармацевтически приемлемая соль, сольват или эфир.
18. Соединение по п.13, имеющее следующую формулу:
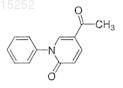
или его фармацевтически приемлемая соль, сольват или эфир.
19. Соединение по п.13, имеющее следующую формулу:
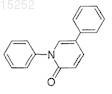
или его фармацевтически приемлемая соль, сольват или эфир.
20. Соединение по п.13, имеющее следующую формулу:
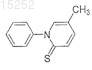
или его фармацевтически приемлемая соль, сольват или эфир.
21. Соединение по п.13, имеющее следующую формулу:
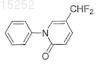
или его фармацевтически приемлемая соль, сольват или эфир.
22. Соединение по п.13, имеющее следующую формулу:
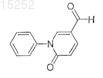
или его фармацевтически приемлемая соль, сольват или эфир.
23. Соединение по п.13, имеющее следующую формулу:
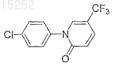
или его фармацевтически приемлемая соль, сольват или эфир.
24. Соединение по п.13, имеющее следующую формулу:
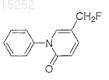
или его фармацевтически приемлемая соль, сольват или эфир.
25. Соединение по п.13, имеющее следующую формулу:

или его фармацевтически приемлемая соль, сольват или эфир.
26. Соединение по п.13, имеющее следующую формулу:
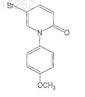
или его фармацевтически приемлемая соль, сольват или эфир.
27. Соединение по п.13, имеющее следующую формулу:
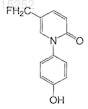
или его фармацевтически приемлемая соль, сольват или эфир.
28. Соединение по п.13, имеющее следующую формулу:
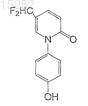
или его фармацевтически приемлемая соль, сольват или эфир.
29. Соединение по п.13, имеющее следующую формулу:
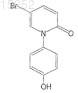
или его фармацевтически приемлемая соль, сольват или эфир.
30. Соединение по п.13, имеющее следующую формулу:

или его фармацевтически приемлемая соль, сольват или эфир.
31. Соединение по п.13, имеющее следующую формулу:
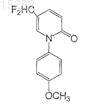
или его фармацевтически приемлемая соль, сольват или эфир.
32. Способ модуляции системы стресс-активированных протеинкиназ (SAPK), включающий в себя взаимодействие соединения с митоген-активированной протеинкиназой (MAPK) р38,
где соединение имеет ЕС50в области приблизительно от 1 до 1000 мкМ для ингибирования по меньшей мере одной MAPK р38,
где взаимодействие осуществляют при SAPK-модулирующей концентрации, составляющей менее чем ЕС30, для ингибирования соединением по меньшей мере одной киназы MAPK р38 и
где соединение представляет собой соединение по любому из пп.1-31.
33. Способ по п.32, в котором MAPK выбрана из группы, состоящей из р38a, р38b, р38g и р38d.
34. Способ по п.32, в котором взаимодействие осуществляют при SAPK-модулирующей концентрации, которая составляет менее чем ЕС20, для ингибирования соединением MAPK р38.
35. Способ по п.32, в котором взаимодействие осуществляют при SAPK-модулирующей концентрации, которая составляет менее чем ЕС10, для ингибирования соединением MAPK р38.
36. Способ по п.32, где величины ЕС50 и величины ЕС30 получают, исходя из кривой зависимости доза-эффект.
37. Способ по п.32, в котором SAPK-модулирующая концентрация является эффективной для того, чтобы изменить высвобождение фактора TNF-a в цельной крови по меньшей мере на 15%.
38. Способ по п.32, в котором ЕС50составляет приблизительно от 50 до 650 мкМ.
39. Способ лечения или профилактики болезненного состояния у субъекта, включающий в себя
идентификацию субъекта с риском развития состояния или субъекта, у которого обнаружено состояние, выбранное из воспалительного состояния и фибротического состояния;
введение субъекту соединения в эффективном количестве с целью лечения или профилактики указанного состояния,
где соединение имеет ЕС50в области приблизительно от 1 до 1000 мкМ для ингибирования по меньшей мере одной MAPK р38,
где эффективное количество соединения продуцирует концентрацию в крови или сыворотке или другой жидкости, которая составляет менее чем ЕС30 для ингибирования по меньшей мере одной MAPK р38, и
где соединение представляет собой соединение по любому из пп.1-31.
40. Способ по п.39, в котором состояние выбрано из группы, состоящей из фиброза, хронической обструктивной болезни легких, воспалительного фиброза легких, идиопатического легочного фиброза, синдрома облитерирующего бронхиолита, хронического фиброза аллотрансплантата, ревматоидного артрита; ревматоидного спондилита; остеоартрита; подагры; сепсиса; септического шока; эндотоксического шока; сепсиса, вызванного грамотрицательными бактериями; синдрома токсического шока; болевого синдрома височно-нижнечелюстного сустава (MPS); шигеллеза; астмы; респираторного дистресс-синдрома взрослых; воспалительного кишечного заболевания; болезни Крона; псориаза; экземы; язвенного колита; гломерулонефрита; склеродермии; хронического тиреоидита; болезни Грейвса; болезни Ормонда; аутоиммунного гастрита; тяжелой миастении; аутоиммунной гемолитической анемии; аутоиммунной нейтропении; тромбоцитопении; фиброза поджелудочной железы; хронического активного гепатита; фиброза печени; почечного заболевания; фиброза почки, синдрома раздраженной кишки; лихорадки; рестеноза; мозговой формы малярии; инсульта и ишемического поражения; травмы нервной системы; болезни Альцгеймера; болезни Гентингтона; болезни Паркинсона; острой и хронической боли; аллергий; гипертрофии сердца, хронической сердечной недостаточности; острого коронарного синдрома; кахексии; малярии; лепры; лейшманиоза; болезни Лайма; синдрома Рейтера; острого синовита; мышечной дегенерации, бурсита; тендонита; теносиновита; синдрома выпячивания, разрыва или выпадения межпозвонкового диска; врожденного системного остеопетроза; тромбоза; силикоза; множественных опухолей легкого мясистой консистенции; резорбции кости; рака; рассеянного склероза, волчанки; фибромиалгии; AID; опоясывающего лишая, простого герпеса; вируса гриппа; тяжелого острого респираторного синдрома (SARS); цитомегаловируса и сахарного диабета.
41. Способ по п.39, где эффективное количество составляет менее чем 50% количества, которое вызывает нежелательные побочные эффекты у субъекта.
42. Способ по п.39, в котором соединение ингибирует киназу, участвующую в SAPK-сигнальном пути.
43. Способ по п.39, где указанное соединение вводят указанному субъекту по схеме, выбранной из режима введения дважды в день, один раз в день, один раз каждые два дня, три раза в неделю, дважды в неделю и один раз в неделю.
44. Способ по п.40, где указанное соединение вводят указанному субъекту по схеме, выбранной из режима введения дважды в день, один раз в день, один раз каждые два дня, три раза в неделю, дважды в неделю и один раз в неделю.
45. Способ по п.40, где состоянием является синдром облитерирующего бронхиолита.
46. Способ по п.40, где состоянием является хронический фиброз аллотрансплантата.
47. Способ по п.40, где состоянием является идиопатический легочный фиброз.
48. Способ по п.40, где состоянием является хроническая обструктивная болезнь легких.
49. Фармацевтическая композиция, содержащая соединение по п.1 и фармацевтически приемлемый наполнитель.
50. Фармацевтическая композиция, содержащая соединение по п.7 и фармацевтически приемлемый наполнитель.
51. Фармацевтическая композиция по п.49, содержащая количество указанного соединения, которое выбирают для введения больному по схеме, выбранной из режима введения дважды в день, один раз в день, один раз каждые два дня, три раза в неделю, дважды в неделю и один раз в неделю.
52. Фармацевтическая композиция по п.50, содержащая количество указанного соединения, которое выбирают для введения больному по схеме, выбранной из режима введения дважды в день, один раз в день, один раз каждые два дня, три раза в неделю, дважды в неделю и один раз в неделю.
53. Фармацевтическая композиция, содержащая соединение по любому из пп.13-16 и фармацевтически приемлемый наполнитель.
54. Фармацевтическая композиция по п.53, содержащая количество указанного соединения, которое выбирают для введения больному по схеме, выбранной из режима введения дважды в день, один раз в день, один раз каждые два дня, три раза в неделю, дважды в неделю и один раз в неделю.
Текст
Изобретение относится к способам модуляции системы стресс-активированных протеинкиназ При этом активное соединение проявляет низкую потенциальную способность к ингибированию по меньшей мере одной MAPK р 38 и где взаимодействие осуществляют при SAPKмодулирующей концентрации, которая является концентрацией, приводящей к низкому проценту ингибирования под действием указанного соединения по меньшей мере одной MAPK р 38. В изобретении описаны также соединения, которые могут модулировать стресс-активированную протеинкиназную (SAPK) систему, фармацевтические композиции на их основе и способы лечения или профилактики состояний, которые связаны с повышенной активностью р 38-киназы. 015252 Перекрестная ссылка Данная заявка претендует на приоритет по предварительной патентной заявке США 60/679471,зарегистрированной 10 мая 2005, и предварительной патентной заявке США 60/732230, зарегистрированной 1 ноября 2005, обе из которых непосредственно включены в данное описание в полном объеме в виде ссылки. Область изобретения Изобретение относится к соединениям и способам, применяемым в лечении различных воспалительных состояний и/или фиброзных состояний, включая состояния, которые связаны с повышенной активностью р 38-киназы. Предшествующий уровень техники Было показано, что большое число хронических и острых состояний связано с нарушением воспалительного ответа. Большое число цитокинов принимает участие в данном ответе, включая IL-1, IL-6, IL8 и TNF-. По-видимому, активность указанных цитокинов в регуляции воспаления может быть связана с активацией фермента в каскаде реакций в пути передачи сигнала в клетке, члена семейства МАР-киназ,обычно известного как р 38-киназа, а также известного как SAPK, CSBP и RK. Некоторые ингибиторы р 38-киназы, такие как NPC 31169, SB239063, SB203580, FR-167653 и пирфенидон, исследовали in vitro и/или in vivo и обнаружили, что они проявляют эффективность в модуляции воспалительных ответов. Безопасные и эффективные лекарственные средства, предназначенные для лечения различных воспалительных состояний и/или фиброзных состояний, таких как воспалительный фиброз легких и/или идиопатический легочный фиброз, до сих пор остаются востребованными. Сущность изобретения Один вариант осуществления настоящего изобретения представляет собой способ модуляции системы стресс-активированных протеинкиназ (SAPK), включающий взаимодействие соединения с митоген-активированной протеинкиназой (MAPK) р 38, где соединение обладает ЕС 50 в области приблизительно от 1 до 1000 мкМ для ингибирования по меньшей мере одной MAPK р 38 и где взаимодействие осуществляют при SAPK-моделирующей концентрации, которая составляет менее чем ЕС 30 для ингибирования соединением по меньшей мере одной MAPK р 38. Другим вариантом осуществления настоящего изобретения является способ лечения или профилактики заболевания у субъекта, включающий в себя идентификацию субъекта, которому угрожает развитие состояния или который имеет состояние, выбранное из воспалительного состояния и фибротического состояния; введение субъекту соединения в эффективном количестве с целью лечения или профилактики состояния, где соединение имеет ЕС 50 в области приблизительно от 1 до 1000 мкМ для ингибирования по меньшей мере одной MAPK р 38 и где эффективное количество соединения составляет концентрацию в крови или сыворотке или другой жидкости организма, которая составляет менее чем ЕС 30 для ингибирования по меньшей мере одной MAPK р 38. Другим вариантом осуществления настоящего изобретения является способ идентификации фармацевтически активного соединения, включающий в себя предоставление библиотеки соединений; испытание множества соединений из библиотеки на их способность ингибировать по меньшей мере одну MAPK р 38, и отбор по меньшей мере одного соединения из множества соединений, где выбранное соединение имеет ЕС 50 в области приблизительно от 1 до 1000 мкМ для ингибирования по меньшей мере однойMAPK р 38. Другим вариантом осуществления настоящего изобретения является способ идентификации фармацевтически активного соединения, включающий в себя предоставление библиотеки соединений; испытание множества соединений из библиотеки на их способность ингибировать секрецию TNF- в жидкости организма in vivo, и отбор по меньшей мере одного соединения из множества соединений, где выбранное соединение имеет ЕС 50 в области приблизительно от 1 до 1000 мкМ для ингибирования секреции TNFв жидкости организма in vivo. Другим вариантом осуществления настоящего изобретения является способ идентификации фармацевтически активного соединения, включающий в себя предоставление библиотеки соединений; испытание множества соединений из библиотеки на их способность ингибировать секрецию TNF- культивируемыми клетками in vitro и отбор по меньшей мере одного соединения из множества соединений, где выбранное соединение имеет ЕС 50 в области приблизительно от 1 до 1000 мкМ для ингибирования секреции TNF- культивируемыми клетками in vitro. Другим вариантом осуществления настоящего изобретения является способ идентификации фармацевтически активного соединения, включающий в себя предоставление библиотеки соединений; испытание множества соединений из библиотеки на их способность ингибировать секрецию TNF- в жидкости организма in vivo и отбор по меньшей мере одного соединения из множества соединений, где выбранное соединение имеет ЕС 50 в области приблизительно от 1 до 1000 мкМ для ингибирования секреции TNFкультивируемыми клетками in vitro. Другим вариантом осуществления настоящего изобретения является способ идентификации фарма-1 015252 цевтически активного соединения, включающий в себя предоставление библиотеки соединений; испытание множества соединений из библиотеки на их способность ингибировать секрецию TNF- культивируемыми клетками in vitro и отбор по меньшей мере одного соединения из множества соединений, где выбранное соединение имеет ЕС 50 в области приблизительно от 1 мкМ до 1000 мкМ для ингибирования секреции TNF- в жидкости организма in vivo. Другим вариантом осуществления настоящего изобретения является соединение формулы класса где Ar является пиридинилом или фенилом; Z означает О или S; Х 3 означает Н, F, Cl, ОН, СН 3 или ОСН 3; R2 означает метил, С(=O)Н, С(=O)СН 3, С(=O)O-гликозил, фторметил, дифторметил, трифторметил, метилметоксил, метилгидроксил или фенил; и R4 означает Н или гидроксил; при условии, что когдаR2 является трифторметилом, Z означает О, R4 является Н и Ar означает фенил, причем фенил замещен в 4'-положения не только Н, F или ОН; где соединение имеет EC50 в области приблизительно от 1 до 1000 мкМ для ингибирования MAPK р 38; или фармацевтически приемлемая соль, сложный эфир, сольват или пролекарство указанного соединения. Другим вариантом осуществления настоящего изобретения является соединение формулы класса где Х 3 означает Н, галоген, C1-C10 алкокси или ОН; Y1,Y2, Y3 и Y4 независимо выбраны из группы,состоящей из Н, С 1-С 10-алкила, замещенного C1-С 10-алкила, C1-С 10-алкенила, C1-C10-галогеналкила, C1 С 10-нитроалкила, C1-С 10-тиоалкила, C1-C10-гидроксиалкила, C1-С 10-алкокси, фенила, замещенного фенила, галогена, гидроксила, С 1-С 10-алкоксиалкила, C1-С 10-карбокси, C1-С 10-алкоксикарбонила; R4 означает Н, галоген или ОН; и где соединение имеет ЕС 50 в области приблизительно от 1 мкМ до 1000 мкМ для ингибирования MAPK р 38; или фармацевтически приемлемая соль, сложный эфир, сольват или пролекарство указанного соединения. Дополнительным вариантом осуществления изобретения является фармацевтическая композиция,содержащая соединение формулы, как описано выше, и фармацевтически приемлемый наполнитель. Указанные и другие варианты осуществления изобретения описаны более подробно ниже. Краткое описание фигур Фиг. 1 представляет собой схематическое изображение каскада передачи сигнала MAPK р 38 (предыдущий уровень техники, фиг. 1 из публикации Underwood et al. 2001 Prog. Respir. Res. 31: 342-345). На схеме показана активация сигнального каскада р 38 под влиянием ряда стимулов и эффектов, расположенных ниже в каскаде реакций, активации р 38 на воспалительную реакцию через активацию транскрипции и трансляцию/мРНК стабилизацию. Фиг. 2 представляет собой график, показывающий частичное ингибирование р 38 различными метаболитами и аналогами пирфенидона как функцию от концентрации соединений. Концентрации ЕС 50 указанных соединений приведены над графиком. Подробное описание исследования можно найти в примере 5. Фиг. 3 представляет собой график, показывающий частичное ингибирование р 38 различными метаболитами и аналогами пирфенидона как функцию от концентрации соединений. Концентрации ЕС 50 указанных соединений приведены над графиком. Подробное описание исследования можно найти в примере 5. На фиг. 4 представлены биохимические данные для различных метаболитов и аналогов пирфенидона. Метаболиты и аналоги пирфенидона, упоминаемые на фиг. 2, 3, 5 и 6, представлены на фиг. 4 в виде структуры с замещениями. Результаты показывают влияние заместителей по трем положениям на концентрацию ЕС 50 для ингибирования р 38 и р 38. Фиг. 5 представляет собой график, показывающий частичную активность (высвобождение TNFиз макрофага в ответ на LPS) различных метаболитов и аналогов пирфенидона как функцию от концентрации каждого соединения. Подробное описание исследования можно найти в примере 5.-2 015252 Фиг. 6 представляет собой ряд гистограмм, показывающих цитотоксичность различных метаболитов и аналогов при различных концентрациях соединений. Цитотоксичность определяли с помощью измерения высвобождения LDH после инкубации клеток в присутствии соединения. Количество высвобожденной LDH приводят к количеству, высвобожденному при обработке тритоном Х-100 и отложенному на графике против концентрации соединения. Подробное описание предпочтительных вариантов осуществления изобретения В настоящее время показано, что терапевтический эффект в лечении различных расстройств, связанных с повышенной активностью р 38-киназы, может быть достигнут при использовании ингибирующего киназу р 38 соединения с относительно низкой потенциальной способностью. Поэтому в одном варианте осуществления изобретения предлагается способ модуляции стрессактивированной киназной (SAPK) системы путем взаимодействия соединения с митоген-активированной протеинкиназой (MAPK) р 38. Предпочтительное соединение имеет ЕС 50 в области приблизительно от 1 мкМ до 1000 мкМ, предпочтительно приблизительно от 50 мкМ до 650 мкМ для ингибирования по меньшей мере одной MAPK р 38. Концентрация, при которой соединение взаимодействует с MAPK р 38,обычно составляет менее чем ЕС 30 для ингибирования р 38 данным соединением. Предпочтительно концентрация является менее чем ЕС 20, даже более предпочтительно концентрация является менее чем ЕС 10."Митоген-активированные протеинкиназы (MAPK)" являются эволюционно консервативными сериновыми/треониновыми киназами, участвующими в регуляции многих клеточных процессов. Некоторые группы MAPK были идентифицированы в клетках млекопитающих, включая внеклеточную сигналрегулируемую киназу (ERK), р 38 и SAPK/JNK. Полагают, что MAPK активируются их специфическимиSAPK/JNK посредством SEK1 (также известной как MKK4) и MKK7 (SEK2). Указанные MAPKK также могут быть активированы различными MAPKK-киназами (MAPKKK), такими как Raf, MLK, MEKK1,TAK1 и ASK1. Полагают, что группа MAPK включает, по меньшей мере, двенадцать клонированных высоко консервативных, пролин-направленных сериновых-треониновых киназ, которые, будучи активированы клеточными стрессами (окислительный стресс, повреждение ДНК, тепловой или осмотический шок, ультрафиолетовое излучение, ишемия-реперфузия), экзогенными средствами (анизомицин, арсенит Na, липополисахарид, LPS) или провоспалительными цитокинами, TNF- и IL-1, могут фосфорилировать и активировать другие киназы или ядерные белки, такие как факторы транскрипции, либо в цитоплазме,либо в ядре (фиг. 1). Используемый в описании термин "MAPK р 38" относится к члену семейства стрессактивированных протеинкиназ, которое включает, по меньшей мере, 4 изоформы (, , , ), некоторые из них рассматриваются как важные факторы, участвующие в процессах, необходимых для воспалительного ответа и тканевого ремоделирования (Lee et al. 2000 Immunopharmacol. 47: 185-201). Преобладающие киназы в моноцитах и макрофагах, р 38 и р 38, по-видимому, более широко экспрессируются по сравнению с р 38 (скелетная мышца) или р 38 (яички, поджелудочная железа, простатическая железа,тонкая кишка и в слюнной, питуитарной и надпочечной железах). Изоформа р 38 экспрессируется в миофибробластах, которые имеют некоторые фенотипические аналогии с мышечными клетками, включая экспрессию альфа-актина гладких мышц. Ряд субстратов МАР-киназы р 38 был идентифицирован,включая другие киназы (MAPKAP К 2/3, PRAK, MNK 1/2, MSK1/RLPK, RSK-B), факторы транскрипции(ATF2/6, фактор усиления 2 миоцитов, ядерный фактор- транскрипции, CHOP/GADD153, Elk1 и SAP1A1) и белки цитозоля (статмин), многие из которых являются физиологически важными.Jiang, Y. et al., 1996 J. Biol. Chem. 271: 17920-17926, охарактеризовал p38P как белок, состоящий из 372 аминокислот, близко родственный белку р 38. Как р 38, так и р 38 активируются провоспалительными цитокинами и стрессом под влиянием факторов окружающей среды, р 38 р предпочтительно активируется МАР-киназой - киназой-6 (MKK6) и предпочтительно фосфорилирует активированный фактор 2 транскрипции (ATF-2). Исследователи Kumar, S. et al. 1997 Biochem. Biophys. Res. Comm. 235: 533-538 и Stein, B. et al. 1997 J. Biol. Chem. 272: 19509-19517 описали вторую изоформу р 38 р, р 38 Р 2, содержащую 364 аминокислоты, идентичные на 73% аминокислотам р 38. Полагают, что р 38 Р активируется провоспалительными цитокинами и стрессом под влиянием факторов окружающей среды, хотя вторая обнаруженная изоформа р 38, р 382, по-видимому, предпочтительно экспрессируется в центральной нервной системе (CNS), сердце и скелетной мышце по сравнению с более распространенной экспрессией р 38 в ткани. Кроме того, полагают, что активированный фактор-2 транскрипции (ATF-2) является лучшим субстратом для р 382, чем для р 38. Идентификация р 38 у была описана Li, Z. et al. 1996 Biochem. Biophys. Res. Comm. 228: 334-340, и идентификация р 385 была описана Wang, X. et al. 1997 J. Biol. Chem. 272: 23668-23674 и Kumar, S. et al. 1997 Biochem. Biophys. Res. Comm. 235: 533-538. Указанные две изоформы р 38 ( и ) образуют уникальную подгруппу семейства MAPK-киназ на основании характера их экспрессии в ткани, утилизации субстрата, ответа на прямые и непрямые стимулы и чувствительности к ингибиторам киназы. Исходя из консервативности первичной последовательности, р 38 и р 38 являются близко родственными, но отли-3 015252 чаются оти , которые являются более близко родственными друг с другом. Обычно путь МАР-киназы р 38 прямо или косвенно активируется рецепторами клеточной поверхности, такими как рецепторные тирозинспецифические киназы, хемокин или рецепторы, сопряженные сG-белками, которые активированы специфическим лигандом, например, цитокинами, хемокинами или липополисахаридом (LPS), связывающимся с родственным рецептором. Потом МАР-киназа р 38 активируется при фосфорилировании по специфическим остаткам треонина и тирозина. После активации МАРкиназа р 38 может фосфорилировать другие внутриклеточные белки, включающие протеинкиназы, и может быть перемещена к ядру клетки, где она фосфорилирует и активирует факторы транскрипции, приводя к экспрессии провоспалительные цитокины и другие белки, которые участвуют в воспалительном ответе, клеточной адгезии и протеолитической деградации. Например, в клетках миелоидного ряда, таких как макрофаги и моноциты, как IL-1, так и TNF- транскрибируются в ответ на активацию р 38. Последующая трансляция и секреция указанных и других цитокинов инициирует местный или системный воспалительный ответ в прилегающей ткани и через инфильтрацию лейкоцитов. Хотя данный ответ является обычной частью физиологических ответов на клеточный стресс, острый или хронический клеточный стресс приводит к избыточной, нерегулируемой или избыточной и нерегулируемой экспрессии провоспалительных цитокинов. Это, в свою очередь, приводит к повреждению ткани, часто сопровождающемуся болью и слабостью. В альвеолярных макрофагах ингибирование киназ р 38 ингибитором р 38, SB203580, уменьшает продукты цитокинового гена. Полагают, что воспалительные цитокины (TNF-, IFN-, IL-4, IL-5) и хемокины (IL-8, RANTES, эотаксин) проявляют способность к регуляции или поддержанию хронического воспаления дыхательных путей. Продукция и действие многих потенциальных медиаторов воспаления дыхательных путей, по-видимому, зависят от стресс-активированной МАР-киназной системы (SAPK) или каскада киназ р 38 (Underwood et al. 2001 Prog. Respir. Res. 31: 342-345). Активация пути киназы р 38 многочисленными стимулирующими факторами окружающей среды приводит к выработке идентифицированных медиаторов воспаления, чья продукция, с точки зрения трансляции, рассматривается как регулируемая. Кроме того, ряд медиаторов воспаления активируют MAPK р 38, которые затем могут активировать последующие мишени MAPK-системы, включающие другие киназы или факторы транскрипции,таким образом, создавая потенциал для усиления воспалительного процесса в легком. Нисходящие [в каскаде реакций] субстраты группы MAP-киназ р 38 Протеинкиназные субстраты р 38 или р 38: активированная МАР-киназой протеинкиназа 2(MAPKAPK2 или М 2), протеинкиназа, взаимосвязанная с МАР-киназой (MNK1), р 38 регулируемая/активированная киназа (PRAK), митоген- и стресс-активированная киназа (MSK:RSK-B или RLPK). Факторы транскрипции, активированные р 38: фактор активации транскрипции (ATF)-1, 2 и 6, SRF добавочный белок 1 (Sap 1), CHOP (ген 153, который индуцируется остановкой роста и повреждением ДНК, или GADD153), р 53, C/EBP, фактор усиления миоцитов 2 С (MEF2C), MEF2A, MITF1, DDIT3,ELK1, NFAT, и высокомобильный групповой белок group-box (HBP1). Другие типы субстратов для р 38: cPLA2, изоформа-2 антипортера Na+/H+, тау, кератин 8 и статмин. Гены, регулируемые [сигнальным] путем р 38: c-jun, c-fos, junB, IL-1, TNF, IL-6, IL-8, MCP-1,VCAM-1, iNOS, PPAR, циклооксигеназа (СОХ)-2, коллагеназа-1 (ММР-1), коллагеназа-3 (ММР-13),HIV-LTR, Fgl-2, натрийуретический пептид мозга (BNP), CD23, CCK, фосфоенолпируват-карбоксикиназа цитозоля, циклин D1, LDL рецептор (Ono et al. 2000 Cellular signaling 12: 1-13). Биологические последствия активации р 38 Р 38 и воспаление Полагают, что острое и хроническое воспаление является центральной стадией в патогенезе многих заболеваний, таких как ревматоидный артрит, астма, хроническая обструктивная болезнь легких (COPD) и острый респираторный дистресс-синдром (ARDS). Активация каскада реакций р 38 может играть центральную роль в (1) продуцировании провоспалительных цитокинов, таких как IL-1, TNF- и IL-6; (2) индукции ферментов, таких как СОХ-2, которая контролирует тканевое ремоделирование при патологическом состоянии; (3) экспрессии внутриклеточного фермента, такого как iNOS, который регулирует окисление; (4) индукции адгезивных белков, таких как VCAM-1, и многих других связанных с воспалением молекул. Кроме указанных реакций, путь р 38 может играть регуляторную роль в пролиферации и дифференцировке клеток иммунной системы. Киназа р 38 может принимать участие в клеточной пролиферации и/или дифференцировке, индуцированной GM-CSF, CSF, ЕРО и CD40. Роль сигнального пути р 38-киназы в заболеваниях, связанных с воспалением, изучали на некоторых моделях животных. Ингибирование р 38 ингибитором SB203580 снижает смертность у модели мыши при вызванном эндотоксином шоке и тормозит развитие коллаген-индуцированного артрита у мыши и адъювантного артрита у крысы. Результаты недавнего исследования показали, что ингибитор SB220025, который является наиболее мощным ингибитором р 38, вызывает существенное дозозависимое заболевание в толще сосудов гранулемы. Полученные результаты указывают на то, что р 38 или компоненты пути р 38 могут служить терапевтической мишенью для воспалительного заболевания.-4 015252 р 38 и апоптоз По-видимому, сосуществующая активация р 38 и апоптоз индуцируется рядом средств, таких как удаление NGF и лигатирование Fas. Цистеиновые протеиназы (каспазы) являются центральными ферментами на пути апоптоза и экспрессируются в виде неактивных зимогенов. Затем ингибиторы каспаз могут блокировать активацию р 38 посредством поперечного связывания Fas. Однако повышенная экспрессия преобладающей активной МКК 6b также может индуцировать каспазную активность и гибель клетки. Роль р 38 в апоптозе является зависимой от типа клетки и раздражителя. Как было показано, в то время как передача сигнала, осуществляемая р 38, стимулирует гибель клетки в некоторых линиях клеток, в других линиях клеток р 38 повышает выживаемость, рост клеток и дифференцировку. р 38 в клеточном цикле Повышенная экспрессия р 38 а в дрожжах приводит к замедлению пролиферации, что указывает на вовлечение р 38 в рост клеток. Замедление пролиферации культивируемых клеток млекопитающих наблюдали, когда клетки обрабатывали ингибитором р 38/, SB203580. р 38 и гипертрофия кардиомиоцитов Активацию и функцию р 38 при гипертрофии кардиомиоцитов изучали. В процессе развития гипертрофии уровни как р 38 а, так и р 38 увеличиваются и конститутивно проявляющиеся гипертрофические реакции, вызванные МКК 3 и МКК 6, усиливаются при формировании саркомера и повышается экспрессия предсердного натрийуретического фактора. Также ослабление процессов передачи сигнала в сердце,осуществляемой р 38, стимулирует дифференцировку миоцитов посредством механизма, вовлекающего кальциневрин-NFAT-зависимый путь. р 38 и развитие Несмотря на нежизнеспособность р 38-нокаутированных мышей, существует доказательство в пользу характерной роли р 38 в развитии. В некоторых исследованиях было показано, что р 38 киназа связана с ангиогенезом плаценты, но не с развитием сосудистой системы сердца. Кроме того, р 38 также связана с экспрессией эритропоэтина, что предполагает роль в эритропоэзе. Недавно было показано, что PRAK участвует в процессах развития клетки при имплантации у мыши. Было обнаружено, что мРНК PRAK, а также изоформы р 38 экспрессируются на всем протяжении развития бластоцисты. р 38 и клеточная дифференцировка Было обнаружено, что р 38 а и/или р 38 играют важную роль в клеточной дифференцировке некоторых различных типов клеток. Дифференцировка клеток 3T3-L1 в адипоциты и дифференцировка РС 12 клеток в нейроны требует участия р 38 и/или . Как было найдено, путь р 38 является необходимым и достаточным для дифференцировки SKT6-клеток в клетки, содержащие гемоглобин, а также для дифференцировки С 2 С 112-клеток в мышечные трубочки. р 38 при физиологическом старении и опухолевой супрессии Киназа р 38 играет роль в онкогенезе и физиологическом старении. Было показано, что активация МКК 6 и МКК 3 приводит к стареющему фенотипу в зависимости от активности MAPK р 38. Также было показано, что активность MAPK р 38 ответственна за старение в ответ на укорачивание теломера, воздействие H2O2 и длительный сигнальный путь RAS-онкогена. Общая черта опухолевых клеток заключается в потере физиологического старения, и р 38 связана с онкогенезом в определенных клетках. Было показано, что активация р 38 снижается в опухолях и что потеря компонентов сигнального пути р 38, таких как МКК 3 и МКК 6, приводит к повышению пролиферации и вероятности туморогенного перехода независимо от клеточной линии или индуцирующего опухоль агента, используемого в данных исследованиях. Ингибиторы МАР-киназы р 38"Ингибитор МАР-киназы р 38" является соединением, которое ингибирует активность р 38. Ингибирующее действие соединения на активность р 38 можно измерить различными способами, хорошо известными специалистам в данной области. Например, ингибирующее действие можно оценить путем измерения уровня ингибирования продуцирования цитокинов, стимулированного липополисахаридомLee et al. 1994 Nature 372: 739-746; Lee et al. 1999 Pharmacol. Ther. 82: 389-397). Усилия исследователей, занимающихся разработкой ингибиторов MAPK р 38, были направлены на повышение их потенциальной способности. Было обнаружено, что SB203580 и другие 2, 4, 5 триарилимидазолы являются эффективными ингибиторами р 38-киназы с величинами ЕС 50 в наномолярной области. Например, обнаруженная для ингибитора SB203580 величина ЕС 50 составляет 48 нМ. Пиридинилимидазолы SKF 86002 (Р 1) и SB203582 (Р 2), представленные ниже, были использованы в качестве образца для большинства ингибиторов р 38. Недавние публикации (Lee et al. 2000 Immunopharmacology 47: 185-201) описывают ингибиторы р 38 (Р 3-Р 6), представленные ниже. Заметными среди указанных ингибиторов являются относительно высокая потенциальная способность и избирательность, описанные для соединения Р 4 (р 38 ЕС 50=0,19 нМ), и ингибирование воспаления посредством SB220025 (Р 6), стимулированного ангиогенезом. Два ингибитора р 38, как было показано, находящиеся в стадии клинической разработки, представ-5 015252 ляют собой НЕР 689 (Р 7) и VX-745 (P8). Ингибитор VX-745, как указывают, находится в фазе II испытаний относительно ревматоидного артрита. Эффективная местная противовоспалительная активность была обнаружена для HRP689, который внедрен в клиническую разработку для исследования его способности в качестве местного средства для лечения псориаза и других кожных заболеваний. Дополнительное обсуждение различных ингибиторов р 38 можно найти в публикациях Boehm et al. 2000 Exp. Opin. Ther. Pat. 10: 25-37; Salituro et al. 1999 Curr. Med. Chem. 6: 807-823. Предпочтительными ингибиторами р 38, описанными в изобретении, являются производные и аналоги пирфенидона, которые проявляют относительно низкую способность к ингибированию р 38, хотя и удивительно, все же имеющие относительно высокий терапевтический эффект (например, для модулирования SAPK-системы) в результате такого ингибирования. Предпочтительно, ингибиторы р 38 вариантов осуществления изобретения проявляют ЕС 50 В области приблизительно от 1 мкМ до 1000 мкМ, предпочтительно приблизительно от 50 мкМ до 650 мкМ для ингибирования MAPK р 38. Производные и аналоги пирфенидона Пирфенидон (5-метил-1-фенил-2-(1 Н)пиридон) сам по себе является известным соединением, и его фармакологические эффекты описаны, например, в патентной заявке Японии KOKAI (Laid-Open) No. 87677/1974 и 1284338/1976. Патент США No. 3839346, выданный 1 октября 1974; патент США No. 3974281, выданный 10 августа 1976; патент США No. 4042699, выданный 16 августа 1977; и патент СШАNo. 4052509, выданный 4 октября 1977, все из которых включены в описание посредством ссылки во всей полноте, описывают способы производства 5-метил-1-фенил-2-(1 Н)пиридона и его использование в качестве противовоспалительного средства. Пирфенидон и его производные являются полезными соединениями для модуляции системы стресс-активированных протеинкиназ (SAPK). Термин "алкил", употребляемый в описании, относится к моновалентному радикалу с прямой или разветвленной цепью, состоящему из одного-десяти атомов углерода, который включает, но не ограничивается ими, метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, н-гексил и тому подобное. Термин "алкенил", употребляемый в описании, относится к моновалентному радикалу с прямой или разветвленной цепью, состоящему из двух-десяти атомов углерода, содержащему углеродную двойную связь, который включает, но не ограничивается ими, 1-пропенил, 2-пропенил, 2-метил-1-пропенил, 1 бутенил, 2-бутенил и тому подобное. Термин "галоген", употребляемый в описании, относится к фтору, хлору, брому или йоду. Термин "галогеналкил", употребляемый в описании, относится к одной или более галогеновым группам, присоединенным к алкильному радикалу. Термин "нитроалкил", употребляемый в описании, относится к одной или более нитрогруппам,-6 015252 присоединенным к алкильному радикалу. Термин "тиоалкил", употребляемый в описании, относится к одной или более тиогруппам, присоединенным к алкильному радикалу. Термин "гидроксиалкил", употребляемый в описании, относится к одной или более гидроксигруппам, присоединенным к алкильному радикалу. Термин "алкокси", употребляемый в описании, относится к алкильному радикалу с прямой или разветвленной цепью, ковалентно связанному с материнской молекулой через -О-связь. Примеры алкоксигрупп включают, но не ограничиваются ими, метокси, этокси, пропокси, изопропокси, бутокси, н-бутокси,втор-бутокси, трет-бутокси и тому подобное. Термин "алкоксиалкил", употребляемый в описании, относится к одной или более алкоксигруппам,присоединенным к алкильному радикалу. Термин "карбокси", употребляемый в описании, относится к группе -СООН, необязательно присоединенной к алкильному радикалу. Примеры карбоксигрупп включают, но не ограничиваются ими, СООН, -СН 2 СООН, -СН 2 СН 2 СООН, -СН(СООН) (СН 3) и тому подобное. Термин "алкоксикарбонил" относится к -(СО)-О-алкилу. Примеры алкоксикарбонила включают, но не ограничиваются ими, метоксикарбонильную группу, этоксикарбонильную группу, пропоксикарбонильную группу и тому подобное. Углеводы являются полигидроксиальдегидами или кетонами или веществами, которые образуют такие соединения при гидролизе. Углеводы включают элементы углерод (С), водород (Н) и кислород (О) при соотношении, составляющем водорода в два раза больше, чем углерода и кислорода. В их основной форме углеводы являются простыми сахарами или моносахаридами. Данные простые сахара можно комбинировать друг с другом с образованием более сложных углеводов. Комбинацией двух простых сахаров является дисахарид. Углеводы, состоящие из двух-десяти простых сахаров, называют олигосахаридами, и углеводы с большим числом простых сахаров называют полисахаридами. Термин "уронид" относится к моносахариду, имеющему карбоксильную группу (-СООН) у углерода, который не является частью кольца. Название уронид сохраняет основу моносахарида, но суффикс-оза сахара изменяется на -уронид. Например, структура глюкуронида соответствует глюкозе. Как используют в описании, радикал указывает на виды с единственным, неспаренным электроном,так что содержащие радикал виды могут быть ковалентно связаны с другими видами. Поэтому в данном контексте радикал является необязательно свободным радикалом. Скорее радикал указывает на отдельную часть большей молекулы. Термин "радикал" может быть использован взаимозаменяемо с термином"группа". Как используют в описании, замещенная группа производится из незамещенной родительской структуры, в которой произведен обмен одного или более атомов водорода на другой атом или группу. При замещении заместительная группа(ы) является(ются) одной группой или более группами, индивидуально и независимо выбранными из C1-С 10-алкила, C1-С 10-циклоалкила, арила, конденсированного арила,гетероциклила, гетероарила, гидрокси, C1-С 10-алкокси, арилокси, меркапто, C1-С 10-алкилтио, арилтио,циано, галогена, карбонила, тиокарбонила, C1-C10-алкоксикарбонила, нитро, силила, тригалогенметансульфонила, трифторметила и амино, включая моно- и дизамещенные аминогруппы, и из защищенных производных. Защитные группы, которые могут образовывать защищенные производные вышеуказанных заместителей, известны специалистам в данной области и могут быть найдены в ссылках, таких какGreene and Wuts Protective Groups in Organic Synthesis; John Wiley and Sons: New York, 1999. Где бы ни был заместитель описан как "необязательно замещенный", такой заместитель может быть замещен вышеуказанными заместителями. Термин "очищенное" относится к соединению, которое отделили от других соединений, так что оно содержит, по меньшей мере, 95% измеренного вещества при его анализе. Асимметричные атомы углерода могут быть представлены в соединениях, описанных в изобретении. Все такие изомеры, включающие диастереомеры и энантиомеры, а также их смеси, предназначены быть включенными в сферу указанного соединения. В некоторых случаях соединения могут существовать в таутомерных формах. Все таутомерные формы предназначены быть включенными в сферу указанного соединения. Также, когда соединение содержит алкенильную или алкениленовую группу, существует возможность существования цис- и транс-изомерных форм соединений. Как цис-, так и трансизомеры, а также смеси цис- и транс-изомеров рассматриваются. Таким образом, ссылка в описании на соединение включает все из вышеупомянутых изомерных форм, если в контексте не указано иное. Различные формы включены в варианты осуществления изобретения, включающие полиморфы,сольваты, гидраты, конформеры, соли и производные пролекарства. Полиморф является композицией,имеющей такую же химическую формулу, но отличную структуру. Сольват является композицией, образованной при сольватации (комбинация молекул растворителя с молекулами или ионами растворенного вещества). Гидрат является соединением, образованным при включении воды. Конформер представляет собой структуру, которая является конформационным изомером. Конформационный изомеризм является феноменом молекул с одинаковой структурной формулой,-7 015252 но с различными конформациями (конформеры) атомов в результате их вращения вокруг связи. Соли соединений могут быть получены способами, известными специалистам в данной области. Например,соли соединений могут быть получены при взаимодействии соответствующего основания или кислоты со стехиометрическим эквивалентом соединения. Пролекарство является соединением, которое подвергается биотрансформации (химическое превращение) до появления фармакологических эффектов. Например, пролекарство можно рассматривать как лекарственное средство, содержащее специализированные защитные группы, используемые в переходном состоянии для изменения или исключения нежелательных свойств, присущих родительской молекуле. Таким образом, ссылка в описании на соединение включает все из вышеупомянутых форм, если в контексте не указано иное. Описанные ниже соединения используют в способах, представленных в описании. В варианте осуществления изобретения описанное ниже соединение имеет ЕС 50 в области приблизительно от 1 мкМ до 1000 мкМ для ингибирования MAPK р 38. Вариант осуществления изобретения относится к группе соединений, представленных следующим классом (класс Ia): где R1, R2, R3 и R4 независимо выбраны из группы, состоящей из Н, C1-С 10-алкила, замещенного C1 С 10-алкила, C1-С 10-алкенила, С 1-С 10-галогеналкила, С 1-С 10-нитроалкила, C1-С 10-тиоалкила, C1-С 10 гидроксиалкила, C1-С 10-алкокси, фенила, замещенного фенила, галогена, гидроксила, С 1-С 10 алкоксиалкила, C1-С 10-карбокси, C1-С 10-алкоксикарбонила, СО-уронида, СО-моносахарида, COолигосахарида и СО-полисахарида; иX1, Х 2, Х 3, Х 4 и Х 5 независимо выбраны из группы, состоящей из Н, галогена, C1-С 10-алкокси и гидрокси. Другой вариант осуществления изобретения относится к группе соединений, представленных следующим классом (класс Ib):R4 выбран из группы, состоящей из Н, галогена и ОН,В другом варианте осуществления изобретения предлагается группа соединений, представленных следующим классом (класс Ic):R4 выбран из группы, состоящей из Н и ОН; при условии, что когда R4 и Х 3 являются Н, R2 не является СН 3. Другой вариант осуществления изобретения относится к группе соединений, представленных следующим подклассом (подкласс II):R4 выбран из группы, состоящей из Н и ОН, при условии, что когда Х 3 является ОН, тогда R2 не является СН 3. Другой вариант осуществления изобретения относится к группе соединений, представленных следующим подклассом (подкласс III):R2 выбран из группы, состоящей из Н, Br, CH2F, CHF2 и CF3. Другой вариант осуществления изобретения относится к группе соединений, представленных следующим подклассом (подкласс IV): где Х 3 выбран из группы, состоящей из Н, галогена, С 1-С 10-алкокси, ОН, C1-С 10-алкила, замещенного Сх-С 10-алкила, C1-C10-алкенила, С 1-С 10-галогеналкила, C1-С 10-нитроалкила, C1-С 10-тиоалкила, С 1-С 10 гидроксиалкила, фенила, замещенного фенила, С 1-С 10-алкоксиалкила, С 1-С 10-карбокси, С 1-С 10 алкоксикарбонила, СО-уронида, СО-моносахарида, СО-олигосахарида и СО-полисахарида. Другой вариант осуществления изобретения относится к группе соединений, представленных следующим подклассом (подкласс V): где Х 3 выбран из группы, состоящей из Н, галогена, С 1-С 10-алкокси, С 1-С 10-алкила, замещенного С 1 С 10-алкила, С 1-С 10-алкенила, С 1-С 10-галогеналкила, С 1-С 10-нитроалкила, С 1-С 10-тиоалкила, С 1-С 10 гидроксиалкила, фенила, замещенного фенила, С 1-С 10 алкоксиалкила, С 1-С 10-карбокси, С 1-С 10 алкоксикарбонила, СО-уронида, СО-моносахарида, СО-олигосахарида и СО-полисахарида. Другой вариант осуществления изобретения относится к группе соединений, представленных следующим классом (класс VI): где Ar является пиридинилом или фенилом;R2 означает метил, С(=O)Н, С(=O)СН 3, С(=O)ОСН 3, С (=O)O-глюкозил, фторметил, дифторметил,трифторметил, бром, метилметоксил, метилгидроксил или фенил иR4 означает Н или гидроксил,при условии, что когда R2 означает трифторметил, Z является О, R4 является Н и Ar означает фенил,причем фенил является замещенным в 4'-положении не только Н, F или ОН. Класс VI включает группы соединений, представленных подклассом VIa и подклассом VIb: где Z, X3, R2 и R4 определены, как в классе VI. Следует отметить, что фенильное кольцо в структуре, представленной подклассом VIa, замещено Х 3 в 4'-положении. Другой вариант осуществления изобретения относится к группе соединений, представленных следующим классом (класс VII)Y1, Y2, Y3 и Y4 независимо выбраны из группы, состоящей из Н, С 1-С 10-алкила, замещенного С 1-С 10 алкила, C1-С 10-алкенила, С 1-С 10-галогеналкила, C1-С 10-нитроалкила, С 1-С 10-тиоалкила, С 1-С 10-гидроксиалкила, С 1-С 10-алкокси, фенила, замещенного фенила, галогена, гидроксила, С 1-С 10-алкоксиалкила,С 1-С 10-карбокси, С 1-С 10-алкоксикарбонила, иR4 выбран из группы, состоящей из Н, галогена и ОН. Следует признать, что отдельное соединение, приведенное в описании, может быть членом более чем одной группы из различных групп, описанных выше. Соединения, приведенные в описании, применимы для модуляции системы протеинкиназ, активированной стрессом (SAPK). Характерные соединения классов Ia-с, подклассов II-V и классов VI и VII, которые применимы для модуляции системы протеинкиназ, активированной стрессом (SAPK), представлены в таблице 1 ниже. Соединения 1-6 являются примерами соединений подкласса II. Соединения 7-12 являются примерами соединений подкласса III. Соединение 13 является пирфенидоном, примером соединения подкласса II. Соединения 14-32 являются примерами соединений класса VI. Соединение 33 является примером класса VII. Таблица 1- 13015252 Другой вариант осуществления изобретения направлен на очищенные соединения, представленные классами Ia-с, подклассами II-V и/или классами VI и VII. Степень чистоты может быть выражена в процентах, как описано выше. В предпочтительных вариантах осуществления изобретения очищенные соединения, представленные классами Ia-с, подклассами II-V и/или классами VI и VII, имеют чистоту приблизительно 96 мас.% или выше, более предпочтительно приблизительно 98% или выше на основании общей массы композиции, которая содержит очищенное соединение. Например, вариант осуществления изобретения относится к очищенному соединению 3 (табл. 1). Соединения классов Ia-с, подклассов II-V и/или классов VI и VII могут быть синтезированы с помощью различных реакций. Примеры синтеза включают следующие указанные схемы синтеза 1, 2 и 3. Схема синтеза 1 Реакция Ульмана: Chera. Pharm. Bull. 45(4) 719-721. Заданные N-арилпиридин-2-оны получают посредством арилирования 2-гидроксипиридинов. Реакцию Ульмана применяют при получении описанных соединений, за исключением 5-броманалогов и соединения 33, которые получают, например, с помощью схемы синтеза 3. Смесь 2-гидроксипиридина (1 ммоль), арилйодида или бромида (2 ммоль), CuI (0,1-0,5 ммоль) и безводного карбоната калия (1 ммоль) в ДМФА (3 мл) перемешивают в течение ночи при 135 С в атмосфере аргона. Темноокрашенную реакционную смесь поглощают этилацетатом и 10% гидроксидом аммония. Органический слой промывают насыщенным раствором соли и сушат над сульфатом магния. Колоночной хроматографией получают заданные соединения в виде твердых веществ не совсем белого цвета с выходом 25-60%. Заданные N-арил-2-пиридоны могут быть получены путем арилирования 2-гидроксипиридинов алкилбороновыми кислотами (Tetrahedron Lett., 42 (2001) 3415-3418). В получении описанных соединений используют способ с применением арилбороновых кислот. Смесь 2-гидроксипиридина (5 ммоль), арилбороновой кислоты (10 ммоль), ацетата меди(II) (0,5-1 ммоль), пиридина (10 ммоль) и молекулярных сит 4 (0,5-1 г) в дихлорметане (25 мл) перемешивают в течение 24-48 ч при комнатной температуре на открытом воздухе. Реакционную смесь промывают насыщенным раствором бикарбоната натрия с ЭДТА и органическую фазу сушат над сульфатом натрия. Заданные N-арил-2-пиридоны выделяют колоночной хроматографией в виде твердых веществ белого цвета с выходом 85-100%. В качестве производных пирфенидона соединения классов Ia-с, подклассов II-V и/или классов VI иVII также могут быть синтезированы любыми стандартными реакциями, известными в данной области,основанными на известных схемах синтеза пирфенидона, таких как описанные схемы синтеза в патентах США No. 3839346; 3974281; 4042699 и 4052509, все из которых точно включены в описание посредством ссылки во всей полноте. Исходные материалы, указанные в описании, являются коммерчески доступными, известными или могут быть получены способами, известными в данной области. Кроме того, исходные материалы, не указанные в описании, являются коммерчески доступными, известными или могут быть получены способами, известными в данной области. Исходные материалы могут иметь соответствующие заместители, чтобы, в конечном счете, получались желаемые продукты с соответствующими заместителями. В качестве альтернативы заместители могут быть добавлены в любой момент синтеза, чтобы, в конечном счете, получались желаемые продукты с соответствующими заместителями. Схемы синтеза 1-3 указывают на способы, которые могут быть использованы для получения соединений классов Ia-с, подклассов II-V и/или классов VI и VII. Специалист в данной области должен признать, что ряд различных схем реакций синтеза можно использовать для синтеза соединений классов Ia-с,подклассов II-V и/или классов VI и VII. Кроме того, специалист в данной области оценит, что ряд различных растворителей, связующих агентов и условий реакции можно использовать в реакциях синтеза для достижения сравнимых результатов. Специалисту в данной области следует принять во внимание, что отклонения в последовательности и, кроме того, отклонения в соответствующих условиях реакций от аналогичных реакций, установленных или иным образом известных, могут быть соответственно использованы в способах, описанных выше, для получения соединений классов Ia-с, подклассов II-V и/или классов VI и VII. В указанных в описании способах получения соединений классов Ia-с, подклассов II-V и/или классов VI и VII применение защитных групп обычно оценивает специалист в области органической химии,и, следовательно, использование соответствующих защитных групп в некоторых случаях можно предположить в способах, указанных на схемах, хотя такие группы могут и не быть точно иллюстрированы. Введение и удаление таких соответствующих защитных групп хорошо известно в области органической химии; см., например, T.W. Greene, "Protective Groups in Organic Synthesis", Wiley (New York), 1999. Продукты реакций, указанные в описании, могут быть выделены обычными способами, такими как экстракция, дистилляция, хроматография и тому подобное. Соли, например фармацевтически приемлемые соли, соединений классов Ia-с, подклассов II-V и/или классов VI и VII могут быть получены путем взаимодействия соответствующего основания или кислоты со стехиометрическим эквивалентом соединений. Аналогично, фармацевтически приемлемые производные (например, сложные эфиры), метаболиты,гидраты, сольваты и пролекарства соединений классов Ia-с, подклассов II-V и/или классов VI и VII могут быть получены способами, как правило, известными специалистам в данной области. Таким образом,другой вариант осуществления изобретения относится к соединениям, которые являются пролекарствами активного соединения. Вообще, пролекарство является соединением, которое метаболизирует in vivo(например, метаболическое превращение, такое как дезаминирование, деалкилирование, деэтерификация и тому подобное) с образованием активного соединения. "Фармацевтически приемлемое пролекарство" означает соединение, которое, в рамках тщательного медицинского обследования, является подходящим для фармацевтического использования больным без чрезмерной токсичности, раздражения, аллергической реакции, и тому подобного, и эффективным для использования по назначению, включающее фармацевтически приемлемый сложный эфир, а также цвиттерионную форму, где возможно, соединений- 15015252 согласно вариантам осуществления изобретения. Примеры фармацевтически приемлемых пролекарственных средств описаны в публикациях Т. Higuchi and V. Stella, Pro-drugs as Novel Delivery System, Vol. 14 of the A.C.S. Symposium Series, и у Edward В. Roche, ed., Bioreversible Carriers in Drug Design, AmericanPharmaceutical Association and Pergamon Press, 1987, которые включены в описание посредством ссылки во всей полноте. Соединения и композиции, приведенные в описании, также могут включать метаболиты. Употребляемый в описании термин "метаболит" означает продукт метаболизма соединения согласно вариантам осуществления изобретения или фармацевтически приемлемой соли, аналога или производного соединения, который проявляет активность in vitro или in vivo, подобную активности соединения согласно вариантам осуществления изобретения. Соединения и композиции, приведенные в описании, также могут включать гидраты и сольваты. Употребляемый в описании термин "сольват" относится к комплексу, образованному растворенным веществом (в данном описании соединение классов Ia-с, подклассов II-V и/или классов VI и VII) и растворителем. В описании вариантов осуществления изобретения такие растворители не должны влиять на биологическую активность растворенного вещества. Растворителями могут быть, в качестве примера, вода, этанол или уксусная кислота. Принимая во внимание вышеизложенное, следует признать, что ссылка в описании на отдельное соединение или класс соединений включает различные виды, описанные выше, включая фармацевтически приемлемые соли, сложные эфиры,пролекарства, метаболиты и сольваты соединения, если не указано иное. Способы ингибирования МАР-киназы р 38 В варианте осуществления изобретения способы предназначены для модуляции SAPK-системы invitro или in vivo. Способы включают взаимодействие соединения при SAPK-модулирующей концентрации, по меньшей мере, с одной MAPK р 38 (например, путем контакта соединения с клеткой или тканью,содержащей, по меньшей мере, одну MAPK р 38), где соединение обладает относительно низкой способностью к ингибированию по крайней мере одной MAPK р 38 при относительно высокой концентрации соединения, ингибирующего по крайней мере одну MAPK р 38."Осуществление контакта с клеткой" относится к условию, при котором соединение или другая композиция, относящаяся к теме, находится в прямом контакте с клеткой или тканью, или достаточно близко расположена, чтобы индуцировать желаемый биологический эффект в клетке или ткани. Например, контакт клетки или ткани, содержащей MAPK р 38, с соединением может быть осуществлен любым способом, который допускает взаимодействие между MAPK р 38 и соединением, приводящее к желаемому биологическому эффекту в клетке. Контакт клетки или ткани может осуществляться, например, путем перемешивания с соединением или путем введения соединения (такого как соединение классов Ia-с, подклассов II-V и/или классов VI и VII и/или соль, сложный эфир, пролекарство и/или его промежуточный продукт, и/или фармацевтическая композиция, содержащая одно или более вышеуказанных соединений). В качестве альтернативы контакт с клеткой или тканью может осуществляться путем внесения соединения таким образом, что соединение должно быть направлено, прямо или косвенно, к клетке или ткани, содержащей MAPK р 38. Контакт с клеткой или тканью может быть осуществлен при таких условиях, что соединение связывается по меньшей мере с одной MAPK р 38. Такие условия могут включать близость соединения и р 38-содержащей клетки или ткани, рН, температуру или любое условие, которое влияет на связывание соединения с MAPK р 38. В некоторых вариантах осуществления изобретения клетка контактирует с соединением in vitro; в других вариантах осуществления изобретения клетка контактирует с соединением in vivo. В случаях, когда клетка контактирует in vivo, эффективная концентрация (ЕС) соединения является концентрацией, которая приводит к снижению определенной конечной точки на заданный процент (например, 50, 40, 30, 20, 10%) относительно максимального наблюдаемого снижения определенной конечной точки под действием данного соединения. Такой конечной точкой может быть физиологический ответ, например уменьшение концентрации TNF- в крови или другой жидкости организма. Например,ЕС 50, ЕС 40, ЕС 30, ЕС 20 и ЕС 10 определяют как концентрации, которые приводят к уменьшениям концентрации TNF- в сыворотке на 50, 40, 30, 20 и 10%, соответственно, относительно максимального наблюдаемого уменьшения на кривой зависимости доза-эффект. В случае, когда клетка контактирует in vitro, за исключением анализа, основанного на клетках, эффективная концентрация (ЕС) является концентрацией, которая приводит к снижению активности определенной мишени на заданный процент (например, 50, 40, 30, 20 и 10%). Например, ЕС 50, ЕС 40, ЕС 30,ЕС 20 и ЕС 10 определяют как концентрации, которые приводят к снижению активности определенной мишени на 50, 40, 30, 20 и 10%, соответственно, на основании кривой зависимости доза-эффект. В случае,когда полного ингибирования активности определенной мишени не получают, эффективная концентрация (ЕС) соединения является концентрацией, которая приводит к снижению активности мишени на заданный процент (например, 50, 40, 30, 20 и 10%) относительно максимального снижения активности мишени под действием данного соединения. В случае, когда клетка контактирует in vitro в исследовании, основанном на клетках, эффективная концентрация (ЕС) соединения является концентрацией, которая приводит к снижению определенной- 16015252 конечной точки на заданный процент (например, 50, 40, 30, 20 и 10%) относительно максимального наблюдаемого снижения определенной конечной точки под действием данного соединения. Такой конечной точкой может быть клеточный ответ, например снижение секреции TNF-a, как установлено путем определения концентрации TNF- в клеточной среде. Например, ЕС 50, ЕС 40, ЕС 30, ЕС 20 И И ЕС 10 определяют как концентрации, которые приводят к снижению концентрации TNF- на 50, 40, 30, 20 и 10%, соответственно, относительно максимального наблюдаемого снижения на кривой зависимости дозаэффект. ЕС 50 соединения, модулирующего SAPK-систему, предпочтительно находится в области приблизительно от 1 до 1000 мкМ, более предпочтительно приблизительно от 50 до 650 мкМ для ингибирования,по меньшей мере одной MAPK р 38. Таким образом, например, модуляция SAPK-системы может включать взаимодействие соединения (например, соединение классов Ia-c, подклассов II-V и/или классов VI иVII), по меньшей мере с одной MAPK р 38 при концентрации, которая составляет менее чем ЕС 40, предпочтительно менее чем ЕС 30, более предпочтительно менее чем ЕС 20, наиболее предпочтительно менее чем ЕС 10 для ингибирования соединением по меньшей мере одной MAPK р 38, как установлено с помощью кривой зависимости доза-эффект in vivo. В некоторых вариантах осуществления изобретения соединение находится в виде фармацевтической композиции вместе с фармацевтически приемлемым носителем. Проверка библиотеки соединений для низкопотенциальных ингибиторов р 38 В другом аспекте способ относится к идентификации фармацевтически активного соединения, например, для установления возможности использования соединения в качестве терапевтического средства, например, для предотвращения или лечения воспалительного состояния (такого состояния, которое связано с р 38 или цитокинами). Способ включает в себя исследование множества соединений на предмет ингибирования по меньшей мере одной MAPK р 38 и отбор соединения, которое проявляет относительно низкую способность к ингибированию MAPK р 38. Предпочтительно, ЕС 50 такого низкопотенциального ингибирующего р 38-киназу соединения находится в области приблизительно от 1 мкМ до 1000 мкМ,предпочтительно приблизительно от 50 до 650 мкМ для ингибирования по меньшей мере одной MAPK р 38. Множество соединений, которые требуется анализировать, предпочтительно выбирают из библиотеки потенциальных соединений. Исследование множества соединений из библиотеки может осуществляться различными путями. Например, в некоторых вариантах осуществления изобретения способы также включают взаимодействие по меньшей мере одной MAPK р 38 с множеством соединений и установление возможности ингибирования соединением активности цитокинов. MAPK р 38 предпочтительно выбирают из группы, состоящей из р 38 а, р 38, р 38 и р 38. В предпочтительных вариантах осуществления изобретения стадия взаимодействия имеет место in vitro; в некоторых предпочтительных вариантах осуществления изобретения стадия взаимодействия заключает в себе контакт клетки, содержащей MAPK р 38, с соединением. В другом варианте осуществления изобретения способы относятся к ингибированию активностиMAPK р 38 в клетке, in vitro или in vivo. Вообще, такие способы заключаются в контакте клетки, содержащей, по меньшей мере, одну MAPK р 38, с эффективным р 38-ингибирующим количеством соединения(например, соединение классов Ia-с, подклассов II-V и/или классов VI и VII), при таких условиях, которые способствуют ингибированию активности р 38 в клетке. Примеры таких способов представлены в разделе "Примеры" ниже. Предпочтительно, соединение имеет ЕС 50 в области приблизительно от 1 до 1000 мкМ, предпочтительно приблизительно от 50 до 650 мкМ для ингибирования по меньшей мере одной MAPK р 38. Взаимодействие по меньшей мере одной MAPK р 38 с соединением предпочтительно осуществляется при концентрации, модулирующей SAPK-систему, которая составляет менее чем ЕС 30,предпочтительно менее чем ЕС 20, более предпочтительно менее чем ЕС 10 для ингибирования соединением по меньшей мере одной MAPK р 38. Способы in vivo включают в себя, например, введение группе животных перорально или путем инъекции заданного соединения (например, соединение классов Ia-с, подклассов II-V и/или классов VI иVII) при различных концентрациях. После введения соединения липополисахарид вводят внутривенно. Уровни TNF- в сыворотке измеряют и сравнивают с уровнями у контрольных животных. Предпочтительные соединения тормозят высвобождение TNF-, таким образом, уровни TNF- в образцах крови испытуемых животных снижаются. Соединение предпочтительно имеет ЕС 50 в области приблизительно от 1 до 1000 мкМ, предпочтительно приблизительно от 50 до 650 мкМ для ингибирования высвобождения TNF-. Способ идентификации фармацевтически активного соединения также может включать в себя определение токсического действия выбранного соединения на млекопитающее. Такие способы обычно известны специалистам в данной области. Способ идентификации фармацевтически активного соединения также может включать в себя введение выбранного соединения испытуемому субъекту, в связи с определением токсического действия на млекопитающее или по другим причинам. В варианте осуществления изобретения испытуемый субъект имеет воспалительный процесс, или ему угрожает развитие воспалительного состояния. Предпочтительно испытуемым субъектом является млекопитающее и может быть человек.- 17015252 Способы лечения и/или предотвращения Другой вариант осуществления изобретения относится к способам лечения или предотвращения патологических состояний, например, воспалительного(ых) процесса(ов) или фибротического(их) состояния(й). Способы включают в себя выявление субъекта, который находится под угрозой развития или имеет по крайней мере одно состояние, выбранное из воспалительного процесса и фибротического состояния, и введение соединения субъекту в эффективном количестве для лечения или профилактики воспалительного процесса и/или фибротического состояния. В предпочтительных вариантах осуществления изобретения соединение имеет ЕС 50 в области приблизительно от 1 мкМ до 1000 мкМ, предпочтительно приблизительно от 50 до 650 мкМ для ингибирования по меньшей мере одной MAPK р 38. В предпочтительных вариантах осуществления изобретения эффективное количество составляет концентрацию в крови или сыворотке или другой жидкости организма менее чем ЕС 30, или предпочтительно ЕС 20, или более предпочтительно, ЕС 10 для ингибирования соединением MAPK р 38. В предпочтительных вариантах осуществления изобретения соединение имеет ЕС 50 в области приблизительно от 1 до 1000 мкМ,предпочтительно приблизительно от 50 до 650 мкМ для ингибирования секреции TNF-. В других предпочтительных вариантах осуществления изобретения эффективное количество составляет концентрацию в крови или сыворотке или другой жидкости организма менее чем ЕС 30, или предпочтительно ЕС 20, или более предпочтительно ЕС 15, или более предпочтительно ЕС 10 для ингибирования соединением высвобождения LPS-стимулированного TNF- в жидкость организма. Эффективное количество предпочтительно составляет приблизительно 70% или меньше, более предпочтительно приблизительно менее чем 50% от количества, которое вызывает нежелательные побочные эффекты у субъекта, такие как, но не ограниченные ими, сонливость, тошнота, симптом простуды, нарушение желудочно-кишечного тракта и светочувствительная сыпь. Соединение, используемое для лечения или профилактики, предпочтительно является соединением классов Ia-с, подклассов II-V и/или классов VI и VII. Способы идентификации субъекта с риском развития воспалительного процесса или имеющего воспалительный процесс известны специалистам в данной области. Примеры воспалительных процессов,которые можно лечить или предупредить способами, приведенными в описании, включают в себя р 38 ассоциированные состояния, например состояния, связанные с изменением активности цитокинов, состояния, связанные с модуляцией SAPK-системы, аутоиммунные заболевания и заболевания, связанные с острым и хроническим воспалением. Цитокин (или цитокины) предпочтительно выбраны из группы, состоящей, но не ограниченной ими, из IL-1, IL-6, IL-8 и TNF-. В варианте осуществления изобретения соединение, используемое для лечения или предупреждения воспалительного процесса, является соединением, которое ингибирует киназу в SAPK-сигнальном пути. Примеры предпочтительных соединений включают в себя соединение классов Ia-с, подклассов II-V и/или классов VI и VII. Термин "р 38-ассоциированное состояние" означает заболевание или другое патологическое состояние, в развитие которого вовлекается сигнальный путь МАР-киназы р 38, прямо или косвенно. Примеры р 38-ассоциированных состояний включают в себя состояния, вызванные нарушением регуляции или повышенной экспрессией IL-1, TNF-, IL-6 или IL-8, являющейся результатом продолжительных или повышенных уровней активности р 38-киназы. Такие состояния включают в себя, без ограничения, воспалительные заболевания, аутоиммунные заболевания, фибротические заболевания, деструктивные процессы в кости, пролиферативные расстройства, инфекционные заболевания, нейродегенеративные заболевания, аллергии, реперфузию-ишемию при ударе, сердечные приступы, ангиогенные расстройства,органную гипоксию, сосудистую гиперплазию, сердечную гипертрофию, тромбин-индуцированную агрегацию тромбоцитов и состояния, связанные с путями простагландина или циклооксигеназы, например,состояния, вовлекающие простагландин-эндопероксидсинтазу. р 38-ассоциированное состояние может включать любое состояние, связанное или опосредованное изоформой р 38-киназы. Термины "фибротическое состояние", "фибропролиферативное состояние", "фибротическое заболевание", "фибропролиферативное заболевание", "фибротическое расстройство" используют взаимозаменяемо, ссылаясь на состояние, заболевание или расстройство, которое характеризуется нарушением пролиферации или активности фибробластов и/или патологическим или избыточным накоплением коллагеновой ткани. Обычно любое такое заболевание, расстройство или состояние поддается лечению путем введения соединения, обладающего антифиброгенной активностью. Фибротические расстройства включают в себя, но не ограничиваются ими, фиброз легких, включающий идиопатический легочный фиброз (IPF) и фиброз легких известной этиологии, фиброз печени и фиброз почки. Другие характерные фибротические состояния включают в себя костно-мышечный фиброз, кардиальный фиброз, послеоперационные спайки, склеродермию, глаукому и кожные поражения,такие как келоиды. Термин "модуляция SAPK-системы" означает увеличение или уменьшение активности системы стресс-активированных протеинкиназ, например, с помощью ингибирования активности р 38-киназы,либо in vitro, либо in vivo. В некоторых вариантах осуществления изобретения SAPK-система модулируется при ингибировании активности р 38 в клетке приблизительно на 50%, предпочтительно приблизительно на 40%, более предпочтительно приблизительно на 30%, даже более предпочтительно приблизи- 18015252 тельно на 20% или наиболее предпочтительно приблизительно на 10% по сравнению с активностью р 38 необработанной контрольной клетки. Состояние, ассоциированное с изменением активности цитокинов, которое указано в описании, относится к состоянию, при котором активность цитокинов изменяется по сравнению с нормальным состоянием. Такие состояния включают в себя, но не ограничивается ими, состояния, вызванные повышением продукции или нарушением регуляции IL-1, TNF-, IL-6 или IL-8, что приводит к постоянному,продолжительному, усиленному или повышенному уровню активности цитокинов, которая может быть связана с активностью р 38-киназы. Такие состояния включают в себя, без ограничения, воспалительные заболевания, аутоиммунные заболевания, фибротические заболевания, деструктивные процессы в кости,пролиферативные расстройства, инфекционные заболевания, нейродегенеративные заболевания, аллергии, реперфузию/ишемию при инсульте, сердечные приступы, ангиогенные расстройства, органную гипоксию, сосудистую гиперплазию, сердечную гипертрофию, тромбин-индуцированную агрегацию тромбоцитов и состояния, связанные с сигнальными путями циклооксигеназы и липоксигеназы, такие как простагландин-эндопероксидсинтаза. Цитокин-ассоциированное состояние может включать в себя любое состояние, связанное или опосредованное IL-1 (особенно IL-1(3), TNF-, IL-6 и IL-8, или любым другим цитокином, который может регулироваться р 38-киназой. В предпочтительных вариантах осуществления изобретения цитокин-ассоциированное состояние является состоянием, связанным с TNF-. Представленные в описании способы могут быть использованы для лечения аутоиммунных заболеваний и заболеваний, связанных с острым и хроническим воспалением. Такие заболевания включают в себя, но не ограничиваются ими, хроническое обструктивное легочное заболевание (COPD), синдром облитерирующего бронхиолита, хронический фиброз аллотрансплантата, воспалительный фиброз легких(IPF), ревматоидный артрит; ревматоидный спондилит; остеоартрит; подагру, другие артрогенные заболевания; сепсис; септический шок; эндотоксический шок; сепсис, вызванный грамотрицательными бактериями; синдром токсического шока; болевой синдром височно-нижнечелюстного сустава (MPS); шигеллез; астму; респираторный дистресс-синдром взрослых; воспалительное заболевание кишечника; болезнь Крона; псориаз; экзему; язвенный колит; гломерулярный нефрит; склеродермию; хронический тиреоидит; болезнь Грейвса; болезнь Ормонда; аутоиммунный гастрит; тяжелую миастению; аутоиммунную гемолитическую анемию; аутоиммунную нейтропению; тромбоцитопению; фиброз поджелудочной железы; хронический активный гепатит, включая фиброз печени; острое и хроническое почечное заболевание; фиброз почки, синдром раздраженной кишки; лихорадку; рестеноз; мозговую форму малярии; инсульт и ишемическое поражение; травму нервной системы; болезнь Альцгеймера; болезнь Гентингтона; болезнь Паркинсона; острую и хроническую боль; аллергии, включающие аллергический ринит и аллергический конъюнктивит; гипертрофию сердца, хроническую сердечную недостаточность; острый коронарный синдром; кахексию; малярию; лепру; лейшманиоз; болезнь Лайма; синдром Рейтера; острый синовит; мышечную дегенерацию, бурсит; тендонит; теносиновит; синдром выпячивания, разрыва или выпадения межпозвонкового диска; врожденный системный остеопетроз; тромбоз; силикоз; множественные опухоли легкого мясистой консистенции; заболевания, ассоциированные с резорбцией кости,такие как остеопороз или костные заболевания, связанные с множественной миеломой; рак, включающий, но не ограниченный ими, метастазирующий рак молочной железы, рак ободочной и прямой кишки,злокачественную меланому, рак желудка и немелкоклеточный рак легкого; реакцию "трансплантат против хозяина"; и аутоиммунные заболевания, такие как рассеянный склероз, волчанку и фибромиалгию;AIDS и другие вирусные заболевания, такие как опоясывающий лишай, простой герпес I или II, вирус гриппа, тяжелый острый респираторный синдром (SARS) и цитомегаловирус; и сахарный диабет. Кроме того, способы согласно вариантам осуществления изобретения могут быть использованы для лечения пролиферативных расстройств (включающих как доброкачественную, так и злокачественную гиперплазию), включая острый миелоидный лейкоз, хронический миелоидный лейкоз, саркому Капоши, метастазирующую меланому, множественную миелому, рак молочной железы, включая метастазирующий рак молочной железы; рак ободочной и прямой кишки; злокачественную меланому; рак желудка; немелкоклеточный рак легкого (NSCLC); метастазы в кости и тому подобное; болевые синдромы, включая нервномышечную боль, головную боль, боль, связанную с раком, и боль, ассоциированную с артритом; ангиогенные расстройства, включая ангиогенез солидной опухоли, неоваскуляризацию глаза и детскую гемангиому; состояния, ассоциированные с сигнальными путями циклооксигеназы и липоксигеназы,включая состояния, связанные с простагландин-эндопероксидсинтазой-2 (включая отек, лихорадку,аналгезию и боль); органную гипоксию; тромбин-индуцированную агрегацию тромбоцитов. Кроме того,приведенные в описании способы могут быть использованы для лечения заболеваний, вызванных простейшими, у животных, включая человека. Объектом может быть одна или более клеток или тканей, или организмы. Предпочтительным объектом является млекопитающее. Млекопитающее может включать любое млекопитающее. В качестве неограничивающего примера предпочтительными млекопитающими являются крупный рогатый скот,свиньи, овцы, козы, лошади, верблюды, буйволы, кошки, собаки, крысы, мыши и люди. Наиболее предпочтительным субъектом из млекопитающих является человек. Соединение(я) может быть введено субъ- 19015252 екту любым способом доставки лекарственного средства, известным в данной области. Отдельные характерные способы введения включают в себя пероральный, глазной, ректальный, буккальный, местный,назальный, офтальмический, подкожный, внутримышечный, внутривенный (болюс и инфузия), внутримозговой, чрескожный и легочный пути введения. Термины "терапевтически эффективное количество" и "профилактически эффективное количество", которые употребляют в описании, относятся к количеству соединения, достаточному для лечения,уменьшения интенсивности или предотвращения идентифицированного заболевания или состояния, или для достижения обнаруживаемого терапевтического, профилактического или ингибиторного эффекта. Эффект может быть выявлен, например, с помощью анализов, описанных в следующих примерах. Определенное эффективное количество для субъекта будет зависеть от массы тела, размера и общего состояния здоровья; характера и степени состояния, и терапии или комбинации терапий, выбранных для введения. Терапевтически и профилактически эффективные количества для данной ситуации могут быть определены с помощью обычного эксперимента, который находится в компетентности клинициста. Предпочтительно, эффективное количество соединения согласно вариантам осуществления изобретения составляет концентрацию в крови, или сыворотке, или другой жидкости организма, которая является менее чем ЕС 30, ЕС 20 или ЕС 10 для ингибирования МАР-киназы р 38. Для любого соединения терапевтически или профилактически эффективное количество может быть установлено вначале либо с помощью анализа в культуре клеток, например неопластических клеток, или на моделях животных, обычно крыс, мышей, кроликов, собак или свиней. Модель животного также может быть использована для определения соответствующей области концентраций и пути введения. Такая информация затем может быть использована для определения пригодных доз и способов введения человеку. Терапевтическая/профилактическая эффективность и токсичность могут быть определены стандартными фармацевтическими методами в культуре клеток или на экспериментальных животных, например, ED50 (терапевтически эффективная доза в 50% популяции) и LD50 (летальная доза для 50% популяции). Отношение доз между терапевтическим и токсическим эффектами представляет собой терапевтический индекс, и он может быть выражен в виде отношения ED50/LD50. Фармацевтические композиции, обнаруживающие большие терапевтические индексы, являются предпочтительными. Однако фармацевтические композиции, которые обнаруживают незначительные терапевтические индексы, также входят в объем вариантов осуществления изобретения. Данные, полученные в результате анализов в культуре клеток и на животных, могут быть использованы в определении области дозировки для использования человеком. Дозировка, содержащаяся в такой композиции, предпочтительно находится в области концентраций в кровотоке, которые включают ED50 с малой токсичностью или без токсичности. Дозировка может изменяться в пределах данной области в зависимости от используемой стандартной лекарственной формы, чувствительности больного и способа введения. Точнее, максимальные концентрации в плазме (Смакс) могут колебаться приблизительно от 65 до 115 мкМ, или приблизительно от 75 до 105 мкМ, или приблизительно от 85 до 95 мкМ, или приблизительно от 85 до 90 мкМ в зависимости от способа введения. Указания относительно отдельных дозировок и методов доставки имеются в литературе и обычно доступны практикующим врачам в данной области. Вообще, доза будет находиться в области приблизительно от 100 мг/день до 10 г/день, или приблизительно от 200 мг до 5 г/день, или приблизительно от 400 мг до 3 г/день, или приблизительно от 500 мг до 2 г/день в виде однократных, разделенных или постоянных доз для больного, который имеет массу тела приблизительно от 40 до 100 кг (указанная доза может быть скорректирована для больных, масса которых находится выше или ниже приведенной области, особенно для детей массой около 40 кг). Обычно доза будет находиться в области приблизительно от 25 до 300 мг/кг массы тела в день. Точную дозировку будет определять практикующий врач с учетом факторов, связанных с субъектом, которому требуется лечение. Дозировку и введение подбирают для достижения достаточных уровней активного агента(ов) или поддержания желаемого эффекта. Факторы, которые могут быть приняты во внимание, включают в себя тяжесть заболевания, общее состояние здоровья субъекта, возраст, массу тела и пол субъекта, питание, время и частоту введения, комбинацию(и) лекарственных средств, чувствительность и толерантность/ответ на терапию. Фармацевтические композиции длительного действия могут быть введены два раза в день, один раз в день, один раз каждые два дня, три раза в неделю, два раза в неделю, каждые 3-4 дня или каждую неделю в зависимости от времени полу-жизни и скорости выведения отдельной композиции. Например, в варианте осуществления изобретения фармацевтическая композиция содержит количество соединения,как приведено в описании, которое выбрано для введения больному с учетом режима введения, выбранного из следующих режимов: два раза в день, один раз в день, один раз каждые два дня, три раза в неделю, два раза в неделю и один раз в неделю. Следует принять во внимание, что лечение, перечисленное в описании, включает в себя предотвращение заболевания, уменьшение симптомов, замедление развития заболевания, устранение повреждения или излечение от болезни. В одном аспекте лечение воспалительного процесса приводит к увеличению среднего времени вы- 20015252 живания популяции субъектов, подвергаемой лечению, по сравнению с популяцией, не подвергаемой лечению. Предпочтительно среднее время выживания увеличивается более чем приблизительно на 30 дней; более предпочтительно более чем приблизительно на 60 дней; более предпочтительно более чем приблизительно на 90 дней и даже предпочтительнее более чем приблизительно на 120 дней. Увеличение времени выживания популяции можно определить любыми воспроизводимыми способами. В предпочтительном аспекте увеличение среднего времени выживания популяции можно определить, например, путем расчета для популяции средней продолжительности выживаемости после начала обработки активным соединением. В другом предпочтительном аспекте увеличение среднего времени выживания популяции можно определить, например, путем расчета для популяции средней продолжительности выживаемости после завершения первого этапа обработки активным соединением. В другом аспекте лечение воспалительного процесса приводит к снижению уровня смертности популяции подвергнутых лечению субъектов по сравнению с популяцией субъектов, получающих только носитель. В другом аспекте лечение воспалительного процесса приводит к снижению уровня смертности популяции подвергнутых лечению субъектов по сравнению с популяцией субъектов, не подвергнутых лечению. В другом аспекте лечение воспалительного процесса приводит к снижению уровня смертности популяции подвергнутых лечению субъектов по сравнению с популяцией, подвергаемой монотерапии лекарственным средством, которое не является соединением вариантов осуществленияизобретения, или его фармацевтически премлемой солью, метаболитом, аналогом или производным. Предпочтительно уровень смертности снижается более чем приблизительно на 2%; предпочтительнее более чем приблизительно на 5%; предпочтительнее более чем приблизительно на 10% и наиболее предпочтительно более чем приблизительно на 25%. В предпочтительном аспекте снижение уровня смертности популяции подвергнутых лечению субъектов можно определить любыми воспроизводимыми способами. В другом предпочтительном аспекте снижение уровня смертности популяции можно определить, например, путем расчета для популяции среднего количества связанных с заболеванием смертей на единицу времени после начала обработки активным соединением. В другом предпочтительном аспекте снижение уровня смертности популяции также можно определить, например, путем расчета для популяции среднего количества связанных с заболеванием смертей на единицу времени после завершения первого цикла обработки активным соединением. В другом аспекте лечение воспалительного процесса приводит к уменьшению скорости роста опухоли. Предпочтительно после обработки скорость роста опухоли снижается по меньшей мере приблизительно на 5% относительно величины до обработки; более предпочтительно скорость роста опухоли снижается по меньшей мере приблизительно на 10%; более предпочтительно снижается по меньшей мере приблизительно на 20%; более предпочтительно снижается по меньшей мере приблизительно на 30%; более предпочтительно снижается по меньшей мере приблизительно на 40%; более предпочтительно снижается по меньшей мере приблизительно на 50%; даже более предпочтительно снижается по меньшей мере приблизительно на 60%; и наиболее предпочтительно снижается по меньшей мере приблизительно на 75%. Скорость роста опухоли можно определить любыми воспроизводимыми способами измерения. В предпочтительном аспекте скорость роста опухоли измеряют соответственно изменению диаметра опухоли в единицу времени. В другом аспекте лечение воспалительного процесса приводит к снижению скорости клеточной пролиферации. Предпочтительно после обработки скорость клеточной пролиферации снижается по меньшей мере приблизительно на 5%; более предпочтительно по меньшей мере приблизительно на 10%; более предпочтительно по меньшей мере приблизительно на 20%; более предпочтительно по меньшей мере приблизительно на 30%; более предпочтительно по меньшей мере приблизительно на 40%; более предпочтительно по меньшей мере приблизительно на 50%; даже предпочтительнее по меньшей мере приблизительно на 60% и наиболее предпочтительно по меньшей мере приблизительно на 75%. Скорость клеточной пролиферации можно определить любыми воспроизводимыми способами измерения. В предпочтительном аспекте скорость клеточной пролиферации определяют, например, путем измерения числа делящихся клеток в тканевом образце на единицу времени. В другом аспекте лечение воспалительного процесса приводит к снижению в популяции пролиферирующих клеток. Предпочтительно, после обработки доля пролиферирующих клеток снижается по меньшей мере приблизительно на 5%; более предпочтительно по меньшей мере приблизительно на 10%; более предпочтительно по меньшей мере приблизительно на 20%; более предпочтительно по меньшей мере приблизительно на 30%; более предпочтительно по меньшей мере приблизительно на 40%; более предпочтительно по меньшей мере приблизительно на 50%; даже предпочтительне, по меньшей мере приблизительно на 60% и наиболее предпочтительно по меньшей мере приблизительно на 75%. Долю пролиферирующих клеток можно определить любыми воспроизводимыми способами измерения. В предпочтительном аспекте долю пролиферирующих клеток определяют, например, путем количественной оценки числа делящихся клеток относительно числа неделящихся клеток в тканевом образце. В другом предпочтительном аспекте доля пролиферирующих клеток является эквивалентной митотическому индексу. В другом аспекте лечение воспалительного процесса приводит к уменьшению размера площади или- 21015252 зоны клеточной пролиферации. Предпочтительно, после обработки размер площади или зоны клеточной пролиферации уменьшается по меньшей мере приблизительно на 5% относительно ее размера до обработки; более предпочтительно уменьшается по меньшей мере приблизительно на 10%; более предпочтительно уменьшается по меньшей мере приблизительно на 20%; более предпочтительно уменьшается по меньшей мере приблизительно на 30%; более предпочтительно уменьшается по меньшей мере приблизительно на 40%; более предпочтительно уменьшается по меньшей мере приблизительно на 50%; даже предпочтительнее уменьшается по меньшей мере приблизительно на 60% и наиболее предпочтительно уменьшается по меньшей мере приблизительно на 75%. Размер площади или зоны клеточной пролиферации можно определить любыми воспроизводимыми способами измерения. В предпочтительном аспекте размер площади или зоны клеточной пролиферации можно определить путем измерения диаметра или ширины площади или зоны клеточной пролиферации. Способы, приведенные в описании, могут включать в себя идентификацию субъекта, нуждающегося в лечении. В предпочтительном варианте осуществления изобретения способы включают в себя выявление млекопитающего, нуждающегося в лечении. В наиболее предпочтительном варианте осуществления изобретения способы включают в себя выявление человека, нуждающегося в лечении. Выявление субъекта, нуждающегося в лечении, может быть осуществлено любыми способами, обнаруживающими субъекта, который может извлечь пользу от лечения. Например, выявление субъекта, нуждающегося в лечении, можно осуществлять посредством клинической диагностики, лабораторного испытания или любыми другими средствами, известными специалисту в данной области, включая любую комбинацию средств обнаружения. Как описано выше, приведенные в описании соединения могут входить в состав фармацевтических композиций, если желательно, и могут быть введены любым путем, который дает возможность лечить заболевание или состояние. Предпочтительным путем введения является пероральное введение. Введение может осуществляться в виде однократной дозы, или соединение согласно вариантам изобретения может быть введено в течение периода времени либо в виде разделенных доз, либо в виде препарата с непрерывным высвобождением или способа введения с непрерывным высвобождением (например, насос). Однако соединения согласно вариантам осуществления изобретения вводят субъекту, количества введенного соединения и выбранный способ введения должны быть отобраны так, чтобы достичь эффективного лечения заболевания. Способы согласно вариантам осуществления изобретения включают в себя использование соединения или соединений, приведенных в описании, вместе с одним или более дополнительными терапевтическими средствами для лечения заболеваний. Таким образом, например, комбинация активных ингредиентов может быть (1) составлена и введена или доставлена одновременно в виде комбинированного препарата; (2) доставлена путем чередования или параллельно в виде раздельных препаратов или (3) доставлена с помощью любого другого режима комбинационной терапии, известного в данной области. В случае, когда доставка осуществляется чередованием, приведенные в описании способы могут включать введение или доставку активных ингредиентов последовательно, например, в раздельном растворе,эмульсии, суспензии, таблетках, пилюлях или капсулах, или различными инъекциями в раздельных шприцах. Вообще, в течение терапии чередованием, эффективная дозировка каждого активного ингредиента вводится последовательно, т.е. сериями, в то время как при одновременной терапии эффективные дозировки двух или более активных ингредиентов вводят вместе. Различные последовательности периодической комбинационной терапии также могут быть использованы. Диагностические тесты рассматриваются как часть способов, приведенных в описании. Например,образец тканевого биоптата может быть взят у субъекта, у которого наблюдается воспалительный процесс, например, р 38-ассоциированное или цитокин-ассоциированное состояние. Биоптат может быть исследован для определения уровня активности р 38-киназы (или уровни цитокина), присутствующей в образце; затем образец может быть подвергнут контакту с соединением согласно вариантам осуществления изобретения, и активность р 38 может быть измерена для установления, оказывает ли соединение желаемый эффект (например, ингибирование активности р 38 или цитокина с ЕС 50 в области приблизительно от 100 мкМ до 1000 мкМ, предпочтительно приблизительно от 50 мкМ до 650 мкМ). Такой тест может быть использован для установления вероятности эффективности обработки таким соединением у данного субъекта. В качестве альтернативы, образец может быть подвергнут контакту с меченым соединением (например, флуоресцентно меченное соединение или радиоактивно меченное соединение), и затем образец исследуют и регистрируют флуоресцентный или радиоактивный сигнал для определения распределения р 38 в тканевом образце. Повторные биоптаты, взятые в течение курса лечения, также могут быть использованы для изучения эффективности обработки. Другие диагностические тесты с использованием приведенных в описании соединений будут очевидны специалисту в данной области в свете базовых положений, изложенных в описании. Таким образом, например, вариант осуществления изобретения относится к способам обнаружения,локализации или определения количества, или любой их комбинации, белка р 38 в клетке или тканевом образце. Способы включают в себя а) осуществление контакта клеточного или тканевого образца с соединением согласно вариантам осуществления изобретения при таких условиях, что соединение может- 22015252 связываться по меньшей мере с одной MAPK р 38; b) установление наличия, локализацию или определение количества, или любую их комбинацию, соединения в клеточном или тканевом образце, тем самым устанавливая присутствие, локализацию или количество, или любую их комбинацию по меньшей мере одной MAPK р 38 в клеточном или тканевом образце. Установление наличия, локализация или определение количества, или любая их комбинация, соединения в клеточном или тканевом образце может быть выполнено любыми способами, которые позволяют выявить присутствие соединения, локализовать соединение или определить количество, или любую их комбинацию, соединения в клеточном или тканевом образце. Например, как описано ранее, способы на основе радиоактивной или флуоресцентной метки могут быть использованы. Дополнительные способы выявления присутствия, локализации или определения количества, или их любых комбинаций, соединения должны быть очевидны квалифицированным специалистам. Другой вариант осуществления изобретения относится к способам определения (1) того, будет ли соединение полезным терапевтическим средством для лечения субъекта, у которого наблюдается воспалительный процесс, или (2) тяжести заболевания, или (3) течения заболевания в процессе обработки средством, корригирующим заболевание. Способы включают в себя а) получение клеточного или тканевого образца от субъекта до обработки, в течение обработки или после окончания обработки соединением, приведенным в описании, или другим средством, корригирующим заболевание; b) осуществление контакта образца с соединением и с) определение количества соединения, которое связывается с образцом, где связывание MAPK р 38 с соединением соотносится с количеством MAPK р 38 в образце. Отдельные примеры заболеваний, которые предполагается лечить соединениями и способами,приведенными в описании COPD Хроническая обструктивная болезнь легких (COPD) характеризуется хроническим воспалительным процессом в легком, при котором отмечается (1) повышенное количество воспалительных клеток (нейтрофилы, макрофаги и SD8+ Т-клетки) в дыхательных путях и паренхиме, (2) повышенная экспрессия воспалительных цитокинов и хемокинов и (3) увеличенное количество протеаз (эластазы, катепсины и матриксные металлопротеиназы, ММР). Полагают, что продуцирование и действие многих потенциальных медиаторов воспаления дыхательных путей зависят от каскада MAPK или р 38-киназы, индуцированного стрессом. Несколько публикаций подтверждают связь активации р 38-киназы с изобилием событий в легком: экспрессия LPS- и TNFиндуцированной межклеточной адгезивной молекулы-1 на эндотелиальных клетках капилляров легкого, активация ММР-9, индуцированная гипоксией стимуляция артериальных клеток легкого, гиперосмолярность-индуцированная экспрессия IL-8 в бронхиальных эпителиальных клетках и усиленная направленная миграция и выживаемость эозинофилов.Trifilieff et al. (2005 Brit. J. Pharmacol. 144: 1002-10) показали, что CGH2466, комбинированный антагонист аденозинового рецептора, ингибитор MAPK р 38-киназы и фосфодиэстеразы типа 4 проявил потенциальные in vitro и in vivo противовоспалительные активности при заболеваниях, таких как астма иCOPD. Underwood et al. (2000 Am. J. Physiol. Lung Cell Mol. Physiol. 279: L895-L902) показал, что потенциальный и селективный ингибитор MAPK р 38-киназы, SB23 9063, снижает продуцирование противовоспалительных цитокинов, включающих IL-1, TNF-, IL-6 и IL-8, которые связаны с фиброзом дыхательных путей вследствие их способности регулировать пролиферацию фибробластов и продукцию матрикса, что приводит к снижению направленной миграции и активации нейтрофилов в легком. Ранее было найдено, что такое же соединение проявляет способность к изменению ответов, ассоциированных с хроническим фиброзом, индуцированным блеомицином. Указанная ингибиторная активность была избирательной для - и -изоформ р 38-киназы. Соединения и способы, приведенные в описании, являются полезными в лечении COPD. Фиброз легких Фиброз легких, также названный как идиопатический легочный фиброз (IPF), интерстициальный диффузный фиброз легких, воспалительный легочный фиброз или фиброзирующий альвеолит, является воспалительным заболеванием легких и представляет собой группу состояний, характеризующихся аномальным образованием фиброзной ткани между альвеолами, вызванным альвеолитом, включающим воспалительную клеточную инфильтрацию в альвеолярные перегородки с результирующим фиброзом. Последствия фиброза являются хроническими, прогрессирующими и часто фатальными. Активация MAPK р 38 была продемонстрирована в легком больных с легочным фиброзом. Ряд исследований относительно легочного фиброза указывает, что длительная и усиленная экспрессия некоторых цитокинов в легких является существенной для увеличения численности воспалительных клеток и накопления компонентов внеклеточного матрикса с последующим ремоделированием легочной архитектуры. В частности, было показано, что провоспалительные цитокины, такие как TNF- и интерлейкин IL-1, играют главные роли в образовании пневмонии и легочного фиброза. Кроме того, профибротические цитокины, такие какTGF- и CTGF, играют критические роли в патогенезе легочного фиброза. Matsuoka et al. (2002 Am. J.Physiol. Lung Ceii Mol. Physiol. 283: L103-L112) показали, что ингибитор р 38-киназы, FR-167653, уменьшает интенсивность блеомицин-индуцированного легочного фиброза у мышей. Кроме того, было обнаружено, что пирфенидон (5-метил-1-фенил-2-(1 Н)пиридон), соединение с комбинированными противо- 23015252 воспалительными, антиоксидантными и антифиброгенными эффектами является эффективным в экспериментальных моделях легочного фиброза, а также в клинических исследованиях (Raghu et al. 1999 Am.Genet. Metab. 76: 234-242; Azuma et al. 2002 Am. J. Respir. Crit. Care Med. 165: A729). Приведенные в описании соединения и способы являются полезными в лечении фиброза легких, такого как IPF. Облитерирующий бронхиолит и синдром облитерирующего бронхиолита Облитерирующий бронхиолит и коррелирующий с ним клиническое состояние синдром облитерирующего бронхиолита характеризуются обструкцией легочных путей вследствие облитерации малых дыхательных путей легких. При облитерирующем бронхиолите в результате медико-патологического обследования обнаруживаются типичные поражения, приводящие к закупорке или облитерации малых дыхательных путей в легком. Указанные поражения представляют собой гранулярную фибромиксоидную ткань и грубую рубцовую соединительную ткань, располагающуюся в подслизистом слое. Поражения прогрессируют в результате длительного, аномального или аберрантного воспаления эпителиальных структур или расположенных в эпителии структур малых дыхательных путей, опосредованного провоспалительными цитокинами, такими как TNF-, и приводят к чрезмерной фибропролиферации. Облитерация малых дыхательных легочных путей постепенно приводит к нарушению проходимости дыхательных путей, характеризующемуся прогрессирующим снижением объема форсированного выхода за одну секунду (FEV1), и часто сопровождается рецидивирующими инфекциями нижнего отдела респираторного тракта и колонизацией легочной ткани патогенными микроорганизмами. Синдром облитерирующего бронхиолита поражает 50-60% больных, выживающих после операции по пересадке легкого, и число выживающих в течение пяти лет после начала появления синдрома облитерирующего бронхиолита составляет только 30-40%. Больные после легочной трансплантации, испытывающие синдром облитерирующего бронхиолита, часто плохо реагируют на усиленную иммуносупрессию. У больных с фиброзирующим альвеолитом, выживание после синдрома облитерирующего бронхиолита короче, чем у больных с эмфиземой. Соединения и способы, приведенные в описании, являются полезными в лечении синдрома облитерирующего бронхиолита. Хронический фиброз аллотрансплантата Поражение аллотрансплантата представляет собой важную проблему в области трансплантологии. Одной из первых причин поражения аллотрансплантата является хроническая дисфункция аллотрансплантата. Признаками хронической дисфункции аллотрансплантата являются хроническое воспаление и хронический фиброз, и оба признака связаны с продуцированием воспалительных цитокинов и факторов роста. Опосредование воспалительных цитокинов и факторов роста, особенно приводящее к нарушению продукции коллагена и TGF, используют в лечении хронического фиброза аллотрансплантата. Термин"хронический фиброз аллотрансплантата", который употребляют в описании, предназначен охватить как хроническое воспаление, так и хронический фиброз, связанный с хроническим фиброзом аллотрансплантата. Соединения и способы, приведенные в описании, являются полезными в лечении хронического фиброза аллотрансплантата. Фиброз почки Независимо от происхождения начинающегося инсульта, фиброз почки рассматривается как конечный этап общего пути, по которому происходит развитие почечного заболевания до конечной стадии почечной недостаточности. Stambe et al. (2004 J. Am. Soc. Nephrol. 15: 370-379) проверяли ингибитор активной (фосфорилированной) формы р 38, NPC 31169, разработанный Scios Inc. (San Francisco, CA), на модели почечного фиброза крысы и обнаружили значительное уменьшение почечного фиброза, определенное по интерстициальному объему, депонированию коллагена типа IV и уровням мРНК растущей соединительной ткани. Соединения и способы, приведенные в описании, являются полезными в лечении фиброза почки. Лейомиома Лейомиомы матки или фибромы являются самыми распространенными опухолями тазовых органов у женщин, причем доступные терапии длительно действующими лекарственными средствами неизвестны. Лейомиомы характеризуются повышенной клеточной пролиферацией и фиброзом ткани. Пирфенидон проверяли относительно действия на клеточную пролиферацию и экспрессию коллагена в культуре гладкомышечных клеток миометрия и лейомиомы, и было найдено, что он является эффективным ингибитором пролиферации клеток миометрия и лейомиомы (Lee et al. 1998 J. Clin. Endocrinol. Metab. 83: 219223). Соединения и способы, приведенные в описании, являются полезными в лечении лейомиом. Эндомиокардиальный фиброз Эндомиокардиальный фиброз (EMF) является расстройством, характеризующимся развитием рестриктивной кардиомиопатии. EMF иногда рассматривают как часть спектра одного патологического процесса, который включает в себя эндокардит Леффлера (нетропический эозинофильный эндомиокардиальный фиброз или фибропластический париетальный эндокардит с эозинофилией). При EMF лежащий в основе процесс приводит к неоднородному фиброзу эндокардиальной поверхности сердца, сопровождающемуся снижением податливости и, в конечном счете, рестриктивной физиологии, поскольку эндомиокардиальная поверхность более широко вовлекается в патологический процесс. Эндокардиальный- 24015252 фиброз преимущественно вовлекает пути притока крови левого и правого желудочков и может влиять на предсердно-желудочковые клапаны, что приводит к регургитации крови при недостаточности трехстворчатого клапана и недостаточности митрального клапана. Как показано, активация MAPK вносит вклад в аритмогенное структурное ремоделирование предсердий при EMF. Соединения и способы, приведенные в описании, являются полезными в лечении и/или профилактике эндомиокардиального фиброза. Другие воспалительные заболевания Многие аутоиммунные заболевания и заболевания, ассоциированные с хроническим воспалением, а также острые ответы связаны с активацией MAP р 38-киназы и повышенной экспрессией или нарушением регуляции воспалительных цитокинов. Указанные заболевания включают в себя, но не ограничиваются ими, ревматоидный артрит; ревматоидный спондилит; остеоартрит; подагру, другие артрогенные заболевания; сепсис; септический шок; эндотоксический шок; сепсис, вызванный грамотрицательными бактериями; синдром токсического шока; астму; респираторный дистресс-синдром взрослых; хроническое обструктивное легочное заболевание; хроническое воспаление легких; воспалительное заболевание кишечника; болезнь Крона; псориаз; экзему; язвенный колит; фиброз поджелудочной железы; фиброз печени; острое и хроническое почечное заболевание; синдром раздраженной кишки; лихорадку; рестеноз; мозговую форму малярии; инсульт и ишемическое поражение; травму нервной системы; болезнь Альцгеймера; болезнь Гентингтона; болезнь Паркинсона; острую и хроническую боль; аллергический ринит; аллергический конъюнктивит; хроническую сердечную недостаточность; острый коронарный синдром; кахексию; малярию; лепру; лейшманиоз; болезнь Лайма; синдром Рейтера; острый синовит; мышечную дегенерацию, бурсит; тендонит; теносиновит; синдром выпячивания, разрыва или выпадения межпозвонкового диска; остеопетроз; тромбоз; рак; рестеноз; силикоз; множественные опухоли легкого мясистой консистенции; заболевания, ассоциированные с резорбцией кости, такие как остеопороз; реакцию "трансплантат против хозяина", и аутоиммунные заболевания, такие как рассеянный склероз, волчанку и фибромиалгию; AIDS и другие вирусные заболевания, такие как опоясывающий лишай, простой герпес I или II, вирус гриппа и цитомегаловирус; и сахарный диабет. Многие исследования показывают, что уменьшение активности MAP р 38-киназы, ее восходящих [в каскаде реакций] активаторов или нисходящих [в каскаде реакций] эффекторов, либо генетическими,либо химическими средствами снижает воспалительный ответ и предотвращает или снижает до минимума повреждение ткани (см., например, English, et al, 2002 Trends Pharmacol. Sci. 23: 40-45, и Dong et al. 2002 Annu. Rev. Immunol. 20: 55-72). Таким образом, ингибиторы р 38, которые также ингибируют избыточную или нерегулируемую продукцию цитокинов и которые могут ингибировать более чем один провоспалительный цитокин, могут быть полезными в качестве противовоспалительных средств и терапий. Кроме того, большое число заболеваний, ассоциированных с воспалительными реакциями, связанными сMAP р 38-киназой, указывает на то, что существует необходимость в эффективных способах лечения данных состояний. Сердечно-сосудистое заболевание Воспаление и активация/инфильтрация лейкоцитов играют главную роль в инициации и развитии сердечно-сосудистых заболеваний, включая атеросклероз и сердечную недостаточность. Ингибирование пути итоген-активированной протеинкиназы (MAPK) р 38 острой фазы ослабляет тканевое повреждение и аккумуляцию лейкоцитов в случае поражения миокарда при ишемии/реперфузии. Соединения и способы, приведенные в описании, являются полезными для лечения сердечно-сосудистого заболевания. Рассеянный склероз. Воспаление в центральной нервной системе имеет место в заболеваниях, таких как рассеянный склероз, и приводит к дисфункции и деструкции аксонов. Наблюдения как in vitro, так и in vivo указывают на важную роль оксида азота (NO) в опосредовании воспалительной аксонопатии. MAP р 38-киназа активируется под действием N0, и, как было показано, ингибирование сигнального пути р 38-киназы приводит к эффектам выживания нейронов и аксонов. ОСМ и IGF-1 снижают активацию р 38-киназы в NOэкспонированных нейронах коры головного мозга и повышают выживаемость аксонов в культурах, подвергающихся воздействию NO, процесс зависит от сигнального пути митоген-активированной протеинкиназы/внеклеточной сигнал-регулируемой киназы. Соединения и способы, приведенные в описании,являются полезными для лечения рассеянного склероза. Отсутствие функции первичного трансплантата Неспецифическое воспаление связано с отсутствием функции первичного трансплантата (PNF). Воспалительное поражение островков опосредуется, по меньшей мере отчасти, провоспалительными цитокинами, такими как интерлейкин-1 (IL-1) и фактор- некроза опухоли (TNF-), продуцируемыми оседлыми макрофагами островков. Путь р 38-киназы, как известно, вовлекается в продуцирование цитокинов в клетках линий моноцит-макрофаг. Ингибирование пути р 38-киназы химическим ингибитором р 38, SB203580, подавляет продуцирование IL-1 и TNF- в островках человека, подвергающихся воздействию липополисахарида (LPS) и/или воспалительных цитокинов. Хотя IL-1 преимущественно продуцируется оседлыми макрофагами, клетки протоков и эндотелиальные клетки сосудов островков, как было обнаружено, являются другим клеточным источником IL-1 в изолированных островках человека.SB203580 также ингибирует экспрессию индуцибельной синтазы оксида азота (iNOS) и циклооксигеназы-2 (СОХ-2) в обработанных островках. Кроме того, островки, обработанные SB203580 в течение 1 ч до трансплантации, проявляют значительно улучшенную функцию трансплантата. Соединения и способы,приведенные в описании, представляются полезными для повышения выживаемости трансплантата при клинической трансплантации островков. Острое поражение почки Цисплатин является важным химиотерапевтическим средством, но он может вызывать острое поражение почки. Частично это острое поражение почки опосредуется через фактор- некроза опухоли(TNF-). Цисплатин активирует MAPK р 38 и индуцирует апоптоз в раковых клетках. Активация MAPK р 38 приводит к повышению продукции TNF- в ишемическом повреждении и в макрофагах. In vitro цисплатин вызывает дозозависимую активацию MAPK р 38 в проксимальных клетках канальцев. Ингибирование активации MAPK р 38 приводит к ингибированию продуцирования TNF-. In vivo у мышей, обработанных однократной дозой цисплатина, развивается сильная дисфункция почки, которая сопровождается увеличением активности MAPK р 38 в почке и повышением уровня инфильтрирующих лейкоцитов. Однако у животных, обработанных ингибитором MAPK р 38, SKF86002, наряду с цисплатином, наблюдается в меньшей степени дисфункция почки, менее серьезное гистологическое повреждение и меньше лейкоцитов по сравнению с животными, обработанными цисплатин+носитель. Соединения и способы,приведенные в описании, представляются полезными для предотвращения острого поражения почки. Периодонтит. Провоспалительный медиатор брадикинин (ВК) стимулирует продуцирование интерлейкина-8 (IL8) в десневых фибробластах человека in vitro и играет важную роль в патогенезе различных воспалительных заболеваний, включая периодонтит. Специфический ингибитор митоген-активированной протеинкиназы р 38 (MAPK), SB203580, снижает продуцирование IL-8, стимулированное комбинацией ВК и IL1, а также продуцирование IL-8, стимулированное IL-1. Соединения и способы, приведенные в описании, представляются полезными для лечения или предотвращения периодонтита. Фармацевтические композиции Хотя введение только соединений, приведенных в тексте, представляется возможным, однако может оказаться предпочтительным приготовление соединений в виде фармацевтических композиций. В другом аспекте фармацевтические композиции, как таковые, применяемые в способах согласно изобретению, предусмотрены. В частности, фармацевтические композиции, приведенные в описании, могут оказаться полезными, между прочим, для лечения или предотвращения воспалительных состояний, например состояний, ассоциированных с активностью р 38 или активностью цитокинов или с их комбинациями. Фармацевтическая композиция является любой композицией, которая может быть введена объекту in vitro или in vivo или обоими путями с целью лечения или улучшения состояния. В предпочтительном варианте осуществления изобретения фармацевтическая композиция может быть введена in vivo. Объект может представлять собой одну или более клеток или тканей, или организмы. Предпочтительным объектом является млекопитающее. Млекопитающее включает любое млекопитающее, такое как и неограниченное примером, крупный рогатый скот, свиньи, овцы, козы, лошади, верблюды, буйволы, кошки,собаки, крысы, мыши и люди. Наиболее предпочтительным субъектом-млекопитающим является человек. В варианте осуществления изобретения фармацевтические композиции могут быть приготовлены с фармацевтически приемлемыми наполнителями, такими как носители, растворители, стабилизаторы,адъюванты, разбавители и т.д., в зависимости от отдельного способа введения и стандартной лекарственной формы. Как правило, фармацевтические композиции должны быть приготовлены с целью достижения физиологически совместимого рН, который может колебаться приблизительно от рН 3 до рН 11,предпочтительно приблизительно от рН 3 до рН 7, в зависимости от препарата и пути введения. В альтернативных вариантах осуществления изобретения предпочтительным может быть доведение рН в области приблизительно от рН 5,0 до рН 8. Подробнее, фармацевтические композиции могут содержать терапевтически или профилактически эффективное количество по меньшей мере одного соединения,приведенного в описании, вместе с одним или более фармацевтически приемлемыми наполнителями. Необязательно, фармацевтические композиции могут содержать комбинацию соединений, приведенных в описании, или могут включать второй активный ингредиент, используемый в лечении или предотвращении бактериальной инфекции (например, антибактериальные или противомикробные средства). Самыми обычными препаратами, например, для парентерального или перорального введения, являются твердые препараты, жидкие растворы, эмульсии или суспензии, в то время как ингаляционные препараты для легочного введения являются обычно жидкостями или порошками, порошкообразные препараты обычно являются предпочтительными. Предпочтительная фармацевтическая композиция также может быть приготовлена в виде лиофилизированного твердого препарата, который можно реконструировать с помощью физиологически совместимого растворителя до введения. Альтернативные фармацевтические композиции могут быть приготовлены в виде сиропов, кремов,мазей, таблеток и тому подобного.- 26015252 Термин "фармацевтически приемлемый наполнитель" относится к наполнителю для введения фармацевтического средства, такого как соединения, приведенные в описании. Термин относится к любому фармацевтическому наполнителю, который может быть введен без чрезмерной токсичности. Фармацевтически приемлемые наполнители определяются, частично, отдельной вводимой фармацевтической композицией, а также отдельным способом, используемым для введения композиции. Таким образом, существует широкий ряд подходящих препаратов фармацевтических композиций (см., например, Remington's Pharmaceutical Sciences). Подходящими наполнителями могут быть молекулы носителей, которые включают в себя большие медленно метаболизирующие макромолекулы, такие как белки, полисахариды, полимолочные кислоты,полигликолевые кислоты, полимерные аминокислоты, сополимеры аминокислот и неактивные вирусные частицы. Другие примеры наполнителей включают в себя антиоксиданты, такие как аскорбиновая кислота; хелатирующие агенты, такие как ЭДТА; углеводы, такие как декстрин, гидроксиалкилцеллюлоза,гидроксиалкилметилцеллюлоза, стеариновая кислота; жидкости, такие как масла, вода, физиологический раствор, глицерин и этанол; смачивающие или эмульгирующие средства; вещества для создания рН и тому подобное. Липосомы также включены в определение фармацевтически приемлемых наполнителей. Фармацевтические композиции, приведенные в описании, могут быть приготовлены в любом виде,подходящем для предназначенного способа введения. В случае, когда фармацевтические композиции предназначены для перорального использования, могут быть приготовлены, например, таблетки, пастилки, леденцы, водные или масляные суспензии, неводные растворы, дисперсные порошки или гранулы(включая тонкоизмельченные частицы или наночастицы), эмульсии, твердые или мягкие капсулы, сиропы или эликсиры. Композиции, предназначенные для перорального использования, могут быть приготовлены способом, известным в данной области для производства фармацевтических композиций, и такие композиции мргут содержать один или более агентов, включающих подсластители, ароматизаторы,красители и консерванты, для получения препарата с привлекательным вкусом. Фармацевтически приемлемые наполнители, особенно подходящие для использования в сочетании с таблетками, включают в себя, например, инертные разбавители, такие как целлюлозы, карбонат кальция или натрия, лактоза, фосфат кальция или натрия; дезинтегрирующие средства, такие как поперечносвязанный повидон, кукурузный крахмал или альгиновая кислота; связывающие средства, такие как повидон, крахмал, желатин или камедь, и смазывающие средства, такие как стеарат магния, стеариновая кислота или тальк. Таблетки могут быть не покрытыми оболочкой или покрытыми с помощью известных способов,включая микроинкапсулирование, для замедления дезинтеграции и всасывания в желудочно-кишечном тракте и, тем самым, достижения пролонгированного действия в течение более длительного периода. Например, в качестве материала, способствующего замедленному высвобождению, может быть использован глицерилмоностеарат или глицерилдистеарат, отдельно или в сочетании с воском. Препараты для перорального использования могут быть представлены в виде твердых желатиновых капсул, где активный ингредиент смешивают с инертным твердым разбавителем, например целлюлозами, лактозой, фосфатом кальция или каолином, или в виде мягких желатиновых капсул, где активный ингредиент смешивают с неводной или масляной средой, такой как глицерин, пропиленгликоль, полиэтиленгликоль, арахисовое масло, жидкий парафин или оливковое масло. В другом варианте осуществления изобретения фармацевтические композиции могут быть приготовлены в виде суспензий, содержащих соединение согласно вариантам осуществления изобретения в смеси по меньшей мере с одним фармацевтически приемлемым наполнителем, подходящим для производства суспензии. В другом варианте осуществления изобретения фармацевтические композиции могут быть приготовлены в виде дисперсных порошков и гранул, подходящих для приготовления суспензии путем добавления подходящих наполнителей. Наполнители, подходящие для использования в связи с суспензиями, включают в себя суспендирующие средства, такие как натрий-карбоксиметилцеллюлоза, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, трагакантовая камедь, аравийская камедь, диспергирующие или смачивающие средства, такие как природный фосфатид (например, лецитин), продукт конденсации алкиленоксида с жирной кислотой (например, полиоксиэтиленстеарат), продукт конденсации оксида этилена с длинноцепочечным алифатическим спиртом (например, гептадекаэтиленоксицетанол), продукт конденсации оксида этилена с частичным сложным эфиром, произведенным из жирной кислоты и ангидрида гексита (например, полиоксиэтиленсорбитанмоноолеат); полисахариды и полисахаридподобные соединения (например, декстрансульфат); гликозаминогликаны и гликозаминогликанподобные соединения (например, гиалуроновая кислота), и загустители, такие как карбомер, пчелиный воск, твердый парафин или цетиловый спирт. Суспензии также могут содержать один или более консервантов, таких как уксусная кислота, метил- и/или н-пропил п-гидроксибензоат; один или более красителей; один или более ароматизаторов, и один или более подсластителей, таких как сахароза или сахарин. Фармацевтические композиции также могут находиться в виде эмульсий масло-в-воде. Масляной фазой может быть растительное масло, такое как оливковое масло или арахисовое масло, минеральное- 27015252 масло, такое как жидкий парафин, или их смесь. Подходящими эмульгаторами являются природные смолы, такие как аравийская камедь и трагакантовая камедь; природные фосфатиды, такие как соевый лецитин, сложные эфиры или частичные сложные эфиры, произведенные из жирных кислот; ангидриды гексита, такие как сорбитанмоноолеат, и продукты конденсации указанных частичных сложных эфиров с оксидом этилена, такие как полиоксиэтиленсорбитанмоноолеат. Эмульсия также может содержать подсластители и ароматизаторы. Сиропы и эликсиры могут быть приготовлены с подсластителями, такими как глицерин, сорбит или сахароза. Такие препараты также могут содержать средство, уменьшающее раздражение, консервант, ароматизатор или краситель. Кроме того, фармацевтические композиции также могут находиться в виде стерилизованного инъецируемого препарата, такого как стерилизованная инъецируемая водная эмульсия или масляная суспензия. Такая эмульсия или суспензия может быть приготовлена известным в данной области способом, используя такие подходящие диспергирующие или смачивающие средства и суспендирующие средства,которые были упомянуты выше. Стерилизованный инъецируемый препарат также может быть стерилизованным инъецируемым раствором или суспензией в нетоксическом парентерально приемлемом разбавителе или растворителе, таком как раствор в 1,2-пропандиоле. Стерилизованные инъецируемые препараты также могут быть приготовлены в виде лиофилизированного порошка. Среди приемлемых носителей и растворителей могут быть использованы вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерилизованные нелетучие масла могут быть использованы в качестве растворителя или суспендирующей среды. Для этой цели может быть использовано любое безвкусное нелетучее масло, включая синтетические моно- и диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, также могут быть использованы при приготовлении инъецируемых препаратов. Для получения устойчивой водорастворимой дозированной формы фармацевтической композиции фармацевтически приемлемую соль соединения, приведенного в описании, можно растворить в водном растворе органической или неорганической кислоты, такой как 0,3 М раствор янтарной кислоты, или,более предпочтительно, лимонной кислоты. Если растворимая солевая форма является недоступной, соединение можно растворить в подходящем сорастворителе или в комбинации сорастворителей. Примеры подходящих сорастворителей включают спирт, пропиленгликоль, полиэтиленгликоль 300, полисорбат 80, глицерин и тому подобное в концентрациях, колеблющихся приблизительно от 0 до 60% общего объема. В одном варианте осуществления изобретения активное соединение растворяют в ДМСО и разбавляют водой. Фармацевтическая композиция также может находиться в виде раствора соли активного ингредиента в соответствующем водном носителе, таком как вода или изотонический физиологический раствор или раствор декстрозы. Также рассматриваемыми являются соединения, которые были модифицированы замещениями или добавлениями химических или биохимических фрагментов, которые делают их более подходящими для доставки (например, повышение растворимости, биоактивности, вкусовой привлекательности, снижения вредных реакций и т.д.), например, путем этерификации, гликозилирования, ПЭГилирования и т.д. В предпочтительном варианте осуществления изобретения соединения, приведенные в описании,могут быть приготовлены для перорального введения в виде препарата на основе липидов, подходящего для соединений с низкой растворимостью. Препараты, основанные на липидах, в целом, могут усиливать пероральную биодоступность таких соединений. По существу, предпочтительная фармацевтическая композиция содержит терапевтически или профилактически эффективное количество приведенного в описании соединения вместе по меньшей мере с одним фармацевтически приемлемым наполнителем, выбранным из группы, состоящей из жирных кислот со средней длиной цепи или их сложных эфиров с пропиленгликолем (например, пропиленгликолевые эфиры пищевых жирных кислот, таких как каприловая и каприновая жирные кислоты) и фармацевтически приемлемых поверхностно-активных веществ, таких как полиоксил-40-гидрогенизованное касторовое масло. В альтернативном предпочтительном варианте осуществления изобретения циклодекстрины могут быть добавлены в качестве повышающих растворимость в воде средств. Предпочтительные циклодекстрины включают гидроксипропил, гидроксиэтил, глюкозильные, мальтозильные и мальтотриозильные производные -, - и -циклодекстрина. Особенно предпочтительным средством, усиливающим растворимость циклодекстрина, является гидроксипропил-о-циклодекстрин (ВРВС), который может быть добавлен к любой из вышеописанных композиций для дальнейшего улучшения характеристик растворимости в воде соединений согласно вариантам осуществления изобретения. В одном варианте осуществления изобретения композиция содержит приблизительно от 0,1 до 20% гидроксипропил-оциклодекстрина, более предпочтительно приблизительно от 1 до 15% гидроксипропил-о-циклодекстрина и наиболее предпочтительно приблизительно от 2,5 до 10% гидроксипропил-о-циклодекстрина. Количество используемого средства, усиливающего растворимость, будет зависеть от количества соединения,согласно вариантам осуществления изобретения, в композиции. Фармацевтическая композиция содержит общее количество активного ингредиента(ов), достаточ- 28015252 ное для достижения намеченного терапевтического эффекта. Точнее, в некоторых вариантах осуществления изобретения фармацевтическая композиция содержит терапевтически эффективное количество(например, количество SAPK-модулирующего соединения, которое является эффективным в предотвращении или лечении симптомов воспалительного заболевания или состояния, где соединение имеет ЕС 50 в области приблизительно от 1 до 1000 мкМ, предпочтительно приблизительно от 50 до 650 мкМ, для ингибирования по меньшей мере одной MAPK р 38). Общие количества соединения, которые могут быть объединены с материалами-носителями для получения однократной дозированной формы, будут зависеть от хозяина, подвергаемого лечению, и отдельного способа введения. Предпочтительно, композиции приготавливают так, что дозу между 0,01 и 100 мг/кг массы тела/день SAPK-модулирующего соединения вводят больному, получающему композиции. Пример 1. Соединения отбирали по их способности ингибировать фосфорилирование ATF-2 МАР-киназой р 38 in vitro. Способность соединений ингибировать фосфорилирование ATF-2 в таком анализе in vitro коррелирует с ингибированием экспрессии МАР-киназы р 38 и TNF- in vivo и поэтому является показателем потенциальной in vivo терапевтической активности (Raingeaud, J. et al. 1995 J. Biol. Chem. 270: 7420-7426; Brinkraan, M.N., et al. 1999 J. Biol. Chem. 274: 30882-30886; и Fuchs, S.Y. et al. J. Biol. Chem. 275: 12560-12564, 2000). Все киназы и субстрат ATF-2 приобретены у Upstate (Charlottsville, VA) . МАР-киназы р 38 являются рекомбинантными человеческими полноразмерными белками с аминоконцевым GST-слиянием, экспрессированными в Е. coli и выделенными из Е. coli. ATF-2 является GST-слитым белком, содержащим аминокислоты 19-96 ATF-2 человека, экспрессированного в Е. coli. Все белки разлиты по аликвотам и хранились при -80 С. Анализ МАР-киназы р 38 осуществляли, используя буфер для анализа, содержащий 25 мМ HEPES,рН 7,5, 10 мМ MgCl2, 2 мМ DTT, 20 мМ -глицерофосфата, 0,1 мМ Na3VO4, 40 мкМ АТР и 1,25 мкМ АТР-2, вместе с 6 нг белка р 38, 12 нг белка р 38, 1,5 нг р 38 или 0,4 нг JNK22. Соединения сериями разбавляли в ДМСО, и 2 мкл испытуемого соединения при различных концентрациях использовали. Для контрольного образца использовали только ДМСО. Испытуемые соединения предварительно инкубировали с 20 мкл фермента в киназном буфере (25 мМHEPES, рН 7,5, 10 мМ MgCl2, 2 мМ DTT, 20 мМ -глицерофосфата и 0,1 мМ Na3VO4) при комнатной температуре в течение 15 мин. Реакции инициировали путем добавления 30 мкл раствора субстрата с получением конечной концентрации 40 мкМ АТР и 1,2 5 мкМ ATF-2 в киназном буфере. Реакционные смеси инкубировали в течение 30 минут при 37 С, и реакции заканчивали путем добавления 18 мкл 200 мМ ЭДТА.ELISA-метод использовали для определения фосфорилирования ATF-2 в положении аминокислотного остатка Thr 69. 96-луночные планшеты с высоким связыванием покрывали слоем 50 мкл реакционного раствора киназы в течение 1 часа при 37 С. Покрытые планшеты промывали 200 мкл буфера для промывки (25 мМ Трис НС 1, рН 8,3, 192 мМ глицина, 0,1% SDS и 0,05% Твина-20) три раза. Затем планшеты промывали три раза SuperBlocK в TBS (Pierce, 37535). После блокировки планшеты инкубировали с 50 мкл кроличьего антитела против фосфо-АТР-2 (Cell Signaling, 9221L, 1:500) в течение 30 мин при 37 С. Планшеты промывали три раза буфером для промывки до инкубации с 50 мкл HRP-конъюгированного козьего антитела против антитела кролика (Cell Signaling, 7074, 1:500) в течение 30 мин при 37 С. Затем планшеты промывали три раза буфером для промывки до инкубации с 50 мкл Ultra TMB-ELISA(Pierce, 34028) в течение 8 минут при комнатной температуре. В заключение, 50 мкл фосфорной кислоты добавляли для остановки реакций, и абсорбцию образцов планшета считывали при 450 нм на планшетридере SpectraMax 250. Соединения ингибируют фосфорилирование ATF-2 в анализе in vitro. Предпочтительные соединения обнаруживают величины ЕС 50 приблизительно между 1 мкМ и 1000 мкМ, предпочтительно приблизительно от 50 мкМ до 650 мкМ. Пример 2. Соединения отбирали по их способности ингибировать высвобождение TNF- из клеток ТНР-1,стимулированных липополисахаридом (LPS) in vitro. Способность соединений ингибировать высвобождение TNF- в этом анализе in vitro коррелирует с ингибированием активности р 38 и TNF-, и поэтому является показателем потенциальной in vivo терапевтической активности (Lee J.С. et al. 1993 Ann. N.Y.Acad. Sci. 696: 149-170, и 1994 Nature 372: 739-746). Клетки ТНР-1 из ATCC (TIB202) поддерживали при 37 С, 5% CO2 в среде RPMI 1640 (MediaTech,Herndon, VA), содержащей 4,5 г/л глюкозы, снабженной 10% эмбриональной бычьей сывороткой, 1% пенициллином/стрептомицином и 50 мкМ -меркаптоэтанола. Испытуемые соединения вначале растворяли в среде RPMI с 1% ДМСО (об./об.). Затем соединения последовательно разбавляли в RPMI-среде для всех последующих разведений. Анализ осуществляли в стерильных условиях. Клетки ТНР-1 при плотности культуры 6-8105 клеток/мл собирали и ресуспендировали в RPMI-среде при плотности 106 клеток/мл. Ресуспендированные клетки в количестве 100 мкл добавляли к каждой лунке, которая содержала 100 мкл испытуемого соединения. Испытуемые соедине- 29
МПК / Метки
МПК: A61P 11/00, A61P 13/12, A61K 31/4412, A61K 31/44, A61P 9/00, A61P 29/00, A61P 43/00, A61K 31/4704
Метки: системы, модуляции, протеинкиназной, стресс-активированной, способ
Код ссылки
<a href="https://eas.patents.su/30-15252-sposob-modulyacii-stress-aktivirovannojj-proteinkinaznojj-sistemy.html" rel="bookmark" title="База патентов Евразийского Союза">Способ модуляции стресс-активированной протеинкиназной системы</a>
Предыдущий патент: Производные хиназолина и их использование при лечении тромбоцитемии
Следующий патент: Производные 3,6-дигидро-2-оксо-6н-1,3,4-тиадиазина
Случайный патент: Фармацевтическая композиция, включающая новый холиновый сокристалл эпалрестата