Триазолофталазины
Номер патента: 14324
Опубликовано: 29.10.2010
Авторы: Клей Ханс-Петер, Вайнбреннер Штеффен, Шмидт Беате, Тенор Германн, Флоккерци Дитер, Кюльцер Раймунд
Формула / Реферат
1. Соединения формулы I
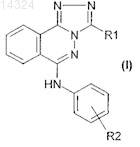
в которой
R1 обозначает -U-A, где
U обозначает непосредственную связь или метилен (-СН2-),
А обозначает фенил, пиридинил, тиофенил, ди-(С1-С4-алкокси)фенил, или R11-замещенный фенил, где
R11 обозначает С1-С4-алкил, галоген, трифторметил, гидроксил, С1-С4-алкоксигруппу, полностью или преимущественно фторзамещенную С1-С4-алкоксигруппу, феноксигруппу, С1-С4-алкоксикарбонил, морфолиновую группу или ди-С1-С4-алкиламиногруппу,
R2 обозначает аминогруппу, карбоксил, С1-С4-алкоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, где
R3 обозначает С1-С4-алкил, С2-С4-алкенил, С3-С7-циклоалкил, трифторметил, фенил, R31-замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный C1-C4-алкил или 1N-(R33)-пиперидинил, где R31 обозначает С1-С4-алкоксигруппу, морфолиновую группу или ди-С1-С4-алкиламиногруппу,
R32 обозначает гидроксил, фенил-С1-С4-алкоксигруппу, С1-С4-алкоксигруппу, фенил, R321-замещенный фенил, ди-С1-С4-алкиламиногруппу, морфолиновую группу или 4N-(R322)пиперазин-1-ил, где
R321 обозначает С1-С4-алкоксигруппу,
R322 обозначает С1-С4-алкил,
R33 обозначает водород, C1-C4-алкил или C1-C4-алкилкарбонил,
R4 обозначает водород, C1-C4-алкил, R41-замещенный С2-С4-алкил, фенил, R42-замещенный фенил или пиридинил, где
R41 обозначает гидроксил, C1-C4-алкоксигруппу, ди-C1-C4-алкиламиногруппу или морфолиновую группу,
R42 обозначает C1-C4-алкоксигруппу или ди-C1-C4-алкиламиногруппу,
R5 обозначает водород или C1-C4-алкил,
или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклический радикал Het, где
Het обозначает морфолиновую группу или 4N-(C1-C4-алкил)пиперазин-1-ил,
и соли этих соединений.
2. Соединения формулы I по п.1, в которой R1 обозначает -U-A, где
U обозначает непосредственную связь или метилен (-СН2-),
А обозначает фенил, пиридинил, тиофенил, диметоксифенил, или R11-замещенный фенил, где
R11 обозначает метил, трет-бутил, хлор, фтор, бром, трифторметил, гидроксил, метоксигруппу, этоксигруппу, трифторметоксигруппу, феноксигруппу, метоксикарбонил, морфолиновую группу или диметиламиногруппу,
R2 обозначает аминогруппу, карбоксил, C1-C4-алкоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, где
R3 обозначает C1-C4-алкил, С2-С4-алкенил, С3-С7-циклоалкил, трифторметил, фенил, R31-замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный C1-C4-алкил или 1N-(R33)-пиперидинил, где R31 обозначает C1-C4-алкоксигруппу, морфолиновую группу или ди-C1-C4-алкиламиногруппу,
R32 обозначает гидроксил, фенил-C1-C4-алкоксигруппу, C1-C4-алкоксигруппу, фенил, R321-замещенный фенил, ди-C1-C4-алкиламиногруппу, морфолиновую группу или 4N-(R322)пиперазин-1-ил,
где R321 обозначает C1-C4-алкоксигруппу,
R322 обозначает C1-C4-алкил,
R33 обозначает водород, C1-C4-алкил или C1-C4-алкилкарбонил,
R4 обозначает водород, C1-C4-алкил, R41-замещенный С2-С4-алкил, фенил, R42-замещенный фенил или пиридинил, где
R41 обозначает гидроксил, C1-C4-алкоксигруппу, ди-C1-C4-алкиламиногруппу или морфолиновую группу,
R42 обозначает C1-C4-алкоксигруппу или ди-C1-C4-алкиламиногруппу,
R5 обозначает водород или C1-C4-алкил,
или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклической радикал Het, где
Het обозначает морфолиновую группу или 4N-(С1-С4-алкил)пиперазин-1-ил,
и соли этих соединений.
3. Соединения формулы I по п.1, в которой R1 обозначает -U-A, где
U обозначает непосредственную связь или метилен (-СН2-), А обозначает фенил или R11-замещенный фенил, где R11 обозначает метил, хлор, фтор, бром, трифторметил, гидроксил, метоксигруппу, феноксигруппу, метоксикарбонил или диметиламиногруппу, R2 обозначает аминогруппу, карбоксил, метоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, где
R3 обозначает метил, винил, циклопропил, циклогексил, трифторметил, фенил, R31-замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный С1-С2-алкил или 1N-(R33)пиперидинил, где R31 обозначает метоксигруппу, морфолиновую группу или диметиламиногруппу,
R32 обозначает гидроксил, бензилоксигруппу, метоксигруппу, фенил, R321-замещенный фенил, диметиламиногруппу, морфолиновую группу или 4N-метилпиперазин-1-ил, где R321 обозначает метоксигруппу, R33 обозначает водород, метил или ацетил,
R4 обозначает водород, метил, 2-(R41)этил, фенил, R42-замещенный фенил или пиридинил, где
R41 обозначает гидроксил, метоксигруппу, диметиламиногруппу или морфолиновую группу,
R42 обозначает метоксигруппу или диметиламиногруппу,
R5 обозначает водород или метил,
или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклический радикал Het, где
Het обозначает морфолиновую группу или 4N-метилпиперазин-1-ил,
и соли этих соединений.
4. Соединения формулы I по п.1, в которой R1 обозначает -U-A, где U обозначает непосредственную связь, А обозначает фенил или R11-замещенный фенил, где R11 обозначает фтор, бром, трифторметил или метоксигруппу, R2 присоединен в мета- или пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе триазолофталазинового скелета, и обозначает аминогруппу, карбоксил, метоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, где
R3 обозначает метил, винил, циклопропил, циклогексил, трифторметил, фенил, R31-замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный C1-С2-алкил или 1N-(R33)пиперидинил, где R31 обозначает метоксигруппу, морфолиновую группу или диметиламиногруппу,
R32 обозначает гидроксил, бензилоксигруппу, метоксигруппу, фенил, R321-замещенный фенил, диметиламиногруппу, морфолиновую группу или 4N-метилпиперазин-1-ил, где R321 обозначает метоксигруппу, R33 обозначает водород, метил или ацетил,
R4 обозначает водород, метил, 2-(R41)этил, фенил, R42-замещенный фенил или пиридинил, где
R41 обозначает гидроксил, метоксигруппу, диметиламиногруппу или морфолиновую группу,
R42 обозначает метоксигруппу или диметиламиногруппу,
R5 обозначает водород или метил,
или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклический радикал Het, где
Het обозначает морфолиновую группу или 4N-метилпиперазин-1-ил,
и соли этих соединений.
5. Соединения формулы I по п.1, в которой R1 обозначает -U-A, где U обозначает непосредственную связь, А обозначает фенил или R11-замещенный фенил, где
R11 обозначает фтор, бром, хлор, трифторметил, метил или метоксигруппу, R2 присоединен в мета- или пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе триазолофталазинового скелета, и обозначает аминогруппу, карбоксил, метоксикарбонил,
-N(H)-C(O)R3 или -C(O)-N(R4)R5, где
R3 обозначает метил, винил, циклопропил, циклогексил, трифторметил, фенил, R31-замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный С1-С2-алкил или 1N-(R33)пиперидинил, где R31 обозначает метоксигруппу, морфолиновую группу или диметиламиногруппу,
R32 обозначает гидроксил, бензилоксигруппу, метоксигруппу, фенил, R321-замещенный фенил, диметиламиногруппу, морфолиновую группу или 4N-метилпиперазин-1-ил, где R321 обозначает метоксигруппу, R33 обозначает водород, метил или ацетил,
R4 обозначает водород, метил, 2-(R41)этил, фенил, R42-замещенный фенил или пиридинил, где
R41 обозначает гидроксил, метоксигруппу, диметиламиногруппу или морфолиновую группу, R42 обозначает метоксигруппу или диметиламиногруппу,
R5 обозначает водород или метил,
или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклический радикал Het, где
Het обозначает морфолиновую группу, 4N-метилпиперазин-1-ил или 4N-этилпиперазин-1-ил,
и соли этих соединений.
6. Соединения формулы I по любому из пп.1-5, в которой R1 обозначает 4-метоксифенил, 2-метоксифенил, 2-бромфенил, 2-фторфенил, 2-(трифторметил)фенил, 2-хлорфенил, 4-бромфенил или 2-метилфенил, и соли этих соединений.
7. Соединения формулы I, выбранные из следующей группы:
{4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенил}амид циклопропанкарбоновой кислоты,
{3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенил}амид циклопропанкарбоновой кислоты и
1-{4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенил}-1-(4-метилпиперазин-1-ил)метанон.
8. Фармацевтическая композиция, включающая одно или более соединений формулы I по любому из пп.1-7 совместно с фармацевтическими инертными наполнителями и/или вспомогательными веществами.
9. Применение соединений формулы I по любому из пп.1-7 для приготовления фармацевтических композиций, предназначенных для лечения заболеваний, связанных с активностью ФДЭ2 (фосфодиэстеразы 2), таких как состояния патологически усиленной эндотелиальной активности и нарушенной функции эндотелиального барьера, таких как септический шок и сосудистый отек.
10. Применение соединений формулы I по любому из пп.1-7 для приготовления фармацевтических композиций, предназначенных для лечения (1) состояний, связанных с патологически усиленным неоангиогенезом, таких как все типы опухолей (доброкачественных или злокачественных), или (2) всех типов воспалительных заболеваний, связанных с неоангиогенезом, таких как нарушения типа артрита.
11. Способ лечения состояний патологически усиленной эндотелиальной активности и нарушенной функции эндотелиального барьера, таких как септический шок и сосудистый отек, у нуждающегося в нем пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по любому из пп.1-7.
12. Способ лечения (1) патологических состояний, связанных с патологически усиленным неоангиогенезом, таких как все типы опухолей (доброкачественных или злокачественных), или (2) всех типов воспалительных заболеваний, связанных с неоангиогенезом, таких как нарушения типа артрита, у нуждающегося в нем пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по любому из пп.1-7.
13. Применение соединений формулы I по любому из пп.1-7 для приготовления фармацевтических композиций, предназначенных для лечения пневмонии или острого респираторного дистресс синдрома (ARDS) при септическом шоке.
14. Применение соединений формулы I по любому из пп.1-7 для приготовления фармацевтических композиций, предназначенных для лечения острых и хронических нарушений дыхательных путей.
15. Применение по п.14, где острые и хронические нарушения дыхательных путей выбраны из ринита, бронхита, бронхиальной астмы, эмфиземы, хронического обструктивного заболевания легких (COPD).
16. Способ лечения пневмонии или острого респираторного дистресс синдрома (ARDS) при септическом шоке у нуждающегося в этом пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по любому из пп.1-7.
17. Способ лечения острых и хронических нарушений дыхательных путей у нуждающегося в этом пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по любому из пп.1-7.
18. Способ по п.17, где острые и хронические нарушения дыхательных путей выбраны из ринита, бронхита, бронхиальной астмы, эмфиземы, хронического обструктивного заболевания легких (COPD).
Текст
В изобретении описаны соединения формулы I в которой R1 и R2 обладают значениями, указанными в описании, являющиеся новыми эффективными ингибиторами ФДЭ 2. 014324 Область техники, к которой относится изобретение Настоящее изобретение относится к новым производным триазолофталазина, которые можно применять в фармацевтической промышленности для изготовления фармацевтических композиций. Предшествующий уровень Триазолофталазины известны в предшествующем уровне техники. Например, в ЕР 85840,WO98/04559, WO98/50385, WO99/06407 (US6313125), WO02/083140, US6525055, ЕР 0728759 (US 6001830); J. Med. Chem., (1988), 31, 1115-1123; J. Med. Chem., (2004), 47, 1807-1822, и J. Med. Chem.,(2004), 47, 2176-2179 описаны различным образом замещенные триазолофталазины. Однако в них не описаны замещенные анилином производные триазолофталазина в значении, соответствующем настоящему изобретению. Кроме того, производные триазолофталазина никогда не были описаны как ингибиторы ФДЭ 2(фосфодиэстеразы). Описание изобретения Согласно изобретению было установлено, что новые производные триазолофталазина, которые подробно описаны ниже, обладают неожиданными и особенно полезными характеристиками. Таким образом, первым объектом (объекта) настоящего изобретения являются соединения формулы IR11 обозначает С 1-С 4-алкил, галоген, трифторметил, гидроксил, С 1-С 4-алкоксигруппу, полностью или преимущественно фторзамещенную С 1-С 4-алкоксигруппу, феноксигруппу, С 1-С 4-алкоксикарбонил,морфолиновую группу или ди-С 1-С 4-алкиламиногруппу,R2 обозначает аминогруппу, карбоксил, С 1-С 4-алкоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5,гдеR31 обозначает С 1-С 4-алкоксигруппу, морфолиновую группу или ди-С 1-С 4-алкиламиногруппу,R32 обозначает гидроксил, фенил-С 1-С 4-алкоксигруппу, С 1-С 4-алкоксигруппу, фенил, R321 замещенный фенил, ди-С 1-С 4-алкиламиногруппу, морфолиновую группу или 4N-(R322)пиперазин-1-ил,гдеR41 обозначает гидроксил, C1-C4-алкоксигруппу, ди-C1-C4-алкиламиногруппу или морфолиновую группу,R42 обозначает C1-C4-алкоксигруппу или ди-C1-C4-алкиламиногруппу,R5 обозначает водород или C1-C4-алкил,или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклической радикал Het, гдеHet обозначает морфолиновую группу или 4N-(C1-C4-алкил)пиперазин-1-ил,и соли этих соединений.C1-C4-алкил означает линейный или разветвленный алкильный радикал, содержащий от 1 до 4 атомов углерода. Примерами являются бутильный, изобутильный, втор-бутильный, трет-бутильный, пропильный, изопропильный и предпочтительно этильный и метильный радикалы. С 2-С 4-алкил означает линейный или разветвленный алкильный радикал, содержащий от 2 до 4 атомов углерода. Примерами являются бутильный, изобутильный, втор-бутильный, трет-бутильный, пропильный, изопропильный и этильный радикалы. С 3-С 7-циклоалкил обозначает циклопропил, циклобутил, циклопентил, циклогексил и циклогептил,из которых следует особо отметить циклопропил, циклопентил и циклогексил.-1 014324 С 2-С 4-алкенил означает линейный или разветвленный алкенильный радикал, содержащий от 2 до 4 атомов углерода. Примерами являются этенильный (винильный), 2-бутенильный, 3-бутенильный, 1 пропенильный и 2-пропенильный (аллильный) радикалы. Галоген в настоящем изобретении означает йод или предпочтительно бром, хлор или фтор.C1-C4-алкоксигруппа означает радикалы, которые в дополнение к атому кислорода содержат линейный или разветвленный алкильный радикал, содержащий от 1 до 4 атомов углерода. Примерами, которые можно отметить, являются бутоксильный, изобутоксильный, втор-бутоксильный, третбутоксильный, пропоксильный, изопропоксильный и предпочтительно этоксильный и метоксильный радикалы.C1-C4-алкоксикарбонил означает карбонильную группу, к которой присоединен один из указанных выше C1-C4-алкоксильных радикалов. Примерами являются метоксикарбонильный (СН 3 О-С(О)-) и этоксикарбонильный (СН 3 СН 2 О-С(О)-) радикал. С 3-С 7-циклоалкилметоксигруппа означает циклопропилметоксигруппу, циклобутилметоксигруппу,циклопентилметоксигруппу, циклогексилметоксигруппу или циклогептилметоксигруппу, из которых следует отметить циклопропилметоксигруппу и циклопентилметоксигруппу.C1-C2-алкилендиоксигруппа означает, например, метилендиоксильный (-O-СН 2-О-) или метилендиоксильный радикал (-О-СН 2-СН 2-О-). Полностью или преимущественно фторзамещенная C1-C4-алкоксигруппа означает, например,2,2,3,3,3-пентафторпропоксильный, перфторэтоксильный, 1,2,2-трифторэтоксильный и предпочтительно,1,1,2,2-тетрафторэтоксильный, 2,2,2-трифторэтоксильный, трифторметоксильный и дифторметоксильный радикал, из которых предпочтительным является дифторметоксильный радикал. "Преимущественно" в этом контексте означает, что более половины атомов водорода С 1-С 4-алкоксигрупп замещены атомами фтора. Ди-C1-C4-алкиламиногруппа означает аминогруппу, которая замещена двумя разными или двумя одинаковыми из указанных выше C1-C4-алкильных радикалов. Примерами являются диметиламиновый,диэтиламиновый и диизопропиламиновый радикал. Ди-(C1-C4-алкокси)фенил означает фенильный радикал, который в любых возможных положениях замещен двумя из указанных выше C1-C4-алкоксильных радикалов, которые могут быть одинаковыми или разными. Моно- или ди-C1-C4-алкиламиновые радикалы в дополнение к атому азота содержат один или два из указанных выше C1-C4-алкильных радикалов. Предпочтительными являются ди-C1-C4-алкиламиновые радикалы, предпочтительно - диметиламиновый, диэтиламиновый и диизопропиламиновый радикал. Фенил-C1-C4-алкоксигруппа означает один из указанных выше C1-C4-алкоксильных радикалов, который замещен фенильным радикалом. Примерами, которые можно отметить, являются бензилоксильный и фенетоксильный радикал.C1-C4-алкилкарбонил означает карбонильную группу, к которой присоединен один из указанных выше C1-C4-алкильных радикалов. Примером является ацетильный радикал (СН 3 СО-). Если не указано иное, то все отмеченные в настоящем изобретении гетероциклические группы означают все их возможные изомерные формы. Если не указано иное, то все отмеченные в настоящем изобретении гетероциклические группы предпочтительно означают все их возможные позиционные изомеры. Так, например, термин пиридил или пиридинил, по отдельности или в качестве части другой группы, включает пиридин-2-ил, пиридин-3-ил и пиридин-4-ил; или 1N-(R33)пиперидинил включает 1N(R33)пиперидин-2-ил, 1N-(R33)пиперидин-3-ил и 1N-(R33)пиперидин-4-ил. 1N-(R33)пиперидинил означает пиперидинильный радикал, который замещен с помощью R33 по атому азота, такой как, например, любой радикал, который выбран из группы, включающей пиперидин 2-ил, пиперидин-3-ил и пиперидин-4-ил, и который замещен с помощью R33 по атому азота. 4N-(R322)пиперазин-1-ил означает пиперазин-1-ильный радикал, который замещен по атому азота в положении 4 с помощью R322. 4N-(С 1-С 4-алкил)пиперазин-1-ил означает пиперазин-1-ильный радикал, который замещен по атому азота в положении 4 одним из указанных выше С 1-С 4-алкильных радикалов, такой как, например, 4Nметилпиперазин-1-ил. 2-(R41)этил означает этильный радикал, замещенный в положении 2 с помощью R41. Следует понимать, что, если в настоящем изобретении указано, что два структурных фрагмента соединений, предлагаемых в настоящем изобретении, соединены компонентом, который означает "связь",то указанные два фрагмента непосредственно присоединены друг к другу с помощью ординарной связи. Соединения, для которых в настоящем изобретении указано, что они являются замещенными, могут быть замещены в любом возможном положении, если не указано иное. Заместитель R2 соединений формулы I может быть присоединен в орто-, мета- или пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе, и предпочтение отдается присоединению в мета-положение или более предпочтительно в пара-положение. Если в любом компоненте какая-либо группа содержится более одного раза, то каждое ее значение-2 014324 является независимым. Подходящими солями соединений, предлагаемых в настоящем изобретении, в зависимости от замещения, являются все соли присоединения с кислотами или все соли с основаниями. Можно особо отметить фармакологически переносимые соли с неорганическими и органическими кислотами и основаниями, обычно применяющиеся в фармацевтике. Подходящими являются, с одной стороны, нерастворимые в воде и предпочтительно - растворимые в воде соли присоединения с кислотами, такими как, например, хлористо-водородная кислота, бромисто-водородная кислота, фосфорная кислота, азотная кислота, серная кислота, уксусная кислота, лимонная кислота, D-глюконовая кислота, бензойная кислота,2-(4-гидроксибензоил)бензойная кислота, масляная кислота, сульфосалициловая кислота, малеиновая кислота, лауриновая кислота, яблочная кислота, фумаровая кислота, янтарная кислота, щавелевая кислота, виннокаменная кислота, эмбоновая кислота, стеариновая кислота, толуолсульфоновая кислота, метансульфоновая кислота и 3-гидрокси-2-нафтойная кислота, при получении соли кислоты - в зависимости от того, являются ли они одно- или многоосновными, и в зависимости от того, какая соль требуется - используются в эквимолярном или не равном ему количестве. С другой стороны, в зависимости от замещения также пригодными являются соли с основаниями. В качестве примеров солей с основаниями отмечаются соли лития, натрия, калия, кальция, алюминия, магния, титана, аммония, меглуминовые и гуанидиниевые соли, и в этом случае основание используется для получения соли в эквимолярном или не равном ему количестве. Фармакологически непереносимые соли, которые можно получить, например, в качестве промежуточных продуктов во время получения соединений, предлагаемых в настоящем изобретении, в промышленном масштабе, превращают в фармакологически переносимые соли по методикам, известным специалисту в данной области техники. Как известно специалистам, соединения, предлагаемые в настоящем изобретении, а также их соли могут содержать, например, при выделении в кристаллической форме, переменные количества растворителей. Поэтому в объем настоящего изобретения входят все сольваты и, в частности, все гидраты соединений, предлагаемых в настоящем изобретении, а также все сольваты и, в частности, все гидраты солей соединений, предлагаемых в настоящем изобретении. Соединениями, предлагаемыми в настоящем изобретении, которые следует отметить, являются такие соединения формулы I, в которой R1 обозначает -U-A, гдеU обозначает непосредственную связь или метилен (-СН 2-),А обозначает фенил, пиридинил, тиофенил, диметоксифенил, или R11-замещенный фенил, гдеR11 обозначает метил, трет-бутил, хлор, фтор, бром, трифторметил, гидроксил, метоксигруппу,этоксигруппу, трифторметоксигруппу, феноксигруппу, метоксикарбонил, морфолиновую группу или диметиламиногруппу,R2 обозначает аминогруппу, карбоксил, С 1-С 4-алкоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5,гдеR31 обозначает С 1-С 4-алкоксигруппу, морфолиновую группу или ди-С 1-С 4-алкиламиногруппу,R32 обозначает гидроксил, фенил-С 1-С 4-алкоксигруппу, С 1-С 4-алкоксигруппу, фенил, R321 замещенный фенил, ди-С 1-С 4-алкиламиногруппу, морфолиновую группу или 4N-(R322)пиперазин-1-ил,гдеR41 обозначает гидроксил, С 1-С 4-алкоксигруппу, ди-С 1-С 4-алкиламиногруппу или морфолиновую группу,R42 обозначает C1-C4-алкоксигруппу или ди-С 1-С 4-алкиламиногруппу,R5 обозначает водород или С 1-С 4-алкил,или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклический радикал Het, гдеHet обозначает морфолиновую группу или 4N-(С 1-С 4-алкил)пиперазин-1-ил,и соли этих соединений. Соединениями, предлагаемыми в настоящем изобретении, которые следует особенно отметить, являются такие соединения формулы I, в которой R1 обозначает -U-A, гдеU обозначает непосредственную связь или метилен (-СН 2-), А обозначает фенил или R11 замещенный фенил, где R11 обозначает метил, хлор, фтор, бром, трифторметил, гидроксил, метоксигруппу, феноксигруппу, метоксикарбонил или диметиламиногруппу, R2 обозначает аминогруппу, карбоксил, метоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, гдеR3 обозначает метил, винил, циклопропил, циклогексил, трифторметил, фенил, R31-замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный С 1-С 2-алкил или 1N-(R33)пиперидинил,где R31 обозначает метоксигруппу, морфолиновую группу или диметиламиногруппу,R32 обозначает гидроксил, бензилоксигруппу, метоксигруппу, фенил, R321-замещенный фенил,диметиламиногруппу, морфолиновую группу или 4N-метилпиперазин-1-ил, где R321 обозначает метоксигруппу, R33 обозначает водород, метил или ацетил,R4 обозначает водород, метил, 2-(R41)этил, фенил, R42-замещенный фенил или пиридинил, гдеR41 обозначает гидроксил, метоксигруппу, диметиламиногруппу или морфолиновую группу,R42 обозначает метоксигруппу или диметиламиногруппу, R5 обозначает водород или метил,или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклический радикал Het, гдеHet обозначает морфолиновую группу или 4N-метилпиперазин-1-ил,и соли этих соединений. Соединениями, предлагаемыми в настоящем изобретении, которые в еще большей степени следует особенно отметить, являются такие соединения формулы I, в которой R1 обозначает -U-A, где U обозначает непосредственную связь, А обозначает фенил или R11-замещенный фенил, где R11 обозначает фтор, бром, трифторметил или метоксигруппу, где предпочтительноR2 присоединен в мета- или пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе триазолофталазинового скелета, и обозначает аминогруппу, карбоксил, метоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, гдеR31 обозначает метоксигруппу, морфолиновую группу или диметиламиногруппу,R32 обозначает гидроксил, бензилоксигруппу, метоксигруппу, фенил, R321-замещенный фенил,диметиламиногруппу, морфолиновую группу или 4N-метилпиперазин-1-ил, где R321 обозначает метоксигруппу, R33 обозначает водород, метил или ацетил,R4 обозначает водород, метил, 2-(R41)этил, фенил, R42-замещенный фенил или пиридинил, гдеR41 обозначает гидроксил, метоксигруппу, диметиламиногруппу или морфолиновую группу, R42 обозначает метоксигруппу или диметиламиногруппу,R5 обозначает водород или метил,или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклической радикал Het, гдеHet обозначает морфолиновую группу или 4N-метилпиперазин-1-ил,и соли этих соединений. Особое значение придается соединениям формулы I, в которой R1 обозначает -U-A, где U обозначает непосредственную связь, А обозначает фенил или R11-замещенный фенил, где R11 обозначает фтор, бром, хлор, трифторметил, метил или метоксигруппу, R2 присоединен в мета- или пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе триазолофталазинового скелета, и обозначает аминогруппу, карбоксил, метоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, гдеR3 обозначает метил, винил, циклопропил, циклогексил, трифторметил, фенил, R31-замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный С 1-С 2-алкил или 1N-(R33)-пиперидинил,где R31 обозначает метоксигруппу, морфолиновую группу или диметиламиногруппу,R32 обозначает гидроксил, бензилоксигруппу, метоксигруппу, фенил, R321-замещенный фенил,диметиламиногруппу, морфолиновую группу или 4N-метилпиперазин-1-ил, где R321 обозначает метоксигруппу, R33 обозначает водород, метил или ацетил,R4 обозначает водород, метил, 2-(R41)-этил, фенил, R42-замещенный фенил или пиридинил, гдеR41 обозначает гидроксил, метоксигруппу, диметиламиногруппу или морфолиновую группу,R42 обозначает метоксигруппу или диметиламиногруппу, R5 обозначает водород или метил,или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклической радикал Het, гдеHet обозначает морфолиновую группу, 4N-метилпиперазин-1-ил или 4N-этилпиперазин-1-ил,и солям этих соединений. Из числа соединений, предлагаемых в настоящем изобретении, особый интерес представляют те соединения формулы I, которые входят в объеме настоящего изобретения в один или, если это возможно, в большее количество указанных ниже вариантов осуществления. Специальным вариантом осуществления (вариантом осуществления 1) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой U обозначает непосредственную связь и А обозначает фенил или R11-замещенный фенил.-4 014324 Другим специальным вариантом осуществления (вариантом осуществления 2) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которойU обозначает непосредственную связь и А обозначает пиридинил или тиофенил, такой как, например, пиридин-4-ил. Другим специальным вариантом осуществления (вариантом осуществления 3) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которойU обозначает метилен и А обозначает фенил или R11-замещенный фенил. Другим специальным вариантом осуществления (вариантом осуществления 3-1) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R1 обозначает -UA, где U обозначает метилен (-СН 2-), А обозначает фенил или R11-замещенный фенил. Другим специальным вариантом осуществления (вариантом осуществления 3-1-1) соединений,предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R1 обозначает (4-метоксифенил)-метил; и соли этих соединений. Другим специальным вариантом осуществления (вариантом осуществления 4) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которойU обозначает метилен и А обозначает пиридинил или тиофенил, такой как, например, тиофен-2-ил. Другим специальным вариантом осуществления (вариантом осуществления 5) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R2 обозначает-N(H)-C(O)R3. Другим специальным вариантом осуществления (вариантом осуществления 6) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R2 обозначает-C(O)-N(R4)R5. Другим специальным вариантом осуществления (вариантом осуществления 7) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R1 обозначает (4 метоксифенил)метил или 4-метоксифенил. Другим специальным вариантом осуществления (вариантом осуществления 8) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R1 обозначает 4 метоксифенил. Другим специальным вариантом осуществления (вариантом осуществления 9) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R1 обозначает (4 метоксифенил)метил, 2-гидроксифенил, фенил, 3-метоксикарбонилфенил или 4-метоксифенил, 2 метоксифенил, 2-бромфенил, 2-фторфенил или 2-(трифторметил)фенил или 2-хлорфенил, 4-бромфенил,2-метилфенил. Другим специальным вариантом осуществления (вариантом осуществления 10) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R1 обозначает 4 метоксифенил, 2-метоксифенил, 2-бромфенил, 2-фторфенил или 2-(трифторметил)фенил. Другим специальным вариантом осуществления (вариантом осуществления 11) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R1 обозначает 2 бромфенил. Другим специальным вариантом осуществления (вариантом осуществления 12) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которойR3 обозначает 1N-H-пиперидинил, предпочтительно - 1N-Н-пиперидин-2-ил или 1N-H-пиперидин 3-ил. Другим специальным вариантом осуществления (вариантом осуществления 13) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R2 присоединен в мета-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе триазолофталазинового скелета. Другим специальным вариантом осуществления (вариантом осуществления 14) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которойR2 присоединен в пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе триазолофталазинового скелета. Другим специальным вариантом осуществления (вариантом осуществления 15) соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которойR2 присоединен в пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе триазолофталазинового скелета; и-5 014324 Особой группой соединений, предлагаемых в настоящем изобретении, являются такие соединения формулы I, в которой R1 обозначает 4-метоксифенил или 2-бромфенил,R2 присоединен в пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе триазолофталазинового скелета, и обозначает -N(H)-C(O)R3, гдеR3 обозначает 1N-H-пиперидинил, предпочтительно - 1N-Н-пиперидин-2-ил или 1N-Н-пиперидин 3-ил. Соединения, предлагаемые в настоящем изобретении, можно получить, например, как в качестве примера описано ниже и по указанным ниже стадиям реакций, или предпочтительно так, как в качестве примера описано в приведенных ниже примерах или аналогичным или сходным образом по методикам получения или схемам синтеза, известным специалисту в данной области техники. Как показано ниже на схеме реакции 1, соединения формулы I, в которой R1 и R2 обладают теми из указанных выше значений, которые являются подходящими для условий реакции нуклеофильного замещения, по которой их получают, можно получить из соответствующих соединений формулы II, в которой X обозначает подходящую отщепляющуюся группу, предпочтительно хлор, по реакции с соответствующим производным анилина формулы III. Указанную реакцию нуклеофильного замещения можно проводить, как это описано в приведенных ниже примерах или как известно специалисту; таким образом, в зависимости от реакционной способности реагентов, ее можно проводить путем сплавления компонентов реакции друг с другом без растворителя или по реакции компонентов реакции друг с другом в подходящем растворителе, таком как, например, N,N-диметилформамид, в присутствии подходящего основания, такого как, например, гидрид натрия или карбонат калия, при температуре, обеспечивающей протекание реакции (такой может быть,например, в зависимости от реагентов, температура окружающей среды, повышенная температура или температура кипения использующегося растворителя или, при соответствующих условиях, превышающая ее), необязательно при воздействии микроволнового излучения. Соединения формулы III являются известными или их можно получить известным образом. Соединения формулы II можно получить так, как описано ниже в настоящем изобретении. Схема реакции 1 Изоамиды формулы Ia', приведенной ниже, в которой R1 и R3 обладают указанными выше значениями, в особенности такие, которые нельзя получить с помощью стратегии синтеза, представленной на схеме реакции 1 выше, можно получить, как это показано на схеме реакции 2 ниже, ацилированием соединений формулы Ia, в которой R1 обладает указанными выше значениями, соединениями формулы R3C(O)Y, в которой Y обозначает подходящую отщепляющуюся группу, такую как, например, хлор, при условиях, которые сами по себе известны специалисту. Альтернативно, соединения формулы Ia' также можно получить из соответствующих соединений формулы Ia и соответствующих соединений формулы R3-C(O)Y, в которой Y обозначает гидроксил, по реакции с реагентами, образующими амидную связь, известными специалисту в данной области техники при условиях, известных специалисту. Примерами реагентов, образующих амидную связь, известных специалисту в данной области техники, которые можно отметить являются, например, карбодиимиды(например,дициклогексилкарбодиимид или предпочтительно 1-этил-3-(3-диметиламинопропил)карбодиимидгидрохлорид), производные азодикарбоновой кислоты (например, диэтилазодикарбоксилат),урониевые соли[например,O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийтетрафторборат или О-(бензотриазол-1 у 1)-N,N,N',N'-тетраметилуронийгексафторфосфат] и N,N'карбонилдииимдазол. В объеме настоящего изобретения следует особо отметить 1-этил-3-(3 диметиламинопропил)карбодиимидгидрохлорид (EDC или EDCl). Соединения формулы R3-C(O)Y являются известными или их можно получить известным образом. Соединения формулы Ia можно получить непосредственно, как это показано на схеме реакции 1 и описано выше, путем использования диаминобензола; или их можно получить восстановлением нитрогруппы соединений формулы I, в которой R1 обладает указанными выше значениями и R2 обозначает нитрогруппу, подходящим восстановительным реагентом, таким как, например, дихлорид олова. Соединения формулы I, в которой R1 обладает указанными выше значениями и R2 обозначает нитрогруппу, можно получить по схеме реакции 1. Амиды формулы Ib, приведенной ниже, в которой R1, R4 и R5 обладают указанными выше значениями, в особенности такие, которые нельзя получить с помощью стратегии синтеза, представленной на схеме реакции 1 выше, можно получить, как это показано на схеме реакции 3 ниже путем амидирования бензойных кислот формулы Ib, в которой R1 обладает указанными выше значениями, соответствующими аминами формулы HN(R4)R5 при условиях, которые сами по себе известны специалисту. Эту реакцию амидирования можно проводить в присутствии подходящих реагентов, образующих амидную связь, таких как, например, указанные выше, предпочтительно 1-этил-3-(3 диметиламинопропил)карбодиимидгидрохлорид (EDC или EDCl). Схема реакции 3 Соединения формулы HN(R4)R5 являются известными или их можно получить известным образом. Бензойные кислоты формулы Ib, в которой R1 обладает указанными выше значениями, можно получить омылением соответствующих сложных эфиров формулы I, в которой R2 обозначает С 1-С 4 алкоксикарбонил, предпочтительно метоксикарбонил. Соединения формулы I, в которой R1 обладает указанными выше значениями и R2 обозначает С 1 С 4-алкоксикарбонил, предпочтительно метоксикарбонил, можно получить по схеме реакции 1. Исходные соединения формулы II можно получить, как это показано на схеме реакции 4 или как указано в приведенных ниже примерах; или они известны в данной области техники, например, из публикации R. W. Carling et al., J. Med. Chem. Vol. 47, No. 7, 1807-1822 (2004), или их можно получить по известным методикам или аналогичным или сходным образом с описанными в данной области техники соединениями. Схема реакции 4 Соединения формулы II, в которой R1 обладает указанными выше значениями и X обозначает подходящую отщепляющуюся группу, предпочтительно хлор, можно получить из соответствующих соединений формулы IV или в одну стадию по реакции циклизации с соответствующими соединениями формулы R1-C(O)Z, в которой Z обозначает подходящую отщепляющуюся группу, такую как, например,-7 014324 хлор; или в две стадии через выделяемый промежуточный продукт формулы III, который можно получить ацилированием соединений формулы IV и который затем ввести в последующую реакцию с образованием соединений формулы II по реакции конденсации. Такие реакции можно проводить, как это описано в приведенных ниже примерах, или при условиях,известных специалисту, или аналогично известным в данной области техники сходным реакциям. Таким образом, указанную выше одностадийную реакцию циклизации можно проводить аналогично методике,описанной в публикации J. Med. Chem. Vol. 31, 1988, p. 1115, в подходящем растворителе, таком как,например, толуол, пиридин или диоксан, в присутствии подходящего основания (например, триэтиламина) при повышенной температуре или температуре кипения использующегося растворителя. Соединения формулы IV можно получить посредством нуклеофильного замещения соединений формулы V, в которой X и X' могут быть одинаковыми и обозначают подходящие отщепляющиеся группы, предпочтительно, если X и X' оба обозначают хлор, с гидразином. Соединения формул R1-C(O)Z и V являются известными или их можно получить известным образом. Специалист должен понимать, что некоторые соединения формулы I, предлагаемые в настоящем изобретении, можно превратить в другие соединения формулы I по известным в данной области техники схемам синтеза и реакциям, которые сами по себе известны специалисту с общей подготовкой в данной области техники, таким как, например, описанные выше. Кроме того, специалисту в данной области техники известно, что при наличии в исходном или промежуточном соединении ряда реакционноспособных центров может потребоваться временное блокирование одного или большего количества реакционноспособных центров защитными группами, чтобы обеспечить протекание реакции именно по необходимому реакционному центру. Подробное описание большого количества проверенных защитных групп приведено, например, в публикациях "ProtectiveGroups (Thieme Foundations Organic Chemistry Series N Group" by P. Kocienski (Thieme Medical Publishers,2000). Соединения формулы I, предлагаемые в настоящем изобретении, выделяют и очищают по методикам, которые сами по себе известны, например, путем отгонки растворителя при пониженном давлении и перекристаллизации полученного остатка их подходящего растворителя или с использованием одной из обычных методик очистки, таких как, например, хроматография на колонке, содержащей подходящий наполнитель. Соли получают путем растворения соединения в форме свободного основания или кислоты в подходящем растворителе (например, кетоне, таком как ацетон, метилэтилкетон или метилизобутилкетон,простом эфире, таком как диэтиловый эфир, тетрагидрофуран или диоксан, хлорированном углеводороде, таком как метиленхлорид или хлороформ, или в обладающем низкой молекулярной массой алифатическом спирте, таком как этанол или изопропанол), который содержит необходимую кислоту или основание или к которому затем прибавляют необходимую кислоту или основание. Соли получают путем фильтрования, повторного осаждения, осаждения с помощью вещества, не являющегося растворителем для соли присоединения, или путем выпаривания растворителя. Полученную соль можно превратить в соответствующие свободные соединения, которые, в свою очередь, можно превратить в соли подщелачиванием или подкислением. Таким образом фармакологически неприемлемые соли можно превратить в фармакологически приемлемые соли. Превращения, указанные в настоящем изобретении, можно легко проводить аналогично или сходным образом с методиками, которые сами по себе известны специалисту в данной области техники. Специалисту в данной области техники на основании его/ее подготовки и на основании путей синтеза, которые приведены и описаны в настоящем изобретении, известно, как найти другие возможные пути синтеза соединений формулы I. Все эти другие возможные пути синтеза также являются частью настоящего изобретения. Настоящее изобретение подробно описано и объем настоящего изобретения не ограничивается только описанными характеристиками или вариантами осуществления. Как должно быть известно специалистам в данной области техники, на основании имеющихся в данной области техники знаний и/или,в особенности, на основании раскрытия (например, явного, неявного и специфического раскрытия) настоящего изобретения без отклонения об сущности и объема настоящего изобретения, определяемых прилагаемой формулой изобретения, в него можно внести модификации, аналогии, изменения, вариации,гомологизации и адаптации. Приведенные ниже примеры дополнительно иллюстрируют настоящее изобретение, не налагая ограничений. Кроме того, другие соединения формулы I, получение которых явно не описано, можно получить по аналогичным или сходным методикам или методикам, которые сами по себе известны специалисту в данной области техники с использованием обычных технологий. Соединения формулы I, предлагаемые в настоящем изобретении, которые указаны в представленных ниже примерах, в особенности указанные в качестве конечных соединений, а также их соли являются предпочтительным объектом настоящего изобретения.-8 014324 В примерах МС означает масс-спектр, а другие аббревиатуры обладают обычными значениями, которые сами по себе известны специалисту. Примеры Конечные соединения: 1. N-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]-бензол-1,4-диамин 1,0 г 6-Хлор-3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин (соединение A1) и 2,7 г пфенилендиамин перемешивают при 170 С в течение 5 ч. Реакционную смесь разбавляют с помощью 6 мл этанола и осадок отфильтровывают с отсасыванием. Твердое вещество перекристаллизовывают из N,Nдиметилформамида и получают 1,04 г искомого соединения (т.пл.: 295 С). ЭФ (элементарная формула):C22H18N6O (382,43) найдено: [М+1] 383,3 Альтернативная методика проведения реакции I: 100 мг 6-Хлор-3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазина (соединение А 1), 1-3 ммоля соответствующего производного анилина и 30 мг карбоната калия перемешивают в 2,5 мл N,Nдиметилформамида при 140 С в течение 4 ч или при 200 С в течение 10 мин при нагревании микроволновым излучением. Реакционную смесь разбавляют смесью дихлорметан/вода или раствором гидроксида натрия, осадок отфильтровывают с отсасыванием, промывают водой и перекристаллизовывают из N,Nдиметилформамида. Альтернативная методика проведения реакции II: 2,5 ммоля соответствующего производного анилина и 2,5 ммоля гидрида натрия (60%) в 2,5 млN,N-диметилформамид обрабатывают с помощью 100 мг 6-хлор-3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазина (соединение А 1) при температуре окружающей среды. Через 10 мин реакционную смесь прибавляют к воде, осадок отфильтровывают с отсасыванием и твердое вещество перекристаллизовывают из N,N-диметилформамида. Альтернативная методика обработки: Продукт очищают с помощью хроматографии на колонке с силикагелем. 2. N-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,3-диамин С использованием в качестве исходных веществ 6-хлор-3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазина (соединение А 1) и м-фенилендиамина искомое соединение можно получить аналогично одной из методик, описанных для соединения 1. т. пл.: 295 С ЭФ: C22H18N6O (382,43) найдено: [М+1] 383,3 С использованием в качестве исходных веществ N-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин 6-ил]бензол-1,4-диамин (соединение 1) и соответствующих производных карбоновой кислоты указанные ниже соединения 3-26 можно получить аналогично тому, как это описано для соединения 22. 3. С-Диметиламино-N-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 26 Н 25N7O2 МС: рассчитано С 26 Н 25N7O2 (467,53), найдено [М+1] 467,9 4. 2-Метокси-N-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 25 Н 22N6O3 МС: рассчитано С 25 Н 22N6O3 (454,49), найдено [М+1] 454,8 5. 3-Метокси-N-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилпропионамид С 26 Н 24N6O3 МС: рассчитано С 26 Н 24N6O3 (468,52), найдено [М+1] 469,0 6. 3-Метокси-N-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбензамид С 30 Н 24N6O3 МС: рассчитано С 30 Н 24N6O3 (516,56), найдено [М+1] 516,9 7. Диметиламино-N-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбензамид С 31 Н 27N7O2 МС: рассчитано С 31 Н 27N7O2 (529,61), найдено [М+1] 529,7 8. Диметиламино-N-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбензамид С 31 Н 27N7O2 МС: рассчитано С 31 Н 27N7O2 (529,61), найдено [М+1] 530,0 9. N-4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилизоникотинамид С 28 Н 21N7O2 МС: рассчитано С 28 Н 21N7O2 (487,53), найдено [М+1] 487,8 10. N-4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилникотинамид С 28 Н 21N7O2 МС: рассчитано С 28 Н 21N7O2 (487,53), найдено [М+1] 487,9 11. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид 1 Н-имидазол-4 карбоновой кислоты С 26 Н 20N8O2 МС: рассчитано С 26 Н 20N8O2 (476,50), найдено [М+1] 476/7 12. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-2 карбоновой кислоты С 28 Н 27N7O2 МС: рассчитано С 28 Н 27N7O2 (493,57), найдено [М+1] 493,8 13. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-3 карбоновой кислоты-9 014324 С 28 Н 27N7O2 МС: рассчитано С 28 Н 27N7O2 (493,57), найдено [М+1] 493,8 14. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид 1-ацетилпиперидин-4-карбоновой кислоты С 30 Н 29N7O3 МС: рассчитано С 30 Н 29N7O3 (535,61), найдено [М+1] 535,9 15. N-4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенил-2-фенилацетамид С 30 Н 24N6 O2 МС: рассчитано С 30 Н 24N6O2 (500,56), найдено [М+1] 500,9 16. 2-(4-Метоксифенил)-N-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 31 Н 26N6O3 МС: рассчитано С 31 Н 26N6O3 (530,59), найдено [М+1] 531,0 17. 2,2,2-Трифтор-N-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 24 Н 17F3N6O2 МС: рассчитано С 24 Н 17F3N6O2 (478,44), найдено [М+1] 478,8 18. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид циклопропанкарбоновой кислоты С 26 Н 22N6O2 МС: рассчитано С 26 Н 22N6O2 (450,50), найдено [М+1] 450,8 19. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид циклогексанкарбоновой кислоты С 29 Н 28N6O2 МС: рассчитано С 29 Н 28N6O2 (492,59), найдено [М+1] 492,8 20. 2-Бензилокси-N-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 31 Н 26N6O3 МС: рассчитано С 31 Н 26N6O3 (530,59), найдено [М+1] 530,9 21. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид фуран-3 карбоновой кислоты С 27 Н 20N6O3 МС: рассчитано С 27 Н 20N6O3 (476,50), найдено [М+1] 476,8 22. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиридин-2 карбоновой кислоты К раствору пиколиновой кислоты (0,27 ммоля) и 1-гидроксибензотриазолгидрата (0,27 ммоля) в ДМФ(5 мл) прибавляют 1-(3-диметиламинопропил)-3 этилкарбодиимидгидрохлорид (0,27 ммоля), а затем N-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазин-6-ил]бензол-1,4-диамин (соединение 1) (0,26 ммоля). Реакционную смесь перемешивают при комнатной температуре в течение ночи и концентрируют в вакууме. Воду (10 мл) прибавляют к остатку и полученный осадок отфильтровывают и промывают этилацетатом и диэтиловым эфиром. Твердое вещество подвергают азеотропной сушке толуолом и получают 103 мг искомого соединения в виде светлокоричневого твердого вещества, т.пл.:301-305 С С 28 Н 21N7O2 МС: рассчитано С 28 Н 21N7O2 (487,53), найдено [М+1] 487,9 23. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-4 карбоновой кислоты С 28 Н 27N7O2 МС: рассчитано С 28 Н 27N7O2 (493,57), найдено [М+1] 494,2 24. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламидгидрохлорид пиперидин-4-карбоновой кислоты С 28 Н 28 С 1N7O2 МС: рассчитано С 28 Н 27N7O2 (493,57), найдено [М+1] 493,8 25.N-4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенил-2-(4-метилпиперазин-1-ил)ацетамид С 29 Н 30N8O2 МС: рассчитано С 29 Н 30N8O2 (522,61), найдено [М+1] 522,8 С использованием в качестве исходных веществ соответствующих аминов, выбранных из числа соединений 67-70, и соответствующих производных карбоновой кислоты указанные ниже соединения 2731 можно получить аналогично тому, как это описано для соединения 22. 27. 4-[3-(2-Трифторметилфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-2-карбоновой кислоты С 28 Н 24F3N7 О МС: рассчитано С 28 Н 24F3 N7 О (531,54), найдено [М+1] 532,1 28. 4-[3-(2-Бромфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-3 карбоновой кислоты С 27 Н 24BrN7O МС: рассчитано С 27 Н 24BrN7 О (542,44), найдено [М+1] 542,2 29. 4-[3-(2-Трифторметилфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-3-карбоновой кислоты С 28 Н 24F3N7 О МС: рассчитано С 28 Н 24F3N7 О (531,54), найдено [М+1] 532,6 30. 4-[3-(2-Бромфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-2 карбоновой кислоты С 27 Н 24BrN7 О МС: рассчитано С 27 Н 24BrN7 (542,44), найдено [М+1] 544,1- 10014324 31. 4-[3-(2-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-2 карбоновой кислоты С 28 Н 27N7O2 МС: рассчитано С 28 Н 27N7O2 (493,57), найдено [М+1] 494,1 С использованием в качестве исходных веществ 6-хлор-3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазина (соединение А 1) и соответствующих производных анилина указанные ниже соединения 3234 можно получить аналогично одной из методик, описанных для соединения 1. 32. N-4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 24 Н 20N6O2 (424,47), найдено: [М+1] 425,3 33. N-4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбензамид С 29 Н 22N6O2 (486,54) т.пл.: 323 С 34. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид фуран-2 карбоновой кислоты С 27 Н 20N6O3 (476,5) т.пл.: 303 С С использованием в качестве исходных веществ N-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазин-6-ил]бензол-1,3-диамина (соединение 2) и соответствующих производных карбоновой кислоты указанные ниже соединения 35-63 можно получить аналогично тому, как это описано для соединения 22. 35. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид циклогексанкарбоновой кислоты С 29 Н 28N6O2 МС: рассчитано С 29 Н 28N6O2 (492,59), найдено [М+1] 492,9 36. N-3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбензамид С 29 Н 22N6O2 МС: рассчитано С 29 Н 22N6O2 (486,54), найдено [М+1] 486,9 37. 2-Бензилокси-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 31 Н 26N6O3 МС: рассчитано С 31 Н 26N6O3 (530,59), найдено [М+1] 530,9 38. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид циклопропанкарбоновой кислоты С 26 Н 22N6O2 МС: рассчитано С 26 Н 22N6O2 (450,50), найдено [М+1] 451,0 39. 2,2,2-Трифтор-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 24 Н 17F3N6O2 МС: рассчитано С 24 Н 17F3N6O2 (478,44), найдено [М+1] 478,7 40. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид фуран-2 карбоновой кислоты С 27 Н 20N6O3 МС: рассчитано С 27 Н 20N6O3 (476,50), найдено [М+1] 476,8 41. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид фуран-3 карбоновой кислоты С 27 Н 20N6O3 МС: рассчитано С 27 Н 20N6O3 (476,50), найдено [М+1] 476,9 42. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид 1 Н-имидазол-4 карбоновой кислоты С 26 Н 20N8 О 2 МС: рассчитано С 26 Н 20N8O2 (476,50), найдено [М+1] 476,8 43. С-Диметиламино-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбензамид С 31 Н 27N7 О 2 МС: рассчитано С 31 Н 27N7O2 (529,61), найдено [М+1] 529,9 44. N-3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилизоникотинамид С 28 Н 21N7O2 МС: рассчитано С 28 Н 21N7O2 (487,53), найдено [М+1] 487,8 45. 2-Метокси-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 25 Н 22N6O3 МС: рассчитано С 25 Н 22N6O3 (454,49), найдено [М+1] 454,8 46. 4-Метокси-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбензамид С 30 Н 24N6O3 МС: рассчитано С 30 Н 24N6O3 (516,56), найдено [М+1] 516,9 47. 3-Метокси-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбензамид С 30 Н 24N6O3 МС: рассчитано С 30 Н 24N6O3 (516,56), найдено [М+1] 516,8 48. 2-(4-Метоксифенил)-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 31 Н 26N6O3 МС: рассчитано С 31 Н 26N6O3 (530,59), найдено [М+1] 531,0 49. N-3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенил-2-фенилацетамид С 30 Н 24N6O2 МС: рассчитано С 30 Н 24N6O2 (500,56), найдено [М+1] 500,9 50. N-3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилникотинамид С 28 Н 21N7 О 2 МС: рассчитано С 28 Н 21N7O2 (487,53), найдено [М+1] 487,7 51. Диметиламино-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбен- 11014324 замид С 31 Н 27N7O2 МС: рассчитано С 31 Н 27N7O2 (529,61), найдено [М+1] 529,9 52. С-Диметиламино-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 26 Н 25N7 О 2 МС: рассчитано С 26 Н 25N7O2 (467,53), найдено [М+1] 467,9 53. 3-Метокси-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилпропионамид С 26 Н 24N6O3 МС: рассчитано С 26 Н 24N6O3 (468,52), найдено [М+1] 469,0 54. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид 1 ацетилпиперидин-4-карбоновой кислоты С 30 Н 29N7O3 МС: рассчитано С 30 Н 29N7O3 (535,61), найдено [М+1] 535,9 55. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиридин-2 карбоновой кислоты С 28 Н 21N7O2 МС: рассчитано С 28 Н 21N7O2 (487,53), найдено [М+1] 487,8 56. Диметиламино-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбензамид С 31 Н 27N7O2 МС: рассчитано С 31 Н 27N7O2 (529,61), найдено [М+1] 529,9 57. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-4 карбоновой кислоты С 28H27N7O2 МС: рассчитано С 28 Н 27N7O2 (493,57), найдено [М+1] 493,8 58. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-3 карбоновой кислоты С 28 Н 27N7O2 МС: рассчитано С 28 Н 27N7O2 (493,57), найдено [М+1] 493,8 59. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид пиперидин-2 карбоновой кислоты С 28 Н 27N7O2 МС: рассчитано С 28 Н 27N7O2 (493,57), найдено [М+1] 493,8 60. 2-Гидрокси-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 24 Н 20N6O3 МС: рассчитано С 24 Н 20N6O3 (440,47), найдено [М+1] 440,9 61. N-3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилакриламид С 25 Н 20N6O2 МС: рассчитано С 25 Н 20N6O2 (436,48), найдено [М+1] 436,8 62. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид 1-метилпиперидин-4-карбоновой кислоты С 29 Н 29N7O2 МС: рассчитано С 29 Н 29N7O2 (507,60), найдено [М+1] 507,9 63. Диметиламино-N-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбутирамид С 28 Н 29N7O2 МС: рассчитано С 28 Н 29N7O2 (495,59), найдено [М+1] 495,9 С использованием в качестве исходных веществ соответствующих аминов, выбранных из числа соединений 71-74, и соответствующих производных карбоновой кислоты указанные ниже соединения 6465 можно получить аналогично тому, как это описано для соединения 22. 64. 3-[3-(2-Фторфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид циклопропанкарбоновой кислоты С 25 Н 19FN6 О МС: рассчитано С 25 Н 19FN6 О (438,47), найдено [М+1] 439,1 65. 3-[3-(2-Метоксифенил)-[1,2,4]триазоло [3,4-а]фталазин-6-иламино]фениламид циклопропанкарбоновой кислоты С 26 Н 22N6O2 МС: рассчитано С 26 Н 22N6O2 (450,50), найдено [М+1] 451,1 С использованием в качестве исходных веществ 6-хлор-3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазина (соединение А 1) и соответствующего производного анилина указанное ниже соединение 66 можно получить аналогично одной из методик, описанных для соединения 1. 66. N-3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилацетамид С 24 Н 20N6O2 424,47 т.пл.: 295 С С использованием подходящих исходных веществ, выбранных из числа соединений А 2-А 9, указанные ниже соединения 67-74 можно получить по реакции восстановления, аналогично тому, как это описано для соединения 74 а; или, альтернативно, указанные ниже соединения 67-74 а можно получить аналогично тому, как это описано для соединения 1. 67. N-[3-(2-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,4-диамин С 22 Н 18N6 О МС: рассчитано С 22 Н 18N6 О (382,43), найдено [М+1] 383,1 68. N-[3-(2-Фторфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,4-диамин 69. N-[3-(2-Бромфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,4-диамин С 21 Н 15BrN6 МС: рассчитано С 21 Н 15BrN6 (431,30), найдено [М+1] 431,0 70. N-[3-(2-Трифторметилфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,4-диамин С 22 Н 15F3N6 МС: рассчитано С 22 Н 15F3N6 (420,40), найдено [М+1] 421,0- 12014324 71. N-[3-(2-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,3-диамин С 22 Н 18NО МС: рассчитано С 22 Н 18N6 О (382,43), найдено [М+1] 383,1 72. N-[3-(2-Фторфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,3-диамин 73. N-[3-(2-Бромфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,3-диамин С 21H15BrN6 МС: рассчитано С 21 Н 15BrN6 (431,30), найдено [М+1] 433,1 74. N-[3-(2-Трифторметилфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,3-диамин 74 а. N-[3-(2-Метилфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,3-диамин К суспензии (3-нитрофенил)-(3-о-толил-[1,2,4]триазоло[3,4-а]фталазин-6-ил)амина (соединение А 10) (263 мг, 0,66 ммоля) в смеси состава 2:1 ледяной уксусной кислоты и 37% хлористо-водородной кислоты (18 мл) прибавляют дигидрат хлорида олова (450 мг, 1,99 ммоля). Смесь перемешивают при 90 С в течение 2 дней. После охлаждения осадок отфильтровывают и фильтрат концентрируют. Очистка остатка с помощью хроматографии на колонке (CH2Cl2/МеОН, 95:5) дает 205 мг почти белого твердого вещества, которое растирают со 1:1 смесью изопропанола и петролейного эфира и получают 77 мг искомого соединения в виде почти белых иголок. С использованием в качестве исходных веществ 6-хлор-3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазина (соединение А 1) и соответствующих производных анилина указанные ниже соединения 75 и 76 можно получить аналогично одной из методик, описанных для соединения 1. 75. Метиловый эфир 4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензойной кислоты С 24 Н 19N5O3 425,45, найдено: [М+1] 426,4 76. Метиловый эфир 3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензойной кислоты С 24 Н 19N5O3 425,45, найдено: [М+1] 426,3 77. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензойная кислота 40 мг метилового эфира 4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6 иламино]бензойной кислоты (соединение 75), 25 мг гидроксида калия и 150 мкл воды перемешивают в 2 мл метанола при 100 С в течение 1 ч. Реакционную смесь отфильтровывают с отсасыванием, фильтрат разбавляют с помощью 10 мл воды и подкисляют до рН 2-3 с помощью 2 М хлористо-водородной кислоты. Осадок отфильтровывают с отсасыванием, промывают водой и сушат и получают 23 мг искомого соединения. ЭФ: C23H17N5O3 (411,42), найдено: [М+1] 412,3 Альтернативная методика проведения реакции: В запаянной трубке к раствору метоксида натрия в метаноле, полученному прибавлением натрия(590 мг, 25,4 ммоля) к безводному метанолу (20 мл) в атмосфере аргона прибавляют метиловый эфир 4[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензойной кислоты (соединение 75) (4,0 г, 9,40 ммоля) и диизопропиламин (32 мл). Смесь перемешивают при 100 С в течение 3 дней и выпаривают. Остаток промывают этилацетатом минимальным количеством метанола и получают 3,78 г искомого соединения в виде светло-желтого порошкообразного вещества, т.пл.: 309 С (с разложением). 78. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензойная кислота С использованием в качестве исходных веществ метилового эфира 3-[3-(4-метоксифенил)[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензойной кислоты (соединение 76) искомое соединение можно получить аналогично тому, как это описано для соединения 77. ЭФ: C23H17N5O3 (411,42), найдено: [М+1] 411,8 С использованием в качестве исходных веществ 4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазин-6-иламино]бензойной кислоты (соединение 77) и соответствующих производных аминов указанные ниже соединения 79-89 можно получить аналогично тому, как это описано для соединения 103. 79. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]-N-(2-морфолин-4-илэтил)бензамид С 29 Н 29N7O3 МС: рассчитано C29 Н 29N7O3 (523,60), найдено [М+1] 524,0 80. N-(3-Метоксифенил)-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензамид С 30 Н 24N6O3 МС: рассчитано С 30 Н 24N6O3 (516,56), найдено [М+1] 516,8 81. N-(4-Метоксифенил)-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензамид С 30 Н 24N6O3 МС: рассчитано С 30 Н 24N6O3 (516,56), найдено [М+1] 516,9 82. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]-N-фенилбензамид С 29 Н 22N6 О 2 МС: рассчитано С 29 Н 22N6O2 (486,54), найдено [М+1] 486,9 83. N-(4-Диметиламинофенил)-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензамид С 31 Н 27N7O2 МС: рассчитано С 31 Н 27N7O2 (529,61), найдено [М+1] 529,8 84. N-(2-Метоксифенил)-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензамид С 30 Н 24N6O3 МС: рассчитано С 30 Н 24N6O3 (516,56), найдено [М+1] 516,9 85. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]-N-метилбензамид С 24 Н 20N6O2 МС: рассчитано С 24 Н 20N6O2 (424,47), найдено [М+1] 424,9- 13014324 86. N-(2-Диметиламиноэтил)-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензамид С 27 Н 27N7O2 МС: рассчитано С 27 Н 27N7O2 (481,56), найдено [М+1] 481,7 87. N-(2-Метоксиэтил)-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензамид С 26 Н 24N6O3 МС: рассчитано С 26 Н 24N6O3 (468,52), найдено [М+1] 468,7 88. 1-4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенил-1-(4-метилпиперазин-1-ил)метанон С 28 Н 27N7O2 МС: рассчитано С 28 Н 27N7O2 (493,57), найдено [М+1] 494,0 89. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]-N,N-диметилбензамид С 25 Н 22N6O2 МС: рассчитано С 25 Н 22N6O2 (438,49), найдено [М+1] 439,0 С использованием в качестве исходных веществ 6-хлор-3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазина (соединение А 1) и соответствующих производных анилина указанные ниже соединения 91 и 92 можно получить аналогично одной из методик, описанных для соединения I. 91. 4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензамид С 23 Н 18N6O2 410,44, найдено: [М+1] 411,3 92. 1-4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенил-1-морфолин-4-ил метанон С 27 Н 24N6O3 480,53 т.пл.: 295 С С использованием в качестве исходных веществ 3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазин-6-иламино]бензойной кислоты (соединение 78) и соответствующих производных аминов указанные ниже соединения 90 и 93-108 можно получить аналогично тому, как это описано для соединения 103. 90.N,N-диметилфенилендиамин (35 мг, 0,26 ммоля). Реакционную смесь перемешивают при комнатной температуре в течение 2 дней и концентрируют в вакууме. Воду (20 мл) прибавляют к остатку и полученный осадок отфильтровывают и промывают метанолом и дихлорметаном. Твердое вещество подвергают азеотропной сушке толуолом и получают 79 мг искомого соединения в виде серого порошкообразного вещества, т.пл.: 314-318 С, С 31 Н 27N7O2 МС: рассчитано С 31 Н 27N7O2 (529,61), найдено [М+1] 530,0N-(2-Диметиламиноэтил)-3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензамидгидрохлорид С 27 Н 28ClN7O2 MC: рассчитано С 27 Н 27N7O2 (481,56), найдено [М+1] 481,8 С использованием в качестве исходных веществ 6-хлор-3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазина (соединение А 1) и соответствующих производных анилина указанные ниже соединения 109 и 110 можно получить аналогично одной из методик, описанных для соединения 1. 109. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]бензамид С 23H18N6O2 410,44 т.пл.: 296 С 110. 3-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]-N-метилбензамид С 24H20N6O2 424,47 т.пл.:316 С 111. N-4-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенил-4-морфолин-4 илбензамид 100 мг N-[3-(4-Метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,4-диамина (соединение 1), 10 мг диметиламинопиридина и 145 мг 4-морфолин-4-илбензоилхлорида перемешивают в 12 мл толуола в течение 1-3 ч при температуре кипения. После охлаждения до температуры окружающей среды осадок отфильтровывают с отсасыванием и твердое вещество перекристаллизовывают из N,Nдиметилформамид и получают 15 мг искомого соединения (т.пл.: 313 С). ЭФ: C33H29N7O3 (571,64), найдено: [М+1] 572,4 С использованием в качестве исходных веществ N-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазин-6-ил]бензол-1,4-диамина (соединение 1) и соответствующего производного карбоновой кислоты указанное ниже соединение 112 можно получить аналогично получению соединений 3-26, как это описано для соединения 22. 112. 4-Метокси-N-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенилбензамид С 30 Н 24N6O3 МС: рассчитано С 30 Н 24N6O3 (516,56), найдено [М+1] 517,3 С использованием в качестве исходных веществ подходящих нитросоединений А 11 (для 113) или А 12 (для 114) указанные ниже соединения 113 и 114 можно получить по реакции восстановления, аналогично тому, как это описано для соединения 74 а; или, альтернативно, с использованием в качестве исходных веществ В 8 (для 113) или В 9 (для 114) указанные ниже соединения 113 и 114 можно получить аналогично тому, как это описано для соединения 1. 113. N-[3-(4-Бромфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,3-диамин С 21 Н 15BrN6 МС: рассчитано С 21 Н 15BrN6 (431,30), найдено [М+1] 431,1 114. N-[3-(2-Хлорфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-ил]бензол-1,3-диамин С 21 Н 15ClN6 МС: рассчитано С 21 Н 15ClN6 (386,85), найдено [М+Н] 387,0 С использованием в качестве исходных веществ N-[3-(4-Бромфенил)-[1,2,4]триазоло[3,4 а]фталазин-6-ил]бензол-1,3-диамина (соединение 113) и соответствующего производного карбоновой кислоты указанное ниже соединение 115 можно получить аналогично получению соединений 3-26, как это описано для соединения 22. 115. 3-[3-(4-Бромфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид циклопропанкарбоновой кислоты С 25 Н 19BrN6 О МС: рассчитано С 25 Н 19BrN6 О (499,37), найдено [М+Н] 499,0 С использованием в качестве исходных веществ соединения 74 а (для 116) или соединения 74 (для 117) и соответствующих производных карбоновой кислоты указанные ниже соединения N6 и N7 можно получить аналогично получению соединений 64/65, как это описано для соединения 22. 116. [3-(3-о-Толил-[1,2,4]триазоло[3,4-а]фталазин-6-иламино)фенил]амид циклопропанкарбоновой кислоты С 26 Н 22N6 О МС: рассчитано С 26 Н 22N6 О (434,5), найдено (М+1) 435,2 117. 3-[3-(2-Трифторметилфенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид циклопропанкарбоновой кислоты С 26 Н 19F3N6 О МС: рассчитано С 26 Н 19F3N6 О (488,48), найдено (М+1)489,1 С использованием в качестве исходных веществ 4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4 а]фталазин-6-иламино]бензойной кислоты (соединение 77) и соответствующего производного амина указанное ниже соединение 118 можно получить аналогично получению соединений 79-89, как это описаноA1. 6-Хлор-3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин 6,0 г (4-Хлорфталазин-1-ил)-гидразин (соединение В 1) суспендируют в смеси 160 мл толуола и 18 мл триэтиламина при 60 С и обрабатывают раствором 6,0 г 4-метоксибензоилхлорида в 48 мл толуола. Смесь перемешивают при 110 С в течение 6 ч, охлаждают до температуры окружающей среды, отфильтровывают с отсасыванием и промывают толуолом. Твердое вещество перекристаллизовывают из N,Nдиметилформамида, осадок промывают водой и сушат и получают 5,2 г искомого соединения (т.пл.: 192193 С). ЭФ:C16H11ClN4O (310,75), найдено: [М+1] 311,2 Альтернативная методика обработки Продукты можно очистить с помощью хроматографии на колонке с силикагелем. С использованием в качестве исходного вещества соответствующего соединения В 2-В 9 и соответствующего производного анилина указанные ниже соединения А 2-А 12 можно получить по методике,аналогичной одной из методик, описанных для соединения 1. А 2. (3-Нитрофенил)-3-(2-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламинB1. (4-Хлорфталазин-1-ил)гидразин 10 г Имеющегося в продаже дихлорфталазина при 90 С порциями прибавляют к раствору 50 мл этанола и 20 мл гидразингидрата. Через 10 мин реакционную смесь охлаждают до температуры окружающей среды, осадок отфильтровывают с отсасыванием и промывают этанолом и получают 8,4 г искомого соединения. ЭФ: C8H7ClN4 (194,62), найдено: [М+1] 195,0 С использованием в качестве исходных веществ (4-хлорфталазин-1-ил)гидразина (соединение В 1) и соответствующих производных бензойной кислоты указанные ниже соединения В 2-В 9 можно получить по методике, аналогичной описанной для соединения А 1 или В 7.B7. 6-Хлор-3-фенил-[1,2,4]триазоло[3,4-а]фталазин Стадия 1: 2,5 г (4-Хлорфталазин-1-ил)-гидразин (соединение В 1) суспендируют в 250 мл толуола и обрабатывают раствором 1,7 мл хлорангидрида бензойной кислоты в 50 мл толуола при температуре кипения. Через 2 ч реакционную смесь охлаждают до температуры окружающей среды и фильтруют с отсасыванием. Фильтрат концентрируют при пониженном давлении и остаток перекристаллизовывают из N,Nдиметилформамида и получают 1,2 г (4-хлор-2H-фталазин-1-илиден)гидразида бензойной кислоты. ЭФ:C15H11ClN4O (298,73), найдено: [М+1] 299,1 Стадия 2: 2,5 г (4-Хлор-2H-фталазин-1-илиден)-гидразида бензойной кислоты и 1 г триэтиламингидрохлорида суспендируют в 60 мл этиленликоля и перемешивают при 130 С в течение 3 ч. Реакционную смесь охлаждают до температуры окружающей среды и прибавляют к 600 мл воды. Продукт экстрагируют дихлорметаном, органический слой сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток перекристаллизовывают из N,N-диметилформамида и получают искомое соединение. ЭФ: C15H9ClN4 (280,72), найдено: [М+1] 281,2 Альтернативная методика обработки Продукты можно очистить с помощью хроматографии на колонке с силикагелем.B9. 6-Хлор-3-(2-хлорфенил)-[1,2,4]триазоло[3,4-а]фталазин С 15 Н 8 С 12N4 МС: рассчитано С 15 Н 8 С 12N4 (315,16), найдено [М+Н] 314,8 Коммерческое применение Соединения, предлагаемые в настоящем изобретении, обладают ценными фармакологическими характеристиками, которые делают их пригодными для коммерческого применения. В качестве селективных ингибиторов гидролизующих циклический ГМФ (гуанозинмонофосфат) (ингибиторов цГМФ-ФДЭ),предпочтительно - типа 2, с одной стороны, они пригодны для использования в качестве лекарственных средств при состояниях патологически усиленной эндотелиальной активности и нарушенной функции эндотелиального барьера, таких как септический шок, сосудистый отек, или заболеваниях, связанных с нежелательным неоангиогенезом. С другой стороны, с учетом экспрессирования ФДЭ 2 в нейронной ткани, эти соединения также могут быть пригодными при нейродегенеративных патологических состояниях. Кроме того, ФДЭ 2 экспрессируется в тромбоцитах человека и показано, что ингибиторы ФДЭ 2 подавляют функции тромбоцитов. Поэтому такие соединения можно использовать в качестве антитромботических средств/ингибиторов агрегации тромбоцитов. Кроме того, поскольку ФДЭ 2 обнаружена в миокарде, эти соединения могут оказаться применимыми для защиты от аритмии. Вследствие своей способности ингибировать цГМФ-ФДЭ (предпочтительно - ФДЭ 2) соединения,предлагаемые в настоящем изобретении, можно использовать в медицине и ветеринарии в качестве лекарственных средств, где их можно применять, например, для лечения и профилактики следующих патологических состояний: (1) всех состояний патологически усиленной эндотелиальной активности/нарушенной функции эндотелиального барьера, таких как множественное повреждение, в частности,острый респираторный дистресс-синдром (ОРДС) при септическом шоке, пневмония, острые и хронические нарушения дыхательных путей различной этиологии (ринит, бронхит, бронхиальная астма, эмфизема, хроническое обструктивное заболевание легких), ангионевротический отек, периферический отек,отек головного мозга, например травматический или после удара; (2) всех патологических состояний,связанных с патологически усиленным неоангиогенезом, таких как все типы опухолей (доброкачественных или злокачественных), которые связаны с неоангиогенезом, и все типы воспалительных заболеваний, связанных с неоангиогенезом, например нарушения типа артрита (ревматоидный артрит, ревматоидный спондилит, остеоартрит и другие артритные патологические состояния), все виды псориаза, сетчаточная слепота, бронхиальная астма, воспалительное заболевание желудка, отторжение трансплантата,отторжения аллотрансплантатов, атеросклероз; (3) всех патологических состояний, для которых необходимо подавление агрегации тромбоцитов совместно с уменьшением усиленной эндотелиальной активацией, таких как тромбоэмболические нарушения и ишемии, включая инфаркт миокарда, инфаркт головного мозга, временные ишемические приступы, стенокардия, нарушения периферического кровообращения, предупреждение рестеноза после тромболитической терапии, чрескожная транслюминальная ангиопластика (ЧТА), чрескожная транслюминальная коронарная ангиопластика (ЧТКА) и шунтирование; (4) всех типов нарушенной познавательной способности, в частности нарушений познавательной способности, таких как слабое нарушение познавательной способности (СНП), болезнь Альцгеймера, слабоумие,развивающееся при болезни телец Леви, болезнь Паркинсона и цереброваскулярное слабоумие; и (5) аритмиях сердца. Настоящее изобретение также относится к способу лечения млекопитающих, включая людей, которые страдают от одного из указанных выше заболеваний. Способ характеризуется тем, что терапевтически активное и фармакологически эффективное и переносимое количество одного или большего количества соединений, предлагаемых в настоящем изобретении, вводят больному млекопитающему. Настоящее изобретение также относится к способу ингибирования ФДЭ, предпочтительно - ФДЭ 2,включающему взаимодействие указанной ФДЭ с эффективным количеством соединения, предлагаемого в настоящем изобретении. Настоящее изобретение также относится к способу ингибирования ФДЭ, предпочтительно - ФДЭ 2,включающему введение фармакологически активного и терапевтически эффективного и переносимого количества по меньшей мере одного соединения, предлагаемого в настоящем изобретении животному,нуждающемуся в таком ингибировании. Настоящее изобретение также относится к соединениям, предлагаемым в настоящем изобретении,предназначенным для применения при лечении и/или профилактике заболеваний, предпочтительно указанных заболеваний. Настоящее изобретение также относится к соединениям, предлагаемым в настоящем изобретении,обладающим ингибирующей активностью по отношению к ФДЭ, предпочтительно по отношению к ФДЭ 2. Настоящее изобретение также относится к применению соединений, предлагаемых в настоящем изобретении, для приготовления фармацевтических композиций, которые применяются для лечения и/или профилактики указанных заболеваний. Настоящее изобретение также относится к применению соединений, предлагаемых в настоящем- 17014324 изобретении, для приготовления фармацевтических композиций, которые применяются для лечения и/или профилактики связанных с ФДЭ, предпочтительно связанных с ФДЭ 2 заболеваний. Кроме того, настоящее изобретение относится к фармацевтическим композициям, предназначенным для лечения и/или профилактики указанных заболеваний, которые содержат одно или большее количество соединений, предлагаемых в настоящем изобретении,. Кроме того, настоящее изобретение относится к фармацевтическим композициям, обладающим ингибирующей активностью по отношению к ФДЭ, предпочтительно по отношению к ФДЭ 2. Кроме того, настоящее изобретение относится к готовому изделию, которое включает упаковочный материал и фармацевтическое средство, находящееся в указанном упаковочном материале, в котором фармацевтическое средство терапевтически эффективно для противодействия воздействию циклической нуклеотид фосфодиэстеразы типа 2 (ФДЭ 2), ослабления симптомов опосредуемого ФДЭ 2 нарушения и в котором упаковочный материал включает этикетку или листок-вкладыш, в котором указано, что это фармацевтическое средство применимо для предупреждения или лечения опосредуемых ФДЭ 2 нарушении, и в котором указанное фармацевтическое средство включает одно или большее количество соединений формулы 1, предлагаемых в настоящем изобретении. Упаковочный материал, этикетка и листоквкладыш в остальном аналогичны или сходны с тем, что обычно рассматривается в качестве стандартных упаковочного материала, этикеток и листков-вкладышей для фармацевтических средств аналогичного применения. Введение фармацевтических композиций, предлагаемых в настоящем изобретении, можно проводить по любому из общепринятых путем введения, возможных в данной области техники. Иллюстративные примеры подходящих путей введения включают внутривенную, пероральную, назальную, парентеральную, местную, чрескожную и ректальную доставку. Предпочтительной является местная и пероральная доставка. Фармацевтические композиции готовят способами, которые известны сами по себе и известны специалисту в данной области техники. В качестве фармацевтических композиций соединения, предлагаемые в настоящем изобретении (= активные соединения), применяются сами по себе или предпочтительно в комбинации с подходящими фармацевтическими вспомогательными веществами и/или инертными наполнителями, например, в виде таблеток, таблеток с покрытием, капсул, таблеток в форме капсул, суппозиториев, пластырей (например, в виде ЧТС (чрескожная терапевтическая система, эмульсий, суспензий, гелей или растворов, содержание активного соединения предпочтительно составляет от 0,1 до 95% и при соответствующем выборе вспомогательных веществ и/или инертных наполнителей можно получить фармацевтическую вводимую форму (например, форму замедленного высвобождения или энтеросолюбильную форму), в точности подходящую для активного соединения и/или обеспечивающую необходимое начало воздействия. Специалист в данной области техники знаком со вспомогательными веществами и инертными наполнителями, которые на основании имеющихся у него профессиональных знаний пригодны для необходимых фармацевтических композиций. В дополнение к растворителям, гелеобразующим веществам,основам мазей и другим инертным наполнителям активного соединения, можно использовать, например,антиоксиданты, диспергирующие вещества, эмульгаторы, консерванты, солюбилизаторы, красители,комплексообразующие агенты или вещества, способствующие проникновению. Для лечения нарушений дыхательных путей соединения, предлагаемые в настоящем изобретении,также предпочтительно вводить путем ингаляции в форме аэрозоля; твердые, жидкие и обладающие смешанным составом аэрозольные частицы предпочтительно обладают диаметром от 0,5 до 10 мкм, более предпочтительно от 2 до 6 мкм. Генерацию аэрозоля можно провести, например, с помощью струйных устройств с распылением под давлением или ультразвуковых распылительных устройств, но предпочтительно - с помощью дозирующих распылительных устройств с использованием пропеллентов или введения тонкоизмельченных активных веществ из ингаляционных капсул без пропеллентов. В зависимости от типа применяющегося ингалятора вводимые формы в дополнение к активным соединениям дополнительно содержат необходимые инертные наполнители, такие как, например, пропелленты (например, Frigen в случае дозируемых аэрозолей), поверхностно-активные вещества, эмульгаторы, стабилизаторы, консерванты, ароматизаторы, наполнители (например, лактозу в случае порошковых ингаляторов) или, при необходимости, дополнительные активные соединения. Для проведения ингаляции имеется большое количество приборов, в которых можно создать аэрозоли с оптимальным размером частиц и ввести их с использованием процедуры ингаляции, которая наилучшим возможным образом подходит для пациента. В дополнение к использованию переходников (разделителей, расширителей) и грушеобразных контейнеров (например, Nebulator, VolumatiC) и автоматических устройств, выполняющих более объемное распыление (Autohaler), для дозирования аэрозолей, в особенности в случае порошковых ингаляторов, имеется ряд технических новинок (например,Diskhaler, Rotadisk, Turbohaler и ингалятор, описанный в Заявке на Европейский патент ЕР 0505321), при использовании которых можно обеспечить оптимальное введение активного соединения.- 18014324 Для лечения заболеваний кожи соединения, предлагаемые в настоящем изобретении, предпочтительно вводить в виде таких фармацевтических композиций, которые пригодны для местного применения. Для приготовления фармацевтических композиций соединения, предлагаемые в настоящем изобретении (= активные соединения), предпочтительно смешивать с подходящими фармацевтическими вспомогательными веществами и обработать и получить подходящие фармацевтические препараты. Подходящими фармацевтическими препаратами являются, например, порошки, эмульсии, суспензии, аэрозоли,масла, мази, жировые мази, кремы, пасты, гели и растворы. Фармацевтические композиции, предлагаемые в настоящем изобретении, получают способами, которые сами по себе известны. Дозировка активных соединений по порядку величины совпадает с обычно применяющейся для ингибиторов ФДЭ. Поэтому формы, предназначенные для местного применения(такие как мази) при лечении дерматозов, содержат активные соединения в концентрациях, составляющих, например, 0,1-99%. Доза для введения путем ингаляции обычно составляет от 0,1 до 3 мг в сутки. Обычная доза при системной терапии (пероральная или внутривенная) составляет от 0,3 до 30 мг/кг в сутки. Биологические исследования Методика измерения ингибирования активности ФДЭ Аббревиатуры: ФДЭ: фосфодиэстераза, ПЦР: полимеразная цепная реакция, ОТ-ПЦР: обратная транскрипцияполимеразная цепная реакция, дНТФ: дезоксинуклеозидтрифосфаты, РНК: рибонуклеиновая кислота,кДНК: комплементарная дезоксирибонуклеиновая кислота, ПО: пары оснований, (dT)15: петнадекатимидиновая кислота, ОРС: открытая рамка считывания, GB по.: номер в базе данных GenBank, рБВ: рекомбинантный бакуловирус, ДТ: дикий тип, АК: аминокислота, КОО: консервативная область в обратном направлении, ПАА: полиакриламид. Аминокислоты обозначают однобуквенными символами: А - аланин, С - цистеин, D - аспартамовая кислота, Е - глутаминовая кислота, F - фенилаланин, G - глицин, Н - гистидин, I - изолейцин, K - лизин, L- лейцин, М - метионин, N - аспарагин, Р - пролин, Q - глутамин, R - аргинин, S - серин, Т - треонин, V валин, W - триптофан, Y - тирозин. Общие методики клонирования рекомбинантных ФДЭ РНК выделяли из линий клеток и очищали с помощью RNeasy Mini Kit, выпускающегося фирмойQiagen. 1 мкг РНК подвергали обратной транскрипции в однотяжевую кДНК в 20 мкл реакционной смеси с использованием обратной транскриптазы Expand (Roche) с использованием 50 пМ праймера (dT)15 и 1 мМ дНТФ (оба выпускающиеся фирмой Roche). 5 мкл кДНК использовали в качестве шаблона для последующей реакции ПЦР. Использовали кДНК из тканей человека, выпускающуюся фирмой Clontech или Invitrogen. Для реакции ПЦР использовали 1 мкл. ПЦР проводили в устройстве для циклической термической обработки Stratagem Robocycler 40 или в MWG Primus 96 plus. Обычно ПЦР проводили в системе Expand Lond Template PCR System, выпускающейся фирмой Roche в буфере 3 с прибавлением 0,75 мМ MgCl2, 0,3 мкМ каждого праймера, 500 мкМ дНТФ. Продукты, полученные с помощью ПЦР, очищали с помощью набора для очистки High Pure PCRProduct Purification Kit (Roche) или из агарозного геля с помощью набора QIAquick Gel Extraction kit, выпускающегося фирмой Qiagen, и клонировали в вектор pCR2.1-TOPO, выпускающийся фирмой Invitrogen. ОРС субклонировали в векторы экспрессии бакуловируса (передающиеся плазмиды). Использовали векторы pCR-Bac и pVL, выпускающиеся фирмой Invitrogen. Использовали векторы pBacPak (pBP8 или рВР 9), выпускающиеся фирмой Clontech. Использовали эндонуклеазы рестрикции, выпускающиеся фирмами Roche и MBI Fermentas. Использовали модифицирующие ферменты и лигазу Т 4 ДНК, выпускающиеся фирмой New England Biolabs. Секвенсирование ДНК выполняла фирма GATC GmbH (Konstanz, Germany, www.gatc.de) или лаборатория ALT ANAPharma с использованием ABI PRISM 310 и краситель Big и набор химикатов для завершающего цикла секвенсирования v2 (Applied Biosystem). Анализ последовательностей проводили с помощью программного обеспечения Hitachi DNASIS Version 2,5 или Vector NTI 7. Мутагенез in vitro при необходимости проводили с помощью набора QuickChange Site-Directed Mutagenesis, выпускающегося фирмойStratagene. Клонирование ФДЭ 2 А 3 человека ФДЭ 2 А 3 (GB no. U67733) амплифицировали в 2 стадии с использованием ПЦР из кДНК головного мозга.CP3PD2AA (5'-GGGATCACTCAGCATCAAGGC-3'). Продукты, полученные с помощью ПЦР, клонировали в вектор pCR2.1-Topo. N-Концевой фрагмент сначала субклонировали с помощью EcoRI вpBluescript II KS (-), а затем фрагмент Bst1107I/EcoRV обменивали с соответствующим фрагментом рестрикции из С-концевого клона и получали полную ОРС. ОРС для ФДЭ 2 А 3 субклонировали в рВР 8 с использованием XbaI и KpnI.- 19014324 Экспрессирование рекомбинантной ФДЭ 2 рБВ получали с помощью гомологичной рекомбинации в клетках насекомых Sf9. Экспрессионные плазмиды совместно трансфицировали с Bac-N-Blue (Invitrogen) или Baculo-Gold ДНК (Pharmingen) с использованием стандартного протокола (Pharmingen). Кондиционированные среды рекомбинантного вируса, не содержащего вируса дикого типа, выбирали с помощью методик анализа бляшкообразования. После этого обладающие большим титром кондиционированные среды вируса готовили путем трехкратной амплификации. ФДЭ 2 экспрессировали в клетки Sf21 путем инфицирования 2106 клеток/мл с помощью МНИ (множественной инфекции) от 1 до 10 в бессывороточной среде SF900 (Life Technologies). Клетки выращивали при 28 С, обычно в течение 48 ч, после чего их центрифугировали с получением таблеток в течение 5-10 мин при 1000 g и 4 С. I В центрифужных пробирках клетки выращивают при скорости вращения, равной 75 оборотов/мин. Клетки насекомых SF21 повторно суспендировали в концентрации, равной примерно 10 клеток/мл, в охлажденном льдом (4 С) буфере для гомогенизации (20 мМ Tris [Tris = трис(гидроксиметиламинометан)], рН 8,2, содержащий следующие добавки: 140 мМNaCl, 3,8 мМ KCl, 1 мМ ЭГТУ (этиленгликольтетрауксусная кислота), 1 мМ MgCl2, 1 мМ рмеркаптоэтанола, 2 мМ бензамидина, 0,4 мМ пефаблока, 10 мкМ лейпептина, 10 мкМ пепстатина А, 5 мкМ ингибитора трипсина) и дезинтегрировалит путем обработки ультразвуком. Затем гомогенизат центрифугировали в течение 10 мин при 1000g и до последующего использования (см. ниже) надосадочную жидкость хранили при -80 С . Содержание белка определяли методом Брэдфорда (BioRad, Munich) с использованием БСА (бычий сывороточный альбумин) в качестве стандарта. Целостность и размер рекомбинантных белков определяли с помощью вестерн-блоттинга. Измерение ингибирования рекомбинантной ФДЭ 2 А 3 человека по методике ПСА Активность рекомбинантной ФДЭ 2 А 3 человека ингибировали исследуемыми образцами с использованием модифицированного ПСА (проксимально-сцинтилляционный анализ фосфодиэстеразы) фирмыAmersham Pharmacia Biotech (см. руководство по применению "phosphodiesterase [3H]сАМР SPA enzymeassay, code TRKQ 7090"), проводимого в 96-луночных планшетах для микротитрования (ПМТ). Исследуемый объем составлял 100 мкл и в нем содержались 20 мМ буфер Tris (рН 7,4), 0,1 мг БСА (бычий сывороточный альбумин)/мл, 5 мМ Mg2+, 0,5 мкМ цАМФ (включая [3 Н]цАМФ в количестве примерно 50000 распадов/мин), 5 мкМ цГМФ (для активации ФДЭ 2 А 3), 2 мкл разведения соответствующего соединения в диметилсульфоксиде и количество рекомбинантной ФДЭ (1000g кондиционированная среда, см. выше), достаточное для того, чтобы при указанных условиях проведения эксперимента подверглись превращению 15-20% цАМФ. После предварительной инкубации в течение 5 мин при 37 С реакцию запускали путем прибавления субстрата (ц-АМФ) и анализируемые пробы инкубировали в течение еще 15 мин; затем реакцию останавливали путем прибавления гранул ПАН (полиакрилонитрилат натрия)(50 мкл). В соответствии с руководством изготовителя гранулы ПАН предварительно были повторно суспендированы в воде и разведены в соотношении 1:3 (об./об.); разведенный раствор также содержал 3 мМ изобутилметилксантина. Затем гранулы осаждали ( 30 мин), ПМТ анализировали с помощью имеющегося в продаже измерительного оборудования и соответствующие значения IC50 для ингибирования активности ФДЭ соединениями определяли по зависимостям концентрация - воздействие с помощью нелинейного регрессионного анализа. Методика оценки ингибирования проникновения макромолекулы в монослои ЭКПВЧ (эндотелиальные клетки пупочной вены человека) Методикой исследования проникновения макромолекулы в монослои эндотелиальных клеток являлась методикой, описанной в публикации Langelervan Hinsbergh (1988), с изменениями. Эндотелиальные клетки пупочной вены человека выделяли из пупочных канатиков по стандартным методикам (Jaffeet al. 1973) и выращивали в базальной среде для эндотелиальных клеток (БСЭ) с прибавлением 2% ФТС(EGM2, выпускающегося фирмой Promocell GmbH, Heidelberg, Germany). После слияния клетки трипсинизировали и пересевали по 73000 клеток/лунка во вставки из поликарбонатного фильтра (размер отверстий - 3 мкм) Transwell (Costar GmbH, Bodenheim, Germany), на которые предварительно нанесен фибронектин, 10 мкг/см (Sigma, Taufkirchen, Germany). ЭКПВЧ выращивали в EGM2 (100 мкл в верхних лунках и 600 мкл в нижних лунках) в течение 4 дней до проведения эксперимента и среду заменяли через день. В день проведения эксперимента культуральную среду заменяли на M199 с прибавлением 1% сывороточного альбумина человека. Эндотелиальные клетки предварительно инкубировали с модификаторами циклического нуклеотида (селективный ингибитор ФДЭ 3 мотапизон, селективный ингибитор ФДЭ 4 RP73401, генераторы цГМФ ПНП (предсердный натрийуретический пептид) или СЯБ (специфический ядерный белок) и ингибиторы ФДЭ 2) в течение 15 мин. Затем ЭКПВЧ стимулировали тромбином(1 Ед.мл-1) (Sigma, Taufkichen, Germany) и пероксидазой хрена (5 мкг/мл) (Sigma, Taufkirchen, Germany) и маркерный белок макромолекулы прибавляли в верхние лунки. После 1 ч инкубации вставки Transwell удаляли и активность пероксидазы хрена, проникшей в монослой эндотелиальных клеток в нижних лун- 20014324 ках, определяли с помощью системы жидкого субстрата, содержащей 3,3',5,5'-тетраметилбензидин, выпускающейся фирмой Sigma (Taufkirchen, Germany). Результаты Типичные значения характеристик ингибирования [измеренные в виде -log IC50 (моль/л)], полученные в описанном выше анализе, приведены в представленной ниже табл. А, в которой номера соединений соответствуют номерам примеров. Таблица А. Ингибирование активности ФДЭ 2 Параллельно соединения, предлагаемые в настоящем изобретении, могут ингибировать вызванную тромбином проницаемость монослоев ЭКПВЧ для пероксидазы хрена (ПОХ) в качестве макромолекулярного маркера. Поэтому предположено, что ингибиторы ФДЭ 2 улучшают эндотелиальную барьерную функцию, которая нарушена при многочисленных патологических состояниях, таких острый респираторный дистресс-синдром (ОРДС) или тяжелая пневмония. Система для исследования этих клеточных эффектов ингибиторов ФДЭ 2 регистрировала энзимологические характеристики ФДЭ 2, которая обнаруживает довольно большие значения Km для цАМФ (циклический аденозинмонофосфат) и действие которой активируется посредством цГМФ. Вызванное тромбином увеличение проницаемости для ПОХ было полностью устранено путем полного ингибирования ФДЭ 3 (10 мкМ мотапизона) и ФДЭ 4 (1 мкМRP73401). Однако при дополнительном присутствии ПНП (100 нМ) или СЯБ (1 мМ) для дополнения ингибирования цГМФ ингибированием посредством ФДЭ 3 и 4, ингибирование проницаемости было частично обращено. Ингибиторы ФДЭ 2 блокируют вызванное тромбином увеличение проницаемости для ПОХ, если содержались 1 мкМ RP73401, 10 мкМ мотапизона, 100 нМ ПНП или 1 мМ СЯБ, что показывает, что ПНП или СЯБ при генерации цГМФ активируют ФДЭ 2. Зависящее от концентрации ингибирование проницаемости для ПНП при различных концентрациях исследовали с помощью выраженного в процентах ингибирования в присутствии или отсутствии ингибиторов ФДЭ 2 и в присутствии 1 мкМRP73401, 10 мкМ мотапизона и 100 нМ ПНП. При отсутствии ингибирования посредством ФДЭ 3 и 4,ПНП или СЯБ ингибиторы ФДЭ 2 оказывали очень слабое влияние на вызванную тромбином повышенную проницаемость для макромолекулы. Ингибирование вызванной СЯБ или ПНП проницаемости монослоев ЭКПВЧ: Клетки ЭКПВЧ на поликарбонатных фильтрах с размером отверстий, равным 3 мкм (Transwells),предварительно инкубировали в 1 мкМ RP73401 (для блокирования ФДЭ 4) и 10 мкМ мотапизона (для блокирования ФДЭ 3), 1 мМ СЯБ или 100 нМ ПНП и 1 мкМ исследуемого образца в течение 15 мин и затем стимулировали с помощью 1 Ед./мл тромбина. Проникновение ПОХ в нижних лунках исследовали через 60 мин. RP73401 и мотапизон полностью блокировали вызванную тромбином повышенную проницаемость, которая частично обращалась при воздействии СЯБ и ПНП. Соединения, предлагаемые в настоящем изобретении, могут ингибировать вызванное СЯБ или ПНП усиление проницаемости зависимым от концентрации образом. Типичные значения характеристик ингибирования [измеренные в виде -log IC50 (моль/л)], полученные в описанном выше анализе, приведены в представленной ниже табл. В, в которой номера соединений соответствуют номерам примеров. Таблица В. Ингибирование проницаемости, вызванной СЯБ или ПНПU обозначает непосредственную связь или метилен (-СН 2-),А обозначает фенил, пиридинил, тиофенил, ди-(С 1-С 4-алкокси)-фенил, или R11-замещенный фенил,R11 обозначает С 1-С 4-алкил, галоген, трифторметил, гидроксил, С 1-С 4-алкоксигруппу, полностью или преимущественно фторзамещенную С 1-С 4-алкоксигруппу, феноксигруппу, С 1-С 4-алкоксикарбонил,морфолиновую группу или ди-С 1-С 4-алкиламиногруппу,R2 обозначает аминогруппу, карбоксил, С 1-С 4-алкоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5,гдеR3 обозначает С 1-С 4-алкил, С 2-С 4-алкенил, С 3-С 7-циклоалкил, трифторметил, фенил, R31 замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный C1-C4-алкил или 1N-(R33)пиперидинил, где R31 обозначает С 1-С 4-алкоксигруппу, морфолиновую группу или ди-С 1-С 4 алкиламиногруппу,R32 обозначает гидроксил, фенил-С 1-С 4-алкоксигруппу, С 1-С 4-алкоксигруппу, фенил, R321 замещенный фенил, ди-С 1-С 4-алкиламиногруппу, морфолиновую группу или 4N-(R322)пиперазин-1-ил,гдеR41 обозначает гидроксил, C1-C4-алкоксигруппу, ди-C1-C4-алкиламиногруппу или морфолиновую группу,R42 обозначает C1-C4-алкоксигруппу или ди-C1-C4-алкиламиногруппу,R5 обозначает водород или C1-C4-алкил,или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклический радикал Het, гдеHet обозначает морфолиновую группу или 4N-(C1-C4-алкил)пиперазин-1-ил,и соли этих соединений. 2. Соединения формулы I по п.1, в которой R1 обозначает -U-A, гдеU обозначает непосредственную связь или метилен (-СН 2-), А обозначает фенил, пиридинил, тиофенил, диметоксифенил, или R11-замещенный фенил, гдеR11 обозначает метил, трет-бутил, хлор, фтор, бром, трифторметил, гидроксил, метоксигруппу,этоксигруппу, трифторметоксигруппу, феноксигруппу, метоксикарбонил, морфолиновую группу или диметиламиногруппу, R2 обозначает аминогруппу, карбоксил, C1-C4-алкоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, гдеR3 обозначает C1-C4-алкил, С 2-С 4-алкенил, С 3-С 7-циклоалкил, трифторметил, фенил, R31 замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный C1-C4-алкил или 1N-(R33)пиперидинил, где R31 обозначает C1-C4-алкоксигруппу, морфолиновую группу или ди-C1-C4 алкиламиногруппу,R32 обозначает гидроксил, фенил-C1-C4-алкоксигруппу, C1-C4-алкоксигруппу, фенил, R321 замещенный фенил, ди-C1-C4-алкиламиногруппу, морфолиновую группу или 4N-(R322)пиперазин-1-ил,где R321 обозначает C1-C4-алкоксигруппу,R322 обозначает C1-C4-алкил,R33 обозначает водород, C1-C4-алкил или C1-C4-алкилкарбонил,R4 обозначает водород, C1-C4-алкил, R41-замещенный С 2-С 4-алкил, фенил, R42-замещенный фенил или пиридинил, гдеR41 обозначает гидроксил, C1-C4-алкоксигруппу, ди-C1-C4-алкиламиногруппу или морфолиновую группу,R42 обозначает C1-C4-алкоксигруппу или ди-C1-C4-алкиламиногруппу,R5 обозначает водород или C1-C4-алкил,или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклической радикал Het, гдеHet обозначает морфолиновую группу или 4N-(С 1-С 4-алкил)пиперазин-1-ил,и соли этих соединений. 3. Соединения формулы I по п.1, в которой R1 обозначает -U-A, гдеU обозначает непосредственную связь или метилен (-СН 2-), А обозначает фенил или R11 замещенный фенил, где R11 обозначает метил, хлор, фтор, бром, трифторметил, гидроксил, метоксигруппу, феноксигруппу, метоксикарбонил или диметиламиногруппу, R2 обозначает аминогруппу, карбоксил, метоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, гдеR3 обозначает метил, винил, циклопропил, циклогексил, трифторметил, фенил, R31-замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный С 1-С 2-алкил или 1N-(R33)пиперидинил,где R31 обозначает метоксигруппу, морфолиновую группу или диметиламиногруппу,- 22014324R32 обозначает гидроксил, бензилоксигруппу, метоксигруппу, фенил, R321-замещенный фенил,диметиламиногруппу, морфолиновую группу или 4N-метилпиперазин-1-ил, где R321 обозначает метоксигруппу, R33 обозначает водород, метил или ацетил,R4 обозначает водород, метил, 2-(R41)этил, фенил, R42-замещенный фенил или пиридинил, гдеR41 обозначает гидроксил, метоксигруппу, диметиламиногруппу или морфолиновую группу,R42 обозначает метоксигруппу или диметиламиногруппу,R5 обозначает водород или метил,или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклический радикал Het, гдеHet обозначает морфолиновую группу или 4N-метилпиперазин-1-ил,и соли этих соединений. 4. Соединения формулы I по п.1, в которой R1 обозначает -U-A, где U обозначает непосредственную связь, А обозначает фенил или R11-замещенный фенил, где R11 обозначает фтор, бром, трифторметил или метоксигруппу, R2 присоединен в мета- или пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе триазолофталазинового скелета, и обозначает аминогруппу, карбоксил, метоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, гдеR3 обозначает метил, винил, циклопропил, циклогексил, трифторметил, фенил, R31-замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный C1-С 2-алкил или 1N-(R33)пиперидинил,где R31 обозначает метоксигруппу, морфолиновую группу или диметиламиногруппу,R32 обозначает гидроксил, бензилоксигруппу, метоксигруппу, фенил, R321-замещенный фенил,диметиламиногруппу, морфолиновую группу или 4N-метилпиперазин-1-ил, где R321 обозначает метоксигруппу, R33 обозначает водород, метил или ацетил,R4 обозначает водород, метил, 2-(R41)этил, фенил, R42-замещенный фенил или пиридинил, гдеR41 обозначает гидроксил, метоксигруппу, диметиламиногруппу или морфолиновую группу,R42 обозначает метоксигруппу или диметиламиногруппу,R5 обозначает водород или метил,или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклический радикал Het, гдеHet обозначает морфолиновую группу или 4N-метилпиперазин-1-ил,и соли этих соединений. 5. Соединения формулы I по п.1, в которой R1 обозначает -U-A, где U обозначает непосредственную связь, А обозначает фенил или R11-замещенный фенил, гдеR11 обозначает фтор, бром, хлор, трифторметил, метил или метоксигруппу, R2 присоединен в метаили пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к аминогруппе триазолофталазинового скелета, и обозначает аминогруппу, карбоксил, метоксикарбонил, -N(H)-C(O)R3 или -C(O)-N(R4)R5, гдеR3 обозначает метил, винил, циклопропил, циклогексил, трифторметил, фенил, R31-замещенный фенил, фуранил, имидазол-4-ил, пиридинил, R32-замещенный С 1-С 2-алкил или 1N-(R33)пиперидинил,где R31 обозначает метоксигруппу, морфолиновую группу или диметиламиногруппу,R32 обозначает гидроксил, бензилоксигруппу, метоксигруппу, фенил, R321-замещенный фенил,диметиламиногруппу, морфолиновую группу или 4N-метилпиперазин-1-ил, где R321 обозначает метоксигруппу, R33 обозначает водород, метил или ацетил,R4 обозначает водород, метил, 2-(R41)этил, фенил, R42-замещенный фенил или пиридинил, гдеR41 обозначает гидроксил, метоксигруппу, диметиламиногруппу или морфолиновую группу, R42 обозначает метоксигруппу или диметиламиногруппу,R5 обозначает водород или метил,или R4 и R5 совместно и с включением атома азота, с которым они связаны, образуют гетероциклический радикал Het, гдеHet обозначает морфолиновую группу, 4N-метилпиперазин-1-ил или 4N-этилпиперазин-1-ил и соли этих соединений. 6. Соединения формулы I по любому из пп.1-5, в которой R1 обозначает 4-метоксифенил, 2 метоксифенил, 2-бромфенил, 2-фторфенил, 2-(трифторметил)-фенил, 2-хлорфенил, 4-бромфенил или 2 метилфенил и соли этих соединений. 7. Соединения формулы I, выбранные из следующей группы: 4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид циклопропанкарбоновой кислоты,3-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фениламид циклопропанкарбоновой кислоты, и 1-4-[3-(4-метоксифенил)-[1,2,4]триазоло[3,4-а]фталазин-6-иламино]фенил-1-(4-метилпиперазин 1-ил)метанон 8. Фармацевтическая композиция, включающая одно или более соединений формулы I по любому из пп.1-7 совместно с фармацевтическими инертными наполнителями и/или вспомогательными вещест- 23014324 вами. 9. Применение соединений формулы I по любому из пп.1-7 для приготовления фармацевтических композиций, предназначенных для лечения заболеваний, связанных с активностью ФДЭ 2 (фосфодиэстеразы 2), таких как состояния патологически усиленной эндотелиальной активности и нарушенной функции эндотелиального барьера, таких как септический шок и сосудистый отек. 10. Применение соединений формулы I по любому из пп.1-7 для приготовления фармацевтических композиций, предназначенных для лечения (1) состояний, связанных с патологически усиленным неоангиогенезом, таких как все типы опухолей (доброкачественных или злокачественных), или (2) всех типов воспалительных заболеваний, связанных с неоангиогенезом, таких как нарушения типа артрита. 11. Способ лечения состояний патологически усиленной эндотелиальной активности и нарушенной функции эндотелиального барьера, таких как септический шок и сосудистый отек, у нуждающегося в нем пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по любому из пп.1-7. 12. Способ лечения (1) патологических состояний, связанных с патологически усиленным неоангиогенезом, таких как все типы опухолей (доброкачественных или злокачественных), или (2) всех типов воспалительных заболеваний, связанных с неоангиогенезом, таких как нарушения типа артрита, у нуждающегося в нем пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по любому из пп.1-7. 13. Применение соединений формулы I по любому из пп.1-7 для приготовления фармацевтических композиций, предназначенных для лечения пневмонии или острого респираторного дистресс синдрома(ARDS) при септическом шоке. 14. Применение соединений формулы I по любому из пп.1-7 для приготовления фармацевтических композиций, предназначенных для лечения острых и хронических нарушений дыхательных путей. 15. Применение по п.14, где острые и хронические нарушения дыхательных путей выбраны из ринита, бронхита, бронхиальной астмы, эмфиземы, хронического обструктивного заболевания легких(COPD). 16. Способ лечения пневмонии или острого респираторного дистресс синдрома (ARDS) при септическом шоке у нуждающегося в этом пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по любому из пп.1-7. 17. Способ лечения острых и хронических нарушений дыхательных путей у нуждающегося в этом пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по любому из пп.1-7. 18. Способ по п.17, где острые и хронические нарушения дыхательных путей выбраны из ринита,бронхита, бронхиальной астмы, эмфиземы, хронического обструктивного заболевания легких (COPD).
МПК / Метки
МПК: C07D 487/04, A61K 31/5025
Метки: триазолофталазины
Код ссылки
<a href="https://eas.patents.su/25-14324-triazoloftalaziny.html" rel="bookmark" title="База патентов Евразийского Союза">Триазолофталазины</a>
Предыдущий патент: Закрепитель анкерных стержней, патронированный минеральный
Следующий патент: 18-метил-9-нор-17-прегн-4-ен-21, 17-карболактоны, а также лекарственные препараты, которые их содержат
Случайный патент: Вкладыш центробежного насоса (варианты), центробежный насос с таким вкладышем, способ установки вкладыша в центробежном насосе (варианты)








