Полипептидные маркеры для диагностики и оценки сосудистых заболеваний
Формула / Реферат
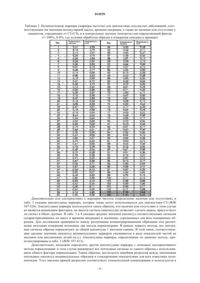
1. Способ диагностики сосудистых заболеваний (СЗ), включающий стадию определения наличия или отсутствия по меньшей мере одного полипептидного маркера в образце, где указанный полипептидный маркер выбирают из маркеров 1-526, которые характеризуются следующими значениями молекулярной массы и времени миграции:
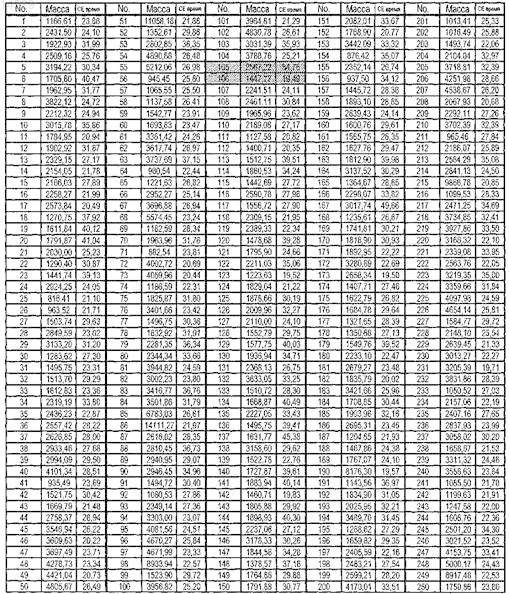
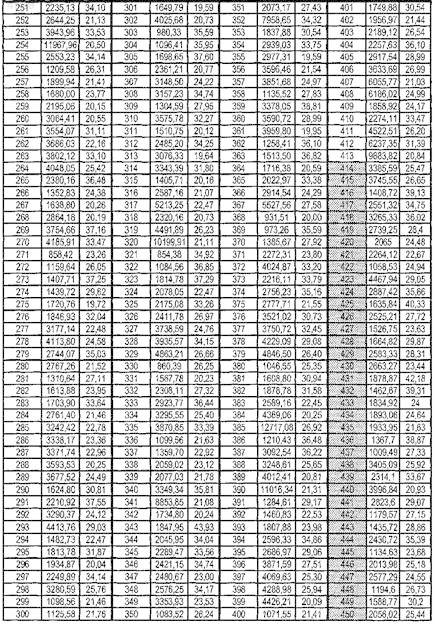
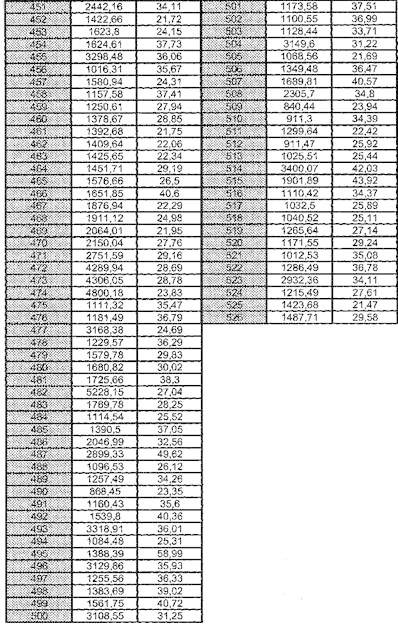
2. Способ по п.1, отличающийся тем, что оценку устанавливаемого наличия или отсутствия маркеров 1-106 проводят с помощью следующих эталонных значений:
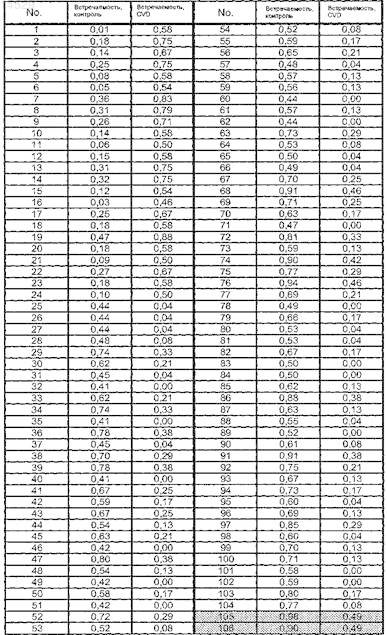
3. Способ по п.1, отличающийся тем, что оценку амплитуды маркеров 107-413 проводят с помощью следующих эталонных значений:
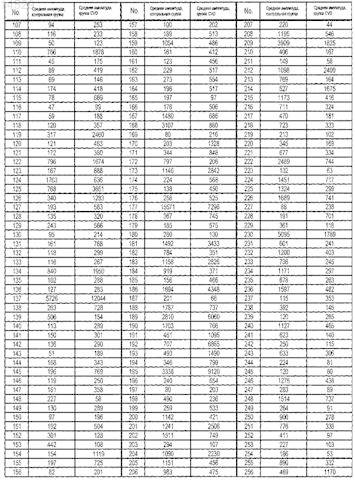
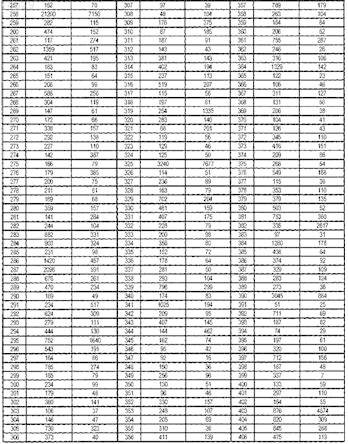
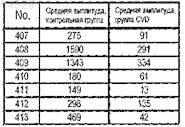
а для маркеров 414-526 ее проводят с помощью следующих эталонных значений:

4. Способ по п.1, где используют по меньшей мере два, или по меньшей мере три, или по меньшей мере пять или шесть, или по меньшей мере десять, или все полипептидные маркеры, определенные в п.1.
5. Способ по любому из пп.1-4, где указанный образец, взятый у субъекта, представляет собой образец мочи или образец крови (образец сыворотки или плазмы крови).
6. Способ по любому из пп.1-5, где используют капиллярный электрофорез, ВЭЖХ, ионную спектрометрию и/или масс-спектрометрию в газовой фазе для выявления наличия или отсутствия указанного полипептидного маркера или маркеров.
7. Способ по любому из пп.1-6, где капиллярный электрофорез проводят перед измерением молекулярной массы указанных полипептидных маркеров.
8. Способ по любому из пп.1-7, где масс-спектрометрию используют для выявления наличия или отсутствия указанного полипептидного маркера или маркеров.
9. Применение по меньшей мере одного полипептидного маркера, выбранного из маркеров 1-526, который характеризуется значениями молекулярной массы и времени миграции по п.1, для диагностики сосудистых заболеваний.
10. Применение по п.9, отличающееся тем, что время СЕ определяют с помощью стеклянного капилляра длиной 90 см, имеющего внутренний диаметр (в/д) 50 мкм, при напряжении 25 кВ, где в качестве растворителя мобильной фазы используют 20% ацетонитрил, 0,25М муравьиную кислоту в воде.
11. Способ диагностики сосудистых заболеваний (СЗ), включающий стадии:
a) разделения образца по меньшей мере на три, предпочтительно 10, подобразцов;
b) анализа по меньшей мере двух подобразцов для определения наличия или отсутствия амплитуды по меньшей мере одного полипептидного маркера в образце, где указанный полипептидный маркер выбирают из маркеров 1-526, которые характеризуются значениями молекулярной массы и времени миграции (времени СЕ) по п.1.
12. Способ по п.11, где проводят измерение по меньшей мере 10 подобразцов.
13. Способ по меньшей мере по одному из пп.1-8 и 11,12, отличающийся тем, что время СЕ определяют с помощью стеклянного капилляра длиной 90 см, имеющего внутренний диаметр (в/д) 50 мкм, при напряжении 25 кВ, где в качестве растворителя мобильной фазы используют 20% ацетонитрил, 0,25М муравьиную кислоту в воде.
14. Комбинация маркеров, включающая по меньшей мере 10 маркеров, выбранных из маркеров 1-526, которые характеризуются значениями молекулярной массы и времени миграции (времени СЕ) по п.1.
Текст
ПОЛИПЕПТИДНЫЕ МАРКЕРЫ ДЛЯ ДИАГНОСТИКИ И ОЦЕНКИ СОСУДИСТЫХ ЗАБОЛЕВАНИЙ Способ диагностики сосудистых заболеваний (СЗ), включающий стадию определения наличия или отсутствия по меньшей мере одного полипептидного маркера в образце, где указанный полипептидный маркер выбирают из маркеров 1-526, которые характеризуются определенными значениями молекулярной массы и времени миграции (времени СЕ).(71)(73) Заявитель и патентовладелец: МОЗАИКС ДАЙОГНОСТИКС ЭНД ТЕРАПЬЮТИКС АГ (DE) 014529 И изобретение относится к использованию данных о наличии или отсутствии одного или более пептидных маркеров в образце, взятом от субъекта, для целей диагностики и оценки тяжести сосудистых заболевания (СЗ) и к способу диагностики и оценки таких сосудистых заболеваний, где наличие или отсутствие одного или более пептидных маркеров является показателем тяжести СЗ. Сосудистые заболевания представляют собой заболевания, поражающие сосуды организма и, следовательно, такие органы, как сердце, головной мозг, почка и т.п. Они включают, например, артериосклероз, нарушение кровообращения, гипертензию и сердечную аритмию. Кровеносные сосуды Артериосклероз относится к процессу затвердевания артерий за счет образования отложений на стенках сосудов. Отложение кристаллов холестерина ведет к созданию воспалительных очагов (атером),в которых могут оседать компоненты крови, липиды, метаболические шлаки и известковые соли. Образуются так называемые бляшки, представляющие собой двумерные уплотнения, в результате чего сосудистая стенка становится более ригидной и сужается. Артерия теряет присущую ей эластичность и с трудом выполняет свою функцию, т.е. транспортировку крови от сердца в отдельные участки организма. Вторичные заболевания включают, например, стенокардию, инфаркт миокарда, сердечную недостаточность, инсульт. Нарушение кровообращения чаще всего поражает нижнюю часть тела на участке от брюшной аорты до артерий ног и ведет к снижению кровотока и доставки кислорода к мышечной ткани,которая постепенно некротизируется. На конечной стадии образуются язвы и закупоривают сосуды до такой степени, что становится неизбежной ампутация. Гипертензия не имеет определенной причины, так что прием лекарственных средств или избыточная секреция гормонов надпочечников может вызвать повышение давления крови. Высокое давление крови также имеет место при постоянном стрессе, что приводит к ангиоспазму. Гипертензия приводит к повреждению сосудистых стенок, так что возникает риск их разрыва или обструкции. Если нарушается регулярность сердцебиения, то такое состояние называется сердечной аритмией. Частота сердечных сокращений может быть либо слишком быстрой (тахикардия),либо слишком медленной (брадикардия), либо нерегулярной (аритмия). Сосудистых заболеваний можно избежать с помощью профилактики, поскольку они также вызываются нездоровым и неестественным образом жизни. Путем радикального изменения образа жизни артериосклероз на ранней стадии его развития может быть остановлен, например, за счет снижения давления крови и уровня липидов в крови. Прогрессирование сосудистых заболеваний может быть дополнительно замедлено с помощью медикаментозной терапии (например, при использовании ацетилсалициловой кислоты, блокаторов бетарецептора, ингибиторов АХЭ и т.п.). Однако следует отметить, что поврежденные сосуды не подвергаются репарации и патологический процесс на развитой стадии является необратимым. Таким образом,раннее выявление сосудистых заболеваний чрезвычайно важно. Сердце При ишемической болезни сердца диагностика СЗ осуществляется в первую очередь косвенно, путем оценки факторов риска и неинвазивных исследований, таких как измерение давления крови, регистрация электрокардиограмм в покое и с нагрузкой, а также определение картины крови для выявления липидного статуса (уровень ЛНП-холестерина, уровень ЛВП-холестерина, уровень триглицеридов), измерение уровня глюкозы натощак и, при необходимости, HbA1c. Если в ходе таких исследований выявляется наличие показателей, сопряженных с высоким риском, то есть в близком будущем могут ожидаться серьезные сосудистые явления (смертельный исход, инфаркт миокарда), то делается более точный диагноз с помощью инвазивных методов диагностики, например с использованием катетерного исследования или коронарной ангиографии. Таким образом, сосуды сердца, коронарные сосуды и другие сосуды могут быть исследованы с помощью катетерных или рентгеновских методов. Методы рентгеновского контрастного исследования используются для лучшей визуализации сердца и сосудов на рентгеновском снимке. Показания для проведения коронарной ангиографии включают предварительные тесты с результатом низкой или средней вероятности развития серьезных сосудистых явлений, когда неинвазивная диагностики не может дать надежных результатов в случае пациентов, для которых неинвазивное тестирование невозможно из-за инвалидности или имеющихся заболеваний, а также в случае пациентов, для которых необходимо однозначно исключить возможность ишемической болезни сердца по причинам,связанным с родом их профессиональной деятельности (например, в случае пилотов, пожарных). Однако коронарная ангиография может быть проведена только в том случае, если исключены различные осложнения, такие как гипертиреоз или аллергия на контрастные среды, в дополнение к указанным выше предварительным обследованиям. Кроме того, поскольку контрастная среда выделяется через почки, должна быть гарантирована в достаточной мере почечная функция или, в случае пациентов, зависимых от диализа, после обследования всегда должен проводиться диализ. Таким образом, становится ясно, что имеется выраженная потребность в неинвазивных способах ранней и надежной диагностики сосудистых заболеваний. Почка Сосудистые заболевания почки включают стеноз почечной артерии; тромбоз почечной артерии;-1 014529 эмболию почечной артерии; тромбоз почечной вены. Стеноз почечной артерии представляет собой одностороннее или двустороннее сужение почечной артерии или ее основных ветвей. Она может вызвать артериальную гипертензию, которая тогда называется реноваксулярной гипертензией. Причиной указанной гипертензии является артериосклероз (в основном в пожилом возрасте), который имеет место примерно в 70% всех случаев, а также фиброзно-мышечная дисплазия (аномалия соединительной ткани), которая имеет место примерно в 20% случаев. Изредка имеют место аневризмы аорты или почечной артерии, васкулиты, механическое сжатие из-за опухоли или кист, эмболии или тромбозы. Сужение почечной артерии ведет к сниженному току крови через пораженную почку. Для компенсации возможного (локального) снижения давления крови почка усиливает продукцию ренина, что ведет к увеличению объема крови и к повышению давления крови во всем организме через механизм, опосредованный ангиотензином-альдостероном, и, в итоге, к артериальной гипертензии. В этой связи, стеноз почечной артерии чаще всего выявляется в том случае, когда гипертензия уже развилась, но лишь примерно в 1-2% всех случаев гипертензии рассматривается как причинный фактор. С точки зрения терапии имеются различные возможности: РТА (чрескожная катетерная транслюминальная ангиопластика): расширение имеющегося сужения с помощью вставляемого баллонного катетера (баллонная дилатация); стент: вставка проволочной сетки (стента), которая позволяет держать сосуд в открытом состоянии; хирургическое устранение стеноза. Часто причиной тромбоза почечной артерии являются эмболии, возникающие в сердце, например,при фибрилляции предсердий, которые сопровождаются такими симптомами, как боль в боку, протеинурия, очень высокий уровень ЛДГ. Боль в боку также наблюдается при тромбозе почечной вены, но при этом дополнительно также выявляется протеинурия и в некоторых случаях гематурия или нефротический синдром. Головной мозг Суженные сосуды в области мозга приводят к снижению снабжения кислородом и в том случае, когда артерии закупориваются (например, в острой фазе образования сгустка крови из-за изменений, вызванных склерозом артерий), возникает инсульт, сопровождающийся потерей чувствительности, параличем, нарушением речи и т.п. В артериях мозга, таких как крупные артерии, склероз артерий может в редких случаях приводить к аневризмам сосудистых стенок и в сочетании с факторами риска, такими как гипертензия, сосудистая стенка может разрываться и приводить к угрожающему жизни внутреннему кровотечению. Неожиданно было показано, что определенные пептидные маркеры, выявленные в образце мочи у субъекта, могут использоваться для диагностики СЗ и, соответственно, для принятия решения о необходимости проведения медикаментозной терапии. Таким образом, настоящее изобретение относится к использованию данных о наличии или отсутствии по меньшей мере одного пептидного маркера, в идеальном случае нескольких пептидных маркеров,в образце мочи у субъекта для целей диагностики сосудистых заболеваний, где указанный один или несколько полипептидных маркеров выбирают из полипептидных маркеров 1-526, которые характеризуются значениями молекулярной массы и временем миграции, приведенными в табл. 1.-2 014529 Таблица 1. Полипептидные маркеры, используемые для диагностики сосудистых заболеваний, и соответствующие им молекулярные массы и время миграции (СЕ время в минутах) Предпочтительно используют маркеры 1-104 и/или 107-413. Применительно к настоящему изобретению, возможно также установить тяжесть указанного СЗ. Информация такого рода помогает определить, какие терапевтические меры следует применить. Время миграции определяют с помощью капиллярного электрофореза (СЕ), например, как описано в приведенном ниже примере, раздел 2. Для этого используют стеклянный капилляр длиной 90 см с внутренним диаметром (в.д.) 75 мкм и наружным диаметром (н.д.) 360 мкм при напряжении 30 кВ. В качестве растворителя для образца используют 30% метанол, 0,5% муравьиную кислоту в воде. Известно, что показатель времени миграции СЕ может варьировать. Тем не менее, порядок значений, при которых элюируются полипептидные маркеры, в типичном случае одинаков для любой исполь-4 014529 зуемой системы СЕ. Для компенсации различий во времени миграций система может быть нормализована с использованием стандартов, для которых показатели времени миграции известны. Указанные стандарты могут представлять собой, например, полипептиды, указанные в примерах (см. пример, раздел 3). Характеристики полипептидных маркеров, показанных в табл. 1-3, были определены с помощью метода капиллярного электрофореза-масс-спектрометрии (CE-MS), который был подробно описан, например, Нейхоффом с соавт. (Neuhoff et al., Rapid Communications in mass spectrometry, 2004, Vol. 20, pp. 149-156). Вариации в значениях молекулярной массы между отдельными измерениями или между измерениями, полученными с использованием разных масс-спектрометров, относительно малые и в типичном случае варьируют в диапазоне 0,1%, предпочтительно в диапазоне 0,05%, более предпочтительно в диапазоне 0,03% и наиболее предпочтительно в диапазоне 0,01%. Полипептидные маркеры согласно настоящему изобретению представляют собой белки или пептиды или продукты разложения белков или пептидов. Они могут быть химически модифицированы, например, за счет посттрансляционных модификаций, таких как гликозилирование, фосфорилирование,алкилирование или формирование дисульфидных мостиковых связей, или с помощью других реакций,например, связанных с деградацией. Кроме того, полипептидные маркеры могут быть также химически изменены, например за счет окисления, возникающего при очистке образцов. На основе параметров, определяющих полипептидные маркеры (молекулярный вес и время миграции), становится возможным идентифицировать последовательность соответствующих полипептидов с использованием известных в данной области методик. Полипептиды согласно настоящему изобретению (см. табл. 1-4) используются для диагностики тяжести СЗ. Термин "диагностика" в контексте настоящего описания обозначает процесс формирования заключения на основании информации о симптомах или явлениях, характерных для того или иного заболевания или повреждения. В данном случае вывод о тяжести СЗ делается на основании наличия или отсутствия конкретных полипептидных маркеров. Таким образом, полипептидные маркеры согласно настоящему изобретению определяют в образце, взятом от субъекта, где наличие или отсутствие маркера позволяет сделать вывод о тяжести СЗ. Наличие или отсутствие полипептидного маркера может быть определено по методу, известному в данной области. Ниже приведены примеры известных методик, которые могут быть использованы с этой целью. Считается, что полипептидный маркер присутствует, если измеряемый соответствующий показатель такой же по величине, как и пороговое значение. Если данный измеряемый показатель по величине ниже указанного порогового значения, то полипептидный маркер расценивается как отсутствующий. Указанное пороговое значение может быть определено либо с учетом данных о чувствительности метода измерения (предела определения), либо эмпирически. В контексте настоящего изобретения считается, что пороговое значение превышено, предпочтительно в том случае, если измеряемый показатель для образца с данной молекулярной массой по меньшей мере в два раза превышает соответствующее значение для образца слепой пробы (например, только буферного раствора или растворителя). Один или несколько полипептидных маркеров могут использоваться таким образом, чтобы измерялось наличие или отсутствие указанного одного или нескольких маркеров, где наличие или отсутствие является показателем тяжести СЗ (маркер частоты). Таким образом, имеются полипептидные маркеры,которые втипичном случае присутствуют у субъектов с СЗ, но встречаются не так часто или отсутствуют у субъектов без СЗ, например см. 1-24 (табл. 2). Дополнительно, имеются полипептидные маркеры,которые выявляются у пациентов с СЗ, такие как полипептидные маркеры No. 25-106, но которые встречаются реже или вовсе отсутствуют у пациентов без СЗ.-5 014529 Таблица 2. Полипептидные маркеры (маркеры частоты) для диагностики сосудистых заболеваний, соответствующие им значения молекулярной массы, времени миграции, а также их наличие или отсутствие у пациентов, страдающих от СЗ (СЗ), и в контрольных группах (контроль) как определяющий фактор(1=100%, 0-0%; где условия обработки образца и измерения описаны в примере) Дополнительно или альтернативно к маркерам частоты (определение наличия или отсутствия), в табл. 3 указаны амплитудные маркеры, которые также могут использоваться для диагностики СЗ ( 107-526). Амплитудные маркеры используются таким образом, что наличие или отсутствие в этом случае не является решающим фактором, но высота сигнала (амплитуда) позволяет сделать вывод, присутствует ли сигнал в обеих группах. В табл. 3 и 4 указаны средние значения амплитуд соответствующих сигналов(охарактеризованных по массе и времени миграции) в значениях, усредненных для всех измеренных образцов. Для достижения сравнимости между различными концентрированными образцами или различными методами измерения возможны два метода нормализации. В рамках первого метода, все пептидные сигналы образца нормализуют до общей амплитуды 1 миллион единиц. В этой связи, соответствующие средние значения амплитуд индивидуальных маркеров указываются в виде показателей частей на миллион или миллионных долей (м.д.). Амплитудные маркеры, определенные по данному методу, проиллюстрированы в табл. 3 ( 107-413). Дополнительно, возможно определить другие амплитудные маркеры с помощью альтернативного метода нормализации: в этом случае ранжируют все пептидные сигналы от одного образца с использованием общего фактора нормализации. Таким образом, достигается линейная регрессия между значениями пептидных амплитуд индивидуальных образцов и стандартными показателями для всех известных полипептидов. Угол наклона прямой регрессии соответствует относительной концентрации и используется в-6 014529 качестве фактора нормализации для данного образца. Биомаркеры, полученные в рамках указанного метода нормализации, приведены в табл. 4 ( 414-526). Во всех использованных в испытании группах было включено по меньшей мере 20 индивидуальных образцов от пациентов или контрольных образцов с целью получения надежных значений средних показателей для амплитуды. Решение о диагнозе (наличие СЗ или нет) принимают, сравнивая, насколько выше амплитуды соответствующих полипептидных маркеров в образце пациента, чем средние значения амплитуд в контрольной группе или группе с СЗ. Если указанная амплитуда скорее соответствует среднему значению амплитуд в группе с СЗ, то рассматривается вариант наличия сосудистого заболевания, и если скорее соответствует среднему значению амплитуд в контрольной группе, то делается вывод об отсутствии СЗ. Расстояние между измеренным значением и средним значением амплитуды может оцениваться как вероятность того, что конкретный образец принадлежит к той или иной группе. Такого рода пояснения могут быть даны с помощью маркера No. 137 (табл. 3). Среднее значение амплитуды указанного маркера существенно повышается при СЗ (12044 м.д. в сравнении с 5726 м.д. в контрольной группе). В этом случае, если значение для данного маркера в образце пациента составляет от 0 до 5726 м.д. или превышает этот диапазон максимум на 20%, например составляет от 0 до 6871 м.д., то делается вывод, что данный образец относится к контрольной группе. Если указанное значение составляет 12044 м.д. или ниже на 20% или выше, то есть его значение составляет от 9635 и более, то данный результат рассматривается как показание на наличие сосудистого заболевания. Альтернативно, расстояние между измеренным значением и средним значением амплитуды может оцениваться как вероятность того, что данный образец принадлежит к той или иной группе. Маркер частоты представляет собой вариант амплитудного маркера, где указанная амплитуда является низкой в некоторых образцах. Возможно превратить такие маркеры частоты в амплитудные маркеры за счет включения соответствующих образцов, в которых указанный маркер не найден, в расчеты амплитуды в случае очень малой амплитуды, относительно предела выявления. Таблица 3. Амплитудные маркеры при их нормализации в соответствии с подходом 1-8 014529 Таблица 4. Амплитудные маркеры, при их нормализации в соответствии с подходом 2 Субъект, для которого отбирают образец и определяют наличие или отсутствие одного или нескольких полипептидных маркеров, может быть любым субъектом, который страдает от СЗ. Предпочтительно указанный субъект представляет собой млекопитающее и наиболее предпочтительно человека. В предпочтительном варианте осуществления настоящего изобретения используют не один полипептидный маркер, но сочетание полипептидных маркеров для определения тяжести СЗ, где заключение о тяжести СЗ делается на основании их наличия или отсутствия. При сравнении множества полипептидных маркеров снижается или устраняется двойственность в общей оценке результатов, в случае нескольких индивидуальных отклонений от типичной вероятности наличия у больного индивидуума или у контрольного индивидуума. Образец, в котором определяют наличие или отсутствие одного или нескольких пептидных маркеров согласно настоящему изобретению, может быть любым образцом, который получают из организма субъекта. Указанный образец представляет собой образец, который имеет полипептидный состав, подхо-9 014529 дящий для обеспечения соответствующей информацией о состоянии субъекта (наличие СЗ или отсутствие). Например, это может быть образец крови, мочи, синовиальной жидкости, тканевой жидкости, секрета организма, пота, цереброспинальной жидкости, лимфы, кишечного, желудочного сока или сока поджелудочной железы, желчи, слезной жидкости, образец ткани, спермы, вагинальной жидкости или образец кала. Предпочтительно образец представляет собой жидкий образец. В предпочтительном варианте осуществления настоящего изобретения указанный образец представляет собой образец мочи или образец крови, где образец крови может представлять сыворотку (крови) или образец плазмы (крови). Образцы крови могут быть отобраны по методике, преимущественно используемой в данной области. Предпочтительно используют образец из средней струи мочи, в качестве образца согласно настоящему изобретению. Например, образец мочи может быть отобран с помощью аппарата для мочеиспускания,описанного в WO 01/74275. Образцы крови могут быть отобраны по известным в данной области методикам, например, из вены, артерии или капилляра. Обычно образец крови получают при отборе венозной крови с помощью шприца, например из руки субъекта. Термин "образец крови" включает образцы, полученные из крови при дальнейшем использовании методов очистки и разделения, с получением образцов плазмы крови или сыворотки крови. Наличие или отсутствие полипептидного маркера в образце может быть определено по любому методу, известному в данной области, который подходит для определения полипептидных маркеров. Такие методы известны специалистам в данной области. В принципе, наличие или отсутствие полипептидного маркера может быть определено с использованием прямых методов, таких как масс-спектрометрия, или опосредованных методов, например, при оценке лигандов. Если требуется или если желательно, образец от субъекта, например образец мочи или крови, может быть подвергнут предварительной обработке любыми подходящими методами и, например, подвергнут очистке или разделению перед определением наличия или отсутствия одного или нескольких полипептидных маркеров. Указанная обработка может включать, например, очистку, разделение, разбавление или концентрирование. Применяемые при этом методы могут представлять собой, например, центрифугирование, фильтрование, ультрафильтрацию, диализ, осаждение или хроматографические методы,такие как аффинное разделение или разделение с помощью ионообменной хроматографии, электрофоретическое разделение, например разделение на основе различного характера миграции электрически заряженных частиц в растворе под действием электрического поля. Конкретные примеры таких методов включают гель-электрофорез, двумерный электрофорез в полиакриламидном геле (2D-ПААГ), капиллярный электрофорез, хроматография, основанная на аффинности к металлу, хроматография, основанная на иммобилизации, определяемой аффинностью к металлу (IMAC), аффинная хроматография, основанная на сродстве к лектину, жидкостная хроматография, высокоэффективная жидкостная хроматография(ВЭЖХ), ВЭЖХ с нормальной и обращенной фазой, катионообменная хроматография и методы, основанные на селективном связывании с поверхностями. Все перечисленные методы хорошо известны в данной области и любой специалист со средним уровней знаний способен выбрать соответствующую методику как функцию используемого образца, а также метод определения наличия или отсутствия одного или нескольких полипептидных маркеров. В одном варианте осуществления настоящего изобретения указанный образец перед проведением разделения с помощью капиллярного электрофореза подвергают разделению, очистке ультрацентрифугированием и/или разделению методами ультрафильтрации на фракции, которые содержат полипептидные маркеры определенного молекулярного размера. Предпочтительно используют метод масс-спектрометрии для определения наличия или отсутствия полипептидного маркера, где очистка или разделение образца могут быть проведены с учетом результатов данного метода. В сравнении с используемыми в настоящее время методиками, массспектрометрический анализ имеет то преимущество, что в ходе одного анализа может быть определена концентрация большого числа (100) полипептидов в образце. При этом может использоваться любой масс-спектрометр. С использованием масс-спектрометрии в сложной смеси возможно измерить полипептидный маркер на уровне 10 фмолей, то есть 0,1 нг белка размером 10 кД, в рамках рутинного исследования с достоверностью примерно 0,01%. В масс-спектрометрах ионобразующую единицу связывают с подходящим анализируемым устройством. Так, например, для измерения в жидких образцах чаще всего используют интерфейсы с электронапылением-ионизацией (ESI), тогда как метод MALDI (лазерная десорбция/ионизация, связанная с матрицей) используют для измерения уровня ионов в образцах, кристаллизованных в матрице. Для анализа образованных ионов могут использоваться анализаторы квадруполей, ионные ловушки или устройства для определения времени полета (TOF). При проведении ионизации электронапылением (ESI) молекулы, присутствующие в растворе, подвергаются атомизации, в частности при воздействии тока высокого напряжения (например, 1-8 кВ), при этом вначале образуются заряженные капельки, которые становятся меньше при испарении растворителя. В итоге, так называемые кулоновские взрывы приводят к образованию свободных ионов, которые могут быть выявлены и проанализированы.- 10014529 При проведении анализа ионов с помощью метода TOF, достигают ускорения при определенном значении напряжения, которое сообщает одинаковое количество кинетической энергии ионам. После этого очень тщательно измеряют время, необходимое соответствующим ионам для преодоления определенного расстояния при полете через трубку. Поскольку при условии равного уровня кинетической энергии скорость ионов зависит от их массы, то последний параметр может быть определен. Анализаторы,функционирующие по принципу TOF, обладают очень высокой скоростью сканирования и, в этой связи,позволяют достичь хорошего разрешения. Предпочтительные методики, используемые для определения наличия или отсутствия пептидных маркеров, включают спектрометрию ионов в газовой фазе, такую как лазерная масс-спектрометрия десорбции/ионизации MALDI-TOF MS, SELDI-TOF MS (лазерная десорбция/ионизация), усиленная поверхностным взаимодействием, MS LC (жидкостная хроматография/масс-спектрометрия), 2D-ПААГ/MS и методы капиллярного электрофореза-масс-спектрометрии (CT-MS). Все указанные методики известны специалистам в данной области. Особенно предпочтительной является методика CE-MS, в рамках которой капиллярный электрофорез объединен с масс-спектрометрией. Данный метод описан более детально, например, в заявке на патент Германии DE 10021737, а также в работах Кайзера с соавт. (Kaiser et al., J. Chromatogr. A, 2003, Vol,1013: 157-171; и Electrophoresis, 2004, 25: 2044-2055) и Виттке с соавт.(Wittke et al., J. Chromatogr. A,2003, Vol, 1013: 173-181). Методика СЕ позволяет определить одновременно в течение короткого периода времени наличие нескольких сотен полипептидных маркеров в образце в малом объеме и с высокой чувствительностью. После измерения образца описывается характер данных полипептидных маркеров с тем, чтобы полученную картину можно было сравнить с эталонными картинами больных или здоровых субъектов. В большинстве случаев достаточно использовать ограниченное число полипептидных маркеров для диагностики UAS. Наиболее предпочтительным методом является метод CE-MS, который включает СЕ, объединенный в формате одного анализа с ESI-TOF MS. В случае CE-MS предпочтительно использование летучих растворителей и лучше всего проводить работу в практически бессолевых условиях. Примеры таких растворителей включают ацетонитрил, изопропанол, метанол и т.п. Данные растворители могут быть разбавлены водой или слабой кислотой (например, 0,1-1% муравьиной кислотой) для протонирования анализируемого компонента, предпочтительно полипептидов. При использовании капиллярного электрофореза можно проводить разделение молекул на основе их заряда и размера. Нейтральные частицы будут мигрировать со скоростью электроосмотического потока при подведении электрического тока, при этом движение катионов ускоряется в направлении к катоду, а поток анионов затормаживается. Преимущество капилляров при проведении капиллярного электрофореза заключается в возможности благоприятного соотношения поверхности к объему, что позволяет достичь хорошего рассеяния джоулевской тепловой энергии, генерированной под действием тока. Это, в свою очередь, позволяет использовать высокое напряжение (обычно до 30 кВ) и, соответственно,достичь высокого качества разделения, проводя анализ в течение короткого периода времени. При проведении капиллярного электрофореза обычно используют капилляры из силикатного стекла, имеющие, в типичном случае, внутренний диаметр от 50 до 75 мкм. Длины используемых капилляров составляют, например, 30-100 см. Следует также отметить, что разделяющие капилляры обычно выполнены из силикатного стекла с пластиковым покрытием. При этом указанные капилляры могут быть также необработанными, то есть могут содержать экспонированные гидрофильные группы на внутренней поверхности или они могут содержать покрытие на внутренней поверхности. Для улучшения разрешения может использоваться гидрофобное покрытие. В дополнение к подаче напряжения, можно также воздействовать за счет давления, которое в типичном случае варьирует от 0 до 1 фунт/дюйм 2 (0-5668,92 Па). Давление может быть также применено только при разделении или в ином соответствующем варианте. В предпочтительном методе измерения полипептидных маркеров указанные маркеры в образце разделяют с помощью капиллярного электрофореза и затем подвергают прямой ионизации и переносят на поточную линию анализа с масс-спектрометром для выявления наличия маркеров. В рамках методики согласно настоящему изобретению удобно использовать несколько полипептидных маркеров при диагностике СЗ, в частности используют по меньшей мере три полипептидных маркера, например маркеры 1, 2 и 3; 1, 2 и 4; и т. п. Более предпочтительно использовать 4, 5 или 6 маркеров. Еще более предпочтительно использовать по меньшей мере 11 маркеров, например маркеры 1-11. Наиболее предпочтительно использовать все 526 маркеров, указанных в табл. 1. Для определения вероятности наличия тяжелой формы СЗ при использовании нескольких маркеров применяют статистическое методы анализа, известные специалистам в данной области. Так, например,может быть использован метод Random Forests, описанный в Вайссингером с соавт. (Weissinger et al.,Kidney Int. 2004, 65; 2426-2434), с включением в данную методику компьютерной программы, такой какS-Plus, или вспомогательных векторных устройств, описанных в той же публикации.- 11014529 Примеры 1. Подготовка образца. Для выявления полипептидных маркеров с целью диагностики СЗ используют мочу. Мочу собирают от здоровых доноров (контрольная группа), а также от пациентов, имеющих тяжелую форму СЗ. Для последующих измерений по методу CE-MS разделяют путем ультрафильтрации белки, которые также содержатся в моче пациентов в повышенных концентрациях, такие как альбумин и иммуноглобулины. Для этого смешивают 700 мкл собранной мочи с 700 мкл буфера для фильтрации (2 М мочевины,10 мМ аммиака, 0,02% ДСН). Указанный образец объемом 1,4 мл подвергают ультрафильтрации (20 кДа,Sartorius, Gottingen, Германия). Ультрафильтрацию проводят со скоростью 3000 об/мин в центрифуге до получения ультрафильтрата объемом 1,1 мл. Затем полученный фильтрат объемом 1,1 мл наносят на колонку PD 10 (Amersham Bioscience, Uppsala, Швеция), проводят элюцию с использованием 2,5 мл 0,01% NH4OH и лиофилизируют. Для измерения в рамках методики CE-MS полипептиды снова ресуспендируют в 20 мкл воды (качества для ВЭЖХ,Merck). 2. Измерение по методу CE-MS. Измерения по методу CE-MS проводят с использованием системы для проведения капиллярного электрофореза от Beckman Coulter (система Р/АСЕ MDQ; Beckman Coulter Inc., Fullerton, CA. США) и масс-спектрометра ESI-TOF от компании Bruker (micro-TOF MS, Bruker Daltonik, Bremen, Германия). СЕ капилляры получают от компании Beckman Coulter, которые характеризуются показателями внутреннего диаметра/наружного диаметра, равными 50/360 мкм, и длиной 90 см. Мобильная фаза для разделения в формате СЕ состоит из 20% ацетонитрила и 0,25% муравьиной кислоты в воде. Для достижения хорошего "оболочечного тока" при проведении MS используют 30% изопропанол с 5% муравьиной кислотой со скоростью течения 2 мкл/мин. Объединение СЕ и MS реализуется в наборе CE-ESI-MSSprayer (Agilent Technologies, Waldbronn, Германия). Для инъекции образца подводят давление от 1 до максимум 6 фунт/дюйм 2 (34013,52 Па) и длительность инъекции составляет 99 с. При соблюдении указанных параметров примерно 150 нл образца инъецируют в капилляр, что соответствует примерно 10% объема капилляра. Используют стекингтехнологию для концентрирования образца в капилляре. Для этого перед инъекцией образца 1 М растворNH3 вводят в течение 7 с (под давлением 1 фунт/дюйм 2 (5668,92 Па и после этого инъецируют образец и 2 М раствора муравьиной кислоты в течение 5 с. При подведении разделяющего напряжения (30 кВ) анализируемые компоненты автоматически концентрируются между указанными растворами. Последующее разделение в рамках СЕ проводят с использованием методики подачи варьирующего давления: 40 мин при давлении 0 фунт/дюйм 2 (0 Па), затем 0,1 фунт/дюйм 2 (566,892 Па) в течение 2 мин,0,2 фунт/дюйм 2 (1133,784 Па) в течение 2 мин, 0,3 фунт/дюйм 2 (1700,676 Па) в течение 2 мин, 0,4 фунт/дюйм 2 (2267,5 68 Па) в течение 2 мин и, наконец, 0,5 фунт/дюйм 2 (2834,46 Па) в течение 32 мин. Общая длительность процесса разделения составляет 80 мин. Для получения максимально возможной интенсивности сигнала на стороне MS газ небулайзера доводят до наименьших возможных значений объема. Напряжение, подводимое к распылительной игле для достижения электронапыления, составляет 3700-4100 В. Оставшиеся параметры масс-спектрометра оптимизируют для целей выявления пептидов, в соответствии с инструкциями производителей. Спектры записывают в диапазоне масс, соответствующих показателям m/z 400 - m/z 3000 и аккумулируют каждые 3 с. 3. Стандарты для проведения измерения СЕ. Для проверки и стандартизации СЕ измерений используют следующие белки или полипептиды, которые охарактеризованы по указанным показателям времени миграции СЕ:- 12014529 Белки/полипептиды используют в концентрации 10 фмоль/мкл, каждый, в воде. "REV", "ELM","KINCON" и "GIVLY" представляют собой синтетические пептиды. Значение молекулярных масс пептидов и показателей m/z для определенных заряженных состояний, наблюдаемых при MS, показаны ниже в таблице: В принципе, для каждого специалиста со средним уровнем знаний в данной области очевидно, что могут иметь место небольшие вариации по времени миграции при разделении методом капиллярного электрофореза. Однако в описанных условиях порядок миграции не меняется. Любой специалист со средним уровнем в данной области, который знает указанные массы и показатели времени СЕ, может без труда сопоставить результаты своих собственных измерений с показателями полипептидных маркеров согласно настоящему изобретению. Так, например, анализ может быть проведен следующим образом: вначале выбирают один из полипептидов, выявленных в данном измерении (пептид 1), и пытаются найти один или несколько вариантов идентичных масс с временным окном, соответствующим указанному времени СЕ (например, 5 мин). Если найдена только одна идентичная масса в данном интервале, сопоставление заканчивают. Если найдено несколько соответствующих масс, следует сделать более точный выбор по результатам поиска соответствий. Так, выбирают второй пептид (пептид 2) из результатов измерений и пытаются идентифицировать соответствующий полипептидный маркер, снова принимая в расчет соответствующий показатель временного окна. И вновь, если обнаруживается несколько маркеров соответствующей массы, самым вероятным соответствием будет такое, для которого отмечается по существу линейная зависимость между сдвигом пептида 1 и соответствующим параметром пептида 2. В зависимости от сложности проблемы сопоставления, можно рекомендовать специалисту в данной области, в необязательном порядке, использовать другие белки из имеющегося образца для сопоставления, например десять белков. В типичном случае показатель времени миграции либо расширяется, либо сокращается на определенные абсолютные величины, либо может иметь место компрессия или расширение всего диапазона. При этом, в таких условиях совместно мигрирующие белки будут продолжать совместно мигрировать. Кроме того, специалист в данной области может использовать характер миграции, описанный Цюрбигом с соавт. (Zuerbig et al., Electrophoresis 27 (2006), pp. 2111-2125). Если строить график по результатам измерений, где в виде простой диаграммы выражают зависимость показателя m/z от времени миграции (например, с использованием программы MS Excel), можно также выявить линейный характер прямой. И в этом случае возможно простое сопоставление индивидуальных полипептидов путем подсчета числа линий. Возможны также другие подходы для проведения сопоставления. В основном, специалист в данной области может использовать пептиды, указанные выше, в качестве внутренних стандартов для сопоставления с результатами, полученными при измерении в рамках СЕ методики. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ диагностики сосудистых заболеваний (СЗ), включающий стадию определения наличия или отсутствия по меньшей мере одного полипептидного маркера в образце, где указанный полипептидный маркер выбирают из маркеров 1-526, которые характеризуются следующими значениями молекулярной массы и времени миграции: 2. Способ по п.1, отличающийся тем, что оценку устанавливаемого наличия или отсутствия маркеров 1-106 проводят с помощью следующих эталонных значений: 3. Способ по п.1, отличающийся тем, что оценку амплитуды маркеров 107-413 проводят с помощью следующих эталонных значений: а для маркеров 414-526 ее проводят с помощью следующих эталонных значений: 4. Способ по п.1, где используют по меньшей мере два, или по меньшей мере три, или по меньшей мере пять или шесть, или по меньшей мере десять, или все полипептидные маркеры, определенные в п.1. 5. Способ по любому из пп.1-4, где указанный образец, взятый у субъекта, представляет собой образец мочи или образец крови (образец сыворотки или плазмы крови). 6. Способ по любому из пп.1-5, где используют капиллярный электрофорез, ВЭЖХ, ионную спектрометрию и/или масс-спектрометрию в газовой фазе для выявления наличия или отсутствия указанного полипептидного маркера или маркеров. 7. Способ по любому из пп.1-6, где капиллярный электрофорез проводят перед измерением молекулярной массы указанных полипептидных маркеров. 8. Способ по любому из пп.1-7, где масс-спектрометрию используют для выявления наличия или отсутствия указанного полипептидного маркера или маркеров.- 22014529 9. Применение по меньшей мере одного полипептидного маркера, выбранного из маркеров 1-526,который характеризуется значениями молекулярной массы и времени миграции по п.1, для диагностики сосудистых заболеваний. 10. Применение по п.9, отличающееся тем, что время СЕ определяют с помощью стеклянного капилляра длиной 90 см, имеющего внутренний диаметр (в/д) 50 мкм, при напряжении 25 кВ, где в качестве растворителя мобильной фазы используют 20% ацетонитрил, 0,25 М муравьиную кислоту в воде. 11. Способ диагностики сосудистых заболеваний (СЗ), включающий стадии:a) разделения образца по меньшей мере на три, предпочтительно 10, подобразцов;b) анализа по меньшей мере двух подобразцов для определения наличия или отсутствия амплитуды по меньшей мере одного полипептидного маркера в образце, где указанный полипептидный маркер выбирают из маркеров 1-526, которые характеризуются значениями молекулярной массы и времени миграции (времени СЕ) по п.1. 12. Способ по п.11, где проводят измерение по меньшей мере 10 подобразцов. 13. Способ по меньшей мере по одному из пп.1-8 и 11, 12, отличающийся тем, что время СЕ определяют с помощью стеклянного капилляра длиной 90 см, имеющего внутренний диаметр (в/д) 50 мкм,при напряжении 25 кВ, где в качестве растворителя мобильной фазы используют 20% ацетонитрил,0,25 М муравьиную кислоту в воде. 14. Комбинация маркеров, включающая по меньшей мере 10 маркеров, выбранных из маркеров 1526, которые характеризуются значениями молекулярной массы и времени миграции (времени СЕ) по п.1.
МПК / Метки
МПК: G01N 33/68
Метки: маркеры, оценки, полипептидные, диагностики, заболеваний, сосудистых
Код ссылки
<a href="https://eas.patents.su/24-14529-polipeptidnye-markery-dlya-diagnostiki-i-ocenki-sosudistyh-zabolevanijj.html" rel="bookmark" title="База патентов Евразийского Союза">Полипептидные маркеры для диагностики и оценки сосудистых заболеваний</a>
Предыдущий патент: Составы, содержащие пептиды, стимулирующие рецептор эритропоэтина и их применение
Следующий патент: Способ получения фармацевтического промежуточного соединения
Случайный патент: Прозрачная панель для присоединения электронных компонентов