Синергетическая травяная композиция, применяемая при глаукоме, и способ ее получения
Номер патента: 16723
Опубликовано: 30.07.2012
Авторы: Кумар Нареш, Нагпал Анкита, Саксена Рохит, Агарвал Рену, Бахри Дипак, Сривастава Сушма, Агравал Шиам Сундер, Гупта Суреш Кумар, Чохан Сатиш Кумар
Формула / Реферат
1. Синергетическая травяная композиция, применяемая при глаукоме, содержащая синергетически эффективное количество экстракта растений, выбранных из видов Ocimum, в количестве от 0,1 до 1,0 мас.%, видов Curcuma - в количестве от 0,01 до 0,5 мас.%, Solanum nigrum, в количестве от 0,1 до 0,75 мас.%, и фармацевтически приемлемые наполнители или носители.
2. Синергетическая травяная композиция, применяемая при глаукоме, содержащая синергетически эффективное количество экстракта растений, выбранных из видов Ocimum, в количестве от 0,1 до 1,0 мас.%, видов Curcuma - в количестве от 0,01 до 0,5 мас.%, Areca catechu - в количестве от 0,1 до 1,0 мас.%, и фармацевтически приемлемые наполнители или носители.
3. Синергетическая травяная композиция по любому из п.1 или 2, в которой виды Ocimum выбирают из группы, состоящей из Ocimum basilicum, Ocimum canum, Ocimum kilimandscaricum, Ocimum sanctum, Ocimum viride, и виды Curcuma выбирают из группы, состоящей из Curcuma longa, Curcumavaleton, Curcuma amad, Curcuma aromatica Salisb.
4. Синергетическая травяная композиция по п.1, где композиция предпочтительно содержит виды Ocimum в количестве 0,50 мас.%, виды Curcuma - в количестве 0,01 мас.% и Solanum nigrum - в количестве 0,25 мас.%.
5. Синергетическая травяная композиция по п.2, где композиция предпочтительно содержит виды Ocimum в количестве 0,50 мас.%, виды Curcuma - в количестве 0,01 мас.% и Areca catechu - в количестве 0,25 мас.%.
6. Синергетическая травяная композиция по любому из п.1 или 4, где композиция предпочтительно содержит вид Ocimum basilicum в количестве 0,50 мас.%, вид Curcuma longa - в количестве 0,01 мас.% и Solanum nigrum - в количестве 0,25 мас.%.
7. Синергетическая травяная композиция по любому из п.2 или 5, где композиция предпочтительно содержит вид Ocimum basilicum в количестве 0,50 мас.%, вид Curcuma longa - в количестве 0,01 мас.% и Areca catechu - в количестве 0,25 мас.%.
8. Синергетическая травяная композиция по любому из п.1 или 2, в которой фармацевтически приемлемые наполнители выбирают из группы, включающей повышающие растворимость агенты, такие как полисорбат, циклодекстрин и их производные, Кремофор RH 40 и другие производные, повышающие вязкость агенты, такие как гидроксипропилметилцеллюлоза, и другие пригодные производные целлюлозы, поливиниловый спирт, повидон, карбопол карагенин, антиоксиданты, такие как лимонная кислота, EDTA и его соли, метабисульфит натрия и другие одобренные водорастворимые антиоксиданты, буферные агенты, такие как цитрат, борат, фосфат, цитрофосфат, и регулирующие осмолярность агенты, такие как хлорид натрия, маннит, глицерин, консерванты, такие как бензалкония хлорид, сорбяновая кислота, метилпарабен, пропилпарабен и их соли.
9. Синергетическая травяная композиция по любому из п.1 или 2, изготовленная в форме глазных капель, мази, крема или геля.
10. Способ получения синергетической травяной композиции по любому из п.1 или 2, включающий следующие стадии:
(a) крупный помол отдельного растения и экстрагирование его растворителями, имеющими разную полярность, выбранными из группы, включающей воду, спирт, ацетон, этилацетат, петролейный эфир, хлороформ или их смеси в различных соотношениях;
(b) необязательно концентрирование экстракта, полученного на стадии (a), под действием вакуума и преобразование его либо в форму густой пасты, включающей около 20-30% твердого вещества, либо в форму сухого порошка;
(c) составление фармацевтически приемлемой травяной композиции посредством комбинирования экстрактов, полученных в стадии (a) или стадии (b), в разных соотношениях, как здесь указано, с получением синергетической травяной композиции в форме глазных капель, мази, крема или геля.
11. Способ получения синергетической травяной композиции по любому из п.1 или 2, включающий следующие стадии:
(a) крупный помол отдельного растения и экстрагирование его с использованием дистилляционного способа;
(b) концентрирование экстракта, полученного на стадии (a), под действием вакуума и преобразование его либо в форму густой пасты, включающей около 20-30% твердого вещества, либо в форму сухого порошка;
(c) составление фармацевтически приемлемой травяной композиции посредством комбинирования экстрактов, полученных в стадии (a) или стадии (b), в разных соотношениях, как заявлено в п.1 или 2, с получением синергетической травяной композиции в форме глазных капель, мази, крема или геля.
Текст
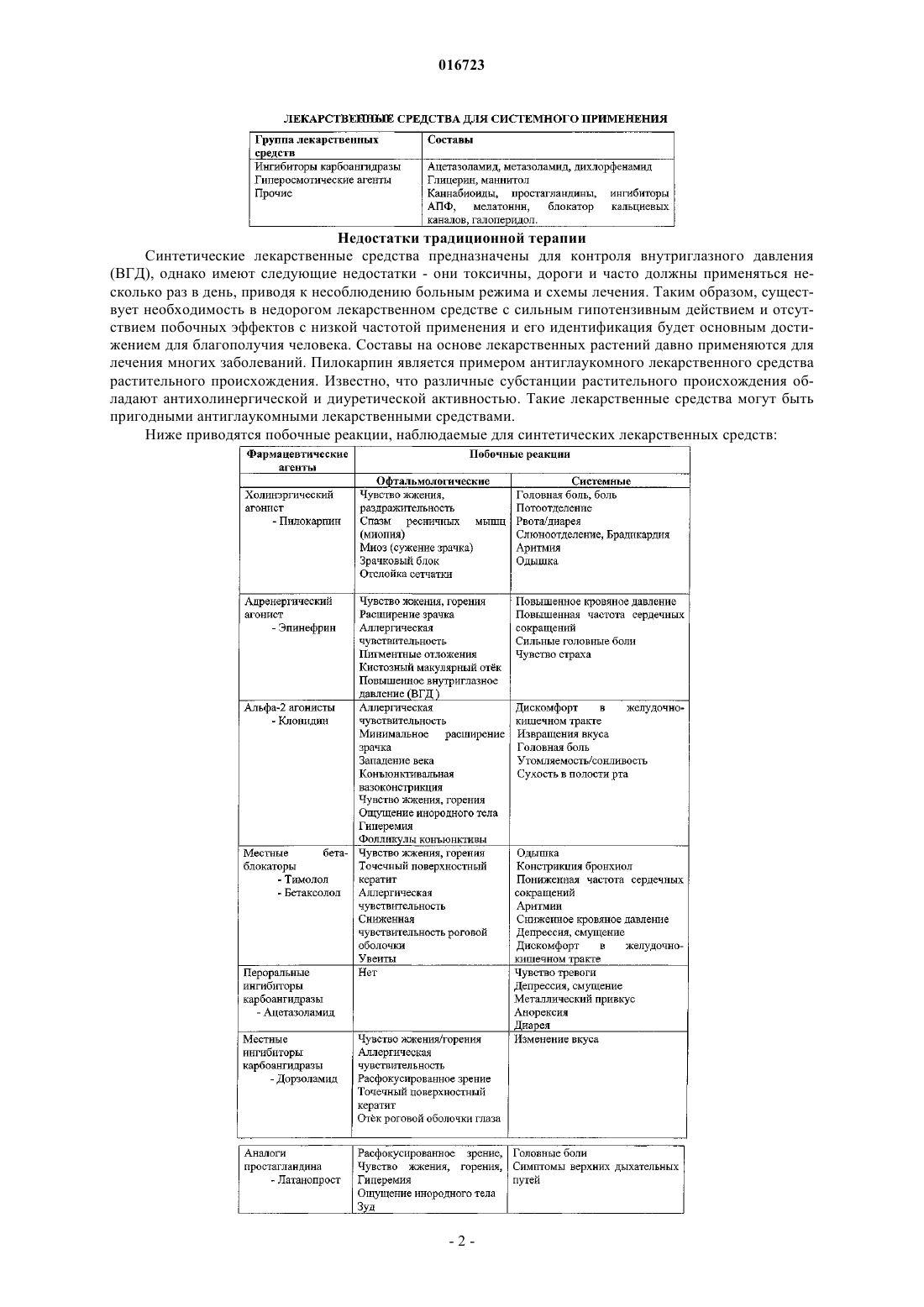
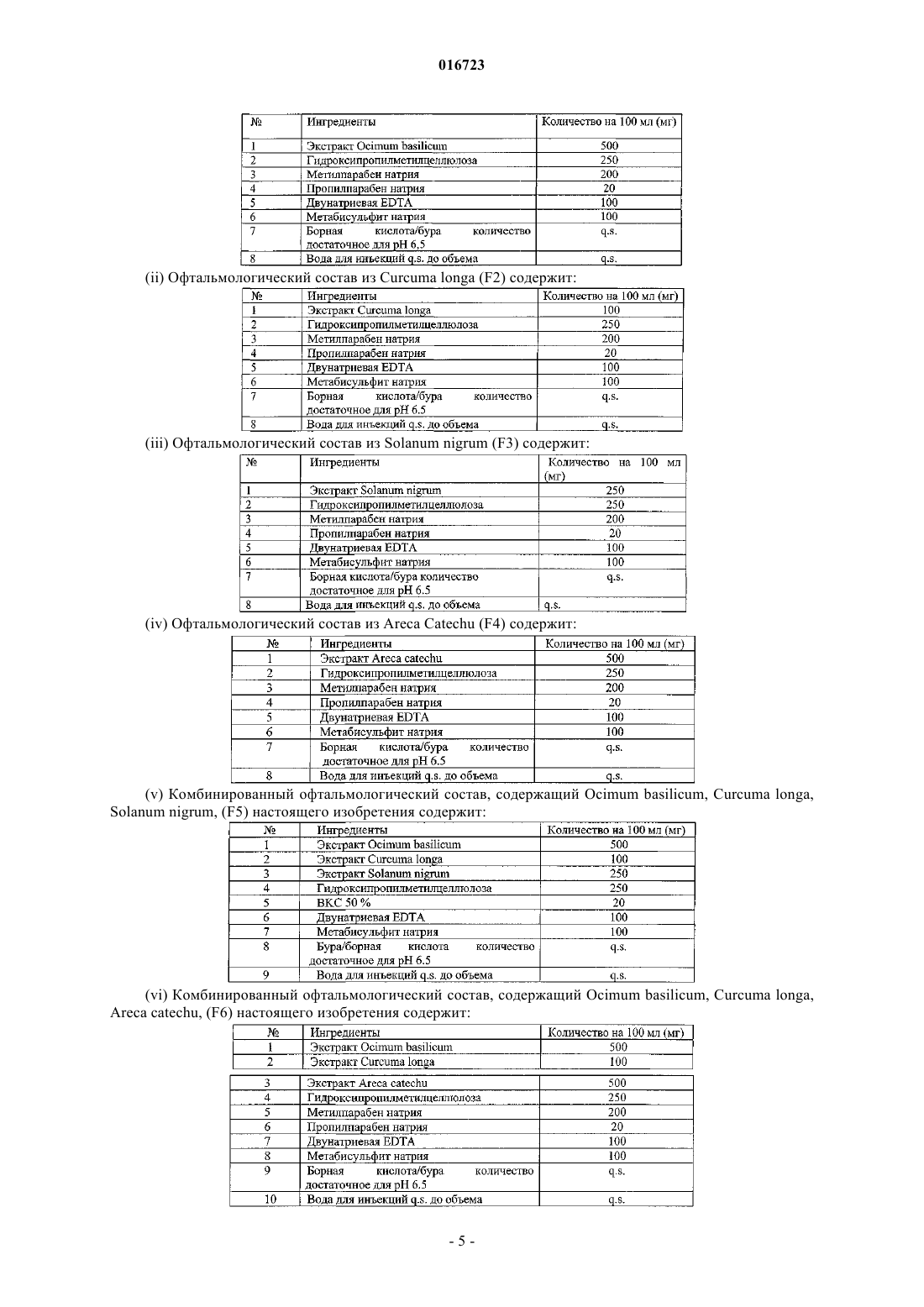
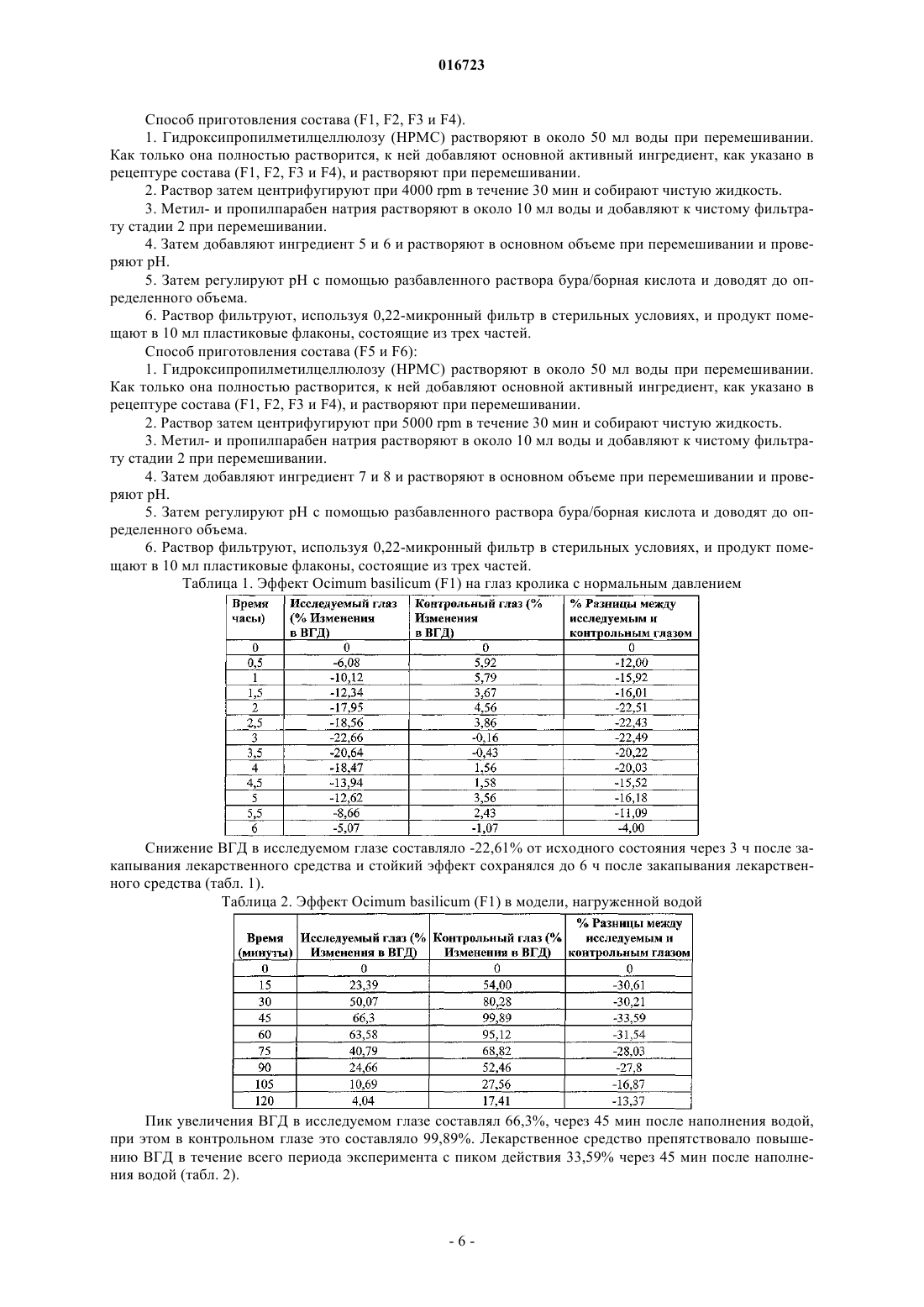
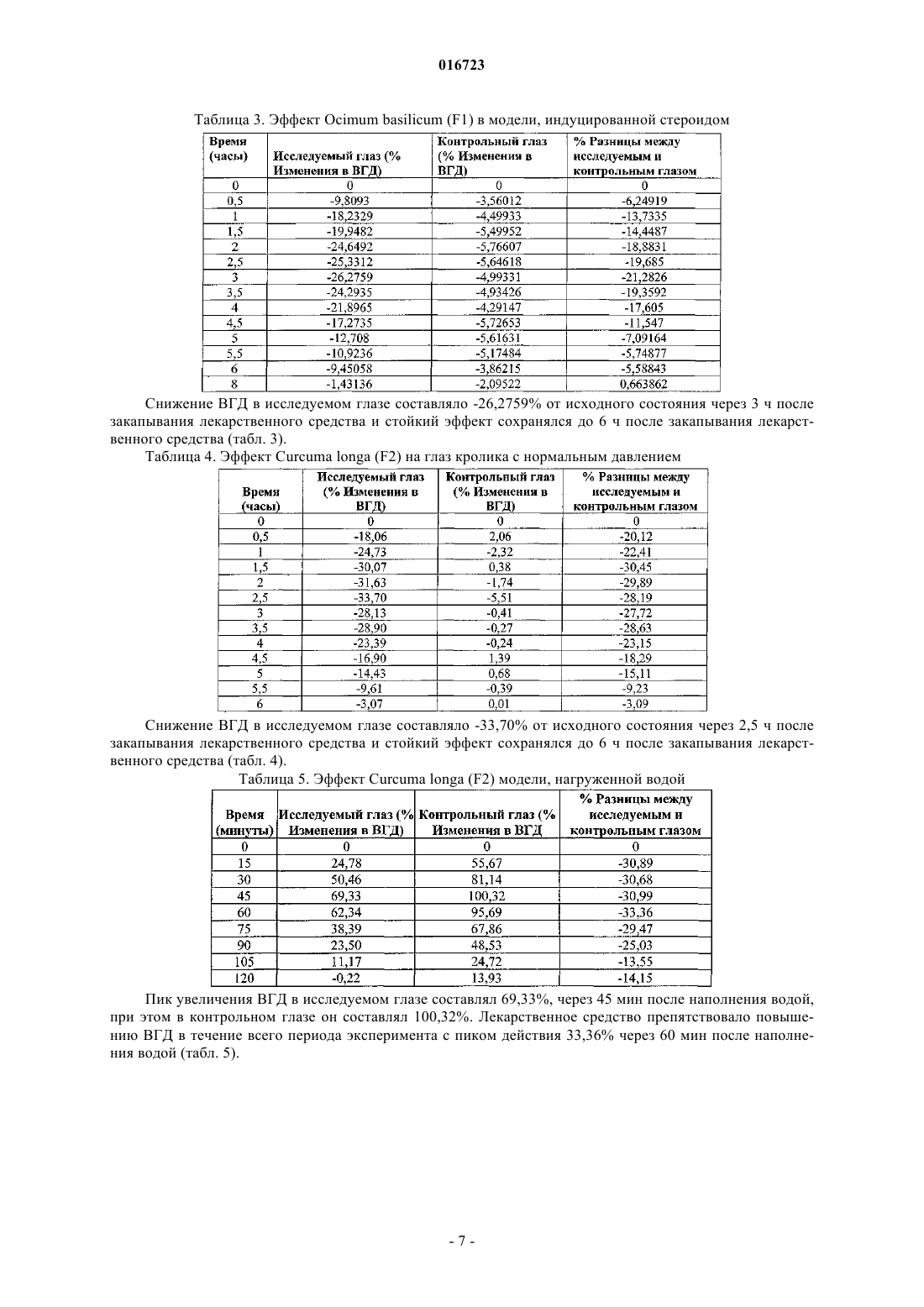
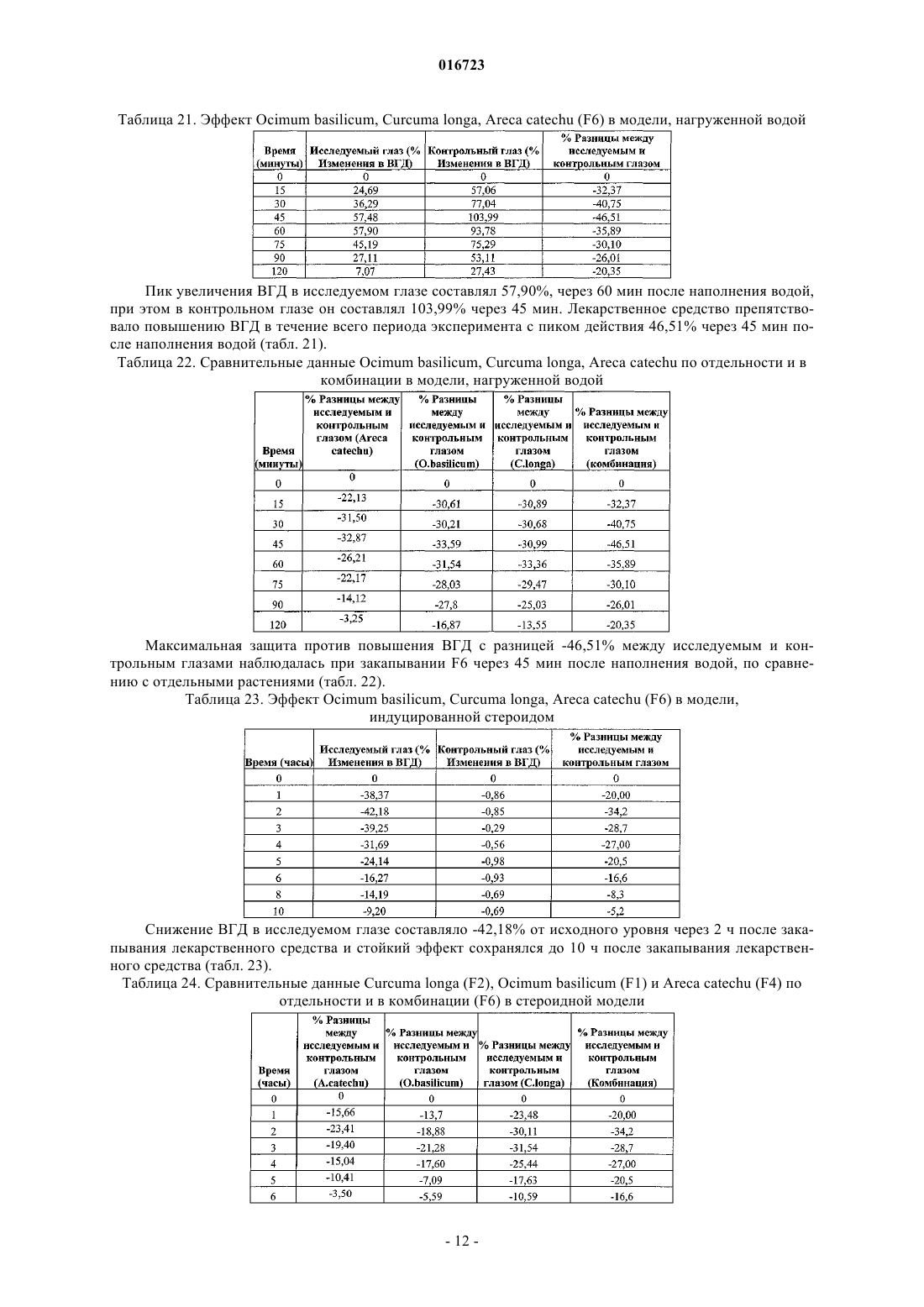
Изобретение относится к синергетической травяной композиции для снижения внутриглазного давления при различных типах глаукомы и способ получения такой композиции в фармацевтически приемлемых лекарственных формах.(71)(73) Заявитель и патентовладелец: ДЕЛИ ИНСТИТЬЮТ ОФ ФАРМАСЬЮТИКАЛ САЙНСИЗ ЭНД РИСЕРЧ (ДИПСАР); ПРОУМЕД ЭКСПОРТС ПРАЙВИТ ЛИМИТЕД 016723 Область техники, к которой относится изобретение Изобретение относится к синергетической травяной композиции для снижения внутриглазного давления при различных типах глаукомы и к способу приготовления такой композиции в виде фармацевтически приемлемых лекарственных форм. Предшествующий уровень техники Глаукома представляет собой заболевание, характеризующееся высоким внутриглазным давлением(ВГД), которое является причиной как преходящего, так и стойкого нарушения зрения. Повышение ВГД может быть следствием: увеличения скорости образования внутриглазной жидкости; снижения скорости оттока жидкости; повышенного давления в дренирующих эписклеральных венах. Затруднение циркуляции жидкости в области зрачка или оттока жидкости через угол передней камеры глаза обуславливает глаукому. Нормальное ВГД индивидуума доходит до 20 мм рт.ст. и может возрастать до 60-70 мм рт.ст. у пациентов с глаукомой. Повышение ВГД до такой величины может привести к потере зрения из-за повреждения нервных волокон сетчатки глаза. Вследствие повышения ВГД в диске зрительного нерва сдавливаются аксоны зрительного нерва глазного яблока. Это сдавливание, вероятно, блокирует аксональный поток цитоплазмы из тел нервных клеток в сетчатке к растянутым волокнам зрительного нерва, входящих в мозг. Это приводит к нарушению питания нервных волокон и, в итоге, обуславливает гибель нейронов. Сдавливание артерии сетчатки может усилить повреждение нервных клеток вследствие снижения питания нервных волокон. Глаукома обычно классифицируется следующим образом: первичная; экспериментальная модель; вторичная. Самой распространенной формой глаукомы является первичная глаукома, которая может быть открытоутольной глаукомой - угол передней камеры глаза всегда открыт, на всех стадиях заболевания, и жидкость постоянно имеет доступ к каналам оттока. Наблюдается повышенное сопротивление оттоку в корнеосклеральной сетчатой структуре. ВГД может быть повышаться или быть высоким. Закрытоугольной глаукомой - не наблюдается абнормального сопротивления оттоку в корнеосклеральной сетчатой структуре. Единственной причиной повышенного давления является закрытие угла. Радужная оболочка препятствует доступу внутриглазной жидкости к каналам оттока. Проявление заболевания Глаукома является третьей основной причиной обратимой потери зрения. Совокупная оценка слепоты составляет более 44 миллионов с глаукомой, составляющих более чем 15% незрячих пациентов во всем мире (2). Во всем мире приблизительно две трети всех незрячих или слабовидящих людей составляют женщины (3). Индия имеет высокий показатель по слепоте (23,5%) в мире и 13% от общего числа незрячих вследствие глаукомы находятся в Индии. Многочисленные обследования населения, выполненные на Западе и в Азии, показали, что глаукома остается нераспознанной в около 50% случаях и,вследствие этого, связанные с глаукомой слепота и нетрудоспособность часто недооценены (4-5). Раннее и эффективное лечение глаукомы является необходимым для снижения числа новых случаев двусторонней слепоты, происходящей вследствие прогрессирования глаукомы. Биологическая революция в медицине обеспечила новые способы терапевтического воздействия. Новые и инновационные стратегии лечения рассматриваются для контроля повышенного внутриглазного давления (ВГД) посредством использования лекарственных средств синтетического и растительного происхождения при глаукоме. Традиционная терапия глаукомы Основная цель лечения глаукомы состоит в снижении ВГД ниже 20 мм рт.ст. у пациентов с легкими изменениями оптического диска и ниже 15 мм рт.ст. у пациентов с более тяжелыми изменениями. Хирургическое вмешательство, направленное на усиление оттока внутриглазной жидкости, предпринимают, когда ВГД остается неконтролируемым даже при проведении лечения многочисленными лекарственными средствами. Следующие группы/лекарственные средства широко распространены при лечении глаукомы: Недостатки традиционной терапии Синтетические лекарственные средства предназначены для контроля внутриглазного давления(ВГД), однако имеют следующие недостатки - они токсичны, дороги и часто должны применяться несколько раз в день, приводя к несоблюдению больным режима и схемы лечения. Таким образом, существует необходимость в недорогом лекарственном средстве с сильным гипотензивным действием и отсутствием побочных эффектов с низкой частотой применения и его идентификация будет основным достижением для благополучия человека. Составы на основе лекарственных растений давно применяются для лечения многих заболеваний. Пилокарпин является примером антиглаукомного лекарственного средства растительного происхождения. Известно, что различные субстанции растительного происхождения обладают антихолинергической и диуретической активностью. Такие лекарственные средства могут быть пригодными антиглаукомными лекарственными средствами. Ниже приводятся побочные реакции, наблюдаемые для синтетических лекарственных средств:-2 016723 Цели изобретения Целью настоящего изобретения является разработка травяной синергетической композиции для снижения ВГД и обладающей антиглаукомной активностью. Другая цель настоящего изобретения заключается в составлении синергетической травяной композиции в виде фармацевтически приемлемой для офтальмологического применения лекарственной формы с оптимальным антиглаукомным действием. Еще другая цель настоящего изобретения состоит в преодолении недостатков, ассоциированных с традиционными аллопатическими лекарственными средствами для лечения глаукомы. Подробное описание изобретения Настоящее изобретение обеспечивает синергетическую травяную композицию для снижения ВГД при глаукоме, содержащую синергетически эффективное количество экстракта растений, выбранных из видов Ocimum, видов Curcuma, Solarium nigrum и Areca catechu, необязательно вместе с фармацевтически приемлемым наполнителем или носителем. В синергетической травяной композиции настоящего изобретения виды Ocimum выбирают из группы, состоящей из Ocimum basilicum, Ocimum canum, Ocimum kilimandscaricum, Ocimum sanctum,Ocimum viride, и виды Curcuma выбирают из группы, состоящей из Curcuma longa, Curcuma avaleton,Curcuma amada, Curcuma aromatica Salisb. Синергетическая травяная композиция настоящего изобретения содержит: Синергетическая травяная композиция настоящего изобретения предпочтительно содержит: В предпочтительном воплощении синергетическая травяная композиция настоящего изобретения предпочтительно содержит Ocimum basilicum, Curcuma longa и Solarium nigrum. В еще другом предпочтительном воплощении синергетическая травяная композиция настоящего изобретения предпочтительно содержит Ocimum basilicum, Curcuma longa и Areca catechu. Использование терминов "синергетическая" и "синергетически эффективная", в используемом в настоящем изобретении значении, подразумевает, что биологический эффект, создаваемый от применения двух или более агентов, больше, чем сумма биологических эффектов, получаемых при применении отдельных агентов. Синергетическая травяная композиция настоящего изобретения необязательно содержит фармацевтически приемлемые наполнители, которые выбирают из группы, включающей повышающие растворимость агенты, такие как полисорбат, циклодекстрин и его производные, Кремофор RH 40 и его производные, повышающие вязкость агенты, такие как гидроксипропилметилцеллюлоза и другие пригодные производные целлюлозы, поливиниловый спирт, повидон, карбопол карагенин, и др., антиоксиданты,такие как лимонная кислота, EDTA и его соли, пиросульфит натрия и другие пригодные водорастворимые антиоксиданты, буферные агенты, такие как цитрат, борат, фосфат, цитрофосфат, и регулирующие осмомолярность агенты, такие как хлорид натрия, маннитол, глицерин, консерванты, такие как бензалконий хлорид, сорбиновая кислота, метилпарабен, пропилпарабен, и их соли, и др. Синергетическая травяная композиция настоящего изобретения предпочтительно составлена в форме глазных капель, мази, крема, геля. Настоящее изобретение также включает способ получения указанного травяного состава. Способ получения указанного травяного офтальмологического состава включает следующие стадии.i. Крупный помол отдельного растения, которое здесь описывается, и экстрагирование его с растворителями, имеющими разную полярность, выбранными из группы, включающей воду, спирт, ацетон,этилацетат, петролейный эфир, хлороформ или их смеси в различных соотношениях.ii. Необязательно концентрирование экстракта, полученного на стадии (a), под действием вакуума и преобразование его либо в форму густой пасты, включающей около 20-30 % твердого вещества, либо в форму сухого порошка.iii. Составление фармацевтически приемлемой травяной композиции посредством комбинирования экстрактов, полученных в стадии (a) или стадии (b), в разных соотношениях, как здесь указано, с получением синергетической травяной композиции в форме глазных капель, мази, крема или геля.iv. Альтернативно, экстракция может выполняться с использованием дистилляционного способа, и дистиллят может непосредственно использоваться для составления синергетической травяной компози-3 016723 ции, как здесь описано. Сведения, подтверждающие возможность осуществления изобретения Изобретение иллюстрируется следующими примерами, которые не ограничивают объем изобретения. Хотя изобретение описывается по отношению к специфическим воплощениям, данное описание не подразумевает ограничения изобретения. Различные модификации описываемых воплощений, а также альтернативные воплощения изобретения, будут очевидны для специалиста в данной области техники относительно описания изобретения. Из чего предполагается, что такие модификации могут быть выполнены, не нарушая объем и сущность настоящего изобретения, как определено. В этих примерах "часть" и "части" означают "часть по массе" и "части по массе", соответственно, если иное не определено. Способ получения травяной композиции включает следующие стадии:(i) Экстракция растения. Растение очищают, крупно измельчают и экстрагируют с водой, используя 8 раз количества воды при нагревании до кипения в течение 10 мин. Экстракт фильтруют и концентрируют до густой пасты, имеющей около 30% твердого содержимого. Затем ее высушивают в вакуумной сушилке при температуре 60C или она может быть высушена посредством распыления или лиофилизации. Собирают высушенный порошок, упаковывают после просеивания в двойной полиэтиленовый пакет. Альтернативно, растения могут подвергать перегонке, и дистиллят может использоваться для дальнейшего получения состава.(ii) Экстракты взвешивают и растворяют в воде, содержащей 0,25% НРМС в качестве повышающего вязкость агента, при перемешивании. Дополнительно добавляют Кремофор RH 40 или его пригодные производные для повышения растворимости.(iii) Препарат центрифугируют при около 4000 rpm в течение 30-60 мин с удалением нежелательных примесей. Альтернативно его можно фильтровать, используя фильтровальную бумагу.(iv) С очищенным фильтратом растворяют пригодный консервант (в данном случае ВКС, метил- и пропилпарабен натрия и сорбиновая кислота, фенилэтиловый спирт и ртуть, содержащие пригодные консерванты).(v) При перемешивании растворяют двунатриевый EDTA и метабисульфит натрия в качестве антиоксидантов.(vi) В конце регулируют pH борной кислотой/бурой, лимонной кислотой, цитратом натрия, фосфатом калия и натрия до 5-7 и объем доводят водой для инъекций.(vii) Затем раствор фильтруют с помощью фильтра Millipore с размером пор 0,22 мкм и помещают в пластиковые флаконы для глазных капель при ламинарном потоке и маркируют.(viii) Итоговый продукт является чистым, прозрачным, имеющим от желтого до желтоватокрасного цвет, имеющим осмолярность 250-350 мосмол/кг и pH 5-7. Антиглаукомную активность травяных офтальмологических растворов определяли на кроликах,используя следующие модели глаукомы: 1. Модель с нормальным давлением. Двенадцати белым кроликам обоих полов массой 1,5-2 кг определяли исходный уровень ВГД с использованием бесконтактного тонометра. Затем закапывали лекарственное средство (50 мкл) в один глаз, принимаемый за контрольный глаз, и в другой глаз закапывали физиологический раствор (50 мкл). Затем измеряли ВГД в 30-минутные интервалы на протяжении 6 часового периода. 2. Модель, нагруженная водой. Двенадцать белых кроликов обоих полов не кормили всю ночь. На следующее утро определяли исходный уровень ВГД и лекарственное средство (50 мкл) закапывали в исследуемый глаз и физиологический раствор (50 мкл) в контрольный глаз. Через 30 мин кроликов анестезировали путем инъцирования тиопентона натрия (16 мг/кг массы тела) в краевую глазную вену. Затем в желудок вставляли трубку для кормления с последующим введением водопроводной воды (100 мл/кг) через трубку. С этого момента ВГД определяли каждые 15 мин в течение 120 мин. Концентрация лекарственного средства, показывающая наилучший эффект в модели с нормальным давлением, дополнительно исследовалась в модели, нагруженной водой. Эта модель имитировала острые глаукомные атаки. 3. Модель глаукомы, индуцированная стероидом. 12 молодых кроликов дрессировали для восприятия проведения тонометрии и затем определяли ВГД ежедневно в течение 15 дней для получения исходного уровня ВГД. Эти кроликам затем закапывали глазные капли, содержащие 1% преднизолон(10 мкл), в исследуемый глаз и физиологический раствор (20 мкл) в контрольный глаз, дважды в день в течение 40 дней. ВГД измеряли дважды в день в течение всего периода закапывания стероида. В конце 40 дней у кроликов определяли антиглаукомную активность. Концентрация лекарственного средства,показывающая наилучший эффект в модели с нормальным давлением, дополнительно исследовалась в модели глаукомы, индуцированной стероидом. Измерения ВГД проводили каждые 30 мин в течение 6 ч. Эта модель имитировала хроническую открытоугольную глаукому. Различные офтальмологические составы были приготовлены при использовании следующих смесей:(i) Офтальмологический состав из Ocimum basilicum (F1) содержит:(ii) Офтальмологический состав из Curcuma longa (F2) содержит:(iii) Офтальмологический состав из Solanum nigrum (F3) содержит:(iv) Офтальмологический состав из Areca Catechu (F4) содержит:-5 016723 Способ приготовления состава (F1, F2, F3 и F4). 1. Гидроксипропилметилцеллюлозу (HPMC) растворяют в около 50 мл воды при перемешивании. Как только она полностью растворится, к ней добавляют основной активный ингредиент, как указано в рецептуре состава (F1, F2, F3 и F4), и растворяют при перемешивании. 2. Раствор затем центрифугируют при 4000 rpm в течение 30 мин и собирают чистую жидкость. 3. Метил- и пропилпарабен натрия растворяют в около 10 мл воды и добавляют к чистому фильтрату стадии 2 при перемешивании. 4. Затем добавляют ингредиент 5 и 6 и растворяют в основном объеме при перемешивании и проверяют pH. 5. Затем регулируют pH с помощью разбавленного раствора бура/борная кислота и доводят до определенного объема. 6. Раствор фильтруют, используя 0,22-микронный фильтр в стерильных условиях, и продукт помещают в 10 мл пластиковые флаконы, состоящие из трех частей. Способ приготовления состава (F5 и F6): 1. Гидроксипропилметилцеллюлозу (HPMC) растворяют в около 50 мл воды при перемешивании. Как только она полностью растворится, к ней добавляют основной активный ингредиент, как указано в рецептуре состава (F1, F2, F3 и F4), и растворяют при перемешивании. 2. Раствор затем центрифугируют при 5000 rpm в течение 30 мин и собирают чистую жидкость. 3. Метил- и пропилпарабен натрия растворяют в около 10 мл воды и добавляют к чистому фильтрату стадии 2 при перемешивании. 4. Затем добавляют ингредиент 7 и 8 и растворяют в основном объеме при перемешивании и проверяют рН. 5. Затем регулируют pH с помощью разбавленного раствора бура/борная кислота и доводят до определенного объема. 6. Раствор фильтруют, используя 0,22-микронный фильтр в стерильных условиях, и продукт помещают в 10 мл пластиковые флаконы, состоящие из трех частей. Таблица 1. Эффект Ocimum basilicum (F1) на глаз кролика с нормальным давлением Снижение ВГД в исследуемом глазе составляло -22,61% от исходного состояния через 3 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 6 ч после закапывания лекарственного средства (табл. 1). Таблица 2. Эффект Ocimum basilicum (F1) в модели, нагруженной водой Пик увеличения ВГД в исследуемом глазе составлял 66,3%, через 45 мин после наполнения водой,при этом в контрольном глазе это составляло 99,89%. Лекарственное средство препятствовало повышению ВГД в течение всего периода эксперимента с пиком действия 33,59% через 45 мин после наполнения водой (табл. 2). Снижение ВГД в исследуемом глазе составляло -26,2759% от исходного состояния через 3 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 6 ч после закапывания лекарственного средства (табл. 3). Таблица 4. Эффект Curcuma longa (F2) на глаз кролика с нормальным давлением Снижение ВГД в исследуемом глазе составляло -33,70% от исходного состояния через 2,5 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 6 ч после закапывания лекарственного средства (табл. 4). Таблица 5. Эффект Curcuma longa (F2) модели, нагруженной водой Пик увеличения ВГД в исследуемом глазе составлял 69,33%, через 45 мин после наполнения водой,при этом в контрольном глазе он составлял 100,32%. Лекарственное средство препятствовало повышению ВГД в течение всего периода эксперимента с пиком действия 33,36% через 60 мин после наполнения водой (табл. 5). Снижение ВГД в исследуемом глазе составляло -34,34% от исходного состояния через 3 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 6 ч после закапывания лекарственного средства (табл. 6). Таблица 7. Эффект Solanum nigrum (F3) на глаз кролика с нормальным давлением Снижение ВГД в исследуемом глазе составляло -25,03% от исходного состояния через 3 ч после закапывания лекарственного средства, стойкий эффект сохранялся до 6 ч после закапывания лекарственного средства (табл. 7). Таблица 8. Эффект Solanum nigrum (F3) в модели, нагруженной водой Пик увеличения ВГД в исследуемом глазе составлял 69,39%, через 60 мин после наполнения водой,при этом в контрольном глазе он составлял 104,10% через 45 мин. Лекарственное средство препятствовало повышению ВГД в течение всего периода эксперимента с пиком действия -37,40% через 45 мин после наполнения водой (табл. 8). Снижение ВГД в исследуемом глазе составляло -33,58% от исходного уровня через 2 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 6 ч после закапывания лекарственного средства (табл. 9). Таблица 10. Эффект areca catechu (F4) в модели с нормальным давлением Снижение ВГД в исследуемом глазе составляло -20,60% от исходного уровня через 2 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 6 ч после закапывания лекарственного средства (табл. 10). Таблица 11. Эффект Areca catechu (F4) в модели, нагруженной водой Пик увеличения ВГД в исследуемом глазе составлял 69,10%, через 45 мин после наполнения водой,при этом в контрольном глазе он составлял 101,96% через 45 мин. Лекарственное средство препятствовало повышению ВГД в течение всего периода эксперимента с пиком действия -32,87% через 45 мин после наполнения водой (табл. 11). Таблица 12. Эффект areca catechu (F4) в стероидной модели Снижение ВГД в исследуемом глазе составляло -25,77% от исходного уровня через 2 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 6 ч после закапывания лекарственного средства (табл. 12). Снижение ВГД в исследуемом глазе составляло -32,03% от исходного уровня через 2 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 8 часов после закапывания лекарственного средства (табл. 13). Таблица 14. Сравнительные данные curcuma longa, Ocimum basilicum и Solanum nigrum (F1, F2, F3) по отдельности и в комбинации (F5) в модели с нормальным давлением Максимальный пик снижения ВГД -31,18% наблюдался при закапывании комбинации из Ocimum Пик увеличения ВГД в исследуемом глазе составлял 62,23%, через 45 мин после наполнения водой,при этом в контрольном глазе он составлял 102,40%. Лекарственное средство препятствовало повышению ВГД в течение всего периода эксперимента с пиком действия 45,26% через 30 мин после наполнения водой (табл. 15). Таблица 16. Сравнительные данные Ocimum basilicum, Curcuma longa, Solanum nigrum по отдельности и в комбинации в модели, нагруженной водой Максимальная защита против повышения ВГД с разницей -45,26% между исследуемым и контрольным глазами наблюдалась при закапывании F5 через 30 мин после наполнения водой, по сравнению с отдельными растениями (табл. 16). Снижение ВГД в исследуемом глазе составляло -42,18% от исходного уровня через 2 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 10 ч после закапывания лекарственного средства (табл. 17). Таблица 18. Сравнительные данные curcuma longa, Ocimum basilicum и Solanum nigrum по отдельности и в комбинации в стероидной модели Максимальный пик снижения ВГД -41,33% наблюдался при закапывания комбинации из Ocimum Снижение ВГД в исследуемом глазе составляло -32,58% от исходного уровня через 2 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 8 ч после закапывания лекарственного средства (табл. 19). Таблица 20. Сравнительные данные curcuma longa, Ocimum basilicum и Areca catechu по отдельности и в комбинации в модели с нормальным давлением Максимальный пик снижения ВГД -30,46% наблюдался при закапывания комбинации из Ocimum Пик увеличения ВГД в исследуемом глазе составлял 57,90%, через 60 мин после наполнения водой,при этом в контрольном глазе он составлял 103,99% через 45 мин. Лекарственное средство препятствовало повышению ВГД в течение всего периода эксперимента с пиком действия 46,51% через 45 мин после наполнения водой (табл. 21). Таблица 22. Сравнительные данные Ocimum basilicum, Curcuma longa, Areca catechu по отдельности и в комбинации в модели, нагруженной водой Максимальная защита против повышения ВГД с разницей -46,51% между исследуемым и контрольным глазами наблюдалась при закапывании F6 через 45 мин после наполнения водой, по сравнению с отдельными растениями (табл. 22). Таблица 23. Эффект Ocimum basilicum, Curcuma longa, Areca catechu (F6) в модели,индуцированной стероидом Снижение ВГД в исследуемом глазе составляло -42,18% от исходного уровня через 2 ч после закапывания лекарственного средства и стойкий эффект сохранялся до 10 ч после закапывания лекарственного средства (табл. 23). Таблица 24. Сравнительные данные Curcuma longa (F2), Ocimum basilicum (F1) и Areca catechu (F4) по отдельности и в комбинации (F6) в стероидной модели- 12016723 Максимальный пик снижения ВГД - 34,20% наблюдался при закапывания комбинации из Ocimumbasilicum, Curcuma longa и Areca catechu (F6) по сравнению с отдельными растениями (табл. 24). Результаты. На основании вышеприведенных результатов, неожиданно травяная композиция настоящего изобретения, содержащая синергетически эффективное количество Solarium nigrum, Curcumalonga, Ocimum basilicum (состав-F5) и Curcuma longa, Ocimum basilicum, Areca catechu (состав-F6), показала усиленное и неожиданное действия по сравнению с отдельными составами (F1, F2,F3 и F4). Следовательно, указанная травяная композиция (F5 и F6) действует синергетически. Пример 1. Для составления офтальмологических капель: Способ получения: 1. Гидроксипропилметилцеллюлозу (HPMC) растворяют в около 50 мл воды при перемешивании. Кремофор RH 40 добавляют к этому раствору и растворяют при перемешивании. Как только раствор полностью растворился, затем добавляют основной активный ингредиент, как указано выше в рецептуре( 1-3), и растворяют при перемешивании. 2. Раствор затем центрифугируют при 5000 rpm в течение 30 мин и собирают чистую жидкость. 3. Метил- и пропилпарабен натрия растворяют в около 10 мл воды и добавляют к чистому фильтрату стадии 2 при перемешивании. 4. Затем добавляют ингредиенты 8 и 9 и растворяют в основном объеме при перемешивании и проверяют pH. 5. Затем к объему добавляют лимонную кислоту и фосфат натрия и доводят до определенного объема. 6. Раствор фильтруют, используя 0,22-микронный фильтр в асептических условиях, и продукт вносят в 10 мл пластиковую пробирку, состоящую из трех частей. Пример 2. Для составления геля: 1. Гидроксипропилметилцеллюлозу (HPMC) растворяют в около 50 мл воды при перемешивании. Кремофор RH 40 добавляют к этому раствору и растворяют при перемешивании. Как только раствор полностью растворился, затем добавляют основной активный ингредиент, как указано выше в рецептуре( 1-3), и растворяют при перемешивании. 2. Раствор затем центрифугируют при 5000 rpm в течение 30 мин и собирают чистую жидкость. 3. Метил- и пропилпарабен натрия растворяют в около 10 мл воды и добавляют к чистому фильтрату стадии 2 при перемешивании. 4. Добавляют ингредиент 8 при медленном перемешивании, как только он растворится, затем повышают pH до около 6,5 с помощью разбавленного раствором раствора гидроксида натрия. Затем добавляют ингредиент 10 и 11 и растворяют в основном объеме при перемешивании и проверяют pH. 5. Затем к объему добавляют лимонную кислоту и фосфат натрия и доводят до определенного объема. 6. Раствор фильтруют, используя 0,22-микронный фильтр в асептических условиях, и продукт вносят в 10 мл пластиковую пробирку, состоящую из трех частей.- 13016723 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Синергетическая травяная композиция, применяемая при глаукоме, содержащая синергетически эффективное количество экстракта растений, выбранных из видов Ocimum, в количестве от 0,1 до 1,0 мас.%, видов Curcuma - в количестве от 0,01 до 0,5 мас.%, Solanum nigrum - в количестве от 0,1 до 0,75 мас.%, и фармацевтически приемлемые наполнители или носители. 2. Синергетическая травяная композиция, применяемая при глаукоме, содержащая синергетически эффективное количество экстракта растений, выбранных из видов Ocimum, в количестве от 0,1 до 1,0 мас.%, видов Curcuma - в количестве от 0,01 до 0,5 мас.%, Areca catechu - в количестве от 0,1 до 1,0 мас.%, и фармацевтически приемлемые наполнители или носители. 3. Синергетическая травяная композиция по любому из п.1 или 2, в которой виды Ocimum выбирают из группы, состоящей из Ocimum basilicum, Ocimum canum, Ocimum kilimandscaricum, Ocimum sanctum, Ocimum viride, и виды Curcuma выбирают из группы, состоящей из Curcuma longa, Curcumavaleton,Curcuma amad, Curcuma aromatica Salisb. 4. Синергетическая травяная композиция по п.1, где композиция предпочтительно содержит видыOcimum в количестве 0,50 мас.%, виды Curcuma - в количестве 0,01 мас.% и Solanum nigrum - в количестве 0,25 мас.%. 5. Синергетическая травяная композиция по п.2, где композиция предпочтительно содержит видыOcimum в количестве 0,50 мас.%, виды Curcuma - в количестве 0,01 мас.% и Areca catechu - в количестве 0,25 мас.%. 6. Синергетическая травяная композиция по любому из п.1 или 4, где композиция предпочтительно содержит вид Ocimum basilicum в количестве 0,50 мас.%, вид Curcuma longa - в количестве 0,01 мас.% иSolanum nigrum - в количестве 0,25 мас.%. 7. Синергетическая травяная композиция по любому из п.2 или 5, где композиция предпочтительно содержит вид Ocimum basilicum в количестве 0,50 мас.%, вид Curcuma longa - в количестве 0,01 мас.% иAreca catechu - в количестве 0,25 мас.%. 8. Синергетическая травяная композиция по любому из п.1 или 2, в которой фармацевтически приемлемые наполнители выбирают из группы, включающей повышающие растворимость агенты, такие как полисорбат, циклодекстрин и их производные, Кремофор RH 40 и другие производные, повышающие вязкость агенты, такие как гидроксипропилметилцеллюлоза, и другие пригодные производные целлюлозы, поливиниловый спирт, повидон, карбопол карагенин, антиоксиданты, такие как лимонная кислота,EDTA и его соли, метабисульфит натрия и другие одобренные водорастворимые антиоксиданты, буферные агенты, такие как цитрат, борат, фосфат, цитрофосфат, и регулирующие осмолярность агенты, такие как хлорид натрия, маннит, глицерин, консерванты, такие как бензалкония хлорид, сорбяновая кислота,метилпарабен, пропилпарабен и их соли. 9. Синергетическая травяная композиция по любому из п.1 или 2, изготовленная в форме глазных капель, мази, крема или геля. 10. Способ получения синергетической травяной композиции по любому из п.1 или 2, включающий следующие стадии:(a) крупный помол отдельного растения и экстрагирование его растворителями, имеющими разную полярность, выбранными из группы, включающей воду, спирт, ацетон, этилацетат, петролейный эфир,хлороформ или их смеси в различных соотношениях;(b) необязательно концентрирование экстракта, полученного на стадии (a), под действием вакуума и преобразование его либо в форму густой пасты, включающей около 20-30% твердого вещества, либо в форму сухого порошка;(c) составление фармацевтически приемлемой травяной композиции посредством комбинирования экстрактов, полученных в стадии (a) или стадии (b), в разных соотношениях, как здесь указано, с получением синергетической травяной композиции в форме глазных капель, мази, крема или геля. 11. Способ получения синергетической травяной композиции по любому из п.1 или 2, включающий следующие стадии:(a) крупный помол отдельного растения и экстрагирование его с использованием дистилляционного способа;(b) концентрирование экстракта, полученного на стадии (a), под действием вакуума и преобразование его либо в форму густой пасты, включающей около 20-30% твердого вещества, либо в форму сухого порошка;(c) составление фармацевтически приемлемой травяной композиции посредством комбинирования экстрактов, полученных в стадии (a) или стадии (b), в разных соотношениях, как заявлено в п.1 или 2, с получением синергетической травяной композиции в форме глазных капель, мази, крема или геля. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2
МПК / Метки
МПК: A61K 36/889, A61P 27/06, A61K 36/9066, A61K 36/81, A61K 36/53, A61K 9/00
Метки: травяная, глаукоме, композиция, применяемая, получения, способ, синергетическая
Код ссылки
<a href="https://eas.patents.su/15-16723-sinergeticheskaya-travyanaya-kompoziciya-primenyaemaya-pri-glaukome-i-sposob-ee-polucheniya.html" rel="bookmark" title="База патентов Евразийского Союза">Синергетическая травяная композиция, применяемая при глаукоме, и способ ее получения</a>
Предыдущий патент: Система мобильной связи, устройство базовой станции и устройство мобильной станции
Следующий патент: Средство для защиты растений и его применение
Случайный патент: Фармацевтические композиции адсорбатов аморфного лекарственного средства