Нераспадающаяся твёрдая композиция для перорального применения с высокой дозой растворимых в воде лекарственных средств
Номер патента: 11374
Опубликовано: 27.02.2009
Авторы: Джаин Раджеш, Сингх Сукхджит, Джиндал Коур Чанд
Формула / Реферат
1. Нераспадающаяся, неразрушающаяся, небиоадгезивная и ненабухающая пероральная фармацевтическая композиция с регулируемым высвобождением, содержащая по меньшей мере один водорастворимый в высокой дозе активный ингредиент, выбранный из группы, включающей от примерно 500 до примерно 800 мг антибиотиков, примерно 500 мг метформина, примерно 500 мг никотиновой кислоты и их фармацевтически приемлемых солей или производных, по меньшей мере один растворитель, по меньшей мере одно связывающее вещество и полимерную систему, содержащую по меньшей мере один регулирующий высвобождение полимер, выбранный из группы, включающей сополимер поливинилпирролидона/поливинилацетата, полимеры метакриловой кислоты, полимеры акриловой кислоты и производные целлюлозы, за исключением этилцеллюлозы, или их смеси, необязательно с одним или более другими фармацевтически приемлемыми эксципиентами, причем композиция, изготовленная в подходящей лекарственной форме, сохраняет свою геометрическую форму даже после диффузии лекарства из лекарственной формы и обеспечивает концентрации активного ингредиента выше эффективных уровней продолжительные периоды времени.
2. Композиция по п.1, где антибиотик выбран из группы, включающей цефалоспорины, пенициллины и их фармацевтически приемлемые соли, гидраты, полиморфные формы, сложные эфиры и производные.
3. Композиция по п.1, где указанным антибиотиком является амоксициллина натрий.
4. Композиция по любому из пп.1-3, где композиция обеспечивает начальный выброс примерно 20-40% активного ингредиента в течение 1 ч для достижения в крови уровней, эквивалентных минимальной ингибирующей концентрации и поддержания этих уровней продолжительный период времени.
5. Композиция по п.1, которая содержит по меньшей мере два антибиотика, выбранных из группы, содержащей амоксициллин, ампициллин, клоксациллин, клавулановую кислоту и цефалоспорины или их фармацевтически пригодные соли или производные.
6. Композиция по п.1, где растворитель выбран из группы, содержащей лактозу, целлюлозу, микрокристаллическую целлюлозу, маннит, дикальция фосфат, прежелатинизированный крахмал, используемый либо отдельно, либо в комбинации.
7. Композиция по п.6, где растворителем является лактоза.
8. Композиция по п.1, где связывающее вещество выбрано из группы, содержащей поливинилпирролидон, производные целлюлозы, такие как гидроксипропилметилцеллюлоза, полимеры метакриловой кислоты и полимеры акриловой кислоты.
9. Композиция по п.1, где полимерная система содержит сополимер поливинилпирролидона/поливинилацетата.
10. Композиция по п.1, где полимерная система содержит полимер метакриловой кислоты и сополимер поливинилпирролидона/поливинилацетата.
11. Композиция по п.10, где полимер метакриловой кислоты выбран из группы, содержащей сополимер метакрилата аммония типа A USP и сополимер метакрилата аммония типа В USP.
12. Композиция по п.10, где соотношение полимера метакриловой кислоты и сополимера поливинилпирролидона/поливинилацетата составляет 20:1 до 1:20 по массе композиции.
13. Композиция по п.1, где фармацевтически пригодные эксципиенты выбраны из группы, содержащей дезинтегранты, связывающие вещества, наполнители, заполняющие объем агенты, агенты для нанесения покрытия, пластификаторы, органические растворители, красители, стабилизаторы, консерванты, смазывающие вещества, глиданты и хелатирующие агенты.
14. Композиция по любому из пп.1-13, которая представлена в виде таблеток, капсул и т.п.
15. Композиция по п.14, которая представлена в форме спрессованных таблеток.
16. Способ получения композиции по п.1, который включает следующие стадии:
1) смешивание активного(ых) ингредиента(ов), растворителя(ей), связывающего(их) вещества(в) и полимера(ов);
2) необязательно добавление одного или нескольких других фармацевтически пригодных эксципиентов;
3) изготовление из смеси пригодной пероральной лекарственной формы.
17. Способ по п.16, где указанный активный ингредиент выбран из группы, содержащей от примерно 500 до примерно 800 мг антибиотиков, примерно 500 мг метформина, примерно 500 мг никотиновой кислоты и их фармацевтически приемлемых солей или производных.
18. Способ по п.16, где указанным активным ингредиентом является амоксициллина натрий.
19. Способ пп.16-18, где композиция обеспечивает начальный выброс примерно 20-40% активного ингредиента в течение 1 ч для достижения в крови уровней, эквивалентных минимальной ингибирующей концентрации и поддержания этих уровней в течение продолжительного периода времени.
20. Способ по п.16, который включает по меньшей мере два активных ингредиента, выбранных из группы, содержащей амоксициллин, ампициллин, клоксациллин, клавулановую кислоту, цефалоспорины и их фармацевтически пригодные соли или производные.
21. Способ по п.16, где разбавитель выбран из группы, содержащей лактозу, целлюлозу, микрокристаллическую целлюлозу, маннит, дикальция фосфат, прежелатинизированный крахмал, применяемый отдельно или в комбинации.
22. Способ по п.16, где связывающее вещество выбрано из группы, содержащей поливинилпирролидон, производные целлюлозы, такие как гидроксипропилметилцеллюлоза, полимеры метакриловой кислоты и полимеры акриловой кислоты.
23. Способ по п.16, где полимерная система содержит полимер метакриловой кислоты и сополимер поливинилпирролидона/поливинилацетата.
24. Способ по п.23, где соотношение полимера метакриловой кислоты и сополимера поливинилпирролидона/поливинилацетата составляет от 20:1 до 1:20 по массе композиции.
Текст
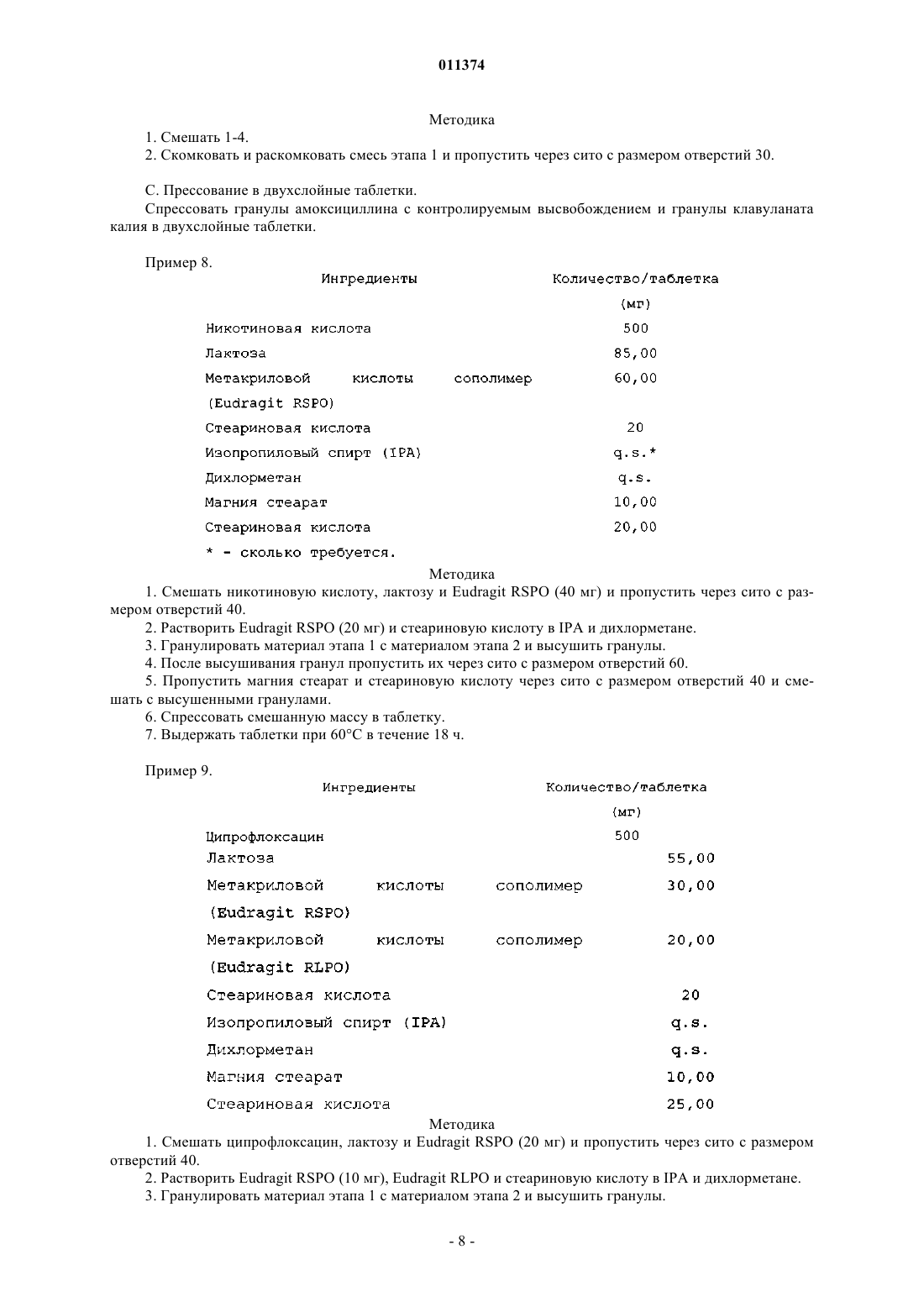
011374 Область техники, к которой относится изобретение Настоящее изобретение относится к фармацевтическим композициям с контролируемым высвобождением, содержащим по меньшей мере одну высокую дозу водорастворимого активного ингредиента, и к способу получения таких композиций, предпочтительно содержащих антибиотик(и) в качестве активного ингредиента, более предпочтительно амоксициллина натрий отдельно или в комбинации с другим(и) антибиотиком(ами). Композиции с контролируемым высвобождением относятся к нераспадающемуся, неразрушающемуся, небиоадгезивному и неразбухающему типу, предназначенному сохранять свою геометрическую форму при прохождении по желудочно-кишечному тракту. Композицию с контролируемым высвобождением применяют для обеспечения терапевтически эффективных уровней указанного активного ингредиента продолжительные периоды времени. Кроме того,указанная композиция, как ожидается, не влияет на биодоступность активного ингредиента в условиях голодания или насыщения. Предшествующий уровень техники Амоксициллин является бета-лактамом, широко применяемым в качестве антибиотика широкого спектра действия для лечения ряда распространенных бактериальных инфекций. Известно, что амоксициллин имеет чувствительность к ингибированию бета-лактамазами, продуцируемыми резистентными организмами. Амоксициллин является доступным в ряде составов, например таких, как капсулы, таблетки, сухие порошки для растворения, жевательные таблетки, рассасывающиеся таблетки и т.п. Амоксициллин является доступным в виде таблеток различной эффективности, такой как 250, 500, 875 мг и т.п. Стандартной дозой для взрослых является 250-500 мг 3 раза в день (tid). Кроме того, таблетка 875 мг предназначена для дозирования дважды в день (bid), вместо 500 мг tid. Высокая доза 3 г bid рекомендована для лечения рецидивирующей гнойной инфекции дыхательных путей. Применение 1 г амоксициллина рекомендуется как одна составляющая комбинированной терапии для уничтожения Helicobacter pilory при заболевании пептическая язва. В прошлом были сделаны попытки разработать составы амоксициллина с модифицированным/контролируемым высвобождением. Такие таблетки с модифицированным/контролируемым высвобождением могут обеспечить лучшее соблюдение больным режима и схемы лечения, так как они должны приниматься дважды в день по сравнению с дозой 500 мг tid. Европейский патент номер ЕР 1044680 раскрывает двухслойные таблетки, содержащие дозу с немедленным высвобождением части амоксициллина и калия клавуланата и дозу второй части амоксициллина с контролируемым высвобождением. Слой с контролируемым высвобождением является гидрофильной матрицей. Недостатком вышеуказанной композиции является необходимость в избыточном количестве эксципиентов для получения двухслойных таблеток. В комбинации с высокой дозой амоксициллина это приводит к получению продукта, имеющего слишком большой объем и неудобного при введении. Патент США 5690959 раскрывает композицию, полученную с использованием гидрофобного материала, полученного с помощью способа термальной инфузии. Амоксициллин, будучи чувствительным к температуре, может разлагаться, если его подвергать воздействию высокой температуры продолжительные периоды времени. Патент США 6399086 раскрывает фармацевтическую композицию амоксициллина, в которой 50% лекарственного средства высвобождается в течение 3-4 ч. Указанная композиция основана на гидрофильных эродирующих полимерах. Патент США 6368635 раскрывает твердую матричную композицию, которая является твердой при температуре окружающей среды, которая содержит средство, создающее вязкость, такое как полимер акриловой кислоты, способный создавать вязкость при контакте с водой как диспергирующей, по меньшей мере, по соседству с поверхностным слоем матричной частицы, содержащей полиглицериновый эфир жирной кислоты или липид и активный ингредиент. Матрица может быть такой, что матричную частицу, содержащую сложный полиглицериновый эфир жирной кислоты или липид и активный ингредиент, покрывают композицией, содержащей по меньшей мере один вискогенный агент. Такая композиция может прилипать к пищеварительному тракту и оставаться там продолжительный период времени,тем самым, усиливая биодоступность активного ингредиента. Такие прилипающие к слизистой оболочке желудка частицы имеют непредсказуемое время пребывания в желудке и оказывают сильное влияние на содержимое желудка. Биодоступность активных агентов в таких композициях сильно варьирует. Европейский патентЕРО 526862 раскрывает фармацевтическую композицию амоксициллина с пролонгированным временем пребывания вследствие высокой плотности композиции. Указанная композиция имеет недостаток, согласно которому неравномерное высвобождение активного ингредиента возникает вследствие вариабельного прохождения таблетки в тонкой кишке вследствие плотности, приводящей к значительной утрате биодоступности. В публикации РСТWO 200384510 описана препаративная форма двухслойной таблетки, содержащей антигистаминную противоотечную комбинацию. Вторая дискретная зона двухслойной таблетки содержит противоотечное лекарство и второй материал основы, второй материал основы содержит смесь, по меньшей мере, соединения с замедленным высвобождением и по меньшей мере одного фармацевтически приемлемого агента, способствующего скольжению или смазывающего вещества, где второй-1 011374 материал основы обеспечивает замедленное высвобождение противоотечного средства. В указанной публикации не описана необходимость применения, по меньшей мере, разбавителя и связующего с полимерной системой, содержащей по меньшей мере один контролирующий высвобождение полимер для получения нераспадающейся, неразрушающейся, небиоадгезивной и неразбухающей пероральной фармацевтической композиции с контролируемым высвобождением, где лекарство выделяется предпочтительно путем диффузии. Публикация РСТWO 2004012700 относится конкретно к лекарственной форме комбинации высокорастворимого активного ингредиента в высокой дозе как ингредиента с модифицированным высвобождением и активного ингредиента в низкой дозе с немедленным высвобождением, пригодной для проглатывания; включающей технику двойного замедления для контроля высвобождения высокой дозы высокорастворимого активного ингредиента, где указанная лекарственная форма содержит внутреннюю часть,имеющую активный ингредиент в низкой дозе с немедленным высвобождением, и наружную часть, имеющую высокорастворимый активный ингредиент в высокой дозе с модифицированным высвобождением, в которой наружняя часть содержит: а) частицы микроматрицы и б) покрытие для частиц микроматрицы.Hilton и Deasy, [J. Pharm. Sci. 82 (7): 737-743 (1993)] описывают таблетку амоксициллина тригидрата с контролируемым высвобождением, основанную на полимере гидроксипропилметилцеллюлозы ацетата сукцината с энтеросолюбильным покрытием. Этот полимер подавлял высвобождение лекарственного средства в присутствии желудочного рН, но мог усиливать его высвобождение в тонкой кишке. Исследование однократной дозы на группе голодающих субъектов показало, что таблетки имеют относительную биодоступность только 64,4%, возможно вследствие очень плохой абсорбции амоксициллина из дистального отдела тощей кишки и подвздошной кишки, чем из двенадцатиперстной кишки и проксимального отдела тощей кишки. Другие фармакокинетические параметры подтверждают отсутствие терапевтического преимущества этих факторов по сравнению с эквивалентной дозой стандартной капсулы.Hilton и Deasy, [Int. J. Pharm. 86 (1): 79=88 (1992)] также описывают плавающую таблетку амоксициллина тригидрата. Сначала была сформирована двухслойная таблетка, в которой слой лекарственного средства с контролируемым высвобождением состоял из амоксициллина и гидроксипропилцеллюлозы. Этот слой был связан со слоем, генерирующим газ. Однако, когда два слоя были соединены вместе, составная таблетка оказалась не способной плавать и преждевременно расщеплялась вдоль соединения двух слоев. Следовательно, было решено отказаться от этого подхода в пользу однойслойной плавающей таблетки. Эта таблетка оставалась плавучей в течение 6 ч и имела удовлетворительное in vitro замедленное высвобождение. Однако по сравнению со стандартными капсулами, принятыми натощак, с дозой,эквивалентной 500 мг амоксициллина, относительная биодоступность таблеток была 80,5% и другие фармакокинетические параметры Т (0,1 мкг/мл) и Т (0,5 мкг/мл) соответствовали интервалу времени, при котором уровни в сыворотке оставались большими чем или равными 0,1 и 0,5 мкг/мл, соответственно,что указывает на отсутствие улучшенной эффективности.Uchida с сотр. [Chem. Pharm. Bull. 37 (12): 3416-3419 (1989)] описывает препарат амоксициллина,микроинкапсулированный в этилцеллюлозу. Эти микрокапсулы проявляют эффект непрерывного высвобождения при введении собакам. Однако такой эффект мог быть предсказан, так как желудочный рН собак, которые были тестированы, значительно выше чем желудочный рН человека (рН около 6 у собак породы бигль по сравнению с рН около 2 у человека). Амоксициллин значительно менее растворим при рН 6, чем при рН 2. Можно было ожидать получения очень быстрого высвобождения лекарственного средства из тех же микрокапсул, если вводить людям. Следовательно, такая комбинация не смогла бы обеспечить контролируемое высвобождение амоксициллина.Arancibia с сотр. [Int. J. Clin. Phrmacol. Ther. Toxicol. 25 (2): 97-100 (1987)] исследовали фармакокинетику и биодоступность амоксициллина тригидрата. Они ссылаются на таблетки с контролируемым высвобождением, композиция которых не описана. В любом случае, лекарственное средство не было определено через 8 ч после перорального введения, и поэтому этот состав не имел преимуществ перед обычными препаратами. Некоторые композиции, описанные в предшествующем уровне техники, относящемся к данной области, получены с использованием гидрофильных набухающих полимеров. Эти композиции требуют применения чрезмерного количества агентов, контролирующих высвобождение. Так, комбинированием с высокой дозой амоксициллина получен продукт, который имеет слишком большой объем для введения перорально. Кроме того, эти продукты имеют значительные пищевые эффекты, вызывающие изменение биодоступности. Другой подход, имеющийся в данной области, включает применение биоадгезивных полимеров. Такие продукты являются высоковариабельными, так как биоадгезивность является свойством, которое достаточно сильно зависит от желудочного содержимого. Присутствие пищи в желудке снижает биоадгезивное свойство, что приводит к сниженной биодоступности. Третий подход, обсуждаемый в данной области, включает использование тонкокишечных полимеров. Так как амоксициллин преимущественно абсорбируется из проксимальной части тонкой кишки, высвобождение в кишечнике лекарства вызывает утрату биодоступности. Следовательно, еще существует необходимость разработки композиций амоксициллина с контролируемым высвобождением или отдельно, или в комбинации с другим(и) антибиотиком(ами), лишенных обсужденных выше ограничений.-2 011374 Сущность изобретения Целью настоящего изобретения является получение нераспадающейся, неразрушающейся, небиоадгезивной и ненабухающей пероральной фармацевтической композиции с контролируемым высвобождением, содержащей по меньшей мере один водорастворимый активный ингредиент в высокой дозе, по меньшей мере один разбавитель, по меньшей мере одно связывающее вещество и полимерную систему,содержащую по меньшей мере один контролирующий высвобождение полимер, где композиция, полученная в подходящей лекарственной форме, сохраняет свою геометрическую форму даже после диффузии лекарственного средства из лекарственной формы и обеспечивает концентрации активного ингредиента выше эффективных уровней в продолжительные периоды времени, необязательно с другими фармацевтически пригодными эксципиентами. Целью настоящего изобретения является получение нераспадающейся, неразрушающейся, небиоадгезивной и неразбухающей пероральной фармацевтической композиции с контролируемым высвобождением, содержащей по меньшей мере один водорастворимый активный ингредиент в высокой дозе, предпочтительно антибиотик, более предпочтительно амоксициллин или его фармацевтически пригодные соли, гидраты, полиморфные формы, сложные эфиры и их производные, наиболее предпочтительно амоксициллина натрий; по меньшей мере один разбавитель; по меньшей мере одно связывающее вещество и одну полимерную систему, содержащую по меньшей мере один контролирующий высвобождение полимер, где композиция, полученная в пригодной лекарственной форме, сохраняет свою геометрическую форму даже после диффузии лекарственного средства из лекарственной формы и обеспечивает концентрации активного ингредиента выше эффективных уровней в продолжительные периоды времени,необязательно с другими фармацевтически пригодными эксципиентами. Также целью настоящего изобретения является получение композиции с контролируемым высвобождением, где композиция содержит антибиотик в качестве активного ингредиента в комбинации с, по меньшей мере, другим антибиотиком. Далее, целью настоящего изобретения является получение композиции с контролируемым высвобождением, где композиция обеспечивает начальное импульсное высвобождение примерно 20-40% активного ингредиента в течение 1 ч для достижения в крови уровней, эквивалентных минимальной ингибирующей концентрации, и поддержания этих уровней продолжительный период времени. Еще другой целью настоящего изобретения является предоставление способа получения такой композиции, которая включает следующие стадии: 1) смешивание активного(ых) ингредиента(ов), разбавителя(ей), связывающего(их) вещества(в) и полимера(в); 2) необязательно добавление одного или нескольких других фармацевтически пригодных эксципиентов и 3) составление смеси в пригодной лекарственной форме. Подробное описание изобретения Настоящее изобретение относится к нераспадающейся, неразрушающейся, небиоадгезивной и неразбухающей пероральной фармацевтической композиции с контролируемым высвобождением, содержащей по меньшей мере один водорастворимый активный ингредиент в высокой дозе, по меньшей мере один растворитель, по меньшей мере одно связывающее вещество и полимерную систему, содержащую по меньшей мере один контролирующий высвобождение полимер необязательно с другими фармацевтически пригодными эксципиентами. Композиция получена в пригодной лекарственной форме, которая сохраняет свою геометрическую форму даже после диффузии лекарства из лекарственной формы и обеспечивает концентрации активного ингредиента выше эффективных уровней в продолжительные периоды времени. Активный ингредиент по настоящему изобретению может быть выбран, но не ограничиваясь ими,из группы, содержащей водорастворимые лекарства в высокой дозе, такие как метформин, калия хлорид,никотиновую кислоту, фенформин, клиндамицин, ципрофлоксацин, эритромицин, кветиапин, бальсалазид, натрия вальпроат, никотиновую кислоту, ванкомицин или их фармацевтически пригодные соли или производные. Активный ингредиент по настоящему изобретению выбран из группы, содержащей антибиотики,такие как цефалоспорины и пенициллины, и их фармацевтически пригодные соли, гидраты, полиморфные формы, сложные эфиры и производные. Активный ингредиент является предпочтительно антибиотиком, более предпочтительно амоксициллином или его фармацевтически пригодными солями, гидратами, полиморфными формами, сложными эфирами и производными, наиболее предпочтительно амоксициллина натрием. В другом варианте осуществления настоящее изобретение относится к препаративным формам амоксициллина натрия с контролируемым высвобождением для поддержания концентраций выше эффективных уровней в продолжительные периоды времени. В механизм высвобождения вовлечена преимущественно диффузия, и продукт находится в форме нераспадающейся таблетки. Таблетка сохраняет свою геометрическую форму даже после диффузии лекарства из системы. Кроме того, обнаружено, что препаративная форма имеет уникальный профиль высвобождения с монолитной структурой. Он обеспе-3 011374 чивает начальное импульсное высвобождение примерно 20-40% в течение 1 ч для достижения в крови уровней, эквивалентных минимальной ингибирующей концентрации, и поддержания этих уровней продолжительный период времени. В другом варианте осуществления по настоящему изобретению таблетки с контролируемым высвобождением, полученные с использованием указанной композиции, могут обеспечить лучшее соблюдение больным режима и схемы лечения, так как они должны приниматься дважды в день по сравнению с дозой 500 мг tid. Изобретение относится к препаративным формам антибиотика с контролируемым высвобождением либо одного, либо в комбинации с другим антибиотиком(ами) для поддержания концентраций выше эффективных уровней в продолжительные периоды времени. Предпочтительно изобретение относится к составу амоксициллина натрия с контролируемым высвобождением. В механизм высвобождения вовлечена преимущественно диффузия, и продукт находится в форме нераспадающейся таблетки. Таблетка сохраняет свою геометрическую форму даже после диффузии лекарства из системы. Никотиновая кислота, известная также как ниацин, длительно применялась для лечения гиперлипидемии. Давно известно, что это соединение проявляет благоприятные эффекты, снижая уровень общего холестерина, липопротеинов низкой плотности или LDL холестерина, триглицеридов и аполипопотеина a (Lp(a в организме человека, в то же время повышая уровень липопротеинов высокой плотности или HDL холестерина. Однако применение никотиновой кислоты стремятся ограничить вследствие ее побочных эффектов, таких как приливы крови к коже и неудобная схема приема лекарственного средства. Наиболее встречающимися препаративными формами никотиновой кислоты являются основанные на гидроксипропилметилцеллюлозе (НРМС) лекарственные формы разбухающего и распадающегося типа,которые обеспечивают начальное непредсказуемое высвобождение лекарства в течение продолжительных периодов времени и неустойчивые профили концентрации лекарства в плазме. В варианте осуществления активным ингредиентом настоящей фармацевтической композиции является никотиновая кислота или ее фармацевтически пригодные соли или производные. В другом варианте осуществления композиция по настоящему изобретению обеспечивает начальное импульсное высвобождение примерно 20-40% активного ингредиента в течение 1 ч для достижения в крови уровней, эквивалентных минимальной ингибирующей концентрации, и поддержания этих уровней продолжительный период времени. В варианте осуществления по настоящему изобретению композиция с контролируемым высвобождением содержит антибиотик в качестве активного ингредиента в комбинации с, по меньшей мере, другим антибиотиком. Антибиотики выбраны, но не ограничиваясь ими, из группы, содержащей амоксициллин, ампициллин, клоксациллин, клавулановую кислоту, цефалоспорины и т.п. или их фармацевтически пригодные соли или производные. В настоящем изобретении разбавитель выбран, но не ограничиваясь ими, из группы, содержащей лактозу, целлюлозу, микрокристаллическую целлюлозу, маннит, дикальция фосфат, прежелатинизированный крахмал и т.п., с применением либо отдельно, либо в комбинации. Предпочтительно применяемым растворителем является лактоза. В настоящем изобретении связующее вещество выбрано, но не ограничиваясь ими, из группы, содержащей поливинилпирролидон, производные целлюлозы, такие как гидроксипропилметилцеллюлоза,полимеры метакриловой кислоты, полимеры акриловой кислоты и т.п. Полимерная система по настоящему изобретению содержит по меньшей мере один полимер с контролируемым высвобождением, выбранный группы, содержащей сополимер поливинилпирролидона/поливинилацетата (Kollidon SR), полимеры метакриловой кислоты, полимеры акриловой кислоты,производные целлюлозы, за исключением этилцеллюлозы, и т.п. Более предпочтительно полимерная система содержит сополимер поливинилпирролидона/поливинилацетата. Полимер метакриловой кислоты выбран из группы, содержащей, но не ограничиваясь ими, Eudragit (Degussa), такой как сополимер аммония метакрилата типа A USP (Eudragit RL), сополимер аммония метакрилата типа В USP (EudragitRS), Eudragit RSPO, Eudragit RLPO и Eudragit RS30D. Соотношение полимера метакриловой кислоты и сополимера поливинилпирролидона/поливинилацетата составляет 20:1 к 1:20 по массе композиции, предпочтительно 10:1 к 1:10 по массе композиции. Фармацевтически пригодные эксципиенты по настоящему изобретению выбраны из группы, содержащей разбавители, дезинтегранты, связывающие вещества, наполнители, увеличивающие объем агенты, антиадгезивные агенты, антиоксиданты, буферные агенты, красители, ароматизаторы, покрывающие агенты, пластификаторы, органические растворители, стабилизаторы, консерванты, смазывающие вещества, вещества, способствующие скольжению (глидаты), хелатирующие агенты и т.п., известные в данной области. В варианте осуществления смазывающее вещество(а), применяемое по настоящему изобретению,выбрано, но не ограничиваясь ими, из группы, содержащей стеариновую кислоту, магния стеарат, цинка стеарат, глицерина бегенат, цитостеариловый спирт, гидрогенизированное растительное масло и т.п.,применяемые либо отдельно, либо в комбинации. В варианте осуществления по настоящему изобретению предлагается способ получения компози-4 011374 ции по п.1, который включает следующие этапы: 1) смешивание активного(ых) ингредиента(ов), растворителя(ей), связывающего(их) вещества(в) и полимера(в); 2) необязательно добавление одного или нескольких других фармацевтически пригодных эксципиентов и 3) составление смеси в пригодной лекарственной форме. В варианте осуществления композиция по настоящему изобретению находится в форме таблеток. Таблетки могут быть получены либо путем прямого прессования, сухого прессования (комкования), либо путем грануляции. В предпочтительном варианте осуществления по настоящему изобретению пероральная композиция находится в форме прямо спрессованных таблеток. Методика грануляции является водной или неводной. Предпочтительно таблетки по настоящему изобретению получены с помощью методики неводной грануляции. Используемый неводный растворитель выбран из группы, содержащей этанол или изопропиловый спирт. Настоящее изобретение относится к составу антибиотика с контролируемым высвобождением либо отдельно либо в комбинации с другим(и) антибиотиком(ами), который является немукоадгезивным, нераспадающимся, неразбухающим и неразрушающимся продуктом. В варианте осуществления по изобретению описывается препаративная форма амоксициллина натрия немукоадгезивного, нераспадающегося, неразбухающего и неразрушающегося типа. Указанная композиция сохраняет свою геометрическую форму повсюду при ее пребывании в желудочно-кишечном тракте. Продукт также имеет преимущество в том, что он оказывает минимальный пищевой эффект. Высвобождение лекарства из продукта происходит преимущественно путем механизма диффузии. Состав с контролируемым высвобождением, полученный в соответствии с настоящим изобретением, не теряет своей геометрической формы при прохождении через желудочно-кишечный тракт. Такой состав не предусматривает применение разбухающих полимеров, гидрофобных пластичных материалов или мукоадгезивных агентов. Композиция с контролируемым высвобождением по настоящему изобретению может быть составлена в виде пероральных лекарственных форм, таких как таблетки, капсулы и т.п. Примеры, приведенные ниже, служат иллюстрацией вариантам осуществления по настоящему изобретению. Однако они не предназначены для ограничения объема настоящего изобретения. Примеры Пример 1.-6 011374 Пример 6. А. Композиция гранул амоксициллина с контролируемым высвобождением. Методика 1. Просеять ингредиенты А.1, А.2 и А.3 и смешать. Растворить А.4 в А.5 и гранулировать смесь. Высушить и отсортировать гранулы. Смешать с ингредиентами А.6 и А.7, предварительно просеянными. 2. Просеять смесь В. 3. Спрессовать гранулы этапа 1 и этапа 2 в таблетки с вкладкой, где смесь клавуланата калия вкладывается в таблетку с гранулами амоксициллина. Пример 7. А. Композиция гранул амоксициллина с контролируемым высвобождением. Методика 1. Просеять ингредиенты 1-3 и смешать. 2. Растворить 4 в 5 и гранулировать смесь. 3. Высушить и отсортировать гранулы и смешать с ингредиентами 6 и 7, предварительно просеянными. В. Композиция гранул клавуланата калия.-7 011374 Методика 1. Смешать 1-4. 2. Скомковать и раскомковать смесь этапа 1 и пропустить через сито с размером отверстий 30. С. Прессование в двухслойные таблетки. Спрессовать гранулы амоксициллина с контролируемым высвобождением и гранулы клавуланата калия в двухслойные таблетки. Пример 8. Методика 1. Смешать никотиновую кислоту, лактозу и Eudragit RSPO (40 мг) и пропустить через сито с размером отверстий 40. 2. Растворить Eudragit RSPO (20 мг) и стеариновую кислоту в IPA и дихлорметане. 3. Гранулировать материал этапа 1 с материалом этапа 2 и высушить гранулы. 4. После высушивания гранул пропустить их через сито с размером отверстий 60. 5. Пропустить магния стеарат и стеариновую кислоту через сито с размером отверстий 40 и смешать с высушенными гранулами. 6. Спрессовать смешанную массу в таблетку. 7. Выдержать таблетки при 60 С в течение 18 ч. Пример 9. Методика 1. Смешать ципрофлоксацин, лактозу и Eudragit RSPO (20 мг) и пропустить через сито с размером отверстий 40. 2. Растворить Eudragit RSPO (10 мг), Eudragit RLPO и стеариновую кислоту в IPA и дихлорметане. 3. Гранулировать материал этапа 1 с материалом этапа 2 и высушить гранулы.-8 011374 4. После высушивания гранул пропустить их через сито с размером отверстий 60. 5. Пропустить магния стеарат и стеариновую кислоту через сито с размером отверстий 40 и смешать с высушенными гранулами. 6. Спрессовать смешанную массу в таблетку. 7. Выдержать таблетки при 60 С в течение 18 ч. Пример 10. Методика 1. Смешать никотиновую кислоту, лактозу и Eudragit RSPO и пропустить через сито с размером отверстий 40. 2. Растворить Eudragit RLPO и этилцеллюлозу в IPA и дихлорметане. 3. Гранулировать материал этапа 1 с материалом этапа 2 и высушить гранулы. 4. После высушивания гранул пропустить их через сито с размером отверстий 60. 5. Пропустить магния стеарат и стеариновую кислоту через сито с размером отверстий 40 и смешать с высушенными гранулами. 6. Спрессовать смешанную массу в таблетку. 7. Выдержать таблетки при 60 С в течение 18 ч. Пример 11. Методика 1. Смешать эритромицин, лактозу и Eudragit RSPO и пропустить через сито с размером отверстий 40. 2. Растворить Eudragit RLPO и этилцеллюлозу в IPA и дихлорметане. 3. Гранулировать материал этапа 1 с материалом этапа 2 и высушить гранулы. 4. После высушивания гранул пропустить их через сито с размером отверстий 60. 5. Пропустить магния стеарат и стеариновую кислоту через сито с размером отверстий 40 и сме-9 011374 шать с высушенными гранулами. 6. Спрессовать смешанную массу в таблетку. 7. Выдержать таблетки при 60 С в течение 18 ч. Пример 12. Методика 1. Смешать никотиновую кислоту, лактозу и Eudragit RSPO и пропустить через сито с размером отверстий 40. 2. Растворить Eudragit RLPO и этилцеллюлозу в IPA и дихлорметане. 3. Гранулировать материал этапа 1 с материалом этапа 2 и высушить гранулы. 4. После высушивания гранул пропустить их через сито с размером отверстий 60. 5. Пропустить магния стеарат и цетостеариловый спирт через сито с размером отверстий 40 и смешать с высушенными гранулами. 6. Спрессовать смешанную массу в таблетку. 7. Выдержать таблетки при 60 С в течение 18 ч. Пример 13. Методика 1. Пропустить гиацин, лактозу, стеариновую кислоту и Eudragit RSPO через сито с размером отверстий 40. 2. Диспергировать Eudragit RS30D в воде и нейтрализовать Eudragit RS30D натрия гидроксидом. Гранулировать объем этапа 1. 3. Высушить гранулы и пропустить через сито с размером отверстий 16. 4. Пропустить магния стеарат и стериновую кислоту через сито с размером отверстий 40 и смешать с высушенными гранулами.- 10011374 5. Спрессовать смешанную массу в таблетку. 6. Выдержать таблетки при 60 С в течение 18 ч. Пример 14. Методика 1. Смешать метформина гидрохлорид, лактозу и Eudragit RSPO (40 мг) и пропустить через сито с размером отверстий 40. 2. Растворить Eudragit RSPO (20 мг) и стеариновую кислоту в IPA и дихлорметане. 3. Гранулировать материал этапа 1 с материалом этапа 2 и высушить гранулы. 4. После высушивания гранул пропустить их через сито с размером отверстий 60. 5. Пропустить магния стеарат и стеариновую кислоту через сито с размером отверстий 40 и смешать с высушенными гранулами. 6. Спрессовать смешанную массу в таблетку. 7. Выдержать таблетки при 60 С в течение 18 ч. Пример 15. Методика 1. Смешать метформина гидрохлорид, лактозу и Eudragit RSPO (40 мг) и пропустить через сито с размером отверстий 40. 2. Растворить Eudragit RLPO и этилцеллюлозу в IPA и дихлорметане. 3. Гранулировать материал этапа 1 с материалом этапа 2 и высушить гранулы. 4. После высушивания гранул пропустить их через сито с размером отверстий 60. 5. Пропустить магния стеарат и глицерила бегенат через сито с размером отверстий 40 и смешать с высушенными гранулами. 6. Спрессовать смешанную массу в таблетку. 7. Выдержать таблетки при 60 С в течение 18 ч.- 11011374 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Нераспадающаяся, неразрушающаяся, небиоадгезивная и ненабухающая пероральная фармацевтическая композиция с регулируемым высвобождением, содержащая по меньшей мере один водорастворимый в высокой дозе активный ингредиент, выбранный из группы, включающей от примерно 500 до примерно 800 мг антибиотиков, примерно 500 мг метформина, примерно 500 мг никотиновой кислоты и их фармацевтически приемлемых солей или производных, по меньшей мере один растворитель, по меньшей мере одно связывающее вещество и полимерную систему, содержащую по меньшей мере один регулирующий высвобождение полимер, выбранный из группы, включающей сополимер поливинилпирролидона/поливинилацетата, полимеры метакриловой кислоты, полимеры акриловой кислоты и производные целлюлозы, за исключением этилцеллюлозы, или их смеси, необязательно с одним или более другими фармацевтически приемлемыми эксципиентами, причем композиция, изготовленная в подходящей лекарственной форме, сохраняет свою геометрическую форму даже после диффузии лекарства из лекарственной формы и обеспечивает концентрации активного ингредиента выше эффективных уровней продолжительные периоды времени. 2. Композиция по п.1, где антибиотик выбран из группы, включающей цефалоспорины, пенициллины и их фармацевтически приемлемые соли, гидраты, полиморфные формы, сложные эфиры и производные. 3. Композиция по п.1, где указанным антибиотиком является амоксициллина натрий. 4. Композиция по любому из пп.1-3, где композиция обеспечивает начальный выброс примерно 2040% активного ингредиента в течение 1 ч для достижения в крови уровней, эквивалентных минимальной ингибирующей концентрации и поддержания этих уровней продолжительный период времени. 5. Композиция по п.1, которая содержит по меньшей мере два антибиотика, выбранных из группы,содержащей амоксициллин, ампициллин, клоксациллин, клавулановую кислоту и цефалоспорины или их фармацевтически пригодные соли или производные. 6. Композиция по п.1, где растворитель выбран из группы, содержащей лактозу, целлюлозу, микрокристаллическую целлюлозу, маннит, дикальция фосфат, прежелатинизированный крахмал, используемый либо отдельно, либо в комбинации. 7. Композиция по п.6, где растворителем является лактоза. 8. Композиция по п.1, где связывающее вещество выбрано из группы, содержащей поливинилпирролидон, производные целлюлозы, такие как гидроксипропилметилцеллюлоза, полимеры метакриловой кислоты и полимеры акриловой кислоты. 9. Композиция по п.1, где полимерная система содержит сополимер поливинилпирролидона/поливинилацетата. 10. Композиция по п.1, где полимерная система содержит полимер метакриловой кислоты и сополимер поливинилпирролидона/поливинилацетата. 11. Композиция по п.10, где полимер метакриловой кислоты выбран из группы, содержащей сополимер метакрилата аммония типа A USP и сополимер метакрилата аммония типа В USP. 12. Композиция по п.10, где соотношение полимера метакриловой кислоты и сополимера поливинилпирролидона/поливинилацетата составляет 20:1 до 1:20 по массе композиции. 13. Композиция по п.1, где фармацевтически пригодные эксципиенты выбраны из группы, содержащей дезинтегранты, связывающие вещества, наполнители, заполняющие объем агенты, агенты для нанесения покрытия, пластификаторы, органические растворители, красители, стабилизаторы, консерванты, смазывающие вещества, глиданты и хелатирующие агенты. 14. Композиция по любому из пп.1-13, которая представлена в виде таблеток, капсул и т.п. 15. Композиция по п.14, которая представлена в форме спрессованных таблеток. 16. Способ получения композиции по п.1, который включает следующие стадии: 1) смешивание активного(ых) ингредиента(ов), растворителя(ей), связывающего(их) вещества(в) и полимера(ов); 2) необязательно добавление одного или нескольких других фармацевтически пригодных эксципиентов; 3) изготовление из смеси пригодной пероральной лекарственной формы. 17. Способ по п.16, где указанный активный ингредиент выбран из группы, содержащей от примерно 500 до примерно 800 мг антибиотиков, примерно 500 мг метформина, примерно 500 мг никотиновой кислоты и их фармацевтически приемлемых солей или производных. 18. Способ по п.16, где указанным активным ингредиентом является амоксициллина натрий. 19. Способ пп.16-18, где композиция обеспечивает начальный выброс примерно 20-40% активного ингредиента в течение 1 ч для достижения в крови уровней, эквивалентных минимальной ингибирующей концентрации и поддержания этих уровней в течение продолжительного периода времени. 20. Способ по п.16, который включает по меньшей мере два активных ингредиента, выбранных из группы, содержащей амоксициллин, ампициллин, клоксациллин, клавулановую кислоту, цефалоспорины и их фармацевтически пригодные соли или производные.- 12011374 21. Способ по п.16, где разбавитель выбран из группы, содержащей лактозу, целлюлозу, микрокристаллическую целлюлозу, маннит, дикальция фосфат, прежелатинизированный крахмал, применяемый отдельно или в комбинации. 22. Способ по п.16, где связывающее вещество выбрано из группы, содержащей поливинилпирролидон, производные целлюлозы, такие как гидроксипропилметилцеллюлоза, полимеры метакриловой кислоты и полимеры акриловой кислоты. 23. Способ по п.16, где полимерная система содержит полимер метакриловой кислоты и сополимер поливинилпирролидона/поливинилацетата. 24. Способ по п.23, где соотношение полимера метакриловой кислоты и сополимера поливинилпирролидона/поливинилацетата составляет от 20:1 до 1:20 по массе композиции.
МПК / Метки
МПК: A61K 31/00, A61K 9/20
Метки: растворимых, композиция, воде, перорального, дозой, нераспадающаяся, высокой, применения, лекарственных, твёрдая, средств
Код ссылки
<a href="https://eas.patents.su/15-11374-neraspadayushhayasya-tvyordaya-kompoziciya-dlya-peroralnogo-primeneniya-s-vysokojj-dozojj-rastvorimyh-v-vode-lekarstvennyh-sredstv.html" rel="bookmark" title="База патентов Евразийского Союза">Нераспадающаяся твёрдая композиция для перорального применения с высокой дозой растворимых в воде лекарственных средств</a>
Предыдущий патент: Модифицированное высвобождение фармацевтической композиции
Случайный патент: Производные пиррола, их получение и их применение в терапии