Композиция таблетки пролонгированного высвобождения, содержащая прамипексол или его фармацевтически приемлемую соль, способ ее изготовления и ее применение
Формула / Реферат
1. Композиция таблетки пролонгированного высвобождения, содержащая прамипексол или его фармацевтически приемлемую соль в матрице, включающей по меньшей мере три набухающих в воде полимера, один из указанных полимеров представляет собой предварительно желатинизированный крахмал, второй полимер представляет собой анионогенный полимер, являющийся сшитым полимером акриловой кислоты, и третий полимер выбран из гидроксипропилцеллюлозы и гидроксипропилметилцеллюлозы.
2. Композиция таблетки пролонгированного высвобождения по п.1, в которой анионогенный полимер представляет собой сшитый полимер акриловой кислоты, причем содержание сшитого полимера акриловой кислоты в матрице равно от 0,25 до 25 мас.%, предпочтительно от 0,5 до 15 мас.% и более предпочтительно от 1 до 10 мас.%.
3. Композиция таблетки пролонгированного высвобождения по п.2, в которой набухающий в воде третий полимер представляет собой гидроксипропилметилцеллюлозу, причем содержание гидроксипропилметилцеллюлозы в матрице равно от 10 до 75 мас.% и предпочтительно от 25 до 65 мас.%.
4. Композиция таблетки пролонгированного высвобождения по п.1, в которой матрица включает:

5. Композиция таблетки пролонгированного высвобождения по п.1, в которой матрица включает


6. Композиция таблетки пролонгированного высвобождения по п.1, в которой матрица включает
от 0,1 до 2 мас.% прамипексола или его соли;
от 25 до 65 мас.% гидроксипропилметилцеллюлозы;
от 0 до 40 мас.% натриевой соли карбоксиметилцеллюлозы;
от 25 до 75 мас.% предварительно желатинизированного крахмала;
от > 0 до 15 мас.% акрилового полимеризата, предпочтительно карбомера 941;
от 0,5 до 50 мас.% других инертных наполнителей, предпочтительно выбранных из группы, включающей коллоидный диоксид кремния, стеарат магния, моногидрат лактозы, маннит, микрокристаллическую целлюлозу, безводный гидрофосфат кальция, гидроксипропилцеллюлозу, повидон, коповидон, тальк, макроголы, додецилсульфат натрия, оксиды железа и диоксид титана.
7. Композиция таблетки пролонгированного высвобождения по п.1, где полученная таблетка обеспечивает зависящее от рН высвобождение с более быстрым высвобождением в диапазоне рН < 4,5 и с более медленным и не зависящим от рН высвобождением в диапазоне рН 4,5-7,5.
8. Композиция таблетки пролонгированного высвобождения по п.7, в которой матрица включает гидроксипропилметилцеллюлозу в количестве от 10 до 75%, предпочтительно от 25 до 65 мас.% и инертные наполнители в количестве от 25 до 90%, предпочтительно от 35 до 75 мас.%.
9. Композиция таблетки пролонгированного высвобождения по любому предыдущему пункту, в которой анионогенный полимер представляет собой полимеризат акриловой кислоты, который выбран из групп карбомеров или Карбополов®.
10. Композиция таблетки пролонгированного высвобождения по п.9, содержащая от 0,25 до 25 мас.%, предпочтительно от 0,5 до 15 мас.%, наиболее предпочтительно от 1 до 10 мас.% полимеризата акриловой кислоты.
11. Композиция таблетки пролонгированного высвобождения по любому предыдущему пункту, содержание прамипексола или его фармацевтически приемлемой соли в которой достаточно для обеспечения суточной дозы, вводимой за один раз.
12. Способ изготовления композиции таблетки пролонгированного высвобождения по одному из предыдущих пунктов методом прямого прессования, включающий стадии:
(1) получения порошка активного ингредиента, в котором активным ингредиентом является прамипексол или его фармацевтически приемлемая соль, путем его предварительного смешивания с частью набухающих в воде полимеров и другим инертным наполнителем (наполнителями) в смесителе, причем перед использованием прамипексол или его фармацевтически приемлемую соль размалывают, предпочтительно размалывают на штифтовой мельнице;
(2) предварительного перемешивания порошка активного ингредиента, полученного на стадии (1), основной части набухающего в воде полимера (полимеров) и инертных наполнителей в смесителе с получением предварительной смеси;
(3) необязательно сухого просеивания предварительной смеси через сито для отделения слипшихся частиц и улучшения однородности смеси;
(4) перемешивания предварительной смеси, полученной на стадии (2) или (3), в смесителе, необязательно с прибавлением оставшихся инертных наполнителей к смеси и продолжения перемешивания;
(5) таблетирования готовой смеси путем ее прессования на подходящем таблеточном прессе с получением матричных таблеток.
13. Способ изготовления композиции таблетки пролонгированного высвобождения по любому из предыдущих пп.1-11 методом мокрого гранулирования, включающий стадии:
(1) получения порошка активного ингредиента, в котором активным ингредиентом является прамипексол или его фармацевтически приемлемая соль, путем его смешивания с частью инертных наполнителей в смесителе, причем перед использованием прамипексол или его фармацевтически приемлемую соль размалывают, предпочтительно размалывают на штифтовой мельнице;
(2) гранулирования порошка активного ингредиента, полученного на стадии (1), путем прибавления гранулирующей жидкости, предпочтительно воды;
(3) сушки гранул, полученных на стадии (2), в сушилке с псевдоожиженным слоем или в сушильной камере;
(4) смешивания высушенных гранул, полученных на стадии (3), с набухающими в воде полимерами и инертными наполнителями в смесителе с получением готовой смеси;
(5) таблетирования готовой смеси, полученной на стадии (4), путем ее прессования на подходящем таблеточном прессе с получением матричных таблеток.
14. Способ изготовления композиции таблетки пролонгированного высвобождения по любому из предыдущих пп.1-11 методом сухого гранулирования, включающий стадии:
(1) смешивания активного ингредиента прамипексола или его фармацевтически приемлемой соли с частью наполнителей или со всеми инертными наполнителями в смесителе, причем перед использованием прамипексол или его фармацевтически приемлемую соль размалывают, предпочтительно размалывают на штифтовой мельнице;
(2) прессования смеси, полученной на стадии (1), на подходящем вальцовом прессе;
(3) измельчения лент, полученных на стадии (1), в небольшие гранулы с помощью подходящих стадий размола или просеивания;
(4) необязательного смешивания гранул, полученных на стадии (3), в смесителе с оставшимися инертными наполнителями с получением готовой смеси;
(5) таблетирования гранул, полученных на стадии (3), или готовой смеси, полученной на стадии (4), путем ее прессования на подходящем таблеточном прессе с получением матричных таблеток.
15. Применение композиции таблетки пролонгированного высвобождения по одному из предыдущих пп.1-11 для изготовления лекарственной композиции, предназначенной для лечения болезни Паркинсона и сопутствующих ей осложнений или нарушений.
Текст
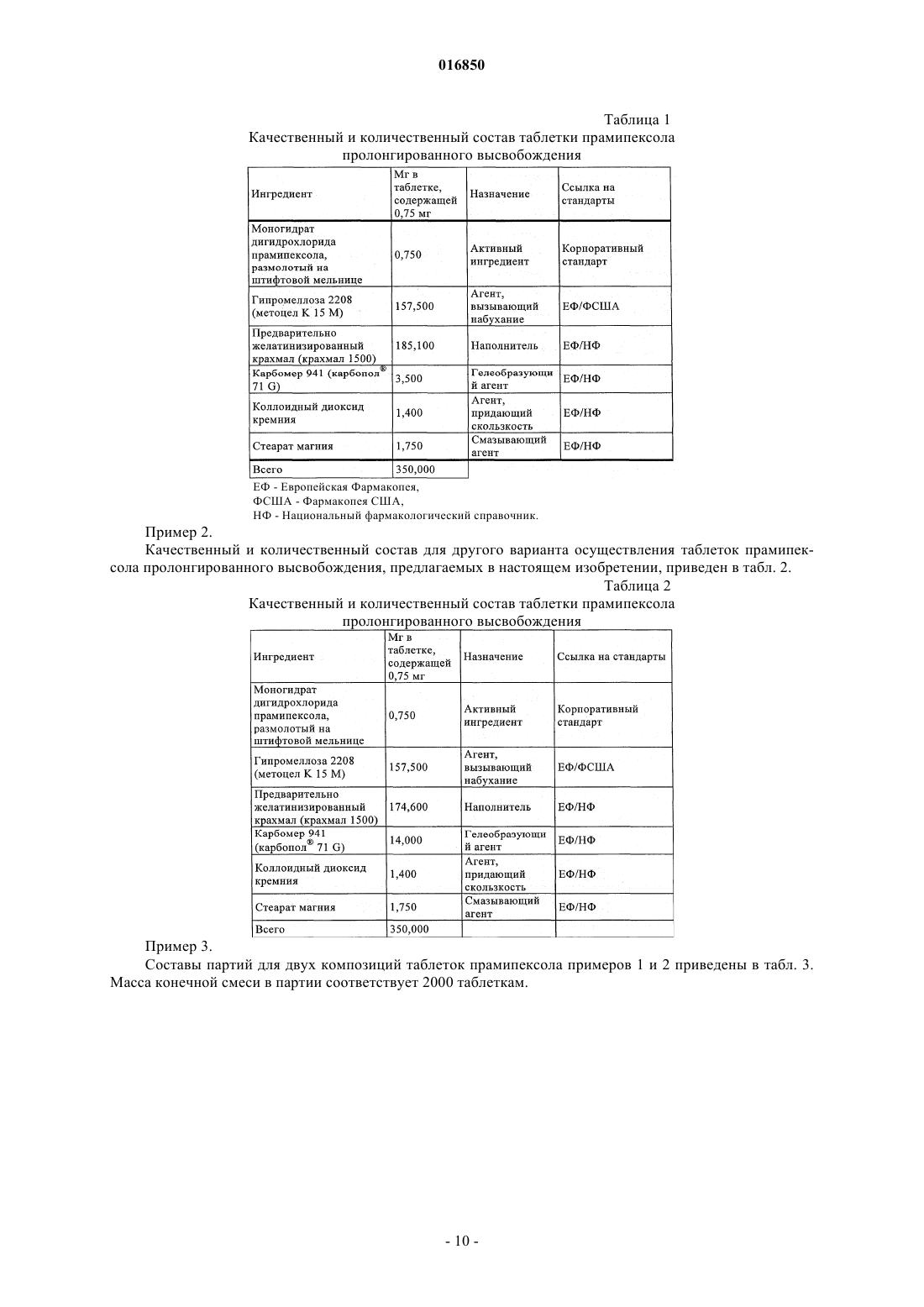
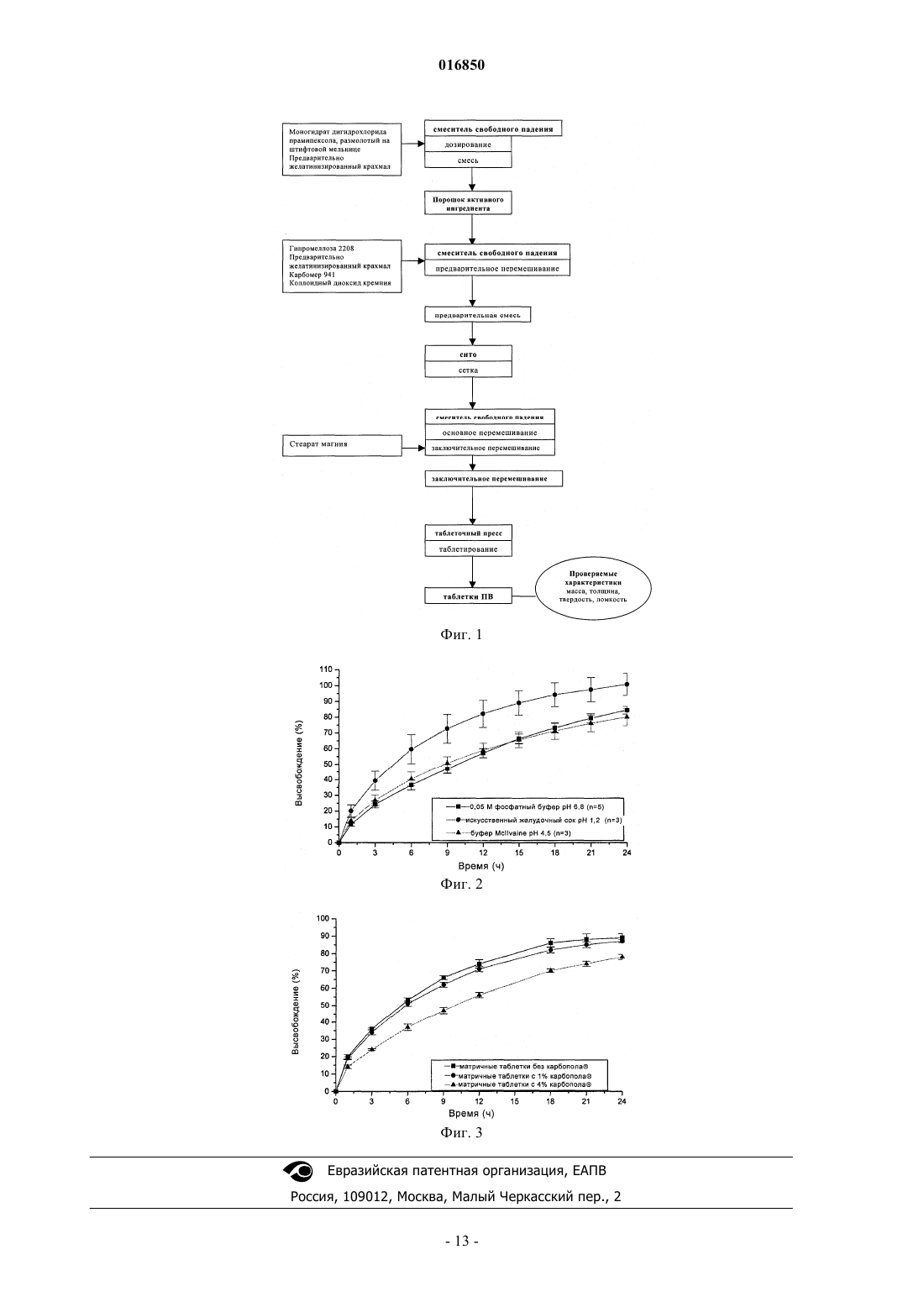
КОМПОЗИЦИЯ ТАБЛЕТКИ ПРОЛОНГИРОВАННОГО ВЫСВОБОЖДЕНИЯ,СОДЕРЖАЩАЯ ПРАМИПЕКСОЛ ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМУЮ СОЛЬ, СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ И ЕЕ ПРИМЕНЕНИЕ В изобретении предложена композиция таблетки с пролонгированным высвобождением,содержащая прамипексол или его фармацевтически приемлемую соль в матрице, где матрица включает по меньшей мере три набухающих в воде полимера, в которой один из указанных полимеров представляет собой предварительно желатинизированный крахмал, второй из указанных полимеров представляет собой анионогенный полимер, являющийся сшитым полимером акриловой кислоты, а третий полимер выбран из гидроксипропилцеллюлозы и гидроксипропилметилцеллюлозы.(71)(73) Заявитель и патентовладелец: БРИНГЕР ИНГЕЛЬХАЙМ ИНТЕРНАЦИОНАЛЬ ГМБХ (DE) 016850 Область техники, к которой относится изобретение Настоящее изобретение относится к композиции таблетки пролонгированного высвобождения, содержащей прамипексол или его фармацевтически приемлемую соль, к способу ее изготовления и к ее применению. Уровень техники Прамипексол является известным агонистом допаминового рецептора D2. По структуре он отличается от лекарственных средств, полученных из спорыньи, например бромкриптина или перголида. С фармакологической точки зрения он также отличается тем, что является полным агонистом и обладает селективностью по отношению к группе D2 допаминовых рецепторов. Химическое название прамипексола - (S)-2-амино-4,5,6,7-тетрагидро-6-(пропиламино)бензотиазол и он обладает молекулярной формулой C10H17N3S и относительной молекулярной массой, равной 211,33. Химическая формула имеет вид Обычно применяющейся солью является моногидрат дигидрохлорида прамипексола (молекулярная формула C10H21Cl2N3OS; относительная молекулярная масса равна 302,27). Моногидрат дигидрохлорида прамипексола представляет собой белый или почти белый безвкусный кристаллический порошок. Плавление происходит в диапазоне от 296 до 301 С с разложением. Прамипексол является хиральным соединением с одним хиральным центром. Чистый (S)-энантиомер получают синтетическим путем с хиральной перекристаллизацией одного из промежуточных продуктов во время синтеза. Моногидрат дигидрохлорида прамипексола является хорошо растворимым соединением. Растворимость в воде превышает 20 мг/мл и растворимость в буферных средах обычно превышает 10 мг/мл при рН от 2 до 7,4. Моногидрат дигидрохлорида прамипексола негигроскопичен и высококристалличен. При размоле кристаллическая модификация (моногидрата) не меняется. Прамипексол весьма стабилен в твердом состоянии, но в растворе чувствителен к воздействию света. Таблетки прамипексола немедленного высвобождения (НВ) впервые были разрешены к применению в США в 1997 г., а затем в течение нескольких лет были разрешены к продаже в Европейском Союзе (ЕС), Швейцарии, Канаде и Южной Америке, а также в странах Восточной Европы, Ближнего Востока и Азии. Таблетки НВ прамипексола в ЕС и США показаны для лечения в комбинации с леводопа при наличии признаков и симптомов ранней или поздней стадии болезни Паркинсона. Таблетки НВ следует принимать 3 раза в сутки. С фармакокинетической точки зрения таблетки НВ прамипексола быстро и полностью всасываются при пероральном введении. Абсолютная биологическая доступность превышает 90% и максимальная концентрация в плазме устанавливается через 1-3 ч. Скорость всасывания уменьшается при приеме пищи, но полностью всасывание не прекращается. Прамипексол характеризуется линейной кинетикой и уровни в плазме у разных пациентов различаются относительно мало. Время полувыведения (t1/2[ч]) составляет от 8 ч для молодых до 12 ч для пожилых пациентов. Общеизвестно, что модифицированное высвобождение активного ингредиента (ингредиентов) позволяет упростить график введения пациентам вследствие уменьшения количества рекомендованных суточных приемов, что улучшает соблюдение пациентом режима лечения и ослабляет побочные эффекты, например, связанные с большими пиковыми уровнями в плазме. В фармацевтических препаратах модифицированного высвобождения регулируется высвобождение содержащегося активного ингредиента или ингредиентов во времени и к ним относятся препараты регулируемого, длительного, замедленного, задержанного, медленного или пролонгированного высвобождения, так что они обеспечивают решение терапевтических или относящихся к удобству приема задач, для решения которых непригодны обычные дозированные формы, такие как растворы или быстрорастворяющиеся дозированные формы. Модифицированное или пролонгированное высвобождение активного ингредиента (ингредиентов) из фармацевтического препарата можно обеспечить путем равномерного включения указанного активного ингредиента (ингредиентов) в гидрофильную матрицу, представляющую собой сетку растворимых,частично растворимых или нерастворимых вязких гидрофильных полимеров, связанных друг с другом физическими или химическими взаимодействиями, ионными или кристаллическими взаимодействиями,путем образования комплексов, водородными связями или ван-дер-ваальсовыми силами. При взаимодействии с водой указанная гидрофильная матрица набухает и тем самым образует защитный слой геля, из которого активный ингредиент (ингредиенты) медленно, постепенно, непрерывно во времени высвобождается посредством диффузии через полимерную сетку вследствие разрушения слоя геля, посредством растворения полимера или путем сочетания указанных механизмов высвобождения. Однако оказалось затруднительно изготовить таблетку, обладающую подходящим сочетанием модифицированного, пролонгированного или замедленного высвобождения и удобства применения, в ко-1 016850 торой содержится лекарственное средство, обладающее относительно высокой растворимостью, как в случае дигидрохлорида прамипексола. В предшествующем уровне техники описано несколько методик изготовления композиций таблеток прамипексола замедленного высвобождения. В WO 2004/010997 описана фармацевтическая композиция замедленного высвобождения в виде таблетки для перорального введения, содержащей растворимую в воде соль прамипексола, диспергированную в матрице, включающей гидрофильный полимер и крахмал, обладающей прочностью на разрыв,равной не менее примерно 0,15 кНсм-2, предпочтительно не менее примерно 0,175 кНсм-2 и более предпочтительно не менее примерно 0,2 кНсм-2 при доле твердого вещества (отношение абсолютной плотности уплотненного крахмала к объемной плотности), типичной для таблетки. Описание в основном относится к композиции, которая при высокоскоростной операции таблетирования обладает достаточной твердостью, предпочтительно достаточной для исключения разрушения при нанесении слоя покрытия. Предпочтительный вариант осуществления относится к фармацевтической композиции в виде таблетки для перорального введения, включающей ядро, содержащее моногидрат дигидрохлорида прамипексола в количестве, равном примерно 0,375, 0,75, 1,5, 3 или 4,5 мг, диспергированный в матрице, включающей:(а) ГПМЦ типа 2208 в количестве от примерно 35 до примерно 50% в пересчете на массу таблетки и (b) предварительно желатинизированный крахмал, обладающий прочностью на разрыв, равной не менее примерно 0,15 кНсм-2 при доле твердого вещества (отношение абсолютной плотности уплотненного крахмала к объемной плотности), равной 0,8, в количестве от примерно 45 до примерно 65% в пересчете на массу таблетки; указанное ядро в основном заключено в покрытие, которое составляет от примерно 2 до примерно 7% в пересчете на массу таблетки, указанное покрытие включает основанный на этилцеллюлозе гидрофобный или нерастворимый в воде компонент и основанный на ГПМЦ порообразующий компонент в количестве от примерно 10 до примерно 40% в пересчете на массу основанного на этилцеллюлозе компонента. Кроме того, в WO 2004/010999 раскрыта фармацевтическая композиция для перорального введения, включающая терапевтически эффективное количество прамипексола или его фармацевтически приемлемой соли и по меньшей мере один фармацевтически приемлемый инертный наполнитель, указанная композиция обладает по меньшей мере одной из следующих характеристик: (а) профилем высвобождения in vitro таким, что через 2 ч после помещения таблетки в стандартное устройство для исследования растворения в среднем растворяется не более примерно 20% прамипексола; (b) профилем всасывания прамипексола in vivo после перорального введения одной дозы здоровым взрослым людям, при котором время, за которое всасывание протекает в среднем на 20%, превышает примерно 2 ч и/или время, за которое всасывание протекает в среднем на 40%, превышает примерно 4 ч. Однако с практической точки зрения представляется, что любая композиция, обладающая профилем пролонгированного или регулируемого высвобождения, предназначенная для введения один раз в сутки, должна отвечать указанным выше требованиям, но не приведены общие рекомендации о том, как обеспечить такой профиль. Объектом настоящего изобретения является композиция таблетки регулируемого высвобождения прамипексола или его фармацевтически приемлемой соли, которая пригодна для перорального введения один раз в сутки. Другим объектом является композиция таблетки, содержащая прамипексол или его фармацевтически приемлемую соль, которая обеспечивает суточное по длительности терапевтическое воздействие и позволяет пациентам проводить симптоматическое лечение с помощью одной суточной дозы, что делает возможным регулирование профиля высвобождения активного ингредиента в соответствии с выбранным профилем высвобождения, зависящим или не зависящим от значений рН. Кроме того, необходим способ изготовления композиции таблетки. Описание изобретения Согласно изобретению неожиданно было установлено, что прамипексол или его фармацевтически приемлемую соль можно применять в композициях в виде вводимых один раз в сутки таблеток пролонгированного (или медленного) высвобождения и две альтернативные методики изготовления обеспечивают разные скорости высвобождения, зависящие или не зависящие от значения рН. Объектом настоящего изобретения является композиция таблетки пролонгированного высвобождения, содержащая прамипексол или его фармацевтически приемлемую соль в матрице, где матрица включает по меньшей мере три набухающих в воде полимера, в которой один из указанных полимеров представляет собой предварительно желатинизированный крахмал, второй из указанных полимеров представляет собой анионогенный полимер, являющийся сшитым полимером акриловой кислоты, и при этом третий полимер не является предварительно желатинизированным крахмалом или анионогенным полимером и выбран из гидроксипропилцеллюлозы и гидроксипропилметилцеллюлозы. Предпочтительной является композиция таблетки пролонгированного высвобождения, в которой анионогенный полимер представляет собой сшитый полимер акриловой кислоты и в которой содержание необязательно сшитого полимера акриловой кислоты в матрице равно от примерно 0,25 до примерно 25 мас.%, предпочтительно от примерно 0,5 до примерно 15 мас.% и более предпочтительно от примерно 1 до примерно 10 мас.%.-2 016850 Также предпочтительной является композиция таблетки пролонгированного высвобождения, включающая набухающий в воде полимер, который не является предварительно желатинизированным крахмалом или анионогенным полимером и который предпочтительно выбран из группы, включающей гидроксипропилцеллюлозу и гидроксипропилметилцеллюлозу. Особенно предпочтительной является композиция таблетки пролонгированного высвобождения, в которой набухающий в воде полимер, который не является предварительно желатинизированным крахмалом или анионогенным полимером, представляет собой гидроксипропилметилцеллюлозу и в которой содержание гидроксипропилметилцеллюлозы в матрице равно от примерно 10 до примерно 75 мас.% и предпочтительно от примерно 25 до примерно 65 мас.%. Особенно предпочтительной является композиция таблетки пролонгированного высвобождения, в которой матрица включает примерно: Частный вариант осуществления настоящего изобретения относится к композиции таблетки пролонгированного высвобождения, содержащей прамипексол или его фармацевтически приемлемую соль в матрице, включающей предварительно желатинизированный крахмал в качестве одного из трех или более набухающих в воде полимеров, набухающий в воде анионогенный полимер, предпочтительно полимеризат акриловой кислоты, необязательно инертные наполнители, при этом полученная таблетка обеспечивает зависящее от рН высвобождение с более быстрым высвобождением в диапазоне рН 4,5 и с более медленным и, кроме того, не зависящим от рН высвобождением в диапазоне рН от 4,5 до 7,5. Композиции пролонгированного высвобождения, предлагаемые в настоящем изобретении, предназначенные для перорального введения, позволяют выбрать и оценить, какие in vitro характеристики высвобождения и временные характеристики композиции являются наиболее подходящими для обеспечения необходимых профилей содержания в плазме in vivo предпочтительно при введении один раз в сутки. Поэтому для матричной таблетки в виде разовой дозы разработана методика изготовления композиций в нескольких вариантах, т.е. изготовления композиций, обладающих разными типами режима высвобождения и разными зависимостями от рН. Эти альтернативные композиции благоприятны для пациентов, поскольку доставка лекарственного средства посредством пролонгированного высвобождения позволяет пациентам проводить симптоматическое лечение с помощью одной дозы в сутки, что удобнее для пациента и улучшает соблюдение режима лечения. Выражение "высвобождение in vitro" при использовании выше или ниже в настоящем изобретении означает высвобождение, происходящее в жидкой среде такого типа, который обычно используется в экспериментах in vitro, при которых может происходить высвобождение активного ингредиента из композиции пролонгированного высвобождения, т.е., например, в средах для растворения in vitro, а также в жидкостях организма или в искусственных жидкостях организма, более предпочтительно в жидкостях желудочно-кишечного тракта. В настоящем изобретении термин "пролонгированное" высвобождение следует понимать, как такое, при котором, в отличие от немедленного высвобождения, активный ингредиент высвобождается постепенно, непрерывно во времени, иногда медленнее или быстрее, в зависимости или независимо от значения рН. В частности, термин указывает, что вся доза активного ингредиента не высвобождается из композиции сразу после перорального введения и что композиция позволяет уменьшить частоту введения, и далее термин "пролонгированное" высвобождение используется, как эквивалентный термину"медленное" высвобождение. Дозированная форма медленного или пролонгированного высвобождения,использующаяся как эквивалентная форма длительного, замедленного или модифицированного высвобождения, является дозированной формой, которая позволяет уменьшить частоту введения или значительно улучшить соблюдение пациентом режима лечения или терапевтические характеристики по сравнению с обеспечиваемыми обычной дозированной формой (например, в виде раствора или обычной твердой дозированной формы немедленного высвобождения лекарственного средства). Таблетки пролонгированного высвобождения, предлагаемые в настоящем изобретении, содержат набухающую и частично разрушающуюся полимерную матрицу, что приводит к высвобождению in vitro,которое описывается зависимостью в диапазоне от пропорциональной квадратному корню из времени до экспоненциальной, причем высвобождение является (немного) более быстрым в искусственном желудочном соке, обладающем рН 4,5, но не зависит от значения рН в диапазоне от 4,5 до 7,5. Более быстрое высвобождение в искусственном желудочном соке и более медленное высвобождение в кишечном соке может быть предпочтительным в случаях, когда необходимо, чтобы с помощью дозированной формы вводилась увеличенная доза, тогда как в основном не зависящий от значения рН профиль высвобождения может быть предпочтительным для уменьшения опасности резкого увеличения дозы и влияния пищи.-3 016850 Набухающий в воде полимер, содержащийся в композициях таблетки, предлагаемой в настоящем изобретении, представляет собой, по меньшей мере, предварительно желатинизированный крахмал в качестве одного гидрофильного набухающего в воде полимера, образующий матрицу пролонгированного высвобождения, из которой в качестве активного ингредиента медленно высвобождается прамипексол или его соль. Полимер набухает после введения вследствие взаимодействия с содержащей воду жидкостью, что приводит к образованию вязкого гелевого слоя, регулирующего высвобождение лекарственного средства. Примерами таких полимеров, содержащихся в композиции, предлагаемой в настоящем изобретении, в дополнение к предварительно желатинизированному крахмалу, являются набухающие в воде в основном нейтральные полимеры и набухающие в воде анионогенные полимеры. Выражение "набухающие в воде в основном нейтральные полимеры" при использовании в настоящем изобретении включает алкилцеллюлозы, такие как метилцеллюлозу; гидроксиалкилцеллюлозы, например гидроксиметилцеллюлозу, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу и гидроксибутилцеллюлозу; гидроксиалкилалкилцеллюлозы, такие как гидроксиэтилметилцеллюлозу и гидроксипропилметилцеллюлозу; сложные эфиры карбоксиалкилцеллюлозы; другие натуральные, полусинтетические и синтетические ди-, олиго- и полисахариды, такие как галактоманнаны, трагакантовую камедь,агар, гуаровую камедь и полифруктаны; метакрилатные сополимеры; поливиниловый спирт; поливинилпирролидон, сополимеры поливинилпирролидона с винилацетатом; комбинации поливинилового спирта с поливинилпирролидоном; полиалкиленоксиды, такие как полиэтиленоксид и полипропиленоксид, и сополимеры этиленоксида и пропиленоксида, предпочтительно простые эфиры целлюлозы, такие как гидроксипропилметилцеллюлозу и гидроксипропилцеллюлозу, наиболее предпочтительно гидроксипропилметилцеллюлозу. Выражение "набухающий в воде анионогенный полимер" при использовании в настоящем изобретении включает полимеризат акриловой кислоты, сополимеры метакриловой кислоты, альгинаты, каррагенаны, камедь акации, ксантановую камедь, производные хитина, такие как хитозан, натриевую соль кармелозы, кальциевую соль кармелозы, предпочтительно полимеризат акриловой кислоты. В продаже имеются марки гидроксипропилцеллюлозы и гидроксипропилметилцеллюлозы, обладающие различной вязкостью. Гидроксипропилметилцеллюлоза (ГПМЦ), предпочтительно применяющаяся в настоящем изобретении, обладает вязкостью, равной от примерно 3500 до примерно 100000 мПас, предпочтительно равной от примерно 4000 до примерно 20000 мПас и наиболее предпочтительно вязкостью, равной от примерно 6500 до примерно 15000 мПас (кажущаяся вязкость 2% водного раствора при 20 С), например гипромеллоза 2208 или 2206 (DOW, Antwerp, Belgium). ГПМЦ типа 2208 содержит 19-24 мас.% метоксильных и 4-12 мас.% гидроксипропоксильных заместителей. Предпочтительной является гидроксипропилцеллюлоза, обладающая вязкостью, превышающей 1500 мПас (кажущаяся вязкость 1% водного раствора при 20 С), в частности гидроксипропилцеллюлоза,обладающая вязкостью, равной от примерно 1500 до примерно 3000 мПас, предпочтительно от 4000 до 6500 мПас (2% водные растворы), например, серии Klucel, такая как Klucel M (Hercules, Wilmington,USA). Если не ограничиваться теоретическими соображениями, то можно предположить, что существуют 3 основных механизма, по которым прамипексол или его соль могут высвобождаться из гидрофильной матрицы: растворение, разрушение и диффузия. Прамипексол или его соль будут высвобождаться по механизму растворения, если он равномерно диспергирован в сетке матрицы, состоящей из растворимого полимера. Сетка будет постепенно растворяться в желудочно-кишечном тракте, в результате чего будет высвобождаться ее содержимое. Матричный полимер также может постепенно разрушаться на поверхности матрицы, что также приведет к постепенному высвобождению прамипексола или его соли. Если прамипексол включен в матрицу, состоящую из нерастворимого полимера, то он будет высвобождаться путем диффузии: желудочно-кишечные жидкости проникают в нерастворимую губчатую матрицу и диффундируют обратно вместе с содержащимся в них лекарственным средством. Поэтому набухающие в воде полимеры, образующие матрицу, в основном обеспечивают регулируемый фармакокинетический профиль высвобождения препарата. Путем изменения количества набухающих в воде полимеров, включаемых в препарат, можно регулировать профиль высвобождения, т.е. более значительные количества набухающих полимеров приводят к более заметному замедлению высвобождения, и наоборот предпочтительно, если количество набухающих в воде полимеров в композиции,предлагаемой в настоящем изобретении, составляет от примерно 30 до примерно 99 мас.%. Кроме того, при использовании комбинации полимеров соотношение количеств указанных полимеров также влияет на профиль высвобождения препарата. Комбинирование разных полимеров дает возможность комбинировать разные механизмы, по которым прамипексол высвобождается из матрицы. Такое комбинирование облегчает проведение необходимой регулировки профиля высвобождения препарата. Например, при использовании набухающих в воде полимеров, предпочтительно гидроксипропилцеллюлозы и гидроксипропилметилцеллюлозы, массовое содержание гидроксипропилметилцеллюлозы предпочтительно составляет от 25 до примерно 62%; массовое содержание гидроксипропилцеллюлозы-4 016850 предпочтительно составляет от 0 до примерно 16%. Высвобождение прамипексола или его соли из матрицы, содержащей гидроксипропилцеллюлозу и гидроксипропилметилцеллюлозу, происходит посредством объединенного набора механизмов высвобождения. Вследствие более высокой растворимости гидроксипропилметилцеллюлозы по сравнению с гидроксипропилцеллюлозой первая будет постепенно растворяться и отделяться от матрицы, тогда как вторая в основном будет выступать в качестве губчатого образующего матрицу вещества, из которого активный ингредиент высвобождается преимущественно путем диффузии. Характеристики композиции таблетки пролонгированного высвобождения не зависят от рН. Поэтому исключается такой недостаток, как возможное увеличение концентрации, связанное с приемом пищи. Связанное с пищей увеличение концентрации у сытых пациентов можно объяснить множеством факторов, таких как механическое воздействие желудка на свое содержимое и тем самым на введенный препарат, а также разными значениями рН в разных отделах желудочно-кишечного тракта. Поскольку значения рН в желудочно-кишечном тракте меняются не только при переходе от одного отдела к другому, но и при приеме пищи, композиция пролонгированного высвобождения предпочтительно также должна обеспечивать профиль пролонгированного высвобождения, предпочтительно такой, чтобы избежать резкого увеличения концентрации независимо от того, находится ли пациент в состоянии натощак или в сытом состоянии. Кроме прамипексола или его соли и набухающих в воде полимеров, композиция, предлагаемая в настоящем изобретении, также необязательно может включать другие инертные наполнители, т.е. фармацевтически приемлемые вспомогательные агенты, облегчающие изготовление, улучшающие прессуемость, внешний вид и вкус препарата. Эти вспомогательные агенты, например, включают разбавители или наполнители, агенты, придающие скользкость, связывающие агенты, гранулирующие агенты, агенты, препятствующие слеживанию, смазывающие агенты, вкусовые добавки, красители и консерванты. Также можно включать другие обычные инертные наполнители, известные в данной области техники. Наполнитель можно выбрать из группы, включающей растворимые наполнители, например сахарозу, лактозу, предпочтительно моногидрат лактозы, трегалозу, мальтозу, маннит и сорбит. Можно использовать разные марки лактозы. Одним типом лактозы, предпочтительно применяющемся в настоящем изобретении, является моногидрат лактозы 200 меш (DMV, Veghel, The Netherlands). Также предпочтительно можно использовать другой моногидрат лактозы, моногидрат лактозы типа DCL 11 (DMV,Veghel, The Netherlands). Аббревиатура DCL обозначает "лактозу, предназначенную для прямого прессования". Число 11 является порядковым номером, установленным изготовителем. В случае растворимого в воде активного ингредиента, такого как описанный в настоящем изобретении, в дополнение к растворимым в воде наполнителям или вместо них более предпочтительно использовать нерастворимые в воде наполнители, такие как крахмал и производные крахмала, не являющиеся предварительно желатинизированным крахмалом, например кукурузный крахмал, картофельный крахмал, рисовый крахмал или пшеничный крахмал, микрокристаллическую целлюлозу, дигидрат гидрофосфата кальция и безводный гидрофосфат кальция, предпочтительно кукурузный крахмал. Полное массовое содержание наполнителя составляет от примерно 5 до примерно 75 мас.%. Агент, придающий скользкость, можно использовать для улучшения сыпучести порошка до и во время таблетирования и для уменьшения слеживания. Подходящие агенты, придающие скользкость,включают коллоидный диоксид кремния, трисиликат магния, порошкообразную целлюлозу, тальк, тризамещенный фосфат кальция и т.п. В качестве агента, придающего скользкость, предпочтительно включать коллоидный диоксид кремния в количестве примерно до 2%, предпочтительно от примерно 0,2 до примерно 0,8% в пересчете на массу таблетки. Смазывающий агент можно использовать для улучшения отделения таблетки от аппарата, в котором ее изготавливают, например, путем предотвращения ее прилипания к верхней или нижней части пресс-формы. Подходящие смазывающие агенты включают стеарат магния, стеарат кальция, масло канолы, глицерилпальмитостеарат, гидрированное растительное масло, оксид магния, минеральное масло,полоксамер, полиэтиленгликоль, поливиниловый спирт, бензоат натрия, лаурилсульфат натрия, стеарилфумарат натрия, стеариновую кислоту, тальк, гидрированное растительное масло, стеарат цинка и т.п. В одном варианте осуществления стеарат магния включают в качестве смазывающего вещества в количестве от примерно 0,1 до примерно 1,5%, предпочтительно от примерно 0,3 до примерно 1% в пересчете на массу таблетки. Из числа необязательных вспомогательных агентов, которые дополнительно можно включать в состав матрицы, можно отметить такие агенты, как повидон; коповидон; крахмал; камедь акации; желатин; вещества, выделенные из морских водорослей, например альгиновую кислоту, альгинат натрия и кальция; целлюлозу, предпочтительно микрокристаллическую целлюлозу, производные целлюлозы, например этилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, обладающие полезными связывающей в сухом или влажном состоянии и гранулирующей способностью; и агенты, препятствующие слипанию, такие как тальк и стеарат магния. В случае композиции, предлагаемой в настоящем изобретении, обеспечивается зависящий от рН профиль высвобождения и высвобождение прамипексола или его соли из таблетки и последующее вса-5 016850 сывание в кровоток может меняться при прохождении дозированной формы по желудочно-кишечному тракту. Таким образом, обеспечивается зависящее от рН высвобождение, такое что высвобождение в диапазоне рН 4,5 является более быстрым, а в диапазоне 4,5 рН 7,5 оно медленнее и не зависит от рН. Кроме того, набухающий в воде анионогенный полимер, предпочтительно полимеризат акриловой кислоты, обязательно содержится в композиции и он предпочтительно выбран из групп карбомеров или карбополов, известных полимеризатов акриловой кислоты, обладающих большими молекулярными массами. Особенно предпочтительными являются, например, Карбомер 941 (Карбопол 71 G, Карбопол 971) и Карбомер 934 (Карбопол 974). Полимеризат акриловой кислоты предпочтительно содержится в количестве, равном от 0,25 до 25 мас.%, более предпочтительно от 0,5 до 15 мас.%, наиболее предпочтительно от 1 до 10 мас.%. Зависимость от рН для композиции обусловлена наличием полимеризата акриловой кислоты, который в кислой среде при значениях рН, превышающих 4,5, набухает в большей степени, чем в щелочной среде. Увеличение содержания акриловой кислоты приводит к уменьшению скорости высвобождения. Поэтому регулирование содержания полимеризата акриловой кислоты делает возможным дополнительное регулирование профилей растворения в соответствии с необходимостью. Регулирование содержания полимеризата акриловой кислоты в предпочтительном диапазоне, составляющем от 0,25 до 25 мас.%, обеспечивает то преимущество, что необходимые или подобранные профили растворения может установить или поддерживать для самых различных композиций, содержащих разные количества и/или типы гелеобразующих агентов, набухающих в воде полимеров, наполнителей и сухих связующих. В предпочтительном варианте осуществления настоящего изобретения матрица композиции таблетки пролонгированного высвобождения содержит предварительно желатинизированный крахмал, гидроксипропилметилцеллюлозу, полимеризат акриловой кислоты и инертные наполнители или в основном состоит из них. Количество предварительно желатинизированного крахмала предпочтительно находится в диапазоне от 10 до 75%, более предпочтительно от 25 до 65%, наиболее предпочтительно от 45 до 55 мас.%. Количество гидроксипропилметилцеллюлозы предпочтительно находится в диапазоне от 10 до 75%, более предпочтительно от 25 до 65%, наиболее предпочтительно от 35 до 55 мас.%. Количество полимеризата акриловой кислоты предпочтительно является таким, как указано выше. Количество инертных наполнителей предпочтительно находится в диапазоне от 0 до 30%, более предпочтительно от 0,5 до 20%, наиболее предпочтительно от 1 до 10 мас.%. Необязательная натриевая соль карбоксиметилцеллюлозы может дополнительно содержаться предпочтительно в диапазоне от 5 до 50%, более предпочтительно от 10 до 40%, наиболее предпочтительно от 15 до 30 мас.%. В качестве активного ингредиента прамипексол или его фармацевтически приемлемая соль могут содержаться в композиции, предлагаемой в настоящем изобретении, в количестве, пригодном для требуемого лечения пациента. Предпочтительной солью прамипексола является дигидрохлорид наиболее предпочтительно в форме моногидрата. Обычные количества составляют от примерно 0,1 до примерно 5 мг соли прамипексола. В особенно предпочтительном варианте осуществления в композиции таблетки пролонгированного высвобождения, предлагаемой в настоящем изобретении, используют, например,0,750 мг моногидрата дигидрохлорида прамипексола, что соответствует 0,524 мг безводного свободного основания. Однако можно использовать любое другое количество активного ингредиента, пригодное для лечения, при единственном условии, чтобы количество прамипексола или его соли было достаточным для одновременного введения суточной дозы с помощью одной или нескольких небольших препаративных форм, например от 1 до примерно 4 таблеток. Предпочтительно, чтобы полная суточная доза вводилась с помощью одной таблетки. Обычно будет подходящим количество соли прамипексола, которое в пересчете на эквивалентное количество моногидрата дигидрохлорида прамипексола равно от примерно 0,1 до примерно 10 мг на таблетку или от примерно 0,05 до примерно 5% в пересчете на массу композиции. Предпочтительно, если содержится количество, равное от примерно 0,2 до примерно 6 мг, более предпочтительно количество, равное от примерно 0,3 до примерно 5 мг на таблетку. Конкретные дозы,содержащиеся в одной таблетке, например, составляют 0,375, 0,5, 0,75, 1,0, 1,5, 3,0 и 4,5 мг моногидрата дигидрохлорида прамипексола. Количество, образующее терапевтически эффективное количество, меняется в зависимости от подвергающегося лечению патологического состояния, тяжести указанного состояния и конкретного пациента, подвергающегося лечению. Композиция таблетки пролонгированного высвобождения, предлагаемая в настоящем изобретении,предпочтительно обладает следующим составом: Соответственно особенно предпочтительная композиция таблетки пролонгированного высвобождения, предлагаемая в настоящем изобретении, включает от 0,1 до 2 мас.% прамипексола или его соли; от 25 до 65 мас.% гидроксипропилметилцеллюлозы; от 0 до 40 мас.% натриевой соли карбоксиметилцеллюлозы; от 25 до 75 мас.% предварительно желатинизированного крахмала; от 0 до 15 мас.% акрилового полимеризата, предпочтительно карбомера 941; от 0,5 до 50 мас.% инертных наполнителей, предпочтительно выбранных из группы, включающей коллоидный диоксид кремния, стеарат магния, моногидрат лактозы, маннит, микрокристаллическую целлюлозу, безводный гидрофосфат кальция, гидроксипропилцеллюлозу, повидон, коповидон, тальк, макроголы, додецилсульфат натрия, оксиды железа и диоксид титана. Крахмал, обладающий прочностью на разрыв, равной не менее примерно 0,15 кНсм-2, при доле твердого вещества, типичной для таблетки, заявленной в WO 2004/010997, не требуется в контексте настоящего изобретения. Особенно предпочтительно, чтобы композиция таблетки, предлагаемой в настоящем изобретении,не содержала покрытия. Однако таблетка пролонгированного высвобождения, предлагаемая в настоящем изобретении, может содержать нефункциональное покрытие. Нефункциональное покрытие может включать полимерный компонент, например ГПМЦ, необязательно вместе с другими ингредиентами, например с одним или большим количеством пластификаторов, красителей и т.п. Термин "нефункциональное" в контексте настоящего изобретения означает, что покрытие не оказывает существенного влияния на параметры высвобождения таблетки, а предназначено для другой полезной цели. Например, такое покрытие может придать таблетке заметный внешний вид, обеспечить защиту от истирания во время упаковки и транспортировки, сделать более легким проглатывание и/или обладать другими полезными свойствами. Нефункциональное покрытие следует наносить в количестве, достаточном для того, чтобы закрыть всю таблетку. Обычно подходящим является количество, равное от примерно 1 до примерно 10%, более предпочтительно от примерно 2 до примерно 5% в пересчете на массу таблетки в целом. Таблетки, предлагаемые в настоящем изобретении, могут обладать любым подходящим размером и формой, например круглой, овальной, многогранной или подушкообразной, и необязательно содержать маркировку нефункциональной поверхности. В контексте настоящего изобретения предпочтительно,чтобы таблетки пролонгированного высвобождения были белыми или почти белыми и обладали овальной или круглой двояковыпуклой формой. Таблетки, предлагаемые в настоящем изобретении, можно упаковать в контейнер с приложением листка-вкладыша с соответствующей информацией, такой как, например, информация о дозировке и введении, противопоказаниях, мерах предосторожности, лекарственных взаимодействиях и побочных эффектах. Настоящее изобретение также относится к применению композиции таблетки пролонгированного высвобождения, предлагаемой в настоящем изобретении, для изготовления лекарственной композиции,предназначенной для лечения болезни Паркинсона и сопутствующих ей осложнений или нарушений. Кроме того, настоящее изобретение предпочтительно относится к способу изготовления композиций таблетки пролонгированного высвобождения с помощью технологии прямого прессования, включающему стадии:(1) получения порошка активного ингредиента, в котором активным ингредиентом является прамипексол или его фармацевтически приемлемая соль, путем его предварительного смешивания с частью набухающих в воде полимеров и другим инертным наполнителем (наполнителями) в смесителе, причем перед использованием прамипексол или его фармацевтически приемлемую соль размалывают, предпочтительно размалывают на штифтовой мельнице;(2) предварительного перемешивания порошка активного ингредиента, полученного на стадии (1),основной части набухающих в воде полимеров и инертных наполнителей в смесителе с получением предварительной смеси;(3) необязательно сухого просеивания предварительной смеси через сито для отделения слипшихся частиц и улучшения однородности смеси;(4) перемешивания предварительной смеси, полученной на стадии (2) или (3), в смесителе, необязательно с прибавлением оставшихся инертных наполнителей к смеси и продолжения перемешивания;(5) таблетирования готовой смеси путем ее прессования на подходящем таблеточном прессе с по-7 016850 лучением матричных таблеток. Таким образом, таблетки изготавливают способом прямого прессования, который применяют для матричных таблеток прамипексола с пролонгированным высвобождением. Для обеспечения достаточной однородности смеси в случае композиции, обладающей таким небольшим содержанием лекарственного вещества, активный ингредиент предпочтительно размалывать на штифтовой мельнице. Предпочтительно, чтобы распределение по размерам частиц размолотого на штифтовой мельнице лекарственного вещества, определенное с помощью лазерной дифрактометрии с использованием сухого дозатора, было таким, чтобы диаметр 90% (об./об.) частиц составлял менее 100 мкм, наиболее предпочтительно, чтобы диаметр 90% (об./об.) частиц составлял менее 75 мкм. Для изготовления таблеток прамипексола пролонгированного высвобождения можно использовать и другие технологии, такие как обычное мокрое гранулирование и вальцовое прессование. В случае мокрого гранулирования прамипексол предпочтительно гранулировать вместе с подходящими наполнителями, такими как, например, крахмал, микрокристаллическая целлюлоза, моногидрат лактозы или безводный гидрофосфат кальция, и связующими для мокрого гранулирования, такими как, например, гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза, повидон, коповидон и крахмальная паста, с получением концентрата активного ингредиента, который после сушки и сухого просеивания смешивают с основной частью гелеобразующих инертных наполнителей, таких как все описанные выше замедляющие высвобождение вещества. В случае вальцового прессования или, другими словами, сухого гранулирования предварительную смесь прамипексола с частью инертных наполнителей, используемых в технологии прямого прессования,или полную смесь, содержащую все инертные наполнители, обрабатывают с помощью обычного вальцового пресса с получением лент, которые затем измельчают в гранулы, которые в заключение смешивают с другими инертными наполнителями, такими как агенты, придающие скользкость, смазывающие агенты и агенты, препятствующие слипанию. Краткое описание чертежей На фиг. 1 приведена блок-схема, иллюстрирующая предпочтительный вариант осуществления способа изготовления прямым прессованием, предлагаемого в настоящем изобретении; на фиг. 2 представлена диаграмма, иллюстрирующая профили растворения композиции матричной таблетки, предлагаемой в настоящем изобретении, которая содержит 4 мас.% Карбопола, в средах с 3 разными значениями рН; на фиг. 3 представлена диаграмма, иллюстрирующая профили растворения 3 композиций матричной таблетки, предлагаемой в настоящем изобретении, которые содержат 0, 1 и 4 мас.% Карбопола соответственно. Фиг. 1 иллюстрирует предпочтительный вариант осуществления способа изготовления с помощью блок-схемы, на которой в качестве примера представлено изготовление таблеток пролонгированного высвобождения, описанных в примерах 1 и 2. На фиг. 1 подробно описаны стадии способа и проверяемые во время его проведения характеристики. Стадия (1) способа относится к получению порошка активного ингредиента, т.е. в данном случае соль прамипексола, моногидрат дигидрохлорида прамипексола, размолотую на штифтовой мельнице,предварительно смешивают с частью набухающего в воде полимера, в данном случае предварительно желатинизированного крахмала, в обычном смесителе. На блок-схеме используют смеситель или мешалку свободного падения Turbula. Смешивание продолжается несколько минут, в данном случае предпочтительно 10 мин. На стадии (2) способа в соответствии с блок-схемой проводят предварительное перемешивание, при котором порошок активного ингредиента и основную часть набухающего в воде полимера (полимеров) и инертных наполнителей предварительно перемешивают в течение нескольких минут с получением предварительной смеси. В данном случае основную часть гидроксипропилметилцеллюлозы (гипромеллозы),предварительно желатинизированного крахмала, карбомера 941 и коллоидного диоксида кремния предварительно перемешивают в течение 5 мин в указанном выше смесителе или мешалке Turbula. На следующей стадии (3) способа необязательно можно провести сухое просеивание. Предварительную смесь можно просеять вручную через сито, например, с размером ячеек, равным 0,8 мм, для отделения слипшихся частиц и улучшения однородности смеси. На следующей стадии (4) способа выполняют стадию основного перемешивания, на которой компоненты после просеивания перемешивают несколько минут, предпочтительно 5 мин в смесителе Turbula. В это время необязательно можно прибавить другие инертные наполнители, на блок-схеме к основной смеси прибавляют стеарат магния и перемешивают еще несколько минут, например 3 мин, в смесителе Turbula (заключительное перемешивание) и получают готовую смесь. Стадией (5) способа, предлагаемого в настоящем изобретении, является таблетирование. Готовую смесь прессуют на подходящем таблеточном прессе с получением, например, матричных таблеток удлиненной формы (таблеток ПВ = таблеток пролонгированного высвобождения). Для проверки и поддержания необходимого качества у полученных матричных таблеток проверяют следующие характеристики: массу таблетки, твердость, толщину и ломкость таблетки.-8 016850 Затем полученные таблетки прамипексола пролонгированного высвобождения, предлагаемые в настоящем изобретении, можно расфасовать, например, во флаконы, изготовленные из полиэтилена высокой плотности (ПЭВП). Флаконы плотно закрывают винтовыми крышками и соответствующим образом маркируют, причем все операции упаковки и маркировки проводят в соответствии с действующими нормами GMP (Надлежащей производственной практики). Альтернативно, можно использовать упаковку блистерного типа, например блистеры типа алюминий/алюминиевая фольга. На фиг. 2 представлена диаграмма, иллюстрирующая профили растворения композиции матричной таблетки, предлагаемой в настоящем изобретении. Матричная таблетка содержит 4 мас.% карбопола,состав подробно описан в примере 2. Приведены характеристики высвобождения матричной таблетки в средах с 3 разными значениями рН, т.е. в 0,05 М фосфатном буфере, рН 6,8, n = х, в искусственном желудочном соке, рН 1,2, n = х, и в буфере McIlvaine, рН 4,5, n = х (х обозначает количество исследованных образцов). Приведена зависимость выраженного в процентах количества высвободившегося активного ингредиента от времени (ч). На фиг. 3 представлена диаграмма, иллюстрирующая профили растворения 3 композиций матричной таблетки, предлагаемых в настоящем изобретении. Матричная таблетка не содержит карбопола или содержит 1 или 4 мас.% карбопола соответственно, составы подробно описаны в примерах 1, 2 и 4. Средой является 0,05 М фосфатный буфер, рН 6,8. Приведена зависимость выраженного в процентах количества высвободившегося активного ингредиента от времени (ч). На фиг. 2 и 3 приведены не зависящие от рН характеристики высвобождения in vitro для диапазона значений рН от 1 до 7,5 в случае отсутствия Карбопола и зависящие от рН характеристики высвобождения, когда в диапазоне рН 4,5 в случае присутствия Карбопола высвобождение является более быстрым. Увеличение количества Карбопола приводит к уменьшению скорости высвобождения. Настоящее изобретение обладает целым рядом преимуществ. Настоящее изобретение относится к таблеткам пролонгированного высвобождения, содержащим прамипексол или его соль, которые обладают разными профилями высвобождения in vitro. Можно специально подобрать характеристики высвобождения в соответствии с потребностями пациента, симптомами и наблюдающейся клинической картиной. Основное показание для применения прамипексола, болезнь Паркинсона, является заболеванием,которое чаще встречается в пожилом возрасте и часто сопровождается ухудшением памяти. Поэтому матричные таблетки, предлагаемые в настоящем изобретении, обеспечивающие пролонгированное или медленное высвобождение прамипексола или его соли, позволяют упростить схему введения пациентам путем уменьшения количества рекомендованных приемов в сутки и улучшить соблюдение режима лечения пациентами, в особенности пожилыми пациентами. Предлагаемая в настоящем изобретении композиция таблетки пролонгированного высвобождения обеспечивает суточную дозу и ее предпочтительно вводить сразу. Кроме того, таблетки, предлагаемые в настоящем изобретении, можно изготовить способами прямого прессования, мокрого или сухого гранулирования, что относится к матричным таблеткам пролонгированного высвобождения обоих типов. Описанное изобретение будет проиллюстрировано с помощью приведенных ниже примеров, и из настоящего описания для специалиста в данной области техники должны быть очевидны различные другие варианты осуществления. Однако специально отмечается, что примеры и описание предназначены только для иллюстрации и их не следует рассматривать в качестве ограничивающих настоящее изобретение. Примеры В соответствии с настоящим изобретением изготовлены таблетки прамипексола пролонгированного высвобождения. Полученные в примерах таблетки представляют собой удлиненные двояковыпуклые таблетки 146,8 мм, цветом от белого до почти белого. Таблетки предназначены для перорального введения и их не следует разделять пополам. В этих примерах таблетки прамипексола содержат 0,75 мг моногидрата дигидрохлорида прамипексола, что соответствует 0,524 мг безводного свободного основания прамипексола. Пример 1. Качественный и количественный состав для одного варианта осуществления таблеток прамипексола пролонгированного высвобождения, предлагаемых в настоящем изобретении, приведен в табл. 1.-9 016850 Таблица 1 Качественный и количественный состав таблетки прамипексола пролонгированного высвобождения Пример 2. Качественный и количественный состав для другого варианта осуществления таблеток прамипексола пролонгированного высвобождения, предлагаемых в настоящем изобретении, приведен в табл. 2. Таблица 2 Качественный и количественный состав таблетки прамипексола пролонгированного высвобождения Пример 3. Составы партий для двух композиций таблеток прамипексола примеров 1 и 2 приведены в табл. 3. Масса конечной смеси в партии соответствует 2000 таблеткам.- 10016850 Таблица 3 Составы партий для ПВ таблеток прамипексола 0,75 мг ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Композиция таблетки пролонгированного высвобождения, содержащая прамипексол или его фармацевтически приемлемую соль в матрице, включающей по меньшей мере три набухающих в воде полимера, один из указанных полимеров представляет собой предварительно желатинизированный крахмал, второй полимер представляет собой анионогенный полимер, являющийся сшитым полимером акриловой кислоты, и третий полимер выбран из гидроксипропилцеллюлозы и гидроксипропилметилцеллюлозы. 2. Композиция таблетки пролонгированного высвобождения по п.1, в которой анионогенный полимер представляет собой сшитый полимер акриловой кислоты, причем содержание сшитого полимера акриловой кислоты в матрице равно от 0,25 до 25 мас.%, предпочтительно от 0,5 до 15 мас.% и более предпочтительно от 1 до 10 мас.%. 3. Композиция таблетки пролонгированного высвобождения по п.2, в которой набухающий в воде третий полимер представляет собой гидроксипропилметилцеллюлозу, причем содержание гидроксипропилметилцеллюлозы в матрице равно от 10 до 75 мас.% и предпочтительно от 25 до 65 мас.%. 4. Композиция таблетки пролонгированного высвобождения по п.1, в которой матрица включает: 5. Композиция таблетки пролонгированного высвобождения по п.1, в которой матрица включает 6. Композиция таблетки пролонгированного высвобождения по п.1, в которой матрица включает от 0,1 до 2 мас.% прамипексола или его соли; от 25 до 65 мас.% гидроксипропилметилцеллюлозы; от 0 до 40 мас.% натриевой соли карбоксиметилцеллюлозы; от 25 до 75 мас.% предварительно желатинизированного крахмала; от 0 до 15 мас.% акрилового полимеризата, предпочтительно карбомера 941; от 0,5 до 50 мас.% других инертных наполнителей, предпочтительно выбранных из группы, включающей коллоидный диоксид кремния, стеарат магния, моногидрат лактозы, маннит, микрокристаллическую целлюлозу, безводный гидрофосфат кальция, гидроксипропилцеллюлозу, повидон, коповидон,тальк, макроголы, додецилсульфат натрия, оксиды железа и диоксид титана. 7. Композиция таблетки пролонгированного высвобождения по п.1, где полученная таблетка обеспечивает зависящее от рН высвобождение с более быстрым высвобождением в диапазоне рН 4,5 и с более медленным и не зависящим от рН высвобождением в диапазоне рН 4,5-7,5. 8. Композиция таблетки пролонгированного высвобождения по п.7, в которой матрица включает гидроксипропилметилцеллюлозу в количестве от 10 до 75%, предпочтительно от 25 до 65 мас.% и- 11016850 инертные наполнители в количестве от 25 до 90%, предпочтительно от 35 до 75 мас.%. 9. Композиция таблетки пролонгированного высвобождения по любому предыдущему пункту, в которой анионогенный полимер представляет собой полимеризат акриловой кислоты, который выбран из групп карбомеров или Карбополов. 10. Композиция таблетки пролонгированного высвобождения по п.9, содержащая от 0,25 до 25 мас.%, предпочтительно от 0,5 до 15 мас.%, наиболее предпочтительно от 1 до 10 мас.% полимеризата акриловой кислоты. 11. Композиция таблетки пролонгированного высвобождения по любому предыдущему пункту, содержание прамипексола или его фармацевтически приемлемой соли в которой достаточно для обеспечения суточной дозы, вводимой за один раз. 12. Способ изготовления композиции таблетки пролонгированного высвобождения по одному из предыдущих пунктов методом прямого прессования, включающий стадии:(1) получения порошка активного ингредиента, в котором активным ингредиентом является прамипексол или его фармацевтически приемлемая соль, путем его предварительного смешивания с частью набухающих в воде полимеров и другим инертным наполнителем (наполнителями) в смесителе, причем перед использованием прамипексол или его фармацевтически приемлемую соль размалывают, предпочтительно размалывают на штифтовой мельнице;(2) предварительного перемешивания порошка активного ингредиента, полученного на стадии (1),основной части набухающего в воде полимера (полимеров) и инертных наполнителей в смесителе с получением предварительной смеси;(3) необязательно сухого просеивания предварительной смеси через сито для отделения слипшихся частиц и улучшения однородности смеси;(4) перемешивания предварительной смеси, полученной на стадии (2) или (3), в смесителе, необязательно с прибавлением оставшихся инертных наполнителей к смеси и продолжения перемешивания;(5) таблетирования готовой смеси путем ее прессования на подходящем таблеточном прессе с получением матричных таблеток. 13. Способ изготовления композиции таблетки пролонгированного высвобождения по любому из предыдущих пп.1-11 методом мокрого гранулирования, включающий стадии:(1) получения порошка активного ингредиента, в котором активным ингредиентом является прамипексол или его фармацевтически приемлемая соль, путем его смешивания с частью инертных наполнителей в смесителе, причем перед использованием прамипексол или его фармацевтически приемлемую соль размалывают, предпочтительно размалывают на штифтовой мельнице;(2) гранулирования порошка активного ингредиента, полученного на стадии (1), путем прибавления гранулирующей жидкости, предпочтительно воды;(3) сушки гранул, полученных на стадии (2), в сушилке с псевдоожиженным слоем или в сушильной камере;(4) смешивания высушенных гранул, полученных на стадии (3), с набухающими в воде полимерами и инертными наполнителями в смесителе с получением готовой смеси;(5) таблетирования готовой смеси, полученной на стадии (4), путем ее прессования на подходящем таблеточном прессе с получением матричных таблеток. 14. Способ изготовления композиции таблетки пролонгированного высвобождения по любому из предыдущих пп.1-11 методом сухого гранулирования, включающий стадии:(1) смешивания активного ингредиента прамипексола или его фармацевтически приемлемой соли с частью наполнителей или со всеми инертными наполнителями в смесителе, причем перед использованием прамипексол или его фармацевтически приемлемую соль размалывают, предпочтительно размалывают на штифтовой мельнице;(2) прессования смеси, полученной на стадии (1), на подходящем вальцовом прессе;(3) измельчения лент, полученных на стадии (1), в небольшие гранулы с помощью подходящих стадий размола или просеивания;(4) необязательного смешивания гранул, полученных на стадии (3), в смесителе с оставшимися инертными наполнителями с получением готовой смеси;(5) таблетирования гранул, полученных на стадии (3), или готовой смеси, полученной на стадии (4),путем ее прессования на подходящем таблеточном прессе с получением матричных таблеток. 15. Применение композиции таблетки пролонгированного высвобождения по одному из предыдущих пп.1-11 для изготовления лекарственной композиции, предназначенной для лечения болезни Паркинсона и сопутствующих ей осложнений или нарушений.
МПК / Метки
МПК: A61P 25/16, A61K 9/20, A61K 9/28
Метки: высвобождения, изготовления, таблетки, содержащая, прамипексол, пролонгированного, фармацевтически, применение, способ, приемлемую, соль, композиция
Код ссылки
<a href="https://eas.patents.su/14-16850-kompoziciya-tabletki-prolongirovannogo-vysvobozhdeniya-soderzhashhaya-pramipeksol-ili-ego-farmacevticheski-priemlemuyu-sol-sposob-ee-izgotovleniya-i-ee-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Композиция таблетки пролонгированного высвобождения, содержащая прамипексол или его фармацевтически приемлемую соль, способ ее изготовления и ее применение</a>
Предыдущий патент: Синергическая гербицидная комбинация кломазона и петоксамида
Следующий патент: Способ и средства для лечения воспалительного заболевания кишечника
Случайный патент: Распадающиеся загружаемые таблетки