Чистые изомеры d-(17α)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-3е и 3z-оксимов, способ синтеза смеси изомеров и чистых изомеров
Номер патента: 8174
Опубликовано: 27.04.2007
Авторы: Туба Золтан, Хорват Янош, Кешеру Дьёрдь, Балог Габор, Махо Шандор, Козма Йожеф
Формула / Реферат
1. Фармацевтическая композиция в виде пластыря, содержащая чистый d-(17a)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Е)-оксим формулы (IA)
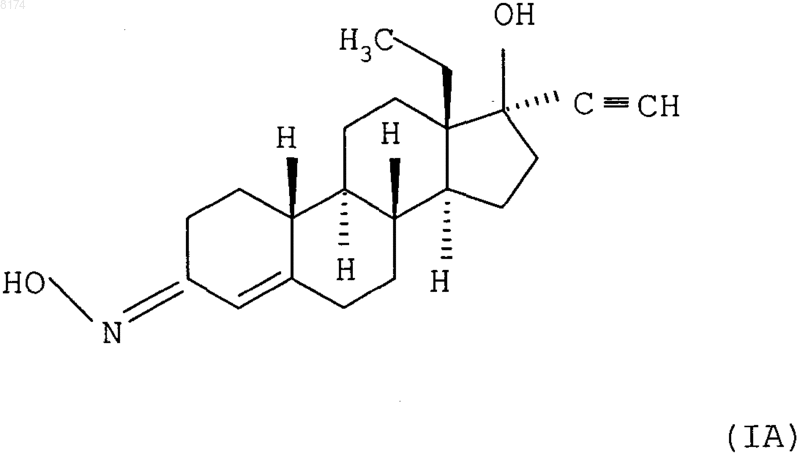
в качестве активного ингредиента - гестагена.
2. Перорально применяемая фармацевтическая композиция, содержащая чистый d-(17a)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Z)-оксим формулы (IB)
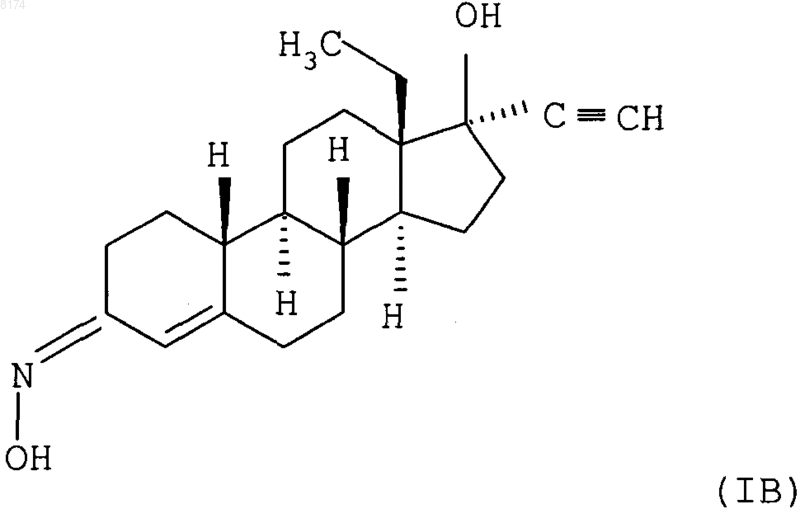
в качестве активного ингредиента - гестагена.
3. Способ синтеза E/Z-изомерной смеси норегестромина а также чистого d-(17a)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Е)-оксима формулы (IA) и чистого d-(17a)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Z)-оксима формулы (IB), включающий следующее:
а) реакцию 1 моля d-норгестрела с 1,2-5 мол.экв. ацетата гидроксиламмония или солью гидроксиламмония и ацетатом щелочного металла в количестве не более чем 1 экв. последней в уксусной кислоте, содержащей не более чем 50 маc.% воды, при 15-50шС в течение 15-45 мин, полученную реакционную смесь, содержащую смесь изомеров норелгестромина,
a) разбавляют приблизительно 10-кратным объемом воды и выпавшую в осадок смесь изомеров выделяют с получением смеси E/Z изомеров в соотношении около 56:44-64:36, или же в данном случае
b) после добавления около 10-25 об.% воды ее перемешивают при 10-30ш в течение 24-72 ч, в данном случае добавляют воду к реакционной смеси и выпавший в осадок продукт выделяют с получением (3Е)-изомера оксима формулы (IA), или же в данном случае
g) после добавления около 10-кратного объема воды выпавшую в осадок смесь изомеров выделяют и перемешивают в дихлорметане, отфильтровывают нерастворимый (3Е)-изомер оксима формулы (IA), фильтрат очищают колоночной хроматографией с использованием силикагеля в качестве адсорбента и смеси неполярного-полярного растворителей в качестве элюента с получением (3Z)-оксимa формулы (IB), или
b) смесь E/Z изомеров норелгестромина в любом соотношении
a) перемешивают с ацетатом гидроксиламмония или солью гидроксиламмония и ацетатом щелочного металла в количестве не более 1 экв. последней в уксусной кислоте, содержащей не более 50 мас.% воды, при 15-30шС в течение 24-72 ч и в данном случае после добавления дополнительного количества воды продукт выделяют с получением (3Е)-изомера оксима формулы (IA), или
b) перемешивают в дихлорметане, отфильтровывают нерастворимый (3Е)-изомер оксима формулы (IA), фильтрат очищают колоночной хроматографией, используя силикагель в качестве адсорбента и смесь неполярного-полярного растворителей в качестве элюента с получением (3Z)-оксима формулы (IB), или
c) гидролизуют ацетатную группу в положении 17 3Е- или 3Z-изомepa норгестимата в спиртовом растворе эквивалентым количеством гидроксида щелочного металла при 5-30шС и полученный таким образом продукт, имеющий такую же конфигурацию, как и исходный, выделяют с получением (3Е)-изомера оксима формулы (IA) или (3Z)-изомера оксима формулы (IB)
и изомеры формул (IA) и (IB), полученные в соответствии со способами а)-с), очищают кристаллизацией.
4. Способ с) по п.3, характеризующийся тем, что гидролиз проводят с гидроксидом лития в метаноле.
Текст
008174 Область техники, к которой относится изобретение Изобретение относится к чистому изомеру d-(17)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20 ин-3-он-3 Е-оксима формулы (IA) проявляющим гестагенную активность, а также к способу синтеза чистых изомеров или их смеси. Изобретение относится также к фармацевтическим композициям, которые содержат в качестве активного ингредиента или чистый изомер формулы (IA), или чистый изомер формулы (IB), как таковых или в сочетании с другими активными ингредиентами (например, с эстрогенным агентом) и вместе с фармацевтическими вспомогательными компонентами, обычно применяемыми на практике, и к способу их получения. Уровень техники Синтез и биологические исследования 3-оксимино-андростеновых и гоненовых производных, содержащих стерановый скелет, были начаты в 1960-ых. Применение производных dl-(17)-13-этил-17 ацилокси-18,19-динорпрегн-4-ен-20-ин-3-он-оксима в качестве посткоитального контрацептива было предложено в патенте US 3780073. С учетом того, что очень важным является уменьшение применяемой дозы активного ингредиента в случае каждого активного ингредиента, используемого в терапии, что особенно актуально для стероидных производных, обладающих высокой биологической активностью, задачей исследования являлось получение и изучение биологического эффекта чистых оптических антиподов стероидных производных,которые ранее были описаны в литературе как рацемические смеси. Синтез d-(17)-13-этил-17-ацетокси 18,19-динорпрегн-4-ен-20-ин-3-оксима (норгестимата) описан в патенте US 4027019. Биологическое и клиническое исследование норгестимата показывает более эффективное ингибирование фертильности. Это соединение в сочетании с этинил-эстрадиолом нашло терапевтическое применение как ORTHO-CYCLEN или CILEST. Использование оптически активного изомера делает возможным применение активного ингредиента в меньшей дозе в сравнении с рацемической смесью. Дальнейшим достижением в исследовании стал синтез 17-деацетил-норгестимата (норелгестромина), а также его фармакологическое и клиническое испытание. Авторы следующих публикаций - Am. J.Obstet. Gynecol., 166, 1969-77 (1992) и Am. J. Obstet. Gynecol. 163, 2127-31, (1990) - обнаружили, что метаболитами орально применяемого норгестимата являются 17-дезацетил-норгестимат и 3-кетоноргестимат (левоноргестрел ацетат), так же, как d-норгестрел (левоноргестрел), которые, в основном, и отвечают за биологическую активность. Патент US 4906169 описывает использование норгестимата и d-норгестрела в сочетании с эстрогенным компонентом в трансдермальном пластыре. Публикация WO 96/40355 раскрывает использование дезацетил-норгестимата как одного из метаболитов норгестимата - как такового или в сочетании с эстрогенным компонентом в трансдермальном пластыре. Синтез dl- и d-(17)-13-этил-17-гидpoкси-18,19-динорпрегн-4-eн-20-ин-3-он-оксима описан в венгерском патенте 165356. Соединения описаны в качестве промежуточных в синтезе рацемического и оптически активного норгестрела, но их биологическая активность не представлена. Вышеупомянутые патенты представляют, по существу, тот же метод синтеза оксимных производных. Используют гидрохлорид гидроксиламмония в качестве реагента, пиридин в качестве растворителя и основания; стероид растворяют при нагревании на водяной бане и нагревают до завершения реакции. Продукт выделяют добавлением воды и перекристаллизовывают. Соотношение E/Z изомеров в полученных таким образом производных оксима составляет приблизительно 60:40-64:36.-1 008174 Разделение некоторых известных стероидов - среди них и норелгестромина - хроматографией под давлением описано в следующей публикации: J. Chromatogr., 392, 464-9 (1987), однако, там представлены только хроматографические параметры, без определения физико-химических характеристик выделенных изомеров оксима, которые бы доказывали их структуру. Анализ некоторых промежуточных соединений в синтезе норгестрела с помощью жидкостной хроматографии высокого разрешения и газожидкостной хроматографии описан в следующей публикации: J.Chromatogr., 191(1), 145-54, (1980). Среди вышеуказанных соединений там описаны рацемические смеси и оптически чистые производные оксимов, такие же, как описаны в венгерском патенте 165356. Но из описания не следует однозначно, исследованы ли оптически чистые или рацемические смеси стероидных оксимов. Согласно вышеуказанной публикации изомеры оксимов разделялись с помощью метода аналитической ВЭЖХ, с нормальными фазами, после чего их структуры были определены. Для определения структуры ссылаются на Наrа с сотр. [Chem. Ind. (London), 832, (1967], где син- и антиизомеры оксимов тестостерона были разделены, определены их структуры методами ЯМР и УФ-спектроскопии, при этом отмечена значительная разница в величинах молярного поглощения для двух изомеров оксима при длине волны 242 нм. Главным направлением фармацевтической промышленности является синтез структурно гомогенных и стереохимически чистых активных ингредиентов и их использование в терапии, что означает применение меньших доз активных ингредиентов, имеющих более четкий профиль биологической активности и, следовательно, более слабые побочные эффекты. Раскрытие изобретения Предпринятая попытка привела авторов к синтезу Е-изомера оксима формулы (IA) и Z-изомера оксима формулы (IB) d-(17)-13-этил-17-гидpoкcи-18,19-динopпpeгн-4-eн-20-ен-3-он-оксима, который используется в терапии как стереохимическая смесь изомеров E/Z оксима. Использование чистого изомера делает возможным увеличить однородность профиля биологической активности и дает воспользоваться преимуществом различных физических свойств (например, растворимости, абсорбции, транспорта) индивидуальных изомеров для реализации более приемлемого способа применения в терапии. Как описано выше, известные методики синтеза стероидных соединений, содержащих оксимную группу в положении 3, - норгестимата и 17-дезацетил-норгестимата - приводят к изомерной смеси оксимов, в которой соотношение изомеров E/Z оксимов равно приблизительно 60:40-64:36. Неожиданно было найдено, что, применяя способ согласно настоящему изобретению для реакции оксимирования и для разработанной процедуры для полученной смеси оксимов, можно получить или d(17)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)-, или -(3Z)-оксим, так же, как и смесь-(3 Е и Z)-оксимов по желанию. Способ согласно изобретению состоит в следующем: а) 1 моль d-норгестела вводят в реакцию с 1,2-5 мол.экв. ацетата гидроксиламмония или с солью гидроксиламмония и ацетатом щелочного металла в количестве не более чем 1 экв. последней в уксусной кислоте, содержащей не более чем 50 мас.% воды, при 15-50 С в течение 15-45 мин и полученную в результате реакции смесь, содержащую смесь изомеров норелгестромина,) разбавляют приблизительно 10-кратным объемом воды и осажденную смесь изомеров выделяют с получением E/Z смеси изомеров в соотношении приблизительно 56:44-64:36, или в данном случае) после добавления около 10-25 об.% воды ее перемешивают при 10-30 С в течение 24-72 ч, в данном случае воду добавляют к реакционной смеси и выпавший в осадок продукт выделяют с получением) после добавления примерно 10-кратного объема воды осажденную смесь изомеров выделяют и перемешивают в дихлорметане, нерастворимый (3 Е)-изомер оксима формулы (IA) отфильтровывают,фильтрат очищают на хроматографической колонке с использованием силикагеля в качестве адсорбента и смеси неполярного-полярного растворителей в качестве элюента с получением (3Z)-оксима формулы) перемешивают с гидроксиламмонийацетатом или с солью гидроксиламмония и ацетатом щелочного металла в количестве не более чем 1 экв. последней в уксусной кислоте, содержащей не более чем 50 маc.% воды, при 15-30 С в течение 24-72 ч и в данном случае после добавления воды продукт выделяют с получением (3 Е)-оксима формулы (IA), или) перемешивают в дихлорметане, нерастворимый (3 Е)-изомер оксима формулы (IA) отфильтровывают, фильтрат очищают на хроматографической колонке с использованием силикагеля в качестве адсорбента и смеси неполярного-полярного растворителей в качестве элюента с получением (3Z)-оксима формулы (IB), или с) ацетатную группу в положении 17 в 3 Е- или 3Z-изомepe норгестимата гидролизуют в спиртовом растворе эквивалентным количеством гидроксида щелочного металла при 5-30 С и полученный продукт,имеющий ту же конфигурацию, как и исходный, выделяют с получением (3 Е)-изомера оксима формулы(IA) или (3Z)-изомера оксима формулы (IB) и изомеры формулы (IA) или (IB), полученные в соответствии со способами а)-с), очищают кри-2 008174 сталлизацией. В способе (с) предпочтительно используют моногидрат гидроксида лития в качестве гидроксида щелочного металла и реакцию проводят в метаноле. В соответствии с изобретением, если образование оксимов проводят с гидрохлоридом гидроксиламмония и ацетатом натрия или ацетатом гидроксиламмония, полученного заранее в ледяной уксусной кислоте, тогда соотношение E/Z изомеров в полученной сырой смеси изомеров может изменяться между 56:44 и 94:6 в зависимости от дальнейшей обработки смеси. Это позволяет, например, выделять Е-изомер оксима прямо из реакционной смеси и помогает выделить Z-изомер оксима колоночной хроматографией,например, из смеси 56:44, так как это соотношение может меняться до 65,5:34,5 после перемешивания в дихлорметане. Z-Изомер можно легко выделить из смеси, например, колоночной хроматографией. Используя способ b) изобретения, можно получить чистый Е-изомер из любой E/Z смеси изомеров или даже из чистого Z-изомера с помощью изомеризации. Детальное описание представлено в примерах. В соответствии со способом с) данного изобретения чистые Е- или Z-изомеры оксима могут быть получены из известных [Journal of Chromatography. 635, 342-345(1993)] d-(17)-13-этил-17-ацетокси 18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)- или -(3Z)-оксимов гидролизом ацетоксигруппы в положении 17. Стереохимическая чистота не изменяется в мягких условиях гидролиза согласно изобретению. Способ в соответствии с изобретением может быть проведен предпочтительно следующим образом. 1,2-5 мол.экв. (в расчете на 1 моль d-норгестрела) хлорида гидроксиламмония и ацетат натрия в количестве не более чем 1 экв. последнего суспендируют в ледяной уксусной кислоте и полученную суспензию (хлорид натрия выпадает в осадок) перемешивают в течение 30 мин, затем хлорид натрия отфильтровывают, d-норгестрел добавляют к фильтрату и реакционную смесь перемешивают до полного завершения реакции, затем разбавляют водой, выпавший в осадок продукт отфильтровывают, промывают водой, высушивают и перекристаллизовывают. Согласно другому варианту изобретения хлорид натрия не отфильтровывают, поскольку после добавления воды он растворяется и не оказывает влияния на выход и качество продукта.E/Z соотношение в таким образом полученной смеси изомеров оксима составляет около 60:40. Ацетат гидроксиламмония, полученный заранее, также может быть использован как реагент. Если реакционную смесь перемешивают дополнительно 24-72 ч, предпочтительно 48 ч, после израсходования исходного материала - без выделения образовавшегося оксима - и проводят реакцию в вышеописанных условиях, используя ледяную уксусную кислоту или 85% водную уксусную кислоту в качестве растворителя, и образовавшийся продукт отфильтровывают или выделяют после добавления воды, то полученная изомерная смесь содержит E/Z изомеры в соотношении 94:6. Согласно другому воплощению изобретения смесь 60:40 E/Z изомеров или даже чистый Z-изомер суспендируют в уксусной кислоте, содержащей гидроксиламмоний гидрохлорид и ацетат натрия в количестве не более чем 1 экв. последнего, и осуществляют способ в вышеописанных условиях. В этом случае получают смесь изомеров, содержащую E/Z изомеры в соотношении 90:10-96:4. Если на первой стадии способа а) реакцию оксимирования проводят при поддержании реакционной смеси гомогенной, и немедленно после израсходования исходного материала реакционную смесь разбавляют водой, и выпавший твердый продукт выделяют, то изомерное соотношение полученной смеси равно 56:44 E/Z оксимов. Эту изомерную смесь перемешивают с дихлорметаном на стадии ) способа а). В этом случае нерастворимый Е-изомер может быть отфильтрован, а соотношение изомеров в фильтрате может измениться в сторону изомера Z (приблизительно E/Z=33/77), что способствует выделению Zизомера колоночной хроматографией. Разделение Е- и Z-изомеров проводят предпочтительно методом колоночной хроматографии с использованием силикагеля в качестве адсорбента и элюирование начинают предпочтительно неполярной смесью растворителей с постепенным увеличением концентрации более полярного растворителя. Фракции, содержащие один из изомеров, концентрируют и остаток перекристаллизовывают. Еще одна возможность получения чистых Е- или Z-изомеров представлена в способе с). Согласно этому способу E/Z изомерную смесь норгестимата разделяют известным хроматографическим способом[J. Chromatogr., 635, 342-345 (1993)], а ацетатную группу в положении 17 чистого Е- или Z-изомера оксима гидролизуют эквивалентным количеством гидроксида щелочного металла, предпочтительно гидроксида лития или натрия в спиртовом растворе в мягких условиях, предпочтительно при 5-20 С. Если гидролиз проводят в этих условиях, стереохимия гидроксильной группы оксима в положении 3 не изменяется. Согласно новому способу по изобретению можно получать чистый Е-изомер оксима в промышленном масштабе. Выделение Z-изомера оксима может быть рентабельным, поскольку соотношение E/Z изомеров может меняться в сторону Z-изомера, и его можно выделить из смеси методом колоночной хроматографии. Помимо нового способа чистые изомеры формулы (IA) и (IB) также являются новыми, поскольку в описании представлены их характеристические свойства, что однозначно подтверждает их структуру. В норелгестромине в соответствии с относительной конфигурацией гидроксильной группы в оксимной группе существуют два геометрических изомера соединения. Эти изомеры можно разделить-3 008174 обычной колоночной хроматографией, причем Z-изомер более полярный, чем Е-изомер. При использовании смеси изомеров норелгестромина в трансдермальных пластырях возникает вопрос, может ли быть разной абсорбция через кожу для изомеров, имеющих различную полярность. Следующее исследование посвящено этому предположению. Исследованию подвергались физико-химические характеристики, так же, как и фармакокинетика in vitro. При физико-химическом исследовании определяли растворимость изомеров в воде, так же, как их липофильные свойства, с помощью стандартной и изократической ВЭЖХ. Фармакокинетическое исследование in vitro включало метаболическую стабильность, метаболический клиренс и проницаемость соединений на модели клеток Сасо-2. Протокол определения растворимости Определение равновесной растворимости Е- и Z-изомеров норелгестромина проводили в дистиллированной воде. 20 мг норелгестромина добавляли к 20 мл дистиллированной воды при комнатной температуре. Суспензию постоянно перемешивали и время от времени брали пробы. Пробы отфильтровывали и спектрометрическим методом определяли содержание норелгестромина в фильтрате. Спектрофотометрические измерения проводили на спектрофотометре VARIAN Саrу 3 Е при комнатной температуре. Протокол определения липофильности Липофильность определяли методом ВЭЖХ. ВЖЭХ-измерения проводили на приборе для ВЭЖХThermo Separation Product (Spectra System P4000 и Spectra FOCUS Forward Optical Scanning Detector). Данные были обсчитаны с помощью программного обеспечения ChromQuest (версия 2.51). Для измерений в ходе обращенно-фазовой ВЭЖХ использовали колонку Nova-Pak С 18 (размером 4 мкм х 4,6 мм х 250 мм: Waters, Ирландия), детекцию проводили при =280 нм и 25 С. Скорость подачи подвижной фазы равна 1,0 мл/мин. В качестве органического компонента использовали ацетонитрил квалификации "для градиента ВЭЖХ" (Merck KGaA, Дармштадт, Герм.). Данные по удерживанию двух изомеров были получены с помощью изократического анализа с подвижными фазами, содержащими различное количество ацетонитрила. Время выхода свободного объема (to) определяли впрыскиванием метанола. Образцы растворяли в смеси 1:1 ацетонитрила:воды в концентрации 1 мг/4 мл. Значения log K' рассчитывали из среднего времени удерживания, измеренного после двух последовательных впрыскиваний объема 10 мкл (log K'=logtR-to)/to. Значения log K' представлены как функция концентрации ацетонитрила. Время истечения (to) было равно 1,49 мин при данных экспериментальных условиях. Хроматографический индекс гидрофобности (о) представляет собой степень липофильного характера соединений при измерениях обращенно-фазовой ВЭЖХ. По определению, за параметр o принимают ту концентрацию ацетонитрила подвижной фазы, при которой log K'=0. Протокол определения метаболической стабильности и клиренса Метаболическую стабильность изомеров Е и Z норелгестромина определяли на микросомах печени человека. Инкубационная смесь (2,5 мл) содержала 6 мМ Na-пирофосфата, 5 мМ MgCl2, 5 мМ глюкозо-6 фосфата, 1 Ед/мл глюкозо-6-фосфатдегидрогеназы, микросомы печени человека (1 мг/мл) и 5 мкМ Е- илиZ-изомеров норелгестромина. Значение рН доводили до 7,4 с помощью 100 мМ трис-HCl буфера. Реакцию инициировали добавлением 5 мМ NADPH. Пробы по 0,5 мл брали через 0, 5 и 20 мин с немедленным осаждением с помощью 0,5 мл ледяного метанола, 1 мл осажденной пробы центрифугировали в течение 30 мин при 1200 g и вводили 10 мкл супернатанта в систему ВЭЖХ. Аналитические измерения проводили с использованием системы ВЭЖХ Merck-Hitachi с УФ-мониторингом при 244 нм. Неизмененный материал измеряли и его характеристический клиренс (Clint) и метаболическую биодоступность (F%) рассчитывали по следующим уравнениям:dc/dt/Co=Clint1 (мл/мин х г белка) где dc/dt - изменение концентрации за данный период времени, а Со представляет собой начальную концентрацию изомера норелгестромина (измеренную в образце в начальное время 0 мин). Так же, какEH=Clint2/Clint2+HBF где ЕН является печеночной экстракцией и HBF - печеночным кровотоком. Окончательно метаболическая стабильность:F%=(100-EH)x100 Для статистического анализа использовали t-тест Стьюдента (Microsoft Excel). Результаты, приведенные в таблице ниже, рассчитаны как средние значения 3 параллельных измерений. Протокол для измерения проницаемости на клетках Сасо-2 Исследования абсорбции лекарства проводили с монослоями культуры клеток человеческой аденокарциномы (эпителиальной) Сасо-2 в качестве in vitro модели. Характеристики пассивного потока лекарственных средств через монослой Сасо-2 показывают корреляцию с биодоступностью при приеме внутрь. Клетки Сасо-2, полученные из Американской коллекции типовых культур (American Type CultureCollection, Rockville, MD (ATCC), выращивали при 37 С в атмосфере 5% СO2 в среде Игла, модифицированной Dulbecco's, с добавлением 10% инактивированной нагреванием фетальной бычьей сыворотки(GIBCOBRL 11360-039) и антибиотиков: пенициллина 100 Ед/мл и стрептомицина 100 мкг/мл (GIBCOBRL 15140-031). Конфлюентные монослои клеток, выращенные в инкубаторе (при 37 С с 5% СО 2, 95% О 2 и 95% влажности), каждые 7 дней субкультивировали путем обработки 25% трипсином, содержащим 1 мМ ЭДТА. 19-23-дневные конфлюентные монослои с полностью дифференцированными клетками Сасо-2 используют для исследования транспорта после 6-10 пассажей. Были использованы матрикс ЕНС для прикрепления клеток (Promega G 5971), минимальная среда Игла с незаменимыми добавками с солями Ерла и L-глютамином (GIBCOBRL 41500-091) и поликарбонатная мембрана для Transwell (Costar 3401). Вкладыши Transwell покрывали матриксом EHS для прикрепления клеток (Promega G 5971) и по 200000500000 клеток Сасо-2 наносили на вкладыш. Е- и Z-изомеры норелгестромина подвергали анализу при концентрации 50 мкМ. [14 С]-маннит использовали как параклеточный маркер (3,7 х 104 Бк/тестовую камеру). После удаления клеточной культуральной среды 3 монослоя клеток Сасо-2 в параллель были преинкубированы для каждого испытуемого соединения с предварительно подогретым (37 С) HBBS-TRIS(по 400 мкл в просвет и по 1,5 мл с базолатеральной стороны на компартмент) в течение 20 мин при 37 С. После этого добавляют 0,4 мл 50-100 мкМ рабочих концентраций исследуемых и контрольных молекул в рабочей концентрации 50-100 мкм в просветный/апикальный компартменты вкладышей. Измерение абсорбции (в направлении от просвета к базолатеральной стороне) производили, отбирая образцы из люминального апикального ("донорного") компартмента в нулевой момент времени и с базолатеральной ("принимающей") стороны каждые 15 мин (трехкратно). Концентрации изомеров определяли методом жидкостной хроматографии с УФ (ВЭЖХ/УФ) анализом. Метод: градиентное элюирование при 35 С. Элюент А: метанол - 0,05 М, ацетат аммония=300-200+500 мкл 10% уксусной кислоты. Элюент В: метанол. Скорость подачи: 0,50 мл/мин, детекция: при длине волны 240 нм. Тип колонки: Merck Purospher С-18 (размеры 125-3 мм + предколонка). Вид хромат: ВЭЖХ, канал: 2, количественный анализ пиков: по высоте, метод расчета: EXT-STD. Концентрации проникших изомеров в базолатеральном отсеке представлены в таблице. Как показывают вышеприведенные данные, растворимость Z-изомера норелгестромина в воде выше, чем у Е-изомера. В случае Z-изомера проникновение через эпителиальный клеточный слой быстрее,метаболическая стабильность выше, так же, как и клиренс меньше, чем в случае Е-изомера. Эти качества показывают, что после приема внутрь абсорбция Z-изомера лучше, чем таковая для Еизомера, следовательно, его применение в перорально вводимых составах (например, в таблетках) имеет преимущества.Siddiqui и соавторы [J. Prarm. Biopharm, 17, 405 (1989)] показали путем проведения экспериментов на изолированных препаратах человеческой кожи, что липофильные стероиды быстрее проникают через эпидермис, чем полярные стероиды, но скорость клиренса примерно одинакова в обоих случаях. Согласно нашим экспериментам по растворимости и полярности Е-изомер норелгестромина является значительно более липофильным, чем Z-изомер. Согласно экспериментам Siddiqui и соавт. проникновение менее липофильного Е-изомера через эпидермис происходит быстрее, чем для Z-изомера, следовательно,применение Е-изомера в трансдермальных пластырях более выгодно. Благотворный эффект увеличения липофильности для трансдермальной абсорбции был доказан путем проведения исследования взаимосвязи структуры с абсорбцией с шестью различными стероидами. В следующих публикациях: Jnt. J. Pharm. 2001, 217, 1 и J. Chromatography, 49, 631 (1993), показано, что хроматографический индекс гидрофобности (CHI), измеренный в изократических условиях, является очень хорошим показателем липофильности. Мы определили значения CHI стероидов, испытанных в этих экспериментах, и соотнесли их с измеренными коэффициентами распределения между клетками рогового слоя эпидермиса (stratum corneam) и водой. Полученная хорошая корреляция (r2=0,88) показывает, что стероид, имеющий более высокий CHI индекс, лучше проникает через клетки рогового слоя эпидермиса. Согласно нашим измерениям индекс CHI Е-изомера выше, чем у Z-изомера, вследствие чего-5 008174 этот анализ также доказывает трансдермальную применимость Е-изомера. Соотношение между коэффициентами проницаемости в системе клетки рогового слоя эпидермиса вода (log Kp) и индексами CHI показано на фиг. 1. Под термином "чистые изомеры" в настоящем описании имеются в виду изомеры, имеющие такую же чистоту, как изомеры, полученные в примерах. Фармацевтические композиции по настоящему изобретению могут предпочтительно представлять собой таблетки, драже или трансдермальные пластыри. Таблетки могут содержать, помимо активного(ых) ингредиента(ов), обычные носители, наполнители, разбавители, стабилизаторы, усилители вкуса или ароматизаторы, так же, как и добавки, ускоряющие или способствующие приготовлению продукта. Приготовление таблеток проводят способами, обычно применяемыми на практике. Приготовление драже проводят нанесением покрытия на гранулы, полученные тем же способом, как и таблетки в соответствии с обычными методами. Пластыри могут быть предпочтительно трансдермальными пластырями матричного типа, состоящими из 3 слоев. Их наружный слой представляет мембрану, которая является не проницаемой для активных ингредиентов и других компонентов матрицы, состоящей из ПВХ-, полиэтиленовойполипропиленовой или полиуретановой пленки. Матрица, содержащая активное начало, находится на этом наружном слое. Матрица также содержит чувствительный к давлению адгезивный компонент, которым может быть полиакрилат, полидиметилсилоксан или полиизобутилен. Один из этих адгезивных агентов смешивают с активными ингредиентами и поливинилпирролидоном в качестве вспомогательного материала, который предотвращает кристаллизацию. Вспомогательные вещества (усилители), способствующие абсорбции стероидов через кожу, также предпочтительно диспергируют в матрице. Этими компонентами могут быть, например, сложные эфиры алифатических спиртов, такие как лауриллактат,олеиновая кислота и т.д. Полученная таким образом дисперсия наносится на внешний слой пластыря и высушивается. Матрица до нанесения покрывается третьим слоем пластыря - защитным слоем, который может быть, например, полиэтилентерефталатной пленкой. Защитный слой должен удаляться перед нанесением(приклеиванием на кожу) пластыря. Изобретение иллюстрируется следующими не ограничивающими объем примерами. Пример 1. d-(17)-13-Этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(E/Z)-оксим. 34,7 г (0,5 моля) гидрохлорида гидроксиламмония и 34 г (0,41 моль) ацетата натрия суспендируют в 500 мл ледяной уксусной кислоты и после перемешивания в течение 1 ч добавляют 31,2 г (0,1 моль) dноргестрела в атмосфере азота. Гетерогенную реакционную смесь перемешивают до полного завершения реакции и затем выливают в 3 л воды. Осажденный продукт отфильтровывают, последовательно промывают водой, 5% водным раствором гидроксида аммония, водой и высушивают при температуре ниже 60 С в вакууме. Полученный сырой продукт растворяют в 320 мл этанола, очищают на древесном угле и после отфильтровывания угля раствор концентрируют до объема, составляющего 10% первоначального. Остаток охлаждают до 0 С и через 5 ч фильтруют. Твердый продукт промывают этанолом и высушивают с получением 29,4 г (90%) указанного в заглавии соединения. Т.пл.: 110-130 С (смесь геометрических изомеров). Соотношение изомеров оксимов: Е-оксим=58%;Z-оксим=42%. Пример 2. d-(17)-13-Этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)-оксим. К интенсивно перемешиваемой суспензии 2,5 г (0,035 моль) гидрохлорида гидроксиламмония, 2 г(0,024 моль) ацетата натрия и 55 мл 70% водной уксусной кислоты добавляют 5 г (0,016 моль) dноргестрела в атмосфере азота и перемешивание продолжают в течение 50 ч. Затем реакционную смесь выливают в 500 мл воды, выпавший в осадок продукт отфильтровывают, промывают последовательно водой, 5% водным раствором гидроксида аммония, водой и высушивают при температуре ниже 60 С. Полученный сырой продукт (соотношение изомеров оксима: Е-оксим - 94,5%, Z-оксим - 5,5%) перекристаллизовывают из дихлорметана с получением 4,65 г (88,7%) указанного в заглавии соединения, чистый Е-изомер. Т.пл.: 198-200 С. Пример 3. d-(17)-13-Этил-17-гидрокси-18,19-динорпрегн -4-ен-20-ин-3-он-(3 Е)-оксим. 5 г (0,07 моль) гидрохлорида гидроксиламмония и 5,8 г (0,07 моль) ацетата натрия суспендируют в 100 мл ледяной уксусной кислоты, суспензию перемешивают в течение 1 ч и образовавшийся хлорид натрия отфильтровывают. В атмосфере азота 10 г (0,032 моль) d-норгестрела добавляют к фильтрату при перемешивании и перемешивание продолжают до полного завершения реакции. Добавляют 30 мл воды к реакционной смеси и перемешивание продолжают еще 50 ч. Реакционную смесь выливают в 1000 мл воды, высадившийся продукт отфильтровывают, промывают согласно способу, описанному в примере 2,и высушивают. Сырой продукт перекристаллизовывают из ацетонитрила с выходом 9,1 г (86,8%) указанного в заголовке соединения, чистый Е-изомер. Т.пл.: 198-200 С.-6 008174 Пример 4. d-(17)-13-Этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)-оксим. К интенсивно перемешиваемой суспензии 10 г (0,027 моль) d-(17)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-3(E/Z)-оксимa (соотношение изомеров: Е-оксим - 58%, Z-оксим - 42%) и 100 мл ледяной уксусной кислоты в атмосфере азота добавляют 2,5 г (0,035 моль) гидрохлорида гидроксиламмония и 2,9 г (0,035 моль) ацетата натрия в 20 мл воды. Реакционную смесь перемешивают в течение 50 ч,затем выливают в 1000 мл воды. Далее продолжают процедуру аналогично способу, описанному в примере 2, с выходом 9,6 г (96%) сырого продукта. Полученный сырой продукт (соотношение изомеров: Еоксим - 94%, Z-оксим - 6%) перекристаллизовывают из этилацетата в соответствии со способом, описанным в примере 2, с выходом 9,1 г (91%) указанного в заглавии соединения, чистый Е-изомер. Т.пл.: 197-199 С. Пример 5. d-(17)-13-Этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Z)-оксим. Суспензию 43,8 г (0,53 моль) ацетата натрия, 50 г (0,72 моль) гидрохлорида гидроксиламмония и 100 мл 90% водной уксусной кислоты интенсивно перемешивают при комнатной температуре в течение 1 ч. Осадок хлорида натрия отфильтровывают, к фильтрату добавляют 100 г (0,32 моль) d-норгестрела в атмосфере азота и полученную смесь перемешивают в течение 1,5 ч. В течение этого времени температура этой реакции поднимается до 45 С. Реакционная смесь становится гомогенной, что указывает на завершение реакции. Реакционную смесь выливают в 4000 мл воды, выпавший в осадок продукт отфильтровывают, последовательно промывают водой, 5% водным раствором гидроксида аммония, водой и высушивают. Полученную смесь изомеров (104 г) оксимов (соотношение изомеров: Е-оксим - 57,4%,Z-оксим - 42,6%) интенсивно перемешивают с 20-кратным объемом дихлорметана в течение 30 мин, нерастворимый продукт отфильтровывают и высушивают при температуре до 60 с выходом 45,6 г продукта (соотношение изомеров: Е-оксим - 94,4%, Z-оксим - 4,6%). Маточную жидкость, полученную после выделения вышеописанного продукта, концентрируют с получением 58 г продукта (соотношение изомеров: Z-оксим - 65,5%, Е-оксим - 33,2%). Концентрат растворяют в 2300 мл (40-кратный объем) дихлорметана и выдерживают при 0-5 С в течение 5 ч. Выпавший кристаллический продукт отфильтровывают, промывают дихлорметаном и высушивают с выходом 17,6 г продукта (соотношение изомеров: Е-оксим - 9%, Z-оксим - 91%). Полученный таким образом маточный раствор также концентрируют и остаток - 39 г - очищают колоночной хроматографией, используя 700 г силикагеля в качестве адсорбента и толуол, с последующей более полярной смесью толуол-ацетон в качестве элюента. Фракции, содержащие одинаковые изомеры,концентрируют с выходом 3,7 г Е-оксима (чистота изомера: 94%) и 25,2 г Z-оксима (чистота изомера: 95%). Соответствующие кристаллы, полученные кристаллизацией и колоночной хроматографией, объединяют и перекристаллизовывают сначала из 20-кратного объема ацетонитрила, затем из 23-кратного объема этилацетата с выходом 29 г Z-оксима (чистота: 99,3%) и 38,4 г Е-оксима (чистота: 99,7%). Т.пл. Z-оксима: 206-207 С, т.пл. Е-оксима: 199-200 С. ЯМР-данные.Z-оксим: 1 Н-ЯМР (500 МГц, ДМСО-d6 (ТМС),(м.д.: 0,92 (3 Н, m, -СН 2-СН 3), 1,40 (2 Н, m, -СН 2-СН 3), 2,05 и 2,24 (2 Н, m и m, Н-2), 3,28 (1H, s, CH), 5,23 (1H, s, 17-OH), 6,40 (1H, m, Н-4), 10,12 (1H, s, =N-OH); 13 С-ЯМР (125 МГц, ДМСО-d6 (ТМС),(м.д.: 9,4 (-СН 2-СН 3), 18,3 (-СН 2-СН 3), 26,9 (С-2), 79,6 (С 17), 89,1 (-С), 74,9 (СН), 111,6 (С-4), 151,2 (С-3), 152,0 (С-5). Е-оксим: 1 Н-ЯМР (500 МГц, ДМСО-d6 (ТМС),(м.д.: 0,92 (3H, t, -CH2-CH3), 1,40 (2 Н, m, -СН 2-СН 3), 1,87 и 2,87 (2 Н, m и m, Н-2), 3,28 (1H, s, CH), 5,23 (1H, s, 17-OH), 5,78 (1H, m, Н-4), 10,38 (1H, s, =N-OH); 13 С-ЯМР (125 МГц, ДМСО-d6 (ТМС),(м.д.: 9,4 (-СН 2-СН 3), 18,3 (-СН 2-СН 3), 20,6 (С-2), 79,6 (С 17), 89,1(-С), 74,9 (CH), 118,6 (С-4), 154,3 (С-3), 148,1 (С-5). Пример 6. d-(17)-13-Этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)-оксим. К интенсивно перемешиваемому раствору 10 г (0,027 моль) d-(17)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Z)-оксима и 100 мл 80% водной уксусной кислоты добавляют 2,5 г (0,035 моль) гидрохлорида гидроксиламмония и 2,9 г (0,035 моль) ацетата натрия. Реакционную смесь перемешивают около 50 ч, затем повторяют способ согласно примеру 4, получая 8,5 г (85%) указанного в заголовке соединения, чистый Е-оксим. Т.пл.: 196-198 С. Пример 7. d-(17)-13-Этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)-оксим. К интенсивно перемешиваемому раствору 5 г (0,01 моль) d-(17)-13-этил-17-ацетокси-18,19 динорпрегн-4-ен-20-ин-3-он-(3Z)-оксима и 50 мл метанола в атмосфере азота добавляют 1,7 г (0,04 моль) моногидрата гидроксида лития при 0-5 С и перемешивание продолжают в течение 2 ч. После завершения реакции, контролируемого тонкослойной хроматографией, реакционную смесь выливают в 500 мл воды и рН полученной суспензии доводят до 7,5-9 уксусной кислотой. Выпавший в осадок продукт отфильт-7 008174 ровывают, промывают водой и высушивают при температуре до 60 С в вакууме. Полученный сырой продукт (4,5 г) перекристаллизовывают из ацетонитрила с выходом 4 г (90,2%) d-(17)-13-этил-17 гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Z)-оксимa. Т.пл.: 203-204 С.d-(17)-13-Этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)-оксим получают согласно способу, описанному выше, из 5 г d-(17)-13-этил-17-ацетокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)-оксима. Выход: 4,1 г (92,45%). Т.пл. 198-200 С. Пример 8. d-(17)-13-Этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)-оксим. К интенсивно перемешиваемой суспензии 1,25 г (0,017 моль) гидрохлорида гидроксиламмония,1,45 г (0,017 моль) ацетата натрия и 60 мл 50% водной уксусной кислоты добавляют в атмосфере азота 2,5 г (0,08 моль) d-норгестрела. После завершения реакции, контролируемого тонкослойной хроматографией, реакционную смесь выливают в 500 мл воды. Выпавший в осадок продукт отфильтровывают, последовательно промывают водой, 5% водным раствором гидроксида аммония, водой и высушивают при температуре до 60 С. Сырой продукт перекристаллизовывают из дихлорметана с выходом 2,27 г (86,7%) указанного в заглавии соединения. Т.пл.: 198-200 С. Пример 9. d-(17)-13-Этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-оксим (смесь изомеров). К интенсивно перемешиваемой суспензии 5,8 г (0,07 моль) ацетата натрия и 80 мл ледяной уксусной кислоты добавляют 5 г (0,007 моль) гидрохлорида гидроксиламмония в 22 мл воды. Затем к реакционной смеси добавляют 10 г (0,032 моль) d-норгестрела в атмосфере азота и перемешивание продолжают до полного завершения реакции. После завершения реакции, контролируемого тонкослойной хроматографией, реакционную смесь выливают в 800 мл воды. Выпавший осадок отфильтровывают, последовательно промывают водой, 5% водным раствором гидроксида аммония, водой и высушивают при температуре до 60 С с выходом 8,9 г (84,92%) соединения, указанного в заголовке, в виде смеси 55,88:44,05E/Z изомеров. Т.пл.: 110-130 С. Пример 10. Фармацевтическая композиция, содержащая d-(17)-13-этил-17-гидрокси-18,19-динорпрегн-4-eн-20-ин-3-он-(3Z)-оксим и этинил-эстрадиол в качестве активных ингредиентов в форме таблеток. 250 мг Z-изомера норелгестромина и 35 мг этинил-эстрадиола перемешивают до гомогенного состояния с 75,715 г лактозы, 22,5 г микрокристаллической целлюлозы, 1 г коллоидного диоксида кремния(Aerosil) и 500 мг стеарата магния. Полученную таким образом порошкообразную смесь прессуют в таблетки по 100 мг без гранулирования. Получено около 1000 штук таблеток. Пример 11. Фармацевтическая композиция, содержащая d-(17)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Z)-оксим и этинил-экстрадиол в качестве активных ингредиентов в форме таблеток. 250 мг Z-изомера норелгестромина и 35 мг этинил-эстрадиола растворяют в 10 мл этанола и полученную таким образом смесь распыляют на гомогенную смесь 75,715 г лактозы и 20,5 г кукурузного крахмала. Этанол удаляют из смеси высушиванием в ожиженном слое. Полученную порошкообразную смесь, содержащую активные ингредиенты, гранулируют с водным раствором 2 г поливинилпирролидона (PVP) в устройстве для псевдоожижения, затем высушивают. 1 г коллоидного диоксида кремния и 0,5 г стеарата магния гомогенизируют с гранулированным материалом и прессуют в таблетки по 100 мг. Получено около 1000 таблеток. Пример 12. Фармацевтическая композиция, содержащая d-(17)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Z)-оксим и этинил-эстрадиол в качестве активных ингредиентов в форме таблеток. 250 мг Z-изомера норелгестромина, 35 мг этинил-эстрадиола и 2 г поливинилпирролидона (PVP) растворяют в 10 мл этанола, таким образом полученную смесь распыляют на гомогенную смесь 75,715 г лактозы и 20,5 г кукурузного крахмала в смесителе с высоким срезывающим напряжением. Смесь гранулируют, и этанол удаляют в микроволновой вакуумной сушке. 1 г коллоидного диоксида кремния и 0,5 г стеарата магния гомогенизируют с гранулированным материалом и прессуют в таблетки по 100 мг. Получено около 1000 таблеток. Пример 13. Фармацевтическая композиция d-(17)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20 ин-3-он-(3 Е)-оксима и этинил-эстрадиола в качестве активных ингредиентов в виде трансдермального пластыря. Один кусок трансдермального 3-слойного пластыря матричного типа содержит 6,0 мг Е-изомера норелгестромина и 0,75 мг этинил-эстрадиола. Для каждого куска пластыря 6,0 мг Е-изомера норелгестромина, 0,75 мг этинил-эстрадиола, 25 мг поливинилпирролидона, 20 мг лауриллактата (агента, стимулирующего абсорбцию) и 248 мг полиизобутилена диспергируют в смеси 8:1:1 гексан/этилацетат/этанола при комнатной температуре в течение 45 мин. Полученную таким образом дисперсию выливают на внешнюю мембрану пластыря и высушивают при 70 С в течение 45 мин. Защитную мембрану наслаивают на поверхность высушенной матрицы. Пример 14. Фармацевтическая композиция, содержащая d-(17)-13-этил-17-гидрокси-18,19-динор-8 008174 прегн-4-ен-20-ин-3-он-(3 Е)-оксим и этинил-эстрадиол в качестве активных ингредиентов в форме трансдермального пластыря. Один кусок 3-слойного пластыря матричного типа содержит 6,0 мг Е-изомера норелгестромина и 0,75 мг этинил-эстрадиола. Для каждого куска пластыря 261 мг полидиметилсилоксана и 17 мг поливинилпирролидона гомогенизируют при комнатной температуре. 15 мг метиллаурата, 6,0 мг Е-изомера норелгестромина и 0,75 мг этинил-эстрадиола добавляют к смеси и диспергируют с 350 мл этанола при комнатной температуре в течение 45 мин. Полученную таким образом дисперсию выливают на внешнюю мембрану пластыря и высушивают при 70 С в течение 45 мин. Защитную мембрану наслаивают на поверхность высушенной матрицы. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Фармацевтическая композиция в виде пластыря, содержащая чистый d-(17)-13-этил-17 гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)-оксим формулы (IA) в качестве активного ингредиента - гестагена. 2. Перорально применяемая фармацевтическая композиция, содержащая чистый d-(17)-13-этил 17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Z)-оксим формулы (IB) в качестве активного ингредиента - гестагена. 3. Способ синтеза E/Z-изомерной смеси норегестромина а также чистого d-(17)-13-этил-17 гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3 Е)-оксима формулы (IA) и чистого d-(17)-13-этил-17 гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-(3Z)-оксима формулы (IB), включающий следующее: а) реакцию 1 моля d-норгестрела с 1,2-5 мол.экв. ацетата гидроксиламмония или солью гидроксиламмония и ацетатом щелочного металла в количестве не более чем 1 экв. последней в уксусной кислоте,содержащей не более чем 50 маc.% воды, при 15-50 С в течение 15-45 мин, полученную реакционную смесь, содержащую смесь изомеров норелгестромина,) разбавляют приблизительно 10-кратным объемом воды и выпавшую в осадок смесь изомеров выделяют с получением смеси E/Z изомеров в соотношении около 56:44-64:36, или же в данном случае) после добавления около 10-25 об.% воды ее перемешивают при 10-30 в течение 24-72 ч, в данном случае добавляют воду к реакционной смеси и выпавший в осадок продукт выделяют с получением) после добавления около 10-кратного объема воды выпавшую в осадок смесь изомеров выделяют и перемешивают в дихлорметане, отфильтровывают нерастворимый (3 Е)-изомер оксима формулы (IA),фильтрат очищают колоночной хроматографией с использованием силикагеля в качестве адсорбента и смеси неполярного-полярного растворителей в качестве элюента с получением (3Z)-оксимa формулы) перемешивают с ацетатом гидроксиламмония или солью гидроксиламмония и ацетатом щелочного металла в количестве не более 1 экв. последней в уксусной кислоте, содержащей не более 50 мас.% воды, при 15-30 С в течение 24-72 ч и в данном случае после добавления дополнительного количества воды продукт выделяют с получением (3 Е)-изомера оксима формулы (IA), или(IA), фильтрат очищают колоночной хроматографией, используя силикагель в качестве адсорбента иc) гидролизуют ацетатную группу в положении 17 3 Е- или 3Z-изомepa норгестимата в спиртовом растворе эквивалентым количеством гидроксида щелочного металла при 5-30 С и полученный таким образом продукт, имеющий такую же конфигурацию, как и исходный, выделяют с получением (3 Е)изомера оксима формулы (IA) или (3Z)-изомера оксима формулы (IB) и изомеры формул (IA) и (IB), полученные в соответствии со способами а)-с), очищают кристаллизацией. 4. Способ с) по п.3, характеризующийся тем, что гидролиз проводят с гидроксидом лития в метаноле.
МПК / Метки
МПК: C07J 41/00
Метки: изомеров, d-(17α)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-3е, изомеры, смеси, чистых, чистые, 3z-оксимов, синтеза, способ
Код ссылки
<a href="https://eas.patents.su/11-8174-chistye-izomery-d-17alpha-13-etil-17-gidroksi-1819-dinorpregn-4-en-20-in-3-on-3e-i-3z-oksimov-sposob-sinteza-smesi-izomerov-i-chistyh-izomerov.html" rel="bookmark" title="База патентов Евразийского Союза">Чистые изомеры d-(17α)-13-этил-17-гидрокси-18,19-динорпрегн-4-ен-20-ин-3-он-3е и 3z-оксимов, способ синтеза смеси изомеров и чистых изомеров</a>
Предыдущий патент: Способ и соединения, стимулирующие процессы заживления и ослабления воспаления
Следующий патент: Ацетали в качестве репеллентов от насекомых
Случайный патент: Водопотребляющий бытовой прибор