Галоидпроизводные 9-деоксо-9а-аза-9а-гомоэритромицина а
Номер патента: 5214
Опубликовано: 30.12.2004
Авторы: Кобрехел Габриела, Марушич-Иштук Зорица, Мутак Степан, Маршич Наташа, Куюнджич Неджелко
Формула / Реферат
1. Галоидпроизводные 9a-N-(N'-арилкарбамоил)- и 9a-N-(N'-арилтиокарбамоил)-9-деоксо-9a-аза-9a-гомоэритромицина A общей формулы (I)
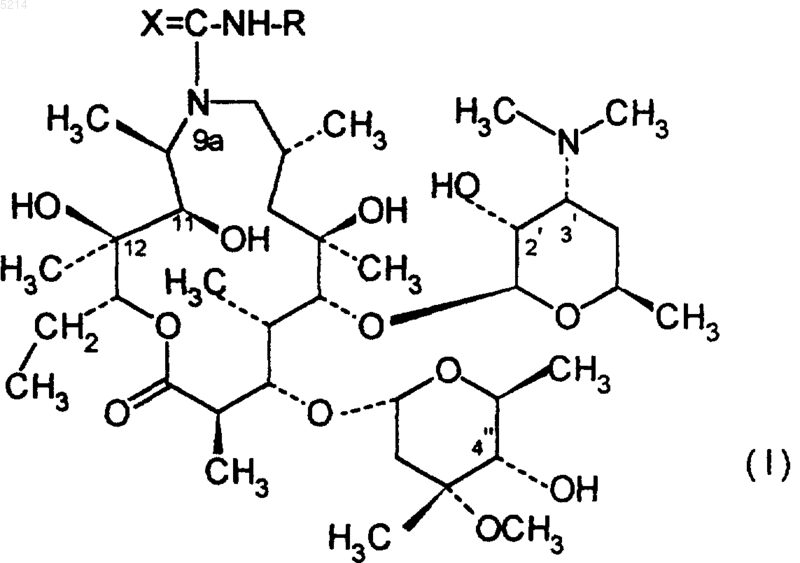
в которой R означает замещенную арильную группу формулы (II)
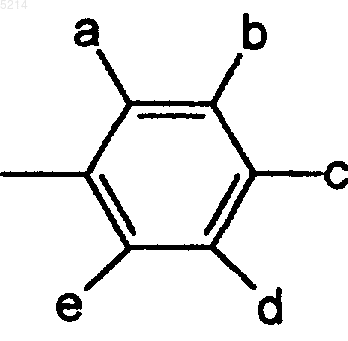
в которой заместители a, b, c, d и e являются одинаковыми или различными и по крайней мере один из них означает галоген, (C1-C6)галоидалкил или (C1-C6)галоидалкоксигруппу, тогда как остальные заместители представляют водород, галоген, (C1-C6)алкил или (C1-C6)алкоксигруппу, и X означает кислород или серу, и их фармацевтически приемлемые аддитивные соли с неорганическими или органическими кислотами.
2. Соединения по п.1, отличающиеся тем, что a означает галоген, b, c, d и e являются одинаковыми и означают водород и X представляет кислород или серу.
3. Соединение по п.2, отличающееся тем, что a означает фтор и X означает кислород.
4. Соединение по п.2, отличающееся тем, что a означает фтор и X означает серу.
5. Соединение по п.2, отличающееся тем, что a означает хлор, а X означает серу.
6. Соединения по п.1, отличающиеся тем, что a означает галоген, b, c, и d являются одинаковыми и означают водород, e представляет (C1-C4)алкил, а X означает кислород или серу.
7. Соединение по п.6, отличающееся тем, что a означает хлор, b, c и d являются одинаковыми и означают водород, e представляет метил, а X является кислородом.
8. Соединения по п.1, отличающиеся тем, что a, c, d и e являются одинаковыми и означают водород, b означает галоген, а X является кислородом или серой.
9. Соединение по п.8, отличающееся тем, что b означает фтор, а X является кислородом.
10. Соединение по п.8, отличающееся тем, что b означает хлор, а X является кислородом.
11. Соединение по п.8, отличающееся тем, что b означает бром, X является кислородом.
12. Соединение по п.8, отличающееся тем, что b означает фтор, а X является серой.
13. Соединение по п.8, отличающееся тем, что b означает хлор, а X является серой.
14. Соединение по п.8, отличающееся тем, что b означает бром, а X является серой.
15. Соединения по п.1, отличающиеся тем, что a, b, d и e являются одинаковыми и означают водород, с означает галоген, а X представляет кислород или серу.
16. Соединение по п.15, отличающееся тем, что с означает хлор, а X представляет кислород.
17. Соединение по п.15, отличающееся тем, что с означает бром, а X представляет кислород.
18. Соединение по п.15, отличающееся тем, что с означает хлор, а X представляет серу.
19. Соединение по п.15, отличающееся тем, что с означает бром, а X представляет серу.
20. Соединения по п.1, отличающиеся тем, что a, d и e являются одинаковыми и означают водород, b представляет (C1-C6)галоидалкил, с означает галоген, а X является кислородом или серой.
21. Соединение по п.20, отличающееся тем, что a, d и e являются одинаковыми и означают водород, b представляет -CF3, c означает хлор, а X представляет кислород.
22. Соединения по п.1, отличающиеся тем, что b, d и e являются одинаковыми и означают водород, a и c являются одинаковыми и означают галоген, а X представляет кислород или серу.
23. Соединение по п.22, отличающееся тем, что a и c являются одинаковыми и означают хлор, а X представляет кислород.
24. Соединение по п.22, отличающееся тем, что a и c являются одинаковыми и означают хлор, а X представляет серу.
25. Соединения по п.1, отличающиеся тем, что a, b, c, d и e являются одинаковыми или различными и означают водород или группу (C1-C4)галоидалкила, а X представляет кислород или серу.
26. Соединение по п.25, отличающееся тем, что a представляет -CF3, b, c, d и e являются одинаковыми и означают водород, а X представляет кислород.
27. Соединение по п.25, отличающееся тем, что a, c, d и e являются одинаковыми и означают водород, b представляет -CF3, а X является кислородом.
28. Соединение по п.25, отличающееся тем, что a, b, d и e являются одинаковыми и означают водород, c представляет -CF3, а X означает кислород.
29. Соединение по п.25, отличающееся тем, что a, c, d и e являются одинаковыми и означают водород, b представляет -CF3, а X означает серу.
30. Соединения по п.1, отличающиеся тем, что a, b, c, d и e являются одинаковыми или различными и означают водород или (C1-C4)галоидалкоксигруппу, а X представляет кислород или серу.
31. Соединение по п.30, отличающееся тем, что b, c, d и e являются одинаковыми и означают водород, а представляет -OCF3, а X означает кислород.
32. Соединение по п.30, отличающееся тем, что a, b, d и e являются одинаковыми и означают водород, c представляет -OCF3, а X означает кислород.
33. Способ получения галоидпроизводных 9a-N-(N'-арилкарбамоил)- и 9a-N-(N'-арилтиокарбамоил)-9-деоксо-9a-аза-9a-гомоэритромицина A общей формулы (I)
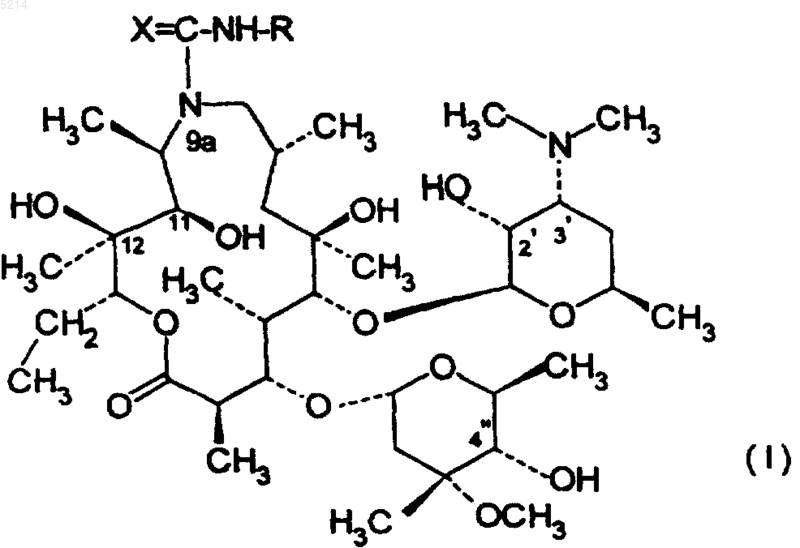
в которой R означает замещенную арильную группу формулы (II)
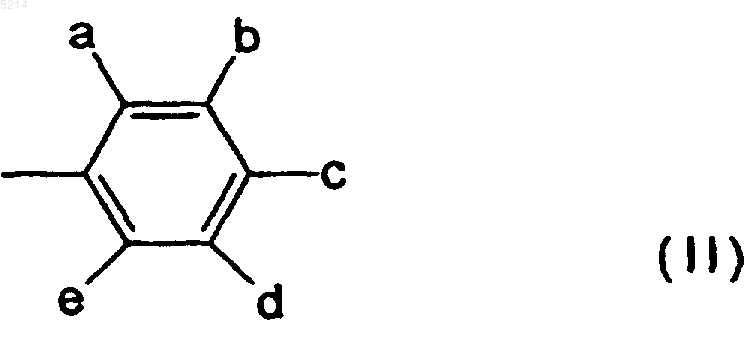
в которой заместители a, b, c, d и e являются одинаковыми или различными и по крайней мере один из них означает галоген, (C1-C6)галоидалкил или (C1-C6)галоидалкоксигруппу, а остальные заместители представляют водород, галоген, (C1-C6)алкил или (C1-C6)алкоксигруппу и X означает кислород или серу, и их фармацевтически приемлемых аддитивных солей с неорганическими или органическими кислотами, отличающийся тем, что 9-деоксо-9a-аза-9a-гомоэритромицин A подвергают реакции с изоцианатами или изотиоцианатами общей формулы (III)
R - N = C = X (III),
в которой R и X имеют указанные выше значения, в апротонном растворителе, предпочтительно толуоле, при комнатной температуре или при повышенной до 60ш.
34. Фармацевтическая композиция, отличающаяся тем, что она содержит фармацевтически приемлемый носитель и антибактериально эффективное количество соединений по п.1.
35. Применение соединений по любому из пп.1-32 для лечения или предотвращения бактериальных инфекций.
Текст
1 Техническая проблема Изобретение относится к новым соединениям из класса макролидного антибиотика эритромицина А. Изобретение, главным образом, относится к галоидпроизводным 9a-N-(N'арилкарбамоил)-и 9a-N-(N'-арилтиокарбамоил)9-деоксо-9 а-аза-9 а-гомоэритромицина А, к его фармацевтически приемлемым аддитивным солям с неорганическими и органическими кислотами, к способу их получения, к фармацевтическим композициям, содержащим их, и к применению данных фармацевтических композиций для лечения или предотвращения или профилактики бактериальных инфекций. Предшествующий уровень техники Эритромицин А является макролидным антибиотиком, структура которого характеризуется 14-членным лактоновым кольцом с кетоном С-9 и двумя сахарами, L-кладинозой и Dдезозамином, присоединенными гликозидно к С-3 и С-5 положениям агликонового фрагмента молекулы (McGuire, Antibiot. Chemother., 1952; 2: 281). С помощью оксимирования кетона С-9 гидрохлоридом гидроксиламина, перегруппировки Бекмана (Beckmann) полученного 9(Е)оксима и восстановления полученного простого 6,9-иминоэфира получен 9-деоксо-9 а-аза-9 агомоэритромицин А, первый полусинтетический макролид с 15-членным азалактоновым кольцом (Kobrehel G. Et al., США 4328334,5/1982). Избирательным ацилированием 9-деоксо 9 а-аза-9 а-гомоэритромицина А ангидридами карбоновых кислот синтезированы соответствующие моно-, ди-, три- или тетраацильные производные, а с помощью реакции переэтерификации этиленкарбонатом с последующим ацилированием синтезированы 11,12 циклический карбонат и его ацильные производные (Djokic S. et al, J. Antibiotics 40, 10061015, 1987). С помощью восстановительного метилирования вторичной 9 а-аминогруппы 9-деоксо 9 а-аза-9 а-гомоэритромицина А согласно способу Эшвейлера-Кларка (Eschweiler-Clark) синтезирован 9-деоксо-9 а-метил-9 а-аза-9 а-гомоэритромицин А (азитромицин), прототип нового класса 9 а-азалидных антибиотиков (Kobrehel G.et al, BE 892357, 7/1982). В дополнение к широкому противомикробному спектру действия,включая грамотрицательные бактерии, азитромицин характеризуется длительным биологическим периодом полувыведения, особым механизмом транспорта к участку применения и коротким периодом терапии. Азитромицин легко проникает в фагоцитные клетки человека и накапливается в них, что приводит в результате к улучшенному действию в отношении внутриклеточных патогенных микроорганизмов классов Legionella, Chlamydia и Helicobacter. Bright 2 азитромицина, описали эпимеризацию 4 гидроксильной группы и получение соответствующего 4-аминопроизводного. Синтез и антибактериальная активность простых 9 а,11-циклических эфиров 9-деоксо-9 ааза-9 а-гомоэритромицина А описаны в патенте США 4492688, 1/1985 (Bright G.M.). Получение и спектр активности 9 а, 11-циклических карбаматов 9-деоксо-9 а-аза-11-деокси-9 а-гомоэритромицина А и его О-метильных производных описан в патенте США 5434140, 7/1995 (Kobrehel G.et al). Недавно Blizzard Т.A. et al (WO 99/00125,7/98) описали новые производные 9a-N, 6-0 метилен-9-деоксо-9 а-аза-9 а-гомоэритромицина А и соответствующих 9a-N,6-О-карбаматов в качестве промежуточных продуктов в синтезе 3 кето-производных из класса 9 а-азалидов. Обнаружено также, что с помощью реакции 9-деоксо-9 а-аза-9 а-гомоэритромицина А с изоцианатами или изотиоцианатами могут быть получены соответствующие 9a-N-(N'-карбамоил)- и 9a-N-(N'-тиокарбамоил)-производные(Kujundzic N. et al, США 5629296, 5/97). Указанное изобретение относится к производнымN'-(C1-С 3)алкилкарбамоилa, N'-арилкарбамоила и N'-аралкилкарбамоила и их тиокарбамоильным аналогам, соответственно. Хотя антибактериальный спектр данных 9 а-азалидов сходен с действием азитромицина, эффективность в 2-8 раз меньше, даже в случае наиболее активных представителей (производных N'-нафтилкарбамоила и N'-бензилтиокарбамоила). Согласно хорошо известному и установленному предыдущему уровню техники до сих пор не описаны галоидпроизводные 9a-N-(N'арилкарбамоил)- и 9a-N-(N'-арилтиокарбамоил)9-деоксо-9 а-аза-9 а-гомоэритромицина А, которые являются объектом данного изобретения, их фармацевтически приемлемые аддитивные соли с неорганическими или органическими кислотами, способ их получения, способ приготовления фармацевтических композиций, содержащих их, и применение данных фармацевтических композиций для лечения или предотвращения бактериальных инфекций. Целью данного изобретения является получение новых 9a-N-(N'-арилкарбамоил)- и 9aN-(N'-арилтиокарбамоил)-9-деоксо-9 а-аза-9 а-гомоэритромицинов А, в которых по крайней мере один из заместителей в ароматическом кольце имеет значение галоген, (C1-С 6)галоидалкил или(C1-С 6)галоидалкоксигруппа. Новые 9 а-азалиды данного изобретения характеризуются широким антибактериальным спектром действия, включая действие на чувствительные и резистентные грамположительные и грамотрицательные микроорганизмы. Изобретательское решение Обнаружено, что галоидпроизводные 9aN-(N'-арилкарбамоил)- и 9a-N-(N'-арилтиокар 3 бамоил)-9-деоксо-9 а-аза-9 а-гомоэритромицина А общей формулы (I) в которой R означает замещенную арильную группу формулы (II) в которой заместители а, b, с, d и е являются одинаковыми или различными и по крайней мере один из них означает галоген, (C1 С 6)галоидалкил или(C1-С 6)галоидалкоксигруппу, тогда как остальные заместители представляют водород, галоген, (C1-С 6)алкил или(C1-С 6)алкоксигруппу и X означает кислород или серу, и их фармацевтически приемлемые аддитивные соли с неорганическими или органическими кислотами могут быть получены по реакции 9-деоксо-9 а-аза-9 а-гомоэритромицина А с изоцианатами или изотиоцианатами общей формулы (III)(III) в которой R и X имеют указанные выше значения, в апотонном растворителе, предпочтительно толуоле, при комнатной температуре или при повышенной температуре. После завершения реакции продукт выделяют выпариванием при пониженном давлении и необязательно с применением стандартных приемов, таких как хроматография на колонке с силикагелем или перекристаллизация. Далее, целью изобретения являются фармацевтически приемлемые аддитивные соли,которые, согласно признанной медицинской практике, являются нетоксичными и при контакте с тканями человека или тканями низших млекопитающих не вызывают раздражения или аллергических реакций. Термин "фармацевтически приемлемые соли" относится к аддитивным солям соединений общей формулы (I) с нетоксичными неорганическими или органическими кислотами. Их получают in situ в процессе выделения или очистки соединений изобретения или впоследствии в результате реакции 3' диметиламиногруппы выделенного основания, по крайней мере, с эквимолярным количеством соответствующей неорганической или органической кислоты. Подходящими неорганическими кислотами являются, например, хлористоводородная, бромисто-водородная, иодистоводородная, серная, фосфорная или перхлорная кислоты, а органическими кислотами являются уксусная, трифторуксусная, пропионовая, бензойная, бензолсульфоновая, метансульфоновая, 005214 4 лаурилсульфоновая, адипиновая, аскорбиновая,камфорная, глюконовая, фумаровая, стеариновая, пальмитиновая, янтарная, этилянтарная,лактобионовая, щавелевая, салициловая кислота и аналогичные кислоты. Реакция основания с соответствующими кислотами осуществляется в инертном растворителе и аддитивные соли выделяют выпариванием растворителей или, альтернативно, фильтрованием после самопроизвольного осаждения или после осаждения добавлением неполярного сорастворителя. Новые галоидпроизводные 9a-N-(N'арилкарбамоил)- и 9a-N-(N'-арилтиокарбамоил)9-деоксо-9 а-аза-9 а-гомоэритромицина А общей формулы (I) и их фармацевтически приемлемые аддитивные соли с неорганическими или органическими кислотами обладают эффективной антибактериальной активностью. In vitro действие новых соединений исследовали на ряде стандартных и резистентных опытных микроорганизмов. В общем, исследованиями эффективности галогенарильных производных на S.aureus, E. faecalis и S. pneumoniae было продемонстрировано, что 9a-N-(N'-тиокарбамоил)производные являются более активными, чем 9a-N-(N'-карбамоил)-производные. Производные N'-фторарила были наиболее активными производными из данного ряда. Положение замещения не оказывало влияния на активность,однако было показано, что производные галоидарилкарбамоила, замещенные в положении 2,проявляют наилучшую антибактериальную активность in vitro. Аналогичные особенности наблюдались для производных N'-(C1-C6)галоидалкилкарбамоила. Однако на ряде тиокарбамоильных аналогов было показано, что производное N'-(3 трифторметил)арилтиокарбамоила является наиболее активным, и в дополнение к активности в отношении испытываемых микроорганизмов, чувствительных к эритромицину, также проявляет активность против резистентных штаммов. Объектом данного изобретения являются фармацевтические композиции, включающие терапевтически эффективное количество соединений общей формулы (I) и один или более нетоксичных фармацевтически приемлемых носителей. Термин фармацевтически приемлемый носитель подразумевает нетоксичное инертное твердое вещество, полутвердое вещество, жидкий наполнитель, разбавитель и др. Материалами, которые могут служить в качестве фармацевтически приемлемых носителей, являются сахара, например, лактоза, глюкоза или сахароза, крахмал, целлюлоза и их производные, например, карбоксиметилцеллюлоза или этилцеллюлоза, затем желатин, тальк, арахисовое масло,кунжутовое масло, соевое масло, гликоли, например, пропиленгликоль, сложные эфиры, например, этилацетат или этиллаурат, агар, буферирующие агенты, например, гидроксид магния 5 или гидроксид алюминия, свободная от пирогенов вода, изотонический раствор, раствор Рингера, этанол, фосфатный буфер, отдушки, окрашивающие агенты, подсластители и т.д. Фармацевтические композиции настоящего изобретения можно вводить перорально, парентерально, интравагинально, ректально или внутриброшинно людям и животным. Жидкие готовые формы композиций для перорального применения включают фармацевтически приемлемые эмульсии, микроэмульсии, растворы,суспензии, сиропы и эликсиры. В дополнение к активному компоненту, жидкие готовые формы также могут содержать инертные разбавители,например воду или другие растворители, и различные добавки. Инъекционные формы, например, стерильные водные суспензии, готовят в соответствии с хорошо известными способами. Следующим объектом изобретения является способ лечения или предотвращения бактериальных инфекций у человека и животных,который, в случае необходимости лечения или профилактики, включает применение терапевтически эффективного количества соединения общей формулы (I) в течение периода времени,необходимого для достижения терапевтического действия. Терапевтически эффективное количество означает достаточное количество вещества для лечения бактериальной инфекции при любом медицинском применении, при тщательном соблюдении взаимосвязи пользы и риска. Общее количество ежедневных доз соединений данного изобретения при применении по отношению к человеку или животным в однократной или многократных дозах составляет в интервале от 0,001 до 50 мг/кг массы тела. Вообще в случае необходимости, режим лечения согласно изобретению включает введение от 10 до 100 мг/день соединения общей формулы (I) в виде однократной или многократных доз. Способ получения галоидпроизводных 9aN-(N'-арилкарбамоил)- и 9a-N-(N'арилтиокарбамоил)-9-деоксо-9 а-аза-9 а-гомоэритромицина А настоящего изобретения иллюстрируется следующими примерами, которые никоим образом не предназначены для ограничения изобретения. Пример 1. 9-деоксо-9 а-N-N'-[(2-фторфенил)карбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (3,0 г; 0,00408 моль), 2-фторфенилизоцианата(0,61 г; 0,00448 моль) и толуола (40 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (3,81 г). Кристаллизацией из смеси диэтиловый эфир - петролейный эфир получали хроматографически гомогенный названный в заголовке продукт (2,74 г), имеющий следующие физико-химические константы: Точка плавления 129-132 С(40 мл) при перемешивании в течение 12 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (3,45 г). Кристаллизацией из смеси ацетон - петролейный эфир получали хроматографически гомогенный продукт (2,05 г), имеющий следующие физикохимические константы: ИК (КВr) см-1 3431, 2971, 2936, 1729, 1620,1514, 1457, 1380, 1314, 1280, 1167, 1094, 1052,1012, 958, 896, 831, 756.FAB-MC 888 [МН+] Пример 3. 9-деоксо-9a-N-N'-[(2-хлорфенил)тиокарбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (3,0 г; 0,00408 моль), 2-хлорфенилизотиоцианата (0,76 г; 0,00448 моль) и толуола (40 мл) при перемешивании в течение 12 ч при температуре 40 С и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (3,51 г). Кристаллизацией из смеси ацетон - петролейный эфир получали хроматографически гомогенный продукт (2,24 г), имеющий следующие физико-химические константы: ИК (КВr) см-1 3411, 2972, 2937, 2058, 1726,1593, 1520, 1494, 1456, 1379, 1310, 1244, 1168,1093, 1054, 1014, 958, 897, 834, 754, 735.FAB-MC 904 [МН+] Пример 4. 9-деоксо-9 а-N-N'-[(2-хлор-6-метилфенил)карбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (1,5 г; 0,0024 моль), 2-хлор-6-метилфенилизоцианата (0,37 г; 0,00228 моль) и толуола (15 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (1,85 г). Хроматографией на колонке с силикагелем с использованием системы растворителей хлористый метилен метанол 90:5 получали хроматографически гомогенный продукт (1,36 г), имеющий следующие физико-химические константы: ИК (КВr) см-1 3437, 2973, 2937, 1732, 1645,1595, 1510, 1456, 1379, 1280, 1167, 1010, 1053,1014, 959, 897, 864, 835, 771. Пример 5. 9-деоксо-9 а-N-N'-[(3-фторфенил)карбамоил]-9 а-аза-9 а-гомоэритромицин А.(0,61 г; 0,00448 моль) и толуола (40 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (3,60 г). Кристаллизацией из смеси ацетон-петролейный эфир получали хроматографически гомогенный продукт (2,64 г),имеющий следующие физико-химические константы: Точка плавления 140-143 С ИК (КВr) см-1 3454, 2975, 2939, 1712, 1651,1602, 1537, 1494, 1443, 1380, 1317, 1278, 1247,1167, 1053, 1013, 959, 896, 865, 835, 772, 681.(0,68 г; 0,00448 моль) и толуола (40 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (3,52 г). Кристаллизацией из диэтилового эфира получали хроматографически гомогенный продукт (1,29 г), имеющий следующие физико-химические константы: ИК (КВr) см-1 3452, 2974, 2939, 2787, 1713,1669, 1592, 1526, 1484, 1456, 1423, 1380, 1300,1274, 1246, 1167, 1110, 1013, 958, 897, 834, 775,681. 1 Н ЯМР (300 Гц, CDCl3)7,44-6,94(Ph),4,93 (Н-13), 4,81 (Н-1"), 4,42 (Н-1'), 4,06 (Н-5"),4,04 (Н-3), 3,90 (Н-11), 3,83 (Н-9 а), 3,56 (Н-5'),3,51 (Н-5), 3,32 (Н-2' ), 3,28 (3"-ОСН 3), 2,96 (Н 4"), 2,70 (Н-2), 2,59 (Н-3'), 2,46 (Н-9b), 2,38 (Н 8), 2,36 (3'-N(CH3)2), 2,30 (Н-2"а), 1,94 (Н-14 а),1,89 (Н-4), 1,72 (Н-4'), 1,58 (Н-14b), 1,54 (Н-2"b),1,42 (10-СН 3), 1,27 (2-СН 3), 1,23 (5"-СН 3), 1,21 8 ремешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (1,94 г). Кристаллизацией из смеси ацетон - петролейный эфир получали хроматографически гомогенный продукт, имеющий следующие физико-химические константы: ИК (КВr) см-1 3446, 3291, 2974, 2936, 1727,1638, 1582, 1546, 1475, 1418, 1402, 1381, 1312,1286, 1226, 1167, 1066, 995, 874, 855, 788, 774,745, 685, 641. FAB-MC [МН+] Пример 8. 9-деоксо-9 а-N-N'-[(3-фторфенил)тиокарбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (3,0 г; 0,00408 моль), 3-фторфенилизотиоцианата (0,6 г; 0,00448 моль) и толуола (40 мл) при перемешивании в течение 24 ч при температуре 50 С и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (3,25 г). Хроматографией на колонке с силикагелем, с использованием системы растворителей хлористый метиленметанол 9:1, получали хроматографически гомогенный продукт (1,08 г), имеющий следующие физико-химические константы: ИК (КВr) см-1 3435, 2971, 2937, 1728, 1712,1611, 1515, 1493, 1456, 1379, 1313, 1279, 1168,1093, 1052, 1011, 959, 896, 832, 778, 727, 636.FAB-MC 888 [МН+] Пример 9. 9-деоксо-9 а-N-N'-[(3-хлорфенил)тиокарбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (3,0 г; 0,00408 моль), 3-хлорфенилизотиоцианата (0,76 г; 0,00448 моль) и толуола (40 мл) при перемешивании в течение 24 ч при температуре 40 С и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (3,51 г). Кристаллизацией из диэтилового эфира получали хроматографически гомогенный продукт (2,25 г), имеющий следующие физико-химические константы: ИК (КВr) см-1 3436, 2974, 2938, 1712, 1683,1594, 1483, 1460, 1424, 1378, 1308, 1167, 1092,1053, 1014, 958, 896, 835, 782, 727. 1 Н ЯМР (300 Гц, CDC13)7,47-7,12(Ph),4,85 (H-l"), 4,81 (Н-13), 4,42 (Н-1'), 4,11 (Н-3),4,08 (Н-5"), 3,50 (Н-5'), 3,48 (Н-5), 3,29 (3"ОСН 3), 3,25 (Н-2'), 3,04 (Н-9 а), 3,02 (Н-4"), 2,80(20 мл) при перемешивании в течение 24 ч при температуре 60 С и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (1,92 г). Кристаллизацией из смеси ацетон-петролейный эфир получали хроматографически гомогенный продукт (0,99 г), имеющий следующие физико-химические константы: ИК (КВr) см-1 3434, 2970, 2936, 2024, 1730,1591, 1456, 1379, 1310, 1167, 1093, 1052, 1012,958, 896, 823, 777, 730, 636.(0,68 г; 0,00448 моль) и толуола (40 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (3,54 г). Кристаллизацией из горячего ацетона получали хроматографически гомогенный продукт (2,16 г), имеющий следующие физико-химические константы: ИК (КВr) см-1 3444, 2975, 2938, 1713, 1651,1593, 1520, 1495, 1457, 1379, 1305, 1244, 1166,1092, 1053, 1013, 959, 896, 829, 755.(0,89 г; 0,00448 моль) и толуола (40 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (4,30 г). Кристаллизацией из смеси ацетон - петролейный эфир получали хроматографически гомогенный продукт (2,20 г),имеющий следующие физико-химические константы: ИК (КВr) см-1 3531, 3438, 2977, 2938, 1708,1683, 1651, 1589, 1520, 1492, 1460, 1377, 1305,1287, 1244, 1165, 1092, 1053, 1012, 959, 864, 825,755, 731, 639. 10 Пример 13. 9-деоксо-9 а-N-N'-[(4-хлорфенил)тиокарбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (3,0 г; 0,00408 моль), 4-хлорфенилизотиоцианата (0,76 г; 0,00448 моль) и толуола (40 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (3,71 г). Кристаллизацией из горячего ацетона получали хроматографически гомогенный продукт (3,26 г), имеющий следующие физико-химические константы: ИК (КВr) см-1 3534, 3422, 2978, 2939, 2879,1699, 1683, 1651, 1586, 1530, 1495, 1461, 1409,1378, 1310, 1279, 1260, 1229, 1167, 1094, 1052,1012, 952, 894, 865, 833, 727.FAB-MC 904 [МН+] Пример 14. 9-деоксо-9 а-N-N'-[(4-бромфенил)тиокарбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (1,5 г; 0,00204 моль), 4-бромфенилизотиоцианата (0,47 г; 0,00228 моль) и толуола (25 мл) при перемешивании в течение 12 ч при температуре 50 С и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (2,01 г). Кристаллизацией из смеси ацетон - петролейный эфир получали хроматографически гомогенный продукт (1,92 г), имеющий следующие физико-химические константы: ИК (КВr) см-1 3533, 3433, 2974, 2937, 2878,2786, 1703, 1682, 1626, 1588, 1526, 1492, 1460,1377, 1312, 1282, 1166, 1093, 1053, 1011, 958,895, 864, 831, 730.(15 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (1,99 г). Кристаллизацией из смеси этилацетат - (н-гексан) получали хроматографически гомогенный продукт(1,28 г), имеющий следующие физикохимические константы: ИК (КВr) см-1 3444, 2976, 2940, 1732, 1713,1663, 1531, 1486, 1456, 1417, 1380, 1325, 1263,1168, 1135, 1112, 1093, 1053, 1031, 1012, 958,896, 830. 11 мл) при перемешивании в течение 3 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (1,89 г). Кристаллизацией из смеси этилацетат - (н-гексан) получали хроматографически гомогенный продукт (1,14 г), имеющий следующие физико-химические константы: ИК (КВr) см-1 3438, 2976, 2939, 1732, 1670,1651, 1582, 1514, 1487, 1464, 1409, 1381, 1300,1167, 1053, 1015, 959, 895, 863, 820, 760.FAB-MC 922,4 [МН+] Пример 17. 9-деоксо-9a-N-N'-[(2,4-дихлорфенил)тиокарбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (1,5 г; 0,00204 моль), 2,4-дихлорфенилизотиоцианата (0,45 г; 0,00228 моль) и толуола (15 мл) при перемешивании в течение 7 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (1,96 г). Кристаллизацией из смеси этилацетат - (н-гексан) получали хроматографически гомогенный продукт (1,22 г), имеющий следующие физикохимические константы: ИК (КВr) см-1 3425, 2975, 2936, 1737, 1590,1505, 1460, 1379, 1311, 1166, 1092, 1051 1013,956, 903, 864, 834, 759, 730.(15 мл) при перемешивании в течение 7 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (1,96 г). Кристаллизацией из смеси этилацетат - (н-гексан) получали хроматографически гомогенный продукт(1,22 г), имеющий следующие физикохимические константы: 1 Н ЯМР (300 Гц, CDC13)8,06 (9aNCONH), 7,57-7,10(Ph), 5,04 (Н-13), 4,82 (H-l"),4,41 (Н-1'), 4,07 (Н-5"), 4,05 (Н-3), 3,87 (Н-11),3,63 (Н-5'), 3,49 (Н-5), 3,32 (Н-2' ), 3,27 (3"ОСН 3), 2,97 (Н-4"), 2,68 (Н-2), 2,61 (Н-3'), 2,38(40 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (10,51 г). Хроматографией на колонке с силикагелем, с использованием системы хлористый метилен - метанол- концентрированный аммиак 9:9:1,5, получали продукт (4,1 г), который после кристаллизации из смеси диэтиловый эфир - петролейный эфир имеет следующие физико-химические константы: Точка плавления 122-125 С ИК (КВr) см-1 3444, 2974, 2939, 1733, 1651,1544, 1494, 1447, 1380, 1259, 1166, 1125, 1093,1070, 1053, 1014, 957, 897, 834, 795, 699.FAB-MC 922,4 [МН+] Пример 20. 9-деоксо-9 а-N-N'-[(4-трифторметилфенил)карбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (3,0 г; 0,00408 моль), 4-трифторметилфенилизоцианата (0,84 г; 0,00448 моль) и толуола (40 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали осадок (3,75 г). Из неочищенного продукта (1,2 г) кристаллизацией из смеси этилацетат - (н-гексан) получали названный в заголовке продукт (0,99 г), имеющий следующие физикохимические константы: ИК (КВr) см-1 3445, 2974, 2939, 1731, 1668,1602, 1526, 1457, 1413, 1380, 1325, 1249, 1166,1115, 1068, 1054, 1015, 959, 897, 838. 1 Н ЯМР (300 Гц, CDCl3)8,25, (9aNCONH), 7,65-7,20(Ph), 4,91 (Н-13), 4,82 (H-l"),4,41 (Н-1'), 4,03 (Н-5"), 4,06 (Н-3), 3,91 (Н-11),3,51 (Н-5'), 3,54 (Н-5), 3,30 (Н-2'), 3,28 (3"ОСН 3), 2,97 (Н-4"), 2,71 (Н-2), 2,55 (Н-3'), 2,39FAB-MC 922,4 [МН+] Пример 21. 9-деоксо-9 а-N-N'-[(3-трифторметилфенил)тиокарбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (7,27 г; 0,00989 моль), 3-трифторметилфенмлизотиоцианата (2,64 г; 0,01299 моль) и толуола (40 мл) при перемешивании в течение 1 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (9,27 г). Из неочищенного продукта (1,0 г) кристаллизацией из смеси ацетон-петролейный эфир получали названный в заголовке продукт (0,6 г), имеющий следующие физико-химические константы: Точка плавления 110-112 С ИК (КВr) см-1 3454, 2975, 2938, 1734, 1599,1531, 1494, 1453, 1378, 1331, 1252, 1166, 1124,1093, 1051, 1012, 957, 904, 698. 1 Н ЯМР (300 Гц, CDC13) 7,85-7,27(Ph),4,86 (H-l"), 4,81 (Н-13), 4,43 (Н-1'), 4,11 (Н-3),4,07 (Н-5"), 3,51 (Н-5' ), 3,46 (Н-5), 3,29 (3"ОСН 3), 3,25 (Н-2'), 3,05 (Н-9 а), 3,04 (Н-4"), 2,80FAB-MC 938,6 [MH+] Пример 22. 9-деоксо-9 а-N-N'-[(2-трифторметоксифенил)карбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (1,5 г; 0,00204 моль), 2-трифторметоксифенилизоцианата (0,44 г; 0,00228 моль) и толуола (15 мл) при перемешивании в течение 3 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (1,94 г). Кристаллизацией из смеси этилацетат - (н-гексан) 14 получали хроматографически гомогенный продукт (1,39 г), имеющий следующие физикохимические константы: Точка плавления 126-128 С ИК (КВr) см-1 3466, 2974, 2938, 1732, 1669,1610, 1531, 1455, 1380, 1315, 1250, 1217, 1169,1109, 1094, 1054, 1013, 958, 897, 836, 758, 630.FAB-MC 938,5 [МН+] Пример 23. 9-деоксо-9 а-N-N'-[(4-трифторметоксифенил)тиокарбамоил]-9 а-аза-9 а-гомоэритромицин А. Из 9-деоксо-9 а-аза-9 а-гомоэритромицина А (1,5 г; 0,00204 моль), 4-трифторметоксифенилизотиоцианата (0,44 г; 0,00228 моль) и толуола (15 мл) при перемешивании в течение 2 ч при комнатной температуре и выпариванием реакционной смеси при пониженном давлении получали неочищенный продукт (1,89 г). Кристаллизацией из смеси этилацетат - (н-гексан) получали хроматографически гомогенный продукт (1,15 г), имеющий следующие физикохимические константы: Точка плавления 139-141 С ИК (КВr) см-1 3456, 2975, 2940, 1731, 1669,1511, 1457, 1414, 1380, 1265, 1199, 1166, 1111,1054, 1015, 958, 897, 836. в которой R означает замещенную арильную группу формулы (II) в которой заместители а, b, с, d и е являются одинаковыми или различными и по крайней мере один из них означает галоген, (C1-С 6)галоидалкил или(С 1-С 6)галоидалкоксигруппу, тогда как остальные заместители представляют водород, галоген, (С 1-С 6)алкил или (С 1-С 6)алкоксигруппу, и X означает кислород или серу, и их фармацевтически приемлемые аддитивные соли с неорганическими или органическими кислотами. 2. Соединения по п.1, отличающиеся тем,что а означает галоген, b, с, d и е являются оди 15 наковыми и означают водород и X представляет кислород или серу. 3. Соединение по п.2, отличающееся тем,что а означает фтор и X означает кислород. 4. Соединение по п.2, отличающееся тем,что а означает фтор и X означает серу. 5. Соединение по п.2, отличающееся тем,что а означает хлор, а X означает серу. 6. Соединения по п.1, отличающиеся тем,что а означает галоген, b, с, и d являются одинаковыми и означают водород, е представляет (C1C4)алкил, а X означает кислород или серу. 7. Соединение по п.6, отличающееся тем,что а означает хлор, b, с и d являются одинаковыми и означают водород, е представляет метил, а X является кислородом. 8. Соединения по п.1, отличающиеся тем,что а, с, d и е являются одинаковыми и означают водород, b означает галоген, а X является кислородом или серой. 9. Соединение по п.8, отличающееся тем,что b означает фтор, а X является кислородом. 10. Соединение по п.8, отличающееся тем,что b означает хлор, а X является кислородом. 11. Соединение по п.8, отличающееся тем,что b означает бром, X является кислородом. 12. Соединение по п.8, отличающееся тем,что b означает фтор, а X является серой. 13. Соединение по п.8, отличающееся тем,что b означает хлор, а X является серой. 14. Соединение по п.8, отличающееся тем,что b означает бром, а X является серой. 15. Соединения по п.1, отличающиеся тем,что a, b, d и е являются одинаковыми и означают водород, с означает галоген, а X представляет кислород или серу. 16. Соединение по п.15, отличающееся тем, что с означает хлор, а X представляет кислород. 17. Соединение по п.15, отличающееся тем, что с означает бром, а X представляет кислород. 18. Соединение по п.15, отличающееся тем, что с означает хлор, а X представляет серу. 19. Соединение по п.15, отличающееся тем, что с означает бром, а X представляет серу. 20. Соединения по п.1, отличающиеся тем,что a, d и е являются одинаковыми и означают водород, b представляет (C1-С 6)галоидалкил, с означает галоген, а X является кислородом или серой. 21. Соединение по п.20, отличающееся тем, что a, d и е являются одинаковыми и означают водород, b представляет -CF3, с означает хлор, а X представляет кислород. 22. Соединения по п.1, отличающиеся тем,что b, d и е являются одинаковыми и означают водород, а и с являются одинаковыми и означают галоген, а X представляет кислород или серу. 23. Соединение по п.22, отличающееся тем, что а и с являются одинаковыми и означают хлор, а X представляет кислород. 16 24. Соединение по п.22, отличающееся тем, что а и с являются одинаковыми и означают хлор, а X представляет серу. 25. Соединения по п.1, отличающиеся тем,что а, b, с, d и е являются одинаковыми или различными и означают водород или группу (С 1 С 4)галоидалкила, а X представляет кислород или серу. 26. Соединение по п.25, отличающееся тем, что а представляет -CF3, b, с, d и е являются одинаковыми и означают водород, а X представляет кислород. 27. Соединение по п.25, отличающееся тем, что а, с, d и е являются одинаковыми и означают водород, b представляет -CF3, a X является кислородом. 28. Соединение по п.25, отличающееся тем, что a, b, d и е являются одинаковыми и означают водород, с представляет -CF3, a X означает кислород. 29. Соединение по п.25, отличающееся тем, что а, с, d и е являются одинаковыми и означают водород, b представляет -CF3, a X означает серу. 30. Соединения по п.1, отличающиеся тем,что а, b, с, d и е являются одинаковыми или различными и означают водород или (С 1 С 4)галоидалкоксигруппу, а X представляет кислород или серу. 31. Соединение по п.30, отличающееся тем, что b, с, d и е являются одинаковыми и означают водород, а представляет -OCF3, a X означает кислород. 32. Соединение по п.30, отличающееся тем, что a, b, d и е являются одинаковыми и означают водород, с представляет -OCF3, a X означает кислород. 33. Способ получения галоидпроизводных 9a-N-(N'-арилкарбамоил)- и 9a-N-(N'-арилтиокарбамоил)-9-деоксо-9 а-аза-9 а-гомоэритромицина А общей формулы (I) в которой R означает замещенную арильную группу формулы (II) в которой заместители а, b, с, d и е являются одинаковыми или различными и по крайней мере один из них означает галоген, (C1-C6)галоидалкил или (С 1-С 6)галоидалко-ксигруппу, а остальные заместители представляют водород,галоген, (С 1-С 6)алкил или (C1-С 6)алкоксигруппу и X означает кислород или серу, и их серу, и их фармацевтически приемлемых аддитивных солей с неорганическими или органическими кислотами, отличающийся тем, что 9 деоксо-9 а-аза-9 а-гомоэритромицин А подвергают реакции с изоцианатами или изотиоцианатами общей формулы (III)R - N = С = X (III),в которой R и X имеют указанные выше значения, в апротонном растворителе, предпочти 18 тельно толуоле, при комнатной температуре или при повышенной до 60. 34. Фармацевтическая композиция, отличающаяся тем, что она содержит фармацевтически приемлемый носитель и антибактериально эффективное количество соединений по п.1. 35. Применение соединений по любому из пп.1-32 для лечения или предотвращения бактериальных инфекций.
МПК / Метки
МПК: C07H 17/08, A61P 31/04, A61K 31/7048
Метки: 9-деоксо-9а-аза-9а-гомоэритромицина, галоидпроизводные
Код ссылки
<a href="https://eas.patents.su/10-5214-galoidproizvodnye-9-deokso-9a-aza-9a-gomoeritromicina-a.html" rel="bookmark" title="База патентов Евразийского Союза">Галоидпроизводные 9-деоксо-9а-аза-9а-гомоэритромицина а</a>
Следующий патент: Алкилированные производные имидазопиридина
Случайный патент: Способ получения легких олефинов в реакционной системе, объединенной с установкой для разделения воздуха











