Твердая лекарственная форма, содержащая полиморфную форму 1 клопидогрела гидросульфата
Номер патента: 15440
Опубликовано: 31.08.2011
Авторы: Левентисне Хусар Магдольна, Жигмонд Жольт, Славине Селл Жужа, Фекете Паль, Пальфи Зольтанне, Сабёне Ревес Пироска, Буресне Папп Цецилла
Формула / Реферат
1. Твердая лекарственная форма, содержащая полиморфную форму 1 клопидогрела гидросульфата формулы
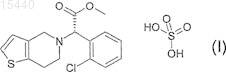
в качестве активного ингредиента, микрокристаллическую целлюлозу и коллоидный диоксид кремния в качестве наполнителя и связывающего вещества, дезинтегрирующий агент и смазывающее вещество в качестве дополнительных эксципиентов.
2. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 20-40 мас.% полиморфной формы 1 клопидогрела гидросульфата, 40-65 мас.% микрокристаллической целлюлозы, 0,5-10 мас.% коллоидного диоксида кремния, 3-20 мас.% дезинтегрирующего агента и 1-5 мас.% смазывающего вещества.
3. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 25-35 мас.% полиморфной формы 1 клопидогрела гидросульфата, 45-65 мас.% микрокристаллической целлюлозы, 0,5-10 мас.% коллоидного диоксида кремния, 3-10 мас.% дезинтегрирующего агента и 1-5 мас.% смазывающего вещества.
4. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 25-35 мас.% композиции полиморфной формы 1 клопидогрела гидросульфата, 55-65 мас.% микрокристаллической целлюлозы, 1-5 мас.% коллоидного диоксида кремния, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы в качестве дезинтегрирующего агента и 1-5 мас.% гидрогенизированного касторового масла в качестве смазывающего вещества.
5. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 20-40 мас.% полиморфной формы 1 клопидогрела гидросульфата, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы в качестве дезинтегрирующего агента и 1-5 мас.% гидрогенизированного касторового масла в качестве смазывающего вещества, где коллоидный диоксид кремния и микрокристаллическая целлюлоза образуют композитный состав, составляющий 40-65 мас.% от массы композиции.
6. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 25-35 мас.% полиморфной формы 1 клопидогрела гидросульфата, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы в качестве дезинтегрирующего агента и 1-5 мас.% гидрогенизированного касторового масла в качестве смазывающего вещества, где коллоидный диоксид кремния и микрокристаллическая целлюлоза образуют композитный состав, составляющий 45-65 мас.% композиции.
7. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 25-35 мас.% композиции полиморфной формы 1 клопидогрела гидросульфата, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы в качестве дезинтегрирующего агента и 1-5 мас.% гидрогенизированного касторового масла в качестве смазывающего вещества, где коллоидный диоксид кремния и микрокристаллическая целлюлоза образуют композитный состав, составляющий 55-65 мас.% композиции.
8. Твердая лекарственная форма по любому из пп.1-7, представляющая собой таблетку, таблетку с пленочным покрытием или капсулу, предпочтительно таблетку с пленочным покрытием.
9. Твердая лекарственная форма по п.8, представляющая собой таблетку с пленочным покрытием, на которую нанесено 2-5 мас.% от общей массы композиции водорастворимого покрытия.
10. Твердая лекарственная форма по любому из пп.1-9, отличающаяся тем, что применяемая микрокристаллическая целлюлоза имеет размер частиц более 90 мкм или представляет собой ProsolvÒ HD 90.
11. Твердая лекарственная форма по любому из пп.1-10, отличающаяся тем, что коллоидный диоксид кремния имеет удельную поверхность 150 м2/г, предпочтительно 200 м2/г.
12. Твердая лекарственная форма по любому из пп.1-3 или 8-11, отличающаяся тем, что применяемый дезинтегрирующий агент выбран из природного или пептизированного крахмала, поперечно-сшитого поливинилпирролидона или низкозамещенной гидроксипропилцеллюлозы, предпочтительно низкозамещенной гидроксипропилцеллюлозы.
13. Твердая лекарственная форма по любому из пп.1-3 и 8-12, отличающаяся тем, что применяемое смазывающее вещество выбрано из жирных кислот, эфиров жирных кислот, гидрогенизированных растительных масел, предпочтительно гидрогенизированного касторового масла.
14. Способ получения твердой лекарственной формы по любому из пп.1-13, отличающийся тем, что полиморфную форму 1 клопидогрела гидросульфата, микрокристаллическую целлюлозу, коллоидный диоксид кремния или композитное вещество, полученное из микрокристаллической целлюлозы и коллоидного диоксида кремния, или их смесь смешивают с дезинтегрирующим агентом и смазывающим веществом, полученную смесь гомогенизируют и формуют с получением твердой лекарственной формы.
15. Способ по п.14, отличающийся тем, что гомогенизированную порошкообразную смесь прессуют в таблетки путем прямого прессования и таблетки, при необходимости, покрывают водорастворимым покрытием.
16. Способ по п.14, отличающийся тем, что гомогенизированной порошкообразной смесью заполняют капсулы.
17. Способ получения твердой лекарственной формы по п.8, характеризующийся тем, что 25-35 мас.% полиморфной формы 1 клопидогрела гидросульфата, 55-65 мас.% микрокристаллической целлюлозы, 1-5 мас.% коллоидного диоксида кремния или 55-65 мас.% композитного состава микрокристаллической целлюлозы и коллоидного диоксида кремния, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы и 1-5 мас.% гидрогенизированного касторового масла относительно общей массы лекарственной формы смешивают, гомогенизируют, полученный гомогенизат помещают в капсулы или прессуют в таблетки путем прямого прессования, и таблетки, при необходимости, покрывают водорастворимым покрытием.
Текст
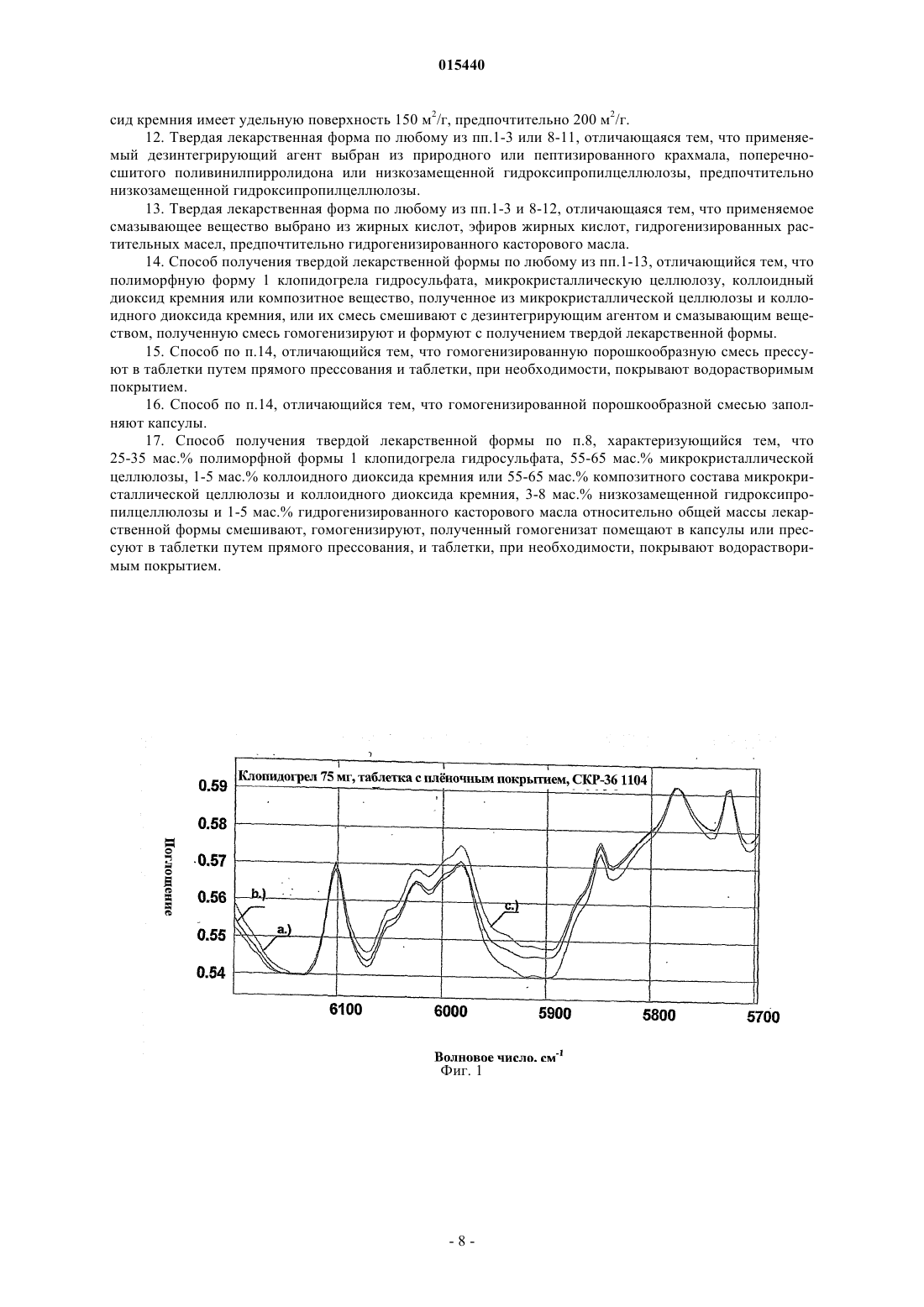
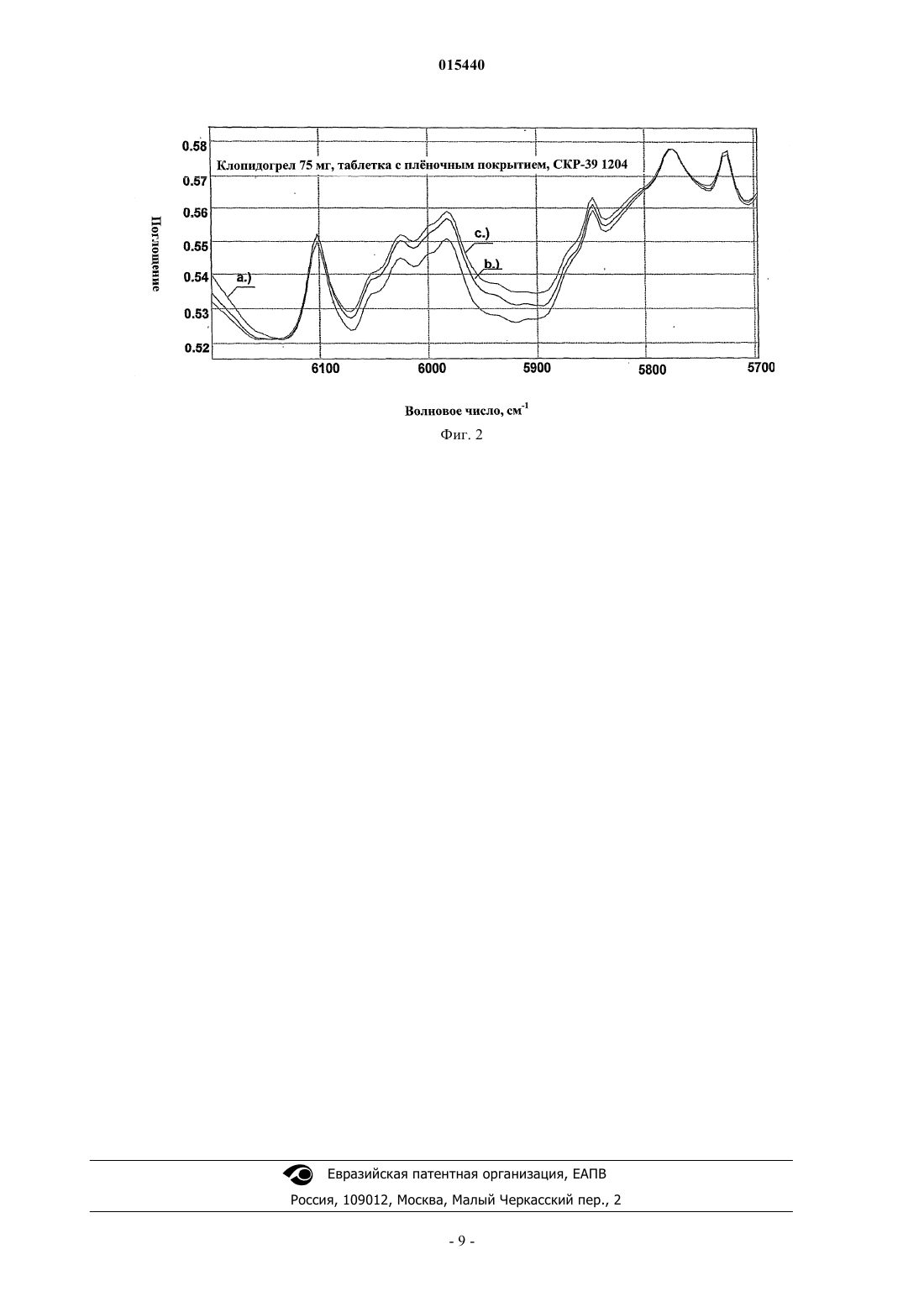
ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ЕВРАЗИЙСКОМУ ПАТЕНТУ Дата публикации и выдачи патента ТВЕРДАЯ ЛЕКАРСТВЕННАЯ ФОРМА, СОДЕРЖАЩАЯ ПОЛИМОРФНУЮ ФОРМУ 1 КЛОПИДОГРЕЛА ГИДРОСУЛЬФАТА Настоящее изобретение относится к твердым лекарственным формам (таблеткам, таблеткам с пленочным покрытием, капсулам), содержащим полиморфную форму 1 клопидогрела гидросульфата. Фекете Паль, Славине Селль Жужа,Сабне Ревес Пироска, Жигмонд Жольт, Левентисне Хусар Магдольна,Пальфи Зольтанне, Буресне Папп Цецилла (HU) Кузнецова Ю.В., Пантелеев А.С.,Ильмер Е.Г. (RU)(71)(73) Заявитель и патентовладелец: ЭГИШ ДЬДЬСЕРДЬЯР НЬИЛЬВАНОШАН МЮКД РЕСВЕНЬТАРШАШАГ (HU) 015440 Область техники, к которой относится изобретение Настоящее изобретение относится к фармацевтическим композициям, содержащим полиморфную форму 1 (S)-(+)-(2-хлорфенил)-2-(6,7-дигидро-4H-тиено[3,2-с]пиридин-5-ил)ацетата гидросульфата (международное непатентованное название клопидогрела гидросульфат) формулы Эти фармацевтические композиции ингибируют образование бляшек в артериях и развитие артериосклероза. Химическая формула клопидогрела гидросульфата C16H16ClNO2SH2SO4. Активный ингредиент представляет собой белый или почти белый порошок, имеющий очень низкую растворимость в воде при нейтральном значении рН, но хорошую растворимость в водных кислых условиях. Растворимость соединения в метаноле и этаноле также хорошая, но в эфире низкая. Известно несколько кристаллических полиморфных форм и аморфная форма клопидогрела гидросульфата. В частности, настоящее изобретение относится к фармацевтическим композициям, содержащим кристаллическую полиморфную форму 1 клопидогрела гидросульфата, другие вспомогательные вещества и наполнители, что приводит к долговременной химической и кристаллографической устойчивости чувствительного активного ингредиента. Фармацевтические композиции по настоящему изобретению имеют очень хорошую скорость растворения, даже после хранения в течение долгого времени. Предшествующий уровень техники Различные полиморфные формы обычно имеют различные физические свойства и устойчивость. С точки зрения химической стабильности и старения фармацевтической композиции выбор подходящей полиморфной формы является решающим. Для клопидогрела гидросульфата известно несколько полиморфных форм. Полиморфизм клопидогрела впервые был упомянут в описании заявки на международный патент WO 99/65915. Различают полиморфные формы 1 и 2. Полиморфную форму 2 описывают как новую полиморфную форму, а полиморфную форму 1 идентифицируют по ее температуре плавления как полиморфную форму, раскрытую в описании европейского патента ЕР 281459. Недавно появившийся в продаже продукт согласно рентгеноструктурным исследованиям содержит полиморфную форму 2, термодинамически более стабильную. В международной заявке на патент WO 03/051362 раскрыты аморфная форма и полиморфные формы III, IV, V, VI. Аморфная форма и различные полиморфные формы имеют различные термические свойства, температуры плавления, кривые ДСК (дифференциальная сканирующая калориметрия), термогравиметрические характеристики, рентгенограммы и инфракрасные спектры. На основании этих данных различные полиморфные формы можно хорошо отличить друг от друга. Эти полиморфные формы имеют сильно отличающиеся растворимость, текучесть, а также прессуемость. Эти свойства очень важны и должны учитываться при разработке новых фармацевтических составов. Скорость растворения аморфной формы и различных полиморфных форм в водных средах очень важна. Растворимость активного ингредиента после введения пациенту в составе фармацевтической композиции может также влиять на терапевтический эффект. Низкая скорость растворения может уменьшать скорость абсорбции или общее количество поглощенного активного фармацевтического ингредиента. Обычно термодинамически менее устойчивые полиморфные формы имеют более высокие скорости растворения. Скорость растворения активного фармацевтического ингредиента фармацевтической композиции,кроме его полиморфной формы, зависит от состава рецептуры и изменений, происходящих при прессовании и хранении таблеток. Меньшая химическая стабильность полиморфных форм, имеющих большую растворимость, является недостатком, поэтому в случае применения этих полиморфных форм обычно изменять рецептуру для композиций, которые были разработаны для применения более устойчивой полиморфной формы. При использовании этих полиморфных форм влажное гранулирование неприемлемо, поскольку в процессе смачивания может очень легко произойти перекристаллизация активного ингредиента, в результате чего образуется менее растворимая полиморфная форма. Химическая стабильность используемого клопидогрела гидросульфата является решающим фактором, потому что известна его несовместимость с некоторыми вспомогательными веществами, такими как стеарат магния, повидон, желатин. В присутствии этих соединений образование продуктов разложения происходит быстрее. Присутствие влаги в фармацевтической композиции также вызывает более быстрое разложение клопидогрела. Ни в описании вышеупомянутой международной заявки на патент WO 99/65915, ни в описании ме-1 015440 ждународной заявки на патент WO 03/0513915 не раскрыты рецептуры фармацевтических композиций,где используются различные полиморфные формы, и ничего не говорится о стабильности их фармацевтических композиций. Несколько полиморфных форм описано в заявке на международный патент WO 03/051362, кроме того, там подробно описаны вспомогательные вещества и наполнители, которые пригодны для получения твердых или жидких лекарственных форм. Информация, раскрытая в данном документе, представляет собой простой список вспомогательных веществ и наполнителей. Нет никакого указания на способ получения устойчивых фармацевтических композиций и выбор подходящих вспомогательных веществ,наполнителей, новых или известных полиморфных форм. Некоторые перечисленные соединения согласно ранее опубликованной заявке на европейский патент ЕР 1310245, например стеарат магния или кальция, могут вызывать разложение до 3,8% активного ингредиента фармацевтической композиции. Кроме того, заявка на международный патент WO 03/051362 не содержит каких-либо данных относительно стабильности фармацевтических композиций и примеров их получения. Активные ингредиенты, имеющие подобную дигидротиен[3,2]пиридиловую химическую структуру, являются очень реакционноспособными. Химическая структура тиклодипина формулы отличается от структуры клопидогрела только тем, что в клопидогреле атом водорода замещен метоксикарбонильной группой. Имеется несколько изобретений, относящихся к фармацевтическим композициям, содержащим тиклодипин. В этих описаниях раскрыты непригодные вспомогательные вещества и наполнители. Согласно авторам патента US 5520928 тиклодипин и подобные соединения разлагаются неожиданно быстро в присутствии некоторых известных наполнителей, таких как желатин, повидон или стеарат магния. Согласно описанию международной заявки на патент WO 00/01364 применение крахмалгликолята натрия также приводит к разложению активного ингредиента. Согласно этому изобретению устойчивые фармацевтические композиции могут быть получены с использованием гидрофильных поверхностно-активных веществ, например полиэтиленгликолей, и приемлемых эксципиентов. Поэтому не удивительно, что в случае фармацевтических композиций, содержащих подобный фармацевтически активный ингредиент, а именно клопидогрел, возникли проблемы стабильности. В литературе предлагаются некоторые технические решения для улучшения устойчивости при хранении фармацевтических композиций, содержащих клопидогрел. Согласно описанию заявки на европейский патент ЕР 1310245 вместо стеарата магния предлагается применять стеарат цинка или стеарилфумарат натрия, поскольку было обнаружено, что смазывающая активность гидрогенизированного касторового масла, используемого в композиции, имеющейся в продаже, является неудовлетворительной. Согласно описанию международной заявки на патент WO 2005/070464 для улучшения стабильности таблеток вместо стеарата магния применяют гидрогенизированные растительные масла, а для решения проблем таблетирования предлагается применение карбоксиметилкрахмала натрия. Применение гидрогенизированных растительных масел для улучшения стабильности хорошо известно из литературы,кроме того, оно уже было описано для имеющейся в продаже композиции. Однако в заявке нет никаких данных об улучшениях по сравнению с известными композициями, являющихся следствием применения большего количества смазывающего вещества, чем обычно. В вышеупомянутых заявках на патент не описаны ни используемые полиморфные формы, ни уменьшение скорости растворения клопидогрела при долговременном хранении композиции. Недавно в продажу поступила фармацевтическая композиция в форме таблетки с покрытием, которая содержит 97,9 мг клопидогрела гидросульфата в виде полиморфной формы 2, что соответствует 75 мг основания клопидогрела. Композиция была разработана с учетом вышеупомянутой несовместимости. В качестве наполнителя применяют маннит, одно из наименее гигроскопичных веществ, (равновесное содержание влаги в нем составляет 0,3% при относительной влажности 75%). В качестве дезинтегрирующего агента применяют гидроксипропилцеллюлозу, инертное вещество эфирного типа. В качестве смазывающего вещества применяют смазывающее вещество эфирного типа - гидрогенизированное касторовое масло (Cutina H), а также смазывающее вещество эфирного и спиртового типа - полиэтиленгликоль. В качестве дополнительного наполнителя композиция содержит микрокристаллическую целлюлозу, а покрытие содержит гидроксипропилметилцеллюлозу, триацетин, карнаубский воск, диоксид титана и железоокисные пигменты. Быстрое растворение клопидогрела гидросульфата является очень важным. Для улучшения скорости растворения больше подходит применение менее устойчивых полиморфных форм, имеющих лучшую растворимость. Авторы венгерской заявки на патент Р 0402633 раскрывают аморфную форму клопидогрела гидросульфата. С точки зрения растворимости композиция, содержащая эту форму, является очень предпочтительной. Однако получение твердой дисперсии имеет некоторые недостатки с точки зрения технологии.-2 015440 Согласно изобретению клопидогрела гидросульфат растворяют в подходящем органическом растворе,затем в этом растворе суспендируют коллоидную или микрокристаллическую целлюлозу или раствор наносят на поверхность микрокристаллической целлюлозы и растворитель удаляют. Применение органических растворителей и испарение в аппарате с псевдоожиженным слоем очень невыгодно с точки зрения экологии и технологии. Дополнительным недостатком является то, что конечную композицию можно получить только после нескольких последовательных технологических стадий. Стабильность вышеупомянутых полиморфных форм неизвестна. Полиморфную форму 1 получают согласно способу, раскрытому в описании европейского патента ЕР 281459. Эта лабильная полиморфная форма в подходящих условиях окружающей среды сохраняет свою химическую чистоту и полиморфную форму до составления рецептуры. Стабильность при хранении является очень важной, т.к. при длительном хранении менее устойчивая полиморфная форма активного ингредиента легко превращается в его более устойчивую полиморфную форму, что хорошо известно специалисту в данной области. Это превращение может происходить при составлении рецептуры или хранении и вызывать изменение растворимости композиции. Цель авторов настоящего изобретения заключалась в том, чтобы разработать устойчивую фармацевтическую композицию, содержащую полиморфную форму 1 клопидогрела гидросульфата, в которой активный ингредиент сохраняет свою химическую стабильность и морфологическую форму, а свойства растворимости отвечают требованиям Фармакопей даже после длительного хранения. Еще одна цель авторов настоящего изобретения заключалась в том, чтобы избежать применения органических растворителей в способе изготовления и найти менее сложный с точки зрения технологии способ получения упомянутой композиции. Краткое описание изобретения Согласно настоящему изобретению предложена фармацевтическая композиция, содержащая полиморфную форму 1 клопидогрела гидросульфата в качестве активного ингредиента, микрокристаллическую целлюлозу и коллоидный диоксид кремния или, при необходимости, силанизированную микрокристаллическую целлюлозу в качестве наполнителя и связывающего вещества, соединение целлюлозы эфирного типа в качестве дезинтегрирующего агента и соединение жирной кислоты эфирного типа в качестве скользящего вещества. Подробное описание изобретения Авторы настоящего изобретения неожиданным образом обнаружили, что скорости растворения фармацевтических композиций, содержащих ингредиенты, раскрытые выше, не уменьшились, несмотря на то, что в европейском патенте ЕР 1310245 раскрыто, что микрокристаллическая целлюлоза уменьшает скорость растворения клопидогрела гидросульфата из композиции. В фармацевтической композиции по настоящему изобретению полиморфная форма 1 не превращается в полиморфную форму 2. Кроме того,химическая стабильность активного ингредиента также является очень хорошей. Как ни странно, относительно высокое содержание микрокристаллической целлюлозы не уменьшает химическую и кристаллографическую стабильность композиции. Микрокристаллическая целлюлоза и коллоидный диоксид кремния представляют собой так называемые гигроскопичные соединения. Равновесное содержание влаги при относительной влажности 75% в микрокристаллической целлюлозе составляет приблизительно 8%, а в коллоидном диоксиде кремния составляет приблизительно 15%. На основании этих фактов, вследствие высокого содержания влаги для смесей полиморфной формы 1 клопидогрела гидросульфата с микрокристаллической целлюлозой и коллоидным диоксидом кремния можно ожидать скорее большего разложения и кристаллографического превращения, чем высокой химической и кристаллографической стабильности. Эти неожиданные факты подтверждаются данными табл. 1, где приведены данные по стабильности фармацевтической композиции согласно примеру 1, содержащей полиморфную форму 1 клопидогрела гидросульфата, как указано далее.-3 015440 Таблица 1 Примеси в таблетках с пленочным покрытием согласно настоящему изобретению Стабильность композиции является очень хорошей. Количество неидентифицированных примесей составляет менее 0,01%, а количество всех посторонних веществ составляет менее 0,5% после хранения в течение 6 месяцев в бутылке, закрытой полиэтиленовой пробкой, при 40 С и относительной влажности 75%. Для специалиста в данной области является неожиданным, что количество известных посторонних веществ, а именно свободной кислоты, образующейся при гидролизе активного ингредиента, составляет менее 0,2%, несмотря на то, что композиция содержит большое количество гигроскопичного ингредиента (приблизительно 60% Prosolv HD 90). Неожиданно оказалось, что полиморфная форма активного ингредиента остается неизменной при хранении. Это доказывается фиг. 1 и 2, на которых показаны спектры ближней инфракрасной области(ближней ИК-области) таблеток после получения и долговременного хранения. На фиг. 1 показаны спектры ближней ИК-области таблеток партии 361104, а на фиг. 2 показаны спектры таблеток ближней ИК-области партии 361204. Эти таблетки получают согласно примеру 1 и содержат клопидогрела гидросульфат полиморфной формы 1. На обоих чертежах спектры: а) сняты во время получения; б) сняты после длительного хранения в течение 3 месяцев при 40 С и относительной влажности 75%; в) сняты после длительного хранения в течение 6 месяцев при 40 С и относительной влажности 75%. Результаты исследований полиморфизма показывают, что оба продукта, полученные из партий 361104 и 361204, представляют собой идентичные полиморфные формы, а именно полиморфную форму 1. Нет никакого существенного различия между спектрами, следовательно композиции устойчивы также с точки зрения полиморфизма. Смесь микрокристаллической целлюлозы и коллоидного диоксида кремния оказывает благоприятное воздействие на растворимость активного ингредиента. Как показано в табл. 2, скорости растворения таблеток, полученных из смеси по настоящему изобретению, не уменьшаются после долговременного хранения. Таблица 2 Данные по растворимости таблеток, содержащих полиморфную форму 1 клопидогрела В случае композиции по настоящему изобретению не происходит никакого уменьшения скорости растворения при хранении вследствие выбора ингредиента, неожиданным образом оказавшегося подходящим. На основании вышеприведенных данных химическая стабильность композиций, содержащих полиморфную форму 1 клопидогрела, а также смесь микрокристаллической целлюлозы и коллоидного диок-4 015440 сида кремния в качестве связующего вещества и наполнителя, отвечает строгим требованиям Фармакопей. В частности, настоящее изобретение обеспечивает твердую лекарственную форму, которая содержит 20-40 мас.%, предпочтительно 25-35 мас.% клопидогрела гидросульфата полиморфной формы 1,40-65 мас.%, предпочтительно 45-65 мас.%, более предпочтительно 55-65 мас.% микрокристаллической целлюлозы, 0,5-10 мас.%, предпочтительно 1-5 мас.% коллоидного диоксида кремния, 3-20 мас.%, предпочтительно 3-10 мас.%, более предпочтительно 3-8 мас.% дезинтегрирующего агента и 1-5 мас.% смазывающего вещества, относительно общей массы композиции. Согласно настоящему изобретению вместо смеси микрокристаллической целлюлозы и коллоидного диоксида кремния можно применять композитный состав, полученный из микрокристаллической целлюлозы и коллоидного диоксида кремния. Твердые лекарственные формы согласно настоящему изобретению представляют собой таблетки или таблетки с плночным покрытием. Таблетки с плночным покрытием содержат 2-5 мас.% водорастворимой полимерной пленки на поверхности таблетки. Согласно наиболее предпочтительному примеру осуществления настоящего изобретения в качестве микрокристаллической целлюлозы композиция содержит микрокристаллическую целлюлозу, имеющую размер частиц более 90 мкм; Prosolv HD 90 в качестве силиконизированной микрокристаллической целлюлозы; коллоидный диоксид кремния, имеющий удельную поверхность более 150 м 2/г, предпочтительно более 200 м 2/г в качестве скользящего вещества; низкозамещенную гидроксипропилцеллюлозу в качестве дезинтегрирующего агента и гидрогенизированное касторовое масло в качестве смазывающего вещества. Еще одним примером осуществления настоящего изобретения является способ получения фармацевтической композиции, где полиморфную форму 1 клопидогрела гидросульфата, микрокристаллическую целлюлозу, коллоидный диоксид кремния или состав, полученный из микрокристаллической целлюлозы и коллоидного диоксида кремния или их смеси, дезинтегрирующий агент и смазывающее вещество смешивают, гомогенизируют и смесь переводят в галенову форму. В случае применения коллоидного диоксида кремния его гомогенизируют с частью микрокристаллической целлюлозы и просеивают. Получение твердых лекарственных форм согласно настоящему изобретению, таблеток, таблеток с плночным покрытием или капсул, содержащих полиморфную форму 1 клопидогрела гидросульфата и вышеупомянутые компоненты, можно выполнить с помощью обычных способов. Оптимизация способа относится к компетенции специалиста в данной области. При получении галеновой формы порошкообразную смесь прессуют в таблетки и, при необходимости, покрывают водорастворимым покрытием или порошкообразную смесь помещают в капсулы. Согласно наиболее предпочтительному примеру осуществления настоящего изобретения 25-35 мас.% относительно массы композиции полиморфной формы 1 клопидогрела гидросульфата смешивают с 55-65 мас.% микрокристаллической целлюлозы, 1-5 мас.% предпочтительно коллоидного диоксида кремния или с 55-65 мас.% композитного состава, содержащего микрокристаллическую целлюлозу и коллоидный диоксид кремния или их смесь, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы и 1-5 мас.% гидрогенизированного касторового масла, смесь гомогенизируют и помещают в капсулы,или гомогенизат прессуют в таблетки с использованием процесса прямого прессования, и, при необходимости, на полученные таблетки наносят водорастворимое покрытие. При разработке способа получения стабильной таблетки, содержащей полиморфную форму 1 клопидогрела, выполнили большое количество экспериментов. В случае применения поливинилпирролидона в качестве связывающего вещества скорость растворения была большой, но таблетки изменяли цвет после хранения в течение нескольких дней и активный ингредиент разлагался. В случае таблеток, содержащих маннит, гидроксипропилцеллюлозу и гидрогенизированное касторовое масло (Cutina H), стабильность полиморфной формы клопидогрела гидросульфата была неприемлемой. Полиморфная форма 1 в композиции частично превращалась в полиморфную форму 2 после хранения в течение двух недель, кроме того, можно было наблюдать химическое разложение активного ингредиента и уменьшение скорости растворения. В ходе дальнейших экспериментов авторы настоящего изобретения неожиданно обнаружили, что в порошкообразных смесях полиморфной формы 1 клопидогрела гидросульфата с микрокристаллической целлюлозой и коллоидным диоксидом кремния химическая и кристаллографическая стабильность активного ингредиента является приемлемой и скорость растворения таблеток, полученных из этих порошкообразных смесей, остается неизменной при хранении. Выгодные эффекты, химическая и кристаллографическая стабильность, а также приемлемая скорость растворения доказаны не только для физической смеси микрокристаллической целлюлозы и коллоидного диоксида кремния, но также и для композитных составов, полученных из микрокристаллической целлюлозы и коллоидного диоксида кремния. Эти вещества представляют собой так называемые силиконизированные микрокристаллические целлюлозы, которые продаются под торговой маркой Prosolv. Эти составы содержат 98% микрокристаллической целлюлозы и 2% коллоидного диоксида крем-5 015440 ния. Микрокристаллическую целлюлозу и силиконизированную микрокристаллическую целлюлозу применяют в качестве связывающего вещества и наполнителя. Для получения фармацевтической композиции, содержащей полиморфную форму 1 клопидогрела гидросульфата, можно применять все типы микрокристаллической целлюлозы или силиконизированной микрокристаллической целлюлозы, которые имеют размер зерен 90 мкм или более и приемлемые свойства текучести. Из силиконизированных микрокристаллических целлюлоз предпочтительным являетсяProsolv HD 90, имеющий большую массу на единицу объема. В качестве вещества для увеличения текучести может применяться любой тип коллоидного диоксида кремния, применяемый в фармацевтической промышленности, независимо от отношения объема к массе или его удельной поверхности. Предпочтительно следует применять такие типы коллоидного диоксида кремния, имеющие удельную поверхность 200 м 2/г, которые обычно применяют для получения капсул или таблеток. В дополнение к наполнителям и связывающим веществам фармацевтические композиции по настоящему изобретению могут содержать дополнительно вспомогательные вещества, такие как дезинтегрирующие агенты и смазывающие вещества. При выборе дезинтегрирующих агентов и смазывающих веществ нужно избегать применения соединений солевого типа, потому что они могут ускорять разложение активного ингредиента. Жирные кислоты, например стеариновая кислота, или эфиры жирных кислот, например глицерил бегенат (Compritol 888), гидрогенизированные растительные масла (например, Lubritab) или гидрогенизированное касторовое масло (Cutina H) могут применяться в качестве смазывающего вещества. Согласно нашим исследованиям применение гидрогенизированного касторового масла (Cutina H) является наиболее предпочтительным с точки зрения прессуемости и химической стабильности. В качестве дезинтегрирующего агента могут применяться различные типы крахмалов, например природный или пептизированный крахмал, поперечно-сшитый поливинилпирролидон (кросповидон) и низкозамещенная гидроксипропилцеллюлоза (low substituted hydroxypropyl methylcellulose - L-HPC). Согласно нашим исследованиям применение L-HPC является наиболее предпочтительным. Дезинтегрирующие агенты и смазывающие вещества применяются предпочтительно в количестве 3-20 мас.% и 1-5 мас.% соответственно относительно общей массы композиции, что является обычным в способах получения таблеток или капсул. Для покрытия таблеток пленкой могут применять гидроксипропилметилцеллюлозу, поливиниловый спирт или сополимер поливинилового спирта и полиэтиленгликоля. В этом случае покрытие не препятствует растворению активного ингредиента. Для получения пленочного покрытия можно получать суспензию путем растворения или суспендирования необходимых компонентов, а именно полимерного покрытия, пластификатора и красящего пигмента, однако также можно применять готовые к применению системы покрытия (например, Opadry, Sepifilm, Aquapolish). Для получения капсул порошкообразную смесь, содержащую активный ингредиент и вспомогательные вещества, помещают в капсулы из твердого желатина или гидроксипропилметилцеллюлозы. Преимущество фармацевтических композиций по настоящему изобретению заключаются в том, что при использовании способа смешивания порошков и последующего прямого прессования таблетки или способа заполнения капсулы можно получить фармацевтическую композицию, содержащую полиморфную форму 1 клопидогрела гидросульфата, в которой активный ингредиент сохраняет свою полиморфную форму и химическую стабильность в течение долгого времени,количество всех примесей составляет менее 0,5% и скорость растворения не уменьшается значительно по сравнению с начальной скоростью даже после долговременного хранения и через 15 мин она составляет более 90%, что значительно превышает ожидаемое значение 80%. Дополнительные детали настоящего изобретения приведены в следующих примерах, без ограничения объема охраны указанными примерами. Пример 1. В аппарат для гомогенизации емкостью 90 л помещают 9,79 кг клопидогрела гидросульфата полиморфной формы 1, 19,92 кг силиконизированной микрокристаллической целлюлозы (Prosolv HD 90),1,2 кг L-HPC B1 и 1,2 кг гидрогенизированного касторового масла (Cutina H). Смесь гомогенизируют при скорости вращения 25 об/мин в течение 20 мин, затем прессуют с получением двояковыпуклых таблеток весом 320 мг. На полученные таблетки наносят покрытие на основе гидроксипропилметилцеллюлозы(Pharmacoat 606). Агент для покрытия Opadry, содержащий Pharmacoat 606, диспергируют при концентрации 10 мас.% в воде в количестве, достаточном для обеспечения покрывающего слоя 10 мг на таблетку. Суспензию для покрытия наносят путем распыления на поверхность таблеток при температуре слоя 40-45 С. Способ повторяли для исследования воспроизводимости. В табл. 1 показано, какие примеси содержатся в продукте, полученном данным способом, после получения и какие содержатся после долговре-6 015440 менного хранения. Кристаллографические свойства этих продуктов показаны на фиг. 1 и 2. Скорости растворения представлены в табл. 2 выше. Пример 2. В смеситель барабанного типа добавляют 0,5 кг коллоидного диоксида кремния Aerosil 200 и 5,0 кг микрокристаллической целлюлозы Avicel PH 102. Смесь гомогенизируют и просеивают через сито с сеткой 0,5 мм. Просеянный гомогенизат, полученный таким образом, 9,79 кг полиморфной формы 1 клопидогрела гидросульфата, 14,42 кг микрокристаллической целлюлозы (Avicel РН 102), 1,2 кг L-HPC B1 и 1,2 кг гидрогенизированного касторового масла (Cutina H) добавляют в аппарат для гомогенизации емкостью 90 л. Смесь гомогенизируют при скорости вращения 25 об/мин в течение 20 мин, затем прессуют с получением двояковыпуклых таблеток весом 320 мг и диаметром 10 мм. На полученные таблетки наносят покрытие на основе гидроксипропилметилцеллюлозы (Pharmacoat 606). Агент для покрытия Opadry, содержащий Pharmacoat 606, диспергируют при концентрации 10 мас.% в воде в количестве, достаточном для обеспечения покрывного слоя 10 мг на таблетку. Суспензию для покрытия наносят путем распыления на поверхность таблеток при температуре слоя 40-45 С. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Твердая лекарственная форма, содержащая полиморфную форму 1 клопидогрела гидросульфата формулы в качестве активного ингредиента, микрокристаллическую целлюлозу и коллоидный диоксид кремния в качестве наполнителя и связывающего вещества, дезинтегрирующий агент и смазывающее вещество в качестве дополнительных эксципиентов. 2. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 20-40 мас.% полиморфной формы 1 клопидогрела гидросульфата, 40-65 мас.% микрокристаллической целлюлозы,0,5-10 мас.% коллоидного диоксида кремния, 3-20 мас.% дезинтегрирующего агента и 1-5 мас.% смазывающего вещества. 3. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 25-35 мас.% полиморфной формы 1 клопидогрела гидросульфата, 45-65 мас.% микрокристаллической целлюлозы,0,5-10 мас.% коллоидного диоксида кремния, 3-10 мас.% дезинтегрирующего агента и 1-5 мас.% смазывающего вещества. 4. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 25-35 мас.% композиции полиморфной формы 1 клопидогрела гидросульфата, 55-65 мас.% микрокристаллической целлюлозы, 1-5 мас.% коллоидного диоксида кремния, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы в качестве дезинтегрирующего агента и 1-5 мас.% гидрогенизированного касторового масла в качестве смазывающего вещества. 5. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 20-40 мас.% полиморфной формы 1 клопидогрела гидросульфата, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы в качестве дезинтегрирующего агента и 1-5 мас.% гидрогенизированного касторового масла в качестве смазывающего вещества, где коллоидный диоксид кремния и микрокристаллическая целлюлоза образуют композитный состав, составляющий 40-65 мас.% от массы композиции. 6. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 25-35 мас.% полиморфной формы 1 клопидогрела гидросульфата, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы в качестве дезинтегрирующего агента и 1-5 мас.% гидрогенизированного касторового масла в качестве смазывающего вещества, где коллоидный диоксид кремния и микрокристаллическая целлюлоза образуют композитный состав, составляющий 45-65 мас.% композиции. 7. Твердая лекарственная форма по п.1, содержащая, относительно ее общей массы, 25-35 мас.% композиции полиморфной формы 1 клопидогрела гидросульфата, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы в качестве дезинтегрирующего агента и 1-5 мас.% гидрогенизированного касторового масла в качестве смазывающего вещества, где коллоидный диоксид кремния и микрокристаллическая целлюлоза образуют композитный состав, составляющий 55-65 мас.% композиции. 8. Твердая лекарственная форма по любому из пп.1-7, представляющая собой таблетку, таблетку с плночным покрытием или капсулу, предпочтительно таблетку с плночным покрытием. 9. Твердая лекарственная форма по п.8, представляющая собой таблетку с плночным покрытием,на которую нанесено 2-5 мас.% от общей массы композиции водорастворимого покрытия. 10. Твердая лекарственная форма по любому из пп.1-9, отличающаяся тем, что применяемая микрокристаллическая целлюлоза имеет размер частиц более 90 мкм или представляет собой Prosolv HD 90. 11. Твердая лекарственная форма по любому из пп.1-10, отличающаяся тем, что коллоидный диок-7 015440 сид кремния имеет удельную поверхность 150 м 2/г, предпочтительно 200 м 2/г. 12. Твердая лекарственная форма по любому из пп.1-3 или 8-11, отличающаяся тем, что применяемый дезинтегрирующий агент выбран из природного или пептизированного крахмала, поперечносшитого поливинилпирролидона или низкозамещенной гидроксипропилцеллюлозы, предпочтительно низкозамещенной гидроксипропилцеллюлозы. 13. Твердая лекарственная форма по любому из пп.1-3 и 8-12, отличающаяся тем, что применяемое смазывающее вещество выбрано из жирных кислот, эфиров жирных кислот, гидрогенизированных растительных масел, предпочтительно гидрогенизированного касторового масла. 14. Способ получения твердой лекарственной формы по любому из пп.1-13, отличающийся тем, что полиморфную форму 1 клопидогрела гидросульфата, микрокристаллическую целлюлозу, коллоидный диоксид кремния или композитное вещество, полученное из микрокристаллической целлюлозы и коллоидного диоксида кремния, или их смесь смешивают с дезинтегрирующим агентом и смазывающим веществом, полученную смесь гомогенизируют и формуют с получением твердой лекарственной формы. 15. Способ по п.14, отличающийся тем, что гомогенизированную порошкообразную смесь прессуют в таблетки путем прямого прессования и таблетки, при необходимости, покрывают водорастворимым покрытием. 16. Способ по п.14, отличающийся тем, что гомогенизированной порошкообразной смесью заполняют капсулы. 17. Способ получения твердой лекарственной формы по п.8, характеризующийся тем, что 25-35 мас.% полиморфной формы 1 клопидогрела гидросульфата, 55-65 мас.% микрокристаллической целлюлозы, 1-5 мас.% коллоидного диоксида кремния или 55-65 мас.% композитного состава микрокристаллической целлюлозы и коллоидного диоксида кремния, 3-8 мас.% низкозамещенной гидроксипропилцеллюлозы и 1-5 мас.% гидрогенизированного касторового масла относительно общей массы лекарственной формы смешивают, гомогенизируют, полученный гомогенизат помещают в капсулы или прессуют в таблетки путем прямого прессования, и таблетки, при необходимости, покрывают водорастворимым покрытием.
МПК / Метки
МПК: A61K 9/28, A61P 9/10, A61K 9/20
Метки: гидросульфата, форму, лекарственная, содержащая, форма, клопидогрела, твердая, полиморфную
Код ссылки
<a href="https://eas.patents.su/10-15440-tverdaya-lekarstvennaya-forma-soderzhashhaya-polimorfnuyu-formu-1-klopidogrela-gidrosulfata.html" rel="bookmark" title="База патентов Евразийского Союза">Твердая лекарственная форма, содержащая полиморфную форму 1 клопидогрела гидросульфата</a>