Гепатопротекторное средство
Формула / Реферат
Способ лечения или профилактики воспалительных заболеваний печени, при котором нуждающемуся в этом пациенту вводят, перорально, гепатопротекторное средство, содержащее масляный раствор β-кариофиллена в виде его cis изомера, trans изомера или их комбинации, включающий очищенные оливковое или подсолнечное масло при следующем соотношении ингредиентов, мас.%: β-кариофиллен в виде его cis изомера, trans изомера или их комбинации - 10, очищенное оливковое или подсолнечное масло - остальное, чем обеспечивают индуцирование поляризации купферовских клеток, обеспечивают доза-зависимое ингибирование внутриклеточного кальция, индуцированного липополисахаридами, предупреждают рост содержания супероксидных радикалов и перекисного окисления липидов, способствуют регрессии, около 50%, имеющегося фиброза печени, предупреждают развитие фиброза, вызванного алкогольной и жировой интоксикацией, доза вводимого упомянутого гепатопротекторного средства составляет от 20 до 200 мг в день.
Текст
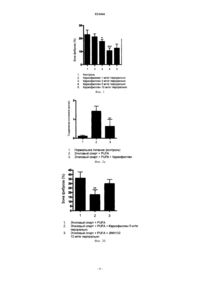
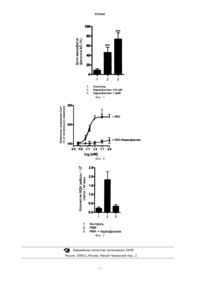
Предложен способ лечения или профилактики воспалительных заболеваний печени, при котором нуждающемуся в этом пациенту перорально вводят гепатопротекторное средство,содержащее масляный раствор -кариофиллена в виде его cis изомера, trans изомера или их комбинации, включающий очищенные оливковое или подсолнечное масло при следующем соотношении ингредиентов, мас.%: -кариофиллен в виде его cis изомера, trans изомера или их комбинации - 10; очищенное оливковое или подсолнечное масло - остальное,чем обеспечивают индуцирование поляризации купферовских клеток, обеспечивают дозазависимое ингибирование внутриклеточного кальция, индуцированного липополисахаридами,предупреждают рост содержания супероксидных радикалов и перекисного окисления липидов,способствуют регрессии, около 50%, имеющегося фиброза печени, предупреждают развитие фиброза, вызванного алкогольной и жировой интоксикацией, доза вводимого упомянутого гепатопротекторного средства составляет предпочтительно от 20 до 200 мг в день. Гетьман Михаил Александрович (RU),Герч Юрг (CH) Петренко И.А. (RU)(71)(73) Заявитель и патентовладелец: ГЕТЬМАН МИХАИЛ АЛЕКСАНДРОВИЧ (RU) Область изобретения Изобретение относится к области лекарственных средств, а именно к средствам для лечения заболеваний печени. Уровень техники Распространенность заболеваний печени в мире составляет более 30%. Самым распространенным среди них является стеатоз или жировая болезнь печени. В Российской Федерации, по некоторым данным, в среднем, у 27% населения имеется неалкогольная жировая болезнь печени. Кроме этого, официально в России насчитывается более 10 млн человек, больных алкоголизмом. Вследствие злоупотребления алкоголем у 90-100% пациентов развивается алкогольный стеатоз, который в 10-20% случаев трансформируется в алкогольный гепатит и цирроз печени. Среди больных с патологией печени летальный исход от цирроза печени вследствие алкогольной болезни печени составляет около 44% смертельных случаев. Причинами стеатоза, кроме злоупотребления алкоголем, являются: воздействие некоторых лекарств и токсических веществ; ожирение; сахарный диабет; метаболический синдром; хронические заболевания пищеварительной системы с нарушением всасывания. Повреждения печени, вызванные гепатотоксинами, такими как, например, этанол, характеризуются различной степенью повреждения гепатоцитов, фиброзом, а также гибелью клеток по типу апоптоза или некроза. В реакциях окисления токсины индуцируют избыточную продукцию и накопление в печеночной клетке свободных радикалов и других токсических метаболитов. В процессе оксидативного стресса происходит чрезмерная мобилизация свободных ионов железа из ферритина, что, в свою очередь, увеличивает содержание гидроксильных радикалов. Свободные радикалы запускают реакции перекисного окисления липидов и секрецию цитокинов, включая фактор некроза опухоли(TNF-), интерлейкин-6 (IL-6) и интерлейкин-8 (IL-8). Эти патологические реакции приводят к некрозу гепатоцитов и развитию воспалительной клеточной инфильтрации. Продукты перекисного окисления липидов, некроз гепатоцитов, TNF-, IL-6, IL-8 являются активаторами стеллатных клеток Ito. Их стимуляция сопровождается избыточной продукцией соединительной ткани с развитием фиброза, а при длительном персистировании процесса - циррозом печени. Процессы, приводящие к клеточной смерти, включают в себя нарушение гомеостаза цитоплазматического кальция, истощение по глутатиону, перекисное окисление липидов и связанное с этим увеличение проницаемости митохондриальной мембраны (МРТ). В свою очередь эти процессы обусловлены возникновением реакционноспособных продуктов метаболизма гепатотоксинов и появлением активных форм кислорода (ROS) во время воспалительной реакции. В последнее время также высказано предположение о том, что предотвращение возникновения митохондриальных пор может помочь снизить гибель клеток. Т.е. воздействовать следует на ключевые моменты повреждения печени: окислительный стресс и перекисное окисление липидов. Таким образом, в профилактике и лечении гепатотоксического повреждения печени основной стратегией является снижение количества реакционноспособных продуктов метаболизма гепатотоксинов,применение антиоксидантов, стабилизация гомеостаза цитоплазматического кальция и модулирование биологического ответа купферовских клеток. В арсенале современных гепатопротекторных средств присутствует разнообразные лекарственные средства и биологически активные добавки, которые в той или иной степени оказывают терапевтическое действие на процессы токсической деградации клеток печени. В основном это препараты фосфолипидов,адеметионина, тиоктовой кислоты, действующих веществ расторопши пятнистой и уродезоксихолевой кислоты. Большое место в связи с практическим отсутствием противопоказаний и незначительным числом побочных эффектов занимают препараты растительного происхождения, например на основе расторопши пятнистой, артишока полевого и куркумы длинной. Общим недостатком растительных средств является низкая эффективность, зависимость от растительного сырья и вариабельность состава. При этом средства растительного происхождения с высокой вероятностью вызывают аллергические реакции. Все перечисленные лекарственные средства являются неспецифическими гепатопротекторами,преимущественно метаболического действия. Молекулярные механизмы их фармакологической активности до конца не понятны, а терапевтическая активность недостаточно прогнозируема. Таким образом, по-прежнему сохраняется потребность в создании новых гепатопротекторных средств. Сущность изобретения Задачей данного изобретения является разработка новых гепатопротекторных средств. Данная задача решается тем, что предложено гепатопротекторное средство на основе-кариофиллена, причем это средство пригодно для перорального введения. Предложены также способ лечения и профилактики воспалительных заболеваний печени, при котором нуждающемуся в этом пациенту вводят терапевтически активное количество -кариофиллена, или его производного, или его фармацевтически приемлемой соли, а также фармацевтическая композиция,содержащая -кариофиллен, или его производные или фармацевтически приемлемые соли и фармацевтически приемлемый эксципиент. Краткое описание графических материалов Фиг. 1 - регрессия фиброза после систематического введения -кариофиллена циррозным крысам. Фиг. 2 - регрессия фиброза, вызванного этанол + PUFA в течение 45 дней на фоне приема-кариофиллена (фиг. 2 а и 2 б). Фиг. 3 - индуцирование -кариофилленом поляризации купферовских клеток при стимулировании липополисахаридами. Фиг. 4 - доза-зависимое ингибирование -кариофилленом индуцированного липополисахаридами(ЛПС) внутриклеточного кальция в Купферовских клетках крыс. Фиг. 5 - ингибирование бета-кариофилленом индуцированного РМА пероксидирования в Купферовских клетках крыс. Подробное описание изобретения Бета-кариофиллен (кариофиллен) представляет собой сесквитерпеновый углеводород, достаточно широко распространенный в природе в составе эфирных масел таких растений как: гвоздика (3,56%),розмарин (до 8,3%), хмель (до 14,5%), каннабис (до 37,5%), черный перец (7,29%) и других. Кариофиллен существует в виде двух изомеров: собственно кариофиллен или транскариофиллен Кариофиллен быстро окисляется на воздухе и очень легко, особенно под действием кислот, претерпевает превращения, связанные с перестройкой углеродного скелета. Применение кариофиллена в основном связано с его ароматическими свойствами, поэтому основной областью использования является парфюмерная промышленность. Известная нестабильность кариофиллена существенно ограничивает возможности его применения. Неожиданно авторами изобретения было обнаружено, что бета-кариофиллен (cis-изомер, transизомер, их комбинация) обладает сочетанием свойств, которые позволяют рационально применять его при лечении заболеваний печени, а именно кариофиллен воздействует на внутриклеточный кальций,проявляет свойства антиоксиданта и модулирует воспалительный ответ путем воздействия на купферовские клетки. Более того, оказалось, что все эти эффекты сохраняются при пероральном применении кариофиллена, что важно для лекарственного средства. Авторами изобретения показано в экспериментах на животных, что кариофиллен снижает степень существующего фиброза и позволяет предупредить развитие индуцируемого алкоголем фиброза. Это воздействие опосредуется влиянием кариофиллена на купферовские клетки, внутриклеточый кальций (восстанавливается гомеостаз кальция, нарушенный воспалительным процессом) и его антиоксидантными свойствами, что, как было отмечено выше, является основной стратегией в предупреждении и лечении стеатоза и последующего цирроза печени. Кариофиллен используют в форме фармацевтических препаратов (лекарственных форм). Фармацевтические препараты кариофиллена могут вводиться перорально, т.е. это такие лекарственные формы как растворы, эмульсии или суспензии, а также таблетки, таблетки покрытые оболочкой, драже, твердые и мягкие желатиновые капсулы. Например, в целях предупреждения окисления и разложения кариофиллена в качестве лекарственной формы для перорального применения может быть использован масляный раствор кариофиллена, помещаемый в изолированную кишечнорастворимую капсулу. Для получения фармацевтических препаратов (лекарственных форм) к кариофиллену добавляют терапевтически инертные, неорганические или органические носители. Лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.п. могут быть использованы, например,в качестве таких носителей для таблеток, таблеток, покрытых оболочкой, драже и твердых желатиновых капсул. Подходящими носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п. Подходящими носителями для получения растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар, глюкоза и т.п. Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие вещества, эмульгаторы, подсластители, красители, корригенты, соли для регулирования осмотического давления, буферы, маскирующие агенты или антиоксиданты и другие, необходимые для приготовления лекарственной формы, компоненты. Указанные выше вспомогательные вещества, используемые для образования лекарственных форм,будут названы далее "терапевтически инертными эксципиентами". Однако лекарственные формы средства по изобретению также могут содержать и другие терапевтически активные вещества. Кариофиллен вводят перорально в дозе от 10 до 500 мг в день. Например, 20-200 мг в день. Конкретные примеры осуществления изобретения Индукция цирроза у крыс. Исследования проводились на мужских особях крыс линии Вистар с циррозом печени, осложненным асцитом или без такового. Контрольная группа также состояла из мужских особей крыс линии Вистар. Цирроз был индуцирован CCI4 (тетрахлорметаном) в соответствии с ранее описанным методомIn Ascites and Renal Dysfunction in Liver Disease. Pathogenesis Diagnosis and Treatment (Arroyo V, Gins P,Rods J, and Schrier RW eds) p. 379-396, Blackwell Science Inc., Maiden, MA). Циррозные крысы без асцита изучались между 11 и 12 неделями после начала программы индукции цирроза. Отсутствие асцита подтверждалось лапаротомическим методом. Циррозные крысы с асцитом изучались между 13 и 17 неделями, когда асцит достигал полного развития. Контрольные крысы изучались в аналогичный период на фоне введения фенобарбитала. В примере 1 использовались асцитные крысы. Исследование проводилось в соответствии с критериями Комитета по исследованиям и этике университета Гвадалахары. Количественная оценка фиброза. Срезы печени (4 мкм) окрашивались 0,1% раствором Сириус красный F3B (Сигма-Олдрич, Сент Луис, МО) в насыщенной пикриновой кислоте (Сигма-Олдрич), специфически окрашивающим коллаген. Относительная площадь фиброза (выраженная в процентах от общей площади печени) определялась посредством анализа 36 полей окрашенных Сириусом красным срезов печени на одно животное. Каждое поле помещалось в 10 and RT-Slider SPOT цифровую камеру и анализировалось при помощи компьютеризированной морфометрической системы. Для определения относительной площади фиброза, измеряемая площадь коллагена делилась на общую площадь поля и умножалась на 100. Вычитание площади просвета сосудов из общей площади давало итоговое значение фактической площади фиброза. Для каждого животного измерялась величина фиброза в процентах и рассчитывалось среднее значение площади фиброза. Содержание коллагена определялось спектрофотометрически методом Весснера. Изолирование купферовских клеток. Крысы анестезировались интраперитонеально Нембуталом. В брюшной полости делался вентральный разрез в срединной линии и стерильная тефлоновая канюля 24-го размера (introcan-w. 24Gi, Braun Melsungen. Melsungen. Germany) вводилась в портальную вену. Печень предварительно промывалась бескальциевым буферным солевым раствором Хэнка (Ca'+-free HBSS с низким содержанием эндотоксинов) (HyClone Laboratories. Logan, UT. USA) при рН 7,4 и 30 С позволяя крови вытекать из разреза в нижней полой вене. Через 2 мин промывающий раствор замещался раствором коллагеназы А (0.163 U/ml в DMEM с высоким содержанием глюкозы) (Boehringer Mannheim. Mannheim. Germany) и печень промывалась 30 с со скоростью 5 мл/мин при 35 С. После промывания печень удалялась из крысы и аккуратно диспергировалась. Печеночная суспензия из 8 крыс объединялась и инкубировалась при постоянном перемешивании при 35 С в течение 10 мин в 40 мл раствора коллагеназы,который использовался для промывания в 50 мл полипропиленовых пробирках. После этого все эксперименты проводились при 4 С. Суспензия клеток печени фильтровалась через нейлоновый фильтр(212 pm) и помещалась в 50 мл HBSS, содержащий 0,3% BSA (фракция V. с низким содержанием эндотоксинов. Sigma, St. Louis, МО, USA) и 2 пг/мл ДНКазы (низкое содержание эндотоксинов, стерильный,Boehringer Mannheim, Mannheim, Germany) и центрифугировалась при 400 X в течение 15 мин. Этот буфер в дальнейшем будет называться "рабочий буфер" (WB). Осадок помещался в 15,6 мл WB и смешивался с 21 мл NycoPrep (низкое содержание эндотоксинов, стерильный раствор Nycodenz с плотностью 1,150 г/мл и осмолярностью 290 миллиосмоль. Nycorned Pharma. Oslo, Norway). Смеси помещались в три 15 мл полипропиленовые пробирки и поверх смеси помещался 1 мл WB. Красные кровяные клетки и тканевая масса осаждались центрифугированием при 1500 X в течение 15 мин. Клетки интерфазы, являющиеся, в основном, синусоидальными клетками, суспендировались в 50 мл WB и дважды промывались для удаления Nycodenz центрифугированием при 400 X в течение 15 мин. Осадок помещался в 5 млWB и дальнейшее фракционирование клеток производилось методом противоточной центрифужной элютриации (ССЕ) с использованием автоклавируемого элютриаторного ротора Beckman JE-5.0 с камерой Sanderson (Beckman Instruments, Palo Alto, CA. USA). Клеточная суспензия вводилась в элютриатор на скорости 12. Статистический анализ результатов, когда применимо, производился с применением непарных критериев Стьюдента. Данные представлены в виде среднего значенияS.E.M. и считаются значимыми на уровне р 0,05 или ниже. Результаты. Как показано в приведенных ниже примерах, оральные дозы ВСР были эффективны при лечении цирроза печени, вызванного ССЦ. Пример 1. Испытуемые крысы с циррозом, вызванным ССЦ, были рандомизированы в 5 групп. Одной группе перорально вводилась питательная среда (нормальная гранулированная пища) в чистом виде, другим группам - та же питательная среда, содержащая 1 мг/кг, 3 мг/кг, 5 мг/кг и 10 мг/кг кариофиллена, соответственно, в течение 9 дней. Размер относительных площадей фиброза определялся по 30 образцам. Как показано на фиг. 1, дневная доза 5 мг/кг показала самое значительное уменьшение относительной площади фиброза (около 50%). Таким образом, как показано в эксперименте, кариофиллен демонстрирует высокую оральную биодоступность и способность вызывать регрессию фиброза у крыс с циррозом. Пример 2. Испытуемые здоровые крысы были рандомизированы в 3 группы по 6 животных в каждой группе. Группа 1 получала нормальную гранулированную пищу, группа 2 получала перорально вместе с питанием 20% этанола и 15% термически окисленных полиненасыщенных жирных кислот (PUFA) в течение 45 дней. Группа 3 получала вместе с питанием 20% этанол и 15% PUFA вместе с 5 мг/кг кариофиллена, растворенного в этаноле, в течение 45 дней. Для сравнения действия кариофиллена, часть животных группы 3 вместо кариофллена получала 10 мг/кг другого экспериментального вещества JWH133 в течение того же срока. В результате эксперимента, у крыс, содержащихся в группе 2, развился фиброз, а у крыс, содержащихся к группе 3, развитие фиброза было значительно замедлено (фиг. 2 а и фиг. 2 б). Результаты эксперимента подтверждают высокую биодоступность кариофиллена при пероральном применении и показывают способность кариофиллена замедлять процесс развития фиброза при хронической алкогольной и жировой интоксикации. Кроме того, как показано на фиг. 2 б, селективный агонист СВ 2 рецепторов JWH133 недостаточно эффективно подавлял развитие цирроза печени, что подтверждает гипотезу о том, что только сочетание нескольких свойств, присущее кариофиллену, обеспечивает эффективное гепатопротекторное действие. Пример 3. Купферовские клетки крыс (макрофаги) (5105), изолированные в соответствии с методикой описанной выше, были инкубированы в течение 30 мин с кариофилленом в дозе 100 нМ и 1 мкМ и затем стимулированы 500 мкг липополисахарида в течение 22 ч. В ходе эксперимента определялось соотношение М 1 и М 2 фенотипов макрофагов. Результаты, представлены на фиг. 3, свидетельствуют, что кариофиллен эффективно индуцирует поляризацию купферовских клеток с М 1 до М 2 при стимулировании липополисахаридами. Из этого следует, что кариофиллен оказывает выраженное модулирующее действие на купферовские клетоки, опосредованное, по всей видимости, его агонистической активностью по отношению к эндоканнабиноидным рецепторам 2-го типа. Пример 4. Исследование влияния на внутриклеточный кальций. Методика. Купферовские клетки, изолированные в соответствии с методикой, описанной выше,были разделены на 3 группы: 1 группа - интактная, 2-я группа была инкубирована в течение 30 мин и затем стимулирована 500 мкг липополисахарида в течение 22 ч, 3-я группа клеток была разделена на 6 подгрупп, каждая из которых была инкубирована в течение 30 мин с кариофилленом в дозах от 5 до 100 нМ и затем стимулирована 500 мкг липополисахарида в течение 22 ч. Клетки каждой группы были смешаны с флуорохромом Fura2-AM и помещены на 30 мин при 37 С в среду Вильямса Е. Покровные стекла с образцами помещались в специально спроектированной пластиковой емкости (Groupe de Recherche en Transport Membranaire, Montre'al, Que'bec) на полку инверсионного микроскопа (Nikon Diaphot TMD) и промывались буфером Кребса-Ханслайта, содержащим (в мМ) 140 NaCl, 25 NaHCO3, 10 Hepes, 5.5 декстрозы, 3.8 KCl, 1.6 CaCl2, 1.2 MgSO4, 1.2 KH2PO4, и 1 пируватаNa (pH 7.4), насыщенный 95% О 2/5% СО 2 при 37 С. Температура емкости контролировалась. Интенсивность флуоресценции измерялась при 340 и 380 нм при помощи охлаждаемой CCD камеры и системы визуализации Hamamatsu (Model C4880; Imaging Research, Inc) Измерение содержания Са 2+ методом флуоресцентной спектроскопии производилось в каждой из 3-х групп клеток. Изменение содержания Са 2+ рассчитывалось по отношению к содержанию Са 2+ в группе 1. Результаты представлены на фиг. 4. Как было показано, кариофиллен доза-зависимо ингибирует внутриклеточный кальций, индуцированный липополисахаридами. Причем, если в группе 2 (без кариофиллена) содержание кальция увеличилось почти 2,3 раза, в группе 3 (с добавлением кариофиллена) увеличение содержания кальция было незначительным. Пример 5. Исследование влияния кариофиллена на процесс перекисного окисления липидов. Методика. Для изучения влияния кариофиллена на процесс перекисного окисления липидов, купферовские клетки инкубировались в 96 чашках в течение 48 ч. Кариофиллен в дозировке 500 нМ был добавлен в питательную среду перед инкубированием и через 1 ч после этого в питательную среду были добавлены липополисахариды. Для измерения супероксидов среда подвергалась аэрации, а купферовские клетки были дважды промыты сбалансированным солевым раствором Ханка (HBSS). После этого,купферовские клетки инкубировались в HBSS вместе с 1 мкМ РМА (Сигма) и гомогенизировались. Для последующих измерений были сформированы 3 группы образцов: 1 группа включала в себя интактный гомогенизат купферовских клеток, 2 группа включала в себя гомогенизат купферовских клеток, стимулированных РМА, но без добавления кариофиллена, 3 группа включала в себя гомогенизат купферовских клеток, стимулированных РМА с добвлением 500 мкМ кариофиллена. Концентрация супероксидных радикалов изучалось по содержанию малонового диальдегида (MDA) методом, предусматривающим использование тиобарбитуровой кислоты (TBA). К 100 мкл гомогената купферовских клеток, изолированных в соответствии с методикой, описанной выше, было добавлено 0,4 мл 0,6% ТВА и 1,2 мл 1% ортофосфорной кислоты и смесь кипятилась в течение 40 мин. После охлаждения к смеси было добавлено 1,6 мл 1-бутанола, образцы перемешивались и центрифугировались при 1200 об/мин в течение 12 мин. Концентрация MDA супернатанте измерялась по оптической плотности при 535 нм с использованием калибровочной кривой ТВА в качестве стандарта. Результаты эксперимента приведены на фиг. 5 и подтверждают способность кариофиллена эффективно предупреждать рост содержания супероксидов в купферовских клетках после стимулирования РМА (разница в концентрациях супероксидов между образцами группы 1 (контроль) и группой 3 (РМА и кариофиллен) практически отсутствует, а концентрация супероксидов в образцах группы 2 (РМА без кариофиллена) более чем в 4 раза превышает аналогичный показатель в образцах группы 3 (РМА и кариофиллен). Пример 6. Приготовление масляного раствора кариофиллена 100 мг в мягких желатиновых капсулах: Чистый кариофиллен в количестве 100 г растворяется в 1 кг очищенного оливкового или подсолнечного масла при комнатной температуре. Полученный раствор помещается в подающую емкость коэкструзионной машины по изготовлению мягких желатиновых капсул. Мягкие желатиновые капсулы,каждая из которых содержит 100 мг кариофиллена в 1 г оливкового или подсолнечного масла, изготавливаются методом коэкструзии. Из указанного количества сырья получают 1000 мягких желатиновых капсул. Таким образом, в ходе проведенных лабораторных экспериментов авторами было убедительно подтверждено, что кариофиллен индуцирует поляризацию купферовских клеток; доза-зависимо ингибирует внутриклеточный кальций; предупреждает рост содержания супероксидных радикалов и перекисного окисления липидов. При этом в опытах in vivo кариофиллен способствует регрессии имеющегося фиброза печени и предупреждает развитие фиброза, вызванного алкогольной и жировой интоксикацией. ФОРМУЛА ИЗОБРЕТЕНИЯ Способ лечения или профилактики воспалительных заболеваний печени, при котором нуждающемуся в этом пациенту вводят, перорально, гепатопротекторное средство, содержащее масляный раствор-кариофиллена в виде его cis изомера, trans изомера или их комбинации, включающий очищенные оливковое или подсолнечное масло при следующем соотношении ингредиентов, мас.%:-кариофиллен в виде его cis изомера, trans изомера или их комбинации - 10, очищенное оливковое или подсолнечное масло - остальное, чем обеспечивают индуцирование поляризации купферовских клеток,обеспечивают доза-зависимое ингибирование внутриклеточного кальция, индуцированного липополисахаридами, предупреждают рост содержания супероксидных радикалов и перекисного окисления липидов, способствуют регрессии, около 50%, имеющегося фиброза печени, предупреждают развитие фиброза, вызванного алкогольной и жировой интоксикацией, доза вводимого упомянутого гепатопротекторного средства составляет от 20 до 200 мг в день.
МПК / Метки
МПК: A61K 31/015, A61P 1/16
Метки: гепатопротекторное, средство
Код ссылки
<a href="https://eas.patents.su/8-24466-gepatoprotektornoe-sredstvo.html" rel="bookmark" title="База патентов Евразийского Союза">Гепатопротекторное средство</a>
Следующий патент: Ингалятор
Случайный патент: Гидравлический механизм ударного действия