Способ получения фармацевтического препарата для фотодинамической терапии онкологических заболеваний
Номер патента: 2318
Опубликовано: 25.04.2002
Авторы: Жаврид Эдвард Антонович, Грубина Людмила Александровна, Кочубеев Георгий Афанасьевич, Хлюстов Станислав Валентинович, Пленина Людмила Васильевна
Формула / Реферат
1. Способ получения фармацевтического препарата для фотодинамической терапии онкологических заболеваний, включающий экстракцию из растительного сырья хлорофилла и его производных органическим растворителем, их окисление с выделением феофитина и последующего превращения его, отличающийся тем, что из растительного сырья путем СО2 экстракции под давлением 10-300 бар до извлечения хлорофилла этанолом отделяют каротиноиды и жирные кислоты, а превращение хлорофилла осуществляют незамедлительно обработкой концентрированной соляной кислотой и после его окислительного расщепления и выделения из солянокислого раствора и осаждения щелочью при рН 4,0+0,2 проводят последующую очистку препарата и вводят стабилизатор.
2. Способ по п.1, отличающийся тем, что в качестве стабилизатора применяют раствор хитозана.
Текст
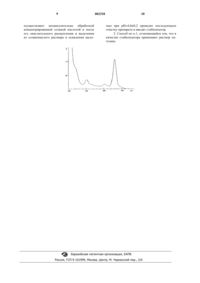
1 Изобретение относится к химикофармацевтической промышленности и касается способа получения фармацевтического препарата, используемого в медицине для фотодинамической терапии онкологических заболеваний. Известны способы получения фотосенсибилизирующих препаратов из растительного сырья путем экстракции свежего или специально высушенного сырья полярными растворителями (спирт, ацетон) и получения экстракта суммы хлорофиллов а и b. Из хлорофильного экстракта осаждают сумму феофитинов а и b, из которых путем хроматографической очистки выделяют чистый феофитин а. Из феофитина а получают "неустойчивый хлорин" путем окисления в спиртах (метиловом, этиловом, пропиловом), содержащих щелочь, и обработкой его при нагревании и кипячении в органических растворителях или декарбоксилирующими агентами [1]. Однако эти способы сложны, многостадийны и имеют низкий выход целевого продукта. Известен способ получения фармацевтического препарата для фотодинамической терапии, модифицированный на стадии очистки целевого продукта [2]. Способ заключается в том, что из растительного сырья выделяют путем его поэтапной обработки органическим растворителем производные хлорофилла. Сначала выделяют путем экстракции сырья полярным растворителем(этанолом) смесь хлорофиллов а и b, из которой при помощи реактива Жирара осаждают феофитины а и b. Далее из этой смеси получают чистый феофитин а путем хроматографической очистки на силикагеле, феофитин а затем подвергают окислительному расщеплению в диэтиловом эфире с добавлением к нему 20-30% едкого калия при барботировании воздухом при комнатной температуре в течение 2 ч до образования "неустойчивого хлорина", который затем обрабатывают, как описано выше. Однако этот способ также многостадийный, трудоемкий и не пригоден для промышленного производства. Выход целевого продукта не высок из-за потерь производных хлорофилла на стадии обработки смеси реактивом Жирара и хроматографической очистки на силикагеле, а также при экстрагировании диэтиловым эфиром из слабокислой среды, при которой часть хлорина не переходит в кислое соединение, а остается в водной фазе. Известный способ получения хлорина в промышленных условиях нетехнологичен, так как требует использования большого количества взрывоопасного и вредного растворителя - диэтилового эфира, содержит значительное количество трудоемких процессов экстрагирования и требует больших объемов сырья. Кроме того, в процессе экстракции этанолом хлорофилл подвергается алломеризации,т.е. в этих условиях может наблюдаться частич 002318 2 ное окисление изоциклического кольца пигмента. При омылении феофитина с окисленным изоциклом основным продуктом реакции получается не хлорин, а ряд хлориноподобных продуктов, таких как пурпурины. Задача, на решение которой направлено предлагаемое изобретение, состоит в упрощении способа получения фармацевтического препарата, предотвращении окисления изоцикла хлорофилла, повышении выхода целевого продукта. Задача решается тем, что в способе получения фармацевтического препарата путем экстракции из растительного сырья хлорофилла и его производных органическим растворителем и окислительного расщепления с выделением феофитина и последующего превращения его в хлорин в качестве сырья используют высушенные листья крапивы, люпина, люцерны и спирулины, а экстракцию проводят в два этапа. Сначала выделяют путем СО 2-экстракции из сырья под давлением 10-300 бар смесь каротиноидов и жирных кислот, а затем этанолом извлекают производные хлорофилла, сразу же обрабатывают их концентрированной соляной кислотой с образованием осадка феофитина и растворяют его в спиртовом растворе в вакууме. Проводят окислительное расщепление фитола и размыкание изоцикла в спиртовом растворе щелочи. Затем растворяют в кислоте и выделяют гидроксидом натрия осадок, состоящий преимущественно из хлорина, который подвергают стабилизации, сушке и очистке от примесей растворением в минимальном количестве ацетона. Новым, согласно изобретению, является то, что растительное сырье подвергают СО 2 экстракции под давлением с извлечением каротиноидов и жирных кислот. И после извлечения каротиноидов и жирных кислот из растительной массы выделяют путем экстракции полярным растворителем этанолом производные хлорофилла. Спиртовой экстракт пигментов сразу же обрабатывается концентрированной соляной кислотой с выделением хлорина. Такая обработка растительного сырья позволяет извлечь производные хлорофилла без потерь и, тем самым, увеличить выход феофитинов. А обработка феофитинов концентрированной соляной кислотой позволяет полнее выделить в раствор хлорин из осадка хлорофильных пигментов. Способ осуществляется следующим образом. Растительное сырье подвергают сушке в токе воздуха при 40-80 С. Обезвоженное сырье помещают в экстрактор для СО 2-экстракции и под давлением 10-300 бар и температуре 25 С проводят экстракцию каротиноидов и жирных кислот. Травяную массу выгружают из СО 2-экстрактора,загружают в сосуд, заливают этанолом и прово 3 дят экстракцию хлорофилла. После экстракции этанольный раствор хлорофиллов а+b отфильтровывают через стеклянный фильтр. К экстракту сразу же добавляют концентрированную соляную кислоту из расчета 2 мл на 1 л экстракта и через 12 ч осаждают сумму феофитинов а+b в виде черного осадка, который отфильтровывают и многократно промывают спиртом. Феофитин а+b растворяют в минимальном количестве ацетона, а затем спирта в вакууме. Далее в реакционный сосуд под вакуумом добавляют спиртовой раствор КОН до концентрации 15%. В результате происходит омыление фитола и размыкание изоцикла. Затем реакционную смесь при атмосферном давлении выливают в четырехкратное количество воды для прекращения реакции омыления. Щелочной раствор подкисляют соляной кислотой до содержания в общем растворе 4,7%. При этом происходит растворение хлорина в кислоте. Затем проводят нейтрализацию раствора 30% раствором гидроксида натрия,получают осадок, состоящий из ряда пигментов,исключая хлорин. Осадок отделяют, а раствор фильтруют, и из раствора при нейтрализации выпадает осадок с содержанием хлорина 5060%, который промывают, собирают и сушат при температуре +37 С. Для очистки хлорина от примесей его растворяют в минимальном количестве ацетона. Не растворившуюся часть препарата отделяют центрифугированием, раствор разводят дистиллированной водой 1:1 и доводят рН до 3,4, при этом образовавшийся осадок отделяют центрифугированием при тех же условиях. Осадок собирают и сушат в термостате при температуре+37 С. Спектрофотометрически установлено, что после процедуры очистки содержание активного вещества в препарате возрастает на 10-15%. Очищенный хлорин растворяют в воде,стерильно фильтруют. Для стабилизации препарата вводят раствор хитозана, который снижает общую токсичность и повышает специфические свойства препарата. Затем раствор разливают во флаконы и лиофильно высушивают из замороженного состояния. Высушенный препарат укупоривают в стерильных условиях и закатывают. Описанный метод получения фармацевтического препарата для фотодинамической терапии удобен тем, что кроме использования легко доступных реактивов не содержит технологически сложных операций. Кроме того, основной растворитель - этиловый спирт - после отделения феофитинов может перегоняться и использоваться многократно в этой технологии. Введение стабилизатора хитозана позволяет получать препарат не только в сухой, но и в жидкой форме. В соответствии с изобретением полученный препарат содержит лиофильно высушенный хлорин в виде тринатриевой соли. 4 Физико-химические показатели препарата следующие. Молекулярная масса 662 Да. В препарате содержится не менее 0,3 мг хлорина на 1 мг сухого вещества. Остальное составляет хлорид натрия, необходимый для лиофильной сушки препарата, и стабилизатор. По внешнему виду препарат представляет собой лиофилизированный аморфный порошок черного цвета с зеленовато-фиолетовым металлическим блеском. Без запаха. рН водного раствора определяют потенциометрически. Содержимое 1 флакона, растворенное в 20 мл воды,должно иметь рН 8,50,5. Водный раствор 0,002 г препарата в 400 мл воды должен быть прозрачным. Препарат умеренно растворим в пиридине(1 г в 100 мл), в воде (1 г в 100 мл), в 0,9% изотоническом растворе хлорида натрия (1 г в 100 мл). Подлинность определяют спектрофотометрически по спектру поглощения при длинах волн от 400 до 700 нм. Хлорин имеет характерный спектр в виде четырех основных пиков при 401,5, 500, 530,560, 605, 665 нм (фиг. 1). В качестве второго теста на подлинность применяют тонкослойную хроматографию на пластинах с силуфолом - UV-256. В качестве растворителя используют гексан, ацетон, хлороформ в соотношении 1:1:1. На хроматографическую пластину наносят 2 мкл раствора хлорина в воде. По окончании процесса хроматографии и подсушивания пластины на хроматограмме выявляют одно ярко-зеленое пятно на старте и до семи слабоокрашенных пятен сRf6=0,850,07; Rf7=0,950,04. Испытание на чистоту и допустимые пределы примесей проводят по ГФ XI, вып. 1,стр.165. Содержание тяжелых металлов определяют методом влажной минерализации по статье"Компедиум Медикаменторум". Содержание меди в препарате не превышает 1,2 х 10-3%, цинка 8,3 х 10-3%, железа 1 х 10-1%,магния 1,25 х 10-2%, алюминия 1,3 х 10-2%, молибдена 0,17%. Препарат не содержит кобальта, ртути,свинца, стронция, мышьяка. Органические примеси в препарате отсутствуют. Остаточная влажность препарата не должна превышать 12%. Количественное определение хлорина основано на спектрофотометрическом измерении оптической плотности раствора при 665 нм. Расчет содержания хлорина в препарате ведут по формулеC = D50/E1 662,где D - оптическая плотность раствора при 665 нм; 5 Е - коэффициент молярной экстинции хлорина в данном растворителе при данной длине волны, равный 5,3 х 10-4 М-1 см;l - толщина слоя кюветы (в см); 662 - молекулярная масса тринатриевой соли хлорина; 50 - коэффициент разведения препарата. Содержание хлорина в сухом препарате должно быть 505 мг. Пример 1 (субстрат - крапива).I. Получение феофитинов. Измельченные до порошка листья крапивы(3,5-4 кг) замачивают в 20 л смеси воды со спиртом в соотношении 1:1 в течение 1,5-2 ч при температуре 15-25 С. Затем воду отсасывают под вакуумом. Обезвоженную растительную массу помещают в СО 2-экстрактор и под давлением 10-300 бар проводят экстракцию каротиноидов и жирных кислот. Травяную массу извлекают из СО 2-экстрактора, помещают в стеклянную трубку (L=120 см, D=40 мм) и заливают 15 л этанола на 1,5-2 ч. Экстракция повторяется 3 раза. Экстракты объединяют, фильтруют через стеклянный, бумажный или ватно-марлевый фильтр. К экстракту сразу же добавляют концентрированную НСl (2 мл на 1 л экстракта), через 12 ч осадок отфильтровывают и сушат на воздухе. Выход - 30 г порошка.II. Синтез хлорина. 30 г порошка феофитина растворяют в 250 мл ацетона. Полученный раствор смешивают с 5 л спирта. Смесь аэрируют азотом в течение 3040 мин при температуре +40 С. Параллельно готовится спиртовой раствор гидроксида калия из расчета 1,2 кг на 5 л 96% спирта в атмосфере азота. Затем раствор щелочи прокачивается в емкость с растворенным в этаноле феофитином. Реакция проводится в течение 40-50 мин при температуре +40 С в азотной атмосфере. По окончании реакции раствор нейтрализуется 28 л заранее приготовленного раствора 9% соляной кислоты до рН=0,4-0,8 при интенсивном перемешивании. При этом выпадает осадок, состоящий из примесных пигментов,который отделяют фильтрацией через мезгу на нутчфильтре. Доводят рН фильтрата до 4,00,2 30% раствором гидроксида натрия. Выпавший осадок,состоящий преимущественно из хлорина, собирают на центрифуге и отмывают дистиллированной водой до рН=3,6. Полученный осадок сушат при температуре +37 С до постоянной массы. Выход продукта - около 5 г.III. Очистка от примесей. Берут навеску препарата и растворяют в минимальном количестве ацетона. Не растворившуюся часть препарата отделяют центрифугированием при 3000 об/мин в течение 15 мин. 6 Затем раствор разводят дистиллированной водой 1:1 и доводят рН до 3,4, при этом выпадает осадок, который отделяют центрифугированием при тех же условиях. Осадок собирают и сушат в термостате при температуре + 37 С.IV. Стабилизация препарата. Полученное сухое вещество растворяют в дистиллированной воде при рН=11,0. Полученный раствор фильтруют через бумажный фильтр. РН фильтрата доводят до значения 8,08,5 и вводят 125 мл стабилизатора, (растворенный 2% раствор хитозана). Далее полученный раствор стерильно фильтруют, разливают во флаконы и леофильно высушивают. Влажность полученного препарата не более 10%. Пример 2 ( субстрат - люпин).I. Получение феофитинов. Схема получения феофитинов из люпина аналогична схеме получения из крапивы как в примере 1. Выход продукта составляет около 50 г.II. Синтез хлорина. 40 г феофитина растворяют в 0,5 л ацетона. Далее см. схему получения хлорина и очистку от примесей как в примере 1. Пример 3 (субстрат - смесь крапивы, люпина, люцерны в весовом соотношении 1:1:1) получение жидкой формы.I. Получение феофитина. Растительную смесь 80 кг, высушенную при температуре 40-80 С в токе воздуха, замачивают в 300 л смеси воды с этанолом (1:1) в течение 1,5 ч при температуре 15-25 С. Затем раствор отсасывают под вакуумом. Обезвоженную траву помещают в экстрактор для СО 2 экстракции под давлением 10-300 бар и температуре 25 С. Затем травяную массу выгружают из СО 2-экстрактора, загружают в сосуд для обработки этанолом и проводят 3 экстракции хлорофилла этанолом (по 200-250 л). Экстракты объединяют и далее проводят получение феофитина по схеме получения из экстракта крапивы по примеру 1. Выход продукта - 800 г.II. Получение хлорина. Полученный феофитин растворяют в 2 л ацетона. Полученный раствор заливают в 15 л этанола на 45-60 мин, добавляют раствор КОН в этаноле (3,5 кг на 15 л спирта). Реакция длится 60 мин при температуре +40 С в атмосфере азота. Раствор нейтрализуют 9% НСl (15 л на 60 л Н 2 О), рН=0,6-75 л. Образовавшийся осадок удаляют на нутчфильтре. Доводят рН фильтрата до 4,0. Образовавшийся осадок собирают на центрифуге и отмывают подкисленной водой. Выход продукта - около 100 г. Вещество растворяют в дистиллированной воде при рН=11,0. 7 Полученный раствор фильтруют через бумажный фильтр. РН фильтрата доводят до значения 8,0-8,5 и вводят стабилизатор - 2% раствор хитозана. Полученный раствор стерильно фильтруют и разливают во флаконы. Фармацевтический препарат, полученный предлагаемым способом, выпускается в сухом виде по 50100 мг во флаконах на 50 мл или в жидкой форме. Содержание активного вещества хлорина составляет не менее 0,3 мг/мг сухого вещества. По своему действию препарат относится к фотосенсибилизаторам, избирательно накапливающимся в опухолевой ткани. Последующее воздействие светом с длиной волны 665 нм приводит (фотодинамическая терапия) к возбуждению молекулы хлорина и последующему разрушению опухолевой ткани. Эффект фотосенсибилизации проявляется в нарушении клеточного дыхания, синтеза белка, подавлении гликолиза, в изменении проницаемости клеточной мембраны. На этих свойствах хлорина основано его применение при лечении опухолей. Введение стабилизатора снижает общую токсичность и повышает его специфические свойства. Препарат вводят внутривенно. Раствор препарата готовят ex tempore. Содержимое флакона разводят в 50 мл физиологического раствора хлорида натрия. Лечебную дозу препарата вводят в вену в течение 20 мин в 200 мл физиологического раствора. Полученное фотосенсибилизирующее средство прошло клинические испытания и показало положительные результаты. Клинические испытания фармакологических свойств фотосенсибилизатора хлорина были проведены при фотодинамической терапии опухолей на мышах и крысах путем внутривенного введения фотосенсибилизатора и последующего облучения опухолевых очагов. Фотосенсибилизатор хлорин имеет максимум поглощения при длине волны 660 нм. Поэтому для фотооблучения опухолей использовался лазер с указанной длиной волны света. Испытания показали, что препарат является малотоксичным веществом. Так, для мышейLD10 составляет 40 мг/кг, для крыс - 30 мг/кг. Для перевитых опухолей крыс и мышей характерно более медленное накопление и выведение препарата по сравнению с нормальными тканями. Через 24-72 ч после введения концентрация хлорина в опухолях превышала его содержание в печени, почках, селезенке и мышцах у животных с саркомой 45 соответственно в 2,6,1,2, 4,3 и 6,5 раз; с саркомой М-1 - в 4,6, 2,1, 7,7 и 11,5 раз; с саркомой 180 - в 6, 12, 10 и 55 раз; с солидной опухолью Эрлиха - в 6,5, 13, 11 и 65 раз. Диапазон терапевтических доз хлорина составлял 1-10 мг/кг. Глубина повреждения ново 002318 8 образований при использовании препарата в этих дозах варьировала от 4 до 16 мм, а противоопухолевый эффект фотодинамического воздействия находился в прямой зависимости от концентрации фотосенсибилизатора в крови,ткани опухоли и от энергетической экспозиции светового облучения. Различные типы опухолей отличались пo чувствительности к фотодинамическому воздействию: излеченность животных с альвеолярным раком печени РС-1, саркомой 45, саркомой М-1 и лимфосаркомой Плисса составила соответственно 100, 100, 50 и 20%. Фотодинамическое воздействие с хлорином вызывает структурно-функциональные изменения и некроз опухолевой ткани. В зависимости от дозы препарата гибель опухолевых клеток может наступать в результате прямого фотоцитотоксического эффекта или опосредованно вследствие необратимого нарушения кровообращения с последующим аутолизом. Основное побочное действие хлорина выражалось в незначительных структурнофункциональных нарушениях в печени при длительном (в течение 30 суток) введении препарата. При 2-3-кратном введении патологических изменений не наблюдалось. В токсических дозах, вызывающих гибель всех или части подопытных животных, наблюдались выраженные морфологические изменения в печени. Максимальное повреждение опухолевой и нормальной тканей наблюдалось при проведении фотооблучения в момент наибольшей концентрации хлорина в крови, а преимущественное повреждение опухолевой ткани - при интервале времени между введением препарата и световым воздействием 24-72 ч. Терапевтическая доза фотооблучения составляет 45-135 Дж/см 2. Результаты испытаний показали, что полученный данным способом фармацевтический препарат является эффективным фотосенсибилизатором для лечении онкологических заболеваний при использовании метода лазеродинамической терапии. Данное соединение превосходит по своим характеристикам применяемые в настоящее время препараты на основе гематопорфирина. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения фармацевтического препарата для фотодинамической терапии онкологических заболеваний, включающий экстракцию из растительного сырья хлорофилла и его производных органическим растворителем, их окисление с выделением феофитина и последующим превращением его, отличающийся тем,что, из растительного сырья путем СО 2 экстракции под давлением 10-300 бар до извлечения хлорофилла этанолом отделяют каротиноиды и жирные кислоты, а превращение хлорофилла осуществляют незамедлительно обработкой концентрированной соляной кислотой и после его окислительного расщепления и выделения из солянокислого раствора и осаждения щело 10 чью при рН=4,00,2 проводят последующую очистку препарата и вводят стабилизатор. 2. Способ по п.1, отличающийся тем, что в качестве стабилизатора применяют раствор хитозана.
МПК / Метки
МПК: A61K 36/00, A61K 31/40
Метки: онкологических, способ, терапии, заболеваний, фотодинамической, фармацевтического, препарата, получения
Код ссылки
<a href="https://eas.patents.su/6-2318-sposob-polucheniya-farmacevticheskogo-preparata-dlya-fotodinamicheskojj-terapii-onkologicheskih-zabolevanijj.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения фармацевтического препарата для фотодинамической терапии онкологических заболеваний</a>
Предыдущий патент: Вакцина в виде геля
Следующий патент: Система сгорания газотурбинного двигателя.
Случайный патент: Способ концентрирования и обесфторивания фосфорной кислоты