Способ твердофазного синтеза альдегидов, кетонов, оксимов, аминов и гидроксамовой кислоты
Номер патента: 2478
Опубликовано: 27.06.2002
Авторы: Мейсон Хелен Дж., Салвино Джозеф М., Мортон Джордж К., Лябодиньер Ричард Ф.
Формула / Реферат
1. Способ получения кетона формулы
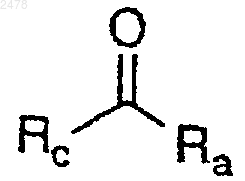
в которой
Rc и Ra независимо представляют собой алифатическую или ароматическую группу, включающий
a) i) сочетание карбоновой кислоты формулы RaCOOH с полимерной смолой гидроксиламина формулы
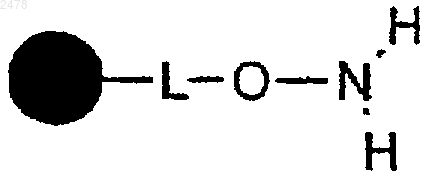
с образованием полимерной смолы гидроксамовой кислоты формулы
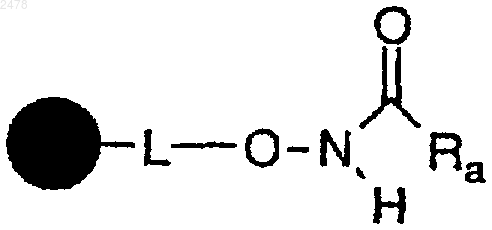
и с последующим взаимодействием полимерной смолы гидроксамовой кислоты с алкилирующим или арилирующим агентом формулы RbLG, где LG является уходящей группой,
с образованием полимерной смолы N-алкилированной или N-арилированной гидроксамовой кислоты общей формулы
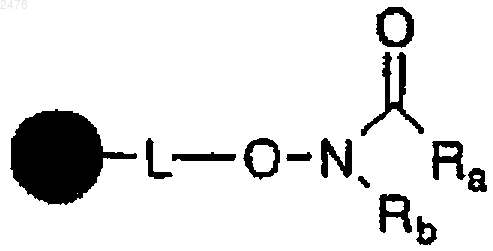
или
ii) взаимодействие полимерной смолы N-защищенного гидроксиламина формулы
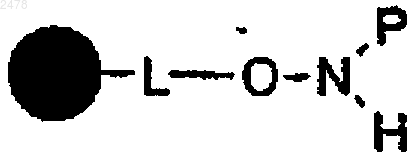
в которой Р является аминозащитной группой с алкилирующим или арилирующим реагентом формулы RbLG, где LG является уходящей группой,
с образованием полимерной смолы N-защищенного, N-алкилированного или N-арилированного гидроксиламина формулы
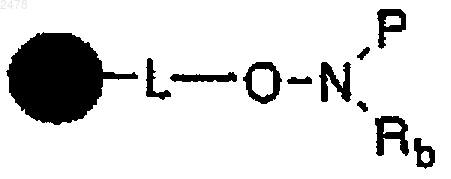
с последующим удалением аминозащитной группы с образованием полимерной смолы N-алкилированного или N-арилированного гидроксиламина формулы

и сочетанием полимерной смолы N-алкилированного или N-арилированного гидроксиламина с соединением карбоновой кислоты формулы RaCOOH с образованием полимерной смолы N-алкилированной или N-арилированной гидроксамовой кислоты формулы
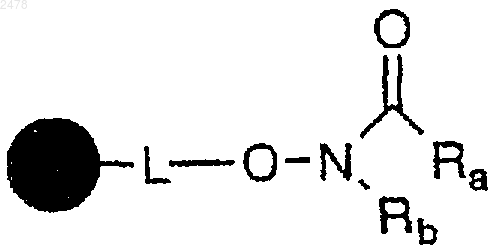
b) взаимодействие полимерной смолы N-алкилированной или N-арилированной гидроксамовой кислоты формулы
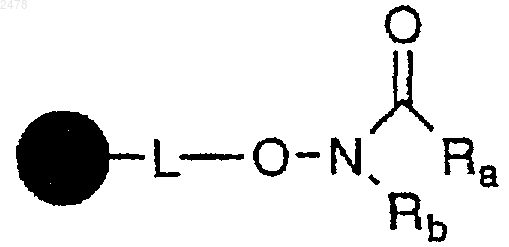
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу с металлоорганическим реагентом формулы RcM, в которой Rc представляет собой алифатический или арильный анион и М является катионом металла; и
представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу с металлоорганическим реагентом формулы RcM, в которой Rc представляет собой алифатический или арильный анион и М является катионом металла; и
с) выделение кетона из смолы.
2. Способ получения альдегида формулы RaCHO, в которой Ra представляет собой алифатическую или арильную группу, включающий
а) взаимодействие полимерной смолы N-алкилированной гидроксамовой кислоты формулы
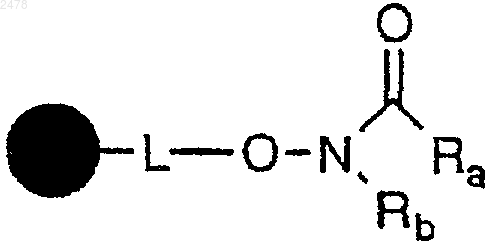
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу,
представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу,
с гидридным восстанавливающим агентом; и
b) выделение альдегида из смолы.
3. Способ получения полимерной смолы N-алкилированной гидроксамовой кислоты формулы
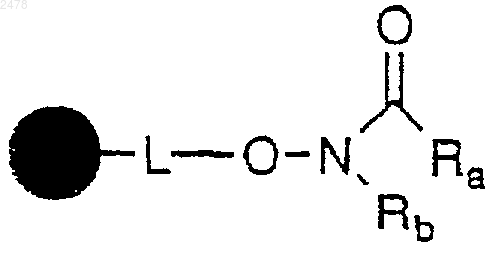
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу, включающий
представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу, включающий
а) сочетание карбоновой кислоты формулы RaCOOH с полимерной смолой гидроксиламина формулы
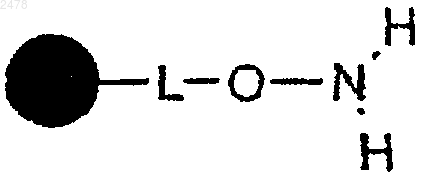
с образованием полимерной смолы гидроксамовой кислоты формулы

и
b) взаимодействие полимерной смолы гидроксамовой кислоты с алкилирующим агентом формулы RbLG, в которой LG является уходящей группой.
4. Способ по п.3, где полимерной смолой гидроксиламина является
смола 4-(О-метилгидроксиламин)феноксиметил-сополимер (стирол-1% дивинилбензол),
смола 4-[4-(O-метилгидроксиламин)-3-метоксифенокси]-(N-4-метилбензгидрил)бутирамид-сополимер (стирол-1% дивинилбензол),
смола 4-(2',4'-диметиоксифенил-O-метилгидроксиламин)феноксиметил-сополимер (стирол-1% дивинилбензол),
смола 4-[4-(1-аминооксиэтил)-2-метокси-5-нитрофенокси]-(N-4-метилбензгидрил)бутирамид-сополимер (стирол-1% дивинилбензол),
смола О-гидроксиламин-2'-хлортритил-сополимер (стирол-1% дивинилбензол),
смола O-гидроксиламинтритил-сополимер (стирол-1% дивинилбензол),
смола 5-(4-O-метилгидроксиламин-3,5-диметоксифенокси)валериановая кислота-сополимер (стирол-1% дивинилбензол),
смола 4-(O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметил-сополимер (стирол-1% дивинилбензол),
смола 4-(2',4'-диметоксифенил-O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметил-сополимер (стирол-1% дивинилбензол),
смола 4-O-метилгидроксиламин-3-метоксифенокси-сополимер (стирол-1% дивинилбензол) или
смола 3-гидроксиксантгидроламин-сополимер (стирол-1% дивинилбензол).
5. Способ получения полимерной смолы N-алкилированной гидроксамовой кислоты формулы
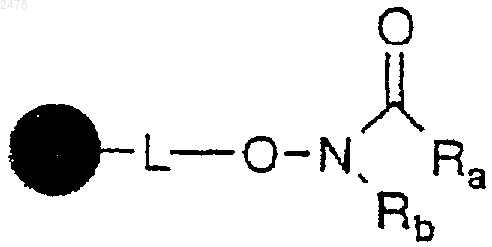
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу, включающий
представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу, включающий
а) взаимодействие полимерной смолы N-защищенного гидроксиламина формулы

в которой Р является аминозащитной группой, с алкилирующим агентом формулы RbLG, в которой LG является уходящей группой,
с образованием полимерной смолы N-защищенного, N-алкилированного гидроксиламина формулы

b) удаление аминозащитной группы с образованием полимерной смолы N-алкилированного гидроксиламина формулы

и
с) сочетание полимерной смолы N-алкилированного гидроксиламина с соединением карбоновой кислоты формулы RaCOOH.
6. Способ по п.5, где Р является аллилоксикарбонилом, бензилоксикарбонилом, п-метоксибензилоксикарбонилом, п-нитробензилоксикарбонилом, триметилсилилэтоксикарбонилом, 2,4-диметоксибензилоксикарбонилом, о-нитробензилоксикарбонилом, о-нитробензoлсульфонилом, п-нитробензoлсульфонилом и 2-нитро-4-трифторметилбензолсульфонилом.
7. Полимерная смола N-защищенного гидроксиламина формулы
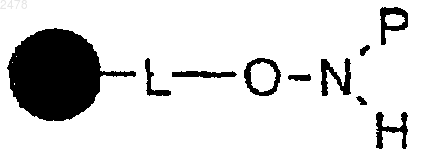
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой, и Р является аминозащитной группой, при условии, что Р отличается от 4-метоксибензила или 2,4-диметоксибензила.
представляет собой твердый носитель, L отсутствует или является связывающей группой, и Р является аминозащитной группой, при условии, что Р отличается от 4-метоксибензила или 2,4-диметоксибензила.
8. Полимерная смола N-защищенного гидроксиламина по п.7, в котором L является связывающей группой.
9. Полимерная смола N-защищенного гидроксиламина по п.8, в котором L является связывающей группой формулы
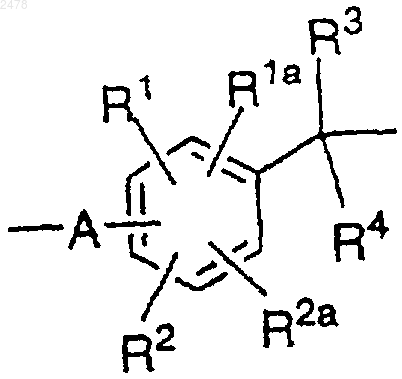
в которой
А отсутствует или представляет собой группу формулы -X1-Z-, в которой
Х1 представляет собой -CHR- или -CHR-Y-CO-(CH2)n-, в которой R является атомом водорода, алкилом, фенилом, замещенным -Н, алкилом, алкокси, атомом галогена, нитрилом или -NO2,
Y представляет собой -О- или -NH-,
n является целым числом от 1 до 6, и
Z представляет собой -О- или -NH-;
R1, R1a, R2 и R2a независшью представляют собой атом водорода, алкил, алкокси, атом галогена, нитрил или -NO2; и
R3 и R4 независимо представляют собой атом водорода, алкил, фенил или фенил, замещенный одним или несколькими заместителями, выбранными из алкила, алкокси, атома галогена, нитрила и -NO2;
или один из R1 и R2, взятый вместе с одним из R3 и R4 и атомами углерода, с которыми они связаны, образуют связывающую группу формулы
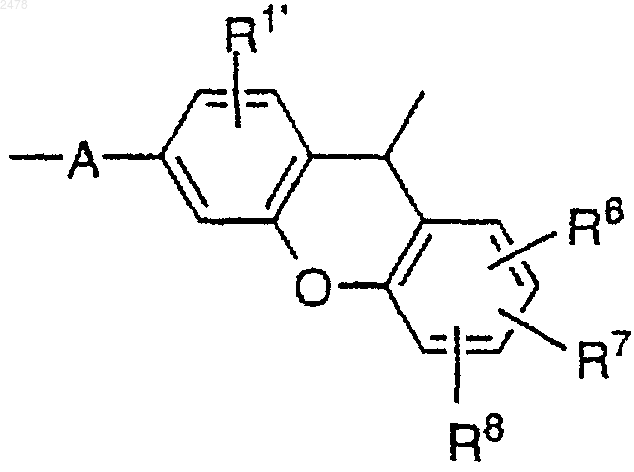
в которой
R1¢ представляет собой атом водорода, алкил, алкокси, атом галогена, нитрил или -NO2; и
R6, R7 и R8 независимо выбирают из атома водорода, алкила, алкокси, атома галогена, нитрила или -NO2.
10. Полимерная смола N-защищенного гидроксиламина по п.9, в котором Р является аллилоксикарбонилом, бензилоксикарбонилом, п-метоксибензилоксикарбонилом, п-нитробензилоксикарбонилом, триметилсилилэтоксикарбонилом, 2,4-диметоксибензилоксикарбонилом, о-нитробензилоксикарбонилом, о-нитробензолсульфонилом, п-нитробензолсульфонилом и 2-нитро-4-трифторметилбензолсульфонилом.
11. Полимерная смола N-защищенного гидроксиламина по п.10, которая представляет собой
смолу N-аллилоксикарбонил-4-(O-метилгидроксиламин)феноксиметил-сополимер (стирол-1% дивинилбензол),
смолу N-аллилоксикарбонил-4-[4-(O-метилгидроксиламин)-3-метоксифенокси]-(N-4-метилбензгидрил)бутирамид-сополимер (стирол-1% дивинилбензол),
смолу N-аллилоксикарбонил-4-(2',4'-диметоксифенил-O-метилгидроксиламин)феноксиметил-сополимер (стирол-1% дивинилбензол),
смолу N-аллилоксикарбонил-4-[4-(1-аминооксиэтил)-2-метокси-5-нитрофенокси]-(N-4-метилбензгидрил)бутирамид-сополимер (стирол-1% дивинилбензол),
смолу N-аллилоксикарбонил-O-гидроксиламин-2'-хлортритил-сополимер (стирол-1% дивинилбензол),
смолу N-аллилоксикарбонил-О-гидроксиламинтритил-сополимер (стирол-1% дивинилбензол),
смолу N-аллилоксикарбонил-5-(4-O-метилгидроксиламин-3,5-диметоксифенокси)валериановая кислота-сополимер (стирол-1% дивинилбензол),
смолу N-аллилоксикарбонил-4-(O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметил-сополимер (стирол-1% дивинилбензол),
смолу N-аллилоксикарбонил-4-(2',4'-диметоксифенил-O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметил-сополимер (стирол-1% дивинилбензол),
смолу N-аллилоксикарбонил-4-O-метилгидроксиламин-3-метоксифенокси-сополимер (стирол-1% дивинилбензол),
смолу N-аллилоксикарбонил-3-гидроксиксантгидроламин-сополимер (стирол-1% дивинилбензол).
12. Способ получения гидроксамовой кислоты формулы

в которой
А2 представляет собой простую связь, или алкиленовую группу, или NR13, в которой R13 является атомом водорода или алкилом;
R9 является группой формулы -L1-R14, где L1 представляет собой простую связь или линейную или разветвленную C1-C6-aлкиленовую группу, необязательно замещенную алкокси, арилом, карбокси, циано, циклоалкилом, атомом галогена, гетероарилом, гидроксилом или оксo, и R14 является атомом водорода, арилом, карбокси, циано, циклоалкилом, циклоалкенилом, циклокарбамоилом, циклоимидилом, гетероциклоалкилом, гетероарилом, группой -NH-C(=O)-NH2, (N-карбамоил)циклическим амином, -C=N-O-C(=O)-NH2, -C(=O)-NY1Y2, [где Y1 и Y2 независимо представляют собой атом водорода, алкил, арилалкил и арил, или заместитель Y1Y2N- образует 4-6-членный циклический амин, который необязательно содержит дополнительный гетероатом, выбранный из кислорода, серы, группы NH или NR13], -NY1SO2-арилом, группой -NHR13, -SR13 или -OR13; или группой -L2-R15, где L2 представляет собой линейную или разветвленную углеродную цепочку, содержащую от 2 до 6 атомов углерода, необязательно замещенную карбокси- или цианогруппой, которая содержит двойную или тройную углерод-углеродную связь, или прерывается атомом кислорода или серы, фениленовой группой, имино(-NН-) или алкилимино группой, или сульфинильной, или сульфонильной группой, и R15 является атомом водорода, арилом, карбокси, циано, циклоалкилом, циклоалкенилом, гетероциклоалкилом или гетероарилом; или R9 или R10, взятые вместе с атомом, с которым они связаны, образуют цикл; или R9 и R11, взятые вместе с атомом, через который они связаны, образуют цикл;
R10 и R12 независимо представляют собой атом водорода или алкил; или
R10 и R12 вместе образуют связь;
R11 представляет собой группу формулы -L3-R16, где L3 представляет собой простую связь или линейную или разветвленную C1-С6-алкиленовую группу, необязательно замещенную алкокси, арилом, карбокси, циано, циклоалкилом, атомом галогена, гетероарилом, гидроксилом или оксо; или L3 представляет собой линейную или разветвленную углеродную цепочку, содержащую от 2 до 6 атомов углерода, которая содержит двойную или тройную углерод-углеродную связь или прерывается атомом кислорода или серы, фениленовой группой, имином(-NН-) или алкилимином, или сульфинильной, или сульфонильной группой; и R16 является атомом водорода, арилом, циклоалкилом, циклоалкенилом, циклокарбамоилом, циклоимидилом, гетероциклоалкилом, гетероарилом, группой -NH-C(=O)-NH2, (N-карбамоил)циклическим амином, -C=N-O-C(=O)-NH2, -С(=O)-NY1Y2 [где Y1 и Y2 независимо представляют собой атом водорода, алкил, арилалкил и арил, или заместитель Y1Y2N- образует 4-6-членный циклический амин, который необязательно содержит дополнительный гетероатом, выбранный из кислорода, серы, группы NH или NR13], -NY1SО2-арилом, илиR11 и R9, взятые вместе с атомом, с которым они связаны, образуют цикл; или R11 и R12, взятые вместе с атомом, с которым они связаны, образуют цикл;
Аr является группой, выбранной из
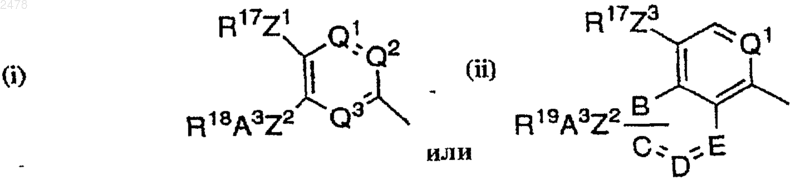
где R17 представляет собой линейную или разветвленную алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную одним или несколькими атомами галогена, или, когда Z3 является простой связью, R17 также может представлять собой атом водорода, алкенильную или алкинильную группу;
R18 представляет собой необязательно замещенный циклоалкил, циклоалкенил, гетероциклоалкил, арил, частично насыщенную бициклоарильную или гетероарильную группу;
R19 представляет собой R20, -OR20, -SR20, -SOR20, -SO2R20, -SO2NR20R21, -NR20SO2NR21, -NR20R21, -ОС(=O)NR20R21, -NR20C(=O)R21, -N(OH)C(=O)R20 или -C(=O)N(OH)R21, где R20 и R21, которые могут быть одинаковыми или различными, каждый представляет собой атом водорода или алкил, алкенил, гетероциклоалкил, циклоалкил, циклоалкенил, арил, гетероарил, арилалкильную или гетероарилалкильную группу, или группа NR20R21 представляет собой 5-7-членный циклический амин, который необязательно содержит один или несколько дополнительных гетероатомов, выбранных из кислорода, азота или серы, в которой, когда R18 является замещенной циклоалкильной группой, циклоалкильная группа замещена одним или несколькими (например, 1, 2 или 3) заместителями, выбранными из OR23, SR24, SOR24, SO2R24, NH2, NR13R24, =NOR24, =NOH, =NNHR24, =NOCONHR24, =NCO2R24, NHCOR24, NHSO2R24, SO2NR13R24, R23, CONHR24, CONHCH2CO2R13, CONR24R13 или N3; где R23 представляет собой атом водорода, алкил, циклоалкил, арил, арилалкил, гетероарил или гетероарилалкил; R24 является алкилом, циклоалкилом, циклоалкенилом, гетероциклоалкилом, арилом, гетероарилом, арилалкилом или гетероарилалкилом; или заместитель NR13R24 образует 4-7-членный циклический амин, который необязательно содержит дополнительный гетероатом, выбранный из кислорода, серы, группы NH или NR13, и в котором R18 является замещенной гетероциклоалкильной группой, содержащей атом азота, причем кольцо замещено по одному или нескольким (например, 1, 2 или 3) атомам углерода, и заместители выбирают из оксо-, циано-, CO2R13, CONHCH2CO2R13, арила, арилалкила или гидроксиалкила, и/или замещено по атому азота в кольце, причем заместитель выбирают из R13, (CH2)nCO2H, (СН2)nСО2R24, (СН2)nCONR13R24, (СН2)nCOR24, CONH2, CONHR24, COR24, SO2R24 или OR24;
А3 представляет собой простую связь или линейную или разветвленную C1-С6-алкиленовую группу, необязательно замещенную атомом галогена, гидроксилом, алкокси, оксо, циклоалкилом, арилом или гетероарилом; или А3 представляет собой линейную или разветвленную углеродную цепочку, содержащую от 2 до 6 атомов углерода, которая содержит двойную или тройную углерод-углеродную связь, или прерывается атомом кислорода или серы, фениленовой группой, имином(-NН-) или алкилимином, или сульфинильной или сульфонильной группой;
Z1 и Z3 каждый представляет собой атом кислорода или серы, простую связь или группу NH;
Z2 представляет собой атом кислорода или серы, или простую связь;
В, С, D и Е независимо представляют собой атом углерода или гетероатом, выбранный из кислорода, серы, азота, группы NOR22 или NR22, в которой R22 является атомом водорода или C1-С4-алкилом с линейной или разветвленной цепочкой, арилом, арил-С1-С4-алкилом, гетероарилом или гетероарил-С1-С4-алкилом, или три из В,С, D или Е представляют собой атом углерода или гетероатом, выбранный из кислорода, азота, группы NR22 или серы, а другой представляет собой простую связь; но исключая соединения, в которых два атома кислорода или серы находятся в соседних положениях, причем связи, соединяющие В, С, D и Е могут быть простыми или двойными;
Q1, Q2 и Q3, которые могут быть одинаковыми или различными, каждый представляет собой группу СН или СХ1 или атом азота; и
X1 представляет собой атом галогена; и
n равно 0, 1 или 2; или
ее N-оксида, пролекарственной формы, кислотной изостеры, фармацевтически приемлемой соли или сольвата, включающий
а) сочетание карбоновой кислоты формулы
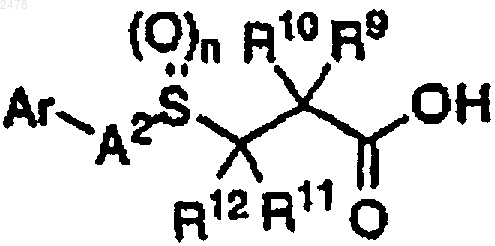
с полимерной смолой гидроксиламина формулы
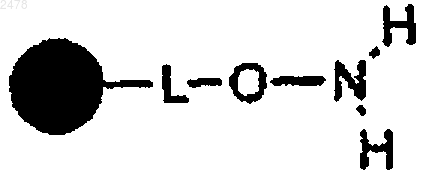
с образованием полимерной смолы гидроксамовой кислоты формулы
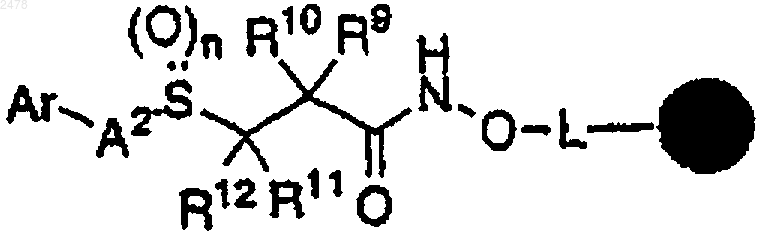
и
b) обработку полимерной смолы гидроксамовой кислоты кислотой.
13. Способ получения полимерной смолы оксима эфира формулы
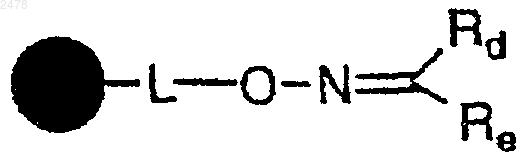
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой, a Rd и Re независимо представляют собой атом водорода, алифатическую или ароматическую группу,
представляет собой твердый носитель, L отсутствует или является связывающей группой, a Rd и Re независимо представляют собой атом водорода, алифатическую или ароматическую группу,
включающий взаимодействие полимерной смолы гидроксиламина формулы
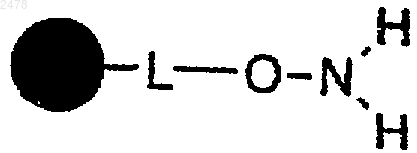
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой,
представляет собой твердый носитель, L отсутствует или является связывающей группой,
с карбонильным соединением формулы

14. Способ получения a-амина формулы
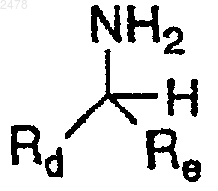
в которой Rd и Re независимо представляют собой атом водорода, алифатическую или арильную группу при условии, что Rd и Re оба не являются атомом водорода,
включающий восстановительное отщепление a-амина от полимерной смолы оксима эфира формулы
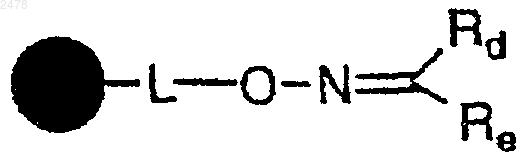
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой.
представляет собой твердый носитель, L отсутствует или является связывающей группой.
15. Способ по п.14, в котором восстановительное отщепление осуществляют последовательной обработкой полимерной смолы оксима эфира NaBH3CN и LiAlH4.
16. Способ получения замещенного a-амина формулы
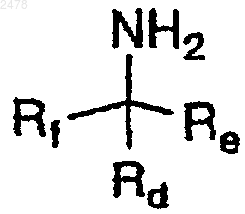
в которой Rd и Re независимо представляют собой атом водорода, алифатическую или ароматическую группу при условии, что Rd и Re оба не являются атомом водорода, и Rf представляет алифатическую или ароматическую группу, включающий
а) взаимодействие полимерного оксима эфира формулы
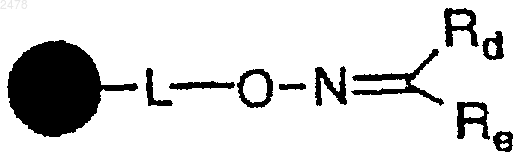
в которой  представляет твердый носитель, L отсутствует или является связывающей группой,
представляет твердый носитель, L отсутствует или является связывающей группой,
с металлоорганическим реагентом формулы RfM, в которой Rf является алифатическим или ароматическим анионом и М представляет катион металла, с образованием полимерной смолы a-замещенного гидроксиламина формулы
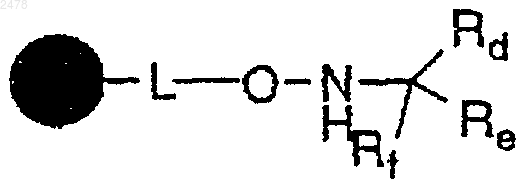
и
b) восстановительное расщепление смолы a-замещенного гидроксиламина.
17. Способ получения лактона формулы
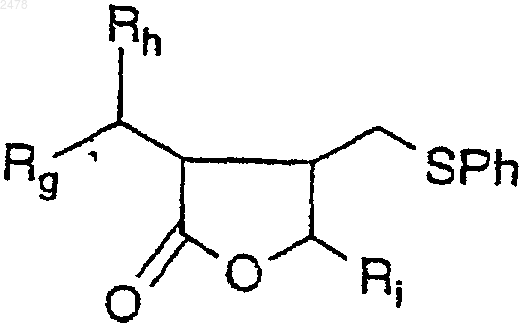
в которой Rg, Rh, Ri представляют алифатическую или ароматическую группу и Ph является фенилом, включающий
а) обработку полимерной смолы a,b-ненасыщенной гидроксамовой кислоты формулы
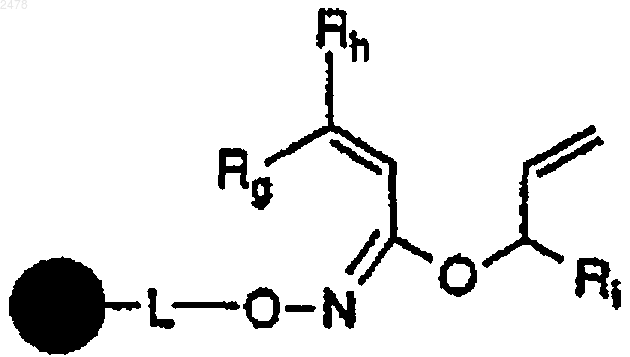
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой, тиофенолом и инициатором радикалов, с образованием полимерного оксимил-лактона формулы
представляет собой твердый носитель, L отсутствует или является связывающей группой, тиофенолом и инициатором радикалов, с образованием полимерного оксимил-лактона формулы
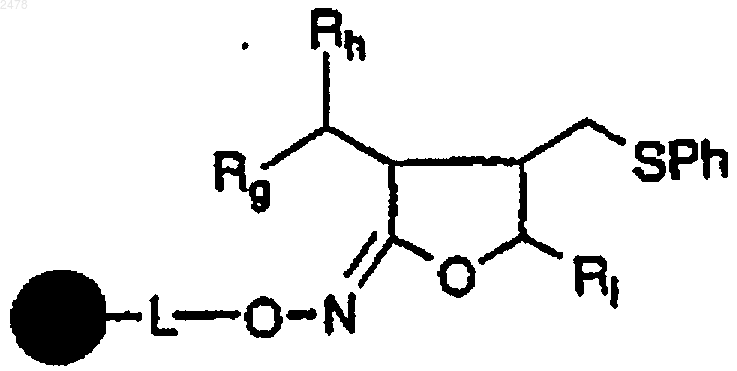
и
b) обработку полимерного оксимиллактона водной кислотой.
18. Способ по п.17, в котором полимерную смолу эфира a,b-ненасыщенной гидроксамовой кислоты формулы
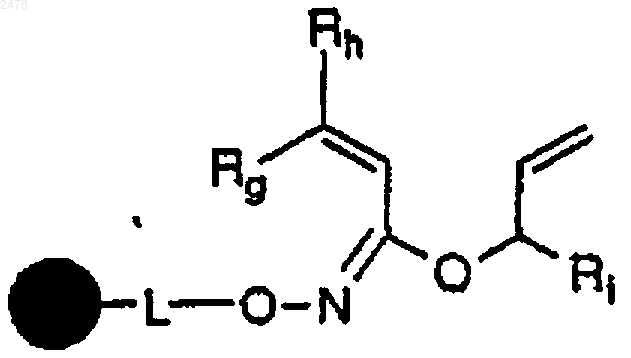
в которой  , L, Rg, Rh и Ri такие, как определено выше, получают взаимодействием полимерной смолы гидроксиламина формулы
, L, Rg, Rh и Ri такие, как определено выше, получают взаимодействием полимерной смолы гидроксиламина формулы
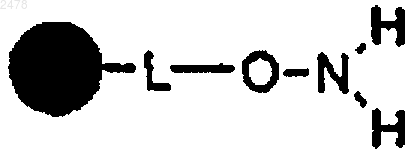
с эфиром a,b-ненасыщенной карбоновой кислоты формулы

19. Способ получения соединения a-циклического гидроксиламина формулы
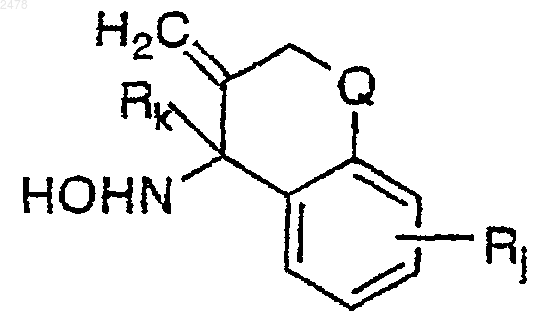
в которой Rj и Rk представляют алифатическую или ароматическую группу и Q является группой -О- или СH2-,
включающий
а) обработку полимерного оксима ацетофенона формулы
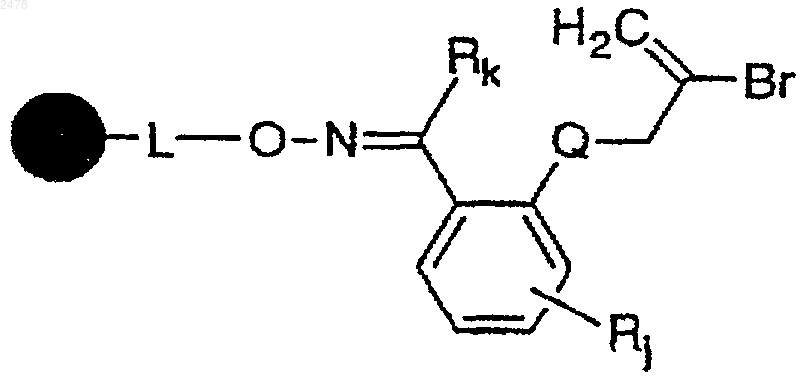
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой, гидридом триалкилолова и инициатором радикалов с образованием полимерной смолы a-циклического гидроксиламина формулы
представляет собой твердый носитель, L отсутствует или является связывающей группой, гидридом триалкилолова и инициатором радикалов с образованием полимерной смолы a-циклического гидроксиламина формулы
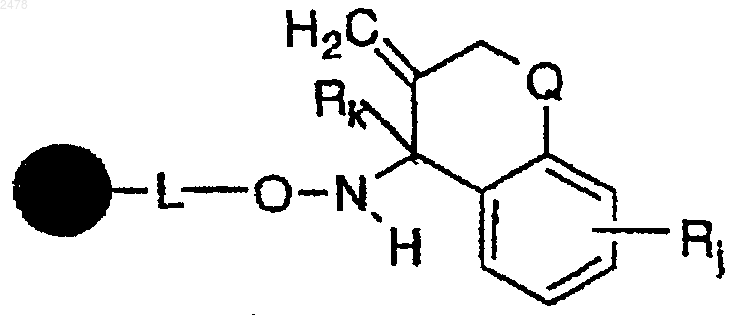
и
b) обработку полимерной смолы a-циклического гидроксиламина водной кислотой.
20. Способ получения соединения a-циклического амина формулы
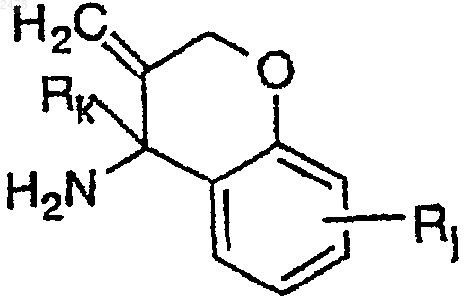
в которой Rj и Rk представляют алифатическую или ароматическую группу и Q является группой -О- или-СН2-,
включающий восстановительное расщепление полимерной смолы a-циклического гидроксиламина формулы

в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой.
представляет собой твердый носитель, L отсутствует или является связывающей группой.
21. Способ получения соединения a-циклического гидроксиламина формулы
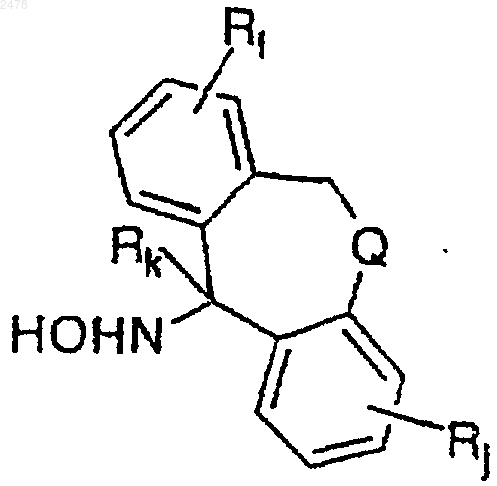
в которой Rj, Rk и Ri являются алифатической или ароматической группой и Q является группой -О- или-СH2-, включающий
а) обработку полимерного оксима ацетофенона формулы
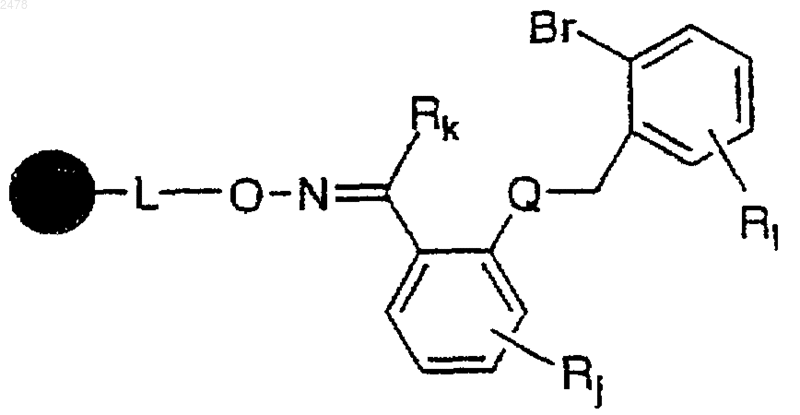
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой,
представляет собой твердый носитель, L отсутствует или является связывающей группой,
гидридом триалкилолова и инициатором радикалов с образованием полимерной смолы a-циклического гидроксиламина формулы
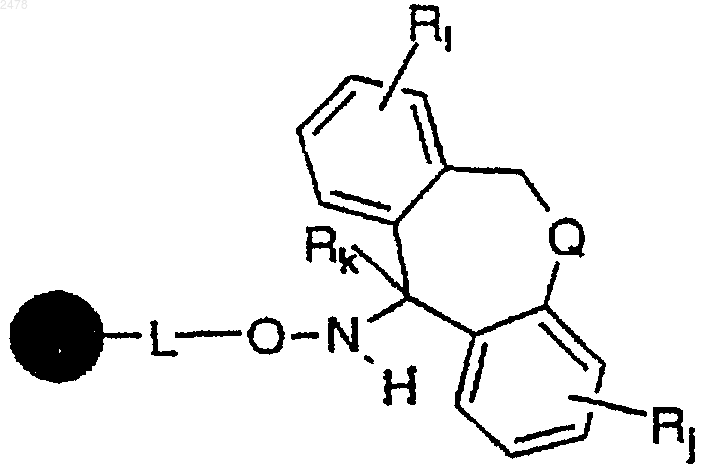
и
b) обработку полимерной смолы a-циклического гидроксиламина водной кислотой.
22. Способ получения a-циклического амина формулы
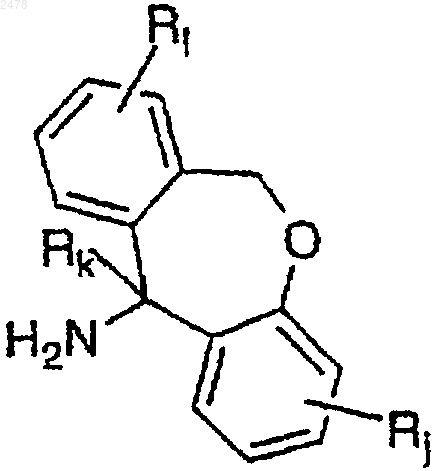
в которой Rj, Rk и Ri представляют алифатическую или ароматическую группу и Q является -О- или -СН2-,
включающий восстановительное расщепление полимерной смолы a-циклического гидроксиламина формулы
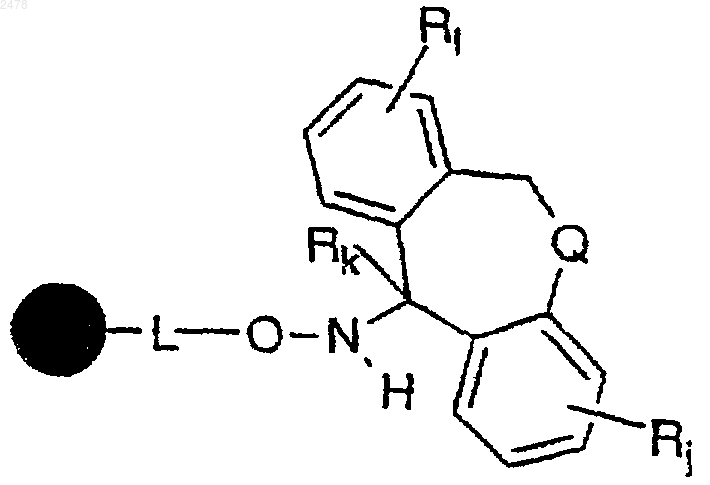
в которой  представляет собой твердый носитель, L отсутствует или является связывающей группой.
представляет собой твердый носитель, L отсутствует или является связывающей группой.
23. Способ по любому из пп.14, 16, 20 или 22, в котором восстановительное расщепление осуществляют, используя гидридный восстанавливающий агент.
24. Способ по любому из пп.1, 2, 3, 5, 13, 14, 16, 17, 19, 20, 21 или 22, в котором L является связывающей группой.
25. Способ по п.24, в котором L является связывающей группой формулы
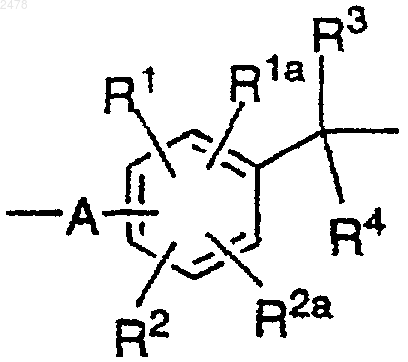
в которой
А отсутствует или представляет собой группу формулы -X1-Z-, в которой
Х1 представляет собой -CHR- или -CHR-Y-CO-(СН2)n, в которой R является атомом водорода, алкилом, фенилом, замещенным -Н, алкилом, алкокси, атомом галогена, нитрилом или -NO2,
Y представляет собой -О- или -NH-,
n является целым числом от 1 до 6, и
Z представляет собой -О- или -NH-;
R1, R1a, R2 и R2a независимо представляют собой атом водорода, алкил, алкокси, атом галогена, нитрил или -NO2; и
R3 и R4 независимо представляют собой атом водорода, алкил, фенил или фенил, замещенный одним или несколькими заместителями, выбранными из алкила, алкокси, атома галогена, нитрила и -NO2;
или один из R1 и R2, взятый вместе с одним из R3 и R4 и атомами углерода, с которыми они связаны, образуют связывающую группу формулы
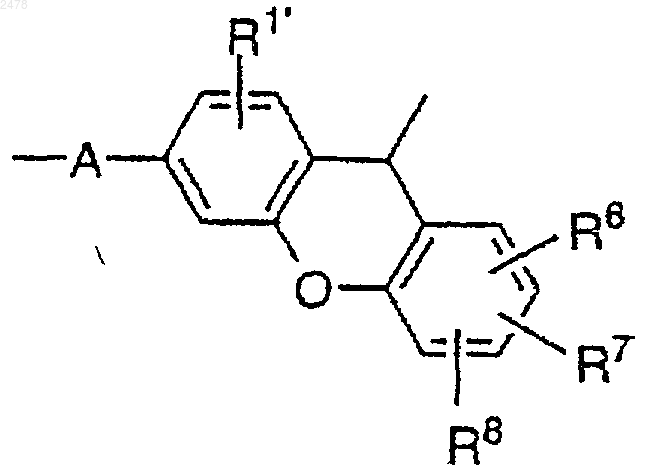
в которой
R1' представляет собой атом водорода, алкил, алкокси, атом галогена, нитрил или -NO2; и
R6, R7 и R8 независимо выбирают из атома водорода, алкила, алкокси, атома галогена, нитрила или -NO2.
26. Полимерная смола тетрафторфенилгидроксиламина формулы
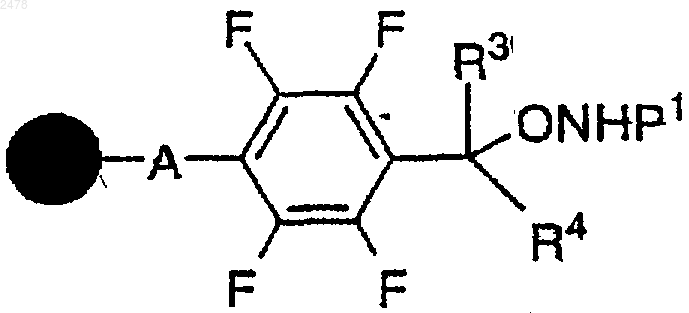
в которой  представляет собой твердый носитель, А отсутствует или представляет собой группу формулы -X1-Z-, в которой
представляет собой твердый носитель, А отсутствует или представляет собой группу формулы -X1-Z-, в которой
Х1 представляет собой -CHR- или -CHR-Y-CO-(СН2)n, в которой R является атомом водорода, алкилом, фенилом, замещенным -Н, алкилом, алкокси, атомом галогена, нитрилом или -NO2,
Y представляет собой -О- или -NH-,
n является целым числом от 1 до 6, и
Z представляет собой -О- или -NH-;
R3 и R4 независимо представляют собой атом водорода, алкил, фенил или фенил, замещенный одним или несколькими заместителями, выбранными из алкила, алкокси, атома галогена, нитрила и -NO2; и
Р1 является атомом водорода или аминозащитной группой.
27. Полимерная смола тетрафторфенилгидроксиламина по п.26, в которой один из радикалов R3 и R4 представляет собой атом водорода, а другой радикал представляет собой атом водорода или 2,4-диметоксифенил.
28. Полимерная смола тетрафторфенилгидроксиламина по п.27, в которой Р1 представляет собой атом водорода или аллилоксикарбонил.
29. Полимерная смола гидроксиламина по п.27, которая представляет собой смолу 4-(O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметил-сополимер (стирол-1% дивинилбензол) или смолу 4-(2',4'-диметоксифенил-O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметил-сополимер (стирол-1% дивинилбензол).
Текст
1 Область изобретения Настоящее изобретение относится к способам твердофазного синтеза альдегидов, кетонов, оксимов, аминов и гидроксамовой кислоты и к полимерной смоле гидроксиламина, используемой в синтезе. Предпосылки создания изобретения Методы твердофазного синтеза, в которых реагент иммобилизован на полимерном материале, который является инертным по отношению к используемым реагентам и условиям реакции, а также нерастворим в используемой среде, имеют важное значение как способы получения амидов, пептидов и гидроксамовых кислот. Краткий обзор многих методов твердофазного синтеза пептидов можно найти в публикациях J.M. Stewart and J.D. Young, Solid(Oxford, 1989). Использование твердофазной методики для получения непептидных молекул описано в работе С.С. Leznoff, Асе. Chem. Res.,v. 11, р. 327-333 (1978). Ряд полимерных реагентов в превращении простых функциональных групп нашли синтетическое применение. См. работы А. Akelah andReagents, Pierre Laszlo, ed., Academic Press Inc.,p. 193-212 (1987). Использование полимерных реагентов в реакциях окисления описано в J.M.J.G. Cainelli, J. Am. Chem. Soc., v. 98, 6737 (1976). Использование полимерных реагентов в реакциях галоидирования описано в J.M.J. Frechet et(1977). Использование полимерных реагентов в реакциях эпоксидирования описано в J.M.J. Frechet et al., Macromolecules, v. 8, 130 (1975) и C.R.Harrison et al., J. Chem. Soc. Chem. Commun.,1009 (1974). Использование полимерных реагентов в реакциях ацилирования описано в М.В.Shambhu et al., J. Chem. Soc. Chem. Commun.,619 (1974). Использование полимерных реагентов в реакциях Виттига описано в S.V. McKinleyet al., J. Chem. Soc. Chem. Commun., 134 (1972). Полимерные реагенты также нашли широкое применение в комбинаторном синтезе и для составления комбинаторных библиотек. Смотри публикации F. Balkenhohl et al. , Angew. Chem.(1996). Преимуществом полимерных реагентов является легкость их отделения от реагентов или продуктов с низкой молекулярной массой фильтрацией или селективным осаждением. Также можно использовать избыток полимерного реагента для осуществления быстрых и количественных превращений, таких как в случае ацилирования, или большой избыток реагентов можно использовать для того, чтобы сдвинуть равновесие реакции в направлении образования продукта, чтобы обеспечить практически количественное превращение в продукте, как в случае твердофазного синтеза пептидов. Дополнительным преимуществом реагентов и катализаторов, нанесенных на подложки, является то,что их можно рециркулировать, они легко применимы для автоматизированных процессов. Кроме того, аналоги токсичных и сильно пахнущих реагентов, нанесенные на подложки, более безопасны для использования. В опубликованной заявке РСТWO 96/26223 описан синтез соединений гидроксамовой кислоты с использованием твердофазного субстрата гидроксиламина. В Prasad et al. описано соединение Oметилгидроксиламинполистироловой смолы в J.Steroid Biochem., v. 18, 257-261 (1983). Краткое описание изобретения Настоящее изобретение относится к способу получения кетона формулы в которой Rc и Ra независимо представляют собой алифатическую или ароматическую группу,включающему а) взаимодействие полимерной смолы Nалкилированной гидроксамовой кислоты формулы в которой представляет собой твердый носитель, L отсутствует или является связывающей группой, Ra и Rb представляют алифатическую или арильную группу, с металлоорганическим реагентом формулы RcM, в которой Rc представляет собой алифатический или арильный анион и М представляет катион металла; иb) выделение кетона из смолы. В другом аспекте это изобретение относится к способу получения альдегида формулыRaCHO, в которой Ra определен выше, включающему а) взаимодействие полимерной смолы Nалкилированной гидроксамовой кислоты формулы 4 В другом аспекте изобретение относится к способу получения гидроксамовой кислоты формулыb) выделение альдегида из смолы. В другом аспекте это изобретение относится к способу получения полимерной смолы, L, Ra и Rb определены выше,включающему а) сочетание карбоновой кислоты формулыRaCOOH с полимерной смолой гидроксиламина формулы с образованием полимерной смолы гидроксамовой кислоты формулыb) взаимодействие полимерной смолы гидроксамовой кислоты с алкилирующим агентом формулы RbLG, в которой LG является уходящей группой. В другом аспекте изобретение относится к способу получения полимерной смолы Nалкилированной гидроксамовой кислоты формулы, L, Ra и Rb определены выше,включающему а) взаимодействие полимерной смолы Nзащищенной гидроксамовой кислоты формулы в которой Р является аминозащитной группой, с алкилирующим агентом формулы RbLG, в которой LG определена выше, с образованием полимерной смолы N-защищенной N-алкилированной гидроксиламина формулыb) удаление аминозащитной группы с образованием полимерной смолы N-алкилированной гидроксиламина формулы и с) сочетание полимерной смолы Nалкилированной гидроксиламина с карбоновой кислотой формулы RaCOOH. где А 2 представляет собой простую связь, или алкиленовую группу, или NR13, в которой R13 является атомом водорода или алкилом;R9 является группой формулы L1-R14, где 1L представляет собой простую связь, или линейную, или разветвленную C1-С 6-алкиленовую группу, необязательно замещенную алкокси,арилом, карбокси, циано, циклоалкилом, атомом галогена, гетероарилом, гидроксилом или оксо,и R14 является атомом водорода, арилом, карбокси, циано, циклоалкилом, циклоалкенилом,циклокарбамоилом, циклоимидилом, гетероциклоалкилом,гетероарилом,группойY1 и Y2 независимо представляют собой атом водорода, алкил, арилалкил и арил, или заместитель Y1Y2N- образует 4-6-членный циклический амин, который необязательно содержит дополнительный гетероатом, выбранный из кислорода, серы, группы NH или NR13], -NY1SO2 арилом, группой -NHR13, -SR13 или -OR13; или группой L2-R15, где L2 представляет собой линейную, или разветвленную углеродную цепочку, содержащую от 2 до 6 атомов углерода, необязательно замещенную карбокси- или цианогруппой, которая содержит двойную или тройную углерод-углеродную связь, или прерывается атомом кислорода или серы, фениленовой группой, имино(-NН-) или алкилимином, или сульфинильной, или сульфонильной группой, иR10 и R12 независимо представляют собой атом водорода или алкил; или R10 и R12 вместе образуют связь;R11 представляет собой группу формулы 3 16-L -R , где L3 представляет собой простую связь, или линейную или разветвленную C1-C6 алкиленовую группу, необязательно замещенную алкокси, арилом, карбокси, циано, циклоалкилом, атомом галогена, гетероарилом, гидроксилом или оксо; или L3 представляет собой линейную или разветвленную углеродную цепочку, содержащую от 2 до 6 атомов углерода,которая содержит двойную или тройную углерод-углеродную связь, или прерывается атомом кислорода или серы, фениленовой группой,имино(-NН-) или алкилимином, или сульфинильной, или сульфонильной группой; и R16 5 является атомом водорода, арилом, циклоалкилом, циклоалкенилом, циклокарбамоилом, циклоимидилом, гетероциклоалкилом, гетероарилом, группой -NH-C(=O)-NH2, (N-карбамоил) циклическим амином,-C=N-O-C(=O)-NH2,-C(=O)-NY1Y2 [где Y1 и Y2 независимо представляют собой атом водорода, алкил, арилалкил и арил, или заместитель Y1Y2N- образует 46-членный циклический амин, который необязательно содержит дополнительный гетероатом,выбранный из кислорода, серы, группы NH или где R17 представляет собой линейную, или разветвленную алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную одним или несколькими атомами галогена, или, когда Z3 является простой связью, R17 также может представлять собой атом водорода,алкенильную или алкинильную группу;R18 представляет собой необязательно замещенный циклоалкил, циклоалкенил, гетероциклоалкил, арил, частично насыщенную бициклоарильную или гетероарильную группу;R21, которые могут быть одинаковыми или различными, каждый представляет собой атом водорода, или алкил, алкенил, циклоалкил, циклоалкенил, гетероциклоалкил, арил, гетероарил,арилалкильную или гетероарилалкильную группу, или группа NR20R21 представляет собой 5-7 членный циклический амин, который необязательно содержит один или несколько дополнительных гетероатомов, выбранных из кислорода, азота или серы, в которой, когда R18 является замещенной циклоалкильной группой, циклоалкильная группа замещена одним или несколькими (например, 1, 2 или 3) заместителями, выбранными из OR23, SR24, SOR24, SO2R24, NH2,NR13R24,=NOR24,=NOH,=NNHR24,24 24 24=NOCONHR , =NCO2R , NHCOR , NHSO2R24,SO2NR13R24, R23, CONHR24, CONHCH2CO2R13,CONR24R13, или N3; где R23 представляет собой атом водорода, алкил, циклоалкил, арил, арилалкил, гетероарил или гетероарилалкил; R24 является алкилом,циклоалкилом, циклоалкенилом, гетероциклоалкилом, арилом, арилалкилом, гетероарилом или гетероарилалкилом; или заместительNR13R24 образует 4-7-членный циклический амин, который необязательно содержит допол 002478 6 нительный гетероатом, выбранный из кислорода, серы, группы NH или NR13, и в которой R18 является замещенной гетероциклоалкильной группой, содержащей атом азота, причем кольцо замещено по одному или нескольким (например, 1, 2 или 3) атомам углерода, и заместители выбирают из оксо-, циано-, СO2R13,CONHCH2CO2R13, арила, арилалкила, алкила или гидроксиалкила, и/или замещено по атому азота кольца, причем заместитель выбирают из(CH2)nCONR R ,(СН 2)nСОR ,CONH2,CONHR24, COR24, SO2R24 или OR24; А 3 представляет собой простую связь, или линейную,или разветвленнуюC1-C6 алкиленовую группу, необязательно замещенную атомом галогена, гидроксилом, алкокси,оксо, циклоалкилом, арилом или гетероарилом; или А 3 представляет собой линейную, или разветвленную углеродную цепочку, содержащую от 2 до 6 атомов углерода, которая содержит двойную или тройную углерод-углеродную связь, или прерывается атомом кислорода или серы, фениленовой группой, имино(-NН-) или алкилимином, или сульфинильной, или сульфонильной группой;Z1 и Z2 каждый представляет собой атом кислорода или серы, простую связь или группуZ2 представляет собой атом кислорода, или серы, или простую связь; В, С, D и Е независимо представляют собой атом углерода или гетероатом, выбранный из кислорода, серы, азота, группы NOR22 илиNR22, в которой R22 является атомом водорода,или С 1-С 4-алкилом с линейной или разветвленной цепочкой, арилом, арил-С 1-С 4-алкилом, гетероарилом или гетероарил-С 1-С 4-алкилом, или три из В, С, D и Е представляют собой атом углерода или гетероатом, выбранный из кислорода, азота или группы NR22 или серы, а другой представляет собой простую связь; но исключая соединения, в которых два атома кислорода или серы находятся в соседних положениях, причем связи, соединяющие В, С, D и Е могут быть простыми или двойными;Q1, Q2 и Q3, которые могут быть одинаковыми или различными, каждый представляет собой группу СН или СХ 1 или атом азота; и X1 представляют собой атом галогена; иn равно 0, 1 или 2; или ее N-оксида, пролекарственной формы, ее кислотной изостеры фармацевтически приемлемой соли или сольвата, включающий обработку полимерной смолы гидроксамовой кислоты формулы В другом аспекте изобретение относится к способу получения полимерной смолы оксима эфира формулыRe независимо представляют собой атом водорода, алифатический или ароматический радикал, включающий взаимодействие полимерной смолы гидроксиламина формулы в которой Rg, Rh и Ri представляет алифатическую или ароматическую группу и Ph является фенилом, включающему а) обработку полимерной смолы эфира В другом аспекте изобретение относится к способу получения -амина формулы в которой Rd и Re независимо представляют собой атом водорода, алифатическую или арильную группу, при условии, что Rd и Re оба не являются атомом водорода, включающему восстановительное расщепление полимерной смолы оксима эфира формулы в которой и L определены выше, с тиофенолом и инициатором радикалов с образованием полимерного оксимиллактона формулыb) обработку полимерного оксимиллактона водной кислотой. В другом аспекте изобретение относится к способу получения полимерной смолы эфира в которой и L такие, как определено выше. В другом аспекте изобретение относится к способу получения замещенного -амина формулы в которой Rd и Re независимо представляют собой атом водорода, алифатическую или ароматическую группу при условии, что Rd и Re оба не являются атомом водорода, и Rf представляет алифатическую или ароматическую группу,включающему а) взаимодействие полимерного оксима эфира формулы в которой и L такие, как определено выше, с металлоорганическим реагентом формулы RfM,в которой Rf представляет алифатический или ароматический анион, а М представляет катион металла, с образованием полимерной смолы замещенного гидроксиламина формулы-замещенного гидроксиламина. В другом аспекте изобретение относится к способу получения лактона формулы, L, Rg, Rh и Ri такие, как определено выше, включающему взаимодействие полимерной смолы гидроксиламина формулы В другом аспекте изобретение относится к способу получения -циклического гидроксиламина формулы в которой Rj и Rk представляют алифатическую или ароматическую группу и Q является -О- или-СН 2-, включающему а) обработку полимерного оксима ацетофенона формулы в которой и L определены выше, гидридом триалкилолова и инициатором радикалов с образованием полимерной смолы -циклического гидроксиламина формулыb) обработку полимерной смолы циклического гидроксиламина водной кислотой. В другом аспекте изобретение относится к способу получения -циклического амина формулыb) обработку полимерной смолы циклического гидроксиламина водной кислотой. В другом аспекте изобретение относится к способу получения -циклического амина формулы в которой Rj и Rk представляют алифатическую или ароматическую группу и Q является -О- или-CH2-, включающему восстановительное расщепление полимерной смолы -циклического гидроксиламина формулы в которой и L определены выше. В другом аспекте изобретение относится к способу получения -циклического гидроксиламина формулы в которой Rj, Rk и Rl представляют алифатическую или ароматическую группу и Q является-О- или -СН 2-, включающему а) обработку полимерного оксима ацетофенона формулы в которой и L определены выше, с гидридом триалкилолова и инициатором радикалов с образованием полимерной смолы -циклического гидроксиламина формулы в которой Rj, Rk и Rl представляют алифатическую или ароматическую группу и Q является-О- или -СН 2-,включающему восстановительное расщепление полимерной смолы -циклического гидроксиламина формулы в которой и L определены выше. В другом аспекте изобретение относится к способу получения полимерной смолы Nзащищенного гидроксиламина формулы в которой и L определены выше и Р является аминозащитной группой, при условии, что Р не является 4-метоксибензилом или 2,4 диметоксибензилом. В другом аспекте изобретение относится к полимерной смоле тетрафторфенилгидроксиламина формулы, А, R3 и R4 определены выше и Р является аминозащитной группой. Подробное описание изобретения Определение используемых терминов Используемые выше и во всем описании изобретения следующие термины имеют указанные ниже значения, если не указано иное."Твердый носитель" означает субстрат, который является инертным в отношении реагентов и описанных здесь условий реакции, а также является практически нерастворимым в используемой среде. Характерные твердые носители включают неорганические субстраты, такие как кизельгур, силикагель и стекло с регулируемым(форма с макропорами), полипропилен, полиэтиленгликоль, полиакриламид, целлюлозу и подобные; и композиционные неорганические/полимерные композиции, такие как полиакриламид, нанесенный внутри матрицы частиц кизельгура. См. J.M. Stewart and J.D. Young,Solid Phase Peptide Synthesis, 2nd. Ed., PierceChemical Co. (Chicago, IL., 1984). Кроме того, "твердый носитель" включает описанный выше твердый носитель, который закреплен на втором инертном носителе, таком как шпильки, описанные в Technical Manual фирмы Multipin SPOC, Chiron Technologies(1995) и содержащихся в нем ссылках, которые включают отделяемую головку на основе полиэтилена или полипропилена, графт-полимеризованную с аминофункционализованным сополимером метакрилата, и инертный стержень. Кроме того, "твердый носитель" включает полимерные носители, такие как полиэтиленгликолевые носители, описанные Janda et al.,Proc. Natl. Acad. Sci. USA, v. 92, 6419-6423(1995) и S. Brenner, WO 95/16918, которые растворимы во многих растворителях, но могут быть осаждены добавлением осаждающего растворителя."Полимерная смола гидроксиламина" означает твердый носитель, определенный выше,который химически модифицирован, как известно из уровня техники, чтобы ввести множество групп гидроксиламина (-ONH2) или защищенных групп гидроксиламина (-ONHP). Группы гидроксиламина или защищенного гидроксиламина ковалентно связаны непосредственно с твердым носителем или присоединены к твердому носителю ковалентными связями посредством связывающих групп. В соответствии со способом изобретения полимерная смола гидроксиламина обозначается здесь как или где является твердым носителем, который определен выше, L отсутствует или представляет связывающую группу, и Р является аминозащитной группой."Связывающая группа" и "линкер" означает группу, с помощью которой амино- или аминометильная функциональная группа может быть ковалентно связана с твердым носителем. Обычно связывающая группа является инертной по отношению к реагентам и описанным здесь условиям реакции."Aминозащитная группа" означает легко удаляемую группу, которая известна из уровня 12 техники для защиты аминогруппы от нежелательных реакций в ходе процедуры синтеза и которая может быть селективно удалена. Использование аминозащитных групп хорошо известно из уровня техники для защиты от нежелательных реакций в ходе синтеза, причем многие такие защитные группы известны, например, из Т.Н. Greene and P.G. Wuts, ProtectiveWileySons, New York (1991), которая включена в описание в качестве ссылки. Типичные аминозащитные группы включают формильную, ацетильную, хлорацетильную, трихлорацетильную,о-нитрофенилацетильную,онитрофеноксилацетильную,трифторацетильную, ацетоацетильную, 4-хлорбутирильную,изобутирильную, о-нитроциннамоильную, пиколиноильную, ацилизотиоцианатную, аминокапроильную, бензоильную, метоксикарбонильную,9-флуоренилметоксикарбонильную"Природная аминокислота" означает карбоновую кислоту, имеющую аминогруппу в положении по отношению к карбоксилатной группе, например, соединение формулы H2NCHR-COOH, в которой R является алифатическим или ароматическим радикалом, определенным в описании. Предпочтительные аминокислоты имеют L-стереохимию при -атоме углерода. Наиболее предпочтительными природными аминокислотами являются так называемые природные -аминокислоты, т.е. аланин,валин, лейцин, изолейцин, пролин, фенилаланин, триптофан, метионин, глицин, серин,треонин, цистеин, тирозин, аспарагин, глутамин, аспаргиновая кислота, глутаминовая кислота, лизин, аргинин и гистидин."Пептид" и "полипептид" означают полимер, в котором мономерами являются остатки природных и синтетических аминокислот, соединенных вместе посредством амидных связей. Термин "пептидный скелет" означает ряд амидных связей, с помощью которых соединяются аминокислотные остатки. Термин "аминокислотные остатки" означает индивидуальные звенья аминокислот, введенных в пептиды или полипептиды. Термин "синтетическая аминокислота" означает карбоновую кислоту, имеющую аминогруппу в положении, отличающемся от положения по отношению к карбоксилатной группе. Представители синтетических аминокислот включают -аланин и -аминомасляную кислоту. Термин "алифатический" означает соединение или радикал, которые не содержат ароматическое кольцо. Представители алифатических групп включают алкил, алкенил, алкинил, циклоалкил, циклоалкенил и подобные. Термин "ароматический" означает соединение или радикал, которые содержат, по меньшей мере, одно ароматическое кольцо. Термин"ароматическое кольцо" включает как арильные,так и гетероарильные кольца, которые определены в описании. Представители ароматических групп включают арил, арилалкенил, арилалкил,арилалкинил, бензил, гетероарил, гетероарилалкенил, гетероарилалкил, гетероарилалкинил и подобные. Термин "биоизостера кислоты" означает группу, которая обладает химическим и физическим подобием, обеспечивая довольно близкие биологические свойства (см. статьи Lipinski,Annual Reports in Medicinal Chemistry, 1986, v. 21, p. 283 "Bioisosterism In Drug Design"; Yun,Hwahak Sekye, 1993, v. 33, p. 576-579 "Application Of Bioisosterism To New Drug Design"; Zhao,Huaxue Tongbao, 1995, p. 34-38 "Bioisosteric Replacement And Development Of Lead CompoundsDesign: ab initio Electronic Distributions In Bioisosteres"). Примеры подходящих биоизостер кислот включают: -С(=O)-NH-OH, -С(=O)-СН 2OН,-C(=O)-CH2SH, -C(=O)-NH-CN, сульфо, фосфоно, алкилсульфонилкарбамоил, тетразолил,арилсульфонилкарбамоил, гетероарилсульфонилкарбамоил,N-метоксикарбамоил,3 гидрокси-3-циклобутен-1,2-дион,3,5-диоксо 1,2,4-оксадиазолидинил, или гетероциклические фенолы, такие как 3-гидроксиизоксазолил и 3 гидрокси-1-метилпиразолил."Ацил" означает группу Н-СО- или алкилСО-, в которой алкильная группа такая, как определено в описании. Предпочтительные ацилы содержат низшую алкильную группу. Примеры ацильных групп включают формил, ацетил, 002478"Ациламино" означает группу ацил-NH-, в которой ацильная группа такая, как определено в описании."Алкенил" означает алифатическую углеводородную группу, содержащую углеродуглеродную двойную связь, которая может быть разветвленной или неразветвленной и имеет приблизительно от 2 до 15 атомов углерода в цепи. Предпочтительные алкенильные группы имеют приблизительно от 2 до 12 атомов углерода в цепи и более предпочтительно приблизительно от 2 до 4 атомов углерода в цепи. Разветвленная цепочка означает, что к линейной алкенильной цепи присоединена одна или несколько низших алкильных групп, таких как метил, этил или пропил. Термин "низший алкенил" означает цепочку, содержащую приблизительно от 2 до 4 атомов углерода в цепи, которая может быть разветвленной или неразветвленной. Алкенильная группа может быть замещена одним или несколькими атомами галогена или циклоалкилом. Примеры алкенильных групп включают этенил, пропенил, н-бутенил,изобутенил, 3-метилбут-2-енил, н-пентенил,гептенил, октенил, циклогексилбутенил и деценил. Термин "алкокси" означает группу алкилO-, в которой алкильная группа такая, как определено в описании. Примеры алкоксигрупп включают метокси, этокси, н-пропокси, изопропокси, н-бутокси и гептокси. Термин "алкоксиалкил" означает группу алкил-O-алкил, в которой алкильные группы независимо представляют собой такие, как определено в описании. Примеры алкоксиалкильных групп включают метоксиэтил, этоксиметил,н-бутоксиметил и циклопентилметилоксиэтил. Термин "алкоксикарбонил" означает группу алкил-O-СО-, в которой алкильная группа такая, как определено в описании. Примеры алкоксикарбонильных групп включают метоксикарбонил и этоксикарбонил."Алкил" означает алифатическую углеводородную группу, которая может быть разветвленной или неразветвленной и имеет приблизительно от 1 до 15 атомов углерода в цепи. Предпочтительные алкильные группы имеют приблизительно от 1 до 12 атомов углерода в цепи. Разветвленная цепочка означает, что к линейной алкильной цепи присоединена одна или несколько низших алкильных групп, таких как метил, этил или пропил. Термин "низший алкил" означает цепочку, содержащую приблизительно от 1 до 4 атомов углерода в цепи, которая может быть разветвленной или неразветвленной. Алкильная группа может быть замещена одним или несколькими атомами галогена,циклоалкилом или циклоалкенилом. Примеры алкильных групп включают метил, фторметил,дифторметил, трифторметил, циклопропилме 15 тил, циклопентилметил, этил, н-пропил, изопропил, н-бутил, трет-бутил, н-пентил, 3 пентил, гептил, октил, нонил, децил и додецил. Предпочтительные алкильные группы для R9 включают метил, фторметил, дифторметил,трифторметил и этил."Алкилсульфинил" означает группу алкилSO-, в которой алкильная группа такая, как определено в описании. Предпочтительны те группы, в которых алкильная группа является низшим алкилом."Алкилсульфонил" означает группу алкилSO2-, в которой алкильная группа такая, как определено выше. Предпочтительны те группы, в которых алкильная группа является низшим алкилом. Термин "алкилтио" означает группу алкилS-, в которой алкильная группа такая, как определено выше. Примеры алкилтиогрупп включают метилтио, этилтио, изопропилтио и гептилтио."Алкинил" означает алифатическую углеводородную группу, содержащую углеродуглеродную тройную связь, которая может быть разветвленной или неразветвленной и имеет приблизительно от 2 до 15 атомов углерода в цепи. Предпочтительные алкинильные группы имеют приблизительно от 2 до 12 атомов углерода в цепи и более предпочтительно приблизительно от 2 до 4 атомов углерода в цепи. Разветвленная цепочка означает, что к линейной алкинильной цепи присоединена одна или несколько низших алкильных групп, таких как метил, этил или пропил. Примеры алкинильных групп включают этинил, пропинил, н-бутинил,изобутинил, 3-метилбут-2-инил, и н-пентинил."Ароил" означает группу арил-СО-, в которой арильная группа такая, как определено выше. Примеры ароильных групп включают бензоил, и 1- и 2-нафтоил."Ароиламино" означает группу ароил-NH-,в которой ароильная группа такая, как определено выше."Арил" как группа или часть группы означает необязательно замещенную моноциклическую или полициклическую ароматическую карбоциклическую группу, содержащую приблизительно от 6 до 10 атомов углерода. Примеры арильных групп включают фенил или нафтил, или фенил, или нафтил, замещенные одним или несколькими заместителями арильной группы, которые могут быть одинаковыми или различными, где "заместитель арильной группы" включает ацил, ациламино, алкокси, алкоксикарбонил, алкил, алкилсульфинил, алкилсульфонил, алкилтио, ароил, ароиламино, арил,арилалкокси, арилалкоксикарбонил, арилалкил,арилалкилтио, арилокси, арилоксикарбонил,арилсульфинил, арилсульфонил, арилтио, карбокси, циано, галоген, гетероароил, гетероарил,гетероарилалкил, гетероариламино, гетероарилокси, атом водорода, гидрокси, гидроксиалкил, 002478Y1 и Y2 независимо представляют собой атом водорода, алкил, арилалкил и арил, или Y1 и Y2,взятые вместе с атомом азота, с которым они связаны, образуют 4-7-членный гетероциклический радикал, который необязательно содержит дополнительный гетероатом, выбранный из кислорода, серы, NH или NR13. Предпочтительные заместители арильной группы включают ацил,ациламино, алкоксикарбонил, алкил, алкилтио,ароил, циано, галоген, атом водорода, гидрокси,нитро, Y1Y2N-, Y1Y2NCO- или Y1Y2NSO2-, гдеY1 и Y2 независимо представляют собой атом водорода и алкил."Арилалкенил" означает арилалкенильную группу, в которой арил и алкенил такие, как определено выше. Предпочтительно арилалкенилы содержат низшую алкенильную группу. Примеры арилалкенильных групп включают стирил и фенилаллил."Арилалкил" означает арилалкильную группу, в которой арил и алкил такие, как определено выше. Предпочтительно арилалкилы содержат низшую алкильную группу. Примеры арилалкильных групп включают бензил, 2 фенэтил и нафталинметил."Арилалкилокси" означает арилалкил-Oгруппу, в которой арилалкильная группа такая,как определено выше. Примеры арилалкилоксигрупп включают бензилокси и 1- или 2-нафталинметокси."Арилалкилоксиалкенил" означает арилалкил-O-алкенильную группу, в которой арилалкильная и алкенильная группы такие, как определено выше. Примером арилалкилоксиалкенильной группы является 3-бензилоксиаллил."Арилалкилоксиалкил" означает арилалкил-O-алкильную группу, в которой арилалкильная и алкильная группы такие, как определено выше. Примером арилалкилоксиалкильной группы является бензилоксиэтил."Арилалкоксикарбонил" означает арилалкил-O-СО-группу. Примером арилалкилоксикарбонильной группы является бензилоксикарбонил. Термин "арилалкилтио" означает группу арилалкил-S-, в которой арилалкильная группа такая, как определено выше. Примером арилалкилтиогруппы является бензилтио."Арилалкинил" означает арилалкинильную группу, в которой арил и алкинил такие, как определено выше. Предпочтительно арилалкинилы содержат низшую алкинильную группу. Примером арилалкинильной группы является фенилацетиленил."Арилокси" означает арил-O-группу, в которой арильная группа такая, как определено выше. Примеры арилоксигрупп включают фенокси и нафтокси."Арилоксиалкенил" означает арил-Oалкенильную группу, в которой арил или алкенильная группы такие, как определено выше. 17 Примером арилоксиалкенильной группы является феноксиаллил."Арилоксиалкил" означает арил-Oалкильную группу, в которой арильная и алкильная группы такие, как определено выше. Примером арилоксиалкильной группы является феноксипропил."Арилоксикарбонил" означает арил-O-СОгруппу, в которой арильная группа такая, как определено выше. Примеры арилоксикарбонильной группы включают феноксикарбонил и нафтоксикарбонил."Арилсульфинил" означает группу арилSO-, в которой арильная группа такая, как определено выше."Арилсульфонил" означает группу арилSO2-, в которой арильная группа такая, как определено выше. Термин "арилтио" означает группу арил-S-,в которой арильная группа такая, как определено выше. Примеры арилтиогрупп включают фенилтио и нафтилтио."(N-карбамоил)циклический амин" означает 5-7-членную циклоалкильную систему, в которой один из атомов углерода в цикле замещен группой N-C(=O)-NH2. Примером (N-карбамоил)циклического амина является"Бензил" означает фенил-СН 2- группу, в которой фенильное кольцо является незамещенным или замещенным одним или несколькими заместителями, независимо выбранными из алкила, алкокси, галогена и галогеналкила."Циклоалкенил" означает неароматическую моноциклическую или полициклическую систему, содержащую двойную углеродуглеродную связь и имеющую приблизительно от 3 до 10 атомов углерода. Предпочтительные моноциклические циклоалкенилы включают циклопентенил, циклогексенил или циклогептенил; более предпочтительным является циклопентенил. Предпочтительным полициклическим циклоалкенилом является норборненил. Циклоалкенильная группа может быть замещена одним или несколькими атомами галогена, метиленом (Н 2 С=) или алкилом."Циклоалкил" означает неароматическую моноциклическую или полициклическую систему, содержащую приблизительно от 3 до 10 атомов углерода. Примеры моноциклических циклоалкилов включают циклопропил, циклопентил, циклогексил и циклогептил. Предпочтительные моноциклические циклоалкилы дляR18 включают циклопентил и циклогексил. Предпочтительный моноциклический циклоалкил для R19 включает циклопропил. Примеры полициклических циклоалкилов включают пергидронафтил, адамант-(1- или 2-)ил и норборнил и спиробициклические группы, например спиро[4,4]нон-2-ил. Циклоалкильная группа может быть замещена одним или несколькими"Циклоалкилокси" означает циклолалкилO- группу, в которой циклолкильная группа такая, как определено выше. Примеры циклоалкилокси-групп включают циклопентилокси и циклогексилокси. в которой циклокарбамоильная группа состоит из оксооксазагетероциклической части, а алкильная группа такая, как описано выше. Алкильная группа может быть присоединена к карбамоилу либо через атом углерода, либо через атом азота карбамоила. Примером циклокарбамоилалкильной группы является Nоксазолидинилпропил. в которой имидная группа включает оксодиазагетероциклическую часть, а алкильная группа такая, как описано выше. Aлкильная группа может быть присоединена к карбамоилу либо через атом углерода, либо через атом азота карбамоила. Примером имидалкильной группы является N-фталимидпропил."Гало" и "галоген" означает фтор, хлор,бром или йод. Предпочтительными являются атомы фтора, хлора или брома и более предпочтительны фтор или хлор."Галогеналкил" означает определенную выше алкильную группу, замещенную одним или несколькими атомами галогена. Представители галогеналкильных групп включают хлорметил, бромэтил, трифторметил и подобные."Гетероароил" означает группу гетероарил-СО-, в которой гетероарильная группа такая, как определено выше. Примером гетероароильной группы является пиридилкарбонил."Гетероарил" как группа или часть группы означает необязательно замещенную моноциклическую или полициклическую ароматическую углеводородную систему, содержащую приблизительно от 5 до 10 атомов углерода, в которой один или несколько атомов и/или групп кольца отличаются от углерода, являясь, например,атомом азота, кислорода или серы. "Гетероарил" также может быть замещен одним или несколькими заместителями арильной группы. Примеры подходящих необязательно замещенных гетероарильных групп включают фурил, изокса 19 золил, изохинолинил, изотиазолил, 1,2,3 оксадиазол, 1,2,4-оксадиазол, 1,2,5-оксадиазол,1,3,4-оксадиазол, пиридазинил, пиридил, пиримидинил, хинолинил, 1,3,4-тиадиазолил, тиазолил, тиенил и 1,2,3- и 1,2,4-триазолильные группы, необязательно замещенные одним или несколькими заместителями арильной группы,которые определены выше. Когда R18 или R19 содержат необязательно замещенную гетероарильную группу, она в частности может представлять собой необязательно замещенную "азагетероарильную группу"(где термин "азагетероарильный" означает гетероарильную группу, содержащую приблизительно от 5 до 10 атомов, из которых один или несколько атомов кольца являются атомом(атомами) азота). Необязательные заместители для гетероарильной группы в пределах R18 илиR19 включают, например, атомы галогена и алкил, арил, арилалкил, гидрокси, оксо, гидроксиалкил, галогеналкил (например, трифторметил),алкокси, галогеналкокси (например, трифторметокси), арилокси и арилалкилоксигруппы. Предпочтительные гетероарильные группы в пределах R18 включают необязательно замещенный тиенил, тиазолил, пиридил, 1,2,4 оксадиазол или 1,3,4-оксадиазол. Предпочтительные гетероарильные группы в пределах R19 включают необязательно замещенный пиридил."Гетероарилалкенил" означает гетероарилалкенильную группу, в которой гетероарил и алкенил такие, как определено выше. Предпочтительно гетероарилалкенилы содержат низшую алкенильную группу. Примером гетероарилалкенильной группы является 4-пиридилвинил."Гетероарилалкил" означает гетероарилалкильную группу, в которой гетероарил и алкил такие, как определено выше. Предпочтительно гетероарилалкилы содержат низшую алкенильную группу. Примером гетероарилалкильной группы является 4-пиридилметил."Гетероарилалкилокси" означает гетероарилалкил-О-группу, в которой гетероарилалкильная группа такая, как определено выше. Примером гетероарилалкилоксигруппы является 4-пиридилметилокси."Гетероарилалкилоксиалкенил" означает гетероарилалкил-O-алкенильную группу, в которой гетероарилалкил и алкенил такие, как определено выше. Примером гетероарилалкилоксиалкенильной группы является 4 пиридилметилоксиаллил."Гетероарилалкилоксиалкил" означает гетероарилалкил-O-алкильную группу, в которой гетероарилалкил и алкил такие, как определено выше. Примером гетероарилалкилоксиалкильной группы является 4-пиридилметилоксиэтил."Гетероарилалкинил" означает гетероарилалкинильную группу, в которой гетероарил и алкинил такие, как определено выше. Предпочтительно гетероарилалкинилы содержат низшую алкинильную группу. Примером гетероа 002478 20 рилалкинильной группы является 4-пиридилэтинил."Гетероциклический радикал" означает моноциклическую или полициклическую систему, содержащую приблизительно от 4 до 10 атомов в цикле, в которой один или несколько атомов в циклической системе отличаются от углерода, причем их выбирают среди атомов азота, кислорода или серы. Гетероциклический радикал необязательно может быть замещен одним или несколькими заместителями алкильной группы. Примеры гетероциклических радикалов включают хинуклидин, пентаметиленсульфид, тетрагидропиранил, тетрагидротиофенил, пирролидинил, пиперидинил или тетрагидрофуранил."Гетероциклилалкил" означает гетероциклилалкильную группу, в которой гетероциклил и алкил такие, как определено выше. Предпочтительно гетероциклилалкил содержит низшую алкильную группу. Примером гетероциклилалкильной группы является тетрагидропиранилметил."Гетероциклилалкилоксиалкил" означает с гетероциклилалкил-О-алкильную группу, в которой гетероциклический радикал и алкил независимо являются такими, как определено выше. Примером гетероциклилалкилоксиалкильной группы является тетрагидропиранилметилоксиметил."Гидроксиалкил" означает НО-алкильную группу, в которой алкил такой, как определено выше. Предпочтительно гидроксиалкилы содержат низшую алкильную группу. Пример гидроксиалкильной группы включает гидроксиметил и 2-гидроксиэтил. Термин "частично насыщенный бициклоарил" означает группу, в которой арильная и циклоалкильная группа конденсированы вместе с образованием бициклической структуры. Примеры арилалкильных групп включают инданил и тетрагиронафтил, в особенности инданил. Предпочтительные варианты воплощения изобретения Способ получения альдегидов и кетонов в соответствии с настоящим изобретением представлен на схеме 1, в которой Ra и Rb независимо представляют собой любую алифатическую или ароматическую группу, совместимую с растворителями и реагентами, применяемыми в описанных здесь способах. Группы Ra и Rb могут быть дополнительно замещены и могут содержать функциональные группы, которые подходят для дальнейших химических превращений, будучи связанными с гидроксиламиновой смолой. Понятно, что когда эти функциональные группы обладают такой реакционной способностью, что они потенциально могут вступать в описанные ниже реакции, такие функциональные группы необходимо соответственно защищать. Исчерпывающая информация о за 21 щите и удалении защиты обычных функциональных групп приведена в Т.Н. Green, P.G.N.Rc представляет собой любую алифатическую или ароматическую группу, совместимую с использованием в качестве металлоорганического реагента. Схема 1 В соответствии с приведенной выше схемой 1 полимерную смолу гидроксиламина 1 подвергают сочетанию с производным карбоновой кислоты формулы RaCOOH, с получением полимерной смолы гидроксамовой кислоты 2. Реакцию сочетания осуществляют в присутствии активирующего агента, который известен в области пептидного синтеза. Представители активирующих агентов включают изопропилхлорформиат, диизопропилкарбодиимид (DIC),1-(3-диметиламинопропил)-3-этилкарбодиимид(HBTU),2-[2-оксо-1-(2 Н)пиридил]-1,1,3,3-биспентаметиленуроний тетрафторборат (TOPPipU), N,N'-дициклогексилкарбодиимид (DCC) и подобные. Подходящие растворители для этой реакции сочетания включают дихлорметан, диметилформамид (ДМФ),диметилсульфоксид, тетрагидрофуран (ТГФ) и подобные. Время реакции сочетания изменяется приблизительно от 2 до 24 ч, в зависимости от сочетаемых смолы и производного карбоновой кислоты, активирующего агента, растворителя и температуры. Сочетание проводят при температуре приблизительно от -10 до 50 С, предпочтительно при комнатной температуре. Предпочтительно реакцию сочетания проводят при комнатной температуре в диметилформамиде, используя гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимид в течение приблизительно около 12 ч. 22 Затем полимерную смолу гидроксамовой кислоты 2 алкилировали алкилирующим агентом формулы RbLG, где LG представляет собой уходящую группу, в присутствии такого ненуклеофильного основания, как 1,8-диазабицикло[5.4.0.]ундец-7-ен (DBU) в среде такого инертного органического растворителя, как толуол, с образованием полимерной смолы Nалкилированной гидроксамовой кислоты 3. Количество добавляемого алкилирующего агентаRbLG может изменяться в интервале от эквимолярного до избыточного, составляющего, примерно, 25 молярных эквивалентов. Предпочтительным является избыток, примерно, 15 молярных эквивалентов. Ненуклеофильное основание может добавляться в количестве от эквимолярного до избыточного, составляющего,примерно, 10 молярных эквивалентов. Предпочтительным является количество около 5 молярных эквивалентов. Уходящая группа представляет собой любую группу, способную к нуклеофильному замещению атомом азота полимерной смолы гидроксамовой кислоты 2 в описанных выше условиях проведения реакции. Предпочтительная уходящая группа представляет собой галоген. С тем чтобы удостовериться в удовлетворительном протекании реакции, образец полимерной смолы N-алкилированной гидроксамовой кислоты 3 может быть подвергнут ацидолизу с целью расщепления замещенной гидроксамовой кислоты. Реакция полимерной смолыNалкилированной гидроксамовой кислоты 3 с металлоорганическим реагентом формулы RcM,в которой Rc представляет собой алифатический или ароматический анион, а М представляет собой катион металла, с последующим кислотным гидролизом, дает кетон 4. Предпочтительными металлоорганическими реагентами могут служить литийорганические реагенты формулыRcLi, а также реагенты Гриньяра формулыRcMgX, где Х представляет собой галоген. В предпочтительном способе получения кетонов согласно этому аспекту изобретения, полимерную N-алкилированную смолу гидроксамовой кислоты 3 обрабатывают RcМgХ в среде диэтилового эфира, при температуре окружающей среды в течение, примерно, 18 ч и затем реакционную смесь гасят добавлением водного раствора НСl или водного раствора KHSO4, с целью выделения кетона 4. Альдегиды получают обработкой полимерной смолы N-алкилированной гидроксамовой кислоты 3 гидридным восстанавливающим агентом, с последующим кислотным гидролизом, как показано на приведенной выше схеме 1. Примерами гидридных восстанавливающих агентов могут служить LiAlH4, (изо-Bu)2 АlН,LiAlH(О-трет.-Bu)3, LiAlH4-EtOH, LiAlH4-MeOH и подобные. Предпочтительными восстанавливающими агентами являются LiAlH4 и LiAlH4 23MeOH. Кислотный гидролиз, предпочтительно,проводят с помощью водного раствора KHSO4. Как показано на схеме 1 полимерная смолаN-алкилированной гидроксамовой кислоты 3 представляет собой вещество подобное амидуWeinreb, используемому для синтеза альдегидов и кетонов (S. Nahm и S. Weinreb, Tet. Lett. 1981,22, 3815-3818). Такая полимерная смола Nалкилированной гидроксамовой кислоты обладает преимуществами перед известными ранее примерами смолы, связанной с амидами типаArmstrong, Tet. Lett., 1996, 37, 1161-1164), состоящими в том, что такое соединение может быть N-алкилировано объемными липофильными группами, такими как бензил, замещенный бензил, нафтил или алкильная группа, необходимыми для оптимизации реакции в твердой фазе. Так например, N-бензил-О-метилполистирильная часть весьма подходит для образования устойчивого металл-хелатированного промежуточного продукта. Предполагают, что липофильная бензильная группа помогает защищать хелат и обеспечивает его устойчивость. Предпочтительный способ получения альдегидов и кетонов представлен на cхеме 2. Вcхеме 2 "Р" представляет собой аминозащитную группу, имеющую указанные выше значения. Схема 2 Как показано на приведенной выше схеме 2, полимерную смолу гидроксиламина защищают с помощью аминозащитной группы с образованием N-защищенной полимерной смолы гидроксиламина 6. Затем полимерную смолу Nзащищенного гидроксиламина 6 алкилируют в соответствии с приведенной выше схемой 1 с образованием полимерной смолыNалкилированного N-защищенного гидроксиламина 7. Удалением аминозащитной группы получают полимерную смолу N-алкилированного гидроксиламина 8. Как показано выше,взаимодействие 8 с карбоновой кислотой приводит к образованию полимерной смолы Nалкилированной гидроксамовой кислоты 3, ко 002478 24 торую превращают в кетон 4 или альдегид 5, как показано на приведенной выше схеме 1. Предпочтительные аминозащитные группы включают аллилоксикарбонил (Aloc), бензилоксикарбонил (Cbz), п-метоксибензилоксикарбонил (Moz), п-нитробензилоксикарбонил(Теос), 2,4-диметилоксибензилоксикарбонил, онитробензилоксикарбонил, о-нитробензилсульфонил (o-Nbs), п-нитробензилсульфонил (pNbs), и 2-нитро-4-трифторметилбензолсульфонил. Наиболее предпочтительная аминозащитная группа представляет собой аллилоксикарбонил. Предпочтительные полимерные смолы Nзащищенного гидроксиламина включают смолу N-аллилоксикарбонил-4-(O-метилгидроксиламин)-феноксиметил-сополимера(стирол-1% дивинилбензол) и смолу N-аллилоксикарбонил-3-гидроксиксантидроламин-сополимера (стирол-1% дивинилбензол). Наиболее предпочтительная полимерная смола N-защищенного гидроксиламина представляет собой смолу N-аллилоксикарбонил-4(O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол). В том случае, когда соединение карбоновой кислоты RaCO2H представляет собой при 25 родную или синтетическую аминокислоту или пептид, способы, описанные на схемах 1 и 2,обеспечивают легкий путь получения альдегидов аминокислоты или пептида, который ранее считался затруднительным. Способ получения аминов согласно настоящему изобретению представлен на схеме 3. На схеме 3 Rd и Re независимо представляют собой Н или любую алифатическую или ароматическую группу, устойчивую к действию растворителей и реагентов, используемых в описанных способах, при условии, что оба радикалаRc и Rd не представляют собой Н. Группы Ra, Rb и Rc могут быть дополнительно замещены и могут содержать функциональные группы, подходящие для дальнейших химических трансформаций, будучи присоединенными к гидроксиламиновой смоле. Следует иметь в виду, что в том случае, когда такие функциональные группы обладают реакционной способностью и потенциально могут вступать в описанные ниже реакции, такие функциональные группы должны быть защищены надлежащим образом. Общий обзор защиты и снятия защиты для традиционных функциональных групп представлен в Т.Н. Greene и P.G.M. Wuts, Protective Groups inOrganic Synthesis, 2nd edition, John WileySons,New York (1991), которая включена сюда в качестве ссылки. Rf представляет собой любую алифатическую или ароматическую группу, которая подходит для применения в качестве части металлоорганического реагента. алифатический или ароматический анион, а М представляет собой указанный выше катион металла,дает полимерную смолу замещенного гидроксиламина 12. ОтщеплениеUkaji с сотр., Chem. Lett., 173, (1991) и R.P. Dieter с сотр Can. J. Chem. 71, 814 (1993). Предпочтительные катионы металла представляют собой Li и МgХ, где Х представляет галоген. Добавление такого хирального вспомогательного агента, как хиральный линкер бензилгидроксиламин, дает хиральные -замещенные амины. На схеме 4 показан способ получения лактонов радикальной циклизацией. На схеме 4 Rg,Rb и Ri представляют собой алифатическую группу или арил, имеющие указанные выше значения. О. Как показано на приведенной выше схеме 4, полимерная смола гидроксиламина 1 реагирует с ,-ненасыщенным сложным эфиром карбоновой кислоты 14 с образованием соединения полимерной смолы оксима 15. Радикальная циклизация 15, например, нагреванием в присутствии 2,2'-азобисизобутиронитрила(АИБН) и тиофенола, в среде такого инертного органического растворителя, как бензол, приводит к образованию полимерной смолы gлактона 16. В результате кислотного гидролиза 16 с использованием, например, 10% водного раствора НСl получают лактон 17. См. О. Miyata с сотр., Tet. Lett., 37, 229-232 (1996). На схеме 5 изображен способ получения карбоциклических или гетероциклических соединений путем радикальной циклизации. Rj, Rk и Rl на схеме 5 представляют алифатические или арильные группы, определенные выше. Методика, описанная на схеме 1, применима для получении 5-, 6- или 7-членных колец. Карбоциклы получают при замене фенольного кислородного атома атомом углерода. Согласно приведенной выше схеме 3, реакция полимерной смолы гидроксиламина 1 с альдегидом или кетоном 9 приводит к получению полимерной смолы простого эфира оксима 10. Предпочтительно образование оксима происходит при температуре окружающей среды в результате набухания полимерной смолы гидроксиламина 1 в таком подходящем инертном органическом растворителе, как дихлорметан, с последующим добавлением избытка альдегида или кетона. Восстановительное расщепление смолы, например, реакцией с NaCNBH3 или ВН 3.THF, и последующая реакция с LiAlH4 дает амин 11. Реакция полимерной смолы простого эфира оксима 10 с металлоорганическим реагентом формулы RfM, где Rf представляет собой В соответствии с приведенной выше схемой 5 полимерная смола гидроксиламина 1 реагирует с ацетофеноном 18 и бромалкеном или обромбензилом с образованием полимерного оксима ацетофенона 19 или 23. Радикальная циклизация 19 или 23, например, нагреванием в присутствии АИБН и гидрида три-нбутилолова, в среде такого инертного органического растворителя, как бензол, приводит к образованию полимерной смолы N-циклил гидроксиламина 20 или 24. Обработка 20 или 24 кислотой, предпочтительно трифторуксусной кислотой, приводит к образованию циклической гидроксамовой кислоты 21 или 25. Восстановительное расщепление 20 или 24, например, с использованием LiAlH4, как описано для схемы 3 выше, приводит к образованию циклического амина 22 или 26. См. S.E. Booth с сотр., J. Chem.Soc. Commun., 1248-1249, (1991). Способ получения гидроксамовой кислоты формулы 29, в которой n и группы Аr, A2, R9,R10, R11 и R12 имеют указанные выше значения,показан на схеме 6. Схема 6b) 50% TFA в CH2Cl2 (100 экв.); 30 мин. В соответствии с приведенной выше схемой 6 карбоновую кислоту 27 связывают с полимерной смолой гидроксиламина 1, как показано выше на схеме 1, с образованием полимерной смолы гидроксамовой кислоты 28. Затем полимерную смолу гидроксамовой кислоты 28 обрабатывают такой кислотой, как трифторуксусная кислота (TFA) в среде такого инертного растворителя, как дихлорметан, с получением гидроксамовой кислоты 29. Необходимо использовать повышенные процентные количества TFA (трифторуксусной кислоты) и большие времена реакции с тем, чтобы отщепить гидроксамовую кислоту от смолы типа Wang по сравнению со смолой типа Rink. В процессе выпаривания TFA при обработке, проводимой для выделения гидроксамовой кислоты, было установлено, что нагревание образца в процессе концентрирования приводит к образованию в качестве побочного продукта значительного количества N,O-диацилированного димера родительской гидроксамовой кислоты. С целью минимизации такой побочной реакции, реакционную смесь концентрируют при комнатной или более низкой температуре в присутствии толуола, используемого для образования азеотропа. Способ твердофазного синтеза карбоновой кислоты 27 показан на схеме 7. На схеме 7 Ar,A2, n, R9, R10, R11 и R12 имеют указанные выше значения. Схема 7 Например, полимерную гидроксисмолу 30 обрабатывают диэтилфосфоноуксусной кислотой в среде такого инертного растворителя, как диметилформамид в присутствии хлористого 2,6-дихлорбензоила и пиридина, при температуре, близкой к комнатной, с образованием соединения полимерной диэтилфосфоноацетокси смолы 31. Полимерную смолу диэтилфосфоноацетокси 31 обрабатывали таким основанием, как бис(триметилсилил)амид в среде такого инертного растворителя, как толуол, при температуре около 0 С, с последующей обработкой альдегидом формулы R11CHO, где R11 имеет указанное выше значение, при температуре, близкой к температуре окружающей среды, с образованием полимерной алкеноатной смолы 32. 29 Затем полимерная смола алкеноата 32 реагировала с тиолом формулы Ar-A2-SH; где Аr и А 2 имеют указанные выше значения, с образованием полимерной смолы алканоата 33. Присоединение обычно проводят в мягких основных условиях, например, в присутствии гидроксида лития, при температуре окружающей среды. Затем полимерная смола алканоата 33 может быть гидролизована обработкой такой кислотой, как трифторуксусная кислота, в среде такого инертного растворителя, как дихлорметан, с получением кислоты 35, где n равно 0. Альтернативно полимерная смола алканоата 33 может быть обработана таким окисляющим агентом, как м-хлорпербензойная кислота в среде такого инертного растворителя,как диоксан, при температуре, близкой к температуре окружающей среды с образованием соединения полимерной смолы сульфоксида (n=1) или сульфона (n=2) 34. В результате гидролиза соединения 34, как указано выше, получают карбоновую кислоту 35. На схеме 8 показано получение полимерной смолы гидроксиламина 1. Схема 8 Согласно приведенной выше схеме 8 полимерную гидроксисмолу 30 превращают в полимернуюN-гидроксифталимидосмолу 36 взаимодействием с N-гидроксифталимидом в условиях Mitsunobu (Mitsunobu, O., Synthesis 1981, 1), превращением гидроксигруппы в такую уходящую группу, как мезилат, с последующим нуклеофильным замещением или реакцией полимерной гидроксисмолы с Nгидроксифталимидом в присутствии такой кислоты, как бензолсульфокислота. В результате удаления фталимидогруппы получают полимерную смолу гидроксиламина 1. Так, например, когда 30 представляет собой смолу 4-(гидроксиметил)феноксиметилсополимера (стирол-1% дивинилбензол) (смолаWang), N-гидроксифталимид сшивается со смолой в присутствии диизопропилазодикарбоксилата и трифенилфосфина в ДМФ. Фталимидную защиту удаляют метиламинолизом в ТГФ при 40 С. Реакция завершается за 2 ч. Применение метиламина для отщепления фталимидной защиты дает значительное преимущество по сравнению с традиционно применяемым методом гидразинолиза (Wolf с сотр., Can. J. Chem.,48, 3572, (1970. При использовании смолы 4-(2',4'диметоксифенил-O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол) (смола Rink), соединение 1 предпочти 002478 30 тельно получают реакцией полимерной гидроксисмолы с N-гидроксифталимидом в среде ДМФ, в присутствии каталитического количества бензолсульфокислоты с образованием полимерной смолы N-гидроксифталимида 36. Затем фталимидозащитную группу удаляют реакцией с гидразингидратом в среде трет.-бутанола при 60 С с образованием соответствующей полимерной смолы гидроксиламина. Альтернативный путь получения полимерной смолы N-защищенного гидроксиламина 6 показан на схеме 9. Схема 9 Согласно приведенной выше схеме 9 полимерную гидроксисмолу 30 связывают с N,Nдизамещенным гидроксиламином 37, в котором Р и Р' представляют собой аминозащитные группы, как это показано выше на схеме 8, с образованием смолы N,N-защищенного гидроксиламина 38. Затем аминозащитную группу Р' селективно удаляют с образованием полимерной смолы N-защищенного гидроксиламина 6. В соответствии с предпочтительным вариантом синтеза, описанного на схеме 9, Р представляет собой бензил, а Р' представляет собой аллилоксикарбонил. Селективное удаление аллилоксикарбонильной защитной группы осуществляют обработкой тетракис(трифенилфосфин)палладием(О).N,N-дизащищенный гидроксиламин 37 получают последовательным введением защитных групп Р и Р' в O-защищенный гидроксиламин формулы H2NOP2, где Р 2 представляет собой гидроксизащитную группу. Предпочтительная гидроксизащитная группа представляет собой алкил. Затем вводят аминозащитные группы Р и Р' с использованием реагентов и условий проведения реакций, которые хорошо известны в области органического синтеза. Так, например,реакция О-трет.-бутилгидроксиламина с аллилоксихлорформиатом приводит к образованиюN-аллилоксикарбонил-О-трет.-бутилгидроксиламина, который затем реагирует с бромистым бензилом с образованиемN-бензил-Nаллилоксикарбонил-О-трет.-бутилгидроксиламина. В результате обработки N-бензил-Nаллилоксикарбонил-О-трет.-бутилгидроксиламина трифторуксусной кислотой получают Nбензил-N-аллилоксикарбонилгидроксиламин. На схеме 10 показано получение полимерной смолы 4-(O-метилгидроксиламин)-2,3,5,6 тетрафторфеноксиметила. Согласно приведенной выше схеме 10 полимерная хлорметильная смола, такая как хлорметилполистирол (39, смола Merrifield) реагирует с 4-гидрокси-2,3,5,6-бензойной кислотой в присутствии основания с образованием 4 карбокси-2,3,5,6-тетрафторфеноксиметильной смолы 40. Восстановлением карбоксильной кислотной группы, например, с использованиемLiAlH4, гидрида диизобутилалюминия или ВН 3-ТГФ, получают 4-гидроксиметил-2,3,5,6 тетрафторфеноксиметильную смолу 41. В результате превращения 41 в соединение гидроксифталимидо смолы 42 с последующим удалением фталимидо группы, как показано выше на схеме 8, получают смолу 4-(O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметил-сополимера (стирол-1% дивинилбензол) 43. Получение полимерной смолы 4-(2',4'диметоксифенил-O-метилгидроксиламин)2,3,5,6-тетрафторфеноксиметила показано на схеме 11. Схема 11 Согласно приведенной выше схеме 11 полимерная хлорметильная смола реагирует с 4 фенокси-2,3,5,6-тетрафторфенил 2,4-диметоксифенил кетоном 44 в присутствии основания,как показано выше на схеме 10, с образованием соединения 4-(2',4'-диметоксифенилкарбонил)2,3,5,6-тетрафторфеноксиметильной смолы 45. Восстановление карбонильной группы с использованием, например, LiBH4 приводит к образованию 4-(гидроксиметил-2',4'-диметоксифенил)2,3,5,6-тетрафторфеноксиметильной смолы 46. Превращение 46 в гидроксифталимидо смолу 47 с последующим удалением фталимидогруппы,как показано выше на схеме 8, приводит к получению 4-(2',4'-диметоксифенил-O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметильной смолы 48. 32 Предпочтительны полимерные смолы гидроксиламина формулы 1, в которой L представляет собой связывающую группу. Предпочтительные связывающие группы L имеют формулу в которой А отсутствует или представляет собой группу -Х 1-Z-,где X1 представляет собой -CHR- или -CHR-YCO-(СН 2)n-; где R представляет собой Н, алкил,фенил или фенил, замещенный -Н, алкилом,алкокси, галогеном, нитрилом или -NO2,Y представляет собой -О- или -NH-,n представляет собой целое число от 1 до 6, аR1, R1a, R2 и R2a независимо представляют собой -Н, алкил, алкокси, галоген, нитрил илиR3 и R4 независимо друг от друга представляют собой -Н, алкил, фенил или фенил,замещенный одним или более заместителями,выбранными из алкила, алкокси, галогена, нитрила и -NO2; либо один из R1 и R2 вместе с одним из R3 4 и R и углеродными атомами, к которым они присоединены, образуют связывающую группу формулыR6, R7 и R8 независимо выбирают из -Н,алкила, алкокси галогена, нитрила или -NO2. Примеры предпочтительных полимерных смол гидроксиламина включают 4-(Oметилгидроксиламин)феноксиметил-сополимер Наиболее предпочтительные полимерные смолы гидроксиламина представляют собой 4-(O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметил-сополимер (стирол-1% дивинилбензольную) смолу,4-(2',4'-диметоксифенил-O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметил-сополимер (стирол-1% дивинилбензольную) смолу,4-(O-метилгидроксиламин)феноксиметилсополимер (стирол-1% дивинилбензольную) смолу, и 4-(2',4'-диметоксифенил-O-метилгидроксиламин)-феноксиметил-сополимер (стирол-1% дивинилбензольную) смолу. Способ Rink (H. Rink, Tet. Lett., 28, 37873790, 1987) обладает преимуществом, состоящим в том, что расщепление можно проводить в условиях мягкого ацидолиза в течение коротких периодов времени (например, 10% TFA в DCM,в течение 10-15 мин). Однако из-за стоимости смолы желательно синтезировать соответствующую функциональную смолу на твердом носителе Wang a) S.S. Wang, J. Am. Chem.Tam и R.B. Merrifield, J. Org. Chem., (1981), 46,3433). Особенно применим тетрафторфенилфенильный способ, поскольку сам по себе он приспособлен для количественного определения наполнения смолы и мониторинга реакций, протекающих на смоле, с использованием фтор ЯМР. Описанные способы применимы также для получения пептидных альдегидов, кетонов и гидроксамовых кислот. Как правило, такой способ включает взаимодействие карбоксильной группы, надлежащим образом N-защищенной первой аминокислоты со смолой с образованием полимерной смолы N-защищенной аминокислотной гидроксамовой кислоты. Затем аминокислотную N-защитную группу удаляют и смолу незащищенной полимерной аминокислотной гидроксамовой кислоты приводят во взаимодействие со второй, надлежащим образом Nзащищенной, аминокислотой. Такой процесс повторяют до тех пор, пока желательные аминокислотные остатки не внедрятся в пептид. Альтернативно пептиды, содержащие большое число аминокислот, получают взаимодействием надлежащим образом N-защищенных пептидных подъединиц, содержащих две или более аминокислот с образованием полимерной смолы N-защищенной пептидной гидроксамовой кислоты. Затем аминокислотную Nзащитную группу удаляют и смолу незащищенной полимерной пептидной гидроксамовой кислоты связывают со второй, надлежащим обра 35 зом N-защищенной, аминокислотой или пептидом. Таким образом, помимо описанного выше последовательного присоединения индивидуальных аминокислотных подъединиц, полипептид может быть получен связыванием пептидных подъединиц. После введения желаемых аминокислот в пептид, полимерная пептидная гидроксамовая кислота реагирует с металоорганическим реагентом, после чего проводят кислотный гидролиз с образованием пептидного кетона; который подвергается восстановительному расщеплению с образованием пептидного альдегида; или расщепляется кислотой с образованием пептидной гидроксамовой кислоты. Любые оставшиеся защитные группы могут быть удалены до или после отщепления пептида от смолы. Описанные N-защитные группы, подходящие для применения в пептидном синтезе,должны обладать свойствами, обеспечивающими устойчивость в условиях реакции присоединения к полимерной смоле гидроксиламина и способность легко удаляться без деструкции растущей пептидной цепочки или рацемизации какого-либо из содержащихся в ней хиральных центров. Подходящие защитные группы включают 9-фторенилметилоксикарбонил (Fmoc),трет.-бутилоксикарбонил (Воc), бензилоксикарбонил (Cbz), бифенилизопропилоксикарбонил,трет.-амилоксикарбонил, изоборнилоксикарбонил,(а,а)диметил-3,5-диметоксибензилоксикарбонил, о-нитрофенилсульфенил, 2-цианотрет.-бутилоксикарбонил и подобные. Кроме этого, такая смола может применяться для конструирования ранжированных рядов альдегидов, кетонов или аминов комбинаторных библиотек или ранжированных рядов альдегидов или кетонов в качестве реагентов в синтезе комбинаторных библиотек, например,реагентов для конденсации Ugi-4-компонента(Ivar Ugi, в Isonitrile Chemistry, 1971, стр. 145,Academic Press). Гидроксиламинсвязанная смола может применяться не только для трансформаций одной функциональной группы, но и для многостадийного твердофазного синтеза с целью создания комбинаторных библиотек. Функционализированная смола изобретения может также применяться для параллельного синтеза множества различных альдегидных,кетонных или аминных конечных продуктов,как это продемонстрировано для кетонов на схемах 12 а и 12b. На схемах 12 а и 12b, Rb и Rc имеют указанные выше значения, n представляет собой целое число, определяющее общее число различных альдегидных, кетонных или аминных продуктов, подлежащих получению.Ral-Ran независимо представляют собой алифатическую или ароматическую группы, имеющие указанные значения. На схеме 12 а изображен параллельный синтез множества кетонных соединений с использованием множества карбоновых кислот,RalCO2H-RanCO2H и единственного металоорганического соединения RcMgX. Согласно схеме 12 а смолу N-алкилированного гидроксиламина 8, полученную в соответствии со схемой 2, разделяют на n порций. Затем каждую порцию смолы соединяют с различной карбоновой кислотой с образованием n частей полимерной смолы N-алкилированной гидроксамовой кислоты. Затем каждая часть полимерной смолыN-алкилированной гидроксамовой кислоты реагирует с реагентом Гриньяра формулы RcX и подвергается кислотному гидролизу с получением n частей кетона, являющегося производным единственного металоорганического реагента. Схема 12b Параллельный синтез n различных кетонных соединений, производных единственной карбоновой кислоты RaCO2H и n различных металоорагнических соединений от RclMgBr доRcnMgBr представлен выше на схеме 12b. Согласно схеме 12b полимерную смолу N-алкилированного гидроксиламина соединяют с карбоновой кислотой формулы RaCO2H. Затем полученную полимерную смолу N-алкилированной гидроксамовой кислоты делят на n частей, и затем каждая часть полимерной смолыN-алкилированной гидроксамовой кислоты реагирует с различными реагентами Гриньяра Rcl 37RcnMgBr и подвергается кислотному гидролизу с получением n различных кетонов, производных единственной карбоновой кислоты. Функционализированные смолы настоящего изобретения могут также применяться для конструирования комбинаторной библиотеки кетонов или аминов, как это проиллюстрировано на схеме 13 для кетонной библиотеки, являющейся производной 4 карбоновых кислот и 4 реагентов Гриньяра. Схема 13 В соответствии с приведенной выше схемой 13 полимерную смолу N-алкилированного гидроксиламина 8 делят на 4 части, и каждую часть связывают с различной карбоновой кислотой для получения 4 различных полимерных смол N-алкилированной гидроксамовой кислоты. Затем 4 части полимерной смолы Nалкилированной гидроксамовой кислоты смешивают друг с другом с образованием одной части, которую далее делят на 4 части полимерной смолы N-алкилированной гидроксамовой кислоты, причем каждая часть содержит примерно равные количества каждой индивидуальной полимерной смолы N-алкилированной гид 002478 38 роксамовой кислоты. Каждая из 4 частей затем реагирует с различными реагентами ГриньяраRcl-Rc4MgBr и подвергается кислотному гидролизу с образованием 4 частей кетона, каждая из которых содержит 4 соединения, представляющие собой продукты реакции каждой из 4 различных полимерных смол N-алкилированной гидроксамовой кислоты с единственным реагентом Гриньяра. С помощью такого метода может быть быстро сконструирована комбинаторная библиотека, содержащая множество кетонов. Аналогичным способом может быть собрана комбинаторная библиотека пептидов, в результате повторения последовательности разделение-рекомбинация для каждого аминокислотного или пептидного строительного блока. Представленное выше описание будет понятнее с помощью следующих примеров, которые приведены для иллюстрации изобретения и не предназначены для ограничения объема изобретения. Пример 1. Получение смолы 4-(2',4'диметоксифенил-O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол). Смоле кислоты Rink (1 г, 0,63 ммоль) дают набухать в 10 мл диметилформамида (ДМФ) в течение 15 мин при комнатной температуре. К суспензии смолы добавляют 514 мг (3,15 ммоль)N-гидроксифталимида и затем 19 мг бензолсульфокислоты (0,13 ммоль). Смесь перемешивают с помощью механической мешалки и нагревают до 50 С в течение 5 ч. Затем смесь охлаждают до комнатной температуры и дополнительно перемешивают в течение 12 ч, после чего смолу отфильтровывают и тщательно промывают ДМФ (5 раз по 25 мл); смесью ДМФ: вода(70:30; 5 раз по 25 мл); ТГФ (10 раз по 25 мл) и диэтиловым эфиром (10 раз по 25 мл). Затем смолу сушат в течение ночи в глубоком вакууме при 40 С. В спектре ИК обнаружено поглощение карбонильной группы при 1773 см-1, которое соответствует области фталимидного карбонила. Элементный анализ: Вычислено 0,28%N. Найдено 0,26% N. Загрузка составляет 18 ммоль/г. Смоле позволяют набухать в 20 мл третбутанола в течение 10 мин. К смеси добавляют 10 мл гидразингидрата, и реакционную смесь нагревают до 60 С с механическим перемешиванием в течение 12 ч. После этого реакционную смесь охлаждают до комнатной температуры. Смолу отфильтровывают и тщательно промывают ДМФ (10 раз по 25 мл); ТГФ (10 раз по 25 мл) и диэтиловым эфиром (10 раз по 25 мл),затем смолу сушат в течение ночи в глубоком вакууме при 40 С. В спектре ИК смолы III от 39 сутствует поглощение в области карбонильной группы при 1733 см-1, которое имело место для исходного материала. Элементный анализ: % N найдено 0,43; 0,42% (соответствует уровню загрузки 0,3 ммоль/г). Пример 2. Получение смолы N-[3-4 метоксифенил)сульфонил)проп-1-илкарбонил]4-(2',4'-диметоксифенил-О-метилгидроксиламин)феноксиметил-сополимера(стирол-1% дивинилбензол) (200 мг) позволяют набухать в 3 мл ДМФ. К этой суспензии добавляют 610 мг (2,5 ммоль) 3-(4-метоксифенилсульфонил)пропионовой кислоты и 477 мг (2,5 ммоль) гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида (EDCI) при комнатной температуре. Реакционную смесь встряхивают при комнатной температуре, используя вихревой встряхиватель, в течение 12 ч, после чего смолу отфильтровывают и тщательно промывают смесью ДМФ:вода (80:20; 5 раз по 5 мл); ДМФ (5 раз по 5 мл); ТГФ (5 раз по 5 мл) и диэтиловым эфиром (5 раз по 5 мл). Затем смолу IV сушат в течение 12 ч в глубоком вакууме при 40 С. В спектре ИК обнаружено поглощение карбонильной группы при 1675 см-1, которое соответствует области связанного гидроксамата. Пример 3. Получение N-гидрокси-3-(4 метоксифенилсульфонил)-пропионамида. Сухой смоле(200 мг), полученной по методике примера 2,позволяют набухать в 3 мл хлористого метилена в течение 10 мин. В эту смесь при комнатной температуре по каплям добавляют 0,3 мл трифторуксусной кислоты (ТФУ), и образовавшуюся смесь встряхивают 30 мин. При добавлении ТФУ смола становится темно-синей. Затем смесь фильтруют и промывают двумя порциями по 5 мл хлористого метилена. Фильтрат выпаривают на роторном испарителе, получая 20 мг сырого продукта. Анализ сырой реакционной смеси микрометодом жидкостной хромато-массспектрометрии (ЖХ/МС) показал, что в ней содержится более 75% (по площади) целевого продукта,а 3-(4-метоксифенилсульфонил) пропионовая кислота составляет 6% (по площади). Спектр 1H-ЯМР (MeOH-d4)2,45 (т, 2 Н),3,45 (т, 2 Н), 3,90 (с, 3 Н), 7,15 (д, 2 Н), 7,85 (д,2 Н). В реактор с рубашкой (емкость 1 л), оборудованный снизу вентилем и сверху мешалкой( 8090 по каталогу фирмы Асе), загружают 18,35 г (20 мг-экв.) смолы Wang и 450 мл безводного ТГФ. Эту смесь осторожно перемешивают приблизительно 15 мин, затем удаляют максимально возможное количество растворителя путем вакуумного отсоса через трубку с пористой стеклянной пластиной. Добавляют новую порцию ТГФ, затем 15,74 г трифенилфосфина (60 ммоль) и 16,31 г (100 ммоль) Nгидроксифталимида. Полученную смесь перемешивают и охлаждают до (-5)-0 С. Медленно добавляют 11,8 мл (60 ммоль) диизопропилазодикарбоксилата, таким образом, чтобы поддерживать температуру ниже 5 С. По завершении добавления, при перемешивании смеси дают медленно нагреться до комнатной температуры,и ее перемешивают в течение ночи. С помощью указанной выше погружной трубки удаляют отсасыванием максимально возможное количество реакционной жидкости. Смолу промывают,добавляя N,N-диметилформамид (200 мл ДМФ),смесь перемешивают 3-5 мин и затем удаляют отсасыванием максимально возможное количество промывной жидкости. Аналогично смолу последовательно промывают дополнительным количеством ДМФ и порциями метанола (2 раза), ТГФ (2 раза) и метанола (1 раз). Часть смолы может быть обработана для анализа: ИКспектр 1734 см-1 (С=O). К оставшейся в реакторе смоле добавляют 400 мл ТГФ и 200 мл 40%-го водного раствора метиламина (2,31 моль). Эту реакционную смесь осторожно перемешивают при 40 С в течение 2 ч, затем охлаждают до комнатной температуры (смесь можно выдерживать при этой температуре в течение ночи). Удаляют отсасыванием максимально возможное количество реакционной жидкости и смолу промывают указанным выше набором растворителей. После окончательной промывки метанолом используют дополнительное количество метанола, чтобы смыть смолу со дна реактора и выделить ее фильтрацией. Отфильтрованную смолу сушат при 40 С в вакууме. Выход смолы составляет 18-18,5 г; содержание амина равно 1,02 мг-экв./г(по данным потенциометрического титрования п-толуолсульфокислотой суспензии смолы в ТГФ); ИК-спектр (микроскопия): 3316 см-1 (слаб. интенс. -NH2). Элементный анализ. Найдено: С-87,07%; Н-7,77%; N-1,58%, что соответствует 1,13 атомов азота на 1 г смолы. 41 Тест: получение 4-нитрофенилэтангидроксамовой кислоты. Образец сухой смолы (200 мг, приблизительно 0,2 ммоль) загружают в реактор для смолы объемом 5 или 10 мл (полипропиленовый шприц, снабженный полипропиленовой пористой пластиной). Смоле позволяют набухать в сухом ДМФ в течение около 15 мин и затем добавляют 115 мг гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида(EDCI,0,6 ммоль). Затем в эту смесь добавляют 115 мг (0,6 ммоль) 4-нитрофенилуксусной кислоты. Реактор закрывают крышкой и смесь медленно перемешивают в течение ночи (используют устройство с качающейся рамкой). Реакционную жидкость удаляют фильтрацией в вакууме (реактор со смолой подсоединяют с помощью небольшой резиновой муфты к вакуумной колбе) и смолу несколько раз промывают порциями (по 2-3 мл) следующих растворителей: ДМФ (4-5 раз), метанол или 50% водный ДМФ (3-4 раза),ТГФ (3-4 раза) и метанол (2-3 раза). Смолу (еще находящуюся в шприцевом реакторе) сушат при 40 С не менее 4 ч. К высушенной смоле добавляют 2 мл дихлорметана и затем 2 мл трифторуксусной кислоты (ТФУ). Кроме того, добавляют 20 мл воды (считается, что это позволит уменьшить образование "ангидрида" из продукта гидроксамовой кислоты). Смеси дают прореагировать примерно в течение 1 ч, и реакционную жидкость декантируют в калиброванный сборник. Смолу промывают 1-2 раза порцией 1 мл дихлорметана и затем 1-2 раза порцией 1 мл толуола. Объединенные фильтраты концентрируют до объема около 2 мл при 30 С, добавляют еще 2 мл толуола и полученный раствор концентрируют досуха в вакууме (в роторном испарителе и затем в вакуумном шкафу при 30 С отмечено,что нагревание в присутствии ТФУ способствует образованию "ангидридной" примеси). Остаток взвешивают и анализируют, чтобы определить его чистоту (в вес.%), используя ВЭЖХ с внутренним стандартом ответа карбоновой кислотой. Типичные результаты для 4-нитpoфeнилэтaнгидpoкcaмoвoй кислоты: 29-30 мг твердого вещества чистотой 60-70 вес.%, чистотой 90-97 А% (261 нм). Спектр 1H-ЯМР (CD3OD) 2 8,13 (д, 2 Н),7,25 (д, 2 Н), 4,85 (шир. с, ОН, NH), 3,55 (с, 2 Н). Спектр 13 С-ЯМР 169,4; 144,3; 131,3; 124,6; 40,2. Это соответствует химическому выходу (на зафиксированную загрузку) 50-55% для смолы емкостью 1 мг-экв./г. Пример 5. Получение смолы N-4 фенилбут-1-оил-4-(O-метилгидроксиламин) феноксиметил-сополимера (стирол-1% дивинилбензол). 42 Сухой смоле 4-(О-метилгидроксиламин) феноксиметил-сополимера (стирол-1% дивинилбензол) (2 г, 1,5 ммоль), полученной по методике примера 4, дают набухнуть в 8 мл ДМФ в течение 10 мин и затем обрабатывают 4 фенилмасляной кислотой и EDC (0,86 г, 4,5 ммоль). Смесь встряхивают в течение 24 ч и фильтруют. Смолу промывают ДМФ, смесью ДМФ/вода, ДМФ, ТГФ и диэтиловым эфиром и сушат при 40 С в вакууме, получая 2,2 г смолы Сухой смоле 4-(O-метилгидроксиламин) феноксиметил-сополимера (стирол-1% дивинилбензол) (4 г, 3 ммоль), полученной по методике примера 4, дают набухать в 32 мл ДМФ в течение 10 мин и затем обрабатывают 4-бром-3 метилбензойной кислотой и EDC (1,725 т, 9 ммоль). Смесь встряхивают в течение 24 ч и фильтруют. Смолу промывают ДМФ, смесью ДМФ/вода, ДМФ, ТГФ и диэтиловым эфиром и сушат при 40 С в вакууме, получая 4,5 г смолыN-1,05%, Найдено Br-5,3%; N-0,91%. Пример 7. Получение N-гидрокси-4-бром 3-метилбензамида. Смолу N-(4-бром-3-метилбензоил)-4-(Oметилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол), полученную по методике примера 6, суспендируют в смеси 50% ТФУ/хлористый метилен в течение 2 ч. Смолу отфильтровывают и промывают три раза хлористым метиленом, получая N-гидрокси-4-бром-3 метилбензамид. Анализ ЖХ/МС: m/z 230/232(стирол-1% дивинилбензол) (1,46 г, 1,095 ммоль), полученную по методике примера 5,суспендируют в 26 мл толуола в течение 10 мин. Добавляют 0,83 мл DBU (5,5 ммоль) и смесь перемешивают в течение 2 ч на шатунном встряхивателе. Добавляют 4,1 г (16,425 ммоль) бромбензилбромида и реакционную смесь интенсивно перемешивают в течение 4 суток. Смолу фильтруют и промывают ДМФ, смесью ДМФ/вода, ДМФ, ТГФ и диэтиловым эфиром и сушат при 40 С в вакууме, получая 1,4 г смолыN-0,94%, Найдено Br-5,4%; N-0,85%. Пример 9. Получение 4-фенилбутиральдегида. Смолу N-(4-бромбензил-N-4-фенилбут-1 оил-4-O-метилгидроксиламин)феноксиметилсополимера (стирол-1% дивинилбензол) (0,2 г,0,6 ммоль/г, 0,12 ммоль) суспендируют в диэтиловом эфире в течение 10 мин и затем охлаждают до 5 С в орбитальном встряхивателе. Суспензию обрабатывают 0,22 мл 0,46-молярного раствора LiAlH3OMe (0,1 ммоль) в диэтиловом эфире и перемешивают в течение 30 мин при этой температуре. Реакционную смесь гасят добавлением 2-молярной водной соляной кислоты и встряхивают в течение 30 мин. Добавляют тартрат натрия-калия и смесь встряхивают еще в течение 10 мин. Добавляют сульфат натрия и смесь фильтруют через слой силикагеля,который тщательно промывают дихлорметаном. Фильтрат концентрируют, получая 4-фенилбутиральдегид. Площадь пика равна 91% (ГХ). Спектр 1 Н-ЯМР (СDСl3)9,75 (с, 1 Н),7,05-7,30 (м, 5 Н), 2,58-2,68 (м, 2 Н), 2,41-2,50 (т,2 Н), 1,91-2,02 (м, 2 Н). МС (ЭИ): m/z=149[М+Н+]. Пример 10. Получение 6-фенилгексан-3 она. Смолу N-(4-бромбензил-N-4-фенилбут-1 оил-4-O-метилгидроксиламин)феноксиметилсополимера (стирол-1% дивинилбензол) (0,15 г,приблизительно 0,75 ммоль/г, 0,11 ммоль) суспендируют в диэтиловом эфире (1 мл) и обрабатывают 0,34 мл 1-молярного раствора этилмагнийбромида (0,1 ммоль) в ТГФ. Реакционную смесь перемешивают в течение 18 ч и затем гасят добавлением 2-молярной соляной кислоты(получают значение рН около 3). Смесь перемешивают в течение 30 мин. Добавляют сульфат натрия и смесь фильтруют через слой силикагеля, который тщательно промывают дихлорметаном. Фильтрат концентрируют, получая 6 фенилгексан-3-он. ГХ/МС (ЭИ): m/z 176,2 (М)+; площадь равна 97,1%. МС (ЭИ-LRP): m/z 176 Смолу N-(4-бром-3-метилбензоил)-4-(Oметилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол) (2,8 г, 2,1 ммоль), полученную по методике примера 6,суспендируют в 27 мл толуола и смесь перемешивают в течение 10 мин. Добавляют 1,6 г DBU(31,5 ммоль) хлорбензилбромида и реакционную смесь интенсивно перемешивают в течение 3 суток. Смолу фильтруют и промывают ДМФ,смесью ДМФ/вода, ДМФ, ТГФ и диэтиловым эфиром и сушат при 40 С в вакууме, получая 3 г смолы N-4-хлорбензил-N-(4-бром-3-метилбензоил)-4-(O-метилгидроксиламин)феноксиметилсополимера (стирол-1% дивинилбензол). Спектр ИК: С=О 1644 см-1. Элементный анализ: Вычислено Вr-4,2%; Сl-1,9%; N-0,8%, Найдено Br3,8%; Cl-2,0%; N-0,9%. Пример 12. Получение N-(4-хлорбензил)N-гидрокси-3-метил-4-бромбензамида. СмолуN-4-хлорбензил-N-(4-бром-3 метилбензоил)-4-(O-метилгидроксиламин) феноксиметил-сополимера (стирол-1% дивинилбензол), полученную по методике примера 11, суспендируют в смеси 50% ТФУ/ дихлорметан в течение 2 ч. Смолу отфильтровывают и промывают три раза дихлорметаном,получая N-(4-хлорбензил)-N-гидрокси-3-метил 4-бромбензамид. Анализ ЖХ/МС (H-ISP) m/z 354/356 (Cl/Br) [M+H]+; площадь равна 64%. Спектр 1 Н-ЯМР (300 МГц, CDCl3)2,3 (шир. с,3 Н), 4,65 (шир. с, 2 Н), 7,2-7,6 (м, 7 Н). Пример 13. Получение 4-бром-3-метилбензальдегида. Смолу N-4-хлорбензил-N-(4-бром-3-метилбензоил)-4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол)(0,2 г, 0,5 ммоль/г, 0,1 ммоль), полученную по методике примера 11, суспендируют в диэтиловом эфире в течение 10 мин и затем охлаждают до 5 С в орбитальном встряхивателе. Суспензию обрабатывают 0,2 мл 0,46-молярного раствора LiАlH3 ОМе (0,092 ммоль) в диэтиловом эфире и перемешивают 30 мин при этой температуре. Реакционную смесь закаливают добавлением 2-молярной соляной кислоты и встряхивают 30 мин. Добавляют тартрат натрия-калия,и смесь встряхивают в течение еще 10 мин. Добавляют сульфат натрия и смесь фильтруют через слой силикагеля, который тщательно про 45 мывают дихлорметаном. Фильтрат концентрируют, получая 4-бром-3-метилбензальдегид. ГХМС (ЭИ): m/z=179/199 Br[M]+. Площадь пика равна 99,5%. Спектр 1H ЯМР (CDCl3)9,94 (с,1 Н), 7,70 (д, 2 Н), 7,52 (д, 1 Н), 2,45 (с, 3 Н). МС(0,23 г, 0,5 ммоль/г, 0,115 ммоль), полученную по методике примера 11, суспендируют в диэтиловом эфире (1 мл) и обрабатывают 0,23 мл 1-молярного раствора этилмагнийбромида (0,23 ммоль) в ТГФ. Реакционную смесь перемешивают в течение 18 ч и затем гасят добавлением 2-молярной водной соляной кислоты (получают значение рН около 3). Смесь перемешивают в течение 30 мин. Добавляют сульфат натрия и смесь фильтруют через слой силикагеля, который тщательно промывают дихлорметаном. Остаток концентрируют, получая 1-(4-бром-3 метилфенил)-пропан-1-он. ГХ: площадь пика равна 78,7%. МС (ЭИ): m/z 226 Вr[M+-Н]; Спектр ЯМР (300 МГц, CDCl3)1,22 (т, J=7,89,3 Н), 2,96 (квадр., J=7,89, 2 Н), 7,6 (шир. с, 2 Н),7,8 (с, 1 Н). Пример 15. Получение смолы N-3 бромбензальдегидоксим-4-(О-метилгидроксиламин)феноксиметил-сополимера(5 мл 4), ТГФ (5 мл 10) и диэтиловым эфиром (5 мл 10). Смолу сушат в вакууме при 40 С в течение 12 ч. ИК пик оксима 1602 см-1. Элементный анализ: Рассчитано Вr-5,52%; N1,04%. Найдено: Br-5,76%; N-1,08%. Пример 16. Получение смолы N-3-(4 метоксифенил)пропан-1-оил-4-(О-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол).N-гидрокси-3-(4-метоксифенил)пропионамид получают взаимодействием смолы N-3-(4 метоксифенил)пропан-1-оил-4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол) с трифторуксусной кислотой(ТФУ) по методике примера 7. 1 Указанную в заголовке смолу получают по методике примера 16,заменяя 3-(4 метоксифенил)пропионовую кислоту на 4 бромфенилуксусную кислоту. ИК: С=O 1713,9 см-1. Элементный анализ: Рассчитано: Br-5,8%;EDS: Общий счет импульсов рентгеновского излучения Указанную в заголовке смолу получают по методике примера 16,заменяя 3-(4 метоксифенил)пропионовую кислоту на 4 бромкоричную кислоту. ИК: С=O 1671,7 см-1EDS: Общий счет импульсов рентгеновского излученияN-гидрокси-4-бромамид коричной кислоты получают обработкой смолы N-4-бромциннамоил-4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол) ТФУ по методике примера 7. ЖХ-МС(Нионизация) m/z 241/243 Вr [М+]. Площадь = 84%. 1 Указанную в заголовке смолу получают по методике примера 16,заменяя 3-(4 метоксифенил)пропионовую кислоту на 4-хлорбензойную кислоту. ИК: С=O 1678 см-1. Элементный анализ: Рассчитано: Сl-2,66%; N1,05%. Найдено: Сl-2,39%; N-1,02%. Пример 22. Получение N-гидрокси-4 хлорбензамида.N-гидрокси-4-хлорбензамид получают обработкой смолы N-(4-хлорбензоил)-4-(O-метилгидроксиламин)феноксиметил-сополимера(стирол-1% дивинилбензол) ТФУ по методике примера 7. ЖХ-МС (Н-ионизация) : m/z 172, 174 Смолу N-(4-хлорбензоил)-4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол 1% дивинилбензол) (0,1 г, 0,075 ммоль, 0,75 ммоль/г) суспендируют в толуоле (2 мл) и охлаждают до 5 С. Смесь обрабатывают метилйодидом (1,5 ммоль, 0,21 г, 93 мкл), затем DBU(0,22 мл, 0,228 г, 1,5 ммоль). Реакционную смесь помещают в смеситель и выдерживают при комнатной температуре. Через несколько минут образуется обильный белый осадок, и смесь далее разбавляют толуолом (2 мл). Перемешивание реакционной смеси продолжается в течение 18 ч. Смолу N-метил-N-(4-хлорбензоил)-4-(O-метилгидроксиламин)феноксиметилсополимера (стирол-1% дивинилбензол) фильтруют и промывают ДМФ, смесью ДМФ/Н 2 О,ДМФ, ТГФ, диэтиловым эфиром и сушат в вакууме при 40 С. 48 Пример 24. Получение 1-(4-хлорфенил)пропан-1-она. Смолу N-метил-N-(4-хлорбензоил)-4-(Oметилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол) суспендируют в диэтиловом эфире (0,7 мл) и обрабатывают этилмагнийбромидом (1,0 М в ТГФ, 0,225 мл,0,225 ммоль). Реакционную смесь перемешивают в течение 18 ч на шатунном встряхивателе и затем нейтрализуют добавкой 5% НСl в этаноле. Далее перемешивание поддерживают в течение 30 мин и затем смесь фильтруют через небольшой слой силикагеля, чтобы удалить неорганическое вещество. Фильтрат концентрируют, выделяя 1-(4-хлорфенил)пропан-1-он. МС (EILRP) m/z 168/170 Cl [M+], 169/171 Cl [M+H]+; 1(стирол-1% дивинилбензол) получают по методике примера 16, заменяя 3-(4-метоксифенил)пропионовую кислоту на 3-(4-метоксифенилсульфонил) пропионовую кислоту. ИК: С=О 1671,7 см-1N-гидрокси-3-(4-метоксифенилсульфонил) пропионамид получают обработкой смолы N-[34-метоксифенил)сульфонил)пропан-1-оилкарбонил]-4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол) ТФУ по методике примера 7. 1 Смолу 4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол) (2 г, 2 ммоль) суспендируют в 15 мл дихлорметана и встряхивают на шатунном встряхивателе в течение 10 мин и добавляют 284 мг(стирол-1% дивинилбензол), полученную по методу примера 27, суспендируют в 15 мл толуола. Добавляют DBU (1,522 г, 1,5 мл, 10 ммоль) и 4-бромбензилбромид (2,5 г, 10 ммоль),и встряхивают смесь в течение 70 ч. Смолу N-4 бромбензил-N-аллилоксикарбонил-4-(O-метилгидроксиламин)феноксиметил-сополимера Смола N-4-бромбензил-N-аллилоксикарбонил-4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол),полученная по методике примера 28, набухает в 6 мл ТГФ, 6 мл ДМСО, 3 мл 0,5 н. НСl. Добавляют Рd(Рh3 Р)4 (347 мг, 15 маc.%) и смесь встряхивают 5 мин. Добавляют морфолин (4,3 мл) и встряхивают смесь в течение ночи. Реагенты отфильтровывают и смолу N-4 бромбензил-4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол) промывают ДМФ (2 раза), 2 раза ТГФ, 2 раза дихлорметаном, 3 раза 0,5%-ным раствором диизопропилэтиламина в дихлорметане,0,5%-ным диэтилдитиокарбаматом натрия в ДМФ (3 раза), ДМФ (3 раза), ТГФ (3 раза) и дихлорметаном (3 раза) и сушат в вакууме в течение ночи. Пример 30. Получение смолы N-(индол-2 илкарбонил)-N-4-бромбензил-4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол 1% дивинилбензол). 50 1% дивинилбензол) (1,17 г, 1 ммоль), полученную по методике примера 29, суспендируют в 15 мл ДМФ. Добавляют индол-2-карбоксильную кислоту (483 мг, 3 ммоль) и 575,1 мг (3 ммоль) 1-(3-диметиламинопропил)-3-диэтилкарбодиимид гидрохлорида и смесь встряхивают в течение 16 ч. Смолу N-(индол-2-илкарбонил)-N-4 бромбензил-4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол) фильтруют и промывают 15 мл ДМФ (3 раза), ТГФ/20% Н 2 О (3 раза), ТГФ (3 раза) и дихлорметаном (3 раза) и сушат в вакууме. Пример 31. Получение индол-2-карбоксальдегида. Сухой смоле N-(индол-2-илкарбонил)-N-4 бромбензил-4-(O-метилгидроксиламин)феноксиметил-сополимера (стирол-1% дивинилбензол) позволяют набухать в 12 мл ТГФ, смесь встряхивают и охлаждают при 0 С в течение 30 мин. Добавляют LiAlH4 (0,62 мл, 3 эквивалента) и встряхивают смесь при 0 С в течение 30 мин. Добавляют насыщенный раствор KHSO4 (0,5 мл) и 0,3 мл раствора виннокислого калия, натрия, и смесь встряхивают в течение 30 мин до тех пор, пока она не нагреется до комнатной температуры. Избыток воды удаляют добавкой сухого Na2SO4 и встряхиванием в течение более 15 мин. Смесь фильтруют под небольшим давлением азота и промывают более 3 раз 8 мл дихлорметана с последующей фильтрацией. Фильтрат сушат Na2SO4 и пропускают дважды через тонкий слой (2,54 см) силикагеля 60 (для хроматографии в колонке, размер частиц 0,0400,063 мм), и растворитель удаляют в вакууме,получая индол-2-карбоксальдегид. 1 Н-ЯМР (CDCl3)9,84 (1H, с), 9,22 (1 Н,шир. с), 7,75 (1 Н, д), 7,14-7,48 (4 Н, м); МС (ЭИ):m/z=146 [М+Н+]. Пример 32. Получение альдегида N-(третбутоксикарбонил)фенилаланина. Указанное в заголовке вещество получают по методике примеров 30 и 31, заменяя индол-2 карбоксальдегид на N-(трет-бутоксикарбонил) фенилаланин. Пример 33. Получение смолы N-(3,4 диметоксициннамил)-4-(О-метилгидроксиламин)феноксиметил-сополимера(0,5 мл, 2 эквивалента) и встряхивают смесь при 0 С в течение 30 мин. Добавляют насыщенный раствор KHSO4 (0,5 мл) и 0,3 мл раствора виннокислого калия, натрия и смесь встряхивают в течение 30 мин до тех пор, пока она не нагреется до комнатной температуры. Избыток Н 2O удаляют добавлением сухого Nа 2SO4 и встряхиванием в течение более 15 мин. Смесь фильтруют под небольшим давлением азота и промывают 3 раза 8 мл дихлорметана и фильтруют. Фильтрат сушат Na2SO4 и пропускают через тонкий слой (2,54 см) силикагеля 60 для хроматографии на колонке (размер частиц 0,040-0,063 мм), и растворитель удаляют в вакууме, получая 3,4-диметоксициннамальдегида. 1H-ЯМP (CDCl3)9,65 (1H, д), 7,40 (1H, д),7,12 (1H, д), 7,06 (1H, с), 6,87 (1H, д), 6,60 (1H,дд), 3,90 (6 Н, с); МС (ЭИ): m/z = 193 [М+Н+]. Примеры 36-43. Соединения примеров 3643 получают из исходных веществ для целевых карбоксильных кислот, используя методики примеров 33-35. Пример 36. Получение антранилового альдегида. 1(20 мл). Добавляют гидрат 2,3,5,6-тетрафтор-4 гидроксибензойной кислоты (2,28 г, 10 ммоль) и карбонат цезия (3,26 г, 10 ммоль) и нагревают реакционную смесь при 85 С в течение 12 ч легким перемешиванием. Реакционную смесь фильтруют и промывают смолу 4-карбокси 2,3,5,6-тетрафторфеноксиметил-сополимера(стирол-1% дивинилбензол) ДМФ (5 раз), 20% водным раствором ДМФ (5 раз), ТГФ (5 раз) и дихлорметаном и сушат в вакууме в течение ночи. ИК (микроскоп, см-1): 1640 (С=O); 19FЯМР (нанопроба) -144,4 (ч/млн),-160,2 (ч/млн).EDS (дифракция электронов со сканированием). Измерения рассеивания энергии рентгеновского излучения проводят на сканирующем электронном микроскопе Electroscan, снабженным PGT цифровым детектором. Слои наносят на алюминиевые подложки и испытывают без 53 проводящего покрытия. Общий счет импульсов рентгеновского излучения приведен после коррекции на подложку. Никаких поправок для атомных номеров, флуоресценции и абсорбции не делается. ФОРМУЛА ИЗОБРЕТЕНИЯb) взаимодействие полимерной смолы Nалкилированной или N-арилированной гидроксамовой кислоты формулы 1. Способ получения кетона формулыRc и Ra независимо представляют собой алифатическую или ароматическую группу,включающийa) i) сочетание карбоновой кислоты формулы RaCOOH с полимерной смолой гидроксиламина формулы с образованием полимерной смолы гидроксамовой кислоты формулы и с последующим взаимодействием полимерной смолы гидроксамовой кислоты с алкилирующим или арилирующим агентом формулы RbLG,где LG является уходящей группой,с образованием полимерной смолы Nалкилированной или N-арилированной гидроксамовой кислоты общей формулыii) взаимодействие полимерной смолы Nзащищенного гидроксиламина формулы в которой представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу с металлоорганическим реагентом формулы RcM,в которой Rc представляет собой алифатический или арильный анион и М является катионом металла; и с) выделение кетона из смолы. 2. Способ получения альдегида формулыRaCHO, в которой Ra представляет собой алифатическую или арильную группу, включающий а) взаимодействие полимерной смолы Nалкилированной гидроксамовой кислоты формулы в которой представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу,с гидридным восстанавливающим агентом; иb) выделение альдегида из смолы. 3. Способ получения полимерной смолы в которой Р является аминозащитной группой с алкилирующим или арилирующим реагентом формулы RbLG, где LG является уходящей группой,с образованием полимерной смолы Nзащищенного, N-алкилированного или Nарилированного гидроксиламина формулы в которой представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу,включающий а) сочетание карбоновой кислоты формулыRaCOOH с полимерной смолой гидроксиламина формулы с последующим удалением аминозащитной группы с образованием полимерной смолы Nалкилированного или N-арилированного гидроксиламина формулы с образованием полимерной смолы гидроксамовой кислоты формулыNалкилированного или N-арилированного гидроксиламина с соединением карбоновой кислоты формулы RaCOOH с образованием полимерной смолы N-алкилированной или N-арилированной гидроксамовой кислоты формулыb) взаимодействие полимерной смолы гидроксамовой кислоты с алкилирующим агентом формулы RbLG, в которой LG является уходящей группой. 4. Способ по п.3, где полимерной смолой гидроксиламина является(стирол-1% дивинилбензол),смола 5-(4-O-метилгидроксиламин-3,5 диметоксифенокси)валериановая кислотасополимер (стирол-1% дивинилбензол),смола 4-(O-метилгидроксиламин)-2,3,5,6 тетрафторфеноксиметил-сополимер (стирол-1% дивинилбензол),смола 4-(2',4'-диметоксифенил-O-метилгидроксиламин)-2,3,5,6-тетрафторфеноксиметил-сополимер (стирол-1% дивинилбензол),смола 4-O-метилгидроксиламин-3-метоксифенокси-сополимер (стирол-1% дивинилбензол) или смола 3-гидроксиксантгидроламин-сополимер (стирол-1% дивинилбензол). 5. Способ получения полимерной смолы в которой представляет собой твердый носитель, L отсутствует или является связывающей группой, a Ra и Rb независимо представляют собой алифатическую или арильную группу,включающий а) взаимодействие полимерной смолы Nзащищенного гидроксиламина формулы в которой Р является аминозащитной группой, с алкилирующим агентом формулы RbLG, в которой LG является уходящей группой,с образованием полимерной смолы Nзащищенного, N-алкилированного гидроксиламина формулыb) удаление аминозащитной группы с образованием полимерной смолы N-алкилированного гидроксиламина формулы 56 с) сочетание полимерной смолы Nалкилированного гидроксиламина с соединением карбоновой кислоты формулы RaCOOH. 6. Способ по п.5, где Р является аллилоксикарбонилом,бензилоксикарбонилом,пметоксибензилоксикарбонилом, п-нитробензилоксикарбонилом, триметилсилилэтоксикарбонилом, 2,4-диметоксибензилоксикарбонилом, онитробензилоксикарбонилом,о-нитробензoлсульфонилом, п-нитробензoлсульфонилом и 2 нитро-4-трифторметилбензолсульфонилом. 7. Полимерная смола N-защищенного гидроксиламина формулы в которой представляет собой твердый носитель, L отсутствует или является связывающей группой, и Р является аминозащитной группой, при условии, что Р отличается от 4 метоксибензила или 2,4-диметоксибензила. 8. Полимерная смола N-защищенного гидроксиламина по п.7, в котором L является связывающей группой. 9. Полимерная смола N-защищенного гидроксиламина по п.8, в котором L является связывающей группой формулы в которой А отсутствует или представляет собой группу формулы -X1-Z-, в которой Х 1 представляет собой -CHR- или -CHR-YCO-(CH2)n-, в которой R является атомом водорода, алкилом, фенилом, замещенным -Н, алкилом, алкокси, атомом галогена, нитрилом или-NO2,Y представляет собой -О- или -NH-,n является целым числом от 1 до 6, иR1, R1a, R2 и R2a независимо представляют собой атом водорода, алкил, алкокси, атом галогена, нитрил или -NO2; иR3 и R4 независимо представляют собой атом водорода, алкил, фенил или фенил, замещенный одним или несколькими заместителями, выбранными из алкила, алкокси, атома галогена, нитрила и -NO2; или один из R1 и R2, взятый вместе с одним 3 из R и R4 и атомами углерода, с которыми они связаны, образуют связывающую группу формулыR1 представляет собой атом водорода, алкил, алкокси, атом галогена, нитрил или -NO2; иR6, R7 и R8 независимо выбирают из атома водорода, алкила, алкокси, атома галогена, нитрила или -NO2. 10. Полимерная смола N-защищенного гидроксиламина по п.9, в котором Р является аллилоксикарбонилом, бензилоксикарбонилом,п-метоксибензилоксикарбонилом, п-нитробензилоксикарбонилом, триметилсилилэтоксикарбонилом, 2,4-диметоксибензилоксикарбонилом,о-нитробензилоксикарбонилом, о-нитробензолсульфонилом, п-нитробензолсульфонилом и 2 нитро-4-трифторметилбензолсульфонилом. 11. Полимерная смола N-защищенного гидроксиламина по п.10, которая представляет собой смолу N-аллилоксикарбонил-4-(O-метилгидроксиламин)феноксиметил-сополимер (стирол-1% дивинилбензол),смолу(стирол-1% дивинилбензол),смолу N-аллилоксикарбонил-3-гидроксиксантгидроламин-сополимер (стирол-1% дивинилбензол). 12. Способ получения гидроксамовой кислоты формулы 58 А 2 представляет собой простую связь, или алкиленовую группу, или NR13, в которой R13 является атомом водорода или алкилом;R9 является группой формулы -L1-R14, где 1L представляет собой простую связь или линейную или разветвленную C1-C6-aлкиленовую группу, необязательно замещенную алкокси,арилом, карбокси, циано, циклоалкилом, атомом галогена, гетероарилом, гидроксилом или оксo,и R14 является атомом водорода, арилом, карбокси, циано, циклоалкилом, циклоалкенилом,циклокарбамоилом, циклоимидилом, гетероциклоалкилом, гетероарилом, группой -NHC(=O)-NH2, (N-карбамоил)циклическим амином, -C=N-O-C(=O)-NH2, -C(=O)-NY1Y2, [где Y1 и Y2 независимо представляют собой атом водорода, алкил, арилалкил и арил, или заместитель Y1Y2N- образует 4-6-членный циклический амин, который необязательно содержит дополнительный гетероатом, выбранный из кислорода, серы, группы NH или NR13], -NY1SO2 арилом, группой -NHR13, -SR13 или -OR13; или группой -L2-R15, где L2 представляет собой линейную или разветвленную углеродную цепочку, содержащую от 2 до 6 атомов углерода, необязательно замещенную карбокси- или цианогруппой, которая содержит двойную или тройную углерод-углеродную связь, или прерывается атомом кислорода или серы, фениленовой группой, имино(-NН-) или алкилимино группой,или сульфинильной, или сульфонильной группой, и R15 является атомом водорода, арилом,карбокси, циано, циклоалкилом, циклоалкенилом, гетероциклоалкилом или гетероарилом; или R9 или R10, взятые вместе с атомом, с которым они связаны, образуют цикл; или R9 и R11,взятые вместе с атомом, через который они связаны, образуют цикл;R10 и R12 независимо представляют собой атом водорода или алкил; илиR11 представляет собой группу формулы 3 16-L -R , где L3 представляет собой простую связь или линейную или разветвленную C1-С 6 алкиленовую группу, необязательно замещенную алкокси, арилом, карбокси, циано, циклоалкилом, атомом галогена, гетероарилом, гидроксилом или оксо; или L3 представляет собой линейную или разветвленную углеродную цепочку, содержащую от 2 до 6 атомов углерода,которая содержит двойную или тройную углерод-углеродную связь или прерывается атомом кислорода или серы, фениленовой группой,имином(-NН-) или алкилимином, или сульфинильной, или сульфонильной группой; и R16 является атомом водорода, арилом, циклоалкилом, циклоалкенилом, циклокарбамоилом, циклоимидилом, гетероциклоалкилом, гетероарилом, группой -NH-C(=O)-NH2, (N-карбамоил) циклическим амином,-C=N-O-C(=O)-NH2,-С(=O)-NY1Y2 [где Y1 и Y2 независимо представляют собой атом водорода, алкил, арилал 59 кил и арил, или заместитель Y1Y2N- образует 46-членный циклический амин, который необязательно содержит дополнительный гетероатом,выбранный из кислорода, серы, группы NH или где R17 представляет собой линейную или разветвленную алкильную группу, содержащую от 1 до 6 атомов углерода и необязательно замещенную одним или несколькими атомами галогена, или, когда Z3 является простой связью, R17 также может представлять собой атом водорода,алкенильную или алкинильную группу;R18 представляет собой необязательно замещенный циклоалкил, циклоалкенил, гетероциклоалкил, арил, частично насыщенную бициклоарильную или гетероарильную группу;R21, которые могут быть одинаковыми или различными, каждый представляет собой атом водорода или алкил, алкенил, гетероциклоалкил,циклоалкил, циклоалкенил, арил, гетероарил,арилалкильную или гетероарилалкильную группу, или группа NR20R21 представляет собой 5-7 членный циклический амин, который необязательно содержит один или несколько дополнительных гетероатомов, выбранных из кислорода, азота или серы, в которой, когда R18 является замещенной циклоалкильной группой, циклоалкильная группа замещена одним или несколькими (например, 1, 2 или 3) заместителями, выбранными из OR23, SR24, SOR24, SO2R24, NH2,NR13R24,=NOR24,=NOH,=NNHR24,24 24 24=NOCONHR , =NCO2R , NHCOR , NHSO2R24,SO2NR13R24, R23, CONHR24, CONHCH2CO2R13,CONR24R13 или N3; где R23 представляет собой атом водорода, алкил, циклоалкил, арил, арилалкил, гетероарил или гетероарилалкил; R24 является алкилом, циклоалкилом, циклоалкенилом, гетероциклоалкилом, арилом, гетероарилом, арилалкилом или гетероарилалкилом; или заместитель NR13R24 образует 4-7-членный циклический амин, который необязательно содержит дополнительный гетероатом, выбранный из кислорода, серы, группы NH или NR13, и в котором R18 является замещенной гетероциклоалкильной группой, содержащей атом азота, причем кольцо замещено по одному или нескольким (например, 1, 2 или 3) атомам углерода, и заместители выбирают из оксо-, циано-, CO2R13,CONHCH2CO2R13, арила, арилалкила или гидро 002478 60 ксиалкила, и/или замещено по атому азота в кольце, причем заместитель выбирают из R13,(CH2)nCO2H, (СН 2)nСО 2R24, (СН 2)nCONR13R24,(СН 2)nCOR24, CONH2, CONHR24, COR24, SO2R24 или OR24; А 3 представляет собой простую связь или линейную или разветвленнуюC1-С 6 алкиленовую группу, необязательно замещенную атомом галогена, гидроксилом, алкокси,оксо, циклоалкилом, арилом или гетероарилом; или А 3 представляет собой линейную или разветвленную углеродную цепочку, содержащую от 2 до 6 атомов углерода, которая содержит двойную или тройную углерод-углеродную связь, или прерывается атомом кислорода или серы, фениленовой группой, имином(-NН-) или алкилимином, или сульфинильной или сульфонильной группой;Z1 и Z3 каждый представляет собой атом кислорода или серы, простую связь или группуZ2 представляет собой атом кислорода или серы, или простую связь; В, С, D и Е независимо представляют собой атом углерода или гетероатом, выбранный из кислорода, серы, азота, группы NOR22 илиNR22, в которой R22 является атомом водорода или C1-С 4-алкилом с линейной или разветвленной цепочкой, арилом, арил-С 1-С 4-алкилом, гетероарилом или гетероарил-С 1-С 4-алкилом, или три из В,С, D или Е представляют собой атом углерода или гетероатом, выбранный из кислорода, азота, группы NR22 или серы, а другой представляет собой простую связь; но исключая соединения, в которых два атома кислорода или серы находятся в соседних положениях, причем связи, соединяющие В, С, D и Е могут быть простыми или двойными;Q1, Q2 и Q3, которые могут быть одинаковыми или различными, каждый представляет собой группу СН или СХ 1 или атом азота; иX1 представляет собой атом галогена; иn равно 0, 1 или 2; или ее N-оксида, пролекарственной формы, кислотной изостеры, фармацевтически приемлемой соли или сольвата, включающий а) сочетание карбоновой кислоты формулы с полимерной смолой гидроксиламина формулы с образованием полимерной смолы гидроксамовой кислоты формулыb) обработку полимерной смолы гидроксамовой кислоты кислотой.
МПК / Метки
МПК: C07D 307/33, C08F 212/08, C07C 45/00
Метки: кислоты, синтеза, аминов, способ, оксимов, кетонов, твердофазного, гидроксамовой, альдегидов
Код ссылки
<a href="https://eas.patents.su/30-2478-sposob-tverdofaznogo-sinteza-aldegidov-ketonov-oksimov-aminov-i-gidroksamovojj-kisloty.html" rel="bookmark" title="База патентов Евразийского Союза">Способ твердофазного синтеза альдегидов, кетонов, оксимов, аминов и гидроксамовой кислоты</a>


































