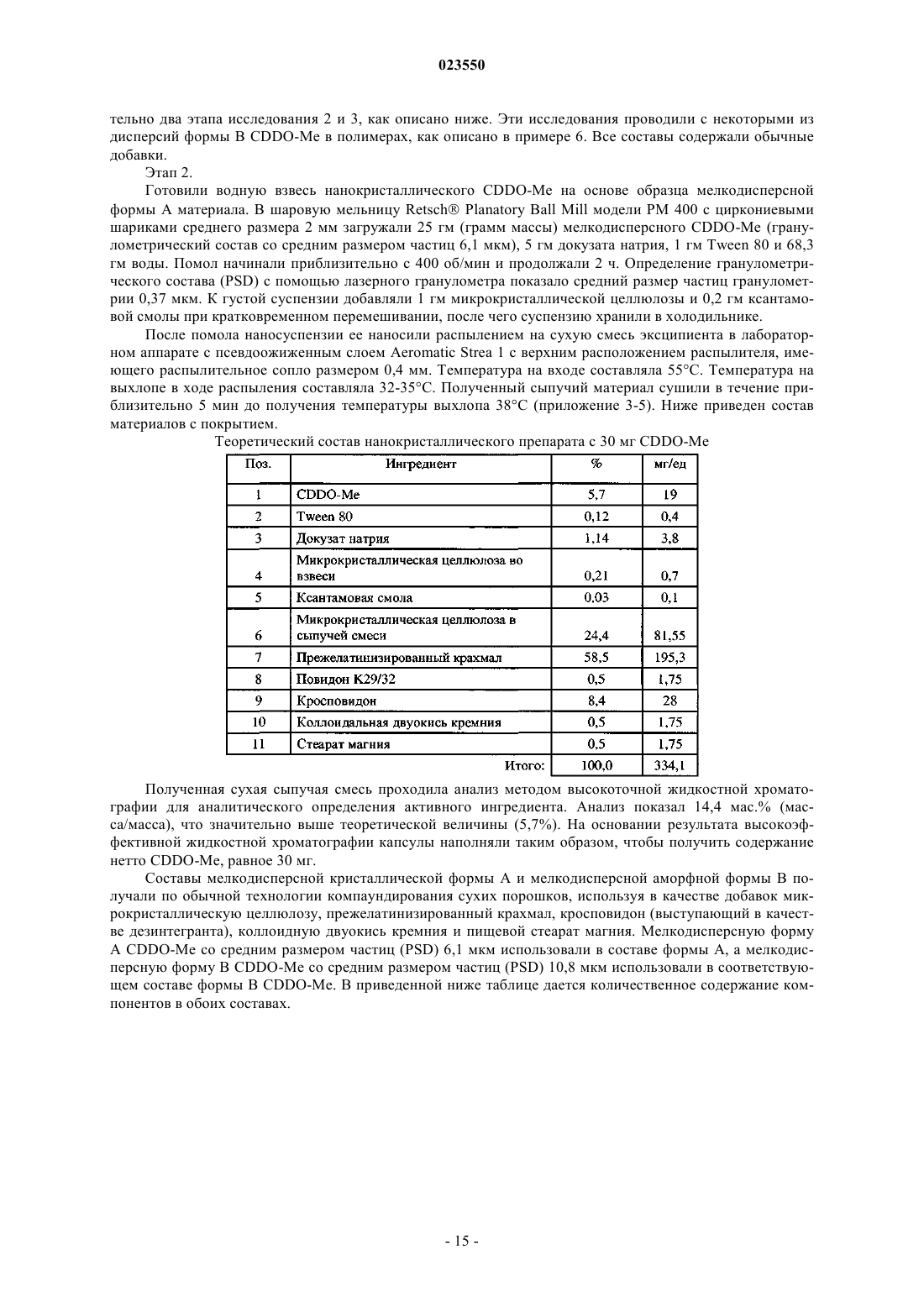
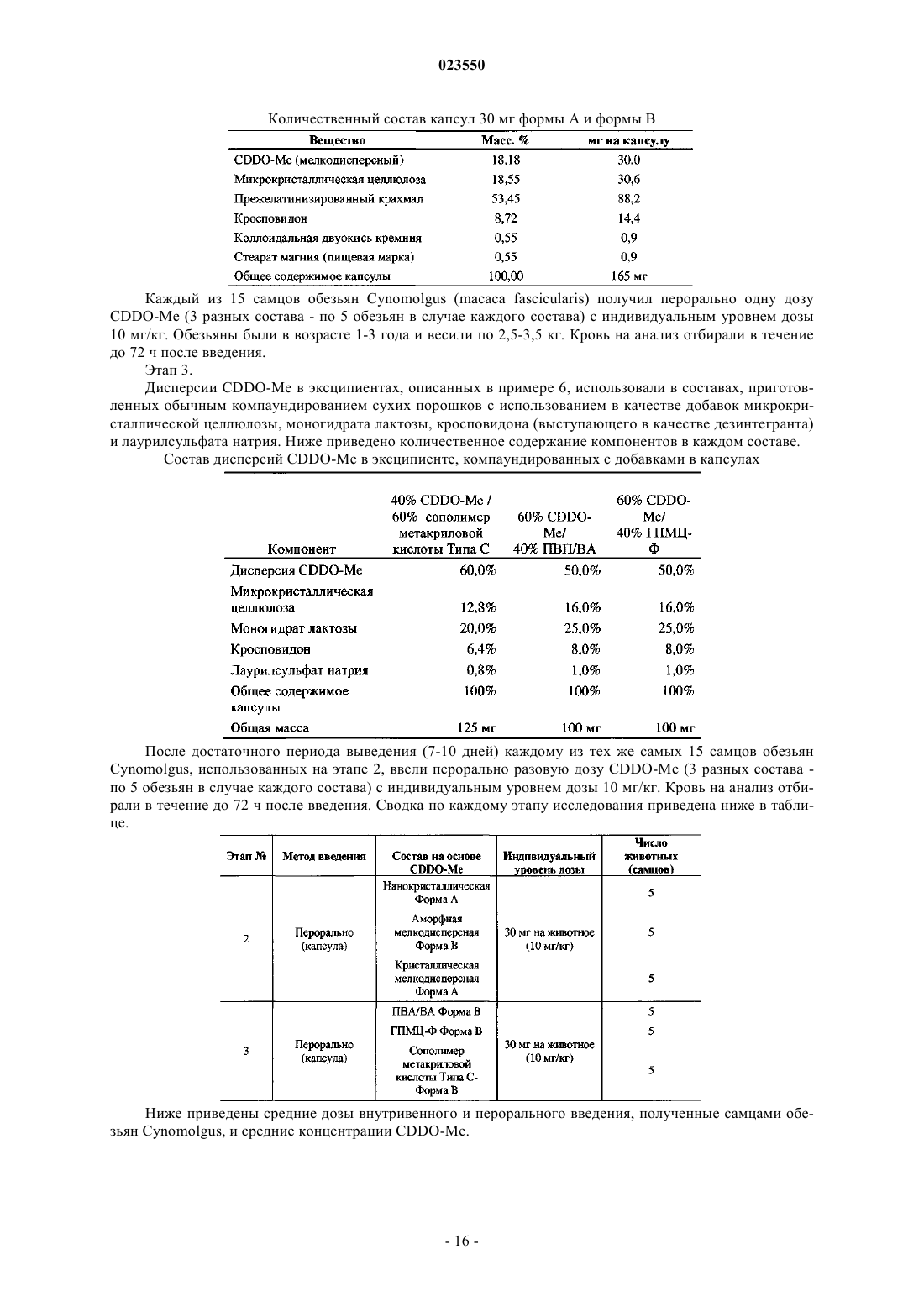
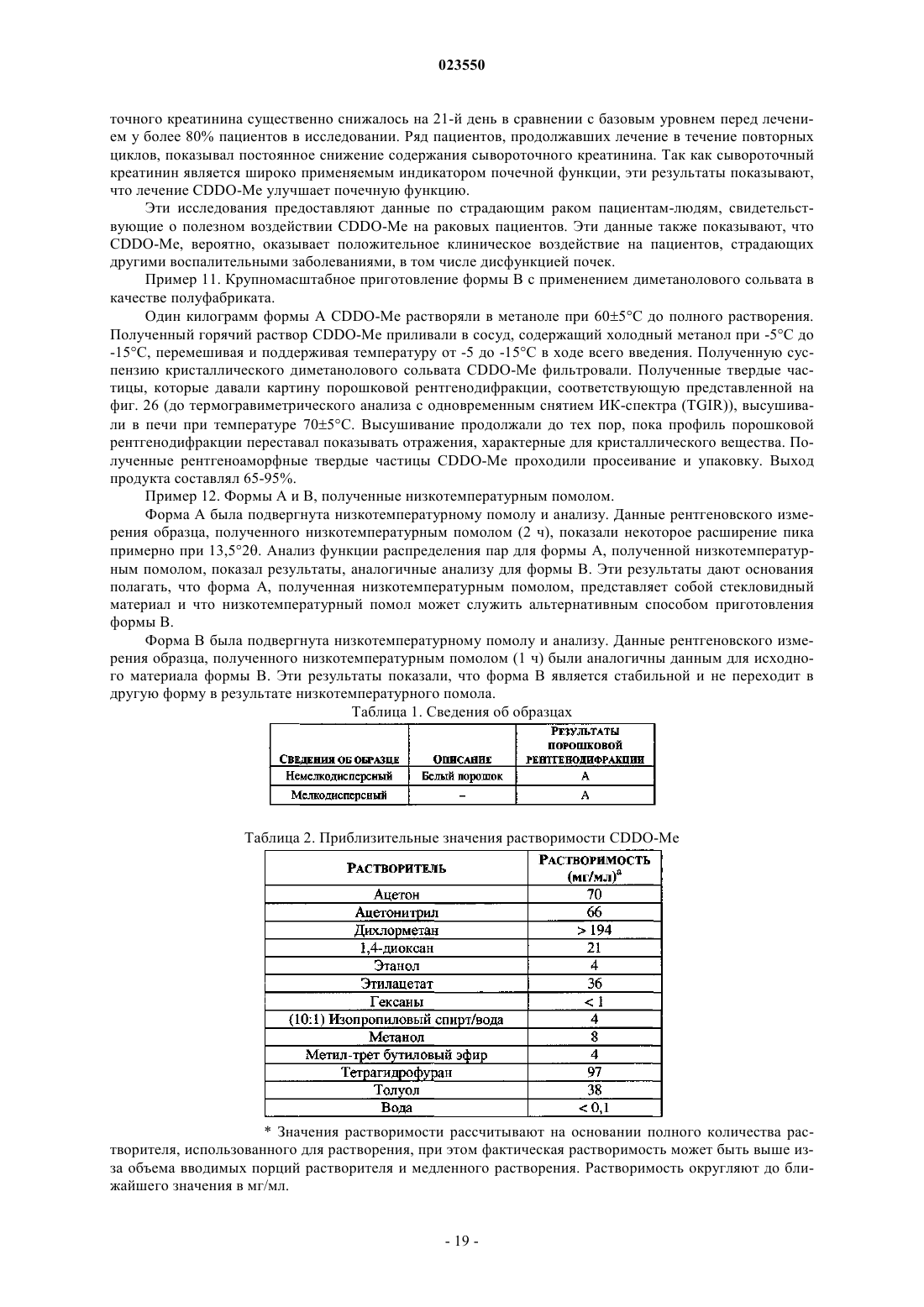
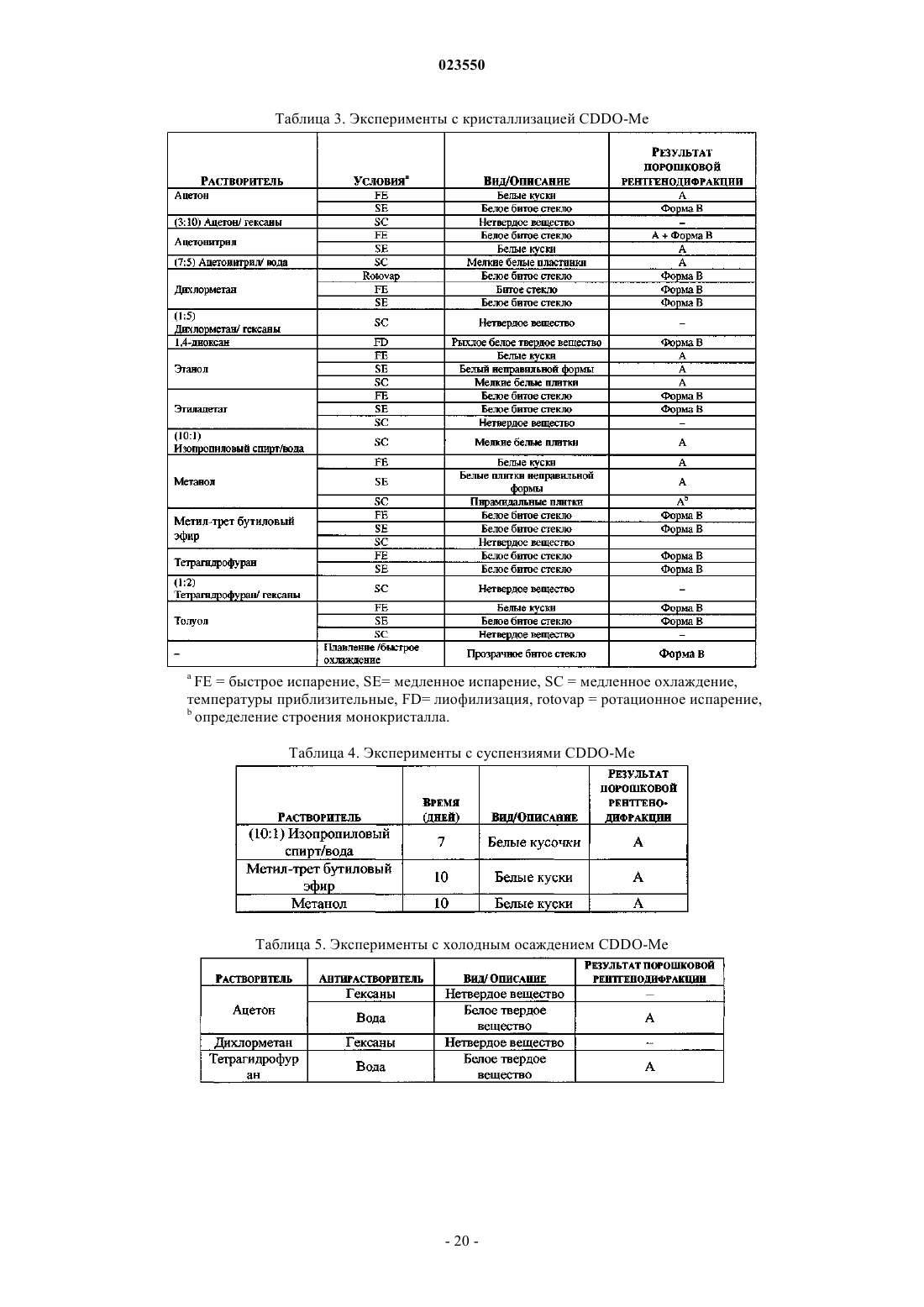
Новые формы метилового эфира 2-циано-3,12-диоксоолеан-1,9(11)-диен-28-овой кислоты (cddo-me)
Номер патента: 23550
Опубликовано: 30.06.2016
Авторы: Уоллинг Джон, Крэл Роберт М., Пэрент Стивен Д., Джонаитис Дэвид Т.
Формула / Реферат
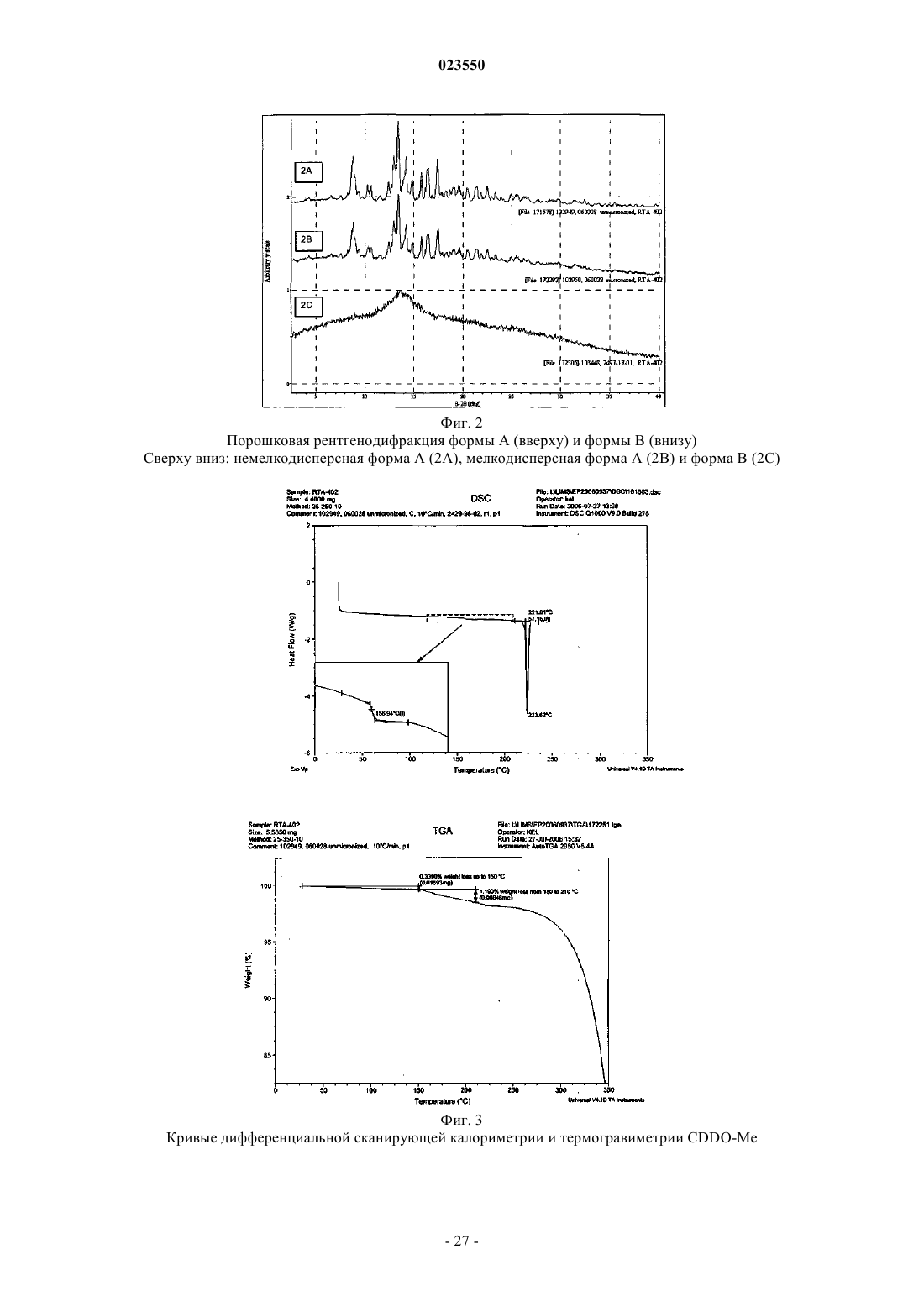
1. Безводный кристаллический метиловый эфир 2-циано-3,12-диоксоолеана-1,9(11)-диен-28-овой кислоты (метиловый эфир CDDO), характеризующийся тем, что его порошковая рентгеновская дифрактограмма содержит пики при 8,78° 2θ, 12,94° 2θ, 13,35° 2θ, 14,18° 2θ и 17,4° 2q±0,2° 2θ по данным, полученным на дифрактометре с облучением Cu Kα.
2. Метиловый эфир CDDO по п.1, отличающийся тем, что порошковая рентгеновская дифрактограмма, по существу, такая, как показано на фиг. 18.
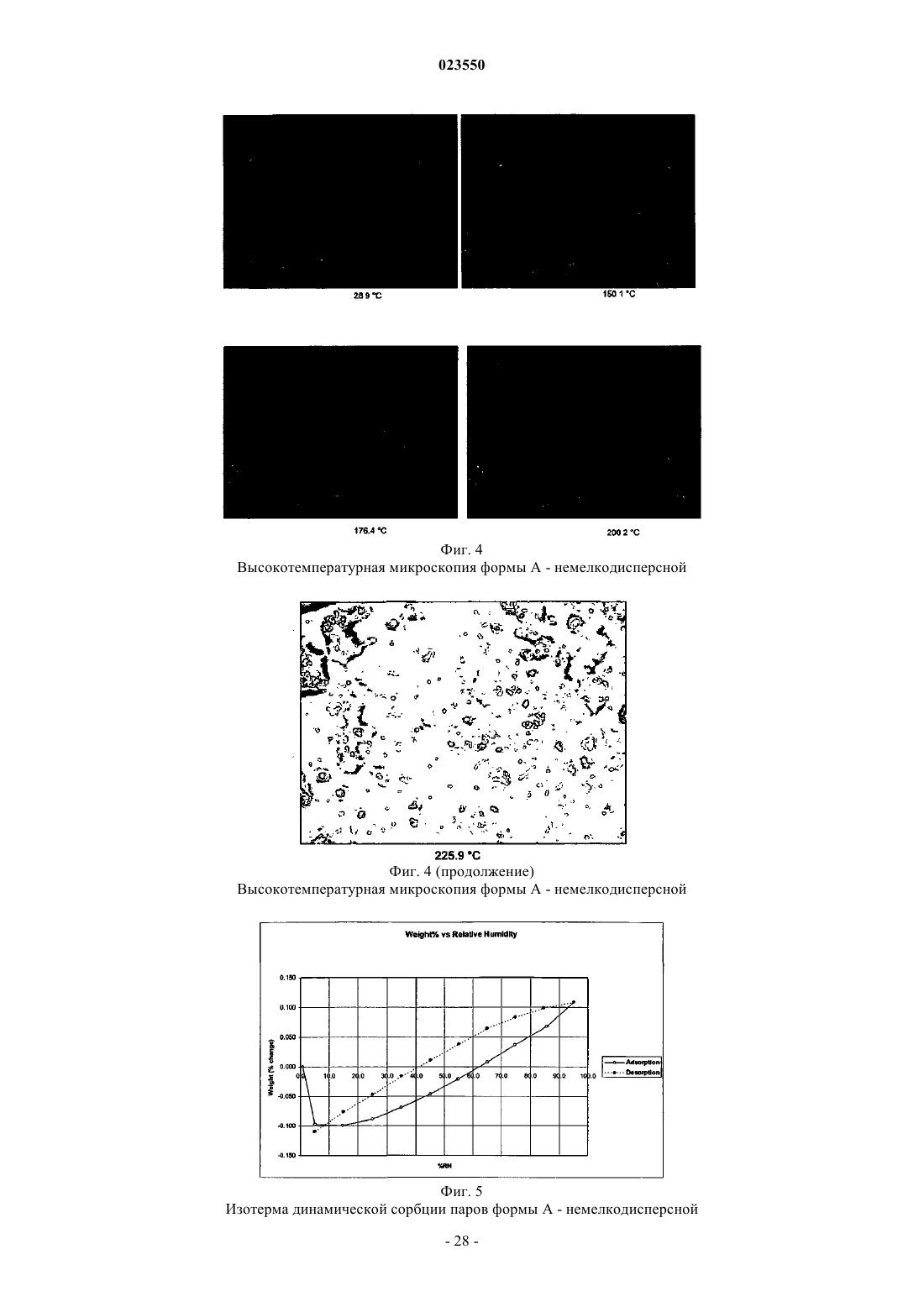
3. Метиловый эфир CDDO по п.1, дополнительно характеризующийся тем, что его кривая дифференциальной сканирующей калориметрии содержит сдвиг базовой линии приблизительно при 157°С и максимум на эндотерме примерно при 224°С.
4. Метиловый эфир CDDO по п.3, отличающийся тем, что кривая дифференциальной сканирующей калориметрии, по существу, такая, как показано на фиг. 3.
5. Фармацевтическая композиция для лечения хронического воспалительного состояния, содержащая терапевтически эффективное количество метилового эфира CDDO по п.1 и один или более твердых фармацевтически приемлемых носителей.
6. Фармацевтическая композиция по п.5, отличающаяся тем, что метиловый эфир CDDO является микронизированным, а указанные твердые фармацевтически приемлемые носители представляют собой съедобные носители.
7. Применение метилового эфира CDDO по п.1 для получения лекарственного средства для лечения хронического воспалительного состояния у субъекта, страдающего указанным состоянием.
8. Кристаллический гемибензольный сольват метилового эфира CDDO, характеризующийся тем, что его порошковая рентгеновская дифрактограмма содержит пики при 9,25° 2θ, 14,17° 2θ, 14,62° 2θ 16,32° 2θ и 17,11° 2θ ±0,2° 2θ по данным, полученным на дифрактометре с облучением Cu Kα.
9. Кристаллический гемибензольный сольват метилового эфира CDDO по п.8, дополнительно характеризующийся тем, что его кривая дифференциальной сканирующей калориметрии, по существу, такая, как показано на фиг. 23.
Текст
НОВЫЕ ФОРМЫ МЕТИЛОВОГО ЭФИРА 2-ЦИАНО-3,12-ДИОКСООЛЕАН-1,9(11)ДИЕН-28-ОВОЙ КИСЛОТЫ (CDDO-Me) Тритерпеноидное соединение - метиловый эфир 2-циано-3,12-диоксоолеан-1,9(11)-диен-28-овой кислоты (CDDO-Me) - находится в безводной кристаллической форме, приготовляемой, например,из насыщенного раствора в метаноле. Безводная кристаллическая форма CDDO-Me является превосходным кандидатом для применения обычно в твердой лекарственной форме при лечении различных заболеваний, как правило, связанных с воспалением. Перекрестная ссылка на родственные заявки на патент Данная заявка подана с испрашиваемым приоритетом по предварительной заявке на патент США 60/955939, поданной 15 августа 2007 г., содержание которой полностью включено в данную заявку посредством ссылки. Уровень техники Тритерпеноиды биосинтезируются в растениях циклизацией сквалена. Хотя они и являются кандидатами на применение в медицине, эти встречающиеся в природе молекулы отличаются сравнительно слабой биологической активностью. В связи с этим химики стремились синтезировать аналоги с повышенной эффективностью (Honda и др., 1997 и 1998). Несколько описанных синтетических аналогов подавляли изначальное образование iNOS и СОХ-2 в макрофагах, стимулируемых посредством IFN- или LPS (Suh и др., 1998; Honda и др., 2002). Другой синтетический тритерпеноид - 2-циано-3,12-диоксоолеан-1,9(11)-диен-28-овая кислота (CDDO) - оказывает противовоспалительное и антипрофилеративное действие (Honda и др., 1998 и 2000). При изучении CDDO-Me, являющегося метиловым эфиром 2-циано-3,12-диоксоолеан-1,9(11)-диен 28-овой кислоты (CDDO-Me), Bore и др. (2002) установили кристаллическую структуру. В этой форме,которая является гидратной, вода координирует взаимодействия, порождающие конкретную упаковку и структуру кристалла. Краткое описание изобретения В одном из вариантов осуществления данного изобретения получают безводную кристаллическую форму CDDO-Me. Безводная кристаллическая форма предпочтительно имеет пространственную группу Р 43212 с размерами элементарной ячейки а=14,2 , b=14,2 и с=81,6 . Изобретение также относится к фармацевтической композиции в виде твердой формы, содержащей (i) терапевтически эффективное количество безводной кристаллической формы CDDO-Me и (ii) съедобный носитель. Изобретение также относится к методологии лечения заболеваний или расстройств, проходящих с острым или хроническим оксидативным стрессом и воспалением, в частности характеризующимися избыточной выработкой (оверэкспрессией) индуцируемой синтазы оксида азота (iNOS) или индуцируемой циклооксигеназы (СОХ-2). Краткое описание чертежей Фиг. 1 представляет химическое строение CDDO-Me; фиг. 2 - порошковую рентгенодифракцию формы А (вверху) и формы В (внизу). Сверху вниз: немелкодисперсная форма А; мелкодисперсная форма А и форма В; фиг. 3 - кривые дифференциальной сканирующей калориметрии (DSC) и термогравиметрии (TG) для CDDO-Me (форма А); фиг. 4 - высокотемпературный анализ формы А - немелкодисперсной; фиг. 5 - динамическую изотерму сорбции паров формы А - немелкодисперсной; фиг. 6 - снимки электронной сканирующей микроскопии формы А - немелкодисперсной; фиг. 7 - форму А до (вверху) и после (внизу) стресса при 195 С; фиг. 8 - ЯМР-спектр формы А - немелкодисперсной; фиг. 9 - кривую дифференциальной сканирующей калориметрии при модулируемой температуре для формы В CDDO-Me; фиг. 10 - форму В CDDO-Me до (вверху) и после (внизу) теплового стресса при 200 С и относительной влажности окружающей среды в течение 60 мин; фиг. 11 - ЯМР-спектр формы В CDDO-Me; фиг. 12 - чертеж ORTEP одной молекулы формы А с маркировкой. Атомы представлены эллипсоидами анизотропных тепловых колебаний с вероятностью 50%; фиг. 13 - чертеж ORTEP содержимого ассиметричного формирования кристаллов формы А. Атомы представлены эллипсоидами анизотропных тепловых колебаний с вероятностью 50%; фиг. 14 - схему упаковки кристаллов формы А, изображенную по кристаллографической оси а; фиг. 15 - схему упаковки кристаллов формы А, изображенную по кристаллографической оси b; фиг. 16 - схему упаковки кристаллов формы А, изображенную по кристаллографической оси с; фиг. 17 - расчетную порошковую рентгенодифракцию формы А; фиг. 18 - порошковую рентгенодифракцию формы А в эксперименте; фиг. 19 - сравнение расчетной и экспериментальной порошковой рентгенодифракции формы ACDDO-Me; фиг. 20 дает представительное изображение области под кривой для форм А и В после перорального введения 4,1 мг/кг обезьянам Cynomolgus. Каждая точка данных представляет среднее содержаниеCDDO-Me в плазме у 8 животных. Планки погрешностей представляют стандартное отклонение в популяции выборки; фиг. 21 представляет сравнение содержания формы В CDDO-Me в плазме с содержанием формы А у животного 505 М (верхняя часть) и у животного 507F (нижняя часть); фиг. 22 - сравнение содержания формы В CDDO-Me в плазме с содержанием формы А у животного 508F (верхняя часть) и у животного 502 М (нижняя часть); фиг. 23 - термограммы гемибензольного сольвата CDDO-Me; фиг. 24 - термограммы диметанолового сольвата CDDO-Me; фиг. 25 - данные термогравиметрического анализа с одновременным снятием ИК-спектра (TGIR) для гемибензольного сольвата CDDO-Me; фиг. 26 - данные порошковой рентгенодифракции для диметанолового сольвата CDDO-Me до(вверху) и после (внизу) расчета TGIR (до 140 С); фиг. 27 - наложение данных PDF (функции распределения пар) для формы А и формы В. Локальный порядок аналогичен от примерно 5 до примерно 20 ; фиг. 28 - наложение функции распределения пар картин порошковой рентгенодифракции формы В,где видно, что эти виды практическианалогичны; фиг. 29 - схематичное изображение пространственной группы Р 43212 ( 96); фиг. 30 - среднее содержание CDDO-Me в крови после разового перорального введения капсулCDDO-Me самцам обезьян Cynomolgus (этапы 2 и 3). Подробное описание предпочтительных вариантов осуществления Как отмечено выше, исследование тритерпеноидов в качестве супрессоров действия iNOS, а более конкретно при ингибировании продуцирования NO показало высокую эффективность CDDO и CDDOMe (IC50 уровня 1 нМ). См. Honda и др. (2000). Эти исследования были сосредоточены на солюбилизированном CDDO-Me, предоставляя очень мало данных по твердому CDDO-Me. Работа Bore и др. (2002) прояснила впервые опубликованное для тритерпеноида строение одной сольватированной кристаллической формы CDDO-Me. Для выявления возможной терапевтической активности CDDO-Me, представленного на фиг. 1 (химическое строение) и на фиг. 12 (чертеж ORTEP), авторы исследовали иные формы соединения, обладающие такими свойствами, как повышенная водорастворимость и химическая стойкость, благоприятными для разработки медикаментозного продукта с подходящей фармакокинетикой. В результате авторы обнаружили две формы CDDO-Me, отличные от кристаллической формы, описанной в работе Bore и др.(2002), обладающие такими свойствами и, следовательно, являющиеся полноправными кандидатами для разработки лекарственных препаратов. Предлагаемая "форма A" CDDO-Me - несольватированная (безводная), при этом она характеризуется особым строением кристалла с пространственной группой P43212( 96), представленной на фиг. 29, с размерами элементарной ячейки а = 14,2 , b= 14,2 и с = 81,6 , а также отличается структурой упаковки, представленной на фиг. 14-16, где три молекулы упакованы по спирали вдоль кристаллографической оси b. В приведенной ниже табл. 10 представлены дополнительные данные по кристаллу формы А вместе с параметрами получения кристаллографических данных. Другая предлагаемая форма В - однофазная, но не имеет выраженного кристаллического строения. Форма В скорее выражена спектром порошковой рентгенодифракции (XRPD), отличающимся от спектра для формы А (см., кроме прочего, фиг. 2). Более того, форма В отличается биодоступностью, которая неожиданно оказалась лучшей, чем у формы А (см. пример 7). Методика синтеза CDDO-Me была опубликована. См. патент США 6326507, Honda и др. (1998) иHonda и др. (2000). Авторы обнаружили, что обе формы CDDO-Me - А и В - легко приготовляются из разнообразных растворов соединений, примеры которых приведены подробно ниже в табл. 3-5. В частности форму В можно получить быстрым выпариванием из МТБЭ, ТГФ, толуола или этилацетата. Точно так же форму А можно получить быстрым испарением, медленным испарением или медленным охлаждением раствора CDDO-Me в этаноле или метаноле. Исходные растворы CDDO-Me в ацетоне можно использовать для получения либо формы А путем быстрого испарения, либо формы В путем медленного испарения. Иные способы приготовления описаны ниже, в том числе в приведенных ниже таблицах. В силу отсутствия выраженного кристаллического строения форма В не имеет и выраженных пиков порошковой рентгенодифракции, которые отличают форму А, а вместо этого характеризуется общей картиной "ореола" порошковой рентгенодифракции. В частности, некристаллическая форма В относится к категории "рентгеноаморфных" твердых тел, так как ее порошковая рентгенодифракция имеет три и менее первичных ореолов дифракции (см., например, фиг. 10). В этой категории форма В является "стекловидным" материалом. Как показывает функция распределения пар (PDF), взаимодействия между соседними атомами совпадают с наблюдаемыми для кристаллической формы А, но при этом понятие средней элементарной ячейки неприменимо, поскольку нет проявления дальнего порядка. В связи с этим, в отличие от формы А форма В не имеет дальней молекулярной корреляции, т.е. приблизительно более 20(см. фиг. 27). Кроме того, тепловой анализ образцов формы В выявляет температуру стеклования (Tg). Напротив, нанокристаллический материал не имеет Tg, а вместо этого отличается только точкой плавления (Tm), выше которой кристаллическая структура становится жидкостью. В данном описании также представлена форма диметанолового сольвата CDDO-Me, которую можно использовать для приготовления формы В (см. пример 9). Приводится также описание формы гемибензольного сольвата CDDO-Me (см. пример 8). Хотя было установлено влияние перевода кристаллического материала в мелкодисперсную форму на спектры порошковой рентгенодифракции, анализ порошковой рентгенодифракции мелкодисперсной формы А дает спектр, аналогичный немелкодисперсной форме А. См. фиг. 2, где рядом показаны немелкодисперсная фформа А, мелкодисперсная форма А и форма ВCDDO-Me. Можно использовать сочетание различных средств определения для различения форм А и В CDDOMe и для выявления их отличия от других форм CDDO-Me. Примерами пригодных для этого методик являются твердотельный ядерно-магнитный резонанс (ЯМР), порошковая рентгенодифракция, рентгенокристаллография, дифференциальная сканирующая калориметрия (DSC), динамическая паровая сорбция/десорбция (DVS), анализ по методу Карла Фишера (КФ), высокотемпературная микроскопия, дифференциальная сканирующая калориметрия с модулируемой температурой, ИК-спектроскопия с преобразованием Фурье (FT-IR) и Рамановская спектроскопия. В частности, анализ данных порошковой рентгенодифракции и дифференциальной сканирующей калориметрии позволяет различать форму А, форму В и формы гемибензольного сольвата CDDO-Me. Свойства предлагаемых согласно изобретению форм CDDO-Me являются отличительными и, как указано выше, также позволяют использовать эти формы в качестве лекарственных препаратов. Например, биодоступность формы В и формы А CDDO-Me у обезьян различалась, когда обезьянам давали одинаковые дозы двух форм перорально в виде желатиновых капсул. См. пример 7. Помимо того, стабильность вновь открытых форм CDDO-Me окажется полезной при производстве фармацевтических композиций. Аналогично установлению отличия форм А и В CDDO-Me друг от друга и от других форм CDDOMe, дисперсии CDDO-Me, сохраняющие "рентгеноаморфный" характер, как подробно описано ниже,можно отличать от дисперсий, содержащих кристаллическую форму A CDDO-Me, с помощью различных методик, в том числе порошковой рентгенодифракции и дифференциальной сканирующей калориметрии. Так, дисперсии, содержащие кристаллическую форму A CDDO-Me, обычно дают дискретные пики,характерные для чистой формы A CDDO-Me, в частности пики, приходящиеся приблизительно на 13,35 и 8,78 (2) (см., например, ниже в табл. 17). Свойства дисперсии CDDO-Me в предлагаемом полимерном эксципиенте являются отличительными и позволяют использовать ее в качестве лекарственных препаратов. Например, биодоступность выбранных дисперсий CDDO-Me, приготовленных с дополнительными неактивными добавками, различалась при введении обезьянам одинаковых доз дисперсий в виде желатиновых капсул. См. ниже пример 7, этапы исследования 2 и 3. В нескольких случаях составы, содержащие CDDO-Me с полимерным эксципиентом, неожиданным образом повышали биодоступность даже в сравнении с составами, приготовленными из чистой формы В CDDO-Me. Наличие в твердых фармацевтических препаратах нескольких форм, в том числе полиморфов, ранее описано, например, в работе Cui(2007). Кристаллические и аморфные формы соединения могут иметь различные физико-химические свойства. Например, аморфные формы могут иметь повышенную стабильность в сравнении с кристаллической формой. В этом смысле каждое соединение уникально, однако степень отличия аморфной формы материала от кристаллической подлежит выяснению в каждом конкретном случае и не является предсказуемой. Помимо этого, некоторые аморфные материалы склонны к рекристаллизации. В этом смысле возможны отклонения при сборе данных в силу огромного количества факторов. Поэтому в данном описании используются уточнения "примерно" или "приблизительно" для указания на возможность отклонения данных при описании форм CDDO-Me. Например, температура плавления может изменяться в зависимости от приборного оснащения или условий испытания. В части точности измерений USP 891 указывает, что "в случае плавления можно объективно и воспроизводимо определять как "начальную", так и "максимальную" температуру, при этом зачастую с точностью до десятых долей градуса". Практический опыт показывает, что это не получается при измерении температуры стеклования материала Tg. Температура Tg зависит от многих факторов: способа приготовления образца, тепловой истории образца (релаксация), наличия остатков растворителя, который мог не улетучиться перед измерением Tg, вида прибора, вида образца (масса образца, размер частиц, упаковка, разбавители), параметров измерения Tg (в частности, скорости сканирования), параметров определения положения Tg (начальная температура, средняя температура, температура в точке перегиба или температура смещения),наличия эндотермы релаксации при температуре Tg и прочих факторов. Некоторые факторы снижают Tg(пластификация из-за остатков воды или растворителя), а иные повышают Tg (увеличение скорости сканирования, релаксация), при этом увеличение может составлять до 10-15 С. Имеют значение также изменения теплоемкости при температуре стеклования Tg (Cp) согласно работе Zhou и др., J. Pharmaceutical Sciences 91: 1863-72 (2002). В данном описании идет речь о различных закономерностях с точки зрения "характеристических" пиков. Скопление или группа таких пиков является уникальной для данной полиморфной формы в рамках неопределенности в силу применения соответствующих приборов и условий эксперимента. В приведенных ниже табл. 17-19 для каждой из кристаллических форм приведена группа из пяти характеристических пиков. Типичные возможные отклонения составляют 0,12, но при этом в некоторых экспериментах положение пика может изменяться на величину до 0,22 и более. Порошковая рентгенодифракция стекловидного материала (форма В) показывает широкое гало примерно при 13,52, которое представляется характерным для формы В. Другие гало не являются ярко выраженными, при этом форма и положение пиков могут изменяться в зависимости от применяемого прибора и условий эксперимента. Флуктуация положения этого широкого пика более существенна, чем флуктуация положения характеристического пика соответствующих кристаллических форм. В частности, при применении некоторых приборов можно ожидать отклонения широкого пика формы В до 12. Порошковая рентгеновская дифракция стекловидных материалов, приготовленных в виде дисперсий CDDO-Me в эксципиенте, также показывает широкое гало обычно с центром приблизительно при 13,52. Эти материалы также имеют температуру стеклования Tg при испытании методом дифференциальной сканирующей калориметрии с модулированной температурой (MDSC). Аналогично образцамCDDO-Me чистой формы В форма и положение пиков порошковой рентгеновской дифракции для дисперсии в эксципиенте может изменяться в зависимости от применяемого прибора, условий эксперимента, а также от конкретного эксципиента, применяемого для приготовления дисперсий. Данное изобретение далее относится к применению соответственно формы А, формы В CDDO-Me для лечения заболеваний, связанных с воспалением, в том числе раковых заболеваний и различных патологий, влияющих на центральную нервную систему. Согласно изобретению лечение таких заболеваний проводят введением требующему лечения пациенту эффективного количества новых указанных в данном описании форм CDDO-Me. Эти соединения полезны тем, что облегчают или предотвращают воспаление в этиологии рака, болезни Альцгеймера (AD), болезни Паркинсона (PD), рассеянного склероза(MS), бокового амиотрофического склероза (ALS), ревматоидного артрита (RA) и прочих аутоиммунных заболеваний, воспалительных заболеваний кишечника и прочих патологических заболеваний, связанных с избыточным продуцированием оксида азота или простагландинов. Как отмечено выше, ненормальную или чрезмерную экспрессию либо циклооксигеназы-2 (СОХ-2), либо индуцируемой синтазы оксида азота(iNOS) связывают с патогенезом многих болезненных процессов, в том числе канцерогенеза в ободочной кишке. Имеются опубликованные сведения о подавлении экспрессии iNOS несколькими синтетическими аналогами тритерпеноидов, в том числе CDDO-Me. Соответствующие исследования показали подавление экспрессии и iNOS, и СОХ-2 в макрофагах, стимулируемых посредством IFN- или LPS (Suh и др.,1998; Honda и др., 2002). Поэтому следует ожидать, что лечение введением форм CDDO-Me повлияет на экспрессию iNOS и СОХ-2. Избыточная экспрессия гена СОХ-2 является ранним и центральным событием в канцерогенезе ободочной кишки (Prescott and White, 1996; Dubois и др., 1996). Мыши с дефектами в гене АРС (аденоматозный полипоз coli) имели множество кишечных полипов в раннем возрасте, при этом в указанных полипах выявили заметные повышения содержания фермента СОХ-2. Эти результаты на животных коррелируют с показаниями повышенных содержаний СОХ-2 мРНА и белка во многих случаях первичного рака ободочной кишки и в линиях клеток рака ободочной кишки (Prescott and White, 1996), при этом по-4 023550 лагают, что такое повышение содержания СОХ-2 приводит к подавлению апоптоза, который обычно приводил бы к гибели предопухолевых клеток (Tsujii and DuBois, 1996). Функциональная важность СОХ 2 для кишечного генеза опухоли показана нокаутом гена СОХ-2 (Oshima и др., 1996). Мышей с таким нокаутом спаривали с полипообразущими мышами, имеющими повреждения в гене АРС, при этом нокаут гена СОХ-2 вызывал резкое снижение числа полипов у потомства. Кроме того, лечение экспериментальных животных либо селективными ингибиторами СОХ-2, либо неселективными ингибиторами СОХ 1/СОХ-2, судя по публикациям, является эффективным подходом к хемопрофилактике рака кишечника(Marnett, 1992; Oshima и др., 1996; Boolbol и др., 1996; Reddy и др., 1996; Sheng и др., 1997). Что касается роли iNOS в канцерогенезе, очевидно, что NO является потенциальным мутагеном (Tamir andTannebaum, 1996) и что окись азота может также активировать СОХ-2 (Salvemini и др., 1993, 1994). Наблюдали также заметное увеличение iNOS в опухолях ободочной кишки у крыс, вызываемое канцерогеном - азоксиметаном (Takahashi и др., 1997). Аналогично избыточная экспрессия iNOS в опухолях у людей в публикациях рассматривается как негативный прогностический фактор (например, Ekemekcioglu и др., 2006). Пути передачи сигнала воспаления и прочие пути связанной с заболеваниями передачи сигнала, такие как вызванные ангитензином II, часто стимулируют избыточное продуцирование химически активных разновидностей кислорода или азота (RONS), в том числе супероксида, перекиси водорода и пероксинтрита. Показано, что CDDO-Me является мощным индуктором антиокислительной активности и эффективным ингибитором воспалительных процессов во многих различных типах клеток (DinkovaKostova и др., 2005; Liby и др., 2006; Ahmad и др., 2006; Shishodia и др., 2006). Тяжелое и острое воспаление, вызванное различными причинами, в том числе инфекцией, травмой, ожогами и химическим воздействием, может представлять угрозу жизни и вызывать отказ печени, почечную недостаточность, остановку дыхания или сердечную недостаточность. Хроническое воспаление и связанный с ним оксидативный стресс приводят к патологии многих серьезных заболеваний, в том числе к аутоиммунным заболеваниям (например, к ревматоидному артриту, волчанке, псориазу и рассеянному склерозу), сердечнососудистым заболеваниям (например, к атеросклерозу и сердечной недостаточности), к диабету (типа I и типа II), заболеваниям дыхательного тракта (например, к хроническому обструктивному заболеванию легких и к астме), к хроническому заболеванию почек, почечной недостаточности, отказу печени, а также к болевым синдромам (например, к невропатической боли, хронической усталости [fibromyalgia] и мигрени). Кроме того, показано, что тритерпеноиды ингибируют репликацию ВИЧ-1 в макрофагах(Vazquez и др., 2005), в результате чего они могут оказаться полезными при лечении вирусных заболеваний, в частности таких, при которых значительная заболеваемость вызвана воспалением органа или ткани (например, вирусный гепатит, грипп и простой герпес). Известно, что рассеянный склероз представляет собой воспалительное заболевание центральной нервной системы (Williams, Ulvestad и Hickey, 1994;Merrill и Beneviste, 1996; Genain и Nauser, 1997). Воспалительные, оксидативные или иммунные механизмы могут участвовать в патогенезе рассеянного склероза, болезни Альцгеймера, болезни Паркинсона и амиотрофического склероза (Bagasra и др., 1995; Griffin и др., 1995; McGeer и McGeer, 1995; Good и др., 1996; Simonian и Coyle, 1996; Kaltschmidt и др., 1997). И реактивные астроциты, и активированные микроглии участвуют в возникновении нейродегенеративных и нейроинвазивных заболеваний. Особое внимание уделяют микроглиям как клеткам, синтезирующим как NO, так и простагландины - продукты соответствующих ферментов - iNOS и СОХ-2. Изначальное образование этих ферментов может быть вызвано воспалительными цитокинами, такими как интерферон- или интерлейкин-1. В свою очередь,избыточное продуцирование NO может вызывать каскадные воспаления и(или) оксидативное повреждение клеток и тканей многих органов, в том числе нейронов и олигодендроцитов нервной системы с последующими проявлениями в болезни Альцгеймера и рассеянном склерозе, а возможно и в болезни Паркинсона и амиотрофическом склерозе (Coyle и Puttfarcken, 1993; Goodwin и др., 1995; Beal, 1996; Good и др., 1996; Merrill и Benvenist, 1996; Simonian и Coyle, 1996; Vodovotz и др., 1996). Эпидемиологические данные показывают, что хроническое применение нестероидных противовоспалительных препаратов,блокирующих синтез простагландинов из арахидоната, заметно снижает риск развития болезни Альцгеймера (McGeer и др., 1996; Stewart и др., 1997). В связи с этим форма А и форма В CDDO-Me в качестве препарата, блокирующего образование NO и простагландинов, должны быть полезными в терапевтическом подходе к лечению и предупреждению нейродегенеративных заболеваний. Как описано выше, в различных предклинических исследованиях CDDO-Me показал способность ингибировать экспрессию СОХ-2 и iNOS - ферментов, связанных как с воспалениям, так и с канцерогенезом. Было также показано, что CDDO-Me ингибирует активацию ядерного фактора каппа-В (NF-В) и сигнального трансдуктора и активатора транскрипции 3 (STAT3), факторов транскрипции, связанных с воспалением, прогрессированием опухоли и стойкостью опухоли к терапии. Первоначальные исследования свидетельствуют о том, что CDDO-Me ингибирует рост многих линий раковых клеток, при этом средняя величина IC50 для CDDO-Me в панели линии опухолевых клеток NCI-60 составляла приблизительно 35 нМ. Исследования в организме подтвердили, что CDDO-Me эффективно ингибирует рост опухолей, образованных линиями опухолевых клеток человека, при имплантации грызунам или сингенетических линий раковых клеток, имплантированных грызунам (табл. 16). Применяемые в этих исследова-5 023550 ниях дозы обычно составляли от 10 до 100 мг/кг в сутки в зависимости от вида животного, штамма и способа введения. Описанные ниже исследования содержат данные для людей, отражающие полезное терапевтическое действие CDDO-Me на пациентов с раковыми заболеваниями. См. пример 10. В свете описанного выше данное изобретение относится к стабильным дозированным формам с контролируемым высвобождением, содержащим форму CDDO-Me. Предлагаемая дозированная форма может быть предназначена для приема один раз в день, для замедленного высвобождения или для порционного высвобождения с тем, чтобы оптимизировать лечение, согласуя фармакокинетические характеристики с фармакодинамическими требованиями. Любая из форм В, А и любой состав, содержащий дисперсию CDDO-Me в эксципиенте, может вводиться перорально. Активное вещество можно покрывать материалом для защиты вещества от воздействия кислот и иных природных факторов, которые могут приводить к потере активности вещества. Данное изобретение также допускает иные методы введения, такие как местное, подкожное, внутривенное и внутрибрюшинное. Для введения лечебного вещества может потребоваться покрытие вещества предотвращающим его инактивирование материалом или введение его совместно с таким материалом. При этом форма В или форма A CDDO-Me может вводиться пациенту на подходящем носителе, например на липосомах или в разбавителе. Фармацевтически приемлемые разбавители включают физиологические и буферные водные растворы. Липосомы включают водно-масляно-водные эмульсии факторов роста хондроцитов (CGF), а также обычные липосомы. См., например, Strejan и др., J. Neuroimmunol. 7: 27(1984). Лечебное вещество можно вводить перорально с инертными разбавителями, с добавками или со съедобным носителем, применяемыми для получения фармацевтической композиции. С этой целью предлагаемое лечебное вещество с другими ингредиентами можно заключать в желатиновую капсулу с твердой или мягкой оболочкой, прессовать в таблетки или непосредственно добавлять в пищу пациента. Для перорального лечебного введения форму А или форму В можно совмещать с эксципиентами и использовать в виде заглатываемых таблеток, таблеток для рассасывания в щечном кармане, пастилок, капсул, эликсиров, суспензий, сиропов, вафель и т.п. Аналогично предлагаемую дисперсию в эксципиенте можно выпускать в разнообразных видах, которые различаются по дозировке, в том числе в виде описанных в данной заявке форм А или В. Процентное содержание лекарственного вещества в композиции и в препаратах может изменяться по известным правилам для получения требуемой дозы активного вещества. Кроме того, данное изобретение относится к фармацевтической композиции, содержащей эффективное количество формы В CDDO-Me или формы А вместе с одним или несколькими фармацевтически приемлемыми носителями и(или) разбавителями и при необходимости с иными активными ингредиентами. Как указано выше, активное вещество может быть получено в виде гомогенной дисперсии в эксципиенте на основе формы В или формы А. Такая дисперсия CDDO-Me в эксципиенте представляет собой твердый раствор и может рассматриваться как гомогенная дисперсия на молекулярном уровне. Такие дисперсии целесообразно совмещать с другими фармацевтически приемлемыми добавками для стабилизации активного вещества и в некоторых случаях -для дополнительного повышения биодоступности. При приготовлении состава CDDO-Me в виде дисперсии в эксципиенте выбор эксципиента для дисперсии определяется требованием к эксципиенту, который должен быть хорошим "стеклообразователем" при обеспечении фармацевтической приемлемости. В общем случае эксципиент должен образовывать стойкую гомогенную стекловидную матрицу, которая стабилизирует дисперсию, обеспечивая температуру стеклования Tg выше типичной окружающей температуры в условиях хранения. В этом смысле дополнительным требованием к эксципиенту для дисперсии является его химическая совместимость с другими добавками, такими как связующие, наполнители, смазки, глиданты и т.п., которые могут использоваться в готовом составе для придания ему требуемых функциональных свойств. Для удовлетворения указанных требований эксципиент может быть выбран согласно изобретению из ряда веществ, отличающихся достаточно высокой температурой стеклования Tg таких как (А) углеводы, производные углеводов и полимеры углеводов; (В) синтетические органические полимеры; (С) соли органических кислот; (D) белки, полипептиды и пептиды; и (Е) высокомолекулярные полисахариды, такие как гепарин, представляющий собой сульфатированный полисахарид, и гиалуроновая кислота мукополисахарид. Примеры класса (А): производные целлюлозы, такие как гидроксипропилцеллюлоза (ГПЦ), гидроксипропилметилцеллюлоза (ГПМЦ) и этилцеллюлоза; полисахариды, такие как раффиноза, мальтотриоза, стакиоза, декстрины (в том числе, среди прочего, мальтодекстрины и циклодекстрины), декстраны и растворимый крахмал; альдитолы, такие как маннитол, ксилитол и сорбитол; и дисахариды, такие как лактоза, трехалоза, мальтоза и сахароза. Предпочтительным эксципиентом из этого класса является гидроксипропилметилцеллюлозы фталат (ГПМЦ-Ф). Примерами класса (В) являются поли[1-(2-оксо-1-пирролидинил)]этилен, известный также как повидон или поливинилпирролидон (ПВП), и связанные с ним полимеры, такие как сополимер винилпирролидона с винилацетатом (ПВП/ВА), с различными молекулярными массами. В этот класс также вклю-6 023550 чено семейство сополимеров метакриловой кислоты, таких как сополимер метакриловой кислоты типа С(USP/NF). Примерами класса (С) являются соли, такие как соли натрия, калия, кальция и магния, соответственно, молочно-кислые соли, соли аскорбиновой кислоты, соли малеиновой кислоты, соли щавелевой кислоты, соли малоновой кислоты, соли яблочной кислоты, соли янтарной кислоты, соли лимонной кислоты, соли глюконовой кислоты и соли глютаминовой кислоты. Так, представительными солями в этом классе являются цитрат натрия, лактат натрия, малеат натрия, глюконат магния и аскорбат натрия. Примеры эксципиентов класса (D): сывороточный альбумин человека; полиаминовая кислота, например полиаланин, полиаргинин, полиглицин, а также полиглютаминовая кислота; казеин; коллаген; желатин и очищенные желатиновые белки; а также некоторые фармакологически активные вещества, такие как инсулин. Как указывалось, эксципиенты могут изменять некоторые физические свойства фармацевтических препаратов. Например, дисперсия в различных полимерных эксципиентах может приводить к снижению наблюдаемой температуры стеклования состава Tg. Обычно температура стеклования Tg является дополнительным свойством, основанным на соотношении применяемых материалов. Поэтому при применении полимеров с величинами Tg, которые ниже, чем у аморфной формы В, можно ожидать снижения наблюдаемой температуры стеклования Tg у дисперсий (смесей). Кроме того, часто присутствует влага или следы остатков органического растворителя, которые также вызывают снижение Tg. Для образования твердой дисперсии CDDO-Me оптимальный выбор эксципиента обычно должен быть определен эмпирическим путем. Например, при попытках получения стекловидных рентгеноаморфных дисперсий с применением эксципиентов из семейства полиэтиленгликолей (PEG), таких какPEG 6000, получали смеси с характеристическими пиками, связанными с присутствием формы A CDDOMe. Аналогичные результаты получали при применении витамина Е - TPGS - эксципиента, получаемого этерификацией эфира янтарной кислоты dтокоферила с полиэтиленгликолем 1000, а также при применении сополимеров этиленоксида с пропиленоксидом, таких как Pluronic. Как показывают приведенные выше примеры, некоторые полимерные эксципиенты, используемые для приготовления предлагаемой дисперсии CDDO-Me, вызывают неожиданные улучшения биодоступности при пероральном введении в сравнении с лекарственным препаратом в виде чистой формы В. Можно применять различные способы приготовления гомогенных стекловидных рентгеноаморфных дисперсий CDDO-Me с фармацевтически приемлемыми эксципиентами, при этом в приведенных в данном описании примерах для получения таких дисперсий используют сушку распылением. Можно использовать другие способы приготовления предлагаемых дисперсий, обладающих равноценными свойствами и полезностью. См. Repka и др., 2002 с указанными в работе ссылками. Такие иные методы включают, среди прочего, испарение растворителей и экструдирование, например экструдирование горячего расплава. Помимо эксципиента можно включать другие добавки для улучшения стабильности активного ингредиента, для корректировки рН (т.е. буфер), улучшения диспергирования, повышения равномерности доставки, а также для обеспечения иных свойств, желательных для фармацевтического состава. Вводимое количество предлагаемого вещества или композиции может меняться в зависимости от пациента и способа введения, при этом речь может идти о любом эффективном количестве. Назначаемую схему введения предлагаемой композиции можно выработать путем обычных общепринятых предклинических и клинических испытаний, которые включают, среди прочих факторов, элементы, зависящие от терапевтического показания. Количество вводимого препарата может изменяться в широких пределах так, чтобы обеспечить в единичной дневной дозе фармакологически эффективное количество, основанное на массе тела пациента, с целью получения желаемого результата. Необходимая доза также может меняться в зависимости от заболевания, подвергаемого лечению. Например, при лечении острого ракового заболевания может потребоваться существенно более высокая доза, чем при лечении воспалительного заболевания, такого как артрит. В частности, предлагаемая композиция представлена в виде разовой дозы для приема от 1 до 3 раз в день, предпочтительно один раз в день с целью получения желаемого результата. Кроме того, предлагаемую композицию можно принимать раз в два дня, раз в три дня, раз в четыре дня, раз в пять дней, раз в шесть дней или раз в неделю. Предлагаемую композицию можно вводить в отдельности или в сочетании с другими лекарственными средствами в соответствии с конкретными потребностями пациента. В частности, предлагаемую композицию можно вводить с противораковыми препаратами в составе схемы лечения. Например,CDDO-Me можно вводить с гемцитабином или иными препаратами для лечения рака, такого как рак поджелудочной железы. В общем случае предлагаемую фармацевтическую композицию получают с использованием обычных материалов и приемов, таких как смешивание, компаундирование и т.п. Кроме того, медикамент,содержащий форму А или форму В, может также содержать другие компоненты, в том числе, среди прочего, подходящие активирующие добавки, носители, эксципиенты, стабилизирующие добавки и т.п. Предлагаемый лекарственный препарат предпочтительно представляет собой твердое вещество,однако в принципе он может быть жидким, например в виде суспензии или эмульсии. Согласно изобретению пероральная поддерживающая доза обычно составляет от примерно 0,1 до примерно 1000 мг предпочтительно при приеме один раз в день. Дозировка может меняться или выбираться в зависимости от веса конкретного пациента. Типичная доза может составлять от примерно 0,01 до 100 мг/кг, при этом предпочтительной формой единичной дозы являются таблетки и капсулы. Приведенные ниже примеры даны лишь с целью иллюстрации и не ограничивают объем данного изобретения. Ниже приведено описание материалов и способов, используемых в примерах.a. Материалы. Растворители и иные реагенты приобретались у коммерческих поставщиков и имели маркировкуi. Приблизительная растворимость - метод добавления растворителя. Навеску обрабатывали аликвотами испытательного раствора при комнатной температуре. Полное растворение испытуемого материала определяли визуальным осмотром. Растворимость подсчитывали на основании полного количества растворителя, использованного для полного растворения. Фактическая растворимость может быть выше расчетной величины вследствие применения слишком больших аликвот растворителя или в силу низкой скорости растворения. Растворимость выражают как "меньше чем", если в ходе эксперимента не было достигнуто растворение. Если растворение произошло после введения одной аликвоты, растворимость выражают как "больше чем".ii. Полиморфный скрининг. Применяли как термодинамическую, так и кинетическую кристаллизацию. Ниже приведено подробное описание этих методик. После отбора твердых образцов от проб кристаллизации их либо исследовали на морфологию под микроскопом, либо рассматривали невооруженным глазом. Отмечалась любая кристаллическая форма, но иногда твердое тело имело неизвестную морфологию из-за малого размера частиц. Далее твердые образцы анализировали методом порошковой рентгенодифракции, при этом спектры сравнивали друг с другом для определения новых кристаллических или некристаллических форм.(i) Холодное осаждение (СР). Растворы приготовляли в различных растворителях при повышенной температуре. Растворы далее фильтровали через нейлоновый фильтр 0,2 мкм или через фильтр из ПТФЭ в антирастворитель при температуре ниже комнатной. Отмечали наличие или отсутствие твердого вещества. При отсутствии твердого вещества или в случае, когда количество вещества было слишком мало для порошковой рентгенодифракции, склянку ставили в морозильник. Полученное твердое вещество выделяли фильтрованием и высушивали перед проведением анализа.(ii) Быстрое испарение (FE). Растворы приготовляли в различных растворителях и обрабатывали ультразвуком для улучшения растворения в промежутках между введением аликвот. После полного растворения смеси по результатам визуального наблюдения раствор фильтровали через нейлоновый фильтр 0,2 мкм. Отфильтрованный раствор оставляли для испарения при комнатной температуре в незакрытой склянке. Образовавшиеся твердые частицы выделяли и анализировали.(iii) Лиофилизация (FD). Растворы приготовляли в 1,4-диоксане, фильтровали через нейлоновый фильтр 0,2 мкм и замораживали на сухом льду. Замороженный образец лиофилизировали с помощью аппарата Flexi-Dry компании FTSsystems. Температуру лиофилизации не регулировали.(iv) Тонкое измельчение. Измельчение материалов можно производить в струйных мельницах с получением частиц размером от 1 до 20 мкм. Подробно этот процесс описан в литературе: Perry's Chemical Engineers' Handbook, 7th ed.(v) Помол. Твердый образец помещали в ротор мельницы из нержавеющей стали с мелкими металлическими шариками. В некоторые образцы добавляли немного воды (мокрый помол). Образец перемалывали при 30 Гц в мельнице типа Retesh MM220 Mixermill приблизительно в течение 20 мин. Полученные твердые частицы выделяли и анализировали.(vi) Низкотемпературный помол. Твердый образец помещали в чашу стержневой мельницы из нержавеющей стали. Далее образец перемалывали при 15 Гц в криогенной мельнице SPEX Certiprep, Модель 6750 в течение заданного времени. В ходе помола чаша мельницы была погружена в ванну с жидким азотом. Твердые частицы выделяли и анализировали. Твердый образец помещали на предметное стекло и разравнивали. Предметное стекло помещали на горячую пластину с определенной температурой до расплавления твердого образца. После расплавления предметное стекло снимали с горячей пластины и помещали на холодную столешницу для быстрого охлаждения. Полученное твердое вещество высушивали под струей азота и анализировали.(viii) Ротационное испарение. Растворы приготовляли в различных растворителях и фильтровали через нейлоновый фильтр 0,2 мкм. Образец помещали в ротационный испаритель и после высушивания снимали. Полученные твердые частицы выделяли и анализировали.(ix) Медленное испарение (SE). Растворы приготовляли в различных растворителях и обрабатывали ультразвуком для улучшения растворения в промежутках между введением аликвот. После полного растворения смеси по результатам визуального наблюдения раствор фильтровали через нейлоновый фильтр 0,2 мкм. Отфильтрованный раствор оставляли для испарения при комнатной температуре или под струей азота в склянке, покрытой алюминиевой фольгой, перфорированной булавочными уколами. Полученные твердые частицы выделяли и анализировали.(х) Медленное охлаждение (SC). Приготовляли насыщенные растворы в различных растворителях приблизительно при 60 С и фильтровали в теплом состоянии через нейлоновый фильтр 0,2 мкм в открытую склянку. Склянку далее покрывали и оставляли для медленного охлаждения до комнатной температуры. Отмечали наличие или отсутствие твердого вещества. Если твердых частиц не было или в случае, когда количество твердых частиц было слишком мало для порошковой рентгенодифракции, склянку помещали в холодильник. Затем снова отмечали наличие или отсутствие твердых частиц и, если их не было, склянку помещали в морозильник. Полученные твердые частицы выделяли фильтрованием и оставляли для высушивания перед анализом.(xi) Эксперименты с суспензиями. Приготовляли растворы, вводя достаточно твердого вещества в растворитель до получения избытка твердых частиц. Далее смесь перемешивали в укупоренной склянке при комнатной температуре. Через 7 или 10 дней твердые частицы выделяли фильтрованием в вакууме и анализировали.(xii) Эксперименты при различных воздействиях. Твердые вещества подвергали воздействию при разных температурах и(или) значениях относительной влажности среды в течение определенного времени. Конкретные величины относительной влажности получали, помещая образцы в герметизированные камеры с насыщенным раствором соли или в климатические камеры ESPEC. Соляные растворы выбирали и приготовляли по стандартной методикеASTM (Американское общество по испытаниям материалов). Образцы анализировали порошковой рентгенодифракцией немедленно после извлечения из среды, в которой осуществляли воздействие.(i) Приготовление образцов. Готовили насыщенный раствор CDDO-Me в метаноле при 60 С и фильтровали через фильтр 0,2 мкм в теплом состоянии в открытую склянку. Склянку закрывали и оставляли для охлаждения до комнатной температуры. Через 1 день наблюдали наличие пирамидальных плиток.(ii) Сбор данных. Бесцветную пластинку CDDO-Me (C32H43NO4) с приблизительными размерами сторон 0,010,01 мм помещали на стекловолокно с произвольной ориентацией. Предварительное исследование и сбор данных проводили с облучением Мо, линия K ( = 0,71073 ) в дифрактометре Nonius KappaCCD с кристаллом графита - монохроматором падающего луча. Уточнения производили с помощью программы SHELX97(Sheldrick, 1997) [1] на ПК с ОС LINUX. Константны ячеек и матрицу ориентации для сбора данных получали путем уточнения методом наименьших квадратов с углами настройки 46742 отражений в пределах 222. Уточненная блочность по DENZO/SCALEPACK [2] составляла 0,32, указывая на хорошее качество кристаллов. Пространственную группу определяли с помощью программы XPREP [3]. На основании систематического выполнения следующих условий: h00 h-2n, 00l l=4n, а также на основании последующего уточнения методом наименьших квадратов была определена пространственная группа Р 43212 ( 96). Данные собирали до максимальной величины 2, равной 44,43 при температуре 150 1 К.(iii) Предварительная обработка данных. Кадры интегрировали по программе DENZO-SMN [2]. Собрали всего 46742 отражения, из которых уникальными были 9168. В данные вводили корректировки по Лоренцу и методом поляризации. Линейный коэффициент поглощения для облучения Mo K составил 0,074 мм-1. Была принята эмпирическая корректировка поглощения посредством программы SCALEPACK [2]. Коэффициент пропускания составлял от 0,9995 до 0,9999. Интенсивности эквивалентных отражений осредняли. Коэффициент сходимости при осреднении по интенсивности составил 9,3%. Строение определяли прямым способом с помощью программы SHELXS97 [1]. Положение остальных атомов определяли методом синтеза Фурье последовательных разностей. В уточнение включали атомы водорода, но не переходили на атом, с которым они связаны. Строение уточняли методом наименьших квадратов по плотной матрице, находя минимум функции Масса w определяется выражением 1/[2(FO2) + (0,0176 Р)2 + (0,0000 Р)], где Р = (Fo2 +2Fc2)/3. Коэффициенты рассеяния взяты из "International Tables for Crystallography" [5]. Из 9168 отражений,использованных при уточнении, в расчете R использованы только отражения с Fo22(Fo2). В расчете использовали всего 5421 отражение. В окончательный цикл уточнения вошли 1024 переменных параметра (наибольшее изменение параметра составило 0,01 его расчетного стандартного отклонения) при невзвешенных и взвешенных коэффициентах сходимости Стандартное отклонение наблюденной элементарной массы составляло 1,05. Наибольший пик по методу конечных разностей с преобразованием Фурье составил 0,22 е/3. Минимальный отрицательный пик имел высоту -0,25 е/3.(v) Расчетная картина порошковой рентгенодифракции (XRPD). Расчетная картина порошковой рентгенодифракции получена для излучения Cu по программе PowderCell 2.3 [6], при этом получены координаты атомов, пространственная группа и параметры элементарной ячейки по данным монокристалла.(vi) Схемы ORTEP и упаковки. Схему ORTEP получали с помощью программы ORTEP III [7][9]. Атомы представлены эллипсоидами анизотропных тепловых колебаний с вероятностью 50%. Схемы упаковки получали с помощью программы моделирования CAMERON [8]. Дополнительные данные и морфологические предсказания BFDH получали с помощью программы Mercury 1.4.1 [4]. с. Методика работы с приборами.i. Дифференциальная сканирующая калориметрия (DSC). Анализы проводили с помощью дифференциального сканирующего калориметра фирмы ТА Instruments модели 2920 или Q1000. Прибор калибровали с использованием индия в качестве эталона. Образец помещали в стандартную алюминиевую чашу для дифференциальной сканирующей калориметрии с загибаемой крышкой и записывали точную массу. Кювету с образцом доводили до равновесного состояния при 25 С и нагревали с продувкой азотом со скоростью 10 С/мин до конечной температуры 250 С.ii. Динамическая сорбция/десорбция паров (DVS). Данные по сорбции и десорбции влаги получали с помощью анализатора сорбции паров VTI SGA100. Данные по сорбции и десорбции получены в диапазоне относительной влажности 5-95% с шагом 10% относительной влажности с продувкой азотом. Образцы перед анализом не высушивали. Критерии равновесного состояния для анализа составляли менее 0,010% изменения массы за 5 мин, при этом максимальное время установления равновесного состояния при невыполнении критерия по массе составляло 3 ч. Данные не корректировали по первоначальной влажности образцов. В качестве калибровочных эталонов использовали хлорид натрия и поливинилпирролидон.iii. Метод Карла Фишера (КФ). Кулонометрический анализ по методу Карла Фишера (КФ) для определения воды проводили с помощью титратора по Карлу Фишеру фирмы Mettler Toledo, модель DL39. Навеску приблизительно 24-32 мг помещали в титровальный стакан прибора для метода КФ, содержащий состав Hydranal - CoulomatAD. Далее навеску титровали с помощью электрода генератора, образующего иод электрохимическим окислением: 2I-I2 + 2 е. Для воспроизводимости получали три результата.iv. Высокотемпературная микроскопия. Высокотемпературную микроскопию проводили с помощью горячей ступени Linkam (модель FTIR 600), смонтированной на микроскопе Leica DM LP. Образцы наблюдали через объектив 20 (obj.) с кросс-поляризаторами (СР) и компенсатором лямбды . Образцы помещали на покровное стекло. Далее на образец помещали второе покровное стекло. Каждый образец наблюдали визуально во время нагревания ступени. Изображения получали с помощью цветной цифровой камеры SPOT Insight с программным обеспечением SPOT Software v. 4.5.9. Горячую ступень тарировали, используя эталоны точки плавления USP.v. Дифференциальная сканирующая калориметрия с модулированной температурой (MDSC). Данные дифференциальной сканирующей калориметрии с модулированной температурой получали с помощью дифференциального сканирующего калориметра фирмы ТА Instruments, оборудованного холодильной системой охлаждения (RCS). Образец помещали в алюминиевую чашу дифференциального сканирующего калориметра и записывали точную массу. Далее чашу закрывали крышкой и загибали края. Данные калориметрии получали с амплитудой модулирования 0,8 С с периодом 60 с при скорости нагрева 2 С/мин от -25 до 250 С. Температуру и теплоемкость калибровали с помощью, соответственно,металлического индия и сапфира, используемых в качестве эталонов. Зарегистрированная температура стеклования получена в точке перегиба при скачкообразном изменении при обратном потоке теплоты на температурной кривой.vi. Ядерный магнитный резонанс (ЯМР). Спектры фазы раствора 1 Н ЯМР получали в компании Spectra Data Services, Inc. На каждом спектре проставлены параметры испытания. Спектры привязаны к внутреннему стандарту - тетраметилсилану при 0,0 ч/млн.vii. Оптическая микроскопия. Наблюдения посредством оптической микроскопии проводили на поляризационном оптическом микроскопе Wolfe с увеличением 4. Для наблюдения двойного лучепреломления образцов использовали кросс-поляризаторы (СР).viii. Сканирующая электронная микроскопия (SEM). Сканирующую электронную микроскопию (SEM) проводили с помощью сканирующего электронного микроскопа FEI Quanta 200. В режиме глубокого вакуума использовали транзисторный детектор обратного рассеивания (Etd). Напряжение пучка составляло 5,0 кВ. Образцы подвергали вакуумному напылению аппаратом вакуумного напыления Cressington 108auto Sputter Coater при токе 20 мА и давлении 0,13 мбар (Ar) с материалом покрытия Au/Pd в течение 75 с. Образцы готовили для анализа, помещая небольшую навеску на углеродную ленту с двусторонним липким покрытием, прикрепляемую к алюминиевому держателю образца. Прибор калибровали на увеличение по стандартам NIST (Национальный институт стандартов и технологий США). Данные получали с помощью xTm (v. 2.01), партия 1564, и анализировали с помощью XT Docu (v. 3.2). Зарегистрированные для изображений сканирующей электронной микроскопии увеличения рассчитывали после первоначального снятия данных. Масштабный столбик, приводимый в нижней части каждого изображения, является точным после изменения размера изображений, при этом его следует использовать при определении размеров.ix. Термогравиметрия (TG). Анализы выполняли с помощью термогравиметрического анализатора модели 2950 фирмы ТА Instruments. Эталоны для градуировки - никель и Alumel. Каждый образец помещали в алюминиевую чашу и устанавливали в термогравиметрическую печь. Образцы сначала доводили до равновесного состояния при 25 С, а затем при отсутствии иных указаний нагревали под струей азота со скоростью нагрева 10 С/мин до конечной температуры 350 С. х. Порошковая рентгенодифракция (XRPD).(i) Inel XRG-3000. Анализы методом порошковой рентгенодифракции проводили с помощью дифрактометра InelXRG-3000, оборудованного криволинейным позиционно-чувствительным детектором с диапазоном 2120. Данные в реальном времени получали с использованием облучения Cu K при разрешении 0,032. Напряжение и ток трубки настраивали, соответственно, на 40 кВ и 30 мА. Рентгенограммы отображали в области от 2,5 до 402 для обеспечения непосредственного сравнения изображений. Образцы готовили для анализа, упаковывая их в тонкостенные стеклянные капилляры. Каждый капилляр устанавливали на угломерную головку с приводом с целью вращения капилляра во время снятия данных. Прибор калибровали с использованием кремния в качестве эталона.i. Функция распределения пар (PDF). Одной из методик, используемых при вычислительном анализе рентгеноаморфных данных, является функция распределения пар (PDF). Как говорит название, функция распределения пар состоит из линейной суммы всех когерентных межатомных взаимодействий в материале. Дефектные (разупорядоченные) материалы будут иметь такие же межатомные взаимодействия, как кристаллическая фаза, но на меньшей длине. Поэтому такие материалы можно сравнивать с исходным кристаллическим материалом путем рассмотрения пиков в функции распределения пар на нескольких первых нанометрах. Сравнения спектров в пределах от 0 до примерно 5 затруднены ввиду наличия в зоне посторонних объектов. При формировании стекловидного материала пики функции распределения пар будут иметь некоторое смещение из положений кристаллического пика по мере релаксации положения молекул. Это явление аналогично тепловому расширению-сжатию, при котором даже в случае слабого смещения пиков функции распределения пар относительные величины пиков будут все еще распознаваемыми как относящиеся к кристаллическому материалу. По мере перехода материала в термодинамически аморфное состояние некоторые отношения в симметрии группы точек будут теряться, выдавая менее сложную функцию распределения пар. При этом также будет иметь место некоторое движение пиков. Стекловид- 11023550 ные/аморфные материалы будут иметь функцию распределения пар, быстро падающую до нуля на 2-3 ближайших соседних расстояниях (NN). Для расчета функции распределения пар по данным измерения рентгенодифракции используют условия измерений для минимизации фоновых рентгеновских изображений и применяют алгоритмы. Функции распределения пар рассчитывали по программе PatternMatch v2.2.1 с использованием всего диапазона данных измерений для всех образцов. Пример 1. Расчеты растворимости. Приблизительные величины растворимости определяли в различных растворителях при комнатной температуре; результаты расчетов приведены в табл. 2. Вещество CDDO-Me показывает высокую растворимость в большинстве использованных органических растворителей. Растворимость в воде оказалась менее 0,1 мг/мл. Пример 2. Результаты полиморфного скрининга. Проведено приблизительно 50 испытаний полиморфного скрининга. Форму А наблюдали приблизительно в 50% образцов. Образование формы А не было ограничено конкретными условиями кристаллизации при приготовлении в самых различных экспериментах и в разных растворителях. Материал формы В был приготовлен в экспериментах с лиофилизацией, при плавлении с быстрым охлаждением и в нескольких экспериментах с испарением. Образцы полиморфного скрининга приведены в табл. 3-5 по использованному растворителю. Представительные порошковые рентгенограммы для материалов формы А и формы В сравниваются на фиг. 2. Данные, характеризующие эти формы, сведены в приведенные ниже примеры. Пример 3. Описание CDDO-Me - форма А (немелкодисперсная). Форма А - несольватированная (табл. 6). Строение монокристалла формы А определено с помощью описанных выше методов. Кристаллы CDDO-Me выращивали и подвергали анализу на строение монокристалла. Строение кристалла определяли по рентгенодифракции монокристалла. Предлагаемое строение CDDO-Me представлено на фиг. 1. Параметры тетрагональной ячейки и расчетный объем: а = 14,21620(10) , b = 14,21620(10) , с = 81,5875(12) , = 90,00,= 90,00, = 90,00, V = 16488,9(3) 3. Молекулярная масса CDDO-Me составляет 505,70 г/мол при Z = 24, что дает расчетную плотность 1,222 г/см-3. Определена пространственная группа: P43212 ( 96). Сводка данных по кристаллу и параметров снятия кристаллографических данных приведена в табл. 10. Полученное строение имеет высокое качество, на что указывает величина R, равная 0,051 (5,1%). Обычно наиболее достоверные строения характеризуются величинами R в пределах 0,02-0,06. Чертеж ORTEP одной молекулы CDDO-Me представлен на фиг. 12. Асимметричное образование,показанное на фиг. 13, содержит три молекулы CDDO-Me. Эти молекулы такие же, как предлагаемое строение согласно фиг. 1. Схемы упаковки по кристаллографическим осям а, b и с представлены, соответственно, на фиг. 14-16. При отсутствии водородных связей строение кристалла имеет множество взаимодействий Ван-дер-Ваальса. На виде по кристаллографической оси b (фиг. 15) показан спиральный характер упаковки винтовой тетрагональной оси, а также предсказываемая морфология BFDH. Предсказываемая морфология хорошо согласуется с наблюдаемыми видами монокристалла при снятии данных. Расчетная картина порошковой рентгенодифракции CDDO-Me, полученная на основании данных по монокристаллу, приведена на фиг. 17. Экспериментальная картина порошковой рентгенодифракции CDDOMe представлена на фиг. 18. В табл. 17 приведены характеристические пики картины порошковой рентгенодифракции формы А. Сравнение расчетной и экспериментальной картин порошковой рентгенодифракции (фиг. 19) показывает, что все пики экспериментальной картины воспроизведены на расчетной картине порошковой рентгенодифракции, указывая на вероятную однофазность насыпного материала. Небольшой устойчивый сдвиг местоположения пиков, вероятно, вызван тем, что экспериментальная порошковая картина была получена при комнатной температуре, а данные по монокристаллу - при 150 К. При анализе монокристаллов используют низкие температуры для улучшения качества строения. Итак, строение монокристалла CDDO-Me формы А определено для подтверждения предлагаемого молекулярного строения. Пространственная группа определена как Р 43212 ( 96). Структура CDDO-Me состоит из трех спирально упакованных по кристаллографической оси b молекул. Все пики в экспериментальных картинах представлены на расчетной картине порошковой рентгенодифракции, указывая на то, насыпной материал, вероятно, является однофазным. Данные термического анализа для формы А приведены на фиг. 3. Кривая дифференциальной сканирующей калориметрии (DSC) показывает сдвиг базы приблизительно при 157 С и эндотерму при начальной температуре приблизительно 222 С (пик сигнала при 224 С). Событие при 224 С подтверждено расплавом при высокотемпературной микроскопии (фиг. 4). Кривая термогравиметрии (TG) показывает ничтожную потерю массы - 1,2% в диапазоне от 150 до 210 С. Данные по Карлу Фишеру показывают, что материал содержит приблизительно 0,38% остаточной воды, что соответствует первоначальной потере массы по термогравиметрии. Данные динамической сорбции/десорбции паров (DVS), показывают, что форма А не является гигроскопичной (фиг. 5). Материал показывает ничтожную потерю массы в ходе эксперимента. Получен- 12023550 ный материал подвергали порошковой рентгенодифракции, показавшей форму А. Изображения сканирующей электронной микроскопии (SEM) показаны на фиг. 6. Наблюдаются несколько видов, в том числе, пирамидальный, плиточный и пластинчатый. Физическую стойкость формы А исследовали в разных условиях (табл. 7). Образцы подвергали стрессу в течение 7 дней либо при 25 С с относительной влажностью 60%, либо при 40 С с относительной влажностью 75%, при этом наблюдали ничтожное изменение веса (соответственно, потерю 0,6% и привес 0,2%), что говорит об отсутствии гигроскопичности формы А. Два образца перемалывали в шаровой мельнице в течение приблизительно 20 мин: один сухой, а другой с небольшим количеством воды. Все образцы снова подвергали порошковой рентгенодифракции, при этом они оставались формой А. Образец подвергали стрессу при 195 С в течение 15 мин, приведшему к потере массы 2%. Порошковая рентгенодифракция полученного материала аналогична результатам для формы А, однако было очевидно увеличение базового шума (фиг. 7). ЯМР-спектр растворов показан на фиг. 8. Этот спектр соответствует строению CDDO-Me. Пики приблизительно при 1,6 и 7,3 ч./млн относятся, соответственно, к воде и хлороформу (ввиду обмена). Форма А не сольватирована и не гигроскопична, поэтому она плавится приблизительно при 228 С на основании наблюдений аналитика в ходе высокотемпературной микроскопии. Пример 4. Описание CDDO-Me - форма А (мелкодисперсная). Мелкодисперсная форма A CDDO-Me определена как форма А порошковой рентгенодифракцией(фиг. 2, табл. 1). Мелкодисперсный материал можно получить по обычной методике, хорошо известной в данной области техники, например использованием воздушной струйной мельницы. Эти данные показывают, что дисперсность не влияет на форму А в плане изменения картины порошковой рентгенодифракции. Пример 5. Описание CDDO-Me - форма В. Материал формы В можно приготовить лиофилизацией, плавлением/быстрым охлаждением и несколькими другими методами испарения, как показано в табл. 3. Данные дифференциальной сканирующей калориметрии (DSC) (дифференциальной сканирующей калориметрии с модулированной температурой -MDSC) приведены на фиг. 9. Обратимая кривая показывает температуру стеклования (Tg), примерно равную 125 С. Необратимая кривая показывает экзотерму с минимумом сигнала при 195 С и эндотерму с пиком сигнала при 223 С. Необратимые события, наиболее вероятно, вызваны кристаллизацией материала формы В (экзотерма), за которой следует расплав кристаллизованного материала (эндотерма). Физическую стабильность материала формы В исследовали в разных условиях (табл. 9). Образцы подвергали воздействию при 22 С с относительной влажностью 97%, 40 С с относительной влажностью 75%, 80 С с относительной влажностью 0% и 195 С при относительной влажности окружающей среды,при этом они оставались формой В. При воздействии на материал при 200 С с относительной влажностью окружающей среды в течение 60 мин получали форму А с небольшим количеством материала формы В (фиг. 10). ЯМР-спектр растворов показан на фиг. 11. Этот спектр соответствует строению CDDO-Me. Пики приблизительно при 1,6, 5,3 и 7,3 ч./млн относятся, соответственно, к воде, дихлорметану и хлороформу. Форма В не гигроскопична и кристаллизуется в форму А приблизительно при 200 С, при этом она имеет температуру стеклования (Tg), приблизительно равную 125-130 С. Таким образом, форма В не гигроскопична. Данные дифференциальной сканирующей калориметрии с модулированной температурой (MDSC) показывают, что температура стеклования (Tg) формы В составляет приблизительно 125-130 С. Материал формы В кристаллизуется в форму А при воздействии приблизительно при 200 С. Пример 6. Исследования стойкости формы В CDDO-Me и дисперсий CDDO-Me в полимерных эксципиентах.(i) Исследования очищенной формы В. Форму В CDDO-Me подвергали воздействию в различных условиях. В табл. 15 представлены некоторые результаты этих исследований. Форма В CDDO-Me, полученная в рамках полезного, но менее предпочтительного варианта осуществления данного изобретения, при котором в качестве растворителя используют этилацетат, показывает значительную стабильность. Тем не менее, при испытаниях образцов формы В в присутствии этилацетата выявлено образование формы А через 28 дней хранения при температуре 60 С и выше. Напротив, все образцы, полученные согласно предпочтительному варианту данного изобретения, иллюстрируемому приведенным ниже примером 11, сохраняли свойства аморфности после испытания воздействием в особо жестких условиях (см. табл. 15). Эти исследования показывают неожиданную стойкость материала формы В, в особенности при его приготовлении согласно указанному выше предпочтительному варианту осуществления. Кроме того, приготовленные в различных условиях образцы формы В анализировали на предмет наличия у них аналогичных химических свойств. Иными словами, как описано выше, образцы формы В приготовляли криогенным помолом, быстрым охлаждением расплава и сушкой распылением. Кроме того, немелкодисперсную форму В измельчали до получения мелкодисперсной формы В. На образцах про- 13023550 водили анализ функции распределения пар (PDF) (фиг. 28), при этом они были определены как стекловидные.(ii) Исследования с приготовлением дисперсий CDDO-Me. Проводили исследования для сравнения эффективности различных твердых дисперсий формы В в полимерах, полученных сушкой распылением. Исследуемые свойства продукта включали стойкость и профиль растворимости лекарства. Использовали разные полимеры при трех отношениях активного фармацевтического ингредиента (API) к полимеру (20:80; 40:60 и 60:40 мас.%). Были выбраны три следующих полимера: сополимер метакриловой кислоты с этилакрилатом (1:1); коповидон [сополимер 1-винил-2-пирролидона с винилацетатом (3:2)]; гидроксипропилметилцеллюлозы фталат. Растворы CDDO-Me - виде кристаллического материала формы А или материала формы В - и выбранный для исследования полимер растворяли в подходящем растворителе при соответствующем массовом отношении, обычно имея в виду получить 10-20 мас.% твердого вещества в растворе. Обычно в качестве растворителя применяли ацетон. Полученные растворы подвергали сушке распылением с помощью лабораторной распылительной сушильной установки (BCHI, модель В-290), имеющей сопла для двух сред, с использованием азота в качестве газа для осушки и в качестве газа-носителя. Обычно температура газа-носителя на входе составляла 65-85 С, а температура на выходе была 50-60 С. Твердые частицы собирали, при этом полученный сушкой распылением порошок подвергали дополнительной сушке в вакууме для дальнейшего снижения содержания органических растворителей. Полученные сушкой распылением порошки анализировали на остаточное содержание органических растворителей, измеряли температуру стеклования (Tg) и объемную плотность. После дополнительной сушки порошки анализировали на чистоту, содержание воды, средний размер частиц, отсутствие кристаллического материала методом порошковой рентгенодифракции (XRPD), а также снимали кривую растворимости. Физико-химические свойства дисперсий оценивали после кратковременного воздействия (через 5 дней, 40 С/ относительная влажность 75%) методом порошковой рентгенодифракции и дифференциальной сканирующей калориметрии с модулированной температурой (MDSC). Эти исследования показали, что температура стеклования Tg снижалась при кратковременном тепловом воздействии, возможно, вследствие набора влаги в ходе испытания. Это снижение было более выраженным в составах с низкими отношениями CDDO-Me к полимеру. В образцах до кратковременного воздействия наблюдали один-два эндотермических перехода при повышенных температурах, хотя эти температуры были несколько ниже наблюдавшихся первоначально. Энтальпия в связи с этими переходами снижалась по мере уменьшения содержания полимера. Это указывает на то, что такой переход,наиболее вероятно, связан с полимером, а не с плавлением кристаллической формы. В действительности,для дисперсий, приготовленных с ПВП/ВА, температура такого эндотермического перехода была аналогична температуре, наблюдаемой для чистого эксципиента в полученном от изготовителя состоянии. В каждом случае профиль порошковой рентгенодифракции после воздействия оставался в виде характеристической картины ореола, сцентрированной относительно 13,52, при этом не было обнаружено ни одного пика, связанного с кристаллической формой. Далее были проведены исследования сушки распылением на двух составах с реальным оборудованием для сушки распылением. В этих испытаниях использовали пилотную установку для сушки распылением Niro, модель PSD-1 (Mobile Minor 2000). При этом применяли равноценные сопла и условия сушки, описанные выше. В табл. 20 и 21 приведены растворы, приготовляемые для сушки распылением и характеристики растворов после сушки распылением. Эти составы имели пониженную температуру стеклования Tg в сравнении с чистой формой В, так как эти составы включали полимеры с величиной Tg ниже, чем у формы В. Пример 7. Введение CDDO-Me: форма В в сравнении с формой А у обезьян Cynomolgus. На этапе 1 данного исследования приготовляли партию твердых желатиновых капсул, содержащих чистую мелкодисперсную форму A CDDO-Me или чистую мелкодисперсную форму В CDDO-Me (i) введением соответствующей навески чистой формы лекарственного вещества в твердую желатиновую капсулу размера 1 и (ii) укупоркой капсулы. Не применяли никаких дополнительных эксципиентов. Обезьянам Cynomolgus CDDO-Me вводили перорально в виде либо формы В, либо формы А в желатиновой капсуле (доза = 4,1 мг/кг во всех случаях). Введение CDDO-Me в виде формы В вызывало у обезьян среднее воздействие, которое было приблизительно на 520% сильнее, чем от эквивалентной дозы CDDO-Me в виде формы А. В табл. 11 приведено сравнение воздействия лекарственного средства на отдельных животных. Это было перекрестное исследование с целью увеличения величины "n" и повышения достоверности данных. В ходе перекрестного исследования проводили вымывание в течение 1 недели. На фиг. 20 показаны во времени концентрации, полученные в плазме для двух форм CDDO-Me в популяции выборки. На фиг. 21 представлены сравнительные концентрации CDDO-Me в плазме животных 505 М и 507F. На фиг. 22 показаны сравнительные концентрации CDDO-Me в плазме животных 508F и 502 М. Для дальнейшей оценки сравнительной биодоступности пероральных лекарственных форм CDDOMe, в том числе, тех, которые содержали дисперсии CDDO-Ме в эксципиенте, были проведены дополни- 14023550 тельно два этапа исследования 2 и 3, как описано ниже. Эти исследования проводили с некоторыми из дисперсий формы В CDDO-Me в полимерах, как описано в примере 6. Все составы содержали обычные добавки. Этап 2. Готовили водную взвесь нанокристаллического CDDO-Me на основе образца мелкодисперсной формы А материала. В шаровую мельницу Retsch Planatory Ball Mill модели РМ 400 с циркониевыми шариками среднего размера 2 мм загружали 25 гм (грамм массы) мелкодисперсного CDDO-Me (гранулометрический состав со средним размером частиц 6,1 мкм), 5 гм докузата натрия, 1 гм Tween 80 и 68,3 гм воды. Помол начинали приблизительно с 400 об/мин и продолжали 2 ч. Определение гранулометрического состава (PSD) с помощью лазерного гранулометра показало средний размер частиц гранулометрии 0,37 мкм. К густой суспензии добавляли 1 гм микрокристаллической целлюлозы и 0,2 гм ксантамовой смолы при кратковременном перемешивании, после чего суспензию хранили в холодильнике. После помола наносуспензии ее наносили распылением на сухую смесь эксципиента в лабораторном аппарате с псевдоожиженным слоем Aeromatic Strea 1 с верхним расположением распылителя, имеющего распылительное сопло размером 0,4 мм. Температура на входе составляла 55 С. Температура на выхлопе в ходе распыления составляла 32-35 С. Полученный сыпучий материал сушили в течение приблизительно 5 мин до получения температуры выхлопа 38 С (приложение 3-5). Ниже приведен состав материалов с покрытием. Теоретический состав нанокристаллического препарата с 30 мг CDDO-Me Полученная сухая сыпучая смесь проходила анализ методом высокоточной жидкостной хроматографии для аналитического определения активного ингредиента. Анализ показал 14,4 мас.% (масса/масса), что значительно выше теоретической величины (5,7%). На основании результата высокоэффективной жидкостной хроматографии капсулы наполняли таким образом, чтобы получить содержание нетто CDDO-Me, равное 30 мг. Составы мелкодисперсной кристаллической формы А и мелкодисперсной аморфной формы В получали по обычной технологии компаундирования сухих порошков, используя в качестве добавок микрокристаллическую целлюлозу, прежелатинизированный крахмал, кросповидон (выступающий в качестве дезинтегранта), коллоидную двуокись кремния и пищевой стеарат магния. Мелкодисперсную форму А CDDO-Me со средним размером частиц (PSD) 6,1 мкм использовали в составе формы А, а мелкодисперсную форму В CDDO-Me со средним размером частиц (PSD) 10,8 мкм использовали в соответствующем составе формы В CDDO-Me. В приведенной ниже таблице дается количественное содержание компонентов в обоих составах. Количественный состав капсул 30 мг формы А и формы В Каждый из 15 самцов обезьян Cynomolgus (macaca fascicularis) получил перорально одну дозуCDDO-Me (3 разных состава - по 5 обезьян в случае каждого состава) с индивидуальным уровнем дозы 10 мг/кг. Обезьяны были в возрасте 1-3 года и весили по 2,5-3,5 кг. Кровь на анализ отбирали в течение до 72 ч после введения. Этап 3. Дисперсии CDDO-Me в эксципиентах, описанных в примере 6, использовали в составах, приготовленных обычным компаундированием сухих порошков с использованием в качестве добавок микрокристаллической целлюлозы, моногидрата лактозы, кросповидона (выступающего в качестве дезинтегранта) и лаурилсульфата натрия. Ниже приведено количественное содержание компонентов в каждом составе. Состав дисперсий CDDO-Me в эксципиенте, компаундированных с добавками в капсулах После достаточного периода выведения (7-10 дней) каждому из тех же самых 15 самцов обезьянCynomolgus, использованных на этапе 2, ввели перорально разовую дозу CDDO-Me (3 разных состава по 5 обезьян в случае каждого состава) с индивидуальным уровнем дозы 10 мг/кг. Кровь на анализ отбирали в течение до 72 ч после введения. Сводка по каждому этапу исследования приведена ниже в таблице. Ниже приведены средние дозы внутривенного и перорального введения, полученные самцами обезьян Cynomolgus, и средние концентрации CDDO-Me. ПО - пероральное введение капсулы. Для доставки составов на этапе 2 использовали желатиновую капсулу размера 2, а для доставки составов на этапе 3 использовали желатиновую капсулу размера 1. Содержание нетто лекарственного препарата в каждой капсуле составляло 30 мг, что соответствовало дозировке лекарственного препарата 10 мг/кг, исходя из допущения, что вес каждой обезьяны составлял 3 кг. Капсулу прикрепляли к желудочному зонду и отделяли от наконечника зонда под давлением воздуха из пустого шприца. После ведения последней капсулы давали небольшое количество воды (приблизительно 10 мл). Последовательный отбор крови (приблизительно по 1 мл) производили из бедренной вены (или артерии) животного и переносили в пробирки, содержащие K2-ЭДТА каждый раз в следующие моменты времени (фактическое время регистрировали): Этап 2. Перед введением, 1, 2, 4, 8, 16, 24, 48 и 72 ч после введения. Этап 3. Перед введением, 1, 2, 4, 8, 16, 24, 48 и 72 ч после введения. Все образцы тщательно перемешивали после отбора и помещали на влажный лед перед помещением в холодильник для хранения приблизительно при 4 С. Концентрации CDDO-Me в крови анализировали высокоэффективной жидкостной хроматографией с масс-спектроскопическим обнаружением (HPLCMS/MS). Результаты приведены в табл. 22 и на фиг. 30. На этапе 2 форма В показала существенно более высокую биодоступность в сравнении с двумя испытанными составами формы А. Результаты этапа 3 показывают, что каждый состав на основе дисперсии CDDO-Me в полимере имел гораздо более высокую биодоступность в сравнении с составами мелкодисперсной формы А или нанокристаллической формы А. Составы с сополимером метакриловой кислоты типа С и с ГПМЦ-Ф показали более высокую биодоступность у подопытных обезьян. Пример 8. Описание формы гемибензольного сольвата CDDO-Me. Проводили различные эксперименты, воспроизводящие последний этап восстановления из синтезаCDDO-Me. Honda и др., 2000. Задача заключалась в выделении кристаллического материала из раствора смеси бензола с ацетоном (10:1). Приблизительно 100 мг CDDO-Me растворяли в 300 мкл смеси бензола с ацетоном (10:1) и фильтровали через нейлоновый фильтр 0,2 мкм. Далее раствор обрабатывали ультразвуком с помощью ультразвукового аппарата в течение 10 мин и оставляли на ночь в открытой склянке для испарения при комнатной температуре. Получали прозрачный гель и приливали 100 мкл смеси бензола с ацетоном (10:1). Раствор обрабатывали ультразвуком с помощью ультразвукового аппарата в течение приблизительно 30 мин. Получали белый осадок. Твердое вещество сушили на воздухе. В других экспериментах растворяли приблизительно 200 мг CDDO-Me в 0,8 мл смеси бензола с ацетоном (10:1) и фильтровали через нейлоновый фильтр 0,2 мкм. Далее раствор делили поровну в две склянки емкостью 1 драхма (3,888 г). Образцы А и В оставляли для быстрого испарения в течение нескольких часов при комнатной температуре. Образец А закрывали крышкой и помещали в морозильник. После замерзания образца его ставили на оттаивание при комнатной температуре. На образце делали небольшой соскоб ланцетом и оставляли для испарения при комнатной температуре. Получали белые твердые частицы, которые оставляли для высушивания на воздухе. Образец В закрывали крышкой, оставляли при комнатной температуре и получали прозрачный раствор после пребывания в течение ночи при комнатной температуре. На образце делали небольшой соскоб ланцетом и оставляли для испарения при комнатной температуре. Получали белые твердые частицы, которые оставляли для высушивания на воздухе. В нескольких таких экспериментах был получен кристаллический материал, определенный как гемибензольный сольват. Как указано выше, небольшие нарушения, такие как ультразвуковая обработка или простой соскоб в емкости для выделения вещества способствовало кристаллизации бензольного сольвата (табл. 12). Данные, характеризующие гемибензольный сольват, сведены в табл. 13. Характеристические пики картины порошковой рентгенодифракции гемибензольного сольвата приведены в табл. 19. Кривая дифференциальной сканирующей калориметрии имеет широкую эндотерму около 133 С, связанную с потерей массы 7,0% в термографе TG (фиг. 23). Потеря массы, вероятно, вызвана улетучиванием бензола (см. приведенное выше описание ЯМР), при этом она соответствует наличию 0,5 моль бензола на каждый моль CDDO-Me. Эндотерма дифференциальной сканирующей калориметрии, наблюдаемая около 223 С, наиболее вероятно, вызвана плавлением десольватированного материала. Эти данные отличают ранее выделенные формы от предлагаемого CDDO-Me. Пример 9. Описание новой формы CDDO-Me - диметанолата. Диметаноловый сольват CDDO-Me готовили по следующей методике. Приблизительно 500 мг CDDO-Me растворяли в 20 мл метанола при 60 С. Далее раствор медленно приливали к 20 мл холодного метанола при -10 С с перемешиванием. Отбирали белые твердые частицы фильтрацией в вакууме и хранили в морозильнике. Данные по свойствам приведены в табл. 14. В табл. 18 приведены характеристические пики картины порошковой рентгенодифракции. Кривая дифференциальной сканирующей калориметрии имеет широкую эндотерму около 102 С,связанную с потерей массы 11% в термографе TG (фиг. 24). Данные термогравиметрического анализа с одновременным снятием ИК-спектра (TGIR) подтверждают потерю массы из-за улетучивания 2,0 моль метанола (фиг. 25). Полученный в эксперименте термогравиметрического анализа с одновременным снятием ИК-спектра материал выделяли, при этом он оказался аморфным по результатам порошковой рентгенодифракции (фиг. 26). На кривой дифференциальной сканирующей калориметрии сдвиг базы приходится приблизительно на 130 С, при этом за широкой экзотермой около 203 С следует резкая эндотерма(начало при 223 С). Эти события, наиболее вероятно, указывают на наличие температуры стеклования Tg аморфного материала (форма В), полученного десольватацией диметанолового сольвата с последующей кристаллизацией аморфного материала в форму А и плавлением этого кристаллического материала. Был снят ЯМР-спектр протонов раствора. Определение химической структуры не проводили, однако представляется, что она соответствует строению CDDO-Me. Пики при 3,51 ч./млн отнесены к метанолу и соответствуют 1,7 моль. Этот результат согласуется с приведенными выше тепловыми данными. Пример 10. Клинические исследования CDDO-Me. Состав на основе мелкодисперсной формы A CDDO-Me был выбран для клинической разработки и сначала исследовался на этапе I на безопасность на пациентах с развитым раком, которые не отвечали в достаточной степени на ранее проводимое лечение. На этапе I испытания, проводимого с увеличением дозы, препарат CDDO-Me, давали 21 взрослому пациенту с разными формами развитого (метастатического) рака. Пациентам давали дневные дозы капсул CDDO-Me в дозировках в пределах от 5 до 900 мг/день (более конкретно 5, 10, 20, 40, 80, 150, 300, 600 или 900 мг/день). Прием CDDO-Me проводили"циклами", которые повторяли до тех пор, пока у пациента не возникала недопустимая токсичность или не проявлялись признаки развития болезни. В этом исследовании один цикл приема CDDO-Me состоял из 21 дня приема подряд с последующим 7-дневным перерывом, после чего пациент мог начинать новый цикл. Рассматривали и безопасность, и противоопухолевое действие CDDO-Me. Кроме того, изучали биологические воздействия CDDO-Me. Эти пациенты очень хорошо переносили CDDO-Me, при этом не было отмечено неблагоприятных событий, связанных с лекарственным препаратом. У нескольких пациентов (приблизительно 75% поддающихся оценке пациентов) болезнь считалась стабильной (на основании стандартных радиологических и клинических критериев) в первый момент оценки после завершения второго цикла лечения. Пациентов, которые имели признаки развития болезни до завершения второго цикла, не проходили формальную оценку и не включались в группу поддающихся оценке пациентов. Пять пациентов, в том числе, пациенты с меланомой и с раком клеток почечного эпителия продолжали показывать стабилизацию болезни, при этом некоторые имели признаки регрессии отдельных опухолевых повреждений тканей после четырех циклов лечения. Четыре пациента рассматривались как случаи стабилизации болезни после не менее шести циклов лечения. Ни у одного из пациентов, получавших дозу не менее 40 мг CDDO-Me в день по прописанной схеме, не развивались новые метастазы. На основании известных противовоспалительных свойств CDDO-Me у пациентов на этапе 1 оценивали циркулирующие воспалительные цитокины. Даже при таких низких дозах, как 5 мг/день, наблюдалось снижение содержания нескольких циркулирующих воспалительных цитокинов и хемокинов, в том числе ММР-9, TNF, IL-8 и VEGF. В частности, содержание TNF, известного своей существенной ролью в воспалительном процессе таких заболеваний, как ревматоидный артрит, значительно понижалось до порога обнаружения и ниже у 3 пациентов с повышенным базовым содержанием TNF (по одному пациенту с дозами для каждого, соответственно, 10, 20 и 40 мг в день). В отличие от моноклональных антител к TNF, которые прикрепляются к мишеням и инактивируют их, CDDO-Me снижает продуцирование TNF и, соответственно, содержание циркулирующего TNF. Кроме того, контролировали в мононуклеарных клетках периферийной крови пациентов на этапе 1 исследования генные продукты фазы 2, включающие антиоксидант и ферменты детоксикации. При дозах 10 мг/день и выше наблюдали существенную индукцию NQO1 (NAD(Р)Н:хинон-оксидоредуктазы) маркера транскрипционной активности фазы 2. Данные биопсии опухолей у нескольких пациентов, проведенной после двух циклов леченияCDDO-Me, показали выраженное снижение содержания циклооксигеназы-2 (СОХ-2), индуцируемой синтазы оксида азота (iNOS) и фосфорилированного STAT3 (pSTAT3) в опухолевой ткани. Известно, что высокие уровни экспрессии каждого из этих белков коррелируют с развитием опухолей и плохими клиническими результатами. Данные биопсии опухолей у нескольких пациентов также указывают на выраженную степень гибели опухолевых клеток после двух циклов лечения CDDO-Me. Содержание сыворо- 18023550 точного креатинина существенно снижалось на 21-й день в сравнении с базовым уровнем перед лечением у более 80% пациентов в исследовании. Ряд пациентов, продолжавших лечение в течение повторных циклов, показывал постоянное снижение содержания сывороточного креатинина. Так как сывороточный креатинин является широко применяемым индикатором почечной функции, эти результаты показывают,что лечение CDDO-Me улучшает почечную функцию. Эти исследования предоставляют данные по страдающим раком пациентам-людям, свидетельствующие о полезном воздействии CDDO-Me на раковых пациентов. Эти данные также показывают, чтоCDDO-Me, вероятно, оказывает положительное клиническое воздействие на пациентов, страдающих другими воспалительными заболеваниями, в том числе дисфункцией почек. Пример 11. Крупномасштабное приготовление формы В с применением диметанолового сольвата в качестве полуфабриката. Один килограмм формы A CDDO-Me растворяли в метаноле при 605 С до полного растворения. Полученный горячий раствор CDDO-Me приливали в сосуд, содержащий холодный метанол при -5 С до-15 С, перемешивая и поддерживая температуру от -5 до -15 С в ходе всего введения. Полученную суспензию кристаллического диметанолового сольвата CDDO-Me фильтровали. Полученные твердые частицы, которые давали картину порошковой рентгенодифракции, соответствующую представленной на фиг. 26 (до термогравиметрического анализа с одновременным снятием ИК-спектра (TGIR, высушивали в печи при температуре 705 С. Высушивание продолжали до тех пор, пока профиль порошковой рентгенодифракции переставал показывать отражения, характерные для кристаллического вещества. Полученные рентгеноаморфные твердые частицы CDDO-Me проходили просеивание и упаковку. Выход продукта составлял 65-95%. Пример 12. Формы А и В, полученные низкотемпературным помолом. Форма А была подвергнута низкотемпературному помолу и анализу. Данные рентгеновского измерения образца, полученного низкотемпературным помолом (2 ч), показали некоторое расширение пика примерно при 13,52. Анализ функции распределения пар для формы А, полученной низкотемпературным помолом, показал результаты, аналогичные анализу для формы В. Эти результаты дают основания полагать, что форма А, полученная низкотемпературным помолом, представляет собой стекловидный материал и что низкотемпературный помол может служить альтернативным способом приготовления формы В. Форма В была подвергнута низкотемпературному помолу и анализу. Данные рентгеновского измерения образца, полученного низкотемпературным помолом (1 ч) были аналогичны данным для исходного материала формы В. Эти результаты показали, что форма В является стабильной и не переходит в другую форму в результате низкотемпературного помола. Таблица 1. Сведения об образцах Таблица 2. Приблизительные значения растворимости CDDO-Me Значения растворимости рассчитывают на основании полного количества растворителя, использованного для растворения, при этом фактическая растворимость может быть выше изза объема вводимых порций растворителя и медленного растворения. Растворимость округляют до ближайшего значения в мг/мл. Таблица 6. Данные свойств формы А Все температуры - в С. Результаты основаны на полученных изображениях. Таблица 7. Исследования стресса формы А Таблица 8. Данные по свойствам формы В CDDO-Me Таблица 9. Исследования стресса формы В CDDO-MeRH = относительная влажность, Tg = температура стеклования. Измеренная влажность лабораторной среды - 74% RH. Таблица 10. Данные кристаллов и параметры снятия данных для формы А Таблица 11. Сводка по зоне под кривой концентрации в плазме (AUC) в зависимости от времени для всех исследованных животных (n=8) Исследование состава CDDO-Me - исходное соединение Таблица 12. Эксперименты по кристаллизации CDDO-MeRE = ротационное испарение, FE = быстрое испарение. Таблица 13. Свойства гемибензольного сольвата CDDO-Me Таблица 14. Свойства диметанолового сольвата CDDO-Me Таблица 15. Исследования стресса мелкодисперсной формы В CDDO-Me Таблица 16. Противораковое действие одиночного препарата CDDO-MeRH = относительная влажность. Фактическая величина была отрицательной. с(Marcel Dekker, 2002), pages 203-06. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Безводный кристаллический метиловый эфир 2-циано-3,12-диоксоолеана-1,9(11)-диен-28-овой кислоты (метиловый эфир CDDO), характеризующийся тем, что его порошковая рентгеновская дифрактограмма содержит пики при 8,78 2, 12,94 2, 13,35 2, 14,18 2 и 17,4 20,2 2 по данным, полученным на дифрактометре с облучением Cu K. 2. Метиловый эфир CDDO по п.1, отличающийся тем, что порошковая рентгеновская дифрактограмма, по существу, такая, как показано на фиг. 18. 3. Метиловый эфир CDDO по п.1, дополнительно характеризующийся тем, что его кривая дифференциальной сканирующей калориметрии содержит сдвиг базовой линии приблизительно при 157 С и максимум на эндотерме примерно при 224 С. 4. Метиловый эфир CDDO по п.3, отличающийся тем, что кривая дифференциальной сканирующей калориметрии, по существу, такая, как показано на фиг. 3. 5. Фармацевтическая композиция для лечения хронического воспалительного состояния, содержащая терапевтически эффективное количество метилового эфира CDDO по п.1 и один или более твердых фармацевтически приемлемых носителей. 6. Фармацевтическая композиция по п.5, отличающаяся тем, что метиловый эфир CDDO является микронизированным, а указанные твердые фармацевтически приемлемые носители представляют собой съедобные носители. 7. Применение метилового эфира CDDO по п.1 для получения лекарственного средства для лечения хронического воспалительного состояния у субъекта, страдающего указанным состоянием. 8. Кристаллический гемибензольный сольват метилового эфира CDDO, характеризующийся тем,что его порошковая рентгеновская дифрактограмма содержит пики при 9,25 2, 14,17 2, 14,62 2 16,32 2 и 17,11 2 0,2 2 по данным, полученным на дифрактометре с облучением Cu K. 9. Кристаллический гемибензольный сольват метилового эфира CDDO по п.8, дополнительно характеризующийся тем, что его кривая дифференциальной сканирующей калориметрии, по существу, такая, как показано на фиг. 23. Фиг. 2 Порошковая рентгенодифракция формы А (вверху) и формы В (внизу) Сверху вниз: немелкодисперсная форма А (2 А), мелкодисперсная форма А (2 В) и форма В (2 С) Фиг. 3 Кривые дифференциальной сканирующей калориметрии и термогравиметрии CDDO-Me Фиг. 4 Высокотемпературная микроскопия формы А - немелкодисперсной Фиг. 4 (продолжение) Высокотемпературная микроскопия формы А - немелкодисперсной Фиг. 5 Изотерма динамической сорбции паров формы А - немелкодисперсной Фиг. 6 Изображения сканирующей электронной микроскопии формы А - немелкодисперсной Фиг. 6 (продолжение) Изображения сканирующей электронной микроскопии формы А - немелкодисперсной
МПК / Метки
МПК: A61K 31/277, A61P 29/00, C07C 255/47, A61P 35/00
Метки: cddo-me, метилового, эфира, 2-циано-3,12-диоксоолеан-1,9(11)-диен-28-овой, формы, кислоты, новые
Код ссылки
<a href="https://eas.patents.su/30-23550-novye-formy-metilovogo-efira-2-ciano-312-dioksoolean-1911-dien-28-ovojj-kisloty-cddo-me.html" rel="bookmark" title="База патентов Евразийского Союза">Новые формы метилового эфира 2-циано-3,12-диоксоолеан-1,9(11)-диен-28-овой кислоты (cddo-me)</a>
Предыдущий патент: Топливный элемент топливной сборки легководного ядерного реактора
Следующий патент: Аппликатор для лекарственного средства и способ его изготовления
Случайный патент: Способ промышленного получения диалкилкарбоната и диола