Производные пирандионов и циклогексатрионов в качестве гербицидов
Номер патента: 20695
Опубликовано: 30.01.2015
Авторы: Ковенкар Мангала, Смит Стивен Кристофер, Жанмарт Стефан-Андре-Мари, Тейлор Джон Бенджамин, Матьюз Кристофер Джон
Формула / Реферат
1. Соединения формулы I
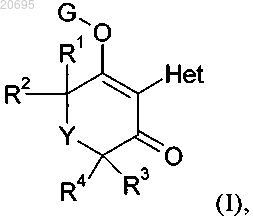
в которой R1, R2, R3 и R4 независимо друг от друга обозначают водород, метил или этил; или
R1 и R3 объединены с образованием 5-7-членного насыщенного или ненасыщенного кольца или 5-7-членного насыщенного или ненасыщенного кольца, замещенного С1алкилом; и R2 и R4 независимо друг от друга обозначают водород, метил или этил;
Y обозначает О или С=О; при условии, что, если Y обозначает С=О, то R3 и R4 не обозначают водород, если или R1, или R2 обозначают водород и R1 и R2 не обозначают водород, если или R3, или R4 обозначают водород; и
Het обозначает группу формулы R1, или R2, или R3
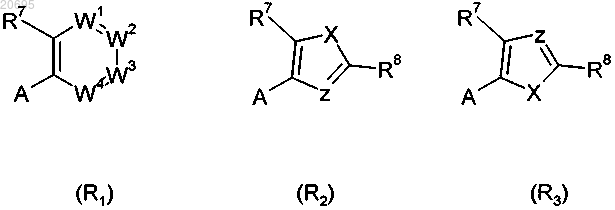
в которых А обозначает положение присоединения кетоенольного фрагмента, и
W1 обозначает CR10;
W2 обозначает N;
W3 обозначает CR8;
W4 обозначает N;
X обозначает О, S или Se;
Z обозначает N или CR14;
R7 обозначает галоген, С1-С4-алкил или С1галогеналкил и
R8 обозначает С1-С4-алкил, который является незамещенным или содержит в качестве заместителей галоген, С2-С4-алкенил, который является незамещенным или содержит в качестве заместителей галоген, или
R8 обозначает тиенил, фурил, изоксазолил, изотиазолил, тиазолил, пиразолил, пиридил или пиримидинил, или их соли, каждый из этих заместителей является незамещенным или содержит в качестве заместителей галоген, С1алкил, галоген-С1алкил, С1алкоксигруппу, С1алкилтиогруппу, С1алкилсульфинил, С1алкилсульфонил или галоген-С1алкоксигруппу, цианогруппу или нитрогруппу;
R10 обозначает водород или метил и
R14 обозначает водород, метил, фтор, хлор или бром; или
Het обозначает группу формулы R2a
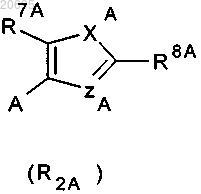
в которой А обозначает положение присоединения кетоенольного фрагмента, и
ХА обозначает серу;
R7A обозначает метил или этил;
R8A обозначает фенил или фенил, замещенный от 1 до 3 заместителями, выбранными из группы, включающей галоген, C1-C2-алкил, C1-C2-алкоксигруппу, С1-С2-галогеналкил, C1-C2-галогеналкоксигруппу, цианогруппу или нитрогруппу; и
Za обозначает азот или С-Н; и
G обозначает водород, катион щелочного металла, катион щелочно-земельного металла или маскирующую группу, в которой, когда G обозначает маскирующую группу, тогда G обозначает C(Xa)-Ra, где Ха обозначает кислород или серу; и где Ra обозначает C1-C18-алкил, С3-С7-циклоалкил-С1-С5-алкил, C3-C8-циклоалкил; или фенил или фенил, содержащий в качестве заместителей C1-C3-алкил, C1-C3-галогеналкил, C1-C3-алкоксигруппу, C1-C3-галогеналкоксигруппу, галоген, цианогруппу или нитрогруппу.
2. Соединения по п.1, в которых R1, R2, R3 и R4 независимо друг от друга обозначают водород, метил или этил.
3. Соединения по п.2, в которых R1, R2, R3 и R4 обозначают метил.
4. Соединения по п.1, в которых R1 и R3 объединены с образованием 5-7-членного насыщенного или ненасыщенного кольца или 5-7-членного насыщенного или ненасыщенного кольца, замещенного С1алкилом, и в которых R2 и R4 независимо друг от друга обозначают водород, метил или этил.
5. Соединения по п.1, в которых G обозначает водород, щелочной металл или щелочно-земельный металл.
6. Соединения по п.1, в которых G обозначает водород.
7. Соединения по любому из пп.1-6, в которых Het обозначает группу формулы R2, где X обозначает серу, R8 обозначает тиенил, фурил, изотиазолил, тиазолил или пиридил, их соли, каждый из которых необязательно замещен от 1 до 3 заместителями, выбранными из группы, включающей галоген, С1алкил, С1алкоксигруппу, С1галогеналкил, С1галогеналкоксигруппу, цианогруппу или нитрогруппу, и Z обозначает азот или С-Н.
8. Соединения по любому из пп.1-6, в которых Het обозначает группу формулы R2A, в которых ХА обозначает серу, R7A обозначает метил или этил, R8A обозначает фенил или фенил, замещенный от 1 до 3 заместителями, выбранными из группы, включающей галоген, C1-C2-алкил, C1-C2-алкоксигруппу, C1-C2-галогеналкил, C1-C2-галогеналкоксигруппу, цианогруппу или нитрогруппу, и Za обозначает азот или С-Н.
9. Способ борьбы с травянистыми растениями и сорняками в культурах полезных растений, который включает нанесение гербицидно эффективного количества соединения формулы I по любому из пп.1-8 или композиции, содержащей такое соединение, на растения или место их произрастания.
10. Гербицидная композиция, которая в дополнение к вспомогательным веществам для приготовления композиций содержит гербицидно эффективное количество соединения формулы I по любому из пп.1-8.
11. Композиция по п.10, которая в дополнение к соединению формулы I содержит дополнительный гербицид в качестве компонента для смешивания.
12. Композиция по п.10, которая в дополнение к соединению формулы I содержит антидот.
13. Композиция по п.10, которая в дополнение к соединению формулы I содержит дополнительный гербицид в качестве компонента для смешивания и антидот.
Текст
В заявке описаны пирандионы, тиопирандионы и циклогексантрионы формулы (I), которые пригодны для применения в качестве гербицидов. Жанмарт Стефан-Андре-Мари (CH),Матьюз Кристофер Джон, Смит Стивен Кристофер, Тейлор Джон Бенджамин (GB), Ковенкар Мангала Настоящее изобретение относится к новым гербицидно активным циклическим дионам и их производным, к способам их получения, к композициям, содержащим эти соединения, и к их применению для борьбы с сорняками, в особенности в культурах полезных растений, таких как рис, кукуруза, злаки,хлопчатник, соя, сахарная свекла, масличный рапс или канола, сахарный тростник, или для подавления роста растения. Циклические дионы, обладающие гербицидной активностью, описаны, например, в WO 01/74770. Согласно изобретению обнаружены новые пирандионы, тиопирандионы и циклогексантрионы, обладающие гербицидной активностью и способностью подавлять рост. В соответствии с этим настоящее изобретение относится к соединениям формулы I в которой R1, R2, R3 и R4 независимо друг от друга обозначают водород, метил или этил; илиR1 и R3 объединены с образованием 5-7-членного насыщенного или ненасыщенного кольца или 5-7 членного насыщенного или ненасыщенного кольца, замещенного С 1 алкилом; и R2 и R4 независимо друг от друга обозначают водород, метил или этил;Het обозначает группу формулы R1, или R2, или R3 в которых А обозначает положение присоединения кетоенольного фрагмента, иR8 обозначает С 1-С 4-алкил, который является незамещенным или содержит в качестве заместителей галоген, С 2-С 4-алкенил, который является незамещенным или содержит в качестве заместителей галоген,илиR8 обозначает тиенил, фурил, изоксазолил, изотиазолил, тиазолил, пиразолил, пиридил или пиримидинил, или их соли, каждый из этих заместителей является незамещенным или содержит в качестве заместителей галоген, алкил, галоген-С 1 алкил, С 1 алкоксигруппу, С 1 алкилтиогруппу, С 1 алкилсульфинил,С 1 алкилсульфонил или галоген-С 1 алкоксигруппу, цианогруппу или нитрогруппу; R10 обозначает водород или метил; и R14 обозначает водород, метил, фтор, хлор или бром; илиHet обозначает группу формулы R2A в которой А обозначает положение присоединения кетоенольного фрагмента, и ХА обозначает серу;R7A обозначает метил или этил;R8A обозначает фенил или фенил, замещенный от 1 до 3 заместителями, выбранными из группы, включающей галоген, C1-C2-алкил, C1-C2-алкоксигруппу, C1-C2-галогеналкил, C1-C2-галогеналкоксигруппу, цианогруппу или нитрогруппу; иZA обозначает азот или С-Н; иG обозначает водород, катион щелочного металла, катион щелочно-земельного металла или маскирующую группу, в которой, когда G обозначает маскирующую группу, тогда G обозначает C(Xa)-Ra, где Ха обозначает кислород или серу; и где Ra обозначает C1-C18-алкил, С 3-С 7-циклоалкил-С 1-С 5-алкил, C3C8-циклоалкил; или фенил или фенил, содержащий в качестве заместителей C1-C3-алкил, C1-C3 галогеналкил, C1-C3-алкоксигруппу, C1-C3-галогеналкоксигруппу, галоген, цианогруппу или нитрогруппу. В определениях заместителей соединений формулы I алкильные заместители и алкильные фрагменты алкоксигруппы, алкиламиногруппы и т.п., содержащие от 1 до 6 атомов углерода, предпочтительно представляют собой метил, этил, пропил, бутил, пентил или гексил, а также их линейные и разветвленные изомеры. Алкенильные и алкинильные радикалы, содержащие от 2 до 6 атомов углерода, а также до 10 атомов углерода, могут быть линейными или разветвленными и могут содержать более 1 двойной или тройной связи. Примерами являются винил, аллил, пропаргил, бутенил, бутинил, пентенил и пентинил. Подходящие циклоалкильные группы содержат от 3 до 7 атомов углерода и представляют собой, например, циклопропил, циклобутил, циклопентил, циклогексил или циклогептил. Циклопропил, циклобутил, циклопентил и циклогексил являются предпочтительными. Гетероциклы, как правило, соответствуют карбоциклам или циклоалкильным радикалам, указанным выше, за исключением того, что одна или две метиленовые группы заменены атомом кислорода, серы или азота, который также может быть замещенным. Предпочтительными галогенами являются фтор, хлор и бром. Предпочтительными примерами гетероарилов R1, R2, R3, R4, R8 и R12 являются тиенил, фурил, пирролил, изоксазолил, оксазолил, изотиазолил, тиазолил, пиразолил, имидазолил, триазолил,тетразолил, пиридил, пиримидинил, пиразинил, триазинил, оксадиазолил, тиадиазолил и пиридазинил и, если это является подходящим, их N-оксиды и соли. Эти гетероарилы могут содержать один или большее количество заместителей и предпочтительные заместители включают, например, галоген, С 1-С 4-алкил, C3-C6 циклоалкил, С 1-С 4-галогеналкил, С 2-С 4-алкенил, С 2-С 4-галогеналкенил, C2-C4-алкинил, С 1-С 4-алкоксигруппу,С 1-С 4-галогеналкоксигруппу, С 1-С 4-алкилтиогруппу, С 1-С 4-алкилсульфинил, С 1-С 4-алкилсульфонил, С 1-С 4 галогеналкилтиогруппу, С 1-С 4-галогеналкилсульфинил, C1-C4-галогеналкилсульфонил, поли-C1-C4-алкоксиС 1-С 4-алкил, С 1-С 4-алкилтио-С 1-С 4-алкил, нитрогруппу, цианогруппу, С 2-С 4-алкенил, С 2-С 4-галогеналкенил,C2-C4-алкинил, арил, арил, содержащий в качестве заместителей C1-C2-алкил, C1-C2-алкоксигруппу, C1-C2 галогеналкил, C1-C2-галогеналкоксигруппу, цианогруппу или нитрогруппу, или гетероарил или гетероарил,содержащий в качестве заместителей C1-C2-алкил, С 1-С 2-алкоксигруппу, C1-C2-галогеналкил, C1-С 2 галогеналкоксигруппу, цианогруппу или нитрогруппу. Группа G представляет собой водород, катион щелочного металла, катион щелочно-земельного металла или маскирующую группу. Эта маскирующая группа G выбрана так, чтобы ее можно было удалить с помощью одной или комбинации биохимических, химических или физических методик и образовать соединения формулы I, в которой G обозначает Н, до, во время или после нанесения на обрабатываемый участок или растения. Примеры этих методик включают ферментативное расщепление, химический гидролиз и фотолиз. Соединения, содержащие маскирующие группы G, могут обеспечивать определенные преимущества, такие как улучшенное проникновение в кутикулы обрабатываемых растений, улучшенная переносимость культурами, улучшенная совместимость или стабильность в приготовленных смесях, содержащих другие гербициды, антидоты гербицидов, регуляторы роста растений, фунгициды или инсектициды, или уменьшенное вымывание из почвы. Предпочтительно, если G обозначает водород, щелочной металл и щелочно-земельный металл, где водород является особенно предпочтительным. В предпочтительной группе соединений формулы I R1, R2, R3 и R4 независимо друг от друга обозначают водород, метил или этил, наиболее предпочтительно - метил. В другой предпочтительной группе соединений формулы I R1 и R3 объединены с образованием 5-7 членного насыщенного или ненасыщенного кольца или 5-7-членного насыщенного или ненасыщенного кольца, содержащего в качестве заместителей С 1 алкил, и где R2 и R4 независимо друг от друга обозначают водород, метил или этил. Предпочтительно, если Het обозначает группу формулы R2, в которой X обозначает серу, R8 обозначает тиенил, фурил, изотиазолил, тиазолил или пиридил, их соли, каждый из которых необязательно замещен от 1 до 3 заместителями, выбранными из группы, включающей галоген, С 1 алкил,С 1 алкоксигруппу, С 1 галогеналкил, С 1 галогеналкоксигруппу, цианогруппу или нитрогруппу, и Z обозначает азот или С-Н. Более предпочтительно, если Het обозначает группу формулы R2A, в которых ХА обозначает серу,7AR обозначает метил или этил, R8A обозначает фенил или фенил, замещенный от 1 до 3 заместителями,выбранными из группы, включающей галоген, С 1-С 2-алкил, C1-C2-алкоксигруппу, С 1-C2-галогеналкил,C1-C2-галогеналкоксигруппу, цианогруппу или нитрогруппу, и ZA обозначает азот или С-Н. Настоящее изобретение также относится к солям, которые соединения формулы I могут образовать с аминами, основаниями щелочных металлов и щелочно-земельных металлов или с четвертичными аммониевыми основаниями. Из являющихся солеобразователями гидроксидов щелочных металлов и щелочно-земельных металлов следует особо отметить гидроксиды лития, натрия, калия, магния и кальция, но предпочтительно гидроксиды натрия и калия. Соединения формулы I, предлагаемые в настоящем изобретении, также включают гидраты, которые могут образоваться при получении солей. Примеры аминов, пригодных для образования солей аммония, включают аммиак, а также первичные,вторичные и третичные C1-C18-алкиламины, С 1-С 4-гидроксиалкиламины и С 2-С 4-алкоксиалкиламины, например, метиламин, этиламин, н-пропиламин, изопропиламин, четыре изомера бутиламина, н-амиламин, изоамиламин, гексиламин, гептиламин, октиламин, нониламин, дециламин, пентадециламин, гексадециламин, гептадециламин, октадециламин, метилэтиламин, метилизопропиламин, метилгексиламин, метилнониламин, метилпентадециламин, метилоктадециламин, этилбутиламин, этилгептиламин, этилоктиламин, гексилгептиламин, гексилоктиламин, диметиламин, диэтиламин, ди-н-пропиламин, диизопропиламин, ди-н-бутиламин, дин-амиламин, диизоамиламин, дигексиламин, дигептиламин, диоктиламин, этаноламин, н-пропаноламин, изопропаноламин, N,N-диэтаноламин, N-этилпропаноламин, N-бутилэтаноламин, аллиламин, н-бут-2-ениламин,н-пент-2-ениламин, 2,3-диметилбут-2-ениламин, дибут-2-ениламин, н-гекс-2-ениламин, пропилендиамин,триметиламин, триэтиламин, три-н-пропиламин, триизопропиламин, три-н-бутиламин, триизобутиламин,три-втор-бутиламин, три-н-амиламин, метоксиэтиламин и этоксиэтиламин; гетероциклические амины, например, пиридин, хинолин, изохинолин, морфолин, пиперидин, пирролидин, индолин, хинуклидин и азепин; первичные ариламины, например, анилины, метоксианилины, этоксианилины, о-, м- и п-толуидины, фенилендиамины, бензидины, нафтиламины и о-, м- и п-хлоранилины; но предпочтительно - триэтиламин, изопропиламин и диизопропиламин. Предпочтительные четвертичные аммониевые основания, применимые для образования солей, соответствуют, например, формуле [N(RaRbRcRd)]OH, в которой Ra, Rb, Rc и Rd все независимо от других обозначают С 1-С 4-алкил. Другие подходящие тетраалкиламмониевые основания с другими анионами можно получить, например, с помощью анионообменных реакций. В зависимости от природы заместителей G, R1, R2, R3, R4, R5, R6, R7 и R8 соединения формулы I могут существовать в различных изомерных формах. Если G обозначает, например, водород, то соединения формулы I могут существовать в различных таутомерных формах. В объем настоящего изобретения входят все такие таутомеры и их смеси во всех соотношениях. Кроме того, если заместители содержат двойные связи, то могут существовать цис- и транс-изомеры. Эти изомеры также входят в объем заявленных соединений формулы I. Соединение формулы I, в которой G обозначает C(Xa)-Ra, где Ха, Ra являются такими, как определено выше, можно получить путем обработки соединения формулы (А), которое представляет собой соединение формулы I, в которой G обозначает Н, реагентом G-Z, где G-Z является алкилирующим реагентом, таким как алкилгалогенид (определение алкилгалогенидов включает простые C1-C8 алкилгалогениды, такие как метилйодид и этилйодид, замещенные алкилгалогениды, такие как фенилС 1-С 8-алкилгалогениды, хлорметилалкиловые простые эфиры, Cl-CH2-Xf-Rh, где Xf обозначает кислород,и хлорметилалкилсульфиды Cl-CH2-Xf-Rh, где Xf обозначает серу), C1-C8-алкилсульфонат или ди-C1-С 8 алкилсульфат, или C3-C8-алкенилгалогенид, или С 3-С 8-алкинилгалогенид, или ацилирующим реагентом,таким как карбоновая кислота, HO-C(Xa)Ra, где Ха обозначает кислород, хлорангидрид кислоты, ClC(Xa)Ra, где Ха обозначает кислород, или ангидрид кислоты, [Рац(Ха)]2 О, где Ха обозначает кислород,или изоцианат, RcN=C=O, или карбамоилхлорид, Cl-C(Xd)-N(Rc)-Rd (где Xd обозначает кислород и при условии, что ни Rc, ни Rd не обозначает водород), или тиокарбамоилхлорид, Cl-C(Xd)-N(Rc)-Rd (где Xd обозначает серу и при условии, что ни Rc, ни Rd не обозначает водород), или хлорформиат, Cl-C(Xb)-XcRb (где Xb и Xc обозначают кислород), или хлортиоформиат Cl-C(Xb)-Xc-Rb (где Xb обозначает кислород и Xc обозначает серу), или хлордитиоформиат Cl-C(Xb)-Xc-Rb (где Xb и Xc обозначают серу), или хлордитиоформиат Cl-C(Xb)-Xc-Rb (где Xb и Xc обозначают серу), или изотиоцианат, RcN=C=S, или путем последовательной обработки дисульфидом углерода и алкилирующим реагентом, или фосфорилирующим реагентом, таким как фосфорилхлорид, Cl-P(Xe)(Rf)-Rg, или сульфонилирующим реагентом, таким как сульфонилхлорид Cl-SO2-Re, предпочтительно - в присутствии по меньшей мере одного эквивалента основания. Если заместители R1 и R2 отличаются от заместителей R3 и R4, то эти реакции в дополнение к соединению формулы I могут привести к образованию второго соединения формулы IA. Таким образом,в объем настоящего изобретения входят и соединение формулы I, и соединение формулы IA вместе со смесями этих соединений в любом соотношении.US 4436666. Альтернативные методики описаны (см. публикации М. Pizzorno and S. Albonico, Chem. Ind. О-Ацилирование циклических 1,3-дионов можно провести по методикам, аналогичным описанным(см., например, публикации R. Haines, US 4175135, и Т. Wheeler, US 4422870, US 4659372 и US 4436666). Типичные дионы формулы (А) можно обработать ацилирующим реагентом, предпочтительно в присутствии по меньшей мере одного эквивалента подходящего основания, и необязательно в присутствии подходящего растворителя. Основание может быть неорганическим, таким как карбонат или гидроксид щелочного металла, или гидрид металла, или органическим основанием, таким как третичный амин или алкоксид металла. Примеры подходящих неорганических оснований включают карбонат натрия, гидроксид натрия или калия, гидрид натрия, и подходящие органические основания включают триалкиламины, такие как триметиламин и триэтиламин, пиридины или другие амины-основания, такие как 1,4 диазабицикло[2.2.2]октан и 1,8-диазабицикло[5.4.0]ундец-7-ен. Предпочтительные основания включают триэтиламин и пиридин. Подходящие для этой реакции растворители выбирают так, чтобы они были совместимы с реагентами и они включают простые эфиры, такие как тетрагидрофуран и 1,2-диметоксиэтан, и галогенированные растворители, такие как дихлорметан и хлороформ. Некоторые основания, такие как пиридин и триэтиламин, можно успешно использовать в качестве и основания, и растворителя. Для случаев, когда ацилирующим реагентом является карбоновая кислота, ацилирование предпочтительно проводят в присутствии известного реагента сочетания, такого как 2-хлор-1-метилпиридиний йодид, N,N'дициклогексилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид или N,N'-карбодиимидазол, и необязательно в присутствии основания, такого как триэтиламин или пиридин, в подходящем растворителе, таком как тетрагидрофуран, дихлорметан или ацетонитрил. Подходящие методики описаны (см., например, публикации W. Zhang and G. Pugh, Tetrahedron Lett., (1999), 40 (43), 7595-7598 и Т. Isobe and T. Ishikawa, J. Org. Chem., (1999), 64 (19), 6984). Фосфорилирование циклических 1,3-дионов можно провести с использованием фосфорилгалогенида или тиофосфорилгалогенида и основания по методикам, аналогичным описанным в публикации L.Hodakowski, US 4409153. Сульфонилирование соединения формулы (А) можно провести с использованием алкил- или арилсульфонилгалогенида, предпочтительно - в присутствии по меньшей мере одного эквивалента основания,например, по методике, описанной в публикации (С. Kowalski and K. Fields, J. Org. Chem., (1981), 46, 197201). Соединения формулы (А), в которой Y обозначает S(O)m и m равно 1 или 2, можно получить из соединений формулы (А), в которой Y обозначает S, путем окисления по методике, описанной в публикации Е. Fehnel and A. Paul, J. Am. Chem. Soc., (1955), 77, 4241. Соединения формулы (А), в которой Y обозначает О, S или С=О, можно получить циклизацией соединений формулы (В), предпочтительно - в присутствии кислоты или основания, и необязательно в присутствии подходящего растворителя, по методикам, аналогичным описанным в публикациях (Т. Teresawa and Т. Okada, J. Org. Chem., (1977), 42 (7), 1163-1167 и Т. Wheeler, US 4209532). Соединения формулы (В) специально разработаны для использования в качестве промежуточных продуктов при синтезе соединений формулы I. Соединения формулы (В), в которой R обозначает водород, можно циклизовать в кислой среде, предпочтительно - в присутствии сильной кислоты, такой как серная кислота, полифосфорная кислота или реагент Итона, необязательно в присутствии подходящего растворителя, такого как уксусная кислота, толуол или дихлорметан. Соединения формулы (В), в которой R обозначает алкил (предпочтительно метил или этил), можно циклизовать в кислой или предпочтительно щелочной среде, предпочтительно в присутствии по меньшей мере одного эквивалента сильного основания, такого как трет-бутоксид калия, диизопропиламид лития или гидрид натрия, и в растворителе, таком как тетрагидрофуран, диметилсульфоксид или N,Nдиметилформамид. Соединения формулы В являются новыми и специально разработаны для синтеза соединений формулы I, предлагаемых в настоящем изобретении. Соединения формулы (В), в которой R обозначает Н,можно получить путем омыления соединений формулы (С), в которой R' обозначает алкил (предпочтительно метил или этил), при стандартных условиях, с последующим подкислением реакционной смеси для проведения декарбоксилирования по методикам, аналогичным описанным (см., например, публикации Т. Wheeler, US 4209532) Соединения формулы (С), в которой R обозначает Н, можно этерифицировать с образованием соединения формулы (С), в которой R обозначает алкил, при стандартных условиях. Соединения формулы (С), в которой R обозначает алкил, можно получить путем обработки соединений формулы (D) подходящим хлорангидридом карбоновой кислоты формулы (Е) в щелочной среде. Подходящие основания включают трет-бутоксид калия, бис(триметилсилил)амид натрия и диизопропиламид лития и реакцию предпочтительно проводят в подходящем растворителе (таком как тетрагидрофуран или толуол) при температуре, равной от -80 до 30 С Альтернативно, соединение формулы (С), в которой R обозначает Н, можно получить путем обработки соединения формулы (D) подходящим основанием (таким как трет-бутоксид калия,бис(триметилсилил)амид натрия и диизопропиламид лития) в подходящем растворителе (таком как тетрагидрофуран или толуол) при подходящей температуре (от -80 до 30 С) и реакции полученного аниона с подходящим ангидридом формулы (F). Соединения формулы (Е) и формулы (F) являются известными (см., например, Т. Terasawa and Т.Okada, J. Org. Chem., 1977, 42 (7), 1163) или их можно получить по аналогичным методикам из имеющихся в продаже исходных веществ. Соединения формулы (D) являются известными соединениями или их можно получить из известных соединений по известным методикам (см., например, Е. Bellur and P.F. Bohlmann et al., Chem. Ber., (1955), 88, 1831-1838; R. Fischer et al., WO 2003/035463; R. Fischer et al.,WO 2005/005428; D O'Mant, GB1226981). Альтернативно, соединение формулы (В), в которой Y обозначает О или S, можно получить из известного соединения формулы (G), в которой Y обозначает О или S, путем алкилирования соединением формулы (Н), в которой L обозначает отщепляющуюся группу, такую как галоген или алкилсульфонат или арилсульфонат, и предпочтительно один или оба R3 и R4 обозначает водород. Реакцию предпочтительно проводить в присутствии подходящего основания и необязательно в присутствии подходящего растворителя. Основание может быть неорганическим, таким как карбонат или гидроксид щелочного металла, или гидрид металла, или органическим основанием, таким как третичный амин или алкоксид щелочного металла. Примеры подходящих неорганических оснований включают карбонат натрия, карбонат калия,гидроксид лития, гидроксид натрия, гидроксид калия или гидрид натрия, и подходящие примеры орга-5 020695 нических оснований включают амины, такие как триметиламин и триэтиламин, пиперидин, пиридин и 1,4-диазабицикло[2.2.2]октан. При их использовании растворители для проведения этой реакции выбирают так, чтобы они были совместимы с реагентами, и они включают, например, простые эфиры, такие как диэтиловый эфир, 1,2-диметоксиэтан и тетрагидрофуран, алифатические кетоны, такие как метилизобутилкетон и ацетон, алифатические спирты, такие как метанол, этанол и изопропанол, амиды, такие как N,N-диметилформамид, N,N-диметилацетамид и N-метилпирролидон, ароматические углеводороды,такие как толуол и ксилол, ацетонитрил и галогенированные растворители, такие как дихлорметан и хлороформ. Некоторые основания, такие как пиридин и триэтиламин, можно успешно использовать в качестве и основания, и растворителя. Соединения формулы (Н) являются известными соединениями, или их можно получить из известных соединений по известным методикам (см., например, N. Kaila et al., J. Med. Chem. (2007), 50 (1), 4064). Альтернативно, соединение формулы (В), в которой Y обозначает О или S и предпочтительно один или оба R1 и R2 обозначает водород, можно получить из соединения формулы (J) по реакции с известным соединением формулы (K) при условиях, аналогичных использованным для получения соединения формулы (В) из соединения формулы (G). Соединения формулы (J) являются известными соединениями или их можно получить из известных соединений по известным методикам (см., например, N. Kaila et al., J. Med. Chem. (2007), 50 (1), 40-64; E.Reimann, EP 647640; V. Dalla and J. Catteau, Tetrahedron, (1999), 55, 6497-6510). В другой методике получения соединений формулы (В) соединение формулы (В), в которой Y обозначает О или S и R2 обозначает водород, можно получить из соединения формулы (L) и известного диазоэфира формулы (М) с помощью фотохимического или катализируемого металлом включения О-Н и SН по методикам, описанным, например, в публикации (D. Miller and С. Moody, Tetrahedron, (1995), 51,10811-10843). Содержащим металл катализатором предпочтительно является катализатор на основе переходного металла, более предпочтительно катализатор на основе родия(II), такой как ацетат родия(II), или катализатор на основе меди, такой как трифторметансульфонат меди(II) или ацетилацетонат меди(II), и реакцию предпочтительно проводят в растворителе, таком как дихлорметан или толуол. По аналогичным методикам соединение формулы (В), в которой Y обозначает О или S и R4 обозначает водород, также можно получить по реакции диазокетона формулы (N) с известным соединением формулы (О), предпочтительно в присутствии подходящего катализатора и в подходящем растворителе при описанных выше условиях. Соединения формулы (N) являются известными соединениями или можно получить по известным методикам (например, по реакции известного хлорангидрида кислоты формулы (Р) с диазоалканом при условиях, описанных в литературе (см., например, A. Boularot et al., J. Med. Chem., (2007, 50 (1), 10-20;M. Salim and A. Capretta, Tetrahedron (2000); 56, 8063-8069; K. Yong et al., J. Org. Chem., (1998); 63 (26),9828-9833; A. Padwa et al., J. Org. Chem., (1989), 54 (2), 299-308). В другой методике получения соединений формулы (А) соединение формулы (Q), которое представляет собой соединение формулы (А), в которой Het обозначает (R2), где R7 обозначает CH2R" и R" обозначает водород, алкил или галогеналкил (предпочтительно водород, метил или трифторметил), можно получить путем перегруппировки соединения формулы (R), необязательно в присутствии подходящего растворителя и необязательно при облучении микроволновым излучением. Перегруппировку предпочтительно проводить путем нагревания соединения формулы (G) при температурах 120-300 С, необязательно в подходящем растворителе, таком как 1,2-диметоксиэтан, метиловый эфир диэтиленгликоля, ксилол, мезитилен или Dowtherm, и необязательно при облучении микроволновым излучением. Аналогичным образом, соединение формулы (S), которое представляет собой соединение формулы(А), в которой Het обозначает (R3), где R7 обозначает CH2R" и R" обозначает водород, алкил или галогеналкил (предпочтительно водород, метил или трифторметил), можно получить из соединения формулы Соединение формулы (R) можно получить из соединения формулы (U) путем алкилирования соединением формулы (V), в которой L обозначает подходящую отщепляющуюся группу, такую как галоген или алкил- или арилсульфонат, необязательно в присутствии подходящего основания и необязательно в подходящем растворителе, как это описано выше для алкилирования соединений формулы (А). Аналогичным образом, соединение формулы (Т) можно получить из соединения формулы (U) путем алкилирования соединением формулы (W), в которой L обозначает подходящую отщепляющуюся группу, такую как галоген или алкил- или арилсульфонат, при аналогичных условиях. В альтернативном подходе соединение формулы (R) можно получить из соединения формулы (U) путем конденсации со спиртом формулы (X), необязательно в присутствии подходящего кислотного катализатора, такого как п-толуолсульфоновая кислота или кислота Льюиса, например, трифторметансульфонат иттербия(III), трифторметансульфонат лантана(III), дигидрат тетрахлорлаурата(III) натрия,хлорид титана(IV), хлорид индия(III) или хлорид алюминия, и необязательно в подходящем растворителе. Подходящие растворители выбирают так, чтобы они были совместимы с использующимися реагентами и они включают, например, толуол, этанол или ацетонитрил. Аналогичные подходы описаны (см.,например, публикации М. Curini; F. Epifano, S. Genovese, Tetrahedron Lett., (2006), 47, 4697-700; A. Альтернативно, конденсацию можно провести в присутствии подходящих реагентов сочетания, таких как 2-хлор-1-метилпиридиний йодид, N,N'-дициклогексилкарбодиимид, 1-(3-диметиламинопропил)3-этилкарбодиимид и N,N-карбодиимидазол, и подходящего основания, такого как триэтиламин или пиридин, в подходящем растворителе, таком как тетрагидрофуран, ацетонитрил или дихлорметан, или в присутствии триарилфосфина (такого как трифенилфосфин) и диалкилазодикарбоксилата (предпочтительно диэтилазодикарбоксилата или диизопропилазодикарбоксилата) и подходящем растворителе, таком как диэтиловый эфир, тетрагидрофуран или 1,4-диоксан, 5 как это описано, например, в публикации(О. Mitsunobu, Synthesis (1981), 1, 1-28). С помощью аналогичных методик соединение формулы (Т) можно получить по реакции соединения формулы (U) с соединением формулы (Y). Дополнительные соединения формулы (R), в которой R8 обозначает ароматический или гетероароматический фрагмент или обозначает алкильную, алкенильную или алкинильную группу, можно получить по реакции соединения формулы (Z), в которой Q обозначает атом или группу, подходящую для проведения реакции перекрестного сочетания (например, Q обозначает хлор, бром или йод, или галогеналкилсульфонат, такой как трифторметансульфонат), и R" является таким, как определено для соединения формулы (Q), с подходящим реагентом сочетания при условиях, описанных в литературе для реакций Судзуки-Мияура, Соногашира, Стилле и родственных реакций перекрестного сочетания. Например, соединение формулы (Z) можно обработать арил-, гетероарил-, алкил-, алкенил- или алкинилбороновой кислотой, R8-B(OH)2, боронатным сложным эфиром, R8-B(OR"')2 (предпочтительно сложным эфиром, в котором фрагмент -B(OR'")2 представляет собой циклический боронатный сложный эфир, полученный из 1,2- или 1,3-алкандиола, такого как пинакол, 2,2-диметил-1,3-пропандиол и 2 метил-2,4-пентандиол), или арил-, гетероарил, алкил-, алкенил- и алкинилтрифторборатом металла(предпочтительно калия), M+[R8-BF3]-, в присутствии подходящего палладиевого катализатора, подходящего лиганда и подходящего основания в присутствии подходящего растворителя, при условиях реакции Судзуки-Мияура (см., например, I. Kondolff, H. Doucet and M. Santelli, Tetrahedron, (2004), 60, 3813-3818; Аналогичным образом, соединение формулы (Т) можно получить из соединения формулы (АА), в которой Q является таким, как определено выше, и R" является таким, как определено для соединения формулы (Z), по аналогичным методикам с использованием соответствующих исходных веществ. Соединение формулы (Z) можно получить из соединения формулы (U), по реакции с соединением формулы (ВВ), в которой L обозначает подходящую отщепляющуюся группу, такую как галоген или алкил- или арилсульфонат, по методикам, аналогичным описанным выше для получения соединения формулы (R) из соединения формулы (U). Альтернативно, соединение формулы (Z) можно получить по реакции соединения формулы (L) с соединением формулы (СС) по методикам, аналогичным описанным выше для получения соединения формулы (R) из соединения формулы (L). По методикам, аналогичным описанным выше, соединение формулы (АА) можно получить из соединения формулы (U) путем алкилирования соединением формулы (DD), в которой L обозначает подходящую отщепляющуюся группу, такую как галоген или алкил- или арилсульфонат, или путем алкилирования соединением формулы (ЕЕ). В альтернативном подходе соединение формулы (U) можно обработать галогенирующим реагентом, таким как оксихлорид фосфора, пентахлорид фосфора, пентабромид фосфора, оксибромид фосфора,оксалилхлорид или оксалилбромид, необязательно в подходящем растворителе, таком как толуол, хлороформ, дихлорметан, необязательно в присутствии диметилформамида, и полученный винилгалогенид формулы (FF), в которой Hal обозначает хлор или бром, можно подвергнуть превращению по реакции со спиртом формулы (X), или формулы (Y), или формулы (СС), или формулы (ЕЕ), необязательно в присутствии подходящего основания, такого как гидрид натрия, трет-бутоксид натрия, трет-бутоксид калия и подходящего растворителя, такого как тетрагидрофуран, 1,4-диоксан, диметиловый эфир диэтиленгликоля, и получить соединение формулы (R), формулы (Т), формулы (Z) и формулы (АА) соответственно(СС), формулы (DD) и формулы (ЕЕ) являются известными или их можно получить по известным методикам из известных соединений (см., например, Т. Denton, X. Zhang, J. Cashman, J. Med. Chem., (2005),48, 224-239; J. Reinhard, W. Hull, C.-W. von der Lieth, U. Eichhorn, H.-C. Kliem, J. Med. Chem., (2001), 44,4050-4061; H. Kraus and H. Fiege, DE 19547076; M. Boys, L. Schretzman, N. Chandrakumar, M. Tollefson, S.Chem., (1993), 58 (1), 272-274). Соединения формулы (U), в которой Y обозначает О, являются известными соединениями или их можно получить по методикам, аналогичным описанным в литературе (см., например, М. Morgan and E.Med. Chem., (2006), 49(23), 6869-6887). Соединения формулы (U), в которой Y обозначает S, являются известными соединениями или или их можно получить по методикам, аналогичным описанным в литературе (см., например, Е. Fehnel and A. Paul, J. Am. Chem Soc, (1955), 77, 4241; E. Er and P. Margaretha,Helvetica Chimica Acta (1992), 75(7), 2265-69; H. Gayer et al., DE 3318648 A1). Соединения формулы (U), в которой Y обозначает С=О, являются известными соединениями или или их можно получить по методикам, аналогичным описанным в литературе (см., например, R. Gotz et al. WO 2000/075095). В другом подходе соединение формулы (А), в которой Y обозначает О, S или С=О, можно получить по реакции соединения формулы (U) с гетероарилтрикарбоксилатом свинца при условиях, описанных в литературе (см., например, J. Pinhey and В. Rowe, Aust. J. Chem., (1979), 32, 1561-6; J. Morgan and J. Pinhey, J. Chem.Soc. Perkin Trans. 1, (1990), 3, 715-20; J. Pinhey and E. Roche, J. Chem. Soc. Perkin Trans. 1, (1988), 2415-21). Предпочтительным гетероарилтрикарбоксилатом свинца является гетероарилтриацетат формулы (GG) и реакцию проводят в присутствии подходящего лиганда (например, N,N-диметиламинопиридина, пиридина,имидазола, бипиридина или 1,10-фенантролина, предпочтительно от 1 до 10 экв. N,N-диметиламинопиридина в пересчете на соединение (U и в подходящем растворителе (например, хлороформе, дихлорметане или толуоле, предпочтительно хлороформе, и необязательно в присутствии сорастворителя, такого как толуол) при температуре от 25 до 100 С (предпочтительно 60-90 С). Соединение формулы (GG) можно получить из соединения формулы (НН) путем обработки тетраацетатом свинца в подходящем растворителе (например, хлороформе) при температуре от 25 до 100 С(предпочтительно 25-50 С), необязательно в присутствии катализатора, такого как диацетат ртути, по методикам, описанным в литературе (см., например, K. Shimi, G. Воуег, J-P. Finet and J-P. Galy, Letters in Предпочтительные реагенты сочетания включают гетероарилбороновые кислоты, (НН 1)-(НН 8), в которых R7, R8, R9, R10, R11, R12, X, W1, W2, W3, W4 и Z являются такими, как определено выше. Гетероарилбороновые кислоты формулы (НН) являются известными соединениями или их можно получить из известных соединений по известным методикам (см., например, A. Voisin et al., TetrahedronHuang and S. Buchwald, J. Am. Chem. Soc, (2003), 125, 11818-11819, и цитированную в них литературу). В другом подходе соединение формулы (А) можно получить из соединений формулы (JJ) по реакции с гетероарилбороновой кислотой формулы (НН) в присутствии подходящего палладиевого катализатора и основания, и предпочтительно в подходящем растворителе. Подходящими палладиевыми катализаторами обычно являются комплексы палладия(II) или палладия(0), например, дигалогениды палладия(II), ацетат палладия(II), сульфат палладия(II), бис(трифенилфосфин)палладий(II)дихлорид, бис(трициклопентилфосфин)палладий(II)дихлорид, бис(трициклогексилфосфин)палладий(II)дихлорид,бис(дибензилиденацетон)палладий(0) или тетракис(трифенилфосфин)палладий(0). Палладиевый катализатор также можно приготовить "in situ" из соединений палладия(II) или палладия(0) путем образования комплексов с необходимыми лигандами, например, путем объединения образующей комплекс соли палладия(II), например, дихлорида палладия(II) (PdCl2) или ацетата палладия(II)(Pd(OAc)2), с необходимым лигандом, например, трифенилфосфином (PPh3), трициклопентилфосфином или трициклогексилфосфином и выбранным растворителем, с соединением формулы (JJ), гетероароматической бороновой кислотой формулы (НН) и основанием. Подходящими также являются бидентатные лиганды, например, 1,1'-бис(дифенилфосфино)ферроцен или 1,2-бис(дифенилфосфино)этан. При нагревании реакционной среды "in situ" образуется комплекс палладия(II) или комплекс палладия(0), необходимый для реакции сочетания С-С, и затем инициируется реакция сочетания С-С. Палладиевые катализаторы используют в количестве, составляющем от 0,001 до 50 мол.%, предпочтительно в количестве, составляющем от 0,1 до 15 мол.% в пересчете на соединение формулы (JJ). Более предпочтительно, если палладиевым катализатором является ацетат палладия, основанием является гидроксид лития и растворителем является смесь 1,2 диметоксиэтана и воды в соотношении от 4:1 до 1:4. Реакцию также можно провести в присутствии других добавок, таких как соли тетраалкиламмония, например, тетрабутиламмонийбромид. Соединение формулы (JJ) можно получить из соединения формулы (U) путем обработки (диацетокси)йодбензолом по методикам, описанным в публикациях (K. Schank and С. Lick, Synthesis, (1983), 392,или Z Yang et al., Org. Lett., (2002), 4(19), 3333). В другом подходе соединение формулы (А) можно получить с помощью перегруппировки соединения формулы (KK), в присутствии реагента, который стимулирует перегруппировку, такого как алкоксид металла (предпочтительно в количестве, равном или превышающем 100% в пересчете на соединение формулы (KK или цианид-анион, например, 0,001-25% цианида калия, 0,001-25% цианида натрия или 0,001-25% циангидрина ацетона в пересчете на соединение формулы (KK). Эту реакцию также необязательно проводят в подходящем растворителе (например, ацетонитриле) при подходящей температуре Соединение формулы (KK) можно получить из соединения формулы (LL) путем обработки катализатором, таким как дихлорид палладия(II) или карбонат серебра (предпочтительно 0,001-50% карбоната серебра в пересчете на соединение формулы (LL, в присутствии подходящего растворителя (например,ацетонитрила), при подходящей температуре (обычно при температуре от 25 до 150 С, предпочтительно 120 С при нагревании микроволновым излучением). Аналогичные реакции лактонизации известны из литературы (см., например, P. Huang и W. Zhou, Tetrahedron Asymmetry (1991), 2(9), 875-878). Соединение формулы (LL) можно получить путем омыления соединения формулы (ММ), в которой R обозначает алкил (предпочтительно метил или этил), при известных условиях, и соединение формулы (ММ) можно получить из соединения формулы (NN) по реакции сочетания Соногашира с подходящим гетероароматическим галогенидом (таким как бромид или йодид), Het-hal, в присутствии палладиевого катализатора(например, бис(трифенилфосфин)палладий(II)дихлорида в количестве, обычно составляющем 0,001-25% в пересчете на соединение формулы (NN, источника меди (например, йодида меди(I) в количестве, обычно составляющем 0,001-50% в пересчете на соединение формулы (NN, основания (такого как диэтиламин или триэтиламин) и необязательно в подходящем растворителе. Аналогичные реакции сочетания известны из литературы (см., например, Z. Gan и R. Roy, Canadian Journal of Chemistry (2002), 80(8), 908-916). Соединения формулы (NN) являются известными соединениями или или их можно получить по методикам, аналогичным описанным в литературе (см., например, I. Drizin et al., WO 2001/066544; М. Yamamoto, Journal of Chemical Research, Synopses (1991), (7), 165; P. Machin, US 4774253; M. Morgan and E.Heyningen, J. Am. Chem. Soc., (1957), 79, 422-424). В другом подходе соединение формулы (А) можно получить из соединения формулы I или IA (в которой G обозначает С 1-С 4-алкил) путем гидролиза, предпочтительно в присутствии кислотного катализатора, такого как хлористо-водородная кислота, и необязательно в присутствии подходящего растворителя, такого как тетрагидрофуран. Соединение формулы I (в которой G предпочтительно обозначает С 1-С 4 алкил) можно получить по реакции соединения формулы (OO) (в которой G предпочтительно обозначает С 1-С 4-алкил и Hal обозначает галоген, предпочтительно бром или йод) с гетероарилбороновой кислотой,Het-B(OH)2, формулы (НН) в присутствии подходящего палладиевого катализатора (например, 0,00150% ацетата палладия(II) в пересчете на соединение (ОО и основания (например, от 1 до 10 экв. фосфата калия в пересчете на соединение (ОО и предпочтительно в присутствии подходящего лиганда (например, 0,001-50% (2-дициклогексилфосфино)-2',6'-диметоксибифенила в пересчете на соединение(ОО, и в подходящем растворителе (например, толуоле), предпочтительно при температуре от 25 до 200 С. Аналогичные реакции сочетания известны из литературы (см., например, Y. Song, В. Kim and J.N. Heo, Tetrahedron Letters (2005), 46(36), 5987-5990). Соединение формулы (ОО) можно получить путем галогенирования соединения формулы (U) с последующим алкилированием полученного галогенида формулы (РР) С 1-С 4-алкилгалогенидом или три-С 1 С 4-алкилортоформиатом при известных условиях, например, по методикам, описанным в публикациях R.Chem. (2002), 10, 685-690). Альтернативно, соединение формулы (ОО) можно получить алкилированием соединения формулы (U) С 1-С 4-алкилгалогенидом или три-С 1-С 4-алкилортоформиатом и галогенированием полученного енона формулы (QQ) при известных условиях (см., например, Y. Song, В. Kim and J.N. Heo, Tetrahedron Letters (2005), 46(36), 5987-5990). В другом подходе соединение формулы (А) можно получить по реакции соединения формулы (U) с подходящим гетероарилгалогенидом (таким как йодид или бромид), Het-hal, в присутствии подходящего палладиевого катализатора (например, 0,001-50% ацетата палладия(II) в пересчете на соединение (U и основания (например, от 1 до 10 экв. фосфата калия в пересчете на соединение (U и предпочтительно в присутствии подходящего лиганда (например, 0,001-50% (2-дициклогексилфосфино)-2',4',6'триизопропилбифенила в пересчете на соединение (U, и в подходящем растворителе (например, диоксане), предпочтительно при температуре от 25 до 200 С. Аналогичные реакции сочетания известны из литературы (см., например, J. Fox, X. Huang, A. Chieffi, and S. Buchwald, J. Am. Chem. Soc. (2000), 122,1360-1370; B. Hong et al. WO 2005/000233). Альтернативно, соединение формулы (А) можно получить по реакции соединения формулы (U) с подходящим гетероарилгалогенидом (таким как йодид или бромид),Het-hal, в присутствии подходящего содержащего медь катализатора (например, 0,001-50% йодида меди(I) в пересчете на соединение (U и основания (например, от 1 до 10 экв. карбоната калия в пересчете на соединение (U и предпочтительно в присутствии подходящего лиганда (например, 0,001-50% Lпролина в пересчете на соединение (U, и в подходящем растворителе (например, диметилсульфоксиде),предпочтительно при температуре от 25 до 200 С. Аналогичные реакции сочетания известны из литературы для арилгалогенидов (см., например, Y. Jiang, N. Wu, H. Wu, and M. He, Synlett, (2005), 18, 27312734). Специалисты в данной области техники должны понимать, что соединения формулы I могут содержать гетероароматический фрагмент, содержащий один или большее количество заместителей, при известных условиях способных превращаться в альтернативные заместители, и что эти соединения сами могут выступать в качестве промежуточных продуктов для получения дополнительных соединений формулы I. Например, гетероцикл формулы (RR), в которой Q1 обозначает алкенил или алкинил, при известных условиях можно восстановить в соединение формулы (Q), в которой R8 обозначает алкил. Кроме того, соединение формулы (RR), в которой Q1 обозначает атом или группу, подходящую для реакций перекрестного сочетания, такую как галоген или галогеналкилсульфонат, при известных условиях могут вступать в реакции Судзуки-Мияура, Стилле, Соногашира и родственные реакции с образованием дополнительных соединений формулы Q. Специалисты в данной области техники должны понимать, что превращения этого типа не ограничиваются соединениями формулы (RR), а в общем случае их можно применить к любому соединению формулы I, в которой Het представляет собой гетероцикл, замещенный атомом или группой Q1, подходящей для получения других производных. В другой методике получения соединений формулы (А), в которой Het обозначает группу формулы(R2), X обозначает S, и Y обозначает N, соединение формулы (SS), в которой L обозначает подходящую отщепляющуюся группу, такую как галоген или алкил- или галогеналкилсульфонат, можно обработать соединением формулы (ТТ), необязательно в присутствии подходящего основания (такого как триэтиламин или пиридин) и необязательно в подходящем растворителе (таком как вода, толуол, ацетон, этанол или изопропанол) по известным методикам (см., например, Е. Knott, J. Chem. Soc., (1945), 455; Н. Brederick, R. Gompper, Chem. Ber. (1960), 93, 723; B. Friedman, M. Sparks и R. Adams, J. Am. Chem. Soc., (1937),59, 2262). Альтернативно, соединение формулы (SS) можно обработать тиомочевиной по известным методикам (см., например, V. Pshenichniya, О. Gulyakevich and V. Kripach, Chemistry of Heterocyclic Compounds,(1990), 10, 1409-1412) и полученный продукт формулы (UU) можно превратить в дополнительные соединения формулы (А) путем превращения в галогенид формулы (VV), в которой Hal обозначает хлор, бром или йод, при условиях реакции Зандмайера, и соединение формулы (VV) можно превратить в соединения формулы (А) с помощью перекрестного сочетания при известных условиях для реакций СудзукиМияура, Соногашира, Стилле и родственных реакций, как это описано выше. Соединение формулы (SS) можно получить из соединения формулы (U) при известных условияхChemistry, (1989), 25 (9), 1882-1888). Соединения формул (В), (R) и (Т) являются новыми и специально разработаны для синтеза соединений формулы I. Соединения формулы I, предлагаемые в настоящем изобретении, можно использовать в качестве гербицидов в неизмененном виде, т.е. в том виде, в котором они получены при синтезе, но обычно их различным образом включают в композиции с использованием вспомогательных веществ, таких как носители, растворители и поверхностно-активные вещества. Композиции могут находиться в различных формах, например, в виде порошков для опудривания, гелей, смачивающихся порошков, диспергирующихся в воде гранул, диспергирующихся в воде таблеток, шипучих прессованных таблеток, эмульгирующихся концентратов, микроэмульгирующихся концентратов, эмульсий масло-в-воде, текучих масел,водных дисперсий, масляных дисперсий, суспоэмульсий, суспензий капсул, эмульгирующихся гранул,растворимых жидкостей, растворимых в воде концентратов (с водой или смешивающимся с водой органическим растворителем в качестве носителя), пропитанных полимерных пленок или в других формах,описанных, например, в руководстве (Manual on Development and Use of FAO Specifications for Plant Protection Products, 5th Edition, 1999). Такие композиции можно использовать непосредственно или можно разбавить перед использованием. Разбавление можно провести, например, водой, жидкими удобрениями,питательными микровеществами, биологическими организмами, маслом или растворителями. Композиции можно получить, например, путем смешивания активного ингредиента со вспомогательными веществами для приготовления композиций и получить композиции в виде тонкоизмельченных твердых веществ, гранул, растворов, суспензий или эмульсий. Активные ингредиенты также можно смешать с другими вспомогательными веществами, такими как тонкоизмельченные твердые вещества,минеральные масла, растительные масла, модифицированные растительные масла, органические растворители, вода, поверхностно-активные вещества или их комбинации. Активные ингредиенты также могут содержаться в очень мелких микрокапсулах, состоящих из полимера. Микрокапсулы содержат активные ингредиенты в пористом носителе. Это обеспечивает выделение активных ингредиентов в окружающую среду в регулируемом количестве (например, медленное выделение). Микрокапсулы обычно обладают диаметром, равным от 0,1 до 500 мкм. Они содержат активные ингредиенты в количестве, составляющем примерно от 25 до 95 мас.% в пересчете на массу капсулы. Активные ингредиенты могут содержаться в виде сплошного твердого вещества, в виде мелких частиц в твердых или жидких дисперсиях или в виде соответствующего раствора. Капсулирующие мембраны включают, например, натуральные и синтетические камеди, целлюлозу, сополимеры стирола с бутадиеном, полиакрилонитрил, полиакрилат, сложный полиэфир, полиамиды, полимочевины, полиуретан или химически модифицированные полимеры и ксантаты крахмала и другие полимеры, известные в этом контексте специалисту в данной области техники. Альтернативно, можно получить очень мелкие микрокапсулы, в которых активный ингредиент содержится в виде тонкоизмельченных твердых частиц в твердой матрице основного вещества, но в этом случае микрокапсулы не капсулированы. Вспомогательные вещества, которые пригодны для получения композиций, предлагаемых в настоящем изобретении, сами по себе известны. В качестве жидких носителей можно использовать воду,толуол, ксилол, петролейный эфир, растительные масла, ацетон, метилэтилкетон, циклогексанон, ангидриды кислот, ацетонитрил, ацетофенон, амилацетат, 2-бутанон, бутиленкарбонаты, хлорбензол, циклогексан, циклогексанол, алкиловые эфиры уксусной кислоты, диацетоновый спирт, 1,2-дихлорпропан,диэтаноламин, п-диэтилбензол, диэтиленгликоль, диэтиленгликольабиетат, бутиловый эфир диэтиленгликоля, этиловый эфир диэтиленгликоля, метиловый эфир диэтиленгликоля, N,N-диметилформамид,диметилсульфоксид, 1,4-диоксан, дипропиленгликоль, метиловый эфир дипропиленгликоля, дипропиленгликольдибензоат, дипроксит, алкилпирролидон, этилацетат, 2-этилгексанол, этиленкарбонат, 1,1,1 трихлорэтан, 2-гептанон, альфа-пинен, d-лимонен, этиллактат, этиленгликоль, бутиловый эфир этиленгликоля, метиловый эфир этиленгликоля, гамма-бутиролактон, глицерин, глицеринацетат, глицериндиацетат, глицеринтриацетат, гексадекан, гексиленгликоль, изоамилацетат, изоборнилацетат, изооктан,изофорон, изопропилбензол, изопропилмиристат, молочную кислоту, лауриламин, мезитилоксид, метоксипропанол, метилизоамилкетон, метилизобутилкетон, метиллаурат, метилоктаноат, метилолеат, метиленхлорид, м-ксилол, н-гексан, н-октиламин, октадекановую кислоту, актиламинацетат, олеиновую кислоту, олеиламин, о-ксилол, фенол, полиэтиленгликоль (ПЭГ 400), пропионовую кислоту, пропиллактат,пропиленгликоль, метиловый эфир пропиленгликоля, п-ксилол, толуол, триэтилфосфат, триэтиленгликоль, ксилолсульфоновую кислоту, парафин, минеральное масло, трихлорэтилен, перхлорэтилен, этилацетат, амилацетат, бутилацетат, метиловый эфир пропиленгликоля, метиловый эфир диэтиленгликоля,метанол, этанол, изопропанол и спирты, обладающие большей молекулярной массой, такие как амиловый спирт, тетрагидрофурфуриловый спирт, гексанол, октанол и т.п., этиленгликоль, пропиленгликоль,глицерин, N-метил-2-пирролидинон и т.п. Для разбавления концентратов в качестве носителя обычно выбирают воду. Подходящими твердыми носителями обычно являются, например, тальк, диоксид титана, пирофиллитовая глина, диоксид кремния, аттапульгитовая глина, кизельгур, известняк, карбонат кальция, бентонит, монтмориллонит кальция, шелуха семян хлопка, пшеничная мука, соевая мука, пемза,древесная мука, размолотая скорлупа грецких орехов, лигнин и аналогичные вещества, такие как описанные, например, в CFR 180.1001. (с)(d). Большое количество поверхностно-активных веществ с успехом можно использовать и в твердых, и в жидких композициях, в особенности в таких, которые перед применением можно разбавить носителем. Поверхностно-активные вещества могут быть анионогенными, катионогенными, неионогенными или полимерными и их можно использовать в качестве эмульгирующих агентов, смачивающих или суспендирующих агентов или для других целей. Типичные поверхностно-активные вещества включают, например, соли алкилсульфатов, такие как диэтаноламмонийлаурилсульфат; соли алкиларилсульфонатов,такие как додецилбензолсульфонат кальция; продукты присоединения алкилфенолов к алкиленоксидам,такие как нонилфенолэтоксилат; продукты присоединения спиртов к алкиленоксидам, такие как этоксилат тридецилового спирта; мыла, такие как стеарат натрия; соли алкилнафталинсульфонатов, такие как дибутилнафталинсульфонат натрия; диалкиловые эфиры сульфосукцинатных солей, такие как ди(2 этилгексил)сульфосукцинат натрия; сложные эфиры сорбита, такие как сорбитолеат; четвертичные амины, такие как лаурилтриметиламмонийхлорид, сложные эфиры полиэтиленгликоля и жирных кислот,такие как полиэтиленгликольстеарат; блок-сополимеры этиленоксида с пропиленоксидом; и соли монои диалкилфосфатов; а также другие вещества, описанные, например, в публикации ("McCutcheon's Detergents and Emulsifiers Annual" MC Publishing Corp., Ridgewood New Jersey, 1981). Другие вспомогательные вещества, которые обычно можно использовать в пестицидных композициях, включают ингибиторы кристаллизации, вещества, модифицирующие вязкость, суспендирующие агенты, красители, антиоксиданты, вспенивающие агенты, поглощающие свет агенты, вспомогательные вещества, способствующие смешиванию, противовспенивающие вещества, комплексообразователи, нейтрализующие или меняющие рН вещества и буферы, ингибиторы коррозии, отдушки, смачивающие агенты, вещества, улучшающие абсорбцию, питательные микроэлементы, пластификаторы, вещества,придающие скользкость, смазывающие вещества, диспергирующие вещества, загущающие агенты, антифризные агенты, микробицидные агенты, а также жидкие и твердые удобрения. Композиции также могут содержать дополнительные активные вещества, например, другие гербициды, антидоты гербицидов, регуляторы роста растений, фунгициды или инсектициды. Композиции, предлагаемые в настоящем изобретении, могут дополнительно включать добавки,включающие масла растительного или животного происхождения, минеральное масло, алкиловые эфиры таких масел или смеси таких масел и производных масел. Количество добавки масла, использующееся в композициях, предлагаемых в настоящем изобретении, обычно составляет от 0,01 до 10% в пересчете на смесь для опрыскивания. Например, добавку масла можно прибавить в бак для опрыскивания в необходимой концентрации после приготовления смеси для опрыскивания. Предпочтительные прибавляемые масла включают минеральные масла и масла растительного происхождения, например, рапсовое масло,- 17020695 оливковое масло или подсолнечное масло, эмульгированное растительное масло, такое как AMIGO(Rhne-Poulenc Canada Inc.), алкиловые эфиры масел растительного происхождения, например, метилпроизводные, или масло животного происхождения, такое как рыбий жир или говяжий жир. Предпочтительная добавка, например, содержит в качестве активных компонентов в основном 80% алкиловых эфиров рыбьего жира и 15 мас.% метилированного рапсового масла и 5 мас.% обычных эмульгаторов и веществ, изменяющих рН. Особенно предпочтительные добавки масла включают алкиловые эфиры C8-C22 жирных кислот, метилпроизводные C12-C18 жирных кислот, например, особенно предпочтительными являются метиловые эфиры лауриновой кислоты, пальмитиновой кислоты и олеиновой кислоты. Эти сложные эфиры известны как метиллаурат (CAS-111-82-0), метилпальмитат (CAS-112-39-0) и метилолеат (CAS-112-62-9). Предпочтительным метилпроизводным жирной кислоты является Emery 2230 и 2231(Cognis GmbH). Эти и другие добавки масла также описаны в публикации (Compendium of Herbicide Adjuvants, 5th Edition, Southern Illinois University, 2000). Внесение и воздействие добавок масла можно дополнительно улучшить путем их комбинирования с поверхностно-активными веществами, такими как неионогенные, анионогенные или катионогенные поверхностно-активные вещества. Примеры подходящих анионогенных, неионогенных и катионогенных поверхностно-активных веществ приведены на с. 7 и 8 в WO 97/34485. Предпочтительными поверхностно-активными веществами являются анионогенные поверхностно-активные вещества типа додецилбензолсульфоната, в особенности их кальциевые соли, а также неионогенные поверхностно-активные вещества типа этоксилатов жирных спиртов. Особое предпочтение отдается этоксилированным С 12-С 22 жирным спиртам, обладающим степенью этоксилирования, составляющей от 5 до 40. Примерами имеющихся в продаже поверхностно-активных веществ являются вещества типа Genapol (Clariant AG). Также предпочтительными являются силиконовые поверхностно-активные вещества, в особенности модифицированные полиалкилоксидом гептаметилтрисилоксаны, которые имеются в продаже, например, под названием Silwet L-77, а также перфторированные поверхностно-активные вещества. Концентрация поверхностно-активных веществ в пересчете на всю добавку обычно составляет от 1 до 30 мас.%. Примерами добавок масел, которые состоят из смеси масел или минеральных масел или их производных с поверхностно-активными веществами, являются Edenor ME SU, Turbocharge (Zeneca Agro, CA) и Actipron (BP Oil UK Limited, GB). Указанные поверхностно-активные вещества также можно использовать в композициях по отдельности, т.е. без добавки масла. Кроме того, прибавление органического растворителя к смеси добавка масла/поверхностноактивное вещество также может привести к дополнительному усилению воздействия. Подходящими растворителями являются, например, Solvesso (ESSO) и Aromatic Solvent (Exxon Corporation). Концентрация таких растворителей может составлять от 10 до 80 мас.% в пересчете на полную массу. Такие добавки масла, которые содержатся в смеси с растворителями, описаны, например, в US-A-4834908. Описанные в нем имеющиеся в продаже добавки масла известны под названием MERGE (BASF Corporation). Другой добавкой масла, которая предпочтительна для настоящего изобретения, является SCORE (Syngenta Crop Protection Canada). В дополнение к добавкам масла, перечисленным выше, для усиления воздействия композиций,предлагаемых в настоящем изобретении, в смесь для опрыскивания также можно прибавлять композиции алкилпирролидонов (например, Agrimax). Для этой цели также можно использовать композиции синтетических латексов, такие как, например, полиакриламиды, поливинилы и поли-1-п-ментен (например, Bond, Courier или Emerald). В качестве усиливающих воздействие агентов со смесью для опрыскивания также можно смешать растворы, содержащие пропионовую кислоту, например, Eurogkem Pene-trate. Гербицидные композиции обычно содержат от 0,1 до 99 мас.%, предпочтительно от 0,1 до 95 мас.%, соединения формулы I и от 1 до 99,9 мас.% вспомогательного вещества композиции, которое предпочтительно содержит от 0 до 25 мас.% поверхностно-активного вещества. В то время как имеющиеся в продаже продукты предпочтительно готовят в виде концентратов, конечный потребитель обычно использует разбавленные композиции. Нормы расхода соединений формулы I могут меняться в широких пределах и зависят от характера почвы, методики внесения (до- или послевсходовое; протравливание семян; внесение в борозды для семян; внесение без обработки почвы и т.п.), возделываемого растения, сорняка или травянистого растения, с которыми необходимо бороться, преобладающих климатических условий и других факторов, зависящих от методики внесения, времени внесения и обрабатываемой культуры. Соединения формулы I,предлагаемые в настоящем изобретении, обычно вносят в дозе, составляющей от 1 до 4000 г/га, предпочтительно от 5 до 1000 г/га. Предпочтительные композиции преимущественно обладают следующими составами: (% = мас.%) Эмульгирующиеся концентраты активный ингредиент от 1 до 95 %, предпочтительно от 60 до 90% поверхностно-активное вещество от 1 до 30 %, предпочтительно от 5 до 20% жидкий носитель от 1 до 80%, предпочтительно от 1 до 35% Дусты активный ингредиент от 0,1 до 10%, предпочтительно от 0,1 до 5% твердый носитель от 99,9 до 90 %, предпочтительно от 99,9 до 99% Концентраты суспензий активный ингредиент от 5 до 75%, предпочтительно от 10 до 50% вода от 94 до 24%, предпочтительно от 88 до 30% поверхностно-активное вещество от 1 до 40%, предпочтительно от 2 до 30% Смачивающиеся порошки активный ингредиент от 0,5 до 90%, предпочтительно от 1 до 80% поверхностно-активное вещество от 0,5 до 20%, предпочтительно от 1 до 15% твердый носитель от 5 до 95%, предпочтительно от 15 до 90% Гранулы активный ингредиент от 0,1 до 30%, предпочтительно от 0,5 до 15% твердый носитель от 99,9 до 70%, предпочтительно от 97 до 85% Приведенные ниже примеры дополнительно иллюстрируют, но не ограничивают настоящее изобретение. Эмульсии любой необходимой концентрации можно получить из таких концентратов путем разбавления водой. Молекулярная масса. Растворы пригодны для применения в виде микрокапелек. Активный ингредиент тщательно смешивают со вспомогательными веществами и смесь тщательно размалывают на подходящей мельнице и получают смачивающиеся порошки, которые можно разбавить водой и получить суспензии любой необходимой концентрации. Активный ингредиент растворяют в метиленхлориде и наносят на носитель путем разбрызгивания,а затем растворитель выпаривают в вакууме. В смесителе тонкоразмолотый активный ингредиент равномерно наносят на носитель, смоченный полиэтиленгликолем. Таким образом получают не образующие пыли гранулы с покрытием. Активный ингредиент смешивают со вспомогательными веществами и смесь увлажняют водой. Смесь экструдируют и затем сушат в потоке воздуха. Готовые к применению дусты получают смешиванием активного ингредиента с носителями и размолом смеси на подходящей мельнице. Тонкоразмолотый активный ингредиент тщательно смешивают со вспомогательными веществами с получением концентрата суспензии, из которых путем разбавления водой можно получить суспензии любой необходимой концентрации. Настоящее изобретение также относится к способу селективной борьбы с травянистыми растениями и сорняками в культурах полезных растений, который включает обработку полезных растений или места их выращивания, или места их произрастания соединением формулы I. Культуры полезных растений, для которых можно применять композицию, предлагаемую в настоящем изобретении, включают злаки, хлопок, сою, сахарную свеклу, сахарный тростник, плантационные культуры, рапс, кукурузу и рис, и их используют для неселективной борьбы с сорняками. Композиции,предлагаемые в настоящем изобретении, являются особенно полезными для селективной борьбы с травянистыми растениями и сорняками в злаках, кукурузе и рисе, в особенности рисе. Термин "культуры" следует понимать и как включающий культуры, которым придана стойкость к гербицидам или классам гербицидов (например, к ингибиторам АЛС (ацетолактатсинтаза), ГС (глутаминсинтетаза), ЕПШФС (5 енолпирувилшикимат-3-фосфатсинтаза), ПФО (полифенолоксидаза), ACCase (ацетил-СоА-карбоксилаза) и ГФПД (4-гидроксифенилпируватдиоксигеназа с помощью обычных методик селекции или генной инженерии. Примером культуры, которой с помощью обычных методик селекции придана стойкость, например,к имидазолинонам, таким как имазамокс, является сурепица Clearfield (канола). Примерами культур, которым с помощью методик генной инженерии придана стойкость к гербицидам, являются сорта кукурузы,стойкие, например, к глифозату или глуфозинату, которые имеются в продаже под торговыми названиямиRoundupReady и LibertyLink соответственно. Сорняками, с которым проводят борьбу, могут быть однодольные и двудольные сорняки, такие как, например, Stellaria, Nasturtium, Agrostis, Digitaria, Avena, Setaria,Sinapis, Lolium, Solanum, Echinochloa, Scirpus, Monochoria, Sagittaria, Bromus, Alopecurus, Sorghum, Rottboellia, Cyperus, Abutilon, Sida, Xanthium, Amaranthus, Chenopodium, Ipomoea, Chrysanthemum, Galium, Viola иVeronica. Под культурами также следует понимать такие, у которых методами генной инженерии была выработана стойкость к насекомым-вредителями и в качестве примера которых можно назвать Bt-кукурузу(стойкую по отношению к кукурузному мотыльку), Bt-хлопчатник (устойчивый к хлопковому долгоносику), а также различные сорта Bt-картофеля (устойчивого к колорадскому жуку). Примерами Btкукурузы являются гибриды кукурузы Bt 176 сорта NK (Syngenta Seeds). Токсин Bt представляет собой белок, вырабатываемый в естественных условиях почвенными бактериями Bacillus thuringiensis. Примеры токсинов и трансгенных растений, способных синтезировать подобные токсины, описаны в ЕР-А 451878, ЕР-А-374753, WO 93/07278, WO 95/34656, WO 03/052073 и ЕР-А-427529. Примерами трансгенных растений, которые содержат один или большее количество генов, которые кодируют стойкость к инсектицидам и вырабатывают один или большее количество токсинов, являются KnockOut (кукуруза),Yield Gard (кукуруза), NuCOTIN33B (хлопок), Bollgard (хлопок), NewLeaf(картофель), NatureGard и Protexcta. Культурные растения и их семенной материал может быть стойким по отношению к гербицидам и одновременно также к поеданию насекомыми (совмещенные трансгенные характеристики). Семена могут, например, обладать способностью вырабатывать обладающий инсектицидной активностью белок Cry3 и одновременно являться стойкими по отношению к глифозату. Термин "культуры" следует понимать как включающий и культуры, полученные по обычным методикам селекции или генной инженерии, которые обладают дополнительными характеристиками (например, улучшенными вкусом, стабильностью при хранении, содержанием питательных веществ). Под посевными площадями следует понимать участки, на которых уже растут культурные растения, а также участки, предназначенные для выращивания этих культурных растений. Соединения формулы I, предлагаемые в настоящем изобретении, также можно применять в комбинации с другими гербицидами. Указанные ниже смеси соединения формулы I являются особенно важными. Предпочтительно, если в этих смесях соединение формулы I является одним из соединений, указанных в приведенных ниже табл. 1-592 соединение формулы I + ацетохлор, соединение формулы I + ацифлюорфен, соединение формулы I нение формулы I + тралкоксидим, соединение формулы I + три-аллат, соединение формулы I + триасульфурон, соединение формулы I + триазифлам, соединение формулы I + трибенурон, соединение формулы I + трибенурон-метил, соединение формулы I + трикамба, соединение формулы I + триклопир, соединение формулы I + триэтазин, соединение формулы I + трифлоксисульфурон, соединение формулы I + трифлоксисульфурон-натрия, соединение формулы I + трифлуралин, соединение формулы I + трифлусульфурон, соединение формулы I + трифлусульфурон-метил, соединение формулы I + тригидрокситриазин, соединение формулы I + тринексапак-этил, соединение формулы I + тритосульфурон, соединение формулы I + этиловый эфир [3-[2 хлор-4-фтор-5-(1-метил-6-трифторметил-2,4-диоксо-1,2,3,4-тетрагидропиримидин-3-ил)фенокси]-2-пиридилокси]уксусной кислоты (регистрационныйCAS 353292-31-6), соединение формулы I + 4-гидрокси-3-2[(2-метоксиэтокси)метил]-6-(трифторметил)-3-пиридинил]карбонил]бицикло [3.2.1]окт-3-ен-2-он (регистрационныйCAS 352010-68-5) и соединение формулы I + 4-гидрокси-3-2-(3-метоксипропил)-6-(дифторметил)-3-пиридинил]карбонил]бицикло [3.2.1]окт-3-ен-2-он. Соединения формулы I, предлагаемые в настоящем изобретении, также можно применять в комбинации с антидотами. Предпочтительно, если в этих смесях соединение формулы I является одним из соединений, указанных ниже в табл. 1-592. В рассмотрение предпочтительно включены указанные ниже смеси с антидотами соединение формулы I + клохинтоцет-мексил, соединение формулы I + клохинтоцетовая кислота и ее соли, соединение формулы I + фенхлоразол-этил, соединение формулы I + фенхлоразоловая кислота и ее соли, соединение формулы I + мефенпир-диэтил, соединение формулы I + мефенпировая дикислота,соединение формулы I + изоксадифен-этил, соединение формулы I + изоксадифеновая кислота, соединение формулы I + фурилазол, соединение формулы I + R-изомер фурилазола, соединение формулы I + беноксакор, соединение формулы I + дихлормид, соединение формулы I + AD-67, соединение формулы II + нафталиновый ангидрид, соединение формулы I + флуразол, соединение формулы I + N-(2 метоксибензоил)-4-[(метиламинокарбонил)амино]бензолсульфонамид, соединение формулы I + CL 304415, соединение формулы I + дициклонон, соединение формулы I + флуксофеним, соединение формулы I + DKA-24, соединение формулы I + R-29148 и соединение формулы I + PPG-1292. Антидотный эффект также можно наблюдать для смесей соединение формулы I + димрон, соединение формулы I + МСРА, соединение формулы I + мекопроп и соединение формулы I + мекопроп-Р. Указанные выше антидоты и гербициды описаны, например, в публикации (Pesticide Manual,Twelfth Edition, British Crop Protection Council, 2000, или других легко доступных источниках). R-29148 описан, например, в публикации (Р.В. Goldsbrough et al., Plant Physiology, (2002), vol. 130 pp. 1497-1505 и цитированной в ней литературе), PPG-1292 известен из WO 09211761 и N-(2-метоксибензоил)-4[(метиламинокарбонил)амино]бензолсульфонамид известен из ЕР 365484. В зависимости от применения гербицидные композиции, предлагаемые в настоящем изобретении,могут содержать соединение формулы I, дополнительный гербицид в качестве компонента для смешивания и антидот, указанные выше. Гербицидные композиции, предлагаемые в настоящем изобретении, пригодны для всех методик внесения, обычно применяющихся в сельском хозяйстве, таких как, например, довсходовое внесение,послевсходовое внесение и протравливание семян. В зависимости от назначения антидоты можно использовать для предварительной обработки семенного материала культурного растения (протравливание семян или черенков) или вносить в почву до или после высевания, с последующим внесением не являющегося антидотом соединения формулы I, необязательно в комбинации со вспомогательным гербицидом. Однако их также можно вносить по отдельности или вместе с гербицидом до или после появления всходов растений. Поэтому обработку растений или семенного материала антидотом, в принципе, можно проводить независимо от времени внесения гербицида. Обработка растения путем одновременного внесения гербицида и антидота (например, в виде баковой смеси) обычно является предпочтительной. Норма расхода антидота по сравнению с гербицидом в значительной степени зависит от методики внесения. В случае обработки в поле обычно вносят от 0,001 до 5,0 кг антидота/га, предпочтительно от 0,001 до 0,5 кг антидота/га. В случае протравливания семян обычно вносят от 0,001 до 10 г антидота/кг семян, предпочтительно от 0,05 до 2 г антидота/кг семян. Если антидот используют в жидком виде при замачивании семян незадолго до высевания, то предпочтительно использовать растворы антидота, которые содержат активный ингредиент в концентрации, равной от 1 до 10000 част./млн, предпочтительно от 100 до 1000 част./млн. Смеси можно с успехом использовать в указанных выше композициях (и в этом случае "активный ингредиент" означает соответствующую смесь соединения формулы I с компонентом для смешивания). Приведенные ниже примеры дополнительно иллюстрируют, но не ограничивают настоящее изобретение. Специалисты в данной области техники должны понимать, что некоторые соединения, описанные ниже, являются -кетоенолами и сами по себе могут находиться в форме одного таутомера или в виде смеси кето-енольного и дикетонного таутомеров, описанных, например, в публикации (J. March, Ad- 24020695vanced Organic Chemistry, third edition, John Wiley and Sons). Соединения, приведенные ниже и в табл. Т 1 и Р 1, изображены в виде произвольного одного енольного таутомера, но следует понимать, что это описание включает и дикетонную форму, и любые возможные енолы, которые могут образоваться вследствие таутомерии. Кроме того, некоторые из соединений, приведенных ниже и в табл. Т 1 и Р 1, изображены в виде одного энантиомера для простоты, но, если не указано, что они являются единственными энантиомерами, то эти структуры следует понимать как описывающие смесь энантиомеров. Кроме того, некоторые из соединений могут находиться в форме диастереоизомеров и следует понимать, что они могут находиться в виде смеси диастереоизомеров или в виде одного возможного диастереоизомера. В представленном ниже экспериментальном разделе названы дикетонные таутомеры даже, если преобладающий таутомер находится в енольной форме. Примеры получения Пример 1. Получение 6-[5-(4-хлор-3-метилфенил)-2-метилтиофен-3-ил]-2,2,4,4-тетраметилциклогексан-1,3,5-триона (соединение Т 4 в табл. Т 1) К раствору 5-бромтиофен-2-илметанол (6,76 г, 35 ммоль) в тетрагидрофуране (100 мл) при 0 С осторожно добавляют гидрид натрия, 60% дисперсию в минеральном масле (1,2 г, 30 ммоль) в течение 10 мин. Реакционной смеси дают нагреться до комнатной температуры и перемешивают в течение еще 1 ч. Затем одной порцией добавляют 5-хлор-2,2,6,6-тетраметилциклогекс-4-ен-1,3-дион (5,02 мг, 25 ммоль) и реакционную смесь перемешивают при комнатной температуре в течение 17 ч. Реакционную смесь концентрируют в вакууме и очищают с помощью флэш-хроматографии на силикагеле и получают искомое соединение в виде белого твердого вещества (4,45 г). Стадия 2. Получение 6-[5-(4-хлор-3-метилфенил)-2-метилтиофен-3-ил]-2,2,4,4-тетраметилциклогексан-1,3,5 триона Смесь 5-(5-бромтиофен-2-илметокси)-2,2,6,6-тетраметилциклогекс-4-ен-1,3-диона (107 мг, 0,3 ммоль), 4-хлор-м-толилбороновой кислоты (60 мг, 0,35 ммоль), ацетата палладия (4 мг, 0,015 ммоль), RuPhos (14 мг, 0,03 ммоль) и карбоната цезия (130 мг, 0,4 ммоль) в толуоле (2 мл) нагревают при 180 С в течение 30 мин при облучении микроволновым излучением и полученное вещество очищают с помощью флэш-хроматографии на силикагеле и получают 6-[5-(4-хлор-3-метилфенил)-2-метилтиофен-3-ил]2,2,4,4-тетраметилциклогексан-1,3,5-трион. Пример 2. Получение 6-[2-(2,5-дихлорфенил)-5-метилтиазол-4-ил]-2,2,4,4-тетраметилциклогексан-1,3,5-триона К суспензии гидрида натрия, 60% дисперсия в минеральном масле (1,6 г, 40 ммоль) в тетрагидрофуране (50 мл) при 0 С добавляют раствор (2-бромтиазол-5-ил)метанола (6,75 г, 35 ммоль) в тетрагидрофуране (50 мл). Затем добавляют раствор 5-хлор-2,2,6,6-тетраметилциклогекс-4-ен-1,3-диона (7,0 г, 35 ммоль) в тетрагидрофуране (50 мл) и реакционную смесь кипятят с обратным холодильником в течение 18 ч. Реакционную смесь выливают в воду, подкисляют до рН 4 разбавленным водным раствором хлористо-водородной кислоты и экстрагируют этилацетатом (450 мл). Объединенные органические слои сушат над безводным сульфатом магния, фильтруют и фильтрат выпаривают и получают коричневое масло. Неочищенный продукт очищают с помощью флэш-хроматографии на силикагеле и получают 5-(2 бромтиазол-5-илметокси)-2,2,6,6-тетраметилциклогекс-4-ен-1,3-дион (6,75 г). Стадия 2. Получение 6-[2-(2,5-дихлорфенил)-5-метилтиазол-4-ил]-2,2,4,4-тетраметилциклогексан-1,3,5-триона 2,5-Дихлорфенилбороновую кислоту (266 мг, 1,39 ммоль), 5-(2-бромтиазол-5-илметокси)-2,2,6,6 тетраметилциклогекс-4-ен-1,3-дион (250 мг, 0,7 ммоль), толуол (3 мл), карбонат цезия (310 мг, 0,95 ммоль) и [1,3-бис(2,6-диизопропил)имидазол-2-илиден](3-хлорпиридил)палладий(II)дихлорид (60 мг,0,12 ммоль) смешивают в сосуде для микроволновой печи и нагревают при 150 С в течение 30 мин при облучении микроволновым излучением. Реакционную смесь охлаждают, фильтруют, выпаривают и очищают с помощью флэш-хроматографии на силикагеле и получают оранжевое масло. Это масло растворяют в диглиме (3 мл) и 1-бутил-3-метилимидазолий-бис(трифторметилсульфонил)имиде (0,1 мл) и нагревают при облучении микроволновым излучением при 210 С в течение 30 мин. Реакционную смесь охлаждают до комнатной температуры, растворитель выпаривают при пониженном давлении и остаток очищают с помощью флэш-хроматографии на силикагеле и получают 6-[2-(2,5-дихлорфенил)-5 метилтиазол-4-ил]-2,2,4,4-тетраметилциклогексан-1,3,5-трион. Пример 3. Получение 4-[2-(4-хлорфенил)-5-этилтиазол-4-ил]-2,2,6,6-тетраметилпиран-3,5-диона (соединение Т 11 в табл. Т 1) К суспензии 2,2,6,6-тетраметилпиран-3,5-диона (741 мг, 4,35 ммоль) в хлороформе (10 мл) добавляют пентахлорид фосфора (454 мг, 2,18 ммоль) и реакционную смесь кипятят с обратным холодильником в течение 5 ч. К охлажденной неочищенной реакционной смеси добавляют силикагель, растворитель выпаривают при пониженном давлении и остаток очищают с помощью флэш-хроматографии на силикагеле и получают 5-хлор-2,2,6,6-тетраметил-6 Н-пиран-3-он (349 мг). Стадия 2. Получение 1-[2-(4-хлорфенил)тиазол-5-ил]этанола При перемешивании к раствору 1-[2-(4-хлорфенил)тиазол-5-ил]этанона (2,38 г, 10 ммоль) в метаноле (20 мл) при 0 С одной порцией добавляют борогидрид натрия (379 мг, 10,5 ммоль). Полученному рас- 26020695 твору дают нагреться до комнатной температуры и затем перемешивают при комнатной температуре в течение 3 ч. Реакцию останавливают насыщенным водным раствором хлорида аммония (200 мл) и экстрагируют хлороформом (200 мл). Органический слой сушат над безводным сульфатом магния и концентрируют в вакууме и получают искомый продукт в виде коричневого твердого вещества (2,32 г) Стадия 3. Получение 5-1-[2-(4-хлорфенил)тиазол-5-ил]этокси-2,2,6,6-тетраметил-6 Н-пиран-3-она К раствору 1-[2-(4-хлорфенил)тиазол-5-ил]этанола (335 мг, 1,4 ммоль) в безводном тетрагидрофуране (5 мл) в атмосфере азота добавляют гидрид натрия, 60% дисперсию в минеральном масле (48 мг, 1,2 ммоль) и полученную желтую суспензию перемешивают при комнатной температуре в течение 1 ч. Затем добавляют раствор 5-хлор-2,2,6,6-тетраметил-6 Н-пиран-3-она (189 мг, 1 ммоль) в безводном тетрагидрофуране (2 мл) и реакционную смесь перемешивают при комнатной температуре в течение 17 ч. Неочищенную реакционную смесь очищают с помощью флэш-хроматографии на силикагеле и получают 51-[2-(4-хлорфенил)тиазол-5-ил]этокси-2,2,6,6-тетраметил-6 Н-пиран-3-он (288 мг). Стадия 4. Получение 4-[2-(4-хлорфенил)-5-этилтиазол-4-ил]-2,2,6,6-тетраметилпиран-3,5-диона(0,1 мл) и раствор нагревают при 210 С в течение 30 мин при облучении микроволновым излучением. Неочищенную реакционную смесь очищают с помощью флэш-хроматографии на силикагеле и получают 4-[2(4-хлорфенил)-5-этилтиазол-4-ил]-2,2,6,6-тетраметилпиран-3,5-дион. Пример 4. Получение 5-[2-(4-хлорфенил)-5-метилселеназол-4-ил]-2,2,6,6-тетраметилпиран-3,5-диона (соединение Т 16 в табл. Т 1) К суспензии 4-хлорселенобензамида (219 мг, 1 ммоль) и 2-хлормалонового альдегида (160 мг, 1,5 ммоль) в 1,2-диметоксиэтане (1,5 мл) добавляют карбонат магния (42 мг, 0,5 ммоль) и полученную смесь перемешивают при 60 С в атмосфере азота в течение 3 ч. Затем неочищенную реакционную смесь фильтруют через слой диоксида кремния и промывают этилацетатом и фильтрат концентрируют и получают коричневое твердое вещество. Неочищенный продукт очищают с помощью флэш-хроматографии на силикагеле и получают 2-(4-хлорфенил)селеназол-5-карбальдегид (162 мг). Стадия 2. Получение [2-(4-хлорфенил)селеназол-5-ил]метанола К суспензии 2-(4-хлорфенил)селеназол-5-карбальдегида (130 мг, 0,48 ммоль) в метаноле (5 мл) при 0 С добавляют борогидрид натрия (19 мг, 0,5 ммоль). Реакционную смесь перемешивают при 0 С в течение 0,5 ч. Реакцию останавливают насыщенным водным раствором хлорида аммония (10 мл) и экстрагируют дихлорметаном (325 мл). Объединенные органические экстракты сушат над безводным сульфа том магния, фильтруют и фильтрат выпаривают досуха и получают [2-(4-хлорфенил)селеназол-5 ил]метанол (127 мг). Стадия 3. Получение 5-[2-(4-хлорфенил)селеназол-5-илметокси]-2,2,6,6-тетраметил-6 Н-пиран-3-она(5 мл) в атмосфере азота одной порцией добавляют гидрид натрия (44 мг, 1,1 ммоль). Реакционную смесь перемешивают в течение 5 мин при комнатной температуре и одной порцией добавляют 5-хлор-2,2,6,6 тетраметил-6 Н-пиран-3-он (208 мг, 1,1 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение ночи. К неочищенной реакционной смеси добавляют силикагель и растворитель выпаривают при пониженном давлении. Остаток очищают с помощью флэш-хроматографии на силикагеле и получают 5-[2-(4-хлорфенил)селеназол-5-илметокси]-2,2,6,6-тетраметил-6 Н-пиран-3-он (261 мг). Стадия 4. Получение 5-[2-(4-хлорфенил)-5-метилселеназол-4-ил]-2,2,6,6-тетраметилпиран-3,5-диона 5-[2-(4-Хлорфенил)селеназол-5-илметокси]-2,2,6,6-тетраметил-6 Н-пиран-3-он (239 мг, 0,56 ммоль) помещают в сосуд для микроволновой печи и растворяют в диметиловом эфире диэтиленгликоля (8 мл). Добавляют 1-бутил-3-метилимидазолий-бис(трифторметилсульфонил)имид (0,1 мл) и реакционную смесь нагревают при 210 С в течение 30 мин при облучении микроволновым излучением. К неочищенной реакционной смеси добавляют силикагель, растворитель выпаривают при пониженном давлении и остаток очищают с помощью флэш-хроматографии на силикагеле и получают 5-[2-(4-хлорфенил)-5 метилселеназол-4-ил]-2,2,6,6-тетраметилпиран-3,5-дион. Пример 5. Получение 3-[2-(4-хлорфенил)-5-этилтиазол-4-ил]-1-метил-8-оксабицикло[3.2.1]октан-2,4-диона (соединение Т 50 в табл. Т 1) Пентахлорциклопропан (100 г, 0,467 моль) добавляют к суспензии гидроксида калия (31,4 г, 0,56 моль) в 1,4-диоксане (3600 мл) и смесь перемешивают при комнатной температуре в течение 30 мин и затем нагревают при 65 С в течение еще 30 мин. К реакционной смеси добавляют 2-метилфуран (38,36 г,0,467 моль), температуру повышают до 85-90 С и смесь перемешивают в течение 16 ч. Реакционную смесь охлаждают до комнатной температуры, фильтруют через слой диатомовой земли и фильтрат выпаривают в вакууме и полученный (1R,5S)-2,3,4,4-тетрахлор-1-метил-8-оксабицикло[3.2.1]окта-2,6-диен(83 г) используют на следующей стадии без дополнительной очистки. Стадия 2. Получение (1R,5S)-3,4-дихлор-5-метил-8-оксабицикло[3.2.1]окта-3,6-диен-2-она Нитрат серебра (166 г, 0,982 моль) при перемешивании добавляют к смеси (1R,5S)-2,3,4,4 тетрахлор-1-метил-8-оксабицикло[3.2.1]окта-2,6-диена (83 г, 0,491 моль), ацетона (1500 мл) и воды (1500 мл) и смесь нагревают при 65 С в течение 16 ч. Реакционную смесь охлаждают до комнатной температу- 28020695 ры и добавляют насыщенный водный раствор натрия бикарбонат для доведения значения рН до 7-8. Смесь фильтруют через слой диатомовой земли и фильтрат концентрируют в вакууме для удаления большей части ацетона. Водную смесь экстрагируют этилацетатом (3500 мл) и органические экстракты объединяют, сушат над безводным сульфатом натрия, фильтруют и фильтрат выпаривают. Остаток очищают с помощью флэш-хроматографии на колонке с силикагелем и получают (1R,5S)-3,4-дихлор-5 метил-8-оксабицикло[3.2.1]окта-3,6-диен-2-он (29,5 г) в виде желтого масла. Стадия 3. Получение 3-хлор-1-метил-4-оксоспиро(1,3-диоксолан-2,2'-[8]оксабицикло[3.2.1]окт-6-ена) Натрий (4,41 г, 0,204 моль) осторожно добавляют к этиленгликолю (99,75 г) и смесь перемешивают при 35-40 С в атмосфере азота до полного растворения натрия. По каплям в течение 30 мин добавляют раствор (1R,5S)-3,4-дихлор-5-метил-8-оксабицикло[3.2.1]окта-3,6-диен-2-она (28 г, 0,136 моль) в тетрагидрофуране (200 мл) и после завершения добавления смесь перемешивают в течение 90 мин при комнатной температуре. Реакционную смесь нейтрализуют путем добавления 10% водного раствора дигидрофосфата натрия и экстрагируют этилацетатом (3100 мл). Органические экстракты объединяют, сушат над безводным сульфатом натрия, фильтруют и фильтрат выпаривают. Остаток очищают с помощью флэш-хроматографии на колонке с силикагелем и получают 3-хлор-1-метил-4-оксоспиро(1,3-диоксолан 2,2'-[8]оксабицикло[3.2.1]окт-6-ен) (24,5 г) в виде смолы. Стадия 4. Получение (1R,5S)-1-метил-4-оксоспиро(1,3-диоксолан-2,2'-[8]оксабицикло[3.2.1]окт-6-ена) Порошкообразный цинк (13,88 г, 0,212 моль) добавляют к раствору 3-хлор-1-метил-4-оксоспиро(1,3 диоксолан-2,2'-[8]оксабицикло[3.2.1]окт-6-ена) (24,5 г, 0,016 моль) в уксусной кислоте (122,5 мл) и реакционную смесь перемешивают при комнатной температуре в течение 24 ч. Смесь разбавляют водой (612,5 мл) и экстрагируют этилацетатом (3150 мл). Органические экстракты объединяют, сушат над безводным сульфатом натрия, фильтруют и фильтрат выпаривают и получают (1R,5S)-1-метил-4-оксоспиро(1,3-диоксолан 2,2'-[8]оксабицикло[3.2.1]окт-6-ен) (20 г) в виде желтого масла, которое используют на следующей стадии без дополнительной очистки. Стадия 5. Получение (1R,5S)-1-метил-8-оксабицикло[3.2.1]окт-6-ен-2,4-диона Хлористо-водородную кислоту (50 мл) тремя порциями добавляют к смеси (1R,5S)-1-метил-4 оксоспиро(1,3-диоксолан-2,2'-[8]оксабицикло[3.2.1]окт-6-ена) (20 г, 0,102 моль) в ацетоне (500 мл) и воде(250 мл) и реакционную смесь перемешивают при 65-70 С в течение 48 ч. Смесь охлаждают до комнатной температуры, большую часть ацетона удаляют путем выпаривания при пониженном давлении и полученный водный раствор экстрагируют этилацетатом (3100 мл). Органические экстракты объединяют,сушат над безводным сульфатом натрия, фильтруют и фильтрат выпаривают. Остаток очищают с помощью флэш-хроматографии на колонке с силикагелем и получают (1R,5S)-1-метил-8 оксабицикло[3.2.1]окт-6-ен-2,4-дион (10,0 г) в виде желтого масла. Стадия 6. Получение (1R,5S)-1-метил-8-оксабицикло[3.2.1]октан-2,4-диона К раствору (1R,5S)-1-метил-8-оксабицикло[3.2.1]окт-6-ен-2,4-диона (12,0 г, 0,079 моль) в этилацетате (100 мл) добавляют 10% палладий на угле (2,4 г), затем перемешивают в атмосфере водорода при давлении 1 бар в течение 24 ч. Затем реакционную смесь фильтруют через диатомовую землю и концентрируют и получают неочищенный продукт, который очищают с помощью флэш-хроматографии (гексан/этилацетат), и получают (1R,5S)-1-метил-8-оксабицикло[3.2.1]октан-2,4-дион (6,90 г) в виде бледно-желтого твердого вещества. Стадия 7. Получение 4-хлор-1-метил-8-оксабицикло[3.2.1]окт-3-ен-2-она
МПК / Метки
МПК: C07D 403/04, C07D 293/06, C07D 277/24, C07D 333/10, C07D 409/04, A01N 43/76, A01N 43/78, C07D 417/04, C07D 263/32
Метки: производные, гербицидов, циклогексатрионов, пирандионов, качестве
Код ссылки
<a href="https://eas.patents.su/30-20695-proizvodnye-pirandionov-i-ciklogeksatrionov-v-kachestve-gerbicidov.html" rel="bookmark" title="База патентов Евразийского Союза">Производные пирандионов и циклогексатрионов в качестве гербицидов</a>
Предыдущий патент: Способ получения фторированных фенолов
Следующий патент: Способ лечения лимфомы ходжкина с использованием комбинации гемцитабина и конъюгата антитела против cd30 с ауристатином
Случайный патент: Колосник и колосниковая решетка












