Пестицидная композиция, содержащая синтетическое соединение, полезное в качестве агента образования клубней бобовых растений, и фунгицидное соединение
Формула / Реферат
1. Пестицидная композиция, содержащая:
а) соединение общей формулы (I)
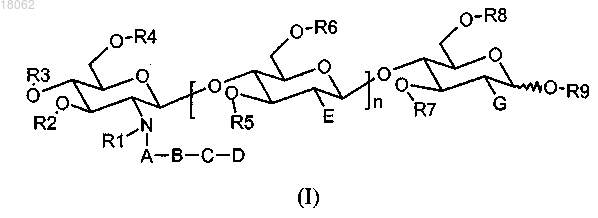
где n равно 2 или 3;
A представляет собой -С(O)-;
B представляет собой фенилен;
C представляет собой -O-;
D представляет собой линейную углеводородную цепь, содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода;
E и G независимо друг от друга представляют собой заместитель NHR20;
R1-R7 представляют собой Н;
R8 представляет собой заместитель, выбранный из Н, фукозила, метилфукозила, SO3H, SO3Li, SO3Na, SO3K, SO3N(C1-8алкила)4;
R9 представляет собой Н;
R20 представляет собой С(O)С1-6алкил;
а также их возможные геометрические и/или оптические изомеры, энантиомеры и/или диастереоизомеры, соли;
b) фунгицидное соединение, выбранное из группы, включающей N-[2-(1,3-диметилбутил)фенил]-5-фтор-1,3-диметил-1Н-пиразол-4-карбоксамид, металаксил, карбендазим, пенцикурон, фенамидон, флуоксастробин, трифлоксистробин, пириметанил, ипродион, битертанол, флуквинконазол, ипконазол, прохлораз, протиоконазол, тебуконазол, триадименол, тритиконазол, карпропамид, толифлуанид, флуопиколид, изотианил, N-{2-[1,1'-би(циклопропил)-2-ил]фенил}-3-(дифторметил)-, 1-метил-1Н-пиразол-4-карбоксамид, пропамокарб фосетилат, триазоксид, N-(3',4'-дихлор-5-фторбифенил-2-ил)-3-(дифторметил)-1-метил-1Н-пиразол-4-карбоксамид, N-{2-[3-хлор-5-(трифторметил)пиридин-2-ил]этил}-2-(трифторметил)бензамид в массовом соотношении (а)/(b) от 1/1 до 1/1014.
2. Композиция по п.1, в которой E и G представляют собой NHC(O)CH3.
3. Композиция по любому из пп.1 или 2, где R8 представляет собой Н, SO3H, SO3Li, SO3Na, SO3K, SO3N(С1-8 алкил)4 или заместитель формулы
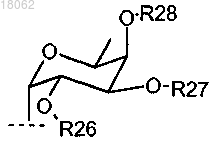
в которой R26 представляет собой заместитель, выбранный из Н и СН3;
R27 и R28 представляют собой Н.
4. Композиция по п.3, где R26, R27 и R28 представляют собой атом водорода.
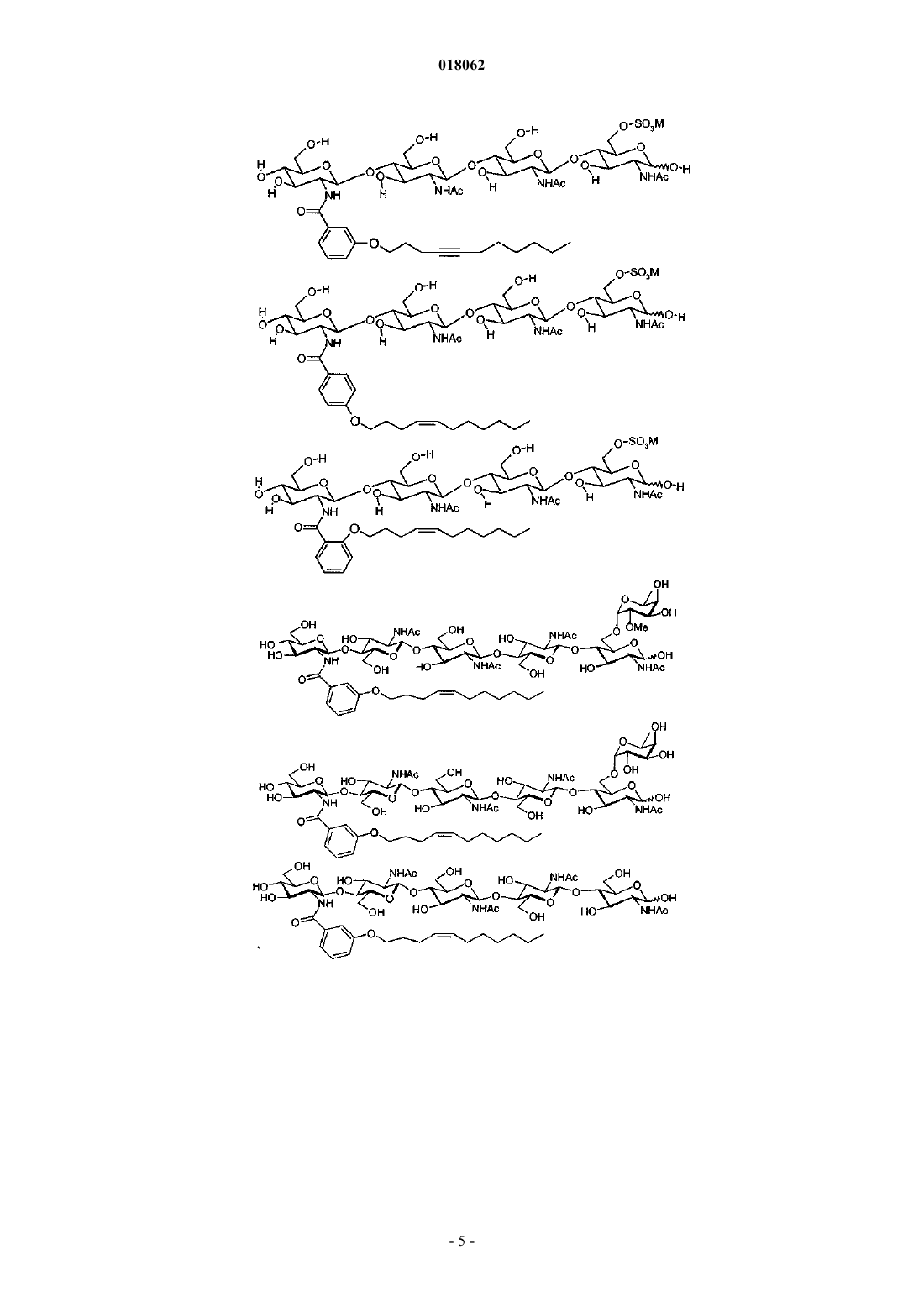
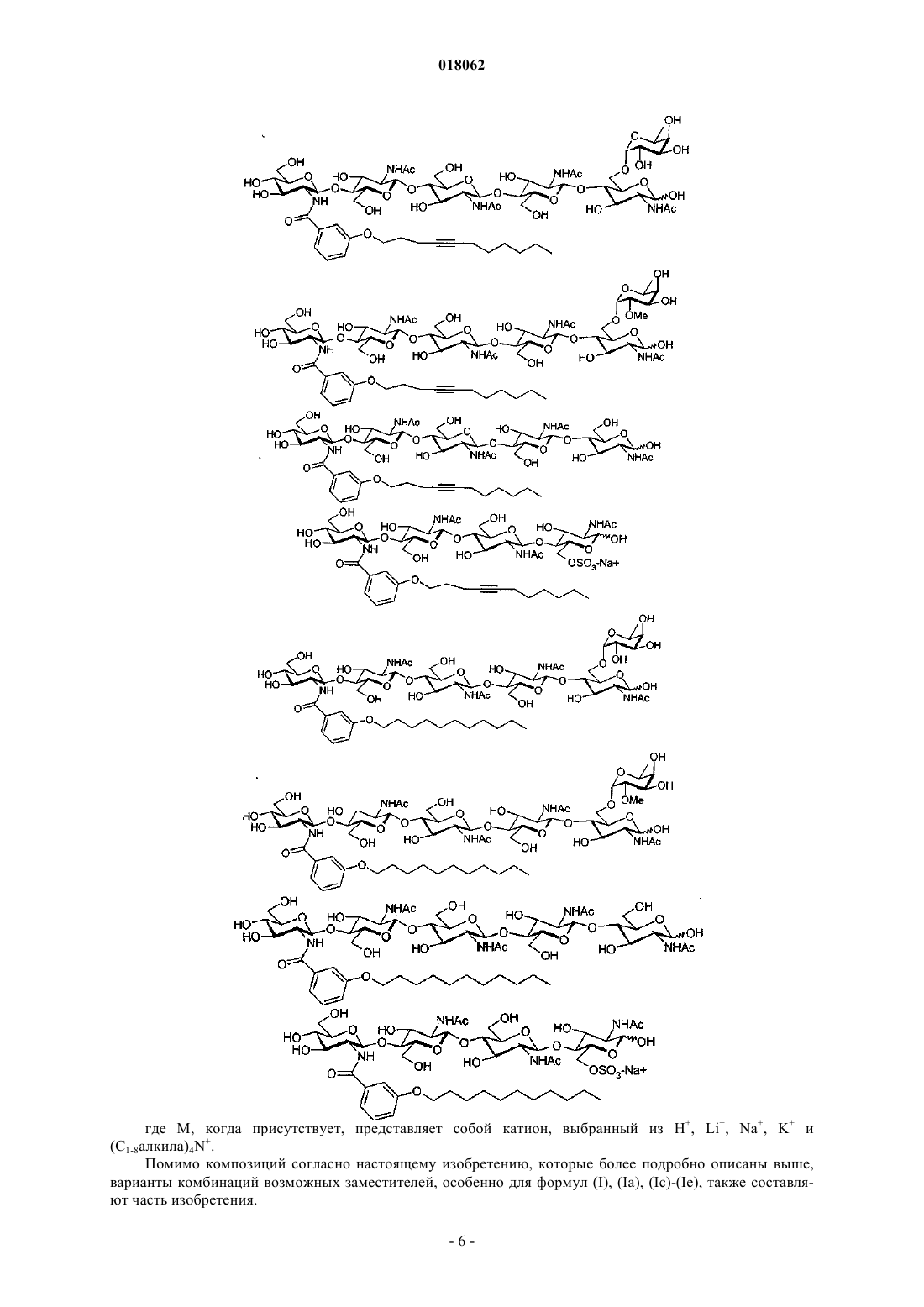
5. Композиция по любому одному из пп.1-3, в которой соединение (I) соответствует одной из следующих формул:
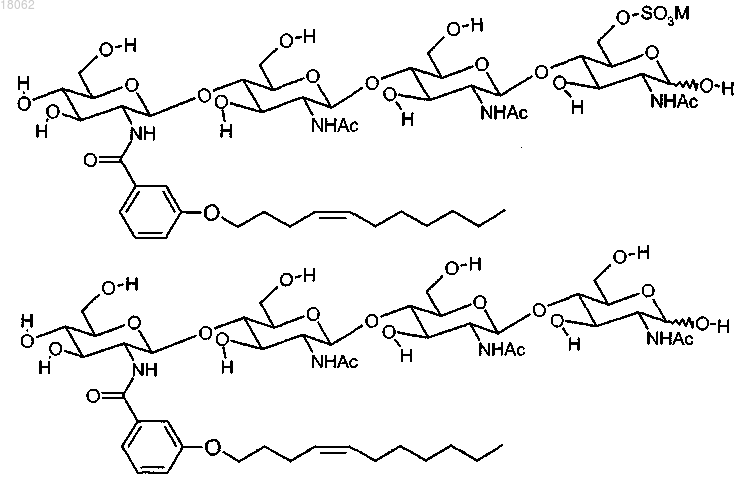
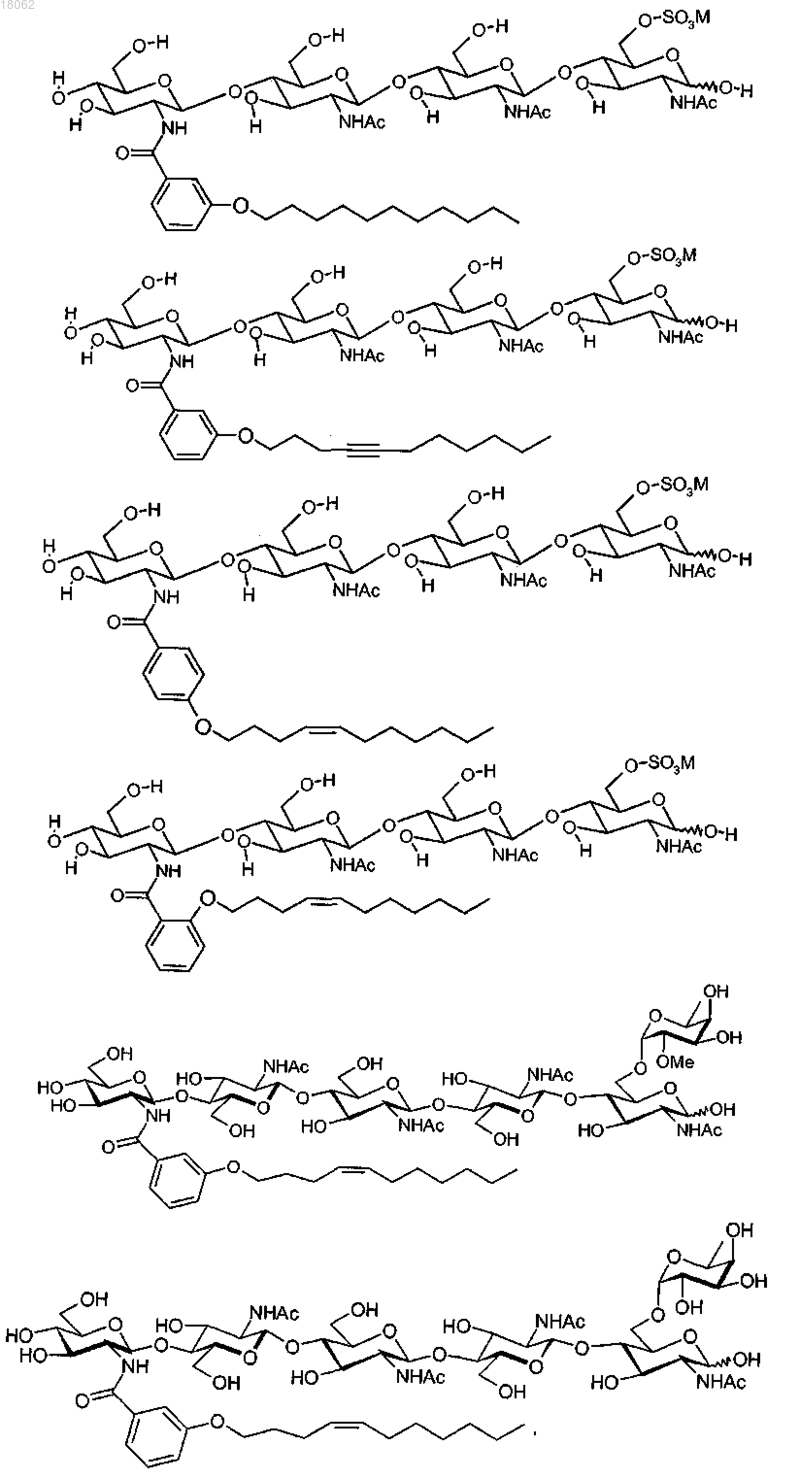
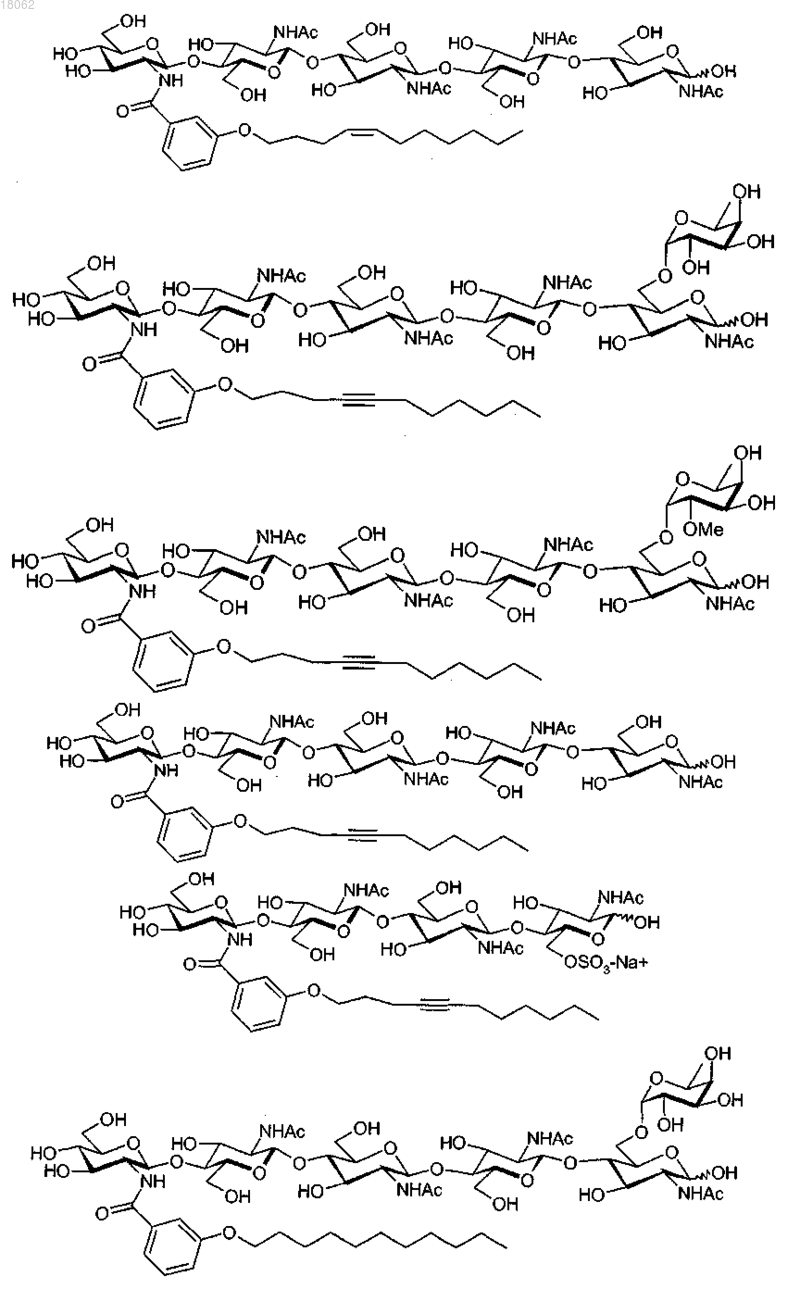
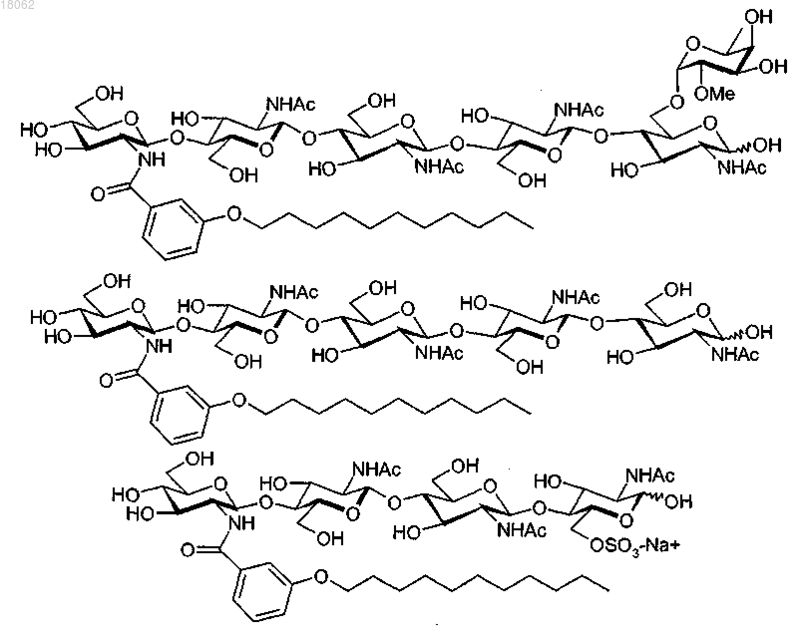
где М, когда присутствует, представляет собой катион, выбранный из Н+, Li+, Na+, K+ и (С1-8алкил)4N+.
6. Композиция по любому из пп.1-5, отличающаяся тем, что фунгицидное соединение (b) выбирают из группы, включающей протиконазол, металаксил, тебуконазол, трифлоксистробин и N-[2-(1,3-диметилбутил)фенил]-5-фтор-1,3-диметил-1Н-пиразол-4-карбоксамид.
7. Композиция по любому одному из пп.1-6, дополнительно содержащая фунгицидное соединение (с), отличающееся тем, что фунгицидное соединение (с) выбирают из группы, включающей N-[2-(1,3-диметилбутил)фенил]-5-фтор-1,3-диметил-1Н-пиразол-4-, металаксил, карбендазим, пенцикурон, фенамидон, флуоксастробин, трифлоксистробин, пириметанил, ипродион, битертанол, флуквинконазол, ипконазол, метконазол, прохлораз, протиоконазол, тебуконазол, триадименол, тритиконазол, карпропамид, толилфлуанид, флуопиколид, изотианил, N-{2-[1,1'-би(циклопропил)-2-ил]фенил}-3-(дифторметил)-, 1-метил-1Н-пиразол-4-карбоксамид, пропамокарб-фосетилат, триазоксид, N-(3',4'-дихлор-5-фторбифенил-2-ил)-3-(дифторметил)-1-метил-1Н-пиразо-4-карбоксамид и N-{2-[3-хлор-5-(трифторметил)пиридин-2-ил]этил}-2-(трифторметил)бензамид, и массовое соотношение (а)/(b/с) составляет от 1/1/1 до 1/1014/1014.
8. Композиция по любому одному из пп.1-7, отличающаяся тем, что дополнительно содержит сельскохозяйственно приемлемые подложку, носитель, наполнитель и/или поверхностно-активное вещество.
9. Способ повышения урожая сельскохозяйственных культур путем стимуляции роста растения с одновременной борьбой с фитопатогенными грибами, отличающийся тем, что эффективным и нефитотоксичным количеством композиции по любому одному из пп.1-8 обрабатывают семена, листья, стебли растения или промачивают/поливают (вносят с поливной водой) семена, растения и/или плоды растения, почву и/или инертный субстрат, пемзу, пирокластический материал/туф, синтетический органический субстрат, органический и/или жидкий субстрат, в котором растение произрастает или в котором его предполагается выращивать.
10. Способ по п.9, отличающийся тем, что композицию вносят в борозду на почве.
11. Способ по п.9 или 10, где культура представляет собой бобовое или небобовое растение.
12. Применение композиции по любому одному из пп.1-8 для повышения образования клубней у растения с одновременным уничтожением или профилактическим контролем фитопатогенных грибов.
13. Применение по п.12, отличающееся тем, что указанным растением является бобовое растение.
14. Применение композиции по любому одному из пп.1-8 для повышения урожая культур с одновременным уничтожением или профилактическим контролем фитопатогенных грибов.
15. Применение композиции по любому одному из пп.1-8 в качестве стимулятора роста растений с одновременным уничтожением или профилактическим контролем фитопатогенных грибов.
16. Применение по п.14 или 15, отличающееся тем, что указанное растение представляет собой бобовое растение или небобовое растение.
Текст
ПЕСТИЦИДНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ СИНТЕТИЧЕСКОЕ СОЕДИНЕНИЕ, ПОЛЕЗНОЕ В КАЧЕСТВЕ АГЕНТА ОБРАЗОВАНИЯ КЛУБНЕЙ БОБОВЫХ РАСТЕНИЙ, И ФУНГИЦИДНОЕ СОЕДИНЕНИЕ(а) общей формулы (I) и фунгицидное соединение (b) в массовом соотношении в интервале от 1/1 до 1/1014, а также к способу профилактической или лечебной борьбы с вредителями и болезнями культур и повышения их урожая посредством применения указанной композиции.(71)(73) Заявитель и патентовладелец: БАЙЕР КРОПСАЙЕНС АГ (DE) Изобретение относится к новым пестицидным композициям, содержащим синтетическое соединение, полезное в качестве агента образования клубней бобовых растений и/или в качестве стимулятора роста растений, и фунгицидное соединение. Кроме того, изобретение относится к способу уничтожения или контроля вредителей и болезней посредством нанесения такой композиции на очаг заражения или место, которое может подвергнуться заражению. В международной заявке на патент WO 2005/063784 приведены описания способа получения синтетических липохитоолигосахаридов (lipochito-oligoccharides-LCO) и некоторых из таких соединений, названных синтетическими LCO факторами, которые полезны в качестве агента образования клубней бобовых растений и/или стимуляторов роста растений. Синтетические LCO факторы структурно отличаются от Nod факторов, выделенных из природных бактериальных организмов, и проявляют различные свойства. В частности, некоторые биологически активные синтетические соединения проявляют сильную абсорбцию в ультрафиолетовой области, что дает возможность легко их анализировать в процессе промышленного получения и обнаруживать и анализировать в продукте, предназначенном для продажи,а также обеспечивает их стабильность и сохранение в таких продуктах, предназначенных для тестирования. Кроме того, некоторые из таких синтезированных соединений проявляют более высокую стабильность, чем природные Nod факторы. Кроме того, показана возможность объединения одного или нескольких таких синтетических соединений, полезных в качестве агента образования клубней бобовых растений и/или стимулятора роста растений, с известными фунгицидными или инсектицидными препаратами. Тем не менее, в указанной публикации не приведен ни конкретный потенциально фунгицидный компонент смеси, ни какое-либо массовое соотношение, при котором синтетический LCO фактор и фунгицидный компонент должны присутствовать в данной композиции. В международной заявке на патент WO 2005/062899 приведено описание смесей, содержащих природный Nod фактор и фунгицид. Природный Nod фактор, включенный в такую смесь, выделен очисткой из бактериальных источников или представляет собой синтетическую или биотехнологическую разновидность природных Nod-генных соединений. Однако при промышленном получении и кондиционировании природных Nod факторов приходится сталкиваться с проблемами двух типов:(1) природные Nod факторы трудно анализировать простыми методами, такими как спектрометрические методы;(2) они являются нестабильными в присутствии растений или в почвах, в частности, ввиду того, что содержат -CO-NH- связь, которая может разрушаться растением или микробиологическими ферментами,присутствующими в ризосфере. Новые пестицидные композиции, приведенные в настоящем описании, продемонстрировали значительное улучшение действия в виде смеси по сравнению с индивидуальными обработками в отношении роста растения, мощности или урожая бобовых и небобовых растений или зерновых культур и/или фунгицидного действия. Получено также значительное улучшение действия с точки зрения эффективности и стабильности смесей, включающих природный Nod фактор или синтетический или биотехнологический вариант такого природного Nod фактора и фунгицид. В сельском хозяйстве всегда проявлялся повышенный интерес к применению новых пестицидных смесей, демонстрирующих более широкий спектр активности. Авторами настоящего изобретения были разработаны некоторые новые пестицидные композиции,которые обладают указанными выше характеристиками. Соответственно настоящее изобретение относится к композиции, содержащей: а) соединение формулы (I)D представляет собой линейную углеводородную цепь, содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода; Е и G независимо друг от друга представляют собой заместитель NHR20; а также их возможные геометрические и/или оптические изомеры, энантиомеры и/или диастереоизомеры, соли;b) фунгицидное соединение, выбранное из группы, включающей N-[2-(1,3-диметилбутил)фенил]-5 фтор-1,3-диметил-1 Н-пиразол-4-карбоксамид, металаксил, карбендазим, пенцикурон, фенамидон, флуоксастробин, трифлоксистробин, пириметанил, ипродион, битертанол, флуквинконазол, ипконазол, прохлораз, протиоконазол, тебуконазол, триадименол, тритиконазол, карпропамид, толифлуанид, флуопиколид, изотианил, N-2-[1,1'-би(циклопропил)-2-ил]фенил-3-(дифторметил)-, 1-метил-1 Н-пиразол-4 карбоксамид,пропамокарб фосетилат,триазоксид,N-(3',4'-дихлор-5-фторбифенил-2-ил)-3(дифторметил)-1-метил-1 Н-пиразол-4-карбоксамид, N-2-[3-хлор-5-(трифторметил)пиридин-2-ил]этил 2-(трифторметил)бензамид в массовом соотношении (а)/(b) от 1/1 до 1/1014. Композиция согласно настоящему изобретению может обеспечивать синергический эффект. Такой синергический эффект дает возможность снижать количество химических веществ, распределяемых в окружающей среде, и снижать стоимость фунгицидной обработки. В контексте настоящего изобретения термин "синергический эффект" имеет значение, определенное Колби в статье "Calculation of the synergistic и antagonistic responses of herbicide combinations" Weeds,(1967), 15, p. 20-22. В указанной статье приводится формула где E представляет собой ожидаемое ингибирование болезни в процентах, которое вызвано совместным применением двух фунгицидов в указанных дозах (например, равных x и y соответственно);x представляет собой наблюдаемое ингибирование болезни в процентах, которое вызвано соединением (I) в определенной дозе (равной x);y представляет собой наблюдаемое ингибирование болезни в процентах, которое вызвано соединением (II) в определенной дозе (равной y). Когда при совместном применении наблюдаемое ингибирование, выраженное в процентах, составляет более Е, имеет место эффект синергизма. Среди соединений могут быть отмечены предпочтительные соединения формулы (I), обладающие одновременно следующими характеристиками:D представляет собой линейную основную углеводородную цепь, содержащую 11 атомов углерода,которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода;R8 представляет собой Н, SO3H, SO3Li, SO3Na, SO3K, SO3N(C1-8 алкил)4, фукозил или метилфукозил. Среди композиций согласно настоящему изобретению композиции, содержащие соединение (I), в котором A представляет собой карбонильную группу и которое может быть представлено формулой (Ia),являются особенно преимущественными:D представляет собой линейную углеводородную цепь, содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода; Е и G независимо друг от друга представляют собой заместитель NHR20;R20 представляет собой С(O)С 1-6 алкил,а также их возможные геометрические и/или оптические изомеры, энантиомеры и/или диастереоизомеры, соли; при этом среди соединений, определенных выше, наиболее важными соединениями являются соли,более конкретно литиевые, натриевые, калиевые или тетраалкиламмониевые соли. Среди соединений формулы (Ia) предпочтительными являются соединения, обладающие одной или несколькими из следующих характеристик, взятых по отдельности или в комбинации:R8 представляет собой Н, SO3H, SO3Li, SO3Na, SO3K, SO3N(C1-8 алкил)4, фукозил или метилфукозил. Среди композиций согласно настоящему изобретению особенно преимущественными являются композиции, содержащие соединение (I), в котором С представляет собой атом кислорода и которое может быть представлено формулой (Ic)D представляет собой линейную углеводородную цепь, содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода; Е и G независимо друг от друга представляют собой заместитель NHR20;R20 представляет собой С(O)С 1-6 алкил; а также их возможные геометрические и/или оптические изомеры, энантиомеры и/или диастереоизомеры, соли; при этом среди соединений, определенных выше, наиболее важными соединениями являются соли,более конкретно литиевые, натриевые, калиевые или тетраалкиламмониевые соли. Среди соединений формулы (Ic) предпочтительными являются соединения, обладающие одной или несколькими из следующих характеристик, взятых по отдельности или в комбинации:D представляет собой линейную углеводородную цепь, содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода; В представляет собой фенилен; Е и G представляют собой NHC(O)CH3;R8 представляет собой Н, SO3H, SO3Li, SO3Na, SO3K, SO3N(C1-8 алкил)4, фукозил или метилфукозил. Среди композиций согласно настоящему изобретению особенно преимущественными являются композиции, содержащие соединение (I), в котором А представляет собой карбонильную группу и которое может быть представлено формулой (Id)D представляет собой линейную углеводородную цепь, содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода; Е и G независимо друг от друга представляют собой заместитель, выбранный NHR20, предпочтительно NHC(O)CH3;R20 представляет собой -C(O)OC1-6 алкил; а также его возможные геометрические и/или оптические изомеры, энантиомеры и/или диастереоизомеры, соли; при этом среди соединений, определенных выше, наиболее важными соединениями являются соли,более конкретно литиевые, натриевые, калиевые или тетраалкиламмониевые соли. Среди композиций согласно настоящему изобретению особенно преимущественными являются композиции, содержащие соединение (I), в котором А представляет собой метиленовую группу и С представляет собой атом кислорода и которое может быть представлено формулой (Ie)D представляет собой линейную углеводородную цепь, содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода; Е и G представляют собой NHC(O)CH3;R20 представляет собой С(O)С 1-6 алкил,а также его возможные геометрические и/или оптические изомеры, энантиомеры и/или диастереоизомеры, соли; при этом среди соединений, определенных выше, наиболее важными соединениями являются соли,более конкретно, литиевые, натриевые, калиевые или тетраалкиламмониевые соли. Среди предпочтительных композиций согласно настоящему изобретению также могут быть особо подчеркнуты композиции, содержащие соединение (I), в которых Е и G представляют собой NHC(O)CH3,в частности соединения, где R8 представляет собой Н, SO3H, SO3Li, SO3Na, SO3K, и SO3N(C1-8 алкил)4,или заместитель формулыR27 и R28 независимо друг от друга представляют собой заместитель, выбранный из Н. В качестве примеров композиций согласно настоящему изобретению, которые являются особенно преимущественными и предпочтительными, могут быть приведены композиции, содержащие соединение, выбранное из перечня соединений L1 представленных ниже формул:(С 1-8 алкила)4N+. Помимо композиций согласно настоящему изобретению, которые более подробно описаны выше,варианты комбинаций возможных заместителей, особенно для формул (I), (Ia), (Ic)-(Ie), также составляют часть изобретения. Известно, что хитиновый олигомер, не содержащий липидной цепи, является неактивным, поэтому разложение Nod факторов посредством разрушения амидной связи в ризосфере приводит к потере активности. Для того чтобы снизить или даже предотвратить такое разложение, был получен ряд аналогичных соединений, некоторые из которых являются более стабильными, чем природные Nod факторы. Примеры таких соединений (I) согласно изобретению описаны ниже. Композиция согласно настоящему изобретению содержит фунгицидное соединение (b). Примеры подходящих фунгицидных компонентов смесей могут быть выбраны из следующих фунгицидных соединений, включающих N-[2-(1,3-диметилбутил)фенил]-5-фтор-1,3-диметил-1 Н-пиразол-4-карбоксамид,металаксил, карбендазим, пенцикурон, фенамидон, флуоксастробин, трифлоксистробин, пириметанил,ипродион, битертанол, флуквинконазол, ипконазол, прохлораз, протиоконазол, тебуконазол, триадименол, тритиконазол, карпропамид, толифлуанид, флуопиколид, изотианил, N-2-[1,1'-би(циклопропил)-2 ил]фенил-3-(дифторметил)-, 1-метил-1 Н-пиразол-4-карбоксамид, пропамокарб фосетилат, триазоксид,N-(3',4'-дихлор-5-фторбифенил-2-ил)-3-(дифторметил)-1-метил-1 Н-пиразол-4-карбоксамид,N-2-[3 хлор-5-(трифторметил)пиридин-2-ил]этил-2-(трифторметил)бензамид. Более предпочтительно фунгицидное соединение (b) выбирают из следующего перечня L2, включающего: протиконазол, металаксил, тебуконазол, трифлоксистробин и N-[2-(1,3-диметилбутил)фенил]5-фтор-1,3-диметил-1 Н-пиразол-4-карбоксамид. Композиция согласно настоящему изобретению включает соединение общей формулы (I) (а) и фунгицидное соединение (b) в массовом соотношении (а)/(b от 1/1 до 1/1014. Предпочтительно массовое соотношение (а)/(b) составляет от 1/10 до 1/1013. Наиболее предпочтительно массовое соотношение (а)/(b) составляет от 1/102 до 1/1012. Для некоторых областей применения, например, когда композиция применяют путем обработки семян, соотношение (а)/(b) преимущественно может составлять от 1/102 до 1/108,предпочтительно от 1/103 до 1/106, наиболее предпочтительно от 1/103 до 1/105. Специалист в данной области сможет определить подходящие соотношения, соответствующие способам применения и соединениям. Неограничивающие примеры подходящих смесей согласно настоящему изобретению могут включать смеси соединения, выбранного из перечня L1, с фунгицидным соединением, выбранным из перечняL2. Композиция согласно настоящему изобретению может дополнительно содержать по меньшей мере один другой фунгицидный активный ингредиент (с). Примеры подходящих компонентов для фунгицидной смеси могут быть выбраны из фунгицидных соединений (с) из группы, включающей N-[2-(1,3 диметилбутил)фенил]-5-фтор-1,3-диметил-1 Н-пиразол-4-, металаксил, карбендазим, пенцикурон, фенамидон, флуоксастробин, трифлоксистробин, пириметанил, ипродион, битертанол, флуквинконазол, ипконазол, метконазол, прохлораз, протиоконазол, тебуконазол, триадименол, тритиконазол, карпропамид,толилфлуанид, флуопиколид, изотианил, N-2-[1,1'-би(циклопропил)-2-ил]фенил-3-(дифторметил)-, 1 метил-1 Н-пиразол-4-карбоксамид, пропамокарб-фосетилат, триазоксид, N-(3',4'-дихлор-5-фторбифенил 2-ил)-3-(дифторметил)-1-метил-1 Н-пиразо-4-карбоксамид и N-2-[3-хлор-5-(трифторметил)пиридин-2 ил]этил-2-(трифторметил)бензамид. Когда в композиции присутствует третий активный ингредиент (с), который определен выше, данное соединение может присутствовать в количестве, обеспечивающем массовое соотношение (а), (b), (с) от 1/1/1 до 1/1014/1014. Предпочтительно массовое соотношение (а)/(b)/(с) составляет от 1/102/102 до 1/1012/1012. В некоторых применениях, например, когда композицию применяют путем обработки семян,соотношение (а)/(b)/(с) может преимущественно составлять от 1/102/102 до 1/108/108, предпочтительно от 1/103/103 до 1/106/106, наиболее предпочтительнее от 1/103/103 до 1/105/105. Специалист в данной области сможет определить подходящие соотношения, соответствующие способам применения и соединениям. Неограничивающие примеры подходящих смесей согласно настоящему изобретению могут включать соединение, выбранное из перечня L1, с первым фунгицидным соединением, выбранным из перечняL2, и вторым фунгицидом, отличным от первого фунгицида, выбранным из перечня L2. Композиция согласно настоящему изобретению может дополнительно содержать другой дополнительный компонент, например подложку, носитель или наполнитель, приемлемые с точки зрения сельскохозяйственного применения. В настоящем описании термин "подложка" означает природный или синтетический, органический или неорганический материал, с которым объединяется активный материал для более легкого нанесения,в частности, на части растения. Поэтому такая подложка обычно является инертной и должна быть приемлемой для сельскохозяйственного применения. Подложка может быть твердой или жидкой. Примеры подходящих подложек включают глины, природные или синтетические силикаты, диоксид кремния,смолы, воски, твердые удобрения, воду, спирты, в частности бутанол, органические растворители, минеральные и растительные масла и их производные. Также могут использоваться смеси таких подложек. Композиция также может содержать другие дополнительные компоненты. В частности, композиция может дополнительно содержать поверхностно-активное вещество. Поверхностно-активное вещество может представлять собой эмульгатор, диспергирующее вещество или смачивающий агент ионогенного или неионогенного типа или смесь таких поверхностно-активных веществ. Могут быть приведены, например, соли полиакриловой кислоты, соли лигносульфоновой кислоты, соли фенолсульфоновой или нафталинсульфоновой кислот, продукты реакции поликонденсации этиленоксида с жирными спиртами,жирными кислотами или жирными аминами, замещенные фенолы (в частности, алкилфенолы или арилфенолы), соли сложных эфиров сульфоянтарной кислоты, производные таурина (в частности, алкилтаураты), сложные эфиры фосфорной кислоты и полиоксиэтилированных спиртов или фенолов, сложные эфиры жирных кислот и многоатомных спиртов и производные указанных выше соединений, содержащие сульфатную, фульфонатную и фосфатную функциональные группы. Обычно присутствие по меньшей мере одного поверхностно-активного вещества имеет большое значение, когда активное вещество и/или инертная подложка являются растворимыми в воде и когда средой для применения является вода. Предпочтительно содержание поверхностно-активного вещества может составлять от 5 до 40% из расчета на массу композиции. Также могут быть включены дополнительные компоненты, например, защитные коллоиды, адгезивы, загустители, тиксотропные добавки, добавки, повышающие проницаемость, стабилизаторы, связующие соединения. В целом, активные вещества могут объединяться с любой твердой или жидкой добавкой, которая соответствует обычным методам получения препаратов. Как правило, композиция согласно изобретению может содержать от 0,05 до 99% (мас.) активного ингредиента, предпочтительно от 10 до 70% (мас.). Композиции согласно настоящему изобретению могут использоваться в различных формах, таких как препарат с дозатором для получения аэрозоля, суспензия капсул, концентрат для холодного туманообразования, распыляемый порошок, концентрат эмульсии, эмульсия типа "масло-в-воде", эмульсия типа"вода-в-масле", инкапсулированная гранула, мелкозернистая гранула, текучий концентрат для обработки семян, газ (под давлением), газогенерирующий препарат, гранула, концентрат для горячего туманообразования, макрогранула, микрогранула, порошок, диспергируемый в масле, текучий концентрат, смешиваемый с маслом, жидкость, смешиваемая с маслом, паста, растительный стержень, порошок для сухой обработки семян, зерно, покрытое пестицидом, растворимый концентрат, растворимый порошок, раствор для обработки семян, концентрат суспензии (текучий концентрат), жидкость для ультрамалообъемного(УМО) опрыскивания, суспензия для ультрамалообъемного (УМО) опрыскивания, вододиспергируемые гранулы или таблетки, вододиспергируемый порошок для обработки взвесью, растворимые в воде гранулы или таблетки, растворимый в воде порошок для обработки семян и смачивающийся порошок. Такие композиции включают не только композиции, которые готовы для нанесения на растение или семена, подлежащие обработке, или внесения в борозду почвы с помощью подходящего устройства, такого как устройство для опрыскивания или распыления, но также концентрированные коммерческие композиции, которые необходимо разбавлять перед нанесением на культуру. Пестицидные композиции согласно настоящему изобретению могут применяться для лечебного или профилактического контроля фитопатогенных грибов культур, а также для повышения урожая, увеличения роста или мощности растения. Таким образом, в соответствии с еще одним аспектом настоящего изобретения предоставлен способ лечебного или профилактического контроля фитопатогенных грибов культур и повышения урожая, роста и мощности растения, где указанный способ отличается тем, что композицию, которая определена выше,применяют путем обработки семян, листьев, путем нанесения на стебель или на семена, растение и/или плоды растения орошением/погружением (хемигацией) или внесением в почву, в частности в борозду и/или на инертную подложку (например, неорганические субстраты (например, песок, минеральный войлок, стекловату, вспененные минеральные вещества (например, перлит, вермикулит, цеолит, керамзит,пемзу, пирокластические материалы/туф, синтетические органические субстраты (например, полиуретан), органические субстраты (например, торф, компосты, опавшую листву (например, кокосовые волокна, древесное волокно/древесная щепа, древесная кора и/или жидкий субстрат (например, плавучие гидропонные системы, метод питательной пленки, аэропоники), в котором растение выращивается или должно выращиваться. Композиция, когда используется против фитопатогенных грибов, содержит эффективное и нефитотоксичное количество фунгицидного соединения. Выражение "эффективное и нефитотоксичное количество" означает количество композиции согласно изобретению, которое достаточно для контроля и уничтожения вредителей и болезней, присутствующих или способных появиться на культурах, и которое не вызывает какого-либо симптома фитотоксичности на указанных культурах. Такое количество может изменяться в широких пределах в зависимости от видов вредителей и болезней, подлежащих уничтожению или контролю, типа культуры, климатических условий и соединений, включенных в композицию согласно изобретению. Такое количество может определяться с помощью методических полевых испытаний, которые может осуществить специалист данной области. Способ обработки согласно настоящему изобретению может быть использован для обработки материала размножения, такого как клубни или корневища, а также семян, саженцев или пикированных сеянцев, растений или пикированной рассады. Такой способ обработки также может применяться для обра-8 018062 ботки корней. Способ обработки согласно настоящему изобретению также может применяться для обработки надземных частей растения, таких как стволы, стебли или цветоножки, листья, цветы и плоды целевого растения. Растения, которые могут защищаться способом согласно изобретению, могут представлять собой бобовые или небобовые растения. Среди растений, которые могут защищаться способом согласно настоящему изобретению, могут быть указаны хлопчатник; лен; виноградная лоза; плодовые или овощные культуры, такие как Rosaceaesp. (например, односемянный плод, такой как яблоки и груши, а также косточковый плод, такой как абрикосы, миндаль и персики), Ribesioidae sp., Juglandaceae sp., Betulaceae sp., Anacardiaceae sp., Fagaceaesp., Moraceae sp., Oleaceae sp., Actinidaceae sp., Lauraceae sp., Musaceae sp. (например, банановые деревья и плантации), Rubiaceae sp., Theaceae sp., Sterculiceae sp., Rutaceae sp. (например, лимоны, апельсины и грейпфрут); Solanaceae sp. (например, томаты), Liliaceae sp., Asteraceae sp. (например, салаты),Umbelliferae sp., Cruciferae sp., Chenopodiaceae sp., Cucurbitaceae sp., Papilionaceae sp. (например, горох),Rosaceae sp. (например, земляника); основные зерновые культуры, такие как Graminae sp. (например,кукуруза, газонные травы или зерновые, такие как пшеница, рис, ячмень и тритикале), Asteraceae sp. (например, подсолнечник), Cruciferae sp. (например, рапс), Fabacae sp. (например, арахис), Papilionaceae sp.(например, соя), Solanaceae sp. (например, картофель), Chenopodiaceae sp. (например, свекла); садовые культуры и лесные насаждения; а также генетически модифицированные гомологи указанных культур. Среди бобовых культур могут быть приведены соя, горох, конские бобы, арахис, бобы, люпин, люцерна или клевер. Среди болезней растений или культур, которые могут контролироваться способом согласно настоящему изобретению, могут быть приведены следующие. Различные виды настоящей мучнистой росы, такие как мучнистая роса, вызываемая грибами рода блумерия (Blumeria), например возбудителем Blumeriagraminis; мучнистая роса, вызываемая грибами рода подосфера (Podosphaera), например возбудителемPodosphaera leucotricha; мучнистая роса, вызываемая грибами рода сферотека (Sphaerotheca), например возбудителемSphaerotheca fuliginea; мучнистая роса или оидиум, вызываемая грибами рода унцикула (Uncinula), например возбудителем Uncinula necator. Различные виды ржавчин, такие как ржавчины яблони, груши вызванные грибами рода гимноспорангиум (Gymnosporangium), например возбудителем Gymnosporangium sabinae; ржавчины, вызываемые ржавчинными грибами рода гемилия (Hemileia), например возбудителемHemileia vastatrix; ржавчины сои, вызванные грибами рода факопсора (Phakopsora), например возбудителемPhakopsora pachyrhizi или Phakopsora meibomiae; ржавчины злаков, вызванные грибами рода пуциния (Puccinia), например возбудителем Pucciniarecondita; ржавчины, вызванные грибами рода уромицес (Uromyces), например возбудителем Uromycesappendiculatus. Болезни, вызванные грибами класса оомицетов (Oomycete), такие как болезни, вызванные грибами рода бремия (Bremia), например возбудителем ложной мучнистой росы Bremia lactucae; пероноспорозы, вызванные грибами рода пероноспора (Peronosporaj, например возбудителемPeronospora pisi или Р.brassicae; фитофторозы, вызванные грибами рода фитофтора (Phytophthora), например возбудителемPhytophthora infestans; ложные мучнисто-росяные болезни, вызванные грибами рода плазмопара (Plasmopara), например возбудителем Plasmopara viticola; пероноспорозы, вызванные грибами рода псевдопероноспора (Pseudoperonospora), например возбудителем Pseudoperonospora humuli или Pseudoperonospora cubensis; питиозные болезни, вызванные грибами рода питиум (Pythium), например возбудителем Pythiumultimum. Пятнистости листьев, окаймленные пятнистости листьев и болезни увядания листьев, такие как альтернариозы, вызванные грибами рода альтернария (Alternaria), например возбудителем Alternariasolani; церкоспорозы, вызванные грибами родом церкоспора (Cercospora), например возбудителемCercospora beticola; кладоспориозы, вызванные грибами рода кладоспориум (Cladiosporum), например возбудителем болезни, вызванные грибами рода колиоболюс (Cochlio bolus), например возбудителем Cochliobolussativus; болезни, вызванные грибами рода коллетотрихиум (Colletotrichum), например возбудителемColletotrichum lindemuthanium; болезни, вызванные грибами рода циклониум (Cycloconium), например возбудителем Cycloconiumoleaginum; диапортозы, вызванные грибами рода диапорте (Diaporthe), например возбудителем Diaporthe citri; болезни, вызванные грибами рода эльсиное (Elsinoe), например возбудителем Elsinoe fawcettii; болезни, вызванные грибами рода глоеоспориум (Gloeosporium), например возбудителемGloeosporium laeticolor; болезни, вызванные грибами рода гломерелла (Glomerella), например возбудителем Glomerellacingulata; болезни, вызванные грибами рода гиньярдия (Guignardia), например возбудителемGuignardia bidwelli; лептосфериозы, вызванные грибами рода лептосферия (Leptosphaeria), например возбудителемLeptosphaeria maculans или Leptosphaeria nodorum; болезни, вызванные грибами рода магнапорте (Magnaporthe), например возбудителем Magnaporthegrisea; болезни, вызванные грибами рода микосферелла (Mycosphaerella), например возбудителемMycosphaerella graminicola, Mycosphaerella arachidicola или Mycosphaerella fijiensis; пятнистости феосфереллезные, вызванные грибами рода феосферия (Phaeosphaeria), например возбудителем Phaeosphaeria nodorum; пятнистости гельминтоспориозные, вызванные грибами рода пиренофора (Pyrenophora), например возбудителем Pyrenophora teres; рамуляриозы, вызванные грибами рода рамулярия (Ramularia), например возбудителем Ramulariacollo-cygni; ринхоспориозы, вызванные грибами рода ринхоспориум (Rhynchosporium), например возбудителемRhynchosporium secalis; септориозы, вызванные грибами рода септория (Septoria), например возбудителем Septoria apii илиSeptoria lycopercisi; тифулезы, вызванные грибами рода тифула (Typhula), например возбудителем Typhula incarnata; паршовые болезни, вызванные грибами вентурия (Venturia), например Venturia inaequalis. Болезни корней и стеблей, такие как болезни, вызванные грибами рода кортициум (Corticium), например возбудителем Corticiumgraminearum; фузариозы, вызванные грибами рода фузариум (Fusarium), например возбудителем Fusariumoxysporum; офиоболзы, вызванные грибами рода геуманномицес (Gaeumannomyces), например возбудителемGaeumannomyces graminis; ризоктониозы, вызванные грибами рода ризоктония (Rhizoctonia), например возбудителемRhizoctonia solani; болезни, вызванные грибами рода тапезия (Tapesia), например возбудителем Tapesia acuformis; корневые гнили, вызванные грибами рода тиелавиопсис (Thielaviopsis), например возбудителемThielaviopsis basicola. Болезни колоса и метелки, такие как альтерназиозы, вызванные грибами рода альтернария (Alternaria), например возбудителямиAlternaria spp.; плесени аспергиллзные, вызванные грибами рода аспергиллиус (Aspergillus), например возбудителем Aspergillus flavus; кладоспорилзы, вызванные грибами рода кладоспориум (Cladosporium), например возбудителямиCladosporium spp.; спорыньвые болезни, вызванные грибами рода клавицепс (Claviceps), например возбудителемClaviceps purpurea; фузариозы, вызванные грибами рода фузариум (Fusarium), например возбудителемFusarium culmorum; гиббереллзы, вызванные грибами рода гибберелла (Gibberella), например возбудителемGibberella zeae; болезни, вызванные грибами рода монографелла (Monographella), например возбудителемMonographella nivalis. Головни и твердые головни, такие как пыльные головни, вызванные грибами рода сфацелотека (Sphacelotheca), например возбудителем твердые головни, вызванные грибами рода тиллетиа (Tilletia), например возбудителем Tilletia caries; пыльные головни стеблей, вызванные грибами рода уроцистис (Urocystis), например возбудителемUrocystis occulta; пыльные головни стеблей, вызванные грибами рода устилаго (Ustilago), например возбудителемUstilago nuda. Плодовые гнили и плесени, такие как аспергиллезные плесени, вызванные грибами рода аспергиллус (Aspergillus), например возбудителем Aspergillus flavus; гнили, вызванные грибами рода ботритис (Botrytis), например возбудителем Botrytis cinerea; плесени, вызванные грибами рода пенициллиум (Penicillium), например возбудителем Penicilliumexpansum; склеротиниозы, вызванные грибами рода склеротиния (Sclerotinia), например возбудителемSclerotinia sclerotiorum; вертициллезы, вызванные грибами рода вертицилиум (Verticilium), например возбудителемVerticilium alboatrum. Болезни, характеризующиеся гнилью, плесенью, увяданием, разложением и выпреванием растений,которые передаются через семена и почвы, такие как фузариозные гнили, вызванные грибами рода фузариум, например возбудителем Fusariumculmorum; фитофторозные гнили, вызванные грибами рода фитофтора (Phytophthora), например возбудителемPhytophthora cactorum; полегания, вызванные грибами рода питиум (Pythium), например возбудителем Pythium ultimum; ризоктониозы, вызванные грибами рода ризоктония (Rhizoctonia), например возбудителемRhizoctonia solani; склероциальные гнили, вызванные грибами рода склеротиум (Sclerotium), например возбудителемSclerotium rolfsii; болезни, вызванные грибами рода микродихум (Microdochium), например возбудителемMicrodochium nivale. Раковые болезни растений, кустистости и отмирания верхних побегов растений, такие как болезни,вызванные грибами рода нектриа (Nectria), например возбудителем Nectria galligena. Болезни растений, характеризующиеся завядание, гниением или прекращением роста, такие как монилиозы, вызванные грибами рода монилиниа (Monilinia), например возбудителем Monilinia laxa. Скручивания или курчавости листьев, такие как болезни, вызванные грибами рода тафринаPhaemoniella clamydospora. Болезни цветов и семян, такие как болезни, вызванные грибами рода ботритис (Botrytis), например возбудителем Botrytis cinerea. Болезни клубней, такие как резоктониозы, вызванные грибами рода ризоктония (Rhizoctonia), например возбудителем Rhizoctonia solani. Фунгицидная композиция согласно настоящему изобретению также может применяться против болезней, вызываемых грибами, которые могут произрастать на лесоматериале или внутри него. Термин"лесоматериал" означает все типы древесных пород и все типы обработки такой древесины, предназначенной для конструирования, например, тяжелую древесину, древесину высокой плотности, ламинированную древесину и фанеру. Способ обработки древесины согласно изобретению состоит, главным образом, в контактировании с одним или несколькими соединениями согласно настоящему изобретению или композиции согласно изобретению; причем он включает, например, непосредственное нанесение, опрыскивание, погружение, инъекцию или любые другие подходящие способы. Композиция согласно настоящему изобретению также может применяться для обработки генетически модифицированных организмов соединениями или агрохимическими композициями согласно изобретению. Генетически модифицированные растения представляют собой растения, в геном которых был стабильно введен гетерологический ген, кодирующий заданный белок. Выражение "гетерологический ген, кодирующий заданный белок", по существу, означает гены, которые придают трансформированному растению новые агрономические свойства, или гены, улучшающие агрономическое качество трансформированного растения. Доза активного вещества, обычно используемая для обработки согласно настоящему изобретению,как правило и преимущественно, при обработке листьев составляет от 10 до 800 г/га, предпочтительно от 50 до 300 г/га. Если возможно применение орошения/капельного введения/введения в борозду, доза может быть ниже, особенно на искусственных субстратах, таких как минеральный войлок или перлит. При обработке семян доза применения активного вещества, обычно и преимущественно, составляет от 0,5 до 200 г на 100 кг семян, предпочтительно от 1 до 150 г на 100 г семян. Следует понимать очевидно, что дозы, указанные выше, приведены в качестве иллюстративных примеров изобретения. Специалисту в данной области будет понятно, как привести величину дозы в соответствие с природой культуры, подлежащей обработке.II-1. Структура соединений (I) согласно изобретению. Синтезированы соединения, содержащие метазамещенную бензамидную группу. Предпочтительно сохранять одинаковое общее количество атомов в цепи (16), а также ненасыщенность цис-типа в положении 9. На практике для получения исходных веществ липидная цепь может присоединяться к ароматическому кольцу через атом кислорода Получены также аналог 4, содержащий метазамещенную бензиламинную функциональную группу,и N-ацетилированный аналог 5, который дает возможность производить возврат общего изменения природного соединения к исходному состоянию. Указанные аналоги были получены в сульфатированных сериях Два других сульфатированных аналога: один, содержащий полностью насыщенную цепь, и другой,содержащий ненасыщенную цепь алкинового типа, дают возможность изучить влияние ненасыщенности Наконец, два сульфатированных аналога, в одном из которых замещение на ароматическом кольце находится в орто-положении, в другом - в пара-положении, дают возможность изучить влияние ненасыщенности транс-типа, находящейся в природном соединении в положении 2 И, наконец, был получен аналог фукозильного пентамера, содержащий метазамещение в цепи Ссылки в биологических испытаниях сделаны на следующие соединения:III.1 Примеры получения различных основных олигосахаридных структур макромолекулы. Основные олигосахаридные структуры, соответствующие формуле (I), могут быть получены биотехнологическими способами, такими как, например, применение рекомбинантных бактериальных клеток, таких как, например, рекомбинантные клетки Escherichia coli, содержащие гетерологический ген микоризы. Например, введение nod.BC генов из Azorhizobium caulinodans в Escherichia coli дает возможность получить тетра-N-ацетилхитопентаозу (Samain E., et al. Carbohydr. Res., 1997, 302, 35-42). Применение nodBC из Rhizobium meliloti дает возможность получить три-N-ацетилхитотетраозу. Кроме того,применение дополнительных генов, таких как, например, nodH (микоризная сульфотрансфераза) илиnodL (микоризная О-ацетилтрансфераза) дает возможность вводить модификации на конкретные гидроксильные группы (Samain E, et al., J. Biotechnol., 1999, 72, 33-47). Другие комбинации микоризных или немикоризных генов дают возможность получить различные хитоолигосахаридные цепи, которые могут использоваться в качестве исходных веществ для ацилирования с целью получения молекул формулы (I) с различными модификациями на гидроксильных или аминогруппах. Основные олигосахаридные структуры макромолекул также могут быть получены стандартным химическим синтезом с использованием методов и стратегий, которые являются классическими и хорошо описаны в химии углеводородов. Описание новых подходящих методик можно найти во многих руководствах и ссылках и, например, в публикации Carbohydrates in Chemistry and Biology, Editors.:B. Ernst, G.W. Hart, P. Sinay, Wiley-VCH, Weinheim; 2000. Точный подбор подходящих защитных групп,которые могут вводиться в точно выбранные положения на гидроксильных или аминогруппах и последовательно или одновременно удаляться с целью высвобождения любой данной группы для селективной модификации, дает возможность вводить специфические модификации в основную олигосахаридную цепь, включая, например, ацилирование, алкилирование или гликозилирование специфических гидроксильных групп или ацилирование и алкилирование специфических аминогрупп. Защитные группы, которые могут использоваться для защиты аминов и которые могут удаляться последовательно или одновременно, включают, например, фталимидную, тетрахлорфталимидную, азидо,трет-бутилоксикарбонильную, 2,2,2-трихлорэтоксикарбонильную и трихлорацетильную группы. Защитные группы, которые могут использоваться для защиты спиртов и которые могут удаляться последовательно или одновременно, включают, например, ацетильную, бензильную, п-метоксибензильную, триметилсилильную, триэтилсилильную, трет-бутилдиметилсилильную и трет-бутилдифенилсилильную группы, а также циклические ацетали, такие как, например, метилиден-, этилиден-, изопропилиден-, бензилиден- или п-метоксибензилиденацетали. Классические способы и условия использования защитных групп можно найти, например, в публикации "Protecting Groups", P.J. Kocienski, 2nd Edition, Georg ThiemeVeRlag, Stuttgart, 2000 или "Protective Groups in Organic Synthesis", T.W. Greene, P.G.M. Wuts, 3rd Edition,Wiley, New York, 1999. Основные олигосахаридные структуры могут быть получены контролируемой сборкой упорядоченной структуры из моносахаридных структурообразующих блоков, содержащих конкретно выбранные защитные группы в нужных положениях. Такая сборка упорядоченной структуры может быть осуществлена в соответствии со способами, которые являются классическими и стандартно применяются в области химического синтеза олигосахаридов. Последовательное удаление защитных групп с последующей модификацией высвобожденных гидроксильных или аминогрупп дает возможность получения молекулы, соответствующей формуле (I). Примеры введения других сахаров, представленных фукозильным фрагментом, можно без труда найти в предшествующем уровне, включая, например, публикацииA.I. Zinin et al., Russ. Chem. Bull., 1998, 47, 496-501, J.S. Debenham et al., J. Org. Chem., 1996, 61, 64786479. Классические способы сборки упорядоченной структуры из моносахаридов включают, например,активацию аномерных трихлорацетимидатной, О-пентенильной, алкилтио-, арилтио-, сульфоксидо-, галогено- или фосфатогрупп. Большое количество примеров синтеза олигосахаридов можно обнаружить во множестве литературных ссылок, в ряде монографий, указанных выше, или, например, в публикации"Glycoscience, Chemistry and Chemical Biology", Editors: B. Fraser-Reid, K. Tatsuta, J. Thiem, SpringerVerkag, BeRlin Heidelberg, 2001. Известно, что соединения формулы (I) могут быть химически синтезированы в соответствии с конкретной методикой, описанной ниже (на данной схеме PxH на аминогруппах может также представлять собой защитную группу, такую как, например, фталимидо- или тетрахлорфталимидозащитная группа,или N2, если в положении 2 карбогидрата находится азидогруппа). P1-P20 представляют собой либо временно введенные защитные группы, либо перманентно введенные модификации, которые желательны в конечной основной цепи, такие как, например, ацильные, алкильные и гликозильные группы. Х 1-Х 4 представляют собой аномерные, способные активироваться удаляемые группы, такие как, например,трихлорацетимидатная, О-пентенильная, алкилтио-, арилтио-, сульфоксидо-, галогено- или фосфатогруппы. Два моносахарида с правильно подобранной схемой размещения защитных групп могут объединяться вместе в соответствии с одной из стандартных методик гликозилирования. Правильно выбранная защитная группа (Р 6) может быть селективно удалена из нужного положения полученного дисахарида в условиях, которые не будут влиять на другие защитные группы. Присоединение другого моносахарида в только что освобожденное положение будет приводить к получению трисахарида. После удаления правильно выбранной защитной группы (Р 10) из полученного трисахарида в условиях, которые не будут влиять на другие защитные группы, может быть проведено присоединение другого моносахарида в только что освобожденное положение с получением тетрасахарида. После удаления правильно выбранной защитной группы (Р 14) из полученного тетрасахарида в условиях, которые не будут влиять на другие защитные группы, может быть осуществлено присоединение другого моносахарида в только что освобожденное положение с получением пентасахарида. Удаление любой правильно выбранной защитной группы из гидроксильной или аминогруппы полученного пентасахарида в условиях, которые не будут влиять на другие защитные группы, дает возможность осуществить специфическую химическую модификацию,такую как, например, ацилирование, алкилирование или гликозилирование, в данном положении. Такой процесс можно повторять много раз, когда необходимо ввести все желаемые модификации в основную цепь. Последнее удаление оставшихся защитных групп дает возможность получения желаемой основной цепи макромолекулы Характерные примеры такой стратегии могут быть найдены в предшествующем уровне, например в публикации K.С. Nicolaou et al., J. Am. Chem. Soc., 1992, 114, 8701. Известно также, что соединения формулы (I) могут быть химически синтезированы в соответствии с другой конкретной методикой, описанной ниже (на данной схеме PxH на аминогруппах также может представлять собой защитную группу, такую как, например, фталимидо-, тетрахлорфталимидозащитную группу или N2, если в положении 2 карбогидрата находится азидогруппа). Р 1-Р 16 представляют собой либо временно введенные защитные группы, либо постоянно введенные модификации, которые желательны в конечной основной цепи, такие как, например, введенные ацильные, алкильные и гликозильные группы. Х 1-Х 4 представляют собой аномерные, способные активироваться удаляемые группы,такие как, например, трихлорацетимидатная, О-пентенильная, алкилтио-, арилтио-, сульфоксидо-, галогено- или фосфатогруппы. Y1-Y4 представляют собой либо защитные группы, либо другие стабильные группы, которые могут трансформироваться в способные активироваться удаляемые группы, такие как,например, трихлорацетимидатная, О-пентенильная, алкилтио-, арилтио-, сульфоксидо-, галогено- или фосфатогруппы. Два моносахарида, содержащие правильно подобранную схему защиты, могут связываться в соответствии со стандартной методикой гликозилирования. Активация правильно выбранной защитной группы (Y1) дает возможность введения аномерной активируемой группы X2, которая даст возможность связывания полученного дисахарида с другим моносахаридом. Активация правильно подобранной группы (Y2) даст возможность введения аномерной активируемой группы X3, которая позволит связать полученный трисахарид с другим моносахаридом. Активация правильно выбранной группы(Y4) даст возможность введения аномерной активируемой группы X3, которая позволит связать полученный тетрасахарид с другим моносахаридом с получением пентасахарида. Удаление любой правильно выбранной защитной группы из гидроксильной или аминогруппы полученного пентасахарида в услови- 14018062 ях, которые не влияют на другие защитные группы, даст возможность ввести в данное положение специфические химические модификации, такие как, например, ацилирование, алкилирование или гликозилирование. Этот процесс можно повторять множество раз, когда это необходимо, для введения всех желаемых модификаций в основную структуру макромолекулы. Последнее удаление оставшихся защитных групп даст возможность получить желаемую основную структуру Характерные примеры такой стратегии могут быть найдены в предшествующем уровне, в том числе, например, в публикации D. Tailler et al., J. Chem. Soc, Chem. Commun., 1994, 1827; J.S. Debenham etal., J. Org. Chem., 1997, 62, 4591-4600. Помимо двух основных примеров, приведенных выше, которые заключаются в добавлении моносахарида на каждом "цикле" стадий, типичные примеры других стратегий также могут быть обнаружены в предшествующем уровне, такие как, например, добавление полученного подходящим способом дисахарида вместо моносахарида. Такой способ включает получение, описанное, например, в публикацияхIII-2. Синтез различных ароматических цепей. Связывание бензамидных LCO с аминотетрамером проводят с использованием бензоилхлоридаIII-2.1. Синтез ароматических цепей, метазамещенных ундец-4Z-енилокси цепью. В соответствии со схемой реакции, представленной ниже, получают сложный метиловый эфир 15,который можно подвергнуть восстановлению до альдегида или омылению до кислоты (ацилхлоридный предшественник). Для этого 1-йодундец-4Z-ен 13 используют для алкилирования метил-3-гидроксибензоата. Сложный эфир 15 выделяют с выходом 76% Преобразование сложного эфира в альдегид 17 проводят в две стадии: Кроме того, ацилхлорид 19 получают омылением сложного эфира 15 с последующим взаимодействием с оксалилхлоридомIII-2.2. Синтез ароматических цепей, метазамещенных ундеканоилокси- и ундец-4-инилокси цепями. Аналогичная методика с использованием 1-бромундекана или 1-йодундец-4-ина в безводном ДМФА с последующим омылением и образованием хлорида приводит к получению хлорангидридов 23 и 27III-2.3. Синтез ароматических цепей, ортозамещенных или паразамещенных ундец-4Z-енилокси цепью. Хлорангидриды кислот 31 и 35 получают аналогично из соединений 29 и 33, которые получены, как описано выше, связыванием в соответствии с реакцией Виллиамса 1-йодундец-4Z-ена 13 с метил-2 гидроксибензоатом 28 (или метилсалицилатом) с выходом 66% и с метил-4-гидроксибензоатом с выходом 79% Реакции омыления и преобразования в хлорангидрид являются количественными в обоих случаях. Связывание может быть осуществлено путем растворения исходного вещества в смеси ДМФА-вода в присутствии гидрокарбоната натрия. В таких условиях ацилированию подвергается только свободный амин. При использовании 6 экв. хлорангидрида и после взаимодействия в течение 18 ч достигается конверсия примерно 60%, но реакция является высокоселективной. В результате выделяется 33% целевого продукта 3. Чистота продукта контролируется с помощью ВЭЖХ. Ультрафиолетовый (УФ) спектр поглощения продукта 3 существенно отличается от справочного спектра соединения 12, главным образом, вследствие присутствия в соединении 3 абсорбционного пика при 289 нм. Такой пик благодаря бензамидной группе не появляется у соединения 12. Это идеально иллюстрирует УФ-свойства некоторых из соединений согласно настоящему изобретению, позволяющие их легко анализировать в отличие от Nod факторов. В отличие от соединения 12 соединение 3 также имеет характеристическую флуоресценцию при 345 нм, когда оно облучено при 289 нм.III-3.2. Связывание с 3-(ундеканоилокси)бензоилхлоридом 23 и 3-(ундец-4-инилокси) бензоилхлоридом 27. Связывание проводят в соответствии с методикой, описанной для предыдущего производного, т.е. растворением в смеси ДМФА-вода с использованием нескольких эквивалентов хлорангидрида. В таких условиях насыщенный аналог 6 получают с выходом 32% (и 47% конверсией) и аналог 7,содержащий тройную связь, с выходом 31% (и 70% конверсией). Чистота также контролируется с помощью ВЭЖХ.III-3.3. Связывание с 2-(ундец-4Z-енилокси)бензоилхлоридом,31 и 4-(ундец-4Zенилокси)бензоилхлоридом 35. Два указанных аналога получают в соответствии с аналогичной методикой с выходом 48% для ортозамещенного производного 8 и с выходом 40% для паразамещенного производного 9. Для двух указанных реакций используют 4 экв. хлорангидрида. Чистоту также контролируют с помощью ВЭЖХ 3-(ундец-4Z Реакцию, как описано выше, проводят в смеси ДМФА-вода, в которой растворимы исходное вещество и хлорангидрид. Для облегчения конечной очистки реакцию проводят в присутствии основной смолы Dowex (НСО 3-). По завершении взаимодействия реакционную смесь разбавляют смесью ацетонитрил/вода и предполагаемый продукт очищают фильтрованием через смолу, пропуская через кислотную смолу Dowex(H+), концентрированием и промывкой твердого остатка этилацетатом и затем водой. Таким образом,целевой продукт 2 выделяют с выходом 22%. Реакцию, как описано выше, проводят в смеси ДМФА-вода, в которой растворимы исходное вещество и хлорангидрид. Для облегчения конечной очистки реакцию проводят в присутствии основной смолы Dowex (HCO3-). По завершении взаимодействия реакционную смесь разбавляют смесью ацетонитрил/вода и предполагаемый продукт очищают фильтрованием через смолу, пропуская через кислотную смолу Dowex(H+), с последующим упариванием смеси и промывкой твердого остатка этилацетатом и затем водой. Таким образом целевой продукт 10 выделяют с выходом 28%.III-6. Восстановительное алкилирование сульфатированного тетрамера с помощью 3-(ундец-4Zенилокси)бензальдегида. Реакцию восстановительного алкилирования проводят в безводном ДМФА в присутствии бромида лития. При использовании 12 экв. альдегида и 15 экв. цианоборогидрида натрия с помощью хроматографии на силикагеле через 24 ч целевой связанный продукт 4 получают с выходом 71%. Реакцию проводят в смеси этилацетат-метанол-вода с добавлением уксусного ангидрида в присутствии гидрокарбоната натрия. По истечении 12 ч исходное вещество 4 удаляют, пропуская смесь через Н+ смолу. После очистки на силикагеле выделяют ожидаемый продукт 5 с выходом 77%. Чистоту контролируют с помощью ВЭЖХ.IV. Примеры соединений. В ароматических производных кольцо нумеруется в соответствии с официальной номенклатурой. Для описания ЯМР спектра для СО и LCO сахара нумерацию начинают от восстанавливающегося конца Традиционную нумерацию адоптируют на каждом сахаре. 7,2 мг CO-IV(NH2) растворяют в 200 мкл воды и 500 мкл ДМФА и затем нагревают до 400 С. Затем добавляют 36 мг смолы Dowex (12-100) (НСО 3-) с последующим добавлением 160 мкл раствора соединения 19 в перегнанном ТГФ (26 мкмоль). Затем тремя порциями в течение 48 ч добавляют 108 мг смолы НСО 3- и 480 мкл раствора соединения 19 в перегнанном ТГФ (78 мкмоль). Реакционную смесь разбавляют 3 мл смеси ацетонитрил/вода (1/1), реакционную смесь собирают, оставляя смолу, и затем фильтруют через вату для удаления оставшихся в реакционной смеси шариков смолы. Фильтраты пропускают через смолу Dowex 508-100 Н+, фильтрат упаривают, полученный твердый остаток промывают этилацетатом и затем водой. Получают 2 мг продукта в виде белого порошка (выход 22 %). 15 мг CO-IV(NH2,S) (17 мкмоль) растворяют в 100 мкл воды и 250 мкл ДМФА. Затем добавляют 3 мг гидрокарбоната натрия (34 мкмоль) и 20 мкл раствора соединения 19 в ТГФ с концентрацией 0,25 г/мл (16,4 мкмоль). Реакционную смесь нагревают до 60 С и к смеси добавляют 100 мкл раствора соединения 48 и 10 мг гидрокарбоната натрия шестью порциями в течение 18 ч. После упаривания смеси полученный остаток очищают на колонке с силикагелем в смеси дихлорметан (ДХМ)/метанол (5/1), значительно разбавляя его для удаления липидной цепи (элюирование: смесь этилацетат/метанол/вода=7/2/1). Получают 6,5 мг продукта в виде твердого белого вещества (выход 33%). 11 мг CO-IV(NH2S) (12 мкмоль) растворяют в 0,5 мл ДМФА и добавляют 12 мг бромида лития. В полученную смесь добавляют 2 мг цианоборогидрида натрия (32 мкмоль) и 100 мкл раствора соединения 17 в ТГФ с концентрацией 73 мг/мл (26 мкмоль). Реакционную смесь нагревают до 40 С и выдерживают при этой температуре в течение 4 ч. Каждые 2 ч добавляют 2 экв. альдегида и 2,5 экв. цианоборогидрида натрия, т.е. всего 12 экв. альдегида и 15 экв. цианоборогидрида натрия. Хотя реакция не завершается,реакцию останавливают разложением избытка цианоборогидрида натрия 0,5 н. хлористо-водородной кислотой. Когда выделение газа прекращается, реакционную среду разбавляют водой и лиофилизуют. Остаток переносят в воду, рН снова доводят до щелочного, добавляя 5 мг гидрокарбоната натрия(59 мкмоль), и полученную смесь дважды выпаривают с метанолом. Твердый белый остаток очищают на колонке с силикагелем в смеси ДХМ/метанол (5/1), значительно разбавляя его для удаления липидной цепи (элюирование: смесь этилацетат/метанол/вода 5/2/1, затем 4/1/1). Получают 10 мг продукта в виде белых игольчатых кристаллов (выход 71%). 20 мг гидрокарбоната натрия и 15 мкл уксусного ангидрида добавляют в раствор 13 мг соединения 4 (11 мкмоль) в 0,3 мл смеси этилацетат/метанол/вода (1/1/1). Реакционную смесь перемешивают при комнатной температуре в течение 12 ч. Смесь упаривают, полученное масло переносят в смесь этилацетат/метанол/вода (1/1/1) и добавляют смолу Довекса (508-100 Н+). Смесь фильтруют и к полученному фильтрату добавляют смолу Amberlite IR120Na+. Смесь фильтруют и концентрируют, продукт очищают хроматографией в смеси этилацетат/метанол/вода (4/1/1). Получают 10 мг продукта в виде твердого белого вещества (выход 77%). 15 мг CO-IV(NH2,S) (17 мкмоль) растворяют в 100 мкл воды и 250 мкл ДМФА. Затем к полученной смеси добавляют 6 мг гидрокарбоната натрия (71 мкмоль) и 25 мкл раствора соединения 23 в ТГФ с концентрацией 210 мг/мл (17 мкмоль). Реакционную смесь нагревают до 60 С и добавляют 200 мкл раствора хлорида и 16 мг гидрокарбоната натрия восемью порциями в течение 24 ч. Смесь упаривают и полученный остаток очищают на колонке с силикагелем в растворе ДХМ/метанол (5/1, значительно разбавляя его для удаления липидной цепи (элюирование: смесь этилацетат/метанол/вода=4/1/1). Получают 6,3 мг продукта в виде твердого белого вещества (выход 32%). 14 мг CO-IV(NH2,S) (16 мкмоль) растворяют в 100 мкл воды и 250 мкл ДМФА. Затем добавляют 5 мг гидрокарбоната натрия (60 мкмоль) и 25 мкл раствора соединения 27 в ТГФ с концентрацией 190 мг/мл (16 мкмоль). Реакционную смесь нагревают до 60C и добавляют 200 мкл раствора хлорида и 16 мг гидрокарбоната натрия восемью порциями в течение 24 ч. Смесь упаривают и полученный остаток очищают на колонке с силикагелем в смеси ДХМ/метанол (5/1) в колонку с силикагелем, значительно разбавляя его для удаления липидной цепи (элюирование: смесь этилацетат/метанол/вода=4/1/1). Получают 5,7 мг продукта в виде твердого белого вещества (выход 31%). 10 мг CO-IV(NH2,S) (11 мкмоль) растворяют в 100 мкл воды и 250 мкл ДМФА. Затем добавляют 2 мг гидрокарбоната натрия (24 мкмоль) и 15 мкл раствора соединения 31 в ТГФ с концентрацией 115 мг/мл (6 мкмоль). Реакционную смесь нагревают до 60 С и далее добавляют 105 мкл раствора хлорида и 6 мг гидрокарбоната натрия семью порциями в течение 18 ч. Смесь упаривают и остаток очищают на колонке с силикагелем в смеси ДХМ/метанол (5/1), значительно разбавляя его для удаления липидной цепи (элюирование: смесь этилацетат/метанол/вода=9/2/1). Получают 6,2 мг продукта в виде твердого белого вещества (выход 48%, конверсия 50%). 10 мг CO-IV(NH2,S) (11 моль) растворяют в 100 мкл воды и 250 мкл ДМФА. Затем добавляют 2 мг гидрокарбоната натрия (24 мкмоль) и 15 мкл раствора соединения 35 в ТГФ с концентрацией 115 мг/мл(6 мкмоль). Реакционную смесь нагревают до 60 С и затем добавляют 105 мкл раствора хлорида и 6 мг гидрокарбоната натрия семью порциями в течение 17 ч. Смесь упаривают, полученный остаток очищают на колонке с силикагелем в смеси ДХМ/метанол (5/1), значительно разбавляя его для удаления липидной цепи (элюирование: смесь этилацетат/метанол/вода=9/2/1). Получают 5,2 мг продукта в виде твердого белого вещества (выход 40%, конверсия 60%). Фукозильный пентамер CO-V(NH2, Fuc) (7,3 мг, 6,4 мкмоль) растворяют в Н 2 О (140 мкл), в полученный раствор добавляют ДМФА (350 мкл) и смесь нагревают до 30 С. К смеси добавляют смолу Довекса 12-100 (НСО 3-) с последующим добавлением раствора (ТГФ, 110 мкл) хлорангидрида 19 (6 мг). Реакционную смесь перемешивают в течение 24 ч, в ходе которых три раза добавляют смолу и раствор хлорангидрида. Затем реакционную смесь разбавляют смесью H2O/CH3CN (1/1, 2 мл), нагревают до 56 С и надосадочную жидкость фильтруют через вату. Шарики и волокна смолы в колбе несколько раз экстрагируют при 56 С смесью H2O/CH3CN (4/1, 7/3, 3/2, 1/1, 2/3, 3/7 и 1/4 по 2 мл). Различные фракции пропускают через смолу Довекса 508-100 (Н+), затем объединяют и упаривают. Остаток последовательно промывают EtOAc (31 мл) и H2O (31 мл) и затем снова растворяют в смеси H2O/CH3CN (1/1, 10 мл) при нагревании до 56 С и последующей обработкой ультразвуком. Затем раствор лиофилизуют и получают целевой продукт в виде белого порошка (2,5 мг, 28%). Исходное вещество, удерживаемое на кислотной смоле, затем элюируют (2,3 мг, 31%), используя водный раствор аммиака (H2O, 2%).(6,07 ммоль) в безводном ДМФА (20 мл). После взаимодействия в течение 4 ч при 90 С реакционную смесь концентрируют, остаток переносят в ДХМ и затем промывают водой. Получают 1,87 г желтого масла, которое очищают хроматографией на силикагеле в смеси пентан/этилацетат (50/1). Получают 1,37 г желтого масла (выход 76%). 35 мг алюмогидрида лития (922 мкмоль) при 0 С добавляют к 140 мг соединения 15 (460 мкмоль) в эфире (3 мл). После взаимодействия в течение 1 ч 30 мин реакционную смесь разбавляют эфиром и гидролизуют двумя каплями воды. Смесь фильтруют через целит, сушат над Na2SO4 и упаривают, получая 127 мг бесцветного масла (выход 99%). 10 мл безводного ДХМ и 190 мг РСС (881 мкмоль) в атмосфере аргона последовательно добавляют к 120 мг спирта 16 (434 мкмоль), высушенного совместным выпариванием с толуолом. Реакционную смесь нагревают до температуры кипения ДХМ и кипятят с обратным холодильником в течение 1 ч. После охлаждения реакционную смесь разбавляют эфиром и фильтруют через флорисил. После упаривания смеси получают 118 мг желтого масла (выход 99%). 4 мл 1 н. раствора гидроксида натрия (4,0 ммоль) небольшими порциями добавляют к раствору 1,14 г соединения 15 (3,74 ммоль) в метаноле (30 мл). Раствор кипятят с обратным холодильником в течение ночи. Добавляют дополнительные 4 мл 1 н. раствора гидроксида натрия и смесь кипятят с обратным холодильником еще 1 ч 30 мин. После выпаривания растворителя реакционную смесь подкисляют 0,5 н. HCl и экстрагируют ДХМ. Получают 1,04 г желтого масла (выход 96%). 1 мл оксалилхлорида (11, ммоль) и две капли безводного ДМФА в атмосфере аргона добавляют к 100 мг высушенного с толуолом соединения 18 (345 мкмоль) в 20 мл безводного ДХМ. Реакционную смесь перемешивают при комнатной температуре в течение 2 ч и затем упаривают, получая 106 мг целевого продукта в виде желтого масла (выход 99%). 350 мг соединения 14 (2,30 ммоль) и 330 мг K2CO3 (2,39 ммоль) добавляют к смеси 554 мг 1-бромундекана (2,35 ммоль) и безводного ДМФА (7 мл). После взаимодействия в течение 16 ч при 90 С реакционную смесь концентрируют, переносят в ДХМ и промывают водой. Получают 607 мг желтого масла, которое очищают хроматографией на силикагеле в смеси пентан/этилацетат (60/1). Выделяют 579 мг целевого связанного продукта в форме желтого масла (выход 82%). 600 мкл 1 н. раствора гидроксида натрия (600 мкмоль) небольшими порциями добавляют к 112 мг соединения 21 (366 мкмоль) в метаноле (4 мл). Раствор кипятят с обратным холодильником в течение 2 ч. После выпаривания растворителя реакционную смесь подкисляют 0,5 н. HCl и экстрагируют ДХМ. Получают 107 мг целевой кислоты в виде твердого белого вещества (выход 99%). 1 мл оксалилхлорида (11,5 ммоль) и две капли безводного ДМФА в атмосфере аргона добавляют к раствору 93 мг высушенной в толуоле кислоты 22 (318 мкмоль) в 20 мл безводного ДХМ. Реакционную смесь перемешивают при комнатной температуре в течение 2 ч и упаривают, получая 99 мг желтого масла (выход 99%). Метил-3-(ундец-4-инилокси) бензоат (25)(2,16 ммоль) в безводном ДМФА (7 мл). После взаимодействия в течение 6 ч при 90 С реакционную смесь концентрируют, промывают ДХМ и затем переносят в воду. Получают 639 мг продукта в виде желтого масла, которое очищают хроматографией на силикагеле в смеси пентан/этилацетат (50/1). Получают 429 мг продукта в виде желтого масла (выход 66%). 300 мкл 1 н. раствора гидроксида натрия (300 мкмоль) небольшими порциями добавляют к смеси 48 мг соединения 25 (157 мкмоль) и метанола (2 мл). Раствор кипятят с обратным холодильником в течение 1 ч 30 мин. После выпаривания растворителя реакционную смесь подкисляют 0,5 н. HCl и экстрагируют ДХМ. Получают 45 мг продукта в виде бледно-желтого масла (выход 99%). 850 мкл оксалилхлорида (9,74 ммоль) и две капли безводного ДМФА в атмосфере аргона добавляют к раствору 80 мг высушенной в толуоле кислоты 26 (278 мкмоль) в 17 мл безводного ДХМ. Реакционную смесь перемешивают при комнатной температуре в течение 2 ч и затем упаривают, получая 85 мг продукта в виде желтого масла (выход 99%). Метил-2-(ундец-4Z-енилокси)бензоат (29) 88 мг соединения 28 (578 мкмоль) и 77 мг K2CO3 (557 мкмоль) добавляют к смеси 140 мг соединения 13 (500 мкмоль) и безводного ДМФА (2 мл). После взаимодействия в течение 8 ч при 90 С реакционную смесь концентрируют, переносят в ДХМ и затем промывают водой. Получают 137 мг желтого масла, которое очищают хроматографией на силикагеле в смеси пентан/этилацетат (40/1). Получают 100 мг продукта в виде желтого масла (выход 66%). 500 мкл 1 н. раствора гидроксида натрия (500 мкмоль) небольшими порциями добавляют к смеси 80 мг соединения 29 (263 мкмоль) и метанола (3 мл). Раствор кипятят с обратным холодильником в течение 24 ч. После удаления растворителя выпариванием реакционную смесь подкисляют 0,5 н. HCl и экстрагируют ДХМ. Получают 76 мг продукта в виде желтого масла (выход 99%).
МПК / Метки
МПК: A01P 3/00, A01P 21/00, A01N 43/16
Метки: растений, качестве, бобовых, клубней, содержащая, пестицидная, образования, синтетическое, полезное, агента, фунгицидное, композиция, соединение
Код ссылки
<a href="https://eas.patents.su/30-18062-pesticidnaya-kompoziciya-soderzhashhaya-sinteticheskoe-soedinenie-poleznoe-v-kachestve-agenta-obrazovaniya-klubnejj-bobovyh-rastenijj-i-fungicidnoe-soedinenie.html" rel="bookmark" title="База патентов Евразийского Союза">Пестицидная композиция, содержащая синтетическое соединение, полезное в качестве агента образования клубней бобовых растений, и фунгицидное соединение</a>
Предыдущий патент: Тетрагидропирролопиримидиндионы и их применение в качестве ингибиторов эластазы нейтрофилов человека
Следующий патент: Способ удаления ионов металла из водного табачного экстракта
Случайный патент: Способ, устройство и катетер для определения в живом организме свойств крови, таких как вязкость