Пестицидная композиция, содержащая синтетическое соединение, полезное в качестве средства для образования клубней у бобовых растений, и инсектицидное соединение
Номер патента: 17507
Опубликовано: 30.01.2013
Авторы: Хунгенберг Хайке, Вор Жан-Пьер, Тилерт Вольфганг
Формула / Реферат
1. Пестицидная композиция, содержащая:
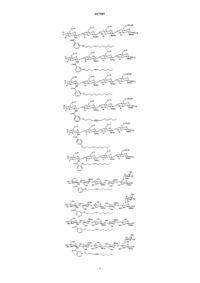
а) соединение общей формулы (I)

где n равно 2 или 3;
А представляет собой -С(О)-;
В представляет собой фенилен;
С представляет собой -О-;
D представляет собой линейную углеводородную цепь, содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода;
Е и G независимо друг от друга представляют собой заместитель NHR20;
R1-R7 представляют собой Н;
R8 представляет собой заместитель, выбранный из Н, фукозила, метилфукозила, SO3H, SO3Li, SO3Na, SO3K, SO3N(C1-8алкила)4;
R9 представляет собой H;
R20 С(О)C1-6алкил;
а также его возможные геометрические и/или оптические изомеры, энантиомеры и/или диастереомеры и сельскохозяйственно приемлемые соли; и
b) инсектицидное соединение, которое является агонистом или антагонистом ацетилхолинового рецептора, в массовом соотношении (а)/(b) от 1/1 до 1/1013.
2. Композиция по п.1, в которой Е и G представляют собой NHC(O)CH3.
3. Композиция по п.1 или 2, где R8 представляет собой Н, SO3H, SO3Li, SO3Na, SO3K, SO3N(C1-8алкил)4 или заместитель формулы
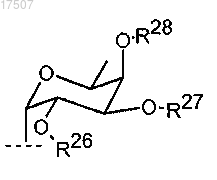
где R26 представляет собой заместитель, выбранный из Н и СН3;
R27 и R28 представляют собой Н.
4. Композиция по п.3, где R26, R27 и R28 представляют собой атом водорода.
5. Композиция по любому одному из пп.1-4, где соединение (I) соответствует одной из следующих формул:
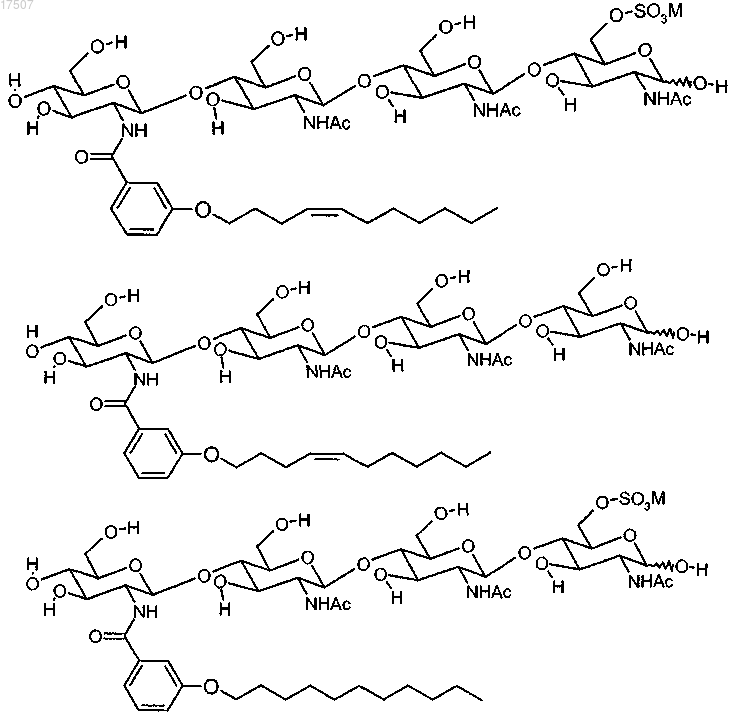

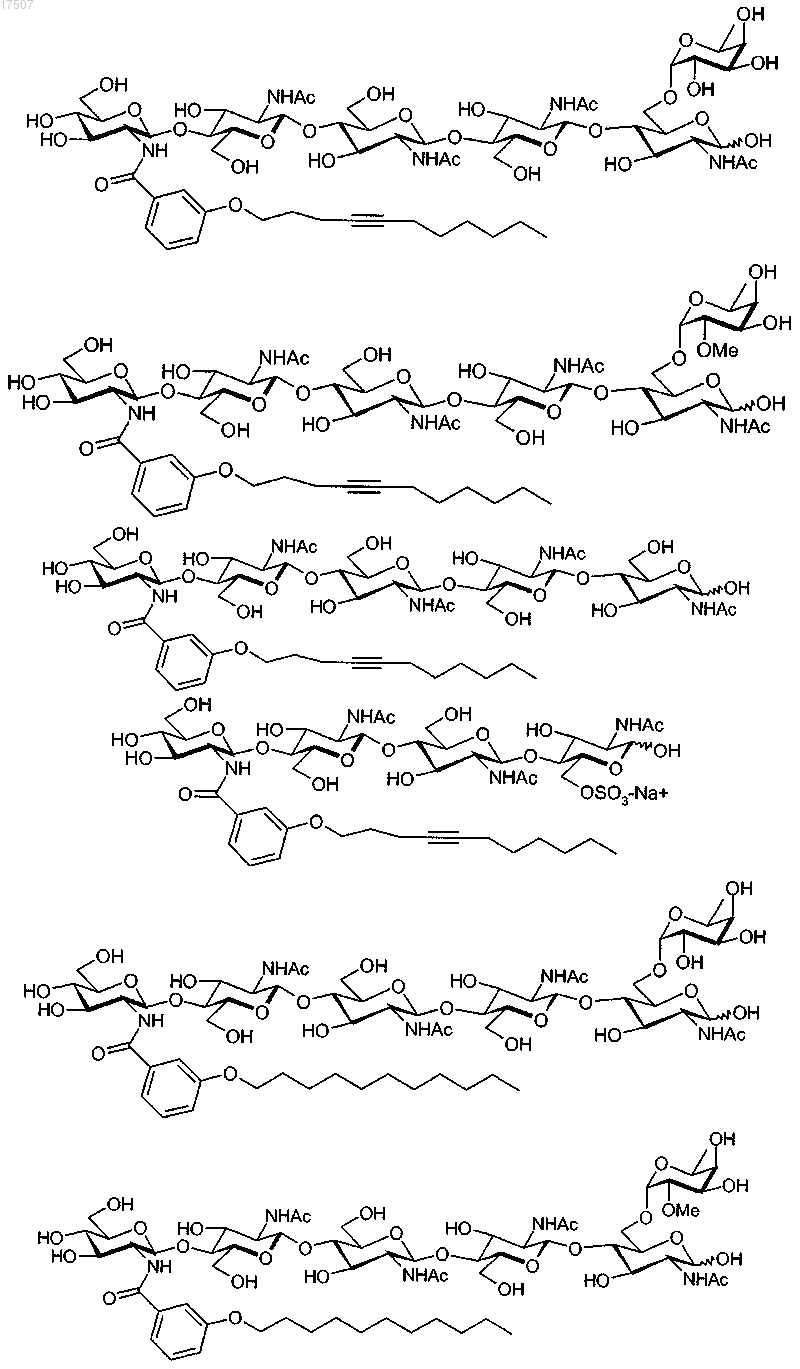
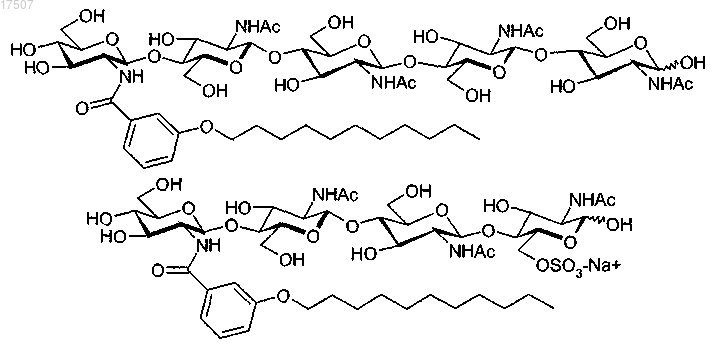
где М, когда присутствует, представляет собой катион, выбранный из Н+, Li+, Na+, K+ и (C1-8алкил)4N+.
6. Композиция по любому из пп.1-5, отличающаяся тем, что инсектицидное соединение (b) выбирают из ацетамиприда, клотианидина, динотефурана, имидаклоприда, имидаклотиза, нитенпирама, нитиазина, тиаклоприда, тиаметоксама.
7. Композиция по п.6, отличающаяся тем, что инсектицидное соединение (b) является имидаклопридом или клотианидином.
8. Композиция по любому одному из пп.1-7, дополнительно содержащая фунгицидное соединение (с).
9. Композиция по п.8, отличающаяся тем, что соединения (а)-(с) присутствуют в массовом соотношении (а)/(b)/(с) от 1/1/1 до 1/1013/1014.
10. Композиция по п.8 или 9, отличающаяся тем, что фунгицидное соединение (с) выбирают из группы, включающей N-[2-(1,3-диметилбутил)фенил]-5-фтор-1,3-диметил-1Н-пиразол-4-карбоксамид, флуопирам, биксафен, металаксил, карбендазим, пенцикурон, фенамидон, флуоксастробин, трифлоксистробин, пириметанил, ипродион, битертанол, флуквинконазол, ипконазол, прохлораз, протиоконазол, тебуконазол, триадименол, тритиконазол, карпропамид, толифлуанид, флуопиколид, изотианил, N-{2-[1,1'-би(циклопропил)-2-ил]фенил}-3-(дифторметил)-, 1-метил-1Н-пиразол-4-карбоксамид, пропамокарбфосэтилат, триазоксид.
11. Композиция по любому из пп.1-10, отличающаяся тем, что дополнительно содержит приемлемые с точки зрения сельского хозяйства подложку, носитель, наполнитель и/или поверхностно-активное вещество.
12. Способ увеличения урожая сельскохозяйственных культур путем стимуляции роста растения с одновременной борьбой с насекомыми, отличающийся тем, что эффективным и нефитотоксичным количеством композиции по любому из пп.1-11 обрабатывают семена, листья, стебли растения или промачивают или поливают (вносят с поливной водой) семена, растения и/или плоды растений, почву и/или инертный субстрат, пемзу, пирокластический материала/туф, синтетический органический субстрат, органический и/или жидкий субстрат, в котором растет растение или в котором его предполагается выращивать.
13. Способ по п.12, отличающийся тем, что композицию вносят в борозды на почве.
14. Способ по п.12 или 13, где сельскохозяйственной культурой является бобовое или небобовое растение.
15. Применение композиции по любому одному из пп.1-11 для увеличения образования клубней у растений с одновременной борьбой с насекомыми.
16. Применение по п.15, где указанным растением является бобовое растение.
17. Применение композиции по любому одному из пп.1-11 для увеличения урожая сельскохозяйственной культуры с одновременной борьбой с насекомыми.
18. Применение композиции по любому из пп.1-11 в качестве фактора, стимулирующего рост растения с одновременной борьбой с насекомыми.
19. Применение по п.17 или 18, где указанным растением является бобовое растение или небобовое растение.
Текст
ПЕСТИЦИДНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ СИНТЕТИЧЕСКОЕ СОЕДИНЕНИЕ, ПОЛЕЗНОЕ В КАЧЕСТВЕ СРЕДСТВА ДЛЯ ОБРАЗОВАНИЯ КЛУБНЕЙ У БОБОВЫХ РАСТЕНИЙ, И ИНСЕКТИЦИДНОЕ СОЕДИНЕНИЕ В изобретении представлена композиция, содержащая, по меньшей мере, соединение (а) общей формулы (I) и инсектицидное соединение (b) в массовом соотношении (а)/(b) от 1/1 до 1/1013. Композиция дополнительно содержит вспомогательное фунгицидное соединение. Также представлен способ борьбы с вредителями и заболеваниями сельскохозяйственных культур и увеличения их урожая путем применения композиции по изобретению.(71)(73) Заявитель и патентовладелец: БАЙЕР КРОПСАЙЕНС АГ (DE) 017507 Настоящее изобретение относится к новым пестицидным композициям, содержащим синтетическое соединение, полезное в качестве средства для образования клубней у бобовых растений и/или в качестве стимулятора роста растения, и инсектицидному соединению. Настоящее изобретение также относится к способу уничтожения или борьбы с вредителями и заболеваниями путем применения такой композиции к зараженному или подверженному заражением участку. В Международной патентной заявке WO 2005/063784 раскрыт способ получения синтетических липохито-олигосахаридов (LCO) и описаны некоторые из указанных соединений, называемые синтетическими LCO-факторами, которые являются полезными в качестве средства для образования клубней у бобовых растений и/или в качестве стимуляторов роста растения. Синтетические LCO-факторы структурно отличаются от Nod-факторов, выделяемых природными бактериальными организмами, и проявляют различные свойства. В частности, конкретные биологически активные синтетические соединения проявляют сильное поглощение в ультрафиолетовом диапазоне, что делает их легко определяемыми во время их промышленного получения, и делает их легко обнаруживаемыми и определяемыми в продукте,предназначенном для рынка сбыта, дает возможность тестировать их стабильность и хранение в таких продуктах. Кроме того, некоторые из таких синтезированных соединений проявляют более высокую стабильность, чем природные Nod-факторы. Также раскрыта возможность комбинирования одного или нескольких таких синтетических соединений, полезных в качестве средства для образования клубней у бобовых растений и/или в качестве стимуляторов роста растения, с известными фунгицидными или инсектицидными продуктами. Несмотря на это, в указанном документе не приводится какого-либо конкретного указания ни на потенциальное соединение-партнер для инсектицида, ни на какие-либо массовые соотношения, в которых должны присутствовать в композиции синтетический фактор LCO и соединение-партнер для инсектицида. В Международной патентной заявке WO 2005/062899 раскрыты смеси, содержащие природныйNod-фактор и инсектицид. Природный Nod-фактор, включенный в такую смесь, является очищенным от источников бактерий или является синтетической или биоинженерной версией встречающихся в природных Nod-генных продуктов. Однако промышленное получение и улучшение природных Nodфакторов имеет два типа недостатков: (1) природные Nod-факторы сложно определять простыми методами, такими как спектрометрические методы; (2) они не стабильны в присутствии растений или в почвах, в частности, поскольку они содержат -СО-NH- связь, разрушаемую растительными или микробными ферментами, присутствующими в ризосфере. Новые пестицидные композиции, описанные в настоящем описании, продемонстрировали значительное улучшение роста, мощности или урожая бобовых растений и небобовых растений или сельскохозяйственных культур и/или инсектицидный эффект при применении в комбинации по сравнению с индивидуальными обработками по отдельности. Также получено значительное улучшение показателей эффективности и стабильности в отношении смесей, содержащих природный Nod-фактор или синтетическую или биоинженерную версию такого природного Nod генного продукта и инсектицида. В сельском хозяйстве всегда вызывает огромный интерес применение новых пестицидных смесей,проявляющих более широкий спектр действия. Авторы настоящего изобретения обнаружили некоторые новые пестицидные композиции, которые обладают вышеуказанными характеристиками. Соответственно настоящее изобретение относится к композиции, содержащей: а) соединение формулы (I)D представляет собой линейную углеводородную цепь, содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода; Е и G независимо друг от друга представляют собой заместитель NHR20;-1 017507 а также их возможные геометрические и/или оптические изомеры, энантиомеры и/или диастереизомеры, соли; иb) инсектицидное соединение, которое является агонистом или антагонистом ацетилхолинового рецептора,в массовом соотношении (а)/(b) от 1/1 до 1/1013. Композиция согласно настоящему изобретению может обеспечивать синергический эффект. Синергический эффект дает возможность сократить количество химических веществ, распыляемых в окружающей среде, и сократить затраты на лечение от грибков. В контексте настоящего изобретения термин "синергический эффект" определен по Colby согласно статье с названием "Calculation of the synergistic and antagonistic responses of herbicide combinations",Weeds, (1967), 15, p. 20-22. В последней статье приведена формула где Е представляет собой ожидаемую процентную долю ингибирования заболевания для комбинации двух фунгицидов при определенных дозах (например, равных х и у соответственно), х представляет собой наблюдаемую процентную долю ингибирования заболевания соединением (I) при дозе (равной х),у представляет собой наблюдаемую процентную долю ингибирования заболевания соединением (II) при определенной дозе (равной у). Когда наблюдаемая процентная доля ингибирования для комбинации больше, чем Е, то имеет место синергический эффект. Композиция согласно настоящему изобретению содержит продукт общей формулы (I). В предпочтительном варианте осуществления изобретения соединения формулы (I) обладают одной или несколькими из следующих характеристик, взятых по отдельности или в комбинации:D представляет собой линейную, насыщенную или ненасыщенную основную углеводородную цепь,содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода; Е и G представляют собой NHC(O)CH3;R8 представляет собой Н, SO3H, SO3Li, SO3Na, SO3K, SO3N(C1-8 алкил)4, фукозил или метилфукозил. можно особенно указать соединения, где В представляет собой фенилен В 1, который может быть замещен одним или двумя заместителями R12 и R13, выбранными независимо друг от друга из галогена,CN, CF3, OCF3, -NO2, N3, OR14, SR14, NR15R16 и C1-6 алкила. Среди предпочтительных композиций настоящего изобретения можно указать соединения, которые включают соединение (I), обладающее одной из следующих характеристик, взятых по отдельности или в комбинации:R9 представляет собой атом водорода; в частности, соединения, где R8 представляет собой Н, SO3H, SO3Li, SO3Na, SO3K, SO3N(C1-8 алкил)4 или заместитель формулыR27 и R28 представляют собой заместитель, выбранный из Н. В качестве примеров композиций по настоящему изобретению, которые особенно полезны и предпочтительны, могут быть указаны композиции, содержащие соединение, выбранное из списка соединений L1, имеющих следующие формулы:(C1-8 алкил)4N+. Кроме композиций по настоящему изобретению, описанных, в частности, выше, варианты комбинаций возможных заместителей, особенно для формул (I), (Ia), (Ib), (Ic), (Id) и (Ie), также составляют часть настоящего изобретения. Известно, что олигомер хитина, не содержащий липидную цепь, не является активным, и что разрушение Nod-факторов посредством разрыва амидной связи в ризосфере приводит, таким образом, к потере активности. Чтобы ограничить или даже предотвратить такое разрушение, был получен ряд аналогичных соединений, некоторые из которых более стабильны, чем природные Nod-факторы. Примеры таких соединений (I) согласно настоящему изобретению приведены ниже в настоящем описании. Композиция согласно настоящему изобретению содержит инсектицидное соединение (b). Подходящий инсектицид выбирают из следующих групп, включающих: b1) агонисты/антагонисты рецептора ацетилхолина, такие как хлорникотинилы/неоникотиноиды, никотин, бенсултап или картап. Подходящие примеры хлорникотинилов/неоникотиноидов включают ацетамиприд, клотианидин, динотефуран, имидаклоприд, имидаклотиз, нитенпирам, нитиазин, тиаклоприд, тиаметоксам. Более предпочтительно инсектицидное соединение (b) выбирают из ацетамиприда, клотианидина,имидаклоприда, тиаклоприда, тиаметоксама. Наиболее предпочтительно инсектицидное соединение (b) выбирают из клотианидина, имидаклоприда и тиаметоксама. Композиция согласно настоящему изобретению содержит соединение общей формулы (I) (а) и инсектицидное соединение (b) в массовом соотношении (а)/(b) от 1/1 до 1/1013. Предпочтительно в массовое соотношение (а)/(b) составляет от 1/10 до 1/1012. Еще более предпочтительно массовое соотношение(а)/(b) составляет от 1/101 до 1/1011. Для некоторых применений, как, например, когда композицию применяют путем обработки семян, соотношение (a)/(b) может составлять преимущественно от 1/102 до-4 017507 1/107, предпочтительно от 1/103 до 1/106, наиболее предпочтительно от 1/104 до 1/105. Специалист в данной области сможет определить подходящие соотношения согласно способам применения и соединениям. Неограничивающие примеры подходящих смесей согласно настоящему изобретению могут включать смеси соединения, выбранного из списка L1, с инсектицидным соединением, выбранным из спискаL2. Композиция по настоящему изобретению может дополнительно содержать по меньшей мере один фунгицидный активный ингредиент (с). Примеры подходящих фунгицидных партнеров для смесей могут быть выбраны из следующего списка, включающего: с 1) соединение, способное ингибировать синтез нуклеиновой кислоты, такое как беналаксил, беналаксил-М, бупиримат, клозилакон, диметиримол, этиримол, фуралаксил, гимексазол, мефеноксам, металаксил, металаксил-М, офурас, оксадиксил, оксолиновая кислота; с 2) соединение, способное ингибировать митоз и деление клетки, такое как беномил, карбендазим,диэтофенкарб, этабоксам, фуберидазол, пенцикурон, тиабендазол, тиофанат-метил, зоксамид; с 3) соединение, способное ингибировать дыхание, например, как CI-ингибитор дыхания, такой как дифлуметорим; как CII-ингибитор дыхания, такой как боскалид, карбоксин, фенфурам, флутоланил, фураметпир,фурмециклокс, мепронил, оксикарбоксин, пентиопирад, тифлузамид; как CIII-ингибитор дыхания, такой как амисулбром, азоксистробин, циазофамид, димоксистробин,энестробин, фамоксадон, фенамидон, флуоксастробин, кресоксим-метил, метоминостробин, оризастробин, пикоксистробин, пираклостробин, трифлоксистробин; с 4) соединение, способное действовать в качестве разобщающего агента, такое как динокап, флузинам, мептилдинокап; с 5) соединение, способное ингибировать образование АТФ, такое как фентинацетат, фентинхлорид, фентингидроксид, силтиофам; с 6) соединение, способное ингибировать биосинтез АА и белка, такое как андоприм, бластицидинS, ципродинил, касугамицин, гидрат касугамицингидрохлорида, мепанипирим, пириметанил; с 7) соединение, способное ингибировать сигнальную трансдукцию, такое как фенпиклонил, флудиоксонил, квиноксифен; с 8) соединение, способное ингибировать синтез липидов и мембраны, такое как бифенил, хлозолинат, эдифенфос, этридиазол, иодокарб, ипробенфос, ипродион, изопротиолан, процимидон, пропамокарб,гидрохлорид пропамокарба, пиразофос, толклофос-метил, винклозолин; с 9) соединение, способное ингибировать биосинтез эргостерола, такое как альдиморф, азаконазол,битертанол, бромуконазол, ципроконазол, диклобутразол, дифеноконазол, диниконазол, диниконазол-М,додеморф, додеморфацетат, эпоксиконазол, этаконазол, фенаримол, фенбуконазол, фенгексамид, фенпропидин, фенпропиморф, флуквинконазол, флурпримидол, флузилазол, флутриафол, фурконазол, цисфурконазол, гексаконазол, имазалил, имазалилсульфат, имибенконазол, ипконазол, метконазол, миклобутанил, нафтифин, нуаримол, окспоконазол, паклобутразол, пефуразоат, пенконазол, прохлораз, пропиконазол, протиоконазол, пирибутикарб, пирифенокс, симеконазол, спироксамин, тебуконазол, тербинафин, тетраконазол, триадимефон, триадименол, тридеморф, трифлумизол, трифорин, тритиконазол, униконазол, виниконазол, вориконазол; с 10) соединение, способное ингибировать синтез клеточной стенки, такое как бентиаваликарб, диметоморф, флуморф, ипроваликарб, мандипропамид, полиоксины, полиоксорим, валидамицин А; с 11) соединение, способное ингибировать биосинтез меланина, такое как карпропамид, диклоцимет, феноксанил, фталид, пироквилон, трициклазол; с 12) соединение, способное вызывать защитные силы организма, такое как ацибензолар-S-метил,пробеназол, тиадинил; с 13) соединение, способное производить мультисайтовое действие, такое как бордосская жидкость,каптафол, каптан, хлороталонил, нафтенат меди, оксид меди, оксихлорид меди, производные меди, такие как гидроксид меди, сульфат меди, дихлофлуанид, дитианон, додин, нейтральное основание додина,фербам, фторфолпет, фолпет, гуазатин, ацетат гуазатина, иминоктадин, иминоктадинальбесилат, иминоктадинтриацетат, mancopper, манкозеб, манеб, метирам, метирам цинка, оксин меди, пропинеб, серные и серные производные, включающие полисульфид кальция, тирам, толифлуанид, цинеб, цирам; с 14) соединение, выбранное из следующего списка, включающего: (2 Е)-2-(2-[6-(3-хлор-2 метилфенокси)-5-фторпиримидин-4-ил]оксифенил)-2-(метоксиимино)-N-метилацетамид,(2 Е)-2-2[([(1 Е)-1-(3-[(Е)-1-фтор-2-фенилвинил]оксифенил)этилиден]аминокси)метил]фенил-2-(метоксиимино)-N-метилацетамид,1-(4-хлорфенил)-2-(1 Н-1,2,4-триазол-1-ил)циклогептанол,1-[(4 метоксифенокси)метил]-2,2-диметилпропил-1 Н-имидазол-1-карбоксилат,1-метил-N-[2-(1,1,2,2-тетрафторэтокси)фенил]-3-(трифторметил)-1 Н-пиразол-4-карбоксамид,2,3,5,6-тетрахлор-4-(метилсульфонил)пиридин, 2-бутокси-6-иод-3-пропил-4 Н-хромен-4-он, 2-хлор-(1,1,3-триметил-2,3-дигидро-1 Нинден-4-ил)никотинамид,2-фенилфенол и соли,3-(дифторметил)-1-метил-N-[2-(1,1,2,2-5 017507 тетрафторэтокси)фенил]-1 Н-пиразол-4-карбоксамид,3-(дифторметил)-N-[(9R)-9-изопропил-1,2,3,4 тетрагидро-1,4-метанонафтален-5-ил]-1-метил-1 Н-пиразол-4-карбоксамид, 3-(дифторметил)-N-[(9S)-9 изопропил-1,2,3,4-тетрагидро-1,4-метанонафтален-5-ил]-1-метил-1 Н-пиразол-4-карбоксамид, 3-(дифторметил)-N-[4'-(3,3-диметилбутил-1-ин-1-ил)биофенил-2-ил]-1-метил-1 Н-пиразол-4-карбоксамид,3,4,5 трихлорпиридин-2,6-дикарбонитрил, 3-[5-(4-хлорфенил)-2,3-диметилизоксазолидин-3-ил]пиридин, 3 хлор-5-(4-хлорфенил)-4-(2,6-дифторфенил)-6-метилпиридазин,4-(4-хлорфенил)-5-(2,6-дифторфенил)3,6-диметилпиридазин,5-хлор-7-(4-метилпиперидин-1-ил)-6-(2,4,6-трифторфенил)[1,2,4]триазол[1,5 а]пиримидин, 8-гидроксихинолинсульфат, бентиазол, бетоксазин, капсимицин, карвон, хинометионат,куфранеб, цифлуфенамид, цимоксанил, дазомет, дебакарб, дихлорофен, дикломезин, диклоран, дифензокват, метилсульфат дифензоквата, дифениламин, экомат, феримзон, флуметовер, флуопиколид, фторимид, флусульфамид, фосэтил-алюминий, фосэтил-кальций, фосэтил-натрий, гексахлорбензол, ирумамицин, изотианил, метасульфокарб, метил(2 Е)-2-2-[(циклопропил[(4-метоксифенил)имин]метилтио)метил]фенил-3-метоксиакрилат,метил-1-(2,2-диметил-2,3-дигидро-1 Н-инден-1-ил)-1 Н-имидазол-5 карбоксилат, метилизотиоцианат, метрафенон, милдиомицин, N-(3',4'-дихлор-5-фторбифенил-2-ил)-3(дифторметил)-1-метил-1 Н-пиразол-4-карбоксамид,N-(3-этил-3,5,5-триметилциклогексил)-3(формиламин)-2-гидроксибензамид, N-(4-хлор-2-нитрофенил)-N-этил-4-метилбензолсульфонамид, N-(4 хлорбензил)-3-[3-метокси-4-(проп-2-ин-1-илокси)фенил]пропанамид, N-[(4-хлорфенил)(циан)метил]-3[3-метокси-4-(проп-2-ин-1-илокси)фенил]пропанамид,N-[(5-бром-3-хлорпиридин-2-ил)метил]-2,4 дихлорникотинамид, N-[1-(5-бром-3-хлорпиридин-2-ил)этил]-2,4-дихлорникотинамид, N-[1-(5-бром-3 хлорпиридин-2-ил)этил]-2-фтор-4-иодникотинамид, N-[2-(1,3-диметилбутил)фенил]-5-фтор-1,3-диметил 1 Н-пиразол-4-карбоксамид,N-(Z)-[(циклопропилметокси)имино][6-(дифторметокси)-2,3-дифторфенил]метил-2-фенилацетамид,N-2-[1,1'-би(циклопропил)-2-ил]фенил-3-(дифторметил)-1-метил-1 Нпиразол-4-карбоксамид, N-2-[3-хлор-5-(трифторметил)пиридин-2-ил]этил-2-(трифторметил)бензамид,натамицин, N-этил-N-метил-N'-2-метил-5-(трифторметил)-4-[3-(триметилсилил)пропокси]фенилимидоформамид, N-этил-N-метил-N'-2-метил-5-(дифторметил)-4-[3-(триметилсилил)пропокси]фенилимидоформамид, диметилдитиокарбамат никеля, нитротализопропил, О-1-[4-метоксифеноки)метил]-2,2 диметилпропил 1 Н-имидазол-1-карботиоат, октилинон, оксамокарб, оксифентиин, пентахлорфенол и соли, фосфористая кислота и ее соли, пипералин, пропамокарбфосэтилат, пропанозин натрия, проквиназид, пирибенкарб, пирролнитрин, квинтозен, 3-аллил-5-амин-2-изопропил-4-(2-метилфенил)-3-оксо-2,3 дигидро-1 Н-пиразол-1-карботиоат, теклофталам, текназин, триазоксид, трихламид, валифенал, зариламид. Предпочтительно фунгицидное соединение (с) выбирают из следующего списка, включающего: Н[2-(1,3-диметилбутил)фенил]-5-фтор-1,3-диметил-1 Н-пиразол-4-карбоксамид, беналаксил, этиримол,гимексазол, мефеноксам, металаксил, М. металаксила, беномил, карбендазим, фуберидазол, пенцикурон,тиабендазол, зоксамид, боскалид, карбоксин, флутоланил, фураметпир, пентиопирад, тифлузамид, азоксистробин, циазофамид, димоксистробин, фамоксадон, фенамидон, флуоксастробин, метоминостробин,оризастробин, пикоксистробин, пираклостробин, трифлоксистробин, флузинам, силтиофам, ципродинил,касугамицин, мепанипирим, пириметанил, фенпиклонил, флудиоксонил, ипродион, процимидон, пропамокарб, толслофос(tolclofos)-метил, битертанол, ципроконазол, дифеноконазол, диниконазол, эпоксиконазол, этаконазол, фенгексамид, флуквинконазол, флутриафол, гексаконазол, имазалил, имибенконазол,ипконазол, метконазол, прохлораз, протиоконазол, симеконазол, спироксамин, тебуконазол, тетраконазол, триадимефон, триадименол, трифлумизол, тритиконазол, карпропамид, толифлуанид, флуопиколид,изотианил,N-2-[1,1'-би(циклопропил)-2-ил]фенил-3-(дифторметил)-,-1-метил-1 Н-пиразол-4 карбоксамид,пропамокарба фосэтилат,триазоксид,N-(3',4'-дихлор-5-фторбифенил-2-ил)-3(дифторметил)-1-метил-1 Н-пиралол-4-карбоксамид, N-2-[3-хлор-5-(трифторметил)пиридин-2-ил]этил 2-(трифторметил)бензамид. Более предпочтительно фунгицидное соединение (с) выбирают из следующего списка L3, включающего: N-[2-(1,3-диметилбутил)фенил]-5-фтор-1,3-диметил-1 Н-пиразол-4-карбоксамид, металаксил,карбендазим, пенцикурон, фенамидон, флуоксастробин, трифлоксистробин, пириметанил, ипродион,битертанол, флуквинконазол, ипконазол, прохлораз, протиоконазол, тебуконазол, триадименол, тритиконазол, карпропамид, толифлуанид, флуопиколид, изотианил, N-2-[1,1'-би(циклопропил)-2-ил]фенил-3(дифторметил)-1-метил-1 Н-пиразол-4-карбоксамид, пропамокарба фосэтилат, триазоксид, N-(3',4'дихлор-5-фторбифенил-2-ил)-3-(дифторметил)-1-метил-1 Н-пиразол-4-карбоксамид,N-2-[3-хлор-5(трифторметил)пиридин-2-ил]этил-2-(трифторметил)бензамид. Где в композиции присутствует третий активный ингредиент (с), как определено выше, такое соединение может присутствовать в количестве согласно массовому соотношению (а)/(b)/(с) от 1/1/1 до 1/1013/1014, соотношения соединения (b) и соединения (с) могут изменяться независимо друг от друга. Предпочтительно массовое соотношение (а)/(b)/(с) может составлять от 1/10/10 до 1/1012/1013, более предпочтительно от 1/100/100 до 1/10011/10012. При применении композиции путем обработки семян массовое соотношение (а)/(b)/(с) может составлять преимущественно от 1/100/100 до 1/107/108, более предпочтительно от 1/103/103 до 1/106/107 и наиболее предпочтительно от 1/104/104 до 1/105/106. Неограничивающие примеры подходящих смесей согласно настоящему изобретению могут вклю-6 017507 чать смеси соединения, выбранного из списка L1, инсектицидного соединения, выбранного из списка L2,и фунгицидного соединения, выбранного из списка L3. Композиция согласно настоящему изобретению может дополнительно содержать другой дополнительный компонент, такой как приемлемая с точки зрения сельского хозяйства подложка, носитель или наполнитель. В настоящем описании термин "подложка" означает природный или синтетический, органический или неорганический материал, с которым объединен активный материал для того, чтобы сделать применение, особенно к частям растений, более удобным. Такая подложка, таким образом, является в целом инертной и должна быть приемлемой с точки зрения сельского хозяйства. Подложка может быть твердым веществом или жидкостью. Примеры подходящих подложек включают глины, природные или синтетические силикаты, кварц, смолы, воски, твердые удобрения, воду, спирты, в частности бутанол, органические растворители, минеральные или растительные масла и их производные. Также можно использовать смеси таких подложек. Композиция также может содержать другие дополнительные компоненты. В частности, композиция может дополнительно содержать поверхностно-активное вещество. Поверхностно-активным веществом может быть эмульгатор, диспергирующее средство или увлажняющее средство ионного или неионогенного типа или смесь таких поверхностно-активных веществ. Можно указать, например, соли полиакриловой кислоты, соли лигносульфокислоты, соли фенолсульфокислоты или нафталинсульфокислоты, поликонденсаты этиленоксида со спиртами жирного ряда, или с кислотами жирного ряда, или с аминами жирного ряда, замещенные фенолы (в частности, алкилфенолы или арилфенолы), соли сульфоэфиров янтарной кислоты, производные соединения таурина (в частности, алкилтаураты), сложные фосфорные эфиры полиоксиэтилированных спиртов или фенолов, сложные эфиры жирных кислот и полиолов, и производные вышеуказанных соединений, содержащих сульфатные, сульфонатные и фосфатные функциональные группы. Присутствие по меньшей мере одного поверхностно-активного вещества, в целом,существенно, когда активный материал и/или инертная подложка не растворимы в воде и когда используемым переносчиком является вода. Предпочтительно содержание поверхностно-активного вещества может составлять от 5 до 40 мас.% композиции. Дополнительные компоненты также могут быть включены, например защитные коллоиды, адгезивы, сгустители, тиксотропные средства, агенты, повышающие проницаемость, стабилизаторы, изоляторы. В общем, активные материалы могут быть объединены с любой твердой или жидкой добавкой, которая удовлетворяет требованиям стандартных способов составления в композицию. Композиции согласно настоящему изобретению можно применять в различных формах, таких как аэрозольный дозатор, суспензия капсул, холодный аэрозольный концентрат, пылящий порошок, эмульгируемый концентрат, эмульсия "масло в воде", эмульсия "вода в масле", капсулированная гранула, тонкая гранула, текучий концентрат для обработки семян, газ (под давлением), газ, газообразующий продукт, гранула, горячий аэрозольный концентрат, макрогранула, диспергируемый в масле порошок, смешиваемый с маслом текучий концентрат, смешиваемая с маслом жидкость, паста, растительный стержень, порошок для сухой обработки семян, семя, покрытое пестицидом, растворимый концентрат, растворимый порошок, раствор для обработки семян, концентрат суспензии (текучий концентрат), жидкость сверхмалого объема (ulv), суспензия сверхмалого объема (ulv), диспергируемые в воде гранулы или таблетки, диспергируемый в воде порошок для шламовой обработки, растворимые в воде гранулы или таблетки, растворимый в воде порошок для обработки семян и смачиваемый порошок. Указанные композиции включают не только композиции, готовые к нанесению на обрабатываемое растение или семя либо в борозду на почве, посредством подходящего устройства, такого как разбрызгивающее или распыляющее устройство, но также и концентрированные коммерческие композиции, которые необходимо разбавлять перед нанесением на сельскохозяйственные культуры. Пестицидные композиции по настоящему изобретению можно применять в лечебных или профилактических целях для борьбы с насекомыми, а также для увеличения урожая, роста или мощности растения. Таким образом, согласно дополнительному аспекту настоящего изобретения, описан способ лечебной или профилактической борьбы с насекомыми и увеличения урожая, роста или мощности растения,отличающийся тем, что определенную выше композицию применяют путем обработки семян, нанесения на листья, нанесения на стебель или нанесения на семена путем пропитывания/окунания (внесение с поливной водой), на растения и/или плод растения, или в почву, особенно в борозду, и/или на инертный субстрат (например, неорганические субстраты (такие как песок, каменная вата, стекловата, набухающие минералы (например, перлит, вермикулит, цеолит, набухающая глина, пемза, пирокластические материалы/туф, синтетические органические субстраты (например, полиуретан), органические субстраты(например, торф, компосты, опавшие листья (например, кокосовая койра, древесное волокно/опилки,древесная кора и/или в жидкий субстрат (например, плавающие гидропониковые системы, пластиковые трубы, по которым течет питательный раствор, аэропоника) в котором растет или желателен рост растения. Композиция, применяемая против вредителей и заболеваний сельскохозяйственных культур, со-7 017507 держит эффективное и нефитотоксичное количество инсектицидного соединения. Выражение "эффективное и нефитотоксичное количество" означает количество композиции согласно настоящему изобретению, достаточное для борьбы или уничтожения вредителей и заболеваний, присутствующих или склонных к появлению на сельскохозяйственных культурах, и которое не влечет за собой заметного признака фитотоксичности для указанных сельскохозяйственных культур. Такое количество может изменяться в широком диапазоне в зависимости от вредителей и заболеваний, с которыми необходимо бороться или уничтожить, типа сельскохозяйственной культуры, климатических условий и соединений,включенных в композицию согласно настоящему изобретению. Данное количество можно определить путем систематических полевых испытаний, известных специалисту в данной области. Способ обработки согласно настоящему изобретению полезен для обработки материала для размножения, такого как клубни или ризомы, а также семена, сеянцы или пикированные сеянцы и растения или пикированные растения. Данный способ обработки также может быть полезным для обработки корней. Способ обработки согласно настоящему изобретению также может быть полезным для обработки открытых частей растения, таких как стволы, стебли или ножки, листья, цветы и плоды представляющего интерес растения. Растениями, которые можно защитить способом согласно настоящему изобретению, могут быть бобовые или небобовые растения. Среди растений, которые можно защитить способом согласно настоящему изобретению, можно указать хлопок; лен; виноградную лозу; фруктовые или овощные культуры, такие как Rosaceae sp. (например, односемянные плоды, такие как яблоки и груши, а также и косточковые плоды, такие как абрикосы, миндаль и персики), Ribesioidae sp., Juglandaceae sp., Betulaceae sp., Anacardiaceae sp., Fagaceae sp.,Moraceae sp., Oleaceae sp., Actinidaceae sp., Lauraceae sp., Musaceae sp. (например, банановые деревья иplantins), Rubiaceae sp., Theaceae sp., Sterculiceae sp., Rutaceae sp. (например, лимоны, апельсины и грейпфрут); Solanaceae sp. (например, томаты), Liliaceae sp., Asteraceae sp. (например, салаты), Umbelliferae sp.,Cruciferae sp., Chenopodiaceae sp., Cucurbitaceae sp., Papilionaceae sp. (например, горох), Rosaceae sp. (например, земляника); главные сельскохозяйственные культуры, такие как Craminae sp. (например, кукуруза, газонная трава или зерновые, такие как пшеница, рис, ячмень и тритикале), Asteraceae sp. (например,подсолнечник), Cruciferae sp. (например, рапс), Fabacae sp. (например, арахис), Papilionaceae sp. (например, соя), Solanaceae sp. (например, картофель), Chenopodiaceae sp. (например, свекла); садовые и лесные сельскохозяйственные культуры; а также генетически модифицированные гомологи указанных сельскохозяйственных культур. Среди бобов можно указать сою, горох, конский боб, арахис, фасоль, люпин, люцерну или клевер. Композиция согласно настоящему изобретению легко переносится растениями, имеет благоприятную токсичность на теплокровных и безвредна для окружающей среды; композиция подходит для защиты растения и органов растения, для увеличения объемов урожая, для улучшения качества собранного материала и для борьбы с вредителями у животных, в частности насекомыми, паукообразными насекомыми и нематодами, встречающимися в сельском хозяйстве, в лесах, в садах и местах отдыха, при защите хранящихся продуктов и материалов и в санитарном секторе. Композиции предпочтительно применяют в качестве защитных средств для сельскохозяйственных культур. Композиции активны против среднечувствительных и среднеустойчивых видов и на всех или некоторых стадиях их развития. Среди вредителей у животных, с которыми также можно бороться способом согласно настоящему изобретению,можно указать: вредителя из отряда Isopoda, например Oniscus asellus, Armadillidium vulgare и Porcelliscaber; вредителя из отряда Diplopoda, например Blaniulus guttulatus; вредителя из отряда Chilopoda, например Geophilus carpophagus и Scutigera spp.; вредителя из отряда Symphyla, например Scutigerella immaculate; вредителя из отряда Thysanura, например Lepisma saccharina; вредителя из отряда Collembola, например Onychiurus armatus; вредителя из отряда Orthoptera, например Acheta domesticus, Gryllotalpa spp., Locusta migratoria migratorioides, Melanoplus spp. и Schistocerca gregaria; вредителя из отряда Blattaria, например Blatta orientalis, Periplaneta americana, Leucophaea maderae иBlattella germanica; вредителя из отряда Dermaptera, например Forficula auricularia; вредителя из отряда Isoptera, например Reticulitermes spp.; вредителя из отряда Phthiraptera, например Pediculus humanus corporis, Haematopinus spp., Linognathus spp., Trichodectes spp., Damalinia spp.; вредителя из отряда Thysanoptera, например Hercinothrips femoralis, Thrips tabaci, Thrips palmi,Frankliniella accidentalis; вредителя из отряда Heteroptera, например Eurygaster spp., Dysdercus intermedius, Piesma quadrata,Cimex lectularius, Rhodnius prolixus и Triatoma spp.; вредителя из отряда Homoptera, например Aleurodes brassicae, Bemisia tabaci, Trialeurodes vaporari-8 017507Psylla spp.; вредителя из отряда Lepidoptera, например Pectinophora gossypiella, Bupalus piniarius, Cheimatobiaoryzae; вредителя из отряда Coleoptera, например Anobium punctatum, Rhizopertha dominica, Bruchidius obtectus, Acanthoscelides obtectus, Hylotrupes bajulus, Agelastica alni, Leptinotarsa decemlineata, Phaedon cochleariae, Diabrotica spp., Psylliodes chrysocephala, Epilachna varivestis, Atomaria spp., Oryzaephilus surinamensis, Anthonomus spp., Sitophilus spp., Otiorrhynchus sulcatus, Cosmopolites sordidus, Ceuthorrhynchus assimilis, Hypera postica, Dermestes spp., Trogoderma spp., Anthrenus spp., Attagenus spp., Lyctus spp., Meligethesaeneus, Ptinus spp., Niptus hololeucus, Gibbium psylloides, Tribolium spp., Tenebrimolitor, Agriotes spp.,Conoderus spp., Melolontha, Amphimallon solstitialis, Costelytra zealandica и Lissorhoptrus oryzophilus; вредителя из отряда Hymenoptera, например Diprion spp., Hoplocampa spp., Lasius spp., Monomoriumpharaonis и Vespa spp.; вредителя из отряда Diptera, например Aedes spp., Anopheles spp., Culex spp., Drosophilapaludosa, Hylemyia spp. и Liriomyza spp.; вредителя из отряда Siphonaptera, например Xenopsylla cheopis и Ceratophyllus spp.; вредителя из класса Archanida, например Scorpimaurus, Latrodectus mactans, Acarus siro, Argas spp.,Ornithodoros spp., Dermanyssus gallinae, Eriophyes ribis, Phyllocoptruta oleivora, Boophilus spp., Rhipicephalus spp., Amblyomma spp., Hyalomma spp., Ixodes spp., Psoroptes spp., Chorioptes spp., Sarcoptes spp., Tarsonemus spp., Bryobia praetiosa, Panonychus spp., Tetany chus spp., Hemitarsonemus spp. и Brevipalpus spp.; нематоды, паразитирующие на растениях, такие как Pratylenchus spp., Radopholus similis, Ditylenchus dipsaci, Tylenchulus semipenetrans, Heterodera spp., Globodera spp., Meloidogyne spp., Aphelenchoidesspp., Longidorus spp., Xiphinema spp., Trichodorus spp. и Bursaphelenchus spp. Композицию согласно настоящему изобретению также можно применять против вредителей и заболеваний, склонных к росту на или внутри древесины. Термин "древесина" означает все виды леса и все типы обработанного леса, предназначенного для строительных работ, например массивную древесину,плотную древесину, слоистую древесину и фанеру. Способ обработки древесины согласно настоящему изобретению, главным образом, состоит во взаимодействии с одним или несколькими соединениями по настоящему изобретению или композиции по настоящему изобретению; это включает, например, прямое нанесение, опрыскивание, погружение, впрыскивание или любые другие подходящие способы. Доза активного вещества, обычно применяемого в обработке согласно настоящему изобретению, в основном и преимущественно составляет от 10 до 800 г/га, предпочтительно от 50 до 300 г/га при применении для обработки листьев. Если возможно пропитывание/обмакивание/внесение в борозды, то доза может быть ниже, особенно, для искусственных субстратов, таких как каменная вата или перлит. Доза применяемого активного вещества, в целом и преимущественно, составляет от 0,5 до 200 г на 100 кг семян, предпочтительно от 1 до 15 г на 100 кг семян в случае обработки семян. Понятно, что дозы, указанные выше, приведены в качестве иллюстративных примеров изобретения. Специалисту в данной области известно, каким образом подобрать дозы внесения согласно природе обрабатываемой сельскохозяйственной культуры. Композицию согласно настоящему изобретению также можно применять для обработки генетически модифицированных организмов соединениями согласно настоящему изобретению или агрохимическими композициями согласно настоящему изобретению. Генетически модифицированные растения являются растениями, в геном которых устойчиво интегрирован гетерологический ген, кодирующий представляющий интерес белок. Выражение "гетерологический ген, кодирующий представляющий интерес белок", по существу, означает гены, которые придают измененному растению новые агрономические свойства, или гены, улучшающие агрономическое качество измененного растения.II-1. Структура соединений (I) согласно настоящему изобретению. Были получены соединения, содержащие метазамещенную бензамидную группу. Предпочтительно сохранять одинаковое общее число атомов вдоль цепи (16), а также ненасыщенность цис-типа в положении 9. На практике для получения исходных веществ липидную цепь можно присоединить к ароматиче-9 017507 скому кольцу через атом кислорода. Также был синтезирован аналог 4, содержащий метазамещенную функциональную бензиламинную группу, а также N-ацетилированный аналог 5, который дает возможность восстановить весь заряд природного продукта. Такие аналоги были получены в серии реакций сульфатирования. Два других сульфатированных аналога, один, содержащий полностью насыщенную цепь, и другой ненасыщенную цепь алкинного типа, дают возможность изучить эффект ненасыщенности Z типа в положении 9, присутствующий в природном продукте. В результате два сульфатированных аналога, замещение в ароматическом кольце которых находится в орто-положении для одного и в пара-положении для другого, дают возможность изучить эффект ненасыщенности транс-типа, находящегося в положении 2 в природном продукте. Стандартами для биологических тестов являются следующие соединения:III.1. Примеры получения различных основных олигосахаридных структур. Основные олигосахаридные структуры, соответствующие формуле (I), могут быть получены биотехнологическими способами, такими как, например, применение рекомбинантных бактериальных клеток, таких как, например, рекомбинантные клетки Escherichia coli, содержащие гетерологический ген из клубневых бактерий. Например, введение nodBC генов из Azorhizobium caulinodans в Escherichia coli дает- 10017507 возможность получить тетра-N-ацетилхитопентаозу (Samain E., et al., Carbohydr. Res., 1997, 302, 35-42). Использование nodBC из Rhizobium meliloti дает возможность получить три-N-ацетилхитотетраозу. Кроме того, использование дополнительных генов, таких как, например, nodH (сульфотрансфераза клубневых бактерий) или nodL (O-ацетилтрансфераза клубневых бактерий), дает возможность вводить модификации в специфичных гидроксильных группах (Samain E., et al., J. Biotechnol., 1999, 72, 33-47). Другие комбинации генов клубневых или неклубневых бактерий дают возможность получать различные хитоолигосахаридные структуры, полезные в качестве исходных веществ в реакции ацилирования для получения молекул формулы (I), с различными модификациями в гидроксильных или аминогруппах. Основные олигосахаридные структуры также можно получить стандартным химическим синтезом с применением классических и хорошо известных в химии углеводов способов и приемов. Описание недавних и соответствующих способов можно найти во многих руководствах и обзорах и, более конкретно,например, в описаниях, приведенных в Carbohydrates in Chemistry and Biology, Editors.: B. Ernst, G.W.Hart, P. Sinay, Wiley-VCH, Weinheim; 2000. Управление правильно выбранными защитными группами,которые можно вводить в очень специфичные положения к гидроксильным или аминогруппам и последовательно или ортогонально удалять, чтобы освободить любую присутствующую группу для избирательного модифицирования, дает возможность вводить определенные модификации в основную олигосахаридную структуру, включая, например, ацилирование, или алкилирование, или гликозилирование определенных гидроксильных групп или ацилирование и алкилирование определенных аминогрупп. Защитные группы, используемые для защиты аминов и удаляемые последовательно или ортогонально,включают,например,фталимидную,тетрахлорфталимидную,азидную,третбутилоксикарбонильную, 2,2,2-трихлорэтоксикарбонильную и трихлорацетильную группы. Защитные группы, используемые для защиты спиртов и удаляемые последовательно или ортогонально, включают,например, ацетильную, бензильную, п-метоксибензильную, триметилсилильную, триэтилсилильную,трет-бутилдиметилсилильную и трет-бутилдифенилсилильную группы, а также циклические ацетали,такие как,например,метилиден,этилиден,изопропилиден,бензилиден или пметоксибензилиденацетали. Классические способы и условия управления защитными группами можно найти, например, в "Protecting Groups", P.J. Kocienski, 2nd Edition, Georg Thieme Verlag, Stuttgart, 2000 или в "Protective Groups in Organic Synthesis", T.W. Greene, P.G.M. Wuts, 3rd Edition, Wiley, New York, 1999. Основные олигосахаридные структуры можно получить путем присоединения правильно выбранных защитных групп в желаемых положениях к контролируемой совокупности моносахаридных строительных блоков. Такую совокупность можно получить классическими и традиционно применяемыми в области химического синтеза олигосахаридов способами. Последовательное удаление защитных групп с последующей химической модификацией в освобожденных гидроксильных или аминогруппах даст возможность получения молекул, соответствующих формуле (I). Примеры введения другого сахара, представленного фрагментом фукозы, можно легко найти в предшествующей области техники, включая, например, A.I. Zinin et al., Russ. Chem. Bull., 1998, 47, 496-501 и J.S. Debenham et al., J. Org. Chem., 1996, 61,6478-6479. Классические способы получения совокупности моносахаридов включают, например, активацию аномерных трихлорацетимидатных, О-пентенильных, алкилтио, арилтио, сульфоксидных, галогеновых или фосфатных групп. Многочисленные примеры синтеза олигосахаридов можно найти во многих обзорах, в ряде монографий, приведенных выше, или, например, в "Glycoscience, Chemistry и ChemicalBiology", Editors: B. Fraser-Reid, K. Tatsuta, J. Thiem, Springer-Verlag, Berlin Heidelberg, 2001. Предусматривается, что продукты формулы (I) могут быть химически синтезированы согласно приведенной в качестве примера методике, описанной ниже (на данной схеме PXH на аминогруппах может также представлять собой защитную группу, такую как, например, фталимидная или тетрахлорфталимидная защитная группа, или N2, если в положении 2 углевода есть азидная группа). P1-P20 представляет собой либо временные защитные группы, либо постоянно вводимую модификацию, желательную для конечной основной структуры, такую как, например, ацилирование, алкилирование или гликозилирование. Х 1-Х 4 представляет собой аномерные активируемые уходящие группы, такие как, например, трихлорацетимидатная, О-пентенильная, алкилтио, арилтио, сульфоксидная, галогеновая или фосфатная группы. Два моносахарида, содержащих правильный подбор защитных групп, можно сочетать в одном из стандартных способов гликозилирования. Правильно выбранную защитную группу (Р 6) можно выборочно удалить из желаемого положения полученного дисахарида в условиях, которые не повлияют на другие защитные группы. Сочетание другого моносахарида в только что освободившемся положении приведет к получению трисахарида. За удалением правильно выбранной защитной группы (Р 10) из полученного трисахарида в условиях, которые не повлияют на другие защитные группы, может следовать сочетание другого моносахарида в только что освободившемся положении, приводя к получению тетрасахарида. За удалением правильно выбранной защитной группы (Р 14) из полученного трисахарида в условиях, которые не повлияют на другие защитные группы, может следовать сочетание другого моносахарида в только что освободившемся положении, приводя к получению пентасахарида. Удаление любой правильно выбранной защитной группы от гидроксильной или аминогруппы полученного пентасахарида в условиях, которые не повлияют на другие защитные группы, даст возможность провести определенную химическую модификацию, такую как, например, ацилирование, алкилирование или гликозилирование в- 11017507 данном положении. Приведенный способ можно повторять необходимое число раз для проведения всех желаемых модификаций основной структуры. Окончательное снятие оставшихся защитных групп даст возможность получить доступ к желаемой основной структуре. Представительные примеры данной стратегии можно найти в предшествующей области техники,включая, например, K.С. Nicolaou et al., J. Am. Chem. Soc, 1992, 114, 8701. Также предусматривается, что продукты формулы (I) можно химически синтезировать согласно альтернативной типовой методике, описанной ниже (на данной схеме PXH на аминогруппах может также представлять собой защитную группу, такую как, например, фталимидная или тетрахлорфталимидная защитные группы, или N2, если в положении 2 углевода есть азидная группа). P1-P16 представляет собой либо временную защитную группу, либо постоянно вводимую модификацию, желаемую для конечной основной структуры, такую как, например, ацилирование, алкилирование или гликозилирование. Х 1-Х 3 представляет собой аномерные активируемые уходящие группы, такие как, например, трихлорацетимидатная, О-пентильная, алкилтио, арилтио, сульфоксидная, галогеновая или фосфатная группы. Y1-Y4 представляет собой либо защитные группы, либо другие стабильные группы, которые могут быть преобразованы в активированные уходящие группы, такие как, например, трихлорацетимидатная, Oпентильная, алкилтио, арилтио, сульфоксидная, галогеновая или фосфатная группы. Два моносахарида,содержащие правильно подобранные защитные группы, можно сочетать стандартным способом гликозилирования. Активация правильно выбранной группы (Y1) даст возможность введения аномерной активируемой группы X2, что даст возможность сочетать полученный дисахарид с другим моносахаридом. Активация правильно выбранной группы (Y2) даст возможность введения аномерной активируемой группы X3, которая даст возможность сочетать полученный трисахарид с другим моносахаридом. Активация правильно выбранной группы (Y4) даст возможность введения аномерной активируемой группыX3, которая даст возможность сочетать полученный трисахарид с другим моносахаридом, приводя к получению пентасахарида. Удаление любой правильно выбранной защитной группы от гидроксильной или аминогруппы полученного пентасахарида в условиях, которые не повлияют на другие защитные группы,даст возможность провести определенную химическую модификацию, такую как, например, ацилирование, алкилирование или гликозилирование в данном положении. Указанный способ можно повторить необходимое число раз для проведения всех желаемых модификаций основной структуры. Окончательное снятие оставшихся защитных групп даст возможность получить доступ к желаемой основной структуре.- 12017507 Представительные примеры приведенной стратегии можно найти в предшествующей области техники, включая, например, D. Tailler et al., J. Chem. Soc, Chem. Commun., 1994, 1827 и J.S. Debenham et al.,J. Org. Chem., 1991, 62, 4591-4600. В дополнение к двум основным общим примерам, приведенным выше, которые состоят в добавлении моносахарида в каждом "цикле" стадий, представительные примеры других стратегий можно также найти в предшествующей области техники, такие как, например, добавление вместо моносахарида должным образом полученного дисахарида. Это включает получение, раскрытое, например, в S. Ikeshita et al.,Tetrahedron Lett., 1994, 3123 и L.X. Wang et al., J. Chem. Soc, Perkin Trans. 1, 1994, 621.III-2. Синтез различных ароматических цепей. Для бензамидов LCO сочетание с тетрамером амина проводят при помощи бензоилхлорида (ацилирование) и для бензилов LCO - при помощи бензальдегида (восстановительное алкилирование).III-2.1. Синтез ароматических цепей, метазамещенных ундек-4Z-енилокси цепью. Согласно схеме реакций ниже получают сложный метиловый эфир 15, из которого можно провести восстановление до альдегида или омыление до кислоты (предшественник хлорангидрида карбоновой кислоты). Для этого используют 1-иодундек-4Z-ен 13 для алкилирования метил-3-гидроксибензоата. Сложный эфир 15 выделяют с выходом 76%. Преобразование сложного эфира в альдегид 17 проводят в две стадии. Кроме того, хлорангидрид карбоновой кислоты 19 получают путем омыления сложного эфира 15 с последующим взаимодействием с оксалилхлоридом.III-2.2. Синтез ароматических цепей, метазамещенных ундеканилокси и ундек-4-инилокси цепями. Аналогичная методика с 1-бромундеканом или 1-иодундек-4-ином в безводном ДМФА с последующим омылением и получением хлорида приводит к получению хлорангидридов 23 и 27.III-2.3. Синтез ароматических цепей, орто- или пара-замещенных ундек-4Z-енилокси цепью. Хлорангидриды кислот 31 и 35 получают аналогичным образом из соединений 29 и 33, полученных реакцией Вильямсона путем сочетания 1-иодундек-4Z-ена 13 с метил-2-гидроксибензоатом 28 (или метилсалицилатом) с выходом 66% и с метил-4-гидроксибензоатом 32 с выходом 79%. Омыление и преобразование в хлорид являются количественными в обоих случаях. Сочетание можно проводить путем растворения исходного вещества в смеси ДМФА-вода в присутствии гидрокарбоната натрия. В данных условиях ацилируется только свободный амин. Через 18 ч взаимодействия с 6 экв. хлорида достигается приблизительно 60% преобразование, но реакция является высокоселективной. Таким образом, выделяют 33% желаемого продукта 3. Чистоту продукта проверяют ВЭЖХ. Спектр поглощения продукта 3 в ультрафиолетовой области (УФ) существенно отличается от спектра поглощения стандартного соединения 12, особенно из-за присутствия в спектре поглощения продукта 3 адсорбционного пика при 289 нм. Такой пик, отвечающий бензамидной группе, не присутствует у соединения 12. Это отлично иллюстрирует УФ свойства некоторых соединений согласно настоящему изобретению, делая их легко определяемыми, в отличие от природных Nod-факторов. В отличие от соединения 12, соединение 3 также обладает характерной флюоресценцией при 345 нм, когда его возбуждают волной с длиной 289 нм.III-3.2. Сочетание с 3-(ундеканилокси)бензоилхлоридом 23 и 3-(ундек-4-инилокси)бензоилхлоридом 27. Повторяют методику, аналогичную для предыдущего производного, т.е. растворение в смеси ДМФА-вода и использование нескольких эквивалентов хлорида. В данных условиях получают насыщенный аналог 6 с выходом 32% (и 47% превращения) и аналог 7, содержащий тройную связь с выходом 31% (70% преобразование). Чистоту также проверяют ВЭЖХ.III-3.3. Сочетание с 2-(ундек-4Z-енилокси)бензоилхлоридом 31 и 4-(ундек-4Zенилокси)бензоилхлоридом 35. Для указанных двух аналогов, путем адаптации аналогичного протокола получают 48% выход для орто-замещенного производного 8 и 40% выход для пара-замещенного производного 9. Для указанных двух реакций используют 4 экв. хлорида. Чистоту также проверяют ВЭЖХ. 3-(ундек-4Z Реакцию проводят, как описано выше, в смеси ДМФА-вода, где исходное вещество и хлорид растворимы. Чтобы способствовать конечной очистке, реакцию проводят в присутствии основной смолыDowex (HCO3-). В конце реакции реакционную смесь разбавляют смесью ацетонитрил/вода и требуемое соединение очищают фильтрованием через смолу, пропуская через кислую смолу Dowex (H+), концентрируют и промывают твердый остаток этилацетатом и затем водой. Таким образом, выделяют 22% целевого продукта 2. Реакцию проводят, как для предыдущего продукта, в смеси ДМФА-вода, где исходное вещество и хлорид растворимы. Чтобы способствовать конечной очистке, реакцию проводят в присутствии основной смолы Dowex (HCO3-). В конце реакции реакционную смесь разбавляют смесью ацетонитрил/вода и требуемое соединение- 15017507 очищают фильтрованием через смолу, пропуская через кислую смолу Dowex (H+), концентрируют и промывают твердый остаток этилацетатом и затем водой. Таким образом, выделяют 28% целевого продукта 10.III-6. Восстановительное алкилирование сульфатированного тетрамера 3-(ундек-4Zенилокси)бензальдегидом. Реакцию восстановительного алкилирования проводят в безводном ДМФА в присутствии бромида лития. Через 24 ч при помощи 12 экв. альдегида и 15 экв. цианборгидрида натрия, посредством хроматографии на силикагеле выделяют 71% целевого продукта сочетания 4. Реакцию проводят в смеси этилацетат-метанол-вода путем добавления уксусного ангидрида в присутствии гидрокарбоната натрия. Через 12 ч исходное вещество 4 удаляют путем пропускания через Н+ смолу. После очистки на диоксиде кремния выделяют требуемый продукт 5 с выходом 77%. Чистоту проверяют ВЭЖХ.IV. Примеры соединения (I). Для производных ароматических соединений кольцо нумеруется согласно официальной номенклатуре. Для описания спектров ЯМР для СО и LCO сахара нумеруют, начиная с восстанавливающего конца Традиционная нумерация принята для каждого сахара. 2-ацетамид-4-О-2-ацетамид-4-О-[2-ацетамид-2-дезокси-4-O-(2-дезокси-2-(N-3-(ундек-4Zенилокси)бензоил)аминD-глюкопиранозил)D-глюкопиранозил]-2-дезоксиD-глюкопиранозил-2 дезокси-D-глюкопираноза (2) 7,2 мг CO-IV(NH2) растворяли в 200 мкл воды и 500 мкл ДМФА и затем нагревали до 40 С. Затем добавляли 36 мг смолы Dowex 12-100 (НСО 3-) с последующим добавлением 160 мкл раствора соединения 19 в перегнанном ТГФ (26 мкмоль). 108 мг НСО 3- смолы и 480 мкл раствора соединения 19 в перегнанном ТГФ (78 мкмоль) добавляли тремя порциями в течение 48 ч. Реакционную смесь разбавляли 3 мл смеси ацетонитрил/вода в соотношении 1/1, реакционную смесь собирали, оставляя смолу, и затем фильтровали через хлопковую вату для удаления захваченных средой шариков смолы. Фильтраты пропускали через смолу Dowex 508-100 (Н+), затем концентрировали и промывали твердый остаток этилацетатом, затем водой. Получали 2 мг белого порошка, т.е. выход составил 22%. 1 Н ЯМР (400 МГц, 20/1 ДМСО-d6/D2O)(м.д.): 7,40-7,31 (м, 3H, ArH-2, ArH-6 и ArH-5), 7,04 (м, 1 Н,ArH-4), 5,41-5,35 (м, 2 Н, СН=СН), 4,87 (д, 0,7 Н, J1,2=2,3 Гц, H-1I), 4,52 (д, 1 Н, J=8,3 Гц, H-1IV), 4,42 (д,0,3H, J=8,0 Гц, H1-I), 4,33 (2 д, 2 Н, J=8,3 Гц, H-1II-III), 3,98 (т, 2 Н, J=6,0 Гц, ArOCH2-СН 2), 3,78-3,05 (м,24 Н, другие атомы Н сахара), 2,16 (дт, 2 Н, J=5,8 и J=6,7 Гц, СН 2-СН=СН), 1,97 (дт, 2 Н, J=6,0 и J=6,2 Гц,СН=СН-СН 2), 1,81/1,81/1,79 (3c, 9 Н, 3 СОСН 3), 1,80-1,72 (м, 2 Н, ArOCH2-СН 2-СН 2), 1,28-1,13 (м, 8 Н, 4 СН 2), 0,81 (т, 3H, СН 3, J=6,5 Гц). Масс-спектр: положительная ионизация электрораспылением (ESI) m/z=1183,5 [M+Na]+. Натриевая соль 2-ацетамид-4-О-2-ацетамид-4-О-[2-ацетамид-2-дезокси-4-O-(2-дезокси-2-(N-3(ундек-4Z-енилокси)бензоил)аминD-глюкопиранозил)D-глюкопиранозил]-2-дезоксиDглюкопиранозил-2-дезокси-6-О-сульфо-D-глюкопиранозы (3) 15 мг CO-IV(NH2,S) (17 мкмоль) растворяли в 100 мкл воды и 250 мкл ДМФА. Затем добавляли 3 мг гидрокарбоната натрия (34 мкмоль) с последующим добавлением 20 мкл раствора соединения 19 в ТГФ в концентрации 0,25 г/мл (16,4 мкмоль). Реакционную смесь нагревали до 60 С и 100 мкл раствора соединения 48 и 10 мг гидрокарбоната натрия добавляли шестью порциями в течение 18 ч. После концентрирования остаток очищали, поместив его в смесь дихлорметан (DCM)/метанол (5/1), на колонке с диоксидом кремния, одновременно сильно разбавляя, для удаления липидной цепи. Затем элюировали смесью E/M/W (7/2/1 этилацетат/метанол/вода). Таким образом, выделяли 6,5 мг белого твердого вещества, т.е. выход составил 33%. 1 11 мг CO-IV(NH2,S) (12 мкмоль) растворяли в 0,5 мл ДМФА, к которому добавляли 12 мг бромида лития. Добавляли 2 мг цианборгидрида натрия (32 мкмоль) и 100 мкл раствора соединения 17 в ТГФ в концентрации 73 мг/мл (26 мкмоль). Реакционную смесь нагревали до 40 С в течение 4 ч. Каждые 2 ч добавляли 2 экв. альдегида и 2,5 экв. цианборгидрида натрия, т.е. в общей сложности 12 экв. альдегида и 15 экв. цианборгидрида натрия. Несмотря на то что преобразование было неполным, реакцию останавливали избытком цианборгидрида натрия с 0,5 н. хлористо-водородной кислотой. Когда выделение газа закончилось, смесь разбавляли водой и сушили вымораживанием. В полученное вещество в воде добавляли 5 мг гидрокарбоната натрия (59 мкмоль) для доведения рН снова до щелочного и полученное вещество затем дважды совместно упаривали с метанолом. Остаточное белое твердое вещество в смесиDCM/метанол (5/1) помещали на колонку с диоксидом кремния, сильно разбавляли для удаления липидной цепи. Затем элюировали смесью E/M/W (5/2/1), затем (4/1/1). Таким образом, выделяли 10 мг белых игл, т.е. выход составил 71%. 1 Н ЯМР (400 МГц, ДМСО-CD3OD (2/1(м.д.): 7,31 (дд, 1 Н, ArH-5, J4,5=8,2 Гц и J5,6=7,8 Гц), 7,02 20 мг гидрокарбоната натрия и 15 мкл уксусного ангидрида добавляли к раствору 13 мг соединения 4 (11 мкмоль) в 0,3 мл E/M/W (1/1/1). Реакционную смесь перемешивали при комнатной температуре в- 17017507 течение 12 ч. После концентрирования в остаточное масло добавляли E/M/W (1/1/1) и смолу Dowex 508-100 Н+. Смесь фильтровали и к фильтрату добавляли смолу Amberlite IR120 Na+. После фильтрования и концентрирования продукт очищали хроматографией в смеси E/M/W (4/1/1). Таким образом,выделяли 10 мг белого твердого вещества, т.е. выход составил 77%. 1 15 мг CO-IV(NH2,S) (17 мкмоль) растворяли в 100 мкл воды и 250 мкл ДМФА. Затем добавляли 6 мг гидрокарбоната натрия (71 мкмоль) и затем 25 мкл раствора соединения 23 в ТГФ при концентрации 210 мг/мл (17 мкмоль). Реакционную смесь нагревали до 60 С и добавляли 200 мкл раствора хлорида и 16 мг гидрокарбоната натрия восемью порциями в течение 24 ч. После концентрирования остаток в смеси DCM/метанол (5/1) очищали, помещая его на колонку с диоксидом кремния, сильно разбавляли для удаления липидной цепи. Затем элюировали смесью E/M/W (4/1/1). Таким образом, выделяли 6,3 мг белого твердого вещества, т.е. выход составил 32%. 1 Н ЯМР (400 МГц, ДМСО-CD3OD (1/3(м.д.): 7,44 (м, 2 Н, ArH-2 и ArH-6), 7,39 (дд, 1 Н, ArH-5,J5,4J5,6=7, 9 Гц), 7,10 (ддд, 1 Н, ArH-4, J4,6J4,2=2,1 Гц), 5,05 (д, 0,7 Н, H-1I, J1,2=3,0 Гц), 4,70-4,40 (м,3,3H, H-1I,II,III,IV), 4,22 (м, 1 Н, Н-6aI), 4,10-3,20 (м, 24 Н, СН 2-OAr и другие атомы Н сахара), 2,03-1,99-1,96 14 мг СО-IV(NH2,S) (16 мкмоль) растворяли в 100 мкл воды и 250 мкл ДМФА. Затем добавляли 5 мг гидрокарбоната натрия (60 мкмоль) и затем 25 мкл раствора соединения 27 в ТГФ при концентрации 190 мг/мл (16 мкмоль). Реакционную смесь нагревали до 60 С и добавляли 200 мкл раствора хлорида и 16 мг гидрокарбоната натрия восемью порциями в течение 24 ч. После концентрирования остаток в смеси DCM/метанол (5/1) очищали на колонке с диоксидом кремния, сильно разбавляли для удаления липидной цепи. Затем элюировали смесью E/M/W (4/1/1). Таким образом, выделяли 5,7 мг целевого продукта в виде белого твердого вещества, т.е. выход составил 31%. 1 Н ЯМР (400 МГц, ДМСО-CD3OD (1/2(м.д.): 7,43 (м, 2 Н, ArH-2 и ArH-6), 7,37 (дд, 1 Н, ArH-5,J5,4=8,1 Гц и J5,6=8,0 Гц), 7,10 (ддд, 1 Н, ArH-4, J4,2J4,6=2,0 Гц), 5,04 (д, 0,7 Н, H-1I, J1,2=3,3 Гц), 4,65-4,59 10 мг CO-IV(NH2,S) (11 мкмоль) растворяли в 100 мкл воды и 250 мкл ДМФА. Затем добавляли 2 мг гидрокарбоната натрия (24 мкмоль) и затем 15 мкл раствора соединения 31 в ТГФ при концентрации 115 мг/мл (6 мкмоль). Реакционную смесь нагревали до 60 С и добавляли 105 мкл раствора хлорида и 6 мг гидрокарбоната натрия семью порциями в течение 18 ч. После концентрирования остаток в смесиDCM/метанол (5/1) очищали на колонке с диоксидом кремния, сильно разбавляли для удаления липидной цепи. Затем элюировали смесью E/M/W (9/2/1). Таким образом, выделяли 6,2 мг белого твердого вещества, т.е. выход составил 48% (но преобразование только 50%). 1 Н ЯМР (400 МГц, ДМСО-CD3OD (1/2(м.д.): 7,99 (дд, 1 Н, ArH-6, J6,5=7,5 Гц и J6,4=1,8 Гц), 7,55 10 мг CO-IV(NH2,S) (11 мкмоль) растворяли в 100 мкл воды и 250 мкл ДМФА. Затем добавляли 2 мг гидрокарбоната натрия (24 мкмоль) и затем 15 мкл раствора соединения 35 в ТГФ при концентрации 115 мг/мл (6 мкмоль). Реакционную смесь нагревали до 60 С и добавляли 105 мкл раствора хлорида и 6 мг гидрокарбоната натрия семью порциями в течение 17 ч. После концентрирования остаток в смесиDCM/метанол (5/1) очищали, помещая его на колонку с диоксидом кремния, сильно разбавляли для удаления липидной цепи. Затем элюировали смесью E/M/W (9/2/1). Таким образом, выделяли 5,2 мг белого твердого вещества, т.е. выход составил 40% (но преобразование только 60%). 1 Н ЯМР (400 МГц, ДМСО-CD3OD (1/2(м.д.): 7,89 (д, 2 Н, ArH-2 и ArH-6, J2,3J6,5=8,8 Гц), 7,04 (д,2 Н, ArH-3 и ArH-5), 5,48 (м, 2 Н, СН=СН), 5,05 (д, 0,6 Н, H-1I, J1,2=3,1 Гц), 4,69-4,55-4,50 (4 д сверхявный, 3,6 Н, H-1I,II,III,IV), 4,30-3,40 (м, 23 Н, другие атомы Н сахаров), 4,10 (т, CH2-OAr, J=6,3 Гц), 2,28-2,09 Пентамер фукозила CO-V(NH2, Fuc) (7,3 мг, 6,4 мкмоль) растворяли в H2O (140 мкл) с последующим добавлением ДМФА (350 мкл) и смесь доводили до 30 С. Затем добавляли смолу Dowex 12-100(НСО 3-) с последующим добавлением раствора (ТГФ, 110 мкл) хлорангидрида 19 (6 мг). Реакционную- 19017507 смесь перемешивали в течение 24 ч, в течение этого времени три раза добавляли дополнительное количество смолы и раствора хлорангидрида. Затем реакционную смесь разбавляли в смеси H2O/CH3CN (1/1,2 мл), нагревали до 56 С и затем надосадочный раствор фильтровали через хлопковую вату. Шарики смолы и стенки колбы экстрагировали несколько раз при 56 С смесью H2O/CH3CN (4/1, 7/3, 3/2, 1/1, 2/3,3/7 и 1/4, по 2 мл каждого). Различные фракции пропускали через смолу Dowex 508-100 (Н+), затем объединяли и концентрировали. Остаток последовательно промывали EtOAc (31 мл), затем Н 2 О (31 мл) и затем повторно растворяли в смеси H2O/CH3CN (1/1, 10 мл) при нагревании до 56 С, с последующей обработкой ультразвуком. Затем раствор сушили вымораживанием и получали целевой продукт в виде белого порошка (2,5 мг, 28%). Исходное вещество, оставшееся в кислой смоле, затем элюировали (2,3 мг, 31%) водным раствором аммиака (Н 2 О, 2%). 1(6,07 ммоль) в безводном ДМФА (20 мл). После реакции в течение 4 ч при 90 С реакционную смесь концентрировали, переводили в раствор DCM и затем промывали водой. Получали 1,87 г желтого масла и выделяли хроматографией на силикагеле в смеси пентан/этилацетат (50/1). Выделяли 1,37 г желтого масла, т.е. выход составил 76%. 1 Н ЯМР (250 МГц, CDCl3)(м.д.): 7,60 (ддд, 1 Н, ArH-6, J6,5=8,0 Гц и J6,4=J6,2=0,5 Гц), 7,52 (дд, 1 Н,ArH-2, J2,4=3,0 Гц), 7,31 (дд, 1 Н, ArH-5, J5,4=8,0 Гц), 7,07 (ддд, 1 Н, ArH-4), 5,38 (м, 2 Н, СН=СН), 3,98 (т,2 Н, CH2-OAr, J=6,3 Гц), 3,89 (с, 3H, ОСН 3), 2,22-1,99 (2 м, 4 Н, СН 2-СН=СН-СН 2), 1,83 (тт, 2 Н, ArO-СН 2 СН 2-СН 2-СН=СН, J=6,8 Гц), 1,55-1,20 (м, 8 Н, 4 СН 2), 0,84 (т, 3H, СН 3, J=7,5 Гц); 13 С ЯМР (62,5 МГц, CDCl3)(м.д.): 131-129-128 (С-5, СН=СН), 122 (С-6), 120 (С-4), 115 (С-2), 66 35 мг литий-алюминий гидрида (922 мкмоль) добавляли при 0 С к 140 мг соединения 15 (460 мкмоль) в простом эфире (3 мл). После реакции в течение 1 ч 30 мин реакционную смесь разбавляли простым эфиром и гидролизовали двумя каплями воды. После фильтрования через Celite, сушки над 10 мл безводного DCM и затем 190 мг РСС (881 мкмоль) добавляли в атмосфере аргона к 120 мг спирта 16 (434 мкмоль), высушенного совместным упариванием с толуолом. Температуру реакции поднимали до температуры кипения с обратным холодильником DCM на 1 ч. После охлаждения реакционную смесь разбавляли простым эфиром и фильтровали через Florisil. После концентрирования получали 118 мг желтого масла, т.е. выход составил 99%. 1 Н ЯМР (250 МГц, CDCl3)(м.д.): 9,95 (с, 1 Н, СНО), 7,42 (м, 2 Н, ArH-6 и ArH-5), 7,36 (д, 1 Н, ArH2, J2,4=2,9 Гц), 7,15 (м, 1 Н, ArH-4), 5,39 (м, 2 Н, СН=СН), 3,99 (т, 2 Н, СН 2-OAr, J=6,3 Гц), 2,21-1,99 (2 м,4 Н, СН 2-СН=СН-СН 2), 1,84 (тт, 2 Н, ArO-СН 2-СН 2-СН 2-СН=СН, J=6,8 Гц), 1,40-1,15 (м, 8 Н, 4 СН 2), 0,84 4 мл 1 н. раствора гидроксида натрия (4,0 ммоль) добавляли порциями к 1,14 г соединения 15 (3,74 ммоль) в метаноле (30 мл). Раствор кипятили с обратным холодильником в течение ночи. Дополнительно добавляли 4 мл 1 н. раствора гидроксида натрия и смесь кипятили с обратным холодильником дополнительно 1 ч 30 мин. После выпаривания растворителя реакционную смесь подкисляли 0,5 н. HCl и экстрагировали DCM. Получали 1,04 г желтого масла, т.е. выход составил 96%. 1 Н ЯМР (200 МГц, CDCl3)(м.д.): 10,00-9,00 (ушир.д, 1 Н, СО 2 Н), 7,69 (д, 1 Н, ArH-6, J6,5=7,8 Гц),7,60 (д, 1 Н, ArH-2, J2,4=2,4 Гц), 7,35 (дд, 1 Н, ArH-5, J5,4=8,3 Гц), 7,14 (дд, 1 Н, ArH-4), 5,40 (м, 2 Н,СН=СН), 4,00 (т, 2 Н, CH2-OAr, J=6,3 Гц), 2,21-2,00 (2 м, 4 Н, СН 2-СН=СН-СН 2), 1,85 (тт, 2 Н, ArO-СН 2 СН 2-СН 2-СН=СН, J=6,8 Гц), 1,35-1,05 (м, 8 Н, 4 СН 2), 0,85 (т, 3H, СН 3, J=6,5 Гц); 13 С ЯМР (50 МГц, CDCl3)(м.д.): 172 (СО 2 Н), 159 (С-3), 131-130-130-128 (С-1, С-5, СН=СН), 121122 (С-4, С-6), 115 (С-2), 67 (СН 2-OAr), 32-23 (7 СН 2), 14 (СН 3). Масс-спектр: отрицательная ESI m/z=289,l [M-H]-. Вычислено для C18H25O3: 289,180370. Найдено: 289,180730. Элементный анализ 1 мл оксалилхлорида (11,5 ммоль) и две капли безводного ДМФА добавляли в атмосфере аргона к 100 мг высушенного толуолом соединения 18 (345 мкмоль), растворенного в 20 мл безводного DCM. Смесь перемешивали при комнатной температуре в течение 2 ч и затем концентрировали, получая 106 мг целевого хлорида в виде желтого масла, т.е. выход составил 99%. 1 Н ЯМР (250 МГц, CDCl3)(м.д.): 7,71 (ддд, 1 Н, ArH-6, J6,5=8,3 Гц, J6,4=2,4 Гц и J6,2=0,9 Гц), 7,57(2,35 ммоль) в безводном ДМФА (7 мл). После реакции в течение 16 ч при 90 С, реакционную смесь концентрировали, разбавляли в DCM и затем промывали водой. Получали 607 мг желтого масла и хроматографировали на силикагеле в смеси пентан/этилацетат (60/1). Выделяли 579 мг целевого продукта сочетания в виде желтого масла, т.е. выход составил 82%. 600 мкл 1 н. раствора гидроксида натрия (600 мкмоль) добавляли порциями к 112 мг соединения 21(366 мкмоль) в метаноле (4 мл). Раствор кипятили с обратным холодильником в течение 2 ч. После выпаривания растворителя реакционную смесь подкислили 0,5 н. HCl и экстрагировали DCM. Получали 107 мг требуемой кислоты в виде белого твердого вещества, т.е. выход составил 99%. 1 Н ЯМР (250 МГц, CDCl3)(м.д.): 7,70 (д, 1 Н, ArH-6, J6,5=7,8 Гц), 7,62 (м, 1 Н, ArH-2), 7,38 (дд, 1 Н,ArH-5, J5,4=8,0 Гц), 7,16 (дд, 1 Н, ArH-4, J4,2=2,1 Гц), 4,02 (т, 2 Н, СН 2-OAr, J=6,5 Гц), 1,99 (тт, 2 Н, ArOCH2-CH2-CH2, J=6,6 Гц), 1,55-1,20 (м, 16 Н, 8 СН 2), 0,89 (т, 3H, СН 3, J=6,5 Гц); 13 С ЯМР (62,5 МГц, CDCl3)(м.д.): 171 (СО 2 Н), 159 (С-3), 130 (С-1), 129 (С-5), 122 (С-6), 121 (С-4),115 (С-2), 68 (СН 2-OAr), 32-23 (9 СН 2), 14 (СН 3). Масс-спектр: отрицательная ESI m/z=291,2 [M-H]-. Вычислено для C18H27O3: 291,196020. Найдено: 291,196560. Инфракрасный (см-1): 2950-2920-2850-2700-2400-1680-1603-1455-1420-1312-1247-757. Точка плавления: 88 С. 3-(Ундеканилокси)бензоилхлорид (23) 1 мл оксалилхлорида (11,5 ммоль) и две капли безводного ДМФА добавляли в атмосфере аргона к 93 мг высушенной толуолом кислоты 22 (318 мкмоль), растворенной в 20 мл безводного DCM. Смесь перемешивали при комнатной температуре в течение 2 ч и затем концентрировали, получая 99 мг желтого масла, т.е. выход составил 99%. Метил-3-(ундек-4-инилокси)бензоат (25)(2,16 ммоль) в безводном ДМФА (7 мл). После реакции в течение 6 ч при 90 С, реакционную смесь концентрировали, промывали DCM и затем разбавляли в воде. Получали 639 мг желтого масла и хроматографировали на силикагеле в смеси пентан/этилацетат (50/1). Выделяли 429 мг желтого масла, т.е. выход составил 66%. 1 Н ЯМР (200 МГц, CDCl3)(м.д.): 7,63 (м, 1 Н, ArH-6), 7,57 (м, 1 Н, ArH-2), 7,31 (дд, 1 Н, ArH-5,J5,4=8,1 Гц и J5,6=7,8 Гц), 7,11 (ддд, 1 Н, ArH-4, J4,6=2,4 Гц и J4,2=0,8 Гц), 4,11 (т, 2 Н, CH2-OAr, J=6,2 Гц),3,92 (с, 3H, ОСН 3), 2,39-2,15 (2 м, 4 Н, СН 2-С=С-СН 2), 1,98 (тт, 2 Н, ArO-CH2-CH2-CH2-C=C, J=6,5 Гц),1,52-1,23 (м, 8 Н, 4 СН 2), 0,88 (т, 3H, СН 3, J=6,7 Гц); 13 С ЯМР (62,5 МГц, CDCl3)(м.д.): 167 (СО 2 СН 3), 159 (С-3), 131 (С-1), 129 (С-5), 122 (С-6), 120 (С 4), 115 (С-2), 81-79 (СС), 67 (СН 2-OAr), 52 (СН 3 О), 31-15 (7 СН 2), 14 (СН 3). Масс-спектр: положительная ESI m/z=325,1 [M+Na]+. Вычислено для C19H26O3Na: 325,177964. Найдено: 325,178070. Инфракрасный (см-1): 2950-2931-2857-1726-1586-1446-1288-1228-756. 3-(Ундек-4-инилокси)бензойная кислота (26) 300 мкл 1 н. раствора гидроксида натрия (300 мкмоль) добавляли порциями к 48 мг соединения 25(157 мкмоль) в метаноле (2 мл). Раствор кипятили с обратным холодильником в течение 1 ч 30 мин. После выпаривания растворителя реакционную смесь подкисляли 0,5 н. HCl и экстрагировали DCM. Получали 45 мг бледного желтого масла, т.е. выход составил 99%. 1 Н ЯМР (250 МГц, CDCl3)(м.д.): 11,00-10,00 (ушир.д, 1 Н, СО 2 Н), 7,72 (д, 1 Н, ArH-6, J6,5=7,7 Гц),7,64 (м, 1 Н, ArH-2), 7,38 (дд, 1 Н, ArH-5, J5,4=8,1 Гц), 7,17 (дд, 1 Н, ArH-4, J4,2=2,7 Гц), 4,13 (т, 2 Н, CH2- 22017507 850 мкл оксалилхлорида (9,74 ммоль) и две капли безводного ДМФА добавляли в атмосфере аргона к 80 мг высушенной толуолом кислоты 26 (278 мкмоль), растворенной в 17 мл безводного DCM. Смесь перемешивали при комнатной температуре в течение 2 ч и затем концентрировали, получая 85 мг желтого масла, т.е. выход составил 99%. Метил-2-(ундек-4Z-енилокси)бензоат (29)(500 мкмоль) в безводном ДМФА (2 мл). После реакции в течение 8 ч при 90 С реакционную смесь концентрировали, разбавляли в DCM и затем промывали водой. Получали 137 мг желтого масла и хроматографировали на силикагеле в смеси пентан/этилацетат (40/1). Выделяли 100 мг желтого масла, т.е. выход составил 66%. 1 Н ЯМР (250 МГц, CDCl3)(м.д.): 7,79 (дд, 1 Н, ArH-6, J6,5=8,1 Гц и J6,4=1,9 Гц), 7,43 (ддд, 1 Н, ArH4, J4,3=8,5 Гц, J4,5=7,3 Гц), 6,94 (м, 2 Н, ArH-5 и ArH-3), 5,40 (м, 2 Н, СН=СН), 4,02 (т, 2 Н, CH2-OAr, J=6,3 Гц), 3,89 (с, 3H, ОСН 3), 2,28-2,01 (2 м, 4 Н, СН 2-СН=СН-СН 2, J=6,6 Гц), 1,89 (тт, 2 Н, ArO-СН 2-СН 2-СН 2,J=6,6 Гц), 1,50-1,16 (м, 8 Н, 4 СН 2), 0,86 (т, 3H, СН 3, J=6,6 Гц); 13 С ЯМР (62,5 МГц, CDCl3)(м.д.): 167 (С=О), 158 (С-2), 133 (С-4), 131 (СН=СН), 128 (С-6), 120 (С 1), 119 (С-5), 113 (С-3), 68 (СН 2-OAr), 52 (СН 3 О), 32-22 (7 СН 2), 14 (СН 3). Масс-спектр: положительная ESI m/z=327,2 [M+Na]+. Вычислено для C19H28O3Na: 327,193914. Найдено: 327,192560. Инфракрасный (см-1): 3000-2962-2925-2855-1734-1601-1491-1456-1305-1250-754. 2-(Ундек-4Z-енилокси)бензойная кислота (30) 500 мкл 1 н. раствора гидроксида натрия (500 мкмоль) добавляли порциями к 80 мг соединения 29(263 мкмоль) в метаноле (3 мл). Раствор кипятили с обратным холодильником в течение 24 ч. После выпаривания растворителя реакционную смесь подкислили 0,5 н. HCl и экстрагировали DCM. Получали 76 мг желтого масла, т.е. выход составил 99%. 1 800 мкл оксалилхлорида (9,17 ммоль) и две капли безводного ДМФА добавляли в атмосфере аргона к 76 мг высушенной толуолом кислоты 30 (262 мкмоль), растворенной в 15 мл безводного DCM. Смесь перемешивали при комнатной температуре в течение 2 ч и затем концентрировали, получая 80 мг желтого масла, т.е. выход составил 99%. 1 Н ЯМР (250 МГц, CDCl3)(м.д.): 7,97 (дд, 1 Н, ArH-6, J6,5=7,9 Гц и J6,4=1,7 Гц), 7,46 (м, 1 Н, ArH-4),6,90 (м, 2 Н, ArH-5 и ArH-3), 5,30 (м, 2 Н, СН=СН), 3,95 (т, 2 Н, СН 2-OAr, J=6,3 Гц), 2,20-1,90 (2 м, 4 Н, СН 2 СН=СН-СН 2), 1,79 (тт, 2 Н, ArO-СН 2-СН 2-СН 2-СН=СН, J=6,6 Гц), 1,20-1,09 (м, 8 Н, 4 СН 2), 0,76 (т, 3H,- 23017507(535 мкмоль) в безводном ДМФА (2 мл). После реакции в течение 7 ч при 90 С реакционную смесь концентрировали, разбавляли в DCM и затем промывали водой. Получали 163 мг желтого масла и хроматографировали на силикагеле в смеси пентан/этилацетат (80/1). Выделяли 129 мг целевого продукта сочетания в виде желтого масла, т.е. выход составил 79%. 1 Н ЯМР (250 МГц, CDCl3)(м.д.): 7,97 (д, 2 Н, ArH-2 и ArH-6, J6,5J2,3=8,8 Гц), 6,89 (д, 2 Н, ArH-3 и 550 мкл 1 н. раствора гидроксида натрия (550 мкмоль) добавляли порциями к 109 мг соединения 33(358 мкмоль) в метаноле (4 мл). Раствор кипятили с обратным холодильником в течение 20 ч. После выпаривания растворителя реакционную смесь подкислили 0,5 н. HCl и экстрагировали DCM. Получали 102 мг белого твердого вещества, т.е. выход составил 98%. 1 1 мл оксалилхлорида (11,5 ммоль) и две капли безводного ДМФА добавляли в атмосфере аргона к 101 мг высушенной толуолом кислоты 34 (348 мкмоль), растворенной в 18 мл безводного DCM. Смесь перемешивали при комнатной температуре в течение 2 ч и затем концентрировали, получая 107 мг желтого масла, т.е. выход составил 99%. 1 Н ЯМР (250 МГц, CDCl3)(м.д.): 7,96 (д, 2 Н, ArH-2 и ArH-6, J2,3J6,5=8,7 Гц), 6,99 (д, 2 Н, ArH-3 иV.1. Тесты на активность у temperate бобовых растений группы Galegoid. У temperate бобов группы Galegoid клубни образуются благодаря клубневым бактериям, которые продуцируют Nod-факторы с гидрофобной цепью, содержащей двойную связь, сопряженную с карбонильной группой. Данная группа включает важные сельскохозяйственные бобовые культуры, такие как люцерна, горох, кормовые бобы, нут и клевер. Композиции тестировали на люцерне на способность индуцировать образование корневых клубней,и на модели бобовых Medicago truncatula на индукцию экспрессии симбиотического гена, кодирующего ранний нодулин.V.1.1. Тесты на образование клубней у люцерны. Сеянцы люцерны выращивали в аксенических условиях в пробирках на бедной азотом агаровой среде (Demont-Caulet et al., Plant Physiol., 120, 83-92, 1999). Необработанные сеянцы или сеянцы, обработанные природными nod-факторами или синтетическими LCO, служили контролем.V.1.2. Тесты на индукцию раннего нодулина у Medicago truncatula. Данные тесты проводили для определения, вызывают ли композиции симбиотическую реакцию, ак- 24017507 тивируя тот же самый путь трансдукции сигнала, что и природные Nod-факторы. Тесты проводили на модели бобовых Medicago truncatula. Действие композиций изучали на растениях "дикого типа" и на мутанте по гену DMI1, измененном в трансдукции сигнала Nod-фактора (Catoira et al., Plant Cell, 12 16471665, 2000). Соединение, которое служит стандартом, является сульфатированным тетрамером 12 ацилированным С 16:22 Е, 9Z цепью, являющимся аналогом природного Nod-фактора. Необработанные сеянцы или сеянцы, обработанные только природными Nod-факторами или синтетическими LCO, служат контролем.V.1.2.1. Репортерный ген. В целом, трудно определить регулирование экспрессии специфического гена во время биологического процесса, поскольку большинство специфических продуктов данных генов не являются легко обнаруживаемыми или измеримыми. Чтобы преодолеть эту проблему, применяют метод слияния с "репортерными генами", т.е. генами, кодирующими легко определяемый белок. Слияние состоит в объединении последовательности ДНК, содержащей области регуляции гена, который желательно изучить, с последовательностью ДНК репортерного гена. Их сборку затем повторно вводят в растение путем трансформации. Таким образом, если экспрессируется целевой ген, автоматически экспрессируется репортерный ген. Далее задача состоит в определении белка репортерного гена. Чтобы избежать негативного влияния на активность растения, используют репортерные гены, которые не кодируют ни один фермент, обычно синтезируемый растениями. Одним из ферментов, используемым наиболее широко, является -гклюкуронидаза (GUS) от Escherichia coli, гидролаза, которая катализирует расщепление большого разнообразия-глюкуронид. В качестве коммерческого субстрата указанного фермента можно использовать X-Gluc (Sigma B-4782): 5-6 ром-4-хлор-3-индолил глюкуронид; образуемый анион имеет синий цвет.V.1.2.2. Enod11GUSA. Гены бобовых растений, вовлеченные в образование клубней, могут быть разделены на два главных типа: гены раннего нодулина (ENOD), которые активируются в первые дни инфекции и активации процесса образования клубней; гены позднего нодулина, которые не активируются в течение нескольких дней с момента появления бактерий и не вмешиваются до периода созревания клубней. Был обнаружен новый ген Medicago truncatula, MtENOD11, кодирующий RPRP (повторяющийся пролин-богатый белок) и транскрибирующийся во время первых стадий инфекции образования клубней на корнях и тканях (Journet et al., Mol. Plant Microbe Interact., 14, 737-748, 2001). При помощи трансгенного растения Medicago truncatula, экспрессирующего сливание MtENOD11GUSA, можно определить,вызывает ли композиция, добавленная к культуральной среде растения, транскрипцию гена ENOD11. Для тестов на транскрипцию ENOD11 использовали среду Fahraeus, как для тестов на модуляцию,но без агара. Сеянцы помещали на бумагу в пакетах, содержащих культуральную смесь. Сравнивали реакцию двух типов трансгенных растений, имеющих MtENOD11GUS: сливание: "дикий тип" (WT) Jemalong растение и растение, имеющее мутацию в гене DMI1, которое неспособно преобразовывать сигналы Nod-фактора. Растения оставляли расти в течение 5 дней и сеянцы затем обрабатывали различными концентрациями LCO. Через 6 ч сеянцы вытаскивали и помещали в водную смесь, содержащую X-Gluc на 1-2 ч. Затем подсчитывали число корней, дающих характерную синюю окраску. Данный тест относительно чувствителен до такой степени, что можно работать с концентрациямиLCO ниже концентраций для тестов на образование клубней.V.2. Тесты на активность у других бобовых растений.Lotus corniculatus является кормовой культурой, у которого появляются корневые клубни благодаря клубневым бактериям, продуцирующим Nod-факторы, весьма схожие с теми, которые продуцируются клубневыми бактериями, вызывающими образование клубней у сои: основная структура олигомера хитина имеет пять остатков глюкозамина, N-ацильная цепь, по существу, является вакценовой кислотой(С 18:1) и восстанавливающий остаток глюкозамина несульфатирован и О-замещен остатком фукозила.Lotus corniculatus выбирали в качестве модели системы, поскольку семена и сеянцы имеют небольшой размер и удобны в обращении.V.2.1. Определение деформации волоска корня у Lotus corniculatus. Стерилизовали семена Lotus corniculatus (условное название Rodeo). Проросшие семена с корешками длиной приблизительно 1 см асептически переносили на чашки с мягким агаром Farhaeus. Чашки запечатывали пленкой Parafilm и помещали вертикально на два дня в камеру роста растения (при 25 С, со световым периодом 16 ч, при относительной влажности 75%, тип освещения OsramVFluora L 77, и при интенсивности освещения на уровне поверхности чашек 30 мкЕ.m-2.S-1), чтобы растение росло и разви- 25017507 вало корневые волоски. Затем наливали 2 мл стерильного раствора производного соединения Nodфактора таким образом, чтобы покрыть корневую систему Lotus, и через 30 мин излишек жидкости удаляли. Дополнительную инкубацию проводили в течение 16 ч в камере роста растения. Корни пяти растений помещали между предметным и покровным стеклами и рассматривали светлопольной микроскопией после окрашивания метиленовым синим. Чтобы оценить реакцию растения, выбирали критерий четко выраженного ветвления волосков(многочисленное ветвление на более чем одном участке корневой системы), и растения, демонстрирующие такую четкую реакцию, классифицировали как "+". Статистическую значимость (при Р=0,05) доли"+" реакции вычисляли с использованием сравнений отношения на основе "точного" критерия ФишераV.3.1. Вычисление эффективности. Ожидаемую эффективность данной комбинации двух соединений вычисляли следующим образомX - эффективность, выраженная в % смертности необработанного контроля для тестируемого соединения А при концентрации m ч./млн., соответственно m г/га;Y - эффективность, выраженная в % смертности необработанного контроля тестируемого соединения В при концентрации n ч./млн., соответственно n г/га; Е - эффективность, выраженная в % смертности необработанного контроля тестируемой смеси соединений А и В при концентрациях m и n ч./млн., соответственно m и n г/га; тогда Если наблюдаемая инсектицидная эффективность комбинации выше эффективности, вычисленной как "Е", то комбинация указанных двух соединений сверхаддитивна, т.е. имеет место синергический эффект.V.3.2. Тест на Myzus persicae. Растворитель: 7 мас.ч. диметилформамида. Эмульгатор: 2 мас.ч. простого полигликолевого эфира алкиларила. Чтобы получить подходящий препарат активного соединения, 1 мас.ч. активного соединения смешивали с установленным количеством растворителя и эмульгатора и концентрат разбавляли водой, содержащей эмульгатор, до желаемой концентрации. Листья капусты (Brassica oleracea), тяжело инфицированные (green peach aphid) тлей персиковой (Myzus persicae), обрабатывали путем окунания в препарат активного соединения желаемой концентрации. Через указанный промежуток времени определяли % смертности. 100% означает, что вся тля уничтожена; 0% означает, что ни одна из тлей не уничтожена. Согласно настоящему изобретению в данном тесте, например, следующая комбинация демонстрирует синергический эффект по сравнению с отдельными соединениями. Таблица А Насекомые, поражающие растения Myzus persicae - тест набл.=наблюдаемая инсектицидная эффективность вычисл.=эффективность, рассчитанная по формуле ColbyV.3.2. Тест на Phaedon cochleariae. Растворитель: 7 мас.ч. диметилформамида. Эмульгатор: 2 мас.ч. простого полигликолевого эфира алкиларила. Чтобы получить подходящий препарат активного соединения, 1 мас.ч. активного соединения смешивали с установленным количеством растворителя и эмульгатора и концентрат разбавляли водой, содержащей эмульгатор, до желаемой концентрации. Листья капусты (Brassica oleracea) обрабатывали пу- 26017507 тем окунания в препарат активного соединения желаемой концентрации и инфицировали личинками листоеда хренового (Phaedon cochleariae), пока листья были еще влажными. Через указанный промежуток времени определяли % смертности. 100% означает, что все личинки листоеда хренового уничтожены; 0% означает, что ни одна из личинок листоеда хренового не уничтожена. Согласно настоящему изобретению в данном тесте, например, следующие комбинации демонстрируют синергический эффект по сравнению с отдельными соединениями. Таблица В Насекомые, поражающие растения Phaedon cochleariae - тест набл.=наблюдаемая инсектицидная эффективность вычисл.=эффективность, рассчитанная по формуле Colby ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Пестицидная композиция, содержащая: а) соединение общей формулы (I)D представляет собой линейную углеводородную цепь, содержащую 11 атомов углерода, которая является насыщенной или содержит ненасыщенную связь между 4 и 5 атомами углерода; Е и G независимо друг от друга представляют собой заместитель NHR20;R20 - С(О)C1-6 алкил; а также его возможные геометрические и/или оптические изомеры, энантиомеры и/или диастереомеры и сельскохозяйственно приемлемые соли; иb) инсектицидное соединение, которое является агонистом или антагонистом ацетилхолинового рецептора, в массовом соотношении (а)/(b) от 1/1 до 1/1013. 2. Композиция по п.1, в которой Е и G представляют собой NHC(O)CH3. 3. Композиция по п.1 или 2, где R8 представляет собой Н, SO3H, SO3Li, SO3Na, SO3K,SO3N(C1-8 алкил)4 или заместитель формулы- 27017507 4. Композиция по п.3, где R26, R27 и R28 представляют собой атом водорода. 5. Композиция по любому одному из пп.1-4, где соединение (I) соответствует одной из следующих формул:
МПК / Метки
МПК: A01N 43/16, A01P 3/00, A01P 7/04
Метки: качестве, композиция, инсектицидное, полезное, клубней, пестицидная, соединение, растений, синтетическое, образования, бобовых, содержащая, средства
Код ссылки
<a href="https://eas.patents.su/30-17507-pesticidnaya-kompoziciya-soderzhashhaya-sinteticheskoe-soedinenie-poleznoe-v-kachestve-sredstva-dlya-obrazovaniya-klubnejj-u-bobovyh-rastenijj-i-insekticidnoe-soedinenie.html" rel="bookmark" title="База патентов Евразийского Союза">Пестицидная композиция, содержащая синтетическое соединение, полезное в качестве средства для образования клубней у бобовых растений, и инсектицидное соединение</a>
Предыдущий патент: Способ превращения нитрильных соединений в карбоновые кислоты и в соответствующие сложные эфиры
Следующий патент: Быстро диссоциирующие антагонисты рецептора 2 дофамина
Случайный патент: Система фиксации элементов заполнения в каркасных конструкциях из алюминиевого профиля и опорная подкладка