Замещённые фенокси- и фенилтиопроизводные для лечения пролиферативных нарушений
Номер патента: 12980
Опубликовано: 26.02.2010
Авторы: Редди Е.Премкумар, Редди М.В.Рамана, Белл Стэнли К.
Формула / Реферат
1. Соединение формулы I
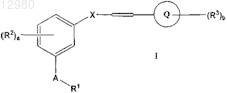
в которой А представляет собой -S- или -O-;
R1 выбран из группы, состоящей из -Н, -C(=O)Rw, -SO2Rw, -((C1-C6)гидрокарбилен)Rzи -Р(=O)(ORv)2;
каждый Rv независимо выбран из группы, состоящей из -Н и -(C1-C7)гидрокарбила;
Rw выбран из группы, состоящей из -(C1-C7)гидрокарбила, NRv2, -ORv, галоген(C1-C3)алкила, -NRvCRvRa-C(=O)-Rn, -CRvRa-N(Rv)-Rc, замещенного и незамещенного арила, замещенного и незамещенного арил(C1-C3)алкила, замещенного и незамещенного гетероарила, замещенного и незамещенного гетероарил(C1-C3)алкила, замещенного и незамещенного гетероциклила, замещенного и незамещенного гетероциклил(C1-C3)алкила, -((C1-C3)алкилен)-Р(=O)(ORv)2, -(C1-C3)перфторалкилен-N(СН3)2, -(C1-C3)алкилен-N((C1-C3)алкил)2, -(C1-C3)алкилен-N+((C1-C3)алкил)3, -(C1-C3)алкилен-N+(СН2СН2ОН)3, -((C1-C4)алкилен)-С(=O)галогена, -(C1-C4)перфторалкилен-CO2Rv, -((C1-C3)алкилен)-С(=O)ORvи -((C1-C3)алкилен)-ОС(=O)-((C1-C3)алкилен)-С(=O)Ry;
Ry выбран из группы, состоящей из -ORv, -NRv2и -(C1-C6)алкила;
Rz выбран из группы, состоящей из -C(=O)Ry, -NRvCRvRa-C(=O)-Rn, -NRv2, -ORv, замещенного и незамещенного арила, замещенного и незамещенного гетероарила, замещенного и незамещенного гетероциклил(C1-C3)алкила и -С(=O)(C1-C3)алкила;
каждый Ra независимо выбран из группы, состоящей из -Н, -(C1-C6)алкила, -(C1-C6)гетероалкила, -(СН2)3-NH-C(NH2)(=NH), -CH2C(=O)NH2, -CH2COOH, -(CH2)2COOH, замещенного и незамещенного арила, замещенного и незамещенного арил(C1-C3)алкила, замещенного и незамещенного гетероциклила и замещенного и незамещенного гетероциклил(C1-C3)алкила;
каждый Rn независимо выбран из группы, состоящей из -ORv, -NRv2 и присоединенного по N-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая карбоксильная группа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -CO2Rv и
-C(=O)NRv2;
каждый Rc независимо выбран из группы, состоящей из -Н и присоединенного по С-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая аминогруппа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -NH2, -NHC(=O)(C1-C6)алкила;
-NH(C1-C6)алкила, -NH((C1-C6)алкил)2и -NHC(=O)О(C1-C7)гидрокарбила;
Q представляет собой арил или гетероарил;
каждый R2 и R3 независимо выбран из группы, состоящей из галогена; -(C1-C7)гидрокарбила, -C(=O)Rv, -NRv2,
-NHC(=O)Rv, -NHSO2Rv, -NHRa, -NHCRvRaC(=O)Rn, -NHSO2Rv, -C(=O)ORv, -C(=O)NHRv, -NO2, -CN, -ORv,
-P(=O)(ORv)2, -C(=NH)NH2, диметиламино(C2-C6)алкокси, -NHC(=NRv)NHRv, -(C1-C6)галогеналкила и -(C1-C6)галогеналкокси;
две группы Rv на Р(=O)(ORv)2 и -NRv2 могут необязательно образовать 5- или 6-членное гетероциклическое кольцо, которое может дополнительно необязательно быть конденсировано с арильным или карбоциклическим кольцом;
а равно 0, 1, 2 или 3;
b равно 0, 1, 2 или 3;
конфигурация заместителей относительно экзоциклической углерод-углеродной двойной связи представляет собой либо Е-, либо Z-;
X представляет собой -C*H(Rx)Y- или -NRx-Z-;
Y представляет собой -SO2-;
Z представляет собой -SO2-;
Rx выбран из группы, состоящей из -Н, -(C1-C6)алкила и -С(=O)(C1-C6)алкила; и
* указывает, что, когда Rx является другим, чем -Н, конфигурация заместителей при обозначенном углеродном атоме представляет (R)-, (S)- или любую смесь (R)- и (S)-,
или соль такого соединения;
при условии, что:
(a) когда А представляет собой -О- и R1 представляет собой -Н,
b больше чем 0 и
R3 является другим, чем (C1-C6)алкил, -ОН и -NO2;
(b) когда X представляет собой -NRx-Z- и А представляет собой -О-,
Rz является другим, чем -C(=O)Ry, -NRv2и незамещенный арил; и
Rw является другим, чем -(C1-C6)алкил; и
(c) когда X представляет собой -C*H(Rx)Y- и А представляет собой -O-,
Rz является другим, чем -NRv2 и незамещенный арил; и
Rw является другим, чем -(C1-C7)гидрокарбил;
где арил означает карбоциклическую ароматическую систему, содержащую один, два или три кольца;
гетероциклил означает моно- или полигетероциклическую кольцевую систему, содержащую углеродные атомы и по крайней мере один гетероатом, выбранный из группы, состоящей из N, О и S, и где гетероатомы азота и серы могут быть необязательно окислены;
гетероарил означает моноциклическую или полициклическую гетероциклическую кольцевую систему, содержащую по крайней мере одно ароматическое кольцо и необязательно одно или несколько частично насыщенных колец; и
где арил, гетероарил и гетероциклил, указанные в определениях R1, Rv, Rw, Rz и Ra, являются независимо необязательно замещенными и где заместители независимо выбирают из группы, состоящей из галогена, -(C1-C7)гидрокарбила, гетероциклила, -C(=O)Rv, -NRv2, -NHC(=O)Rv, -NHSO2Rv, -NHRa, -NHCRvRaC(=O)Rn,
-NHSO2Rv, -C(=O)ORv, -C(=O)NHRv, -NO2, -CN, -ORv, -P(=O)(ORv)2, -C(=NH)NH2, -O(C2-C6)алкилен-NRv2, -(C2-C6)алкилен-NRv2, -SO2-NRv2, -NHC(=NRv)NHRv, -(C1-С6)галогеналкила и -(C1-C6)галогеналкокси.
2. Соединение по п.1, где Q представляет собой арил.
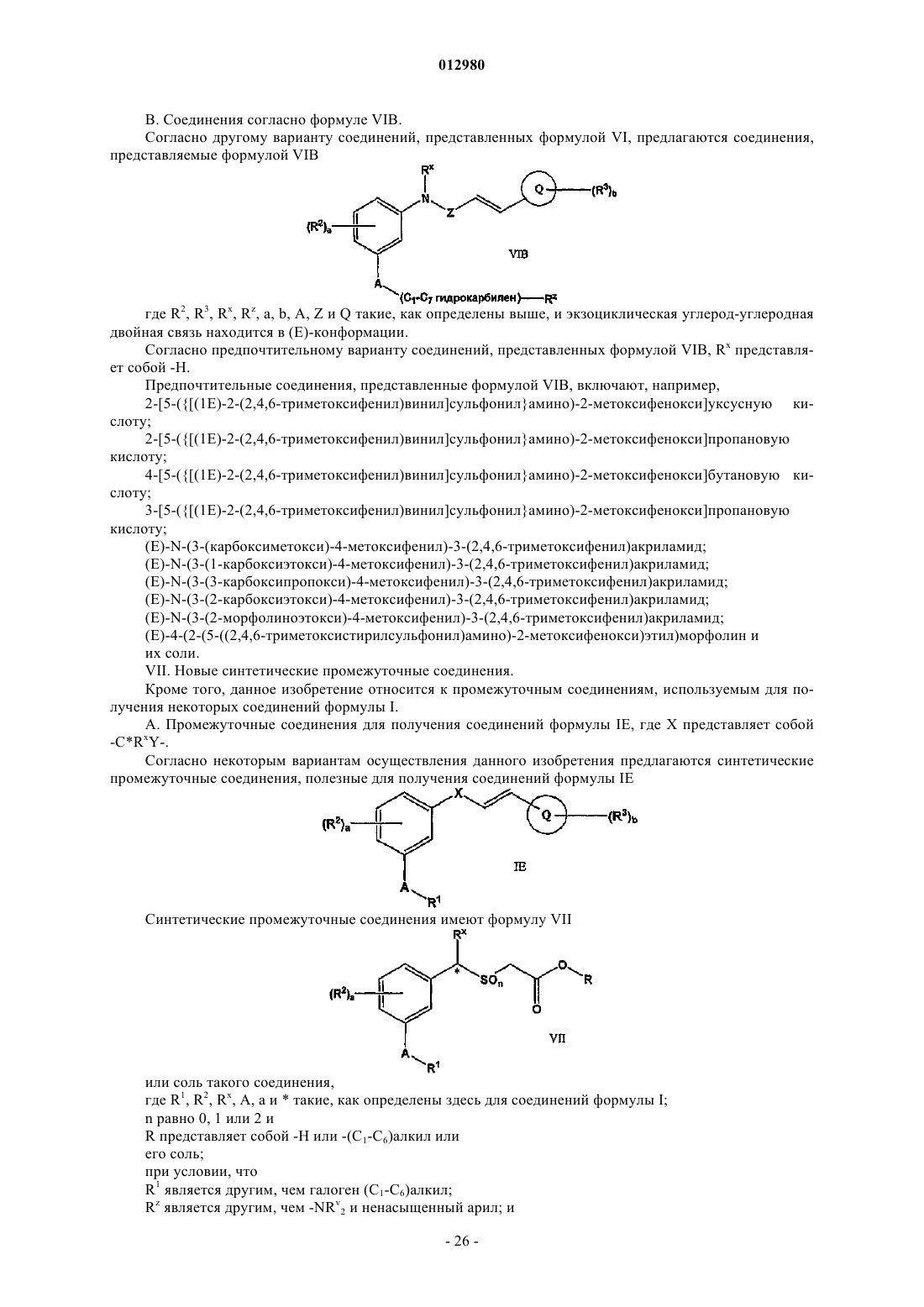
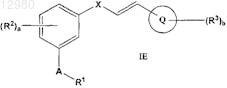
3. Соединение по п.1 формулы IE
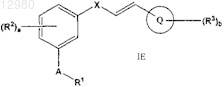
где экзоциклическая углерод-углеродная двойная связь находится в (Е)-конфигурации и
R1, R2, R3, А, а, b, X и Q определены в п.1,
или его соль.
4. Соединение по п.1 формулы IZ
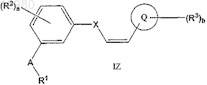
где экзоциклическая углерод-углеродная двойная связь находится в (Z)-конфигурации и
R1, R2, R3, А, а, b, X и Q определены в п.1,
или его соль.
5. Соединение по п.1, где сумма а и b равна по крайней мере 2.
6. Соединение по п.1, где R1 представляет собой Н.
7. Соединение по п.1 формулы IA
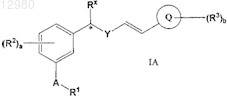
где R2, R3, A, a, b и Q определены в п.1;
R1 выбран из группы, состоящей из -Н, -Р(=O)(ORv)2, -C(=O)Rw, SO2Rw и -((C1-C6)гидрокарбилен)Rz;
Y представляет собой -SO2-;
* указывает, что, когда Rx является другим, чем -Н, конфигурация заместителей на обозначенном атоме углерода представляет (R)-, (S)- или любую смесь (R)- и (S)-; и
Rx выбран из группы, состоящей из -Н, -(C1-C6)алкила и -С(=O)(C1-C6)алкила,
или его соль.
8. Соединение по п.1 формулы IB
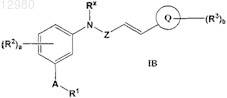
где R2, R3, A, a, b и Q определены в п.1;
R1 выбран из группы, состоящей из -Н, -Р(=O)(ORv)2, -C(=O)Rw, -((C1-C6)гидрокарбилен)Rzи -SO2Rw;
Z представляет собой -SO2- и
Rx выбран из группы, состоящей из -Н, -(C1-C6)алкила и -С(=O)(C1-C6)алкила,
или его соль.
9. Соединение по п.7 или 8, где Rx представляет собой -Н.
10. Соединение по любому из пп.7, 8 или 9, где R1представляет собой Н.
11. Соединение по любому из пп.7, 8 или 9, где R1представляет собой -Р(=О)(ORv)2.
12. Соединение по любому из пп.7, 8 или 9, где R1представляет собой -C(=O)Rw.
13. Соединение по любому из пп.7, 8 или 9, где R1представляет собой -SO2Rw.
14. Соединение по любому из пп.7, 8 или 9, где R1представляет собой -((C1-C6)гидрокарбилен)Rz.
15. Соединение по п.1, выбранное из группы, состоящей из
(Е)-5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенола;
(Е)-5-(2,4,6-триметоксистирилсульфонамидо)-2-метоксифенола;
(Е)-5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенилдигидрофосфата;
(Е)-5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенилдиэтилфосфата;
(Е)-5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенилдибензилфосфата;
(Е)-5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенил-2-(4-метилпиперазин-1-ил)ацетата;
(Е)-5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенилбензоата;
(Е)-5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенил-4-(4-метилпиперазин-1-ил)бензоата;
(Е)-5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенилметилсукцината;
(Е)-5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенил-2-(диметиламино)ацетата;
(Е)-5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенил-4-метилбензолсульфоната;
(Е)-4-(3-(5-((2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенокси)пропил)морфолина и
его соли.
16. Способ получения соединения по п.3 формулы IE
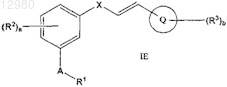
или его соли; включающий следующие стадии:
(а) взаимодействие соединения формулы VII
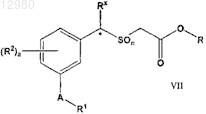
где n равно 2;
R представляет собой -Н;
А представляет собой -S- или -O-;
R1 выбран из группы, состоящей из -Н, -C(=O)Rw, -SO2Rw, -(C1-C6-гидрокарбилен)Rzи -Р(=O)(ORv)2;
каждый Rv независимо выбран из группы, состоящей из -Н и -(C1-C7)гидрокарбила;
Rw выбран из группы, состоящей из -(C1-C7)гидрокарбила, NRv2, -ORv, галоген(C1-C3-алкила), -NRvCRvRa-C(=O)-Rn, -CRvRa-N(Rv)-Rc, замещенного и незамещенного арила, замещенного и незамещенного арил(C1-C3)алкила, замещенного и незамещенного гетероарила, замещенного и незамещенного гетероарил(C1-C3)алкила, замещенного и незамещенного гетероциклила, замещенного и незамещенного гетероциклил(C1-C3)алкила, -((C1-C3)алкилен)-Р(=O)(ORv)2, -(C1-C3)перфторалкилен-N(СН3)2, -(C1-C3)алкилен-N+((C1-C3)алкил)3, -(C1-C3)алкилен-N+(СН2СН2ОН)3, -((C1-C4)алкилен)-С(=O)галогена, -(C1-C4)перфторалкилен-CO2Rv, -((C1-C3)алкилен)-С(=O)ORvи -((C1-C3)алкилен)-ОС(=O)-((C1-C3)алкилен)-С(=O)Rv;
Ry выбран из группы, состоящей из -ORv, -NRv2и -(C1-C6)алкила;
Rz выбран из группы, состоящей из -C(=O)Ry, -NRvCRvRa-C(=O)-Rn, -NRv2, -ORv, замещенного и незамещенного арила, замещенного и незамещенного гетероарила и -С(=O)(C1-C3)алкила;
каждый Ra независимо выбран из группы, состоящей из -Н, -(C1-C6)алкила, -(C1-C6)гетероалкила, -(СН2)3-NH-C(NH2)(=NH), CH2C(=O)NH2, -CH2COOH, -(CH2)2COOH, замещенного и незамещенного арила, замещенного и незамещенного арил(C1-C3)алкила, замещенного и незамещенного гетероциклила и замещенного и незамещенного гетероциклил(C1-C3)алкила;
каждый Rn независимо выбран из группы, состоящей из -ORv, -NRv2, и присоединенного по N-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая карбоксильная группа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -CO2Rv и
-C(=O)NRv2;
каждый Rc независимо выбран из группы, состоящей из -Н и присоединенного по С-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая аминогруппа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -NH2, -NHC(=O)(C1-C6)алкила,
-NH(C1-C6)алкила, -NH(C1-C6-алкил)2и -NHC(=O)О(C1-C7)гидрокарбила;
каждый R2 независимо выбран из группы, состоящей из галогена, -(C1-C7)гидрокарбила, -C(=O)Rv, -NRv2,
-NHC(=O)Rv, -NHSO2Rv, -NHRa, -NHCRvRaC(=O)Rn, -NHSO2Rv, -C(=O)ORv, -C(=O)NHRv, -NO2, -CN, -ORv,
-P(=O)(ORv)2, -C(=NH)NH2, диметиламино(C2-C6)алкокси, -NHC(=NRv)NHRv, -(C1-C6)галогеналкила и -(C1-C6)галогеналкокси;
две группы Rv на Р(=O)(ORv)2 и -NRv2 могут необязательно образовать 5- или 6-членное гетероциклическое кольцо, которое дополнительно необязательно может быть конденсировано с арильным или карбоциклическим кольцом;
а равно 0, 1, 2 или 3;
Rx выбран из группы, состоящей из -Н, -(C1-C6)алкила и -С(=O)(C1-C6)алкила; и
* указывает, что, когда Rx является другим, чем -Н, конфигурация заместителей при обозначенном углеродном атоме представляет (R)-, (S)- или любую смесь (R)- и (S)-,
или его соли;
при условии, что
Rz является другим, чем -NRv2 и незамещенный арил; и
Rw является другим, чем -(C1-C7)гидрокарбил;
с соединением формулы XVI
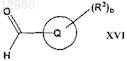
где Q представляет собой арил или гетероарил;
каждый R3 независимо выбран из группы, состоящей из галогена, -(C1-C7)гидрокарбила, -C(=O)Rv, -NRv2,
-NHC(=O)Rv, -NHSO2Rv, -NHRa, -NHCRvRaC(=O)Rn, -NHSO2Rv, -C(=O)ORv, -C(=O)NHRv, -NO2, -CN, -ORv,
-P(=O)(ORv)2, -C(=NH)NH2, диметиламино(C2-C6)алкокси, -NHC(=NRv)NHRv, -(C1-C6)галогеналкила и -(C1-C6)галогеналкокси; и
b равно 0, 1, 2 или 3; и
(b) выделение соединения формулы IE или его соли, где X представляет собой -C*H(Rx)Y- и Y представляет собой -SO2-, из реакционных продуктов.
17. Способ получения соединения по п.4 формулы IZ
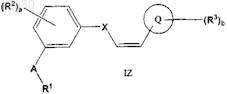
или его соли;
где А представляет собой -O-;
включающий следующие стадии:
(а) взаимодействие соединения формулы XI
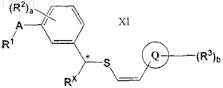
где А представляет собой -O-;
R1 выбран из группы, состоящей из -Н, -C(=O)Rw, -SO2Rw, -(C1-C6-гидрокарбилен)Rzи -Р(=O)(ORv)2;
каждый Rv независимо выбран из группы, состоящей из -Н и -(C1-C7)гидрокарбила;
Rw выбран из группы, состоящей из -(C1-C7)гидрокарбила, NRv2, -ORv, галоген(C1-C3-алкила), -NRvCRvRa-C(=O)-Rn, -CRvRa-N(Rv)-Rc, замещенного и незамещенного арила, замещенного и незамещенного арил(C1-C3)алкила, замещенного и незамещенного гетероарила, замещенного и незамещенного гетероарил(C1-C3)алкила, замещенного и незамещенного гетероциклила, замещенного и незамещенного гетероциклил(C1-C3)алкила, -((C1-C3)алкилен)-Р(=O)(ORv)2, -(C1-C3)перфторалкилен-N(СН3)2, -(C1-C3)алкилен-N+((C1-C3)алкил)3, -(C1-C3)алкилен-N+(СН2СН2ОН)3, -((C1-C4)алкилен)-С(=O)-галогена, -(C1-C4)перфторалкилен-CO2Rv, -((C1-C3)алкилен)-С(=O)ORvи -((C1-C3)алкилен)-ОС(=O)-((C1-C3)алкилен)-С(=O)Ry;
Ry выбран из группы, состоящей из -ORv, -NRv2и -(C1-C6)алкила;
Rz выбран из группы, состоящей из -C(=O)Ry, -NRvCRvRa-C(=O)-Rn, -NRv2, -ORv, замещенного и незамещенного арила, замещенного и незамещенного гетероарила и -С(=O)(C1-C3)алкила;
каждый Ra независимо выбран из группы, состоящей из -Н, -(C1-C6)алкила, -(C1-C6)гетероалкила, -(СН2)3-NH-C(NH2)(=NH), CH2C(=O)NH2, -CH2COOH, -(CH2)2COOH, замещенного и незамещенного арила, замещенного и незамещенного арил(C1-C3)алкила, замещенного и незамещенного гетероциклила и замещенного и незамещенного гетероциклил(C1-C3)алкила;
каждый Rn независимо выбран из группы, состоящей из -ORv, -NRv2 и присоединенного по N-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая карбоксильная группа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -CO2Rv и
-C(=O)NRv2;
каждый Rc независимо выбран из группы, состоящей из -Н и присоединенного по С-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая аминогруппа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -NH2, -NHC(=O)(C1-C6)алкила;
-NH(C1-C6)алкила, -NH(C1-C6-алкил)2и -NHC(=O)О(C1-C7)гидрокарбила;
Q представляет собой арил или гетероарил;
каждый R2 и R3 независимо выбран из группы, состоящей из галогена, -(C1-C7)гидрокарбила, -C(=O)Rv, -NRv2,
-NHC(=O)Rv, -NHSO2Rv, -NHRa, -NHCRvRaC(=O)Rn, -NHSO2Rv, -C(=O)ORv, -C(=O)NHRv, -NO2, -CN, -ORv,
-P(=O)(ORv)2, -C(=NH)NH2, диметиламино(C2-C6)алкокси, -NHC(=NRv)NHRv, -(C1-C6)галогеналкила и -(C1-C6)галогеналкокси;
две группы Rv на Р(=O)(ORv)2 и -NRv2 могут необязательно образовать 5- или 6-членное гетероциклическое кольцо, которое дополнительно может необязательно быть конденсировано с арильным или карбоциклическим кольцом;
а равно 0, 1, 2 или 3;
b равно 0, 1, 2 или 3;
конфигурация экзоциклической углерод-углеродной двойной связи представляет Z-;
Rx выбран из группы, состоящей из -Н, -(C1-C6)алкила и -С(=O)(C1-C6)алкила; и
* указывает, что, когда Rx является другим, чем -Н, конфигурация заместителей при обозначенном углеродном атоме представляет (R)-, (S)- или любую смесь (R)- и (S)-,
или его соль;
с окислителем, способным окислить сульфид в сульфон; и
b) выделение соединения формулы IZ или его соли, где X представляет собой -C*H(Rx)Y- и Y представляет собой -SO2-, из реакционных продуктов.
18. Способ получения соединения по п.3 формулы IE
или его соли; включающий следующие стадии:
(а) взаимодействие соединения формулы XIV
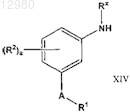
где А представляет собой -S- или -O-;
R1 выбран из группы, состоящей из -Н, -С(=O)Rw, -SO2Rw, -(C1-C6-гидрокарбилен)Rzи -Р(=O)(ORv)2;
каждый Rv независимо выбран из группы, состоящей из -Н и -(C1-C7)гидрокарбила;
Rw выбран из группы, состоящей из -(C1-C7)гидрокарбила, NRv2, -ORv, галоген(C1-C3-алкила), -NRvCRvRa-C(=O)-Rn, -CRvRa-N(Rv)-Rc, замещенного и незамещенного арила, замещенного и незамещенного арил(C1-C3)алкила, замещенного и незамещенного гетероарила, замещенного и незамещенного гетероарил(C1-C3)алкила, замещенного и незамещенного гетероциклила, замещенного и незамещенного гетероциклил(C1-C3)алкила, -((C1-C3)алкилен)-Р(=O)(ORv)2, -(C1-C3)перфторалкилен-N(СН3)2, -(C1-C3)алкилен-N+((C1-C3)алкил)3, -(C1-C3)алкилен-N+(СН2СН2ОН)3, -((C1-C4)алкилен)-С(=O)-галогена, -(C1-C4)перфторалкилен-CO2Rv, -((C1-C3)алкилен)-С(=O)ORvи -((C1-C3)алкилен)-ОС(=O)-((C1-C3)алкилен)-С(=O)Rv;
Ry выбран из группы, состоящей из -ORv, -NRv2и -(C1-C6)алкила;
Rz выбран из группы, состоящей из -C(=O)Ry, -NRvCRvRa-C(=O)-Rn, -NRv2, -ORv, замещенного и незамещенного арила, замещенного и незамещенного гетероарила и -С(=O)(C1-C3)алкила;
каждый Ra независимо выбран из группы, состоящей из -Н, -(C1-C6)алкила, -(C1-C6)гетероалкила, -(СН2)3-NH-C(NH2)(=NH), CH2C(=O)NH2, -СН2СООН, -(СН2)2СООН, замещенного и незамещенного арила, замещенного и незамещенного арил(C1-C3)алкила, замещенного и незамещенного гетероциклила и замещенного и незамещенного гетероциклил(C1-C3)алкила;
каждый Rn независимо выбран из группы, состоящей из -ORv, -NRv2 и присоединенного по N-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая карбоксильная группа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -CO2Rv и
-C(=O)NRv2;
каждый Rc независимо выбран из группы, состоящей из -Н и присоединенного по С-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая аминогруппа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -NH2, -NHC(=O)(C1-C6)алкила;
-NH(C1-C6)алкила, -NH(C1-C6-алкил)2и -NHC(=O)O(C1-C7)гидрокарбила;
каждый R2 независимо выбран из группы, состоящей из галогена, -(C1-C7)гидрокарбила, -C(=O)Rv, -NRv2,
-NHC(=O)Rv, -NHSO2Rv, -NHRa, -NHCRvRaC(=O)Rn, -NHSO2Rv, -C(=O)ORv, -C(=O)NHRv, -NO2, -CN, -ORv,
-P(=O)(ORv)2, -C(=NH)NH2, диметиламино(C2-C6)алкокси, -NHC(=NRv)NHRv, -(C1-C6)галогеналкила и -(C1-C6)галогеналкокси;
две группы Rv на Р(=O)(ORv)2 и -NRv2 могут необязательно образовать 5- или 6-членное гетероциклическое кольцо, которое, кроме того, может быть необязательно конденсировано с арильным или карбоциклическим кольцом;
а равно 0, 1, 2 или 3;
Rx выбран из группы, состоящей из -Н, -(C1-C6)алкила и -С(=O)(C1-C6)алкила;
или его соль;
с соединением формулы XV
![]()
где R представляет собой -(C1-C6)алкил;
L представляет собой галоген и
Z представляет собой -SO2-;
с получением соединения формулы XIII или его соли
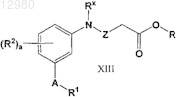
где R представляет собой -(C1-C6)алкил;
(b) гидролиз соединения формулы XIII, полученного на стадии (а), с получением соединения формулы XIII, где R представляет собой -Н;
(c) необязательно, если R1 представляет собой защитную группу, включающую -Si[(C1-C6)алкил]3 или
-CH2CH2Si[(C1-C6)алкил]3, удаление указанной защитной группы с получением соединения формулы XIIIA

где A, R2, Rx и Z определены выше;
(d) связывание либо соединения формулы XIII со стадии (а), либо соединения формулы XIIIA со стадии (с) с ароматическим альдегидом формулы XVI
![]()
где Q представляет собой арил или гетероарил;
каждый R3 независимо выбран из группы, состоящей из галогена, -(C1-C7)гидрокарбила, -C(=O)Rv, -NRv2,
-NHC(=O)Rv, -NHSO2Rv, -NHRa, -NHCRvRaC(=O)Rn, -NHSO2Rv, -C(=O)ORv, -C(=O)NHRv, -NO2, -CN, -ORv,
-P(=O)(ORv)2, -C(=NH)NH2, диметиламино(C2-C6)алкокси, -NHC(=NRv)NHRv, -(C1-C6)галогеналкила и -(C1-C6)галогеналкокси; и
b равно 0, 1, 2 или 3;
(е) выделение соединения формулы IE или его соли, где X представляет собой -NRx-Z-,
или его соли.
19. Способ получения соединения формулы I
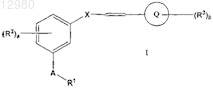
или его соли,
где R2, R3, X, A, Q, а и b определены в п.1;
R1 представляет собой -Р(=O)(ORv)2и
Rv представляет собой -(C1-C7)гидрокарбил, включающий cледующие стадии:
(а) взаимодействие соединения формулы II
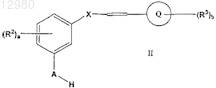
где А представляет собой -S- или -O-;
каждый Rv независимо выбран из группы, состоящей из -Н и -(C1-C7)гидрокарбила;
каждый Ra независимо выбран из группы, состоящей из -Н, -(C1-C6)алкила, -(C1-C6)гетероалкила, -(СН2)3-NH-C(NH2)(=NH), CH2C(=O)NH2, -СН2СООН, -(СН2)2СООН, замещенного и незамещенного арила, замещенного и незамещенного арил(C1-C3)алкила, замещенного и незамещенного гетероциклила и замещенного и незамещенного гетероциклил(C1-C3)алкила;
каждый Rn независимо выбран из группы, состоящей из -ORv, -NRv2 и присоединенного к N-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая карбоксильная группа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -CO2Rv и
-C(=O)NRv2;
Q представляет собой арил или гетероарил;
каждый R2 и R3 независимо выбран из группы, состоящей из галогена, -(C1-C7)гидрокарбила, -C(=O)Rv, -NRv2,
-NHC(=O)Rv, -NHSO2Rv, -NHRa, -NHCRvRaC(=O)Rn, -NHSO2Rv, -C(=O)ORv, -C(=O)NHRv, -NO2, -CN, -ORv,
-P(=O)(ORv)2, -C(=NH)NH2, диметиламино(C2-C6)алкокси, -NHC(=NRv)NHRv, -(C1-C6)галогеналкила и -(C1-C6)галогеналкокси;
две группы Rv на -NRv2 могут необязательно образовать 5- или 6-членное гетероциклическое кольцо, которое дополнительно необязательно может быть конденсировано с арильным или карбоциклическим кольцом;
а равно 0, 1, 2 или 3;
b равно 0, 1, 2 или 3;
конфигурация заместителей относительно экзоциклической углерод-углеродной двойной связи представляет либо Е-, либо Z-;
X представляет собой -C*H(Rx)Y- или -NRx-Z-;
Y представляет собой -SO2-;
Z представляет собой -SO2-;
Rx выбран из группы, состоящей из -Н, -(C1-C6)алкила и -C(=O)(C1-C6)алкила; и
* указывает, что, когда Rx является другим, чем -Н, конфигурация заместителей при обозначенном углеродном атоме представляет (R)-, (S)- или любую смесь (R)- и (S)-,
или его соль;
при условии, что:
(a) когда А представляет собой -О- и R1 представляет собой -Н, b больше чем 0 и R3 является другим, чем (C1-C6)алкил, -ОН и -NO2;
(b) когда X представляет собой -NRx-Z- и А представляет собой -O-, Rz является другим, чем -C(=O)Ry, -NRv2и незамещенный арил; и
(c) когда X представляет собой -C*H(Rx)Y- и А представляет собой -О-, Rz является другим, чем -NRv2и незамещенный арил;
где арил означает карбоциклическую ароматическую систему, содержащую один, два или три кольца;
гетероциклил означает моно- или полигетероциклическую кольцевую систему, содержащую углеродные атомы и по крайней мере один гетероатом, выбранный из группы, состоящей из N, О и S, и где гетероатомы азота и серы могут быть необязательно окислены;
гетероарил означает моноциклическую или полициклическую гетероциклическую кольцевую систему, содержащую по крайней мере одно ароматическое кольцо и необязательно одно или несколько частично насыщенных колец; и
где арил, гетероарил и гетероциклил, указанные в определениях R1, Rv, Rw, Rz и Ra, являются независимо необязательно замещенными и где заместители независимо выбирают из группы, состоящей из галогена, -(C1-C7)гидрокарбила, -C(=O)Rv, -NRv2, -NHC(=O)Rv, -NHSO2Rv, -NHRa, -NHCRvRaC(=O)Rn, -NHSO2Rv, -C(=O)ORv,
-C(=O)NHRv, -NO2, -CN, -ORv, -P(=O)(ORv)2, -C(=NH)NH2, -О(C2-C6)алкилен-NRv2, -(C2-C6)алкилен-NRv2, -SO2-NRv2, -NHC(=NRv)NHRv, -(C1-C6)галогеналкила и -(C1-C6)галогеналкокси;
с дигидрокарбилфосфитилгалогенидом формулы
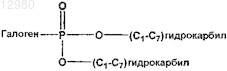
(b) выделение из реакционных продуктов соединения формулы I или его соли, где
R2, R3, X, A, Q, а и b определены в п.1;
R1 представляет собой -Р(=O)(ORv)2и
Rv представляет собой -(C1-C7)гидрокарбил.
20. Способ получения соединения формулы I
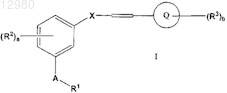
или его соли,
где R2, R3, X, A, Q, а и b определены в п.1;
R1 представляет собой -Р(=O)(ORv)2и
Rv представляет собой -Н;
включающий следующие стадии:
(а) взаимодействие соединения формулы I, где R1представляет собой -Р(=O)(ORv)2 и Rv представляет собой
-(C1-C7)гидрокарбил, с галогентриалкилсиланом формулы

(b) выделение из реакционных продуктов соединения формулы I или его соли, где R2, R3, X, A, Q, а и b определены в п.1; R1представляет собой -Р(=O)(ORv)2 и Rvпредставляет собой -Н.
21. Конъюгат формулы I-L-Ab, в которой
I представляет собой соединение по любому из пп.1-15;
Ab представляет собой антитело и
-L- представляет собой простую ковалентную связь или линкер, ковалентно связывающий указанное соединение с указанным антителом.
22. Фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и соединение по любому из пп.1-15 или его фармацевтически приемлемую соль, или конъюгат по п.21.
23. Применение соединения по любому из пп.1-15 в медицине.
24. Способ лечения индивидуума, страдающего пролиферативным нарушением, включающий введение указанному индивидууму эффективного количества соединения по любому из пп.1-15, или его фармацевтически приемлемой соли, или конъюгата по п.21.
25. Способ по п.24, где пролиферативное нарушение представляет собой рак.
26. Способ снижения или устранения воздействий ионизирующего излучения на здоровые клетки у индивидуума, который испытал или имеет риск быть подвергнутым воздействию ионизирующего излучения, включающий введение эффективного количества по крайней мере одного радиопротектора по любому из пп.1-15 или его фармацевтически приемлемой соли индивидууму до или после экспозиции ионизирующего излучения.
27. Применение конъюгата по п.21 в медицине.
28. Соединение по п.1, представляющее собой (Е)-5-(2,4,6-триметоксистирилсульфонамидо)-2-метоксифенолдигидрофосфат, или его соли.
Текст
012980 Перекрестная ссылка на родственную заявку Заявка на данное изобретение имеет притязание на эффект (положительный результат) находящейся в процессе одновременного рассмотрения предварительной заявки на патент США 60/554008, поданной 16 марта 2004 г., раскрытие которой входит в настоящее описание в полном объеме в виде ссылки. Область техники Данное изобретение относится к композициям и способам лечения пролиферативных нарушений,включая, но не ограничиваясь, рак. Кроме того, данное изобретение относится к композициям, которые позволяют обеспечить защиту от цитотоксических воздействий ионизирующего излучения и цитотоксических химиотерапевтических средств. Предшествующий уровень техники Соединения ,-ненасыщенных сульфонов. Некоторые ,-ненасыщенные сульфоны, в частности некоторые стирилбензилсульфоны, как было показано, обладают антипролиферативной, противолучевой и химиозащитной активностью. Химиозащитное действие, как было показано, защищает здоровые клетки от цитотоксических побочных действий ингибиторов митотической фазы клеточного цикла и ингибиторов топоизомеразы, используемых для лечения рака и других пролиферативных расстройств. См. патенты США 6599932, 6576675, 6548553,6541475, 6486210, 6414034, 6359013, 6201154, 6665973 и 6667346, раскрытия которых входят в настоящее описание в полном объеме. Соединения ,-ненасыщенные сульфонамидов. Некоторые ,-ненасыщенные сульфонамиды, в частности стирилбензилсульфонамиды, как было показано, обладают антипролиферативной, противолучевой и химиозащитной (защищая здоровые клетки от цитотоксических побочных действий ингибиторов митотической фазы клеточного цикла и ингибиторов топоизомеразы) активностью. См. патент США 6646009 и РСТ WO 03072063, раскрытия которых входят в настоящее описание в полном объеме. Соединения ароматических пропенамидов. Некоторые ароматические пропенамиды, в частности N-ароматические циннамиды, как было показано, обладают антипролиферативной, противолучевой и химиозащитной (защищая здоровые клетки от цитотоксических побочных действий ингибиторов митотической фазы клеточного цикла и ингибиторов топоизомеразы) активностью. См. РСТ WO 04037751, раскрытие которой входит в настоящее описание в полном объеме в виде ссылки. Лечение пролиферативных нарушений. Некоторые факторы роста, как было продемонстрировано, играют существенную роль в клеточной пролиферации и дифференцировке. Пролиферативные нарушения, в частности раки, возникают в результате прогрессирования событий. Такие события включают нарушение контролируемой экспрессии факторов роста или их компонентов, участвующих в каскаде путей передачи сигнала. События фосфорилирования тирозина, инициируемые рецептором, цитоплазматическими и ядерными киназами, и регулируемые фосфатазами, являются центральными для этих процессов. Мутация, гиперактивация, транслокация и сверхэкспрессия протеинтирозинкиназ, все, связаны с онкогенезом. Некоторые соединения, как было показано, являются ингибиторами тирозинкиназ. Благодаря их способности ингибировать фосфорилирование тирозина, эти соединения могут вносить изменения в клеточные ответы, включая нерегулируемую пролиферацию, на факторы роста или другие процессы, ассоциируемые с тирозинкиназной активностью. Ингибирование тирозинкиназ, связанных с путями передачи сигналов, ассоциируемыми с пролиферативными нарушениями, может быть достаточным для того, чтобы переключить злокачественную (раковую) клетку из пролиферативного клеточного цикла в другое состояние - запрограммированную гибель клетки, или апоптоз. Селективное ингибирование конкретных тирозинкиназ обеспечивает способ целенаправленной атаки роста злокачественных клеток с высокой степенью специфичности и минимальной токсичностью по отношению к здоровым клеткам. Поэтому специфические ингибиторы тирозинкиназ имеют большой потенциал для применения в клинических противораковых лечениях. Ингибирование тирозинкиназ предлагает один механизм, согласно которому может подавляться пролиферация клеток. Специалисту в данной области техники очевидно, что другие механизмы ингибирования также могут быть вовлечены. В данной области техники существует потребность в идентифицировании соединений, которые подавляют клеточную пролиферацию. Риск для здоровья от ионизирующего излучения. Ионизирующее излучение оказывает нежелательное действие на клетки и ткани, главным образом,через цитотоксические воздействия. У людей воздействие ионизирующего излучения имеет место в основном при вынужденном использовании специальных методов лечения (например, противораковая лучевая терапия) или вследствие облучения, связанного с профессиональной деятельностью или вызванного состоянием окружающей среды.-1 012980 Терапевтическое применение облучения. Основным источником воздействия ионизирующего излучения является применение терапевтического облучения для лечения рака или других пролиферативных нарушений. В зависимости от курса лечения, предписанного лечащим врачом, индивидуум может получать множественные дозы на протяжении курса лечения от нескольких недель до нескольких месяцев. Терапевтическое облучение обычно применяют к определенной области тела индивидуума, которая содержит анормальную пролиферативную ткань, чтобы максимизировать дозу, поглощаемую анормальной тканью, и свести к минимуму дозу, поглощаемую близлежащей здоровой тканью. Однако трудно(если не невозможно) реализовать (на практике) селективное воздействие терапевтического ионизирующего излучения на область патологической ткани. Поэтому здоровая ткань, расположенная в непосредственной близости к патологической ткани, на протяжении курса лечения также подвергается воздействию потенциально поражающих доз ионизирующего излучения. Кроме того, существуют некоторые программы лечения, которые требуют облучения всего организма индивидуума, так называемое "общее облучение всего организма", или "TBI." Эффективность радиотерапевтических методов в разрушении анормальных пролиферирующих клеток поэтому нейтрализуется побочными цитотоксическим действиями на близлежащие здоровые клетки. Из-за этого методы лучевой терапии имеют по своей природе низкий терапевтический показатель, что приводит к неадекватному лечению большинства опухолей. Даже самые лучшие радиотерапевтические методы могут приводить к неполной редукции роста опухоли, рецидиву опухоли, увеличению общей массы злокачественной опухолевой ткани и индукции резистентных к облучению опухолей. Были разработаны многочисленные методы для снижения поражения здоровой ткани, реализуя при этом все же доставку эффективных терапевтических доз ионизирующего излучения. Эти методы включают брахитерапию, фракционированное и гиперфракционированное дозирование, усложненные программы дозирования ионизирующего излучения с использованием модернизированных систем доставки доз облучения и терапию с использованием аппаратуры с высоким напряжением генерирования излучения. Однако такие методы представляли собой только попытку свести баланс между терапевтическим действием и нежелательными воздействиями ионизирующего излучения, и при их использовании полной эффективности достичь не удалось. Например, одно лечение индивидуумов с метастазирующими опухолями включает забор их кроветворных стволовых клеток и затем лечение индивидуума высокими дозами ионизирующего излучения. Это лечение предназначено для разрушения опухолевых клеток индивидуума, но имеет побочное действие, заключающееся в уничтожении также здоровых кроветворных клеток. Поэтому часть костного мозга индивидуума (содержащую кроветворные стволовые клетки) извлекают до проведения лучевой терапии. Сразу после проведения лечения индивидуума аутогенные кроветворные стволовые клетки возвращают в его организм. Однако, если опухолевые клетки метастазировали в другое место из основного места расположения опухоли, существует высокая вероятность, что некоторые опухолевые клетки могут заражать извлеченную популяцию кроветворных клеток. Извлеченная популяция кроветворных клеток может также содержать неопластические клетки, если индивидуум страдает злокачественными новообразованиями костного мозга, такими как различные подтипы French-American-British (FAB) острого миелоидного лейкоза (AML), хронический миелоидный лейкоз (CML) или острый лимфоцитарный лейкоз (ALL). Поэтому клетки метастазирующей опухоли или резидентные неопластические клетки должны быть удалены или убиты до того, как стволовые клетки будут заново введены индивидууму. Если какие-либо живые онкогенные или неопластические клетки заново ввести индивидууму, то они могут привести к рецидиву. Предшествующие методы удаления онкогенных или неопластических клеток из извлеченного костного мозга основаны на стратегии отделения или уничтожения всей популяции опухолевых клеток, которая, как правило, не убивает или не удаляет все заражающие злокачественные клетки. Такие методы включают лейкофорез мобилизованных периферических гемоцитов, отбор или устранение опухолевых клеток на основе иммуносродства или использование цитотоксических или фотосенсибилизирующих средств для селективного уничтожения опухолевых клеток. В наилучшем случае общая масса злокачественных клеток может еще составлять от 1 до 10 опухолевых клеток на каждые 100000 клеток, присутствующих в начальном заборе (Lazarus et al. J. of Hematotherapy, 2 (4):457-66, 1993). Таким образом, существует потребность в способе очистки, предназначенном для селективного разрушения злокачественных клеток, присутствующих в костном мозге, при сохранении здоровых кроветворных стволовых клеток, необходимых для кроветворного восстановления у трансплантационного субъекта. Профессиональное радиоактивное облучение/Радиоактивное облучение, вызванное факторами окружающей среды. Воздействие ионизирующего излучения может также произойти в профессиональной обстановке. Профессиональные дозы ионизирующего излучения могут быть получены людьми, чья работа включает воздействие (или потенциальное воздействие) облучения, например, в отраслях промышленности, связанных с атомной энергетикой и ядерным вооружением. Военный персонал, размещенный на судах, при-2 012980 водимых в действие ядерными реакторами, или солдаты, требуемые для работы в зонах, зараженных выпадением радиоактивных осадков, рискуют подвергнуться подобному воздействию ионизирующего излучения. Профессиональное облучение может также иметь место у персонала службы спасения и работающего в аварийных ситуациях, вызванного, чтобы иметь дело с катастрофическими событиями, связанными с работой ядерного реактора или вызванными выбросами радиоактивных веществ. Другими источниками профессионального облучения могут быть части машин, пластик и растворители - отходы производства радиоактивных лекарственных препаратов, дымовых пожарных сигнализаторов, аварийных знаков и других потребительских товаров. Профессиональное облучение может также иметь место у людей, которые работают на атомных суднах, в частности на тех, которые имеют ядерные реакторы, у военного персонала, работающего в областях, зараженных в результате применения ядерного вооружения, и у персонала, работающего в аварийных ситуациях, связанных с ядерными авариями. Воздействие ионизирующего излучения, вызванное состоянием окружающей среды, также может быть следствием детонаций ядерного оружия (либо экспериментальных, либо во время военного времени), выгрузки актинидов из хранилища ядерных отходов и обработки и переработки ядерного топлива и может исходить от радиоактивных материалов природного происхождения, таких как газ-родон или уран. Растет беспокойство по поводу использования артиллерийских орудий, содержащих обедненный уран, которое может привести к малоинтенсивному радиоактивному заражению зон боевых действий. Радиоактивное облучение от любого источника может быть классифицировано как острое (однократная большая лучевая нагрузка) или хроническое (ряд небольших малоинтенсивных лучевых нагрузок или непрерывные малоинтенсивные лучевые нагрузки, растянутые во времени). Лучевая болезнь обычно является результатом острого облучения достаточной дозы и отличается рядом характерных симптомов, которые появляются упорядоченным образом, включая выпадение волос, слабость, рвоту,понос, ожоги кожи, кровотечение из различных участков желудочно-кишечного тракта и кровоточимость слизистых оболочек. Генетические нарушения, бесплодие и раки (в частности, рак костного мозга) зачастую развиваются на протяжении некоторого времени. Хроническое облучение обычно ассоциируется с отсроченными лечебными проблемами, такими как рак и преждевременное старение. Острое общее облучение всего организма дозой 125000 мбэр может вызвать лучевую болезнь. Локализованные дозы, такие, которые используют при лучевой терапии, не могут вызвать лучевую болезнь, однако могут привести к поражению или гибели подвергнутых воздействию здоровых клеток. Например, острая доза общего облучения всего организма 100000-125000 мбэр (эквивалентная 1 Gy), полученная меньше чем за одну неделю, приводит к заметным физиологическим воздействиям,таким как ожоги или высыпания кожи, кровоточивость слизистых оболочек и желудочно-кишечные кровотечения, тошнота, понос и/или чрезмерное утомление. Через некоторое время могут также проявляться отсроченные цитотоксические и генетические последствия, такие как разрушение кроветворных и иммунокомпетентных клеток, потеря волос (алопеция), отторжение некроотических масс слизистой желудочно-кишечного тракта и слизистой рта, облитерирующий эндофлебит печеночных вен и хроническая сосудистая гиперплазия церебральных сосудов, катаракты, пневмонит, кожные изменения и повышенная заболеваемость раком. Острые дозы меньше чем 10000 мбэр (эквивалентная 0,1 Gy) обычно не приводят к тотчас же проявляемым биологическим или физиологическим эффектам, хотя могут иметь место отсроченные цитоксические или генетические последствия. Достаточно большая острая доза ионизирующего излучения, например от 500000 до свыше 1 млн мбэр (эквивалентная 5-10 Gy), может убить индивидуума сразу. Дозы в сотни тысяч мбэр могут убить в течение от 7 до 21 дней при состоянии, называемом "острое лучевое отравление". Как сообщают,некоторые из пожарных в Чернобыле умирали от состояния острого лучевого отравления, получив острые дозы в диапазоне 200000-600000 мбэр (эквивалентных 2-6 Gy). Острые дозы ниже приблизительно 200000 мбэр не приводят к смерти, однако индивидуум, подвергнутый такому облучению, будет, вероятно, испытывать отсроченные цитотоксические или генетические последствия, которые обсуждались выше. Острые профессиональные облучения обычно имеют место у рабочих атомной электростанции,подвергнутых случайным выбросам радиации, или у персонала службы тушения пожара и службы спасения, который реагирует на катастрофические события, связанные с работой ядерных реакторов и других источников выброса радиоактивных веществ. Рекомендованные пределы (доз) для острых профессиональных облучений в чрезвычайных ситуациях были разработаны Брукхейвенскими национальными лабораториями и представлены в табл. 1. 100000 мбэр равняются 1 зиверту (Sv). Для проникающего излучения, такого как гаммаизлучение, 1 Sv равняется приблизительно 1 грэй (Gy). Таким образом, доза в Gy может быть оценена как 1 Gy на каждые 100000 мбэр. Хроническая доза представляет собой малоинтенсивную (т.е. 100-5000 мбэр) инкрементальную или непрерывную дозу облучения, получаемую на протяжении некоторого времени. Примеры хронических доз включают дозу при общем облучении тела 5000 мбэр за год, которая является дозой, обычно получаемой взрослым человеком, работающим на атомной электростанции. В противоположность этому, по рекомендациям Комиссия по ядерной энергии представители широкой публики не должны получать больше чем 100 мбэр в год. Хронические дозы могут вызывать отсроченные цитотоксические и генетические воздействия, например, проявляясь в виде повышенного риска возникновения позже, при жизни,индуцированного ионизирующим излучением рака. В табл. 2 представлены рекомендуемые пределы в случае хронического воздействия ионизирующего излучения. Таблица 2 В качестве сравнения в табл. 3 приводятся дозы облучения от обычных источников. Таблица 3 Хронические дозы больше чем 5000 мбэр в год (0,05 Gy в год) могут привести к длительным цито-4 012980 токсическим или генетическим воздействиям, подобным тем, которые описаны для людей, получивших острые дозы. Некоторые неблагоприятные цитоксические или генетические действия могут также возникнуть и при хронических дозах, которые существенно меньше чем 5000 мбэр в год. Для целей защиты от излучения предполагают, что любая доза выше нуля может увеличить риск возникновения индуцированного ионизирующим излучением рака (т.е. что не существует никакого порога). Эпидемиологические исследования обнаружили, что риск умереть от рака за предполагаемое время жизни повышается приблизительно на 0,04% на бэр. Несмотря на то что противорадиационные костюмы или другие защитные принадлежности могут быть эффективными для снижения лучевой нагрузки, такие принадлежности являются дорогостоящими,громоздкими и обычно не доступны людям. Кроме того, противолучевые приспособления могут не защитить расположенную рядом с опухолью здоровую ткань от воздействия паразитного излучения во время лучевой терапии. Поэтому то, что необходимо, так это изыскание практического пути защиты индивидуумов, которым предстоит подвергнуться или которые имеют риск быть подвергнутыми воздействию ионизирующего излучения. В контексте терапевтического облучения желательно усилить защиту здоровых клеток, заставляя при этом опухолевые клетки оставаться уязвимыми для губительных воздействий облучения. Кроме того, желательно обеспечить системную защиту от ожидаемого или непреднамеренного общего облучения всего организма, такого, которое может произойти в случае воздействий ионизирующего излучения, обусловленных профессиональной деятельностью или вызванных состоянием окружающей среды, или применения некоторых терапевтических методов. Фармацевтические радиопротекторы представляют экономически-эффективную, эффективную и легкодоступную альтернативу приспособлениям, предназначенным для защиты от радиационного облучения. Однако предшествующие попытки осуществления радиопротекции здоровых клеток с помощью фармацевтических композиций не были полностью успешными. Например, цитокины, направленные на мобилизацию периферических кровяных клеток-предшественников, оказывают миелозащитное действие при введении до облучения (Neta et al., Semin. Radiat. Oncol. 6:306-320, 1996), но не оказывают системной защиты. Другие химические радиопротекторы, вводимые как таковые или в комбинации с модификаторами биологического ответа, показали незначительные защитные действия на мышах, но применение этих соединений к крупным млекопитающих оказалось менее успешным, и возникло сомнение по поводу того, имеет ли химическая радиопротекция какую-либо значимость (Maisin, J.R., Bacq and AlexanderAward Lecture. "Chemical radioprotection: past, present, and future prospects", Int J. Radiat Biol. 73:443-50,1998). Фармацевтические радиосенсибилизаторы, которые, как известно, предпочтительно усиливают действие облучения в раковых тканях, безусловно, являются неподходящими для общей системной защиты здоровых клеток от воздействия ионизирующего излучения. То, что необходимо, так это разработка терапевтических средств для защиты индивидуумов, которым предстоит подвергнуться или которые имеют риск быть подвергнутыми, воздействию ионизирующего излучения. В контексте терапевтического облучения желательно усилить защиту здоровых клеток,заставляя при этом опухолевые клетки оставаться уязвимыми для губительных воздействий облучения. Кроме того, желательно обеспечить системную защиту от ожидаемого или непреднамеренного тотального облучения всего организма, такого, которое может произойти в случае воздействий ионизирующего излучения, обусловленных профессиональной деятельностью или вызванных состоянием окружающей среды, или применения некоторых терапевтических методов. Защита от токсических побочных действий экспериментальной химиотерапии. Экспериментальная химиотерапия была основой лечения, предоставляемой пациентам с диагнозом хирургически неоперабельных запущенных раков или раков, не поддающихся обычной химиотерапии и лучевой терапии. Даже для более эффективных классов лекарственных средств лечебные свойства все же ограничены из-за их относительно низкого терапевтического показателя, ограниченной дозы, замедленного действия при лечении и относительно большой доли лишь частичной редукции опухолевого роста. За этим состоянием обычно следует рецидив, увеличение общей массы злокачественной опухолевой ткани и возникновение резистентных к лекарственному средству опухолей. А. Ингибиторы митотической фазы клеточного цикла. Ингибиторы митотической фазы клеточного цикла составляют один класс химиотерапевтических соединений, используемых в раковой терапии. Обычное описание клеточного цикла охватывает весь период существования индивидуальной клетки в терминах ряда фаз - интерфазы и митотической (М) фазы - и подразделение интерфазы по временам, на периоды, когда происходит синтез ДНК, известный как S-фаза (для фазы синтеза), и гэпы (периоды), которые отделяют S-фазу от митоза. G1 представляет собой гэп после митоза, но до начала синтеза ДНК, и G2 представляет собой гэп после завершения синтеза ДНК перед митозом и делением клетки. Таким образом, интерфаза состоит из последовательных G1,S и G2 фаз и обычно занимает 90% или больше суммарного времени клеточного цикла. Фаза М состоит из ядерного деления (митоз) и цитоплазматического деления (цитокинез). Во время ранней части М-фазы реплицированные хромосомы конденсируются из их протяженного состояния в интерфазе. Оболочка ядра разрывается, и каждая хромосома приобретает подвижность, что приводит к разделению пар сестринских хроматид по мере того, как содержимое ядра делится. Затем образуются две новые ядерные-5 012980 оболочки, и цитоплазма делится, генерируя две дочерние клетки, каждая с одним ядром. Этот процесс цитокинеза завершает М-фазу и обозначает начало интерфазы следующего клеточного цикла. Дочерние клетки, являющиеся результатом завершения М-фазы, начинают интерфазу нового цикла. Ингибитор митотической фазы клеточного цикла представляет собой химический агент, механизм действия которого включает ингибирование прохождения клетки через любую часть М-фазы клеточного цикла. В. Ингибиторы топоизомеразы. Ингибитор топоизомеразы представляет собой химический агент, механизм действия которого включает противодействие функции топоизомеразы. Топоизомеразы составляют группу ферментов, которые катализируют превращение ДНК из одной топологической формы в другую путем внесения неустойчивых разрывов в одну или обе цепи ДНКдуплекса. Топологические изомеры представляют собой молекулы, которые отличаются только своим состоянием суперспирализации. Топоизомеразы служат для уменьшения торсионного напряжения во время репликации и транскрипции. Они изменяют структуру ДНК, но не последовательность цепи. Сообщалось о наличии у человека трех различных типов топоизомераз. Они представляют собой топоизомеразу I (91 кДа-мономер) и топоизомеразу II, которая, кроме того, подразделяется на подклассы в виде II (170 кДа-димер) и II (180 кДа-димер). Три различных типа кодируются генами на трех отдельных хромосомах. Более простые организмы имеют только топоизомеразу I; однако высшие организмы имеют все три типа топоизомераз. В то время как топоизомераза II присутствует у всех эукариот,II присутствует только у позвоночных и, по-видимому, более тесно связана с дифференцировкой клеток, чем пролиферацией. Топоизомераза II, по-видимому, является высокогомологичной по отношению к типу II. Топоизомеразы действуют, катализируя разрыв и реакции воссоединения в фосфодиэстерном остове молекул ДНК. Топоизомераза I обратимо расщепляет одну цепь в дуплексе ДНК, в то время как топоизомераза II расщепляет и воссоединяет обе цепи ДНК. Эти реакции, как полагают, протекают через образование переходных реакционных промежуточных соединений, известных как "расщепляемые комплексы", где ферменты (или субъединицы фермента) образуют ковалентные связи с участием тирозина и расщепленной фосфодиэстерной связи остова субстрата ДНК. В последние годы топоизомеразы стали важными химиотерапевтическими мишенями для лечения рака. Камптотецин и его производные, как предполагают, действуют специфически на уровне комплекса топоизомераза I-ДНК и стимулируют расщепление ДНК. Средства, такие как -лапахон, действуют, блокируя образование комплекса топоизомераза I-ДНК. Было разработано несколько новых соединений,которые могут целенаправленно атаковать либо топоизомеразу I, либо изоформы топоизомеразы II/II,либо все три типа топоизомераз. Ингибирование топоизомеразы II, как полагают, является более перспективным вследствие комплексности взаимодействий. Большинство ингибиторов топоизомеразы II блокируют стадию лигирования, ведя к образованию стабилизированных "расщепляемых комплексов" между ДНК и ферментом. Большинство ингибиторов фермента функционируют путем встраивания в активный сайт фермента или соседний аллостерический сайт, блокируя реакцию нормального субстрата. В ингибирование топоизомеразы II вовлечены две части молекулы ингибитора: ароматическая часть молекулы ингибитора внедряется между парами оснований ДНК и другая, более полярная часть взаимодействует с топоизомеразой. Так как ингибиторы топоизомеразы II (например, доксорубицин и этопозид) действуют как яды, а не как классические конкурирующие ингибиторы, их действие зависит от уровня фермента в клетках. Быстро пролиферирующие клетки, которые содержат относительно более высокие уровни топоизомеразы II, по-видимому, более чувствительны к этим средствам. С другой стороны, дифференцированные клетки имеют относительно низкие уровни топоизомеразы II и они гораздо более резистентные к действию этих ингибиторов. С. Цитозащитные средства. Отдельные цитозащитные средства, как было предположено, повышают терапевтический показатель противораковых лекарственных средств. В случае токсичности метотрексата такие средства включают аспарагиназу, лейковорум-фактор, тимидин и карбипептидазу. Ввиду экстенсивного использования антрациклинов были предложены специфические и неспецифические цитозащитные средства, которые имеют изменчивые степени эффективности; к ним относятся кортикостероиды, дезразоксан и стауроспорин. Последний представляет интерес в том смысле, что он включает блокаду рестрикции G1/S в здоровых клетках (Chen et al., Proc. AACR 39:4436A, 1998). Цисплатин широко используют, и он имеет небольшой терапевтический показатель, что стимулировало исследование и поиск цитопротекторов (цитозащитных средств). Среди цитопротекторов для цисплатина с клиническим потенциалом - месна, глутатион, трисульфат натрия и амифостин (Griggs, Leuk.Cancer 33 (10):1693-8, 1997). Ни один из вышеуказанных или других предполагаемых цитопротекторов,таких как оксоновая кислота для токсичности фторопиримидина или прозардин для токсичности паклитаксела в отношении клеток РС 12, по-видимому, не функционирует по механизму, который приводит-6 012980 здоровые реплицирующие клетки в состояние покоя. Необходима разработка новых эффективных цитопротекторов, которые были бы эффективными для защиты животных, включая людей, от цитотоксических действий химиотерапевтических средств. Определения. Общие. Термин "индивидуум" или "субъект" включает людей и животных, не принадлежащих к человеческому роду. Что касается раскрываемых способов защиты от воздействий облучения и воздействия цитотоксических химиотерапевтических средств, то эти термины относятся, если в контексте не определено иначе, к организму, которому предстоит подвергнуться, или организму с риском быть подверженным,или который уже испытал воздействие ионизирующего излучения или воздействие одного или нескольких цитотоксических химиотерапевтических средств. Выражение "эффективное количество" при использовании для описания лечения, имеющего отношение к пациенту, страдающему пролиферативным нарушением, относится к количеству соединения,представленного формулой I, конъюгата, представленного формулой I-L-Ab, которое ингибирует рост опухолевых клеток или альтернативно индуцирует апоптоз раковых клеток, предпочтительно опухолевых клеток, обеспечивая тем самым терапевтически полезное и селективное цитотоксическое действие на пролиферативные клетки при введении пациенту, страдающему раком или другим нарушением, при котором проявляется патологическая пролиферация клеток. Термин "эффективное количество" включает количество соединения по данному изобретению, которое может метаболизироваться в активный метаболит в количестве, которое ингибирует рост опухолевых клеток или индуцирует апоптоз раковых клеток. Используемый здесь термин "антитело" относится к молекуле иммуноглобулина в целом или к активной части молекулы иммуноглобулина в целом, т.е. молекуле, которая содержит антигенсвязывающий сайт, который иммуноспецифично связывается с антигеном мишени, представляющей интерес, например, анормально пролиферирующими клетками, в частности раковыми клетками. Антитело может быть любого типа, например IgG, IgE, IgM, IgD, IgA или IgY; любого класса, например IgG1, IgG2, IgG3,IgG4, IgA1 и IgA2, или подкласса иммуноглобулина. Антитело может быть производным любого вида,предпочтительно антитело представляет собой антитело человеческого или мышиного происхождения,более предпочтительно человека. Антитела могут включать поликлональные, моноклональные, биспецифические, человеческие, гуманизированные, химерные, одноцепочечные антитела, Fv, фрагменты антител, например Fab, F(ab'), F(ab)2, и фрагменты, продуцированные при помощи библиотеки экспрессируемых последовательностей Fab. Выражение "гуманизированное антитело" относится к антителу, которое имеет гипервариабельные участки (CDR), полученные из иммуноглобулина нечеловеческого вида, и остаток молекулы антитела,полученный из иммуноглобулина человека. Термин "химерное антитело" относится к моноклональному антителу, содержащему вариабельную область, т.е. область связывания от одного источника или вида, и по крайней мере часть константной области, полученную из другого источника или вида. Выражение "гуманизированное химерное антитело" подразумевает химерное антитело, в котором,по крайней мере, константная область является областью, полученной от человека. Выражение "моноспецифическое поликлональное антитело" означает препарат антитела, содержащий множественную разновидность антител, имеющую специфичность по отношению к единственному антигену. Термин "пролиферативное нарушение" означает нарушение, при котором клетки продуцируются организмом с атипично ускоренной скоростью. Радиопротекция (противолучевая защита). Используемый здесь термин "ионизирующее излучение" представляет собой излучение достаточной энергии, которое при поглощении клетками и тканями индуцирует образование разновидности реакционноспособного кислорода и поражение ДНК. Этот тип излучения включает рентгеновские лучи, гамма-лучи, и бомбардировку частицами (например, пучок нейтронов, пучок электронов, протоны, мезоны и другие), и его используют для медицинского исследования и лечения, научных целей, промышленного испытания, производства и стерилизации, оружия и усовершенствования оружия и многих других применений. Радиацию обычно измеряют в единицах поглощаемой дозы, таких как радиан или грэй (Gy),где 1 рад=0,01 Gy, или в единицах дозовой эквивалентности, таких как бэр или зиверт (Sv), где 1 бэр=0,01 Sv.Sv представляет собой дозу в Gy, умноженную на фактор, который включает степень нанесенного тканепоражения. Например, проникающее ионизирующее излучение (например, гамма- и бетаизлучение) имеет фактор около 1, поэтому 1 Sv=1 Gy. Альфа-лучи имеют фактор 20, поэтому 1 Gy альфа-излучения=20 Sv.-7 012980 Под термином "эффективное количество ионизирующего излучения" подразумевают количество ионизирующего излучения, эффективное для уничтожения или уменьшения пролиферации, анормально пролиферирующих клеток у индивидуума. Термин "эффективное количество ионизирующего излучения", используемый в отношении очистки костного мозга, означает количество ионизирующего излучения, эффективное для уничтожения или уменьшения пролиферации, злокачественных клеток в образце костного мозга, извлеченного у индивидуума. Под термином "острое воздействие ионизирующего излучения" или "острая доза ионизирующего излучения" подразумевают дозу ионизирующего излучения, поглощенную индивидуумом в течение меньше чем 24 ч. Острая доза может быть локализована, как при методах лучевой терапии, или может быть поглощена всем телом индивидуума. Острые дозы обычно выше 10000 мбэр (0,1 Gy), но могут быть и ниже. Под термином "хроническое воздействие ионизирующего излучения" или "хроническая доза ионизирующего излучения" подразумевают дозу ионизирующего излучения, поглощенную индивидуумом на протяжении периода времени больше чем 24 ч. Указанная доза может быть прерывистой или непрерывной и может быть локализована или поглощена всем телом индивидуума. Хронические дозы обычно меньше чем 10000 мбэр (0,1 Gy), но могут быть и больше. Под термином "с риском быть подвергнутым воздействию ионизирующего излучения" подразумевают, что индивидуум может преднамеренно, например согласно планируемым сеансам лучевой терапии, или неумышленно подвергнут ионизирующему излучению в будущем. Непреднамеренное облучение включает случайное или незапланированное воздействие ионизирующего излучения, вызванное факторами окружающей среды или обусловленное профессиональной деятельностью. Под термином "эффективное количество радиопротектора (противолучевого соединения)" подразумевают количество соединения формулы I, эффективное для ослабления или устранения токсичности,связанной с облучением здоровых клеток индивидуума, и, кроме того, передачи прямого цитотоксического действия, направленного на анормально пролиферирующие клетки у индивидуума. Термин "эффективное количество радиопротектора соединения формулы I", используемый в отношении очистки костного мозга, означает количество соединения, эффективное для уменьшения или устранения токсичности, связанной с облучением костного мозга, извлеченного у индивидуума, и, кроме того, обеспечения прямого цитотоксического воздействия на злокачественные клетки, присутствующие в костном мозге,извлеченного из индивидуума. Цитозащита. Под термином "ингибитор митотической фазы клеточного цикла" подразумевают химический агент, механизм действия которого включает подавление прохождения клетки через любую часть митотической (М) фазы клеточного цикла. Под термином "эффективное количество ингибитора митотической фазы клеточного цикла или ингибитора топоизомеразы" подразумевают количество указанного ингибитора, эффективное для подавления или уменьшения пролиферации раковых клеток у животного-хозяина. Под термином "эффективное количество цитозащитного соединения формулы I" подразумевают количество соединения, эффективное для снижения токсичности ингибитора митотической фазы клеточного цикла или ингибитора топоизомеразы в отношении здоровых клеток животного. Выражение "клеточный цикл" относится к обычному описанию развития клеток в терминах цикла,состоящего из ряда фаз - интерфазы и митотической (М) фазы - и подразделения интерфазы, по временам, на периоды, когда происходит синтез ДНК, известный как S-фаза (для фазы синтеза), и гэпы (периоды), которые отделяют S-фазу от митоза. G1 представляет собой гэп после митоза, но до начала синтеза ДНК, и G2 представляет собой гэп после завершения синтеза ДНК перед митозом и делением клетки. Таким образом, интерфаза состоит из последовательных G1, S и G2 фаз и обычно занимает 90% или больше суммарного времени клеточного цикла. Фаза М состоит из ядерного деления (митоз) и цитоплазматического деления (цитокинез). Во время ранней части М-фазы реплицированные хромосомы конденсируются из их протяженного состояния интерфазы. Оболочка ядра разрывается, и каждая хромосома приобретает подвижность, что приводит к разделению пар сестринских хроматид по мере того, как содержимое ядра делится. Затем образуются две новые ядерные оболочки, и цитоплазма делится, генерируя две дочерние клетки, каждая с одним ядром. Этот процесс цитокинеза завершает М-фазу и обозначает начало интерфазы следующего клеточного цикла. Дочерние клетки, являющиеся результатом завершения М-фазы, начинают интерфазу нового цикла. Под термином "топоизомераза" подразумевают фермент, который катализирует превращение ДНК из одной топологической формы в другую путем внесения неустойчивых разрывов в одну или обе цепи ДНК-дуплекса. Под термином "ингибитор топоизомеразы" подразумевают химический агент, механизм действия которого включает противодействие функции топоизомеразы."Топологические изомеры" представляют собой молекулы, которые различаются только своим состоянием суперспирализации. Топоизомераза типа I разрезает одну цепь ДНК и релаксирует отрицательно суперспирализованную ДНК, но не действует на положительно суперспирализованную ДНК. Топои-8 012980 зомераза типа II разрезает обе цепи ДНК и увеличивает число отрицательных супервитков в ДНК. Химические. Термин "алкил", отдельно или как часть другого заместителя, например алкокси, галогеналкил или аминоалкил, означает, если не оговорено иначе, насыщенный углеводородный радикал, содержащий обозначенное число углеродных атомов (т.е. C1-C6 означает один, два, три, четыре, пять или шесть углеродов), и включает группы с прямой, разветвленной цепью; циклические и полициклические группы. Примеры включают метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, пентил, неопентил,гексил, циклогексил, норборнил и циклопропилметил. Предпочтительными алкильными группами являются -(C1-C6)алкил. Наиболее предпочтителен"Замещенный алкил" означает алкил, определенный выше, замещенный одним, двумя или тремя заместителями, предпочтительно независимо выбранными из группы, состоящей из галогена, -ОН,-О(C1-C4)алкила, -NH2, -N(CH3)2, -CO2H, -CO2(C1-C4)алкила, -CF3, -CONH2, -SO2NH2, -C(=NH)NH2, -CN и-NO2. Более предпочтительно замещенный алкил содержит один или два заместителя, независимо выбранные из галогена, -ОН, -NH2, -N(CH3)2, трифторметила и -СО 2 Н; наиболее предпочтительно независимо выбранные из галогена и -ОН. Примеры замещенных алкилов включают, но ими не ограничиваются, 2,2-дифторпропил, 2-карбоксициклопентил и 3-хлорпропил. Термин "алкилен", отдельно или как часть другого заместителя, означает, если не оговорено иначе,дивалентный прямой, разветвленный или циклический цепной углеводородный радикал, содержащий обозначенное число углеродов. Замещение другой группы на алкилене может быть при любом замещаемом углероде, т.е. выражение -С(=O)(C1-C4-алкилен)Rw должно включать, например, Термин "алкокси", используемый один или в комбинации с другими терминами, означает, если не оговорено иначе, алкильную группу, имеющую обозначенное число углеродных атомов, как определено выше, связанную с остатком молекулы через атом кислорода, такую как, например, метокси, этокси,1-пропокси, 2-пропокси (изопропокси) и более высшие гомологи и изомеры. Предпочтительными являются (C1-C3)алкокси, в частности этокси и метокси. Термин "амин" или "амино" относится к радикалам общей формулы -NRR', где R и R' независимо выбраны из водорода или гидрокарбильного радикала или где R и R', объединенные вместе, образуют гетероцикл. Примеры аминогрупп включают -NH2, метиламино, диэтиламино, анилино, бензиламино,пиперидинил, пиперазинил и индолинил. Термин "водное основание", используемый для реакции гидролиза, относится к основанию, содержащемуся в среде растворителя, которая может быть водой или может быть смесью воды и по крайней мере одного смешивающегося с водой органического растворителя, такого как, например, метанол, этанол или тетрагидрофуран. Термин "ароматический" относится к карбоциклу или гетероциклу, имеющему один или несколько полиненасыщенных циклов, имеющих ароматическую природу, характеризуемую наличием (4n+2) делокализованныхэлектронов. Термин "арил", используемый один или в комбинации с другими терминами, означает, если не оговорено иначе, карбоциклическую ароматическую систему, содержащую один или несколько циклов(обычно один, два или три), где такие циклы связаны вместе висячим образом, как, например, бифенил,или могут быть конденсированы, как, например, нафталин. Примеры включают фенил; антрацил и нафтил. Предпочтительны фенил и нафтил, наиболее предпочтительным является фенил. Термин "арил(C1-C3)алкил" означает радикал, где содержащая от одного до трех углеродов алкиленовая цепь связана с арильной группой, например -СН 2 СН 2=-фенил. Предпочтительны -(СН 2)арил и-(СН(СН 3 арил. Термин "замещенный арил(C1-C3)алкил" означает арил(C1-C3)алкильный радикал, в котором арильная группа замещена. Предпочтительным является замещенный -(СН 2)арил. Аналогично, термин "гетероарил(C1-C3)алкил" означает радикал, где содержащая от одного до трех углеродов алкиленовая цепь связана с гетероарильной группой, например -СН 2 СН 2-пиридил. Предпочтительным является замещенный -(СН 2)гетероарил. Термин "замещенный гетероарил(C1-C3)алкил" означает гетероарил(C1-C3)алкильный радикал, в котором гетероарильная группа замещена. Предпочтительным является замещенный -(СН 2)гетероарил. Термин "арилен", отдельно или как часть другого заместителя, означает, если не оговорено иначе,дивалентный арильный радикал. Предпочтительны дивалентные фенильные радикалы, в частности 1,4-дивалентные фенильные радикалы. Термин "циклоалкил" относится к циклсодержащим алкильным радикалам. Примеры включают циклогексил, циклопентил, циклопропилметил и норборнил.-9 012980 Выражение "экзоциклическая двойная связь", если не оговорено иначе, относится здесь к углеродуглеродной двойной связи, расположенной вне химической циклической структуры. В частности, выражение относится к углерод-углеродной двойной связи в соединениях по данному изобретению, которая не содержится ни в фенильном кольце, ни в ароматическом кольце Q, а скорее представляет собой двойную связь, которая находится в альфа-положении к ароматическому кольцу Q. Термины "гало" или "галоген", отдельно или как часть другого заместителя, например галогеналкил, означают, если не оговорено иначе, атом фтора, хлора, брома или йода, предпочтительно атом фтора, хлора или брома, более предпочтительно атом фтора или хлора. Термин "галогеналкил" означает, если не оговорено иначе, определенную здесь алкильную группу,содержащую по крайней мере один галогеновый заместитель и не содержащую никакого другого заместителя. Многочисленные галогензаместители, вплоть до замещения всех способных к замещению водородов на алкильной группе, могут быть одинаковыми или отличными друг от друга. Предпочтительные галогеналкильные группы включают, например, перфтор(C1-C4)алкил, гем-дифтор(C1-C4)алкил и хлор(C1-C4)алкил. Более предпочтительные галогеналкильные группы включают, например, -CF3, -C2F5,-CH2CF3, -CHF2, -CF2CH3 и -CH2Cl. Термин "гетероалкил", отдельно или в комбинации с другим термином, означает, если не оговорено иначе, стабильный радикал с прямой или разветвленной цепью, содержащий установленное число углеродных атомов и один или два гетероатома, выбранных из группы, состоящей из О, N и S, и в котором гетероатомы серы могут быть необязательно окислены и гетероатомы азота могут быть необязательно кватернизованы или окислены. В гетероалкильной группе помимо одного или двух гетероатомов могут присутствовать кислороды, связанные с окисленной серой или окисленным азотом. Гетероатом(ы) может(ут) быть расположен(ы) в любом положении гетероалкильной группы, включая положение между остатком гетероалкильной группы и фрагментом, к которому она присоединена, а также может быть связан с наиболее отдаленным по цепи углеродом в гетероалкильной группе. Примеры включают-CH2CH2-S(=O)-СН 3. Вплоть до двух гетероатомов могут находиться в цепи (алкила) последовательно,один за другим, например -CH2-NH-OCH3, или -CH2-CH2-S-S-CH3. Термин "гетероцикл" или "гетероциклил", отдельно или как часть другого заместителя, означает,если не оговорено иначе, незамещенную или замещенную, стабильную моно- или многоядерную гетероциклическую структуру, которая содержит углеродные атомы и по крайней мере один гетероатом, выбранный из группы, состоящей из N, О и S, и где гетероатомы азота и серы могут быть необязательно окислены и атом азота может быть необязательно кватернизован. Гетероциклическая структура может быть присоединена, если не указано иначе, при любом гетероатоме или атоме азота, который позволяет обеспечить стабильную структуру. Термин "гетероарил" или "гетероароматический" относится к гетероциклу, имеющему ароматический характер. Моноциклическая гетероарильная группа представляет собой 5-, 6- или 7-членный цикл,примерами которой являются пирролил, фурил, тиенил, пиридил, пиримидинил и пиразинил. Полициклический гетероарил может включать множественные ароматические кольца или может включать одно или несколько колец, которые являются частично насыщенными. Примеры полициклических гетероарильных групп, содержащих частично насыщенное кольцо, включают тетрагидрохинолил и 2,3-дигидробензофурил. Для соединений формулы I точка присоединения на кольце Q, как подразумевается, находится на атоме, который является частью ароматической моноциклической структуры или кольцевого компонента полициклической ароматической структуры, который как таковой является ароматическим кольцом. Точкой присоединения на кольце Q может быть углерод кольца или азот кольца и включает присоединение с образованием ароматических солей кватернизованного аммония, как, например, пиридиния. Примеры неароматических гетероциклов включают моноциклические группы, такие как азиридин,оксиран, тииран, азетидин, оксетан, тиетан, пирролидин, пирролин, имидазолин, пиразолидин,диоксолан, сульфолан, 2,3-дигидрофуран, 2,5-дигидрофуран, тетрагидрофуран, тиофан, пиперидин,1,2,3,6-тетрагидропиридин, 1,4-дигидропиридин, пиперазин, морфолин, тиоморфолин, пиран,2,3-дигидропиран, тетрагидропиран, 1,4-диоксан, 1,3-диоксан, гомопиперазин, гомопиперидин,1,3-диоксепан, 4,7-дигидро-1,3-диокспин и гексаметиленоксид. Примеры гетероарильных групп включают пиридил, пиразинил, пиримидинил, в частности 2- и 4-пиримидил, пиридазинил, тиенил, фурил, пирролил, в частности 2-пирролил, имидазолил,тиазолил, оксазолил, пиразолил, в частности 3- и 5-пиразолил, изотиазолил, 1,2,3-триазолил,1,2,4-триазолил, 1,3,4-триазолил, тетразолил, 1,2,3-тиадиазолил, 1,2,3-оксадиазолил, 1,3,4-тиадиазолил и 1,3,4-оксадиазолил. Примеры полициклических гетероциклов включают индолил, в частности 3-, 4-, 5-, 6- и 7-индолил,индолинил, хинолил, тетрагидрохинолил, изохинолил, в частности 1- и 5-изохинолил, 1,2,3,4 тетрагидроизохинолил, циннолинил, хиноксалинил, в частности 2- и 5-хиноксалинил, хиназолинил, фталазинил, 1,8-нафтиридинил, 1,4-бензодиоксанил, кумарин, дигидрокумарин, бензофурил, в частности 3-,4-, 1,5-нафтиридинил, 5-, 6- и 7-бензофурил, 2,3-дигидробензофурил, 1,2-бензизоксазолил, бензотиенил,- 10012980 в частности 3-, 4-, 5-, 6- и 7-бензотиенил, бензоксазолил, бензтиазолил, в частности 2-бензотиазолил и 5-бензотиазолил, пуринил, бензимидазолил, в частности 2-бензимидазолил, бензтриазолил, тиоксантинил, карбазолил, карболинил, акридинил, пирролизидинил и хинолизидинил. Термин "гетероарилен" отдельно или как часть другого заместителя, означает, если не оговорено иначе, дивалентный гетероарильный радикал. Предпочтителен 5- или 6-членный моноциклический гетероарилен. Более предпочтительными являются части гетероарилена, содержащие дивалентные гетероарильные кольца, выбранные из пиридина, пиперазина, пиримидина, пиразина, фурана, тиофена, пиррола,тиазола, имидазола и оксазола. Для соединений формулы I, когда ароматическая или гетероароматическая циклическая структура присоединена в положении и эта структура включает полициклическую структуру, которая является частично насыщенной, точка присоединения на ароматической или гетероароматической циклической структуре находится на кольцевом атоме ароматического кольцевого компонента полициклической структуры. Например, на частично насыщенной гетероароматической циклической структуре, 1,2,3,4 тетрагидроизохинолине точками присоединения являются кольцевые атомы в 5-, 6-, 7- и 8-положениях. Подразумевается, что вышеприведенный перечень гетероциклильных и гетероарильных остатков является репрезентативным и не предполагает ограничения. Термин "гидрокарбил" относится к любой части, содержащей только атомы водорода и углерода. Предпочтительными гидрокарбильными группами являются (C1-C12)гидрокарбильные группы, более предпочтительны (C1-C7)гидрокарбильные, наиболее предпочтительными являются бензил и(C1-C6)алкил. Термин "гидрокарбилен", отдельно или как часть другого заместителя, означает, если не оговорено иначе, дивалентную часть, содержащую только атомы водорода и углерода. Замещение другой группы на гидрокарбилене может иметь место при любом замещаемом углероде, т.е. выражение-(C1-C6)гидрокарбилен-Rw обычно включает, например, Выражение "присоединенный по С-концу пептидильный остаток" относится к пептидному радикалу в качестве заместителя на молекуле формулы I. Радикал связан через карбоксильную функциональность пептидильного остатка с образованием карбоксамида, сложного эфира карбоновой кислоты или ацилсульфида (-S-C(=O)-). Схема 1 иллюстрирует, каким образом типичный пептидильный остаток может быть присоединен по карбоксиконцу в качестве заместителя в соединении формулы I. Схема 1 Аминокислотные остатки, содержащие присоединенный по С-концу пептидильный остаток, могут включать природные и синтетические аминокислоты или их комбинации. Синтетические аминокислоты представляют собой аминокислоты другие, чем 20 незаменимых аминокислот. Одним примером синтетической аминокислоты является D-аминокислота, т.е. аминокислота, имеющая стереохимию, противоположную стереохимии природных L-аминокислот. Другим примером синтетической аминокислоты является аминокислота, имеющая боковую цепь, которая отличается от боковых цепей, встречающихся в природных аминокислотах, например -этилглицин или -фенилглицин. Третьим примером является аминокислота, имеющая вариацию остова. Примеры вариаций аминокислотного остова включают-аланин и -обращенные миметики, такие как лактам Фрайдингера. См. публикацию Freidinger et al.,Science, 1980, 210, 656, содержание которой входит в полном объеме в виде ссылки. Четвертый пример синтетической аминокислоты представляет собой аминокислоту, имеющую два -заместителя, например- 11012980 Аминоконец присоединенного по С-концу пептидильного остатка может быть незамещенной аминогруппой или может быть замещен. Замещения на аминоконце включают моно- и ди(C1-C6-алкил),-С(=О)(C1-C6-алкил), -С(=O)О(C1-C7)гидрокарбил и обычно используемые азотзащитные группы, такие как трет-N-бутоксикарбонил (BOC), карбобензилокси (CBZ), 2,4-диметоксибензил и флуоренилметоксикарбонил (FMOC). Выражение "присоединенный по аминоконцу пептидильный остаток" относится к пептидному радикалу в виде заместителя в соединении формулы I. Радикал связан через концевую аминофункциональность пептидильного остатка, образуя карбоксамид, сульфонамид, мочевину или тиомочевину. Схема 2 иллюстрирует, каким образом типичный пептидильный остаток может быть присоединен по аминоконцу в качестве заместителя в соединении, представленном формулой I. Схема 2 Карбоксиконец присоединенного по N-концу пептидильного остатка может быть свободной карбоксильной группой или ее солью или может быть превращен в производное в виде сложного эфира или амида. Подходящие сложные эфиры включают алкиловые, предпочтительно (C1-C6)алкиловые и арилалкиловые, предпочтительно бензиловые сложные эфиры. Подходящие амиды включают первичный амид и вторичный и третичный амиды, содержащие один или два заместителя на амидном азоте, независимо выбранные из (C1-C3)алкила, предпочтительно метила или этила; арила, предпочтительно фенила и арил(C1-C3)алкильных групп, предпочтительно бензила или замещенного бензила. Как и в случае присоединенных по С-концу пептидильных остатков, аминокислотные остатки,включающие присоединенный по N-концу пептидильный остаток, могут включать природные и синтетические аминокислоты или их комбинации. Термин "(Сх-Су) перфторалкил", где ху, означает алкильную группу минимум с х углеродными атомами и максимум с у углеродными атомами, где все атомы водорода замещены атомами фтора. Предпочтительным является -(C1-C6)перфторалкил, более предпочтителен -(C1-C3)перфторалкил, наиболее предпочтительным является -CF3. Термин "трифтор(Сх-Су)алкил" означает алкильную группу минимум с х углеродными атомами и максимум с у углеродными атомами, где три атома водорода на концевом углероде (-СН 3) замещены атомами фтора. Примеры включают -CH2CF3, -(CH2)2-CF3 и -СН(СН 3)-CF3. Термин "дифтор(Сх-Су)алкил" означает алкильную группу минимум с х углеродными атомами и максимум с у углеродными атомами, где один углеродный атом сдвоенно замещен двумя атомами фтора. Замещенный фтором углерод может быть любым углеродом в цепи, имеющим по крайней мере два замещаемых водорода, включая концевую группу -СН 3 и проксимальный углерод, посредством которого дифтор(Сх-Су)алкил связан с остатком молекулы. Примеры включают -CH2CF2H, -(CH2)2-CF2H и-CF2-CH3 и 3,3-дифторциклогексил. Термин "замещенный" означает, что атом или группа атомов имеет замещенный водород в виде заместителя, связанного с другой группой. Для арильных и гетероарильных групп термин "замещенный" относится к любой степени замещения, а именно моно-, ди-, три-, тетра- или пентазамещению, в тех случаях, когда такое замещение допустимо. Заместители выбраны независимо, и замещение может быть в любом химически допустимом положении. Выражение "изолированный оптический изомер" означает соединение, которое, по существу, было очищено от соответствующего оптического изомера(ов) той же самой формулы. Предпочтительно чистота изолированного изомера составляет по крайней мере около 80 мас.%, более предпочтительно по крайней мере 90 мас.%, еще более предпочтительно по крайней мере 98 мас.%, наиболее предпочтительно по крайней мере около 99 мас.%. Название соединений, раскрываемых в настоящем описании, представлено с использованием программ названия структур, включенных в пакеты программного обеспечения CHEMDRAW. Соединения, кроме ,-ненасыщенных сульфонамидов, названы с использованием программы "Structure to- 12012980 Краткое изложение существа изобретения Целью настоящего изобретения является разработка соединений, конъюгатов, фармацевтических композиций и терапевтических способов. Биологически активные соединения находятся в форме ароматических олефинов, структурно связанных через необязательно замещенный метиленсульфоновый линкер, необязательно замещенный метиленсульфоксидный линкер, необязательно N-замещенный сульфонамидный линкер или необязательно N-замещенный карбоксамидный линкер с фенольной или тиофенольной функциональностью или производным такой фенольной или тиофенольной функциональности. Целью настоящего изобретения является разработка соединений, конъюгатов, композиций и способов лечения и/или профилактики рака и других пролиферативных нарушений. Целью настоящего изобретения является разработка соединений и конъюгатов, которые являются селективными для уничтожения опухолевых клеток при терапевтически применимых концентрациях. Целью изобретения является разработка соединений, конъюгатов, композиций и способов индуцирования неопластических клеток селективно подвергаться апоптозу. Другой целью данного изобретения является разработка соединений, конъюгатов, композиций и способов, которые создают возможность профилактического лечения пролиферативных нарушений. Другой целью данного изобретения является разработка соединений, композиций и способов защиты здоровых клеток и тканей от цитотоксических и генетических последствий воздействия ионизирующего излучения у индивидуумов, которые испытали, могут в будущем подвергнуться или имеют риск быть подвергнутыми воздействию ионизирующего излучения. Воздействие ионизирующего излучения может происходить в режиме контролируемых доз во время лечения рака и других пролиферативных нарушений. Альтернативно, воздействие ионизирующего излучения может происходить в режиме неконтролируемых доз за пределами нормы, принятой для всего населения, во время облучений, связанных с профессиональной деятельностью с высоким риском или вызванных факторами окружающей среды. Целью настоящего изобретения является разработка соединений, композиций и способов защиты индивидуумов от цитотоксических побочных действий ингибиторов митотической фазы клеточного цикла и ингибиторов топоизомераз, используемых для лечения рака и других пролиферативных нарушений. Целью данного изобретения является разработка способа лечения рака или других пролиферативных нарушений, который снижает или устраняет цитотоксические воздействия на здоровые клетки. Целью данного изобретения является повышение воздействий ингибиторов митотической фазы клеточного цикла и ингибиторов топоизомераз, используемых для лечения рака или других пролиферативных нарушений. Целью данного изобретения является разработка терапевтической программы для лечения рака или другого пролиферативного нарушения, которая включает введение цитозащитного соединения до введения химиотерапевтического средства, и это цитозащитное соединение индуцирует обратимое состояние покоя в неопухолевых тканях. Целью данного изобретения является разработка способа безопасного увеличения дозы ингибиторов митотической фазы клеточного цикла и ингибиторов топоизомераз, используемых для лечения рака и других пролиферативных нарушений.I. Соединения формулы I. Согласно одному аспекту изобретение относится к новым соединениям, представленным формулой I-(C1-C6-гидрокарбилен)Rz, предпочтительно -(C1-C6)алкилен-Rz, более предпочтительно -(C1-C3)алкиленR2; -Р(=O)(ORv)2; каждый Rv независимо выбран из группы, состоящей из -Н и -(C1-C7)гидрокарбила, предпочтительно бензила и -(C1-C6)алкила, более предпочтительно бензила и -(C1-C3)алкила, наиболее предпочтительноRz выбран из группы, состоящей из -C(=O)Ry; -NRvCRvRa-C(=O)-Rn; -NRv2; -ORv; замещенного и незамещенного арила, предпочтительно замещенного и незамещенного фенила; замещенного и незамещенного гетероарила, предпочтительно замещенного и незамещенного моноциклического гетероарила; замещенного и незамещенного гетероциклил(C1-C3)алкила, предпочтительно незамещенного гетероциклил(C1-C3)алкила, более предпочтительно незамещенного 6-членного гетероциклил(C1-C3)алкила,наиболее предпочтительно пиперазин-1-ил-(C1-C3)алкила и морфолин-1-ил-(C1-C3)алкила и-С(=O)(C1-C3)алкила; каждый Ra независимо выбран из группы, состоящей из -Н; -(C1-C6)алкила; -(C1-C6)гетероалкила, в частности -CH2SH, -(CH2)2C(=O)-NH2, -СН 2-ОН, -СН(ОН)-СН 3, -(CH2)4-NH2, и -(CH2)2-S-СН 3;-(CH2)3-NH=C(NH2)(=NH); -СН 2 С(=O)NH2; -CH2COOH; -(СН 2)2 СООН; замещенного и незамещенного арила, предпочтительно замещенного и незамещенного фенила; замещенного и незамещенного арил(C1-C3)алкила, предпочтительно замещенного и незамещенного фенил(C1-C3)алкила, более предпочтительно замещенного и незамещенного бензила, в частности 4-гидроксибензила; замещенного и незамещенного гетероциклила, предпочтительно замещенного и незамещенного гетероарила, более предпочтительно замещенного и незамещенного моноциклического гетероарила и замещенного и незамещенного гетероциклил(C1-C3)алкила, предпочтительно замещенного и незамещенного гетероарил(C1-C3)алкила, в частности -СН 2-(3-индолила), более предпочтительно замещенного и незамещенного моноциклического гетероарил(C1-C3)алкила, наиболее предпочтительно замещенного и незамещенного моноциклического гетероарил-СН 2-, в частности -СН 2-индазолила; каждый Rn независимо выбран из группы, состоящей из -ORv, -NRv2 и присоединенного по N-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая карбоксильная группа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -CO2Rv и -C(=O)NRv2; каждый Rc независимо выбран из группы, состоящей из -Н и присоединенного по С-концу пептидильного остатка, содержащего от 1 до 3 аминокислот, в котором концевая аминогруппа пептидильного остатка присутствует в виде функциональной группы, выбранной из группы, состоящей из -NH2;Q представляет собой арил или гетероарил; каждый R2 и R3 независимо выбран из группы, состоящей из галогена; -(C1-C7)гидрокарбила, предпочтительно -(C1-C6)алкила, более предпочтительно -(C1-C3)алкила, наиболее предпочтительно -СН 3 и-OCHF2; две группы Rv на Р(=O)(ORv)2 и -NRv2 могут необязательно вместе образовать 5- или 6-членное гетероциклическое кольцо, предпочтительно 5-членное кольцо, которое необязательно может быть конденсировано с арильным или карбоциклическим кольцом, предпочтительно арильным кольцом, более предпочтительно фенильным кольцом; а равно 0, 1, 2 или 3;b равно 0, 1, 2 или 3; где сумма а и b равна предпочтительно по крайней мере 1; конформация заместителей относительно экзоциклической углерод-углеродной двойной связи представляет либо Е-, либо Z-;Rx выбран из группы, состоящей из -Н; -(C1-C6)алкила, предпочтительно -(C1-C3)алкила, более предпочтительно метила и этила и -С(=O)(C1-C6)алкила, предпочтительно -С(=O)(C1-C3)алкила, более предпочтительно ацетила и пропионила; иуказывает, что, когда Rx является другим, чем -Н, конформация заместителей при обозначенном- 14012980 углеродном атоме представляет (R)-, (S)- или любую смесь (R)- и (S)- или соль такого соединения, предпочтительно фармацевтически приемлемая соль такого соединения; при условии, что:Rw является другим, чем -(C1-C7)гидрокарбил. В соответствии с одним вариантом соединений по данному изобретениюRz выбран из группы, состоящей из -C(=O)Ry; -NRvCRvRa-C(=O)-Rn; -NRv2; -ORv; замещенного и незамещенного арила, предпочтительно замещенного и незамещенного фенила; замещенного и незамещенного гетероарила, предпочтительно замещенного и незамещенного моноциклического гетероарила и-С(=O)(C1-C3)алкила; и каждый Rv независимо выбран из группы, состоящей из -Н и -(C1-C7)гидрокарбила, предпочтительно -(C1-C6)алкила, более предпочтительно -(C1-C3)алкила, наиболее предпочтительно -СН 3 или -С 2 Н 5 иRw является другим, чем -(C1-C7)гидрокарбил. Согласно некоторым вариантам соединений формулы I Q представляет собой арил, предпочтительно фенил или нафтил, более предпочтительно фенил. Согласно другим вариантам соединений формулы I Q представляет собой гетероарил, предпочтительно моноциклический гетероарил. Согласно некоторым вариантам соединений формулы I предлагаются соединения формулы IE где экзоциклическая углерод-углеродная двойная связь находится в (Е)-конфигурации. Согласно другим вариантам соединений формулы I предлагаются соединения формулы IZ где экзоциклическая углерод-углеродная двойная связь находится в (Z)-конфигурации. Согласно некоторым вариантам соединений формулы I R представляет собой -Н. Согласно другим вариантам соединений формулы I R1 является другим, чем -Н. Предпочтительно, когда один или несколько из Q, R1, Rw, Ra или Rz представляют собой моноциклическую гетероарильную группу, указанная моноциклическая гетероарильная группа независимо вы- 15012980 брана из группы, состоящей из пиридила, пиразинила, пиримидинила, пиридазинила, тиенила, фурила,пирролила, имидазолила, тиазолила, оксазолила, пиразолила, изотиазолила, 1,2,3-триазолила,1,2,4-триазолила 1,3,4-триазолила,тетразолила,1,2,3-тиадиазолила,1,2,3-оксадиазолила,1,3,4-тиадиазолила и 1,3,4-оксадиазолила. Более предпочтительно, когда один или несколько из Q, R1, Ra, Rw или Rz представляют собой моноциклическую гетероарильную группу, указанная моноциклическая гетероарильная группа независимо выбрана из группы, состоящей из пиридила, тиенила, фурила, пирролила, имидазолила, тиазолила, оксазолила, пиразолила и изотиазолила. Наиболее предпочтительно, когда один или несколько из Q, R1, Ra, Rw или Rz представляют собой моноциклическую гетероарильную группу, указанная моноциклическая гетероарильная группа независимо выбрана из группы, состоящей из пиридила, тиенила и фурила. Предпочтительно, когда один или несколько из Q, R1, Ra, Rw или Rz представляют собой гетероарильную группу, другую, чем моноциклическая гетероарильная группа, в этих случаях гетероарильная группа выбрана из группы, состоящей из индолила, хинолила, изохинолила, циннолинила, хиноксалинила, хиназолила, фталазинила, 1,8-нафтиридинила, 1,4-бензодиоксанила, кумарина, бензофурила,1,2-бензизоксазолила, бензотиенила, бензоксазолила, бензтиазолила, пуринила, бензимидазолила,бензтриазолила, тиоксантинила, карбазолила, карболинила, акридинила, пирролизинила и хинолизидинила. Более предпочтительно, когда один или несколько из Q, R1, Ra, Rw или Rz представляют собой гетероарильную группу, другую, чем моноциклическая гетероарильная группа, в этих случаях гетероарильная группа выбрана из группы, состоящей из индолила, хинолила, изохинолила, бензофурила, бензотиенила, бензоксазолила, бензтиазолила и бензимидазолила. Наиболее предпочтительно, когда один или несколько из Q, R1, Ra, Rw или Rz представляют собой гетероарильную группу, другую, чем моноциклическая гетероарильная группа, и в этих случаях гетероарильная группа выбрана из группы, состоящей из индолила, хинолила, изохинолила, бензофурила и бензотиенила. Предпочтительно, когда замещенные арильные и гетероарильные кольца в группах R1, Ra, Rw и Rz являются моно-, ди- или тризамещенными, более предпочтительно моно- или дизамещенными заместителями, выбранными из группы, состоящей из галогена; (C1-C7)гидрокарбила, предпочтительно бензила и (C1-C6)алкила, более предпочтительно бензила и (C1-C3)алкила, наиболее предпочтительно бензила,метила и этила; -NRv2; -NO2; -CN; гетероциклила, предпочтительно N-метилпиперазинила, морфолинила и тиоморфолинила; -ORv и -О(C1-C7)гидрокарбила, предпочтительно -О(C1-C6)алкила и -О-бензила, более предпочтительно -О(C1-C3)алкила, наиболее предпочтительно бензила, метокси и этокси. Более предпочтительно, когда замещенные арильные и гетероарильные кольца в группах R1, Ra, Rwz и R являются моно-, ди- или тризамещенными, более предпочтительно моно- или дизамещенными заместителями, выбранными из группы, состоящей из хлора; фтора; брома; (C1-C6)алкила, предпочтительно (C1-C3)алкила, более предпочтительно метила и этила; -NH2; -NO2; -CN; гетероциклила, предпочтительно N-метилпиперазинила, морфолинила и тиоморфолинила; -ОН; и -О(C1-C6)алкила, предпочтительно -О(C1-C3)алкила, более предпочтительно метокси и этокси. Наиболее предпочтительно, когда замещенные арильные и гетероарильные кольца в группах R1, Ra,wR и Rz являются моно-, ди- или тризамещенными, более предпочтительно моно- или дизамещенными заместителями, выбранными из группы, состоящей из хлора, фтора, брома, метила, -NO2, -CN, -ОН и метокси. Предпочтительно замещенные гетероциклические группы, содержащиеся в группах Rz, Ra и Rw, являются моно-, ди- или тризамещенными, более предпочтительно моно- или дизамещенными заместителями, выбранными из группы, состоящей из -(C1-C7)гидрокарбила, предпочтительно бензила и-С(=O)(C1-C3)алкила, более предпочтительно ацетила и -(C1-C6)перфторалкила, предпочтительно-(C1-C3)перфторалкила, более предпочтительно -CF3. Более предпочтительно замещенные гетероциклические группы, содержащиеся в группах Rz, Ra и-(C1-C6)алкила, предпочтительно метила и этила и -С(=O)(C1-C3)алкила, предпочтительно ацетила. Согласно некоторым вариантам данного изобретения сумма а и b равна по крайней мере 2. Согласно другим вариантам данного изобретения сумма а и b равна по крайней мере 3. Согласно следующим вариантам данного изобретения сумма а и b равна по крайней мере 4. Согласно некоторым вариантам данного изобретения как а, так и b равны по крайней мере 1. Согласно другим вариантам данного изобретения а равно по крайней мере 1 и b равно по крайней мере 2. Согласно другим вариантам данного изобретения b равно по крайней мере 1 и а равно по крайней мере 2. Согласно следующим вариантам данного изобретения как а, так и b равны по крайней мере 2. Согласно предпочтительным вариантам соединений формулы I когда b равно 1, замещение групп R3 на Q имеет место в орто- или пара-положении; когда b равно 2, замещение групп R3 на Q имеет место либо в орто- и пара-положениях, либо в обо- 16012980 их орто-положениях и когда b равно 3, замещение групп R3 на Q имеет место в пара-положении и в обоих ортоположениях. Предпочтительно для соединений, представленных формулой I, Q представляет арил; b равно 1, 2 или 3 и каждый R2 представляет собой -ORv или галоген, где многочисленные группы -ORv или галогены могут быть одинаковыми или отличными друг от друга. Более предпочтительно для соединений, представленных формулой I, Q представляет собой фенил;b равно 2 или 3 и каждый R2 представляет собой -ORv, где многочисленные группы -ORv могут быть одинаковыми или отличными друг от друга. Наиболее предпочтительно, когда каждая R2 представляет собой -ОСН 3. Соединения по данному изобретению, кроме того, включают варианты формулы I, представленные ниже формулами II, III, IV, V и VI. Необходимо иметь в виду, что варианты и предпочтительные варианты, определенные выше для соединений согласно формуле I, являются также вариантами и предпочтительными вариантами соединений согласно формулам II-VI, как описано ниже.II. Соединения согласно формуле II. В соответствии с одним вариантом соединений, представленных формулой I, предлагаются соединения формулы II где R2, R3, А, а, b, X и Q такие, как определены выше для соединений формулы I; или их соли. А. Соединения согласно формуле IIA. В соответствии с одним вариантом соединений, представленных формулой II, предлагаются соединения, представленные формулой IIA где R2, R3, Rx, a, b, A, Y, Q итакие, как определены выше для соединений формулы I; и экзоциклическая углерод-углеродная двойная связь находится в (Е)-конформации. Согласно некоторым вариантам соединений, представленных формулой IIA, Rx представляет собой-Н. Предпочтительные соединения формулы IIA включают, например,(Е)-5-2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенол;(Е)-5-2,4,6-триметоксистирилсульфинил)метил)-2-метоксибензолтиол и их соли. В. Соединения согласно формуле IIB. Согласно другому варианту соединений, представленных формулой II, предлагаются соединения,представляемые формулой IIB где R2, R3, Rx, a, b, A, Z и Q такие, как определены выше для соединений, представленных формулой I, и экзоциклическая углерод-углеродная двойная связь находится в (Е)-конформации. Согласно предпочтительному варианту соединений, представленных формулой IIB, Rx представляет собой -Н.II. Соединения согласно формуле III. Согласно другому варианту соединений в соответствии с формулой I предлагаются соединения,представленные формулой III где R2, R3, Rv, A, a, b, X и Q такие, как определены выше для соединений формулы I; или их соли. А. Соединения согласно формуле IIIA. Согласно одному варианту соединений, представленных формулой III, предлагаются соединения,представляемые формулой IIIA где R2, R3, Rv, Rx, a, b, A, Y, Q итакие, как определены выше для соединений, представленных формулой I, и экзоциклическая углерод-углеродная двойная связь находится в (Е)-конформации. Согласно предпочтительному варианту соединений, представленных формулой IIIA, Rx представляет собой -Н. Предпочтительные соединения согласно формуле IIIA включают, например,(Е)-5-2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенилдигидрофосфат;- 18012980 В. Соединения согласно формуле IIIB. Согласно другому варианту соединений, представленных формулой III, предлагаются соединения,представляемые формулой IIIB где R2, R3, Rx, Rv, a, b, A, Z и Q такие, как определены выше для соединений, представленных формулой I, и экзоциклическая углерод-углеродная двойная связь находится в (Е)-конформации. Согласно предпочтительному варианту соединений, представленных формулой IIIB, Rx представляет собой -Н. Предпочтительные соединения согласно формуле IIIB включают, например,(Е)-5-2,4,6-триметоксистирилсульфонамидо)-2-метоксифенилдигидрофосфат;IV. Соединения согласно формуле IV. Согласно другому варианту соединений, представленных формулой I, предлагаются соединения,представляемые формулой IV где R2, R3, Rw, A, a, b, X и Q такие, как определены выше для соединений, представленных формулой I; или их соли. А. Соединения согласно формуле IVA.- 19012980 Согласно одному варианту соединений, представленных формулой IV, предлагаются соединения,представляемые формулой IVA где R2, R3, Rx, A, Rw, a, b, Y, Q итакие, как определены выше для соединений, представленных формулой I, и экзоциклическая углерод-углеродная двойная связь находится в (Е)-конформации. Согласно предпочтительному варианту соединений, представленных формулой IVA, Rx представляет собой -Н. Предпочтительные соединения согласно формуле IVA включают, например,(Е)-2-5-2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенокси)карбонил)уксусную кислоту;- 21012980 В. Соединения согласно формуле IVB. Согласно другому варианту соединений в соответствии с формулой IV, предлагаются соединения,представляемые формулой IVB где R2, R3, Rx, A, Rw, a, b, Z и Q такие, как определены выше для соединений, представленных формулой I, и экзоциклическая углерод-углеродная двойная связь находится в (Е)-конформации. Согласно предпочтительному варианту соединений, представленных формулой IVB, Rx представляет собой -Н. Предпочтительные соединения согласно формуле IVB включают, например,2-[5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил]оксикарбонилуксусную кислоту; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-3,5-динитробензоат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-3,5-диаминобензоат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-хлорацетат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-(4-метилпиперазинил)ацетат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенилбензоат; 5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-4-нитробензоат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-4-аминобензоат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-(2R)-2,6 диаминогексаноат; 5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-(2R)-2-амино-3 гидроксипропаноат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-(2S)-2-амино-3 гидроксипропаноат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенилкарбамат; 5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-(диметиламино)ацетат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-4-(4-метилпиперазинил)бензоат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-гидроксиацетат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-пирид-1-илацетат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-ацетилоксиацетат; 5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-гидроксипропаноат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-(триэтиламмоний)ацетат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-[трис-(2-гидроксиэтил)аммоний]ацетат; 5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-гидрокси-2-метилпропаноат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-ацетилокси-2 метилпропаноат; 5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2,2,2-трифторацетат; 3-[5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил]оксикарбонилпропановую кислоту; 5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-3-(хлоркарбонил)пропаноат; 3-[([5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил]оксикарбонилметил)оксикарбонил]пропановую кислоту; 4-[5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил]оксикарбонилбутановую кислоту; 5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенил-2-(фосфоноокси)ацетат; 5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенилметоксиформиат;V. Соединения согласно формуле V. Согласно другому варианту соединений, представленных формулой I, предлагаются соединения,представляемые формулой V где R2, R3, Rw, A, a, b, X и Q такие, как определены выше для соединений, представленных формулой I; и их соли. А. Соединения согласно формуле VA. Согласно одному варианту соединений, представленных формулой V, предлагаются соединения,представляемые формулой VA где R2, R3, Rx, Rw, A, a, b, Q итакие, как определены выше для соединений, представленных формулой I, и экзоциклическая углерод-углеродная двойная связь находится в (Е)-конформации. Согласно предпочтительному варианту соединений, представленных формулой VA, Rx представляет собой -Н. Предпочтительные соединения согласно формуле VA включают, например,(Е)-5-2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенилкарбоксиметансульфонат;(Е)-5-2,4,6-триметоксистирилсульфинил)метил)-2-метоксифенил-4-метилбензолсульфонат и их соли. В. Соединения согласно формуле VB. Согласно другому варианту соединений в соответствии с формулой V предлагаются соединения,представляемые формулой VB где R2, R3, Rw, Rx, a, b, A, Z и Q такие, как определены выше для соединений, представленных формулой I, и экзоциклическая углерод-углеродная двойная связь находится в (Е)-конформации. Согласно предпочтительному варианту соединений, представленных формулой VB, Rx представляет собой -Н.VI. Соединения согласно формуле VI. Согласно другому варианту соединений, представленных формулой I, предлагаются соединения,представляемые формулой VI где R2, R3, Rz, A, a, b, X и Q такие, как определены выше для соединений, представленных формулой I, или их соли. А. Соединения формулы VIA. Согласно одному варианту соединений, представленных формулой VI, предлагаются соединения,представляемые формулой VIA где R2, R3, Rx, Rz, a, b, A, Y, Q итакие, как определены выше для соединений, представленных формулой I, и экзоциклическая углерод-углеродная двойная связь находится в (Е)-конформации. Согласно предпочтительному варианту соединений, представленных формулой VIA, Rx представляет собой -Н. Предпочтительные соединения, представленные формулой VIA, включают, например,(Е)-2-(5-2,4,6-триметоксистирилсульфонил)метил)-2-метоксифенокси)уксусную кислоту;- 25012980 В. Соединения согласно формуле VIB. Согласно другому варианту соединений, представленных формулой VI, предлагаются соединения,представляемые формулой VIB где R2, R3, Rx, Rz, a, b, A, Z и Q такие, как определены выше, и экзоциклическая углерод-углеродная двойная связь находится в (Е)-конформации. Согласно предпочтительному варианту соединений, представленных формулой VIB, Rx представляет собой -Н. Предпочтительные соединения, представленные формулой VIB, включают, например,2-[5-([(1 Е)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенокси]уксусную кислоту; 2-[5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенокси]пропановую кислоту; 4-[5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенокси]бутановую кислоту; 3-[5-([(1E)-2-(2,4,6-триметоксифенил)винил]сульфониламино)-2-метоксифенокси]пропановую кислоту;VII. Новые синтетические промежуточные соединения. Кроме того, данное изобретение относится к промежуточным соединениям, используемым для получения некоторых соединений формулы I. А. Промежуточные соединения для получения соединений формулы IE, где X представляет собой-CRxY-. Согласно некоторым вариантам осуществления данного изобретения предлагаются синтетические промежуточные соединения, полезные для получения соединений формулы IE Синтетические промежуточные соединения имеют формулу VII или соль такого соединения,где R1, R2, Rx, А, a итакие, как определены здесь для соединений формулы I;Rw является другим, чем -(C1-C7)гидрокарбил. Согласно одному варианту соединений формулы VII А представляет собой -О-. Согласно другому варианту соединений формулы VII Rx представляет собой -Н. Соединения, представленные формулой VII, где n равно 1, включают, например,2-(3-гидрокси-4-метоксибензилсульфинил)уксусную кислоту; 2-(3-меркапто-4-метоксибензилсульфинил)уксусную кислоту; 2-(3-трет-бутилдиметилсилилокси-4-метоксибензилсульфинил)уксусную кислоту; 2-(3-трет-бутилдиметилсилил)сульфанил)-4-метоксибензилсульфинил)уксусную кислоту;S-2-метокси-5-(карбоксиметилсульфинилметил)фенил-O,O-дибензилфосфоротиоат и их соли. Соединения согласно формуле VII, где n равно 2, включают, например,2-(3-гидрокси-4-метоксибензилсульфонил)уксусную кислоту; 2-(3-меркапто-4-метоксибензилсульфонил)уксусную кислоту; 2-(3-трет-бутилдиметилсилилокси-4-метоксибензилсульфонил)уксусную кислоту; 2-(3-трет-бутилдиметилсилил)сульфанил)-4-метоксибензилсульфонил)уксусную кислоту;S-2-метокси-5-(карбоксиметилсульфонилметил)фенил-O,O-дибензилфосфоротиоат и их соли. Соединения формулы VII, где n равно 1 или 2 и R представляет собой -(C1-C6)алкил, включают, например, метиловые и этиловые сложные эфиры типичных соединений формулы VII, перечисленных выше. Соединения формулы VII, где R представляет собой -Н, могут быть получены, например, путем (1) взаимодействия соединения формулы VII, где R представляет собой -(C1-C6)алкил, в условиях, способных гидролизовать сложный эфир карбоновых кислот до соответствующей карбоновой кислоты, предпочтительно в водном основании, таком как, например, водный гидроксид лития, водный гидроксид натрия или водный гидроксид калия; и (2) выделения из реакционной смеси соединения, соответствующего формуле VII, где R представляет собой -Н. Соединения формулы VII, где n равно 1 и А представляет собой -O-, могут быть получены, например, путем (1) взаимодействия промежуточного соединения формулы VII, где n равно 0 и А представляет собой -O-, или его соли с окислителем, способным окислить сульфид в сульфоксид; и (2) отделения от продуктов реакции соединения, соответствующего формуле VII, где n равно 1. Соединения формулы VII, где n равно 2 и А представляет собой -O-, можно получить, например,путем (1) взаимодействия либо (а) промежуточного соединения формулы VII, где n равно 0 и А представляет собой -O-, с окислителем, способным окислить сульфид в сульфон; либо (b) промежуточного соединения VII, где n равно 1 и А представляет собой -O-, с окислителем, способным окислить сульфоксид в сульфон; и (2) выделения из продуктов реакции соединения формулы VII, где n равно 2. Соединения формулы VII, где n равно 0, включают, например,2-(3-гидрокси-4-метоксибензилсульфанил)уксусную кислоту; 2-(3-трет-бутилдиметилсилилокси-4-метоксибензилсульфанил)уксусную кислоту;O-2-метокси-5-(карбоксиметилсульфанилметил)фенилдибензилфосфат и их соли. Соединения формулы VII, где n равно 0 и R представляет собой -(C1-C6)алкил, включают, например, метиловые и этиловые сложные эфиры типичных соединений формулы VII, приведенных выше.(а) взаимодействия соединения формулы IX где R1, R2, Rx, А, а итакие, как определены для соединений формулы VII, при условии, что R1 является другим, чем -Н; иL представляет собой удаляемую группу, предпочтительно выбранную из группы, состоящей из галогена, тозила, нозила, трифила и мезила; с соединением формулы X где R представляет собой -(C1-C6)алкил, предпочтительно метил или этил;n равно 1 или 2 и М+ представляет собой противоион, предпочтительно выбранный из группы, состоящей из щелочных металлов, предпочтительно лития, натрия и калия; щелочно-земельных металлов, предпочтительно кальция и магния и переходных металлов, предпочтительно цинка, железа, никеля, меди, титана, марганца, кадмия и олова;(b) выделения из реакционных продуктов соединения формулы VII, где n равно 1 или 2 и R представляет собой -(C1-C6)алкил;(c) взаимодействия соединения формулы VII, выделенного со стадии (b), в условиях, способных гидролизовать сложный эфир карбоновых кислот в соответствующую карбоновую кислоту, предпочтительно в водном основании, таком как, например, водный гидроксид лития, водный гидроксид натрия или водный гидроксид калия; и(d) выделения соединения формулы VII, где n равно 1 или 2, из реакционной смеси. Соединения формулы VII, где n равно 0 и А представляет собой -S- или -O-, можно получить, например, путем(а) взаимодействия соединения формулы IX(b) выделения соединения формулы VII, где n равно 0, от реакционных продуктов;VII, выделенного со стадии (b), в условиях, способных гидролизовать сложный эфир карбоновой кислоты в соответствующую карбоновую кислоту, предпочтительно в водном основании, таком как, например,водный гидроксид лития, водный гидроксид натрия или водный гидроксид калия; иO,О-дибензил-S-5-(хлорметил)-2-метоксифенилфосфоротиоат; О,О-дибензил-S-5-(бромметил)-2-метоксифенилфосфоротиоат; О,О-диметил-S-5-(хлорметил)-2-метоксифенилфосфоротиоат; О,О-диметил-S-5-(бромметил)-2-метоксифенилфосфоротиоат; О,О-диэтил-S-5-(хлорметил)-2-метоксифенилфосфоротиоат; О,О-диэтил-S-5-(бромметил)-2-метоксифенилфосфоротиоат и их соли. Соединения согласно формуле VIII включают, например, 2-меркаптоуксусную кислоту, метил-2 меркаптоацетат и этил-2-меркаптоацетат. В. Промежуточные соединения для получения соединений формулы IZ, где X представляет собой-CRx-Y-. Кроме того, данное изобретение относится к синтетическим промежуточным соединениям, полезным для получения некоторых соединений формулы IZ. Синтетические промежуточные соединения имеют формулу XI где R1, R2, Rx, А, а итакие, как определены здесь для соединений формулы IX; и А представляет собой -О-. Согласно одному варианту соединений формулы XI Rx представляет собой -Н. Соединения формулы XI включают, например,(Z)-5-2,4,6-триметоксистирилтио)метил)-2-метоксифенол;(Z)-5-2,4,6-триметоксистирилтио)метил)-2-метоксифенилдибензилфосфат и их соли. Кроме того, данное изобретение относится к синтетическим промежуточным соединениям, применимым для получения некоторых соединений по данному изобретению. Синтетические промежуточные соединения имеют формулу XII где R1, R2, Rx, А, а итакие, как определены здесь для соединений формулы IX; и М+ представляет собой противоион, предпочтительно выбранный из группы, состоящей из щелочных металлов, более предпочтительно лития, натрия и калия; щелочно-земельных металлов, более предпочтительно кальция и магния и переходных металллов, более предпочтительно цинка, железа, никеля,меди, титана, марганца, кадмия и олова. Согласно одному варианту соединений формулы XII Rx представляет собой -Н. Соединения согласно формуле XII включают, например, соли щелочных и щелочно-земельных металловS-5-(меркаптометил)-2-метоксифенил-O,О-дигидрофосфоротиоата. С. Промежуточные соединения для получения соединений формулы IE, где X представляет собой-NRx-Z-. Кроме того, данное изобретение относится к синтетическим промежуточным соединениям, полезным для получения некоторых сульфонамидных и пропенамидных соединений формулы IE, в частности для получения ,-ненасыщенных сульфонамидных и пропенамидных соединений формул IIB, IIIB,IVB, VB и VIB. Синтетические промежуточные соединения имеют формулу XIII где R1, R2, Rx, A, Z и а такие, как определены здесь для соединений формулы I, и R представляет собой -Н или -(C1-C6)алкил; или их соли. Согласно одному варианту соединений формулы XIII, А представляет собой -О-. Согласно другому варианту соединений формулы XIII, Rx представляет собой -Н. Соединение формулы XIII, где R представляет собой -Н, или соль такого соединения можно получить путем(a) взаимодействия соответствующего соединения формулы XIII, где R представляет собой-(C1-C6)алкил, в условиях, способных гидролизовать сложный эфир карбоновой кислоты в соответствующую карбоновую кислоту, предпочтительно в водном основании, таком как, например, водный гидроксид лития, водный гидроксид натрия или водный гидроксид калия; и(b) выделения из реакционных продуктов соединения, соответствующего формуле XIII, где R представляет собой -Н. Согласно одному варианту соединений формулы XII предлагается соединение, представленное формулой XIIIA где R1, R2, Rx, А, а и R такие, как определены ранее для соединений формулы XIII; или соль такого соединения. Согласно другому варианту соединений формулы XII предлагается соединение, представленное формулой XIIIB где R1, R2, Rx, a, R и А такие, как определены ранее для соединений формулы XII; или соль такого соединения. Соединения согласно формуле XIIIA включают, например,N-(3-гидрокси-4-метоксифенил)карбоксиметилсульфонамид;
МПК / Метки
МПК: C07C 321/00, C07C 233/00
Метки: фенокси, фенилтиопроизводные, лечения, пролиферативных, нарушений, замещённые
Код ссылки
<a href="https://eas.patents.su/30-12980-zameshhyonnye-fenoksi-i-feniltioproizvodnye-dlya-lecheniya-proliferativnyh-narushenijj.html" rel="bookmark" title="База патентов Евразийского Союза">Замещённые фенокси- и фенилтиопроизводные для лечения пролиферативных нарушений</a>
Предыдущий патент: Способ повышения нефтеотдачи продуктивного пласта
Следующий патент: Фармацевтическая композиция в форме таблетки для нахождения в желудке, содержащая активное вещество
Случайный патент: Способ и устройство для буксирования морских сейсмических кос