Выделенная молекула нуклеиновой кислоты, содержащая аллель полиморфного участка гена свиньи, связанного с устойчивостью к энтеротоксикогенной e. coli, и способы ее применения
Номер патента: 11240
Опубликовано: 27.02.2009
Авторы: Сирера Сузанна, Йоргенсен Клаус Боттхер, Эдфорс-Лилйа Ингер, Арчибалд Алан, Андерсон Лиф, Фредхолм Мерет
Формула / Реферат
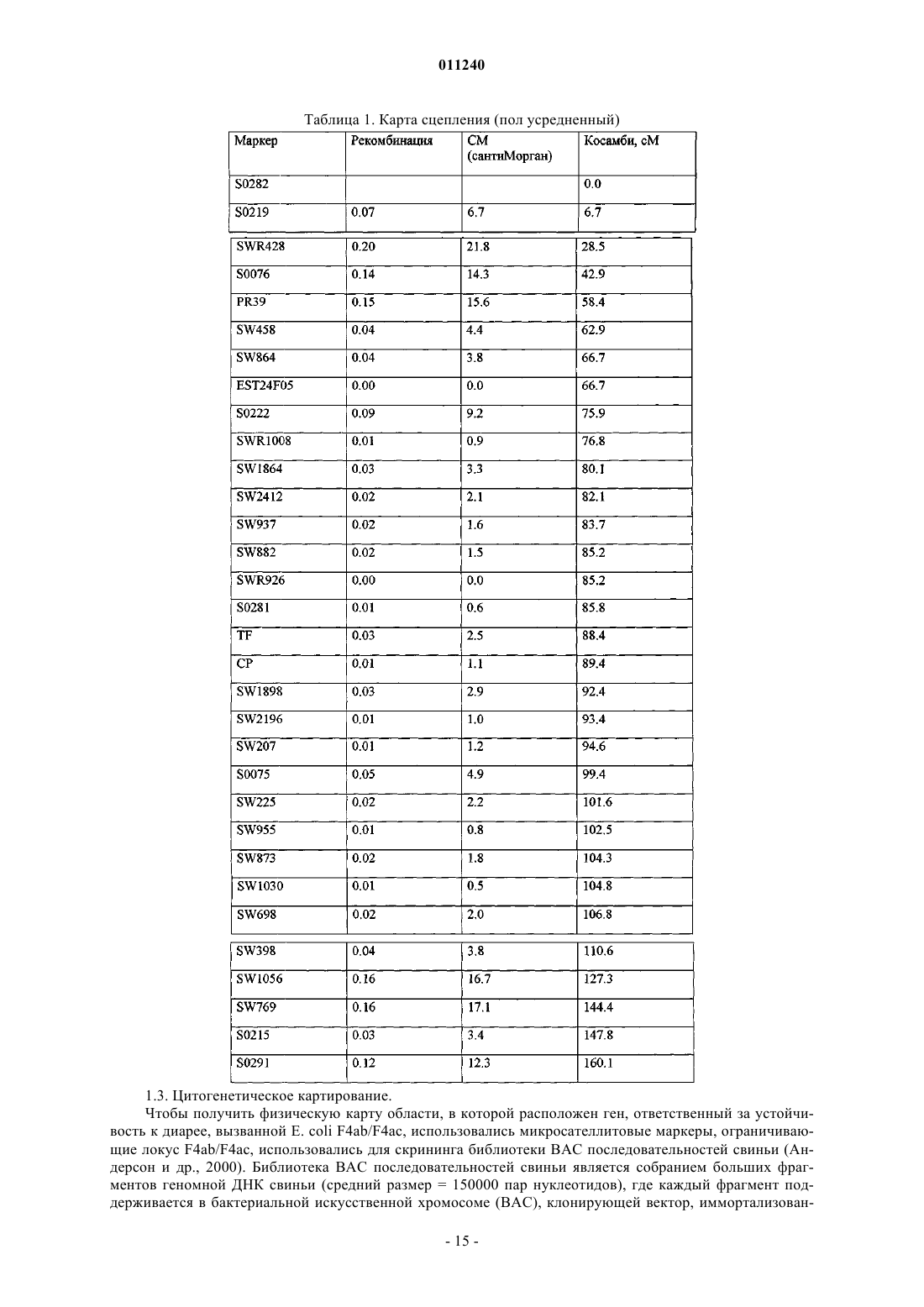
1. Выделенная молекула нуклеиновой кислоты (НК), содержащая аллель полиморфного участка гена свиньи, связанного с устойчивостью к энтеротоксигенной Е. coli (ETEC), где указанный полиморфный участок гена расположен в области между маркерами SW2196 и SW225 включительно, на хромосоме SSC 13 свиньи.
2. Выделенная молекула НК по п.1, в которой аллель полиморфного участка гена, связанного с устойчивостью к ЕТЕС, определяет свинью, гомозиготную по указанному аллелю, как устойчивую к ЕТЕС.
3. Выделенная молекула НК по п.1 или 2, содержащая аллель полиморфного участка гена, связанного с устойчивостью к ЕТЕС с LOD-баллом по крайней мере 3,0.
4. Выделенная молекула НК по п.1 или 3, содержащая указанную аллель полиморфного участка гена, которая расположена в MUC4 гене свиньи.
5. Выделенная молекула НК по п.1 или 4, содержащая указанную аллель полиморфного участка гена, которая является идентичной или имеет по крайней мере 90%-ную гомологию с последовательностью, выбранной из группы, включающей SEQ ID NO 1, SEQ ID NO 2, SEQ ID NO 3, SEQ ID NO 4, SEQ ID NO 5, SEQ ID NO 6, SEQ ID NO 7, SEQ ID NO 8, SEQ ID NO 9, SEQ ID NO 10, SEQ ID NO 11, SEQ ID NO 12, SEQ ID NO 13, SEQ ID NO 14, SEQ ID NO 15, SEQ ID NO 16, SEQ ID NO 17, SEQ ID NO 67, SEQ ID NO 68, SEQ ID NO 81, SEQ ID NO 82, SEQ ID NO 83, SEQ ID NO 84, SEQ ID NO 85, SEQ ID NO 86, SEQ ID NO 87, SEQ ID NO 88, SEQ ID NO 89, SEQ ID NO 90, SEQ ID NO 91, SEQ ID NO 92, SEQ ID NO 93, SEQ ID NO 94, SEQ ID NO 95, SEQ ID NO 96, SEQ ID NO 97, SEQ ID NO 98, SEQ ID NO 99, SEQ ID NO 100, SEQ ID NO 101, SEQ ID NO 102, SEQ ID NO 103, SEQ ID NO 104, SEQ ID NO 105, SEQ ID NO 106, SEQ ID NO 107, SEQ ID NO 108, SEQ ID NO 109, SEQ ID NO 110, SEQ ID NO 111, SEQ ID NO 112, SEQ ID NO 113, SEQ ID NO 114, SEQ ID NO 115, SEQ ID NO 116, SEQ ID NO 117, SEQ ID NO 118, SEQ ID NO 119, SEQ ID NO 120, SEQ ID NO 121, SEQ ID NO 122, SEQ ID NO 123, SEQ ID NO 124, SEQ ID NO 125, SEQ ID NO 126, SEQ ID NO 127, SEQ ID NO 128, SEQ ID NO 129, SEQ ID NO 130, SEQ ID NO 131, SEQ ID NO 132, SEQ ID NO 133, SEQ ID NO 134, SEQ ID NO 135, SEQ ID NO 136, SEQ ID NO 137, SEQ ID NO 138, SEQ ID NO 139, SEQ ID NO 140, SEQ ID NO 141, SEQ ID NO 142, SEQ ID NO 143, SEQ ID NO 144, SEQ ID NO 145, SEQ ID NO 146, SEQ ID NO 147, SEQ ID NO 148, SEQ ID NO 149, SEQ ID NO 150, SEQ ID NO 151, SEQ ID NO 152, SEQ ID NO 153, SEQ ID NO 154, SEQ ID NO 155, SEQ ID NO 156, SEQ ID NO 157, SEQ ID NO 158, SEQ ID NO 159, SEQ ID NO 160, SEQ ID NO 161, SEQ ID NO 162, SEQ ID NO 163, SEQ ID NO 164, SEQ ID NO 165, SEQ ID NO 166, SEQ ID NO 167, SEQ ID NO 168, SEQ ID NO 169, SEQ ID NO 170, SEQ ID NO 171, SEQ ID NO 172, SEQ ID NO 173, SEQ ID NO 174, SEQ ID NO 175, SEQ ID NO 176, SEQ ID NO 177, SEQ ID NO 178, SEQ ID NO 179, SEQ ID NO 180, SEQ ID NO 181, SEQ ID NO 182, SEQ ID NO 183, SEQ ID NO 184, SEQ ID NO 185, SEQ ID NO 186, SEQ ID NO 187, SEQ ID NO 188, SEQ ID NO 189, SEQ ID NO 190, SEQ ID NO 191, SEQ ID NO 192, SEQ ID NO 193, SEQ ID NO 194, SEQ ID NO 195, SEQ ID NO 196 и SEQ ID NO 197, комплементарные им последовательности и какие-либо их фрагменты.
6. Выделенная молекула нуклеиновой кислоты по любому из пп.1-5, содержащая указанную аллель полиморфного участка гена, которая отличает особей свиньи, устойчивых к ЕТЕС, от восприимчивых к ЕТЕС.
7. Образец НК, содержащий последовательность НК, которая является гомологичной фрагменту выделенной молекулы НК по любому из пп.1-6.
8. Образец НК по п.7, который является специфическим для аллеля по крайней мере одного однонуклеотидного полиморфного участка, выбранного из группы, включающей A1059G в SEQ ID NO 6, T1125G в SEQ ID NO 6, A1134G в SEQ ID NO 6, C1138G в SEQ ID NO 6, C1849G в SEQ ID NO 8, C2129T в SEQ ID NO 8, A4847G в SEQ ID NO 82, T4913G в SEQ ID NO 82, A4922G в SEQ ID NO 82, C4926G в SEQ ID NO 82, A1659T в SEQ ID NO 83, T1666G в SEQ ID NO 83, C1684A в SEQ ID NO 83, T1740A в SEQ ID NO 83, C1795T в SEQ ID NO 83, T1820G в SEQ ID NO 83, C1912T в SEQ ID NO 83, G2997A в SEQ ID NO 83, G3277C в SEQ ID NO 83 и комплементарные им последовательности.
9. Образец НК по п.7, содержащий последовательность НК, которая является гомологичной последовательности SEQ ID NO 66, или комплементарные ей последовательности.
10. Способ определения устойчивости свиньи к ЕТЕС, при котором:
i) от указанной свиньи получают образец, включающий генетический материал;
ii) определяют при помощи образца по любому из пп.7-9, является ли особь гомозиготной по аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС, который располагается в области между маркерами SW2196 и SW225, включительно, на хромосоме SSC13; и
iii) определяют особь как устойчивую к ЕТЕС, если она гомозиготна по аллелю полиморфного участка гена, связанному с устойчивостью.
11. Способ определения, является ли свинья восприимчивой к ЕТЕС и несущей или не несущей признак устойчивости, при котором:
i) от указанной свиньи получают образец, включающий генетический материал;
ii) определяют с помощью образца по любому из пп.7-9, является ли особь гетерозиготной или не несущей указанный аллель полиморфного участка гена, связанный с устойчивостью к ЕТЕС; и
iii) определяют особь как
a) восприимчивую к ЕТЕС и не несущую признак устойчивости, если особь не имеет указанного аллеля полиморфного участка гена, связанного с устойчивостью; или
b) восприимчивую к ЕТЕС, но несущую признак устойчивости, если особь гетерозиготна по указанному аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС.
12. Способ по любому из пп.10-11, согласно которому указанный полиморфный участок гена, связанный с устойчивостью к ЕТЕС, расположен в области между маркерами SW207 и S0075 включительно.
13. Способ по любому из пп.10-12, согласно которому указанный полиморфный участок гена связан с устойчивостью к ЕТЕС с LOD-баллом по крайней мере 3,0.
14. Способ по любому из пп.10-13, согласно которому указанный полиморфный участок гена расположен в MUC4 гене свиньи.
15. Способ по любому из пп.10-14, согласно которому устойчивость к ЕТЕС выбрана из группы, включающей устойчивость к адгезии ЕТЕС в кишечнике, устойчивость к колонизации ЕТЕС в кишечнике, устойчивость к кишечным нарушениям, таким как диарея, вызванная ЕТЕС, и какую-либо их комбинацию.
16. Способ по любому из пп.10-15, согласно которому свинья выбрана из группы, включающей вид Sus scrofa (Suidae), породы - йоркшир, датский йоркшир, датский дюрок, ландрас, датский ландрас, белый датский ландрас, черно-пестрый датский ландрас, гемпшир, датский гемпшир, польско-китайскую, герефорд и какие-либо гибриды этих пород.
17. Способ по любому из пп.10-16, согласно которому свинья выбрана из группы, включающей самца, самку, молочного поросенка, отнятого поросенка, свинью-производителя и свинью завершающего периода откорма.
18. Способ по любому из пп.10-17, согласно которому указанный полиморфный участок гена выбран из группы, включающей однонуклеотидный полиморфный участок (ОНП), различное число тандемных дупликаций полиморфных участков, рассеянный повтор ДНК, вставки, делеции, амплификации, перестановки, комбинацию однонуклеотидных полиморфных участков, короткие тандемные дупликации, динуклеотидные повторы, отделенные промежутками повторяющиеся ДНК и какие-либо их комбинации.
19. Способ по п.18, согласно которому полиморфным участком гена является однонуклеотидный полиморфный участок или комбинация однонуклеотидных полиморфных участков.
20. Способ по п.19, согласно которому однонуклеотидным полиморфным участком является G/C однонуклеотидный полиморфный участок.
21. Способ по п.19, согласно которому однонуклеотидный полиморфный участок выбирают из группы, включающей A1059G в SEQ ID NO 6, T1125G в SEQ ID NO 6, A1134G в SEQ ID NO 6, C1138G в SEQ ID NO 6, C1849G в SEQ ID NO 8, C2129T в SEQ ID NO 8, A4847G в SEQ ID NO 82, T4913G в SEQ ID NO 82, A4922G в SEQ ID NO 82, C4926G в SEQ ID NO 82, A1659T в SEQ ID NO 83, T1666G в SEQ ID NO 83, C1684A в SEQ ID NO 83, T1740A в SEQ ID NO 83, C1795T в SEQ ID NO 83, T1820G в SEQ ID NO 83, C1912T в SEQ ID NO 83, G2997A в SEQ ID NO 83 и G3277C в SEQ ID NO 83.
22. Способ по любому из пп.10-21, при котором
на этапе ii) согласно п.10 или 11 определяют, является ли свинья вдобавок к первому аллелю полиморфного участка гена, связанного с устойчивостью к ЕТЕС, гомозиготной или гетерозиготной по крайней мере по второму аллелю указанного полиморфного участка гена, связанного с устойчивостью к ЕТЕС, или не несущей данного аллеля;
на этапе iii) согласно п.10 или 11 определяют особь как устойчивую к ЕТЕС, если она гомозиготна по первому аллелю полиморфного участка гена, связанного с устойчивостью к ЕТЕС и по крайней мере по второму аллелю полиморфного участка гена, связанного с устойчивостью к ЕТЕС.
23. Способ по п.22, согласно которому по крайней мере второй аллель указанного полиморфного участка гена включает по крайней мере 3 полиморфных участка, например 4, 5, 6, 7, 10, 20 или 50.
24. Способ по п.22 или 23, согласно которому по крайней мере второй аллель указанного полиморфного участка гена выбран из группы, включающей однонуклеотидный полиморфный участок, различное число тандемных дупликаций полиморфных участков, рассеянный повтор ДНК, вставки, делеции, амплификации, перестановки, комбинацию однонуклеотидных полиморфных участков, короткие тандемные дупликации, динуклеотидные повторы, отделенные промежутками повторяющиеся ДНК и какие-либо их комбинации.
25. Способ по п.24, согласно которому по крайней мере второй аллель указанного полиморфного участка гена выбран из группы, включающей A1059G в SEQ ID NO 6, T1125G в SEQ ID NO 6, A1134G в SEQ ID NO 6, C1138G в SEQ ID NO 6, C1849G в SEQ ID NO 8, C2129T в SEQ ID NO 8, A4847G в SEQ ID NO 82, T4913G в SEQ ID NO 82, A4922G в SEQ ID NO 82, C4926G в SEQ ID NO 82, A1659T в SEQ ID NO 83, T1666G в SEQ ID NO 83, C1684A в SEQ ID NO 83, T1740A в SEQ ID NO 83, C1795T в SEQ ID NO 83, T1820G в SEQ ID NO 83, C1912T в SEQ ID NO 83, G2997A в SEQ ID NO 83 и G3277C в SEQ ID NO 83.
26. Способ по любому из пп.10-25, согласно которому тестируемый образец выбран из группы, представленной материалом, включающим ДНК и/или РНК, кровью, слюной, тканью, мазком из горла, спермой и их комбинациями.
27. Способ по любому из пп.10-26, согласно которому этап ii) пп.10, 11 или 22 выполняют с помощью методики, выбранной из группы, включающей аллель-специфическую ПЦР (полимеразно-цепная реакция), минисеквенирование, удлинение праймера, пиросеквенирование, ПЦР-ПДРФ (полимеразно-цепная реакция - полиморфизм длины рестрикционного фрагмента), аллель-специфическую амплификацию по типу "катящегося кольца", амплификацию рефракционной мутационной системы, гибридизацию, например, с последовательностями ДНК, ДАСГ (динамическая аллель-специфическая гибридизация), измерение кривой плавления, метод удлинения затравки с последующей MALDI-TOF масс-спектрометрией (лазерная десорбция/ионизация в присутствии матрицы - времяпролетная масс-спектрометрия) или их комбинации.
28. Способ по любому из пп.10-27, согласно которому этап ii) пп.10, 11 или 22 осуществляют следующим образом:
i) выделяют геномную ДНК из указанного образца;
ii) амплифицируют, по крайней мере, фрагмент геномной ДНК для получения продукта амплификации;
iii) проводят реакцию продукта амплификации с рестриктазой;
iv) разделяют полученные фрагменты электрофорезом в геле;
v) определяют соответствующие количества и длины фрагментов и
vi) определяют на основе полученных данных, какой из полиморфных участков присутствует.
29. Способ по п.28, где рестриктазой является XbaI.
30. Способ по какому-либо из пп.10-29, согласно которому устойчивость к ЕТЕС выбрана из группы, включающей Е. coli F4ab/F4ac, E. coli 0149, Е. coli F4, Е. coli F18, Е. coli F5, Е. coli F6, Е. coli 987P, Е. coli F41, Е. coli F18ab, E. coli F107, Е. coli F18ac, E. coli 2134P, Е. coli Av24 и какие-либо комбинации этих организмов.
31. Применение выделенной молекулы НК по любому из пп.1-6 и/или образца НК по любому из пп.7-9 для обнаружения аллеля полиморфного участка гена, связанного с устойчивостью к ЕТЕС.
32. Комплект для определения, является ли свинья гомозиготной, гетерозиготной или не несущей аллель полиморфного участка гена, связанного с устойчивостью к ЕТЕС, где указанный комплект содержит компонент, выбранный из группы, включающей образец НК по пп.7-9, молекулу НК по пп.1-6, пару ПЦР-праймеров, рестриктазу или какую-либо их комбинацию.
33. Комплект по п.32, где пара ПЦР-праймеров выбрана из группы, включающей SEQ ID NO 18 и SEQ ID NO 19, SEQ ID NO 20 и SEQ ID NO 21, SEQ ID NO 22 и SEQ ID NO 23, SEQ ID NO 24 и SEQ ID NO 25, SEQ ID NO 26 и SEQ ID NO 27, SEQ ID NO 28 и SEQ ID NO 29, SEQ ID NO 30 и SEQ ID NO 31, SEQ ID NO 32 и SEQ ID NO 33, SEQ ID NO 34 и SEQ ID NO 35, SEQ ID NO 36 и SEQ ID NO 37, SEQ ID NO 38 и SEQ ID NO 39, SEQ ID NO 40 и SEQ ID NO 41, SEQ ID NO 42 и SEQ ID NO 43, SEQ ID NO 44 и SEQ ID NO 45, SEQ ID NO 46 и SEQ ID NO 47, SEQ ID NO 48 и SEQ ID NO 49, SEQ ID NO 50 и SEQ ID NO 51, SEQ ID NO 52 и SEQ ID NO 53, SEQ ID NO 54 и SEQ ID NO 55, SEQ ID NO 56 и SEQ ID NO 57, SEQ ID NO 58 и SEQ ID NO 59, SEQ ID NO 60 и SEQ ID NO 61, SEQ ID NO 62 и SEQ ID NO 63, SEQ ID NO 64 и SEQ ID NO 65 и комплементарные им последовательности.
34. Применение пары праймеров, охарактеризованных в п.33, для определения устойчивости или восприимчивости свиньи к ЕТЕС, где указанная пара праймеров выбрана из группы, включающей SEQ ID NO 18 и SEQ ID NO 19, SEQ ID NO 20 и SEQ ID NO 21, SEQ ID NO 22 и SEQ ID NO 23, SEQ ID NO 24 и SEQ ID NO 25, SEQ ID NO 26 и SEQ ID NO 27, SEQ ID NO 28 и SEQ ID NO 29, SEQ ID NO 30 и SEQ ID NO 31, SEQ ID NO 32 и SEQ ID NO 33, SEQ ID NO 34 и SEQ ID NO 35, SEQ ID NO 36 и SEQ ID NO 37, SEQ ID NO 38 и SEQ ID NO 39, SEQ ID NO 40 и SEQ ID NO 41, SEQ ID NO 42 и SEQ ID NO 43, SEQ ID NO 44 и SEQ ID NO 45, SEQ ID NO 46 и SEQ ID NO 47, SEQ ID NO 48 и SEQ ID NO 49, SEQ ID NO 50 и SEQ ID NO 51, SEQ ID NO 52 и SEQ ID NO 53, SEQ ID NO 54 и SEQ ID NO 55, SEQ ID NO 56 и SEQ ID NO 57, SEQ ID NO 64 и SEQ ID NO 65 и комплементарные им последовательности.
35. Способ выведения свиней, устойчивых к ЕТЕС, при котором:
i) определяют первую особь свиньи как устойчивую к ЕТЕС с использованием способа по любому из пп.10-30;
ii) отбирают указанную первую особь и
iii) указанную первую особь скрещивают со второй,
для получения потомства, которое является более устойчивым к ЕТЕС, чем потомство от беспорядочно скрещиваемых родителей.
36. Способ по п.35, при котором:
i) определяют первую особь свиньи как устойчивую к ЕТЕС с использованием способа по любому из пп.10-30;
ii) отбирают указанную первую особь;
iii) определяют вторую особь свиньи как устойчивую к ЕТЕС с использованием способа по любому из пп.10-30 и
iv) скрещивают первую особь со второй;
для получения потомства, которое является более устойчивым к ЕТЕС, чем потомство от беспорядочно скрещиваемых родителей.
37. Способ производства свинины, при котором:
i) получают потомство свиньи по п.35 или 36;
ii) получают свинину из потомства свиньи.
38. Способ скрининга потенциального препарата-кандидата для лечения восприимчивости свиней к ЕТЕС, при котором:
i) выбирают тестируемую популяцию свиней, которые определены как восприимчивые к ЕТЕС, с помощью способа по любому из пп.10-30;
ii) вводят потенциальный препарат-кандидат животным тестируемой популяции и
iii) оценивают эффективность потенциального препарата-кандидата на тестируемой популяции.
Текст
011240 Область изобретения Данное изобретение касается в своем широком аспекте определения устойчивости или восприимчивости свиньи к энтеротоксигенной Е. coli (ETEC). В частности, данное изобретение представляет способы, образцы и молекулы ДНК, включенные в определение устойчивости или восприимчивости свиньи к ЕТЕС. Данное изобретение касается также способов выведения свиней с использованием данных по устойчивости/восприимчивости, смешанной спермы самцов свиней и способов подбора лекарственных средств для компенсирования восприимчивости к ЕТЕС. Уровень техники При выведении свиней главной проблемой является содержание новорожденных и, в частности, отнятых поросят здоровыми. В этом отношении желудочно-кишечные нарушения являются наиболее распространенными и серьезными проблемами, ежегодно и свиноводство, и животноводство во всем мире испытывает существенные потери поголовья скота от вспышек этих заболеваний. Косвенные потери происходят от затрат на лекарственные средства, замедления роста и других последствий заболеваний,которые могут быть более существенные, чем прямой ущерб от падежа. Известно, что болезнетворные организмы, вызывающие значительное число случаев диареи у поросят, являются энтеротоксигенными штаммами Е. coli (ЕТЕС). Отдельные ЕТЕС выделены у инфицированных животных, и такие обнаруженные у поросят типы штаммов Е. coli, как Е. coli F18 и Е. coli F4 (ранее известный как K88) являются среди них главными штаммами, приводящими к летальному исходу. Обозначения F18 и F4 относятся к типам ЕТЕС, имеющим ворсинки, и используются для того, чтобы отличать различные штаммы. Адгезивные ворсинки позволяют Е. coli колонизировать в кишечнике. Колонизация зависит от прилипания бактерии к энтероцистам, а последующая пролиферация и выделение токсинов ЕТЕС вызывает диарею. Болезнь развивается после попадания ЕТЕС в желудочно-кишечный тракт поросят. Бактерии ЕТЕС прилипают к стенкам тонкого кишечника с помощью их белковых антигенов (ворсинок), размножаются там в большом количестве и передают свои токсины прямо клеткам кишечного эпителия. Из-за воздействия, оказываемого токсинами, всасывающая активность эпителиальных клеток кишечника прекратится, и клетки будут секретировать большое количество жидкости в кишечную полость, что приведет к развитию более или менее тяжелой диареи. В данной области сделаны попытки контролировать диарею, вызванную ЕТЕС, у таких животных,как свиньи. В патенте США 4443549 описывается способ получения моноклональных антител против адгезии патогенной бактерии, адгезия которой способствует присоединению бактерии к коже и слизистой ткани. Антитела могут использоваться в фармацевтической композиции, приемлемой для орального введения животным. Патент США 4761372 описывает гены, содержащие плазмиды, кодирующие иммуногенный, нетоксичный, термолабильный энтеротоксин и/или нетоксичный, термостабильный энтеротоксин, и Е. coli,содержащие такие плазмиды, применяемые в качестве живой вакцины для вакцинации человека и животных против заболеваний, вызывающих диарею. Кроме того, патент WO 00/58476 описывает способ получения живой вакцины Е. coli орального применения для профилактики диареи у отнятых поросят. Штаммы Е. coli, не выделяющие энтеротоксины, образующие два типа адгезивных ворсинок (F4 и F18), вводятся поросятам для попытки создать локальный иммунитет. Тем не менее, не все свиньи поддаются инфекции Е. coli. Восприимчивость к адгезии, например экспрессия рецепторов свиней для связывания отдельной реснички, как показано, генетически контролируется хозяином. Механизм устойчивости, видимо, препятствует Е. coli колонизировать слизистую оболочку кишечника, бактерия не может удерживаться на стенках кишечника устойчивых животных. Попытка определить устойчивость к Е. coli описывалась в заявке на патент WO 98/53101. Заявка касается способа, разделяющего свиней на устойчивых и восприимчивых к болезням, вызываемым F18 Е.coli. Дифференциация осуществляется с использованием ДНК тестов для полиморфных участков ДНК в гене (1,2)трансферазы-1 в хромосоме 6 свиньи. Энтеротоксигенные клетки Escherichia coli (ЕТЕС), которые экспрессируют ворсинки типа F4ab илиF4ac (ранее известные как K88ab и К 88 ас), являются основными причинами диареи и смерти новорожденных и молодых поросят (Wilson и Francis, 1986). В Дании ЕТЕС F4 является причиной около 25% случаев диареи, о которых сообщалось (Ojeniyi и др., 1994). В 1975 г. Селвуд с сотрудниками опубликовал описание наблюдения за двумя фенотипами свиней по отношению к ЕТЕС F4, а именно устойчивых и восприимчивых соответственно. В 1977 г. Гиббонс и др. обнаружили, что устойчивость к ЕТЕС F4ac наследовалась как аутосомный рецессивный менделевский признак, и предположили наличие сцепления с трансферриновым локусом, что позже подтвердилось (Guerin и др. 1993). Картирование сцепления локусов свиньи, ответственных за восприимчивость к ЕТЕС F4ac и F4ab, приводит к предположению, что потенциальный ген-кандидат расположен в хромосоме 13 (Edfors-Lilja и др., 1995), но ген-кандидат не был обнаружен. Это означает, что существует только один доступный диагностический тест на этот тип устойчивости к ETEC F4 - это тест на адгезию, разработанный Селвудом и др. в 1975 г. С тех пор тест на адгезию необходим и при серьезной кишечной-1 011240 хирургии и при забое свиней, однако, этот метод очень трудоемкий, что мешает включить его в программы по выведению. Необходимое условие, которое должно быть выполнено, чтобы включить диагностический тест в программу выведения, это то, что тест должен быть быстрый, удобный в использовании и позволяющий точно определить генотип живых животных; однако, пока ни один из применяемых методов не отвечает этому требованию. Краткое описание изобретения Данное изобретение представляет недавно обнаруженные полиморфные участки генов, связанные с устойчивостью к Е. coli и расположенные в области между маркерами SW2196 и SW225 включительно,на хромосоме 13 свиньи (SSC). Некоторые из преимуществ данного изобретения включают легкость в использовании, воздействие,неинвазивное тестирование и быстрое получение результата. Более широко, преимуществами различных аспектов данного изобретения являются, например, экологически более безопасное производство мяса с уменьшенным применением антибиотиков, более выгодное производство мяса и использование более здоровых животных в производстве. Согласно первому аспекту данное изобретение относится к выделенной молекуле нуклеиновой кислоты (НК), включающей аллель полиморфного участка гена, связанный с устойчивостью к энтеротоксигенной Е. coli (ETEC), указанный полиморфный ген находится в области между маркерами SW2196 иSW225 включительно, на хромосоме 13 свиньи. Следующий аспект изобретения представляет образец НК, который включает последовательность НК, гомологичную фрагменту вышеупомянутой молекулы НК. Следующий аспект данного изобретения касается способа определения устойчивости свиньи к ЕТЕС, включающего:i) получение образца у свиньи, указанный образец содержит генетический материал,ii) определение с помощью образца, является ли свинья гомозиготной по аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС, указанный полиморфный участок гена находится в области между маркерами SW2196 и SW225 включительно, на хромосоме 13 свиньи, иiii) определение свиньи как устойчивой к ЕТЕС, если она гомозиготна по аллелю полиморфного участка гена, связанному с устойчивостью. Следующий аспект данного изобретения относится к использованию выделенной молекулы НК и/или образцу НК, как образцу для нахождения у свиньи аллеля полиморфного участка гена, связанного с устойчивостью к ЕТЕС. Другой аспект данного изобретения касается использования пары молекул НК как праймеров для метода ПЦР (полимеразная цепная реакция), указанный метод ПЦР используется для определения устойчивости или восприимчивости свиньи к ЕТЕС, указанная пара молекул НК выбирается из группы,включающей SEQ ID NO 18 и SEQ ID NO 19, SEQ ID NO 20 и SEQ ID NO 21, SEQ ID NO 22 и SEQ IDNO 62 и SEQ ID NO 63, SEQ ID NO 64 и SEQ ID NO 65 и комплементарные им последовательности. Следующий аспект данного изобретения представляет комплект для определения, является ли свинья гомозиготной, гетерозиготной или не несущей аллель полиморфного участка гена, связанный с устойчивостью к ЕТЕС, указанный комплект включает первый компонент, выбранный из группы, состоящей из пробы НК, молекулы НК, пары ПЦР-праймеров, рестриктазы и какой-либо их комбинации. Другой аспект данного изобретения касается способа выведения свиней, устойчивых к ЕТЕС, метод включаетi) отбор первой особи, указанная особь определена как устойчивая к ЕТЕС с использованием описанного здесь способа; иii) скрещивание указанных особей; получение потомства свиней, которое более устойчиво к ЕТЕС, чем потомство произвольно отобранных родительских особей. В следующем аспекте изобретение представляет выделенные молекулы НК для использования их в качестве антисмысловой НК, информационной рибонуклеиновой кислоты (и-РНК), рибозимы, эндотелина (ETC) для генетической медицины, генотерапии или кинетопластической репарации ДНК. Данное изобретение также относится к способу производства свинины, способ включает:i) получение потомства свиньи, как описано здесь,ii) получение свинины из этого потомства. В одном из аспектов изобретение касается способа подбора потенциального лекарственного препарата для лечения особей, восприимчивых к ЕТЕС, включающего:i) отбор тестируемой популяции свиней, которые определены как восприимчивые к ЕТЕС, данное определение выполняется с использованием способа, описанного здесь;ii) введение потенциального лекарственного препарата особям тестируемой популяции иiii) оценка эффективности потенциального лекарственного препарата на особях тестируемой популяции. В следующем аспекте данное изобретение представляет смесь спермы самцов свиньи, включая сперму по крайней мере от двух самцов, при этом указанные самцы определены как устойчивые к ЕТЕС с использованием описанного здесь способа. Детальное описание данного изобретения Выражение "молекула нуклеиновой кислоты" или "молекула НК" относится в данном контексте к олигомерной или полимерной рибонуклеиновой кислоте (РНК) или дезоксирибонуклеиновой кислоте(ДНК) или их миметикам. Это выражение включает молекулы естественного происхождения, состоящие из азотистых оснований, углеводных компонентов и ковалентных межнуклеозидных (основных) связей,а также молекулы не природного происхождения, состоящие из азотистых оснований, углеводных компонентов и ковалентных межнуклеозидных (основных) связей, которые функционируют подобным образом, или их комбинации. Такие модифицированные или замещенные нуклеиновые кислоты часто предпочитаются природным формам, потому что обладают желательными свойствами, такими как, например,повышенной клеточной поглотимостью красителя, повышенным сродством к мишени нуклеиновой кислоты и увеличением стабильности в присутствии нуклеаз и других ферментов, и описаны в данном контексте терминами "аналоги нуклеиновых кислот" или "миметики нуклеиновых кислот". Предпочтительными примерами миметиков нуклеиновых кислот являются пептидная нуклеиновая кислота (ПНК),замкнутая нуклеиновая кислота (ЗНК), ксило-ЗНК, фосфоротиоат-, 2'-метокси-, 2'-метоксиэтокси-, морфолино- и фосфорамидатсодержащие молекулы или т.п. Используемое здесь выражение "ЕТЕС" относится к бактериям из рода Escherichia и вида Escherichia coli, которые являются энтеротоксигенными и/или энтеропатогенными бактериями Е. coli(ЕТЕС). Штаммы ЕТЕС отличаются типами своих ворсинок, и группа штаммов ЕТЕС включает, но не ограничивается, Е. coli F4 (ранее известный как K88), такой как Е. coli F4ab/F4ac, Е. coli F4ab, E. coliF4ac, E. coli F4ad, E. coli 0149, E. coli F5 (ранее известный как K99), E. coli F6 (ранее известный как 987 Р), Е. coli F41, Е. coli F18, Е. coli F18ab, Е. coli F107, F18ac, E. coli 2134P, E. coli Av24 и какие-либо их комбинации. Выражение "аллель полиморфного участка гена, связанного с устойчивостью к ЕТЕС" касается последовательности НК, которая отмечена в связи с устойчивостью к ЕТЕС, и выражение "аллель полиморфного участка гена, связанного с восприимчивостью к ЕТЕС" является последовательностью нуклеотидов, которая отмечена в связи с восприимчивостью к ЕТЕС. Выражение "последовательность НК" может быть использована для определения молекулы нуклеиновой кислоты. Точнее, выражение "последовательность НК" охватывает нуклеиновый материал непосредственно и, таким образом, не ограничиваясь информацией о последовательности (то есть последовательность букв, обозначающих четыре основания), что биохимически характеризует определенную молекулу ДНК или РНК. Выражение "гомология" определяет количественную меру степени соответствия между двумя аминокислотными последовательностями равной длины или между двумя нуклеотидными последовательностями равной длины. Если две сравниваемые последовательности не одинаковой длины, они должны быть приравнены с наиболее точным соответствием. Идентичность последовательности может быть рассчитана как [(Nref-Ndif)100/(Nref)], где Ndif - общее количество различных остатков в двух выровненных последовательностях и Nref - число остатков в одной из последовательностей. Следовательно, последовательность ДНК AGTCAGTC будет иметь идентичность последовательности на 75% с последовательностью ААТСААТС (Ndif=2 и Nref=8). Несоответствие рассчитано как не идентичность определенного остатка(ков), например последовательность ДНК AGTGTC будет иметь идентичность последовательности на 75% с последовательностью ДНК AGTCAGTC (Ndif=2 и Nref=8). Идентичность последовательности может альтернативно быть рассчитана в соответствии с программой BLASTP (Pearson и Lipman (1988)(www.ncbi.nim.nih.gov/cgi-bin/BLAST). В одном из вариантов осуществления данного изобретения выравнивание выполнено в соответствии с общим алгоритмом выравнивания с параметрами по умолчанию,как описано Хуангом и Миллером (1991), доступно на сайте http://www.ch.embnet.org/software/LALIGNform. html. Выражение "гомологичный" означает, что одна одноцепочечная последовательность нуклеиновой кислоты может гибридизироваться с комплементарной одноцепочечной последовательностью нуклеиновой кислоты. Степень гибридизации может зависеть от ряда факторов, включая количество идентичности между последовательностями и условия гибридизации, такие как температура и концентрация соли. Выражение "LOD-балл (количественный показатель сцепления генов, выраженный в логарифмической шкале)" имеет следующее значение: чтобы определять, связан ли аллель полиморфного участка гена с устойчивостью к ЕТЕС, может быть применен LOD-балл. LOD-балл, который иногда также обозначается как Zmax, показывает вероятность (логарифм отношения вероятности), что участок генетиче-3 011240 ского маркера и определенный участок гена сцеплены на определенном расстоянии. LOD-баллы могут,например, быть рассчитаны с применением компьютерной программы типа MLINK пакета LINKAGE(Lathrop и др., 1985). LOD-балл более чем 3.0, как полагают, является существенным доказательством существования сцепления между полиморфными участками гена и устойчивостью к ЕТЕС или участком гена, отвечающим за устойчивость к ЕТЕС. Выражение "фрагмент" касается набора нуклеотидов молекулы НК, где указанный набор включает по крайней мере 10 нуклеотидов, например 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35,40, 50, 60, 70, 80, 90, 100, 150, 200, 250, 300, 400, 500, 1000, 2000, 5000 или 10000 нуклеотидов. Если фрагмент молекулы НК используется как праймер для метода ПЦР, предпочтительно, чтобы набор включал 10-30 нуклеотидов, и более предпочтительно - 15-23 нуклеотидов, например 15, 16, 17, 18, 19,20, 21, 22 или 23 нуклеотидов. Выражение "полиморфный участок гена" касается переменной нуклеотидной последовательности(полиморфной), которая может присутствовать в геномной ДНК свиньи в хромосоме. Полиморфные участки гена выбраны из группы, состоящей из однонуклеотидного полиморфного участка (ОНП), непостоянного числа тандемных дупликаций полиморфного участка, рассеянного повтора ДНК, вставок, дубликаций, делеций, амплификаций, хромосомных перестановок, комбинации однонуклеотидных полиморфных участков, коротких тандемных дупликаций, динуклеотидных повторов и каких-либо их комбинаций. Переменная нуклеотидная последовательность может быть определена, например, с помощью нуклеиново-кислотной амплификации и изучения различия в размере или последовательности нуклеотидов, что обусловлено полиморфизмом. Термин "свинья" включает всех представителей семейства Suidae вида Sus scrofa. На сегодня существует большое количество относительно хорошо охарактеризованных пород свиней, и многие из этих пород в различной степени восприимчивы к энтеротоксигенным или энтеропатогенным штаммам Е. coli. Очевидно, что способ по данному изобретению заключается в том, что из группы особей, состоящих из представителей Sus scrofa, отбирается такая особь, с помощью которой можно было бы вывести породу,устойчивую к ЕТЕС. В настоящее время существует 10 пород свиней, которые признаны и могут быть зарегистрированы как чистопородные в Соединенных Штатах. Это такие породы, как беркшир, белый честер, дюрок, гэмпшир, ландрас, польско-китайская, пятнистая, йоркшир, герефорд и тамворс. В высокоразвитом промышленном производстве мяса сегодня наиболее важны четыре породы: ландрас, йоркшир, дюрок и гэмпшир. Особи всех четырех пород могут быть восприимчивыми к ЕТЕС,поэтому все страны могли бы извлечь пользу из программы выведения, включающей способ, описанный в данном изобретении. Известны следующие породы свиней - ландрас, дюрок, йоркшир, датский йоркшир, датский дюрок,датский ландрас, белый датский ландрас, черно-пестрый датский ландрас, гэмпшир, датский гэмпшир,польско-китайская, герефор, американский ландрас, американский йоркшир, арава айленд, ба хуен, банту, базна, пекинская черная, белорусская черно-пестрая, бельгийский ландрас, беркшир, английский ландрас, английская длинноухая, болгарская белая, кантонская, честер белый, чешская улучшенная белая, дермантская черно-пестрая, голландский ландрас, фенджинская, финский ландрас, французский ландрас, немецкий ландрас, глостерширская пятнистая, гвинейская, хезуо, иберийская, итальянский ландрас, джинхуа, келейская, крскопольская, кьюнкьюн, лакомб, крупная черная, крупная черно-белая,крупная белая, литовская, мейшан, белая средняя, минжу, монг кэй, мукота, мора ромагнола, моура,мулфут, нейджейн, нингксианг, норвежский ландрас, оссабау айленд, оксфордская песочная и черная,филиппинская, питрэйн, ред ватл, седлбек, пятнистая, шведский ландрас, свалоу белид мангалица, тамворс, туок найю, тибетская, теропотдж, вьетнамская толстобрюхая, уэльская и вузишан. Следует отметить, что способ по данному изобретению может использоваться для выявления устойчивых животных от какого-либо скрещивания какой-либо породы свиней, упомянутых выше. Выражение "генетический материал" должен в данном контексте интерпретироваться в самом широком своем смысле и может включать одно или более понятий, выбранных из группы, содержащей геномные ДНК, такие как хромосомы, матричную РНК (мРНК), фрагменты и/или гидролизаты этих молекул. Выражение "геномная ДНК" следует понимать в самом широком смысле. Выражение может пояснять одно или более понятий, выбранных из группы, включающей геномные ДНК, такие как хромосомы,фрагменты и/или гидролизаты этих молекул. Следует подчеркнуть, что все выражения, варианты осуществления и особенности, описанные здесь, могут использоваться во всех упоминаемых в данном изобретении аспектах. В первом аспекте данного изобретения представлена выделенная молекула нуклеиновой кислоты(НК), включающая аллель полиморфного участка гена, связанный с устойчивостью к энтеротоксигенной Е. coli (ETEC). Указанный полиморфный участок гена расположен в области между маркерами SW2196 и SW225 включительно, на хромосоме 13 свиньи. В практическом варианте осуществления полиморфный участок гена расположен в области между маркерами SW207 и S0075 включительно. В одном из вариантов осуществления данного изобретения аллель полиморфного участка гена, связанный с устойчивостью к ЕТЕС, определяет свинью, гомозиготную по данному аллелю, как устойчивую-4 011240 к ЕТЕС. В следующем варианте осуществления данного изобретения свинья, гомозиготная по указанному аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС, является устойчивой к ЕТЕС. В предпочтительном варианте осуществления данного изобретения ЕТЕС является Е. coli штамм F4 и/или Е. coli штамм F4 ab/ac. В предпочтительных вариантах осуществления выделенная молекула НК может включать аллель полиморфного участка гена, который связан с устойчивостью к ЕТЕС с LOD-баллом, равным по крайней мере 3.0, включая 4.0, 5.0, 6.0, 7.0, 8.0, 9.0, 10 или 50. В предпочтительном варианте осуществления по данному изобретению выделенная молекула НК включает аллель полиморфного участка гена, связанный с устойчивостью к ЕТЕС. Выделенная молекула НК может также включить последовательность НК, которая расположена в MUC4 гене свиньи. В некоторых предпочтительных вариантах осуществления по данному изобретению выделенная молекула НК включает последовательность НК, которая является идентичной или имеет по крайней мере 90%-ную гомологию, например 95 или 99%-ную гомологию последовательности, выбранной из группы последовательностей, включающей SEQ ID NO 1, SEQ ID NO 2, SEQ ID NO 3, SEQ ID NO 4, SEQ ID NO 5, SEQ ID NO 6, SEQ ID NO 7, SEQ ID NO 8, SEQ ID NO 9, SEQ ID NO 10, SEQ ID NO 11, SEQ ID NO 12,SEQ ID NO 13, SEQ ID NO 14, SEQ ID NO 15, SEQ ID NO 16, SEQ ID NO 17, SEQ ID NO 67, SEQ ID NO 68, SEQ ID NO 81, SEQ ID NO 82, SEQ ID NO 83, SEQ ID NO 84, SEQ ID NO 85, SEQ ID NO 86, SEQ IDNO 182, SEQ ID NO 183, SEQ ID NO 184, SEQ ID NO 185, SEQ ID NO 186, SEQ ID NO 187, SEQ ID NO 188, SEO ID NO 189, SEQ ID NO 190, SEQ ID NO 191, SEQ ID NO 192, SEQ ID NO 193, SEQ ID NO 194,SEQ ID NO 195, SEQ ID NO 196, SEQ ID NO 197, комплементарные им последовательности и какие-либо их фрагменты. В следующих предпочтительных вариантах осуществления по данному изобретению выделенная молекула НК включает последовательность НК, которая является идентичной или имеет по крайней мере 90%-ную гомологию, например 95 или 99%-ную гомологию последовательности, выбранной из группы последовательностей, состоящей из SEQ ID NO 1, SEQ ID NO 2, SEQ ID NO 3, SEQ ID NO 4, SEQ ID NO 5, SEQ ID NO 6, SEQ ID NO 7, SEQ ID NO 8, SEQ ID NO 9, SEQ ID NO 10, SEQ ID NO 11, SEQ ID NO 12,SEQ ID NO 13, SEQ ID NO 14, SEQ ID NO 15, SEQ ID NO 16, SEQ ID NO 17, SEQ ID NO 67, SEQ ID NO 68, SEQ ID NO 81, SEQ ID NO 82, SEQ ID NO 83, SEQ ID NO 84, SEQ ID NO 85, SEQ ID NO 86, SEQ IDID NO 94, SEQ ID NO 95, SEQ ID NO 96, SEQ ID NO 97, SEQ ID NO 98, SEQ ID NO 99, SEQ ID NO 100,SEQ ID NO 101, комплементарные им последовательности и какие-либо их фрагменты. В особо предпочтительном варианте осуществления данного изобретения выделенная молекула НК включает последовательность НК, которая является идентичной или имеет по крайней мере 90%-ную гомологию, например 95 или 99%-ную гомологию последовательности, выбранной из группы последовательностей, включающей SEQ ID NO 6, SEQ ID NO 8, SEQ ID NO 82, SEQ ID NO 83, SEQ ID NO 87, SEQID NO 88, комплементарные им последовательности и какие-либо их фрагменты. В одном из вариантов осуществления выделенная молекула НК включает последовательность НК,которая отличает свиней, устойчивых к ЕТЕС от восприимчивых к ЕТЕС. В другом варианте осуществления данного изобретения выделенная молекула НК является молекулой НК, которая является полностью или почти полностью неслучайно распределенной с какими-либо молекулами НК, описанными выше. Аллели двух или более соседних участков показывают неслучайное распределение, если они встречаются вместе с частотами, значительно отличающимися от предсказанных индивидуальных частот аллеля. Полное неслучайное распределение обычно происходит, когда две последовательности НК (например, полиморфный участок MUC4 гена свиньи) физически расположены очень близко друг к другу на хромосоме, и если возможности для рекомбинации были ограничены. Если две последовательности НК-5 011240 находятся в равновесном сцеплении, тогда необходимо определить фазу сцепления (то есть как аллели сцеплены) в каждой родословной до того, как маркеры будут использованы для прогнозирования генотипов по интересующему гену. Полиморфные участки гена, которые находятся в частичном, а не в полном, неслучайном распределении с интересующим геном, могут быть полезными в прогнозирующих тестах. В предпочтительном варианте осуществления данного изобретения молекула НК включает участок полиморфного гена, такой как A1059G в SEQ ID NO 6, T1125G в SEQ ID NO 6, A1134G в SEQ ID NO 6,C1138G в SEQ ID NO 6, C1849G в SEQ ID NO 8, C2129T в SEQ ID NO 8, A4847G в SEQ ID NO 82,T4913G в SEQ ID NO 82, A4922G в SEQ ID NO 82, C4926G в SEQ ID NO 82, A1659T в SEQ ID NO 83,T1666G в SEQ ID NO 83, C1684A в SEQ ID NO 83, T1740A в SEQ ID NO 83, C1795T в SEQ ID NO 83,T1820G в SEQ ID NO 83, C1912T в SEQ ID NO 83, G2997A в SEQ ID NO 83, G3277C в SEQ ID NO 83 или какую-либо из комплементарных им последовательностей. Молекула НК может быть выделена так, чтобы был охвачен участок полиморфного гена, например изменчивость, обнаруженная в положении 1726 SEQ ID NO 83, где нуклеотиды AACGTG присутствуют у устойчивой особи, и 6 пар нуклеотидов удалены у восприимчивой к ЕТЕС особи; изменчивость, обнаруженная в положении 2009 SEQ ID NO 83, где у свиней Т либо отсутствует, либо удален; изменчивость,обнаруженная в положении 332 SEQ ID NO 87, где присутствует перемещение однонуклеотидного полиморфного участка между G и А; или изменчивость, обнаруженная в положении 3530 из SEQ ID NO 88,где присутствует перемещение однонуклеотидного полиморфного участка между G и А. Не вдаваясь в подробную теорию, эти три полиморфных участка, как полагают, являются связанными с устойчивостью к ЕТЕС. Изобретение представляет во втором аспекте образец НК, включающий последовательность НК,гомологичную фрагменту выделенной молекулы НК, как описано выше. Образец НК может быть определенным для аллеля по крайней мере одного однонуклеотидного полиморфного участка, выбранного из группы однонуклеотидных полиморфных участков, включающейA1059G в SEQ ID NO 6, T1125G в SEQ ID NO 6, A1134G в SEQ ID NO 6, C1138G в SEQ ID NO 6,C1849G в SEQ ID NO 8, C2129T в SEQ ID NO 8, A4847G в SEQ ID NO 82, T4913G в SEQ ID NO 82,A4922G в SEQ ID NO 82, C4926G в SEQ ID NO 82, A1659T в SEQ ID NO 83, T1666G в SEQ ID NO 83,C1684A в SEQ ID NO 83, T1740A в SEQ ID NO 83, C1795T в SEQ ID NO 83, T1820G в SEQ ID NO 83,C1912T в SEQ ID NO 83, G2997A в SEQ ID NO 83, G3277C в SEQ ID NO 83 и комплементарные им последовательности. Образец НК может быть специфическим для аллеля по крайней мере одного полиморфного участка гена, включающего изменчивость, обнаруженную в положении 1726 SEQ ID NO 83, где нуклеотидыAACGTG присутствуют у устойчивой особи, и 6 пар нуклеотидов отсутствуют у восприимчивой к ЕТЕС особи. Образец НК может быть специфическим для аллеля по крайней мере одного полиморфного участка гена, включающего изменчивость, обнаруженную в положении 2009 SEQ ID NO 83, где у свиньи Т либо отсутствует, либо удален; изменчивость, обнаруженную в положении 332 SEQ ID NO 87, где присутствует перемещение однонуклеотидного полиморфного участка между G и А; и изменчивость, обнаруженную в положении 3530 SEQ ID NO 88, где присутствует перемещение однонуклеотидного полиморфного участка между G и А. Не вдаваясь в теорию, эти три полиморфных участка, как полагают, связаны с устойчивостью к ЕТЕС. В предпочтительном варианте осуществления по данному изобретению образец НК способен к гибридизации с частью аллеля, который включает полиморфный участок гена или с последовательностью НК, которая является комплементарной части аллеля, включающего полиморфный участок гена. Образец НК может быть специфическим для аллеля полиморфного участка гена, связанного с устойчивостью к ЕТЕС, указанный аллель полиморфного участка гена, связанный с устойчивостью к ЕТЕС, является связанным с устойчивостью к ЕТЕС с LOD-баллом по крайней мере 3.0, включая 4.0, 5.0,6.0, 7.0, 8.0, 9.0, 10 или 50. Образец НК может также в одном из вариантов осуществления включать последовательность НК,которая гомологична последовательности НК SEQ ID NO 66 или комплементарной ей последовательности. В практических вариантах осуществления образец НК включает по крайней мере 10 нуклеотидов,например 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40, 50, 60, 70, 80, 90, 100, 150, 200,250, 300, 400 или 500 нуклеотидов. Предпочтительно образец НК включает от 10 до 30 нуклеотидов, например от 15 до 23 нуклеотидов. В следующих предпочтительных вариантах осуществления образец НК включает 15 нуклеотидов, например 16, 17, 18, 19, 20, 21, 22 или 23 нуклеотида. В следующем аспекте данного изобретения представлен способ определения устойчивости свиньи к ЕТЕС, способ включает:i) получение образца данной особи, содержащего генетический материал;ii) определение при помощи данного образца, является ли особь гомозиготной по аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС, при этом указанный полиморфный участок-6 011240 гена располагается в области между маркерами SW2196 и SW225 включительно, на хромосоме 13 свиньи; иiii) определение особи как устойчивой к ЕТЕС, если она гомозиготна по аллелю полиморфного участка гена, связанному с устойчивостью. В одном из вариантов осуществления по данному изобретению способ далее включает определение,является ли свинья восприимчивой к ЕТЕС и несущей или не несущей признак устойчивости. Данный способ включает:iv) определение при помощи указанного образца, является ли особь гетерозиготной или не несущей аллель полиморфного участка гена, связанного с устойчивостью к ЕТЕС; иv) определение а) особи как восприимчивой к ЕТЕС и не несущей признак устойчивости, если она не несет аллель полиморфного участка гена, связанный с устойчивостью; или b) особи как восприимчивой к ЕТЕС, но несущей признак устойчивости, если она гетерозиготна по аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС. В другом варианте осуществления по данному изобретению полиморфный участок гена не расположен в хромосоме 6 свиньи. В следующем варианте осуществления полиморфный участок гена не расположен в гене -(1,2)фукозил-трансферазы (FUT1 ген). В предпочтительном варианте осуществления полиморфный участок гена расположен в области между маркерами SW2196 и SW225 включительно, например в области между маркерами SW207 иS0075 включительно. Обычно для картирования генов свиньи используются генетические маркеры-микросателлиты (например, SW2196, SW225, SW207, S0075 и другие маркеры из табл. 1, ниже), при этом ядром маркера является тандемно дуплицированная последовательность двух (обычно) или небольшого количества нуклеотидов, где различные аллели отличаются наличием различного числа повторов. Для микросателлитов(и для многих других возможных типов маркеров) полимеразная цепная реакция (ПЦР) используется для амплификации небольшого образца ДНК и представляет первый этап в идентификации альтернативных аллелей (т.е. генотипирование). Уникальные ПЦР-праймеры используются для гарантии того, что аллели определенного интересующего маркера амплифицированы только с образца ДНК данного животного. Продукты ПЦР затем разделяются электрофорезом и могут быть визуализированы, например, с помощью радиоактивных или флуоресцентных меток. Использование ПЦР на ДНК-маркерах позволяет выполнять генотипирование на очень маленьких образцах ДНК, которые можно относительно легко получить в любое время. Следовательно, животных можно генотипировать сразу после рождения, используя ДНК, выделенную из крови, пробы из уха или другой материал. Полиморфный участок гена может быть каким-либо полиморфным участком, расположенным в области между маркерами SW2196 и SW225 включительно, на хромосоме 13 свиньи, при этом аллель полиморфного участка гена, связанного с устойчивостью к ЕТЕС, связан с устойчивостью к ЕТЕС с LODбаллом, равным по крайней мере 3.0, включая 4.0, 5.0, 6.0, 7.0, 8.0, 9.0, 10.0 или 50. В другом варианте осуществления полиморфный участок расположен в MUC4 гене и/или в геномных последовательностях, смежных с 3' и/или 5' концами MUC4 гена свиньи. Смежные геномные последовательности могут иметь менее чем 500 т.п.н. (тысяч пар нуклеотидов), например менее чем 300 т.п.н. или даже менее чем 100 т.п.н. В предпочтительном варианте осуществления по данному изобретению полиморфный участок гена расположен в геномной последовательности, соответствующей SEQ ID NO 6 и/или SEQ ID NO 8. Эти последовательности, как полагают, являются частью MUC4 гена свиньи. Однако полиморфный участок гена может также быть расположен в геномной последовательности, соответствующей последовательности нуклеотидов, выбранной из группы, включающей SEQ ID NO 1, SEQ ID NO 2, SEQ ID NO 3, SEQ IDNO 184, SEQ ID NO 185, SEQ ID NO 186, SEQ ID NO 187, SEQ ID NO 188, SEQ ID NO 189, SEQ ID NO 190, SEQ ID NO 191, SEQ ID NO 192, SEQ ID NO 193, SEQ ID NO 194, SEQ ID NO 195, SEQ ID NO 196,SEQ ID NO 197, какие-либо их фрагменты и какие-либо их комбинации. В одном из вариантов осуществления по данному изобретению полиморфный участок гена расположен в MUC4 гене свиньи. Также полиморфный участок гена включает полиморфные участки гена, которые находятся в полном или почти полном неслучайном распределении с полиморфным участком гена, упомянутым выше. Полиморфные участки гена согласно данному изобретению могут быть идентифицированы, как описано в примерах, например в примере 6. Выражения "устойчивый к ЕТЕС" или "устойчивость к ЕТЕС" касаются в данном контексте особи свиньи, которая является устойчивой к одному или более типам инфекции Е. coli, например, устойчивой к адгезии ЕТЕС в кишечнике, устойчивой к колонизации ЕТЕС в кишечнике, устойчивой к кишечным нарушениям, типа диареи, вызванной ЕТЕС, и какой-либо их комбинации. Если две особи свиньи подвергнуть заражению одинаковой дозой ЕТЕС, то особь, устойчивая к определенному штамму ЕТЕС, будет менее восприимчивой к адгезии ЕТЕС в кишечнике, и/или к кишечной колонизации ЕТЕС, и/или к кишечными нарушениям, вызванным ЕТЕС, по сравнению с восприимчивой особью. В практическом варианте осуществления по данному изобретению устойчивая свинья не восприимчива к ЕТЕС вообще. В случае адгезии в кишечнике устойчивость в сравнении с восприимчивостью определяется с использованием теста на адгезию, описанным Селвудом и др., 1975. Вкратце, тест на адгезию может быть выполнен следующим образом. Эпителиальные клетки верхней части тонкой кишки брали у особей свиней при забое. Тест на адгезию выполняли, инкубируя эпителиальные клетки с, например, штаммами Е. coli F4ab и Е. coli F4ac соответственно. Образцы, содержащие, например, 10-20 эпителиальных клеток, могут быть исследованы на адгезию Е. coli F4ab и Е. coliF4ac микроскопией по методу интерференционного контраста. Результаты можно оценить по 4-балльной шкале, где 1 - ни одна бактерия не прилипла к кишечным клеткам и 4 - бактерии слоем покрыли все клетки. Балл 1 означает, что животное является устойчивым к адгезии ЕТЕС в кишечнике (в данном случае, Е. coli F4ab и Е. coli F4ac). To есть свинья, можно полагать, будет устойчивой к адгезии ЕТЕС в кишечнике, если балл = 1 или 2. В случае кишечной колонизации ЕТЕС устойчивость в сравнении с восприимчивостью можно определить, например, с использованием подсчета клеток ЕТЕС в образце фекалий свиньи или определением концентрации ворсинок ЕТЕС в образце фекалий. Устойчивая инфицированная свинья будет иметь значительно более низкое количество ЕТЕС или более низкую концентрацию ворсинок ЕТЕС в образце фекалий, чем восприимчивая инфицированная свинья. В случае кишечного заболевания, вызванного ЕТЕС, устойчивость в сравнении с восприимчивостью можно определить, например, путем добавления в корм свинье дозы ЕТЕС и наблюдением за проявлением кишечного заболевания, вызванного ЕТЕС. Если у свиньи проявляется болезнь, она является восприимчивой. Если у свиньи не проявляется болезнь, это может означать, что свинья является устойчивой или что свинья является восприимчивой, но по каким-либо причинам инфицирование не привело к кишечному заболеванию. Применение лекарственных препаратов или специальных диет компенсирует восприимчивость свиньи, возможно потому, что у восприимчивой свиньи не развивается кишечное заболевание после воздействия ЕТЕС. Свинья может быть мужской или женской особью, может иметь любой возраст во время определения и/или идентификации устойчивости или восприимчивости. Таким образом, свинья может быть выбрана из группы, состоящей из самца, самки, молочного поросенка, отнятого поросенка, молодняка и свиньи на завершающем периоде откорма. Во время определения и/или идентификации устойчивости или восприимчивости, свинья может быть новорожденной или иметь возраст от 1 дня до 1 месяца, 1-2 месяца, 2-3 месяца, 3-4 месяца, 4-5 месяцев, 5-6 месяцев, 6-7 месяцев, 7-8 месяцев, 8-9 месяцев, 9-10 месяцев, 10-11 месяцев, 11-12 месяцев, 12-14 месяцев, 14-16 месяцев, 16-18 месяцев, 18-20 месяцев, 20-24 месяца, 2-3 года, 3-4 года, 4-5 лет, 5-6 лет, 6-7 лет, 7-8 лет или 8-10 лет. В одном из вариантов осуществления по изобретению свинья имеет известную родословную, например с известными предками, по крайней мере в 1 поколении, например в 2 поколениях, включая 3, 4,5, 6, 7, 8, 9, 10, 15 или 20 поколений. Свинья может быть высокоинбредной и может иметь сертифицированную родословную. В данном предпочтительном варианте осуществления по изобретению полиморфным участком гена является однонуклеотидный полиморфный участок или комбинация однонуклеотидных полиморфных участков. Однонуклеотидный полиморфный участок может, например, быть однонуклеотидным полиморфным участком G/C. Данный предпочтительный однонуклеотидный полиморфный участок может быть выбран из группы, включающей A1059G в SEQ ID NO 6, T1125G в SEQ ID NO 6, A1134G в SEQ ID NO 6, C1138G вNO 83, C1684A в SEQ ID NO 83, T1740A в SEQ ID NO 83, C1795T в SEQ ID NO 83, T1820G в SEQ ID NO 83, C1912T в SEQ ID NO 83, G2997A в SEQ ID NO 83 и G3277C в SEQ ID NO 83. При упоминании об однонуклеотидном полиморфном участке используется выражение "X положение Y в SEQ ID NO ZZ", где "положение" означает число нуклеотидов однонуклеотидного полиморфного участка в SEQ ID NO ZZ, "X" - нуклеотид в восприимчивом гаплотипе и "Y" - нуклеотид в устойчивом гаплотипе. Например, A1059G в SEQ ID NO 6, означает, что в нуклеотиде NO 1059 последовательности нуклеотида SEQ ID NO 6 есть однонуклеотидный полиморфный участок, и что нуклеотид NO 1059 является аденозин монофосфатной группой, если свинья восприимчивая, и что нуклеотид NO 1059 является гуанозин монофосфатной группой, если свинья устойчивая. При более подробном описании однонуклеотидного полиморфного участка используется выражение "X/Y однонуклеотидный полиморфный участок". Это относится к однонуклеотидному полиморфному участку, если восприимчивая свинья имеет X нуклеотид в положении однонуклеотидного полиморфного участка и устойчивая свинья имеет Y нуклеотид в положении однонуклеотидного полиморфного участка. Таким образом, G/C однонуклеотидный полиморфный участок означает гуанозин монофосфатную группу, если свинья устойчивая, и цитозин монофосфатную группу, если свинья восприимчивая. Согласно данному изобретению однонуклеотидный полиморфный участок может быть каким-либо однонуклеотидным полиморфным участком, например, G/C однонуклеотидным полиморфным участком,G/A однонуклеотидным полиморфным участком, Т/С однонуклеотидным полиморфным участком, G/T однонуклеотидным полиморфным участком, А/Т однонуклеотидным полиморфным участком или С/А однонуклеотидным полиморфным участком. В одном из вариантов осуществления по данному изобретению способ включает на этапе ii) определение по образцу, является ли свинья в дополнение к аллелю первого полиморфного участка гена, связанному с устойчивостью к ЕТЕС, гомозиготной, гетерозиготной или не несущей аллель по крайней мере второго полиморфного участка гена, связанного с устойчивостью к ЕТЕС, и на этапе iii) идентификацию свиньи как устойчивой к ЕТЕС, если она гомозиготна по первому аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС, и/или по крайней мере по второму аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС. По крайней мере второй полиморфный участок гена может включать по крайней мере 3 полиморфных участка, например 4, 5, 6, 7, 10, 20, 30 или 50 полиморфных участков. В предпочтительных вариантах осуществления по крайней мере второй полиморфный участок гена является полиморфным участком, выбранным из группы, включающей однонуклеотидный полиморфный участок, переменное количество тандемно дуплицированных полиморфных участков, рассеянный повтор ДНК, вставки, делеции, амплификации, перестановки, комбинацию однонуклеотидных полиморфных участков, коротких тандемных повторов, динуклеотидных повторов и каких-либо их комбинаций. По крайней мере второй полиморфный участок может быть однонуклеотидным полиморфным участком, выбранным из группы, включающей A1059G в SEQ ID NO 6, T1 125G в SEQ ID NO 6, A1134G вNO 83, T1666G в SEQ ID NO 83, C1684A в SEQ ID NO 83, T1740A в SEQ ID NO 83, C1795T в SEQ ID NO 83, T1820G в SEQ ID NO 83, C1912T в SEQ ID NO 83, G2997A в SEQ ID NO 83 и G3277C в SEQ ID NO 83. В следующем варианте осуществления по изобретению по крайней мере второй полиморфный участок гена расположен в FUT1 гене свиньи. Согласно способу данного изобретения образец, полученный от особи свиньи, может быть выбран из группы, включающей материал ДНК и/или РНК, кровь, слюну, ткань, мазок из горла, сперму и их комбинации. Способ согласно изобретению включает получение образца генетического материала. Такой материал включает ДНК свиньи, которая может быть получена каким-либо известным способом или средствами. Материал ДНК свиньи может быть извлечен, выделен и очищен, например, из крови (свежей или замороженной), образцов тканей (например, селезенка, соскоб щеки), образцов волос, содержащих фолликулярные клетки, и спермы. Образец может включать кровь, частично или полностью гидролизированную, слюну, ткань, мазок из горла, сперму или их комбинации. Определение, является ли свинья гомозиготной, гетерозиготной по аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС или не несущей этот аллель, может быть выполнено, с использованием методики, выбранной из группы, включающей аллель-специфическую ПЦР, минисеквенирование, метод удлинения затравки, пиро-секвенирование, метод ПЦР-ПДФР (полимеразная цепная реакция - полиморфизм длины фрагментов рестрикции), аллель-специфическую амплификацию по типу "катящегося кольца", амплификацию рефрактерной мутационной системы (ARMS), гибридизацию, например, с последовательностями ДНК, динамическую аллель-специфическую гибридизацию(ДАСГ), измерение кривой плавления, метод удлинения затравки с последующей матричной лазерной десорбционной времяпролетной масс-спектрометрией (MALDI-TOF) и какие-либо их комбинации. Пример 4 иллюстрирует применение ПЦР и ДАСГ, соответственно, для определения, является ли-9 011240 свинья гомозиготной или гетерозиготной по аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС, или не несущей данный аллель. Существует множество методов, которые можно использовать для обнаружения мутаций отдельных оснований и других типов полиморфизма. Детальное описание практических методов можно найти у Ausubel и др. (2000) и у Sambrook и др. (1989). Среди наиболее важных методов: ДНК секвенирование; метод обнаружения мутаций путем оценки конформационного полиморфизма одноцепочечных фрагментов ДНК (SSCP); электрофорез продуктов ПЦР в денатурирующем градиентном геле (DGGE); расшифровка последовательности НК фингерпринтметодом, рестриктазный фингерпринтметод и электрофорез продуктов ПЦР в денатурирующем постоянном геле (CDGE). Мутации также можно обнаружить специфической гибридизацией олигонуклеотидов с анализируемой нуклеиновой кислотой. Определение, является ли свинья гомозиготной, гетерозиготной по аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС, или не несущей этот аллель, может быть выполнено с использованием способа, который включает по крайней мере один из следующих этапов:a) получение образца от особи, при этом указанный образец включает генетический материал;b) выделение геномной ДНК из данного образца;c) амплифицирование, по крайней мере, фрагмента геномной ДНК для получения продукта амплификации;d) взаимодействие продукта амплификации с рестриктазой;e) разделение полученных фрагментов электрофорезом в геле;f) определение соответствующих количеств и длин фрагментов;g) определение полиморфизма по количеству и длинам фрагментов. Способ определения может быть выполнен в последовательности а), b), с), d), e), f) и g). Рестриктаза может быть таким ферментом, как Aat II, Bam HI, BgI II, Cla I (Bsu 151), Dpn I, Eco RI,Eco RV, Esp I (Bpu 1102I), Hind III, Nco I, Nde I, Not I, Pae I (Sph I), Pau I, Pst I, Pvu I, Sac I, Sal I, Sma I,Xba I или Xho I. Рестриктаза XbaI является предпочтительным ферментом, если аллель полиморфного участка гена,связанного с устойчивостью к ЕТЕС, - SNP C1849G. В предпочтительных вариантах осуществления ЕТЕС выбран из группы, включающей Е. colicoli F107, Е. coli F18ac, E. coli 2134 Р, Е. coli Av24 и какие-либо комбинации этих организмов. Данное изобретение далее касается использования выделенной молекулы НК, как описано здесь,и/или образца НК, как описано здесь, как образца для обнаружения аллеля полиморфного участка гена,связанного с устойчивостью к ЕТЕС. Следующий аспект данного изобретения касается использования пары молекул НК в качестве праймеров для ПЦР анализа. ПЦР анализ применяется для определения устойчивости или восприимчивости свиньи к ЕТЕС, указанная пара молекул НК выбрана из группы, включающей SEQ ID NO 18 и SEQNO 64 и SEQ ID NO 65 и комплементарные им последовательности. Данное изобретение не ограничено использованием пар молекул НК, упомянутых здесь, таким образом, последовательности в SEQ ID NO 18, SEQ ID NO 19, SEQ ID NO 20, SEQ ID NO 21, SEQ ID NO 22, SEQ ID NO 23, SEQ ID NO 24, SEQ ID NO 25, SEQ ID NO 26, SEQ ID NO 27, SEQ ID NO 28, SEQ IDID NO 63, SEQ ID NO 64 и SEQ ID NO 65 могут быть использованы в качестве праймеров для ПЦР анализа, указанный ПЦР анализ является этапом в определении устойчивости или восприимчивости свиньи к ЕТЕС. Также пара молекул НК, как праймеров для ПЦР анализа, может включать молекулы НК, выбираемые из группы, включающей SEQ ID NO 18 и SEQ ID NO 19, SEQ ID NO 20 и SEQ ID NO 21, SEQ ID NO 22 и SEQ ID NO 23, SEQ ID NO 24 и SEQ ID NO 25, SEQ ID NO 26 и SEQ ID NO 27, SEQ ID NO 28 иNO 61, SEQ ID NO 62 и SEQ ID NO 63, SEQ ID NO 64 и SEQ ID NO 65 и комплементарные им последовательности. Будет понято, что данное изобретение не ограничено использованием пар, упомянутых здесь, так последовательности НК в SEQ ID NO 18, SEQ ID NO 19, SEQ ID NO 20, SEQ ID NO 21, SEQ ID NO 22,SEQ ID NO 23, SEQ ID NO 24, SEQ ID NO 25, SEQ ID NO 26, SEQ ID NO 27, SEQ ID NO 28, SEQ ID NO 29, SEQ ID NO 30, SEQ ID NO 31, SEQ ID NO 32, SEQ ID NO 33, SEQ ID NO 34, SEQ ID NO 35, SEQ IDNO 63, SEQ ID NO 64 и SEQ ID NO 65 могут служить праймерами для ПЦР анализа, указанный ПЦР анализ является этапом в определении устойчивости или восприимчивости свиньи к ЕТЕС. По крайней мере один праймер из пары праймеров может включать последовательность НК или фрагмент последовательности НК, где последовательность НК выбрана из группы, включающей SEQ IDID NO 52, SEQ ID NO 53, SEQ ID NO 54, SEQ ID NO 55, SEQ ID NO 56, SEQ ID NO 57, SEQ ID NO 58,SEQ ID NO 59, SEQ ID NO 60, SEQ ID NO 61, SEQ ID NO 62, SEQ ID NO 63, SEQ ID NO 64 и SEQ ID NO 65. Используемый праймер может включать фрагмент последовательности НК, выбранной из группы,включающей SEQ ID NO 1, SEQ ID NO 2, SEQ ID NO 3, SEQ ID NO 4, SEQ ID NO 5, SEQ ID NO 7, SEQID NO 193, SEQ ID NO 194, SEQ ID NO 195, SEQ ID NO 196, SEQ ID NO 197 и комплементарные им последовательности. Предпочтительные праймеры могут включать фрагмент последовательности НК, выбранной из группы, включающей SEQ ID NO 1, SEQ ID NO 2, SEQ ID NO 3, SEQ ID NO 4, SEQ ID NO 5, SEQ ID NO 7, SEQ ID NO 9, SEQ ID NO 10, SEQ ID NO 11, SEQ ID NO 12, SEQ ID NO 13, SEQ ID NO 14, SEQ ID NO 15, SEQ ID NO 16, SEQ ID NO 17, SEQ ID NO 81, SEQ ID NO 82, SEQ ID NO 83, SEQ ID NO 84, SEQ IDID NO 92, SEQ ID NO 93, SEQ ID NO 94, SEQ ID NO 95, SEQ ID NO 96, SEQ ID NO 97, SEQ ID NO 98,SEQ ID NO 99, SEQ ID NO 100, SEQ ID NO 101. Используемая пара праймеров может включать два праймера, как определено выше. Предпочтительно, один из этих праймеров комплементарен последовательностям упомянутых номеров SEQ ID. В предпочтительном варианте осуществления пары праймеров SEQ ID NO 62 и SEQ ID NO 63 илиSEQ ID NO 64 и SEQ ID NO 65 используются как амплифицированные части MUC4 гена свиньи. Согласно данному изобретению представлен также комплект для определения, является ли свинья гомозиготной, гетерозиготной по аллелю полиморфного участка гена, связанному с устойчивостью к ЕТЕС, или не несущей этот аллель. Указанный комплект содержит первый компонент, выбранный из группы, включающей образец НК, описанный здесь, молекулу НК, описанную здесь, пару ПЦРпраймеров, как описано здесь, рестриктазу и какую-либо их комбинацию.- 11011240 Используемые праймеры могут включить праймеры, описанные здесь, такие как пары ПЦРпраймеров, выбранные из группы, включающей SEQ ID NO 18 и SEQ ID NO 19, SEQ ID NO 20 и SEQ IDNO 60 и SEQ ID NO 61, SEQ ID NO 62 и SEQ ID NO 63, SEQ ID NO 64 и SEQ ID NO 65 и комплементарные им последовательности. Комплект может, кроме того, включать по крайней мере второй компонент, выбранный из группы,состоящей из рестриктазы, рН-буфера, геля, промывного буфера и инкубационного буфера или какойлибо их комбинации. Комплект может, кроме того, включать по крайней мере третий компонент, выбранный из группы,состоящей из рестриктазы, рН-буфера, геля, промывного буфера и инкубационного буфера или какойлибо их комбинации. В следующем аспекте данное изобретение касается способа выведения свиней, устойчивых к ЕТЕС,способ включает:i) отбор первой особи, при этом указанная особь определена как устойчивая к ЕТЕС с использованием способа, описанного здесь; иii) скрещивание указанной первой особи со второй для получения потомства, которое с большей вероятностью будет устойчивым к ЕТЕС по сравнению с потомством, полученным от беспорядочно выбранных родителей. Также способ может быть осуществлен путем скрещивания первой особи, которая идентифицирована как устойчивая к ЕТЕС с использованием метода, описанного здесь, со второй особью. Их потомство будет иметь большую вероятность устойчивости к ЕТЕС по сравнению с потомством, полученным от беспорядочно выбранных родителей. Устойчивость/восприимчивость второй особи свиньи не нуждается в определении. Однако в предпочтительном варианте осуществления вторая особь является выбранной из свиней,которые идентифицированы как устойчивые к ЕТЕС с использованием способа определения, как описано здесь. Согласно данному изобретению может быть эффективным использование физической маркировки свиньи для определения ее устойчивости или восприимчивости к ЕТЕС. Физическая маркировка могла бы включать визуально различимую метку, штрих-код, устройство маркировки, способное передавать информацию об устойчивости/восприимчивости с помощью радиосвязи на приемное устройство. В следующем аспекте данное изобретение касается выделенных молекул НК, описанных здесь, для использования их в качестве антисмысловой НК, иРНК, рибозимов, эндотелинов (ETC) для генетической медицины, генотерапии или кинетопластической репарации ДНК. Согласно данному изобретению также представлен способ производства свинины, включающий этапы i) получение потомства свиньи с лучшей устойчивостью, как описано здесь, и ii) получение мяса от этого потомства. Согласно данному изобретению может быть эффективным использование физической маркировки свиньи для определения ее устойчивости или восприимчивости к ЕТЕС. Физическая маркировка могла бы включать визуально различимую метку, штрих-код, устройство маркировки, способное передавать информацию об устойчивости/восприимчивости с помощью радиосвязи на приемное устройство. В следующем аспекте изобретение касается использования полиморфного участка гена для рассмотрения свиньи как восприимчивой к ЕТЕС, если указанный полиморфный участок гена располагается между маркерами SW2196 и SW225 включительно, на хромосоме 13 свиньи. В практическом варианте осуществления полиморфный участок гена расположен между маркерами SW207 и S0075 включительно. В следующем аспекте данное изобретение касается способа подбора потенциального лекарственного препарата-кандидата для лечения восприимчивости к ЕТЕС. Способ включает следующие этапы:i) селективное тестирование популяции свиней, которые определены восприимчивыми к ЕТЕС, как описано здесь;ii) введение потенциального лекарственного препарата-кандидата тестируемой популяции иiii) оценку эффективности потенциального лекарственного препарата-кандидата на тестируемой популяции. Согласно данному изобретению MUC4 белок свиньи может использоваться как препарат для превращения восприимчивой к ЕТЕС особи в устойчивую. Также данным изобретением представлена смешанная сперма самцов свиньи, включающая сперму по крайней мере двух самцов, при этом указанные самцы определены как устойчивые к ЕТЕС с использованием способа, описанного здесь. Количество самцов, от которых получена смесь, может составлять,например, 3, 4, 5, 6, 7, 8, 10, 12, 15, 20, 25 или 100.- 12011240 Будет понятно, что информацию о присутствии или отсутствии генетического полиморфизма у свиньи удобно заносить в запоминающее устройство. Такую информацию об устойчивости/восприимчивости в системе обработки данных можно использовать, например, при откорме, лечении или выведении свиней. Еще один аспект данного изобретения представляет способ определения, является ли свинья устойчивой или восприимчивой к энтеротоксигенной или энтеропатогенной Е. coli (ЕТЕС), способ включает:i) получение образца от указанной особи, данный образец включает генетический материал;ii) определение в данном образце наличия или отсутствия маркера, связанного с устойчивостью к ЕТЕС; иiii) заключение о том, что свинья является устойчивой к ЕТЕС, если маркер, связанный с устойчивостью ЕТЕС, присутствует в образце. В практическом варианте осуществления изобретения маркер включает один или более компонентов, выбранных из группы, содержащей белок, гормон и полиморфный участок гена. Маркер можно считать присутствующим в образце, если компонент присутствует в образце. Также маркер можно считать присутствующим в образце, если концентрация компонента в образце, например, выше определенного порога, ниже определенного порога, находится в пределах определенного интервала концентрации или вне определенного интервала концентрации. Если маркер включает белок, то этот белок может быть MUC4 белком свиньи или муциноподобным белком свиньи. Белок может также быть белком трансферринового рецептора или белком,активность которого подобна активности белка трансферринового рецептора. Также данным изобретением представлен образец для определения маркера, связанного с устойчивостью к ЕТЕС. Образец может включать связывающий элемент, выбранный из группы, включающей поликлональное антитело, моноклональное антитело, рецептор, лиганд. В предпочтительном варианте осуществления образцом являются антитело или лиганд, специфические для MUC4 белка. Изобретение далее иллюстрируется следующими не ограничивающими примерами и фигурами, где фиг. 1 иллюстрирует карту сцепления, показывая местоположение локусов F4ab/F4ac (жирный шрифт); фиг. 2 показывает сравнительное картирование хромосомы 13 свиньи (SSC13) и хромосомы 3 человека (HSA3) с ВАС последовательностями; фиг. 3 показывает сравнительную карту между SSC13 и HSA3 с использованием результатов картирования в этой заявке; фиг. 4 иллюстрирует контиг последовательностей MUC4 ЕВАС свиньи; фиг. 5 иллюстрирует статус секвенирования вместе с информацией об однонуклеотидном полиморфном участке гена с использованием муцин 4 гена человека как каркаса. Выровненные последовательности свиньи обозначены жирными линиями над экзонами, вертикальные полоски обозначают экзоны; фиг. 6 показывает последовательность, включающую XbaI полиморфный участок (SEQ ID NO 67). Однонуклеотидный полиморфный участок аллеля устойчивости показан жирным шрифтом с подчеркиванием; и фиг. 7 показывает последовательность, включающую XbaI полиморфный участок (SEQ ID NO 68). Однонуклеотидный полиморфный участок аллеля восприимчивости показан жирным шрифтом с подчеркиванием. Примеры Пример 1. Идентификация гена, ответственного за устойчивость к диарее, вызванной штаммами Е.coli ETEC F4ab/F4ac. 1.1. Введение. Для того чтобы охарактеризовать ген, ответственный за устойчивость к диарее, вызванной Е. coliF4ab/F4ac, решили основываться на так называемой стратегии "позиционного клонирования генакандидата" (Collins 1995). Отправной точкой служило исследование, описанное Edfors-Lilja и сотрудниками в 1995 г. Это исследование было значительно расширено с помощью увеличения плотности ДНКмаркера на карте сцепления хромосомы 13 свиньи (SSC13) в той же родословной межпородного скрещивания, которая использовалась в работе Edfors-Lilja. Кроме того, было уточнено картирование гена в области хромосомы, в которой локализован ген устойчивости к ETEC F4ab/F4ac. Далее работа описывает, что было выполнено для идентификации генов-кандидатов и что привело к идентификации полиморфных участков в гене-кандидате, показывающем сильное неслучайное распределение с ЕТЕС F4ab/F4ac статусом у свиней. 1.2. Анализ групп сцепления. Животные. При анализе групп сцепления мы использовали родословную, описанную Edfors-Lilja и др. (1995). Родительское поколение включало двух самцов европейской дикой свиньи, каждого из которых скрещивали с четырьмя свиноматками шведского йоркшира. Поколение F1 скрестили (четыре самца и 22 самки)- 13011240 и получили 200 свиней поколения F2. Чтобы получить больше близкородственных семейств, скрещивания повторили, и в результате родилось две партии потомства. Тест на адгезию. Эпителиальные клетки верхней части тонкой кишки были получены при забое животных. Тест на адгезию выполнили путем инкубирования эпителиальных клеток со штаммами Е. coli F4ab и Е. coli F4ac соответственно. Образцы, содержащие 10-20 клеток, были исследованы микроскопией по методу интерференционного контраста на адгезию обоих штаммов и Е. coli F4ab и Е. coli F4ac. Результаты оценили по 4-балльной шкале, где 1 - нет бактерий и 4 - бактерии слоем покрыли все клетки (Edfors-Lilja и др., 1996). Генотипирование. Микросателлитные маркеры (т.е. маркеры, у которых ядром является тандемно повторяющаяся последовательность обычно двух или небольшого количества нуклеотидов, если различные аллели отличаются наличием различного числа повторений) использовались как генетические маркеры для сцепленного картирования. В данной работе 60 микросателлитных маркеров хромосомы 13 свиньи (SSC13) были выбраны из карты сцепления департамента сельского хозяйства США (USDA) (Rohrer и др., 1996;http://www.marc.usda.gov/). Один ПЦР-праймер от каждого из этих 60 маркеров был флуоресцентно мечен либо 6-FAM, HEX,либо ТЕТ (Applied Biosystems, Foster City, CA, USA), и полимеразная цепная реакция (ПЦР) была выполнена в РЕ 9600 термоблоке для проведения реакций (Applied Biosystems, Foster City, CA, USA) или в АВ 1877 (Applied Biosystems, Foster City, CA, USA) с использованием реакционного объема 10 мкл, содержащего 25 нг геномной ДНК, 1 ПЦР буфера, 1,5-2,0 мМ MgCl2, 200 мкМ каждого дезоксирибонуклеозидтрифосфата (дНТФ), 0,35 мкМ каждого праймера, и 0,25 единиц полимеразы ДНК AmpliTaq Gold(Applied Biosystems, Foster City, CA, USA). Условия в термоблоке для проведения реакций были следующие: предварительная денатурация в течение 10 мин при 95 С с последующими 10 циклами с уменьшением температур отжига (15 с при 95 С, 30 с при 64-55 С, 60 с при 72 С), 25 циклов реакции с фиксированной температурой отжига (15 с при 89 С, 30 с при 55 С, 60 с при 72 С), и удлинение при 72 С до 1 ч. ПЦР-продукты были загружены в 4,25% полиакриламидный денатурирующий градиентный гель и налиты в ABI PRISM 377 ДНК секвенатор. ПЦР-продукты проанализировали с использованием программы GeneScan 2 (Applied Biosystems, Foster City, CA, USA). Хорошо амплифицированные маркеры,которые легко оценивались и показывали гетерозиготность в поколении F1, были отобраны для сцепленного картирования у всех 236 животных. В алфавитном порядке перечислены следующие используемые маркеры: СР, EST24F05, PR39, S0075, S0076, S0215, S0219, S0222, S0281, 50282, 50291, SW1030, SW1056,SW1864, SW1898, SW207, SW2196, SW225, SW2412, SW398, SW458, SW698, SW769, SW864, SW873,SW882, SW937, SW955, SWR1008, SWR428, SWR926 и TF. Детальные описания генетических маркеров можно найти на веб-сайте USDA Исследовательского центра животноводства (http://www.marc.usda.gov/) и в базе данных генома свиньи(http://www.thearkdb.org/pig). Аллели были определены и данные генотипирования были обработаны с использованием программы GEMMA (Iannuccelli, 1996). Данные генотипирования использовались для построения карты сцепления SSC13. Анализ сцепления был выполнен с использованием CRIMAP версия 2,4 (Green и др., 1990). Первоначально опция TWOPOINT использовалась для обнаружения сцепления между маркерами с LODбаллом выше чем три. Впоследствии использовалась опция BUILD для построения карты структуры, и остальные маркеры были включены с использованием опции ALL. Наконец, генотипы были проверены с использованием опции CHROMPIC, и данные тщательно исследовались на предмет каких-либо маловероятных парных рекомбинант. Результаты карты сцепления показаны в табл. 1. Если данные для локуса F4ab/F4ac (местоположение гена, отвечающего за устойчивость/восприимчивость к болезни, вызванной штаммом ETEC F4) добавляются, то наиболее вероятно этот локус близко расположен к S0075, и это подтверждается LOD-баллом, равным 1,91, по сравнению со следующим лучшим размещением, где ETEC F4ab/F4ac локус расположен далеко от S0075. В результате анализа сцепления установлено, что F4ab/F4ac расположен в CEN-SW207-F4ab/F4ac-S0075-TEL. Карта сцепления, на которой показано положение F4ab/F4ac, представлена на фиг. 1. 1.3. Цитогенетическое картирование. Чтобы получить физическую карту области, в которой расположен ген, ответственный за устойчивость к диарее, вызванной Е. coli F4ab/F4ac, использовались микросателлитовые маркеры, ограничивающие локус F4ab/F4ac, использовались для скрининга библиотеки ВАС последовательностей свиньи (Андерсон и др., 2000). Библиотека ВАС последовательностей свиньи является собранием больших фрагментов геномной ДНК свиньи (средний размер = 150000 пар нуклеотидов), где каждый фрагмент поддерживается в бактериальной искусственной хромосоме (ВАС), клонирующей вектор, иммортализован- 15011240 ный в клоне бактерии Е. coli. В данном исследовании PigEBAC библиотека (ВАС библиотека генома свиньи) (Рослин), которая состоит приблизительно из 100000 независимых ВАС клонов, хранится в виде индивидуальных клонов в 96-луночных и 384-луночных микропланшетах. Эта библиотека представляет приблизительно пять зон генома свиньи. ВАС клоны были идентифицированы с использованием ПЦР праймеров от маркеровSW207, S0283, S0075, SW1876 и SW225 на ДНК пулах ВАС клонов. ДНК была выделена из маркер-позитивных ВАС клонов с использованием комплекта из приборов и препаратов для элюции ДНК (Квиаген, Германия), ВАС последовательности были индивидуально мечены биотин-14-дАТФ или дигоксигенин-11-дУТФ (Boehringer-Mannheim, Германия) для одноцветной и двуцветной флуоресцентной гибридизации (FISH) с метафазными хромосомами и интерфазными ядрами свиньи (как описано Chowdhary и др., 1995). Физический порядок маркеров был показан в соответствии с данными карты сцепления, а именноCEN-SW207-S0283-50075-SW1876-SW225-TEL. ВАС содержащие маркеры SW207, S0283 и S0075 были гибридизированы с зоной q41 хромосомы 13 свиньи, что указывает на то, что данная область является кандидатной. Праймеры для амплификации упомянутых маркеров внесены в табл. 2. Таблица 2. Последовательности по изобретению 1.4. Сравнительное картирование. Для облегчения поиска гена, ответственного за устойчивость к диарее, вызываемой Е. coliF4ab/F4ac, было решено использовать обширное количество информации о последовательности, представленной последовательностью полного генома человека. Чтобы использовать эту информацию, было выполнено сравнительное картирование генов на соответствующих частях хромосомы 13 свиньи (SSC13) и хромосомы 3 человека (HSA3). Рассматриваемые с помощью ДНК FISH анализа ВАС последовательности были перенесены с использованием Sau3AI, и фрагменты были заключены в BamHI сайт pUC19 и трансформированы в XL1BLUE клетки Epicurian coli (Стратаген). Трансформанты поместили на чашки Петри со средой LB, содержащей ампициллин, и произвольно отобрали приблизительно 100 субклонов. Плазмидную ДНК выделили из субклонов с использованием комплекта из приборов и препаратов для элюции ДНК (Квиаген,Германия). Вставки, клонированные в плазмидных векторах, были секвенированы с использованием Т 3 и Т 7 праймеров и BigDye терминатором секвенирования (Applied Biosystems, Foster City, CA, USA) и подвержены электрофорезу на ABI377 (Applied Biosystems, Foster City, CA, USA). Полученные последовательности были введены в программу BLAST в базе данных с неповторяющимися нуклеотидными последовательностями на NCBI веб-сайте (http://www.ncbi.nim.nih.gov/). Гены, идентифицированные при шот-ган-секвенировании (пулеметное секвенирование) ВАС последовательностей, помещены в табл. 3. Данные по геному человека были взяты из базы данных Entrez Genome, представленной наhttp://www.ncbi.nlm.nih.gov/cgi-bin/Entrez/mapsearch. Особенности генов человека (например, TRAD),обнаруженные при исследованиях базы данных последовательности ДНК, можно найти на нескольких веб-сайтах, включая (LOCUSLINK на http://www.ncbi.nim.nih.gov/ и Ensembl на http://www.ensembl.org/). Следует помнить, что SSC13 является хромосомой 13 свиньи и что HSA3 является хромосомой 3 человека. Основываясь на совмещениях последовательностей, полученных от ВАС клонов свиньи, и последовательности человеческого генома, составили сравнительную карту SSC13 и HSA3, см. фиг. 2. 1.5. Сравнительное детальное картирование. Для дальнейшего улучшения сравнительной карты SSC13 и HSA3, были отобраны последовательности, полученные шот-ган-секвенированием, которые показали сходство с KIAA0804, TRAD и SEC22A. Кроме того, маркерные экспрессирующиеся последовательности (EST), спрогнозированные для нанесения на карту SSC13 на основании подобия последовательности генам и маркерным экспрессирующимся последовательностям, известным для нанесения на карту гомологичной хромосоме человека (HSA3),были отобраны из ресурса коротких маркерных экспрессирующихся последовательностей кишечника свиньи (Winter и др., 1996; Winters и Fredholm, неопубликовано). Критериями выбора при использовании BLAST-поиска в базе данных с неповторяющимися нуклеотидными последовательностями служило то, что 5' концы последовательностей ДНК соответствующих клонов имели существенную идентичность последовательности (ожидаемое значение е-6) с ортологическими генами человека. Праймеры были предназначены для 3' нетранслируемой области (3'UTR) отобранных клонов (см. табл. 4), чтобы увеличить специфичность свиньи. Использовали веб-сайт Праймер 3 на http://wwwgenome.wi.mit.edu/cgi-bin/primer/primer3www.cgi (Rozen и Skaletsky, 2000) для разработки праймеров. Для определения зон и картирования использовались гибридный набор соматических клеток свиньи(Yerle и др., 1996) и гибридный радиационный набор клеток свиньи (IMpRH) (Yerle и др., 1998). Условия ПЦР были отработаны с использованием геномной ДНК свиньи, мыши и хомяка. ПЦР выполняли на 10 и 25 нг ДНК от каждой гибридной линии для соматических и радиационных наборов клеток соответственно. Условия ПЦР: 0,35 М каждого праймера, от 2 до 4 мМ Mg2+ и 0,05 единиц маркера "горячего старта"(Квиген, Германия) в 10 М реакционного объема, в течение 35 циклов с касанием (TD) 60 или 64. ПЦР выполняли с использованием 15-минутной предварительной денатурации при 95 С и последующей денатурации при 95 С в 15-секундных дополнительных циклах. Удлинение было выполнено при 72 С в течение 1 мин. Касание было выполнено при понижении температуры отжига на 1 С после каждого цикла в первых 10 циклах, старт - при 64 или 60 С для TD64 и TD60 соответственно. Последние 25 циклов были выполнены при температуре отжига 54 или 50 С для TD64 и TD60 соответственно. Продукты амплификации растворили в 2%-ных гелях агарозы и вручную пометили. Результаты ПЦР были непосредственно введены в программы анализа данных SCH и RH наhttp://www.toulouse.inra.fr/lgc/pig/pcr/pcr.htm и http://imprh.toulouse.inra.fr/ соответственно. Определение зон осуществили, используя компьютерную программу, разработанную Chevalet и др. (1997). Результаты радиационного гибридного продукта ПЦР проанализировали методом картирования IMpRH, разработанным Миланом и др. (2000). Гены и их расположение показаны в табл. 4. Сравнительная карта SSC13 и HSA3, в которой использованы результаты табл. 4, показаны на фиг. 3. Когда данные сравнения, о которых сообщали ранее, добавили (Sun и др., 1999; Van Poucke и др.,1999, Pinton и др., 2000, Van Poucke и др., 2001) к данным, полученным в данном исследовании, была составлена обширная карта сравнения SSC13 и HSA3. Если масштабировать изображение кандидатной области (SCC13q41), становится очевидным, что кандидатными областями в HSA3 являются q21 и q28qtel.- 27011240 1.6. Гены-кандидаты. При просмотре литературы по вопросу о возможных генах-кандидатах для ЕТЕС F4ab/F4ac статуса у свиней нашли несколько сообщений о белках, связанных с восприимчивостью к ЕТЕС F4ab/F4ac (Metcalfe и др., 1991; Grange и Mouricout, 1996; Francis и др., 1998; Grange и др., 1998). Одно из сообщений указывает на то, что это гликопротеин 74 кДа, который принадлежит к трансферриновому семейству(Grange и Mouricout, 1996), другое сообщение представляет гликопротеины 40 кДа (Metcalfe и др., 1991) и более поздние - сообщают о сиалогликопротеидах муцинового типа (Francis и др., 1998; Grange и др.,1998). При рассмотрении этих сообщений, стало очевидным, что поиск гена должен концентрироваться или на трансферрин-подобных генах или на муцин-подобных генах. Когда данные сцепления и сравнения добавили, то один ген из кандидатных областей HSA3, а именно Муцин 4 (MUC4) в Hsa3q29, проявился как позиционный кандидат. Таблица 4. Список генов, выбранных для картирования гибридной клетки Пример 2. Клонирование MUC4 гена свиньи. 2.1. Скрининг ВАС последовательностей, содержащих MUC4 ген. Для того чтобы доказать, действительно ли MUC4 ген является геном, ответственным за устойчивость к диарее, вызываемой Е. coli ETEC F4ab/F4ac, большие участки гена были клонированы и секвенированы. Плазмида S1325, содержащая фрагмент ПЦР расы 3229 bp MUC4 кДНК человека (Moniaux и др.,1999), была получена по методике профессора J.Р. Aubert. Фрагмент синтезировали с использованием полной РНК слизистой оболочки толстого кишечника человека. Для синтеза первой цепи кДНК с 1 г РНК применяли Advantage RT-комплект препаратов и приборов для ПЦР (Clontech, Heidelberg, Германия), используя олиго (dT)-якорный праймер 5'/3'-набора хромосомных рас (Boehringer Mannheim, RocheDiagnostics, Meylan, Франция). Удлинение считывания при ПЦР было выполнено с применением системы считывания ПЦР (Boehringer Mannheim) со смысловым праймером NAU 491 (5'AGCAGGCCGAGTCTTGGATTA-3', SEQ ID NO 50) и ПЦР якорным праймером 5'/3'-набора хромосом- 28011240 ных рас в качестве антисмыслового праймера. Реакционная смесь ПЦР амплификации (50 l) содержала 5 l кДНК, 10 мМ натрия дезоксирибонуклеозидтрифосфата, 0,4 l каждого праймера, 5 l 10 буфераExpand шаблона считывания при ПЦР 3, 0,75 мМ MgCl2 и 2,5 единицы ферментной смеси. ПЦР выполнили с использованием Perkin-Elmer Thermal Cycler Gene Amp ПЦР системы 9700. Условия ПЦР: 94 С в течение 2 мин, последующие 30 циклов при 94 С по 30 с, отжиг при 60 С в течение 45 с и элонгации при 71 С в течение 4 мин, в 20 последних циклах продлили время элонгации на 40 с для каждого нового цикла, за которыми следовала заключительная элонгация при 71 С в течение 15 мин. Гнездовая ПЦР была выполнена с использованием NAU 483 (5'-CTGTTTCTCTACCAGAGCGGT-3', SEQ ID NO 51) и ПЦР-якорного праймера. Продукт амплификации подвергли электрофорезу на 1% ТВЕ (1 ТВЕ=45 мМ трис-борат 1 мМ этилендиаминтетрауксусной кислоты (ЭДТА агарозном геле со следами бромида этидия. Полоску срезали, очистили с помощью комплекта QIAquick Gel Extraction (Квиген) и субклонировали в комплекте Original ТА Clonings (Invitrogen, Leek, Нидерланды). Вставку очистили и произвольно пометили с использованием 32 Р-2'диоксицитидин 5'-трифосфата. После промывания на сетчатых фильтрах высокой плотности ВАС библиотека свиньи (Anderson и др., 2000), предоставленная Британским Центром HGMP Ресурсов (htlp://www.hgmp.mrc.ac.uk/geneservice/reagents/products/descriptions/ pigBAC.shtml), была гибридизирована с образцом MUC4 человека. Четыре позитивных ВАС клона выбрали и внесли в табл. 5. Таблица 5. Mucin 4 позитивные ЕВАС клоны 2.2. Контиг MUC4 Е ВАС клонов свиньи. Концы четырех MUC4 PigE ВАС клонов вместе с субклонами от каждого из четырех MUC4 PigE ВАС клонов секвенировали с применением BigDye терминаторного окрашивания и получили маркированные сайты последовательности. Маркированные сайты последовательности внесли в табл. 6. Таблица 6. Маркированные сайты последовательности,используемые для ВАС контига Это позволило частично определить, как ВАС клоны перекрываются. Контиг показан на фиг. 4. По ВАС концу последовательности показали, что PigEBAC250fl6 содержит 5'-конец MUC4 гена.PigEBAC 53fl4 и 222b07, содержащие ген, расположенный выше по цепи от MUC4, а именно АСK1, и таким образом, эти клоны - хорошие кандидаты, содержащие полную геномную MUC4 последовательность свиньи. Из-за меньшего размера клон 222b07 был выбран для дальнейшего секвенирования. 2.3. Шот-ган секвенирование PigEBAC222b07. ВАС ДНК приготовили с применением комплекта Qiagen Large-construct (Квиген, Германия), и ВАС ДНК субклонировали с применением комплекта ТОРО для шот-ган субклонирования (Invitrogen,CA, USA). Клоны поместили в чашки со средой LB, содержащей ампициллин, 1536 клонов были отобраны на четыре 384-луночных микропланшета. Плазмиды приготовили с использованием комплекта препаратов и приборов для элюции плазмидных ДНК (Квиген, Германия). Вставки секвенировали с использованием Т 3 и Т 7 праймеров и BigDye терминаторной последовательности (Applied Biosystems, Foster City, CA,USA) и подвергли электрофорезу на АВ 13100 (Applied Biosystems, Foster City, CA, USA). В полученных полосах определили основания и качественно проверили с использованием программы PHRED (Ewing и др., 1998), векторные последовательности определили с использованием методаCROSS MATCH (http://www.phrap.org/), последовательности собрали в контиги с использованием программы PHRAP (http://www.phrap.org/) и рассмотрели с применением программы CONSED (Gordon и др.,1998). Все полученные последовательности (т. е. контиги и синглет) были найдены с помощью програм- 29011240 мы BLAST в базе данных неповторяющихся нуклеотидных последовательностей на NCBI веб-сайте(http://www.ncbi.nlm.nih.gov/). Кроме того, выполнили FASTA33 поиск с использованием MUC4 геномных последовательностей человека (Регистрация в ГенбанкеAJ430032, AJ430033, AJ430034). Около 1200 субклонов секвенировали, и последовательности от всех 25 экзонов MUC4 свиньи идентифицировали сравнением последовательностей MUC4 генов свиньи и человека. Имеется полная информация о последовательностях всех экзонов, кроме экзонов 1 и 25. Кроме того, имеется информация о последовательностях всех нитронов, кроме нитронов 1, 11, 14, 16, 19 и 24 (см. табл. 2 "Последовательности по изобретению"). Пример 3. Идентификация полиморфных участков гена MUC4, связанных с устойчивостью к диарее, вызванной Е. coli ETEC F4ab/F4ac. Чтобы идентифицировать возможные генетические вариации в MUC4 гене свиньи, который связан с устойчивостью к диарее, вызванной Е. coli ETEC F4ab/F4ac, использовалась информация о последовательностях, полученная в примере 2. После получения последовательностей экзонов 4 и 8 были намечены следующие ПЦР-праймеры:SSMUC4ex8L: 5'-CGA TAC TTC TCC CAC ACT GG (SEQ ID NO 61). Используя эти праймеры на геномной ДНК свиньи, получили ПЦР продукт длиной приблизительно 4 т.п.н. с помощью Элонгазы (Invitrogen, CA, USA). Предварительную денатурацию осуществили при 94 С в течение 2 мин, затем 35 циклов при 94 С в течение 30 с, при 60 С в течение 1 мин при 68 С в течение 10 мин. После амплификации различные рестриктазы были проверены на амплифицированных фрагментах, полученных от животных, у которых известен F4ab/F4ac генотип, и обнаружен полиморфный участок XbaI. 3.1. Анализ сцепления с MUC4 геном. Родословная, которая используется в анализе сцепления, генотипирована для полиморфного участка XbaI, и показана полная сегрегация с F4ab/F4ac. Многоточечный анализ жестко ограничил MUC4 в интервале между Sw207 и S0075, не показывая рекомбинацию с локусом F4ab/F4ac. 3.2. Неустойчивость сцепления. У 10 родительских животных, 18 хромосом родословной которых картирована, известен F4ab/F4ac статус (т.е. хромосомная область известна как восприимчивая или как устойчивая). Гаплотипы, окружающие F4ab/F4ac локус, показывают максимально неустойчивое сцепление с MUC4. Вероятность этого наблюдения по точному критерию Фишера составляет Р=0,00005. Ни один из других маркеров в области не показывает такую же степень неустойчивости сцепления. 3.3. РТ-ПЦР (реакция обратной транскрипции-полимеразная цепная реакция). Комплементарная ДНК синтезировалась на РКН, выделенной от ткани слизистой оболочки тонкой кишки, подвздошной кишки и толстой кишки. SSMUC4ex4U/SSMUC4ex8L праймеры использовали в ПЦР на 5 нг кДНК из различных тканей в общем объеме 20 l с 1 ПЦР буфером, 200 М каждого дезоксирибонуклеозидтрифосфата, 0,4 М каждого праймера и 0,25 единиц маркера "горячего старта" (Квиген, США). Термоциклирование вьшолняли с 15-минутной начальной денатурацией при 95 С и затем при 95 С в течение 15 с в дополнительных циклах. Удлинение выполняли при 72 С в течение 1 мин. Касание выполняли понижением температуры отжига на 1 С после каждого цикла в первых 10 циклах, начальный цикл при 60 С. Последние 25 циклов выполняли при температуре отжига 50 С. Электрофорез в 2%-ом агарозном геле показал в РТ-ПЦР продукте приблизительно 600 пар оснований во всех трех тканях. Результат четко показал, что Mucin 4 экспрессирован в тонкой кишке, подвздошной кишке и толстой кишке свиней. 3.4. Характеристика полиморфных участков XbaI. С помощью ПЦР и секвенирования продуктов ПЦР получили геномные последовательности с известными F4ab/F4ac генотипами в используемой родословной. Обнаружили семнадцать полиморфных участков в геномной последовательности MUC4 гена. В области от экзона 5 до экзона 8 описаны дваMUC4-гаплотипа, которые отличаются по крайней мере 14 отдельными нуклеотидными заменами и 6 делениями пар оснований. Один из этих гаплотипов совместим с аллелем устойчивости к диарее, вызываемой Е. coli F4ab/F4ac, а другой гаплотип - с восприимчивостью к диарее, вызываемой Е. coliF4ab/F4ac, в данном материале. На фиг. 5 показан статус текущего секвенирования с использованием геномной организации MUC4 человека как каркаса. В табл. 7A-D показаны различия между двумя гаплотипами.
МПК / Метки
МПК: C12Q 1/68, A01K 67/02
Метки: энтеротоксикогенной, молекула, участка, выделенная, аллель, способы, гена, нуклеиновой, полиморфного, устойчивостью, свиньи, кислоты, связанного, содержащая, coli, применения
Код ссылки
<a href="https://eas.patents.su/30-11240-vydelennaya-molekula-nukleinovojj-kisloty-soderzhashhaya-allel-polimorfnogo-uchastka-gena-svini-svyazannogo-s-ustojjchivostyu-k-enterotoksikogennojj-e-coli-i-sposoby-ee-primeneniya.html" rel="bookmark" title="База патентов Евразийского Союза">Выделенная молекула нуклеиновой кислоты, содержащая аллель полиморфного участка гена свиньи, связанного с устойчивостью к энтеротоксикогенной e. coli, и способы ее применения</a>
Предыдущий патент: Конъюгаты aβ иммуногенных пептидных носителей и способы их получения
Следующий патент: Новые производные 4-бензилиденпиперидина
Случайный патент: Гранулированный взрывчатый материал (варианты)