Бензоилпиразолы, их применение в качестве гербицидов и промежуточные вещества
Номер патента: 15425
Опубликовано: 31.08.2011
Авторы: Ичихара Теруюки, Диттген Ян, Накамура Шин, Розингер Кристофер, Хилльс Мартин, Кене Хайнц, Фойхт Дитер, Укава Сейджи, Нарабу Шиничи, Янаги Акихико, Ёнета Язуши, Ширакура Шиничи
Формула / Реферат
1. Бензоилпиразолы, представленные формулой (I)
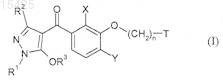
где R1представляет собой C1-С6-алкил;
R2 представляет собой C1-С6-алкил или С3-С7-циклоалкил;
R3 представляет собой водород, C1-С6-алкил, С3-С7-алкенил, С3-С7-алкинил, С7-С12-аралкил, C1-С6-алкилсульфонил, необязательно C1-С6-алкилзамещенный фенилсульфонил, C1-С6-алкилкарбонил, бензоил или бензоил-C1-С6-алкил;
X представляет собой галоген или C1-С6-алкил;
Y представляет собой галоген;
n имеет значение 2 или 3 и
Т представляет собой группу Т1
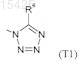
или группу Т2
![]()
где R4представляет собой водород, C1-С6-алкил, C1-С6-алкокси или C1-С6-алкилтио.
2. Соединение по п.1, в котором
R1 представляет собой метил или этил;
R2 представляет собой метил, этил или циклопропил;
R3 представляет собой водород, метилаллил, пропаргил, бензил, метансульфонил, н-пропансульфонил, необязательно метилзамещенный фенилсульфонил, ацил, бензоил или фенацил;
X представляет собой хлор, бром или метил;
Y представляет собой хлор или бром;
n имеет значение 2 или 3 и
Т представляет собой группу Т1
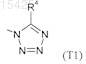
или группу Т2
![]()
где R4представляет собой водород, метил, этил, метокси или метилтио.
3. Гербицид, содержащий в качестве активного ингредиента соединение по п.1 или 2.
4. Соединение, представленное формулой (II)
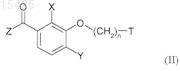
где X1, Y, n и Т имеют указанное в п.1 или 2 значение и
Z представляет собой группу

где R1 и R2имеют указанное в п.1 или 2 значение.
Текст
ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ЕВРАЗИЙСКОМУ ПАТЕНТУ Дата публикации и выдачи патента Предложены бензоилпирадозолы, представленные следующей формулой (I), и их применение в качестве гербицидовR3 представляет собой водород, C1-С 6-алкил, С 3-С 7-алкенил, С 3-С 7-алкинил, С 7-С 12-аралкил, C1-С 6 алкилсульфонил, необязательно C1-С 6-алкилзамещенный фенилсульфонил, C1-С 6-алкилкарбонил,бензоил или бензоил-C1-С 6-алкил; Х представляет собой галоген или C1-С 6-алкил; Y представляет собой галоген; n имеет значение 2 или 3 и Т представляет собой приведенную выше группу (Т 1) или (Т 2), где R4 представляет собой водород, C1-С 6-алкил, C1-С 6-алкокси или C1-С 6-алкилтио.(71)(73) Заявитель и патентовладелец: БАЙЕР КРОПСАЙЕНС АГ (DE) 015425 Область техники Настоящее изобретение относится к новым бензоилпиразолам, их применению в качестве гербицидов, способу их получения и их новым промежуточным веществам. Предшествующий уровень техники Ранее было известно, что некоторые виды бензоилпиразолов демонстрируют действие, как гербициды (например, РСТ Международные публикации WO 03/66607, WO 01/10850 и WO 01/53275). Раскрытие изобретения Однако соединения, раскрытые в указанных выше публикациях, не в полной мере удовлетворяют требованиям с точки зрения их эффективности в качестве гербицидов и/или их безопасности. Авторы данного изобретения провели интенсивные исследования с целью создания новых соединений, имеющих повышенную эффективность в качестве гербицидов и являющихся безопасными. В результате, авторы настоящего изобретения нашли новые бензоилпиразолы, представленные формулой,приведенной ниже, которые демонстрируют превосходную гербицидную активность и безопасность по отношению к зерновым культурам. Бензоилпиразолы представлены формулой (I)X представляет собой галоген или C1-С 6-алкил;n имеет значение 2 или 3 и Т представляет собой группу (Т 1) где R4 представляет собой водород, C1-С 6-алкил, C1-С 6-алкокси или C1-С 6-алкилтио. Соединения вышеуказанной формулы (I) по настоящему изобретению могут быть синтезированы,например, с помощью способов получения (а) или (b), приведенных ниже. Способ получения (а): соединения формулы (I), где R3 представляет собой водород. Способ перегруппировки соединений, представленных формулой (II) где R1, R2, X, Y, n и Т являются такими, как определено выше, с соединениями, представленными формулой (III) где R3 является таким, как определено выше, и L представляет собой галоген. Бензоилпиразолы формулы (I), представляемые настоящим изобретением, имеют более высокую гербицидную активность, чем соединения, описанные в упомянутых выше документах из уровня техники, в то же время демонстрируют в наивысшей степени превосходную действенность в качестве селективных гербицидов, по существу, без фитотоксичности по отношению к зерновым культурам. В частности, бензоилпиразолы формулы (I) демонстрируют в наивысшей степени превосходную действенность в качестве гербицидов для бобовых культур засушливых областей, таких как соевые бобы, и для злаковых культур засушливых областей, таких как пшеница, ячмень, овес и кукуруза. Таким образом, бензоилпиразолы формулы (I) по настоящему изобретению являются особенно применимыми в качестве гербицидов для засушливых областей. Лучший вариант осуществления изобретения. В настоящем описании термин "галоген" означает фтор, хлор, бром или йод, предпочтительно хлор и бром. Термин "алкил" может являться линейной или разветвленной цепью и означает C1-С 6-алкил. В особенности, примеры "алкила" включают метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил, н-,изо-, нео- или трет-фенил, н- или изогексил и т.п. Примеры "С 3-С 7-циклоалкила" включают циклопропил, циклобутил, циклопентил, циклогексил,циклогептил и т.п. Примеры "С 3-С 7-алкенила" включают аллил, 1-метилаллил, 1,1-диметилаллил, 2-бутенил, 2 пентенил, 2-гексенил, 2-гептенил и т.п. Примеры "С 3-С 7-алкинила" включают этинил, 2-пропинил, 1-метил-2-пропинил, 1,1-диметил-2 пропинил, 2-бутинил, 2-пентинил, 2-гексинил, 2-гептинил и т.п. Термин "С 7-С 12-аралкил" означает, например, аралкильную группу, алкильная часть которой имеет упомянутые выше значения, и "арил" означает, например, фенил, нафтил и т.п., в особенности бензил. Термин "C1-С 6-алкокси" означает, например, алкил-О-группу, алкильная часть которой имеет упомянутые выше значения, и может представлять собой, например, C1-С 6-алкокси. В особенности, примеры"алкокси" включают метокси, этокси, н- или изопропокси, н-, изо-, втор- или трет-бутокси, н-пентилокси,н-гексилокси и т.п. Термин "C1-С 6-алкилтио" означает алкил-S-группу, алкильная часть которой имеет упомянутые выше значения, и может представлять собой, например, C1-С 6-алкилтио. В особенности, примеры"алкилтио" включают метилтио, этилтио, н- или изопропилтио, н-, изо-, втор- или трет-бутилтио,н-пентилтио, н-гексилтио и т.п. Термин "алкилсульфонил" означает алкил-SO2-группу, алкильная часть которой имеет упомянутые выше значения, и может представлять собой, например, C1-С 6-алкилсульфонил. В особенности, примеры"Ацил" представляет собой ацильную группу, производную насыщенной алифатической монокарбоновой кислоты или алифатического или ароматического углеводородного кольца карбоновой кислоты и означает, например, C1-С 6-алкил-СО-группу, алкильная часть которой имеет упомянутые выше значения, или арил-СО-группу, арильная часть которой такая, как определено выше. В особенности, примеры"Ацилалкил" представляет собой ацилалкильную группу, ацильная и алкильная части которой имеют упомянутые выше значения и означают, например, бензоил-С 1-С 6-алкилгруппу, в особенности включают фенацил и т.п. Предпочтительная группа соединений по настоящему изобретению включает соединения формулыX представляет собой галоген или C1-С 6-алкил; где R4 представляет собой водород, C1-С 6-алкил, C1-С 6-алкокси или C1-С 6-алкилтио. Более предпочтительная группа соединений по настоящему изобретению включает соединения формулы (I), гдеR1 представляет собой метил или этил;Y представляет собой хлор или бром; где R4 представляет собой водород, метил, этил, метокси или метилтио. При использовании, например, 5-2,4-дихлор-3-[2-(1 Н-тетразол-1-ил)этилокси]бензоилокси-1,3 диметилпиразола, цианогидрина ацетона в качестве цианида и триэтиламина в качестве основания упомянутый выше способ получения (а) представлен следующей реакционной схемой: При использовании, например, 4-2,4-дихлор-3-[2-(1 Н-тетразол-1-ил)этилокси]бензоил-1,3 диметил-5-гидроксипиразола, бромида бензила и карбоната калия в качестве связывающего кислоту реагента упомянутый выше способ получения (b) представлен следующей реакционной схемой: Соединения формулы (I) по настоящему изобретению могут существовать в виде таутомеров, R3 представляет собой водород, как показано с помощью следующих формул (Ia)-(Ic): Соединения формулы (II), используемые в качестве исходных веществ в описанном выше способе получения (а), представляют собой новые соединения, не описанные в литературе из уровня техники. Они могут быть получены в соответствии со способами, описанными, например, в публикации 2-173 не прошедшей экспертизу японской заявки на изобретение (Japanese Patent KOKAI Publication No. 2-173)"JP-A-"), WO 93/18031 и т.п. А именно, они могут быть получены реакцией соединений, представленных формулой (IV) где Z является таким, как определено выше, с соединениями, представленными формулой (V) где X, Y, n и Т являются такими, как определено выше, и Hal представляет собой галоген, предпочтительно хлор или бром, в присутствии подходящего связывающего кислоту реагента, например триэтиламина, и подходящего разбавителя, например дихлорметана. Соединения, представленные упомянутой выше формулой (IV), сами по себе известны и могут быть получены в соответствии со способами, описанными в литературе, например JP-A-61-257974, JP-A-10109976 и т.п. Часть соединений, представленных упомянутой выше формулой (V), являются новыми соединениями, не описанными в литературе из уровня техники, и могут быть получены в соответствии со способами, описанными в литературе, например JP-A-2-173, WO 93/18031, WO 03/66607 и т.п. А именно, они могут быть получены реакцией соединений, представленных формулой (VI) где X, Y, n и Т являются такими, как описано выше, с галогенирующим реагентом, таким как, например,оксихлорид фосфора, оксибромид фосфора, трихлорид фосфора, трибромид фосфора, фосген, оксалил дихлорид, тионил хлорид и тионил бромид. Часть соединений, представленных упомянутой выше формулой (VI), представляют собой новые соединения, не описанные в предшествующей литературе, и могут быть получены в соответствии со способами, описанными в литературе, например JP-A-2-173, WO 03/66607 и т.п. А именно, они могут быть получены путем гидролизации соединений, представленных формулой (VII) где X, Y, n и Т такие, как определено выше, и R5 представляет собой C1-С 4-алкил, предпочтительно метил или этил, в присутствии подходящего основания, например гидроксида натрия, в разбавителе, например водном диоксане. Часть соединений, представленных упомянутой выше формулой (VII), представляют собой новые соединения, не описанные в предшествующей литературе, и могут быть получены в соответствии со спо-4 015425 собами, описанными в литературе, например немецкий патент 10039723, WO 03/66607 и т.п. А именно, они могут быть получены реакцией соединений, представленных формулой (VIII) где X, Y и n такие, как определено выше, и R5 представляет собой С 1-С 4-алкил, предпочтительно метил или этил, и Hal представляет собой галоген, предпочтительно хлор или бром, с соединениями, представленными формулой (IX) где Т такой, как определено выше, в присутствии подходящего конденсирующего реагента, например карбоната калия, в присутствии разбавителя, например N,N-диметилформамида. Соединения, представленные упомянутой выше формулой (VIII), сами по себе известны и могут быть без труда получены способами, описанными, например, в JP-A-6-247891, JP-A-7-206808, европейском патенте 369803 и т.п. Соединения, представленные упомянутой выше формулой (IX), сами по себе известны и могут быть без труда получены способами, описанными, например, в Journal of the American Chemical Society,vol. 80, p. 3908-3911 (1958), Journal of Organic Chemistry, vol. 22, p. 1142-1145 (1957), Journal of OrganicChemistry, vol. 56, p. 2395-2400 (1991), JP-A-9-309883 и т.п. Типичные примеры соединений формулы (II), используемых в качестве исходных веществ в упомянутом выше способе получения (а), включают соединения, описанные ниже: 5-2,4-дихлор-3-[2-(1 Н-тетразол-1-ил)этилокси]бензоилокси-1,3-диметилпиразол,5-2,4-дихлор-3-[2-(2 Н-тетразол-2-ил)этилокси]бензоилокси-1,3-диметилпиразол,5-2,4-дихлор-3-[2-(1 Н-тетразол-1-ил)этилокси]бензоилокси-1-метил-3-циклопропилпиразол,5-2-метил-3-[2-(5-метил-1 Н-тетразол-1-ил)этилокси]-4-бромбензоилокси-1,3-диметилпиразол,5-2-метил-3-[2-(5-метил-2 Н-тетразол-2-ил)этилокси]-4-бромбензоилокси-1,3-диметилпиразол,5-2-метил-3-[2-(5-метил-1 Н-тетразол-1-ил)этилокси]-4-хлорбензоилокси-1,3-диметилпиразол,5-2-метил-3-[2-(5-этил-1 Н-тетразол-1-ил)этилокси]-4-бромбензоилокси-1,3-диметилпиразол,5-2,4-дихлор-3-[2-(5-метилтио-1 Н-тетразол-1-ил)этилокси]бензоилокси-1,3-диметилпиразол,5-2-метил-3-[2-(5-метокси-1 Н-тетразол-1-ил)этилокси]-4-бромбензоилокси-1,3-диметилпиразол,5-2-метил-3-[2-(2 Н-тетразол-2-ил)этилокси]-4-бромбензоилокси-1-метил-3-этилпиразол,5-2,4-дихлор-3-[3-(1 Н-тетразол-1-ил)пропилокси]бензоилокси-1,3-диметилпиразол,1-2,4-дихлор-3-[2-(1H-тетразол-1-ил)этилокси]бензоил-2,5-диметил-1,2-дигидро-3 Н-пиразол-3-он и т.д. Типичные примеры соединений формулы (IV), используемых в качестве исходных веществ в получении соединений упомянутой выше формулы (II), включают соединения, описанные ниже: 1,3-диметил-5-гидроксипиразол,1-метил-3-этил-5-гидроксипиразол,1-метил-3-циклопропил-5-гидроксипиразол,1-этил-3-метил-5-гидроксипиразол,1-этил-3-циклопропил-5-гидроксипиразол и т.д. Типичные примеры соединений формулы (V), используемых в качестве исходных веществ в получении соединений упомянутой выше формулы (II), включают соединения, описанные ниже: 2,4-дихлор-3-[2-(1 Н-тетразол-1-ил)этилокси]бензоил хлорид,2,4-дихлор-3-[2-(2 Н-тетразол-2-ил)этилокси]бензоил хлорид,2-метил-3-[2-(5-метил-1H-тетразол-1-ил)этилокси]-4-бромбензоил хлорид,2-метил-3-[2-(5-метил-2 Н-тетразол-2-ил)этилокси]-4-бромбензоил хлорид,2-метил-3-[2-(1 Н-тетразол-1-ил)этилокси]-4-хлорбензоил хлорид,2,4-дихлор-3-[2-(5-тиометил-1 Н-тетразол-1-ил)этилокси]бензоил хлорид,2-метил-3-[2-(5-метокси-1 Н-тетразол-1-ил)этилокси]-4-бромбензоил хлорид,2,4-дихлор-3-[3-(1H-тетразол-1-ил)пропилокси]бензоил хлорид и т.д. Типичные примеры соединений формулы (VI), используемых в качестве исходных веществ в получении соединений упомянутой выше формулы (V), включают соединения, описанные ниже: 2,4-дихлор-3-[2-(1H-тетразол-1-ил)этилокси]бензойная кислота,2,4-дихлор-3-[2-(2 Н-тетразол-2-ил)этилокси]бензойная кислота,2-метил-3-[2-(5-метил-1 Н-тетразол-1-ил)этилокси]-4-бромбензойная кислота,2-метил-3-[2-(5-метил-2 Н-тетразол-2-ил)этилокси]-4-бромбензойная кислота,2-метил-3-[2-(1 Н-тетразол-1-ил)этилокси]-4-хлорбензойная кислота,2,4-дихлор-3-[2-(5-тиометил-1 Н-тетразол-1-ил)этилокси]бензойная кислота,2-метил-3-[2-(5-метокси-1 Н-тетразол-1-ил)этилокси]-4-бромбензойная кислота,2,4-дихлор-3-[3-(1H-тетразол-1-ил)пропилокси]бензойная кислота и т.д.-5 015425 Типичные примеры соединений формулы (VII), используемых в качестве исходных веществ в получении соединений упомянутой выше формулы (VI), включают соединения, описанные ниже: этил 2,4-дихлор-3-[2-(1H-тетразол-1-ил)этилокси]бензоат,этил 2,4-дихлор-3-[2-(2 Н-тетразол-2-ил)этилокси]бензоат,этил 2-метил-3-[2-(5-метил-1 Н-тетразол-1-ил)этилокси]-4-бромбензоат,этил 2-метил-3-[2-(5-метил-2 Н-тетразол-2-ил)этилокси]-4-бромбензоат,метил 2-метил-3-[2-(1 Н-тетразол-1-ил)этилокси]-4-хлорбензоат,этил 2,4-дихлор-3-[2-(5-тиометил-1 Н-тетразол-1-ил)этилокси]бензоат,этил 2-метил-3-[2-(5-метокси-1 Н-тетразол-1-ил)этилокси]-4-бромбензоат,этил 2,4-дихлор-3-[3-(1 Н-тетразол-1-ил)пропилокси]бензоат и т.д. Типичные примеры соединений формулы (VIII), используемых в качестве исходных веществ в получении соединений приведенной выше формулы (VII), включают соединения, описанные ниже: этил 2,4-дихлор-3-(2-бромэтокси)бензоат,этил 2-метил-3-(2-бромэтокси)-4-бромбензоат,метил 2-метил-3-(2-бромэтокси)-4-хлорбензоат,этил 2,4-дихлор-3-(2-хлорэтокси)бензоат,этил 2,4-дихлор-3-(2-йодэтокси)бензоат,этил 2,4-дихлор-3-(3-бромпропилокси)бензоат и т.д. Типичные примеры соединений формулы (IX), используемых в качестве исходных веществ в получении соединений упомянутой выше формулы (VII), включают соединения, описанные ниже: 1 Н-тетразол,5-метил-1 Н-тетразол,5-этил-1 Н-тетразол,5-метилтио-1 Н-тетразол,5-метокси-1H-тетразол и т.д. Соединения формулы (Ia), которые являются исходными веществами в упомянутом выше способе получения (b), составляют часть соединений, представленных формулой (I) по настоящему изобретению,и могут быть без труда получены в соответствии с описанным выше способом получения (а). Типичные примеры соединений формулы (Ia), используемых в качестве исходных веществ в способе получения (b), включают соединения, описанные ниже, которые охватываются формулой (I): 4-2,4-дихлор-3-[2-(1 Н-тетразол-1-ил)этилокси]бензоил-1,3-диметил-5-гидроксипиразол,4-2,4-дихлор-3-[2-(2 Н-тетразол-2-ил)этилокси]бензоил-1,3-диметил-5-гидроксипиразол,4-2,4-дихлор-3-[2-(1 Н-тетразол-1-ил)этилокси]бензоил-1-метил-3-циклопропил-5-гидроксипиразол,4-2-метил-3-[2-(1 Н-тетразол-1-ил)этилокси]-4-бромбензоил-1,3-диметил-5-гидроксипиразол,4-2-метил-3-[2-(2 Н-тетразол-2-ил)этилокси]-4-бромбензоил-1,3-диметил-5-гидроксипиразол,4-2-метил-3-[2-(1H-тетразол-1-ил)этилокси]-4-хлорбензоил-1,3-диметил-5-гидроксипиразол и т.д. Соединения формулы (III), которые являются исходными веществами в описанном выше способе получения (b), представляют собой галогенированный алкил, галогенированный алкенил, галогенированный алкинил, галогенированный аралкил, галогенированный ацил, галогенированный сульфонил и ацилалкил галид, которые хорошо известны сами по себе в области органической химии и которые описаны ниже в качестве иллюстративных примеров: метил йодид,пропаргил бромид,бензил бромид,н-пропан сульфонил хлорид,4-метилбензен сульфонил хлорид,ацетил хлорид,фенацил бромид и т.д. Реакция описанного выше способа получения (а) может быть осуществлена в подходящем разбавителе, и примеры разбавителей, которые могут быть использованы в течение способа, включают алифатические, алициклические и ароматические углеводороды (которые могут быть необязательно хлорированными), например пентан, гексан, циклогексан, петролейный эфир, лигроин, толуол, ксилол,дихлорметан, 1,2-дихлорэтан и т.д.; простые эфиры, такие как, например, этиловый эфир, метилэтиловый эфир, изопропиловый эфир,бутиловый эфир, диоксан, диметоксиэтан (DME), тетрагидрофуран (THF) и диэтиленгликоль диметиловый эфир (DGM); кетоны, такие как, например, ацетон, метил-этил-кетон (MEK), метил-изопропил-кетон и метилизобутил-кетон (MIBK); нитрилы, такие как, например, ацетонитрил и пропионнитрил; спирты, такие как, например, метанол, этанол и изопропанол; сложные эфиры, такие как, например, этилацетат, амилацетат; кислые амиды, такие как, например, диметилформамид (DMF), диметилацетамид (DMA),-6 015425N-метилпироллидон и 1,3-диметил-2-имидазолидон; сульфоны и сульфоксиды, такие как диметилсульфоксид (DMSO) и сульфолан; основания, такие как, например, пиридин. Способ получения (а) может быть осуществлен в присутствии основания. Примеры оснований включают неорганические основания, карбонаты и бикарбонаты щелочных и щелочно-земельных металлов,такие как, например, бикарбонат натрия, бикарбонат калия, карбонат натрия и карбонат калия; органические основания, третичные амины, диалкиламиноанилины и пиридины, такие как, например, триэтиламин, 1,1,4,4-тетраметилэтилендиамин (TMEDA), N,N-диметиланилин, N,N-диэтиланилин,пиридин, 4-диметиламинопиридин (DMAP), 1,4-диазабицикло[2,2,2]октан (DABCO) и 1,8 диазабицикло[5,4,0]ундек-7-ен (DBU). Способ получения (а) может быть осуществлен в присутствии цианида. Примеры катализаторов включают цианид натрия, цианид калия, ацетон цианогидрин, цианид водорода и т.п. Когда упомянутый выше способ получения (а) осуществляется в присутствии цианида, он также может быть осуществлен методом, использующим катализатор фазового переноса. Примеры разбавителей, которые могут быть использованы в ходе способа получения, включают алифатические, алициклические и ароматические углеводороды (которые могут быть необязательно хлорированными), например пентан, гексан, циклогексан, петролейный эфир, лигроин, толуол, ксилол,дихлорметан и т.п.; простые эфиры, такие как, например, этиловый эфир, метилэтиловый эфир, изопропиловый эфир,бутиловый эфир, диоксан, диметоксиэтан (DME), тетрагидрофуран (THF) и диэтиленгликоль диметиловый эфир (DGM); нитрилы, такие как, например, ацетонитрил и пропионитрил. Примеры катализаторов фазового переноса включают краун-эфиры, такие как, например, дибензо 18-краун-6, дициклогексил-18-краун-6, 18-краун-6 и 15-краун-5. Способ получения (а) может быть осуществлен, по существу, в широком диапазоне температур. В общем подходящий диапазон температур находится между от около 5 до около 200 С и предпочтительно от около 25 до около 130 С. Кроме того, реакция проводится желательно при нормальном давлении, но может также проводиться под повышенным давлением или пониженным давлением. При осуществлении способа получения (а) в реакцию вступают от 0,5 до 2 моль карбоната натрия на 1 моль соединения формулы (II) в разбавителе, например диоксане, с получением целевого соединения формулы (I). Когда способ получения (а) осуществляют в присутствии цианида, он может быть осуществлен, по существу, в широком диапазоне температур. А общем случае подходящий диапазон температур находится между около -10 и около 80 С и предпочтительно между около 5 и около 40 С. Кроме того, реакция проводится желательно при нормальном давлении, но может также проводиться при повышенном давлении или пониженном давлении. При осуществлении способа получения (а) в присутствии цианида реагируют от 1 до 4 моль триэтиламина на 1 моль соединение формулы (II) в присутствии от 0,01 до 0,5 моль цианогидрина ацетона в разбавителе, например ацетонитриле, до получения целевого соединения формулы (I). При осуществлении способа получения (а) соединения формулы (I) могут быть получены исходя из соединения формулы (VI) при непрерывном осуществлении реакции однореакторного синтеза без отделения соединения формулы (V) и соединений формулы (II). Реакция упомянутого выше способа получения (b) может быть осуществлена в подходящем разбавителе, и примеры разбавителей, которые могут быть использованы во время процесса, включают воду; алифатические, алициклические и ароматические углеводороды (которые могут быть необязательно хлорированными), например пентан, гексан, циклогексан, петролейный эфир, лигроин, бензол, толуол,ксилол, дихлорметан, хлороформ, тетрахлорид углерода, 1,2-дихлорэтан, хлорбензол, дихлорбензол и т.п.; простые эфиры, такие как, например, этиловый эфир, метилэтиловый эфир, изопропиловый эфир,бутиловый эфир, диоксан, диметоксиэтан (DME), тетрагидрофуран (THF) и диэтиленгликоль диметиловый эфир (DGM); кетоны, такие как, например, ацетон, метил-этил-кетон (MEK), метил-изопропил-кетон и метилизобутил-кетон (MIBK); нитрилы, такие как, например, ацетонитрил, пропионитрил и акрилонитрил; сложные эфиры, такие как, например, этилацетат и амилацетат; кислые амиды, такие как, например, диметилформамид (DMF), диметилацетамид (DMA), Nметилпирролидон и 1,3-диметил-2-имидазолидинон, гексаметилфосфорный триамид (НМРА); сульфоны и сульфоксиды, такие как, например, диметилсульфоксид (DMSO) и сульфолан; основания, такие как, например, пиридин. Способ получения (b) может быть осуществлен в присутствии связывающего кислоту реагента.-7 015425 Связывающие кислоту реагенты включают неорганические основания, гидриды, гидроксиды, карбонаты и бикарбонаты щелочных и щелочноземельных металлов, такие как, например, гидрид натрия, гидрид лития, бикарбонат натрия, бикарбонат калия, карбонат натрия, карбонат калия, гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид кальция; и органические основания, алколаты, третичные амины, диалкиламиноанилины и пиридины, такие как, например, триэтиламин, 1,1,4,4-тетраметилэтилендиамин (TMEDA), N,N-диметиланилин, N,Nдиэтиланилин, пиридин, 4-диметиламинопиридин (DMAP), 1,4-диазабицикло[2,2,2]октан (DABCO) и 1,8-диазабицикло[5,4,0]ундек-7-ен (DBU). Способ получения (b) может также быть осуществлен методом с использованием катализатора фазового переноса. Примеры разбавителей, которые могут быть использованы в ходе получения, включают воду; алифатические, алициклические и ароматические углеводороды (которые могут быть необязательно хлорированными), например пентан, гексан, циклогексан, петролейный эфир, лигроин, бензол, толуол,ксилол, дихлорметан, хлорбензол, дихлорбензол и т.п.; эфиры, такие как, например, этиловый эфир, метилэтиловый эфир, изопропиловый эфир, бутиловый эфир, диоксан, диметоксиэтан (DME), тетрагидрофуран (THF) и диэтиленгликоль диметиловый эфир (DGM); нитрилы, такие как, например, ацетонитрил, пропионитрил и акрилонитрил; и т.п. Примеры катализаторов фазового переноса включают четвертичные ионы, такие как, например, тетраметиламмония бромид, тетрапропиламмония бромид, тетрабутиламмония бромид, тетрабутиламмония бисульфат, тетрабутиламмония йодид, триоктилметиламмония хлорид, бензилтриэтиламмония бромид, бутилпиридина бромид, гептилпиридина бромид и бензилтриэтиламмония хлорид; краун-эфиры, такие как, например, дибензо-18-краун-6, дициклогексил-18-краун-6 и 18-краун-6; криптанды, такие как, например, [2.2.2]-криптат, [2.1.1]-криптат, [2.2.1]-криптат, [2.2.В]-криптат,[2 О 2 О 2S]-криптат и [3.2.2]-криптат. Способ получения (b) может быть осуществлен, по существу, в широком диапазоне температур. В общем случае, подходящий диапазон температур находится между около -20 и около 140 С и предпочтительно между около 0 и около 100 С. Кроме того, реакция проводится желательно при нормальном давлении, но может также проводиться под повышенным давлением или пониженным давлением. При осуществлении способа получения (b), реагирует от 1 до 5 моль соединения формулы (III) на моль соединения формулы (Ia) в присутствии карбоната калия в разбавителе, например DMF, с получением целевого соединения. Активные соединения формулы (I) в соответствии с настоящим изобретением демонстрируют превосходную гербицидную активность по отношению к различным сорнякам, как показано в примерах биологических испытаний, которые будут описаны позже, и могут быть использованы в качестве гербицидов. В рамках настоящего описания сорняки означают, в широком смысле, все растения, которые произрастают в местах, где они нежелательны. Соединения по настоящему изобретению действуют как селективные гербициды в зависимости от применяемой концентрации. Активные соединения согласно настоящему изобретению могут быть использованы, например, как для сорняков, так и для сельскохозяйственных культур, приведенных ниже. Из семейств двудольных сорняков: Sinapis, Capsella, Leipiduum, Galium, Stellaria, Chenopoduum,Kochia, Urtica, Senecio, Amaranthus, Portulaca, Xanthium, Ipomoea, Polygonum, Ambrosia, Cirsium, Sonchus,Solanum, Rorippa, Lamium, Veronica, Datura, Viola, Galeopsis, Papaver, Centaurea, Galinsoga, Rotala,Lindernia, Sesbania, Trifolium, Abutilon, Lamium, Matricaria, Artemisia, Sesbania, Pharbitis, Amaranthus и т.п. Из семейств двудольных сельскохозяйственных культур: Gossypium, Glycine, Beta, Daucus,Phaseolus, Pisum, Solanum, Linum, Ipomoea, Vicia, Nicotiana, Lycopersicon, Arachis, Brassica, Lactuca,Cucumis, Cucurbita и т.п. Из семейств однодольных сорняков: Echinochlona, Setaria, Panicum, Dugitaria, Phleum, Poa, Festuca,Eleusine, Lolium, Bromus, Avena, Cyperus, Sorghum, Agropyron, Monochoria, Fimbristylis, Sagittaria,Eleocharis, Scirpus, Paspalum, Ischaemum, Agrostis, Alopecurus, Cynodon, Commelina, Brachiaria, Leptochloa и т.п. Из семейств однодольных сельскохозяйственных культур: Oryza, Zea, Triticum, Hordeum, Avena,Secale, Sorghum, Panicum, Saccharum, Ananas, Asparagus, Allium и т.п. Однако применение активных соединений формулы (I) по настоящему изобретению не ограничивается упомянутыми выше видами сорняков и может быть также подобным образом использовано по отношению к другим видам сорняков. Применение активных соединений по настоящему изобретению не ограничивается указанными выше растениями и может быть также подобным образом использовано по отношению к другим растениям. Кроме того, активные соединения по настоящему изобретению могут неселективно контролиро-8 015425 вать сорняки и могут быть использованы, например, в промышленных зонах, таких как промышленные предприятия, железнодорожные пути, дороги, зонах зеленых насаждений, вне зон зеленых насаждений и т.п., в зависимости от применяемой концентрации. Подобным образом, эти соединения могут также быть использованы для контроля сорняков при выращивании многолетников, таких как, например, лесонасаждения, посадки декоративных деревьев, фруктовые сады, виноградники, цитрусовые рощи, ореховые сады, банановые плантации, кофейные плантации, чайные плантации, каучуковые плантации, плантации масличных пальм, какао плантации, плантации ягод и плантации хмеля. Соединения по настоящему изобретению могут также применяться для селективного контроля сорняков при выращивании однолетних растений. Активные соединения по настоящему изобретению могут быть переработаны в стандартные препаративные формы для конкретного применения. Примеры препаративных форм включают растворы, смачивающиеся порошки, эмульсии, суспензии, пылевидные препараты, диспергируемые в воде гранулы,таблетки, гранулы, суспендированные эмульсифицируемые концентраты, микрокапсулы в полимерных веществах и т.д. Эти препаративные формы могут быть произведены известными сами по себе способами. Например, они могут быть приготовлены путем смешения активного соединения с наполнителями, а именно жидкими или твердыми разбавителями или носителями и, при необходимости, с поверхностноактивными веществами, а именно эмульгаторами, и/или диспергаторами, и/или пенообразователями. Примеры жидких разбавителей или носителей включают ароматические углеводороды (например,ксилол, толуол, алкилнафтален и т.п.), хлорированные ароматические углеводороды или хлорированные алифатические углеводороды (например, хлорбензолы, этилен хлориды, метилен хлориды и т.п.), алифатические углеводороды [например, циклогексан и т.п., парафины (фракции минерального масла и т.п.)],спирты (например, бутанол, гликоль и т.п.), и их простые и сложные эфиры, кетоны (например, ацетон,метил-этил-кетон, метил-изобутил-кетон, циклогексанон и т.п.), сильно полярные растворители (например, диметилформамид, диметилсульфоксид и т.п.), вода и т.д. В случае использования воды в качестве наполнителя, например в качестве вспомогательного растворителя, может быть использован органический растворитель. Примеры твердых разбавителей могут включать размолотые природные минералы (например, каолины, глины, тальк, мел, кварц, аттапульгит, монтмориллонит или диатомовая земля) и размолотые синтетические минералы (например, высокодиспергированная кремниевая кислота, глинозем и силикат). Примеры твердых носителей для гранул могут включать дробленые и фракционированные горные породы (например, кальцит, мрамор, пемза, сепиолит и доломит), искусственные гранулы неорганических или органических порошков, и органических материалов (например, опилки, скорлупа кокосовых орехов, кочерыжки кукурузных початков и стебли табака). Примеры эмульгаторов и/или пенообразователей могут включать неионные и анионные эмульгаторы [например, полиоксиэтиленовые сложные эфиры жирных кислот, полиоксиэтиленовые простые эфиры спиртов жирных кислот (например, алкиларил полигликолиевый простой эфир), алкил сульфонаты,алкил сульфаты и арил сульфонаты] и гидролизаты альбумина. Диспергаторы включают лигнинсодержащий отработанный сульфитный щелок и метилцеллюлозу. В препаративных формах могут также быть использованы связующие вещества (порошки, гранулы и эмульгируемые концентраты). Примеры связующих веществ могут включать карбоксиметил целлюлозу, натуральные или синтетические полимеры (например, гуммиарабик, поливиниловый спирт и поливинилацетат). Могут быть также использованы красители. Примеры красителей могут включать неорганические пигменты (например, оксид железа, оксид титана и берлинская лазурь), органические красители, такие как ализариновые красители, азокрасители или металлические фталоциановые красители, и, кроме того,следовые элементы, такие как соли железа, марганца, бора, меди, кобальта, молибдена или цинка. Препаративные формы могут содержать активные соединения формулы (I) в диапазоне, в общем случае, от 0,1 до 95 мас.% и предпочтительно в диапазоне от 0,5 до 90 мас.%. Далее, активные соединения формулы (I) по настоящему изобретению могут быть использованы для контроля сорняков, как таковые или в виде препаративных форм. Активные соединения формулы (I) по настоящему изобретению могут также использоваться в комбинации с известными гербицидами. Смешанные гербицидные композиции с известными гербицидами могут быть предварительно приготовлены в виде окончательной готовой к применению препаративной формы или могут быть приготовлены путем смешения в емкости в отдельных случаях применения. Например, следующие гербициды, обозначенные их общепринятыми наименованиями, могут быть приведены в качестве характерных примеров гербицидов, которые могут быть использованы в комбинации с активными соединениями формулы (I) по настоящему изобретению: гербициды типа сульфонилмочевины, например хлорсульфурон, сульфометурон метил, хлоримурон этил, триасульфурон, амидосульфурон, оксасульфурон, трибенурон этил, просульфурон, этаметсульфурон метил, трифлусульфурон метил, трифенсульфурон метил, флазасульфурон, римсульфурон, никосульфурон, флупирсульфурон, бенсульфурон метил, пиразосульфурон этил, форамсульфурон, сульфо-9 015425 сульфурон, циносульфурон, азимсульфурон, метсульфуронметил, галосульфурон метил, этоксисульфурон, циклосульфамурон и йодосульфурон; гербициды типа карбамата, например фенмедифам, хлорпрофам, асулам, бентиокарб, молинат, эспрокарб, пирибутикарб, димепиперат и свеп; гербициды типа хлорацетанилида, например пропахлор, метазахлор, алахлор, ацетохлор, метолахлор, бутахлор, претилахлор и тенилхлор; гербициды типа дифенилэфира, например ацифлуорфен, оксифлуорфен, лактофен, фомесафен, аклонифен, хлометоксинил, бифенокс и CNP; гербициды типа триазина, например симазин, атразин, пропазин, цианазин, аметрин, симетрин, диметаметрин и прометрин; гербициды типа феноксикислотных или типа бензойной кислоты, например 2,3,6-ТВА, дикамба,квинхлорак, квинмерак, клопиралид, пиклорам, триклопир, флуроксипир, феноксапроп, диклофор метил,флуазифоп бутил, галоксифоп метил, квизалофоп этил, цигалофоп бутил, 2,4-РА, МСР, МСРВ и фенотиол; гербициды типа кислого амида или мочевины, например изоксабен, дифлуфеникан, даиурон, линурон, флуометурон, дифеноксурон, метилдимрон, изопротурон, изоурон, тебутиурон, метабензотиазурон,пропанил, мефенацет, хломепроп, напроанилид, бромбутид, диамурон, куморуон, этобензанид и оксадихломефон; гербициды типа органических фосфорсодержащих соединений, например глифосат, балафос, глуфосинат, амипрофос метил, анилофос, бенсулид, пиперофос и бутамифос; гербициды типа динитроанилина, например трифлуралин и продиамин; гербициды фенольного типа, например бромоксинил, иоксинил и диносеб; гербициды типа циклогександиона, например аллоксидим, сетоксидим, клопроксидим, клетодим,циклоксидим и тралкоксидим; гербициды типа имидазолина, например имазаметабенз, имазапир, имазаметапир, имазаэтапир,имазамокс и имазаквин; гербициды типа бипиридина, например паракват и дикват; гербициды типа карбамоилтетразолинона, например фентразамид; гербициды нитрильного типа, например дихлобенил; и другие гербициды, например бентазон, тридифан, инданофан, амитрол, карфентразон этил, сульфентразон, фенхлоразол этил, изоксафлутол, кломазон, гидразид малеиновой кислоты, пиридат, хлоридазон, норфлуразон, пиритиобак, бромацил, тербацил, метрибузин, оксазикломефон, цинметилин, флумиклорак пентил, флумиоксадин, флутиацет метил, азафенидин, бенфуресат, оксадиазон, оксадиаргил, пентоксазон, кафенстрол, пириминобак, биспирибак натрий, пирибензоксим, пирифталид, пирафлуфен этил,бензобициклон, дитиопир, далапон и хлортиамид. Активные соединения, перечисленные выше, являются известными гербицидами, описанными в"Руководстве по пестицидам" ("Pesticide Manual," 2000, опубликованном Британским советом по защите растений (British Crop Protect Council. Далее, активные соединения формулы (I) по настоящему изобретению также могут быть смешаны с антидотами для снижения фитотоксичности и для обеспечения более широкого спектра контролируемых сорняков путем смешения, тем самым может быть расширено их применение в качестве селективных гербицидов. В качестве примеров антидотов могут быть упомянуты следующие соединения, обозначенные их общеупотребительными наименованиями или расширенными кодами:AD-67, BAS-145138, беноксакор, клоквинтоцет-метил, циометринил, 2,4-D, DKA-24, дихлормид,димрон, фенклорин, фенхлоразол-этил, флуразол, флуксофеним, фурилазол, изоскадифен-этил, мефенпир-диэтил, MG-191, нафтойный ангидрид, оксабетринил, PPG-1292, R-29148 и т.д. Упомянутые выше антидоты также описаны в "Руководстве по пестицидам" ("Pesticide Manual" 2000), опубликованном Британским советом по защите растений. Кроме того, смешанные гербицидные композиции, содержащие активные соединения формулы (I) по настоящему изобретению и упомянутые выше гербициды, могут быть дополнительно смешаны с упомянутыми выше антидотами для снижения фитотоксичности и для обеспечения более широкого спектра контролируемых сорняков путем смешения, тем самым может быть расширено их применение в качестве селективных гербицидов. Неожиданно, некоторые из смешанных гербицидных композиций соединений согласно настоящему изобретению с известными гербицидами и/или антидотами показывают синергические эффекты. В случае применения активных соединений формулы (I) по настоящему изобретению они могут применяться напрямую как таковые или применяться в виде препаративных форм, таких как рецептурные растворы для распыления, эмульгируемые концентраты таблетки, суспензии, порошки, гранулы, или в форме для применения, приготовленной путем дополнительного разбавления. Активные соединения по настоящему изобретению могут вноситься, например, смачиванием, разбрызгиванием, распылением,разбрасыванием гранул и т.д.- 10015425 Активные соединения формулы (I) по настоящему изобретению могут применяться на любой стадии до или после прорастания растений. Далее они также могут быть внесены в почву до обсеменения. Дозы внесения активного соединения формулы (I) могут варьироваться и в корне различаются в зависимости от природы желаемого эффекта. В случае использования активных соединений в качестве гербицидов, примеры доз внесения, в расчете на активное соединение, могут находиться в диапазоне от около 0,005 до около 4 кг/га и предпочтительно в диапазоне от около 0,01 до около 2 кг/га. Получение и применение соединений по настоящему изобретению будет описано более подробно в виде нижеследующих примеров, но настоящее изобретение ни в коем случае не должно ограничиваться ими. Примеры соединений. Пример синтеза 1. 5-2,4-Дихлор-3-[2-(1 Н-тетразол-1-ил)этилокси]бензоилокси-1,3-диметилпиразол (0.65 г) разбавляли в ацетонитриле (10 мл), туда добавляли триэтиламин (0.33 г) и ацетон цианогидрин (40 мг) и смесь взбалтывали при комнатной температуре в течение 12 ч. Растворитель отгоняли, подкисляли путем добавления разбавленной соляной кислоты и экстрагировали этилацетатом (150 мл). Органическую фазу промывали насыщенным рассолом и высушивали безводным сульфатом магния. Этилацетат отгоняли до получения целевого 4-2,4-дихлор-3-[2-(1 Н-тетразол-1-ил)этокси]бензоил-1,3-диметил-5-гидроксипиразола (0.59 г). Т.пл.: 63-68 С. Пример синтеза 2.(0.40 г) и карбонат калия (0.15 г) были суспендированы в DMF (3 мл), туда был добавлен бензил бромид(0.17 г) и смесь перемешивали при комнатной температуре в течение 5 ч. По завершении реакции добавляли холодную воду, смесь экстрагировали этилацетатом (100 мл) и высушивали над безводным сульфатом магния. Осадок, полученный путем отгонки этилацетата, очищали колоночной хроматографией на силикагеле (элюент; этилацетат:гексан=1:1) до получения целевого 5-2-метил-3-[2-(1H-тетразол-1 ил)этилокси]-4-бромбензоилокси-1,3-диметил-5-бензилоксипиразола (0.37 г). Т.пл.: 122-125 С. Соединения, полученные с помощью процесса в соответствии со способами получения соединения по настоящему изобретению, проиллюстрированные в приведенных выше примерах синтеза 1 и 2, показаны в нижеследующей табл. 1 вместе с соединениями, синтезированными в примерах синтеза 1 и 2. В табл. 1 Т 1 представляет собой группу Далее, Me представляет собой метил, Et представляет собой этил, Pr-n представляет собой nпропил, цикло-Pro представляет собой циклопропил, ОМе представляет собой метокси, SMe представляет собой метилтио, SO2Me представляет собой метансульфонил (метилсульфонил), Ph представляет собой фенил и Ph-4-Me представляет собой 4-метилфенил.(5 мл), этот раствор добавляли по каплям к раствору 1,3-диметил-5-гидроксипиразола (0.22 г) в тетрагидрофуране (5 мл) и триметиламину (0.23 г) при температуре 5 С и смесь взбалтывали при комнатной температуре в течение 6 ч. По завершении реакции смесь экстрагировали этилацетатом (100 мл) и затем промывали разбавленной соляной кислотой и водным раствором бикарбоната натрия и высушивали над безводным сульфатом магния. Этил ацетат отгоняли до получения целевого 5-2,4-дихлор-3-[2-(1 Нтетразол-1-ил)этилокси]бензоилокси-1,3-диметилпиразола (0.65 г). Т.пл.: 138-140 С. Ссылочный пример 2. 2,4-Дихлор-3-[2-(1 Н-тетразол-1-ил)этокси]бензойную кислоту (0.46 г) и тионил хлорид (0.36 г) добавляли в 1,2-дихлорэтан (10 мл), добавляли две капли DMF и смесь нагревали в сосуде с обратным холодильником при нагревании в течение 3 ч. После охлаждения отгоняли растворитель до получения целевого 2,4-дихлор-3-[2-(1H-тетразол-1-ил)этокси]бензоил хлорида (0.49 г). Т.пл.: 69-73 С. Ссылочный пример 3. К раствору этил 2,4-дихлор-3-[2-(1H-тетразол-1-ил)этокси]бензоата (0.88 г) в метаноле (15 мл) добавляли гидрохлорид натрия (0.16 г) и воду (5 мл), смесь перемешивали при комнатной температуре в течение 7 ч. После добавления воды (20 мл) и концентрировании при пониженном давлении добавляли водный раствор гидрохлорида натрия и смесь промывали этилацетатом (50 мл). Водную фазу окисляли соляной кислотой и экстрагировали этилацетатом. Органическую фазу промывали насыщенным рассолом и высушивали над безводным сульфатом магния. Этилацетат отгоняли до получения целевой 2,4- 17015425 дихлор-3-[2-(1H-тетразол-1-ил)этилокси]бензойной кислоты (0.69 г). Т.пл.: 145-146 С. Ссылочный пример 4.(15 мл), туда добавляли карбонат калия (1.21 г) и йодид натрия (0.04 г) и смесь взбалтывали при температуре 80 С в течение 3 ч. По завершении реакции добавляли холодную воду, экстрагировали этилацетатом (100 мл) и высушивали над безводным сульфатом магния. Осадок, полученный путем отгонки этилацетата, очищали с помощью колоночной хроматографии на силикагеле (элюент; этилацетат:гексан=1:1) с получением целевого этил 2,4-дихлор-3-[2-(1H-тетразол-1-ил)этокси]бензоата (0.88 г) и этил 2,4 дихлор-3-[2-(1 Н-тетразол-2-ил)этокси]бензоата (0.99 г). Этил 2,4-дихлор-3-[2-(1 Н-тетразол-1-ил)этокси]бензоат; nD20=1.5535. Этил 2,4-дихлор-3-[2-(1 Н-тетразол-2-ил)эткси]бензоат; nD20=1.5483. Примеры биологических испытаний. Сравнительное соединение Пример испытаний 1. Испытания на гербицидную эффективность против сорняков полевых культур (обработка почвы распылением до появления всходов). Приготовление препаративной формы активного соединения. Носитель: DMF 5 мас.ч. Эмульгатор: Бензилоксиполигликолевый эфир 1 мас.ч. Соответствующую препаративную форму активного соединения в виде эмульгируемого концентрата получали путем смешения 1 мас.ч. активного соединения с определенными количествами носителя и эмульгатора. Заданное количество препаративной формы разбавляли водой. В теплице высевали семена сорняков полевых культур (щирица синеватая (Amaranthus lividus) и щетинник зеленый (Setaria viri dus по одному виду на горшок на поверхностный слой горшков площадью 16 см 2, наполненных полевой почвой (супесь), и засыпали почвой. Незамедлительно после посева на почву распыляли приготовленный в соответствии с описанным выше способом предусмотренный и разбавленный раствор препаративной формы соответствующего активного соединения. Через 2 недели после обработки исследовали гербицидную эффективность соответствующего активного соединения. Оценку гербицидной эффективности осуществляли путем количественной оценки полной гибели как 100 и как 0% - в случае отсутствия гербицидной эффективности. В случае если активные соединения показывают гербицидную эффективность 80% или более, такие активные соединения оцениваются, как целесообразные для применения в качестве гербицидов. В качестве типичных примеров в табл. 2 ниже показаны результаты исследований соединений 19 и 96 и результаты такого же исследования сравнительного соединения С-1. Таблица 2 Обработка почвы распылением до появления всходов Примечание: а.в. = активное вещество. Пример испытаний 2. Тест на гербицидную эффективность против сорняков полевых культур (послевсходовая распылительная обработка стеблей и листьев). В теплице молодые растения (в стадии 2-3-листьев) сорняков полевых культур (щетинник зеленый(Setaria viridis были пересажены в горшки площадью 16 см 2, наполненные полевой почвой (супесь), и приготовленный в соответствии с описанным выше примером испытаний 1 предусмотренный и разбав- 18015425 ленный раствор препаративной формы соответствующего активного соединения сверху распыляли на растения. Через 2 недели после обработки исследовали гербицидную эффективность соответствующего активного соединения. Оценку гербицидной эффективности осуществляли таким же образом, что и в примере испытаний 1, упомянутом выше. В качестве типичных примеров в табл. 3 ниже показаны результаты исследований соединений 19 и 96 и результаты такого же исследования сравнительного соединения С-1. Таблица 3 Послевсходовая распылительная обработка стеблей и листьев Пример испытаний 3. Тест на селективную гербицидную эффективность против полевых культур (предвсходовая распылительная обработка почвы). В теплице высевали семена полевых культур [Zea mays (кукуруза) и Glycine max (соя)] и сорняков полевых культур (куриное просо (Echinochloa crus-galli), росичка реснитчатая (Digitaria ciliaris), щирица синеватая (Amaranthus lividus) и марь белая (Chenopodium album на поверхностный слой горшков площадью 16 см 2, наполненных полевой почвой (супесь), и засыпали почвой. Через один день на почвы распыляли приготовленный в соответствии с описанным выше примером испытаний 1 предусмотренный и разбавленный раствор препаративной формы соответствующего активного соединения. Через две недели после обработки исследовали фитотоксичность по отношению к полевым культурам и гербицидную эффективность активного соединения. Оценку гербицидной эффективности и фитотоксичности для сельскохозяйственных культур осуществляли путем количественной оценки полной гибели как 100% и как 0% в случае отсутствия гербицидной эффективности и в случае отсутствия фитотоксичности для сельскохозяйственных культур. В случае если активные соединения показывают гербицидную эффективность 80% или более, такие активные соединения оцениваются, как целесообразные для применения в качестве гербицидов, и в случае если активные соединения показывают фитотоксичность 20% и менее,такие активные соединения оцениваются, как лучшие по безопасности в качестве гербицидов. В качестве типичных примеров в табл. 4 ниже показаны результаты исследования соединения 12. Таблица 4 Предвсходовая распылительная обработка почвы Примеры препаративных форм. Пример препаративной формы 1 (гранулы). К смеси соединения 14 (10 частей (ч. по настоящему изобретению, бетонита (монтмориллонита) (30 ч.), талька (58 ч.) и лигнинсульфоната (2 ч.) добавляли воду (25 ч.), смесь хорошо вымешивали,перерабатывали в гранулы размером 10-40 меш. с помощью экструзионного гранулятора, которые высушивают при температуре 40-50 С с получением гранул. Пример препаративной формы 2 (гранулы). Частицы глинистого минерала (95 ч.) с распределением размера частиц 0.2-2 мм загружали в роторный смеситель, соединение 14 (5 ч.) по настоящему изобретению распыляли при вращении вместе с жидким разбавителем, равномерно смачивали и затем высушивали при температуре 40-50 С с получением гранул.- 19015425 Пример препаративной формы 3 (эмульгируемый концентрат). Соединение 103 (30 ч.) по настоящему изобретению, ксилол (55 ч.), полиоксиэтилен алкилфенил эфир (8 ч.) и кальций алкилбензол сульфонат (7 ч.) смешивали путем перемешивания до получения эмульсии. Пример препаративной формы 4 (смачивающийся порошок). Соединение 154 (15 ч.) по настоящему изобретению, смесь белой сажи (тонкоизмельченный порошок водосодержащего аморфного оксида кремния) и измельченной в порошок глины (1:5) (80 ч.), натрий алкилбензол сульфонат (2 ч.) и полимер (3 ч.) натрий алкилнафтален сульфонат формалин полимера смешивали в виде порошка и перерабатывали в смачивающийся порошок. Пример препаративной формы 5 (диспергируемые в воде гранулы). Хорошо перемешивали соединение 104 (20 ч.) по настоящему изобретению, лигнинсульфонат натрия (30 ч.), бентонит (15 ч.) и порошок кальцинированной диатомовой земли (35 ч.), туда добавляли воду и смесь экструдировали с получением гранул размером 0,3 мм и высушивали с получением диспергируемых в воде гранул. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Бензоилпиразолы, представленные формулой (I)X представляет собой галоген или C1-С 6-алкил;n имеет значение 2 или 3 и Т представляет собой группу Т 1R1 представляет собой метил или этил;Y представляет собой хлор или бром;n имеет значение 2 или 3 и Т представляет собой группу Т 1 где R4 представляет собой водород, метил, этил, метокси или метилтио. 3. Гербицид, содержащий в качестве активного ингредиента соединение по п.1 или 2. 4. Соединение, представленное формулой (II)
МПК / Метки
МПК: A01N 43/713, C07D 403/12, A01N 43/56
Метки: бензоилпиразолы, применение, промежуточные, качестве, вещества, гербицидов
Код ссылки
<a href="https://eas.patents.su/22-15425-benzoilpirazoly-ih-primenenie-v-kachestve-gerbicidov-i-promezhutochnye-veshhestva.html" rel="bookmark" title="База патентов Евразийского Союза">Бензоилпиразолы, их применение в качестве гербицидов и промежуточные вещества</a>
Предыдущий патент: Соединения диосметина, способ их получения и фармацевтические композиции, которые их содержат
Следующий патент: Способ получения галогенидов n-алкилнальтрексона
Случайный патент: Электронный звуковой имитатор












