Противоревматические средства
Номер патента: 1798
Опубликовано: 27.08.2001
Авторы: Ву Хуа-Канг, Кояма Нобуто, Охноги Хирому, Хагия Митио, Като Икуносин, Еноки Тацудзи, Томинага Таканари, Нисияма Ейдзи
Формула / Реферат
1. Фармацевтическое средство, которое отличается тем, что содержит, по меньшей мере, одно соединение, выбранное из группы, состоящей из 4,5-дигидрокси-2-циклопентен-1-она, представленного нижеследующей формулой [I], и оптически активного вещества и соли его, в качестве эффективного компонента, где указанное фармацевтическое средство выбирают из группы, состоящей из противоревматического средства, превентера ревматизма, противовоспалительного средства, превентера воспаления, ингибитора продуцирования фактора некроза опухоли, превентера продуцирования фактора некроза опухоли, ингибитора продуцирования моноксида азота, ингибитора для неоваскуляризации, превентера канцерогенеза, улучшающего средства при ишемическом нарушении головного мозга, индуцирующего средства для продуцирования Fas-антигена, иммуномодулирующего средства и ингибитора топоизомеразы.
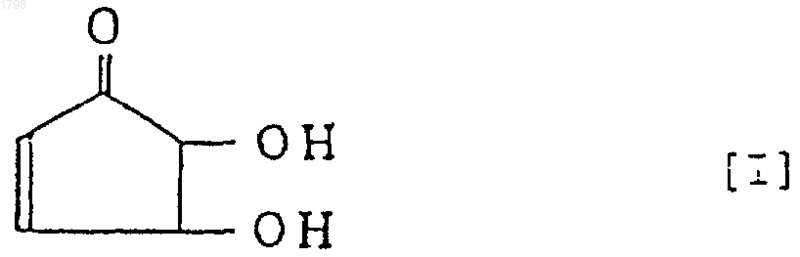
2. Фармацевтическое средство по п.1, где указанное фармацевтическое средство представляет собой иммуномодулирующее средство, выбранное из группы, состоящей из энхансера продуцирования интерлейкина-10, ингибитора продуцирования IgE, ингибитора гиперчувствительности замедленного типа, ингибитора пролиферации лимфоцитов и ингибитора отека.
3. Продукт питания или напиток, который отличается тем, что содержит, по меньшей мере, одно соединение, выбранное из группы, состоящей из 4,5-дигидрокси-2-циклопентен-1-она, представленного формулой [I], и оптически активного вещества и соли его, в качестве эффективного компонента, где указанный продукт питания или напиток выбирают из группы, состоящей из продукта питания или напитка для улучшения или профилактики ревматизма, для улучшения или профилактики воспаления, для ингибирования продуцирования фактора некроза опухоли, для усиления продуцирования интерлейкина-10, для ингибирования продуцирования монооксида азота, для индуцирования продуцирования Fas-антигена, для иммуномодулирования, для ингибирования продуцирования IgE и для ингибирования топоизомеразы.
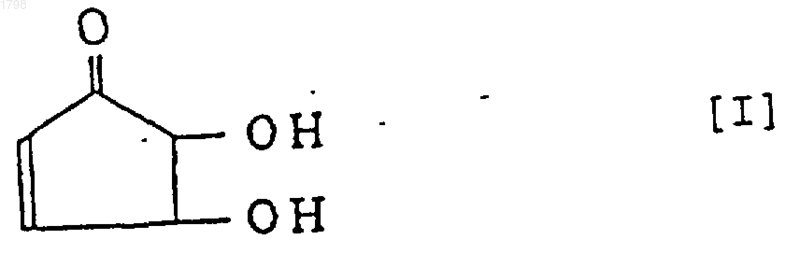
Текст
1 Область техники Настоящее изобретение относится к фармацевтическим препаратам, продуктам питания и напиткам, используемым для лечения и профилактики воспалительных заболеваний, таких как хронический суставной ревматизм. Предшествующий уровень техники Воспаление, как полагают, возникает тогда, когда живой организм в защитных целях действует против инвазии извне и продуцирует внутреннее активное вещество, чтобы адаптировать состояние организма к этому. Однако существует много случаев, когда индуцированная при этом реакция оказывается вредной и вызывает болезненное состояние. Кроме того,воспаление при аутоиммунных заболеваниях является результатом того, что иммуноциты воспринимают сами себя как чужеродные вещества и действуют концентрацептивным образом даже по отношению к нормальным клеткам. Сообщалось, что в Т-клетках-хелперах(Th), существуют Тh1-клетки, которые продуцируют интерлейкин-2 и интерферон(IFN-),которые представляют собой цитокины, промотирующие активацию клеточного иммунитета,такие как макрофаги (Мф), и также Тh2-клетки,которые продуцируют интерлейкин-4, интерлейкин-5 и интерлейкин-10, активирующие гуморальный иммунитет, участвующий в продукции антител. Кроме того показано, что Тh1-клетки иTh2-клетки контролируют друг друга при помощи цитокинов, продуцируемых каждой из них. Таким образом, IFN-, продуцируемый Тh1-клетками, контролирует активацию Th2 клеток и индуцирует активацию Тh1-клеток. С другой стороны, интерлейкин-10, продуцируемый Th2 клетками, контролирует активацию Тh1-клеток, и интерлейкин-4 индуцирует активацию Th2-клеток. Аутоиммунные болезни грубо классифицируют на органоспецифические и системные болезни. Полагают, что при системном аутоиммунном заболевании и аллергическом заболевании симптом вызывается Th2-доминантным иммунным ответом, в то время как при органоспецифическом аутоиммунном заболевании и воспалительном заболевании симптом вызывается Th1-доминантным иммунным ответом. Хронический суставной ревматизм, который представляет собой одно из аутоиммунных заболеваний, как полагают, является воспалением, возникающим в суставе локально и, как предполагают, по-видимому, является органоспецифическим заболеванием или, другими словами, Th1-опосредованным аутоимунным заболеванием. В самом деле, в местах воспаления у пациентов, страдающих ревматизмом, отмечается инвазия М и нейтрофилов, которые, как полагают, индуцируются и активируются цитокинами, производимыми Th1-клетками, и зна 001798 2 чительное увеличение некроза опухоли фактора- продуцируемого М. При других органоспецифических иммунных болезнях и воспалительных заболеваниях также наблюдаются те же самые гистологические картины, и полагают,что воспаление обостряется теми воспалительными клетками и воспалительными цитокинами, которые продуцируются Thl-клетками. Исходя из этих фактов, полагают, что для лечения воспалительных заболеваний и органоспецифических аутоиммунных болезней, таких как хронический суставной ревматизм, подавление фактора некроза опухоли, продуцируемого М, и индукция интерлейкина-10, который является Th1-ингибирующим цитокином,являются важными [Igaku no Ayumi, publishedby Ishiyaku Shuppan KK, volume 182, pages 523528 and 661-665 (1997)]. В качестве лекарственной терапии хронического суставного ревматизма проводят наружное лечение стероидами, нестероидными противовоспалительными средствами и средствами, вызывающими ремиссию, такими как золото и D-пеницилламин. Цели изобретения Целью настоящего изобретения является разработка соединения, которое было бы полезным для лечения воспалительных заболеваний,таких как хронический суставной ревматизм, и предложение фармацевтических препаратов,продуктов питания и напитков, содержащих указанное соединение. Сущность изобретения Для достижения вышеупомянутой цели настоящими изобретателями было проведено интенсивное исследование и было обнаружено,что 4,5-дигидрокси-2-циклопентен-1-он, который представлен формулой (I) (в дальнейшем называемый просто "циклопентенон"), является полезным для лечения или профилактики воспалительных заболеваний, таких как хронический суставной ревматизм, и иммунных заболеваний, что и составляет предмет настоящего изобретения. В общих чертах, настоящее изобретение заключается в том, что первый аспект его относится к противоревматическому средству, которое отличается тем, что содержит, по меньшей мере, одно соединение, выбранное из группы,состоящей из 4,5-дигидрокси-2-циклопентен-1 она, представленного нижеследующей формулой [I], и оптически активного вещества и соли его в качестве эффективного компонента. Второй аспект настоящего изобретения относится к продукту питания или напитку для улучшения состояния или профилактики хронического суставного ревматизма, который характеризуется тем, что содержит, по меньшей мере, 3 одно соединение, выбранное из группы, состоящей из 4,5-дигидрокси-2-циклопентен-1 она, представленного формулой [I], и оптически активного вещества и соли его в качестве эффективного компонента. Краткое описание чертежей Фиг. 1 демонстрирует влияние циклопентенона на рост клеток Jurkat. Фиг. 2 демонстрирует влияние циклопентенона на рост клеток Molt-3. На фиг. 3 представлена экспрессия Fasантигена в Molt-3-клетках. На фиг. 4 представлена экспрессия Fasантигена в клетках Jurkat. На фиг. 5 представлено изменение уровня клеток, экспрессирующих Fas-антиген, когда инкубацию проводят после добавления 10 мкМ циклопентенона к Molt-3-клеткам. Фиг. 6 демонстрирует взаимосвязь между количеством циклопентенона и степенью увеличения отека ступни. Фиг. 7 демонстрирует взаимосвязь между количеством циклопентенона и продуцируемым количеством фактора некроза опухоли. Фиг. 8 демонстрирует взаимосвязь между концентрацией циклопентенона и концентрацией NO2-. Фиг. 9 демонстрирует взаимосвязь между временем инкубации и числом жизнеспособных клеток в присутствии циклопентенона. Фиг. 10 демонстрирует ингибирующую активность циклопентенона в реакции гиперчувствительности замедленного типа. Фиг. 11 демонстрирует ингибирующую активность циклопентенона в пролиферации лимфоцитов. Фиг. 12 демонстрирует ингибирующую активность циклопентенона в смешанной реакции лимфоцитов. На фиг. 13 представлен спектр (КД) (CD) п-диметиламинобензоильного производного (-)циклопентенона и структура стереоизомера (-)циклопентенона. На фиг. 14 представлен спектр КД (CD) пдиметиламинобензоильного производного (+)циклопентенона и структура стереоизомера (+)циклопентенона. Варианты осуществления изобретения Настоящее изобретение конкретно иллюстрируется ниже. Используемый в настоящем изобретении циклопентенон, представленный формулой [I], охватывает оба изомера, где конфигурации гидроксильных групп при 4-и 5 положениях представляют цис- и транс-(форму). В настоящем изобретении может быть использован любой из цис-циклопентенона, трансциклопентенона и смесь цис- и трансциклопентенона. Кроме того, возможно использование их оптически активных веществ. Цис-циклопентенон можно получить путем химического синтеза [Helvetica Chimica 4 циклопентенон можно получить либо путем химического синтеза [Carbohydrate Res., volume 247, pages 217-222 (1993)], либо путем нагревания уроновой кислоты, такой как глюкуроновая кислота, производного уроновой кислоты, такого как глюкуронолактон, или вещества, содержащего те же компоненты (смотри PCT/JP97/ 03052). В настоящем изобретении, кроме того,возможно использование также их продукта,подвергнутого нагреванию или частично очищенного, или очищенного. Например,когда используютDглюкуроновую кислоту в качестве уроновой кислоты, и ее 1% раствор нагревают при 121 С в течение 4 ч, циклопентенон получается в веществе, обработанном нагреванием. Циклопентенон, образовавшийся в этом обработанном нагреванием веществе, экстрагируют растворителем и экстракт концентрируют. Затем этот концентрированный экстракт отделяют с помощью колоночной хроматографии на силикагеле,элюированную фракцию циклопентенона концентрируют, циклопентенон экстрагируют хлороформом из концентрата, и экстракт концентрата подвергают колоночной хроматографии с обычной фазой, в результате чего из обработанного нагреванием вещества выделяют циклопентенон. Физические свойства циклопентенона будут даны ниже. В связи с этим проводят массспектрометрический анализ циклопентенона,используя масс-спектрометр DX302 (производимый Nippon Denshi). Кроме того измерение ЯМР, используя тяжелый хлороформ в качестве растворителя, проводят с помощью JNM-A 500(произвол. Nippon Denshi). Удельное вращение измеряют с помощью DIP-370 поляриметраH-ЯМР (CDCl3):4,20 (1H, д, J=2,4 Гц, 5 Н), 4,83 (1H, м, 4-Н), 6,30 (1H, дд, J=1,2, 6,1 Гц,2-Н), 7,48 (1H, дд, J=2,1, 6,1 Гц, 3-Н). В этой связи, значения химического сдвига 1H-ЯМР представлены с учетом, что значение химического сдвига СНСl3 составляет 7,26 ррм. Оптическое вращение: []D20 0 (с 1,3, вода) УФ: макс 215 нм (вода) ИК (КВr метод): поглощения отмечались при 3400, 1715, 1630, 1115, 1060, 1025 см-1. Когда выделенный циклопентенон подвергают оптическому разделению, получают (-)4,5-дигидрокси-2-циклопентен-1-он и (+)-4,5 дигидрокси-2-циклопентен-1-он. Само собой разумеется, что циклопентенон, полученный 5 синтетическим способом, можно также подвергнуть оптическому разделению. Например, циклопентенон растворяют в этаноле. К этому раствору далее добавляют смесь гексан/этанол (94/6), получая раствор циклопентенона. Циклопентенон может быть оптически разделен, если раствор этого образца подвергнуть ВЭЖХ (HPLC), используя, например, Chiral Pack AS (произв. Daicel ChemicalIndustries), при таком условии, что температура колонки составляет 40 С и подвижной фазой является смесь гексан/этанол (94/6). Оптическое вращение оптически разделенного (-)-транс-4,5-дигидрокси-2-циклопентен-1-она [в дальнейшем называемого (-)циклопентенон] составляет []D20 -105 (с 0,30,этанол), в то время как оптическое вращение[в дальнейшем называемого (+)-циклопентенон] составляет []D20 +104 (с 0,53, этанол). В данном случае оптическое вращение измеряют с помощью вышеупомянутого поляриметра типаDIP-370 (произв. Nippon Bunko). После этого как (-)-циклопентенон, так и(+)-циклопентенон подвергают структурному анализу с помощью методов массспектрального анализа и ядерного магнитного резонанса (ЯМР), измерению УФ-спектра поглощения и измерению инфракрасного спектра поглощения с помощью уже упомянутого выше метода. Как результат, оба оптически активных вещества показывают тот же самый результат,что и циклопентенон до оптического разделения. Как оптически разделенный(-)циклопентенон, так и (+)-циклопентенон, превращают в п-диметиламинобензоил производное, измеряют спектр кругового дихроизма, используя дисперсиметр кругового дихроизма типа J-720 (произв. Nippon Bunko), и результат соотносят с правилом хиральности дибензоата(1969)], чтобы определить конфигурацию. КД п-диметиламинобензоильного производного (-)-циклопентенона и структура стереоизомера(-)-циклопентенона представлены на фиг. 6. Здесь ордината соответствует молярному круговому дихроизму, в то время как абсцисса соответствует длине волны (нм). В данном случае вышеупомянутая структура стереоизомера представлена ниже в виде формулы [II] КД п-диметиламинобензоильного производного (+)-циклопентенона и структура стереоизомера (+)-циклопентенона представлены на фиг. 7. Здесь ордината соответствует молярному круговому дихроизму, в то время как абсцисса соответствует длине волны (нм). В данном случае вышеупомянутая структура стерео 001798 6 изомера представлена ниже в виде формулы Как показано на фиг. 13, фиг. 14, формула[II] и формула [III], (-)-циклопентенон представляет собой (-)-(4R, 5S)-транс-4,5-дигидрокси-2 циклопентен-1-он, в то время как (+)циклопентенон представляет (+)-(4S, 5R)-транс 4,5-дигидрокси-2-циклопентен-1-он. Вышеупомянутые циклопентеноны или их оптически активное вещество можно получить с помощью любого способа, т.е. они могут быть получены способом, раскрытым в этом описании, или путем химического синтеза; и транс-, и цис-циклопентенон или смесь их и оптически активное вещество их могут быть с успехом использованы в настоящем изобретении. Примерами соли циклопентенона или его оптически активного вещества являются фармацевтически приемлемые соли и их можно получить с помощью известных способов превращения. Циклопентенон взаимодействует, например, с SH-cодержащим соединением (таким как цистеин и глутатион) in vivo с получением метаболического производного, которое используют в качестве лекарственного средства. Поэтому полагают, что фармацевтическое действие метаболического производного достигается,даже когда применяют циклопентенон. Продукт реакции циклопентенона с SH-содержащим соединением in vivo, как полагают, представляет собой одно из метаболически эффективных веществ. Таким образом, когда иллюстративный пример дается для SH-содержащего соединения(R-SH), оно взаимодействует с SH-содержащим соединением, давая соединение, представленное, например, нижеследующей формулой [IV] или [V]. Кроме того соединение, представленное формулой [V], превращается в соединение,представленное формулой [IV]. Как таковой, циклопентенон превращается в каждое из метаболических производных в присутствии SH-содержащего соединения (RSH), и такое метаболическое производное, продуцируемое in vivo, также обеспечивает эффект как лекарственное средство.(R представляет собой остаточную группу после удаления SH-группы из SH-содержащего соединения).(R представляет собой остаточную группу после удаления SH-группы из SH-содержащего соединения). Таким образом, использование циклопентенона, его оптически активного вещества или соли его, имеющее целью получение такого продукта реакции in vivo, т.е. метаболического производного, также охватывается настоящим изобретением. Циклопентенон, его оптически активные вещества или их соли являются соединениями,имеющими физиологическое действие, такое как противоревматическое действие и ингибирующее действие в отношении хронического суставного ревматизма. Когда используют, по меньшей мере, одно соединение, выбранное из циклопентенона, его оптически активного вещества или его соли в качестве эффективного компонента, и составляют его в фармацевтический препарат путем комбинирования с известными фармацевтическими носителями, то можно получить противоревматическое средство. В общем, по меньшей мере, одно из соединений,выбранное из циклопентенона, его оптически активного вещества или его соли, объединяют с фармацевтически приемлемым жидким или твердым носителем и, при необходимости, туда добавляют растворитель, диспергатор, эмульгатор, буфер, стабилизатор, наполнитель, связующее, дезинтегратор, смазку, и т.д., получая указанный фармацевтический препарат, который может быть в твердом виде, таком как таблетки, гранулы, разбавленные порошки, порошки, капсулы, и т.д., или жидким, таким как растворы, суспензии, эмульсии, и т.д. Кроме того это может быть сухой препарат, который может быть превращен в жидкий путем добавления в него соответствующего носителя перед использованием. Фармацевтический носитель может быть выбран в зависимости от вышеупомянутого способа введения и формы препарата. В случае пероральных препаратов можно использовать крахмал, лактозу, сахар, маннит, карбоксиметилцеллюлозу, кукурузный крахмал, неорганические соли и т.д. При получении пероральных препаратов связующие, дезинтеграторы, поверхностно-активные вещества, смазки, промоторы разжижения, вкусовые корригенты, красители, ароматизаторы, и т.д. могут быть добавлены туда дополнительно. С другой стороны, в случае парентеральных препаратов они могут быть получены обычными способами, где, по меньшей мере,одно из соединений, выбранное из циклопентенона, его оптически активного вещества или его соли, которое представляет собой эффективный компонент настоящего изобретения, растворяют или суспендируют в разбавителе, таком как дистиллированная вода для инъекции, физиологический солевой раствор, водный раствор глюкозы, растительное масло для инъекции, кунжут 001798 8 ное масло, арахисовое масло, соевое масло, кукурузное масло, пропиленгликоль, полиэтиленгликоль и т.д., с последующим добавлением туда, при необходимости, бактерицидов, стабилизаторов, изотонических средств, анальгетиков, и т.д. Противоревматическое средство настоящего изобретения применяют, используя подходящий путь введения, в зависимости от формы препарата. Нет также особого ограничения для способа применения и препарат можно применять перорально, наружно или с помощью инъекции. Препараты для инъекции применяют,например, внутривенно, внутримышечно, подкожно, внутрикожно, и т.д., в то время как препараты для наружного применения включают суппозитории и т.д. Доза противоревматического средства особо не устанавливается, но может быть соответствующим образом определена в зависимости от лекарственной формы, способа введения,цели использования и возраста, массы тела, состояния пациента и т.д. Обычно, однако, количество, по меньшей мере, одного соединения,выбранного из циклопентенона, его оптически активного вещества или его соли, содержащееся в препарате для взрослого, составляет 0,1 мкг 200 мг/кг в день. Как нечто само собой разумеющееся, доза может варьироваться, в зависимости от различных факторов, и поэтому в некоторых случаях доза, меньшая вышеупомянутой, может оказаться достаточной, в то время как в других случаях может быть необходима доза, большая, чем вышеупомянутая. Средство настоящего изобретения можно применять перорально как таковое и, кроме того, средство можно принимать ежедневно, добавляя в обычный продукт питания и/или напиток. Помимо вышеупомянутых противоревматической активности и ингибирующей активности в отношении хронического суставного ревматизма, циклопентенон, его оптически активное вещество или его соль имеет различную физиологическую активность, такую как противовоспалительная активность в отношении артрита, и т.п., активность в ингибировании каррагенного отека, активность в ингибировании продуцирования фактора некроза опухоли, активность в усилении продуцирования интерлейкина-10, активность в ингибировании продуцирования моноксида азота,апоптозиндуцирующую активность в синовиальных клетках, активность в индуцировании продуцирования Fas-антигена, иммуномодулирующую активность, такую как активность в ингибировании гиперчувствительности замедленного типа, активность в ингибировании пролиферации лимфоцитов, активность в ингибировании реакции смешанных лимфоцитов, активность в ингибировании продуцирования IgE, активность в ингибировании топоизомеразы, и т.п. Таким образом, фармацевтическое средство, такое как 9 противовоспалительное средство или контрацепт воспаления, ингибитор продуцирования фактора некроза опухоли или контрацепт продуцирования фактора некроза опухоли, усилитель продуцирования интерлейкина-10, ингибитор продуцирования моноксида азота, индуктор продуцирования Fas-антигена, иммуномодулятор, ингибитор продуцирования IgE, ингибитор гиперчувствительности замедленного типа и ингибитор топоизомеразы, содержащее, по меньшей мере, одно соединение, выбранное из циклопентенона, его оптически активного вещества или его соли может быть составлено в фармацевтические препараты тем же самым способом, как в случае вышеупомянутого противоревматического средства, и может применяться тем же самым способом, как и вышеупомянутое противоревматическое средство. Доза этих препаратов может соответствующим образом определяться, в зависимости от вышеупомянутого противоревматического средства. Например, в случае противовоспалительного средства и ингибитора продуцирования фактора некроза опухоли, количество одного или нескольких соединений, выбранных из циклопентенона, его оптически активных веществ или их солей, содержащееся в препарате,составляет предпочтительно 10 пг-50 мг/кг в день для взрослого, в то время как, в случае ингибитора продуцирования моноксида азота, количество одного или нескольких соединений,выбранных из циклопентенона, его оптически активных веществ или их солей, содержащееся в препарате, составляет предпочтительно 0,1 мкг-20 мг/кг в день для взрослого. В зависимости от цели использования, количество эффективного компонента в препарате можно контролировать. Эти средства можно применять перорально как таковые и, кроме того, средство можно также принимать ежедневно, добавляя в обычный продукт питания и/или напиток. Ревматизм представляет собой аутоиммунное заболевание, где препятствие имеет место в перисотеальных (perisoteal) клетках и хрящевых клетках, и противоаллергическое средство настоящего изобретения также используют в качестве терапевтического средства для аутоиммунных заболеваний. Циклопентенон, его оптически активное вещество или его соль ингибирует продуцирование фактора некроза опухоли, который, как полагают, непосредственно вызывает воспаление при органоспецифических аутоиммунных заболеваниях, таких как хронический ревматоидный артрит или воспалительные заболевания,и усиливает продуцирование интерлейкина-10,который является Тh1 ингибирующим цитокином. Соответственно, симптомы воспаления,такого как ревматизм, который представляет собой органоспецифическое аутоиммунное заболевание, в частности, хронический ревматоидный артрит, ослабляются; показатели воспа 001798 10 ления, такие как уровень С-реактивного белка(CRP), уровень ревматоидного фактора (RF) и скорость оседания эритроцитов (седиментация крови), в значительной степени снижаются; и осложнения, такие как дисбазия (расстройство ходьбы), также значительно снижаются. Фактор некроза опухоли определяют как фактор, который индуцирует геморрагический некроз в месте опухоли, и в настоящее время он признан как цитокин, который прямо участвует в биоиммунитете, вызванном воспалением, и иммунной функции. Нарушение в регуляции продуцирования этого фактора некроза опухоли вызывает различные неудобства для хозяина, и избыток или немодулируемое продуцирование фактора некроза опухоли связано с многими болезнями, включая ревматоидный артрит, ревматический миелит, остеоартрит, подагрический артрит,сепсис,септический шок,эндоксиновый бактериально-токсический шок,сепсис грамотрицательными бактериями, синдром токсического шока, церебральная малярия,хроническая пневмония, реакция "трансплантат против хозяина", реакция отторжения аллогенного трансплантата и другие лихорадочные состояния и мышечная боль при инфекционных болезнях, таких как грипп, вторичная кахексия при инфекции или злокачественой опухоли,вторичная кахексия при синдроме приобретенного иммунного дефицита (СПИД, AIDS),СПИД, СПИД-родственный синдром, келоидное образование, неспецифический язвенный колит,рассеянный склероз, аутоиммунный сахарный диабет и системная красная волчанка [MolecularMedicine, volume 33, pages 1010-1020 and pages 1182-1189(1996)]. Противоревматическое средство настоящего изобретения используют для лечения болезней, которые опосредованы или усугубляются фактором некроза опухоли. Кроме того настоящее изобретение предлагает способ контролирования продуцирования фактора некроза опухоли, где, по меньшей мере, одно соединение, выбранное из циклопентенона, его оптически активного вещества и его соли, используют в качестве эффективного компонента. Кроме того, настоящее изобретение предлагает продукт питания или напиток, содержащий, по меньшей мере, одно соединение, выбранное из циклопентенона, его оптически активного вещества или соли его, который ослабляет симптом болезни или который предотвращает болезнь,опосредованную или усугубляемую фактором некроза опухоли. Моноксид азота (в дальнейшем аббревиатура NO) представляет собой основной фактор эндотелий-зависимого расслабляющего фактора(1987). Настоящее изобретение предлагает фармацевтическое средство, содержащее, по меньшей мере, одно соединение, выбранное из циклопентенона, его оптически активного вещества и его соли, в качестве эффективного компонента 11 для лечения или профилактики болезней, требующих ингибирования продуцирования NO.He существует конкретного ограничения для болезней, которые требуют ингибирования продуцирования NO, и примерами их являются системная гипотензия, вызванная токсическим шоком или лечением определенным цитокином,понижение кровяного давления, аутоиммунные болезни, воспаление, артрит, ревматоидный артрит, сахарный диабет, воспалительные кишечные заболевания, недостаточность функции кровеносных сосудов, этиологическое расширение кровеносного сосуда, повреждение тканей,сердечно-сосудистая ишемия, чувствительность к боли, церебральная ишемия, болезни, вызванные ангиогенезом, рак, и т.п. Сюда входят болезни, которые упоминаются в публикациях выложенных заявок на патент Японии Hei09/504524; 09/505288; 08/501069; 08/512318; и 06/508849. Ингибитор продукции NO, содержащий,по меньшей мере, одно соединение, выбранное из циклопентенона, его оптически активного вещества или соли его, в качестве эффективного компонента, используют для изучения механизма продуцирования NO и механизма биологической активности NO и, кроме того, его можно использовать для скрининга веществ, участвующих в механизме продуцирования NO. Циклопентенон, его оптически активное вещество или соль его имеет ингибирующую активность продуцирования NO в NOпродуктивных клетках. Например, когда эндотоксин (липополисахарид или ЛПС) добавляют в клеточный штамм макрофага, экспрессируется индуцируемая NO-синтетаза (NOS), и NO секретируется в среду, в то время как когда ЛПС добавляют при совместном присутствии циклопентенона, производных циклопентенона или их оптически активных веществ, продуцированиеNO ингибируется. Когда продуцирование NO вызывается обработкой ЛПС, степень выживания клеток понижается вследствие цитопатологической активности NO, но если циклопентенон, его оптически активное вещество или соль его добавляют во время обработки ЛПС, то продуцирование NO уменьшается, также как и повреждение клеток. Ангиогенез является существенным для роста твердой карциномы, и ангиоэндотелиальный фактор роста/сосудистый эндотелиальный фактор роста (VEGF) играет важную роль на этой стадии. В различных раковых клеткахVEGF индуцируется с помощью NO. Когда циклопентенон, его оптически активное вещество или его соль ингибирует продуцированиеNO, продуцирование VEGF раковых клеток также ингибируется и, как результат, ингибируется ангиогенез вокруг раковых тканей. Когда циклопентенон, его оптически активное вещество или соль его вводят мыши, у которой твердая злокачественная опухоль образована путем под 001798 12 кожной трансплантации раковых клеток, образование кровеносного сосуда вблизи раковых тканей становится недостаточным, и злокачественная опухоль отслаивается. Нитрозоамины представляют собой ряд соединений, которые синтезируют введением нитрозогруппы во вторичный амин, и известно несколько сотен нитрозоаминов. Многие из них повреждают ДНК и обладают канцерогенным действием на животных. Сообщается, что нитрозоамины в значительной степени связаны с образованием рака у человека и обычно образуются в желудке путем реакции нитрита с амином. Даже в физиологических условиях при нейтральных рН NO взаимодействует с амином с получением нитрозоамина. Кроме того, продуцирование NO возрастает у пациентов, инфицированных восточной печеночной двуусткой, и у пациентов, страдающих циррозом печени, который в значительной степени связан с раком иммунологически. Таким образом, когда увеличение продуцирования NO подавляется введением циклопентенона, его оптически активного вещества или его соли, можно предотвратить образование рака, особенно в группе высокого риска. Таким образом, циклопентенон, его оптически активное вещество или его соль ингибирует противораковое действие в двух стадиях ингибирования канцерогенеза и, кроме того,ингибирования ангиогенеза в раковых тканях. Кроме того, NO индуцирует отек, который является характерным при воспалительных повреждениях, т.е., проницаемость кровеносного сосуда [Maeda, et al., Japanese Journal of CancerResearch, volume 85, pages 331-334 (1994)], и кроме того, индуцирует биосинтез простагландинов, которые являются медиаторами воспаления [Salvemini, et al., Proceedings of NationalAcademy of Science, U.S.A., volume 90, pages 7240-7244 (1993)]. С другой стороны, считают,что NO быстро взаимодействует с супероксидными радикалами, и полученный пероксинитрит вызывает образование затронутых воспалением клеток и тканевые повреждения. Когда активированные иммунные клетки захватываются органом и из них высвобождается цитокин, индуцируется продукция NO. Инсулинозависимый сахарный диабет представляет собой болезнь, вызванную специфическим разрушением -клеток Лангерганса, и разрушение осуществляется с помощью NO. Кроме того,синовиальная жидкость пораженных суставов пациентов, страдающих хроническим суставным ревматизмом, остеосуставным ревматизмом, подагрическим артритом и артритом, сопровождаемом болезнью Бехчета, содержит более высокие концентрации NO по сравнению с синовиальной жидкостью в нормальных суставах таких пациентов или в суставах здоровых индивидуумов. Когда циклопентенон, его оптически активное вещество или соль его применяют к таким пациентам, продуцирование NO в 13 пораженных суставах ингибируется, и симптом ослабляется. Во время церебральной ишемии и после повторной перфузии продуцирование NO возрастает и, как результат, церебральные ткани повреждаются. Когда циклопентенон, его оптически активное вещество или соль его вводят пациенту во время церебральной ишемии, поражение церебральных тканей снижается, и прогноз улучшается. Антиген клеточной поверхности, который называют Fas-антигеном (АРО-1 антиген илиCD95), привлекает к себе внимание как молекула, способствующая индукции апоптоза [Cell,volume 66, pages 233-243 (1991); J. Exp. Med.,volume 169, pages 1747-1765 (1989); J. Biol.Fasантиген экспрессируется в иммунных клетках, таких как клетки тимуса. Т-клетки, цитотоксические Т-клетки, В-клетки и NK-клетки. Против инвазии чужеродного не-аутоантигенад,иммунная система индуцирует иммунную реакцию, посредством чего не-аутоантиген исключается. Однако против аутоантигена иммунная реакция не развивается, и устанавливается самотолерантность. Это потому, что лимфоцитарные стволовые клетки, имеющие аутореактивность,подвергаются удалению клонов, что является негативным отбором, при помощи которого исключение происходит путем гибели клеток с помощью апоптоза. Однако когда эти клетки не подвергаются апоптозу вследствие некоторой аномалии (патологии) в живом организме, такой как генетическая недостаточность Fas-антигена,аутореактивные Т-клетки, например, аккумулируются в периферических областях. В нормальном живом организме самотолерантность имеет место даже для В-клеток, которые являются клетками, ответственными за иммунитет, и эти аутореактивные В-клетки обычно погибают вследствие апоптоза, но, когда аутореактивные В-клетки не подвергаются апоптозу вследствие патологии, такой как генетическая недостаточность Fas-антигена, аутореактивные В-клетки аккумулируются в периферических областях. Кроме того, в случае суставного ревматизма вышеупомянутая аномалия в аутореактивных лимфоцитах и аномалия в кругообороте синовиальных клеток представляют собой некоторые из причин заболеваний. Индуктор продуцирования Fas-антигена, в котором, по меньшей мере, одно соединение,выбранное из циклопентенона, его оптически активного вещества или соли его, представляет эффективный компонент, используют для индуцирования апоптоза ненужных клеток для построения живого организма, которые не выделяются из живого организма вследствие аномалий кругооборота и аутореактивных лимфоцитов, и может быть использован в способе инду 001798 14 цирования продуцирования Fas-антигена. Средство, содержащее, по меньшей мере, одно соединение, выбранное из циклопентенона, его оптически активного вещества или его соли,также используют в качестве эффективного компонента как средство для профилактики или лечения болезней, сопровождаемых аномальным продуцированием Fas-антигена. В настоящем изобретении нет особого ограничения для болезней, сопровождаемых аномальным продуцированием Fas-антигена, и примерами их являются суставной ревматизм и аутоиммунные заболевания, вызванные аутореактивными Тклетками и аутореактивными В-клетками, и т.п.,включая болезни, упомянутые в описанииW097/0965. Циклопентенон, его оптически активное вещество или его соль имеют иммуномодулирующую активность, такую как энхансерная активность продуцирования интерлейкина-10,активность в ингибировании реакции гиперчувствительности замедленного типа, активность в ингибировании пролиферации лимфоцитов, активность в ингибировании реакции смешанных лимфоцитов, активность в ингибировании продуцирования IgE и активность в ингибировании отека, вызванного каррагеном, и иммуномодулятор, содержащий, по меньшей мере, одно соединение, выбранное из циклопентенона, его оптически активного вещества или соли его, в качестве эффективного компонента, используют в качестве средства для лечения или профилактики болезней, вызванных аномалией иммунной системы и иммунного фактора. Таким образом, как результат снижения продукции интерлейкина-10, активируется Тh1,и индуцируется воспаление по типу Th1 доминантного аутоиммунитета. Это воспаление участвует в органоспецифических аутоиммунных заболеваниях, таких как нефрит и гепатит, а также отторжение трансплантата и аллергический контактный дерматит. Вышеупомянутый иммуномодулятор усиливает продуцирование интерлейкина-10 и ингибирует Тh1-активность,тем самым является полезным для лечения и профилактики этих заболеваний. Пролиферация лимфоцитов представляет собой реакцию, в которой митоген связывается с рецептором на поверхности лимфоцита, активируя лимфоцит, посредством чего промотируется деление и рост его. Реакция смешанных лимфоцитов является реакцией, в которой различные штаммы лимфоцитов, полученных от животных одного и того же вида, подвергают смешанному культивированию в результате чего происходит активация лимфоцитов вследствие несоответствия основных тканеспецифических антигенов и индуцируется деление и рост лимфоцитов. Вышеупомянутый иммуномодулятор ингибирует эти реакции и, в частности, является полезным для лечения или профилактики хронических аутоиммунных болезней, 15 вызванных аномальной промоцией лимфоцитов,таких как хронический нефрит, хронический колит, сахарный диабет типа I и хронический суставной ревматизм и, кроме того, его используют для ингибирования отторжения трансплантата. Модель карраген-индуцированного отека стопы представляет реакцию, в которой карраген, который является индуктором воспаления,подкожно инъецируют в лапы, чтобы индуцировать воспалительные клетки, такие как макрофаг и нейтрофилы, тем самым проницаемость кровеносного сосуда повышается под действием воспалительных факторов, продуцируемых этими клетками, вызывая отек. Ингибирующее действие вышеупомянутого иммуномодулятора на образование отека используют для лечения или профилактики болезней, требующих контроля за повышением проницаемости кровеносного сосуда, таких как хронический суставной ревматизм. При аллергических заболеваниях, представленных астмой и атопическим дерматитом, высвобождение химических медиаторов из тучных клеток играет важную роль в аллергической реакции. Эта реакция индуцируется, когда IgE связывается с рецепторами на клеточной мембране, образуя поперечные сшивки, и вышеупомянутый иммуномодулятор ингибирует продуцирование IgE и является весьма полезным для улучшения симптомов и/или профилактики болезней, опосредованных или усугубляемых продуцированием IgE, таких как аллергические болезни, вызываемые IgE, включая бронхиальную астму, аллергический ринит, атонический дерматит, аллергический конъюнктивит, крапивница, анафилактический шок, и т.п. Кроме того, вышеупомянутый иммуномодулятор ингибирует реакцию гиперчувствительности замедленного типа и является полезным для лечения и профилактики болезней,сопровождаемых гиперчувствительностью замедленного типа, таких как контактная гиперчувствительность, аллергический контактный дерматит,бактериальная аллергия, грибковая аллергия, вирусная аллергия, лекарственная аллергия, тиреоидит и аллергический энцефалит. В настоящем изобретении циклопентенон,его оптически активные вещества или соль его и вещество, выбранное из обработанного нагреванием продукта циклопентенона и частично очищенного циклопентенона из указанного обработанного нагреванием продукта, используют для того, чтобы предложить функциональный продукт питания или напиток, имеющий противоревматическую активность, противовоспалительную активность, ингибирующую активность в продуцировании фактора некроза опухоли, активность, усиливающую продуцирование интерлейкина-10, ингибирующую активность в продуцировании моноксида азота, апоптоз-индуцирующую активность в синовиальных клетках, индуцирующую активность в продуцировании Fаs-антигена, иммуномодулирующую 16 активность, такую как ингибирующая активность гиперчувствительности замедленного типа, ингибирующая активность пролиферации лимфоцитов, ингибирующая активность в реакции смешанных лимфоцитов, ингибирующая активность в продуцировании IgE и ингибирующая активность в отношении топоизомеразы, такой как продукт питания или напиток для улучшения при ревматизме, продукт питания или напиток для ослабления воспаления, продукт питания или напиток для ингибирования продуцирования фактора некроза опухоли, продукт питания или напиток для усиления продуцирования интерлейкина-10, продукт питания или напиток для ингибирования продуцирования моноксида азота, продукт питания или напиток для индуцирования продуцирования Fasантигена, продукт питания или напиток для иммуномодуляции, продукт питания или напиток для ингибирования продуцирования IgE и продукт питания или напиток для ингибирования топоизомеразы. Нет особого ограничения для способа получения продукта питания или напитка настоящего изобретения, но можно применять способы варки, переработки и обычно используемые способы получения продукта питания или напитка при условии, что, по меньшей мере, одно соединение, выбранное из циклопентенона, оптически активного вещества его или его соли,имеющее физиологическое действие, такое как противоревматическое действие, содержится в полученном продукте питания или напитке в качестве эффективного компонента. Продукт питания или напиток, где одно или несколько соединений, выбранных из циклопентенона, его оптически активных веществ или его солей, содержится/содержатся в нем, добавленное туда и/или разбавленное в нем, определяют как продукт питания или напиток настоящего изобретения. Нет особого ограничения на форму продукта питания или напитка настоящего изобретения, когда речь идет о том, что, по меньшей мере, одно соединение, выбранное из циклопентенона, оптически активного вещества его или его соли, содержится в нем, добавленное туда и/или разбавленное в нем, в качестве эффективного компонента. Таким образом, форма включает в себя таковые, которые можно принимать перорально, такие как таблетки, гранулы, капсулы, гель или золь. Благодаря тому, что продукт питания или напиток настоящего изобретения имеет физиологические активности, по меньшей мере, одного или нескольких соединений, выбранных из циклопентенона, его оптически активных веществ или солей его, такие как противоревматическая активность, противовоспалительная активность, ингибирующая активность продуцирования фактора некроза опухоли, активность,усиливающая продуцирование интерлейкина 17 10, активность, ингибирующая продуцирование монооксида азота, активность, индуцирующая продуцирование Fas-антигена, иммуномодулирующая активность, такая как активность, ингибирующая гиперчувствительность замедленного типа, активность, ингибирующая продуцирование IgE и ингибирующая активность по отношению к топоизомеразе, и т.п., он представляет собой оздоравливающий продукт питания или напиток, имеющий симптом-улучшающее действие на заболевания, чувствительные к циклопентенону, его оптически активному веществу или его соли, и профилактическое действие на указанные заболевания, и, кроме того, он является продуктом питания или напитком, который используют для поддержания живого организма. Теперь возможно в соответствии с настоящим изобретением, чтобы в продукте питания или напитке содержалось соответствующее количество циклопентенона или оптически активного вещества его или соли его, имеющего физиологическую активность. Благодаря физиологическому действию этих соединений, такому как апоптоз-индуцирующая активность в синовиальных клетках, индуцирующая активность продуцирования Fas-антигена, ингибирующая активность продуцирования фактора некроза опухоли, ингибирующая активность продуцирования NO и активность в улучшении и/или профилактике симптома ревматизма, в частности,симптома хронического суставного ревматизма,продукт питания или напиток настоящего изобретения, действительно, является полезным для улучшения или предотвращения симптомов ревматизма, осложнения, связанного с ревматизмом, трудности в ходьбе, и т.п. Не обнаружено никакой токсичности при использовании соединения настоящего изобретения, даже когда применяли дозу, которая является эффективной для достижения этих физиологических активностей. В случае перорального применения, например, не наблюдалось смертного случая у крыс при разовом пероральном введении 100 мг/кг любого из циклопентенона, оптически активного вещества его или его соли. Примеры Настоящее изобретение далее иллюстрируется посредством нижеследующих примеров,хотя настоящее изобретение никоим образом не ограничивается этими примерами. В данном случае, "%", используемый в примерах, означаетSigma) (10 г) растворяют в 1 л воды, нагревают при 121 С в течение 4 ч и концентрируют в вакууме приблизительно до 10 мл. Этот объем смешивают с 40 мл верхнего слоя 3:2:2 смеси бутилацетата, уксусной кислоты и воды и центрифугируют,и полученную жидкость 001798 18 супернатант концентрируют в вакууме приблизительно до 10 мл. Вышеупомянутый экстракт наносят на силикагель колонки (BW-300SP; 2 х 28 см; произв.Fuji Silycia) для колоночной хроматографии и разделяют, используя верхний слой 3:2:2 смеси бутилацетата, уксусной кислоты и воды в качестве элюента при скорости протока около 5 мл/мин под давлением 0,2 кг/см 2, используя компрессор. Фракционирование проводят, получая объем одной фракции 10 мл, и часть каждой фракции анализируют с помощью тонкослойной хроматографии, после чего циклопентенон высокой чистоты содержится в 61-ой-80-ой фракциях. Эти фракции собирают, концентрируют в вакууме, экстрагируют 40 мл хлороформа и экстракт концентрируют в вакууме, получая 100 мг циклопентенона. Фракцию разделяют с помощью ВЭЖХ с нормальной фазой, используя колонку Palpack тип S и, когда детектирование проводят при ультрафиолетовом поглощении 215 нм, чистота,как установлено, составляет 98%. Вышеупомянутый циклопентенон (113,9 мг) растворяют в 2,85 мл этанола. К этому этанольному раствору добавляют 3,85 мл смеси гексан/этанол (94/6), получая раствор циклопентенона (17 мг/мл). Этот раствор фильтруют через фильтр 0,5 мкм, чтобы получить раствор образца для ВЭЖХ с оптическим разделением. Этот раствор образца подвергают ВЭЖХ с оптическим разделением, каждую из фракций (-)циклопентенона в более раннем пике и (+)циклопентенона в более позднем пике собирают и выпаривают досуха в вакууме, получая 43,2 мг(-)-циклопентенона и 43,0 мг (+)-циклопентенона. Условия для ВЭЖХ с оптическим разделением. Колонки: Chiral Pack AS (произв. Daicel) 2,0 см х 25,0 см. Температура колонки: 40 С. Подвижная фаза: гексан/этанол (94/6). Скорость протока: 14,0 мл/мин. Детектирование: УФ 210 нм. Количество загружаемого образца: 150 мкл(2,55 мг). Каждая из полученных (фракций) (-)циклопентенона и (+)-циклопентенона содержит около 1% энантиомера и поэтому их еще раз подвергают оптическому разделению в вышеупомянутых условиях. В результате, получают 19,7 мг (-)-циклопентенона, не содержащего энантиомера, из 30,0 мг (-)-циклопентенона более раннего пика, в то время как, из 37,4 мг (+)циклопентенона более позднего пика получают 27,7 мг (+)-циклопентенона, не содержащего энантиомера. В данном случае, времена элюирования при ВЭЖХ с оптическим разделением для (-)-циклопентенона и (+)-циклопентенона составляли 33 мин и 40 мин, соответственно. 19 Пример 1. После того как пациенту-женщине (возраста 56 лет), у которой пять лет назад был диагностирован хронический суставной ревматизм и которую лечили при помощи стероидов, противоревматических средств, седативных противовоспалительных средств и т. д. в качестве терапевтических средств, но при этом не наблюдали улучшения в симптомах заболевания, причем значение CRP составляло не менее чем 3 мг/дл, значение RF составляло не менее чем 300 Е/мл, и скорость оседания эритроцитов составляла не менее чем 20 мл/ч, и которая практически была прикована болезнью к постели вследствие трудности передвижения, давали 50 мл(содержащие 2 мг циклопентенона) напитка,полученного в соответствии с примером 12-(2),один раз в день в течение одного месяца, были отмечены гематологические улучшения в симптомах хронического суставного ревматизма,таких как данные CRP, данные RF и скорость оседания эритроцитов. Кроме того кинетическая функция повседневной жизни, такая как ходьба,была значительна улучшена наряду с понижениями в значениях вышеупомянутых показателей. Пример 2. Клетку DSEK(клеточный штамм, хранимый вMedical Center, Saitama College of Medicine), которая представляла собой штамм фибробласта, созданный из синовиальной мембраны пациента, страдающего хроническим суставным ревматизмом, инкубируют в модифицированной Iscob среде Dulbecco (IMDM,произв. Gibco, 12440-053), содержащей 10% фетальную бычью сыворотку (FCS, произв. Gibco, 26140079) при 37 С в присутствии 5% газа-диоксида углерода до слияния и затем клетки собирают, отслаивая с помощью трипсин-EDTA (произв. Gibco, 25300054). Клетки суспендируют в вышеупомянутой среде до получения 25000 клеток/мл и по 100 мкл помещают в каждую лунку 96-луночного титрационного микропланшета. После инкубации в течение пяти дней, когда практически достигается состояние слияния, среду отделяют и затем добавляют вышеупомянутую среду, содержащую 2,5, 5, 10, 20 или 30 мкМ циклопентенона. После инкубирования в течение 24, 48 или 72 ч туда добавляют 10 мкл премиксаWST-1 (произв. Takara Shuzo, MK400) и затем эту смесь подвергают взаимодействию при 37 С в течение 4 ч. Значение, полученное путем вычитания абсорбции при 650 нм (А 650) из абсорбции при 450 нм(А 450), определяют как степень роста клетки. Результат представлен в таблице 1. Концентрация (мкМ) 0 2,5 5 10 20 30 В обоих случаях инкубирования как в течение 24 ч, так и 48 ч, рост клетки ингибировался в секциях, где добавляли 5 мкМ или более циклопентенона по сравнению с контролем, где добавляли воду, и в секции, где добавляли 10 мкМ циклопентенона, было отмечено продуцирование апоптотических тел. В секции, где добавляли 20 мкМ или более циклопентенона,жизнеспособные клетки едва определялись. Как таковой, циклопентенон демонстрировал апоптоз-индуцирующее действие и ингибирующее рост действие на синовиальные клетки. Кроме того,(-)-циклопентенон иTIB-152) и Molt-3 клеток (ATCC CRL-1552),которые представляют собой клеточный штамм Т-клеточного лейкоза человека, инкубируют в среде RPMI-1640 (произв. Gibco BRL), содержащей 10% фетальную телячью сыворотку(ФТС, FCS, произв. Bio Whittaker) при 37 С в присутствии 5% СO2, и туда добавляют 0,5, 10 или 20 мкМ циклопентенона с последующим инкубированием в течение еще 24 ч. Рост клеток измеряют МТТ методом [Mosmann, et al.: J.(1983)], где степень роста клеток определяют по поглощению 560 нм. Результат оказался таким, что в обоих клеточных штаммах, рост клеток ингибировался примерно на 50% и не менее чем 75% в секциях,где добавляли 10 мкМ и 20 мкМ циклопентенона, соответственно, по сравнению с контролем,где добавляли воду. В случае, когда добавляли 5 мкМ или менее циклопентенона, существенного влияния на рост клеток не обнаружено. Как таковой, циклопентенон ингибировал,концентрационно зависимым способом, рост клеток Jurkat и клеток Molt, которые представляют собой клеточные штаммы Т-клеточного лейкоза. Результаты представлены на фиг. 1 и фиг. 2. Фиг. 1 демонстрирует влияние циклопентенона на рост клеток Jurkat, в то время как фиг. 2 демонстрирует влияние циклопентенона на рост клеток Molt. На фиг. 1 и фиг. 2, абсциссса обозначает концентрацию циклопентенона (мкМ), в то время как ордината обозначает поглощение при 560 нм.(2) Влияние циклопентенона на экспрессию Fas-антигена (продуктивная индукция) в клетках Jurkat и клетках Molt измеряют следующим образом. В 10% FCS-содержащей среде RPMI-1640, содержащей 0, 1, 5, 10 или 20 мкМ циклопентенона или GM, 5 х 105 клеток/мл клеток Jurkat или Moll-3-клеток инкубируют при 37 С в течение 24 ч в присутствии 5% СO2 и затем подвергают двуступенчатому иммунному прокрашиванию, используя анти-Fas антитело(произв. Boehringer-Ingelheim), в соответствии с методом Munker [Munker, R.: Ann. Hematol.,volume 70, pages 15-17 (1995)]. Интенсивность флуоресценции окрашенных 1 х 104 клеток измеряют проточным цитометром (Orthocytron; произв. Ortho DiagnosticSystems) и рассчитывают уровень клеток, показывающий заданную или более высокую интенсивность флуоресценции, что и отвечает Fasантиген-экспрессирующим клеткам. Результат оказался таким, что в обоих клеточных штаммах уровеньFas-антигенэкспрессирующих клеток увеличивается концентрационно-зависимым способом в тех случаях, когда добавляют 1-20 мкМ циклопентенона. Результаты представлены на фиг. 3 и фиг. 4. Таким образом, фиг. 3 показывает экспрессиюFas-антигена в Molt-3-клетках, в то время как фиг. 4 показывает экспрессию в клетках Jurkat. На фиг. 3 и фиг. 4, абсцисса обозначает концентрацию циклопентенона (мкМ), в то время как ордината обозначает уровень (%) Fas-антигенэкспрессирующих клеток, посредством чего отмечается действие циклопентенона на индуцирование продуцирования Fas-антигена.(3) Molt-3-клетки инкубируют в течение 1,3, 6, 12 или 24 ч после добавления 10 мкМ циклопентенона, и затем измеряют уровень клеток,которые экспрессируют Fas-антиген. Результат был таким, что в том случае, когда добавляли 10 мкМ циклопентенона, уровеньFas-антиген-экспрессирующих клеток начинал возрастать спустя час после инкубации и постепенно продолжал увеличиваться до 24 ч после инкубации. Результат представлен на фиг. 5. Соответственно, фиг. 5 показывает изменение в уровнеFas-антиген-экспрессирующих клеток, когда инкубацию проводят после добавления 10 мкМ циклопентенона в Molt-3-клетки, где абсцисса обозначает время инкубации (часы), в то время как ордината обозначает уровень (%) Fasантиген-экспрессирующих клеток. Таким образом, как указано в примере 3(1) до (3), было установлено действие циклопентенона на индуцирование экспрессии Fasантигена. Кроме того, (-)-циклопентенон и (+)циклопентенон дают аналогичные результаты. Пример 4. Модели вызванного каррагеном отека стопы, которые представляли собой животную модель хронического суставного ревматизма, получают, как следует ниже, используя крыссамцов Lewis [приобретенные у Seac-Yoshitomi в возрасте пяти недель (масса тела: около 130 г) и затем подвергнутые предварительному выкармливанию в течение одной недели] и проводят оценку испытываемых лекарственных средств. Крысам, которые голодали 18 ч до начала эксперимента, вводят перорально 10 мл/кг циклопентенона, который готовят на дистиллиро 001798 22 ванной воде (произв. Otsuka Pharmaceutical),получая 1 и 5 мг/мл. Спустя 0,5 ч после введения испытываемого лекарственного средства 100 мкл/крысу 1% суспензии каррагена (произв. Wako) в физиологическом солевом растворе (произв. OtsukaPharmaceutical) инъецируют в правую лапу, чтобы вызвать отек стопы. Через 3 ч после инъекции каррагена измеряют объем правой лапы крысы с помощью устройства для измерения объема стопы (произв. UGO BASILE). В данном случае измеряемый объем выражают, рассчитывая степень увеличения от объема правой лапы каждой крысы, измеряемого до введения каррагена. Результат представлен на фиг. 6. Соответственно, на фиг. 6 представлена взаимосвязь между количеством циклопентенона и степенью увеличения отека стопы, где ордината обозначает степень увеличения (%) , в то время как абсцисса обозначает дозу циклопентенона (мг/кг). Циклопентенон демонстрирует значительную ингибирующую активность на отек стопы при дозе 50 мг/кг. Кроме того, (-)циклопентенон и (+)-циклопентенон оказывают аналогичные действия. Пример 5.Abortus equi, растворенный в физиологическом солевом растворе, вводят внутрибрюшинно (0,1 мг/кг) мышам-самкам линии CDF1 20 недельного возраста, чтобы получить модели эндоксинового бактериально-токсического шока. Циклопентенон вводят либо внутрибрюшинно, либо перорально при дозе 30 мг/кг за 30 мин до введения ЛПС. С другой стороны, контрольной группе его не вводят. Спустя 90 мин после введения ЛПС отбирают кровь у мышей и отделяют сыворотку. Затем измеряют количество фактора некроза опухоли в сыворотке с помощью набора TNF-ELISA (произв. Genzyme) и оценивают действие ингибирования на продуцирование фактора некроза опухоли при введении циклопентенона. Результат представлен в табл. 2. Так, по сравнению с контрольной группой, концентрации фактора некроза опухоли в сыворотке были низкими в группах, которым вводили циклопентенон, как в группах внутрибрюшинного введения, так и в группах перорального введения,иными словами продуцирование фактора некроза опухоли значительно подавляется при введении циклопентенона. Контрольная группа 5 Группа, которой вводили цик 5 лопентенон внутрибрюшинно Группа, которой вводили 5 1,80 0,30 циклопентенон перорально: имеющее значительное отличие по отношению к контролю при р 0,001: имеющее значительное отличие по отношению к контролю при р 0,01(2) ЛПС инъецируют внутрибрюшинно (10 мкг/мышь) мышам-самкам CDF1 в возрасте восьми недель и получают модели эндоксинового бактериально-токсического шока. Циклопентенон вводят подкожно при дозе 0,03, 0,3,3 и 30 мг/кг за пятнадцать минут до введения ЛПС (причем каждая группа состоит из четырех мышей). Спустя один час после введения ЛПС отбирают кровь у мышей, отделяют сыворотку и измеряют количество фактора некроза опухолив сыворотке и количество интерлейкина-10 при помощи коммерчески доступного набораELISA (произв. Endogen). Результат представлен в табл. 3. Таким образом, циклопентенон подавляет увеличение концентрации фактора некроза опухолив сыворотке при введении ЛПС дозозависимым способом. Кроме того, по сравнению с контрольной группой, которой вводили дистиллированную воду (по четыре мыши в каждой группе), концентрации интерлейкина-10 в сыворотке значительно возрастали в группе, которой вводили циклопентенон (30 мг/кг). Доза (мг/кг) Таблица 3 Фактор некКоличество роза опухоли интерлейки(нг/мл) на-10 в сывоСреднееСО ротке (нг/мл) СреднееСО(3) Парафиновое масло (Cosmo Bio) (2 мл) вводят внутрибрюшинно мышам-самкам CDF1 в возрасте восьми недель, чтобы индуцировать М брюшины. Спустя одну неделю после введения парафинового масла 4 мл Среды RPMI1640 (Gibco) вводят с помощью вливания внутрибрюшинно, хорошо массируют и выделяют,чтобы получить брюшные клетки. Брюшные клетки дважды промывают средой RPMI-1640 и суспендируют в среде RPMI164, содержащей 10% фетальную телячью сыворотку (FCS; High-Clone), доводя концентрацию клеток до 1 х 106 клеток/мл. Раствор клеток(1 мл), полученный как таковой, высевают на 24-луночный планшет и инкубируют в СO2 инкубаторе при 37 С в течение двух часов. Не 24 адгезивные клетки, содержащиеся в супернатанте после инкубации, удаляют, а адгезивные клетки используют в качестве брюшных М. В каждую лунку планшета добавляют по 800 мкл среды RPMI-1640, содержащей 10%FCS, затем добавляют по 100 мкл 1, 10, 100 и 1000 мкМ циклопентенона, растворенного в физиологическом солевом растворе (произв.Otsuka Pharmaceutical), и проводят инкубацию в СO2-инкубаторе при 37 С в течение одного часа. После инкубации добавляют 100 мкл 100 нг/мл ЛПС (произв. Sigma) и проводят инкубацию в течение еще 24 ч. После завершения инкубации супернатант отделяют оттуда, и количество TNF-, продуцированного в ней, определяют, используя коммерчески доступный наборELISA (произв. Endogen). Результат представлен на фиг. 7. Так, фиг. 7 демонстрирует взаимосвязь между концентрацией циклопентенона и продуцируемым количеством фактора некроза опухоли, где ордината обозначает количество фактора некроза опухоли(пг/мл), в то время как абсцисса обозначает концентрацию циклопентенона (мкМ) каждого образца. Циклопентенон при концентрации не менее чем 10 мкМ значительно ингибирует продуцирование фактора некроза опухоли из брюшного макрофага мыши, вызванное ЛПС. Как показано в вышеупомянутом примере 5-(1) до (3), циклопентенон имеет ингибирующую активность продуцирования фактора некроза опухоли и активность, повышающую продуцирование интерлейкина-10. Кроме того, (-)циклопентенон и (+)-циклопентенон демонстрируют одинаковые результаты. Пример 6. Ингибирующую активность циклопентенона на продукцию NO и на поражение клеток измеряют, как следует ниже, используя линию клеток RAW264.7 мышиных макрофагов (АТССTechnologies Oriental; 25030-149), не содержащую Фенолового Красного, содержащую 5 мл 10% фетальной телячьей сыворотки (произв.Gibco), содержащую 1,5 х 106 клеток RAW 264.7, инкубируют в шестилуночном планшете для культивирования ткани в присутствии 5% газа-диоксида углерода при 37 С в течение 12 ч,добавляют 50 мкл 50 мкг/мл ЛПС (произв.Sigma), затем в каждую лунку добавляют по 50 мкл одного из 500 мкМ циклопентенона, 250 мкМ циклопентенона, 100 мкМ циклопентенона или 50 мкМ циклопентенона, инкубацию далее продолжают в течение еще дополнительных 12 ч и, после этого, измеряют NO2-, полученный окислением NO в среде, и количество жизне 25 способных клеток. В данном случае секция, где не добавляют ЛПС, и секция, где не добавляют циклопентенон, служат в качестве контроля. Для измерения NO2- 100 мкл инкубированной жидкости-супернатанта выделяют из каждой лунки, добавляют 10 мкл 50 мкг/мл раствора 2,3-диаминонафталина (произв. DojindoLaboratories; 341-07021) (раствор в 0,62N хлористоводородной кислоте), смесь выдерживают в течение 15 мин, затем добавляют 5 мкл 2.8N водного раствора гидроксида натрия и измеряют флуоресценцию образовавшегося нафталинтриазола при помощи Titertec Fluoroscan II (поставляемого Dainippon Pharmaceutical) при длине волны возбуждения 355 нм и длине волны измерения 460 нм. Все эксперименты проводят в двух сериях, контрольное значение секции, в которую не добавляли ЛПС, вычитают из среднего значения их и проводят сравнение, исходя из относительного значения каждой секции к значению секции, в которую добавляли ЛПС. Результатом является то, что циклопентенон ингибирует продукцию NO, вызванную ЛПС, в RAW 264.7-клетках, и кроме того, то,что он ингибирует поражение клеток в клеткахRAW 264.7 вызванное ЛПС. Результаты представлены на фиг. 8 и фиг. 9. Фиг. 8 демонстрирует взаимосвязь между концентрацией циклопентенона и концентрацией NO2- в культуральной жидкости, где ордината обозначает относительное значение (%) концентрации NO2-. Фиг. 9 демонстрирует взаимосвязь между временем инкубации и числом жизнеспособных клеток в присутствии циклопентенона, где ордината представляет собой число жизнеспособных клеток (х 105 клеток/5 мл), содержащихся в 5 мл культуральной жидкости, в то время как абсцисса обозначает время инкубации (часы). На фиг. 9. незакрашенный квадрат ( ) соответствует контролю; незакрашенный ромбсоответствует ЛПС; незакрашенный кружок (О) соответствует 5 мкМ циклопентенона; незакрашенный треугольниксоответствует случаю 5 мкМ циклопентенона + ЛПС; черный квадратсоответствует 2,5 мкМ циклопентенона + ЛПС; черный ромбсоответствует 1 мкМ циклопентенона + ЛПС; и черный кружоксоответствует 0,5 мкМ циклопентенона + ЛПС. Как таковой, циклопентенон демонстрирует ингибирующее действие на продукцию NO. Кроме того,(-)-циклопентенон и(в возрасте пяти недель по пять мышей в группе) сенсибилизируют путем внутрибрюшинного введения 100 мкл 0,01% физиологического солевого раствора альбумина яичного белка (Sigma) и 100 мкл квасцов (торговое на 001798 26 звание: Imject Alum; Pearce) и, спустя 11 дней после этого, собирают периферическую кровь из вены глазного яблока. Отобранную кровь центрифугируют (2000 об/мин в течение 5 мин) отделяют плазму и измеряют суммарное количество IgE в плазме с помощью ELISA (IgE Mouse EIA набор; Seikagaku Corporation). В группе, которой вводят циклопентенон,10 мг/кг принудительно вводят один раз, ежедневно, начиная от дня активной сенсибилизации, до дня перед отбором крови. В контрольной группе перорально вводят дистиллированную воду тем же самым способом, как указано выше, и несенсибилизированную группу называют необработанной группой. Результат представлен в таблице 4. Увеличение в суммарном количестве IgE в плазме при сенсибилизации альбумином яичного белка подавляется путем введения циклопентенона. Необработанная группа Контрольная группа Группа, которой вводили циклопентенон(2) Крыс, самцов, линии Wistar, в возрасте пяти недель (по пять крыс на группу) (NipponSLC) сенсибилизируют при помощи внутрибрюшинной инъекции 100 мкл 0,01% раствора альбумина яичного бека (Sigma) в водном физиологическом солевом растворе и 100 мкл квасцов (торговое название: Imject Alum; Pierce) и, спустя 14 дней, собирают кровь из брюшной артерии. Отобранную кровь центрифугируют (при 2000 об/мин в течение пяти минут), плазму отделяют, и количество антиген-специфическогоIgE измеряют при помощи 48-часовой реакции пассивной кожной анафилаксии (РСА) крысы. Сыворотку разбавляют физиологическим солевым раствором способом последовательного удвоения, начиная от 1/4 и кончая 1/64, и по 0,1 мл каждого разведения подкожно инъецируют в участок спинки с выбритыми волосами крыс-самцов линии Wistar в возрасте семи недель. Спустя 48 ч после подкожной инъекции 1 мл смеси 0,05% альбумина яичного белка и 0,5% Evans Blue (произв. Nacalai Tesque) инъецируют в хвостовую вену. Спустя 30 мин после инъекции в хвостовую вену крыс подвергают декапитации и наблюдают синие пятна, проявляющиеся на спине; пятна диаметром 5 мм или более, как полагают, являются позитивными и наибольшее разбавление принимают как титрIgE. В группах, которым вводят циклопентенон, 1 мг/кг или 10 мг/кг циклопентенона вводят внутрибрюшинно один раз ежедневно в течение трех дней, начиная от дня активной сенсибили 27 зации, в то время как в контрольной группе вводят внутрибрюшинно дистиллированную воду тем же самым способом. Результат представлен в таблице 5. Контрольная группа Группы, которым вводят циклопентенон 1 мг/кг/день 10 мг/кг/день Увеличение в количестве антигенспецифического IgE при сенсибилизации альбумином яичного белка ингибируется введением циклопентенона дозозависимым способом. Таким образом, продуцирование IgE ингибируется циклопентеноном. Аналогичная ингибирующая активность по отношению к продуцированию(1) Мыши C57BL/6 (самки в возрасте пяти недель) были приобретены у Nippon SLC, и их используют для эксперимента после предварительного выкармливания на протяжении одной недели. Эритроциты барана (произв. ShimiziJikken Zairyo), которые представляют собой антиген, вызывающий реакцию чувствительности замедленного типа, промывают три раза физиологическим солевым раствором (произв. OtsukaPharmaceutical), получая 1 х 109 клеток/мл, и 200 мкл его инъецируют внутрибрюшинно мышам,чтобы подвергнуть их активной сенсибилизации. Спустя пять дней после сенсибилизации 40 мкл антигена, который получают тем же самым способом, инъецируют в правую лапу, индуцируя антиген, посредством чего вызывают отек стопы. С даты активной сенсибилизации мышам внутрибрюшинно вводят циклопентенон (причем в одну группу включается пять мышей) один раз ежедневно при дозе 1 мг/кг или 10 мг/кг в течение трех дней. Спустя два дня от индуцирования антигена объем правой лапы мыши измеряют с помощью измеряющего устройства для отека стопы (произв. Ugo Basile) и используют как показатель для реакции чувствительности замедленного типа. Измеренное значение получают, рассчитывая степень увеличения, исходя из объема правой лапы мыши, измеренного до индуцирования антигена. Результат представлен на фиг. 10. Таким образом, фиг. 10 демонстрирует ингибирующую активность циклопентенона на реакцию гиперчувствительности замедленного типа, где ордината обозначает степень увеличения (%), в то время как абсцисса обозначает дозу циклопентенона (мг/кг). В данном случаена рисунке означает, что она значима по отношению к контролю при р 0,01. Введение 1 мг/кг циклопентенона подавляет реакцию гиперчувствительности замедленно 28 го типа, и введение 10 мг/кг демонстрирует значительную ингибирующую активность на реакцию гиперчувствительности замедленного типа. В данном случае (-)-циклопентенон и (+)циклопентенон демонстрируют сходные действия.(Nippon SLC; самцы возраст пять недель), тонко измельчают и суспендируют в среде RPMI-1640(произв. Gibco), содержащей 10% фетальной бычьей сыворотки (произв. High Clone), получая раствор, состоящий из отдельных клеток. Раствор свободно плавающих клеток высевают на пластиковую чашку Петри, инкубируют при 37 С в инкубаторе в атмосфере газа-диоксида углерода в течение двух часов, адгезивные клетки удаляют, адгезируя на чашке Петри, и неадгезивные клетки используют в качестве лимфоцитов селезенки. Концентрацию клеток доводят до 2 х 106 клеток/мл и высевают в 96 луночный титрационный микропланшет при 200 мкл/лунку, циклопентенон различных концентраций добавляют в каждую из лунок за исключением лунки для контрольной группы, затем 5 мкг конканавалина А (СоnА; произв. NacalaiTesque) добавляют во все лунки и инкубацию проводят при 37 С в инкубаторе в атмосфере газа-диоксида углерода в течение одного дня. После инкубации по 1 мкКюри 3H-тимидина добавляют во все лунки, и проводят инкубацию в течение еще одного дня, и измеряют его количество, включенное в клетки, с помощью жидкостного сцинтилляционного счетчика. Результат представлен на фиг. 11. Таким образом, фиг. 11 демонстрирует ингибирующую активность циклопентенона в пролиферации лимфоцита, где ордината показывает количество включенного 3H-тимидина (и/мин, СРМ), в то время как абсцисса показывает добавление СоnА, контроль без добавления и концентрацию циклопентенона (мкг/мл). Из чертежа следует,что циклопентенон демонстрирует дозозависимую ингибирующую активность в пролиферации лимфоцитов мышей, стимулированной митогеном, и пролиферация лимфоцитов подавляется практически полностью при 10 мкг/мл, посредством чего отмечается ингибирующая активность на активацию лимфоцитов. В данном случае, также, (-)-циклопентенон и (+) -циклопентенон демонстрируют аналогичные действия.(3) Иссекают селезенки мышей BALB/c(Nippon SLC; самец; возраст пять недель) и мышей C57BL (Nippon SLC; самец; возраст пять недель), и лимфоциты селезенки получают вышеупомянутым способом. Концентрацию каждого из клеточных растворов доводят до 2 х 106 клеток/мл, и по 100 мкл каждого смешивают и высевают в 96-луночный титрационный микропланшет. Циклопентенон различных концентраций добавляют в каждую из лунок за исключением лунки для контрольной группы, и инку 29 бируют при 37 С в инкубаторе в атмосфере газа-диоксида углерода в течение четырех дней. После инкубации по 1 мкКи 3H-тимидина добавляют в каждую из лунок и инкубируют в течение еще одного дня, и включенное в клетки количество 3H-тимидина измеряют при помощи жидкостного сцинтилляционного счетчика. Результат представлен на фиг. 12. Так,фиг. 12 демонстрирует ингибирующую активность циклопентенона в реакции смешанных лимфоцитов, где на ординате представлено количество включенного 3H-тимидина (имп./мин,СРМ), в то время как абсцисса показывает контроль BALB/c лимфоцитов селезенки (показано как BALB/c на чертеже), контроль C57BL/6 лимфоцитов селезенки (показано как C57BL/6 на чертеже), смешанный контроль BALB/c лимфоцитов селезенки и C57BL/6 лимфоцитов селезенки и концентрации циклопентенона(мкг/мл). Из чертежа следует, что циклопентенон демонстрирует дозозависимую ингибирующую активность на лимфоциты, активированные аллогенной антигенной стимуляцией, и отмечается почти полное подавление при 10 мкг/мл, посредством чего отмечается ингибирующая активность в активации лимфоцитов реакцией смешанных лимфоцитов. В данном случае, также, (-)-циклопентенон и (+)-циклопентенон демонстрируют сходную ингибирующую активность в реакции смешанных лимфоцитов. Пример 9.(произв. Takara Shuzo) добавляют в смесь 2 мкл топоизомеразы II (произв. Торо-GEN, 2 единицы/мкл), 2 мкл буфера с десятикратно разбавленной концентрацией [0,5 М Трис-НСl (рН 8,0),1,2 М КСl, O, 1 М MgCl2, 5 мМ аденозин трифосфата и 5 мМ дитиотреитола], 2 мкл 0,1% бычьего сывороточного альбумина (произв. Takara Shuzo), 11 мкл дистиллированной воды и 2 мкл дистиллированной воды (контроль) или образца (50, 100, 200, 500, 1000 или 2500 мкМ циклопентенона) и оставляют взаимодействовать при 37 С. После реакции в течение 30 мин реакцию останавливают, добавляя 2 мкл водного раствора 1% додецилсульфата натрия, 50% глицерина и 0,02% бромфенолового Синего. Вышеуказанный реакционный раствор (20 мкл) наносят на 1% агарозный гель, полученный из агарозы L03 (произв. Takara Shuzo), и ТАЕ буфера [40 мМ трис, 5 мМ ацетат натрия и 1 мМ этилендиаминтетраацетат натрия (EDTA); доведен до рН 7,8 уксусной кислотой], и проводят электрофорез в ТАЕ-буфере. После электрофореза гель погружают в водный раствор 1 мкг/мл бромида этидия и облучают ультрафиолетовыми лучами, чтобы наблюдать электрофоретическую картину ДНК. В контроле, который представляет собой водный раствор, ДНК полностью переходит из суперсвернутого типа в релаксированный тип, но когда активность то 001798 30 поизомеразы II ингибируется, переход из суперсвернутого типа в релаксированный тип частично или полностью ингибируется. Результат представлен в таблице 6. Концентрация (мкМ) в реакционном растворе 0 10 20 50 100 250 В контроле, где добавляют воду, ДНК полностью переходит из суперсвернутого типа в релаксированный тип, но когда концентрация циклопентенона составляет 20 мкМ или выше,переход ДНК из суперсвернутого типа в релаксированный тип частично или полностью ингибируется, посредством чего устанавливается активность циклопентенона в ингибировании топоизомеразы II. В таблице 6 "-" означает полный переход из суперсвернутого типа в релаксированный тип; "+" означает переход средней степени; означает, что большая часть суперсвернутого типа осталась; и означает,что совсем нет уменьшения в суперсвернутом типе.(2) Активность циклопентенона в ингибировании топоизомеразы I измеряют таким же способом, как в примере 9-(1), за исключением того, что топоизомеразу I [произв. TopoGEN,0,01 единица/мкл] используют вместо топоизомеразы II; и 100 мМ Трис-НСl (рН 7,9), 10 мМEDTA, 1 мМ спермидин и 50% глицерин используют в качестве буфера с десятикратно разбавленной концентрацией. В данном случае, в качестве образца добавляют циклопентенон,получая финальную концентрацию 1 мМ. Результат заключается в том, что топоизомераза I ингибируется 1 мМ циклопентеноном. Как таковой, циклопентенон демонстрирует ингибирующую активность по отношению к топоизомеразе II, которая экспрессируется только временно (скоротечно) во время митотической фазы в нормальных клетках, но становится сильно экспрессируемой посредством всего клеточного цикла при развитии раковой опухоли, и также, по отношению к топоизомеразе I,которая увеличивается в своем экспрессирующем количестве и активности при развитии раковой опухоли. Кроме того, (-)-циклопентенон и(1) Циклопентенон добавляют в физиологический солевой раствор (приведенный в Japanese Pharmacopoeia) в концентрации 1%, получая препарат для инъекции.(2) (-)-Циклопентенон и глицирризиновую кислоту добавляют в физиологический солевой раствор (такой же, как вышеупомянутый) в кон 31 центрации 0,5% и 1,0%, соответственно, получая препарат для инъекции. Пример 11. Таблетки. 1) Получают таблетку, содержащую 100 мг циклопентенона и соответствующее количество микрокристаллической целлюлозы, и покрывают сахаром, получая препарат в виде таблетки.(+)-циклопентенона, 10 мг дикалий глицирризината и соответствующее количество микрокристаллической целлюлозы, и покрывают сахаром,получая препарат в виде таблетки. Пример 12.(1) Пектин (Pomosin Pectin LM-13CG; произв. Hercules) (5 кг) добавляют к 100 л водопроводной воды и смесь нагревают от температуры жидкости 28 С до 120 С посредством продувки водяного пара через нее в течение 35 мин, поддерживают при 120 С в течение 5 ч при перемешивании и охлаждают, получая 135 л охлажденной смеси. К ней добавляют 1,35 кг Celite 545 (произв. Celite) и 1,35 кг Silica tt600-S(произв. Chuo Silica) в качестве вспомогательного фильтровального вещества, и фильтрацию проводят, используя компактный фильтр (6 дюймовая фильтровальная бумага в 16 ярусов;ADVANTEC 327), предварительно покрытый 0,1 кг Celite 545 и 0,1 кг Silica 600-S. Полученный фильтрат подвергают непрерывному быстрому нагреванию (при 98 С в течение 60 с),используя плиту-нагреватель (произв. NichihanSeisakusho), и затем охлаждают, получая 150 л обработанного нагреванием раствора пектина,содержащего циклопентенон. Указанный обработанный нагреванием раствор пектина, содержащий циклопентенон,имел рН около 3,5, кислотность 6,2 мл и градус сахара 5,8 Brix%. В данном случае рН измеряют рН-метром, кислотность выражают в терминах количества (мл) 0,1N NaOH, используемого для нейтрализации до рН 7,0, и градус сахара измеряют с помощью Brix сахариметра.(2) Напиток получают согласно следующему составу. Фруктоза-глюкоза-жидкость-сахар Сахар Кислое средство Отдушки Циклопентенон-содержащее вещество Очищенная вода Итого Обработанный нагреванием раствор пектина, содержащий циклопентенон, упомянутый в примере 12-(1), используют в качестве циклопентенон-содержащего вещества и его добавляют в количестве, рассчитанном, исходя из твердого вещества. Этот напиток (100 мл) содержит 4 мг циклопентенона. Достоинство изобретения В соответствии с настоящим изобретением, предлагается фармацевтический препарат,содержащий, по меньшей мере, одно соедине 32 ние, выбранное из циклопентенона или оптически активных веществ его или солей его в качестве эффективного компонента. Указанный фармацевтический препарат действительно является полезным в качестве противоревматического средства или профилактического средства при ревматизме и в качестве терапевтического средства или профилактического средства для заболеваний, сопровождаемым воспалением, в качестве противовоспалительного средства или профилактического средства при воспалении посредством контроля воспалительного цитокина. Кроме того теперь возможно, в соответствии с настоящим изобретением, чтобы соответствующее количество циклопентенона или оптически активного вещества его или соли его,имеющее физиологическую активность, содержалось в продукте питания или напитке. Благодаря физиологической функции этих соединений, функциональный продукт питания или напиток настоящего изобретения оказывает улучшающее действие и/или профилактическое действие на симптомы ревматизма, в частности,хронического суставного ревматизма, и потому действительно является полезным для лечения,профилактики, и т.п. осложнений, связанных с ревматизмом, трудностью при ходьбе, и т.п. Кроме того, благодаря ингибирующей активности по отношению к воспалительному цитокину, продукт питания или напиток настоящего изобретения полезен для улучшения или профилактики симптомов заболеваний, сопровождаемых воспалением. Кроме того, продуцирование фактора некроза опухоли подавляется фармацевтическим препаратом настоящего изобретения, и фармацевтический препарат настоящего изобретения является полезным для лечения или профилактики заболеваний, таких как болезни, опосредованные продуцированием фактора некроза опухоли, болезни, усугубляемые продуцированием указанного фактора, сепсис, СПИД, хронический суставной ревматизм, и т.п. Кроме того,продукт питания или напиток настоящего изобретения действительно является полезным для ослабления симптомов заболеваний, таких как болезни, опосредованные продуцированием фактора некроза опухоли, болезни, усугубляемые продуцированием указанного фактора, сепсис, СПИД, хронический суставной ревматизм,и т.п. и также для профилактики указанных болезней. Таким образом, способ настоящего изобретения, использующий, по меньшей мере,одно соединение, выбранное из циклопентенона, оптически активных веществ его и солей его в качестве эффективного компонента, является действительно полезным для контроля продуцируемого количества фактора некроза опухоли. Кроме того, настоящее изобретение предлагает фармацевтический препарат, содержащий циклопентенон, оптически активное веще 33 ство его или соль его, имеющий ингибирующую активность по отношению к продуцированиюNO, и указанный фармацевтический препарат является полезным для лечения или профилактики заболеваний, которые требуют подавления продуцирования NO, таких как системное понижение кровяного давления, уменьшение реакции на кровяное давление, аутоиммунные заболевания, воспаление, артрит, ревматоидный артрит, воспалительные кишечные болезни, недостаточность функции кровеносного сосуда,этиологическое расширение кровеносных сосудов, повреждение ткани, сердечно-сосудистая ишемия, повышенная чувствительность к боли,церебральная ишемия, болезни, сопровождаемые неоваскуляризацией, и рак и также для поддержания гомеостаза живых организмов. Кроме того, предлагается ингибитор продуцирования NO, ингибитор для неоваскуляризации, профилактическое средство для канцерогенеза, противораковое средство, противовоспалительное средство и улучшающее средство при ишемическом повреждении головного мозга,содержащий, по крайней мере, одно соединение,выбранное из циклопентенона, оптически активного вещества его и соли его. Указанный ингибитор продуцирования NO также является полезным для биохимического исследования и скринирования лекарственных средств. В соответствии с настоящим изобретением, теперь возможно, чтобы соответствующее количество циклопентенона, оптически активного вещества его или соли его, имеющее физиологическую активность, содержалось в продукте питания или напитке. Благодаря ингибирующей активности циклопентенона или оптически активного вещества или соли его по отношению к продуцированию NO, продукт питания или напиток настоящего изобретения представляет собой оздоровляющий продукт питания или напиток, имеющий функцию, заключающуюся в поддержании гомеостаза живого организма, опосредованную ингибирующей активностью продуцирования NO, такую как профилактика канцерогенеза, противораковое действие, противовоспалительное действие и улучшающее действие при ишемическом повреждении головного мозга и потенцирование биоиммунного действия. Настоящее изобретение предлагает индуцирующее средство для продуцирования Fasантигена, содержащее, по крайней мере, одно соединение, выбранное из циклопентенона или оптически активного вещества его или соли его,в качестве эффективного компонента; способ индуцирования продуцирования Fas-антигена,используемый для изучения физиологической функции Fas-антигена или для исследования антагонистов, использующий эти соединения в качестве эффективных компонентов; и профилактическое или терапевтическое средство для заболеваний, сопровождаемых аномальным (па 001798 34 тологическим) продуцированием Fas-антигена,таких как аутоиммунные болезни и суставной ревматизм. Кроме того продукт питания или напиток,содержащий эффективное количество, по меньшей мере, одного соединения, выбранного из циклопентенона или оптически активного вещества его и соли его, представляет собой функциональный продукт питания или напиток настоящего изобретения благодаря действию этих соединений, заключающемуся в индуцировании продукции Fas-антигена, и поэтому является полезным для улучшения симптомов заболеваний и для предотвращения начала вышеупомянутых заболеваний. Кроме того, циклопентенон или оптически активное вещество его или соль его имеет апоптоз-индуцирующую активность в синовиальных клетках, и фармацевтический препарат, продукт питания или напиток настоящего изобретения, в частности, используют в качестве противоревматического фармацевтического препарата, продукта питания или напитка. Настоящее изобретение предлагает иммуномодулирующее средство, содержащее, по меньшей мере, одно соединение, выбранное из циклопентенона или оптически активного вещества его или соли его, имеющее ингибирующую активность в продуцировании IgE, ингибирующую активность в реакции гиперчувствительности замедленного типа, ингибирующую активность в пролиферации лимфоцитов и ингибирующую активность в смешанной реакции лимфоцитов. Благодаря иммуномодулирующему действию циклопентенона, оптически активного вещества его или соли его, продукт питания или напиток, содержащий соединение, выбранное из этих соединений, является полезным для улучшения симптомов заболеваний, которые требуют модуляции иммунной функции, таких как аутоиммунная болезнь, или для профилактики иммунной аномалии (патологии), как иммуномодулирующий продукт питания или иммуномодулирующий напиток. Помимо этого, способ настоящего изобретения является полезным для модуляции продуктивного количества IgE и, кроме того, для иммуномодуляции. Кроме того, настоящее изобретение предлагает ингибитор для топоизомеразы, содержащий, по крайней мере, одно соединение, выбранное из циклопентенона, оптически активного вещества его и соли его, в качестве эффективного компонента, и также способ ингибирования топоизомеразы, содержащий, по меньшей мере, одно соединение, выбранное из этих соединений в качестве эффективного компонента. Указанный ингибитор топоизомеразы является полезным в качестве противоракового лекарственного средства и указанный способ ингибирования топоизомеразы является полезным в био 35 химическом исследовании, скринировании противораковых лекарственных средств, и т.п. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Фармацевтическое средство, которое отличается тем, что содержит, по меньшей мере,одно соединение, выбранное из группы, состоящей из 4,5-дигидрокси-2-циклопентен-1 она, представленного нижеследующей формулой [I], и оптически активного вещества и соли его, в качестве эффективного компонента, где указанное фармацевтическое средство выбирают из группы, состоящей из противоревматического средства, превентера ревматизма, противовоспалительного средства, превентера воспаления, ингибитора продуцирования фактора некроза опухоли, превентера продуцирования фактора некроза опухоли, ингибитора продуцирования моноксида азота, ингибитора для неоваскуляризации, превентера канцерогенеза,улучшающего средства при ишемическом нарушении головного мозга, индуцирующего средства для продуцирования Fas-антигена, иммуномодулирующего средства и ингибитора топоизомеразы. 36 ставляет собой иммуномодулирующее средство,выбранное из группы, состоящей из энхансера продуцирования интерлейкина-10, ингибитора продуцирования IgE, ингибитора гиперчувствительности замедленного типа, ингибитора пролиферации лимфоцитов и ингибитора отека. 3. Продукт питания или напиток, который отличается тем, что содержит, по меньшей мере,одно соединение, выбранное из группы, состоящей из 4,5-дигидрокси-2-циклопентен-1 она, представленного формулой [I], и оптически активного вещества и соли его, в качестве эффективного компонента, где указанный продукт питания или напиток выбирают из группы, состоящей из продукта питания или напитка для улучшения или профилактики ревматизма, для улучшения или профилактики воспаления, для ингибирования продуцирования фактора некроза опухоли, для усиления продуцирования интерлейкина-10, для ингибирования продуцирования монооксида азота, для индуцирования продуцирования Fas-антигена, для иммуномодулирования, для ингибирования продуцирования IgE и для ингибирования топоизомеразы. 2. Фармацевтическое средство по п.1, где указанное фармацевтическое средство пред Фиг. 1
МПК / Метки
МПК: A61P 29/00, A23L 1/30, A61K 31/122
Метки: противоревматические, средства
Код ссылки
<a href="https://eas.patents.su/21-1798-protivorevmaticheskie-sredstva.html" rel="bookmark" title="База патентов Евразийского Союза">Противоревматические средства</a>
Предыдущий патент: Хинолиновые антагонисты лейкотриенов
Следующий патент: Способный к отверждению состав и его использование
Случайный патент: Производные 2h-1-бензопирана и содержащая их фармацевтическая композиция