Электрод для активных форм кислорода и сенсор, использующий электрод
Номер патента: 6719
Опубликовано: 24.02.2006
Авторы: Абе Масахико, Исикава Масухиде, Юаса Макото, Эгути Кацуя, Сиозава Асако, Кидо Сигеру, Ямагути Аритомо
Формула / Реферат
1. Электрод для активных форм кислорода, включающий проводящий компонент с образованной на поверхности полимерной мембраной из металлопорфиринового комплекса, представленного следующими формулами (I) или (II):
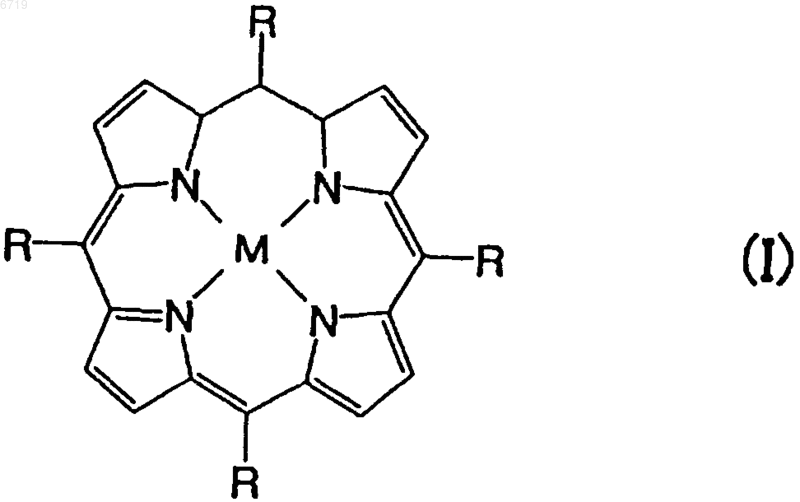
где M обозначает металл, выбранный из группы, состоящей из железа, марганца, кобальта, хрома и иридия, по крайней мере одна из четырех групп R выбрана из группы, состоящей из тиофурильной группы, пирролильной группы, фурильной группы, меркаптофенильной группы, аминофенильной группы, а другие группы R обозначают любую из вышеуказанных групп, алкильную группу, арильную группу или водород,
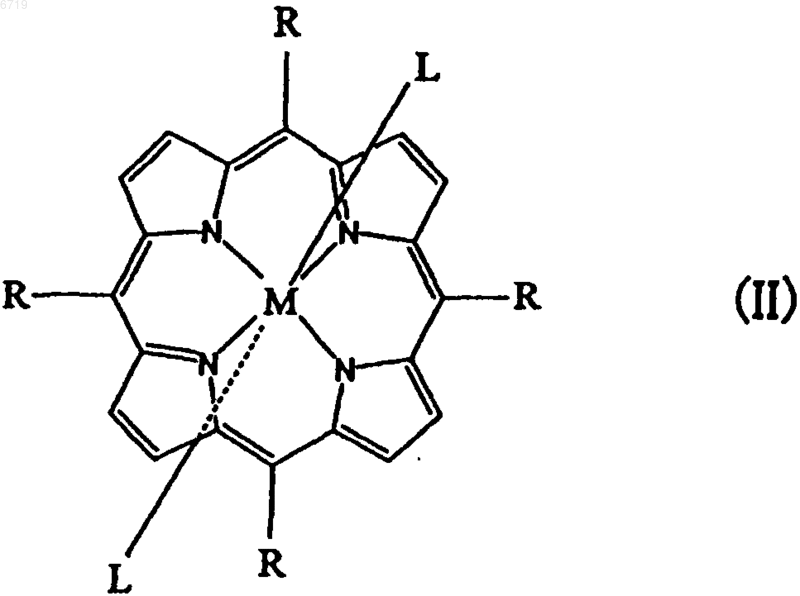
где M и R имеют то же значение, что и указанное ранее, по крайней мере один из двух L обозначает азотсодержащий аксиальный лиганд, такой как имидазол и его производное, пиридин и его производное, анилин и его производное, гистидин и его производное, и триметиламин и его производное, серусодержащий аксиальный лиганд, такой как тиофенол и его производное, цистеин и его производное, метионин и его производное, или кислородсодержащий аксиальный лиганд, такой как бензойная кислота и ее производное, уксусная кислота и ее производное, фенол и его производное, алифатический спирт и его производное, и воду, и другой L обозначает любой один из указанных аксиальных лигандов или группу без лиганда.
2. Электрод по п.1, где порфириновое соединение, образующее металлопорфириновый комплекс, выбрано из группы, состоящей из
5,10,15,20-тетракис(2-тиофурил)порфирина,
5,10,15,20-тетракис(3-тиофурил)порфирина,
5,10,15,20-тетракис(2-пирролил)порфирина,
5,10,15,20-тетракис(3-пирролил)порфирина,
5,10,15,20-тетракис(2-фурил)порфирина,
5,10,15,20-тетракис(3-фурил)порфирина,
5,10,15,20-тетракис(2-меркаптофенил)порфирина,
5,10,15,20-тетракис(3-меркаптофенил)порфирина,
5,10,15,20-тетракис(4-меркаптофенил)порфирина,
5,10,15,20-тетракис(2-аминофенил)порфирина,
5,10,15,20-тетракис(3-аминофенил)порфирина,
5,10,15,20-тетракис(4-аминофенил)порфирина,
[5,10,15-трис(2-тиофурил)-20-моно(фенил)]порфирина,
[5,10,15-трис(3-тиофурил)-20-моно(фенил)]порфирина,
[5,10-бис(2-тиофурил)-15,20-ди(фенил)]порфирина,
[5,10-бис(3-тиофурил)-15,20-ди(фенил)]порфирина,
[5,15-бис(2-тиофурил)-10,20-ди(фенил)]порфирина,
[5,15-бис(3-тиофурил)-10,20-ди(фенил)]порфирина,
[5-моно(2-тиофурил)-10,15,20-три(фенил)]порфирин и
[5-моно(3-тиофурил)-10,15,20-три(фенил)]порфирина.
3. Электрод по п.1 или 2, где проводящий компонент помещен в маленькую трубку, изготовленную из электроизолирующего материала, при этом внешняя часть указанной маленькой трубки покрыта материалом, который действует как противоэлектрод, таким как металл, с образованием противоэлектрода, металлопорфириновая полимерная мембрана сформирована на кончике проводящего компонента, а электрод имеет игольчатую форму.
4. Электрод по п.1 или 2, где проводящий компонент помещен в электроизолирующий материал, который помещен в материал противоэлектрода, который, в свою очередь, помещен в электроизолирующий материал, снаружи покрытый материалом, действующим в качестве заземления, при этом металлопорфириновая полимерная мембрана сформирована на кончике проводящего компонента, а электрод имеет игольчатую форму.
5. Применение электрода по любому из пп.1-4 для измерения супероксидных анион-радикалов.
6. Сенсор для определения концентрации активных форм кислорода, включающий электрод для активных форм кислорода по пп.1-4.
7. Сенсор по п.6, где порфириновое соединение, образующее металлопорфириновый комплекс, выбирают из группы, состоящей из
5,10,15,20-тетракис(2-тиофурил)порфирина,
5,10,15,20-тетракис(3-тиофурил)порфирина,
5,10,15,20-тетракис(2-пирролил)порфирина,
5,10,15,20-тетракис(3-пирролил)порфирина,
5,10,15,20-тетракис(2-фурил)порфирина,
5,10,15,20-тетракис(3-фурил)порфирина,
5,10,15,20-тетракис(2-меркаптофенил)порфирина,
5,10,15,20-тетракис(3-меркаптофенил)порфирина,
5,10,15,20-тетракис(4-меркаптофенил)порфирина,
5,10,15,20-тетракис(2-аминофенил)порфирина,
5,10,15,20-тетракис(3-аминофенил)порфирина,
5,10,15,20-тетракис(4-аминофенил)порфирина,
[5,10,15-трис(2-тиофурил)-20-моно(фенил)]порфирина,
[5,10,15-трис(3-тиофурил)-20-моно(фенил)]порфирина,
[5,10-бис(2-тиофурил)-15,20-ди(фенил)]порфирина,
[5,10-бис(3-тиофурил)-15,20-ди(фенил)]порфирина,
[5,15-бис(2-тиофурил)-10,20-ди(фенил)]порфирина,
[5,15-бис(3-тиофурил)-10,20-ди(фенил)]порфирина,
[5-моно(2-тиофурил)-10,15,20-три(фенил)]порфирина и
[5-моно(3-тиофурил)-10,15,20-три(фенил)]порфирина.
8. Сенсор по п.6 или 7, в котором электрод включает проводящий компонент, помещенный в маленькую трубку, изготовленную из электроизолирующего материала, внешняя часть указанной маленькой трубки покрыта материалом, который действует как противоэлектрод, таким как металл, с образованием противоэлектрода, при этом металлопорфириновая полимерная мембрана сформирована на кончике проводящего компонента, а электрод имеет игольчатую форму.
9. Сенсор по п.6 или 7, в котором электрод включает проводящий компонент, помещенный в электроизолирующий материал, который помещен в материал противоэлектрода, который в свою очередь помещен в электроизолирующий материал, снаружи покрытый материалом, действующим в качестве заземления, при этом металлопорфириновая полимерная мембрана сформирована на кончике проводящего компонента, а электрод имеет игольчатую форму.
10. Применение сенсора по любому из пп.6-9 для измерения супероксидных анион-радикалов.
11. Способ определения активных форм кислорода в образце, включающий измерение тока, возникающего в результате окислительно-восстановительной реакции между металлом в металлопорфириновой полимерной мембране и активными формами кислорода, с использованием сенсора по любому из пп.6-10.
12. Способ по п.11, где определяемыми активными формами кислорода являются супероксидные анион-радикалы.
Текст
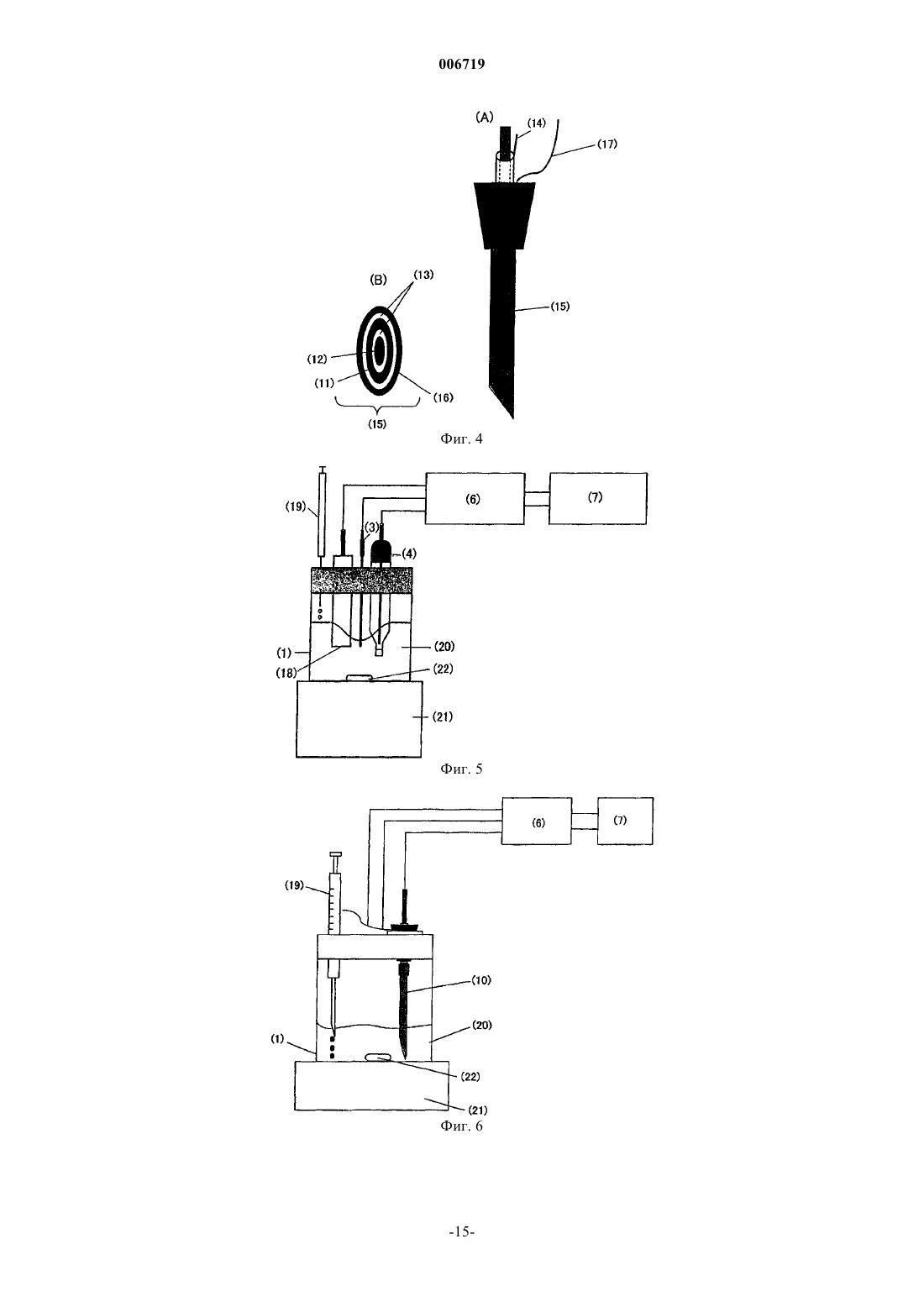
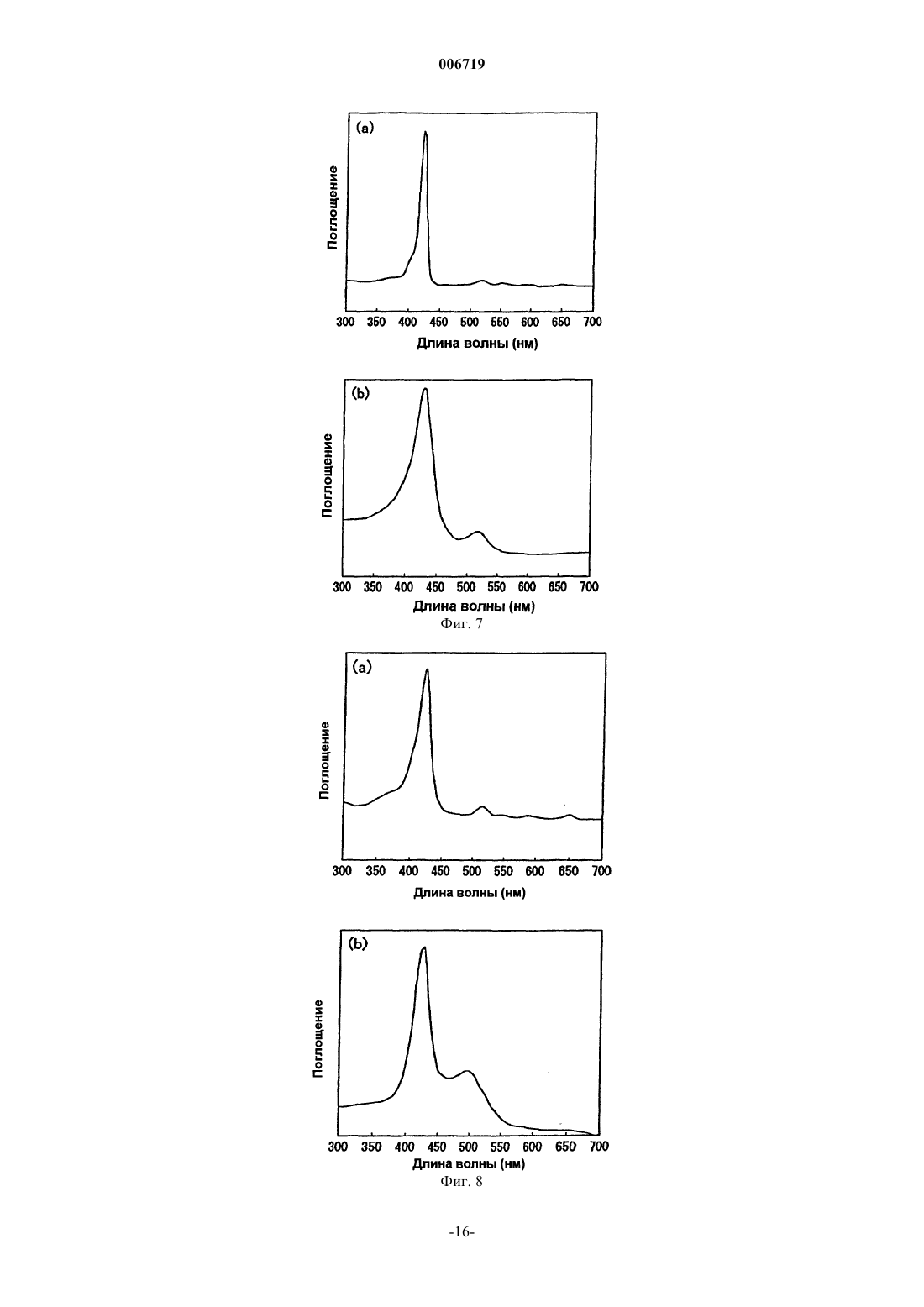
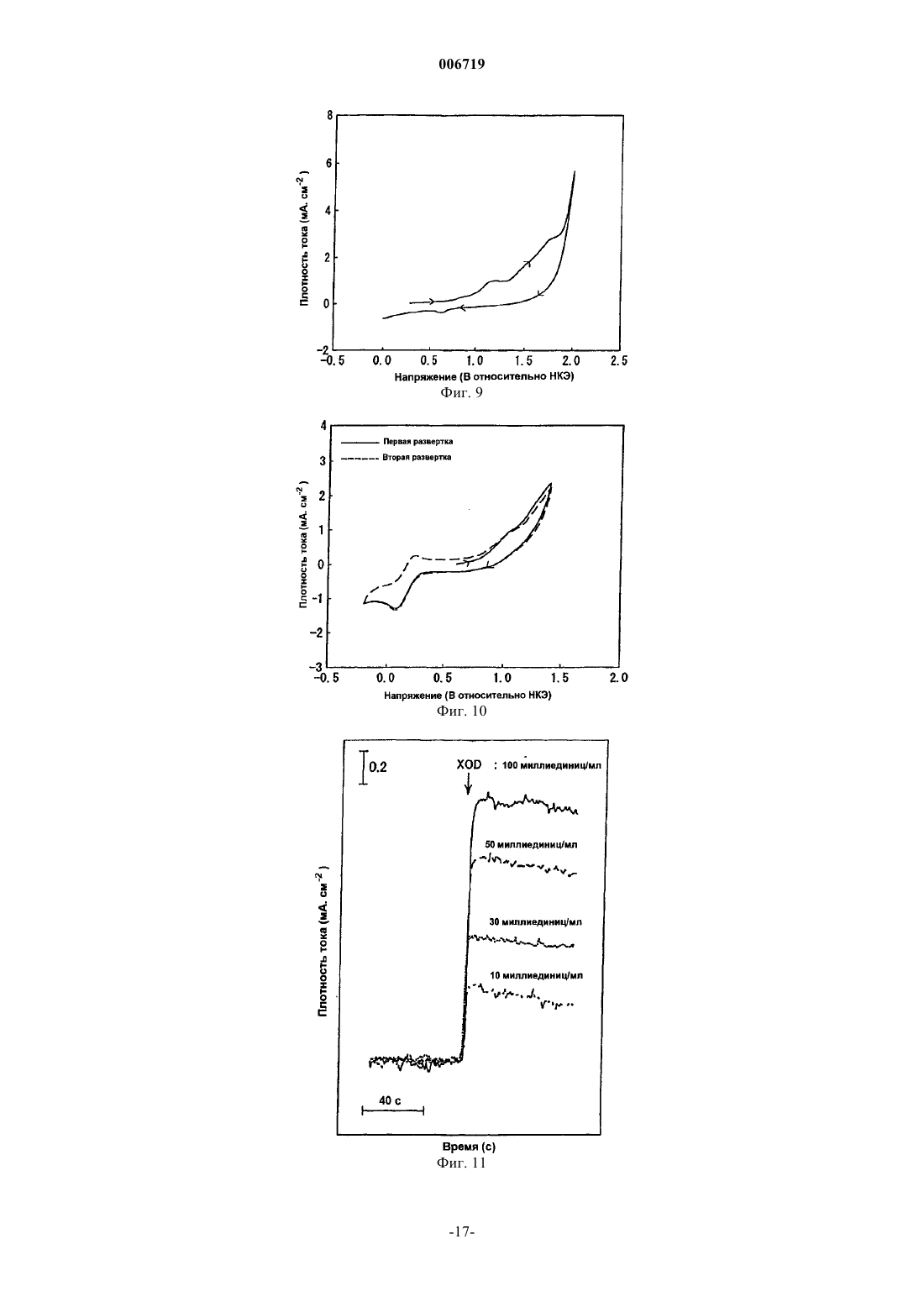
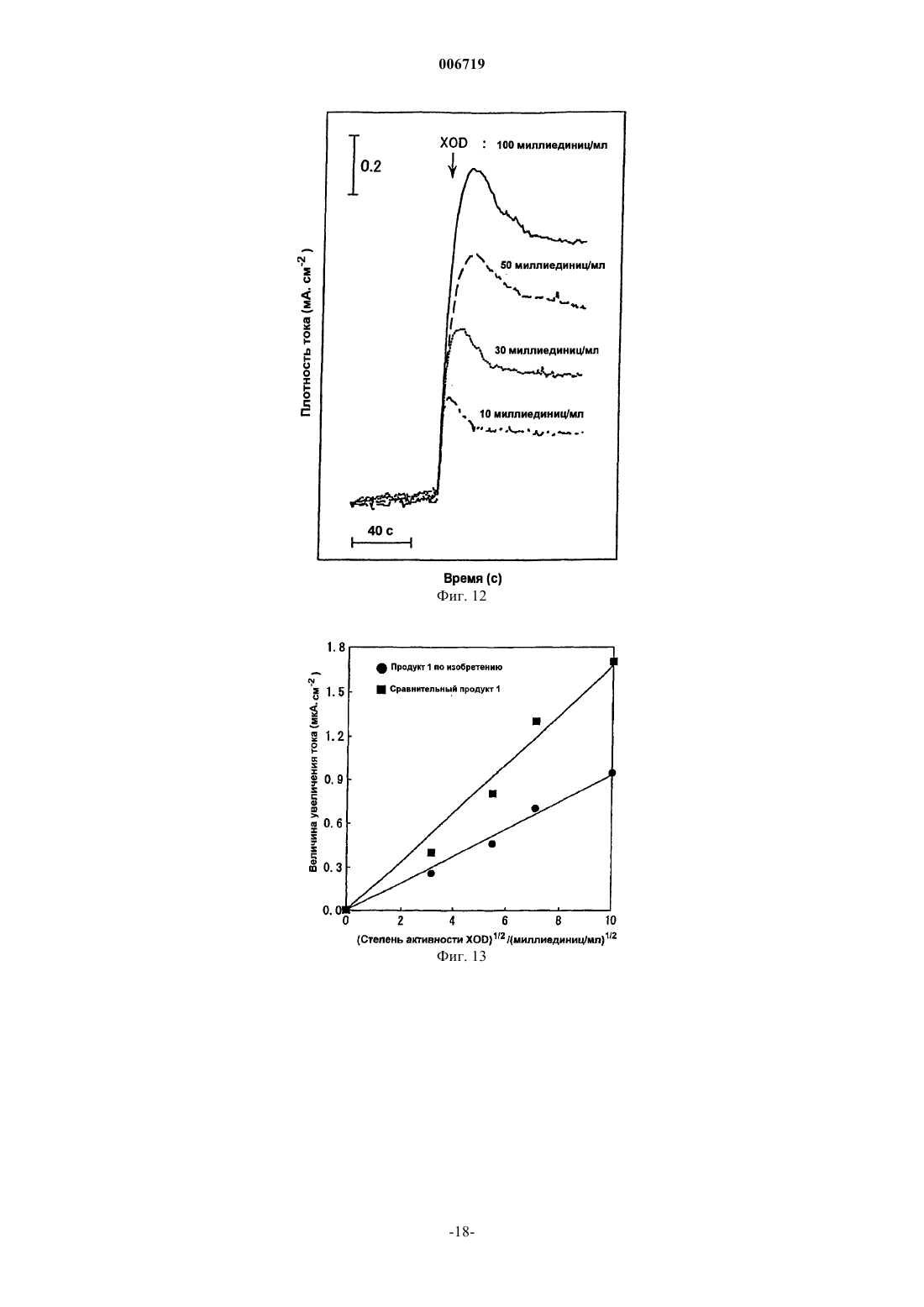
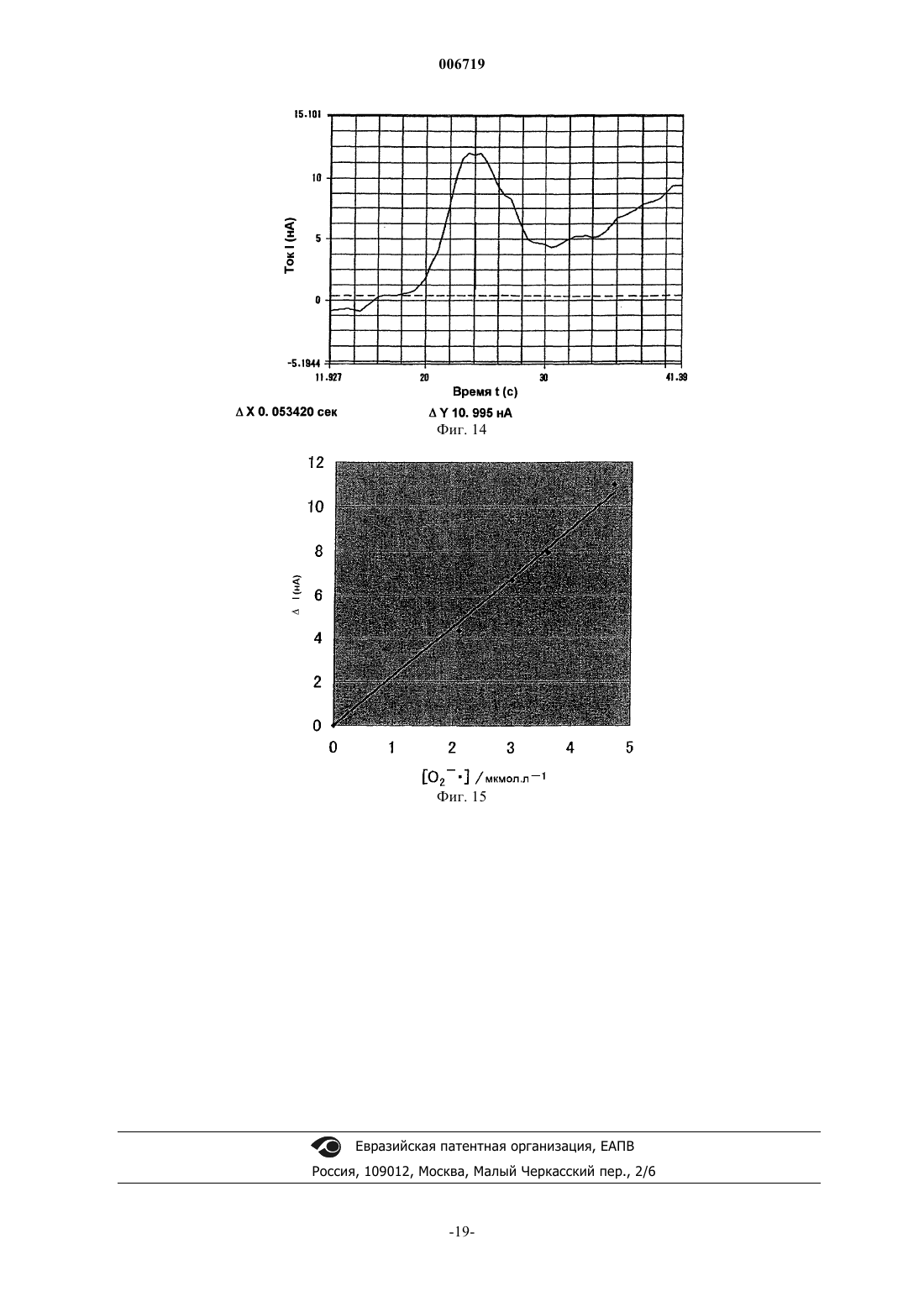
006719 Область техники Настоящее изобретение относится к электроду для активных форм кислорода в живом организме,таких как супероксидные анион-радикалы (O2-), и к сенсору для определения концентрации активных форм кислорода с использованием электрода. Изобретение, в частности, относится к электроду для активных форм кислорода и к сенсору для определения концентрации активных форм кислорода, который может быть применен для проведения измерений in vivo без использования больших количеств ферментов и не вызывает проблем дезактивирования ферментов. Предпосылки изобретения Супероксидные анион-радикалы (O2-), которые являются активными формами кислорода, образуются in vivo при окислении ксантина, гипоксантина и т.п. в мочевую кислоту с участием ксантинксантин оксидазы (XOD), при восстановлении кислорода гемоглобином и т.п. Супероксидные анионрадикалы играют важную роль в синтезе физиологически активных веществ, при бактерицидном воздействии, при старении и т.д. Сообщалось, что различные активные формы кислорода, полученные из супероксидных анион-радикалов, вызывают различные болезни, такие как рак. Поэтому предполагают, что определение концентрации активных форм кислорода в живом организме, в том числе супероксидных анион-радикалов, является важным для точного установления указанных заболеваний. В отсутствие субстрата указанные супероксидные анион-радикалы превращаются в молекулы пероксида водорода (Н 2O2) и кислорода (O2) по реакции дисмутации, как показано в формуле (1). Указанная реакция дисмутации заключается в образовании НO2 путем присоединения протона к супероксидным анион-радикалам, в образовании молекул пероксида водорода и кислорода по реакции НO2 с активным кислородом и в образовании молекул пероксида водорода и кислорода при взаимодействии радикалов НO2 (формулы (1)-(4. В данной реакционной системе супероксидный анион-радикал действует в качестве акцептора электронов (окислитель), донора электронов (восстановитель) и акцептора ионов водорода (основание). Первые две функции используют для определения концентрации супероксидных анион-радикалов. Например, концентрацию супероксидных анион-радикалов определяли с использованием реакции превращения феррицитохрома с (трехвалентного) в ферроцитохром с (двухвалентный), реакции получения голубого формазана из нитроголубого тетразолия (NBT) и реакции восстановления тетранитрометана (TNM). Все эти реакции проводили в условиях in vitro. С другой стороны, был исследован способ количественного определения концентрации супероксидных анион-радикалов в условиях in vivo. Так, McNeil et al., Tariov et al. и Cooper et al. сообщали, что концентрацию супероксидных анион-радикалов можно определить электрохимически за счет получения ферментного электрода (электрода с иммобилизованным цитохромом с) путем модифицирования поверхности золотого или платинового электрода ферментом, N-ацетилцистеином, и путем иммобилизации посредством связи S-Au белка, такого как цитохром с, который представляет собой металлопротеин,включающий в качестве окислительно-восстановительного центра комплекс железа, называемый гемом(1991); and J.M. Cooper, K.R. Greenough and C.J. McNeil, J, Electroanal. Chem., 347, 267 (1993). Способ основан на следующем принципе проведения измерений. А именно: цитохром с (трехвалентный) (cyt. с (Fе 3+ взаимодействует с супероксидными анион-радикалами и восстанавливается в цитохром с (двухвалентный) (cyt. с (Fe2+ в соответствии с реакцией по формуле (5). Затем цитохром с(двухвалентный), восстановленный по реакции с O2-, электрохимически вновь окисляется в соответствии с реакцией по формуле (6). Измеряют ток окисления, который генерируется при протекании этой реакции, а концентрацию супероксидных анион-радикалов количественно определяют косвенным путем. Тем не менее, поскольку цитохром с является белком-транспортером электрона и in vivo находится во внутриклеточной мембране митохондрий, то для формирования электрода, на котором цитохром с иммобилизуется в количестве, достаточном для проведения измерений, требуется большое количество клеток (например, 105-106 клеток). Кроме того, используемый фермент дезактивируется в течение нескольких дней. Следовательно, необходимо получить электрод, способный детектировать активные формы кислорода, такие как супероксидные анион-радикалы, не требуя большого количества ферментов и не вызывая проблем вследствие дезактивации ферментов.-1 006719 Описание изобретения В связи с вышеизложенным, авторы настоящего изобретения провели интенсивные исследования с целью получения электрода, который может детектировать активные формы кислорода, такие как супероксидные анион-радикалы, по окислительно-восстановительной реакции. Было обнаружено, что электрод, который получают путем формирования на поверхности проводящего компонента полимерной мембраны из металлопорфиринового комплекса, образованного введением атома металла в центр порфиринового соединения, не требует большого количества ферментов, не создает проблем с дезактивацией и может быть использован для детектирования активных форм кислорода и измерения их концентрации. В настоящем изобретении, в частности, предлагается электрод для активных форм кислорода,включающий проводящий компонент с образованной на его поверхности полимерной мембраной из металлопорфиринового комплекса. В настоящем изобретении далее предлагается сенсор для определения концентрации активных форм кислорода, содержащий электрод для активных форм кислорода, включающий проводящий компонент с образованной на его поверхности полимерной мембраной из металлопорфиринового комплекса,противоэлектрод и электрод сравнения. Далее в настоящем изобретении предлагается способ детектирования активных форм кислорода в образце, включающий измерение тока, который возникает между металлом в металлопорфириновой полимерной мембране и активными формами кислорода, с использованием вышеуказанного сенсора. Краткое описание фигур На фиг. 1 приведен рисунок, показывающий пример трехэлектродной ячейки, которую используют для получения электрода по настоящему изобретению. На фиг. 2 приведен рисунок, показывающий пример двухкамерной трехэлектродной ячейки, которую используют для получения электрода по настоящему изобретению. На фиг. 3 приведен рисунок, показывающий пример электрода игольчатого типа и двухкамерной трехэлектродной ячейки, которую используют для получения электрода по настоящему изобретению, где(А) обозначает двухкамерную трехэлектродную ячейку, (В) обозначает электрод игольчатого типа в целом, и (С) обозначает кончик электрода игольчатого типа. На фиг. 4 приведен рисунок улучшенного игольчатого электрода, который используют для получения электрода по настоящему изобретению. Этот электрод является улучшением электрода игольчатого типа, приведенного на фиг. 3, где (А) обозначает улучшенный электрод игольчатого типа в целом, и (В) обозначает кончик улучшенного электрода игольчатого типа. На фиг. 5 приведен рисунок, показывающий пример измерительного устройства, которое используют для определения активных форм кислорода. На фиг. 6 приведен рисунок, показывающий пример измерительного устройства, которое используют для определения активных форм кислорода. На фиг. 7 приведены графики УФ-видимого спектра Н 2 Т 3 ТhР (7(а и УФ-видимого спектраFeT2AmP (8(b. На фиг. 9 представлен график, показывающий CV-кривую в процессе электролитической полимеризации FeT3ThP. На фиг. 10 представлен график, показывающий CV-кривую в процессе электролитической полимеризации при получении электрода FeT2AmP. На фиг. 11 приведен график, показывающий изменение с течением времени тока окисления в процессе добавления XOD в сравнительном продукте 1. На фиг. 12 приведен график, показывающий изменение с течением времени тока окисления в процессе добавления XOD в продукте 1 по изобретению. На фиг. 13 приведен график, показывающий отношение между (степенью активности XOD)1/2 и величиной возрастания тока в продукте 1 по изобретению и сравнительном продукте 1. На фиг. 14 приведен график, показывающий изменение с течением времени тока, когда в продукт 4 по изобретению добавляют XOD до концентрации 100 миллиединиц/мл. На фиг. 15 приведен график, показывающий отношение количества супероксидных анионрадикалов к количественному изменению тока. Наилучший способ осуществления настоящего изобретения Электрод для активных форм кислорода по настоящему изобретению (далее обозначают как "электрод") включает проводящий компонент, на поверхности которого сформирована полимерная мембрана из металлопорфиринового комплекса. Любой компонент, который обычно используют для электродов, может быть без каких-либо специальных ограничений использован в качестве проводящего компонента для электрода по настоящему изобретению. Примеры включают различные виды углерода, такие как стеклоуглерод (GC), графит, пирографит (PG), высокоориентированный пирографит (HOPG) и активированный углерод, благородные ме-2 006719 таллы, такие как платина, золото и серебро, и In2 О 3/SnО 2 (РТО). Из них стеклоуглерод является наиболее предпочтительным с точки зрения экономической эффективности, технологичности, малого веса и т.п. Не существует специальных ограничений формы проводящего компонента, кроме того, что эта форма могла бы быть использована в качестве электрода. Могут быть использованы различные формы, такие как цилиндры, прямоугольные столбиковые контакты, иглы и волокна. Игольчатая форма является предпочтительной, например, для определения концентрации активных форм кислорода in vivo. В настоящем изобретении полимерная мембрана металлопорфиринового комплекса образуется на поверхности проводящего компонента. В качестве примеров металлопорфириновых комплексов, используемых для получения полимерной мембраны, могут быть приведены следующие соединения формулы где М обозначает металл, выбранный из группы, состоящей из железа, марганца, кобальта, хрома и иридия по крайней мере одну из четырех групп R выбирают из группы, состоящей из тиофурильной группы,пирролильной группы, фурильной группы, меркаптофенильной группы, аминофенильной группы и гидроксифенильной группы, и остальные группы R обозначают любую из указанных групп, алкильную группу, арильную группу или водород. где М и R имеют то же значение, что и указанное ранее по крайней мере один из двух L обозначает азотсодержащий аксиальный лиганд, такой как имидазол и его производное, пиридин и его производное,анилин и его производное, гистидин и его производное и триметиламин или его производное, серусодержащий аксиальный лиганд, такой как тиофенол и его производное, цистеин и его производное, метионин и его производное, или кислородсодержащий аксиальный лиганд, такой как бензойная кислота и ее производное, уксусная кислота и ее производное, фенол и его производное, алифатический спирт и его производное, и воду, а другой L обозначает любой один из указанных аксиальных лигандов или группу без лиганда. Металлопорфириновый комплекс, представленный вышеуказанной формулой (I) или формулой (II),является комплексным соединением, в котором атом металла координационно связан с порфириновым соединением. Указанное порфириновое соединение представляет собой циклическое соединение, образованное четырьмя пиррольными кольцами, в которых четыре метиновые группы соединены друг с другом в -положении, а четыре атома азота расположены так, что они направлены лицом к лицу в сторону центра комплекса. Комплексное соединение (металлопорфириновый комплекс) можно получить, поместив атом металла в центр. Для получения этого соединения можно использовать обычный способ получения комплекса металла, такой как введение атома металла в центр порфирина с помощью металлирования. В настоящем изобретении в качестве металла, который вводят в центр порфиринового соединения, могут быть использованы разнообразные металлы, такие как железо, марганец, кобальт, хром и иридий. Подходящий атом металла может быть выбран в зависимости от типа измеряемых активных форм кислорода. Например, железо, марганец, кобальт и т.п. предпочтительно используют при измерении супероксидных анион-радикалов; железо, кобальт, марганец, хром, иридий и т.п. предпочтительно используют при измерении молекулярного кислорода; железо, марганец и т.п. предпочтительно используют при измерении пероксида водорода; а железо, марганец и т.п. предпочтительно используют при измерении ОН, NO, ONOO- и т.п. Порфириновое соединение, которое используют по настоящему изобретению, предпочтительно представляет собой порфириновое соединение, в котором по крайней мере одно из положений 5, 10, 15 и 20, в соответствии с нумерацией положений по номенклатуре IUPAC, замещено тиофурильной группой,пирролильной группой, фурильной группой, меркаптофенильной группой, аминофенильной группой,гидроксифенильной группой или подобным, а другие положения замещены любой из указанных групп,-3 006719 алкильной группой, арильной группой или водородом. В качестве конкретных примеров можно привести следующие соединения: 5,10,15,20-тетракис(2-тиофурил)порфирин,5,10,15,20-тетракис(3-тиофурил)порфирин,5,10,15,20-тетракис(2-пирролил)порфирин,5,10,15,20-тетракис(3-пирролил)порфирин,5,10,15,20-тетракис(2-фурил)порфирин,5,10,15,20-тетракис(3-фурил)порфирин,5,10,15,20-тетракис(2-меркаптофенил)порфирин,5,10,15,20-тетракис(3-меркаптофенил)порфирин,5,10,15,20-тетракис(4-меркаптофенил)порфирин,5,10,15,20-тетракис(2-аминофенил)порфирин,5,10,15,20-тетракис(3-аминофенил)порфирин,5,10,15,20-тетракис(4-аминофенил)порфирин,5,10,15,20-тетракис(2-гидроксифенил)порфирин,5,10,15,20-тетракис(3-гидроксифенил)порфирин,5,10,15,20-тетракис(4-гидроксифенил)порфирин,[5,10,15-трис(2-тиофурил)-20-моно(фенил)]порфирин,[5,10,15-трис(3-тиофурил)-20-моно(фенил)]порфирин,[5,10-бис(2-тиофурил)-15,20-ди(фенил)]порфирин,[5,10-бис(3-тиофурил)-15,20-ди(фенил)]порфирин,[5,15-бис(2-тиофурил)-10,20-ди(фенил)]порфирин,[5,15-бис(3-тиофурил)-10,20-ди(фенил)]порфирин,[5-моно(2-тиофурил)-10,15,20-три(фенил)]порфирин и[5-моно(3-тиофурил)-10,15,20-три(фенил)]порфирин. Среди лигандов, представленных L в соединении формулы (II), в качестве примеров производного имидазола можно назвать метилимидазол, этилимидазол, пропилимидазол, диметилимидазол и бензимидазол; в качестве примеров производного пиридина можно назвать метилпиридин, метилпиридилацетат,никотинамид, пиридазин, пиримидин, пиразин и триазин; в качестве примеров производного анилина можно назвать аминофенол и диаминобензол; в качестве примеров производного гистидина можно назвать метиловый эфир гистидина, гистамин и гиппурил-гистидил-лейцин; в качестве примеров производного триметиламина можно привести триэтиламин и трипропиламин; в качестве примеров производного тиофенола можно привести тиокрезол, меркаптофенол, меркаптобензойную кислоту, аминотиофенол, дитиол бензола и дитиол метилбензола; в качестве примеров производного цистеина можно привести метиловый эфир цистеина и этиловый эфир цистеина; в качестве примеров производного метионина можно привести метиловый эфир метионина и этиловый эфир метионина; в качестве примеров производного бензойной кислоты можно привести салициловую кислоту, фталевую кислоту, изофталевую кислоту и терефталевую кислоту; в качестве примеров производного уксусной кислоты можно привести трифторуксусную кислоту, меркаптоуксусную кислоту, пропионовую кислоту и масляную кислоту; в качестве примеров производного фенола можно привести крезол и дигидроксибензол; в качестве примеров производного алифатического спирта можно привести этиловый спирт и пропиловый спирт. Различные способы полимеризации, такие как электролитическая полимеризация, полимеризация в растворе и гетерогенная полимеризация могут использоваться в настоящем изобретении для получения полимерной мембраны металлопорфиринового комплекса на поверхности проводящего компонента. Предпочтительной из них является электролитическая полимеризация. Полимерная мембрана металлопорфиринового комплекса, в частности, может быть получена на поверхности проводящего компонента с помощью полимеризации. Полимеризацию осуществляют двухэлектродным электролизом (рабочий электрод и противоэлектрод) или трехэлектродным электролизом (рабочий электрод, противоэлектрод и электрод сравнения), включая трехэлектродный электролиз при постоянном потенциале, трехэлектродный электролиз при постоянной силе тока, трехэлектродный электролиз с инверсной разверткой потенциала и трехэлектродный импульсный электролиз, с использованием подходящего базового электролита,такого как перхлорат тетрабутиламмония (ТВАР: BU4NClO4), перхлорат тетрапропиламмония (ТРАР:Pr4NClO4) или перхлорат тетраэтиламмония (TEAP: Et4NClO4) в органическом растворителе, таком как дихлорметан, хлороформ или четыреххлористый углерод, с использованием проводящего компонента в качестве рабочего электрода, с использованием нерастворимого электрода, такого как электрод из благородного металла (например, платиновый электрод), титановый электрод, углеродный электрод или электрод из нержавеющей стали в качестве противоэлектрода, и с использованием насыщенного каломельного электрода (SCE), серебро-хлорсеребряного электрода или подобного в качестве электрода сравнения. Электролитическую полимеризацию предпочтительно проводят электролизом с инверсной разверткой потенциала или подобным электролизом с использованием, например, трехэлектродной ячейки, показанной на фиг. 1. На фиг. 1 - 1 обозначает контейнер ячейки; 2 - проводящий компонент; 3 - противо-4 006719 электрод; 4 - электрод сравнения; 5 - раствор металлопорфиринового комплекса; 6 - потенциостат; и 7 координатный самописец. При использовании раствора металлопорфиринового комплекса с высокой концентрацией может быть применена, например, двухкамерная трехэлектродная ячейка, приведенная на фиг.2. На фиг. 2 цифры 1-7 имеют те же значения, что и на фиг. 1, 8 обозначает раствор электролита, а 9 - ампулу с образцом. Для получения упрощенного электрода для активных форм кислорода (электрода игольчатого типа) могут быть использованы, например, электрод игольчатого типа 10 и трехэлектродная ячейка, приведенные на фиг. 3(А) и 3(В). На фиг. 3 - 1 обозначает контейнер ячейки; 4 - электрод сравнения; 5 - раствор металлопорфиринового комплекса; 6 - потенциостат; 7 координатный самописец; 8 - раствор электролита; 9 - ампулу с образцом; 10 - электрод игольчатого типа; 11 - противоэлектрод; 12 - кончик проводящего компонента (область металлопорфириновой полимерной мембраны); 13 - электроизолирующий материал; и 14 - проволочное соединение противоэлектрода. Как показано на фиг. 3(С), указанный электрод использует противоэлектрод 11, полученный путем заполнения маленькой трубки из электроизолирующего материала 13 проводящим компонентом и путем покрытия указанной маленькой трубки металлом, который используют в качестве противоэлектрода. Электрод может быть использован как электрод игольчатого типа за счет формирования металлопорфириновой полимерной мембраны на поверхности кончика 12 проводящего компонента. Толщину полимерной мембраны металлопорфиринового комплекса подбирают соответствующим образом в зависимости от типа электрода и металлопорфиринового комплекса и от типа измеряемых активных форм кислорода. С точки зрения активности электрода, устойчивости модификации и т.п. предпочтительна толщина 1 мкм или менее. Для получения упрощенного электрода для активных форм кислорода (улучшенного электрода игольчатого типа), на основе упрощенного электрода для активных форм кислорода (электрод игольчатого типа), приведенного на фиг. 3, с целью удаления ненужного тока в живом организме, токовых шумов и т.п. и с целью улучшения чувствительности, отношение сигнал/шум (S/N) и т.п., могут быть использованы, например, улучшенный электрод игольчатого типа 15, приведенный на фиг. 4(А), и трехэлектродная ячейка, приведенная на фиг. 3(А). На фиг. 4 - 11 обозначает противоэлектрод; 12 - кончик проводящего компонента (область металлопорфириновой полимерной мембраны); 13 - электроизолирующий материал; 14 - проволочное соединение противоэлектрода; 15 - улучшенный электрод игольчатого типа; 16 - заземление; и 17 - проволочное соединение заземления. Как показано на фиг. 4(В), в указанном электроде проводящий компонент помещен в электроизолирующий материал 13 (двухслойная структура). Электроизолирующий материал 13 помещают в материал противоэлектрода 11 (трехслойная структура), материал противоэлектрода 11 размещают в электроизолирующем материале 13 (четырехслойная структура) и, наконец, снаружи полученная маленькая трубка покрыта материалом, таким как металл, способный выполнять функцию заземления (пятислойная структура). Покрытие действует как заземление 16. Указанный электрод может быть использован как улучшенный упрощенный электрод для активных форм кислорода (улучшенный/игольчатый электрод) путем формирования металлопорфириновой полимерной мембраны на поверхности кончика 12 проводящего компонента. Толщину полимерной мембраны металлопорфиринового комплекса подбирают соответствующим образом в зависимости от типа электрода и металлопорфиринового комплекса и от типа измеряемых активных форм кислорода. С точки зрения активности электрода, устойчивости модификации и т.п. предпочтительна толщина 1 мкм или менее. Указанный улучшенный/игольчатый электрод может быть также использован для измерения композитных материалов и т.п. В этом случае можно изготовить электрод,имеющий структуру из десяти или более слоев. В качестве металла для заземления может быть использован благородный металл, такой как платина, золото, титан, нержавеющая сталь, и серебро, коррозионностойкий сплав, такой как железохромовый сплав, углерод или подобное. Поскольку заземление часто используют в условиях in vivo, то предпочтительным является материал, обладающий высокой безопасностью, такой как благородный металл (например, платина, золото, серебро), титан, нержавеющая сталь и углерод. С целью использования электрода по настоящему изобретению для измерения активных форм кислорода, в частности, для измерения концентрации активных форм кислорода, предпочтительно объединяют электрод (1) с противоэлектродом и электродом сравнения (трехэлектродный тип) или (2) с противоэлектродом (двухэлектродный тип). В качестве материала для указанного противоэлектрода может быть использован благородный металл, такой как платина, золото и серебро, титан, нержавеющая сталь, коррозионностойкий сплав, такой как железохромовый сплав, углерод или подобное. Поскольку противоэлектрод часто используют в условиях in vivo, то предпочтительным является материал, обладающий высокой безопасностью, такой как благородный металл (например, платина, золото, серебро), титан и углерод. В качестве электрода сравнения могут быть использованы различные электроды сравнения, такие как серебро/хлорсеребряный электрод и ртуть/хлорртутный электрод. Может также использоваться стандартный твердотельный электрод.-5 006719 Специфический пример измерительного устройства, которое может быть использовано для измерения активных форм кислорода, приведен на фиг. 5. На фиг. 5 цифры 1, 3, 4, 6 и 7 имеют те же значения,что и на фиг. 1, 18 обозначает измерительный электрод (рабочий электрод), 19 - микрошприц, 20 - измеряемый раствор, 21 - магнитную мешалку, 22 - мешалку. Другой специфический пример измерительного устройства для измерения активных форм кислорода приведен на фиг. 6. На фиг. 6 числа 1, 6, 7 и 19-22 имеют те же значения, что и на фиг. 4, а 10 обозначает электрод игольчатого типа. Несмотря на то, что электрод для активных форм кислорода по настоящему изобретению может быть использован в качестве электрода для обнаружения активных форм кислорода, таких как супероксидные анион-радикалы, с помощью вышеуказанного устройства, этот электрод может также использоваться в качестве сенсора для измерения концентрации активных форм кислорода использованием в комбинации с (1) противоэлектродом и электродом сравнения (трехэлектродный тип) или (2) противоэлектродом (двухэлектродный тип). Если сенсор для измерения концентрации активных форм кислорода с такой конфигурацией используют в системе, содержащей, например, супероксидные анион-радикалы,то металл в металлопорфириновом комплексе, образующем полимерную мембрану, восстанавливается супероксидными анион-радикалами. Так, если металлом является железо, то Fe3+ восстанавливается супероксидными анион-радикалами до Fe2+ (формула (7. Если Fe2+, восстановленное супероксидными анион-радикалами, вновь электрохимически окисляется (формула (8 при сохранении на электроде для измерения концентрации значения потенциала (в случае трехэлектродного типа (1 или напряжения (в случае двухэлектродного типа (2, при которых Fe2+ может быть окислен, то в таком случае протекающий ток (ток окисления) соответствует концентрации супероксидных анион-радикалов. Таким образом, концентрацию супероксидных анион-радикалов, растворенных в растворе образца, можно количественно определить по величине тока окисления. В частности, концентрацию супероксидных анион-радикалов можно определить, используя тот же принцип, что и в приведенных выше формулах (5) и (6). Количественное определение на основе этого принципа возможно также и для активных форм кислорода, таких как пероксид водорода и ОН, других активных форм радикалов, таких как NO, ONOO- и т.п. где "Роr" обозначает порфирин. Поскольку электрод для активных форм кислорода по настоящему изобретению имеет на поверхности проводящего элемента полимерную мембрану из металлопорфиринового комплекса, то электрод достаточно прочен и не вызывает проблем с дезактивацией, по сравнению с обычным электродом с иммобилизованным цитохромом с. Далее, поскольку полимерную мембрану из металлопорфирина формируют электролитической полимеризацией или подобным способом, то получение электрода по настоящему изобретению является простым по сравнению с обычным электродом. Электроду по настоящему изобретению можно при изготовлении придать форму, особенно пригодную для использования in vivo,например, игольчатую форму. Таким образом, электрод для активных форм кислорода по настоящему изобретению может не только определять активные формы кислорода, такие как супероксидные анион-радикалы, пероксид водорода и ОН и другие активные формы радикалов (NO, ONOO- и т.п.), но также количественно измерять эти активные формы кислорода в сочетании с противоэлектродом и электродом сравнения в любой среде, включая условия in vivo, а также условия in vitro. Электрод по настоящему изобретению может широко использоваться в различных областях техники. В частности, поскольку различные заболевания можно определить in vivo по наличию активных форм кислорода и других активных форм радикалов, то можно обнаружить такие заболевания, как рак,путем например, измерения концентрации активных форм кислорода в крови. С другой стороны, что касается применения в условиях in vitro, можно наблюдать условия разложения пищи путем определения активных форм кислорода и измерения их концентрации в пище. Состояние воды с точки зрения загрязнений можно также наблюдать путем определения активных форм кислорода и измерения их концентрации в водопроводной и сточной воде. Далее, концентрацию супероксидных анион-радикалов и супероксиддисмутазы (SOD), представляющей собой фермент, функция которого заключается в удалении анионов, можно измерить путем определения степени уменьшения содержания супероксидных анион-радикалов после добавления образца,содержащего SOD. Примеры Изобретение далее более подробно поясняется в сравнительных примерах, примерах и тестовых примерах, которые не следует рассматривать как ограничивающие настоящее изобретение. Сравнительный пример 1. Синтез 5,10,15,20-тетракис(3-тиофенил) порфирина (Н 2 Т 3 ТhР). В круглодонную колбу емкостью 100 мл помещают 50 мл пропионовой кислоты, 2,0 мл 3 тиофенкарбальдегида и 1,4 мл пиррола. Смесь кипятят с обратным холодильником при перемешивании в-6 006719 течение часа при температуре 160 С. По окончании кипячения реакционной смеси дают остыть до комнатной температуры, затем охлаждают льдом и добавляют 200 мл охлажденного метанола. Смесь фильтруют с помощью вакуума. Фильтрат промывают метанолом и очищают методом хроматографии на силикагеле (проявляющий растворитель - хлороформ). Растворитель выпаривают досуха и твердое вещество перекристаллизовывают и сушат при пониженном давлении, получая H2T3ThP в виде кристаллического порошка черного цвета (выход: 0,63 г, 19%). Продукт идентифицируют с помощью УФ-видимого спектрофотометра (UV-2100, изготовитель - Shimadzu Corp.) и с помощью измерения 1H-NMR (ЯМР). Результаты приведены в табл. 1 и 2. Сравнительный пример 2. Синтез 5,10,15,20-тетракис(2-аминофенил)порфирина (Н 2 Т 2 АmР). В четырехгорлую колбу емкостью 2 л, снабженную обратным холодильником, помещают 500 мл пропионовой кислоты. После добавления 25 г 2-нитробензальдегида смесь при перемешивании кипятят с обратным холодильником при температуре 110 С. Добавляют 12 мл пиррола и смесь кипятят с обратным холодильником в течение 30 мин. Добавляют 50 мл хлороформа, смесь охлаждают льдом и фильтруют с помощью вакуума. Фильтрат промывают 400 мл хлороформа, сушат при пониженном давлении (100 С, 6 ч, 0,1 кПа) и получают предшественник 5,10,15,20-тетракис (2-нитрофенил)порфирин (Н 2 Т 2NО 2 Р) в виде кристаллов темно-пурпурного цвета (выход: 5,0 г, 14%). В четырехгорлую колбу емкостью 2 л помещают 300 мл 12N раствора НСl. Добавляют 5,0 г синтезированного, как описано выше, 5,10,15, 20-тетракис(2-нитрофенил)порфирина (H2T2NO2P) и 20,0 г дигидрата хлорида олова (II) и смесь нагревают при температуре 65-70 С в течение 30 мин. Постепенно добавляют водный раствор аммиака и смесь фильтруют с помощью вакуума. Фильтрат сушат при пониженном давлении. В колбу емкостью 2 л загружают фильтрат. Фильтрат экстрагируют 10 л ацетона и экстракт упаривают досуха, используя испаритель. Сухое твердое вещество растворяют в 2 л хлороформа. Раствор промывают водным раствором аммиака и деионизованной водой и сушат над безводным сульфатом натрия. Растворитель упаривают досуха с помощью испарителя и твердое вещество перекристаллизовывают и сушат при пониженном давлении, получая Н 2 Т 2 АmР в виде кристаллов пурпурного цвета (выход: 4,0 г, 90%). Продукт идентифицируют с помощью УФ-видимого спектрофотометра (UV2100, изготовитель -Shimadzu Corp.) и путем измерения 1H-ЯMP аналогично сравнительному примеру 1. Результаты приведены в табл. 1 и 2. На фиг. 7(а) приведен УФ-видимый спектр H2T3ThP, а на фиг. 8(а) приведен УФ-видимый спектр Н 2 Т 2 АmР. Таблица 1 Результаты идентификации Результаты идентификации для Н 2 Т 3 ТhР и Н 2 Т 2 АmР в табл. 1 подтверждают наличие пиков протонов, образующих порфириновое кольцо, и пиков, специфичных для порфириновых соединений. Н 2 Т 2 АmР подтверждают по пику при 4,0 м.д., который соответствует пику протонов, образующих ами-7 006719 ногруппу. Результаты в табл. 2 и на фиг. 7(а) и 8(а) подтверждают УФ-видимые спектры Н 2 Т 3 ТhР и Н 2 Т 2 АmР. Приведенные результаты подтверждают, что в сравнительных примерах 1 и 2 синтезированы Н 2 Т 3 ТhР и Н 2 Т 2 АmР. Сравнительный пример 3. Синтез металлопорфиринового комплекса (1) (введение центрального металла (Fe) в Н 2 Т 3 ТhР путем металлирования). В трехгорлую колбу емкостью 50 мл помещают 10 мл 48%-ной бромисто-водородной кислоты. Продувают азотом в течение 30 мин, а затем добавляют 100 мг восстановленного железа. Смесь перемешивают при 100 С до тех пор, пока восстановленное железо не растворится. После перемешивания растворитель упаривают при пониженном давлении и получают ангидрид бромида железа в виде порошка белого цвета. К продукту добавляют 250 мг порфирина (H2T3ThP), полученного в сравнительном примере 1, и 200 мл диметилформамида (ДМФА), в который предварительно подают азот в течение 30 мин. Дают полученной смеси прореагировать в атмосфере азота в течение 4 ч. По окончании реакции к полученному продукту добавляют 200 мл хлороформа. Смесь промывают деионизованной водой, сушат над безводным сульфатом натрия и фильтруют. Растворитель упаривают в испарителе и полученное твердое вещество очищают колоночной хроматографией на оксиде алюминия (проявляющий растворитель: хлороформ/метанол=20/1). Затем к элюату добавляют 48%-ную бромисто-водородную кислоту, сушат смесь безводным сульфатом натрия и отфильтровывают. Растворитель упаривают, и твердое вещество перекристаллизовывают и сушат при пониженном давлении, получая металлопорфирин (Н 2 Т 3 ТhР, содержащий в центре железо; далее обозначают как "FeT3ThP") в виде кристаллов черного цвета (выход: 230 мг,84%). Сравнительный пример 4. Синтез металлопорфиринового комплекса (2) (введение центрального металла (Fe) в H2T2AmP путем металлирования). Черные кристаллы металлопорфиринового комплекса, содержащего железо в центре Н 2 Т 2 АmР (далее обозначают как "FeT2AmP"), получают аналогично тому, как описано в сравнительном примере 3, за исключением того, что используют 250 мг Н 2 Т 2 АmР (полученного в сравнительном примере 2) в качестве порфиринового соединения (выход: 224 мг, 83%). Продукты, полученные в сравнительных примерах 3 и 4, идентифицируют с помощью УФ-видимого спектрофотометра. Результаты приведены на фиг. 7 и 8 и в табл. 2. На фиг. 7(а) приведен УФ-видимый спектр H2T3ThP, а на фиг. 7(b) приведен УФ-видимый спектрFeT2AmP. В табл. 3 приведены результаты измерения УФ-видимых спектров. Порфириновые соединения, в которых металл не координирован в центре (H2T3ThP и Н 2 Т 2 АmР),имеют пик при около 400 нм, соответствующий сопряженному кольцу. Коэффициент молекулярной экстинкции пика составляет 3,6-6,0 х 105 М-1 см-1. Этот пик называют полосой Сорета. Далее, порфириновое соединение имеет четыре пика, называемых Q-полосами, коэффициент молекулярной экстинкции которых в видимой области спектра составляет 104 М-1 см-1. Введение металла обычно подтверждают по спектральным изменениям в Q-полосах. Сравнение (а) и (b) на фиг. 7 и в табл. 2 показывает, что имеется четыре пика в Q-полосах в (а), а на рисунке (b) количество пиков уменьшается до одного. Это согласуется с типичным поведением при образовании порфирином комплекса с металлом. Таким образом, подтверждается, что порфирин образовал комплекс с железом, и тем самым подтверждается синтез металлопорфиринового комплекса. Сравнительный пример 5. Синтез металлопорфиринового комплекса (3) (введение центрального металла (Мn) в Н 2 Т 3 ТhР путем металлирования). В четырехгорлую колбу емкостью 300 мл, которую можно нагревать над масляной баней при перемешивании на магнитной мешалке, и снабженную обратным холодильником и трубкой для подачи аргона из баллона, расположенной сверху, помещают 100 мл ДМФА, содержащего 0,5 г ацетата марганца и 0,5 г H2T3ThP, полученного в сравнительном примере 1. После насыщения аргоном, смесь кипятят с обратным холодильником при температуре 140 С в течение 1 ч. Полученный раствор выливают в делительную воронку и промывают хлороформом и деионизованной водой. Затем добавляют безводный сульфат магния, и смесь сушат в течение часа, а затем отфильтровывают. Фильтрат упаривают досуха в испарителе. Сухое твердое вещество отделяют и очищают методом колоночной хроматографии (наполнитель: основной оксид алюминия, элюент: хлороформ/метанол = 20/1). После фильтрации фильтрат упаривают досуха. Твердое вещество сушат при пониженном давлении (0,1 кПа, 100 С) и получают МnТ 3 ТhР в виде темно-пурпурных кристаллов (выход: 0,36 г). Для подтверждения введения металла измеряют УФ-видимый спектр поглощения. Пики поглощения МnТ 3 ТhР наблюдают при 380 нм, 405 нм, 480 нм, 533 нм, 583 нм и 623 нм, которые отличаются от приведенных ранее для Н 2 Т 3 ТhР. Таким образом, подтверждают введение металла. Сравнительный пример 6. Синтез металлопорфиринового комплекса, содержащего аксиальный лиганд (1) (синтез FeT3ThP, с которым координационно связан 1-метилимидазол).(FeT3ThP: 1-метилимидазол=1-50 (молярное отношение добавляют к 0,5 мл дихлорметана. Смесь перемешивают при ультразвуковой обработке (15 Вт) в течение 5 мин или без такой обработки в течение 6 ч или более. Для подтверждения координирования лиганда измеряют УФ-видимый спектр поглощения. Пик поглощения комплекса, полученного координированием 1-метилимидазола к FeT3ThP, появляется при 421 нм и отличается от рассмотренного выше спектра FeT3ThP. Тем самым подтверждают координирование лиганда. Комплекс упаривают досуха в испарителе и оставляют на хранение или же используют для изготовления электрода для активных форм кислорода. Пример 1. Изготовление электрода для активных форм кислорода (1). Электрод из стеклоуглерода (GC) (диаметр: 1,0 мм, изготовитель - BAS Inc.) полируют с помощью полирующего агента на основе оксида алюминия (0,05 мкм). Электрод промывают водой и затем метанолом. Полимерную мембрану формируют на поверхности указанного электрода методом электролитической полимеризации с использованием следующего раствора электролита и способа получения электрода из стеклоуглерода со сформированной на его поверхности полимерной мембраной FeT3ThP (продукт по изобретению 1) и электрода из стеклоуглерода со сформированной на его поверхности полимерной мембраной FeT2AmP (продукт по изобретению 2).(Анализируемый раствор) В качестве металлопорфиринового комплекса используют FeT3ThP или FeT2AmP, синтезированные в сравнительных примерах 3 или 4, в растворе с концентрацией 0,05 М. В качестве растворителя используют дихлорметан (безводный), содержащий 0,1 М перхлората тетрабутиламмония (Bu4NClO4/(Методика) Электролитическую полимеризацию осуществляют электролизом с инверсной разверткой потенциала, используя трехэлектродную ячейку, которая имеет конфигурацию, показанную на фиг. 1 (рабочий электрод: стеклоуглерод, противоэлектрод: Pt, электрод сравнения: насыщенный каломельный электрод(SCE). Диапазон развертки составляет от 0 до 2,0 В для SCE в случае изготовления электрода для активных форм кислорода с использованием FeT3ThP; диапазон развертки составляет от минус 0,2 до 1,4 В для SCE в случае изготовления электрода для активных форм кислорода с использованием FeT2AmP. Скорость развертки в обоих случаях составляет 0,05 В/с. Количество разверток составляет одну дляFeT3ThP и три для FeT2AmP. Циклическую вольтаммограмму, полученную при осуществлении указанного электролитического процесса (CV-кривая), записывают на координатном самописце (изготовительRiken Denshi Co., Ltd.). Результаты приведены на фиг. 9 и 10. Фиг. 9 показывает CV-кривую в процессе электролитической полимеризации при получении электрода с использованием FeT3ThP в качестве металлопорфиринового комплекса. На основе полученной кривой делают вывод, что катион-радикалы тиофена образуются при +1,74 В (для SCE). Поскольку вследствие восстановления катион-радикалов при обращении развертки потенциала практически никакого катодного тока не протекает, то считают, что образовавшиеся катион-радикалы мгновенно полимеризуются в растворе. Пик восстановления при около 0,6 В (для SCE), как предполагают, является окислительно-восстановительной характеристикой полимера. Полученные результаты подтверждают, что на поверхности электрода из стеклоуглерода образовалась полимерная мембрана металлопорфиринового комплекса (FeT3ThP). Фиг. 10 показывает CV-кривую в процессе электролитической полимеризации при получении электрода с использованием FeT2AmP в качестве металлопорфиринового комплекса. На основе полученной кривой делают вывод, что катион-радикалы анилина (аминобензола) образуются при +1,02 В (для SCE). Поскольку вследствие восстановления катион-радикалов при обращении развертки потенциала практически никакого катодного тока не протекает, то считают, что образовавшиеся катион-радикалы мгновенно полимеризуются в растворе. Пик восстановления при около 0,1 В (для SCE), как предполагают, является окислительно-восстановительной характеристикой полимера. Такой же пик обнаруживается и при второй развертке. Так подтверждается дальнейшее протекание реакции полимеризации. Пик восстановления при около 0,23 В (для SCE), как предполагают, является окислительно-восстановительной характеристикой полимера. Полученные результаты подтверждают, что на поверхности электрода из стеклоуглерода образовалась полимерная мембрана металлопорфиринового комплекса (FeT2AmP). Пример 2. Получение электрода для активных форм кислорода (2). Готовят электрод из стеклоуглерода, покрытый полиэфир(эфир)кетоном (PEEK, ПЭЭК) таким образом, что открытым остается только один конец (диаметр ПЭЭК: 3 мм; диаметр стеклоуглерода: 1 мм,площадь кончика: 0,0079 см 2; другой конец выполнен из латуни). Стеклоуглеродный конец электрода последовательно полируют алмазной пастой с размером зерен 6 мкм, а затем алмазной пастой с размером зерен 1 мкм. По окончании финишной полировки на полировальнике из оксида алюминия с использова-9 006719 нием полирующего средства на основе оксида алюминия (0,05 мкм) электрод промывают деионизованной водой и ацетоном. 0,0037 г FeT2AmP, полученного в сравнительном примере 4, и 0,171 г ТВАР помещают в мензурку емкостью 5 мл. К смеси добавляют ацетонитрил и доводят общий объем до 5 мл, получая анализируемый раствор. Анализируемый раствор помещают в пробирку ячейки. Готовят трехэлектродную электрохимическую ячейку со стеклоуглеродным электродом в качестве рабочего электрода, приведенную на фиг. 1. Воздух из ячейки вытесняют аргоном. Развертку потенциала проводят трижды в диапазоне развертки потенциала от минус 0,3 до 1,0 В дляAg/Аg+ при скорости развертки потенциала 200 мВ/с. Исходный и конечный потенциал развертки дляAg/Ag+ составляют 0 В. Вначале проводят развертку в отрицательном направлении. По завершении развертки ячейку последовательно промывают ацетонитрилом и деионизованной водой и получают стеклоуглеродный электрод со сформированной на его поверхности полимерной мембраной из FeT2AmP (продукт по изобретению 3). Пример 3. Получение электрода для активных форм кислорода (3). 0,171 г ТВАР помещают в мензурку емкостью 5 мл. Добавляют дихлорметан и доводят общий объем до 5 мл, получая раствор электролита. 0,0182 г FeT2AmP, полученного в сравнительном примере 4, 0,0171 г ТВАР и 0,5 мл дихлорметана помещают в пробирку для образца, при этом кончик пробирки, который герметизируют вайкором, погружают в раствор электролита. Платиновый противоэлектрод и стеклоуглеродный электрод, который используют в примере 2, помещают в пробирку для образца, a Ag/Ag+ электрод размещают с внешней стороны пробирки, как показано на фиг.2, и получают двухкамерную трехэлектродную электрохимическую ячейку. Воздух из камер вытесняют аргоном. Развертку потенциала проводят трижды в диапазоне развертки потенциала от минус 0,3 до 2,5 В дляAg/Ag+ при скорости развертки потенциала 50 мВ/с. Исходный потенциал развертки для Ag/Ag+ составляет 0 В, а конечный потенциал развертки для Ag/Ag+ составляет минус 0,3 В. Вначале проводят развертку в отрицательном направлении. По завершении развертки ячейку последовательно промывают дихлорметаном и деионизованной водой и получают стеклоуглеродный электрод со сформированной на его поверхности полимерной мембраной из FeT2AmP (продукт по изобретению 4). Пример 4. Получение электрода для активных форм кислорода (4). Электрод в виде стержня из стеклоуглерода (диаметр: 0,28-0,30 мм) помещают в стеклянный капилляр (внутренний диаметр: 0,3 мм). Полученный продукт помещают в иглу (изготавливают из платины, нержавеющей стали или подобного, и она соответствует приблизительно игле для инъекций 18G). Эти продукты объединяют и герметизируют с помощью эпоксидного адгезива, акрилового адгезива, маникюра или подобного. Затем стеклоуглерод и внешнюю иглу с помощью проводящего адгезива, такого как серебряная паста или углеродная паста, соединяют, соответственно, с платиновым электродом, электродом из нержавеющей стали, медным электродом или подобным. Кончик полируют на шлифовальном станке и получают электрод игольчатого типа, имеющий трехслойную структуру, показанную на фиг. 3(стеклоуглерод: рабочий электрод, внутренний стеклянный капилляр: изолятор между рабочим электродом и противоэлектродом, внешняя игла: противоэлектрод). Раствор электролита (5 мл), который получают так же, как в примере 3, помещают в контейнер ячейки. Дихлорметановый раствор FеТ 3 ТhР, полученного в сравнительном примере 6, к которому координирован 1-метилимидазол, содержащий 0,0171 г ТВАР, помещают в пробирку для образца, при этом кончик пробирки, который герметизируют вайкором, погружают в раствор электролита. Полученные, как описаны выше, электроды игольчатого типа (рабочий электрод и противоэлектрод) помещают в пробирку для образца, а Аg/Аg+ электрод размещают с внешней стороны пробирки,как показано на фиг. 3, и получают двухкамерную трехэлектродную электрохимическую ячейку. Ячейку электролитически полимеризуют методом инверсной развертки потенциала (диапазон развертки потенциала: от минус 0,1 до +2,0 В для Ag/Ag+, скорость развертки потенциала: от 10 до 500 мВ/с) и методом при постоянном потенциале (потенциал: +2,0 В для Ag/Ag+) в течение 5-120 мин. После электролитической полимеризации ячейку последовательно промывают дихлорметаном и деионизованной водой и получают электрод игольчатого типа с трехслойной структурой, включающий стеклоуглеродный электрод со сформированной на его поверхности полимерной мембраной из FеТ 3 ТhР, к которому координирован 1-метилимидазол (стеклоуглерод, поверхность которого модифицирована полимерной мембраной: рабочий электрод, внутренний стеклянный капилляр: изоляция между рабочим электродом и противоэлектродом, внешняя игла: противоэлектрод; продукт по изобретению 5). Сравнительный пример 1. Получение золотого электрода с иммобилизованным цитохромом с. В качестве сравнительного продукта для электродов по настоящему изобретению указанным ниже способом получают золотой электрод с иммобилизованным цитохромом с в качестве электрода для определения концентрации супероксидных анион-радикалов.-10 006719 Золотой электрод (диаметр: 1,6 мм, изготовитель - ВАS Inc.) полируют с помощью полирующего средства на основе оксида алюминия (0,05 мкм) и промывают водой. Электрод подвергают электролитической обработке в 1 М растворе H2SO4 и промывают водой. Далее, электрод погружают в 10 мМ раствор 3-меркаптопропионовой кислоты (далее обозначают как МРА, изготовитель - Aldrich Co.) (растворитель: 10 мМ кислый фосфатный буферный раствор (рН 7,0) в течение 24 ч и получают МРАмодифицированный золотой электрод. После промывки электрода водой проводят развертку потенциала в 0,48 мМ растворе цитохрома с (тип IV из сердца лошади, изготовитель - Sigma Co.) (растворитель: 10 мМ кислый фосфатный буферный раствор (рН 7,0 в течение 30 мин (диапазон развертки: от минус 0,4 до 0,4 В (для Ag/AgCl), скорость развертки: 0,05 В/с). Добавляют 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC) (изготовитель - Pierce ChemicalCo.), чтобы получить конечную концентрацию 0,5 М, и затем погружают электрод в смесь на два часа. Наконец, электрод промывают кислым фосфатным буферным раствором и получают золотой электрод с иммобилизованным цитохромом с (сравнительный продукт 1). Указанный ранее кислый фосфатный буферный раствор представляет собой смесь раствора динатрийгидрофосфата и натрийдигидрофосфата. Для проведения разбавлении используют однократно дистиллированную воду. Тестовый пример 1. Измерение количества супероксидных анион-радикалов (1). Количество супероксидных анион-радикалов измеряют с использованием продукта 1 по изобретению и сравнительного продукта 1. Во-первых, электрод продукта 1 по изобретению или сравнительного продукта 1 в качестве рабочего электрода и платиновый электрод в качестве противоэлектрода помещают в контейнер ячейки, а серебряный/хлорсеребряный электрод (Ag/AgCl) используют в качестве электрода сравнения и получают тестовую трехэлектродную ячейку. Аппарат, приведенный на фиг. 5, получают, размещая в центре тестовую трехэлектродную ячейку. В этом тесте диапазон развертки потенциала устанавливают при от минус 0,2 до 0,25 В (для Аg/АgСl) для электрода сравнительного продукта 1 и при от минус 0,5 до 0,5 В(для Ag/AgCl) для электрода продукта 1 по изобретению. Измерения проводят, применяя несколько скоростей развертки. Готовят 2 мМ водный раствор гидроксида калия, содержащий 14,4 мМ ксантина (изготовитель Sigma Co.) и 10 мМ буферного раствора Tris трис(гидроксиметил)аминометана, содержащего 10 мМ раствора хлорида калия (рН 7,5). 0,365 мл первого раствора и 14,635 мл второго раствора смешивают и получают 0,35 мМ раствор ксантина, который используют в качестве тестового раствора. Растворенный в тестовом растворе кислород удаляют с помощью газообразного аргона высокой чистоты. Во-вторых, тестовый раствор добавляют в трехэлектродную ячейку для проведения теста. Прикладывают потенциал 0,2 В (для Ag/AgCl), который значительно выше, чем оксилительновосстановительный потенциал каждого электрода. К тестовому раствору добавляют ксантиноксидазу(XOD, Grade III из жидкого молока, изготовитель - Sigma Со.) до конечной концентрации 0-100 миллиединиц/мл. Регистрируют изменения тока окисления с течением времени. Полученные результаты приведены на фиг. 12 для продукта 1 по изобретению и на фиг. 11 для сравнительного продукта 1. XOD перед использованием подвергают диализу в 10 мл кислого фосфатного буферного раствора (рН 7,0). Все измерения проводят при комнатной температуре.XOD добавляют к ксантину для получения зависимого от дозы количества супероксидных анионрадикалов. Фиг. 11, где показано изменение с течением времени тока окисления при добавлении XOD к сравнительному продукту 1 в качестве контроля, указывает на то, что ток окисления быстро возрастает сразу же после добавления XOD и остается практически постоянным. Фиг. 12, где показано изменение с течением времени тока окисления при добавлении XOD к продукту 1 по изобретению, указывает на то, что ток окисления быстро возрастает сразу же после добавления XOD, как и на фиг. 11, и затем снижается и остается практически постоянным и что величина тока зависит от концентрации XOD, в частности, от количества супероксидных анион-радикалов. На фиг. 13 показана зависимость между (степенью активности XOD)1/2 и величиной увеличения тока при добавлении XOD в продукте 1 по изобретению и сравнительном продукте 1. Активность XOD определяют, учитывая значения согласно следующим документам: Fridovich et al. and Cooper et al. (J.M.McCord and I. Fridovich, J. Boil. chem. , 243, 5753 (1968), J. M. McCord and I. Fridovich, J. Boil. chem., 244,6049 (1969), I. Fridovich, J. Boil. chem., 245, 4053 (1970), and J.M. Cooper, K.R. Greenough, and C.J. McNeil,J. Electroanal. Chem., 347, 267 (1993. Результаты показывают, что величина увеличения тока в продукте 1 по изобретению пропорциональна (степени активности XOD)1/2 и между ними существует линейная зависимость, аналогичная наблюдаемой для сравнительного продукта 1, который используют в качестве контрольного. Эти факты подтверждают, что концентрацию супероксидных анион-радикалов можно измерить с помощью электрода для активных форм кислорода по настоящему изобретению. Тестовый пример 2. Измерение количества супероксидных анион-радикалов (2). Количество супероксидных анион-радикалов измеряют с использованием электрода продукта 5 по изобретению.-11 006719 Электрод продукта 5 по изобретению, в частности, электрод игольчатого типа с трехслойной структурой (стеклоуглерод, поверхность которого модифицирована полимерной мембраной: рабочий электрод, внутренний стеклянный капилляр: изоляция между рабочим электродом и противоэлектродом,внешняя игла: противоэлектрод; продукт 5 по изобретению), измеряют с помощью двухэлектродного способа. В качестве раствора для измерений используют буферный раствор Tris, содержащий 0,15 мМ ксантина (рН 7,5). К раствору добавляют XOD в количестве 0-100 миллиединиц/мл. Приложенное напряжение составляет 0-1,0 В. Изменение тока с течением времени при добавлении XOD до концентрации 100 миллиединиц/мл при приложенном напряжении +0,5 В показано на фиг. 14. График зависимости количества супероксидных анион-радикалов и величины изменения тока, полученной измерением пика величины тока, приведен на фиг. 15. Коэффициент корреляции между количеством супероксидных анион-радикалов и величиной изменения тока, определенный из фиг. 15, составляет 0,995. Это указывает на то, что электрод по настоящему изобретению может эффективно использоваться для измерения количества супероксидных анионрадикалов. Промышленная применимость Электрод для активных форм кислорода по настоящему изобретению может определять активные формы кислорода, такие как супероксидные анион-радикалы, пероксид водорода и ОН и другие активные формы радикалов (NO, ONOO- и т.п.) в любых условиях, включая условия in vivo, а также условия invitro. Кроме того, возможно количественно определить указанные активные формы кислорода и другие активные радикальные формы путем комбинирования электрода с противоэлектродом или электродом сравнения. Таким образом, электрод может широко использоваться в различных областях техники. Например, при использовании в условиях in vivo, по количеству активных форм кислорода и других активных форм радикалов в живом организме можно установить различные болезни. С другой стороны, при использовании в условиях in vitro можно определять активные формы кислорода и измерять их концентрацию в пищевых продуктах, на основании чего можно установить условия разложения пищевых продуктов. Можно также следить за загрязнением воды путем определения активных форм кислорода и измерения их концентрации в водопроводной и сточной воде. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Электрод для активных форм кислорода, включающий проводящий компонент с образованной на поверхности полимерной мембраной из металлопорфиринового комплекса, представленного следующими формулами (I) или (II): где М обозначает металл, выбранный из группы, состоящей из железа, марганца, кобальта, хрома и иридия, по крайней мере одна из четырех групп R выбрана из группы, состоящей из тиофурильной группы,пирролильной группы, фурильной группы, меркаптофенильной группы, аминофенильной группы, а другие группы R обозначают любую из вышеуказанных групп, алкильную группу, арильную группу или водород, где М и R имеют то же значение, что и указанное ранее, по крайней мере один из двух L обозначает азотсодержащий аксиальный лиганд, такой как имидазол и его производное, пиридин и его производное,анилин и его производное, гистидин и его производное, и триметиламин и его производное, серусодержащий аксиальный лиганд, такой как тиофенол и его производное, цистеин и его производное, метионин и его производное, или кислородсодержащий аксиальный лиганд, такой как бензойная кислота и ее про-12 006719 изводное, уксусная кислота и ее производное, фенол и его производное, алифатический спирт и его производное, и воду, и другой L обозначает любой один из указанных аксиальных лигандов или группу без лиганда. 2. Электрод по п.1, где порфириновое соединение, образующее металлопорфириновый комплекс,выбрано из группы, состоящей из 5,10,15,20-тетракис(2-тиофурил)порфирина,5,10,15,20-тетракис(3-тиофурил)порфирина,5,10,15,20-тетракис(2-пирролил)порфирина,5,10,15,20-тетракис(3-пирролил)порфирина,5,10,15,20-тетракис(2-фурил)порфирина,5,10,15,20-тетракис(3-фурил)порфирина,5,10,15,20-тетракис(2-меркаптофенил)порфирина,5,10,15,20-тетракис(3-меркаптофенил)порфирина,5,10,15,20-тетракис(4-меркаптофенил)порфирина,5,10,15,20-тетракис(2-аминофенил)порфирина,5,10,15,20-тетракис(3-аминофенил)порфирина,5,10,15,20-тетракис(4-аминофенил)порфирина,[5,10,15-трис(2-тиофурил)-20-моно(фенил)]порфирина,[5,10,15-трис(3-тиофурил)-20-моно(фенил)]порфирина,[5,10-бис(2-тиофурил)-15,20-ди(фенил)]порфирина,[5,10-бис(3-тиофурил)-15,20-ди(фенил)]порфирина,[5,15-бис(2-тиофурил)-10,20-ди(фенил)]порфирина,[5,15-бис(3-тиофурил)-10,20-ди(фенил)]порфирина,[5-моно(2-тиофурил)-10,15,20-три(фенил)]порфирин и[5-моно(3-тиофурил)-10,15,20-три(фенил)]порфирина. 3. Электрод по п.1 или 2, где проводящий компонент помещен в маленькую трубку, изготовленную из электроизолирующего материала, при этом внешняя часть указанной маленькой трубки покрыта материалом, который действует как противоэлектрод, таким как металл, с образованием противоэлектрода,металлопорфириновая полимерная мембрана сформирована на кончике проводящего компонента, а электрод имеет игольчатую форму. 4. Электрод по п.1 или 2, где проводящий компонент помещен в электроизолирующий материал,который помещен в материал противоэлектрода, который, в свою очередь, помещен в электроизолирующий материал, снаружи покрытый материалом, действующим в качестве заземления, при этом металлопорфириновая полимерная мембрана сформирована на кончике проводящего компонента, а электрод имеет игольчатую форму. 5. Применение электрода по любому из пп.1-4 для измерения супероксидных анион-радикалов. 6. Сенсор для определения концентрации активных форм кислорода, включающий электрод для активных форм кислорода по пп.1-4. 7. Сенсор по п.6, где порфириновое соединение, образующее металлопорфириновый комплекс, выбирают из группы, состоящей из 5,10,15,20-тетракис(2-тиофурил)порфирина,5,10,15,20-тетракис(3-тиофурил)порфирина,5,10,15,20-тетракис(2-пирролил)порфирина,5,10,15,20-тетракис(3-пирролил)порфирина,5,10,15,20-тетракис(2-фурил)порфирина,5,10,15,20-тетракис(3-фурил)порфирина,5,10,15,20-тетракис(2-меркаптофенил)порфирина,5,10,15,20-тетракис(3-меркаптофенил)порфирина,5,10,15,20-тетракис(4-меркаптофенил)порфирина,5,10,15,20-тетракис(2-аминофенил)порфирина,5,10,15,20-тетракис(3-аминофенил)порфирина,5,10,15,20-тетракис(4-аминофенил)порфирина,[5,10,15-трис(2-тиофурил)-20-моно(фенил)]порфирина,[5,10,15-трис(3-тиофурил)-20-моно(фенил)]порфирина,[5,10-бис(2-тиофурил)-15,20-ди(фенил)]порфирина,[5,10-бис(3-тиофурил)-15,20-ди(фенил)]порфирина,[5,15-бис(2-тиофурил)-10,20-ди(фенил)]порфирина,[5,15-бис(3-тиофурил)-10,20-ди(фенил)]порфирина,[5-моно(2-тиофурил)-10,15,20-три(фенил)]порфирина и[5-моно(3-тиофурил)-10,15,20-три(фенил)]порфирина. 8. Сенсор по п.6 или 7, в котором электрод включает проводящий компонент, помещенный в маленькую трубку, изготовленную из электроизолирующего материала, внешняя часть указанной малень-13 006719 кой трубки покрыта материалом, который действует как противоэлектрод, таким как металл, с образованием противоэлектрода, при этом металлопорфириновая полимерная мембрана сформирована на кончике проводящего компонента, а электрод имеет игольчатую форму. 9. Сенсор по п.6 или 7, в котором электрод включает проводящий компонент, помещенный в электроизолирующий материал, который помещен в материал противоэлектрода, который в свою очередь помещен в электроизолирующий материал, снаружи покрытый материалом, действующим в качестве заземления, при этом металлопорфириновая полимерная мембрана сформирована на кончике проводящего компонента, а электрод имеет игольчатую форму. 10. Применение сенсора по любому из пп.6-9 для измерения супероксидных анион-радикалов. 11. Способ определения активных форм кислорода в образце, включающий измерение тока, возникающего в результате окислительно-восстановительной реакции между металлом в металлопорфириновой полимерной мембране и активными формами кислорода, с использованием сенсора по любому из пп.6-10. 12. Способ по п.11, где определяемыми активными формами кислорода являются супероксидные анион-радикалы.
МПК / Метки
МПК: G01N 27/416, G01N 27/48
Метки: форм, электрод, активных, сенсор, использующий, кислорода
Код ссылки
<a href="https://eas.patents.su/20-6719-elektrod-dlya-aktivnyh-form-kisloroda-i-sensor-ispolzuyushhijj-elektrod.html" rel="bookmark" title="База патентов Евразийского Союза">Электрод для активных форм кислорода и сенсор, использующий электрод</a>
Предыдущий патент: Реформинг природного газа в синтез-газ с использованием окисления водорода в пар
Следующий патент: Железосодержащие соединения декстрина для лечения железодефицитной анемии
Случайный патент: N-арилпиперидинзамещенные бифенилкарбоксамиды в качестве ингибиторов секреции аполипопротеина в