Гетероциклические тиоэфиры и кетоны
Формула / Реферат
1. Соединение формулы II
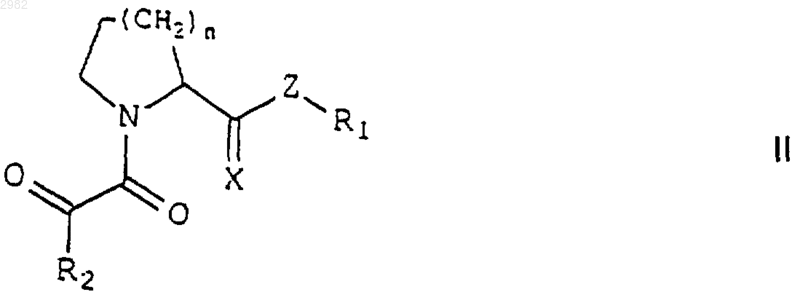
или его фармацевтически приемлемая соль, где
n равно 1 или 2;
Х представляет собой О или S;
Z выбран из группы, состоящей из S, CH2 и CHR1;
R1 представляет собой нормальный или разветвленный С1-С5алкил, замещенный по одному или более чем одному положению Ar1;
R2 выбран из группы, состоящей из нормального или разветвленного С3-С5алкила, С5-С7циклоалкила и Ar1;
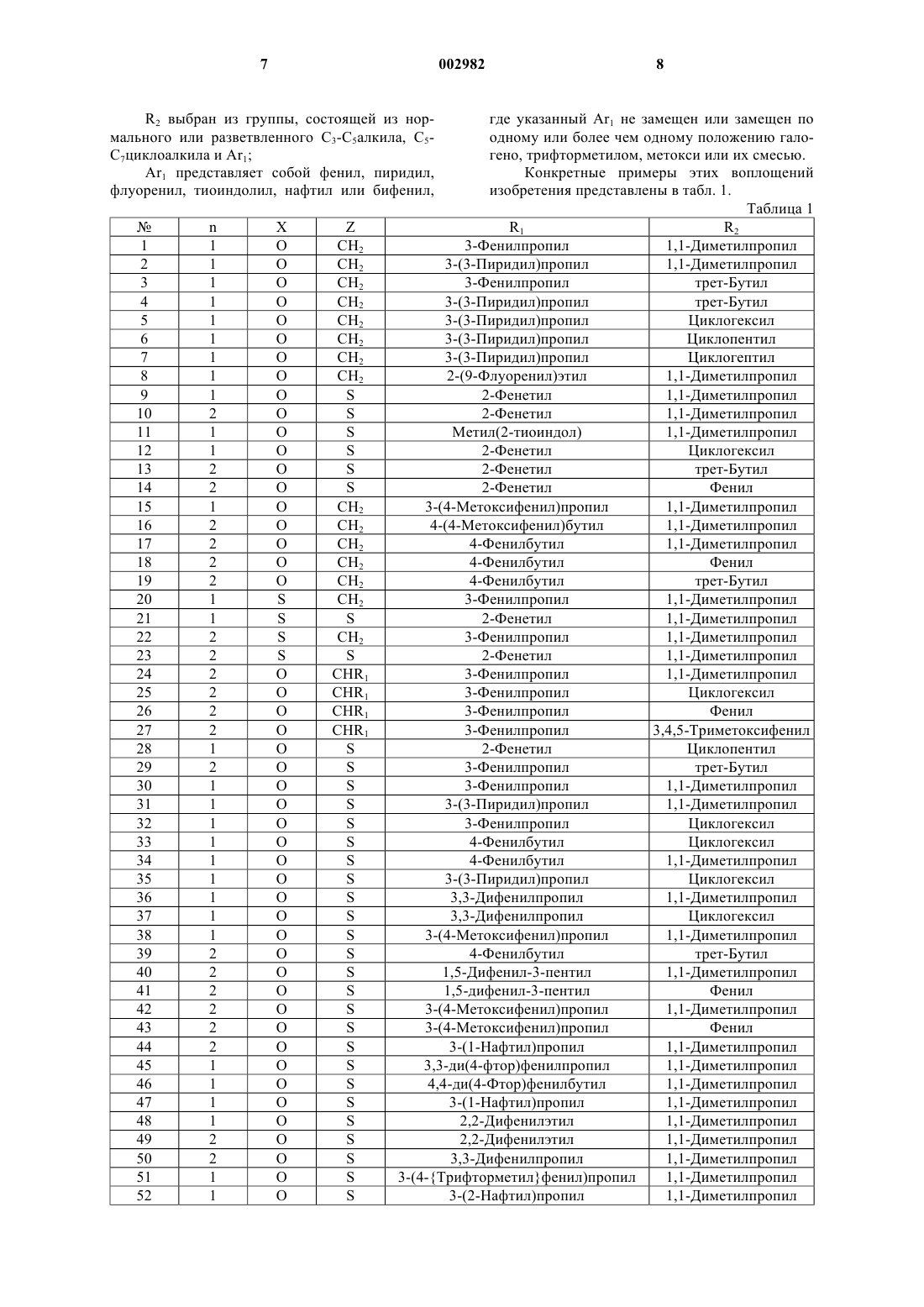
Ar1 представляет собой фенил, пиридил, флуоренил, тиоиндолил, нафтил или бифенил, где указанный Ar1 не замещен или замещен по одному или более чем одному положению галогено, трифторметилом, метокси или их смесью.
2. Соединение по п.1, где
n равно 1; и
Х представляет собой О.
3. Соединение по п.2, где Z представляет собой СН2.
4. Соединение по п.3, которое выбрано из группы, состоящей из
(2S)-2-(1-оксо-5-фенил)пентил-1-(3,3-диметил-1,2-диоксопентил)пирролидина;
3,3-диметил-1-[(2S)-1-(5-(3-пиридил)пентаноил)-1-пирролидин]-1,2-пентандиона;
(2S)-2-(1-оксо-4-фенил)бутил-1-(3,3-диметил-1,2-диоксобутил)пирролидина;
(2S)-2-(1-оксо-4-фенил)бутил-1-(2-циклогексил-1,2-диоксоэтил)пирролидина и
2-(1-оксо-4-фенил)бутил-1-(3,3-диметил-1,2-диоксобутил)пирролидина.
5. Соединение по п.2, где Z представляет собой S.
6. Соединение по п.5, которое выбрано из группы, состоящей из
2-фенил-1-этилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
1-{2-[(бензо[b]тиофен-3-илметилтио)карбонил]пирролидинил}-3,3-диметилпентан-1,2-диона;
2-фенил-1-этилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
2-фенил-1-этилового эфира (2S)-1-(2-циклопентил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
3-фенил-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3-(3-пиридил)-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3-фенил-1-пропилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
4-фенил-1-бутилового эфира (2S)-1-(2-цикпогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
4-фенил-1-бутилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3,3-дифенил-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3,3-дифенил-1-пропилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
3-(параметоксифенил)-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3,3-ди(парафтор)фенил-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
4,4-ди(парафторфенил)бутилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(1-нафтил)-1-пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
2,2-дифенилэтилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-[4-(трифторметил)фенил]пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-нафтил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(3-хлорфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-[3-(трифторметил)фенил]пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-бифенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-фторфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(3-фторфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-хлорфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты; и
3-(3,4-диметоксифенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты.
7. Соединение по п.1, где
n равно 2; и
Х представляет собой О.
8. Соединение по п.7, где Z представляет собой СН2.
9. Соединение по п.8, которое выбрано из группы, состоящей из
2-(1-оксо-6-фенил)гексил-1-(3,3-диметил-1,2-диоксобутил)пиперидина;
3,3-диметил-1-[2-(4-фенилбутаноил)пиперидино]-1,2-пентандиона и
3,3-диметил-1-[2-(5-фенилпентаноил)пиперидино]-1,2-пентандиона.
10. Соединение по п.7, где Z представляет собой S.
11. Соединение по п.10, которое выбрано из группы, состоящей из
2-фенил-1-этилового эфира 1-(3,3-диметил-1,2-диоксопентил)-2-пиперидинкарботионовой кислоты;
2-фенил-1-этилового эфира 1-(2-фенил-1,2-диоксоэтил)-2-пиперидинкарботионовой кислоты;
3-фенил-1-пропилового эфира 1-(3,3-диметил-1,2-диоксобутил)-2-пиперидинкарботионовой кислоты;
4-фенил-1-бутилового эфира 1-(1,2-диоксо-3,3-диметилбутил)-2-пиперидинкарботионовой кислоты;
1,5-дифенил-3-пентилового эфира 1-(3,3-диметил-1,2-диоксопентил)-2-пиперидинкарботионовой кислоты;
1,5-дифенил-3-пентилового эфира 1-(2-фенил-1,2-диоксоэтил)-2-пиперидинкарботионовой кислоты;
3-(параметоксифенил)-1-пропилового эфира 1-(1,2-диоксо-3,3-диметилпентил)пиперидин-2-карботионовой кислоты;
3-(параметоксифенил)-1-пропилового эфира 1-(2-фенил-1,2-диоксоэтил)пиперидин-2-карботионовой кислоты;
3-(1-нафтил)-1-пропилового эфира 1-(3,3-диметил-1,2-диоксопентил)пиперидин-2-карботионовой кислоты;
2,2-дифенилэтилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3,3-дифенилпропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(1-нафтил)-1-пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
4-фенилбутилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-фенилпропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(3-хлорфенил)-1-пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(2-фторфенил)пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты и
3-(3-фторфенил)пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты.
12. Соединение по п.7, где Z представляет собой CHR1.
13. Соединение по п.12, которое выбрано из группы, состоящей из
2-{1-оксо-[2-(2'-фенил)этил]-4-фенил}-бутил-1-(3,3-диметил-1,2-диоксобутил)пиперидина.
14. Соединение, которое представляет собой 3,3-дифенил-1-пропиловый эфир (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты.
15. Соединение, которое представляет собой 3-(1-нафтил)-1-пропиловый эфир (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты.
16. Соединение, которое представляет собой 2,2-дифенилэтиловый эфир (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты.
17. Соединение, которое представляет собой 3,3-дифенилпропиловый эфир 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты.
18. Соединение, которое представляет собой 3-[4-(трифторметил)фенил]пропиловый эфир (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты.
19. Соединение, которое представляет собой 3-(2-нафтил)пропиловый эфир (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты.
20. Соединение, которое представляет собой 3,3-диметил-1-[(2S)-2-(5-(3-пиридил)пентаноил)-1-пирролидин]-1,2-пентандион.
21. Соединение, которое представляет собой (2S)-2-(1-оксо-4-фенил)бутил-1-(3,3-диметил-1,2-диоксобутил)пирролидин.
22. Фармацевтическая композицшя, содержащая
1) эффективное количество соединения формулы II
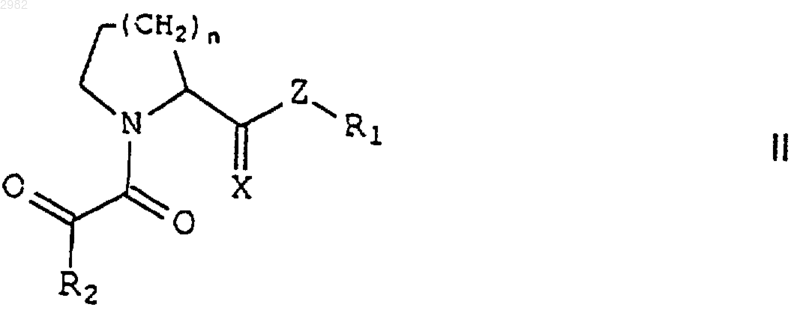
или его фармацевтически приемлемой соли, где
n равно 1 или 2;
Х представляет собой О или S;
Z выбран из группы, состоящей из S, CH2 и CHR1;
R1 представляет собой нормальный или разветвленный С1-С5алкил, замещенный по одному или более чем одному положению Ar1;
R2 выбран из группы, состоящей из нормального или разветвленного С3-С5алкила, С5-С7циклоалкила и Ar1;
Ar1 представляет собой фенил, пиридил, флуоренил, тиоиндолил, нафтил или бифенил, где указанный Ar1 не замещен или замещен по одному или более чем одному положению галогено, трифторметилом, метокси или их смесью; и
2) фармацевтически приемлемый носитель.
23. Фармацевтическая композиция по п.22, где указанное соединение выбрано из группы, состоящей из
(2S)-2-(1-оксо-5-фенил)пентил-1-(3,3-диметил-1,2-диоксопентил)пирролидина;
3,3-диметил-1-[(2S)-1-(5-(3-пиридил)пентаноил)-1-пирролидин]-1,2-пентандиона;
(2S)-2-(1-оксо-4-фенил)бутил-1-(3,3-диметил-1,2-диоксобутил)пирролидина;
(2S)-2-(1-оксо-4-фенил)бутил-1-(2-циклогексил-1,2-диоксоэтил)пирролидина;
2-(1-оксо-4-фенил)бутил-1-(3,3-диметил-1,2-диоксобутил)пирролидина;
2-фенил-1-этилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
1-{2-[(бензо[b]тиофен-3-илметилтио)карбонил]пирролидинил}-3,3-диметилпентан-1,2-диона;
2-фенил-1-этилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
2-фенил-1-этилового эфира (2S)-1-(2-циклопентил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
3-фенил-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3-(3-пиридил)-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3-фенил-1-пропилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
4-фенил-1-бутилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
4-фенил-1-бутилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3,3-дифенил-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3,3-дифенил-1-пропилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
3-(параметоксифенил)-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3,3-ди(парафтор)фенил-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
4,4-ди(парафторфенил)бутилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(1-нафтил)-1-пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
2,2-дифенилэтилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-[4-(трифторметил)фенил]пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-нафтил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(3-хлорфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-[3-(трифторметил)фенил]пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-бифенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-фторфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(3-фторфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-хлорфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(3,4-диметоксифенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
2-(1-оксо-6-фенил)гексил-1-(3,3-диметил-1,2-диоксобутил)пиперидина;
3,3-диметил-1-[2-(4-фенилбутаноил)пиперидино]-1,2-пентандиона;
3,3-диметил-1-[2-(5-фенилпентаноил)пиперидино]-1,2-пентандиона;
2-фенил-1-этилового эфира 1-(3,3-диметил-1,2-диоксопентил)-2-пиперидинкарботионовой кислоты;
2-фенил-1-этилового эфира 1-(2-фенил-1,2-диоксоэтил)-2-пиперидинкарботионовой кислоты;
3-фенил-1-пропилового эфира 1-(3,3-диметил-1,2-диоксобутил)-2-пиперидинкарботионовой кислоты;
4-фенил-1-бутилового эфира 1-(1,2-диоксо-3,3-диметилбутил)-2-пиперидинкарботионовой кислоты;
1,5-дифенил-3-пентилового эфира 1-(3,3-диметил-1,2-диоксопентил)-2-пиперидинкарботионовой кислоты;
1,5-дифенил-3-пентилового эфира 1-(2-фенил-1,2-диоксоэтил)-2-пиперидинкарботионовой кислоты;
3-(параметоксифенил)-1-пропилового эфира 1-(1,2-диоксо-3,3-диметилпентил)пиперидин-2-карботионовой кислоты;
3-(параметоксифенил)-1-пропилового эфира 1-(2-фенил-1,2-диоксоэтил)пиперидин-2-карботионовой кислоты;
3-(1-нафтил)-1-пропилового эфира 1-(3,3-диметил-1,2-диоксопентил)пиперидин-2-карботионовой кислоты;
2,2-дифенилэтилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3,3-дифенилпропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(1-нафтил)-1-пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
4-фенилбутилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-фенилпропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(3-хлорфенил)-1-пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(2-фторфенил)пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(3-фторфенил)пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты и
2-{1-оксо-[2-{2'-фенил}этил]-4-фенил}-бутил-1-(3,3-диметил-1,2-диоксобутил)пиперидина.
24. Фармацевтическая композиция по любому из пп.22-23, которая дополнительно содержит один или более чем один дополнительный нейротрофический агент.
25. Фармацевтическая композиция по п.24, где указанный один или более чем один дополнительный нейротрофический агент независимо выбран из группы, состоящей из фактора роста нервной ткани (NGF), глиального фактора роста, мозгового фактора роста, цилиарного нейротрофического фактора и нейротропина-3.
26. Фармацевтическая композиция по п.25, где указанный один или более чем один дополнительный нейротрофический агент представляет собой фактор роста нервной ткани (NGF).
27. Способ нейронального воздействия у животного, при котором животному вводят эффективное количество соединения формулы II
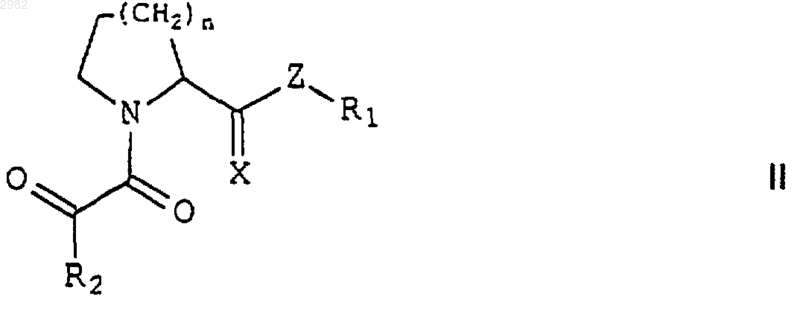
или его фармацевтически приемлемой соли, где
n равно 1 или 2;
Х представляет собой О или S;
Z выбран из группы, состоящей из S, CH2 и CHR1;
R1 представляет собой нормальный или разветвленный С1-С5алкил, замещенный по одному или более чем одному положению Ar1;
R2 выбран из группы, состоящей из нормального или разветвленного С3-С5алкила, С5-С7циклоалкила и Ar1;
Ar1 представляет собой фенил, пиридил, флуоренил, тиоиндолил, нафтил или бифенил, где указанный Ar1 не замещен или замещен по одному или более чем одному положению галогено, трифторметилом, метокси или их смесью.
28. Способ по п.27, где указанное соединение выбрано из группы, состоящей из
(2S)-2-(1-оксо-5-фенил)пентил-1-(3,3-диметил-1,2-диоксопентил)пирролидина;
3,3-диметил-1-[(2S)-1-(5-(3-пиридил)пентаноил)-1-пирролидин]-1,2-пентандиона;
(2S)-2-(1-оксо-4-фенил)бутил-1-(3,3-диметил-1,2-диоксобутил)пирролидина;
(2S)-2-{1-оксо-4-фенил}бутил-1-(2-циклогексил-1,2-диоксоэтил)пирролидина;
2-(1-оксо-4-фенил)бутил-1-(3,3-диметил-1,2-диоксобутил)пирролидина;
2-фенил-1-этилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
1-{2-[(бензо[b]тиофен-3-илметилтио)карбонил]пирролидинил}-3,3-диметилпентан-1,2-диона;
2-фенил-1-этилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
2-фенил-1-этилового эфира (2S)-1-(2-циклопентил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
3-фенил-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3-(3-пиридил)-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3-фенил-1-пропилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
4-фенил-1-бутилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
4-фенил-1-бутилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3,3-дифенил-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3,3-дифенил-1-пропилового эфира (2S)-1-(2-циклогексил-1,2-диоксоэтил)-2-пирролидинкарботионовой кислоты;
3-(параметоксифенил)-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
3,3-ди(парафтор)фенил-1-пропилового эфира (2S)-1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты;
4,4-ди(парафторфенил)бутилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(1-нафтил)-1-пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
2,2-дифенилэтилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-[4-(трифторметил)фенил]пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-нафтил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(3-хлорфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-[3-(трифторметил)фенил]пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-бифенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-фторфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(3-фторфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(2-хлорфенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
3-(3,4-диметоксифенил)пропилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты;
2-(1-оксо-6-фенил)гексил-1-(3,3-диметил-1,2-диоксобутил)пиперидина;
3,3-диметил-1-[2-(4-фенилбутаноил)пиперидино]-1,2-пентандиона;
3,3-диметил-1-[2-(5-фенилпентаноил)пиперидино]-1,2-пентандиона;
2-фенил-1-этилового эфира 1-(3,3-диметил-1,2-диоксопентил)-2-пиперидинкарботионовой кислоты;
2-фенил-1-этилового эфира 1-(2-фенил-1,2-диоксоэтил)-2-пиперидинкарботионовой кислоты;
3-фенил-1-пропилового эфира 1-(3,3-диметил-1,2-диоксобутил)-2-пиперидинкарботионовой кислоты;
4-фенил-1-бутилового эфира 1-(1,2-диоксо-3,3-диметилбутил)-2-пиперидинкарботионовой кислоты;
1,5-дифенил-3-пентилового эфира 1-(3,3-диметил-1,2-диоксопентил)-2-пиперидинкарботионовой кислоты;
1,5-дифенил-3-пентилового эфира 1-(2-фенил-1,2-диокcоэтил)-2-пиперидинкарботионовой кислоты;
3-(параметоксифенил)-1-пропилового эфира 1-(1,2-диоксо-3,3-диметилпентил)пиперидин-2-карботионовой кислоты;
3-(параметоксифенил)-1-пропилового эфира 1-(2-фенил-1,2-диоксоэтил)пиперидин-2-карботионовой кислоты;
3-(1-нафтил)-1-пропилового эфира 1-(3,3-диметил-1,2-диоксопентил)пиперидин-2-карботионовой кислоты;
2,2-дифенилэтилового эфира (2S)-1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3,3-дифенилпропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(1-нафтил)-1-пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
4-фенилбутилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-фенилпропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(3-хлорфенил)-1-пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(2-фторфенил)пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты;
3-(3-фторфенил)пропилового эфира 1-(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты и
2-{1-оксо-[2-{2'-фенил}этил]-4-фенил}-бутил-1-(3,3-диметил-1,2-диоксобутил)пиперидина.
29. Способ по любому из пп.27-28, где нейрональное воздействие выбрано из группы, состоящей из стимуляции поврежденных нейронов, активации нейронной регенерации, предотвращения нейродегенерации и лечения неврологического расстройства.
30. Способ по п.29, где неврологическое расстройство выбрано из группы, состоящей из периферической невропатии, вызванной физической травмой или болезненным состоянием, травмы головного мозга, физического повреждения спинного мозга, инсульта, связанного с повреждением головного мозга, и неврологического расстройства, относящегося к нейродегенерации.
31. Способ по п.30, где неврологическое расстройство, относящееся к нейродегенерации, выбрано из группы, состоящей из болезни Альцгеймера, болезни Паркинсона и бокового амиотрофического склероза.
Текст
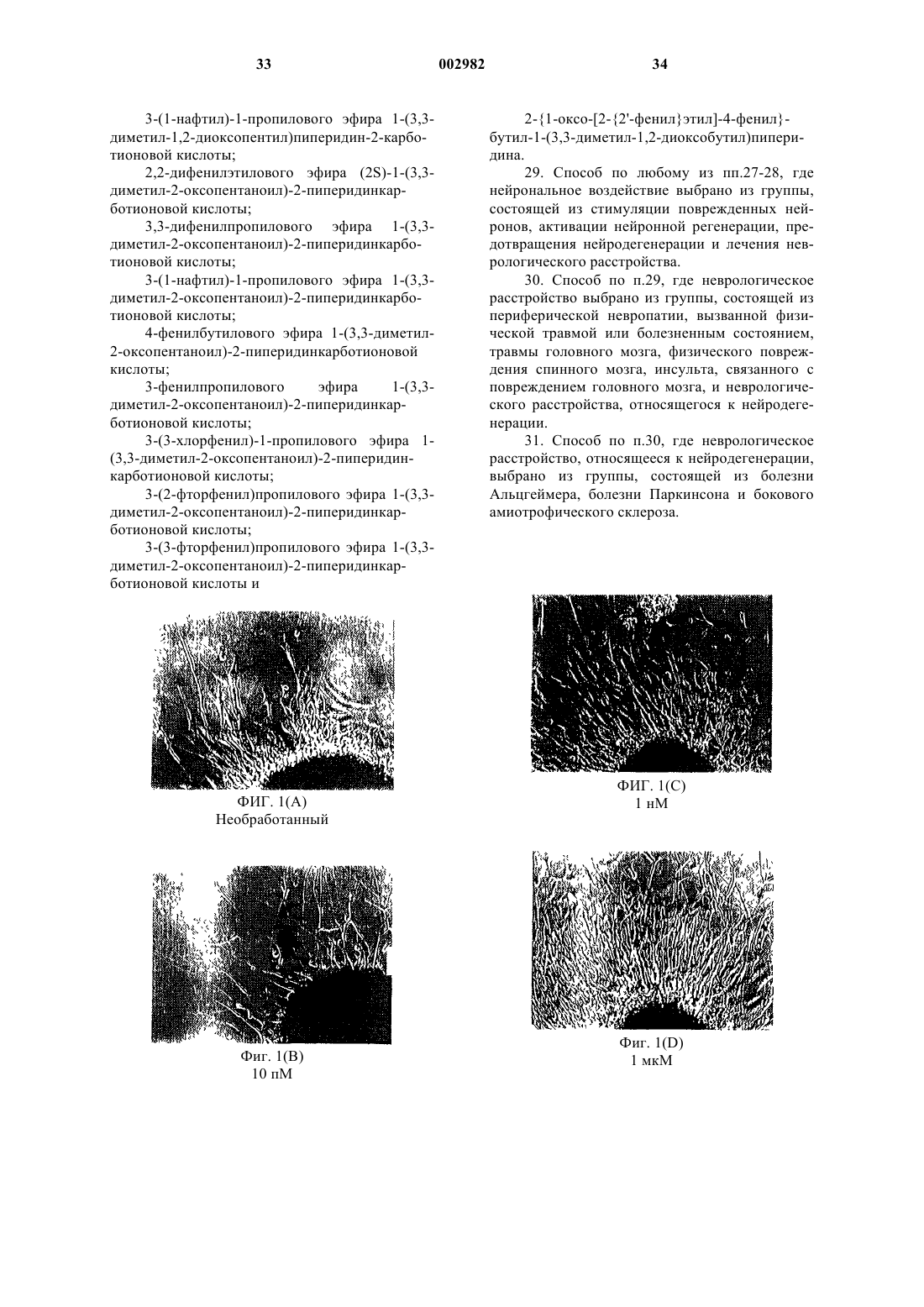
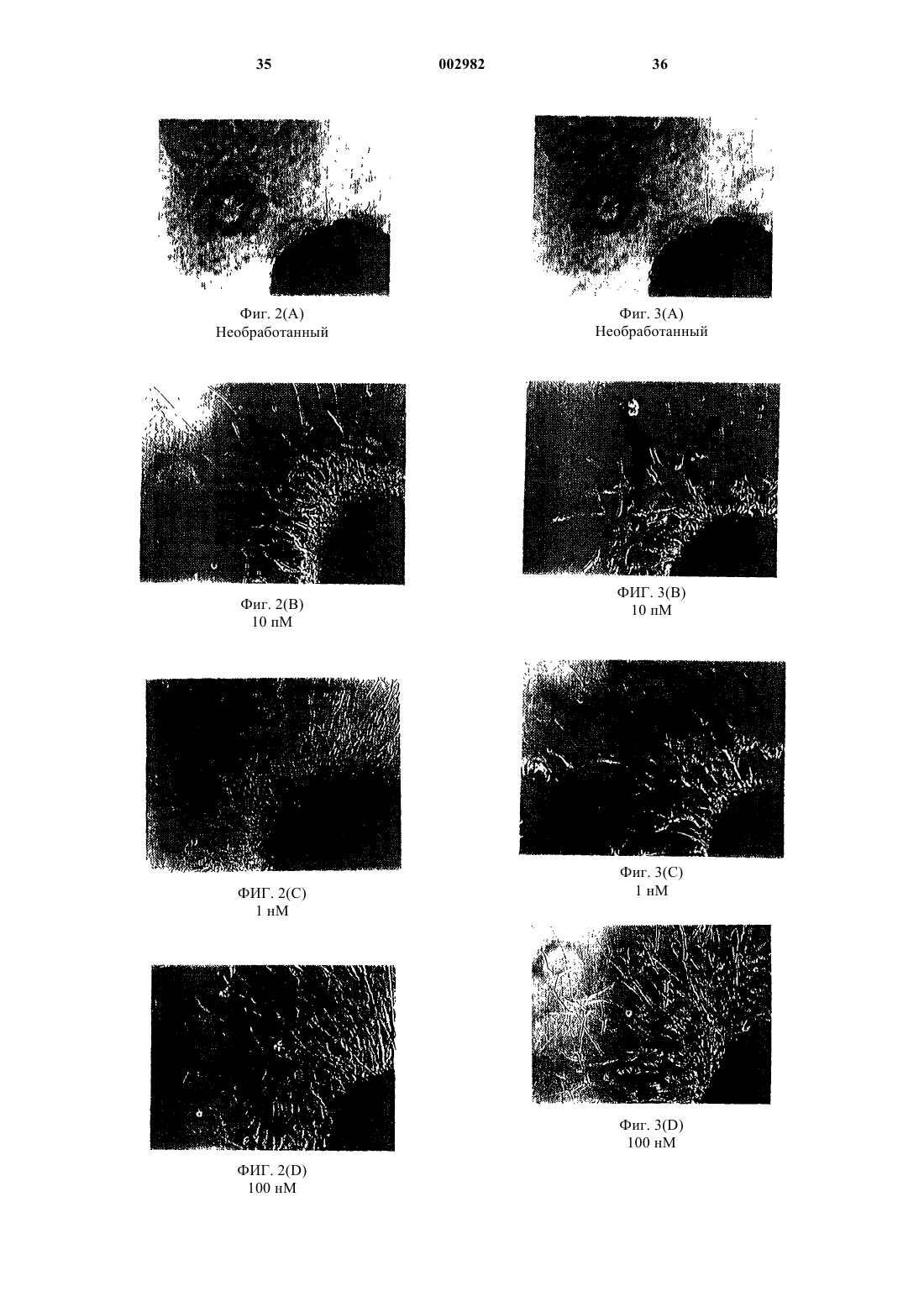
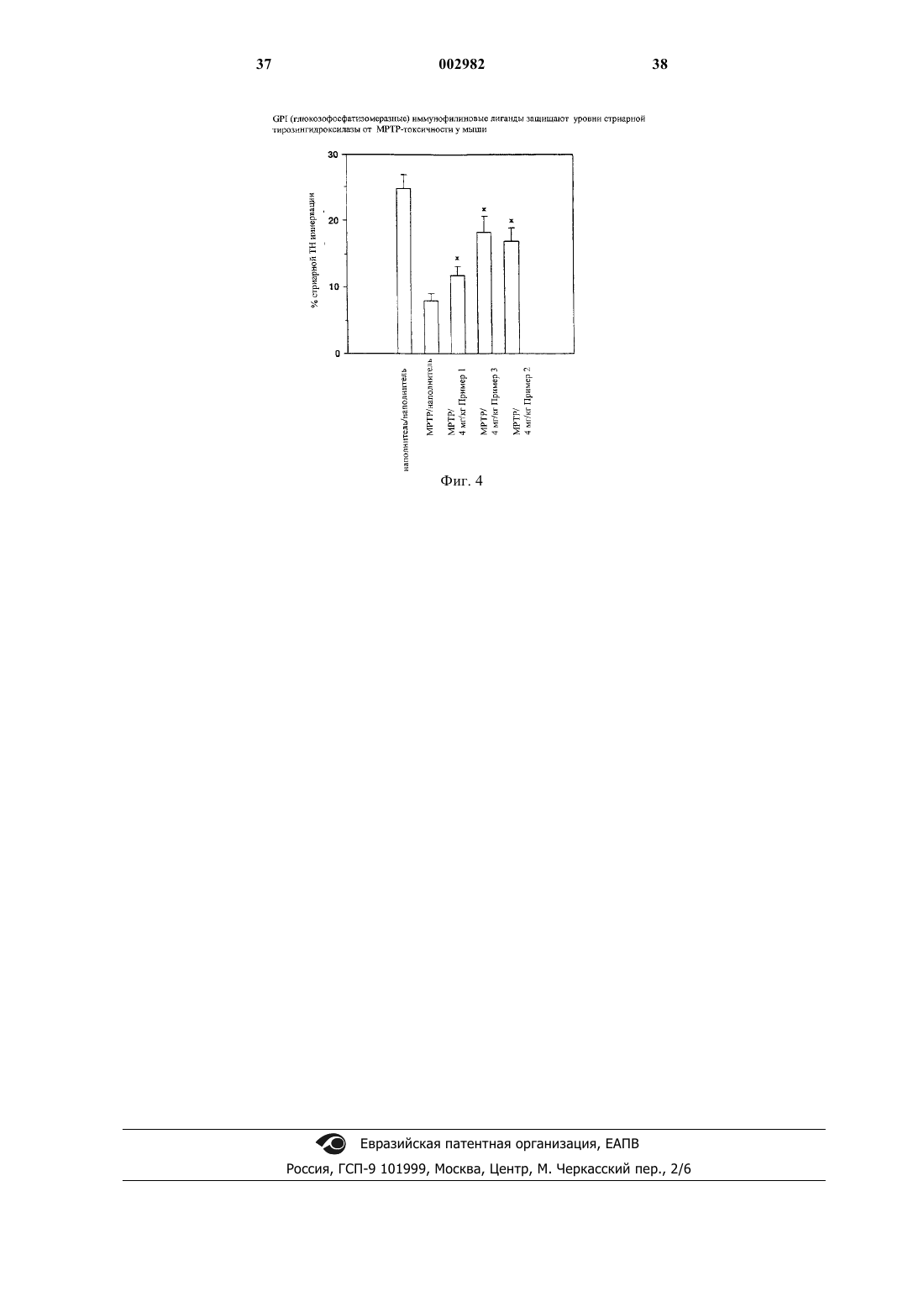
1 Настоящая заявка является частичным продолжением заявки на патент США 08/721765, поданной 25 сентября 1996 г., полное содержание которой включено в этот документ ссылкой. Предпосылки изобретения 1. Область изобретения. Настоящее изобретение относится к нейротрофическим гетероциклическим тиоэфирам и кетонам с низкой молекулярной массой и небольшим размером молекулы, обладающим сродством к иммунофилинам типа FKBP, и их применению в качестве ингибиторов ферментативной активности, ассоциированной с иммунофилиновыми белками, в частности, в качестве ингибиторов ферментативной активности пептидилпролилизомеразы или ротамазы. 2. Описание уровня техники. Термин "иммунофилин" относится к ряду белков, которые служат рецепторами основных иммунодепрессивных лекарственных средств,циклоспорина A (CsA), FK506 и рапамицина. Известными классами иммунофилинов являются циклофилины и FК 506-связывающие белки,или FKBP. Циклоспорин А связывается с циклофилином А, тогда как FK506 и рапамицин связываются с FKBP12. Эти комплексы, образованные иммунофилином и лекарственным средством, задействованы в целом ряде внутриклеточных систем сигнальной трансдукции, в особенности в иммунной и нервной системах. Известно, что иммунофилины обладают пептидилпролилизомеразной (PPI), или ротамазной, ферментативной активностью. Установлено, что ротамазная ферментативная активность участвует в катализе взаимного превращения цис- и транс-изомеров пептида и белковых субстратов иммунофилиновых белков. Иммунофилины были впервые открыты и изучены в иммунной ткани. Сначала специалисты предполагали, что ингибирование ротамазной активности иммунофилинов приводит к ингибированию пролиферации Т-клеток, что в свою очередь вызывает иммунодепрессивную активность, свойственную иммунодепрессивным лекарственным средствам, таким как циклоспорин А, FKBP и рапамицин. Дальнейшие исследования показали, что само по себе ингибирование ротамазной активности не приводит к иммунодепрессивной активности (Schreiber etal., Science, 1990, vol. 250, pp. 556-559). Вместо этого иммунодепрессия, по-видимому, происходит вследствие образования комплекса иммунодепрессивного лекарственного средства и иммунофилина. Было показано, что способ действия комлексов иммунофилина и лекарственного средства обусловлен их взаимодействием с тройными белками-мишенями (Schreiber et al.,Cell, 1991, vol. 66, pp. 807-815). Комплексы, образованные лекарственным средством и иммунофилином (такие как FKBP-FK506 и FKBPCsA), связываются с ферментом кальцинейри 002982 2 ном, ингибируя передачу сигнала рецепторов Тклеток, что приводит к пролиферации Т-клеток. Комплекс, образованный иммунофилином и лекарственным средством - FKBP и рапамицином, взаимодействует аналогичным образом с белком RAFT1/FRAP и подавляет передачу сигнала от рецептора IL-2. Обнаружено, что иммунофилины присутствуют в высоких концентрациях в центральной нервной системе, где их количество в 10-50 раз больше, чем в иммунной системе. В нервных тканях иммунофилины, по-видимому, оказывают влияние на синтез оксида азота, выделение нейромедиаторов и процесс роста нейрона. Найдено, что пикомолярные концентрации иммунодепрессанта, такого как FK506 и рапамицин, стимулируют рост аксонов в клетках РС 12 и чувствительных нейронах, а именно, в клетках спинномозговых узлов (DRGs) (Lyons etal., Proc. of Natl. Acad. Sci., 1994, vol. 91, pp. 3191-3195). В экспериментах, проводимых на целых животных, было показано, что FK506 стимулирует регенерацию нерва после повреждения лицевого нерва. Удивительным оказался тот факт, что некоторые соединения с высоким сродством кFKBP, являются мощными ингибиторами ротамазы и обладают превосходным нейротрофическим действием. Более того, у этих ингибиторов ротамазы отсутствует иммунодепрессивная активность. Из этих наблюдений следует, что ингибиторы ротамазы можно использовать при лечении различных периферических невропатий и для усиления процесса возобновления роста нейронов в центральной нервной системе(ЦНС). Исследования показали, что причиной нейродегенеративных расстройств, таких как болезнь Альцгеймера, болезнь Паркинсона и боковой амиотрофический склероз (БАС), может служить потеря или снижение доступности нейротрофического вещества, специфичного для конкретной популяции нейронов, пораженных заболеванием. Выявлено несколько нейротрофических факторов, воздействующих на специфичные популяции нейронов в центральной нервной системе. Например, было высказано предположение, что болезнь Альцгеймера возникает в результате уменьшения содержания или потери фактора роста нервной ткани (ФРН). Поэтому было предложено лечить пациентов, страдающих старческой деменцией Альцгеймеровского типа (СДАТ), экзогенным фактором роста нервной ткани или другими нейротрофическими белками, такими как мозговой фактор роста,глиальный фактор роста, цилиарный нейротрофический фактор и нейротропин-3, чтобы увеличить выживаемость деградирующих популяций нейронов. Клиническое применение этих белков для различных неврологических болезненных состояний затруднено сложностями введения и 3 биологической доступности крупных белков к мишеням нервной системы. Напротив, иммунодепрессивные лекарственные средства с нейротрофической активностью обладают относительно небольшими размерами и проявляют превосходную биологическую доступность и специфичность. Однако при постоянном введении иммунодепрессивные лекарственные средства проявляют ряд потенциально серьезных побочных эффектов, в том числе нефротоксичность, такую как нарушение гломерулярной фильтрации и необратимый интерстициальный фиброз (Корр et al., J. Am. Soc. Neprol., 1991,1:162); неврологические нарушения, такие как непроизвольные треморы, или неспецифическая церебральная стенокардия, такая как нелокализованные головные боли (De Groen et al., N.Engl. J. Med., 1987, 317: 861; и сосудистая гипертензия с проистекающими от нее осложнениями (Каhаn et al., N. Engl. J. Med., 1989,321:1725). Для того чтобы предотвратить побочные эффекты, ассоциированные с применением иммунодепрессивных соединений, согласно настоящему изобретению предложены неиммунодепрессивные соединения, содержащие ингибиторы ротамазы FKBP, имеющие небольшие молекулы, предназначенные для усиления отрастания аксонов и активирования и регенерации роста нейронов при различных невропатологических состояниях, при которых может быть облегчено восстановление нейронов, в том числе при повреждении периферических нервов,вызванном физической травмой или болезненным состоянием, таким как диабет; при физическом повреждении центральной нервной системы (спинного или головного мозга); при повреждении головного мозга, связанном с инсультом; при неврологических расстройствах, связанных с нейродегенерацией, таких как болезнь Паркинсона, болезнь Альцгеймера (СДАТ) и боковой амиотрофический склероз. Сущность изобретения Настоящее изобретение относится к нейротрофическим соединениям с низкой молекулярной массой и небольшим размером молекулы, обладающим сродством к иммунофилинам типа FKBP. Связанные с такими белками, нейротрофические соединения являются мощными ингибиторами ферментативной активности, ассоциированной с иммунофилиновыми белками,в частности, ферментативной активности пептидилпролилизомеразы, или ротамазы. Ключевым отличительным признаком соединений по настоящему изобретению является то, что они не проявляют никакой значительной иммунодепрессивной активности в дополнение к их нейротрофической активности. Конкретно настоящее изобретение относится к соединению формулы II или его фармацевтически приемлемой соли, гдеR1 представляет собой нормальный или разветвленный С 1-С 5 алкил, замещенный по одному или более чем одному положению Аr1);R2 выбран из группы, состоящей из нормального или разветвленного С 3-С 5 алкила, С 5 С 7 циклоалкила иАr1;Ar1 представляет собой фенил, пиридил,флуоренил, тиоиндолил, нафтил или бифенил,где указанный Ar1 не замещен или замещен по одному или более чем одному положению галогено, трифторметилом, метокси или их смесью. Настоящее изобретение также относится к фармацевтической композиции, содержащей 1) эффективное количество соединения формулы II или его фармацевтически приемлемой соли и 2) фармацевтически приемлемый носитель. Кроме того, настоящее изобретение относится к способу нейронального воздействия у животного, при котором животному вводят эффективное количество соединения формулы II или его фармацевтически приемлемой соли. Краткое описание фигур Фиг. 1(А) представляет собой типичную микрофотографию необработанных чувствительных нейронов; фиг. 1(В) - типичную микрофотографию активированного соединением 1 (10 пМ) выроста аксонов в чувствительных нейронах; фиг. 1(С) - типичную микрофотографию активированного соединением 1 (1 нМ) выроста аксонов в чувствительных нейронах; фиг. 1(D) - типичную микрофотографию активированного соединением 1 (1 мкМ) выроста аксонов в чувствительных нейронах; фиг. 2(А) - типичную микрофотографию необработанных чувствительных нейронов; фиг. 2(В) - типичную микрофотографию активированного соединением 9 (10 пМ) выроста аксонов в чувствительных нейронах; фиг. 2(С) - типичную микрофотографию активированного соединением 9 (1 нМ) выроста аксонов в чувствительных нейронах; фиг. 2(D) - типичную микрофотографию активированного соединением 9 (100 нМ) выроста аксонов в чувствительных нейронах; фиг. 3(А) - типичную микрофотографию необработанных чувствительных нейронов; фиг. 3(В) - типичную микрофотографию активированного соединением 10 (10 пМ) выроста аксонов в чувствительных нейронах; 5 фиг. 3(С) - типичную микрофотографию активированного соединением 9 (1 нМ) выроста аксонов в чувствительных нейронах; фиг. 3(D) - типичную микрофотографию активированного соединением 9 (100 нМ) выроста аксонов в чувствительных нейронах; фиг. 4 - количественную оценку восстановления ТН-положительных дофаминергических нейронов в полосатом теле животных, получающих соединения 1, 9 и 10. Подробное описание изобретения Определения"Алкил" относится к разветвленной или нормальной насыщенной углеводородной цепи,содержащей от 1 до 6 атомов углерода, такой как метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, н-пентил, н-гексил и им подобные, если не указано особо."Алкокси" относится к группе -OR, где R представляет собой алкил, как он определен выше. Предпочтительно R представляет собой разветвленную или нормальную насыщенную углеводородную цепь, содержащую от 1 до 3 атомов углерода."Галогено", если не указано особо, относится к фторо, хлоро, бромо или йодо."Изомеры" представляют собой разные соединения, которые имеют одинаковую молекулярную формулу. "Стереоизомеры" представляют собой изомеры, которые различаются только тем, как атомы расположены в пространстве. "Энантиомеры" представляют собой пару стереоизомеров, которые являются несовместимыми зеркальными изображениями друг друга."Диастереоизомеры" представляют собой стереоизомеры, которые не являются зеркальными изображениями друг друга. "Рацемическая смесь" означает смесь, которая содержит равные части индивидуальных энантиомеров. "Нерацемическая смесь" представляет собой смесь,которая содержит неодинаковые части индивидуальных энантиомеров или стереоизомеров."Фармацевтически приемлемая соль" относится к соли соединений по изобретению,которая обладает требуемой фармакологической активностью и которая не является ни биологически, ни в другом отношении нежелательной. Примеры соли, которая может быть образована с органическими кислотами, включают в себя ацетат, адипат, альгинат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфорсульфонат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, фумарат, глюкогептаноат, глицерофосфат,полусульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидроиодид, 2-гидроксиэтансульфонат, лактат, малеат, метансульфонат, 2 нафталинсульфонат, никотинат, оксалат, тиоционат, тозилат и ундеканоат. Примеры основной соли включают в себя соли аммония, соли щелочных металлов, такие как натриевые и калиевые соли, соли щелочно-земельных метал 002982 6 лов, такие как кальциевые и магниевые соли,соли, образованные с органическими основаниями, такие как соли дициклогексиламина, Nметил-D-глюкамина, и соли, образованные с аминокислотами, такими как аргинин и лизин. Также основные азотсодержащие группы могут быть кватернизированы агентами, включающими в себя (низший алкил)галогениды, такие как метил-, этил-, пропил- и бутилхлориды,-бромиды и -иодиды; диалкилсульфаты, такие как диметил-, диэтил-, дибутил- и диамилсульфаты; длинноцепочечные галогениды, такие как децил-, лаурил-, миристил- и стеарилхлориды,-бромиды и -иодиды; и аралкилгалогениды, такие как бензил- и фенетилбромиды."Фенил" относится к любому возможному изомерному фенильному радикалу, возможно однозамещенному или мультизамещенному заместителями, выбранными из группы, состоящей из алкила, алкокси-, гидрокси-, галогено- и галогеналкила.(1) предотвращению заболевания, расстройства или состояния у животного, которое может быть предрасположено к заболеванию,расстройству и/или состоянию, но еще не диагностировано как имеющее его;(3) ослаблению болезни, расстройства или состояния, т.е. созданию условий для регрессии болезни, расстройства и/или состояния. Соединения по изобретению Нейротрофические FKBP-ингибирующие соединения по данному изобретению, имеющие низкую молекулярную массу и небольшой размер молекул, обладают сродством к иммунофилинам типа FKBP, таким как FKBP12. Обнаружено, что когда нейротрофические соединения по данному изобретению связываются с иммунофилином типа FKBP, то они ингибируют пептидилпролил цис-транс-изомеразную активность или ротамазную активность связывающего белка и неожиданно стимулируют рост аксонов. Данное изобретение конкретно относится к соединениям формулы II или их фармацевтически приемлемой соли, гдеR1 представляет собой нормальный или разветвленный С 1-С 5 алкил, замещенный по одному или более чем одному положению Ar1;R2 выбран из группы, состоящей из нормального или разветвленного С 3-С 5 алкила, С 5 С 7 циклоалкила и Аr1; где указанный Аr1 не замещен или замещен по одному или более чем одному положению галогено, трифторметилом, метокси или их смесью. Конкретные примеры этих воплощений изобретения представлены в табл. 1. Таблица 1 Наиболее предпочтительные примеры из табл. 1 называются следующим образом: 1) (2S)-3,3-диметил-1-[2-(5-фенилпентаноил)пирролидинил]пентан-1,2-дион,2)(2S)-2-[5,5-ди(4-фторфенил)пентаноил]-1-(3,3-диметил-1,2-пентандион)пирролидин,71) 3,3-диметил-1-[2-(5-фенилпентаноил) пиперидино]-1,2-пентандион. Соединения по данному изобретению обладают асимметрическими центрами и, таким образом, их можно получать в виде смесей стереоизомеров или в виде индивидуальных стереоизомеров. Индивидуальные стереоизомеры могут быть получены путем использования оптически активного исходного материала, путем разделения рацемической или не рацемической смеси промежуточного соединения на соответствующей стадии синтеза или путем разделения соединения формулы (I). Следует понимать, что индивидуальные стереоизомеры, также как и смеси (рацемические или не рацемические) стереоизомеров включены в объем настоящего изобретения. Соединения по данному изобретению обладают, по меньшей мере, одним асимметрическим центром и, таким образом, могут быть получены в виде смеси стереоизомеров или в виде индивидуальных R- и S-стереоизомеров. Индивидуальные энантиомеры могут быть получены путем разделения рацемической или не рацемической смеси промежуточного соединения на соответствующей стадии синтеза. Следует понимать, что индивидуальные R- и Sстереоизомеры, также как и смеси стереоизомеров включены в объем настоящего изобретения.S-стереоизомер является наиболее предпочтительным из-за его более высокой активности. Способы использования соединений по изобретению Соединения по настоящему изобретению обладают сродством к FK506-связывающему белку , в частности к FKBP12, который присутствует в головном мозге. Когда соединения по изобретению связываются с FKBP в головном мозге, то они проявляют превосходную нейротрофическую активность. Эта активность полезна при стимуляции поврежденных нейронов,активации нейронной регенерации, предотвращения нейродегенерации и лечения некоторых неврологических расстройств, которые, как известно, связаны с нейронной дегенерацией и периферическими невропатиями. Кроме того, по упомянутым выше причинам настоящее изобретение относится к способу нейронального воздействия у животного, при котором животному вводят эффективное количество соединения формулы II или его фармацевтически приемлемой соли. В предпочтительном воплощении изобретения нейрональное воздействие выбрано из группы, состоящей из стимуляции поврежден 13 ных нейронов, активации нейронной регенерации, предотвращения нейродегенерации и лечения неврологического расстройства. Неврологические расстройства, которые можно лечить, включают в себя, но не ограничиваются ими, невралгию тройничного нерва; невралгию языко-глоточного нерва; паралич Белла; тяжелую миастению; мышечную дистрофию; боковой амиотрофический склероз; прогрессирующую мышечную атрофию; прогрессирующую бульбарную наследственную мышечную атрофию; синдромы грыжи межпозвоночного диска или опущения межпозвоночного диска; шейный спондилез; расстройства сплетений; синдромы сквозных повреждений грудной клетки; периферические невропатии,такие как невропатии, вызываемые отравлениями свинцом, дапсоном, укусами клещей, порфирией или синдромом Гийена-Барре-Штроля; болезнь Альцгеймера; и болезнь Паркинсона. Соединения по настоящему изобретению особенно полезны для лечения неврологического расстройства, выбранного из группы, состоящей из периферической невропатии, вызванной физической травмой или болезненным состоянием, травмы головного мозга, физического повреждения спинного мозга, инсульта,связанного с повреждением головного мозга, и неврологического расстройства, относящегося к нейродегенерации. Примерами неврологических расстройств, относящихся к нейродегенерации,являются болезнь Альцгеймера, болезнь Паркинсона и боковой амиотрофический склероз. Для этих целей соединения можно вводить перорально, парентерально, посредством ингаляции, местно, ректально, назально, буккально,вагинально, или через имплантированный резервуар в виде лекарственных препаратов, содержащих традиционные нетоксичные фармацевтически приемлемые носители, адъюванты и наполнители. Термин "парентеральное введение", применяемый в этом документе, включает в себя подкожный, внутривенный, внутримышечный, внутрибрюшинный, внутриоболочечный, внутрижелудочковый, внутригрудинный или внутричерепной путь введения с помощью инъекции или вливания. Для того чтобы быть терапевтически эффективным в отношении мишеней центральной нервной системы, соединения при периферическом введении должны легко проникать через гематоэнцефалический барьер. Соединения,которые не способны преодолевать гематоэнцефалический барьер, можно эффективно вводить внутрижелудочковым путем. Соединения можно вводить в виде стерильных препаратов для инъекций, например в виде стерильных водных или маслянистых суспензий для инъекций. Эти суспензии могут быть приготовлены в соответствии с хорошо известными из уровня техники способами с использованием подходящих диспергирующих или сма 002982 14 чивающих агентов и суспендирующих агентов. Стерильные препараты для инъекций могут также представлять собой предназначенные для инъекций стерильные растворы или суспензии в нетоксичных парентерально приемлемых разбавителях или растворителях, например в виде растворов в 1,3-бутандиоле. К числу приемлемых носителей и растворителей, которые можно использовать, относятся вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителей или суспензионных сред традиционно используют стерильные стабильные масла. Для этих целей может быть использовано любое стабильное мягкое масло,такое как синтетический моно- или диглицерид. Жирные кислоты, такие как масляная кислота и ее глицеридные производные, в том числе оливковое масло и касторовое масло, особенно в своих полиоксиэтилированных формах, можно использовать при приготовлении препаратов для инъекций. Также эти масляные растворы или суспензии могут содержать в качестве разбавителей или диспергирующих агентов длинноцепочечные спирты. Кроме того, соединения можно вводить перорально в форме капсул, таблеток, водных суспензий или растворов. Таблетки могут содержать носители, такие как лактоза и кукурузный крахмал, и/или смазывающие агенты, такие как стеарат магния. Капсулы могут содержать разбавители, в том числе лактозу и сухой кукурузный крахмал. Водные суспензии могут содержать эмульгирующие и суспендирующие агенты в комбинации с активным ингредиентом. Кроме того, пероральные лекарственные формы могут содержать подсластители и/или корригенты и/или красители. Соединения также можно вводить ректально в форме суппозиториев. Эти композиции могут быть приготовлены путем смешивания лекарственного средства с подходящим не раздражающим эксципиентом, который является твердым при комнатной температуре, но жидким при температуре прямой кишки, и поэтому будет таять в прямой кишке с высвобождением лекарственного средства. Такие вещества включают в себя масло какао, пчелиный воск и полиэтиленгликоли. Далее соединения можно вводить местно,особенно когда состояния, предназначенные для лечения, затрагивают части тела или органы,легкодоступные для местного применения; в том числе неврологические расстройства глаз,кожи, и нижней части кишечного тракта. Подходящие препараты для местного применения могут быть легко приготовлены для каждой из этих частей тела. Для местного нанесения в глаз, или офтальмологического применения, соединения могут быть приготовлены в виде микронизированных суспензий в изотоническом стерильном физиологическом растворе с отрегулированным 15 рН или предпочтительно в виде раствора в изотонических стерильных физиологических растворах с отрегулированным рН, возможно содержащих консервант, такой как хлорид бензилалкония. Альтернативно, для офтальмологического применения соединение может входить в состав мазей, таких как вазелин. Для местного нанесения на кожу соединения могут быть приготовлены в виде подходящих мазей, содержащих соединения, суспендированные или растворенные например в смесях с одним или более чем одним из следующих веществ: минеральное масло, жидкий вазелин,белый вазелин, пропиленгликоль, полиоксиэтиленовое или полиоксипропиленовое соединение, эмульгирующий воск и вода. Альтернативно, соединения могут быть приготовлены в виде подходящих лосьонов или кремов, содержащих активное соединение, суспендированное или растворенное например в смеси с одним или более чем одним из следующих веществ: минеральное масло, моностеарат сорбитана, полисорбат 60, цетилэфирный воск, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и вода. Местное нанесение в нижний отдел кишечного тракта может быть осуществлено препаратами в виде ректального суппозитория (см. выше) или подходящими для клизмы препаратами. Для лечения вышеупомянутых состояний пригодными являются уровни дозировки порядка от примерно 0,1 до примерно 10000 мг соединения активного ингредиента с предпочтительными уровнями от примерно 0,1 до примерно 1000 мг. Количество активного ингредиента, который можно объединять с материалами носителя, чтобы получить форму разовой дозы,будет изменяться в зависимости от хозяина, которого лечат, и от конкретной схемы введения. Однако следует понимать, что конкретный уровень дозы для каждого конкретного пациента будет зависеть от ряда факторов, в том числе активности используемого конкретного соединения; возраста, веса тела, общего состояния здоровья, пола и диеты пациента; периода времени введения; скорости выведения; комбинации лекарственных средств; степени тяжести конкретной болезни, которую лечат; и формы введения. Соединения можно вводить совместно с другими нейротрофическими агентами, такими как фактор роста нервной ткани (NGF), глиальный фактор роста, мозговой фактор роста, цилиарный нейротрофический фактор и нейротропин-3. Уровень дозировки других нейротрофических лекарственных средств будет зависеть от предварительно установленных факторов и нейротрофической эффективности комбинации лекарственных средств. 16 Фармацевтические композиции по изобретению Настоящее изобретение также относится к фармацевтической композиции, содержащей 1) эффективное количество соединения формулы II или его фармацевтически приемлемой соли и 2) фармацевтически приемлемый носитель. Приведенное выше обсуждение, которое относится к использованию и введению соединений по настоящему изобретению, также относится к фармацевтическим композициям по настоящему изобретению. Примеры Следующие примеры иллюстрируют настоящее изобретение и не предназначены для того, чтобы ограничивать его. Если не оговорено особо, все проценты приведены в расчете на 100 мас.% конечного соединения. Пример 1. Синтез (2S)-2-(1-оксо-5-фенил) пентил-1-(3,3-диметил-1,2-диоксопентил)пирролидина (1).(2S)-2-(1-оксо-5-фенил)пентил-N-бензилпирролидин. 1-Хлор-4-фенилбутан (1,78 г; 10,5 ммоль) в 20 мл ТГФ добавляют к 0,24 г (10 ммоль) магниевой стружки в 50 мл нагреваемого с обратным холодильником ТГФ. После того как добавление заканчивают, смесь нагревают с обратным холодильником в течение дополнительных 5 ч, а затем медленно добавляют к нагреваемому с обратным холодильником раствору этилового эфира N-бензил-L-пролина (2,30 г, 10 ммоль) в 100 г ТГФ. Через 2 ч дополнительного нагревания с обратным холодильником смесь охлаждают и обрабатывают 5 мл 2 н. HCl. Реакционную смесь разбавляют эфиром (100 мл) и промывают насыщенным NаНСО 3, водой и рассолом. Органическую фазу сушат, концентрируют и подвергают хроматографии, элюируя смесью CH2Cl2:EtOAc (5:1) с образованием 2,05 г (64%) кетона в виде масла,1(2S)-2-(1-Оксо-5-фенил)пентилпирролидин. Кетонное соединение (500 мг) и гидроксид палладия (20% на углероде, 50 мг) гидрируют при 275,79 кПа (40 фунт/кв.дюйм) в шейкере Парра в течение ночи. Катализатор удаляют фильтрованием и растворитель удаляют в вакууме. Получают свободный амин в виде желтого масла (230 мг; 100%),1 17 мл) при 0 С по каплям добавляют метилоксалилхлорид (135 мг; 1,1 ммоль). После перемешивания при 0 С в течение 3 ч реакционную смесь охлаждают путем смешивания с насыщенным NH4Cl и органическую фазу промывают водой и рассолом и сушат и концентрируют. Неочищенный остаток очищают на колонке с силикагелем, элюируя смесью CH2Cl2:EtOAc(20:1) с образованием 300 мг оксамата в виде прозрачного масла (98%),1 Н ЯМР (CDCl3; 300 МГц): 1,68 (m, 4H); 1,91-2,38 (m, 4H); 2,64 (t, 2H); 3,66-3,80 (m, 2H); 3,77, 3,85 (s, 3H общее); 4,16 (m, 2H); 4,90 (m,1H); 7,16 (m, 3H), 7,27 (m, 2H).(250 мг; 0,79 ммоль) в безводном эфире (15 мл),охлажденному до -78 С, добавляют 1,1 диметилпропилмагнийхлорид (0,8 мл 1,0 М раствор в эфире; 0,8 ммоль). После перемешивания полученной смеси при -78 С в течение 2 ч реакционную смесь охлаждают путем смешивания с 2 мл насыщенного NH4Cl, а впоследствии 100 мл ЕtOАс. Органическую фазу промывают рассолом, сушат, концентрируют и очищают на колонке с силикагелем, элюируя смесью(m, 5H). Анализ: Вычислено для С 22 Н 31NО 3 Н 2O: С, 70,37; Н, 8,86; N, 3,73; Найдено: С, 70,48; Н, 8,35; N, 3,69. Пример 2. Синтез 2-фенил-1-этилового эфира 1-(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты (9). Метиловый эфир (2S)-1-(1,2-диоксо-2 метоксиэтил)-2-пирролидинкарбоновой кислоты. Раствор гидрохлорида метилового эфираL-пролина (3,08 г; 18,60 ммоль) в сухом метиленхлориде охлаждают до 0 С и обрабатывают триэтиламином (3,92 г; 38,74 ммоль; 2,1 экв.). После перемешивания полученной взвеси в атмосфере азота в течение 15 мин по каплям добавляют раствор метилоксалилхлорида (3,20 г; 26,12 ммоль) в метиленхлориде (45 мл). Полученную смесь перемешивают при 0 С в течение 1,5 ч. После фильтрования с удалением твердых веществ органическую фазу промывают водой,сушат над МgSO4 и концентрируют. Неочищенный остаток очищают на колонке с силикагелем, элюируя 50% этилацетата в гексане с образованием 3,52 г (88%) продукта в виде красноватого масла. Смесь цис-транс-амидных ротамеров; данные представлены для трансротамера.H ЯМР (CDCl3):1,93 (dm, 2H); 2,17 (m,2H); 3,62 (m, 2H); 3,71 (s, 3H); 3,79, 3,84 (s, 3H общий); 4,86 (dd, 1H, J=8,4, 3,3). Метиловый эфир (2S)-1-(1,2-диоксо-3,3 диметилпентил)-2-пирролидинкарбоновой кислоты. Раствор метилового эфира (2S)-1-(1,2 диоксо-2-метоксиэтил)-2-пирролидинкарбоновой кислоты (2,35 г; 10,90 ммоль) в 30 мл тетрагидрофурана (ТГФ) охлаждают до -78 С и обрабатывают 14,2 мл 1,0 М раствора 1,1-диметилпропилмагнийхлорида в ТГФ. После перемешивания полученной гомогенной смеси при -78 С в течение 3 ч смесь вливают в насыщенный хлорид аммония (100 мл) и экстрагируют этилацетатом. Органическую фазу промывают водой, сушат и концентрируют, а неочищенное вещество, полученное после удаления растворителя, очищают на колонке с силикагелем, элюируя 25% этилацетата в гексане с образованием 2,10 г (75%) оксамата в виде бесцветного масла,1(2S)-1-(1,2-Диоксо-3,3-диметилпентил)-2 пирролидинкарбоновая кислота. Смесь метилового эфира (2S)-1-(1,2 диоксо-3,3-диметилпентил)-2-пирролидинкарбоновой кислоты (2,10 г; 8,23 ммоль), 1 н. LiOH(15 мл) и метанола (50 мл) перемешивают при 0 С в течение 30 мин и при комнатной температуре в течение ночи. Смесь подкисляют до рН 1 1 н. HCl, разбавляют водой и экстрагируют 100 мл метиленхлорида. Органический экстракт промывают рассолом и концентрируют, получая 1,73 г (87%) белоснежного твердого вещества,которое не требует дальнейшей очистки,1(m, 1H); 2,25 (m, 1H); 3,53 (dd, 2H, J=10,4, 7,3); 4,55 (dd, 1H, J=8,6, 4,1). 2-Фенил-1-этиловый эфир 1-(3,3-диметил 1,2-диоксопентил)-2-пирролидинкарботионовой кислоты (9). К раствору (2S)-1-(1,2-диоксо-3,3-диметилпентил)-2-пирролидинкарбоновой кислоты (241 мг; 1,0 ммоль) в CH2Cl2 (10 мл) добавляют дициклогексилкарбодиимид (226 мг; 1,1 ммоль). После перемешивания полученной смеси в течение 5 мин раствор охлаждают до 0 С и обрабатывают раствором фенилмеркаптана (138 мг; 1,0 ммоль) и 4-диметиламинопиридина (6 мг) в 5 мл CH2Cl2. Смесь оставляют нагреваться до комнатной температуры при перемешивании в течение ночи. Твердые вещества удаляют фильтрованием, а фильтрат концентрируют в вакууме; неочищенный остаток очищают флешхроматографией (10:1 гексан:ЕtOАс) с получением 302 мг (84%) 9 в виде масла, 19 1(100 мл) охлаждают до 0 С и обрабатывают триэтиламином (10,5 г; 103 ммоль; 2,1 экв). После перемешивания полученной взвеси в атмосфере азота в течение 15 мин по каплям добавляют раствор метилоксалилхлорида (8,50 г; 69,4 ммоль) в метиленхлориде (75 мл). Полученную смесь перемешивают при 0 С в течение 1,5 ч. После фильтрования с удалением твердых веществ органическую фазу промывают водой,сушат над МgSO4 и концентрируют. Неочищенный остаток очищают на колонке с силикагелем, элюируя 50% этилацетата в гексане с образованием 9,34 г (86%) продукта в виде красноватого масла. Смесь цис-транс-амидных ротамеров; данные представлены для трансротамера. 1(dd, 1H). Метиловый эфир 1-(1,2-диоксо-3,3-диметилпентил)-2-пиперидинкарбоновой кислоты. Раствор метилового эфира 1-(1,2-диоксо-2 метоксиэтил)-2-пиперидинкарбоновой кислоты(ТГФ) охлаждают до -78 С и обрабатывают 20,7 мл 1,0 М раствора 1,1-диметилпропилмагнийхлорида в ТГФ. После перемешивания полученной гомогенной смеси при -78 С в течение 3 ч смесь вливают в насыщенный хлорид аммония(100 мл) и экстрагируют этилацетатом. Органическую фазу промывают водой, сушат и концентрируют, а неочищенное вещество, полученное после удаления растворителя, очищают на колонке с силикагелем, элюируя 25% этилацетата в гексане с получением 3,32 г (74%) оксамата в виде бесцветного масла,1 Н ЯМР (CDCl3):0,88 (t, 3H); 1,21, 1,25(s, 3H каждый); 1,35-1,80 (m, 7H); 2,35 (m, 1H); 3,24 (m, 1H); 3,41 (m, 1H); 3,76 (s, 3H); 5,32 (d,1H). 1-(1,2-Диоксо-3,3-диметилпентил)-2-пиперидинкарбоновая кислота. Смесь метилового эфира 1-(1,2-диоксо-3,3 диметилпентил)-2-пиперидинкарбоновой кислоты (3,30 г; 12,25 ммоль), 1 н. LiOH (15 мл) и метанола (60 мл) перемешивают при 0 С в течение 20 30 мин и при комнатной температуре в течение ночи. Смесь подкисляют до рН 1 1 н. HCl, разбавляют водой и экстрагируют 100 мл метиленхлорида. Органический экстракт промывают рассолом и концентрируют, получая 2,80 г(87%) белоснежного твердого вещества, которое не требует дальнейшей очистки,1(s, 3H каждый); 1,42-1,85 (m, 7H); 2,35 (m, 1H); 3,22 (d, 1H); 3,42 (m, 1H); 5,31 (d, 1H). 2-Фенил-1-этиловый эфир (2S)-1-(3,3 диметил-1,2-диоксопентил)-2-пиперидинкарботионовой кислоты (10). К раствору 1-(1,2-диоксо-3,3-диметилпентил)-2-пиперидинкарбоновой кислоты (255 мг; 1,0 ммоль) в СН 2 Сl2 (10 мл) добавляют дициклогексилкарбодиимид (226 мг; 1,1 ммоль). После перемешивания полученной смеси в течение 5 мин раствор охлаждают до 0 С и обрабатывают раствором фенилмеркаптана (138 мг; 1,0 ммоль) и 4-диметиламинопиридина (6 мг) в 5 мл CH2Cl2. Смесь оставляют нагреваться до комнатной температуры при перемешивании в течение ночи. Твердые вещества удаляют фильтрованием, а фильтрат концентрируют в вакууме; неочищенный остаток очищают флешхроматографией (10:1 гексан:ЕtOАс) с образованием 300 мг (80%) 10 в виде масла,1 Н ЯМР (CDCl3; 300 МГц):0,94 (t, 3 Н,J=7,5); 1,27 (s, 3 Н); 1,30 (s, 3 Н); 1,34-1,88 (m,7H); 2,45 (m, 1 Н); 2,90 (t, 2H, J=7,7); 3,26 (t, 2H,J=7,7); 3,27 (m, 1H); 3,38 (m, 1H); 5,34 (m, 1H); 7,24-7,36 (m, 5 Н). Анализ: Вычислено для С 21 Н 29NО 3S: С,67,17; Н, 7,78; N, 3,73; Найдено: С, 67,02; Н, 7,83; N, 3,78. Как обсуждалось выше, соединения по настоящему изобретению обладают сродством кFKBP12. Показателем этого сродства может быть измеренное ингибирование активности пролилпептидил цис-транс-изомеразы FKBP. Методика определения Кi Способность соединений по изобретению ингибировать пептидил-пролил-изомеразную(ротамазную) активность можно оценить с помощью известных методов, описанных в литературе (Harding et al., Nature, 1989, 341: 758-760;Holt et al. J. Am. Chem. Soc., 115: 9923-9938). Эти значения получены как кажущиеся Кi и представлены для типичных соединений в табл. 4. Цис-транс-изомеризацию аланин-пролиновой связи на модели субстрата, N-сукцинил-Аlа-АlаРrо-Рhе-п-нитроанилида, регистрируют спектрометрически с использованием теста со связанным химотрипсином, который высвобождает паранитроанилид из транс-формы субстрата. Определяют ингибирование этой реакции, вызванное добавлением различных концентраций ингибитора, и данные анализируют, рассматривая изменение константы скорости первого по 21 рядка как функцию от концентрации ингибитора, с получением значений кажущейся Ki. В пластиковую кювету добавляют 950 мл образца ледяного буфера для тестирования (25 мМ HEPES, рН 7,8; 100 мМ NaCl), 10 мл FKBP(2,5 мМ в 10 мМ Tris-Cl, pH 7,5; 100 мМ NaCl; 1 мМ дитиотрейтола), 25 мл химотрипсина (50 мг/мл в 1 мМ HCl), и 10 мл тестируемого соединения при различных концентрациях в диметилсульфоксиде. Инициируют реакцию, добавляя 5 мл субстрата (сукцинил-Аlа-Рhе-Рrо-Рhе-паранитроанилид, 5 мг/мл в 2,35 мМ LiCl в трифторэтаноле). Поглощение при 390 нм во времени регистрируют в течение 90 с, используя спектрофотометр, и на основании данных о поглощении во времени, определяют константы скорости. Данные этих экспериментов для типичных соединений представлены в табл. 2 в графе "Кi". Нейротрофические эффекты соединений по настоящему изобретению могут быть продемонстрированы на клеточных биологических экспериментах in vitro, как описано ниже. Культуры спинно-мозгового ганглия цыпленка и вырост аксонов Нейротрофические эффекты соединений FKBP-ингибиторов были продемонстрированы путем оценки способности соединений активировать рост аксонов в культуральных чувствительных нейронах цыпленка из спинномозговых ганглиев (DRG). Спинно-мозговые ганглии вырезали из зародышей цыпленка на десятый день после оплодотворения. Целые экспланты ганглиев культивировали при температуре 37 С в атмосфере, содержащей 5% СO2,в 12-луночных планшетах, покрытых тонким слоем Matrigel, на среде Либовица (Liebovitz)L15 плюс глюкозная среда с добавками 2 мМ глутамина и 10%-й фетальной сыворотки теленка, а также 10 мкМ цитозинD арабинофуранозида (Аrа С). Через 24 ч спинно-мозговые ганглии обрабатывали различными концентрациями фактора роста нервной ткани (NGF), иммунофилиновыми лигандами, или комбинациями NGF плюс лекарственные средства. Через 48 ч после обработки лекарственным средством проводили визуальное исследование ганглиев под инвертированным фазово-контрастным илиZeiss Axiovert. Получали микрофотографии эксплантов и измеряли вырост аксонов. Аксоны,длина которых превышала диаметр DRG, рассматривали в качестве позитивных, кроме того,подсчитывали общее количество аксонов в каждом из вариантов эксперимента. В одной лунке культивировали от 3 до 4 DRG, и каждую обработку выполняли два раза. Строили кривые "доза-ответ", из которых получали значения ED50. Результаты этих экспериментов представлены в табл. 2 в графе"ED50". Типичные микрофотографии необработанных (контрольных) чувствительных нейро 002982 22 нов и активированного соединениями 1 (10 пМ,1 нМ, 1 мкМ), 9 (10 пМ, 1 нМ, 100 нМ) и 10 (10 пМ, 1 нМ, 100 нМ) выроста аксонов в чувствительных нейронах показаны на фиг. 1(A-D),2(A-D) и 3(A-D) соответственно. МРТР-модель болезни Паркинсона Значительные нейротрофические и нейрорегенеративные эффекты соединений по настоящему изобретению далее были продемонстрированы на животной модели нейродегенеративной болезни. В качестве животной модели болезни Паркинсона использовали МРТРповреждение дофаминергических нейронов. Четырехнедельные самцы белой мыши линииCD1 в течение 5 дней внутрибрюшинно получали дозу МРТР 30 мг/кг. Тестируемые соединения (4 мг/кг), или носитель, подкожно вводили вместе с МРТР в течение 5 дней, а потом продолжали их введение в течение следующих 5 дней без обработки МРТР. На 18 день после обработки МРТР животных умерщвляли, вырезали полосатое тело и гомогенизировали его. Чтобы произвести количественную оценку выживаемости и восстановления дофаминергических нейронов, на сагиттальных и венечных срезах головного мозга осуществляли иммуноокрашивание с использованием антитирозингидроксилазы (1 г). У животных, обработанных МРТР и носителем, наблюдали заметную потерю функциональных дофаминэргических окончаний по сравнению с неповрежденными животными. Поврежденные животные,получающие тестируемые соединения, показали значительное восстановление ТН-окрашенных дофаминергических нейронов. Результаты этих экспериментов представлены в табл. 2 в графе "% ТН-восстановления". Количественная оценка восстановления ТНположительных дофаминэргических нейронов в полосатом теле животных, получающих соединения 1, 9 и 10, и для типичных контрольных и поврежденных животных, не получающих тестируемые лекарственные средства, представлены на фиг. 4. Таблица 2 Результаты экспериментов in vitro Пример Ki, нМ ED50, нМ % ТН-восстановления 1 31 0,4 23 2 210 3 85 9 104 0,5 61 10 12 0,8 54 11 299 0,36 53 12 442 0,025 14 313 0,9 48 28 108 0,9 41 29 59 0,003 50 30 11 0,00025 65 31 8,7 31 32 362 52 33 1698 Все публикации и патенты, указанные выше, включены в этот документ ссылкой. Очевидно, что описанное таким образом изобретение может варьировать во многих отношениях. Такие варианты не должны рассматриваться как отклонения от сущности и объема изобретения, и подразумевают, что все такие модификации включены в объем следующей формулы изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы II или его фармацевтически приемлемая соль, гдеR1 представляет собой нормальный или разветвленный С 1-С 5 алкил, замещенный по одному или более чем одному положению Ar1;R2 выбран из группы, состоящей из нормального или разветвленного С 3-С 5 алкила, С 5 С 7 циклоалкила и Ar1;Ar1 представляет собой фенил, пиридил,флуоренил, тиоиндолил, нафтил или бифенил,где указанный Ar1 не замещен или замещен по одному или более чем одному положению галогено, трифторметилом, метокси или их смесью. 2. Соединение по п.1, гдеn равно 1; и Х представляет собой О. 3. Соединение по п.2, где Z представляет собой СН 2. 4. Соединение по п.3, которое выбрано из группы, состоящей из(2S)-2-(1-оксо-4-фенил)бутил-1-(2-циклогексил-1,2-диоксоэтил)пирролидина и 2-(1-оксо-4-фенил)бутил-1-(3,3-диметил 1,2-диоксобутил)пирролидина. 5. Соединение по п.2, где Z представляет собой S. 6. Соединение по п.5, которое выбрано из группы, состоящей из 2-фенил-1-этилового эфира (2S)-1-(3,3 диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты; 1-2-[(бензо[b]тиофен-3-илметилтио)карбонил]пирролидинил-3,3-диметилпентан-1,2 диона; 2-фенил-1-этилового эфираn равно 2; и Х представляет собой О. 8. Соединение по п.7, где Z представляет собой СН 2. 9. Соединение по п.8, которое выбрано из группы, состоящей из 2-(1-оксо-6-фенил)гексил-1-(3,3-диметил 1,2-диоксобутил)пиперидина; 3,3-диметил-1-[2-(4-фенилбутаноил)пиперидино]-1,2-пентандиона и 3,3-диметил-1-[2-(5-фенилпентаноил)пиперидино]-1,2-пентандиона. 26 10. Соединение по п.7, где Z представляет собой S. 11. Соединение по п.10, которое выбрано из группы, состоящей из 2-фенил-1-этилового эфира 1-(3,3 диметил-1,2-диоксопентил)-2-пиперидинкарботионовой кислоты; 2-фенил-1-этилового эфира 1-(2-фенил-1,2 диоксоэтил)-2-пиперидинкарботионовой кислоты; 3-фенил-1-пропилового эфира 1-(3,3 диметил-1,2-диоксобутил)-2-пиперидинкарботионовой кислоты; 4-фенил-1-бутилового эфира 1-(1,2 диоксо-3,3-диметилбутил)-2-пиперидинкарботионовой кислоты; 1,5-дифенил-3-пентилового эфира 1-(3,3 диметил-1,2-диоксопентил)-2-пиперидинкарботионовой кислоты; 1,5-дифенил-3-пентилового эфира 1-(2 фенил-1,2-диоксоэтил)-2-пиперидинкарботионовой кислоты; 3-(параметоксифенил)-1-пропилового эфира 1-(1,2-диоксо-3,3-диметилпентил)пиперидин 2-карботионовой кислоты; 3-(параметоксифенил)-1-пропилового эфира 1-(2-фенил-1,2-диоксоэтил)пиперидин-2 карботионовой кислоты; 3-(1-нафтил)-1-пропилового эфира 1-(3,3 диметил-1,2-диоксопентил)пиперидин-2-карботионовой кислоты; 2,2-дифенилэтилового эфира (2S)-1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 3,3-дифенилпропилового эфира 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 3-(1-нафтил)-1-пропилового эфира 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 4-фенилбутилового эфира 1-(3,3-диметил 2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 3-фенилпропилового эфира 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 3-(3-хлорфенил)-1-пропилового эфира 1(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 3-(2-фторфенил)пропилового эфира 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты и 3-(3-фторфенил)пропилового эфира 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты. 12. Соединение по п.7, где Z представляет собой CHR1. 13. Соединение по п.12, которое выбрано из группы, состоящей из 2-1-оксо-[2-(2'-фенил)этил]-4-фенилбутил-1-(3,3-диметил-1,2-диоксобутил)пиперидина. 27 14. Соединение, которое представляет собой 3,3-дифенил-1-пропиловый эфир (2S)-1(3,3-диметил-1,2-диоксопентил)-2-пирролидинкарботионовой кислоты. 15. Соединение, которое представляет собой 3-(1-нафтил)-1-пропиловый эфир (2S)-1(3,3-диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты. 16. Соединение, которое представляет собой 2,2-дифенилэтиловый эфир (2S)-1-(3,3 диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты. 17. Соединение, которое представляет собой 3,3-дифенилпропиловый эфир 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты. 18. Соединение, которое представляет собой 3-[4-(трифторметил)фенил]пропиловый эфир (2S)-1-(3,3-диметил-2-оксопентаноил)-2 пирролидинкарботионовой кислоты. 19. Соединение, которое представляет собой 3-(2-нафтил)пропиловый эфир (2S)-1-(3,3 диметил-2-оксопентаноил)-2-пирролидинкарботионовой кислоты. 20. Соединение, которое представляет собой 3,3-диметил-1-[(2S)-2-(5-(3-пиридил)пентаноил)-1-пирролидин]-1,2-пентандион. 21. Соединение, которое представляет собой (2S)-2-(1-оксо-4-фенил)бутил-1-(3,3-диметил-1,2-диоксобутил)пирролидин. 22. Фармацевтическая композиция, содержащая 1) эффективное количество соединения формулы II или его фармацевтически приемлемой соли, гдеR1 представляет собой нормальный или разветвленный С 1-С 5 алкил, замещенный по одному или более чем одному положению Ar1;R2 выбран из группы, состоящей из нормального или разветвленного С 3-С 5 алкила, С 5 С 7 циклоалкила и Ar1;Ar1 представляет собой фенил, пиридил,флуоренил, тиоиндолил, нафтил или бифенил,где указанный Ar1 не замещен или замещен по одному или более чем одному положению галогено, трифторметилом, метокси или их смесью; и 2) фармацевтически приемлемый носитель. 23. Фармацевтическая композиция по п.22,где указанное соединение выбрано из группы,состоящей из 30 3,3-дифенилпропилового эфира 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 3-(1-нафтил)-1-пропилового эфира 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 4-фенилбутилового эфира 1-(3,3-диметил 2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 3-фенилпропилового эфира 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 3-(3-хлорфенил)-1-пропилового эфира 1(3,3-диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 3-(2-фторфенил)пропилового эфира 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты; 3-(3-фторфенил)пропилового эфира 1-(3,3 диметил-2-оксопентаноил)-2-пиперидинкарботионовой кислоты и 2-1-оксо-[2-2'-фенилэтил]-4-фенилбутил-1-(3,3-диметил-1,2-диоксобутил)пиперидина. 24. Фармацевтическая композиция по любому из пп.22-23, которая дополнительно содержит один или более чем один дополнительный нейротрофический агент. 25. Фармацевтическая композиция по п.24,где указанный один или более чем один дополнительный нейротрофический агент независимо выбран из группы, состоящей из фактора роста нервной ткани (NGF), глиального фактора роста, мозгового фактора роста, цилиарного нейротрофического фактора и нейротропина-3. 26. Фармацевтическая композиция по п.25,где указанный один или более чем один дополнительный нейротрофический агент представляет собой фактор роста нервной ткани (NGF). 27. Способ нейронального воздействия у животного, при котором животному вводят эффективное количество соединения формулы II или его фармацевтически приемлемой соли, гдеR1 представляет собой нормальный или разветвленный С 1-С 5 алкил, замещенный по одному или более чем одному положению Ar1;R2 выбран из группы, состоящей из нормального или разветвленного С 3-С 5 алкила, С 5 С 7 циклоалкила и Ar1;Ar1 представляет собой фенил, пиридил,флуоренил, тиоиндолил, нафтил или бифенил, 31 где указанный Ar1 не замещен или замещен по одному или более чем одному положению галогено, трифторметилом, метокси или их смесью. 28. Способ по п.27, где указанное соединение выбрано из группы, состоящей из 34 2-1-оксо-[2-2'-фенилэтил]-4-фенилбутил-1-(3,3-диметил-1,2-диоксобутил)пиперидина. 29. Способ по любому из пп.27-28, где нейрональное воздействие выбрано из группы,состоящей из стимуляции поврежденных нейронов, активации нейронной регенерации, предотвращения нейродегенерации и лечения неврологического расстройства. 30. Способ по п.29, где неврологическое расстройство выбрано из группы, состоящей из периферической невропатии, вызванной физической травмой или болезненным состоянием,травмы головного мозга, физического повреждения спинного мозга, инсульта, связанного с повреждением головного мозга, и неврологического расстройства, относящегося к нейродегенерации. 31. Способ по п.30, где неврологическое расстройство, относящееся к нейродегенерации,выбрано из группы, состоящей из болезни Альцгеймера, болезни Паркинсона и бокового амиотрофического склероза.
МПК / Метки
МПК: A61K 31/40, A61P 25/00, C07D 207/06
Метки: кетоны, гетероциклические, тиоэфиры
Код ссылки
<a href="https://eas.patents.su/20-2982-geterociklicheskie-tioefiry-i-ketony.html" rel="bookmark" title="База патентов Евразийского Союза">Гетероциклические тиоэфиры и кетоны</a>
Предыдущий патент: Способ полимеризации этилена, пиридинбисимины и комплексы пиридинбисиминов с железом и кобальтом
Следующий патент: Способ изменения гуморального иммунного ответа с помощью агентов, блокирующих рецепторы бета-лимфотоксина
Случайный патент: Лифт с канатоведущим шкивом, не имеющий противовеса