Мультивалентная адъювантная конструкция
Формула / Реферат
1. Адъювант-полимерная конструкция, содержащая
синтетическую линейную основную цепь полимера, которая является биологически неактивной; и
3 или более адъювантов, ковалентно связанных с основной цепью полимера либо непосредственно, либо с помощью спейсерной группы, где 3 или более адъювантов являются одинаковыми или разными и каждый присутствует в подвешенной боковой цепи,
где основная цепь полимера образована из мономерных звеньев, выбранных из (мет)акрилатов, (мет)акриламидов, стирольных мономеров, виниловых мономеров, простого винилового эфира, сложного винилового эфира, сиаловой кислоты, маннозы, N-(2-гидроксиэтил)-1-глутамина (HEG) и этиленгликоль-олигопептида;
где адъюванты выбраны из липогликанов, липополисахарида, липотейхоевой кислоты, пептидогликана, синтетических липопротеинов, зимозана, гликолипидов, полиинозин-полицитидиловой кислоты, монофосфориллипида А, флагеллина, имидазохинолиновых соединений, гуанозина, TNF-альфа (фактор некроза опухоли альфа) или его пептидов, IL-2, IL-4, IL-8, CD40, ОХ40, GM-CSF и CpG-содержащих последовательностей в бактериальной ДНК или синтетических олигонуклеотидах;
где спейсерные группы являются одинаковыми или разными и каждая выбрана из олиго(алкилоксид)ов, олигопептидов, С1-С12-алкильных группировок, С6-С10-арильных группировок, комбинаций таких алкильных и арильных группировок, сложных полиэфиров и поликарбонатов.
2. Адъювант-полимерная конструкция по п.1, где средневесовая молекулярная масса полимера находится в диапазоне от 1 до 100 кДа.
3. Адъювант-полимерная конструкция по п.1 или 2, где основная цепь полимера является, по меньшей мере частично, водорастворимой.
4. Адъювант-полимерная конструкция по любому из пп.1-3, где основная цепь полимера образована из мономерных звеньев, выбранных из N-2-гидроксипропилметакриламида (НРМА), N-(2-гидроксиэтил)-1-глутамина (HEG) и этиленгликоля, или представляет собой полисиаловую кислоту или полиманнановый полимер.
5. Адъювант-полимерная конструкция по любому из пп.1-4, где адъюванты связывают Toll-подобные рецепторы.
6. Адъювант-полимерная конструкция по любому из пп.1-5, где основная цепь полимера и/или спейсерная(ые) группа(ы) содержат разлагаемые связи.
7. Адъювант-полимерная конструкция по любому из пп.1-6, где средневесовая молекулярная масса полимера составляет от 5 до 40 кДа.
8. Адъювант-полимерная конструкция по любому из пп.1-7, где основная цепь полимера ковалентно связана с 10-50 адъювантами либо непосредственно, либо посредством спейсерной группы.
9. Адъювант-полимерная конструкция по любому из пп.1-8, связанная с вакциной с образованием вакцинного конъюгата.
10. Композиция, содержащая адъювант-полимерную конструкцию по любому из пп.1-9 и фармацевтически приемлемый носитель или разбавитель.
11. Композиция по п.10, которая дополнительно содержит вакцину.
12. Способ стимулирования или усиления иммунного ответа у человека, включающий введение указанному человеку эффективного, нетоксичного количества адъювант-полимерной конструкции по любому из пп.1-9 или композиции по п.10 или 11, где при введении адъювант-полимерной конструкции по любому из пп.1-8 или композиции по п.10 дополнительно проводят стадию введения пациенту эффективного и нетоксичного количества вакцины.
13. Применение адъювант-полимерной конструкции по любому из пп.1-9 в способе стимулирования или усиления иммунного ответа.
14. Применение по п.13, где адъювант-полимерная конструкция по любому из пп.1-8 применяется при дополнительном введении вакцины.
15. Применение композиции по п.10 или 11 в способе стимулирования или усиления иммунного ответа.
16. Применение по п.15, где композиция по п.10 применяется при дополнительном введении вакцины.
Текст
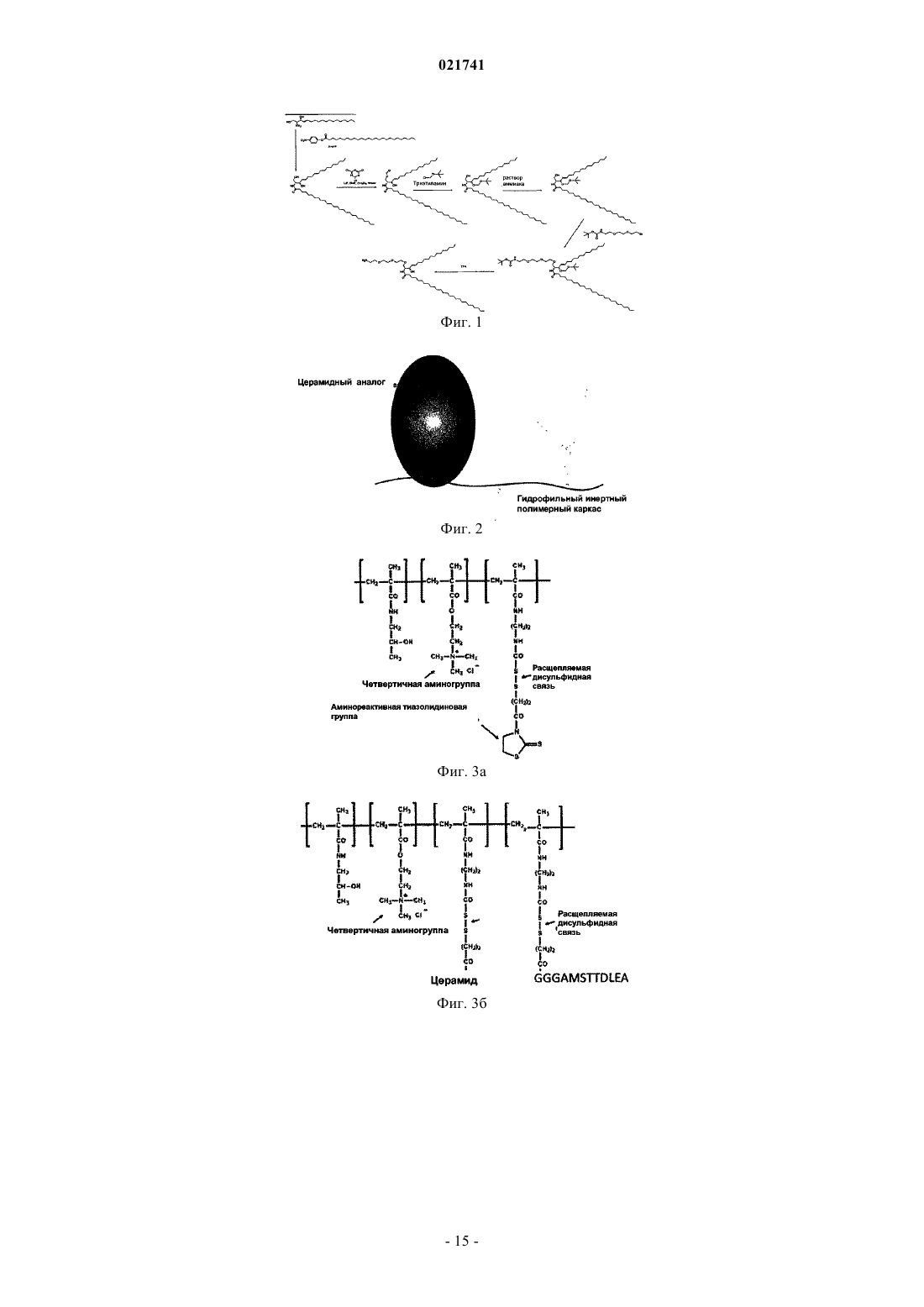
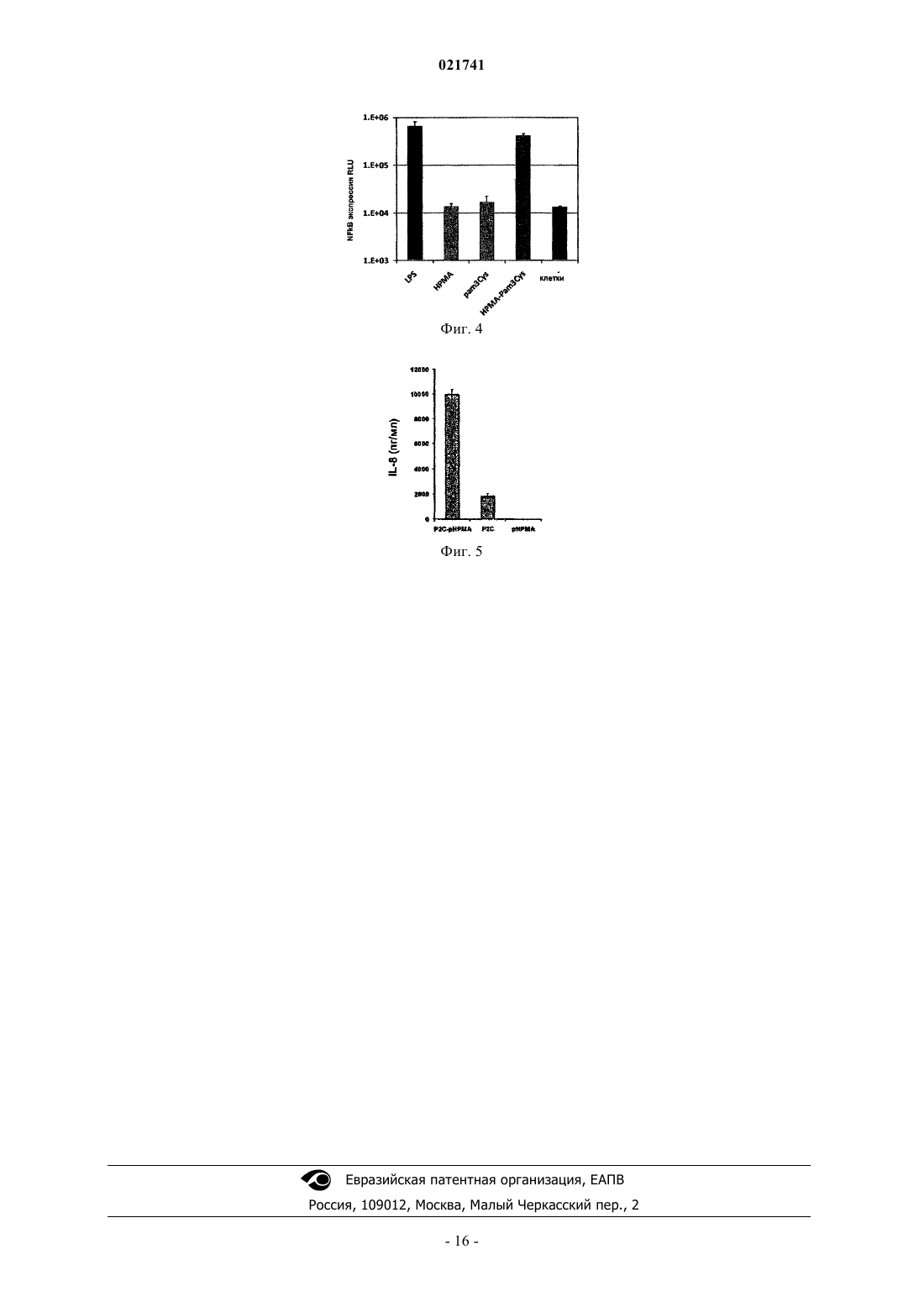
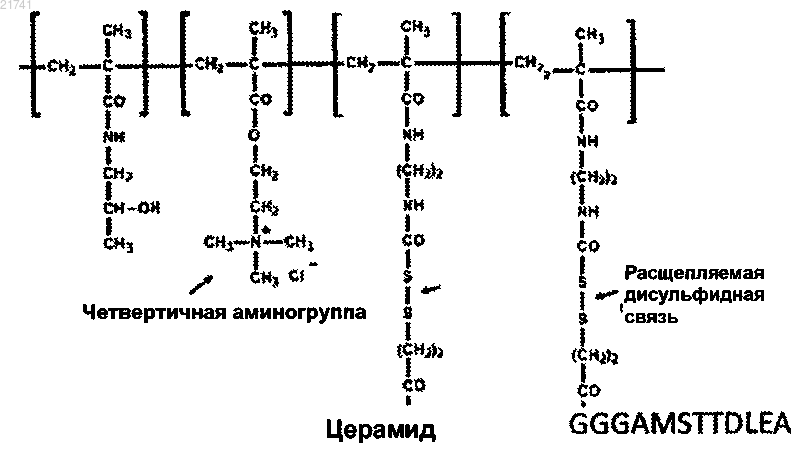
Сеймур Леонард Чарлз Уильям,Фишер Керри (GB) Поликарпов А.В. (RU) В изобретении предлагается конструкция адъювант-полимер, содержащая основную цепь полимера, которая ковалентно соединена с 3 или более адъювантами, где каждый из 3 или более адъювантов присутствует в подвешенной боковой цепи, где адъюванты соединены с основной цепью полимера либо непосредственно, либо с помощью спейсерной группы.(71)(73) Заявитель и патентовладелец: ПСИОКСУС ТЕРАПЬЮТИКС ЛИМИТЕД (GB) Мультивалентная адъювантная конструкция Настоящее изобретение относится к усовершенствованным способам стимулирования иммунной системы с использованием адъювантов. В частности, изобретение относится к новым адъювантсодержащим продуктам, которые представляют собой адъюванты в формате сложной конструкции, к композициям, включающим такие продукты, и к применению таких продуктов в иммунизации. Предшествующий уровень техники Адъюванты обычно представляют собой компоненты (или аналоги) обычных патогенов, таких как вирусы, бактерии или грибы. Они, как правило, распознаются образ-распознающими рецепторами, фагоцитарными рецепторами и toll-подобными рецепторами (TLR). Наиболее успешные адъюванты связываются с такими рецепторами с низким сродством, но высокой авидностью вследствие многократно повторяющейся презентации. Лучшие адъюванты обычно представляют собой целые (или частично разрушенные) бактерии или двухнитевую вирусную ДНК. Однако в настоящее время в данной области техники имеется склонность к более определенным композициям с одним идентифицируемым и предпочтительно полностью синтетическим компонентом. К сожалению, чистые, обособленные и монодисперсные адъюванты не стимулируют врожденную иммунную систему в той же степени, что и исходные "грязные" композиции. Современные синтетические адъюванты, такие как имиквимод и Pam2Cys, являются плохо растворимыми низкомолекулярными агентами, которые трудно приготовить в виде препарата и доставлять. Конкретные примеры адъювантов, описанных в данной области техники, включают синтетические адъюванты, такие как адъюванты, описанные в US 6149222. Такие адъюванты представляют собой полоксамеры, составленные из блок-сополимеров полиоксиэтилен/полиоксипропилен, и они стимулируют ряд рецепторов клеточной поверхности посредством плохо определенных неионных взаимодействий. ВUS 6610310 описаны полианионные синтетические полимеры, составленные из многочисленных отрицательных зарядов на синтетическом сахаре или другом полимере. Однако такие синтетические адъюванты, как правило, обладают плохой авидностью и недостаточной активностью адъюванта. Были предприняты усилия по включению синтетических адъювантов в композиции с целью улучшения доставки. Например, в US 2005/0233105 описаны композиции, которые включают низкомолекулярный синтетический адъювант. Однако такие композиции представляют собой простые смеси адъювантов с вирусной вакциной и они не предоставляют возможность улучшения внутренней активности синтетических адъювантов. Аналогично, в WO 2007/078879 описаны композиции, содержащие самособирающиеся липосомы,полимерные комплексы и эмульгированные липиды. Такие композиции предназначены для представления адъювантов в более естественном формате, но их трудно готовить в виде препарата, и большая часть адъювантного вещества является недоступной, так как это вещество заключено в гидрофобное ядро. Такие композиции застывают при определенных условиях, и вследствие своей нестабильности их, как правило, следует готовить непосредственно перед введением. Таким образом, существует необходимость нового подхода в разработке синтетических адъювантов, которые обеспечивают улучшенное стимулирование иммунной системы. Краткое изложение сущности изобретения Таким образом, в настоящем изобретении предлагается адъювант-полимерная конструкция (также называемая в данном изобретении полимер-адъювантной конструкцией), содержащая основную цепь полимера, которая ковалентно связана с 3 или более адъювантами, где каждый из 3 или более адъювантов присутствует в подвешенной боковой цепи, где адъюванты соединены с основной цепью полимера либо непосредственно, либо с помощью спейсерной группы. Авторы данного изобретения обнаружили, что связывание нескольких небольших синтетических адъювантов с полимером так, чтобы адъюванты присутствовали в формате мультивалентного дисплея,может увеличивать иммунное стимулирование по сравнению с применением одних синтетических адъювантов. Полагают, что презентация многочисленных адъювантов, напоминающая патогенассоциированные молекулярные структуры (РАМР), таким образом улучшает авидность рецептора и обеспечивает более естественную презентацию toll-подобным рецепторам и образ-распознающим рецепторам. Кроме того, мультивалентный дисплей адъювантов стимулирует сшивание рецепторов и передачу сигналов рецепторами. Все эти факторы приводят к увеличенному иммунному стимулированию и тем самым обеспечивают возможность применения более низких доз адъюванта и уменьшения побочных эффектов. Связывание адъювантов с полимерной цепью таким образом также увеличивает размер молекулы адъювантного компонента, что способствует предотвращению вымывания в кровоток и тем самым уменьшает неэффективную токсичность. В предпочтительных воплощениях изобретения сама основная цепь полимера является гидрофильной, что способствует солюбилизации обычно липофильных адъювантов. Это облегчает доставку адъюванта и позволяет использовать более простые композиции. Еще одно преимущество заключается в увеличении количества молекул, которые могут взаимодействовать с рецепторами, что также дает возможность применения более низких доз. Адъювант-полимерную конструкцию по изобретению обычно вводят в сочетании с вакциной. Та-1 021741 ким образом, в настоящем изобретении также предлагается вакцинный конъюгат, содержащий адъювантполимерную конструкцию по изобретению, которая связана с вакциной. Также предлагается композиция, содержащая адъювант-полимерную конструкцию или вакцинный конъюгат по изобретению и фармацевтически приемлемый носитель или разбавитель. В настоящем изобретении также предлагается способ стимулирования или усиления иммунного ответа у человека, нуждающегося в этом, включающий введение указанному человеку эффективного, нетоксичного количества адъювант-полимерной конструкции, вакцинного конъюгата или композиции по изобретению. Когда адъювант-полимерная конструкция или композиция не содержит вакцину, способ дополнительно включает стадию введения вакцины либо одновременно или по отдельности. Также предлагается адъювант-полимерная конструкция, вакцинный конъюгат или композиция по изобретению для применения в способе стимулирования или усиления иммунного ответа. Краткое описание чертежей На фиг. 1 представлена схема, показывающая синтез церамидного аналога (3). На фиг. 2 изображена структура полимер-адъювантной конструкции по изобретению. На фиг. 3 а изображена структура реакционноспособного полимера для использования в получении полимер-адъювантной конструкции; на фиг. 3 б изображен тот же самый полимер, связанный с церамидным адъювантом и пептидным антигеном. На фиг. 4 показано, что множественная презентация агониста TLR2 Pam3Cys на том же самом полимере приводит к более высокому стимулированию клеток. U937 представляет собой клеточную линию лимфомы с моноцит-подобным фенотипом, которая экспрессирует ряд TLR-рецепторов, включая TLR2. Стимулирование TLR2 приводит к активированию NfkB, и эти клетки трансфицировали репортерной плазмидой (люциферазой) под контролем промотора NfkB. Через 8 ч воздействия тестируемым веществом клетки лизировали и анализировали в отношении экспрессии люциферазы. Все тестируемые вещества добавляли в концентрации 100 нг/мл (примечание: только 5,22 нг Pam3Cys-полимерного конъюгата представляет собой Pam3Cys). Данные показывают, что Pam3Cys, связанный с полимером, демонстрирует значительно более высокий уровень стимулирования по сравнению с самим Pam3Cys и сравнимый с положительным контролем LPS (липополисахарид). RLU - относительные световые единицы. На фиг. 5 показано, что множественная презентация агониста TLR2 Pam2Cys на том же самом полимере приводит к более высокому стимулированию клеток. На DC (дендритные клетки) из костного мозга воздействовали 50 нг/мл Pam2Cys (P2C) или Р 2 С, соединенным с НРМА (гидроксипропилметакриламид), в течение 24 ч. Супернатант клеток затем оценивали в отношении IL-8 с помощью ELISA(твердофазный иммуноферментный анализ). Примечание: только 5 мас.% (2,5 нг) Pam2Cys присутствовало в 50 нг/мл образце Р 2 С-рНРМА. Подробное описание изобретения При использовании в данном описании изобретения адъювант представляет собой агент, который может стимулировать иммунную систему и усиливать ответ на вакцину, не обладая сам по себе какимлибо специфическим антигенным эффектом. Конструкции по настоящему изобретению содержат по меньшей мере 3 адъюванта, которые могут быть одинаковыми или разными. В одном предпочтительном воплощении 3 или более адъюванта являются одинаковыми. Каждый адъювант присоединен к основной цепи полимера в подвешенной боковой цепи. Таким образом, адъюванты не являются частью самой основной цепи полимера. Это обеспечивает лучшую презентацию адъювантов для распознавания клеточными рецепторами, так как пространственно-ассоциированная совокупность адъювантов более точно напоминает эпитопы РАМР на поверхности целой бактерии или вируса или их компонент, такой как двухнитевая вирусная РНК, и приводит к более значительной авидности связывания для клеточного рецептора или рецепторов. По меньшей мере 3 адъюванта, предпочтительно по меньшей мере 5, более предпочтительно по меньшей мере 10 адъювантов ковалентно связаны с каждым полимером, где каждый адъювант обычно присутствует на отдельной подвешенной боковой цепи. Обычно вплоть до 50 адъювантов присутствует на одной основной цепи полимера. В одном воплощении по меньшей мере 20 адъювантов присутствуют на основной цепи полимера. Адъюванты могут содержат широкий ряд структур, отличающихся по своей способности стимулировать улучшенный иммунный ответа против вакцины. Один класс рецепторов, с которыми связываются адъюванты, представляет собой Toll-подобные рецепторы (TLR; также известные как "образраспознающие рецепторы" из-за их способности распознавать повторяющиеся последовательности РАМР на поверхности патогенов). TLR распознают консервативные молекулярные продукты из различных классов патогенов, включая грамположительные и грамотрицательные бактерии, ДНК и РНКвирусы, грибы и простейшие. Гены TLR были распознаны в ряде геномов позвоночных и многие частичные и полноразмерные последовательности являются доступными. У человека были идентифицированы одиннадцать TLR, в то время как в исследованиях мышиного генома можно обнаружить 13 TLR. Было показано, что члены семейства человеческих и мышиных TLR имеют отчетливые лигандные специфичности, распознавая разные молекулярные структуры. Все TLR1, TLR2, TLR4, TLR5 и TLR6 расположены в плазматической мембране, распознавая компоненты клеточной стенки, в то время как TLR3, TLR7,-2 021741TLR8 и TLR9 преимущественно экспрессируются во внутриклеточных компартментах, таких как эндосомы, и распознают нуклеиново-кислотные структуры. Требования к лигандам разных TLR были частично охарактеризованы: гетеродимеры TLR2 (главным образом с TLR1 или TLR6) - липопротеины, пептидогликаны, липогликаны, липотейхоевая кислота, липополисахарид, пептидогликаны, зимозан,TLR5 - бактериальные флагеллины,TLR7 - имидазохинолины (имиквимод, гардиквимод), CL264, локсорибин,TLR8 - однонитевая РНК, РНК Е. coli, гетеродимеры TLR7/TLR8: CL075, CL097, поли(dT), R848,TLR9 - неметилированные CpG-островки в ДНК, включая CpG-содержащие олигонуклеотиды,TLR4 - липополисахарид, монофосфориллипид А,TLR3 - двухнитевая РНК. Примеры лигандов TLR включают имиквимод - лиганд TLR7,MALP-2 (диацилированный липопептид, выделенный из Mycoplasma Fermentans) - лигандTLR обнаруживают в клетках наследственного иммунитета (DC, макрофаги, естественные клеткиубийцы), клетках приобретенного иммунитета (Т- и В-лимфоциты), а также в неиммунных клетках (эпителиальные и эндотелиальные клетки, фибробласты). Предпочтительными адъювантами для применения в изобретении являются липогликаны, липополисахарид, липоарабиноманнан, липотейхоевую кислоту, пептидогликан, натуральные и синтетические липопротеины и липопептиды, зимозан, гликолипиды, полиинозин-полицитидиловая кислота, монофосфориллипид A, TNF-альфа (фактор некроза опухоли альфа), TNF-пептиды, лиганд CD40, ОХ 40, IL-4, IL6, IL-8, IL-2, IL-12, манноза, GM-CSF (гранулоцитарно-макрофагальный колониестимулирующий фактор), IFN-гамма (интерферон-гамма), IFN-альфа, флагеллин, имидазохинолиновые соединения, гуанозин,двухнитевая РНК (ds-РНК), однонитевая ДНК (ss-ДНК) и неметилированные CpG-содержащие последовательности в бактериальной ДНК или синтетических олигонуклеотидах. Основная цепь полимера по настоящему изобретению может представлять собой синтетический или имеющийся в природе полимер. При использовании в данном описании изобретения полимер включает биополимеры, такие как нуклеиновые кислоты, белки и крахмал, а также синтетические полимеры. В одном воплощении полимер не является нуклеиновой кислотой. В другом воплощении полимер представляет собой синтетический полимер. В одном воплощении полимеры представляют собой гидрофильные полимеры, которые наделяют адъювант-полимерную конструкцию растворимостью в воде. Например, адъювант-полимерные конструкции могут иметь растворимость в воде по меньшей мере 100 мкг/мл, например по меньшей мере 150 или по меньшей мере 200 мкг/мл. Сам полимер может быть биологически активным, например сам полимер может обладать свойствами адъюванта. В одном воплощении сам полимер, по существу, не имеет адъювантной активности (то есть полимер СА по себе не будет увеличивать иммунное стимулирование). Измерение адъювантной активности полимера можно выполнять, например, используя анализ подколенных лимфатических узлов(PLN), где полимер инъецируют в подушечку задних лап мышей вместе с антигеном. Адъювантную активность определяют в виде увеличения массы PLN и количества клеток у животных, получающих антиген вместе с исследуемым веществом, по сравнению с массой PLN и количеством клеток у животных,получавших антиген без интересующего вещества, и животных, получавших только предполагаемый адъювант. В другом воплощении полимер является биологически неактивным. Подходящие синтетические полимеры включают полимеры на основе мономеров, имеющих виниловую группировку, например (мет)акрилаты, (мет)акриламиды, винил, виниловый эфир, виниловый сложный эфир и стириловые группировки. Конкретные примеры мономеров в этой категории представляют собой (мет)акрилаты и (мет)акриламиды, в частности N-2-гидроксипропилметакриламид (НРМА) и гидроксиэтилметакрилат (НЕМА), и винилпирролидон (PVP). Также можно использовать циклические мономеры, подходящие для полимеризации с раскрытием кольца и реакции обмена с раскрытием кольца,например циклические амиды, циклические сложные эфиры, циклические уретаны, циклические простые эфиры, циклические ангидриды, циклические сульфиды, циклические амины и моно- и мультициклические алкены. Альтернативные основные цепи полимера включают нуклеиновые кислоты (например, поли-I:полиС, поли-А:поли-U, однонитевую ДНК, двухнитевую ДНК), полиэтиленгликоль, поли(этиленгликольолигопептид), поли(аминокислоты) (например, поли[N-(2-гидроксиэтил)-L-глутамин) и полисахариды,такие как гликоген, целлюлоза, декстран, циклодекстрин, альгинат, гиалуроновая кислота, полисиаловая кислота, полиманнан или другие полимеры на основе глюкозы или галактозы. Дополнительные природ-3 021741 ные продукты, которые можно использовать в качестве основной цепи полимера, включают гепарин,декстран и крахмал. Когда основная цепь основана на этиленгликоль-олигопептиде, олигопептидная группа предпочтительно содержит от 1 до 4 аминокислот и подвешенные боковые цепи обычно поддерживаются олигопептидной частью основной цепи полимера. Обычно основная цепь полимера основана на мономерных единицах, выбранных из (мет)акрилатов,(мет)акриламидов, стириловых мономеров, виниловых мономеров, мономеров винилового эфиры, мономерах винилового сложного эфира, мономерах сиаловой кислоты, мономерах маннозы, N-(2 гидроксиэтил)-L-глутаминовых (HEG) мономерах и этиленгликоль-олигопептидных мономерах. Предпочтительно основная цепь полимера основана на мономерных единицах, выбранных из N-2 гидроксипропилметакриламида (НРМА), N-(2-гидроксиэтил)-L-глутамина (HEG) и этиленгликольолигопептида, или представляет собой полисиаловую кислоту или полиманнановый полимер. Основные цепи полимера на основе НРМА являются более предпочтительными. Средневзвешенная молекулярная масса полимера обычно находится в диапазоне от 1 до 100 кДа,например по меньшей мере 2, более предпочтительно по меньшей мере 5 и вплоть до 80 кДа, более предпочтительно вплоть до 40 кДа. Предпочтительные полимеры имеют средневзвешенную молекулярную массу от 5 до 40 кДа. Основная цепь полимера может представлять собой линейный полимер, имеющий 3 или более подвешенные боковые цепи, содержащие адъювант. Альтернативно, сама основная цепь полимера может представлять собой разветвленную структуру. Например, предусматриваются дендритные и гребенчатые полимеры. В некоторых воплощениях основная цепь полимера может быть сшита с дополнительными полимерами, так что образуется гидрогель. Гидрогель является предпочтительно гидролитически нестабильным или разлагаемым с помощью фермента, например матриксных металлопротеиназ 2 или 9. Это делается для того, чтобы иммобилизовать адъюванты в гидрогеле, и так, чтобы можно было регулировать высвобождение адъювантов. Таким образом, согласно одному предпочтительному аспекту изобретения способ по изобретению выполняют в условиях, подходящих для стимулирования сшивания и образования гидрогеля (например, высокие концентрации реагентов, причем ни один из них не присутствует в избытке) или в присутствии агентов, таких как диамины, подходящих для стимулирования сшивания. Образование гидрогелей, содержащих модифицированные адъюванты, как правило, можно выполнять, используя химические подходы, описанные в Subr, V., Duncan, R. and Kopeck, J. (1990) "Release of macromolecules anddaunomycin from hydrophilic gels containing enzymatically degradable bonds", J. Biomater. Sci. Polymer Edn.,1(4) 61-278. Когда основная цепь полимера содержит нуклеиновую кислоту, полимер может быть соединен с еще одной нуклеиновой кислотой с образованием двухнитевой спиралевидной структуры. Адъюванты могут быть связаны с основной цепью полимера либо непосредственно, либо с помощью спейсерной группы. В предпочтительном воплощении присутствует спейсерная группа, так что адъювант-полимерная конструкция имеет структуру где Р представляет собой основную цепь полимера; S представляет собой спейсерную группу; А представляет собой адъювант и n равно 3 или более. Спейсерные группы могут быть одинаковыми или разными и обычно их выбирают из олиго(алкилоксид)ов (например, цепей pEG длиной от 2 до 200 атомов углерода); олигопептидов, содержащих, например, вплоть до примерно 20 аминокислот; С 1-С 12-алкильных группировок (например, С 1-С 6 алкильных группировок, таких как метилен, этилен, пропилен или бутилен); С 6-C10-арильных группировок (например, фенила); комбинаций таких алкильных и арильных группировок; сложных полиэфиров и поликарбонатов. Подходящими сложными полиэфирами и поликарбонатами являются, например, имеющие цепи из 10-30 атомов углерода. Спейсерная группа обычно является гидрофильной и может включать разлагаемую связь, такую как восстанавливаемая дисульфидная связь, связь, чувствительная к гидролизу, катализируемому кислотой, или связь, расщепляемую посредством ферментативного расщепления. Предпочтительные спейсерные группы представляют собой олиго(алкоксид)ы и олигопептиды, в частности олигопептиды. В одном воплощении изобретения спейсерная группа представляет собой олигопептид. Предпочтительно олигопептид содержит вплоть до 10, например вплоть до 5 аминокислот. Более предпочтительно олигопептид содержит от 1 до 4, например 2 или 4 аминокислоты. Подходящие олигопептиды представляют собой -Gly-Phe-Leu-Gly-, -Gly-Gly- и Glu-Lys-Glu-. В другом воплощении спейсерная группа содержит разлагаемую связь. Например, спейсерная группа может расщепляться при восстановлении, например, -NH-(CH2)2NHCO-(CH2)2-SS-(CH2)2-CO-. Альтернативно, спейсерная группа может расщепляться посредством катализируемого кислотой гидролиза, например где х и у независимо представляют собой целые числа от 1 до 5, например 1, 2 или 3, и R представляет собой, например, С 1-С 8-алкильную группу, например метил или этил. Величина n отражает число подвешенных боковых цепей, которые содержат адъювант. По меньшей мере 3 адъюванта присутствуют на каждой молекуле полимера, таким образом n равно по меньшей мере 3. Обычно вплоть до 50 адъювантов присутствуют на одной основной цепи полимера, таким образом, n равно вплоть до 50. В одном воплощении по меньшей мере 20 адъювантов присутствуют на основной цепи полимера. В одном воплощении изобретения группы -S-A содержат по меньшей мере 2 мол.% адъювантполимерной конструкции. Например, группы -S-A могут содержать по меньшей мере 5 мол.% конструкции. Обычно группы -S-A содержат не более 20 мол.% адъювант-полимера, например вплоть до 10 мол.%. Адъювант-полимерная конструкция по изобретению может содержать подвешенные боковые цепи,несущие функциональные группы, отличные от адъювантов. Такие функциональные группы могут быть связаны с основной цепью полимера непосредственно или с помощью спейсерной группы. Подходящими спейсерными группами являются группы, описанные выше. Примерами функциональных групп, которые могут присутствовать, являются солюбилизирующие группы, такие как аминная, гидроксильная,карбоксильная и олиго(алкиленовая) группы. Примерами адъювант-полимерных конструкций по изобретению являются конструкции формулыP-[S-A]n, где Р представляет собой полимер на основе мономерных единиц, выбранных из N-2 гидроксипропилметакриламида (НРМА), N-(2-гидроксиэтил)-1-глутамина (HEG) и этиленгликольолигопептида, или представляет собой полисиаловую кислоту или полиманнановый полимер; S представляет собой -Gly-Phe-Leu-Gly-, -Gly-Gly- или Glu-Lys-Glu-; n равно 3-10 и А представляет собой адъювант, как определено выше. Предусматриваются несколько разных подходов к синтезу конструкций по изобретению. 1. Сополимеризация простых мономеров с функционализированными мономерами для создания основной цепи полимера, имеющей реакционноспособные группы на подвешенных боковых цепях, с последующим присоединением адъювантов к этим реакционноспособным группам. 2. Функционализация адъювантов или адъювант-спейсерных молекул для включения полимеризуемых групп и добавление функционализированного адъюванта или адъювант-спейсера к полимеризационной смеси. 3. Адаптация природного или синтетического полимера посредством связывания адъювантов либо непосредственно, либо через спейсерную группу. В случае синтезированного полимера подходящие методы полимеризации включают методы свободнорадикальной полимеризации, такие как обычные и регулируемые способы, например NMP (нитроксид-опосредованная полимеризация), ATRP (радикальная полимеризация с переносом атома), RAFT(обратимый перенос цепи по механизму присоединение-фрагментация) или полимеризация на основе цианоксила, например, как описано в Scales, С.W.; Vasilieva, Y.A.; Convertine, A.J.; Lowe, A.В.; McCormick, С.L. Biomacromolecules 2005, 6, 1846-1850; Yanjarappa, M.J.; Gujraty, K.V.; Joshi, A.; Saraph, A.;McCormick, С.L. Biomacromolecules 2004, 5, 1177-1180, которые включены в данное описание изобретения во всей их полноте посредством ссылки. Циклические мономеры могут быть полимеризованы с использованием полимеризации с раскрытием кольца или реакции обмена с раскрытием кольца. Релевантные указания также можно найти в "Macromolecular design via reversible additionfragmentation chain transfer (RAFT)/xanthates (MADIX) polymerization" Perrier, Sebastien; Takolpuckdee,Pittaya. J. Polym. Sci., Part A: Polym. Chern. (2005), 43(22), 5347-5393, которая включена в данное описание изобретения посредством ссылки. Обычно в реакции сополимеризации используют инициатор, предпочтительно AIBN (,'азоизобутиронитрил). Взаимодействие, как правило, происходит в органическом растворителе, обычноDMSO. Реакционную смесь обычно нагревают до температуры от 50 до 70C, предпочтительно примерно 60C. Реакционную смесь обычно нагревают до вышеуказанной температуры в течение 4-8 ч, предпочтительно от 5 до 7 ч, более предпочтительно примерно 6 ч. Полученные таким образом полимеры обычно осаждают в смеси ацетон-диэтиловый эфир (3:1), отфильтровывают, промывают ацетоном и ди-5 021741 этиловым эфиром и сушат в вакууме. Полученные таким образом полимеры могут быть дополнительно очищены на колонках Sephadex-LH 20 с использованием метанола. Мономеры для реакции полимеризации обычно имеются в продаже или могут быть получены по аналогии известными способами, например, как описано в Konak, et al., Langmuir, 2008, 24, 7092-7098. Синтез (1), описанный выше, предполагает включение функционализированных мономеров в реакцию полимеризации. Такие функционализированные мономеры обычно имеют структуру PG-S-F илиPG-F, где PG представляет собой полимеризуемый мономер, такой как НРМА или метакриламид (подходящие мономеры также определены выше), S представляет собой спейсерную группу, как определено выше, и F представляет собой функциональную группу. При необходимости можно использовать смеси двух или более разных функционализированных мономеров. В этом случае полимеризационная смесь будет включать как нефункционализированные мономеры,так и функционализированные мономеры. Функционализированные мономеры обычно включены в полимерную цепь в количестве вплоть до примерно 20 мол.%, например вплоть до 10 мол.%. Предпочтительно функционализированный мономер включен в количестве по меньшей мере 2 мол.%, например по меньшей мере 5 мол.%. Подходящие функциональные группы F включают солюбилизирующие группы, такие как группы,описанные выше, и реакционноспособные группы. Также можно использовать защищенные группы, которые являются предшественниками таких солюбилизирующих или реакционноспособных групп. Следует понимать, что термин "реакционноспособная группа" используется в данном описании изобретения для обозначения группы, которая демонстрирует значительную химическую реакционную способность, особенно в отношении реакций сочетания или связывания с комплементарными реакционноспособными группами других молекул, обычно с группами на адъюванте. Реакционноспособные группы можно использовать в качестве точки присоединения адъюванта или вакцины или альтернативной функциональной группы, такой как солюбилизирующая группа. Например,реакционноспособная группа может быть способна образовать ковалентную связь, например, с аминогруппой, тиоловой группой, гидроксигруппой, альдегидом, кетоном, карбоновой кислотой или сахарной группой на адъюванте, вакцине или другой молекуле, содержащей альтернативную функциональную группу. В случае взаимодействия с адъювантом или вакциной эти адъювант или вакцина могут быть функционализированы, если это необходимо, с целью включения такой группы, способной образовывать ковалентную связь с реакционноспособной группой. В одном воплощении реакционноспособная группа способна образовывать ковалентную связь с аминогруппой. Примеры подходящих типов реакционноспособной группы в этом воплощении включают хлорангидриды кислот, изоцианаты, изотиоцианаты, ацил-тиазолидин-2-тионы, малеимиды, N-гидроксисукцинимидные сложные эфиры (NHS-сложные эфиры), сульфо-N-гидрокси-сукцинимидные сложные эфиры (сложные эфиры сульфо-NHS), 4-нитрофеноловые сложные эфиры, эпоксиды, 2-имино-2 метоксиэтил-1-тиогликозиды, хлорангидриды циануровой кислоты, имидазолилформиаты, сукцинимидилсукцинаты, сукцинимидилглутараты, ацилазиды, ацилнитрилы, дихлортриазины, 2,4,5-трихлорфенолы, азлактоны и хлорформиаты. Такие группы легко взаимодействуют с аминами. Ацилтиазолидин-2-тионы и сложные эфиры сульфо-NHS являются предпочтительными. Ацил-тиазолидин-2 тионы являются предпочтительными вследствие их высокой реакционной способности и относительной стабильности в водных растворах. В другом воплощении реакционноспособная группа способна образовывать ковалентную связь с тиоловой группой. Примеры подходящих типов реакционноспособных групп в данном воплощении включают алкилгалогениды, галогенацетамиды и малеимиды. В другом воплощении реакционноспособная группа способна образовывать ковалентную связь с гидроксильной группой. Примеры подходящих типов реакционнеспособной группы в данном воплощении включают хлорформиаты и галогенангидриды кислот. Альтернативно, гидроксильные группы могут быть окислены оксилителем, например периодатом, с последующим взаимодействием с реакционноспособными группами, которые включают гидразины, гидроксиламины или амины. В другом воплощении реакционноспособная группа способна образовывать ковалентную связь с альдегидной или кетонной группой. Примеры подходящих типов реакционноспособной группы в данном воплощении включают гидразиды, семикарбазиды, первичные алифатические амины, ароматические амины и карбогидразиды. В другом воплощении реакционноспособная группа способна образовывать ковалентную связь с карбоновой кислотой. Это может быть осуществлено, например, посредством активирования карбоновой кислоты с использованием водорастворимого карбодиимида, 1-этил-3-(3-диметиламинопропил)карбодиимида гидрохлорида с последующим взаимодействием с амином в качестве реакционноспособной группы. В другом воплощении реакционноспособная группа способна взаимодействовать с сахаром с образованием ковалентной связи. Это можно осуществлять, например, посредством опосредованного ферментом окисления сахара галактооксидазой с образованием альдегида с последующим взаимодействием с альдегидным реакционноспособным соединением, таким как гидразид, в качестве реакционноспособ-6 021741 ной группы. Предпочтительными примерами реакционноспособных групп являются сложные эфиры нитрофенола (ONp), N-гидроксисукцинимид (NHS), тиазолидин-2-тион (ТТ) и эпоксигруппы. После полимеризации реакционноспособные группы, включенные в полимер, могут непосредственно взаимодействовать с адъювантами или превращаться в другие функциональные группы, такие как солюбилизирующие группы. Альтернативно, реакционноспособные группы могут быть частично приведены во взаимодействие с молекулой, содержащей альтернативную реакционноспособную группу, что приводит к присутствию двух разных реакционноспособных функциональных групп. Эти реакционноспособные группы можно затем модифицировать, используя два независимых способа. Примеры подходящих полимеров, содержащих функционализированные подвешенные боковые цепи, раскрыты в WO 98/19710 и включают поли-НРМА-GlyPheLeuGly-ONp, поли-НРМА-GlyPheLeuGlyNHS, поли-НРМА-Gly-Gly-ONp, поли-НРМА-Gly-Gly-NHS, поли(pEG-олигопептид(-ONp, поли(pEGGluLysGlu(ONp, pHEG-ONp, pHEG-NHS. Получение этих соединений раскрыто в WO 98/19710. Содержание WO 98/19710 включено в данное описание изобретения посредством ссылки. Другой такой функционализированный полимер, подходящий для применения в изобретении, представляет собой поли-НРМА-GlyPheLeuOly-TT (где ТТ представляет собой тиазолидин-2-тион), синтез которого описан вWO 2005/007798. Содержание WO 2005/007798 включено в данное описание изобретения посредством ссылки. Альтернативные способы синтеза конструкций по изобретению включают функционализацию адъюванта для включения в полимеризационную смесь (синтез (2) выше). В этом воплощении полимеризацию обычно выполняют, как описано выше, но используя функционализированный мономер, имеющий структуру PG-S-A или PG-A, где PG и S такие, как определено выше, и А представляет собой адъювант. Можно использовать смеси двух или более таких функционализированных мономеров или смеси таких функционализированных мономеров с мономерами формулы PG-S-F или PG-F, как описано выше. Как описано выше, функционализированные мономеры включают в количестве вплоть до примерно 20 мол.%, например вплоть до 10 мол.%. Предпочтительно функционализированный мономер включают в количестве по меньшей мере 2 мол.%, например по меньшей мере 5 мол.%. В еще одном воплощении конструкцию по изобретению получают путем адаптирования ранее образованного полимера, такого как природный полимер (синтез (3) выше). В этом случае подходящие реакционноспособные группы на полимере используют для добавления адъювантов возможно с помощью спейсерной группы и любых дополнительных желательных функциональных групп, таких как солюбилизирующие группы. В одном воплощении изобретения основная цепь полимера содержит два или более разных адъювантов. В этом воплощении адъюванты могут быть расположены случайным образом или в конкретной последовательности. Например, полимер может содержать блок-сополимер структуры -А-В-А-В-, где А представляет собой сегмент полимера, имеющий одну или более подвешенных боковых цепей, включающих адъювант (а), и В представляет собой сегмент полимера, имеющий одну или более подвешенных боковых цепей, включающих адъювант (б). Такие подобранные последовательности адъювантов могут обеспечивать синергический эффект. В еще одном воплощении изобретения основная цепь полимера и/или спейсерные группы на подвешенных боковых цепях являются разлагаемыми. Разлагаемые связи могут, следовательно, присутствовать в основной цепи полимера и/или в одной или более подвешенных боковых цепях. Разлагаемые связи представляют собой связи, которые могут разрываться in vivo либо самопроизвольно, либо вследствие специально инициированного события. Обычно разлагаемыми связями сшивают для самопроизвольного гидролиза после эндосомального поглощения при понижении эндосомального рН, или они могут представлять собой связи, которые восстановительно расщепляют во внутриклеточной восстанавливающей среде. Альтернативно, разлагаемые связи могут быть предназначены для расщепления конкретными ферментами. Использование биоразлагаемых связей полезно для стимулирования разрушения конъюгата полимер-адъювант, ограничения его адъювантной активности и облегчения окончательного выведения, чтобы избежать нежелательной токсичности. Некоторые полимеры для применения в настоящем изобретении являются разлагаемыми по своей природе, например некоторые нуклеиновые кислоты. Альтернативно, разлагаемые связи могут быть включены в основную цепь полимера или в боковые цепи. Примеры таких разлагаемых связей включают дисульфидные связи, которые обычно расщепляют, используя мягкие восстанавливающие условия, такие как сульфит металла или соответствующим образом выбранный фермент; гидразоновые связи, цисаконитиловые связи и сложные орто-эфиры, которые расщепляют посредством рН-зависимого гидролиза; или связи, которые являются ферментативно расщепляемыми. Ферментативно расщепляемые связи предназначены для расщепления конкретными ферментами и обычно включают короткие олигопептиды, такие как олигопептиды, описанные в данном описании изобретения как спейсерные группы. Нестабильность, обусловленная ферментативной разлагаемостью, может быть желательной, так как это позволяет сконструировать полимер (или связь между полимером и адъювантом) для расщепления избирательно выбранными ферментами. Такие ферменты могут присутствовать в участке-мишени, обеспечивая модифицированному адъюванту возможность инициированного распада в участке-мишени, посредством чего высвобождается адъювант для взаимодействия с тканью-мишенью. Также ферменты могут представлять собой внутриклеточные ферменты, которые могут вызывать разрушение модифицированного адъюванта в выбранных клеточных компартментах клетки-мишени для усиления активности адъюванта. Альтернативно, участки расщепления ферментом могут быть сконструированы, чтобы способствовать разрушению модифицированного адъюванта в ответ на соответствующую биологическую активность (например, появление инвазивной или метастатической опухолевой клетки, экспрессирующей металлопротеиназу). В еще одном варианте ферменты, способные активировать модифицированный адъювант, можно вводить в соответствующее время или участок, чтобы опосредовать желательное разрушение модифицированного адъюванта и затем взаимодействие адъюванта с тканью. Адъювант-полимерные конструкции по изобретению подходят для введения человеку или млекопитающему в сочетании с вакциной для усиления или стимулирования иммунного ответа этого пациента на вакцину. Примеры подходящих вакцин, которые можно применять с настоящим изобретением, включают вирусы, белки, пептиды, сахара и нуклеиновые кислоты. Вакцины могут быть профилактическими (вводимыми для защиты реципиента от заболевания) или терапевтическими (для содействия иммунной системе в воздействии на существующую инфекцию или расстройство). В общем случае вакцины могут представлять собой неживые или инактивированные организмы, произведенные из них очищенные продукты, синтетические пептиды, рекомбинантные белки или нуклеиново-кислотные вакцины, которые кодируют компоненты организма-мишени. Некоторые вакцины содержат убитые микроорганизмы, которые представляют собой ранее вирулентные микроорганизмы, которые были убиты химическими веществами или теплом. Примерами являются вакцины против гриппа, холеры, бубонной чумы и гепатита А. Аттенуированные вакцины содержат живые аттенуированные вирусные микроорганизмы, которые представляют собой живые микроорганизмы, которые были спроектированы или культивировались в условиях, блокирующих их вирулентные свойства, или где используются близкородственные, но менее опасные организмы для продуцирования интенсивного иммунного ответа. Они обычно вызывают более стойкие иммунологические ответы и представляют собой предпочтительный тип для здоровых взрослых. Примеры включают желтую лихорадку, корь, краснуху и свинку. Живая туберкулезная вакцина представляет собой не инфекционный штамм, а родственный штамм, называемый "BCG"; его используют в Соединенных Штатах очень редко. Дополнительными примерами классов вакцин являются следующие. Токсоиды - инактивированные токсичные соединения в случаях, когда они (а не сам микроорганизм) вызывают заболевание. Примеры вакцин на основе токсоида включают столбнячную и дифтерийную вакцину. Не все токсоиды являются вакцинами против микроорганизмов; например токсоид Crotalisatrox используют для вакцинации собак против укусов гремучей змеи. Пептидные вакцины - синтетические пептиды, содержащие антигенные эпитопы белков заболевания, например пептид вируса гриппа М 2 е. В принципе любой пептид может быть включен в полимер,содержащий адъювант, или в единственном числе, или в многочисленных копиях (1-20). Предпочтительные пептиды не содержат критический лизиновый остаток в последовательности, отличный от того, который добавляют для облегчения конъюгирования с полимером. Для пептидов, содержащих лизиновые остатки в активном участке, можно использовать альтернативное конъюгирование посредством боковой цепи цистеиновых остатков. Субъединичные белковые вакцины - вместо введения инактивированного или аттенуированного микроорганизма в иммунную систему (которая составляет вакцину из "цельного агента"), фрагмент которой может генерировать иммунный ответ. Характерные примеры включают субъединичную вакцину против вируса гепатита В, которая состоит только из поверхностных белков вируса (продуцируемых в дрожжах), и вакцина, содержащая вирусоподобные частицы (VLP), против вируса папилломы человека(HPV), которая состоит из вирусного основного капсидного белка. Конъюгатные вакцины - некоторые бактерии имеют полисахаридные наружные оболочки, которые являются слабоиммуногенными. Посредством связывания этих наружных оболочек с белками (например, с токсинами) иммунная система может быть подведена к распознаванию полисахарида, как если бы это был белковый антиген. Этот подход используют в вакцине гемофильного гриппа В типа. Рекомбинантными вакцинами являются те, в которых вектор (иногда безвредный вирус, иногда плазмида) используют в качестве "троянского коня" для ввода и экспрессии генов, кодирующих компоненты патогена-мишени, в клетки реципиента, включая антиген-представляющие клетки, такие как дендритные клетки. Например, аттенуированные аденовирусные векторы можно использовать для экспрессии белков из патогенов-мишеней (например, компонентов малярии, туберкулеза, гриппа) в клеткаххозяевах, облегчая продуцирование иммунного ответа против целевого патогена, не подвергая реципиента воздействию какого-либо инфекционного вещества. Подобные подходы можно использовать для ряда вирусных векторов, особенно альфа-вируса. В одном воплощении вакцину конъюгируют с адъювант-полимерной конструкцией с образованием вакцинного конъюгата. Таким образом, можно конъюгировать очень широкий диапазон вакцин, включая пептидные, липидные, белковые, нуклеиново-кислотные вакцины, углеводные и синтетические вакцины,включая вакцины смешанного состава. Вакцины могут быть произведены из многих мишеней, включая вирусы, простейшие, нематоды, грибы, дрожжи или бактерии, или они могут быть предназначены для вакцинации против ассоциированных с раком антигенов. Связь между вакциной и полимерадъювантным конъюгатом может быть сконструирована для разрушения после объединения с клетками,для усиления клеточной миграции компонента вакцины. Такие биоразлагаемые связи могут представлять собой восстанавливаемые связи, гидролитически нестабильные связи и связи, которые являются субстратами для разрушения ассоциированными с мишенью ферментами. Ряд возможных вакцин включает, но, безусловно, не ограничивается следующими: пептиды гриппа и белки гриппа, например, используемые в стандартных гриппозных вакцинах,включающих Н- и N-белки и М 2,пептиды из HIV, включая эпитопы из gp120, gp41, gag, nef и pol,поверхностный антиген НерВ,раковые антигены, такие как СЕА, MUC-1 и 5 Т 4,белки, субъединицы и пептиды сибирской язвы,норовирусные белки и пептиды,токсоиды (см. выше),белки, субъединицы и пептидные антигены разных штаммов чумы (Yersinia pestis),белки и пептиды, произведенные из малярии, например антиген циркумспорозоита или синтетическая цепь TRAP-эпитопа,вирусы и вирусоподобные частицы (VLP), включая аденовирус, респираторно-синцитиальный вирус, альфавирус, вирус герпеса, вирус коровьей оспы, вирус кори, реовирус и лентивирусы. Конъюгирование полимер-адъювантной конструкции и вакцины достигается посредством получения одной или более реакционноспособных групп на полимер-адъювантной конструкции, которые способны связываться с группами на вакцине. Связывание может быть ковалентным или посредством другого типа взаимодействия, такого как электростатическое притяжение. Обычно получают более одной реакционноспособной группы, например по меньшей мере 5 реакционноспособных групп, так чтобы образовались несколько связей между вакциной и полимер-адъювантной конструкцией. В случае ковалентного связывания между полимер-адъювантной конструкцией и вакциной можно использовать реакционноспособные группы, подробно описанные выше. Точная природа реакционноспособной группы будет зависеть от доступных участков связывания на вакцине. Примеры предпочтительных реакционноспособных групп для использования с вирусными вакцинами, которые будут ковалентно связываться с участками на поверхности вируса, включают N-гидроксисукцинимид (NHS), сложный эфир нитрофенола (ONp) и тиазолидин-2-тионовые (ТТ) группы. В случае электростатического взаимодействия с вакциной заряженные группы могут быть включены в полимерную цепь, чтобы способствовать электростатическому притяжению к вакцине. В одном конкретном примере частица рекомбинантной вакцины на основе аденовирусного вектора,содержащего ДНК, кодирующую ген патогена-мишени, может быть покрыта по поверхности полимерадъювантным конъюгатом с целью увеличения ее способности стимулировать иммунный ответ после экспрессии патогенного белка в клетках реципиента. Для достижения этого полимер-адъювантный конъюгат синтезируют с совокупностью групп, которые могут связываться с поверхностью аденовирусного вектора, соединяя полимер с поверхностью и тем самым презентируя адъювант на поверхности вирусной частицы. В данном воплощении подходящие реакционноспособные группы представляют собой группы, способные образовывать ковалентную связь с вирусом (например, NHS, ONP, ТТ-группы) или заряженными группами. Участки связывания на вакцине могут быть естественного происхождения или могут быть включены. Когда участки связывания включены, они должны быть комплементарными реакционноспособным группам на полимер-адъювантной конструкции. Например, вирусный вектор может быть сконструирован для экспрессии конкретных реакционноспособных групп на ее поверхностных белках (например,свободных тиоловых групп) и соответствующую реакционную способность можно включать в полимерадъювантную конструкцию (например, малеимидные группы) для облегчения непосредственного ковалентного связывания с вирусной частицей. Когда и полимер-адъювантная конструкция, и вакцина имеют множество комплементарных реакционноспособных групп, возможно, что продукт их соединения может представлять собой агрегат или даже осадок. Несмотря на то что получение локального депо адъювантированной вакцины может быть полезным, эффект сшивания можно минимизировать, используя один из компонентов (как правило полимер-адъювантную конструкцию) в избытке. Альтернативно, полимер-адъювантную конструкцию можно получать только с одной остаточной реакционноспособной группой, обеспечивая одновалентное соединение с вакциной. В одном воплощении это может быть достигнуто путем создания полутелехелатного реакционноспособного полимера, где один конец каждой молекулы полимера дериватизи-9 021741 рован реакционноспособной группой и несколько адъювантов включены (в виде дериватизированных соомономеров) в полимерную цепь. Терминальную реакционноспособную группу выбирают так, чтобы она не взаимодействовала с адъювантами, но могла использоваться для соединения конъюгата с вакциной. В альтернативном воплощении вакцина и адъювант-полимерная конструкция присутствуют в одной композиции вместе с фармацевтически приемлемым носителем или разбавителем. В еще одном альтернативном воплощении вакцину и адъювант-полимерную конструкцию по отдельности готовят в виде препаратов с получением двух отдельных композиций. В этом последнем случае две композиции можно вводить пациенту одновременно или по отдельности. В настоящем изобретении, следовательно, предлагаются композиции, содержащие адъювантполимерную конструкцию или конъюгат вакцины по изобретению вместе с фармацевтически приемлемым носителем или разбавителем и возможно вместе с вакциной. Предпочтительные композиции не загрязнены микроорганизмами и пирогенами. Композиции по изобретению могут быть приготовлены в виде препарата для введения в разных лекарственных формах. Таким образом, их можно вводить перорально, например, в виде водных или масляных суспензий. Композиции по изобретению можно приготовить в виде препаратов для введения парентерально или подкожно, внутривенно, внутримышечно, интрастернально, внутрибрюшинно, внутрикожно, чрескожно или посредством инфузии. Кожное и внутримышечное введение является предпочтительным. Композиции по изобретению можно приготовить в виде препарата для введения ингаляцией в форме аэрозоля с помощью ингалятора или небулайзера. Композиции для перорального введения, например, могут содержать вместе с активными ингредиентами, упомянутыми выше, солюбилизирующие агенты, например циклодекстрины или модифицированные циклодекстрины; разбавители, например лактозу, декстрозу, сахарозу, целлюлозу, кукурузный крахмал или картофельный крахмал; смазывающие вещества, например диоксид кремния, тальк, стеариновую кислоту, стеарат магния или кальция и/или полиэтиленгликоли; связывающие агенты; например крахмалы, аравийские камеди, желатин, метилцеллюлозу, карбоксметилцеллюлозу или поливинилпирролидон; дезагрегирующие агенты, например крахмал, альгиновую кислоту, альгинаты или натрия крахмала гликолят; вспенивающие смеси; красители; подсластители; смачивающие агенты, такие как лецитин, полисорбаты, лаурилсульфаты; и, в общем случае, нетоксичные и фармакологически неактивные вещества, используемые в фармацевтических композициях. Жидкие дисперсии для перорального введения могут представлять собой растворы, сиропы, эмульсии и суспензии. Растворы могут содержать солюбилизирующие агенты, например циклодекстрины или модифицированные циклодекстрины. Сиропы могут содержать в качестве носителей, например, сахарозу или сахарозу с глицерином, и/или маннит, и/или сорбит. Суспензии и эмульсии могут содержать в качестве носителя, например, природную камедь, агар,альгинат натрия, пектин, метилцеллюлозу, карбоксметилцеллюлозу или поливиниловый спирт. Суспензии или растворы для внутримышечных инъекций могут содержать вместе с активным соединением фармацевтически приемлемый носитель, например стерильную воду, оливковое масло, этилолеат, гликоли, например пропиленгликоль; солюбилизирующие агенты, например циклодекстрины или модифицированные циклодекстрины и, при необходимости, подходящее количество лидокаина гидрохлорида. Растворы для внутривенного введения или вливаний могут содержать в качестве носителя, например, стерильную воду и солюбилизирующие агенты, например циклодекстрины или модифицированные циклодекстрины, или предпочтительно они могут находиться в форме стерильных водных изотонических растворов. Терапевтически эффективное количество адъювант-полимерной конструкции по изобретению вводят человеку. Мультивалентный дисплей адъюванта позволяет применять более низкие концентрации адъюванта, чем было предложено ранее для несвязанных с полимером адъювантов. Количество введенного адъюванта, следовательно, равно или предпочтительно меньше дозировки для соответствующей композиции с использованием того же самого адъюванта, но не связанного с полимером. Адъювантполимерную конструкцию по изобретению обычно вводят человеку в нетоксичном количестве. Вакцину также вводят в терапевтически эффективном и нетоксичном количестве. Полимер-адъювантные конструкции по изобретению полезны в усилении и стимулировании иммунного ответа в широком диапазоне различных областей медицины. Следовательно, изобретение полезно для лечения или профилактики инфекционных заболеваний, раковых заболеваний и аутоиммунных заболеваний и для лечения аллергии и повышенной чувствительности. Примеры инфекционных заболеваний включают заболевания, вызванные агентом, выбранным из группы, состоящей из вируса, бактерии, паразита и гриба. Вирусное инфекционное заболевание может представлять собой сезонный грипп, птичий грипп, респираторно-синцитиальный вирус, вирус папилломы человека, вирус гепатита, ВИЧ/СПИД, простой герпес, ветряную оспу, цитомегаловирус, лихорадку Денге, геморрагическую лихорадку Эбола, вирусную пузырчатку полости рта и конечностей, лихорадку Ласса, корь, марбургскую геморрагическую лихорадку, инфекционный мононуклеоз, вирус Эпштейн-Барра, свинку, норовирус, полиомиелит, бешенство,- 10021741 краснуху, САРС (тяжелый острый респираторный синдром), оспу (Variola), заболевание Западного Нила,желтую лихорадку, ротавирус, японский энцефалит, колорадскую клещевую лихорадку, обычную простуду, вирусный энцефалит, вирусный гастроэнтерит, вирусный менингит или вирусную пневмонию. Бактериальное инфекционное заболевание может представлять собой бактериальный менингит,Staphylococcus aureus (включая MRSA (метициллин-резистентный Staphylococcus aureus), сальмонеллез,шигеллез, кампилобациллярный энтерит, хламидиоз, болезнь Лайма, пневмококковую пневмонию, сибирскую язву, ботулизм, бруцеллез, трахому, туберкулез, заболевание от кошачьих царапин, холеру,дифтерию, эпидемический сыпной тиф, гонорею, импетиго, болезнь легионеров, проказу, лептоспироз,листериоз, мелиоидоз, нокардиоз, коклюш, чуму, пситтакоз, ку-лихорадку, пятнистую лихорадку Скалистых гор, скарлатину, сифилис, столбняк, туляремию, брюшной тиф, сыпной тиф, бактериальную инфекцию мочевых путей, Chlamydia trachomatis, Heliobacter pylori. Паразитарные инфекции могут представлять собой малярию, трипаносомоз, шистосомоз, цистицеркоз, болезнь Шагаса, лямблиоз, кала-азар, лейшманиоз, филяриоз, амебиоз, аскаридоз, бабезиоз, клонорхоз, криптоспоридиоз, дифиллоботриоз, дракункулез, эхинококкоз, энтеробиоз, фасциолез, фасциолопсидоз, свободно живущую амебную инфекцию, гнатостомиоз, гименолипедоз, изоспороз, метагонимиоз,миаз, онхоцеркоз, педикулез, энтеробиоз, чесотку, тениоз, токсокароз, токсоплазмоз, трихинеллез, трихиноз, трихуроз, трихомоноз. Грибковое инфекционное заболевание может представлять собой кандидоз, аспергиллез, бластомикоз, кокцидиоидомикоз, криптококкоз, гистоплазмоз, трихофитию стопы. Примеры раковых заболеваний включают колоректальный рак, немелкоклеточный рак легкого, рак предстательной железы, рак молочной железы, рак поджелудочной железы, рак яичников, рак печени,рак кожи, меланому, рак желудка, мелкоклеточный рак легкого, саркому, рак мочевого пузыря, рак пищевода, рак шейки матки, рак эндометрия, рак яичка, почечно-клеточный рак, рак носоглотки, рак головы и шеи, рак щитовидной железы, глиому, астроцитому, лимфому, лейкемию, миелопролиферативное расстройство, ретинобластому, эмбриому или метастатический рак. Примеры аутоиммунных заболеваний включают ревматоидный артрит, сахарный диабет, рассеянный склероз, псориаз, болезнь Крона, анкилозирующий спондилит, болезнь Грейвса, тиреоидит Хашимото, идиопатическую микседему, синдром Гийена-Барре, системную красную волчанку, иммунную тромбоцитопеническую пурпуру, обыкновенную пузырчатку, фибромиалгию, миастению, саркоидоз,синдром Шегрена, болезнь Кавасаки, болезнь Лу Герига, демиелинизирующее заболевание, гемолитическую анемию, аутоиммунный артериит, аутоиммунный колит, аутоиммунный увеит, аутоиммунный миозит, аутоиммунный артрит и аутоиммунный гепатит. Примеры Пример 1. Синтез соединений для связывания с растворимыми полимерами для применения в качестве полимерных усиленных адъювантов. Синтез N-Pam3Cys-(N'-трет-бутилоксикарбонил-2,2'-(этилендиокси)диэтиламина) (1)Pam3Cys модифицировали посредством карбодиимидного сочетания с моно-Вос-защищенным диамином. Pam3Cys-OH (95 мг, 104 мкмоль) растворяли в безводном DCM (5 мл), добавляли к PSкарбодиимидной смоле (1,33 ммоль/г, 138 мг, 185 мкмоль) и встряхивали в течение 5 мин в атмосфереAr. Добавляли N-Вос-2,2'-(этилендиокси)диэтиламин) (33 мг, 132 мкмоль) в безводном DCM (1 мл) и встряхивание продолжали в течение 16 ч. ТСХ (тонкослойная хроматография) (чистый EtOAc) не обнаружила остаточного Pam3Cys-OH. Смолу удаляли фильтрованием и добавляли 50 мг PS-бензальдегидной смолы в качестве аминопоглотителя. Через 24 ч встряхивания раствор фильтровали и растворитель удаляли при пониженном давлении. Неочищенное твердое вещество очищали колоночной хроматографией(градиент элюирования 0-20% МеОН в DCM, Rf (фактор удерживания) продукта 0,6) и выделяли в виде белого твердого вещества.DCM/TFA (4 мл) и осторожно перемешивали в течение 1 ч. Растворитель и избыток кислоты удаляли посредством азеотропной перегонки с толуолом и затем с диэтиловым эфиром. Полученное белое твердое вещество растворяли в смеси DCM и насыщенного водного NaHCO3 и интенсивно перемешивали в течение 2 ч. Органический слой собирали и водный слой экстрагировали DCM (210 мл). Экстракты объединяли, сушили над MgSO4 и упаривали с получением 53 мг белого твердого вещества. MS (ESI+) обнаружено m/z 1041,8 [М+Н+], требуется 1040,8. Синтез церамидного аналога (3). Церамидный аналог получали согласно схеме, представленной на фиг. 1. Пример 2. Получение адъюванта, конъюгированного с полимером. Гидрофильные полимеры, такие как поли[N-(2-гидроксипропил)метакриламид], несущий множество подвешенных амино-, гидроксильных или тиоловых реакционноспособных групп, можно модифицировать, чтобы они несли иммуностимулирующие молекулы, такие как N-Pam3Cys-(2,2'(этилендиокси)диэтиламин) (2) или церамидные аналоги, такие как (3). В данном примере описан синтез поли[НРМА][МА-GG-ТТ] и его конъюгирование с церамидным аналогом (3). Синтез мультивалентного аминореакционного гидрофильного сополимера. Синтез поли[N-(2-гидроксипропил)метакриламид-3-(N-метакрилоилглицилглицил)тиазолидин-2 тиона]. НРМА (1,00 г, 6,99 ммоль), MA-GG-TT (N-метакрилоилглицилглицилтиазолидин-2-тион) (234 мг,0,77 ммоль) и AIBN (200 мг, 1,21 ммоль) растворяли в безводном DMSO до итогового объема 10 мл(приблизительно 12,5 мас.% мономера). Раствор деаэрировали посредством барботирования Ar в течение 20 мин, после чего колбу герметично закрывали и помещали в масляную баню при 60C с осторожным перемешиванием в течение 6 ч. После этого полимер осаждали путем добавления раствора по каплям в безводную смесь ацетон/эфир (3/1). Порошок отделяли центрифугированием (15 мин при 3000 об/мин),повторно суспендировали в смеси ацетон/эфир, центрифугировали и затем сушили под вакуумом. Содержание ТТ измеряли спектроскопией в ультрафиолетовой и видимой областях спектра в МеОН. Конъюгирование аминонесущего адъюванта с мультивалентным аминореакционным сополимером. Ковалентное конъюгирование адъюванта с сополимером выполняли путем смешивания в безводном диметилсульфоксиде. Затем полимерный конъюгат осаждали и сушили. Избыток реакционноспособных групп удаляли гидролизом и полимерный конъюгат очищали диализом и лиофилизировали. Структура полученного конъюгата изображена на фиг. 2. Пример 3. Соединение адъюванта, связанного с полимером, с вакциной. В данном примере связанное с полимером церамидное производное соединяют с AMSTTDLEA,пептидом, производным белка X вируса гепатита В и, как известно, распознаваемым цитотоксическими Т-лимфоцитами. Церамид-полимерный конъюгат синтезировали, как описано в предыдущем примере, за исключением того, что условия реакции и относительные концентрации реагентов оптимизировали путем сравнения влияния времени взаимодействия, температуры и концентрации реагентов, чтобы сохранять приблизительно 1 мол.% свободных реакционноспособных групп на полимерах во время осаждения. Это вещество сушили и хранили. Олигопептид со структурой GGGAMSTTDLEA с блокированным карбоксильным концом и свободным аминным концом получали путем отщепления от твердофазной смолы. Олигопептид растворяли вDMF и оставляли взаимодействовать до окончания с полимер-церамидным конъюгатом, несущим 1 мол.% реакционноспособных групп ТТ. Затем этот агент осаждали, диализовали и хранили при -20. Пример 4. Соединение положительно заряженного полимера с церамидным адъювантом и с олигопептидной вакциной с помощью биоразлагаемых связей. В данном примере сополимеры на основе N-(2-гидроксипропил)метакриламида (НРМА) содержат мономеры, несущие четвертичные аммониевые группы (1,5 мол.% в полимеризационной смеси) и несущие дисульфид боковые цепи, оканчивающиеся тиазолидиновыми группами (3,4 мол.% в продукте для взаимодействия с первичными аминами в адъюванте и также в вакцине). Структура реакционноспособного полимера показана на фиг. 3 а. Реакционноспособный полимер синтезировали и характеризовали, как описано в других местах(Subr V., Kostka L., Selby-Milic T., Fisher K., Ulbrich K., et al. (2009) Покрытие аденовируса 5 типа полимерами, содержащими четвертичные амины, предупреждает связывание с компонентами крови; J. Control Release 135: 152-158). Он имел средневзвешенную молекулярную массу 77200 и среднечисловую молекулярную массу 32200. Церамид соединяли, как описано выше, с 1 мол.% тиазолидиновых групп, остающихся непрореагировавшими, обеспечивая возможность последующего ковалентного связывания пептидного антигена. В данном примере пептидный антиген происходил из антигена X вируса гепатита, и он имел структуру:GGGAMSTTDLEA с блокированным карбоксильным концом и свободным аминоконцом (см. фиг. 3 б). Пример 5. Получение адъюванта, связанного с наногелем. Частицы наногелевых ядер синтезировали посредством свободнорадикальной полимеризации осаждением, как сообщалось ранее (Blackburn et al., Colloid Polym Sci. 2008; 286(5): 563-569). Применение полимеров с термическим разделением фаз делает возможным применение полимеризации осаждением для синтеза высокомонодисперсных наногелей. Молярная композиция представляла собой 98% Nизопропилметакриламида (NIPMAm), 2% N,N'-метиленбис(акриламид)а (BIS) с суммарной концентрацией мономера 140 мМ. Раствор также содержал небольшое количество (примерно 0,1 мМ) акриламидофлуоресцеина (AFA), чтобы сделать наногели флуоресцентными для визуализации с помощью конфокальной микроскопии. В типичном синтезе 100 мл отфильтрованного водного раствора NIPMAm, BIS и додецилсульфата натрия (SDS, общая концентрации 8 мМ) добавляли в реакционную колбу, которую затем нагревали до 70C. Раствор продували газообразным N2 и интенсивно перемешивали до тех пор,пока температура не оставалась стабильной. Добавляли AFA и через 10 мин взаимодействие инициировали добавлением 1 мл раствора 800 мМ персульфата аммония (APS) для получения конечной концентрации APS в реакционной смеси 8 мМ. Раствор становился мутным, что указывало на успешное инициирование. Реакции позволяли продолжаться в течение 4 ч в атмосфере N2. После синтеза раствор фильтровали через фильтровальную бумагу Whatman для удаления небольшого количества коагулята. 10 мл раствора ядер наногеля и 0,0577 г SDS сначала добавляли в трехгорлую круглодонную колбу и нагревали в атмосфере газообразного N2 до 70C. Получали 50 мМ раствор мономера с молярными отношениями 97,5% NIPMAm, 2% BIS и 0,5% N-глицилметакриламида в 39,5 мл dH20. Раствор добавляли в трехгорлую круглодонную колбу и температуру стабилизировали при 70C при постоянном перемешивании. Взаимодействие инициировали с помощью 0,5 мл аликвоты 0,05 М APS. Взаимодействие продолжалось в течение 4 ч в атмосфере газообразного N2. После синтеза раствор фильтровали через фильтровальную бумагу Whatman и наногели очищали центрифугированием с последующим ресуспендированием в dH20. Конъюгиоование аминосвязанного адъюванта с ядром наногеля. Наногели, функционализированные кислотой, конъюгировали с несущим аминогруппы адъювантом сначала посредством активирования кислотной функциональной группы N-гидроксисукцинимидом,используя дициклогексилкарбодиимид. После очистки добавление несущего аминогруппы адъюванта вызывает взаимодействие непосредственно с поверхностью наногеля. Пример 6. Оценка активности in vitro с использованием NfkB-люциферазных репортерных клетокTLR2-агониста Pam3Cys, конъюгированного с НРМА-сополимерами. Адъювантную активность конъюгата полимер-Pam3Cys оценивали in vitro, используя клетки ТНР 1, трансфицированные плазмидой, содержащей люциферазу под контролем NfkB-промотора (U937-luc). Клетки U937-luc выращивали до плотности 1 е 6 на 1 мл, затем воздействовали 100 нг/мл LPS, 100 нг/млPam3Cys, 100 нг/мл рНРМА или 100 нг/мл pHPMA-Pam3Cys. Через 8 ч клетки осаждали, лизировали и оценивали в отношении экспрессии люциферазы (фиг. 4). В данном исследовании используемый НРМАсополимер имел среднюю молекулярную массу приблизительно 20 кДа и содержал 5,22 мас.% Pam3cys(GCMS). НРМА связывали с Pam3cys посредством глицин-глицинового спейсера. Связанный с полимером адъювант получали в соответствии с методиками, описанными в примерах 1 и 2. Данные показывают, что люциферазный сигнал от 100 нг Pam3Cys-HPMA был в 24,1 раза выше сигнала от одногоPam3Cys, хотя только 5,22 нг данного вещества представляли собой Pam3Cys. Удельная активностьPam3Cys на молекулу, представленную полимером, в 24,119,2 = 462 раз выше. Пример 7. Оценка активности in vitro TLR2-агониста Pam2Cys, конъюгированного с НРМА, с использованием дендритных клеток костного мозга (BMDC) мышей. Известно, что BMDC откликаются на TLR2-агонисты, что приводит к экспрессии воспалительных цитокинов, включая IL-8. Авторы изобретения использовали данную модель для демонстрации эффективности Pam2Cys, соединенного с НРМА. В данном примере полимер имел массу приблизительно 80 кДа и был получен с 5 мас.%. Pam2Cys. НРМА связывали с Pam2Cys посредством глицинглицинового спейсера. Адъювант, связанный с полимером, получали в соответствии с методиками, описанными в примерах 1 и 2. На BMDC воздействовали 50 нг/мл Pam2Cys или Pam2Cys, связанным с полимером, в течение 24 ч. После этого супернатант собирали и определяли экспрессию IL-8 при помощиELISA. На фиг. 5 показано, что множественная презентация Pam2Cys на НРМА приводит к более высоким уровням активации дендритных клеток и в 20 раз более низкому количеству лиганда относительно Пример 8. Вакцинный конъюгат, состоящий из антигенного пептида (грипп М 2 е) и агониста TLR(Pam3Cys), экспонированного вдоль основной цепи полимера (НРМА). Пептид вируса гриппа М 2 е (SLLTEVETPIRNEWGCRCNDSSD) представляет собой поверхностный антиген, высококонсервативный в разных штаммах вируса. Несмотря на то что сам по себе М 2 е является слабо иммуногенным, его часто вводят совместно с адъювантами. В данном примере мультивалентный поли-НРМА, несущий 5 мас.%. Pam3cys и 1 мол.% свободных реакционноспособных ТТ-групп на подвешенных GSGS-боковых цепях взаимодействовал до завершения (в DMSO) со свободным аминоконцом олигопептида. Свободный олигопептид удаляли посредством колоночной хроматографии. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Адъювант-полимерная конструкция, содержащая синтетическую линейную основную цепь полимера, которая является биологически неактивной; и 3 или более адъювантов, ковалентно связанных с основной цепью полимера либо непосредственно,либо с помощью спейсерной группы, где 3 или более адъювантов являются одинаковыми или разными и каждый присутствует в подвешенной боковой цепи,где основная цепь полимера образована из мономерных звеньев, выбранных из (мет)акрилатов,(мет)акриламидов, стирольных мономеров, виниловых мономеров, простого винилового эфира, сложного винилового эфира, сиаловой кислоты, маннозы, N-(2-гидроксиэтил)-1-глутамина (HEG) и этиленгликоль-олигопептида; где адъюванты выбраны из липогликанов, липополисахарида, липотейхоевой кислоты, пептидогликана, синтетических липопротеинов, зимозана, гликолипидов, полиинозин-полицитидиловой кислоты,монофосфориллипида А, флагеллина, имидазохинолиновых соединений, гуанозина, TNF-альфа (фактор некроза опухоли альфа) или его пептидов, IL-2, IL-4, IL-8, CD40, ОХ 40, GM-CSF и CpG-содержащих последовательностей в бактериальной ДНК или синтетических олигонуклеотидах; где спейсерные группы являются одинаковыми или разными и каждая выбрана из олиго(алкилоксид)ов, олигопептидов, С 1-С 12-алкильных группировок, С 6-С 10-арильных группировок, комбинаций таких алкильных и арильных группировок, сложных полиэфиров и поликарбонатов. 2. Адъювант-полимерная конструкция по п.1, где средневесовая молекулярная масса полимера находится в диапазоне от 1 до 100 кДа. 3. Адъювант-полимерная конструкция по п.1 или 2, где основная цепь полимера является, по меньшей мере частично, водорастворимой. 4. Адъювант-полимерная конструкция по любому из пп.1-3, где основная цепь полимера образована из мономерных звеньев, выбранных из N-2-гидроксипропилметакриламида (НРМА), N-(2-гидроксиэтил)1-глутамина (HEG) и этиленгликоля, или представляет собой полисиаловую кислоту или полиманнановый полимер. 5. Адъювант-полимерная конструкция по любому из пп.1-4, где адъюванты связывают Tollподобные рецепторы. 6. Адъювант-полимерная конструкция по любому из пп.1-5, где основная цепь полимера и/или спейсерная(ые) группа(ы) содержат разлагаемые связи. 7. Адъювант-полимерная конструкция по любому из пп.1-6, где средневесовая молекулярная масса полимера составляет от 5 до 40 кДа. 8. Адъювант-полимерная конструкция по любому из пп.1-7, где основная цепь полимера ковалентно связана с 10-50 адъювантами либо непосредственно, либо посредством спейсерной группы. 9. Адъювант-полимерная конструкция по любому из пп.1-8, связанная с вакциной с образованием вакцинного конъюгата. 10. Композиция, содержащая адъювант-полимерную конструкцию по любому из пп.1-9 и фармацевтически приемлемый носитель или разбавитель. 11. Композиция по п.10, которая дополнительно содержит вакцину. 12. Способ стимулирования или усиления иммунного ответа у человека, включающий введение указанному человеку эффективного, нетоксичного количества адъювант-полимерной конструкции по любому из пп.1-9 или композиции по п.10 или 11, где при введении адъювант-полимерной конструкции по любому из пп.1-8 или композиции по п.10 дополнительно проводят стадию введения пациенту эффективного и нетоксичного количества вакцины. 13. Применение адъювант-полимерной конструкции по любому из пп.1-9 в способе стимулирования или усиления иммунного ответа. 14. Применение по п.13, где адъювант-полимерная конструкция по любому из пп.1-8 применяется при дополнительном введении вакцины. 15. Применение композиции по п.10 или 11 в способе стимулирования или усиления иммунного ответа. 16. Применение по п.15, где композиция по п.10 применяется при дополнительном введении вакцины.
МПК / Метки
МПК: A61P 37/04, A61K 47/48
Метки: адъювантная, мультивалентная, конструкция
Код ссылки
<a href="https://eas.patents.su/17-21741-multivalentnaya-adyuvantnaya-konstrukciya.html" rel="bookmark" title="База патентов Евразийского Союза">Мультивалентная адъювантная конструкция</a>
Предыдущий патент: Производные пиразола, используемые в качестве антагонистов рецептора ccr4
Следующий патент: Способ очистки твердых поверхностей
Случайный патент: Способ литья, узел верхней литейной полуформы и способ крепления стержня к верхней литейной полуформе