Производные аминоарилпиразинов и их применение
Номер патента: 2102
Опубликовано: 24.12.2001
Авторы: Эдни Дин Дейвид, Кокс Брайан, Ша Джайта Панджэбхэй, Лофт Майкл Саймон, Ноббс Малком Стюарт
Формула / Реферат
1. Соединение формулы (I)
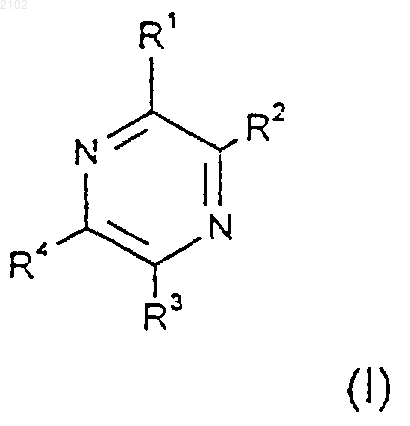
где R1 выбран из группы, состоящей из фенила, замещенного одним или более чем одним атомом галогена, нафтила и нафтила, замещенного одним или более чем одним атомом галогена;
R2 выбран из группы, состоящей из -NH2 и -NHC(=O)Ra;
R3 выбран из группы, состоящей из NRbRc, -NНС(=O)Ra и водорода;
R4 выбран из группы, состоящей из водорода, -С1-4алкила, -С1-4алкила, замещенного одним или более чем одним атомом галогена, -CN, -СН2ОН, -CH2ORd и -CH2S(O)xRd;
где Ra представляет собой С1-4алкил или С3-7 циклоалкил, а
Rb и Rc, которые могут быть одинаковыми или разными, выбраны из водорода и С1-4алкила, или, вместе с атомом азота, к которому они присоединены, образуют 6-членный азотсодержащий гетероцикл, причем этот гетероцикл может быть далее замещен одним или более чем одним С1-4алкилом;
Rd выбран из С1-4алкила или С1-4алкила, замещенного одним или более чем одним атомом галогена;
х представляет собой целое число ноль, один или два;
и его фармацевтически приемлемые производные;
при условии, что R1 не представляет собой
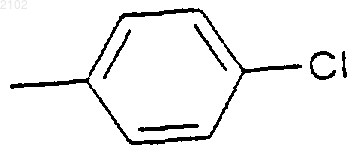
когда R2 представляет собой -NH2, a R3 и R4 оба представляют собой водород.
2. Соединение по п.1, где R1 представляет собой фенил, замещенный одним или более чем одним атомом галогена.
3. Соединение по п.2, где R1 представляет собой 2,3,5-трихлорфенил.
4. Соединение по любому из пп.1-3, где R2 и R3 представляют собой -NH2.
5. Соединение по любому из пп.1-4, где R4 представляет собой водород или -СН2OН.
6. Соединение по п.5, где R4 представляет собой водород.
7. Соединение, которое представляет собой 2,6-диамино-3-(2,3,5-трихлорфенил)пиразин и его фармацевтически приемлемые производные.
8. Применение соединения по любому из пп.1-7 в терапии.
9. Фармацевтическая композиция, содержащая соединение по любому из пп.1-7 вместе с фармацевтически приемлемым носителем.
10. Применение соединения по любому из пп.1-7 в изготовлении лекарства для использования в лечении эпилепсии, биполярного расстройства или маниакальной депрессии, боли, нейродегенеративных заболеваний, в нейрозащите, в лечении нейродегенерации, или в предотвращении или уменьшении зависимости от вызывающего зависимость агента, или в предотвращении или уменьшении толерантности или обратной толерантности к вызывающему зависимость агенту.
11. Способ лечения пациента при необходимости нейрозащиты, или страдающего эпилепсией, биполярным расстройством или маниакальной депрессией, болью, нейродегенеративными заболеваниями, нейрозащитой, нейродегенерацией или восприимчивого к ним, или зависимого от вызывающего зависимость агента, или обладающего толерантностью или обратной толерантностью к вызывающему зависимость агенту, при котором вводят эффективное количество соединения по любому из пп.1-7.
12. Способ получения соединения формулы (I), как определено в п.1, при котором соединение формулы (II)
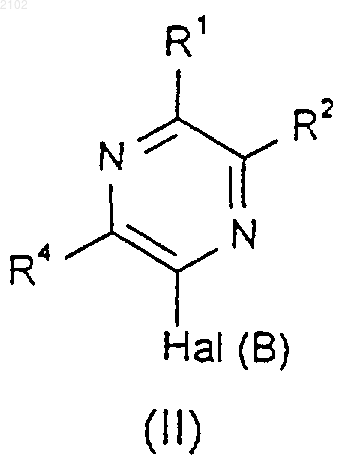
где Hal (В) представляет собой атом галогена, подвергают соответствующим реакционным условиям;
при этом соединения формулы (I) могут быть превращены в соответствующие соединения формулы (I) с использованием подходящих реакционных методик.
13. Способ получения соединения формулы (I), как определено в п. 1, при котором соединение формулы (VII)

где Hal представляет собой атом галогена, подвергают взаимодействию с соединением формулы (IV) R1B(OH)2;
при этом соединения формулы (I) могут быть превращены в соответствующие соединения формулы (I) с использованием подходящих реакционных методик.
14. Способ получения соединения формулы (I), как определено в п. 1, при котором, если R2 представляет собой NН2, то соединение формулы (XI)
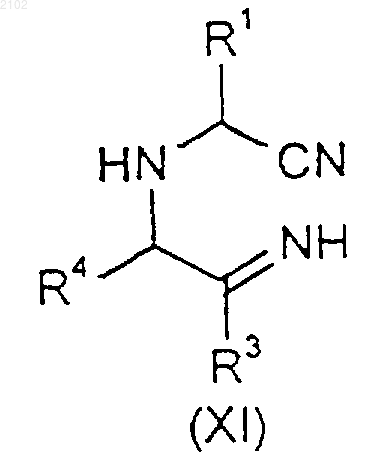
или его соль подвергают циклизации и окислению согласно общепринятым методикам;
при этом соединения формулы (I) могут быть превращены в соответствующие соединения формулы (I) с использованием подходящих реакционных методик.
Текст
1 Настоящее изобретение относится к классу соединений пиразина, которые полезны при лечении заболеваний и расстройств центральной нервной системы (ЦНС), к их фармацевтически приемлемым производным, к содержащим их фармацевтическим композициям, к их использованию в лечении таких расстройств и к способам их получения. Из уровня техники известны многочисленные фенильные производные пиразина. Например, известны (Synthesis, 1987 (10), 914-915) фенильные производные пиразина, которые включают в себя, среди прочих, 3-(4 хлорфенил)-пиразинамин. Однако в этом источнике фармацевтическое использование не описано. Настоящее изобретение относится к ряду производных пиразина, которые являются блокаторами натриевого канала. Эти соединения являются, в частности, хорошими противосудорожными средствами и по существу полезны при лечении заболеваний ЦНС. Согласно настоящему изобретению предложено соединение формулы (I)R1 выбран из группы, состоящей из фенила, замещенного одним или более чем одним атомом галогена, нафтила и нафтила, замещенного одним или более чем одним атомом галогена;R4 выбран из группы, состоящей из водорода, -С 1-4 алкила (предпочтительно метила),-С 1-4 алкила (предпочтительно метила), замещенного одним или более чем одним атомом галогена, -CN, -CH2OH, -CH2ORd и -СН 2S(O)хRd; гдеRb и Rс, которые могут быть одинаковыми или разными, выбраны из водорода и С 1-4 алкила, или, вместе с атомом азота, к которому они присоединены, образуют 6-членный азотсодержащий гетероцикл, причем этот гетероцикл может быть далее замещен одним или более чем одним C1-4 алкилом;Rd выбран из С 1-4 алкила или С 1-4 алкила,замещенного одним или более чем одним атомом галогена; х представляет собой целое число ноль,один или два; и его фармацевтически приемлемые производные; 2 при условии, что R1 не представляет собой когда R2 представляет собой -NН 2, а R3 и R4 оба представляют собой водород. Под фармацевтически приемлемым производным подразумевается любая фармацевтически приемлемая соль или сольват соединений формулы (I), или любое другое соединение, которое при введении реципиенту способно давать(прямо или косвенно) соединение формулы (I),или его активный метаболит, или остаток (например пролекарство). В дальнейшем ссылка на соединения формулы (I) включает в себя соединение формулы (I) и его фармацевтически приемлемые производные. Подходящие пролекарства хорошо известны из уровня техники и включают в себя Nацильные производные, например по любому из атомов азота в соединениях формулы (I), например простые ацильные производные, такие как ацетил, пропионил и тому подобное, или группы, такие как R-O-СН 2-азот или R-O-С(O)азот. Термин "атом галогена", как он используется здесь, включает в себя фтор, хлор, бром или иод. Термин "С 1-4 алкил", как он используется здесь, включает в себя алкильные группы с прямой и разветвленной цепью, содержащие от 1 до 4 атомов углерода, и в частности включает в себя метил и изопропил. Термин "С 3-7 циклоалкил" включает в себя группы, содержащие от 3 до 7 атомов углерода,и в частности включает в себя циклопропил. Термин "гетероцикл", как он используется здесь, включает в себя 6-членные гетероциклы,содержащие, по меньшей мере, один гетероатом азота, а предпочтительно два гетероатома азота. Особенно подходящим гетероциклом является пиперазинил. Подходящий R1 выбран из незамещенного нафтила и фенила, замещенного одним или более чем одним атомом галогена. В частности, R1 представляет собой фенил, замещенный более чем одним атомом галогена, такой как ди- или тригалогенированный фенил. Предпочтительно галогеновый заместитель в R1 представляет собой хлоро. Соответствующий R1 выбран из 2,3,5-трихлорфенила, 2,3-дихлорфенила, 2,5 дихлорфенила, 1-нафтила и 2-нафтила. В частности, R1 представляет собой 2,3,5-трихлорфенил. Подходящий R2 выбран из -NH2, изопропилкарбониламино и циклопропилкарбониламино. R2 предпочтительно представляет собой -NH2. Подходящий R3 выбран из водорода, -NH2,диметиламино, 4-метил-1-пиперазинила, ацетамидо, изопропилкарбониламино, циклопропилкарбониламино. R3 предпочтительно представляет собой -NH2.-СН 2 OН или, более предпочтительно, водород. Более предпочтительно, R2 и R3 оба представляют собой -NH2. Предпочтительный класс соединений формулы (I) включает в себя соединения, в которых(предпочтительно метила), замещенного одним или более чем одним атомом галогена. Предпочтительное соединение формулы (I) представляет собой соединение, гдеR4 представляет собой водород. Согласно конкретному воплощению настоящего изобретения предложено соединение формулы (Ia) где Hal представляет собой атом галогена, выбранный из фтора, хлора, брома и йода;R4 выбран из группы, состоящей из водорода, -С 1-4 алкила (предпочтительно метила),-С 1-4 алкила (предпочтительно метила), замещенного одним или более чем одним атомом галогена, -CN, -СН 2 ОН, -СН 2 ОRd и -СН 2S(O)хRd; гдеRa представляет собой С 1-4 алкил или С 3-7 циклоалкил, а Rb и Rc, которые могут быть одинаковыми или разными, выбраны из водорода и С 1-4 алкила, или вместе с атомом азота, к которому они присоединены, образуют 6-членный азотсодержащий гетероцикл, причем этот гетероцикл может быть дополнительно замещен одним или более чем одним С 1-4 алкилом;Rd выбран из С 1-4 алкила или С 1-4 алкила,замещенного одним или более чем одним атомом галогена; х представляет собой целое число ноль,один или два; и его фармацевтически приемлемые производные; Понятно, что R2, R3 и R4, как они определены выше для формулы (Ia), по существу та 002102 4 кие, как описано выше в отношении формулыR оба представляют собой -NH2. ПодходящийR4 представляет собой -CN, метил, или более подходит -СН 2OН, или еще более подходит водород. Подходящий Hal в формуле (Ia) представляет собой хлор. Подходящее n равно 3, и, соответственно, полученное тризамещенное соединение представляет собой соединение следующей формулы (Ib) где R2, R3 и R4 по существу такие, как описано выше в отношении формулы (Ia); и его фармацевтически приемлемые производные. Предпочтительными соединениями по настоящему изобретению являются 2,6-диамино-3-(2,3-дихлорфенил)пиразин,2,6-диамино-3-(2,5-дихлорфенил)пиразин,2,6-диамино-3-(1-нафтил)пиразин,2,6-диамино-3-(2-нафтил)пиразин,2-амино-6-(4-метил-1-пиперазинил)-3(2,3,5-трихлорфенил)пиразин,2-амино-6-диметиламино-3-(2,3 дихлорфенил)пиразин,2-амино-6-диметиламино-3-(1-нафтил)пиразин,2,6-дициклопропилкарбониламино-3(2,3,5-трихлорфенил)пиразин,2-амино-6-циклопропилкарбониламино-3(2,3,5-трихлорфенил)пиразин,2,6-диизопропилкарбониламино-3-(2,3,5 трихлорфенил)пиразин,2-амино-6-изопропилкарбониламино-3(2,3,5-трихлорфенил)пиразин,2-изопропилкарбониламино-6-амино-3(2,3,5-трихлорфенил)пиразин,2-циклопропилкарбониламино-6-амино-3(2,3,5-трихлорфенил)пиразин,2-амино-6-ацетамидо-3-(2,3,5-трихлорфенил)пиразин,2-амино-6-ацетамидо-3-(2,5-дихлорфенил)пиразин,2-амино-6-ацетамидо-3-(2-нафталин)пиразин,5-метил-2,6-диамино-3-(2,3,5-трихлорфенил)пиразин,5-циано-2,6-диамино-3-(2,3,5-трихлорфенил)пиразин,и их фармацевтически приемлемые производные. Кроме того, предпочтительным соединением является 5-гидроксиметил-2,6-диамино-3 5(2,3,5-трихлорфенил)пиразин и его фармацевтически приемлемые производные. Особенно предпочтительным соединением по настоящему изобретению является 2,6 диамино-3-(2,3,5-трихлорфенил)пиразин и его фармацевтически приемлемые производные. Следует понимать, что настоящее изобретение охватывает все комбинации конкретных и предпочтительных групп, описанных выше. Соединения формулы (I) особенно полезны в качестве противосудорожных средств. Следовательно, они полезны в лечении эпилепсии. Их можно использовать для улучшения состояния хозяина, обычно человека, страдающего эпилепсией. Их можно использовать для облегчения симптомов эпилепсии у хозяина. Подразумевается, что "эпилепсия" включает в себя следующие припадки: простые эпилептические парциальные припадки, эпилептические припадки автоматизма, большие вторичные эпилептические припадки, большие эпилептические припадки, включающие в себя абсанс,миоклонические припадки, клонические припадки, тонические припадки, тонические клонические припадки и атонические припадки. Соединения формулы (I), кроме того, полезны в лечении биполярного расстройства,иначе известного как маниакальная депрессия. Можно лечить биполярное расстройство типа I или II. Соединения формулы (I), таким образом,могут быть использованы для улучшения состояния пациента-человека, страдающего биполярным расстройством. Их можно использовать для облегчения симптомов биполярного расстройства у хозяина. Соединения формулы (I) можно также использовать в лечении униполярной депрессии. Соединения формулы (I) полезны в качестве анальгетиков. Следовательно, они полезны в лечении или предотвращении боли. Их можно использовать для улучшения состояния хозяина,обычно являющегося человеком, страдающего от боли. Их можно использовать для облегчения боли у хозяина. Таким образом, соединения формулы (I) можно использовать в качестве преимущественных анальгетиков для лечения острой боли, такой как скелетно-мышечная боль, послеоперационная боль и хирургическая боль, хронической боли, такой как хроническая воспалительная боль (например при ревматоидном артрите и остеоартрите), невропатической боли (например при постгерпетической невралгии, невралгии тройничного нерва и симпатически держащейся боли) и боли, связанной с раком и фибромиалгией. Соединения формулы (I) можно также использовать в лечении или предотвращении боли, связанной с мигренью. Соединения формулы (I), кроме того, полезны в лечении функциональных расстройств кишечника, которые включают в себя неязвенную диспепсию, несердечную боль в груди,особенно синдром раздраженной толстой киш 002102 6 ки. Синдром раздраженной толстой кишки представляет собой желудочно-кишечное расстройство, отличающееся болью в брюшной полости и измененными кишечными отправлениями без какого-либо доказательства органического заболевания. Соединения формулы (I),следовательно, можно использовать для облегчения боли, связанной с синдромом раздраженной толстой кишки. Состояние пациентачеловека, страдающего синдромом раздраженной толстой кишки, таким образом, может быть улучшено. Соединения формулы (I) могут быть полезны также в лечении нейродегенеративных заболеваний, таких как болезнь Альцгеймера,ALS, болезнь двигательных нейронов и болезнь Паркинсона. Соединения формулы (I) могут быть также полезны в нейрозащите и в лечении нейродегенерации, являющейся следствием удара, остановки сердца, легочного шунтирования, травматического повреждения головного мозга, повреждения спинного мозга или т.п. Кроме того, соединения формулы (I) также полезны в предотвращении или уменьшении зависимости от вызывающего зависимость агента или в предотвращении или уменьшении толерантности или обратной толерантности к вызывающему зависимость агенту. Примеры вызывающих зависимость агентов включают в себя опиоиды (например морфин), депрессанты ЦНС (например этанол), психостимуляторы(например кокаин) и никотин. Поэтому далее согласно настоящему изобретению предложено применение соединения формулы (I) в изготовлении лекарства для использования в лечении расстройства, по существу такого, как описано выше. Далее, согласно настоящему изобретению предложен способ лечения пациента, страдающего расстройством,или восприимчивого к расстройству, по существу такому, как описано выше, при котором пациенту вводят терапевтически эффективное количество соединения формулы (I). Термин "лечение", как он используется здесь, включает в себя лечение установленных расстройств, а также их профилактику. Соединения по изобретению особенно полезны в лечении эпилепсии и биполярного расстройства, особенно эпилепсии. Точное количество соединения формулы(I) или его соли, вводимой хозяину, в частности пациенту-человеку, находится на ответственности лечащего врача. Однако применяемая доза зависит от ряда факторов, включая возраст и пол пациента, конкретное состояние, которое лечат, и его тяжесть, и путь введения. Соединение формулы (I) и его соли можно вводить в дозе от 0,1 до 10 мг/кг веса тела в сутки и более конкретно от 0,5 до 5 мг/кг веса тела в сутки в расчете на свободное основание. Дозовый интервал для взрослого человека составляет, как правило, от 5 до 1000 мг/сутки, напри 7 мер от 5 до 200 мг/сутки, предпочтительно от 10 до 50 мг/сутки в расчете на свободное основание. Хотя соединение формулы (I) или его фармацевтически приемлемое производное можно вводить в виде исходного химического соединения, предпочтительно представлять его в виде фармацевтического препарата. Препараты по настоящему изобретению содержат соединение формулы (I) или его фармацевтически приемлемое производное вместе с одним или более чем одним приемлемым носителем или разбавителем для него и возможно другими терапевтическими ингредиентами. Носитель(и) должен быть приемлемым в смысле совместимости с другими ингредиентами препарата и не должен наносить вред реципиенту. Эти препараты включают в себя препараты, подходящие для перорального, парентерального (в том числе подкожного, например инъекцией, или посредством депо-таблетки,внутрикожного, внутриоболочечного, внутримышечного, например посредством депо, или внутривенного), ректального и местного (в том числе кожного, трансбуккального и подъязычного) введения, хотя наиболее подходящий путь может зависеть от конкретного состояния и расстройства реципиента. Препараты могут быть удобно представлены в стандартной лекарственной форме и могут быть приготовлены любым из способов, хорошо известных в области фармации. Все способы включают в себя стадию объединения соединения формулы (I) или его фармацевтически приемлемой соли присоединения кислоты ("активный ингредиент") с носителем, который составляет один или более чем один дополнительный ингредиент. В общих чертах, препараты готовят равномерным и однородным объединением активного ингредиента с жидкими носителями или тонко измельченными твердыми носителями, или ими обоими, а затем, если необходимо, формированием продукта в желаемый препарат. Препараты по настоящему изобретению,подходящие для перорального введения, могут быть представлены в виде дискретных единиц,таких как капсулы, облатки или таблетки (например жевательные таблетки, в частности для педиатрического введения), причем каждая содержит предопределенное количество активного ингредиента; в виде порошка или гранул; в виде раствора или суспензии в водной жидкости или неводной жидкости; или в виде жидкой эмульсии типа "масло в воде", или жидкой эмульсии типа "вода в масле". Активный ингредиент может быть также представлен в виде болюса,электуария или пасты. Таблетка может быть изготовлена прессованием или формованием, возможно с использованием одного или более чем одного дополнительного ингредиента. Прессованные таблетки могут быть приготовлены прессованием ак 002102 8 тивного ингредиента в сыпучей форме, такой как порошок или гранулы, возможно смешанного со связующим веществом, смазочным материалом, инертным разбавителем, смазывающим,поверхностно-активным или диспергирующим агентом, на соответствующей машине. Формованные таблетки могут быть изготовлены формованием смеси порошкообразного соединения,смоченного инертным жидким растворителем,на соответствующей машине. Таблетки возможно могут быть покрыты оболочкой или маркированы, и могут быть приготовлены так, чтобы обеспечить медленное или регулируемое высвобождение активного ингредиента. Препараты для парентерального введения включают в себя водные и неводные стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостаты и растворенные вещества, которые делают препарат изотоничным с кровью предполагаемого реципиента; и водные и неводные стерильные суспензии, которые могут включать в себя суспендирующие агенты и загущающие агенты. Препараты могут быть представлены в однодозовых или многодозовых контейнерах, например запаянных ампулах и флаконах, и могут храниться в лиофилизированном состоянии,которое требует только добавления жидкого стерильного носителя, например воды для инъекций, непосредственно перед применением. Импровизированные растворы для инъекций и суспензии могут быть приготовлены из стерильных порошков, гранул и таблеток описанного выше типа. Препараты для ректального введения могут быть представлены в виде суппозитория с обычными носителями, такими как масло какао,твердый жир или полиэтиленгликоль. Препараты для местного введения в рот,например трансбуккального или подъязычного,включают в себя лепешки, содержащие активный ингредиент в корригентной основе, такой как сахароза и аравийская камедь или трагакант,и пастилки, содержащие активный ингредиент в такой основе, как желатин и глицерин или сахароза и аравийская камедь. Соединения по изобретению также могут быть приготовлены в виде депо-препаратов. Такие препараты длительного действия можно вводить имплантацией (например подкожно или внутримышечно) или внутримышечной инъекцией. Так, например, соединения по изобретению могут быть приготовлены в виде препарата,в состав которого входят соответствующие полимерные или гидрофобные материалы (например в виде эмульсии в приемлемом масле) или ионообменные смолы, либо в виде умеренно растворимых производных, например в виде умеренно растворимой соли. В дополнение к ингредиентам, особо упомянутым выше, препараты могут включать в себя другие традиционные в данной области 9 агенты, имеющие отношение к рассматриваемому типу препарата, например препараты,подходящие для перорального введения, могут включать в себя корригенты. Предпочтительными стандартными лекарственными препаратами являются препараты,содержащие эффективную суточную дозу, как указано выше, или ее соответствующую часть,активного ингредиента. Приемлемо она может составлять от 5 до 1000 мг, более удобно от 5 до 200 мг (например 5, 25 и 100 мг) и наиболее удобно от 10 до 50 мг в расчете на свободное основание. Когда соединения формулы (I) используют в комбинации с другими терапевтическими агентами, эти соединения можно вводить либо последовательно, либо одновременно любым удобным путем. Соединения формулы (I) (которые, конечно, включают в себя соединения формул (Ia) и(Ib и их фармацевтически приемлемые соли и сольваты могут быть получены известными из уровня техники способами получения конкретных аналогичных соединений. В частности, соединения формулы (I) могут быть получены изложенными ниже способами, которые и составляют еще один аспект данного изобретения. В приведенных далее способах R1, R2, R3 и R4 являются такими, как определено выше для формулы (I), если не указано иначе. Согласно общему способу (А) соединение формулы (I) может быть получено в соответствующих реакционных условиях из соединения формулы II где Hal (В) представляет собой атом галогена,приемлемо хлорид. Например, Hal (В) можно превратить в -NRbRc взаимодействием с соответствующим амином в растворителе, таком как этанол. Соединение формулы (II) приемлемо может быть получено из соединения формулы (III) 10 приемлемый Hal(A) выбран из бромида и иодида, в то время как приемлемый Hal(B) является хлоридом. Соединения формулы (IV) либо коммерчески доступны, либо могут быть получены из коммерчески доступных аналогов бензола,например 1-бром-2,3-дихлорбензола или 2 бром-4,6-дихлоранилина, как более подробно описано далее в сопровождающих примерах. Далее, соединение формулы (III) приемлемо может быть получено галогенированием соединения формулы (V) например взаимодействием с галогенирующим агентом, таким как N-бромсукцинимид, при перемешивании при комнатной температуре в течение нескольких часов. Соединение формулы (V) может быть получено из дигалогеносоединения формулы (VI) взаимодействием с R2H, где Наl(В) и Наl(С),которые могут быть одинаковыми или разными галогеновыми заместителями. Подходящие Наl(В) и Наl(С) оба являются хлоридом. Соединения формулы (VI) коммерчески доступны. Согласно следующему общему способу (Б) соединение формулы (I) может быть получено из соединения формулы (VII) где Hal представляет собой атом галогена, приемлемо бромид или иодид, путем взаимодействия с соединением формулы (IV), как описано выше. В случае, когда R3 и R4 оба представляют собой водород, соединение формулы (VII) может быть коммерчески доступным. Альтернативно, соединение формулы (VII) может быть получено из соединения формулы (VIII) где Y представляет собой группу, которую легко превратить в R3. Например, в случае, когда Y представляет собой NH2, эта аминогруппа может быть превращена в -NНС(=O)СН 3 нагреванием с обратным холодильником в присутствии ацетилирующего агента, такого как уксусный ангидрид. 11 Соединение формулы (VIII) может быть получено из соединения формулы (IX) путем взаимодействия с R2H в соответствующих условиях. Например, соединение формулы (IX) может быть подвергнуто взаимодействию с аммиаком в автоклаве в течение нескольких часов. Соединение формулы (IX) может быть получено из соединения формулы (X) которое, в свою очередь, может быть получено из коммерчески доступных соединений формулы (VI), описанных выше. Согласно следующему способу В соединения формулы (I), где R2 представляет собой NH2,могут быть получены циклизацией или окислением соединения формулы (XI) или его соли по общепринятым методикам, например нейтрализацией соли соединения формулы (XI), например гидроксидом лития в подходящем растворителе, таком как спирт, например метанол, причем в данных условиях происходит спонтанное окисление до соединения формулы (I). Соединения формулы (XI) могут быть получены путем взаимодействия соединений формулы (XII) R1C(O)H с соединениями формулы(XIII) или его солью в присутствии источника цианида, например цианида калия. Соединения формулы (XII), где R1 представляет собой тригалогенозамещенный фенил, например 2,3,5 трихлорбензальдегид, известны и могут быть получены согласно способам, описанным вW095/07877. Соединения, где R1 представляет собой альтернативные значения, либо известны,либо могут быть получены согласно известным способам получения известных соединений. Соединения формулы (XIII), например аминоацетамидин, могут быть получены по известным методикам, например методикам, которые описаны в Chem. Berichte, 89, 1185 (1956). Согласно следующему способу Г соединения формулы (I) могут быть превращены в соответствующие соединения формулы (I) с использованием соответствующих реакционных технологий. Например, соединения формулы (I),где R3 представляет собой -NHC(=O)Ra, могут 12 быть превращены в соединения, где R3 представляет собой NH2, гидролизом, например при взаимодействии с водной соляной кислотой. Кроме того, соединения формулы (I), где R4 представляет собой водород, могут быть превращены в соединения, где R4 представляет собой -CN, сначала галогенированием посредством взаимодействия с галогенирующим агентом, таким как N-бромсукцинимид, с последующим взаимодействием с подходящим источником цианид-ионов, например смесью цианида натрия и цианида меди (I). Далее, соединения формулы (I), где R4 представляет собой CN,могут быть превращены в соединения, где R4 представляет собой -СН 2 ОН, через формильное производное, которое может быть получено путем взаимодействия -CN-соединения с диизобутилалюминийгидридом в толуоле с последующим гидролизом. Формильное производное затем восстанавливают до -СН 2 ОН-соединения,используя, например, борогидрид натрия в этаноле. Соединения, где R4 представляет собой -СН 2 ОН,могут быть превращены в соединения, где R4 представляет собой -СН 2 ОR,d путем алкилирования. Кроме того, соединения формулы (I), где R4 представляет собой -CN, могут быть превращены в соединения, где R4 представляет собой метил, через формильное производное, полученное как описано выше, которое затем превращают в тозилгидразон взаимодействием с п-толуолсульфонгидразидом с последующим взаимодействием с катехолбораном в смеси хлороформ/тетрагидрофуран. Различные общие способы, описанные выше, можно использовать для введения желаемых групп на любой стадии многостадийного образования целевого соединения, и понятно,что эти общие способы можно по-разному комбинировать в таких многостадийных процессах. Последовательность реакций в многостадийных процессах следует, конечно, выбирать таким образом, чтобы используемые реакционные условия не влияли на те группы в молекуле, которые являются желательными в конечном продукте. Следующие примеры, которые не следует воспринимать как ограничение данного изобретения, предназначены для иллюстрации данного изобретения. Пример 1. 2,6-Диамино-3-(2,3,5-трихлорфенил)пиразин. 1. 2,3,5-Трихлорбромбензол. Нитрит натрия (3,88 г, 0,056 моль) добавляют по частям к концентрированной серной кислоте (28,16 мл), перемешиваемой при температуре ниже 10 С. Поддерживая температуру ниже 10 С, добавляют раствор 2-бром-4,6 дихлоранилина (12 г, 0,05 моль, Lancaster) в ледяной уксусной кислоте (126 мл). Смесь перемешивают при температуре ниже 10 С в течение 1 ч, а затем к перемешиваемому раствору медленно добавляют хлорид меди (10,11 г, 0,10 моль) в концентрированной соляной кислоте(101,05 мл) при комнатной температуре. Смесь затем перемешивают при комнатной температуре в течение 17 ч. Продукт фильтруют, промывают водой (3 х 50 мл), растворяют в хлороформе(150 мл), сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме с получением целевого продукта. Выход 10 г (77%), т.пл. 55-57 С. 2. 2,3,5-Трихлорбензолбороновая кислота. Раствор 2,3,5-трихлорбромбензола (8,60 г,0,033 моль) в сухом эфире (33 мл) и бромэтане(4,73 мл, 7,31 г, 0,067 моль) добавляют по каплям к суспензии магниевой стружки (2,80 г, 0,12 моль) в сухом эфире (21,50 мл) при комнатной температуре. Смесь нагревают с обратным холодильником в течении 0,50 ч и охлаждают до комнатной температуры. Смесь затем в атмосфере азота по каплям добавляют к раствору триметилбората (5,16 мл, 5,16 г, 0,05 моль) в сухом эфире (8,60 мл), поддерживая температуру ниже -60 С. Затем эту смесь нагревают до комнатной температуры в течение ночи, затем охлаждают на ледяной бане и обрабатывают 2 М соляной кислотой (10 мл). Эфирный слой отделяют, промывают водой (2 х 20 мл), сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток растирают с 40-60 С петролейным эфиром, фильтруют и сушат в вакууме. Выход 4,57 г(61%),т.пл.257-260 С. Путь А. 3. 2-Хлор-6-аминопиразин. Суспензию 2,6-дихлорпиразина (100 г, 0,67 моль, Lancaster) в 0,880 аммиаке (500 мл) перемешивают и нагревают при 150 С в стеклянном автоклаве при 20 атм. в течение 16 ч. Охлажденную смесь фильтруют, хорошо промывают водой (200 мл) и сушат. Продукт перекристаллизовывают из хлороформа. Выход 41,98 г(48%), Т.пл. 150-152 С. 4. 2-Хлор-3-бром-6-аминопиразин и 2 амино-3-бром-6-хлорпиразин. Раствор 2-хлор-6-аминопиразина (20 г, 0,15 моль) в хлороформе (1940 мл) перемешивают при температуре от -5 до 0 С. Добавляют по частям Nбромсукцинимид (27,58 г, 0,15 моль), поддерживая температуру между -5 и 0 С. Эту смесь нагревают до комнатной температуры и перемешивают в течение 3,50 ч. Затем смесь промывают водным насыщенным бикарбонатом натрия (1 х 300 мл),затем водой (1 х 500 мл), сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток очищают "флэшхроматографией", используя хлороформ в качестве элюента. Выход 2-хлор-3-бром-6 аминопиразина 13,89 г (43%), т.пл. 146-147 С. Выход 2-амино-3-бром-6-хлорпиразина 4,90 г(2,05 мл) медленно добавляют к смеси 2-амино-3 бром-6-хлорпиразина (1 г, 5,1 х 10-3 моль) и тетракис(трифенилфосфин)палладия(0) (0,344 г, 2,89 х 10-4 моль) в смеси бензол (10,20 мл)/2 М водный карбонат натрия (5,50 мл). Смесь нагревают с обратным холодильником в течение 17 ч. Охлажденную реакционную смесь выпаривают в вакууме, а затем экстрагируют хлороформом (50 мл). Хлороформный слой промывают водой (2 х 30 мл), сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток растирают с 40-60 С петролейным эфиром,фильтруют и сушат в вакууме. Выход 0,205 г(14%), т.пл. 211-214 С. 6. 2,6-Диамино-3-(2,3,5-трихлорфенил)пиразин. Суспензию 2-амино-6-хлор-3-(2,3,5-трихлорфенил)пиразина (0,3 г, 9,71 х 10-4 моль) в абсолютном этаноле (4 мл) и водном аммиаке 0,880 (8,24 мл) перемешивают и нагревают в автоклаве при 180 С в течение 44 ч. Охлажденную смесь выпаривают в вакууме, остаток экстрагируют хлороформом (3 х 30 мл). Объединенные хлороформные экстракты сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток очищают "флэшхроматографией", используя градиент от хлороформа до смеси 98:2 хлороформ: метанол в качестве элюента. Продукт растирают с 40-60 С петролейным эфиром, фильтруют и сушат в вакууме. Выход 0,155 г (56%). т.пл. 178-180 С. Путь Б. 7. 2,6-Диамино-3-бромпиразин. Суспензию 2-хлор-3-бром-6-аминопиразина (15 г, 0,072 моль) в абсолютном этаноле (150 мл) и аммиаке 0,880 (375 мл) перемешивают и нагревают в автоклаве при 160 С и 20 атм в течение 16 ч. Охлажденную смесь выпаривают в вакууме и экстрагируют горячим метанолом(3 х 100 мл). Объединенные метанольные экстракты выпаривают в вакууме. Остаток растворяют в горячем хлороформе, сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток растирают с 4060 С петролейным эфиром, фильтруют и сушат в вакууме. Выход 5,51 г (40%), т.пл. 176-178 С. 8. 2-Амино-3-бром-6-ацетамидопиразин. Смесь 2,6-диамино-3-бромпиразина (10,50 г, 0,056 моль) в сухом 1,1-диметоксиэтане (168 мл) и уксусном ангидриде (7,91 мл, 8,56 г, 0,084 моль) нагревают с обратным холодильником в атмосфере азота в течение 2,5 ч. Охлажденную смесь выпаривают в вакууме. Остаток растирают с эфиром, фильтруют и сушат в вакууме. Выход 10,31 г (80%), т.пл. 218-221 С. 9. 2-Амино-6-ацетамидо-3-(2,3,5-трихлорфенил)пиразин. Смесь 2-амино-3-бром-6-ацетамидопиразина (7,00 г, 0,03 моль) в бензоле (60,90 мл) и тетракис(трифенилфосфин)палладия (0) перемешивают в атмосфере азота при комнатной температуре в течение 10 мин. К смеси добавляют 2 М 15 водный карбонат натрия (30,24 мл), а затем раствор 2,3,5-трихлорбензолбороновой кислоты(6,83 г, 0,03 моль) в абсолютном этаноле (7,07 мл), и смесь нагревают с обратным холодильником в атмосфере азота в течение 17 ч. Добавляют еще эквивалент 2,3,5-трихлорбензолбороновой кислоты в абсолютном этаноле, и смесь нагревают с обратным холодильником в течение дополнительных 7,5 ч. Наконец, к смеси добавляют еще один эквивалент 2,3,5-трихлорбензолбороновой кислоты в абсолютном этаноле и продолжают нагревание с обратным холодильником в течение 17 ч. Охлажденную смесь выпаривают в вакууме. Остаток растворяют в хлороформе (150 мл), промывают водным насыщенным бикарбонатом натрия (1 х 100 мл) и водой (1 х 100 мл), сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток очищают"флэшхроматографией", используя градиент от хлороформа до смеси 98:2 хлороформ: метанол в качестве элюента. Выход 3,02 г (30%), т.пл. 200203 С. 10. 2,6-Диамино-3-(2,3,5-трихлорфенил)пиразин. Суспензию 2-амино-6-ацетамидо-3-(2,3,5 трихлорфенил)пиразина (2,97 г, 8,96 х 10-3 моль) в 12 М соляной кислоте (1,31 мл) и воде (4,04 мл) нагревают с обратным холодильником в течение 1,75 ч. Охлажденную смесь затем подщелачивают водным аммиаком 0,880 (5 мл) и экстрагируют хлороформом (3 х 50 мл). Объединенные хлороформные экстракты сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме при 80 С. Выход 2,29 г (88%), т.пл. 178-180 С. Путь В. 11. 2-[Циано-(2,3,5-трихлорфенил)-метил] амино-ацетамидина гидробромид. Аминоацетамидина дигидробромид (162,1 г, 0,744 моль) добавляют по частям к раствору 2,3,5-трихлорбензальдегида (200,0 г, 0,851 моль) в метаноле (2,43 л) при комнатной температуре. Сразу после окончании добавления к полученной смеси одной порцией добавляют цианид калия (50,4 г, 0,744 моль). Затем суспензию,перед тем как нагреть до 50 С, перемешивают при 25 С в течение 4 ч. Смесь перемешивают в течение 50 С в течение 24 ч. Затем в вакууме удаляют метанол, полученное твердое вещество суспендируют в воде (1,5 л) и этилацетате (2,5 л) и собирают фильтрацией. Твердое вещество затем сушат в вакууме при 50 С в течение ночи с получением целевого продукта. Выход 96,31 г 2-[Циано-(2,3,5-трихлорфенил)-метил]амино-ацетамидина гидробромид (95,36 г,0,256 моль) добавляют по частям к раствору моногидрата гидроксида лития (16,11 г, 0,384 моль) в метаноле (1,9 л) при комнатной температуре. Перед тем как выпарить до сухости в вакууме, полученный раствор перемешивают при комнатной температуре в течение 3 ч. Полученное твердое вещество суспендируют в воде (1,15 л) и собирают фильтрацией. После сушки при 50 С в вакууме неочищенный материал очищают путем перекристаллизации из толуола с получением целевого продукта. Выход 69,51 г(44,24 мл) добавляют по каплям к раствору нбутиллития (1,6 М в гексане, 66,36 мл, 0,11 моль) в безводном тетрагидрофуране (16 мл), поддерживая температуру ниже -65 С. Полученную бледножелтую суспензию перемешивают при -78 С в течение 75 мин. По каплям добавляют триметилборат(13,28 мл, 12,16 г, 0,12 моль), поддерживая температуру ниже -55 С. Полученный бледно-желтый раствор нагревают до комнатной температуры в течение ночи. Избыток н-бутиллития разлагают водой (30 мл) и реакционную смесь выпаривают в вакууме. Полученный остаток суспендируют в воде и подкисляют 2 М соляной кислотой (10 мл). Нерастворимое твердое вещество фильтруют, хорошо промывают водой и сушат. Твердое вещество суспендируют в 60-80 С петролейном эфире, перемешивают при комнатной температуре в течение 10 мин, фильтруют, сушат в вакууме. Выход 8,42 г (50%), т.пл. 235238 С. 2. 2-Амино-6-хлор-3-(2,3-дихлорфенил)пиразин. Это соединение получают способом, аналогичным способу Пути А примера 1, из 2 амино-3-бром-6-хлорпиразина. Выход 0,343 г(26%), т.пл. 179-181 С. 3. 2,6-Диамино-3-(2,3-дихлорфенил)пиразин. Это соединение получают способом, аналогичным способу пути А примера 1, из 2 амино-6-хлор-3-(2,3-дихлорфенил)пиразина,путем взаимодействия с аммиаком 0,880. Выход 0,195 г, т.пл. 169-170 С. Пример 3. 2.6-Диамино-3-(2,5-дихлорфенил)пиразин. 1. 2,5-Дихлорбензолбороновая кислота. Это соединение получают способом, аналогичным способу получения соединения примера 2, из 2,5-дихлорбромбензола (Aldrich). Выход 2,19 г (55%), т.пл. 278-280 С. 2. 2-Амино-6-ацетамидо-3-(2,5-дихлорфенил)пиразин. Это соединение получают способом, аналогичным способу пути Б примера 1, из 2 17 амино-3-бром-6-ацетамидопиразина. Выход 0,45 г, т.пл. 152-154 С. 3. 2,6-Диамино-3-(2,5-дихлорфенил)пиразин. Это соединение получают способом, аналогичным способу пути Б примера 1, из 2 амино-6-ацетамидо-3-(2,5-дихлорфенил)пиразина. Выход 0,123 г, т.пл. 159-160 С. Пример 4. 2,6-Диамино-(1-нафталин)пиразин. 1. 2-Амино-6-хлор-3-(1-нафталин)пиразин. Это соединение получают способом, аналогичным способу пути А примера 1, из 2 амино-3-бром-6-хлорпиразина и 1-нафталинбороновой кислоты (Lancaster). Выход 0,709 г (58%), т.пл. 138-139 С. 2. 2,6-Диамино-(1-нафталин)пиразин. Это соединение получают способом, аналогичным способу пути А примера 1, из 2 амино-6-хлор-3-(1-нафталин)пиразина путем взаимодействия с аммиаком 0,880. Выход 0,167 г (50%), т.пл. 180-183 С. Пример 5. 2,6-Диамино-3-(2-нафталин)пиразин. 1. 2-Нафталинбороновая кислота. Это соединение получают способом, аналогичным способу получения соединения примера 2, из 2-бромнафталина (Aldrich). Выход 1,71 г (40%), т.пл. 280-282 С. 2. 2-Амино-6-ацетамидо-3-(2-нафталин)пиразин. Это соединение получают способом, аналогичным способу пути Б примера 1, из 2 амино-3-бром-6-ацетамидопиразина. Выход 0,46 г, т.пл. 235-237 С. 3. 2,6-Диамино-3-(2-нафталин)пиразин. Это соединение получают способом, аналогичным способу пути Б примера 1, из 2 амино-6-ацетамидо-3-(2-нафталин)пиразина. Выход 0,121 г, т.пл. 168-70 С. Пример 6. 2-Амино-6-(4-метил-1-пиперазинил)-3-(2,3,5-трихлорфенил)пиразин. 2-Амино-6-хлор-3-(2,3,5-трихлорфенил)пиразин (0,215 г, 7,0 х 10-3 моль) из пути А примера 1 и 1-метилпиперазин (5 мл, Aldrich) нагревают при 140 С в течение 1 ч. Смесь выпаривают в вакууме, а остаток очищают "флэш-хроматографией", элюируя смесью этанол:дихлорметан,0-4%. Продукт растворяют в минимуме дихлорметана и гексане (10 мл), добавляемом медленно, с получением желтых игл. Выход 0,247 г(95%), т.пл. 185 С. Пример 7. 2-Амино-6-диметиламино-3(2,3-дихлорфенил)пиразин. Это соединение получают способом, аналогичным способу получения соединения примера 6, из 2-амино-6-хлор-3-(2,3-дихлорфенил)пиразина (пример 2) и диметиламина 18 Это соединение получают способом, аналогичным способу получения соединения примера 6, из 2-амино-6-хлор-3-(1-нафталин)пиразина (пример 4). Т.пл. 131 С. Пример 9. 2.6-Дициклопропилкарбониламино-3-(2,3,5-трихлорфенил)пиразин и 2 амино-6-циклопропилкарбониламино-3-(2,3,5 трихлорфенил)пиразин. Безводный пиридин (0,137), 4-диметиламинопиридин (0,114) и циклопропанкарбонилхлорид (0,33 г), 0,286 мл, 3,14 х 10-3 моль,Aldrich) добавляют к раствору 2,6-диамино-3(2,3,5-трихлорфенил)пиразина (пример 1) в безводном тетрагидрофуране (12 мл), и полученную реакционную смесь нагревают с обратным холодильником при 90 С в течение 2,5 ч. Полученную суспензию охлаждают до комнатной температуры и выпаривают в вакууме. Остаток экстрагируют этилацетатом (3 х 20 мл), промывают водой (2 х 20 мл), сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток очищают "флэшхроматографией", используя в качестве элюента смесь гексан:эфир с градиентом от 15:25 до 5:35. Выход 2,6-дициклопропилкарбониламино 3-(2,3,5-трихлорфенил)пиразина 0,340 г (51%),т.пл. 212-214 С. Выход 2-амино-6-циклопропилкарбониламино-3-(2,3,5-трихлорфенил)пиразина 0,147 г (31%), т.пл. 240-244 С. Пример 10. 2,6-Диизопропилкарбониламино-3-(2,3,5-трихлорфенил)пиразин и 2 амино-6-изопропилкарбониламино-3-(2,3,5 трихлорфенил)пиразин. Эти соединения получают способом, аналогичным способу получения соединений примера 9, из 2,6-диамино-3-(2,3,5-трихлорфенил)пиразина (пример 1), путем взаимодействия с изобутирилхлоридом (Aldrich). Выход 2,6 диизопропилкарбониламино-3-(2,3,5-трихлорфенил)пиразина 0,313 г (46%), т.пл. 227-229 С. Выход 2-амино-6-изопропилкарбониламино-3(2,3,5-трихлорфенил)пиразина 0,166 г (29%). т.пл. 230-232 С. Пример 11. 2-Изопропилкарбониламино-6 амино-3-(2,3,5-трихлорфенил)пиразин. 1. 2-Изопропилкарбониламино-6-ацетамидо-3-(2,3,5-трихлорфенил)пиразин Это соединение получают способом, аналогичным способу получения соединения примера 9, из 2-амино-6-ацетамидо-3-(2,3,5 трихлорфенил)пиразина (пример 1) и одного эквивалента изобутирилхлорида (Aldrich). Выход 0,102 г, т.пл. 230-232 С. 2. 2-Изопропилкарбониламино-6-амино-3(2,3,5-трихлорфенил)пиразин. Хлорид олова (0,182 г, 0,0096 моль) добавляют к суспензии 2-изопропилкарбониламино 6-ацетамидо-3-(2,3,5-трихлорфенил)пиразина(6,50 мл), и полученную смесь перемешивают при 50-60 С в течение 1 ч 20 мин. Реакционную смесь охлаждают и выпаривают в вакууме. Ос 19 таток экстрагируют этилацетатом (3 х 20 мл),промывают водой (2 х 20 мл), сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток очищают флэшхроматографией, используя в качестве элюента смесь хлороформ: метанол, 99:1. Выход 0,046 г(40%),т.пл. 105-108 С. Пример 12. 2-Циклопропилкарбониламино-6-амино-3-(2,3,5-трихлорфенил)пиразин. 1. 2-Циклопропилкарбониламино-6-ацетамидо-3-(2,3,5-трихлорфенил)пиразин. Это соединение получают способом, аналогичным способу получения соединения примера 9, из 2-амино-6-ацетамидо-3-(2,3,5 трихлорфенил)пиразина (пример 1) и циклопропилкарбонил хлорида (Aldrich). Выход 0,387 г (61%), ЯМР (D6 ДМСО) : 0.53 (2H, m), 0.7 (2 Н, m), 1.75 (1H, m), 2,18 (3H,s), 7.43 (1H, d), 7.87 (1H, d), 9.22 (1H, s), 10.36(1H, b), 10.83 (1 Н, b). 2. Циклопропилкарбониламино-6-амино-3(2,3,5-трихлорфенил)пиразин. Это соединение получают способом, аналогичным способу получения соединения примера 11, из 2-циклопропилкарбониламино-6 ацетамидо-3-(2,3,5-трихлорфенил)пиразина. Выход 0,102 г (35%), т.пл. 188-190 С. Пример 13. 2-Амино-3-(2,3,5-трихлорфенил)пиразин. Раствор 2,3,5-трихлорбензолбороновой кислоты (1,54 г, 6,82 ммоль) в абсолютном этаноле(1,5 мл) медленно добавляют к смеси 2-амино-3 хлорпиразина (0,589 г, 4,54 ммоль) и тетракис(трифенилфосфин)палладия(0) (0,299 г,0,259 ммоль) в смеси бензол (10,5 мл)/2 М водный карбонат натрия (4,54 мл). Смесь нагревают с обратным холодильником в течение 17 ч. Охлажденную реакционную смесь распределяют между водой и этилацетатом (50 мл). Органический слой промывают водой (2 х 30 мл), сушат(МgSO4) и выпаривают. Неочищенный продукт очищают флэш-хроматографией, используя в качестве элюента градиент от хлороформа до смеси 0,5% метанола в хлороформе. Продукт затем кристаллизуют из 40-60 бензина. Выход 0,15 г, 12%. Т.пл. 142-143 С. Пример 14. 2-Амино-6-ацетамидо-3-(2,3,5 трихлорфенил)пиразин. Получают как описано выше (см. пример 1.9). Пример 15. 2-Амино-6-ацетамидо-3-(2,5 дихлорфенил)пиразин. Получают, как описано выше (см. пример 3.2). Пример 16. 2-Амино-6-ацетамидо-3-(2 нафталин)пиразин. Получают, как описано выше (см. пример 5.2). Пример 17. 5-Циано-2,6-диамино-3-(2,3,5 трихлорфенил)пиразин. 1. 5-Бром-2,6-диамино-3-(2,3,5-трихлорфенил)пиразинN-Бромсукцинимид (0,194 г, 1,09 х 10-3 моль) добавляют в течение 20 мин к смеси 2,6 диамино-3-(2,3,5-трихлорфенил)пиразина (0,3 г,1,04 х 10-3 моль) в диметилсульфоксиде (10 мл) и воды (0,25 мл) при температуре ниже 15 С. Полученную реакционную смесь перемешивают при 15 С в течение 1 ч, вливают в ледяную воду(150 мл) и экстрагируют этилацетатом (2 х 75 мл). Экстракт затем промывают 2 М раствором карбоната натрия (50 мл) и водой (100 мл), сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток очищают флэш-хроматографией, используя в качестве элюента 5-13% этилацетата в циклогексане. Выход 0,183 г (48%), т.пл. 222-224 С. 2. 5-Циано-2,6-Диамино-3-(2,3,5-трихлорфенил)пиразин. Смесь 97% цианида натрия (0,064 г,1,306 х 10-3 моль) и 90% цианида меди (I) в сухом диметилформамиде (5 мл) перемешивают и нагревают до 130 С. К полученному прозрачному раствору небольшими порциями добавляют 5 бром-2,6-диамино-3-(2,3,5-трихлорфенил)пиразин (0,35 г, 0,95 х 10-3 моль) и поддерживают температуру раствора 140-150 С в течение 16 ч. Реакционную смесь охлаждают и выпаривают в вакууме. Остаток экстрагируют этилацетатом(100 мл), сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток очищают флэш-хроматографией, используя в качестве элюента 5-17% этилацетата в циклогексане. Выход 0,152 гC11H6N5Cl30,02C6H12: С, 42,23; Н, 1,99; N, 22,15. Обнаружено: С, 42,36; Н, 1,78; N, 21,.79. Пример 18. 5-Гидроксиметил-2,6-диамино 3-(2,3,5-трихлорфенил)пиразин. 1. 5-Формил-2,6-диамино-3-(2,3,5-трихлорфенил)пиразин. Диизобутилалюминийгидрид (1,5 М в толуоле) (2,12 мл, 3,18 х 10-3 моль) добавляют по каплям при 0 С в атмосфере азота к суспензии 5-циано-2,6-диамино-3-(2,3,5-трихлорфенил)пиразина (0,5 г, 1,59 х 10-3 моль) в сухом толуоле(70 мл), и реакционную смесь перемешивают при 0 С в течение 1 ч. Затем добавляют еще один эквивалент диизобутилалюминийгидрида,и реакционную смесь снова перемешивают при 0 С в течение 1 ч. Осторожно добавляют метанол (1 мл) при 0 С в атмосфере азота, чтобы разрушить избыток гидрида, и реакционную смесь нагревают до комнатной температуры. Добавляют этилацетат (100 мл), и раствор промывают 5%-ным раствором лимонной кислоты(2 х 100 мл). Органический слой отделяют, промывают рассолом (100 мл), сушат над сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме с получением целевого продукта. Выход 0,340 г (67%), ЯМР (D6 ДМСО) : 7.53 (1 Н,d), 7.91 (1 Н, d), 6.90-7.80 (4 Н, b), 9.49 (1 Н, s).(0,198 г, 6,24 х 10-4 моль) в этаноле (100 мл) добавляют борогидрид натрия (0,035 г, 9,35 х 10-4 моль) при комнатной температуре. Реакционную смесь перемешивают при комнатной температуре в атмосфере азота в течение 1 ч, добавляют воду (1 мл), и раствор выпаривают в вакууме. Остаток растворяют в этилацетате (200 мл), промывают рассолом, сушат над сульфатом магния, фильтруют и выпаривают в вакууме. Продукт очищают "флэш-хроматографией",используя в качестве элюента 11-40% этилацетата в циклогексане. Выход 0,104 г (52%), т.пл. 185-186 С. ЯМР (D6 ДМСО) : 4.32 (2 Н, d), 4.98(1H, d). Пример 19. 5-Метил-2,6-диамино-3-(2,3,5 трихлорфенил)пиразин. 1. 5-Формил-2,6-диамино-3-(2,3,5-трихлорфенил)пиразин, тозилгидразон. 5-Формил-2,6-диамино-3-(2,3,5-трихлорфенил)пиразин (0,330 г, 1,04 х 10-3 моль) добавляют к раствору п-толуолсульфонгидразида (0,3 г,1,61 х 10-3 моль) в метаноле (50 мл). Раствор нагревают с обратным холодильником в атмосфере азота в течение 4 ч, охлаждают до комнатной температуры, и растворитель выпаривают в вакууме. Остаток очищают флэш-хроматографией, используя в качестве элюента 0-30% этилацетата в циклогексане. Выход 0,270 г (53%). Масс-спектрометрия:(1,09 мл, 1,09 х 10-3 моль) добавляют по каплям при 0 С в атмосфере азота к суспензии 5 тозилгидразон-2,6-диамино-3-(2,3,5-трихлорфе 22 нил)пиразина (0,265 г, 5,46 х 10-4 моль) в сухом хлороформе (15 мл) и тетрагидрофуране (20 мл). Реакционную смесь перемешивают при 0 С в течение 1 ч, гасят реакцию и добавляют тригидрат ацетата натрия (5,46 х 10-4 моль). Смесь нагревают до комнатной температуры, перемешивают в течение 1 ч, и растворители выпаривают в вакууме. Остаток растворяют в этилацетате(100 мл), промывают 5%-ным раствором карбоната натрия, затем водой, сушат над безводным сульфатом магния, фильтруют, и фильтрат выпаривают в вакууме. Остаток очищают флэшхроматографией, используя в качестве элюента 10-25% этилацетата в циклогексане. Выход 0,017 г (10%), ЯМР (CDCl3) : 2.35 (3 Н, s), 4.10(электрораспылительная ионизация) 305 (МН+) Время удерживания 2,89 мин (условия как для примера 19.1). Фармацевтические примеры Стерильные препараты Пример А. Соединение по изобретению Хлорид натрия (Фармакопея США) Вода для инъекций (Фармакопея США) мг/мл 0,1 мг 9,0 мг Сколько требуется до 1 мл Компоненты растворяют в части воды для инъекций и доводят раствор до конечного объема таким образом, чтобы обеспечить 0,1 мг/мл соединения по изобретению. Когда используют соль этого соединения, количество соединения увеличивают таким образом, чтобы обеспечить 0,1 мг/мл свободного основания. Раствор может быть упакован для инъекции, например путем заполнения и запаивания ампул, флаконов и шприцов. Они могут быть заполнены асептически и/или окончательно стерилизованы, например, автоклавированием при 121 С. Кроме того, стерильные препараты могут быть приготовлены подобным образом с получением альтернативных концентраций соединения. Пример Б. Соединение по изобретению Маннит Вода для инъекций мг/м=8 л 0,5 мг 50,0 мг Сколько требуется до 1,0 мл Компоненты растворяют в части воды для инъекций. Доводят раствор до конечного объема и перемешивают до гомогенного состояния. Препарат фильтруют через стерилизующий фильтр и заполняют им стеклянные флаконы. Флаконы лиофилизируют и запаивают. С соответствующим растворителем объединяют непосредственно перед употреблением. Препараты для перорального введения Таблетки могут быть приготовлены обычными способами, такими как прямое прессование или влажное гранулирование. Таблетки мо 23 гут быть покрыты пленкой с использованием подходящих пленкообразующих материалов,таких как Opadry, применяя стандартные методики. Альтернативно, таблетки могут иметь сахарное покрытие. Пример В. Таблетка, приготовленная прямым прессованием. Соединение по изобретению Стеарат магния Микрокристаллическая целлюлоза Соединение по изобретению пропускают через сито 30 меш и смешивают с Avicel и стеаратом магния. Полученную смесь прессуют в таблетки, используя подходящий таблеточный пресс, снабженный пуансонами диаметром 11,0 мм, так, чтобы обеспечить 5 мг соединения по изобретению на таблетку. Таблетки других составов, содержащие например 25 или 100 мг на таблетку соединения по изобретению, могут быть получены аналогичным образом. Пример Г. Таблетка, приготовленная влажным гранулированием. Соединение по изобретению Предварительно желатинизированный крахмал Крахмальный гликолят натрия Стеарат магния Лактоза мг/таблетку 5,0 мг 28,0 мг 16,0 мг 4,0 мг Сколько требуется до 400,0 мг Соединение по изобретению, лактозу,предварительно желатинизированный крахмал и крахмальный гликолят натрия смешивают в сухом виде, а затем гранулируют, используя соответствующий объем очищенной воды. Полученные гранулы сушат, а затем смешивают со стеаратом магния. Высушенные гранулы прессуют,используя подходящий таблеточный пресс,снабженный пуансонами диаметром 11,0 мм,так, чтобы обеспечить 5 мг соединения по изобретению на таблетку. Получают таблетки других составов, таких как 25 и 100 мг на таблетку. Пример Д. Твердая желатиновая капсула. Соединение по изобретению Микрокристаллическая целлюлоза (Avicel PH102) мг/капсулу 5,0 мг Сколько требуется до 700,0 мг Соединение по изобретению пропускают через сито 30 меш и смешивают с микрокристаллической целлюлозой с получением гомогенной смеси. Смесью заполняют оболочки твердых желатиновых капсул размера OEL таким образом, чтобы получить капсулы, содержащие 5,0 мг на капсулу соединения по изобретению. Альтернативные составы, такие как 25 или 100 мг на капсулу соединения по изобретению, могут быть получены аналогично. 24 Пример Е. Мягкая желатиновая капсула. Соединение по изобретению Полиэтиленгликоль Пропиленгликоль мг/капсулу 10,0 мг 90,0 мг сколько требуется до 200,0 мг Смешивают вместе полиэтиленгликоль и пропиленгликоль, используя нагревание, когда необходимо. Перемешивают до гомогенного состояния. Добавляют соединение по изобретению и перемешивают до гомогенного состояния. Загружают в соответствующую желатиновую массу с получением мягких желатиновых капсул, содержащих 200 мг препарата, чтобы обеспечить 10,0 мг на капсулу соединения по изобретению. Альтернативные составы, например 5 и 25 мг на капсулу соединения по изобретению, могут быть получены аналогично. Пример Ж. Сироп. Соединение по изобретению Раствор сорбита Глицерин Бензоат натрия Корригент Очищенная вода 5,0 мг 1500,0 мг 1000,0 мг 5,0 мг 12,5 мг Сколько требуется до 5,0 мл Бензоат натрия растворяют в части очищенной воды и добавляют раствор сорбита. Добавляют соединение по изобретению, корригент и глицерин, и перемешивают до гомогенного состояния. Полученную смесь доводят до объема очищенной водой. Другие препараты Пример З. Суппозиторий. Соединение по изобретению мг/суппозиторий 10,0 мг Сколько требуется до 2000,0 мг Растапливают Witepsol W32 при приблизительно 36 С. К части его добавляют соединение по изобретению и перемешивают. Вводят остальной растопленный Witepsol W32 и перемешивают до гомогенного состояния. Форму заполняют 2000 мг этого препарата с получением 10,0 мг на суппозиторий соединения по изобретению. Пример И. Чрескожный Соединение по изобретению Силиконовая жидкость Коллоидный силикон диоксид Смешивают вместе силиконовую жидкость и активный ингредиент и добавляют коллоидный диоксид кремния. Этот материал затем дозируют в впоследствии запаянный нагреванием полимерный ламинат, состоящий из следующего: полиэфирная высвобождающая прокладка,адгезионный слой для контакта с кожей, состоящий из силиконовых или акриловых полимеров, регулирующая мембрана, которая пред 25 ставляет собой полиолефин (например полиэтилен или поливинилацетат) или полиуретан, и непроницаемое покрытие из многослойного полиэфирного материала с обратной стороны. Биологические данные Было показано, что соединения по изобретению обладают противоэпилептической активностью на примере их способности ингибировать разгибание задней конечности в модели выше максимального электрошока. Самцам крыс линии Han Wistar (150-200 мг) дозируют внутрибрюшинно суспензию тестируемого соединения в 0,25% метилцеллюлозе за 2 ч до тестирования. Визуальное наблюдение относительно наличия атаксии проводят непосредственно перед тестированием. Используя аурикулярные электроды, прикладывают ток 200 мА,продолжительность 200 миллисекунд, и отмечают наличие или отсутствие разгибания задней конечности. Соединения по изобретению продемонстрировали ЭД 50 в диапазоне от 1 до 20 мг/кг при тестировании в вышеуказанном тесте. В ходе вышеуказанного in vivo теста никаких явных неблагоприятных или токсических эффектов вследствие введения соединений по изобретению не наблюдалось. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I)R1 выбран из группы, состоящей из фенила, замещенного одним или более чем одним атомом галогена, нафтила и нафтила, замещенного одним или более чем одним атомом галогена;R4 выбран из группы, состоящей из водорода, -С 1-4 алкила, -С 1-4 алкила, замещенного одним или более чем одним атомом галогена, -CN,-СН 2 ОН, -CH2ORd и -CH2S(O)xRd; гдеRb и Rc, которые могут быть одинаковыми или разными, выбраны из водорода и С 1-4 алкила, или, вместе с атомом азота, к которому они присоединены, образуют 6-членный азотсодержащий гетероцикл, причем этот гетероцикл может быть далее замещен одним или более чем одним С 1-4 алкилом;Rd выбран из С 1-4 алкила или С 1-4 алкила,замещенного одним или более чем одним атомом галогена; х представляет собой целое число ноль,один или два; и его фармацевтически приемлемые производные; при условии, что R1 не представляет собой когда R2 представляет собой -NH2, a R3 и R4 оба представляют собой водород. 2. Соединение по п.1, где R1 представляет собой фенил, замещенный одним или более чем одним атомом галогена. 3. Соединение по п.2, где R1 представляет собой 2,3,5-трихлорфенил. 4. Соединение по любому из пп.1-3, где R2 3 и R представляют собой -NH2. 5. Соединение по любому из пп.1-4, где R4 представляет собой водород или -СН 2OН. 6. Соединение по п.5, где R4 представляет собой водород. 7. Соединение, которое представляет собой 2,6-диамино-3-(2,3,5-трихлорфенил)пиразин и его фармацевтически приемлемые производные. 8. Применение соединения по любому из пп.1-7 в терапии. 9. Фармацевтическая композиция, содержащая соединение по любому из пп.1-7 вместе с фармацевтически приемлемым носителем. 10. Применение соединения по любому из пп.1-7 в изготовлении лекарства для использования в лечении эпилепсии, биполярного расстройства или маниакальной депрессии, боли,нейродегенеративных заболеваний, в нейрозащите, в лечении нейродегенерации, или в предотвращении или уменьшении зависимости от вызывающего зависимость агента, или в предотвращении или уменьшении толерантности или обратной толерантности к вызывающему зависимость агенту. 11. Способ лечения пациента при необходимости нейрозащиты, или страдающего эпилепсией, биполярным расстройством или маниакальной депрессией, болью, нейродегенеративными заболеваниями, нейрозащитой, нейродегенерацией или восприимчивого к ним, или зависимого от вызывающего зависимость агента, или обладающего толерантностью или обратной толерантностью к вызывающему зависимость агенту, при котором вводят эффективное количество соединения по любому из пп.17. 12. Способ получения соединения формулы (I), как определено в п.1, при котором соединение формулы (II) где Hal (В) представляет собой атом галогена,подвергают соответствующим реакционным условиям; при этом соединения формулы (I) могут быть превращены в соответствующие соединения формулы (I) с использованием подходящих реакционных методик. 13. Способ получения соединения формулы (I), как определено в п.1, при котором соединение формулы (VII) 28 где Hal представляет собой атом галогена, подвергают взаимодействию с соединением формулы (IV) R1B(OH)2; при этом соединения формулы (I) могут быть превращены в соответствующие соединения формулы (I) с использованием подходящих реакционных методик. 14. Способ получения соединения формулы (I), как определено в п.1, при котором, еслиR2 представляет собой NН 2, то соединение формулы (XI) или его соль подвергают циклизации и окислению согласно общепринятым методикам; при этом соединения формулы (I) могут быть превращены в соответствующие соединения формулы (I) с использованием подходящих реакционных методик.
МПК / Метки
МПК: A61P 25/00, A61K 31/4965, C07D 241/20
Метки: аминоарилпиразинов, применение, производные
Код ссылки
<a href="https://eas.patents.su/15-2102-proizvodnye-aminoarilpirazinov-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Производные аминоарилпиразинов и их применение</a>
Предыдущий патент: Производные пиразола
Следующий патент: Усовершенствованный способ для получения противопаразитарного агента
Случайный патент: Ингибиторы 11-бета-гидроксистероид дегидрогеназы 1












