5, 6-диалкил-7-аминотриазолопиримидины, способ их получения и их применение для борьбы с патогенными грибами, а также содержащие их средства
Номер патента: 10411
Опубликовано: 29.08.2008
Авторы: Райнхаймер Йоахим, Шёфль Ульрих, Штирль Райнхард, Швёглер Аня, Шэфер Петер, Гевер Маркус, Шерер Мария, Вагнер Оливер, Мюллер Бернд, Тормо И Бласко Хорди, Шивек Франк, Блеттнер Карстен, Ниденбрюкк Маттиас, Штратманн Зигфрид, Грамменос Вассилиос, Гроте Томас
Формула / Реферат
1. Триазолопиримидины формулы I
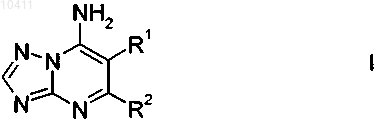
в которой заместители имеют следующие значения:
R1 означает С5-С12-алкил или С5-С14-алкоксиалкил, причем алифатические группы могут быть замещены от одной до трех следующих групп:
циано, нитро, гидрокси, С3-С6-циклоалкил, C1-С6-алкилтио и NRaRb;
Ra, Rb означают водород или C1-С6-алкил;
R2 означает этил, СН=СН2 или СН2СН=СН2.
2. Соединения формулы I по п.1, где R2 означает этил.
3. Соединения формулы I по п.1, где R1 означает незамещенную, неразветвленную или одно-, двух- или трехкратно разветвленную алкильную цепь с числом атомов углерода до 12.
4. Триазолопиримидины формулы I по п.1, выбранные из группы, включающей
5-этил-6-(1-метилгептил)[1,2,4]триазоло[1,5-a]пиримидин-7-иламин;
5-этил-6-окстил[1,2,4]триазоло[1,5-a]пиримидин-7-иламин;
5-этил-6-(3,5,5-триметилгексил)[1,2,4]триазоло[1,5-a]пиримидин-7-иламин;
5-этил-6-пентил[1,2,4]триазоло[1,5-a]пиримидин-7-иламин;
5-этил-6-гексил[1,2,4]триазоло[1,5-a]пиримидин-7-иламин;
5-этил-6-гептил[1,2,4]триазоло[1,5-a]пиримидин-7-иламин;
5-этил-6-нонил[1,2,4]триазоло[1,5-a]пиримидин-7-иламин;
5-этил-6-ундецил[1,2,4]триазоло[1,5-a]пиримидин-7-иламин;
5-этил-6-(3-пентилоксипропил)[1,2,4]триазоло[1,5-a]пиримидин-7-иламин.
5. Способ получения соединений формулы I по одному из пп.1-4, отличающийся тем, что сложный b-кетоэфир формулы II
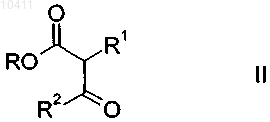
в которой R означает С1-С4-алкил, подвергают взаимодействию с 3-амино-1,2,4-триазолом формулы III
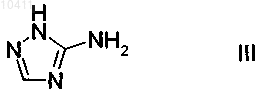
с получением 7-гидрокситриазолопиримидинов формулы IV
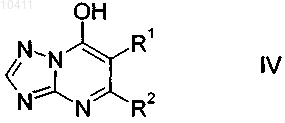
который галогенируют до соединений формулы V
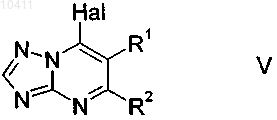
в которой Hal означает хлор или бром, и соединения формулы V подвергают взаимодействию с аммиаком.
6. Соединения формул IV и V по п.5, где R1 и R2 имеют значения, определенные в п.1.
7. Способ получения соединений формулы I по одному из пп.1-4, отличающийся тем, что ацилцианиды формулы VI
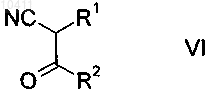
подвергают взаимодействию с 3-амино-1,2,4-триазолом формулы III по п.5.
8. Фунгицидное средство, содержащее твердый или жидкий наполнитель и соединение формулы I по одному из пп.1-4.
9. Посевной материал, содержащий соединение формулы I по одному из пп.1-4 в количестве от 1 до 1000 г на 100 кг.
10. Способ борьбы с фитопатогенными грибами, отличающийся тем, что грибы или подлежащие защите от поражения грибами материалы, растения, почву или посевной материал обрабатывают эффективным количеством соединения формулы I по одному из пп.1-4.
Текст
010411 Настоящее изобретение относится к 5,6-диалкил-7-аминотриазолопиримидинам формулы I в которой заместители имеют следующие значения:R1 означает С 5-С 12-алкил или С 3-С 14-алкоксиалкил, причем алифатические группы могут быть замещены посредством от одной до трех следующих групп: циано, нитро, гидрокси, С 3-С 6-циклоалкил, C1-С 6-алкилтио и NRaRb;Ra, Rb означают водород или C1-С 6-алкил;R3 означает водород, СН 3 или СН 2 СН 3. Кроме того, изобретение относится к способу получения этих соединений, к содержащим их средствам, а также к их применению для борьбы с фитопатогенными грибами. В документе GB 1148629 в общем предлагаются 5,6-диалкил-7-аминотриазолопиримидины. Из документа ЕР-А 141317 известны отдельные фунгицидно активные 5,6-диалкил-7-аминотриазолопиримидины. Их действие во многих случаях не удовлетворительно. Исходя из этого, в основу изобретения положена задача разработки соединений с улучшенным действием и/или с более широким спектром действия. В соответствии с этим были разработаны вышеприведенные соединения. Далее были разработаны способ и промежуточные продукты для их получения, содержащие их средства, а также способы борьбы с патогенными грибами при применении соединений I. Соединения формулы I отличаются от приведенных выше документов специальным выполнением заместителей в 5-положении скелета триазолопиримидина. Соединения формулы I имеют повышенную по отношению к известным соединениям эффективность против патогенных грибов. Соединения согласно изобретению могут быть получены различными путями. Предпочтительно соединения согласно изобретению получают таким образом, что замещенные сложные -кетоэфиры формулы II подвергают взаимодействию с 3-амино-1,2,4-триазолом формулы III с получением 7 гидрокситриазолопиримидинов формулы IV. Группы R1 и R2 в формулах II и IV имеют значения как для формулы I и группа R в формуле II означает C1-С 4 алкил, из практических соображений в ней предпочтителен метил, этил или пропил. Взаимодействие замещенных сложных -кетоэфиров формулы II с аминоазолами формулы III может осуществляться в присутствии или в отсутствии растворителей. Преимущественно применяют такие растворители, по отношению к которым исходные вещества в основном инертны и в них полностью или частично растворимы. В качестве растворителей пригодны, в частности, спирты, такие как этанол, пропанолы, бутанолы, гликоли или гликольмоноэфиры, диэтиленгликоли или их моноэфиры, ароматические углеводороды, такие как толуол, бензол или мезитилен, амиды, такие как диметилформамид, диэтилформамид, дибутилформамид, N,N-диметилацетамид, низшие алкановые кислоты, такие как муравьиная кислота, уксусная кислота, пропионовая кислота или основания, такие как гидроксиды щелочных и щелочно-земельных металлов, оксиды щелочных и щелочно-земельных металлов, гидриды щелочных и щелочно-земельных металлов, амиды щелочных металлов, карбонаты щелочных и щелочно-земельных металлов, а также гидрокарбонаты щелочных металлов, металлорганические соединения, в частности,алкилы щелочных металлов, галогениды алкилмагния, а также алкоголяты щелочных и щелочноземельных металлов и диметоксимагний, кроме того, органические основания, например, третичные амины, такие как триметиламин, триэтиламин, триизопропилэтиламин, трибутиламин и N-метилпиперидин,N-метилморфолин, пиридин, замещенные пиридины, такие как коллидин, лютидин и 4 диметиламинопиридин, а также бициклические амины и смеси этих растворителей с водой. В качестве катализаторов пригодны основания, приведенные выше, или кислоты, такие как сульфокислоты или минеральные кислоты. Особенно предпочтительно взаимодействие проводят без растворителя или в хлорбензоле, ксилоле, диметилсульфоксиде, N-метилпирролидоне. Особенно предпочтительными основаниями являются третичные амины, такие как триизопропиламин, трибутиламин, N-метилморфолин илиN-метилпиперидин. Температура реакции взаимодействия составляет от 50 и до 300 С, предпочтительно от 50 до 180 С, если применяется растворитель [см. ЕР-А 770615; Adv. Het. Chem. Bd. 57, с. 81 и д.(1993)]. Основания в основном применяются в каталитических количествах, они могут также применяться в эквимолярных количествах, в избытке или, в случае необходимости, в качестве растворителя. Полученные таким образом продукты конденсации формулы IV осаждаются из реакционного раствора в основном в чистой форме и после промывки тем же растворителем или водой и заключительной сушки подвергаются взаимодействию с агентом галогенирования, в частности, с агентом хлорирования или бромирования с получением соединений формулы V, в которой Hal означает хлор или бром, в частности хлор. Предпочтительно взаимодействие осуществляется с агентом хлорирования, таким как фосфороксихлорид, тионилхлорид или сульфурилхлорид при температуре от 50 до 150 С, предпочтительно в избыточном фосфорокситрихлориде при температуре кипения обратного холодильника. После испарения избыточного фосфорокситрихлорида остаток обрабатывается ледяной водой, в случае необходимости, при добавке не смешиваемого с водой растворителя. Выделенный из сухой органической фазы, в случае необходимости, после испарения инертного растворителя продукт хлорирования является в большинстве случаев очень чистым и затем подвергается взаимодействию с аммиаком в инертном растворителе при температуре от 100 до 200 С с получением 7-аминотриазоло[1,5-]пиримидинов. Реакция проводится предпочтительно с 1- до 10-молярным избытком аммиака при давлении от 1 до 100 бар. Новые 7-амино-азоло[1,5-]пиримидины выделяют, в случае необходимости, после испарения растворителя дигерированием в воде в качестве кристаллических соединений. Сложные -кетоэфиры формулы II могут быть получены, как описано в публикации Organic Synthesis Coll. Vol. 1, с. 248, соответственно, имеются в продаже. Новые соединения формулы I могут быть альтернативно получены таким образом, что замещенные ацилцианиды формулы VI, в которой R1 и R2 имеют вышеприведенные значения, подвергают взаимодействию с 3-амино-1,2,4-триазолом формулы III. Взаимодействие может осуществляться в присутствии или в отсутствии растворителей. Предпочтительно применять такие растворители, по отношению к которым исходные вещества в основном инертны и в которых они полностью или частично растворимы. В качестве растворителя пригодны, в частности,спирты, такие как этанол, пропанолы, бутанолы, гликоли или гликольмоноэфиры, диэтиленгликоли или их моноэфиры, ароматические углеводороды, такие как толуол, бензоли или мезитилен, амиды, такие как диметилформамид, диэтилформамид, дибутилформамид, N,N-диметилацетамид, низшие алкановые кислоты, такие как муравьиная кислота, уксусная кислота, пропионовая кислота или основания, приведенные выше, и смеси этих растворителей с водой. Температура реакции взаимодействия составляет от 50 и до 300 С, предпочтительно от 50 до 150 С,если применяется растворитель. Новые 7-амино-азоло[1,5-]пиримидины в случае необходимости после испарения растворителя или разбавления водой выделяются в качестве кристаллических соединений. Необходимые для получения 7-амино-азоло[1,5-]пиримидинов замещенные алкилцианиды формулы VI частично известны или могут быть получены известными методами из алкилцианидов и сложных эфиров карбоновой кислоты с сильными основаниями, например, алкилгидридами, алкоголятами щелочных металлов, алкалиамидами или алкиленами металлов (ср., например, публикацию: J. Amer.Chem. Soc. Bd. 73, (1951) S. 3766). Если отдельные соединения I не могут быть получены вышеописанными путями, они могут быть получены дериватизацией (образованием производных) других соединений формулы I. Если при синтезе имеются смеси изомеров, в общем разделение не обязательно необходимо, так как отдельные изомеры частично во время переработки для применения или при применении (например, под воздействием света, кислот или оснований) могут преобразовываться друг в друга. Соответствующие превращения могут происходить также после применения, например, при обработке растений в обработанном растении или в грибе, с которым ведут борьбу. При указанных в вышеприведенных формулах определениях обозначений применялись сборные понятия, которые в общем действительны для нижеследующих заместителей: галоген: означает фтор, хлор, бром и йод; алкил: означает насыщенные, неразветвленные или одно- или двукратно разветвленные углеводородные остатки с количеством атомов углерода от 1 до 4 или от 5 до 9, например, C1-С 6-алкил, такой как метил,этил, пропил, 1-метилэтил, бутил, 1-метилпропил, 2-метилпропил, 1,1-диметилэтил, н-пентил, 1-метилбутил,2-метилбутил, 3-метилбутил, 2,2-диметилпропил, 1-этилпропил, гексил, 1,1-диметилпропил, 1,2 диметилпропил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2 диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1-этилбутил, 2 этилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этил-1-метилпропил и 1-этил-2-метилпропил;-2 010411 галогенметил: означает метильную группу, в которой атомы водорода могут быть частично или полностью заменены атомами галогена, приведенного выше, в частности, хлорметил, бромметил, дихлорметил, трихлорметил, фторметил, дифторметил, трифторметил, хлорфторметил, дихлорфторметил,хлордифторметил; циклоалкил: означает моно- или бицикличные насыщенные углеводородные группы с углеродными членами кольца от 3 до 6, такие как циклопропил, циклобутил, циклопентил и циклогексил; алкоксиалкил: означает насыщенную, неразветвленную или одно-, двух- или трехкратно разветвленную углеводородную цепь, которая прервана атомом кислорода, например С 5-С 12-алкоксиалкил: углеводородная цепь, приведенная выше, с числом атомов углерода от 5 до 12, которая может быть прервана атомом кислорода в любом месте, такая как пропоксиэтил, бутоксиэтил, пентоксиэтил, гексилоксиэтил, гептилоксиэтил, окстилоксиэтил, нонилоксиэтил, 3-(3-этил-гексилокси)этил, 3-(2,4,4 триметилпентилокси)этил, 3-(1-этил-3-метил-бутокси)этил, этоксипропил, пропоксипропил, бутоксипропил, пентоксипропил, гексилоксипропил, гептилоксипропил, октилоксипропил, нонилоксипропил, 3(3-этил-гексилокси)пропил, 3-(2,4,4-триметил-пентилокси)пропил, 3-(1-этил-3-метил-бутокси)пропил,этоксибутил, пропоксибутил, бутоксибутил, пентоксибутил, гексилоксибутил, гептилоксибутил, октилоксибутил, нонилоксибутил, 3-(3-этил-гексилокси)бутил, 3-(2,4,4-триметил-пентилокси)бутил, 3-(1 этил-3-метил-бутокси)бутил, метоксипентил, этоксипентил, пропоксипентил, бутоксипентил, пентоксипентил,гексилоксипентил,гептилоксипентил,3-(3-метил-гексилокси)пентил,3-(2,4-диметилпентиокси)пентил, 3-(1-этил-3-метил-бутокси)пентил; В объем настоящего изобретения включены (R)- и (S)-изомеры и рацематы соединений формулы I,которые имеют центры хиральности. При учете применения триазолопиримидинов формулы I согласно их предназначению предпочтительны следующие значения заместителей, а именно как отдельно, так и в сочетании друг с другом. Предпочтительны соединения формулы I, при которых группа R1 имеет максимально 12 атомов углерода. Алкильные группы в остатке R1 в формуле I представляют собой неразветвленную или одно-, двухили трехкратно или более разветвленную, в частности неразветвленную алкильную группу. Наряду с этим предпочтительны соединения формулы I, в которой R1 на -углеродном атоме имеет одно разветвление. Они описываются формулой IaR12 означает C1-С 4-алкил, в частности, метил, причем R11 и R12 вместе имеют не более 12 атомов углерода и являются незамещенными или могут быть замещены как R1 в формуле I. Если R1 представляет собой замещенную посредством циано алкильную группу, то цианогруппа находится предпочтительно на конечном атоме углерода. Предпочтительны соединения формулы I, в которых R1 означает неразветвленную или одно-, двух-,трех- или многократно разветвленную С 5-С 12-алкильную группу, которая больше не имеет заместителей. При одной форме выполнения соединений согласно изобретению формулы I остаток R1 означает С 5-С 12-алкил или C1-С 11-алкокси-C1-С 11-алкил, причем общее число атомов углерода предпочтительно имеет значение от 5 до 12. При этом С 2-С 9-алкоксипропилгруппы особенно предпочтительны. Особенно предпочтительны соединения формулы I, в которых R1 означает н-пентил, 1-метилбутил, 2 метилбутил, 3-метилбутил, 2,2-диметилпропил, 1-этилпропил, н-гексил, 1,1-диметилпропил, 1,2 диметилпропил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2 диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1-этилбутил, 2 этилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этил-1-метилпропил или 1-этил-2-метилпропил. Наряду с этим предпочтительны соединения формулы I, в которых R1 означает н-гептил, 1 метилгексил, н-октил, 1-метилгептил, н-нонил, 1-метилоксил и 3,5,5-триметилгексил, н-децил, 1 метилнонил, н-ундецил, 1-метилдецил, н-додецил и 1-метилундецил. При особенной форме выполнения соединений согласно изобретению формулы I остаток R2 означает этил. При еще одной особенной форме выполнения соединений согласно изобретению формулы I остатокR2 означает изопропил. При еще одной особенной форме выполнения соединений согласно изобретению формулы I остатокR2 означает 1-метил-пропил. При еще одной особенной форме выполнения соединений согласно изобретению формулы I остатокR2 означает циклопропил. Особенно в отношении их применения предпочтительны приведенные в нижеследующей таблице соединения формулы I. Названные в таблице для одного заместителя группы представляют собой осо-3 010411 бую форму выполнения соответствующего заместителя.I-1 Соединения формулы I, в которых R1 соответствует одной строке табл. А и R2 означает этил.I-2 Соединения формулы I, в которых R1 соответствует одной строке табл. А и R2 означает изопропил.I-3 Соединения формулы I, в которых R1 соответствует одной строке табл. А и R2 означает 1-метилпропил.I-4 Соединения формулы I, в которых R1 соответствует одной строке табл. А и R2 означает этилен.I-5 Соединения формулы I, в которых R1 соответствует одной строке табл. А и R2 означает аллил.I-6 Соединения формулы I, в которых R1 соответствует одной строке табл. А и R2 означает циалопропил. Таблица А Соединения формулы I пригодны в качестве фунгицидов. Они отличаются прекрасным действием против широкого спектра фитопатогенных грибов из класса Ascomyceten, Deuteromyceten, Oomyceten иBasidiomyceten, в особенности из класса Oomyceten. Они частично эффективны систематически и могут применяться при защите растений в качестве лиственных, почвенных фунгицидов, а также протравливающих фунгицидов. Они имеют особое значение при борьбе с множеством грибов на различных культурных растениях,таких как пшеница, рожь, ячмень, овес, рис, кукуруза, дернина, бананы, хлопчатник, соя, кофе, сахарный тростник, виноград, плодовые культуры и декоративные растения и овощные культуры, такие как огурцы, бобовые, картофель и тыквенные, а также на семенах этих растений. Особенно они пригодны для борьбы со следующими болезнями растений: виды Alternaria на овощных и плодовых культурах,виды Bipolaris- и Drechslera на зерновых, рисе и дернине,Blumeria graminis (настоящая мучнистая роса) на зерновых,Botrytis cinerea (серая гниль) на клубнике, овощных и декоративных культурах и на виноградных лозах,Bremia lactucae на салате,Erysiphe cichoracearum и Sphaerotheca fuliginea на тыквенных растениях,виды Fusarium- и Verticillium на различных растениях,виды Mycosphaerella на зерновых, бананах и земляном орехе,виды Peronospora на капусте и луке,-8 010411Phakopsora pachyrhizi и P. meibomiae на сое,Phytophthora infestans на картофеле и томатах,Phytophthora capsici на сладком перце,Plasmopara viticola на виноградных лозах,Podosphaera leucotricha на яблонях,Pseudocercosporella herpotrichoides на пшенице и ячмене,виды Pseudoperonospora на хмеле и огурцах,Puccinia-Arten на зерновых культурах,Pyricularia oryzae на рисе,Pythium aphanidermatum на дернине,виды Rhizoctonia-Arten на хлопчатнике, рисе и дернине,Septoria tritici und Stagonospora nodorum на пшенице,Uncinula necator на виноградных лозах,виды Ustilago на зерновых и сахарном тростнике, а также виды Venturia (парша) на яблонях и грушах. В особенности они пригодны для борьбы с патогенными грибами из класса Oomyceten, такими как виды Peronospora, виды Phytophthora, виды Plasmopara viticola и Pseudoperonospora. Соединения формулы I пригодны, кроме того, для борьбы с такими патогенными грибами, как Paecilomyces variotii при защите материалов (например, древесины, бумаги, дисперсий для покрытий, волокон, соответственно, тканей) и при защите запасов. Соединения формулы I применяются таким образом, что грибы или подлежащие защите от поражения грибами растения, посевной материал, материалы или почву обрабатывают фунгицидно активным количеством действующего вещества. Применение может осуществляться как перед, так и после инфекции грибами материалов, растений или семян. Фунгицидные средства содержат в общем между 0,1 и 95, предпочтительно между 0,5 и 90 вес.% действующего вещества. Нормы расхода при применении при защите растений в зависимости от вида желаемого эффекта составляют между 0,01 и 2,0 кг действующего вещества на 1 га. При обработке посевного материала в общем требуется количество действующего вещества от 1 до 1000 г/100 кг, предпочтительно от 5 до 100 г/100 кг посевного материала. При применении для защиты материалов, соответственно, запасов нормы расхода ориентируется на область применения и желаемый эффект. Обычно нормы расхода при защите материалов составляют,например, от 0,001 г до 2 кг, предпочтительно от 0,005 г до 1 кг действующего вещества на 1 м 2 обрабатываемого материала. Соединения формулы I могут быть переведены в обычные препаративные формы, например, растворы, эмульсии, суспензии, тонкие порошки, порошки, пасты и грануляты. Форма применения ориентируется на цель применения; в любом случае она должна обеспечивать тонкое и равномерное распределение соединения согласно изобретению. Композиции согласно изобретению приготавливаются известным образом, например разбавлением действующего вещества растворителями и/или наполнителями, по желанию с применением эмульгаторов и диспергаторов. В качестве растворителей/вспомогательных агентов пригодны, в основномI-1 вода, ароматические растворители (например, продукты Solvesso, ксилол), парафины (например, фракции сырой нефти), спирты (например, метанол, бутанол, пентанол, бензиловый спирт), кетоны (например, циклогексанон, гамма-бутриолактон), пирролидоны (Nметилпирролидон, N-октилпирролидон), ацетаты (гликольдиацетат), гликоли, амиды диметиловых кислот жирного ряда, кислоты жирного ряда и сложные эфиры кислот жирного ряда. В принципе могут применяться также и смеси растворителей;I-2 наполнители, такие как природные горные породы (например, каолины, глинозем, тальк, мел) и синтетические горные породы (например, высокодисперсная кремниевая кислота, силикаты); эмульгаторы, такие как неионогенные и анионные эмульгаторы (например, простые эфиры полиоксиэтиленовых спиртов жирного ряда, алкилсульфонаты и арилсульфонаты) и диспергаторы, такие как лигнинсульфитные отработанные щелочи или метилцеллюлоза. В качестве поверхностно-активных веществ пригодны щелочные, щелочно-земельные, аммониевые соли лингнинсульфокислоты, фенолсульфокислоты, нафталин-сульфокислоты, дибутилнафталинсульфокислоты, алкиларилсульфонаты, алкилсульфонаты, алкилсульфаты, сульфаты спиртов жирного ряда,жирные кислоты и сульфатированные гликолевые эфиры спиртов жирного ряда, далее продукты конденсации сульфонированного нафталина или его производных с формальдегидом, продукты конденсации нафталина, соответственно нафталинсульфокислоты с фенолом или формальдегидом, полиоксиэтиленоктилфенольный эфир, этоксилированный изооктилфенол, октилфенол, нонилфенол, алкилфенолполигликолевый эфир, трибутилфенилполигликолевый эфир, тристерилфенилполигликолевый эфир, алкиларилполиэфирные спирты, конденсаты этиленоксида спирта жирного ряда, этоксилированное касторовое масло, полиоксиэтиленалкиловый эфир или полиоксипропилен, полигликольэфирный ацетат лауриловых-9 010411 спиртов, сложный эфир сорбита, лигнинсульфитные отработанные щелочи или метилцеллюлоза. Для получения непосредственно распрыскиваемых растворов, эмульсий, паст или маслянных дисперсий пригодны фракции минеральных масел со средней до высокой точек кипения, такие как керосин или дизельное масло, далее каменно-угольные масла, а также масла растительного или животного происхождения, алифатические, циклические или ароматические углеводороды, например толуол, ксилол, парафин, тетрагидронафталин, алкилированные нафталины или их производные, метанол, этанол, пропанол, бутанол, циклогексанол, циклогексанон, изофорон, сильно полярные растворители, например, диметилсульфоксид, N-метилпирролидон или вода. Порошок, препарат для распыления и опудривания можно получить посредством смешения или совместного размола действующих веществ с твердым носителем. Гранулят, например покрытый, пропитанный или гомогенный, получают обычно посредством соединения действующих веществ с твердым наполнителем. В качестве твердых наполнителей служат,например, минеральные земли, такие как силикагель, силикаты, тальк, каолин, известняк, известь, мел,болюс, лсс, глина, доломит, диатомовая земля, сульфат кальция, сульфат магния, оксид магния, размолотые пластмассы, а также такие удобрения, как сульфаты аммония, фосфаты аммония, нитраты аммония, мочевины и растительные продукты, такие как, например, мука зерновых культур, мука древесной коры, древесная мука и мука ореховой скорлупы, целлюлозный порошок или другие твердые наполнители. Готовые композиции содержат в общем от 0,01 до 95 мас.%, предпочтительно от 0,1 до 90 мас.% действующего вещества. Действующие вещества применяются при этом с чистотой от 90 до 100%, предпочтительно от 95 до 100% (по спектру ЯМР). Примеры для композиций. 1. Продукты для разбавления в воде. А. Водорастворимые концентраты (SL). 10 вес.ч. соединения согласно изобретению растворяют в воде или в водорастворимом растворителе. Альтернативно добавляют смачивающий агент или другие вспомогательные агенты. При разбавлении в воде действующее вещество растворяется. В. Способные к диспергированию концентраты (DC). 20 вес.ч. соединения согласно изобретению растворяют в циклогексаноне при добавке диспергатора, например поливинилпирролидона. При разбавлении в воде получают дисперсию. С. Способные к эмульгированию концентраты (ЕС). 15 вес.ч. соединения согласно изобретению растворяют в ксилоле при добавке Ca-додецилбензолсульфоната и этоксилата касторового масла (по 5% каждого). При разбавлении в воде образуется эмульсия.D. Эмульсии (EW, ЕО). 40 вес.ч. соединения согласно изобретению растворяют в ксилоле при добавке Ca-додецилбензолсульфоната и этоксилата касторового масла (по 5% каждого). Эту эмульсию вводят в воду с помощью эмульгирующего устройства (Ultraturax) и доводят до гомогенной эмульсии. При разбавлении в воде образуется эмульсия. Е. Суспензии (SC, OD). 20 вес.ч. соединения согласно изобретению измельчают при добавке диспергатора и смачивающего агента и воды или органического растворителя в шаровой мельнице с мешалкой. При разбавлении в воде образуется стабильная суспензия действующего вещества.F. Диспергируемый в воде и растворимый в воде гранулят (WG, SG). 50 вес.ч. соединения согласно изобретению тонко измельчают при добавке диспергатора и смачивающего агента и посредством технических устройств (например, экструзионного устройства, распылительной башни, псевдоожиженного слоя) получают диспергируемый в воде или водорастворимый гранулят. При разбавлении в воде образуется стабильная дисперсия или раствор действующего вещества.G. Диспергируемый в воде и растворимый в воде порошок (WP, SP). 75 вес.ч. соединения согласно изобретению перемалываются при добавке диспергатора и смачивающего агента, а также силикагеля в роторно-статорной мельнице. При разбавлении в воде образуется стабильная дисперсия или раствор действующего вещества.I.1 Продукты для непосредственного применения.H. Порошки (DP). 5 вес.ч. соединения согласно изобретению тонко измельчают и тщательно перемешивают с 95% тонкого каолина. Таким образом получают средство распыления.I. Грануляты (GR, FG, GG, MG). 0,5 вес.ч. соединения согласно изобретению тонко измельчают и связывают с 95,5% наполнителей. Обычным способом при этом является экструзия, распылительная сушка или псевдоожиженный слой. Получают гранулят для непосредственного применения.J. ULV-растворы (UL). 10 вес.ч. соединения согласно изобретению растворяют в органическом растворителе, например- 10010411 ксилоле. Получают продукт для непосредственного применения. Действующие вещества могут применяться как таковые, в форме своих препаративных форм или в приготовляемых из них формах, например, приготавливаться в форме предназначенных для непосредственного опрыскивания растворов, порошков, суспензий или дисперсий, эмульсий, масляных дисперсий,паст, препаратов для опыливания, препаратов для опудривания или гранулятов и могут применяться путем опрыскивания, мелкокапельного опрыскивания, опыливания, опудривания или полива. Используемые формы зависят от цели применения, но во всех случаях должно быть обеспечено максимально тонкое и равномерное распределение действующих веществ по изобретению. Водные композиции могут приготавливаться из концентратов эмульсий, паст или смачиваемых порошков (распыляемые порошки, масляные дисперсии) посредством добавки воды. Для получения эмульсий, паст или масляных дисперсий вещества могут как таковые или растворенные в масле или растворителе гомогенизироваться в воде посредством смачивающих агентов, адгезионных составов, диспергаторов или эмульгаторов. Также могут приготавливаться состоящие из действующих веществ и смачивающих агентов, адгезионных составов, диспергаторов или эмульгаторов или масла концентраты, которые пригодны для разведения водой. Концентрации действующих веществ в композициях могут варьироваться в широком диапазоне. В общем такие концентрации составляют от 0,0001 и до 10%, предпочтительно от 0,01 и до 1%. Действующие вещества могут также использоваться с хорошим успехом в способе с низкими объемами применения Ultra-Low-Volume (ULV), причем возможно применение композиций с более чем 95 вес.% действующего вещества или даже действующего вещества без добавок. К действующим веществам могут примешиваться масла различных типов, смачивающие агенты,добавки, гербициды, фунгициды, другие пестициды, бактерициды, в случае необходимости, непосредственно перед применением (смесь в баке). Эти средства могут примешиваться к средствам согласно изобретению в весовом соотношении 1:10 до 10:1. Средства согласно изобретению при форме применения как фунгициды могут содержать также и другие действующие вещества, например гербициды, инсектициды, регуляторы роста или же удобрения. При смешивании соединений формулы I, соответственно содержащих их средств в форме применения как фунгициды, с другими фунгицидами получают во многих случаях увеличение спектра фунгицидного действия. Нижеследующий перечень фунгицидов, вместе с которыми могут применяться соединения согласно изобретению, поясняет возможности комбинации, не сужая их: ацилаланины, такие как беналаксил, металаксил, офураце, оксадиксил; производные амина, такие как альдиморф, додин, додеморф, фенпропиморф, фенпропидин, гуазатин, иминоктадин, спироксамин, тридеморф; анилинопиримидины, такие как пириметанил, мепанипирим или ципродинил; антибиотики, такие как циклогексимид, гризеофульвин, казугамицин, натамицин, полиоксин или стрептомицин; азолы, такие как битертанол, бромоконазол, ципроконазол, дифеноконазол, динитроконазол, энилконазол, эпоксиконазол, фенбуконазол, флуквиконазол, флузилазол, флутриафол, гексаконазол, имазалил, ипконазол, метконазол, миклобутанил, пенконазол, пропиконазол, прохлорац, протиоконазол, симеконазол, тетраконазол, тебуконазол, триадимефон, триадименол, трифлумизол, тритиконазол; дикарбоксимиды, такие как ипродион, миклозолин, процимидон, винклозолин; дитиокарбаматы, такие как фербам, набам, манеб, манкозеб, метам, метирам, пропинеб, поликарбамат, тирам, зирам, зинеб; гетероциклические соединения, такие как анилазин, беномил, боскалид, карбендазим, карбоксим,оксикарбоксин, циазофамид, дазомет, дитианон, фамоксадон, фенамидон, фенаримол, фуберидазол, флутолинил, фураметпир, изопропиолан, мепронил, нуаримол, пробеназол, пироквиилон, сильтиофам, тиабендазол, тифлузамид, тиофанат-метил, тиадинил, трициклазол, трифорин; медьсодержащие фунгициды, такие как бородосская жидкость, ацетат меди, оксихлорид меди, основный сульфат меди; нитрофениловые производные, такие как бинапакрил, динокап, динобутон, нитрофтал-изопропил; фенилпирролы, такие как фенпиконил или флудиоксонил; сера; прочие фунгициды, такие как ацибензолар-S-метил, бентиаваликарб, карпропамид, хлороталонил,цифлуфенамид, цимоксанил, дикломезин, диклоцимет, диэтофенкарб, эдифенфос, этабоксам, фенгексамид, фентин-ацетат, феноксанил, феримзон, флуазинам, фосфористая кислота, фосетил, фозетиалюминий, ипроваликарб, гексахлорбензол, метрафенон, пенцикурон, пропамокарб, фталид, толоклофосметил, квинтоцен, зоксамид; стробилурины, такие как озоксистробин, димоксистробин, энестробурин, флуоксастробин, крезоксим-метил, метоминостробин, орисастробин, пикозистробин, пираклостробин или трифлоксистробин; производные сульфеновой кислоты, такие как каптафол, каптан, дихлофлуанид, фолпет, толифлуанид;- 11010411 амиды коричной кислоты и аналоги, такие как диметоформ, флуметовер или флуморф. Примеры синтеза. Отраженные в нижеприведенных примерах синтеза приемы при соответствующем изменении исходных соединений использовались для получения других соединений формулы I. Полученные таким образом соединения приведены в нижеследующей таблице с физическими данными. Пример 1. Получение 4-циано-ундекан-3-она. Раствор из 0,45 моль деканитрила в 300 мл тетрагидрофурана (THF) смешивают при -70 С с раствором 0,495 моль бутиллития в гексане, потом перемешивают в течение 3 ч при этой температуре и добавляют 0,45 моль сложного этилового эфира пропионовой кислоты. Затем реакционную смесь перемешивают еще 16 ч при 20-25 С, потом смешивают с 200 мл воды и подкисляют раствором разбавленнойHCl. После разделения фаз органическую фазу отделяют, промывают водой, сушат и освобождают от растворителя. Остается 91 г указанного в заголовке соединения. Пример 2. Получение 7-амино-5-этил-6-октил[1,2,4]триазоло[1,5-]пиримидина. Смесь, состоящую из 5-циано-ундекан-3-она из примера 1, 3-амино-1,2,4-триазола по 1,27 моль каждый и из 0,25 моль п-толуолсульфокислоты в 900 мл мезитилена нагревают в течение 4 ч до 170 С. После охлаждения до 20-25 С отфильтровывают осадок, который затем загружают в дихлорметан. Из раствора после промывания водой и сушки отгоняют растворитель, в качестве остатка имеются 124 г указанного в заголовке соединения с т.пл. 196 С. Таблица I Соединения формулы I Примеры активности против патогенных грибов. Фунгицидное действие соединения формулы I можно показать с помощью следующих экспериментов. Действующие вещества подготавливают в качестве основного раствора из 25 мг действующего вещества, который дополняют смесью ацетона и/или диметилсульфоксида и эмульгатора Uniperol EL(смачивающий агент с эмульгирующим и диспергирующим действием на базе этоксилированных алкилфенолов) в объемном соотношении от 99 к 1 до 10 мл, затем дополняют до 100 мл водой. Этот основной раствор разбавляют описанной смесью растворителя и эмульгатора в соответствии с нижеуказанной концентрацией. Пример применения 1. Эффективность против пероноспоры виноградных лоз, вызванной Plasmopara viticola. Листья выращенных в горшках ростков виноградных лоз опрыскивают до образования капель водной суспензией с нижеуказанной концентрацией действующего вещества. На следующий день нижнюю сторону листьев инокулируют водным раствором зооспор Plasmopara viticola. После этого виноградные лозы ставят сначала на 48 ч в насыщенную водяным паром камеру при температуре 24 С и затем на 5 дней в теплицу с температурой между 20 и 30 С. По окончании этого времени растения для ускорения вспышки спорангиеносцев ставят еще раз на 16 ч во влажную камеру. Потом визуально определяют степень развития поражения на нижней стороне листьев.- 12010411 В этом эксперименте обработанные посредством 250 млн ч. соединений растения I-1, соответственно I-2 не проявляют поражения, в то время как необработанные растения поражены на 90%. Пример применения 2. Активность против фитофтороза на томатах, вызванного Phytophthora infestans при защитной обработке. Листья растений томатов опрыскивают водной суспензией действующих веществ до образования капель. На следующий день листья инфицируют водной суспензией спорангиеносцев Phytophthora infestans. Затем растения ставят в насыщенную водяным паром камеру при температуре между 18 и 20 С. Через 6 дней фитофтороз на необработанных, однако инфицированных контрольных растениях развился так сильно, что можно было визуально определить поражение в %. В этом эксперименте обработанные посредством 250 млн ч. соединений I-1, I-2, I-8, I-9, I-10, bzw. I11 растения не имели поражения, в то время как необработанные растения были поражена на 100%. Пример применения 3. Эффективность против пероноспоры виноградных лоз, вызванной Plasmopara viticola при защитной обработке. Листья выращенных в горшках ростков виноградных лоз сорта "Muller-Thurgau" опрыскивают до образования капель водной суспензией с нижеуказанной концентрацией действующего вещества. Чтобы оценить длительное действие веществ, растения после подсыхания напрысканного слоя ставят на 7 дней в теплице. Только после этого листья инокулируют водным раствором зооспор Plasmopara viticola. После этого виноградные лозы ставят сначала на 48 ч в насыщенную водяным паром камеру при температуре 24 С и затем на 5, соответственно 7 дней в теплицу с температурой между 20 и 30 С. По окончании этого времени растения для ускорения вспышки спорангиеносцев ставят еще раз на 16 ч во влажную камеру. Потом визуально определяют степень развития поражения на нижней стороне листьев. В эксперименте с 5 днями защитного применения обработанные посредством 250 млн ч. соединений растения I-4 проявляют 3% поражения, в то время как необработанные растения поражены на 75%. В эксперименте с 5 днями защитного применения обработанные посредством 250 млн ч. соединений растения I-8, I-9, I-10, I-11, I-12, соответственно I-13 имеют максимально 7% поражения, в то время как необработанные растения были поражены на 80%. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Триазолопиримидины формулы I в которой заместители имеют следующие значения:R1 означает С 5-С 12-алкил или С 5-С 14-алкоксиалкил, причем алифатические группы могут быть замещены от одной до трех следующих групп: циано, нитро, гидрокси, С 3-С 6-циклоалкил, C1-С 6-алкилтио и NRaRb;Ra, Rb означают водород или C1-С 6-алкил;R2 означает этил, СН=СН 2 или СН 2 СН=СН 2. 2. Соединения формулы I по п.1, где R2 означает этил. 3. Соединения формулы I по п.1, где R1 означает незамещенную, неразветвленную или одно-, двухили трехкратно разветвленную алкильную цепь с числом атомов углерода до 12. 4. Триазолопиримидины формулы I по п.1, выбранные из группы, включающей 5-этил-6-(1-метилгептил)[1,2,4]триазоло[1,5-]пиримидин-7-иламин; 5-этил-6-окстил[1,2,4]триазоло[1,5-]пиримидин-7-иламин; 5-этил-6-(3,5,5-триметилгексил)[1,2,4]триазоло[1,5-]пиримидин-7-иламин; 5-этил-6-пентил[1,2,4]триазоло[1,5-]пиримидин-7-иламин; 5-этил-6-гексил[1,2,4]триазоло[1,5-]пиримидин-7-иламин; 5-этил-6-гептил[1,2,4]триазоло[1,5-]пиримидин-7-иламин; 5-этил-6-нонил[1,2,4]триазоло[1,5-]пиримидин-7-иламин; 5-этил-6-ундецил[1,2,4]триазоло[1,5-]пиримидин-7-иламин; 5-этил-6-(3-пентилоксипропил)[1,2,4]триазоло[1,5-]пиримидин-7-иламин. 5. Способ получения соединений формулы I по одному из пп.1-4, отличающийся тем, что сложный который галогенируют до соединений формулы V в которой Hal означает хлор или бром, и соединения формулы V подвергают взаимодействию с аммиаком. 6. Соединения формул IV и V по п.5, где R1 и R2 имеют значения, определенные в п.1. 7. Способ получения соединений формулы I по одному из пп.1-4, отличающийся тем, что ацилцианиды формулы VI подвергают взаимодействию с 3-амино-1,2,4-триазолом формулы III по п.5. 8. Фунгицидное средство, содержащее твердый или жидкий наполнитель и соединение формулы I по одному из пп.1-4. 9. Посевной материал, содержащий соединение формулы I по одному из пп.1-4 в количестве от 1 до 1000 г на 100 кг. 10. Способ борьбы с фитопатогенными грибами, отличающийся тем, что грибы или подлежащие защите от поражения грибами материалы, растения, почву или посевной материал обрабатывают эффективным количеством соединения формулы I по одному из пп.1-4.
МПК / Метки
МПК: A01P 21/00, C07D 487/04
Метки: способ, патогенными, грибами, 6-диалкил-7-аминотриазолопиримидины, также, средства, борьбы, получения, применение, содержащие
Код ссылки
<a href="https://eas.patents.su/15-10411-5-6-dialkil-7-aminotriazolopirimidiny-sposob-ih-polucheniya-i-ih-primenenie-dlya-borby-s-patogennymi-gribami-a-takzhe-soderzhashhie-ih-sredstva.html" rel="bookmark" title="База патентов Евразийского Союза">5, 6-диалкил-7-аминотриазолопиримидины, способ их получения и их применение для борьбы с патогенными грибами, а также содержащие их средства</a>
Предыдущий патент: Получение производных соединения 1,3-дифенилпроп-2-ен-1-он
Следующий патент: Трехфазный двигатель переменного тока с регулируемой скоростью
Случайный патент: Фунгицидные и биорегуляторные смеси