Способы и композиции для стимуляции роста невритов
Формула / Реферат
1. Фармацевтически приемлемая композиция, содержащая
а) нейротрофическое количество соединения, имеющего структурную формулу (I)
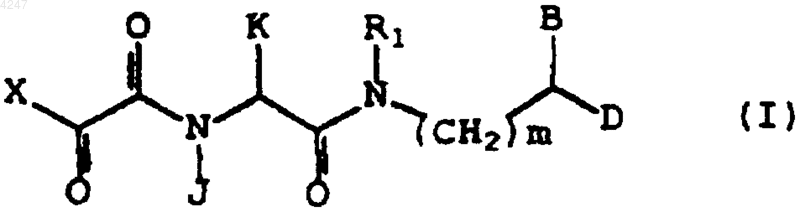
и его фармацевтически приемлемые производные,
где R1, B и D - это независимо водород, Ar, линейный или разветвленный алкил (C1-C6), линейный или разветвленный алкенил или алкинил (C2-C6), замещенный циклоалкилом (C5-C7) линейный или разветвленный алкил (C1-C6), замещенный циклоалкилом (C5-C7) линейный или разветвленный алкенил или алкинил (C3-C6), замещенный циклоалкенилом (C5-C7) линейный или разветвленный алкил (C1-C6), замещенный циклоалкиленом (C5-C7) линейный или разветвленный алкенил или алкинил (C3-C6), Ar-замещенный линейный или разветвленный алкил (C1-C6), Ar-замещенный линейный или разветвленный алкенил или алкинил (C3-C6);
при условии, что R1 не является водородом или линейным или разветвленным алкилом (C1-C6); и
где любая из групп CH2 указанных алкильных цепочек с R1, B и D необязательно заменена на O, S, SO, SO2 и NR;
где R - это водород, линейный или разветвленный алкил (C1-C6), линейный или разветвленный алкенил или алкинил (C3-C4) или мостиковый алкил (C1-C4), в котором мостик образован между азотом и атомом углерода указанной алкильной цепочки, образуя кольцо, и в котором указанное кольцо необязательно конденсировано с Ar;
где каждый Ar независимо выбирают из фенила, 1-нафтила, 2-нафтила, инденила, азуленила, флуоренила и антраценила, 2-фурила, 3-фурила, 2-тиенила, 3-тиенила, 2-пиридила, 3-пиридила, 4-пиридила, пирролила, оксазолила, тиазолила, имидазолила, пиразолила, 2-пиразолинила, пиразолидинила, изоксазолила, изотриазолила, 1,2,3-оксадиазолила, 1,2,3-триазолила, 1,3,4-тиадиазолила, пиридазинила, пиримидинила, пиразинила, 1,3,5-триазинила, 1,3,5-тритианила, индолизинила, индолила, изоиндолила, 3H-индолила, индолинила, бензо[b]фуранила, бензо[b]тиофенила, 1H-индазолила, бензимидазолила, бензтиазолила, пуринила, 4H-хинолизинила, хинолинила, 1,2,3,4-тетрагидроизохинолинила, изохинолинила, 1,2,3,4-тетрагидрохинолинила, циннолинила, фталазинила, хиназолинила, хиноксалинила, 1,8-нафтиридинила, птеридинила, карбазолила, акридинила, феназинила, фенотиазинила или феноксазинила и
где каждый Ar необязательно и независимо замещен 1-3 заместителями независимо выбранными из водорода, галогена, гидроксила, нитро-, -SO3H, трифторметила, трифторметокси, линейного или разветвленного алкила (C1-C6), O-(линейного или разветвленного алкила (C1-C6)), O-бензила, O-фенила, 1,2-метилендиокси, -NR5R6, карбоксила, N-(линейного или разветвленного алкила (C1-C6))карбоксамида или N-(линейного или разветвленного алкенила (C3-C5) карбоксамида, N,N-ди-((линейного или разветвленного алкила (C1-C6))карбоксамида или N,N-ди-((линейного или разветвленного алкенила (C3-C5))карбоксамида, морфолинила, пиперидинила, O-M, CH2-(CH2)q-M, O-(CH2)q-M, (CH2)q-O-M или CH=CH-M;
где R5 и R6 независимо выбирают из группы, состоящей из водорода, линейного или разветвленного алкила (C1-C6), линейного или разветвленного (C2-C6) алкенила или алкинила, бензила, или R5 и R6 могут вместе образовывать 5-7-членное гетероциклическое кольцо;
M выбирают из группы, состоящей из 4-метоксифенила, 2-пиридила, 3-пиридила, 4-пиридила, пиразила, хинолила, 3,5-диметилизоксазолила, 2-метилтиоазолила, тиазоила, 2-тиенила, 3-тиенила, 4-тиенила или пиримидила; и
q равно 0-2;
J выбирают из группы, состоящей из линейного или разветвленного алкила (C1-C6), линейного или разветвленного алкенила или алкинила (C3-C6), Ar-замещенного линейного или разветвленного алкила (C1-C6), Ar-замещенного линейного или разветвленного алкенила или алкинила (C3-C6) и циклогексилметила;
K выбирают из группы, состоящей из линейного или разветвленного алкила (C1-C6), Ar-замещенного линейного или разветвленного алкила (C1-C6), линейного или разветвленного алкенила или алкинила (C2-C6) и Ar-замещенного линейного или разветвленного алкенила или алкинила (C3-C6); или
J и K вместе с атомами азота и углерода, с которыми они соответственно связаны, образуют 5-7-членное гетероциклическое кольцо, которое может содержать гетероатом, выбранный из O, S, SO и SO2;
X выбирают из группы, состоящей из Ar, -OR2 и -N(R3)R4;
где R2 имеет те же значения, что R1;
R3 и R4 независимо имеют те же значения, что B и D соответственно или R3 и R4 вместе образуют 5-7-членное гетероциклическое алифатическое или ароматическое кольцо и
m равен 0 или 1;
б) нейротропный фактор и
в) фармацевтически приемлемый носитель.
2. Фармацевтически приемлемая композиция по п.1, в которой указанное соединение имеет структурную формулу
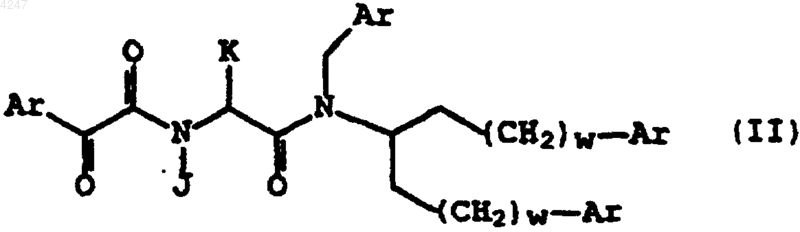
где J и K независимо являются линейным или разветвленным алкилом (C1-C6) или Ar-замещенным линейным или разветвленным алкилом (C1-C6) и w равно 1 или 2.
3. Фармацевтически приемлемая композиция по п.1, в которой по меньшей мере один из B или D независимо представлен формулой -(CH2)r-Z-(CH2)s-Ar,
где r равно 1-4;
s равно 0-1 и
каждый Z независимо выбирают из группы, состоящей из O, S, SO, SO2 и NR, где R выбирают из группы, состоящей из водорода, линейного или разветвленного алкила (C1-C4), линейного или разветвленного алкенила или алкинила (C3-C4) и мостикового алкила (C1-C4), где мостик образован между азотом и Ar-группой.
4. Фармацевтически приемлемая композиция по п.3, в которой указанное соединение имеет структурную формулу

где J и K независимо являются линейным или разветвленным алкилом (C1-C6) или Ar-замещенным линейным или разветвленным алкилом (C1-C6).
5. Фармацевтически приемлемая композиция по п.1, в которой
каждый Ar независимо выбирают из фенила, 2-пиридила, 3-пиридила, 4-пиридила, имидазолила, индолила, изоиндолила, хинолинила, изохинолинила, 1,2,3,4-тетрагидроизохинолинила или 1,2,3,4-тетрагидрохинолинила и
каждый Ar необязательно содержит 1-3 заместителя, независимо выбранных из гидроксила, нитро-, трифторметила, линейного или разветвленного алкила (C1-C6), O-(линейного или разветвленного алкила (C1-C6)), галогена, SO3H или -NR3R4.
6. Фармацевтически приемлемая композиция по п.2, в которой указанное соединение выбирают из соединений 6-10, 12, 16-19, 21 или 23 приведенной ниже таблицы.

| Соед. | B | D | K | R1 |
| 6 | 4-Pyr-(CH2)2- | 4-Pyr-(CH2)2- | PhCH2- | 4-F-PhCH2- |
| 7 | 4-Pyr-(CH2)2- | 4-Pyr-(CH2)2- | PhCH2- | PhCH2- |
| 8 | 4-Pyr-(CH2)2- | 4-Pyr-(CH2)2- | PhCH2- | 4-Cl-PhCH2- |
| 9 | 4-Pyr-(CH2)2- | 4-Pyr-(CH2)2- | 4-Cl-PhCH2- | PhCH2- |
| 10 | H | Ph-(CH2)3- | PhCH2- | 4-PyCH2- |
| 12 | 4-Pyr-(CH2)3- | 4-Pyr-(CH2)3- | PhCH2- | PhCH2- |
| 16 | 4-Pyr-(CH2)2- | 4-Pyr-(CH2)2- | (CH3)2CH-CH2- | PhCH2- |
| 17 | 4-Pyr-(CH2)2- | 4-Pyr-(CH2)2- | (CH3)2CH-CH2- | 4-F-PhCH2- |
| 18 | 4-Pyr-(CH2)2- | 4-Pyr-(CH2)2- | (CH3)2CH-CH2- | 4-Cl-PhCH2- |
| 19 | 4-Pyr-(CH2)2- | 4-Pyr-(CH2)2- | 4-Cl-PhCH2- | 4-F-PhCH2- |
| 21 | H | 3-Im-(CH2)2- | PhCH2- | PhCH2- |
| 23 | Ph-(CH2)2- | Ph-(CH2)2- | PhCH2- | 1H-Im-CH2- |
7. Фармацевтически приемлемая композиция по п.6, выбранная из
(S)-N-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-фенил-N-(3-пиридин-4-ил-1-(2-пиридин-4-ил-этил)пропил)пропионамида (соединение 7);
(S)-N-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-фенил-N-(3-пиридин-3-ил-1-(2-пиридин-3-илпропил)бутил)пропионамида (соединение 8);
(S)-N-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-(4-хлорфенил)-N-(3-пиридин-4-ил-1-(2-пиридин-4-ил-этил)пропил)пропионамида и
(S)-N-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-(4-хлорфенил)-N-(3-пиридин-3-ил-1-(2-пиридин-3-ил-пропил)бутил)пропионамида.
8. Фармацевтически приемлемая композиция по п.1, в которой указанный нейротропный фактор выбирают из фактора роста нервной ткани (ФРН), инсулинового фактора роста (ИФР) и их активных стволовых производных, кислотного фибробластного фактора роста (кФФР), основного фибробластного фактора роста (оФФР), факторов роста, полученных из тромбоцитов (ФРПТ), нейротропного фактора, полученного из головного мозга (НФПГМ), цилиарных нейротропных факторов (ЦНТФ), нейротропного фактора, полученного из линии глиальных клеток (НФПГК), нейротрофина-3 (НТ-3) и нейротрофина 4/5 (НТ-4/5).
9. Фармацевтически приемлемая композиция по п.8, в которой указанный нейротропный фактор представляет собой фактор роста нервной ткани (ФРН).
10. Способ стимуляции роста невритов у пациента или в нервных клетках ex vivo, включающий введение указанному пациенту или в указанные нервные клетки нейротропного количества соединения, имеющего структурную формулу (I)
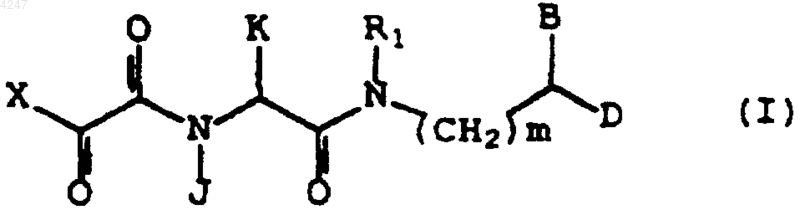
и его фармацевтически приемлемых производных, в которой
R1, B, D, J, K, X и m являются такими, как определено в п.1.
11. Способ по п.10, в котором указанное соединение имеет структурную формулу
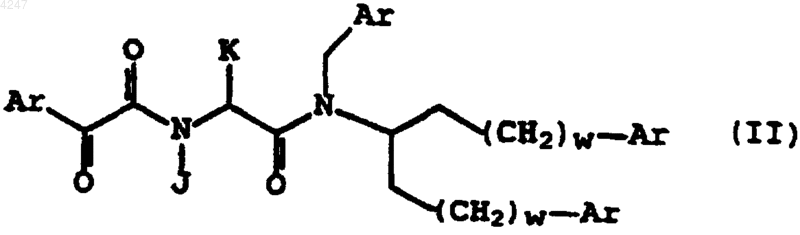
в которой J, K и w являются такими, как определено в п.2.
12. Способ по п.10, в котором по меньшей мере один из B или D независимо представлен формулой -(CH2)r-Z-(CH2)s-Ar, где r, s и Z являются такими, как определено в п.3.
13. Способ по п.12, в котором указанное соединение имеет структурную формулу
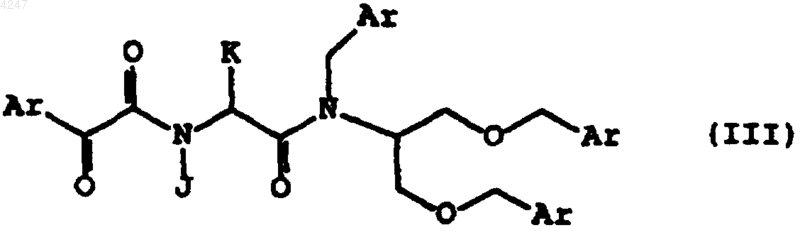
где J и K являются такими, как определено в п.4.
14. Способ по п.10, в котором
каждый Ar выбирают независимо из фенила, 2-пиридила, 3-пиридила, 4-пиридила, имидазолила, индолила, изоиндолила, хинолинила, изохинолинила, 1,2,3,4-тетрагидроизохинолинила или 1,2,3,4-тетрагидрохинолинила и
каждый Ar необязательно и независимо содержит 1-3 заместителя, независимо выбранные из гидроксила, нитро-, трифторметила, линейного или разветвленного алкила (C1-C6), O-(линейного или разветвленного алкила (C1-C6)), галогена, SO3H или -NR3R4.
15. Способ по п.11, в котором указанное соединение выбирают из соединений 6-10, 12, 16-19, 21 или 23 таблицы.
16. Способ по п.15, в котором указанное соединение выбирают из группы, состоящей из
(S)-N-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-фенил-N-(3-пиридин-4-ил-1-(2-пиридин-4-ил-этил)пропил)пропионамида (соединение 7);
(S)-N-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-фенил-N-(3-пиридин-3-ил-1-(2-пиридин-3-ил-пропил)бутил)пропионамида (соединение 8);
(S)-N-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-(4-хлорфенил)-N-(3-пиридин-4-ил-1-(2-пиридин-4-илэтил)пропил)пропионамида и
(S)-N-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-(4-хлорфенил)-N-(3-пиридин-3-ил-1-(2-пиридин-3-илпропил)бутил)пропионамида.
17. Способ по любому из пп.10-16, в котором указанное соединение вводят пациенту вместе с фармацевтически приемлемым носителем в виде фармацевтически приемлемой композиции.
18. Способ по п.17, в котором указанный способ используется для лечения пациента, страдающего болезнью Альцгеймера, болезнью Паркинсона, ALS, рассеянным склерозом, инсультом и ишемией, связанной с инсультом, невральной паропатией, другими невральными дегенеративными заболеваниями, заболеваниями двигательных нейронов, раздавленным седалищным нервом, периферической невропатией, диабетической невропатией, повреждением спинного мозга или поражением лицевого нерва.
19. Способ по п.18, включающий дополнительную стадию введения указанному пациенту нейротропного фактора, в котором указанный нейротропный фактор соединяют с указанным соединением с получением разовой дозовой формы или указанный нейротропный фактор и указанное соединение вводят в виде отдельных дозовых форм.
20. Способ по п.19, в котором указанный нейротропный фактор выбирают из фактора роста нервной ткани (ФРН), инсулинового фактора роста (ИФР) и их активных стволовых производных, кислотного фибробластного фактора роста (кФФР), основного фибробластного фактора роста (оФФР), факторов роста, полученных из тромбоцитов (ФРПТ), нейротропного фактора, полученного из головного мозга (НФПГМ), цилиарных нейротропных факторов (ЦНТФ), нейротропного фактора, полученного из глиальных клеток (НФПГК), нейротрофина-3 (НТ-3) и нейротрофина 4/5 (НТ-4/5).
21. Способ по п.20, в котором указанный нейротропный фактор представляет собой фактор роста нервной ткани (ФРН).
22. Способ по любому из пп.18-21, в котором указанный пациент страдает от периферической невропатии, связанной с диабетом.
23. Способ по любому из пп.10-16, в котором указанный способ используют для стимуляции регенерации нервов ex vivo.
24. Способ по п.23, включающий дополнительную стадию контактирования указанных нервных клеток с нейротропным фактором.
25. Способ по п.24, в котором указанный нейротропный фактор выбирают из фактора роста нервной ткани (ФРН), инсулинового фактора роста (ИФР) и их активных стволовых производных, кислотного фибробластного фактора роста (кФФР), основного фибробластного фактора роста (оФФР), факторов роста, полученных из тромбоцитов (ФРПТ), нейротропного фактора, полученного из головного мозга (НФПГМ), цилиарных нейротропных факторов (ЦНТФ), нейротропного фактора, полученного из глиальных клеток (НФПГК), нейротрофина-3 (НТ-3) и нейротрофина 4/5 (НТ-4/5).
26. Способ по п.25, в котором указанный нейротропный фактор представляет собой фактор роста нервной ткани (ФРН).
Текст
1 Область техники Настоящее изобретение относится к способам и фармацевтическим композициям для стимуляции роста невритов в нервных клетках. Эти композиции включают нейротрофическое количество соединения и нейротрофический фактор, такой как фактор роста нервной ткани(ФРН). Способы предусматривают обработку нервных клеток вышеуказанными композициями или композициями, включающими соединение без нейротрофического фактора. Способы по данному изобретению могут использоваться для ускорения репарации повреждений нейронов, вызванных патологическим процессом или физической травмой. Предшествующий уровень техники Неврологические болезни ассоциируются с гибелью или повреждением нервных клеток. Утрата допаминэргических нейронов в substantia nigra является этиологической причиной болезни Паркинсона. Хотя молекулярный механизм нейродегенерации при болезни Альцгеймера пока не установлен, очевидным является то, что воспаление головного мозга и отложение бета-амилоидного протеина, а также других таких веществ, может подавлять выживаемость нейронов и замедлять рост невритов, выполняющих функцию коммуникации между нейронами. У пациентов, страдающих ишемией головного мозга или травмами спинного мозга,наблюдается экстенсивная гибель нервных клеток. В настоящее время не существует удовлетворительного лечения этих заболеваний. Стандартное лечение неврологических болезней предусматривает использование препаратов, способных ингибировать гибель нервных клеток. Подход, разработанный в последнее время, предусматривает создание условий, способствующих регенерации нервов за счет ускорения роста невритов. Рост невритов, который имеет решающее значение для выживания нейронов, стимулируется in vitro факторами роста нервной ткани(ФРН). Например, нейротрофический фактор,производный от линии глиальных клеток(НФПГК), демонстрирует нейротрофическую активность как in vivo, так и in vitro и в настоящее время исследуется для применения в лечении болезни Паркинсона. Показано, что инсулиновый и инсулиноподобные факторы роста стимулируют рост невритов в клетках феохромоцитомы РС 12 крысы, а также в культуре симпатических и сенсорных нейронов [Recio-Pintoet al., J. Neurosci., 6, pp. 1211-1219 (1986)]. Инсулиновый и инсулиноподобные факторы роста стимулируют также регенерацию поврежденных двигательных нервов in vivo и in vitro [Near etet al., Brain Res., 641, pp. 76-82 (1994)]. Подобным же образом фибробластный фактор роста[М.A. Walter et al., Lymphokine Cytokine Res., 12,p. 135 (1993)] нервных клеток. Однако существуют недостатки, связанные с использованием факторов роста нервов для лечения неврологических заболеваний. Они с трудом преодолевают гематоэнцефалический барьер. Они нестабильны в плазме. И они обладают неудовлетворительными свойствами в отношении доставки лекарственного вещества. В последнее время было показано, что маленькие молекулы стимулируют рост невритовin vivo. У индивидуумов, страдающих неврологическими заболеваниями, такая стимуляция роста невритов защищает нейроны от дальнейшей дегенерации и ускоряет регенерацию нервных клеток. Например, показано, что эстроген способствует росту аксонов и дендритов, которые являются невритами, используемыми нервными клетками для коммуникации между собой в развивающемся или поврежденном взрослом головном мозге [(С. Dominique Toran-Allerand etBrain Res., 87, pp. 91-95 (1995)]. Прогрессирование болезни Альцгеймера замедляется у женщин, принимающих эстроген. Выдвигалось предположение о том, что эстроген дополняет ФРН и другие нейротрофины и тем самым помогает нейронам дифференцировать и выживать. Было продемонстрировано, что такролимус, иммуносупрессивный препарат, синергически действует с ФРН в стимуляции роста невритов в клетках РС 12, а также в сенсорных ганглиях [Lyons et al., PNAS, 91, pp. 3191-3195(1994)]. Показано также, что это соединение является нейропротекторным при очаговой ишемии головного мозга [J. SharkeyS.P.Butcher, Nature, 371, pp. 336-339 (1994)] и увеличивает скорость регенерации аксонов в поврежденном седалищном нерве [Gold et al., J.Neurosci., 15, pp. 7509-16 (1995)]. Несмотря на то, что посредством стимуляции роста невритов можно лечить широкий круг неврологических дегенеративных расстройств,известно относительно небольшое количество препаратов, обладающих такими свойствами. Таким образом, испытывается большая потребность в новых, фармацевтически приемлемых соединениях и композициях, которые обладают способностью стимулировать рост невритов у пациентов. Сущность изобретения Заявители решили вышеуказанную проблему, установив, что соединения, ранее разработанные одним из созаявителей для преодоления резистентности ко многим лекарственным препаратам, неожиданно и поразительно обладают также нейротропной активностью. Эти производные аминокислот описаны в патенте США 5543423. 3 Такие соединения стимулируют рост невритов в присутствии экзогенного или эндогенного ФРН. Заявленные композиции включают соединение из родов, описанных выше, и фактор роста нейронов. Способы стимуляции роста невритов, описанные здесь, используют вышеуказанные производные аминокислот или отдельно, или в комбинации с фактором роста нейронов. Эти способы используют при лечении повреждения нервов, вызванного различными неврологическими заболеваниями и физическими травмами, а также при регенерации нервовex vivo. Подробное описание изобретения Настоящее изобретение касается фармацевтических композиций, которые включают три компонента. Первым компонентом является соединение, имеющее структурную формулу (I): и его фармацевтические приемлемые производные, где R1, В и D выбирают независимо из следующего перечня: водород, Аr, линейный или разветвленный алкил (С 1-С 6), линейный или разветвленный алкенил или алкинил (С 2-С 6),замещенный циклоалкилом (С 5-С 7) линейный или разветвленный алкил (С 1-С 6), замещенный циклоалкилом (С 5-С 7) линейный или разветвленный алкенил или алкинил (С 3-С 6), замещенный циклоалкенилом (С 5-С 7) линейный или разветвленный алкил (С 1-С 6), замещенный циклоалкилом (С 5-С 7) линейный или разветвленный алкенил или алкинил (С 3-С 6), замещенный Аr линейный или разветвленный алкил (С 1-С 6) или замещенный Аr линейный или разветвленный алкенил или алкинил (С 3-С 6), при условии, чтоR1 не является водородом. Любая из групп СН 2 в алкильных цепочках с R1, В и D необязательно может быть замещена гетероатомом, выбранным из О, S, SO, SO2 иNR; где R - это водород, линейный или разветвленный алкил (С 1-С 6), линейный или разветвленный алкенил или алкинил (С 3-С 4) или соединительный алкил (С 1-С 4). Этот соединительный алкил (С 1-С 4), вместе с азотом и атомом углерода указанной цепочки, содержащей гетероатом,образуют кольцо. Это кольцо необязательно можно конденсировать с Аr-группой. Предпочтительно В и D выбирают независимо из Н, 3-Руr-(СН 2)3-, 4-Pyr-(CH2)2-, 3-Im(CH2)2-, Ph-(CH2)2-. R1 предпочтительно выбирают из СН 3-, PhCH2-, 4-Cl-PhCH2-, 4-F-PhCH2-,4-PyCH2- и 1H-Im-CH2-. Каждый Аr независимо выбирают из фенила, 1-нафтила, 2-нафтила, инденила, азуленила, флуоренила и антраценила, 2-фурила, 3-фурила, 2-тиенила, 3-тиенила, 2-пиридила, 3-пиридила, 4-пиридила, пирролила, оксазолила, тиазолила, имидазолила, пираксолила, 2-пиразолинила, пиразолидинила, изоксазолила, изотриазоли 004247 4 ла, 1,2,3-оксадиазолила, 1,2,3-триазолила, 1,3,4 тиадиазолила, пиридазинила, пиримидинила,пиразинила, 1,3,5-триазинила, 1,3,5-тритианила,индолизинила, индолила, изоиндолила, 3 Ниндолила, индолинила, бензо[b]фуранила, бензо[b]тиофенила, 1H-индазолила, бензимидазолила, бензтиазолила, пуринила, 4 Н-хинолизинила, хинолинила, 1,2,3,4-тетрагидроизохинолинила, изохинолинила, циннолинила, фталазинила, хиназолинила, хиноксалинила, 1,8-нафтиридинила, птеридинила, карбазолила, акридинила,феназинила, фенотиазинила или феноксазинила. Предпочтительными Аr-группами по данному изобретению являются фенил, 2-пиридил,3-пиридил, 4-пиридил, имидазолил, индолил,изоиндолил, хинолинил, изохинолинил, 1,2,3,4 тетрагидроизохинолинил и 1,2,3,4-тетрагидрохинолинил. Любая Аr-группа необязательно может быть замещена 1-3 заместителями, независимо выбранными из галогена, гидроксильной, нитро-, -SО 3 Н, трифторметила, трифторметокси-,линейного или разветвленного алкила (С 1-С 6),О-(линейного или разветвленного алкила (С 1 С 6, O-бензильной, O-фенильной, 1,2-метилендиокси-, -NR5R6, карбоксильной группы, N-(линейного или разветвленного алкила (С 1-С 6, N(линейного или разветвленного алкенила (С 3 С 5 карбоксамида, N,N-ди-(линейного или разветвленного алкила (С 1-С 6, N,N-ди-(линейного или разветвиленного алкенила (С 3-С 5, карбоксамида, морфолинила, пиперидинила, O-М,CH2-(CH2)q-M, O-(CH2)q-M, (СН 2)q-O-M или СН=СН-М. R5 и R6 независимо выбирают из водорода, линейного или разветвленного алкила(С 1-С 6), линейного или разветвленного алкенила или алкинила (С 2-С 6) или бензила. Как вариант,R5 и R6 могут вместе образовывать 5-7-членное гетероциклическое кольцо. М выбирают из 4 метоксифенила, 2-пиридила, 3-пиридила, 4-пиридила, пиразила, хинолила, 3,5-диметилизоксазоила, 2-метилтиоазоила, тиазоила, 2-тиенила,3-тиенила, 4-тиенила или пиримидила; q равно 0-2. Предпочтительными замещающими группами для Аr являются галоген, гидроксильная группа, нитро-, -SО 3 Н, трифторметил, линейный или разветвленный алкил (С 1-С 6), О-(линейный или разветвленный алкил (С 1-С 6 и -NR5R6. Компонент J в структурной формуле (I) выбирают из линейного или разветвленного алкила (С 1-С 6), линейного или разветвленного алкенила или алкинила (С 3-С 6), Аr-замещенного линейного или разветвленного алкила (С 1-С 6),Аr-замещенного линейного или разветвленного алкенила или алкинила (С 3-С 6) или циклогексилметила. Предпочтительно J является метилом. К выбирают из линейного или разветвленного алкила (С 1-С 6), Аr-замещенного линейного или разветвленного алкила (С 1-С 6), линейного или разветвленного алкенила или алкинила (С 2 5 С 6), Аr-замещенного линейного или разветвленного алкенила или алкинила (С 3-С 6). Предпочтительно К выбирают из фенилметила, 4 хлорфенилметила и изопропила. Как вариант, J и К берутся вместе с атомами азота и углерода, с которыми они соответственно связаны, так что образуется 5-7-членное гетероциклическое кольцо, которое может содержать гетероатом, выбранный из О, S, SO иD, соответственно. Как вариант, R3 и R4 могут вместе образовывать 5-7-членное гетероциклическое алифатическое или ароматическое кольцо. Предпочтительно Х является 3,4,5 триметоксифенилом. Компонент m равен 0 или 1, предпочтительно 0. Соединения по данному изобретению включают все оптические и рацемические изомеры. Термин фармацевтически приемлемое производное, как он используется здесь, означает любую фармацевтически приемлемую соль, сложный эфир или соль такого эфира соединения по данному изобретению или любого другого соединения, которое после введения пациенту способно дать (прямо или косвенно) соединение по данному изобретению, его метаболит или остаток, обладающие способностью способствовать или усиливать рост невритов. В соответствии с предпочтительным воплощением, фармацевтические композиции по данному изобретению содержат соединение,имеющее структурную формулу (II) и фармацевтически приемлемые его производные, где J и K выбирают независимо из линейного или разветвленного алкила (С 1-С 6) или Аrзамещенного линейного или разветвленного алкила (С 1-С 6);w равно 1 или 2. Другая предпочтительная фармацевтическая композиция по данному изобретению содержит соединение со структурной формулойZ независимо выбирают из О, S, SO, SO2 илиNR; a R выбирают из водорода, линейного или разветвленного алкила (С 1-С 4), линейного или разветвленного алкенила или алкинила (С 3-С 4) и соединительного алкила (С 1-С 4), в котором мостик находится между азотом и Аr-группой. Другое предпочтительное воплощение этих композиций содержит соединение, имеющее структурную формулу (III) и его фармацевтически приемлемые производные, где J и K выбирают независимо из линейного или разветвленного алкила (С 1-С 6) или Аrзамещенного линейного или разветвленного алкила (С 1-С 6);w равно 1 или 2. Таблица дает примеры предпочтительных соединений по данному изобретению.R1 4-F-PhCH2PhCH24-Cl-PhCH2PhCH24-PyCH2PhCH2 СН 3 СН 3PhCH24-F-PhCH24-Cl-PhCH24-F-PhCH2PhCH21 Н-Im-СН 2 Если используются фармацевтически приемлемые соли этих соединений, то эти соли предпочтительно являются производными от неорганических или органических кислот и оснований. В число таких кислотных солей входят следующие: ацетат, адипат, альгинат, аспартат,бензоат, бензолсульфонат, бисульфат, бутират,цитрат, камфорат, камфорсульфонат, циклопентапропионат, диглюконат, додецилсульфат,этансульфонат, фумарат, глюкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат,гидрохлорид, гидробромид, гидройодид, 2-гидроксиэтансульфонат, лактат, малеат, метансульфонат, 2-нафталинсульфонат, никотинат, оксалат, памоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат,тартрат, тиоцианат, тозилат и ундеканоат. Основные соли включают соли аммония, соли щелочных металлов, такие как натриевые и калиевые соли, соли щелочно-земельных металлов,такие как кальциевые и магниевые соли, соли с органическими основаниями, такие как соли дициклогексиламина, N-метил-D-глюкамин и соли с аминокислотами, такие как аргинин, лизин и тому подобное. Кроме этого, основные азотсодержащие группы могут быть кватернизированы такими агентами, как галогениды низших алкилов, такие как метил, этил, пропил и бутилхлорид, бромиды и йодиды; диалкилсульфаты, такие как диметил, диэтил, дибутил и диамилсульфаты, галогениды с длинной цепоч 7 кой, такие как децил, лаурил, миристил и стеарилхлориды, бромиды и йодиды; аралкилгалогениды, такие как бензил и фенетилбромиды и другие. Таким способом получают водо- или маслорастворимые или диспергируемые продукты. Соединения, используемые в композициях и способах по данному изобретению, могут также модифицироваться за счет соответствующих функциональных групп с целью усиления избирательных биологических свойств. Такие модификации известны в данной области и включают те, которые увеличивают биологическое проникание в данную биологическую систему (например, кровь, лимфатическую систему, центральную нервную систему), повышают оральную биодоступность, повышают растворимость, что позволяет вводить их путем инъецирования, изменяют метаболизм и изменяют скорость экскреции. Вторым компонентом во всех фармацевтических композициях, описанных выше, является нейротрофический фактор. Термин нейротрофический фактор, как он используется здесь,относится к соединениям, которые способны стимулировать рост или пролиферацию нервной ткани. Термин нейротрофический фактор, как он используется в данной заявке, исключает те соединения, которые в ней описаны. Идентифицированы многочисленные нейротрофические факторы, и любой из этих факторов может использоваться в композициях по данному изобретению. Такие нейротрофические факторы включают, не ограничиваясь ими, фактор роста нервной ткани (ФРН), инсулиновый фактор роста (ИФР-1) и его активные стволовые производные, такие как gИФР-1, кислотный и основный фибробластные факторы роста (аФФР и bФФР соответственно), полученные из тромбоцитов факторы роста (ФРПТ), полученные из головного мозга нейротрофические факторы(НФПГМ), цилиарные нейротрофические факторы (ЦНТФ), полученный из линии глиальных клеток нейротрофический фактор (НФПГК),нейротрофин-3 (НТ-3) и нейротрофин 4/5 (НТ 4/5). Самым предпочтительным нейротрофическим фактором в композициях по данному изобретению является ФРН. Третьим компонентом фармацевтически приемлемых композиций по данному изобретению является фармацевтически приемлемый носитель. Фармацевтически приемлемые носители, которые могут использоваться в этих фармацевтических композициях, включают, не ограничиваясь ими, ионообменные смолы, глинозем, алюминия стеарат, лецитин, сывороточные белки, такие как альбумин сыворотки человека,буферные вещества, такие как фосфаты, глицин,сорбиновая кислота, калия сорбат, смеси глицеридов, не полностью этерифицированных насыщенными растительными жирными кислотами, вода, соли или электролиты, такие как про 004247 8 тамин сульфат, динатрия гидрофосфат, калия гидрофосфат, натрия хлорид, соли цинка, коллоидный кремнезем, магния трисиликат, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, натриевая соль карбоксиметилцеллюлозы, полиакрилаты, воски, блокполимеры полиэтилена и полиоксипропилена,полиэтиленгликоль и ланолин. Композиции по данному изобретению могут вводиться орально, парентерально, в виде аэрозоля для ингаляции, местно, ректально, назально, буккально, вагинально или посредством имплантированного резервуара. Термин парентеральное введение, как он используется здесь,включает подкожное, внутривенное, внутримышечное, внутрисуставное, интрасиновиальное, интрастернальное, подоболочечное, внутрипеченочное, внутрь поражения и интракраниальное инъецирование или вливание. Предпочтительно эти композиции вводятся орально,интраперитонеально или внутривенно. Стерильные инъецируемые формы композиций по данному изобретению могут представлять собой водные или маслянистые суспензии. Эти суспензии могут быть приготовлены в соответствии с методами, известными в данной области, с использованием соответствующих диспергирующих или увлажняющих агентов или суспендирующих агентов. Такой стерильный препарат, предназначенный для инъецирования, может также представлять собой стерильный раствор или суспензию в нетоксичном,парентерально приемлемом разбавителе или растворителе,например растворе 1,3 бутандиола. Приемлемыми носителями и растворителями, которые могут использоваться,являются вода, раствор Рингера и изотонический раствор натрия хлорида. Кроме этого, в качестве растворителя или среды для суспендирования широко используются стерильные жирные масла. Для этой цели может использоваться любое легкое жирное масло, включая синтетические моно- и диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, используются при получении инъецируемых форм, как и природные фармацевтически приемлемые масла, такие как оливковое и касторовое, особенно в их полиоксиэтилированных версиях. Такие масляные растворы или суспензии могут также содержать разбавитель или диспергатор в виде спирта с длинной цепочкой, такого как Ph. Helv или подобный спирт. Фармацевтические композиции по данному изобретению могут вводиться орально в любой орально приемлемой лекарственной форме,включая, но не ограничиваясь ими, капсулы,таблетки, водные суспензии или растворы. В случае таблеток для орального использования широко используемыми наполнителями являются лактоза и кукурузный крахмал. Обычно добавляются также смазывающие агенты, такие 9 как магния стеарат. Для орального введения в виде капсул используемые наполнители включают лактозу и высушенный кукурузный крахмал. Если для орального использования требуется приготовить водную суспензию, активный ингредиент комбинируется с эмульгирующими или суспендирующими агентами. По желанию могут добавляться подсластители, отдушки и красители. Как вариант, фармацевтические композиции по данному изобретению могут вводиться в виде суппозиториев для ректального введения. Их можно приготовить путем смешивания лекарственного вещества с подходящим нераздражающим наполнителем, который является твердым при комнатной температуре, но жидким при температуре прямой кишки, где он будет плавиться, высвобождая лекарственное вещество. Такие материалы включают масло какао, пчелиный воск и полиэтиленгликоли. Фармацевтические композиции по данному изобретению могут также вводиться местно,особенно когда объектом лечения являются участки или органы, легко доступные при местном нанесении препарата, например при заболеваниях глаз, кожи и нижнего отдела кишечного тракта. Соответствующие составы для местного применения легко готовятся для каждого из этих участков или органов. Местное применение для нижнего отдела кишечного тракта можно осуществить с помощью ректальных суппозиториев (смотри выше) или соответствующего состава для клизмы. Можно использовать и трансдермальные накладки. Для местного применения фармацевтические композиции могут быть составлены в виде соответствующей мази, содержащей активный компонент, суспендированный или растворенный в одном или более носителей. Носители для местного введения соединений по данному изобретению включают, не ограничиваясь ими,минеральное масло, вазелиновое масло, вазелин,пропиленгликоль, полиоксиэтилен, полиоксипропилен, эмульгиругощий воск и воду. Как вариант, фармацевтические композиции могут быть приготовлены в виде соответствующего лосьона или крема, содержащего активные компоненты, суспендированные или растворенные в одном или более фармацевтически приемлемых носителей. Такие носители включают, не ограничиваясь ими, минеральное масло, сорбитана моностеарат, полисорбат 60, цетиловые эфиры воска, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду. Для офтальмологического использования фармакологические композиции могут быть приготовлены в виде суспензий, пропущенных через микронную коллоидную мельницу, в изотоническом стерильном солевом растворе с отрегулированным рН, к которым может добавляться консервант, такой как бензилалконий 004247 10 хлорид. Как вариант, для офтальмологического применения фармацевтические композиции могут быть приготовлены в виде мази на основе вазелина. Фармацевтические композиции по данному изобретению могут вводиться также в виде назального аэрозоля или ингаляции. Такие композиции получают методами, хорошо известными в данной области, в виде растворов в солевом растворе, с использованием бензилового спирта или других подходящих консервантов,веществ, способствующих всасыванию для усиления биодоступности, фторуглеродов и/или других обычных солюбилизирующих или диспергирующих агентов. Количество соединения и нейротрофического фактора, которые могут комбинироваться с носителями, для получения отдельных лекарственных форм может варьироваться в зависимости от пациента и конкретного способа введения. Два активных ингредиента в фармацевтических композициях по данному изобретению действуют синергически в стимуляции роста нейритов. Следовательно, количество нейротрофического фактора в таких композициях будет меньше того количества, которое требуется для монотерапии, использующей только этот фактор. Предпочтительно композиции должны готовиться таким образом, чтобы доза вводимого пациенту соединения составляла 0,01-100 мг/кг веса тела/день, а доза вводимого нейротрофического фактора - 0,01-100 мкг/кг веса тела/день. Должно быть понятно, что конкретная доза и схема лечения для каждого отдельного пациента будут зависеть от множества факторов,включая активность используемого соединения,возраст, вес тела, общее состояние здоровья,пол, рацион питания, время введения, скорость экскреции, сочетание с другими лекарственными препаратами, а также решения лечащего врача и тяжести состояния, подлежащего лечению. Количество активных ингредиентов будет также зависеть от того, какие соединение и нейротрофический фактор использованы в данной фармацевтической композиции. В соответствии с другим воплощением данное изобретение касается способов стимуляции роста невритов. В соответствии с одним аспектом этого воплощения такой метод используется для стимуляции роста невритов у пациента и осуществляется путем введения этому пациенту фармацевтически приемлемой композиции, содержащей любое из вышеописанных соединений и фармацевтически приемлемый носитель. Количество соединения, используемого в этих методах, находится между 0,01 и 100 мг/кг веса тела/день. В соответствии с другим аспектом этого воплощения такой способ используется для стимуляции роста нервов ex vivo. Для этой цели вышеописанные соединения могут вводиться 11 непосредственно в культуру нервных клеток. Этот аспект изобретения используется для регенерации нервов ех vivo. В соответствии с другим воплощением способ стимуляции роста невритов предусматривает дополнительную стадию лечения пациента или обработки нервных клеток в культуре ех vivo нейротрофическим фактором, таким как те, которые содержатся в фармацевтических композициях по данному изобретению, описанных выше. Это воплощение предусматривает введение пациенту такого соединения и такого нейротрофического средства в виде разовой лекарственной формы или нескольких отдельных лекарственных форм. Если используются отдельные лекарственные формы, их можно вводить одновременно, последовательно или с интервалом, не превышающим примерно 5 ч. Методы и композиции по данному изобретению могут использоваться для лечения повреждения нервов, вызванных широким кругом заболеваний или физических травм. Они включают, не ограничиваясь ими, болезнь Альцгеймера, болезнь Паркинсона, ALS, рассеянный склероз, инсульт и ассоциируемая с ним ишемия, невральная паропатия, другие невральные дегенеративные заболевания, болезни двигательных нейронов, раздавливание седалищного нерва, периферическая нейропатия, особенно нейропатия, связанная с диабетом, травмы спинного мозга и поражения лицевого нерва. Для лучшего понимания описанного изобретения ниже приведены конкретные примеры его воплощения. Должно быть понятно, что эти примеры служат только иллюстративным целям и никоим образом не ограничивают объем данного изобретения. Примеры Общие методы Спектры протонного ядерного магнитного резонанса (1 Н ЯМР) были записаны при 500 МГц на приборе Bruker AMX 500. Химические сдвиги приведены в частях на миллионпо отношению к Me4Si ( 0,0). Аналитическая высокоэффективная жидкостная хроматография осуществлялась на жидкостном хроматографеWaters 600 Е или Hewlett Packard 1050. Пример 1. 1,5-Ди(пиридин-4-ил)-пент-1,4 диен-3-он (соединение 1). К раствору 1,3-ацетондикарбоновой кислоты (21,0 г; 0,144 ммоль) в абсолютном этиловом спирте (200 мл) добавляли по каплям 4 пиридинкарбоксальдегид (30,8 г; 0,288 ммоль). Выделение газа происходило на протяжении всего добавления. После перемешивания при комнатной температуре в течение 2 ч к реакционной смеси добавляли концентрированную соляную кислоту (100 мл) и нагревали до 80 С,наблюдая медленное образование желтого осадка. Дополнительные 500 мл этилового спирта добавляли для того, чтобы обеспечить переме 004247 12 шивание суспензии. После выдержки в течение 1 ч при 80 С осадок отделяли фильтрованием,промывали этиловым спиртом и высушивали под вакуумом, чтобы получить целевой продукт в виде желтого твердого вещества. Полученная дигидрохлоридная соль перекристаллизировалась из метиленхлорида, чтобы получить чистое соединение 1. Пример 2. 1,5-Ди(пиридин-4-ил)-пентан-3 он (соединение 2). К суспензии соединения 1 (21,3 г; 67,4 ммоль) в 1,4-диоксане (40 мл) добавляли триэтиламин (48,1 мл; 0,346 моль), муравьиную кислоту (6,54 мл; 0,145 мол) и 10% палладия-науглероде (0,7 г) и нагревали полученную смесь до температуры дефлегмации. После перемешивания при температуре дефлегмации в течение 1 ч реакционную смесь охлаждали до комнатной температуры, фильтровали и концентрировали под вакуумом. Полученный остаток хроматографировали на силикагеле (элюирование 5% метиловым спиртом/метиленхлоридом), чтобы получить целевой материал. Пример 3. (4-Фторбензил)-(3-(пиридин-4 ил)-1-(2-(пиридин-4-ил)-этил)пропил)амин (соединение 3). В колбу, снабженную улавливателем Дина-Старка, добавляли соединение 2 (12,46 г; 51,91 ммоль), 4-фторбензиламин (5,93 мл; 51,91 ммоль) и бензол (50 мл) и нагревали полученную смесь до температуры дефлегмации. После собирания 930 мкл воды реакционная смесь охлаждалась и концентрировалась. Остаток растворяли в этиловом спирте (50 мл) и добавляли в суспензию натрия борогидрида (2,96 г; 77,8 ммоль) в этиловом спирте (50 мл). Полученную смесь нагревали до 80 С и перемешивали в течение 1 ч. Реакционную смесь охлаждали и концентрировали. Остаток растворяли в воде,подкисляли до рН 3,0 с помощью 6N соляной кислоты. Водную фазу промывали этилацетатом(2 Х). Водную фазу доводили до щелочной реакции с помощью гидроокиси натрия (рН 10) и экстрагировали продукт метиленхлоридом (2 Х). Органические фракции объединяли, промывали соляным раствором, высушивали над безводным сульфатом магния, фильтровали и концентрировали под вакуумом. Хроматография остатка на силикагеле (элюирование 5% метиловым спиртом/метиленхлоридом) давала соединение 3. Пример 4. (S)-N-(4-Фторбензил)-2-(N-метил-N-трет-бутилкарбамоил)-амино-3-фенил-N(3-(пиридин-4-ил)-1-(2-(пиридин-4-ил)-этил)пропил)пропионамид (cоединение 4). К раствору cоединения 3 (550 мг; 1,66 ммоль) и (L)-BOC-N-метилуфенилаланина (700 мг; 2,5 ммоль) в метиленхлориде (4,0 мл), содержащему диизопропилэтиламин (300 мкл; 1,72 ммоль), добавляли (3-диметиламинопропил)-3-этилкарбодиимида гидрохлорид (480 мг; 2,5 ммоль) и перемешивали реакционную смесь в течение 48 ч. Реакционную смесь раз 13 бавляли этилацетатом и водой. Слои разделяли,и водную фазу экстрагировали повторно этилацетатом. Органические фракции объединяли,промывали насыщенным бикарбонатом натрия,водой и соляным раствором, высушивали над безводным сульфатом магния, фильтровали и концентрировали под вакуумом. Хроматография остатка на силикагеле (элюирование 5% метиловым спиртом/метиленхлоридом) давалаcоединение 4. Пример 5. (S)-N-(4-Фторбензил)-2-метиламино-3-фенил-N-(3-(пиридин-4-ил)-1-(2-(пиридин-4-ил)-этил)пропил)пропионамид (соединение 5). Соединение 4 растворяли в метиленхлориде (10 мл) и обрабатывали трифторуксусной кислотой (4,0 мл). После перемешивания при комнатной температуре в течение 1,5 ч реакционную смесь концентрировали под вакуумом. Остаток нейтрализовали насыщенным карбонатом калия и экстрагировали этилацетатом (2 Х). Экстракты объединяли, промывали водой, высушивали над безводным сульфатом магния,фильтровали и концентрировали под вакуумом,чтобы получить соединение 5. Пример 6. (S)-N-(4-Фторбензил)-2-(метил(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-фенил-N-(3-пиридин-4-ил)-1-(2-(пиридин 4-ил)этил)пропил)пропионамид (cоединение 6). К раствору соединения 5 (500 мг; 0,98 ммоль) и 3,4,5-триметоксибензоилмуравьиной кислоты (294 мг; 1,22 ммоль) в метиленхлориде(0,4 мл), добавляли (3-диметиламинопропил)-3 этилкарбодиимида гидрохлорид (235 мг; 1,22 ммоль) и перемешивали реакционную смесь в течение 24 ч. Реакционную смесь разбавляли этилацетатом и водой. Слои разделяли и водную фазу экстрагировали повторно этилацетатом. Органические фракции объединяли, промывали насыщенным бикарбонатом натрия, водой и соляным раствором, высушивали над безводным сульфатом магния, фильтровали и концентрировали под вакуумом. Остаток хроматографировали на силикагеле (элюирование 5% метиловым спиртом/метиленхлоридом), чтобы получить целевой продукт. 1 Н ЯМР как смесь ротомеров (500 МГц,CDCl3)8,48-8,44 (м), 8,38 (дд), 7,36-7,33 (м),7,28-7,18 (м), 7,13-7,02 (м), 6,97-6,87 (м), 6,58 14 Соединение 7 было получено в соответствии с протоколами для примеров 3-6 с заменой 4-фторбензиламина на бензиламин. 1H ЯМР как смесь ротомеров (500 МГц,СDСl3)8,48 (дд), 8,53 (дд), 8,43 (дд), 8,35 (дд),7,38 (д), 7,30-7,18 (м), 7,17-7,02 (м), 6,93 (с), 6,89(с), 3,03 (с), 2,97 (дд), 2,63 (дт), 2,57-2,37 (м),2,24 (дт), 2,06 (м), 1,95-1,76 (м), 1,74-1,63 (м),1,54-1,44 (м). Пример 8. (S)-N-(4-Хлорбензил)-2-(метил(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-фенил-N-(3-(пиридин-4-ил)-1-(2-(пиридин-4-ил)-этил)пропил)пропионамид (соединение 8). Соединение 8 было получено в соответствии с протоколами для примеров 3-6 с заменой 4-фторбензиламина на 4-хлорбензиламин. 1H ЯМР как смесь ротомеров (500 МГц,CDCl3)8,49 (дт), 8,45 (дд), 8,40 (дд), 7,69 (д),7,31-7,14 (м), 7,12 (с), 7,08-7,03 (м), 6,98 (с),6,94-6,91 (м), 6,85 (д), 6,02 (дд), 5,79 (т), 4,99(дт), 1,90-1,80 (м), 1,75-1,66 (м), 1,52-1,43 (м). Пример 9. (S)-N-Бензил-3-(4-хлорфенил)-2(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил) амино)-N-(3-(пиридин-4-ил)-1-(2-(пиридин-4-ил)этил)пропил)пропионамид (соединение 9). Соединение 9 было получено в соответствии с протоколами для примеров 3-6 с заменой 4-фторбензиламина на бензиламин и (L)-BOCN-метилфенил-аланина на (L)-ВОС-N-метил-4 хлорфенилаланин. 1H ЯМР как смесь ротомеров (500 МГц,СDСl3)8,48 (дд), 8,45 (дт), 8,38 (дд), 7,32-6,87(м), 3,05-2,96 (м), 3,01 (с), 3,00 (с), 2,91 (дд),2,65-2,38 (м), 2,26 (дт), 1,94-1,47 (м). Пример 10. (S)-2-(Метил-(2-оксо-2-(3,4,5 триметоксифенил)ацетил)амино)-3-фенил-N-(4 фенилбутил)-N-[(пиридин-4-ил)метил]пропионамид (соединение 10). Соединение 10 было получено в соответствии с протоколами для примеров 3-6 с заменой 4-фторбензиламина на 4-фенилбутиламин и соединения 2 на 4-пиридинкарбоксальдегид. 1H ЯМР как смесь ротомеров (500 МГц,СDСl3)8,46 (дд), 8,42 (дд), 7,30-7,23 (м), 7,187,11 (м), 7,11 (с), 7,10 (с), 6,90 (д), 6,77 (д), 5,88(4,1 г; 15,2 ммоль) в метиленхлориде (50 мл) при 0 С добавляли калия бромид (180 мг) и 2,2,6,6 тетраметил-1-пиперидинилокси, свободный радикал (71 мг). К полученной смеси добавляли по каплям раствор бикарбоната натрия (510 мг) в гипохлорите натрия (65 мл). После добавления всего количества реакционную смесь нагревали до комнатной температуры и перемешивали в течение 30 мин. Полученную смесь разбавляли этилацетатом и водой. Слои разделяли, и водную фазу экстрагировали повторно этилацетатом. Органические фракции объединяли, промывали насыщенным бикарбонатом натрия, водой и соляным раствором, высушивали над безводным сульфатом магния,фильтровали и концентрировали под вакуумом. Остаток хроматографировали на силикагеле (элюирование 5% метиловым спиртом/метиленхлоридом), чтобы получить соединение 11. Пример 12. (S)-N-Бензил-2-(метил-(2-оксо 2-(3,4,5-триметоксифонил)ацетил)амино)-3-фенил-N-(4-(пиридин-4-ил)-1-(3-пиридин-4-илпропил)бутил)пропионамид (соединение 12). Соединение 12 было получено в соответствии с протоколами для примеров 3-6 с заменой 4-фторбензиламина на бензиламин и соединения 2 на соединение 11. 1H ЯМР как смесь ротомеров (500 МГц,СDСl3)8,43-8,38 (м), 8,30 (м), 8,16 (м), 7,537,45 (м), 7,34 (м), 7,32 (м), 7,26-7,22 (м), 7,197,07 (м), 7,00-6,83 (м), 5,89 (дд), 5,72 (т), 4,90 (д),4,72 (д), 4,10 (д), 4,00 (д), 3,93 (с), 3,91 (с), 3,85(1,7 г; 25,4 ммоль) и натрия ацетата (2,5 г; 30,48 ммоль) в метиловом спирте (20 мл) добавляли раствор cоединения 2 (1,21 г; 5,08 ммоль) в метиловом спирте (5 мл). Полученную смесь обрабатывали раствором натрия цианоборогидрида(370 мг; 6,09 ммоль) в метиловом спирте (5 мл) и нагревали до 80 С. После выдержки в течение 1 ч при 80 С реакционную смесь охлаждали до комнатной температуры и концентрировали под вакуумом. Остаток растворяли в метиленхлориде и 2N гидроокиси натрия. Слои разделяли и органическую фазу промывали соляным раствором, высушивали над безводным сульфатом магния, фильтровали и концентрировали под вакуумом, чтобы получить соединение 13. Пример 14. (S)-N-Метил-2-(метил-(2-оксо 2-(3,4,5-триметоксифенил)ацетил)амино)-3-фенил-N-(3-(пиридин-4-ил)-1-(2-пиридин-4-илэтил)пропил)пропионамид (соединение 14). Соединение 14 было получено и соответствии с протоколами для примеров 4-6 с заменой соединения 3 на соединение 13.H ЯМР как смесь ротомеров (500 МГц,CDCl3)8,50-8,46 (м), 8,37 (д), 7,32-7,26 (м),7,21-7,16 (м), 7,10-7,06 (м), 6,97 (дд), 6,93 (д),5,93 (д), 5,54 (т), 4,72 (ушир. с), 4,17 (м), 3,94 (с),3,92 (с), 3,84 (с), 3,82 (с), 3,51 (дд), 3,38 (дд),3,29 (с), 3,11 (дд), 3,06 (с), 3,00 (с), 2,97 (дд),2,86 (с), 2,82 (с), 2,49 (м), 2,37-2,23 (м), 2,17-1,98(м), 1,85-1,55 (м). Пример 15. (S)-N-Метил-2-(метил-(2-оксо 2-(3,4,5-триметоксифенил)ацетил)амино)-3-фенил-N-(4-(пиридин-4-ил)-1-(3-пиридин-4-илпропил)бутил)пропионамид (соединение 15). Соединение 15 было получено в соответствии с протоколами для примеров 13 и 14 с заменой соединения 2 на соединение 11. 1H ЯМР как смесь ротомеров (500 МГц,CDCl3)8,44-8,38 (м), 8,37-8,30 (м), 7,50-7,43(м), 7,38-7,08 (м), 7,04 (с), 7,03-6,98 (м), 6,906,86 (м), 5,83 (дд), 5,74 (т), 4,75 (т), 4,65 (м),3,94-3,93 (м), 3,92 (с), 3,90 (с), 3,84 (с), 3,83 (с),3,44 (дд), 3,32 (дд), 3,20 (с), 3,01 (дд), 2,95 (с),2,91 (с), 2,87 (дд), 2,59 (с), 2,58-2,37 (м), 1,681,00 (м). Пример 16. (S)-4-Мeтил-2-(метил-(2-оксо 2-(3,4,5-триметоксифенил)ацетил)амино)пентановая кислота бензил(3-(пиридин-4-ил)-1-(2-пиридин-4-илэтил)пропил)амид (соединение 16). Соединение 16 было получено в соответствии с протоколами для примеров 3-6 с заменой 4-фторбонзиламина на бензиламин и (L)BOC-N-метилфенилаланина на (S)-BOC-Nметиллейцин. Пример 17. (S)-4-Метил-2-(метил-(2-оксо 2-(3,4,5-триметоксифенил)ацетил)амино)пентановая кислота 4-фторбензил(3-пиридин-4-ил-1(2-пиридин-4-илэтил)пропил)амид (соединение 17). Соединение 17 было получено в соответствии с протоколами для примеров 4-6 с заменой (L)-N-ВОС-N-метилфенилаланина на (S)-NBOC-N-метиллейцин. 1H ЯМР как смесь ротомеров (500 МГц,CDCl3)8,48 (м), 8,45 (д), 7,32 (м), 7,18 (с), 7,12(м), 1,03 (т), 0,90 (д), 0,69 (д). Пример 18. (S)-4-Метил-2-(метил-(2-оксo2-(3,4,5-триметоксифенил)ацетил)амино)пентановая кислота 4-хлорбензил(3-пиридин-4-ил-1(2-пиридин-4-илэтил)пропил)амид (соединение 18). Соединение 18 было получено в соответствии с протоколами для примеров 3-6 с заменой 4-фторбензиламина на 4-хлорбензиламин и(L)-N-BOC-N-метилфенилаланина на (S)-NBOC-N-метиллейцин. 1 Н ЯМР как смесь ротомеров (500 МГц,CDCl3)8,50 (м), 8,47 (д), 7,38 (д), 7,30-7,26 (м), 17 7,19 (с), 7,13 (с), 7,10 (д), 7,04 (д), 6,98 (д), 6,84(м), 2,12-1,56 (м), 1,48-1,40 (м), 1,25 (м), 1,04 (т),0,91 (д), 0,70 (д). Пример 19. (S)-N-(4-фторбензил)-3-(4 хлорфенил)-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-N-(3-пиридин-4-ил-1(2-пиридин-4-илэтил)пропил)пропионамид (соединение 19). Соединение 19 было получено в соответствии с протоколами для примеров 4-6 с заменой (L)-N-BOC-N-метилфенилаланина на (S)-NВОС-N-метил-4-хлорфенилаланин. 1 Н ЯМР как смесь ротомеров (500 МГц,СDСl3)8,49-8,41 (м), 7,34 (с), 7,28-7,20 (м),7,10-6,90 (м), 6,64 (д), 5,92 (дд), 5,74 (т), 4,95(15 мл) при 0 С добавляли по каплям 4 хлорбензоилхлорид (2,1 мл; 16,8 ммоль). Затем реакционной смеси давали нагреться до комнатной температуры. Через 5 ч реакционную смесь разбавляли метиленхлоридом, промывали 1N гидроокисью натрия, соляным раствором,высушивали над безводным сульфатом магния,фильтровали и концентрировали под вакуумом,чтобы получить белое твердое вещество. Этот материал промывали диэтиловым эфиром, чтобы получить N-(3-имидазол-1-ил-пропил)-4 хлорбензамид. К суспензии вышеуказанного амида (1,58 г; 6,0 ммоль) в тетрагидрофуране(30 мл) медленно добавляли алюмогидрид (456 мг; 12,0 ммоль), после чего реакция становилась экзотермической. Смесь нагревали до 80 С, перемешивали в течение 1 ч, охлаждали до 0 С и гасили добавлением воды (0,5 мл), 15% гидроокиси натрия (0,5 мл) и дополнительных 1,5 мл воды. Реакционную смесь разбавляли этилацетатом, сушили над безводным сульфатом магния, фильтровали и концентрировали под вакуумом, чтобы получить соединение 20. Пример 21. (S)-N-(4-хлорбензил)-N-(3-имидазол-1-ил-пропил)-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-фенилпропионамид (соединение 21). Соединение 21 было получено в соответствии с протоколами для примеров 4-6 с заменой соединения 3 на соединение 20. 1H ЯМР как смесь ротомеров (500 МГц,CDCl3)8,48 (м), 7,44 (ушир. с), 7,37 (ушир. с),7,30-7,16 (м), 7,10-7,02 (м), 6,95 (д), 6,83 (м), 004247(с), 3,93 (с), 3,88-3,77 (м), 3,80 (с), 3,48 (дт),3,42-3,33 (м), 3,19-3,14 (м), 3,13 (с), 3,12 (с),3,13-2,97 (м), 2,89 (т), 2,80 (м), 2,74 (т), 2,65 (м),2,08-1,98 (м), 1,90 (м), 1,80-1,60 (м). Пример 22. N-(1 Н-имидазол-2-ил-метил)N-(1-фенетил-3-фенилпропил)амин (соединение 22). К раствору 1,5-дифенилпентан-3-она (5,26 г; 22,1 ммоля), аммония ацетата (8,52 г; 110,5 ммоль) и натрия ацетата (9,06 г; 110,5 ммоль) в метиловом спирте (80 мл) добавляли раствор натрия цианоборогидрида (1,67 г; 26,52 ммоль) в метиловом спирте (20 мл) и нагревали реакционную смесь до температуры дефлегмации. После перемешивания при температуре дефлегмации в течение 30 мин реакционную смесь охлаждали и концентрировали досуха. Остаток разделяли между метиленхлоридом и 2N гидроокисью натрия. Органическую фазу отделяли, промывали соляным раствором, высушивали над безводным сульфатом магния, фильтровали и концентрировали под вакуумом. Хроматография остатка на силикагеле (элюирование 2-5% метиловым спиртом/метиленхлоридом) дала N(1-фенетил-3-фенилпропил)амин. К раствору вышеуказанного амина (2,1 г; 8,82 ммоль) в этиловом спирте (50 мл) добавляли 2 имидазолкарбоксальдегид (813 мг; 8,47 ммоль) и нагревали реакционную смесь до 50 С. После перемешивания в течение 2 ч полученный гомогенный раствор обрабатывали натрия борогидридом (400 мг; 10,58 ммоль) и перемешивали в течение ночи. Реакционную смесь концентрировали досуха и разделяли остаток между метиленхлоридом и 2N гидроокисью натрия. Органическую фазу отделяли, промывали соляным раствором, высушивали над безводным сульфатом магния, фильтровали и концентрировали под вакуумом. Хроматография этого остатка на силикагеле (элюирование 5% метиловым спиртом/метиленхлоридом) дала cоединение 22. Пример 23. (S)-N-(1 Н-имидазол-2-ил-метил)-2-(метил(2-оксо-2-(3,4,5-триметоксифенил) ацетил)амино)-N-(1-фенетил-3-фенилпропил)-3 фенилпропионамид (соединение 23). Соединение 23 было получено в соответствии с протоколами для примеров 4-6 с заменой соединения 3 на соединение 22. 1 Н ЯМР как смесь ротомеров (500 МГц,СDСl3)7,40-7,00 (м), 6,95-6,87 (м), 5,95 (т),5,69 (т), 4,66 (д), 4,46 (д), 4,12 (м), 3,94 (с), 3,92(с), 3,82 (с), 3,81 (с), 3,80 (с), 3,47 (с), 3,43 (дд),3,34 (дд), 3,22 (с), 3,15 (с), 3,03 (дд), 3,00 (с),2,60 (дт), 2,45-2,22 (м), 1,80-1,78 (м). Пример 24. Чтобы непосредственным образом определить нейротрофическую активность соединений, описанных в этом изобретении, проба на рост невритов выполнялась на клетках феохромоцитомы РС 12, как описано Lyons et al. (1994). 19 Клетки РС 12 поддерживались при 37 С и 5% СО 2 в модифицированной Дульбекко среде Игля (МДСИ), дополненной 10% лошадиной сывороткой, инактивированной нагреванием,5% фетальной бычьей сывороткой (ФБС), инактивированной нагреванием, и 1% глютамата. Затем клетки переносили по 105 на лунку на 96 луночные пластины, покрытые 5 мкг/см 2 коллагеном из хвоста крысы, и давали прикрепиться в течение ночи. Эта среда затем заменялась на МДСИ, 2% лошадиной сыворотки, инактивированной нагреванием, 1% глютамата, 1-5 нг/мл ФРН (Sigma) и различные концентрации соединения (0,1-10 нМ). В фоновую контрольную культуру вводили только 105 нг/мл ФРН без соединения. В положительные контрольные культуры вводили высокую концентрацию ФРН(50 нг/мл). Соединения, описанные в этом изобретении, вызывают достоверное увеличение роста невритов по сравнению с фоновыми контрольными культурами. Несмотря на то, что заявители представили здесь целый ряд воплощений данного изобретения, очевидно, что основной замысел можно изменить таким образом, чтобы получить другие воплощения, которые используют способы по данному изобретению. Следовательно,должно быть понятно, что объем данного изобретения определяется скорее прилагаемой формулой изобретения, чем представленными здесь конкретными воплощениями, которые служат только для целей иллюстрации. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Фармацевтически приемлемая композиция, содержащая а) нейротрофическое количество соединения, имеющего структурную формулу (I) и его фармацевтически приемлемые производные,где R1, В и Dэто независимо водород, Аr, линейный или разветвленный алкил (С 1-С 6), линейный или разветвленный алкенил или алкинил (С 2-С 6), замещенный циклоалкилом (С 5-С 7) линейный или разветвленный алкил (С 1-С 6),замещенный циклоалкилом (С 5-С 7) линейный или разветвленный алкенил или алкинил (С 3 С 6), замещенный циклоалкенилом (С 5-С 7) линейный или разветвленный алкил (С 1-С 6), замещенный циклоалкиленом (С 5-С 7) линейный или разветвленный алкенил или алкинил (С 3-С 6), Аrзамещенный линейный или разветвленный алкил (С 1-С 6), Аr-замещенный линейный или разветвленный алкенил или алкинил (С 3-С 6); 20 при условии, что R1 не является водородом или линейным или разветвленным алкилом (С 1 С 6) и где любая из групп CH2 указанных алкильных цепочек с R1, В и D необязательно заменена на О, S, SO, SO2 и NR; где R - это водород, линейный или разветвленный алкил (С 1-С 6), линейный или разветвленный алкенил или алкинил (С 3-С 4) или мостиковый алкил (С 1-С 4), в котором мостик образован между азотом и атомом углерода указанной алкильной цепочки, образуя кольцо, и в котором указанное кольцо необязательно конденсировано с Аr; где каждый Аr независимо выбирают из фенила, 1-нафтила, 2-нафтила, инденила, азуленила,флуоренила и антраценила, 2-фурила, 3-фурила, 2 тиенила, 3-тиенила, 2-пиридила, 3-пиридила, 4 пиридила, пирролила, оксазолила, тиазолила,имидазолила, пиразолила, 2-пиразолинила, пиразолидинила, изоксазолила, изотриазолила, 1,2,3 оксадиазолила, 1,2,3-триазолила, 1,3,4-тиадиазолила, пиридазинила, пиримидинила, пиразинила, 1,3,5-триазинила, 1,3,5-тритианила, индолизинила, индолила, изоиндолила, 3 Н-индолила,индолинила, бензо[b]фуранила, бензо[b] тиофенила, 1H-индазолила, бензимидазолила, бензтиазолила, пуринила, 4 Н-хинолизинила, хинолинила,1,2,3,4-тетрагидроизохинолинила, изохинолинила, 1,2,3,4-тетрагидрохинолинила, циннолинила, фталазинила, хиназолинила, хиноксалинила, 1,8-нафтиридинила, птеридинила, карбазолила, акридинила, феназинила, фенотиазинила или феноксазинила, и где каждый Аr необязательно и независимо замещен 1-3 заместителями, независимо выбранными из водорода, галогена, гидроксила,нитро-, -SО 3 Н, трифторметила, трифторметокси,линейного или разветвленного алкила (С 1-С 6),О-(линейного или разветвленного алкила (С 1 С 6, O-бензила, O-фенила, 1,2-метилендиокси,-NR5R6, карбоксила, N-(линейного или разветвленного алкила (С 1-С 6 карбоксамида или N(линейного или разветвленного алкенила (С 3-С 5) карбоксамида, N,N-ди-линейного или разветвленного алкила (С 1-С 6 карбоксамида или N,Nди-линейного или разветвленного алкенила(С 3-С 5 карбоксамида, морфолинила, пиперидинила, O-М, СН 2-(CH2)q-M, O-(CH2)q-M, (CH2)qO-M или СН=СН-М; где R5 и R6 независимо выбирают из группы, состоящей из водорода, линейного или разветвленного алкила (С 1-С 6), линейного или разветвленного (С 2-С 6) алкенила или алкинила,бензила, или R5 и R6 могут вместе образовывать 5-7-членное гетероциклическое кольцо; М выбирают из группы, состоящей из 4 метоксифенила, 2-пиридила, 3-пиридила, 4 пиридила, пиразила, хинолила, 3,5-диметилизоксазолила, 2-метилтиоазолила, тиазоила, 2 тиенила, 3-тиенила, 4-тиенила или пиримидила; иJ выбирают из группы, состоящей из линейного или разветвленного алкила (С 1-С 6), линейного или разветвленного алкенила или алкинила (С 3-С 6), Аr-замещенного линейного или разветвленного алкила (С 1-С 6), Аr-замещенного линейного или разветвленного алкенила или алкинила (С 3-С 6) и циклогексилметила;K выбирают из группы, состоящей из линейного или разветвленного алкила (С 1-С 6), Аrзамещенного линейного или разветвленного алкила (С 1-С 6), линейного или разветвленного алкенила или алкинила (С 2-С 6), и Аrзамещенного линейного или разветвленного алкенила или алкинила (С 3-С 6); илиJ и K вместе с атомами азота и углерода, с которыми они соответственно связаны, образуют 5-7-членное гетероциклическое кольцо, которое может содержать гетероатом, выбранный из О, S, SO и SO2; Х выбирают из группы, состоящей из Ar, OR2 и -N(R3)R4; где R2 имеет те же значения, что R1;R3 и R4 независимо имеют те же значения,что В и D соответственно или R3 и R4 вместе образуют 5-7-членное гетероциклическое алифатическое или ароматическое кольцо иm равен 0 или 1; б) нейротропный фактор и в) фармацевтически приемлемый носитель. 2. Фармацевтически приемлемая композиция по п.1, в которой указанное соединение имеет структурную формулу где J и K независимо являются линейным или разветвленным алкилом (С 1-С 6) или Аrзамещенным линейным или разветвленным алкилом (С 1-С 6). 5. Фармацевтически приемлемая композиция по п.1, в которой каждый Аr независимо выбирают из фенила, 2-пиридила, 3-пиридила, 4-пиридила, имидазолила, индолила, изоиндолила, хинолинила,изохинолинила, 1,2,3,4-тетрагидроизохинолинила или 1,2,3,4-тетрагидрохинолинила и каждый Аr необязательно содержит 1-3 заместителя, независимо выбранных из гидроксила, нитро-, трифторметила, линейного или разветвленного алкила (С 1-С 6), О-(линейного или разветвленного алкила (С 1-С 6, галогена, SО 3 Н или -NR3R4. 6. Фармацевтически приемлемая композиция по п.2, в которой указанное соединение выбирают из соединений 6-10, 12, 16-19, 21 или 23 приведенной ниже таблицы. где J и K независимо являются линейным или разветвленным алкилом (С 1-С 6) или Arзамещенным линейным или разветвленным алкилом (С 1-С 6) и w равно 1 или 2. 3. Фармацевтически приемлемая композиция по п.1, в которой по меньшей мере один из В или D независимо представлен формулойs равно 0-1 и каждый Z независимо выбирают из группы, состоящей из О, S, SO, SO2 и NR, где R выбирают из группы, состоящей из водорода, линейного или разветвленного алкила (С 1-С 4), линейного или разветвленного алкенила или алкинила (С 3-С 4) и мостикового алкила (С 1-С 4), где мостик образован между азотом и Аr-группой. 4. Фармацевтически приемлемая композиция по п.3, в которой указанное соединение имеет структурную формулу 7. Фармацевтически приемлемая композиция по п.6, выбранная из(S)-N-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-(4-хлорфенил)N-(3-пиридин-3-ил-1-(2-пиридин-3-ил-пропил) бутил)пропионамида. 8. Фармацевтически приемлемая композиция по п.1, в которой указанный нейротропный фактор выбирают из фактора роста нервной ткани (ФРН), инсулинового фактора роста(ИФР) и их активных стволовых производных,кислотного фибробластного фактора роста(кФФР), основного фибробластного фактора роста (оФФР), факторов роста, полученных из тромбоцитов (ФРПТ), нейротропного фактора,полученного из головного мозга (НФПГМ), цилиарных нейротропных факторов (ЦНТФ), нейротропного фактора, полученного из линии глиальных клеток (НФПГК), нейротрофина-3 (НТ 3) и нейротрофина 4/5 (НТ-4/5). 9. Фармацевтически приемлемая композиция по п.8, в которой указанный нейротропный фактор представляет собой фактор роста нервной ткани (ФРН). 10. Способ стимуляции роста невритов у пациента или в нервных клетках ex vivo, включающий введение указанному пациенту или в указанные нервные клетки нейротропного количества соединения, имеющего структурную формулу (I) и его фармацевтически приемлемых производных, в которойR1, В, D, J, K, Х и m являются такими, как определено в п.1. 11. Способ по п.10, в котором указанное соединение имеет структурную формулу в которой J, K и w являются такими, как определено в п.2. 12. Способ по п.10, в котором по меньшей мере один из В или D независимо представлен формулой -(СН 2)r-Z-(СН 2)s-Ar, где r, s и Z являются такими, как определено в п.3. 13. Способ по п.12, в котором указанное соединение имеет структурную формулу где J и K являются такими, как определено в п.4. 14. Способ по п.10, в котором каждый Аr выбирают независимо из фенила, 2-пиридила, 3-пиридила, 4-пиридила, имидазолила, индолила, изоиндолила, хинолинила,изохинолинила, 1,2,3,4-тетрагидроизохинолинила или 1,2,3,4-тетрагидрохинолинила и каждый Аr необязательно и независимо содержит 1-3 заместителя, независимо выбранные из гидроксила, нитро-, трифторметила, линейного или разветвленного алкила (С 1-С 6), О(линейного или разветвленного алкила (С 1-С 6,галогена, SО 3 Н или -NR3R4. 15. Способ по п.11, в котором указанное соединение выбирают из соединений 6-10, 12,16-19, 21 или 23 таблицы. 24 16. Способ по п.15, в котором указанное соединение выбирают из группы, состоящей из(S)-N-метил-2-(метил-(2-оксо-2-(3,4,5-триметоксифенил)ацетил)амино)-3-(4-хлорфенил)N-(3-пиридин-3-ил-1-(2-пиридин-3-ил-пропил) бутил)пропионамида. 17. Способ по любому из пп.10-16, в котором указанное соединение вводят пациенту вместе с фармацевтически приемлемым носителем в виде фармацевтически приемлемой композиции. 18. Способ по п.17, в котором указанный способ используется для лечения пациента,страдающего болезнью Альцгеймера, болезнью Паркинсона, ALS, рассеянным склерозом, инсультом и ишемией, связанной с инсультом,невральной паропатией, другими невральными дегенеративными заболеваниями, заболеваниями двигательных нейронов, раздавленным седалищным нервом, периферической невропатией,диабетической невропатией, повреждением спинного мозга или поражением лицевого нерва. 19. Способ по п.18, включающий дополнительную стадию введения указанному пациенту нейротропного фактора, в котором указанный нейротропный фактор соединяют с указанным соединением с получением разовой дозовой формы или указанный нейротропный фактор и указанное соединение вводят в виде отдельных дозовых форм. 20. Способ по п.19, в котором указанный нейротропный фактор выбирают из фактора роста нервной ткани (ФРН), инсулинового фактора роста (ИФР) и их активных стволовых производных, кислотного фибробластного фактора роста (кФФР), основного фибробластного фактора роста (оФФР), факторов роста, полученных из тромбоцитов (ФРПТ), нейротропного фактора, полученного из головного мозга(ЦНТФ), нейротропного фактора, полученного из глиальных клеток (НФПГК), нейротрофина-3(НТ-3) и нейротрофина 4/5 (НТ-4/5). 21. Способ по п.20, в котором указанный нейротропный фактор представляет собой фактор роста нервной ткани (ФРН). 22. Способ по любому из пп.18-21, в котором указанный пациент страдает от периферической невропатии, связанной с диабетом. 23. Способ по любому из пп.10-16, в котором указанный способ используют для стимуляции регенерации нервов ex vivo. 24. Способ по п.23, включающий дополнительную стадию контактирования указанных нервных клеток с нейротропным фактором. 25. Способ по п.24, в котором указанный нейротропный фактор выбирают из фактора роста нервной ткани (ФРН), инсулинового фактора роста (ИФР) и их активных стволовых производных, кислотного фибробластного фактора роста (кФФР), основного фибробластного 26 фактора роста (оФФР), факторов роста, полученных из тромбоцитов (ФРПТ), нейротропного фактора, полученного из головного мозга(ЦНТФ), нейротропного фактора, полученного из глиальных клеток (НФПГК), нейротрофина-3(НТ-3) и нейротрофина 4/5 (НТ-4/5). 26. Способ по п.25, в котором указанный нейротропный фактор представляет собой фактор роста нервной ткани (ФРН).
МПК / Метки
МПК: A61K 38/18, A61P 25/00
Метки: стимуляции, роста, композиции, невритов, способы
Код ссылки
<a href="https://eas.patents.su/14-4247-sposoby-i-kompozicii-dlya-stimulyacii-rosta-nevritov.html" rel="bookmark" title="База патентов Евразийского Союза">Способы и композиции для стимуляции роста невритов</a>
Предыдущий патент: Фотодинамическое лечение и облучение уф-в лучами суспензии тромбоцитов
Следующий патент: Производные 4-, 5-, 6- и 7-замещенного индола и индолина, их получение и применение
Случайный патент: Способ получения хирально чистого n-(транс-4- изопропилциклогексилкарбонил)-d-фенилаланина и его кристаллических модификаций


















