Соединения бензотиазина и бензотиадиазина, способ их получения и фармацевтические композиции, которые их содержат
Формула / Реферат
1. Соединения формулы (I)

где R1 представляет собой арильную или гетероарильную группу,
R2 представляет собой атом водорода, атом галогена или гидроксильную группу,
X представляет собой атом кислорода или атом серы,
Y представляет собой атом кислорода, атом серы или группу NR, где R представляет собой атом водорода или линейную или разветвленную C1-С6-алкильную группу,
А представляет собой NR4-группу,
R3 представляет собой атом водорода, линейную или разветвленную C1-С6-алкильную группу или С3-С7-циклоалкильную группу,
R4 представляет собой атом водорода или линейную или разветвленную C1-С6-алкильную группу, или
А представляет собой атом азота и, вместе со смежной -CHR3-группой, образует кольцо 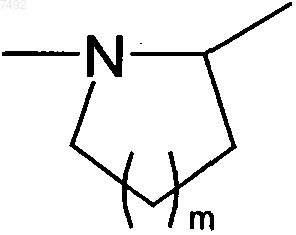 , где m представляет собой 1, 2 или 3,
, где m представляет собой 1, 2 или 3,
R5 представляет собой атом водорода или атом галогена,
их изомеры и их аддитивные соли с фармацевтически приемлемой кислотой или основанием,
где подразумевается, что
"арильная группа" обозначает ароматическую моноциклическую группу или бициклическую группу, в которой по крайней мере одно из колец является ароматическим, необязательно замещенную одной или более одинаковыми или разными группами: галогеном, линейным или разветвленным C1-С6-алкилом, линейным или разветвленным C1-С6-алкокси, линейным или разветвленным C1-С6-пергалоалкилом, линейным или разветвленным C1-С6-пергалоалкокси, гидрокси, циано, нитро, амино (необязательно замещенным одной или более линейной или разветвленной C1-С6-алкильными группами), аминосульфонилом (необязательно замещенным одной или более линейной или разветвленной C1-С6-алкильными группами), C1-С6-алкилсульфониламино или фенилом (необязательно замещенным одной или более одинаковыми или разными группами: галогеном, линейным или разветвленным C1-С6-алкилом, линейным или разветвленным C1-С6-пергалоалкилом, гидрокси или линейным или разветвленным C1-С6-алкокси),
"гетероарильная группа" обозначает ароматическую моноциклическую группу или бициклическую группу, в которой по крайней мере одно из колец является ароматическим, содержащую один, два или три одинаковых или разных гетероатома, выбранных из азота, кислорода и серы, необязательно замещенную одной или более одинаковыми или разными группами: галогеном, линейным или разветвленным C1-С6-алкилом, линейным или разветвленным C1-С6-алкокси, линейным или разветвленным C1-С6-пергалоалкилом, линейным или разветвленным C1-С6-пергалоалкокси, гидрокси, циано, нитро, амино (необязательно замещенным одной или более линейной или разветвленной C1-С6-алкильными группами), аминосульфонилом (необязательно замещенного одной или более линейной или разветвленной C1-С6-алкильными группами) или C1-С6-алкилсульфониламино.
2. Соединения формулы (I) по п.1, в которых R1 представляет собой арильную группу.
3. Соединения формулы (I) по п.1 или 2, в которых R2 представляет собой атом водорода.
4. Соединения формулы (I) по любому из пп.1-3, в которых А представляет собой группу NR4.
5. Соединения формулы (I) по любому из пп.1-3, в которых А, вместе со смежной группой -CHR3-, образует кольцо 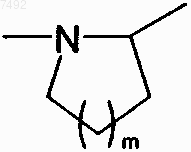 .
.
6. Соединения формулы (I) по п.5, в которых m представляет собой 1.
7. Способ получения соединений формулы (I), который характеризуется тем, что в качестве исходного вещества применяют соединение формулы (II)
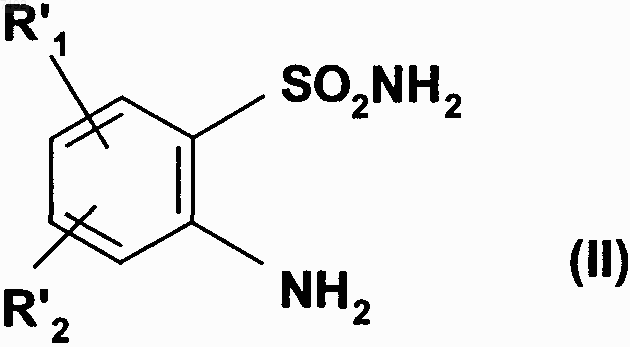
где R'1 представляет собой линейную или разветвленную C1-С6-алкоксигруппу,
R'2 представляет собой атом водорода, атом галогена или линейную или разветвленную C1-С6-алкоксигруппу,
которое подвергают реакции с хлорангидридом кислоты формулы (III) в присутствии основания в среде тетрагидрофурана или ацетонитрила
Сl-СН2-(СН2)m-СН2-СОСl (III),
где m имеет значения, указанные для формулы (I),
с получением соединения формулы (IV)
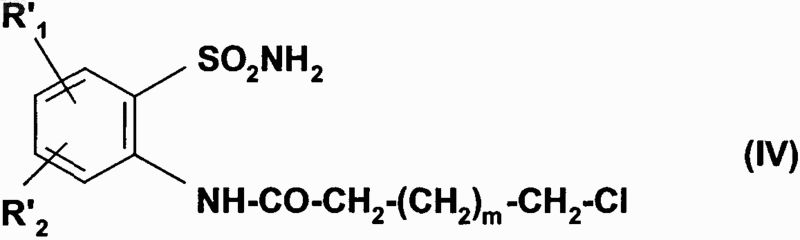
где R'1, R'2 имеют значения, указанные выше,
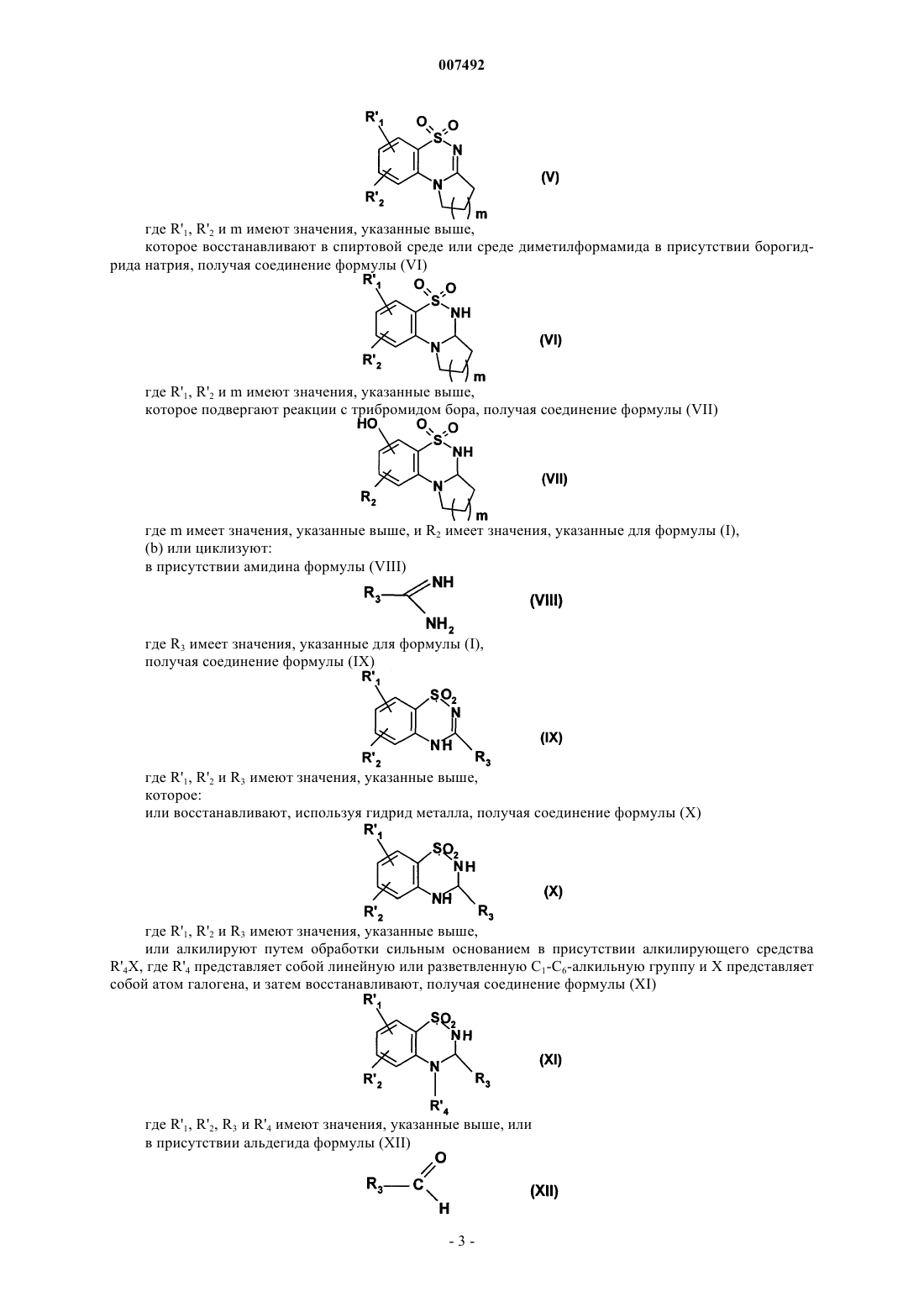
которое затем циклизуют в щелочной среде с получением соединения формулы (V)
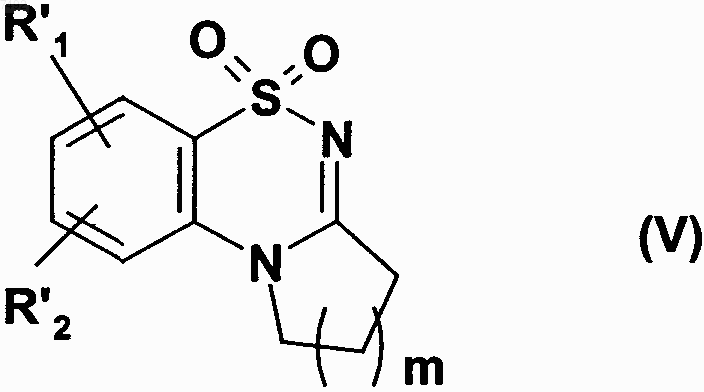
где R'1, R'2 и m имеют значения, указанные выше,
которое восстанавливают в спиртовой среде или среде диметилформамида в присутствии борогидрида натрия, с получением соединения формулы (VI)
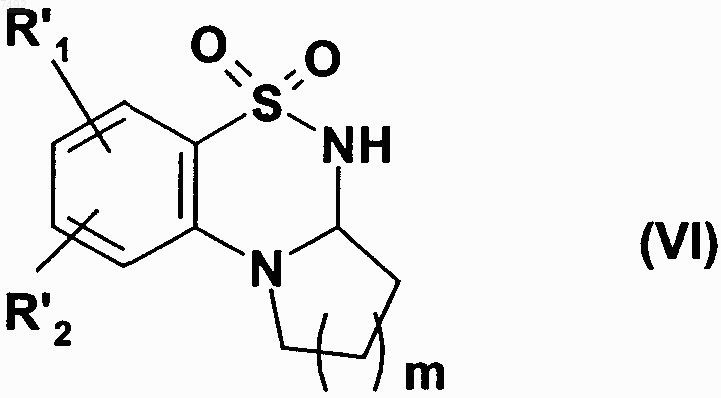
где R'1, R'2 и m имеют значения, указанные выше,
которое подвергают реакции с трибромидом бора, с получением соединения формулы (VII)
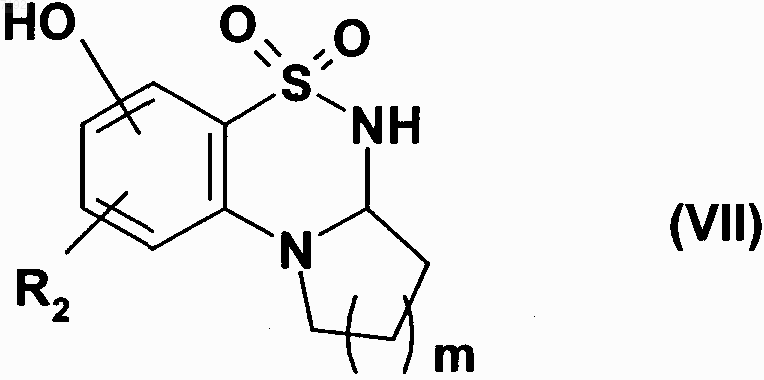
где m имеет значения, указанные выше, и R2 имеет значения, указанные для формулы (I),
которое подвергают реакции с соединением формулы (XIVa)
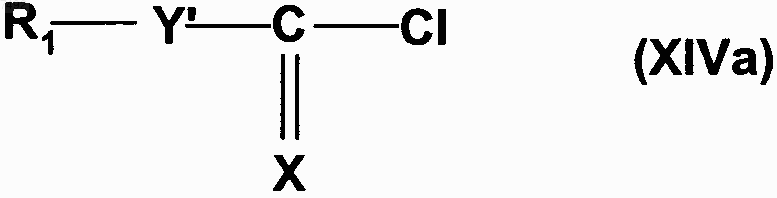
где R1, X имеют значения, указанные для формулы (I), и Y' представляет собой атом кислорода, атом серы или группу NR', где R' представляет собой линейную или разветвленную C1-С6-алкильную группу,
или с соединением формулы (XIVb)
R1-N=С=X (XIVb),
где R1 и X имеют значения, указанные для формулы (I),
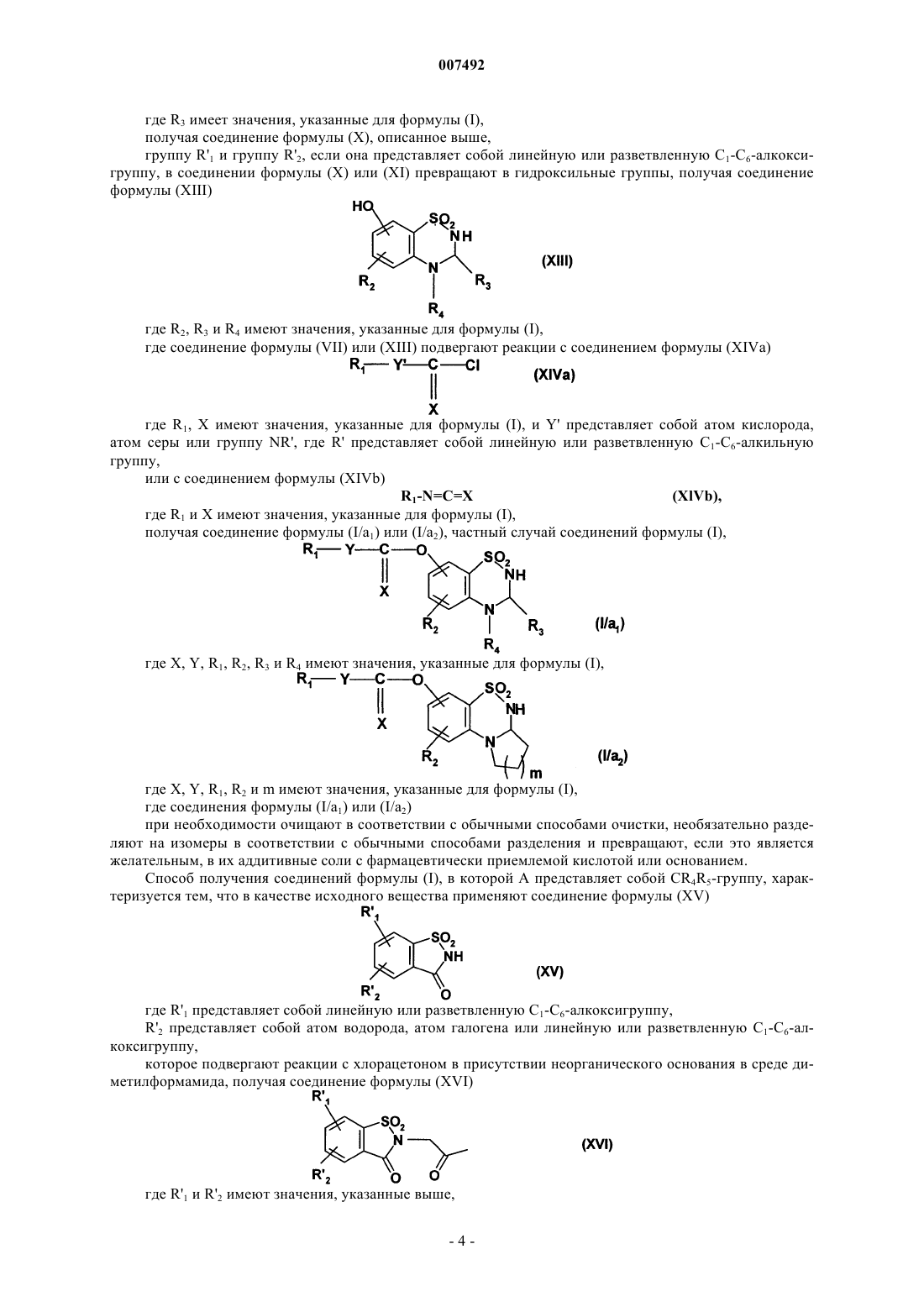
с получением соединения формулы (I/a1) или (I/а2), частного случая соединений формулы (I),
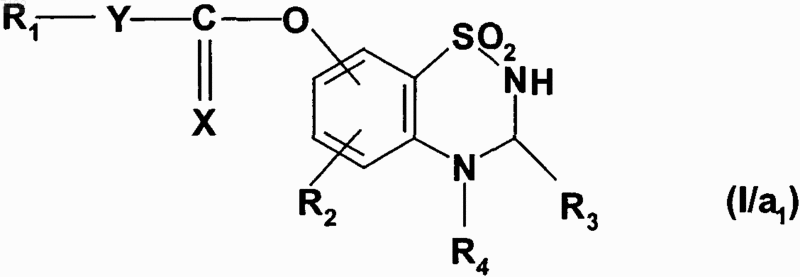
где X, Y, R1, R2, R3 и R4 имеют значения, указанные для формулы (I),
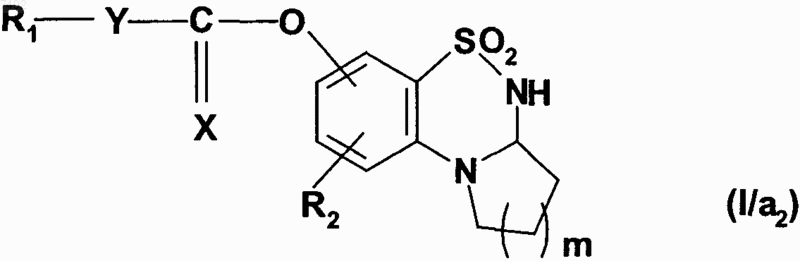
где X, Y, R1, R2 и m имеют значения, указанные для формулы (I),
где соединения формулы (I/a1) или (I/а2) при необходимости очищают в соответствии с обычными способами очистки, необязательно разделяют на изомеры в соответствии с обычными способами разделения и превращают, если это является желательным, в их аддитивные соли с фармацевтически приемлемой кислотой или основанием.
8. Фармацевтические композиции, которые содержат в качестве активного компонента соединение по любому из пп.1-6 в сочетании с одним или более фармацевтически приемлемыми, инертными, нетоксичными наполнителями или носителями.
9. Фармацевтические композиции по п.8, предназначенные для применения в качестве лекарственных средств, таких как АМРА модуляторы.
Текст
007492 Настоящее изобретение относится к новым соединениям бензотиазина и бензотиадиазина, к способу их получения и к фармацевтическим композициям, которые их содержат. В настоящее время известно, что "инициирующие" аминокислоты, особенно глутамат, играют очень важную роль в физиологических процессах приспосабливаемости нейронов к воздействиям внешней среды и в механизмах, лежащих в основе обучения и памяти. Патофизиологические исследования свидетельствуют о том, что нарушение в глутаматэргической нейротрансмиссии тесно связано с развитием болезни Альцгеймера (Neuroscience and Biobehavioral reviews, 1992, 16, 13-24; Progress in Neurobiology,1992, 39, 517-545). Кроме того, во многих исследованиях в последние годы показано, что существуют подтипы рецепторов "инициирующих" аминокислот и их функциональное взаимодействие (Molecular Neuropharmacology,1992, 2, 15-31). Среди этих рецепторов рецептор АМРА ("-амино-3-гидрокси-5-метил-4-изоксазолпропионовая кислота") в наибольшей степени вовлечен в процессы физиологической возбудимости нейронов, и в особенности в те процессы, которые связаны с запоминанием. Например, было показано, что обучаемость связана с увеличением связывания АМРА с его рецептором в гиппокампе, одном из участков головного мозга, который отвечает за процессы памяти и распознавания. Также в последнее время описаны ноотропные средства, такие как анирацетам, в качестве положительных модуляторов рецепторов АМРА нейронов (Journal of Neurochemistry, 1992, 58, 1199-1204). В литературе описаны соединения, имеющие бензамидную структуру, в качестве средств, имеющих такой же механизм действия и улучшающих память (Synapse, 1993, 15, 326-329). Из этих новых фармакологических средств наиболее активным является, в частности, соединение ВА 74. Дополнительно, в патентной заявке ЕР 692 484 описано соединение бензотиадиазина, которое способствует току, вызываемому АМРА, и в международной патентной заявке WO 99/42456 также описаны частные соединения бензотиадиазина в качестве модуляторов рецепторов АМРА. Соединения бензотиазина и бензотиадиазина, раскрытые в настоящем изобретении, кроме того, что являются новыми, неожиданно обнаруживают фармакологическое действие на ток, вызываемый АМРА,которое существенно выше по сравнению с соединениями, обладающими подобной структурой, описанными в уровне техники. Они являются пригодными в качестве модуляторов АМРА для лечения или предотвращения нарушений памяти и распознавания, которые связаны с возрастом, с синдромами тревоги или депрессии, с прогрессирующими нейродегенеративными заболеваниями, с болезнью Альцгеймера, с болезнью Пика (предстарческая органическая атрофия мозга), с хореей Хантингтона, с шизофренией, с последствиями острых нейродегенеративных заболеваний, с последствиями ишемии и с последствиями эпилепсии. В частности, настоящее изобретение относится к соединениям формулы (I) где R1 представляет собой арильную или гетероарильную группу,R2 представляет собой атом водорода, атом галогена или гидроксильную группу,X представляет собой атом кислорода или атом серы,Y представляет собой атом кислорода, атом серы или группу NR, где R представляет собой атом водорода или линейную или разветвленную C1-С 6-алкильную группу,А представляет собой CR4R5 группу или NR4-группу,R3 представляет собой атом водорода, линейную или разветвленную C1-С 6-алкильную группу или С 3-С 7-циклоалкильную группу,R4 представляет собой атом водорода или линейную или разветвленную C1-С 6-алкильную группу,или,А представляет собой атом азота и, вместе со смежной -CHR3- группой, образует кольцо где m представляет собой 1, 2 или 3,R5 представляет собой атом водорода или атом галогена,к их изомерам и их аддитивным солям с фармацевтически приемлемой кислотой или основанием,где подразумевается, что"арильная группа" обозначает ароматическую моноциклическую группу или бициклическую группу, в которой по крайней мере одно из колец является ароматическим, необязательно замещенную одной или более одинаковыми или разными группами: галогеном, линейным или разветвленным C1-С 6-алкилом, линейным или разветвленным C1-С 6-алкокси, линейным или разветвленным C1-С 6-пергалоалкилом,линейным или разветвленным C1-С 6-пергалоалкокси, гидрокси, циано, нитро, амино (необязательно за-1 007492 мещенным одной или более линейной или разветвленной C1-С 6-алкильными группами), аминосульфонилом (необязательно замещенным одной или более линейной или разветвленной C1-С 6-алкильными группами), C1-С 6-алкилсульфониламино или фенилом (необязательно замещенным одной или более одинаковыми или разными группами: галогеном, линейным или разветвленным C1-С 6-алкилом, линейным или разветвленным C1-С 6-пергалоалкилом, гидрокси или линейным или разветвленным C1-С 6-алкокси),"гетероарильная группа" обозначает ароматическую моноциклическую группу или бициклическую группу, в которой по крайней мере одно из колец является ароматическим, содержащую один, два или три одинаковых или разных гетероатома, выбранных из азота, кислорода и серы, необязательно замещенную одной или более одинаковыми или разными группами: галогеном, линейным или разветвленным C1-С 6-алкилом, линейным или разветвленным C1-С 6-алкокси, линейным или разветвленным C1-С 6 пергалоалкилом, линейным или разветвленным C1-С 6-пергалоалкокси, гидрокси, циано, нитро, амино(необязательно замещенным одной или более линейной или разветвленной C1-С 6-алкильными группами),аминосульфонилом (необязательно замещенным одной или более линейной или разветвленной C1-С 6 алкильными группами) или C1-С 6-алкилсульфониламино. Среди фармацевтически приемлемых кислот можно отметить, но не ограничиваясь только ими, соляную кислоту, бромисто-водородную кислоту, серную кислоту, фосфоновую кислоту, уксусную кислоту, трифторуксусную кислоту, молочную кислоту, пировиноградную кислоту, малоновую кислоту, янтарную кислоту, глутаровую кислоту, фумаровую кислоту, винную кислоту, малеиновую кислоту, лимонную кислоту, аскорбиновую кислоту, метансульфокислоту, камфорную кислоту и т.д. Среди фармацевтически приемлемых оснований можно отметить, но не ограничиваясь только ими,гидроокись натрия, гидроокись калия, триэтиламин, трет-бутиламин и т.д. Предпочтительной арильной группой является фенильная группа. Предпочтительной группой R2 является атом водорода. А предпочтительно представляет собой NR4-группу или представляет собой атом азота и, вместе соY предпочтительно представляет собой атом кислорода или атом серы. Изобретение также относится к способу получения соединений формулы (I). Способ получения соединений формулы (I), в которой А представляет собой NR4-группу или А, где m представляет собой атом азота и вместе со смежной группой CHR3 образует кольцо представляет собой 1, 2 или 3, характеризуется тем, что в качестве исходного вещества применяют соединение формулы (II) где R'1 представляет собой линейную или разветвленную C1-С 6-алкоксигруппу,R'2 представляет собой атом водорода, атом галогена или линейную или разветвленную C1-С 6-алкоксигруппу,которое:(а) или подвергают реакции с хлорангидридом кислоты формулы (III) в присутствии основания в среде тетрагидрофурана или ацетонитрила:(III),где m имеет значения, указанные для формулы (I),получая соединение формулы (IV) где R'1, R'2 и m имеют значения, указанные выше,которое затем циклизуют в щелочной среде, получая соединение формулы (V) где R'1, R'2 и m имеют значения, указанные выше,которое восстанавливают в спиртовой среде или среде диметилформамида в присутствии борогидрида натрия, получая соединение формулы (VI) где R'1, R'2 и m имеют значения, указанные выше,которое подвергают реакции с трибромидом бора, получая соединение формулы (VII) где m имеет значения, указанные выше, и R2 имеет значения, указанные для формулы (I),(b) или циклизуют: в присутствии амидина формулы (VIII) где R3 имеет значения, указанные для формулы (I),получая соединение формулы (IX) где R'1, R'2 и R3 имеют значения, указанные выше,которое: или восстанавливают, используя гидрид металла, получая соединение формулы (X) где R'1, R'2 и R3 имеют значения, указанные выше,или алкилируют путем обработки сильным основанием в присутствии алкилирующего средстваR'4X, где R'4 представляет собой линейную или разветвленную C1-С 6-алкильную группу и X представляет собой атом галогена, и затем восстанавливают, получая соединение формулы (XI) где R'1, R'2, R3 и R'4 имеют значения, указанные выше, или в присутствии альдегида формулы (XII)-3 007492 где R3 имеет значения, указанные для формулы (I),получая соединение формулы (X), описанное выше,группу R'1 и группу R'2, если она представляет собой линейную или разветвленную C1-С 6-алкоксигруппу, в соединении формулы (X) или (XI) превращают в гидроксильные группы, получая соединение формулы (XIII) где R2, R3 и R4 имеют значения, указанные для формулы (I),где соединение формулы (VII) или (XIII) подвергают реакции с соединением формулы (XIVa) где R1, X имеют значения, указанные для формулы (I), и Y' представляет собой атом кислорода,атом серы или группу NR', где R' представляет собой линейную или разветвленную C1-С 6-алкильную группу,или с соединением формулы (XIVb)(XlVb),R1-N=С=X где R1 и X имеют значения, указанные для формулы (I),получая соединение формулы (I/a1) или (I/а 2), частный случай соединений формулы (I), где X, Y, R1, R2, R3 и R4 имеют значения, указанные для формулы (I), где X, Y, R1, R2 и m имеют значения, указанные для формулы (I),где соединения формулы (I/a1) или (I/а 2) при необходимости очищают в соответствии с обычными способами очистки, необязательно разделяют на изомеры в соответствии с обычными способами разделения и превращают, если это является желательным, в их аддитивные соли с фармацевтически приемлемой кислотой или основанием. Способ получения соединений формулы (I), в которой А представляет собой CR4R5-группу, характеризуется тем, что в качестве исходного вещества применяют соединение формулы (XV) где R'1 представляет собой линейную или разветвленную C1-С 6-алкоксигруппу,R'2 представляет собой атом водорода, атом галогена или линейную или разветвленную C1-С 6-алкоксигруппу,которое подвергают реакции с хлорацетоном в присутствии неорганического основания в среде диметилформамида, получая соединение формулы (XVI) где R'1 и R'2 имеют значения, указанные выше,-4 007492 которое подвергают перегруппировке в щелочной среде, получая соединение формулы (XVII) где R'1 и R'2 имеют значения, указанные выше,которое деацетилируют путем нагревания с обратным холодильником в среде бензола в присутствии избытка этиленгликоля и каталитического количества n-толуолсульфокислоты, получая соединение формулы где R'1 и R'2 имеют значения, указанные выше,которое подвергают гидролизу в кислой среде, получая соединение формулы (ХIХа) где R'1 и R'2 имеют значения, указанные выше,в котором, необязательно, если R3 не представляет собой атом водорода, атом азота защищают защитной группой и которое затем, после обработки сильным основанием, подвергают реакции с соединением формулы R'3-P, где R'3 представляет собой линейную или разветвленную C1-С 6-алкильную группу или С 3-С 7-циклоалкильную группу и Р представляет собой уходящую группу,получая, после снятия защиты с атома азота, соединение формулы (XIX'a) где R'1 и R'2 имеют одинаковые значения и R3 имеет значения, указанные для формулы (I),или подвергают каталитическому восстановлению, получая соединение формулы (XX) где R'1, R'2 и R3 имеют значения, указанные выше,или превращают в спирт путем реакции с гидридом и гидроксильную группу полученного соединения превращают в атом галогена путем взаимодействия с подходящим реагентом, получая соединение формулы (XXI) где R'1, R'2 и R3 имеют значения, указанные выше, R'5 представляет собой атом галогена,или подвергают реакции с магнийорганическим соединением R'4 MgBr, где R'4 представляет собой линейную или разветвленную C1-С 6-алкильную группу, получая соединение формулы (XIXb) где R'1, R'2, R3 и R'4 имеют значения, указанные выше,где соединение формулы (XIXb) или подвергают каталитическому восстановлению, получая соединение формулы (XXII) где R'1, R'2, R3 и R'4 имеют значения, указанные выше,или гидроксильную группу которого превращают в атом галогена путем взаимодействия с подходящим реагентом, получая соединение формулы (XXIII) где R'1, R'2, R3 и R'4 имеют значения, указанные выше, и R'5 представляет собой атом галогена,группу R'1 и группу R'2, если она представляет собой линейную или разветвленную C1-С 6 алкоксигруппу, в соединениях формул (XX)-(XXIII) превращают в гидроксильные группы, получая соединение формулы (XXIV) где R2, R3, R4 и R5 имеют значения, указанные для формулы (I),где соединение формулы (XXIV) подвергают реакции с соединением формулы (XIVa) где R1, X имеют значения, указанные для формулы (I), и Y' представляет собой атом кислорода,атом серы или группу NR', где R' представляет собой линейную или разветвленную C1-С 6-алкильную группу,или с соединением формулы (XIVb)(XIVb),R1-N=С=X где R1 и X имеют значения, указанные для формулы (I),получая соединение формулы (I/b), частный случай соединений формулы (I),где X, Y, R1, R2, R3, R4, R5 имеют значения, указанные для формулы (I),которое очищают, при необходимости, в соответствии с обычными способами очистки, необязательно разделяют на изомеры в соответствии с обычными способами разделения и превращают, если это является желательным, в аддитивные соли с фармацевтически приемлемой кислотой или основанием. Изобретение также относится к фармацевтическим композициям, которые содержат в качестве активного компонента соединение формулы (I) с одним или более подходящими, инертными, нетоксичными наполнителями. Среди фармацевтических композиций согласно изобретению особенно можно отметить те, которые являются пригодными для перорального, парентерального (внутривенного или подкожного) или назального введения, таблетки или драже, подъязычные таблетки, желатиновые капсулы, лепешки, суппозитории, кремы, мази, кожные гели, составы для инъекций, суспензии для питья и т.д. Полезная дозировка может адаптироваться в зависимости от природы и тяжести расстройства, пути введения и возраста и веса пациента. Дозировка находится в пределах от 1 до 500 мг в сутки на одно или больше введений. Примеры, представленные далее, приведены только с целью иллюстрации и никоим образом не ограничивают изобретение. Используемые исходные вещества являются известными продуктами или их получают в соответствии с известными способами. Структуры соединений, описанных в примерах, были определены в соответствии с обычными спектрофотометрическими способами (инфракрасная спектрометрия, ядерный магнитный резонанс, массспектрометрия и т.п). Пример 1. 5,5-Диоксидо-2,3,3 а,4-тетрагидро-1H-пирроло[2,1-с][1,2,4]бензотиадиазин-7-ил фенил карбонат. Стадия А. N-[2-(аминосульфонил)-4-метоксифенил 1-4-хлорбутанамид. 144 ммоль триэтиламина и затем по каплям раствор, содержащий 135 ммоль хлорангидрида 4 хлорбутановой кислоты в 30 мл тетрагидрофурана (ТГФ) добавляли к раствору, содержащему 96,4 ммоль 2-амино-5-метоксибензолсульфонамида в 200 мл ТГФ. После перемешивания в течение ночи при температуре окружающей среды ТГФ выпаривали и остаток ресуспендировали в воде. После экстрагирования этилацетатом органическую фазу промывали и высушивали. После выпаривания получали требуемый продукт в виде масла. Стадия В. 5,5-Диоксидо-7-метокси-2,3-дигидро-1H-пирроло[2,1-c][1,2,4]бензотиадиазин. Продукт, полученный на вышеописанной стадии, перемешивали всю ночь при температуре окружающей среды в 320 мл водного 1 н. раствора гидроксида натрия. После добавления 50 мл этилацетата и интенсивного перемешивания требуемый продукт, который выпадал в осадок, отфильтровывали, промывали и высушивали. Стадия С. 5,5-Диоксидо-7-метокси-2,3,3 а,4-тетрагидро-1H-пирроло[2,1-c][1,2,4]бензотиадиазин. 106,5 ммоль борогидрида натрия добавляли к суспензии, содержащей 35,5 ммоль продукта, полученного на вышеописанной стадии, в 40 мл диметилформамида (ДМФА). После перемешивания в течение ночи при температуре окружающей среды реакционную смесь охлаждали и затем к вышеописанной смеси добавляли 150 мл ледяного раствора 1 н. соляной кислоты. Требуемый продукт осаждали и отфильтровывали. Точка плавления: 193-198 С. Стадия D. 5,5-Диоксидо-2,3,3 а,4-тетрагидро-1H-пирроло[2,1-с][1,2,4]бензотиадиазин-7-ол. 79,3 ммоль трибромида бора по каплям добавляли к суспензии, содержащей 26,7 ммоль продукта,полученного на вышеописанной стадии, в 350 мл дихлорметана, выдерживая при -60 С в атмосфере азота. Температуру поддерживали в течение 1 ч и затем температуру доводили до температуры окружающей среды и перемешивали всю ночь. После охлаждения реакционной смеси на ледяной бане добавляли 100 мл воды и образованную двухфазную систему интенсивно перемешивали. Образованную таким образом суспензию фильтровали. Полученное белое твердое вещество промывали водой, эфиром и высушивали, получая требуемый продукт. Точка плавления: 237-242 С. Стадия Е. 5,5-Диоксидо-2,3,3 а,4-тетрагидро-1H-пирроло[2,1-с][1,2,4]бензотиадиазин-7-ил фенил карбонат. К суспензии, содержащей 0,83 ммоль соединения, описанного на стадии выше, в 30 мл СН 2 Сl2 добавляли 0,175 мл триэтиламина, 5 мг 4-диметиламинопиридина и по каплям 0,136 мл фенилхлорформиата, растворенного в 2 мл дихлорметана (CH2Cl2). После перемешивания в течение одной ночи при температуре окружающей среды раствор промывали 1 н. соляной кислотой и затем насыщенным раствором хлорида натрия, высушивали и выпаривали. После ресуспендирования остатка в эфире получали требуемый продукт путем фильтрации. Точка плавления: 197-198 С. Элементный микроанализ: Следующие примеры осуществляли в соответствии с методикой, описанной в примере 1, используя подходящие исходные вещества. Пример 2. O-(5,5-Диоксидо-2,3,3 а,4-тетрагидро-1H-пирроло[2,1-с][1,2,4]бензотиадиазин-7-ил) О-фенил тиокарбонат. Получали требуемый продукт путем замены фенилхлорформиата на стадии Е фенилтионохлорформиатом. Точка плавления: 252-254 С. Элементный микроанализ: С НS Теоретический % 54,24 4,28 7,44 17,03 Эмпирический % 53,55 5,02 7,39 17,47 Пример 3. O-(5,5-Диоксидо-2,3,3 а,4-тетрагидро-1H-пирроло[2,1-с][1,2,4]бензотиадиазин-7-ил S-фенил дитиокарбонат. Получали требуемый продукт путем замены фенилхлорформиата на стадии Е фенилдитиохлорформиатом. Точка плавления: 210-214 С. Элементный микроанализ: С НS Теоретический % 52,02 4,11 7,14 24,51 Эмпирический % 51,85 4,10 7,36 24,69 Пример 4. O-(5,5-Диоксидо-2,3,3 а,4-тетрагидро-1H-пирроло[2,1-c][1,2,4]бензотиадиазин-7-ил) O-(4 хлорфенил) тиокарбонат. Получали требуемый продукт путем замены фенилхлорформиата на стадии Е 4-хлорфенилтионолорформиатом. Точка плавления: 189-194 С. Элементный микроанализ: С НS Сl Теоретический % 49,69 3,68 6,82 15,61 8,63 Эмпирический % 49,39 3,64 7,06 16,20 9,70 Пример 5. O-(4-Этил-1,1-диоксидо-3,4-дигидро-2H-1,2,4-бензотиадиазин-7-ил) О-фенил тиокарбонат. Стадия А. 7-Метокси-4H-1,2,4-бензотиадиазин 1,1-диоксид. В течение одной ночи перемешивали при 80 С суспензию 3,0 г 2-амино-5-метоксибензолсульфонамида в присутствии 1,31 г гидрохлорида формамидина и 2,27 мл триэтиламина в 50 мл толуола. Толуол выпаривали в вакууме. Остаток ресуспендировали в воде и осадок отфильтровывали. Стадия В. 7-Метокси-4-этил-4H-1,2,4-бензотиадиазин 1,1-диоксид. 2,88 г продукта, полученного на вышеописанной стадии, добавляли порциями к суспензии 9 мл ДМФА, содержащей 570 мг 60% NaH в минеральном масле. Смесь перемешивали в течение 30 мин до получения черного раствора. К нему по каплям добавляли 929 мкл йодоэтана. Продолжали перемешивать в течение 1 ч и реакционную смесь осаждали путем добавления воды. Осадок отфильтровывали и промывали водой и затем эфиром, получая требуемый продукт. Стадия С. 7-Метокси-4-этил-3,4-дигидро-2H-1,2,4-бензотиадиазин 1,1-диоксид. 1,19 г борогидрида натрия добавляли к суспензии 2,37 г продукта, полученного на вышеописанной стадии, в 40 мл этанола. Смесь постепенно становилась гомогенной. После взаимодействия в течение 1 ч при температуре окружающей среды смесь охлаждали на ледяной бане и нейтрализовали путем прибавления 1 н. НСl. Белый осадок перемешивали в течение 15 мин и указанный в заглавии продукт отфильтровывали. Стадия D. 4-Этил-3,4-дигидро-2H-1,2,4-бензотиадиазин-7-ол 1,1-диоксид. 79,3 ммоль трибромида бора по каплям добавляли к суспензии, содержащей 2 г продукта, полученного на вышеописанной стадии, в 200 мл дихлорметана, выдерживая при -60 С в атмосфере азота. Температуру поддерживали в течение 1 ч и затем температуру доводили до температуры окружающей среды и перемешивали всю ночь. После охлаждения реакционной смеси на ледяной бане добавляли 100 мл воды и двухфазную систему интенсивно перемешивали. Образованную таким образом суспензию фильтровали. Полученное твердое вещество промывали водой, эфиром и высушивали, получая требуемый продукт. Точка плавления: 214-218 С. Стадия Е. O-(4-Этил-1,1-диоксидо-3,4-дигидро-2H-1,2,4-бензотиадиазин-7-ил) О-фенил тиокарбонат. Получали требуемый продукт в соответствии с методикой, описанной на стадии Е примера 1, заменяя фенилхлорформиат фенилтионохлорформиатом. Точка плавления: 173-175 С. Элементный микроанализ: Пример 6. О-(4-Этил-1,1-диоксидо-3,4-дигидро-2H-1,2,4-бензотиадиазин-7-ил) S-фенил дитиокарбонат. Получали требуемый продукт в соответствии с методикой, описанной в примере 5, заменяя фенилтионохлорформиат на стадии Е фенилдитиохлорформиатом. Точка плавления: 228-232 С. Элементный микроанализ: С НS Теоретический % 50,50 4,24 7,36 25,28 Эмпирический % 50,07 4,09 7,57 25,31 Пример 7. O-(4-Этил-1,1-диоксидо-3,4-дигидро-2H-1,2,4-бензотиадиазин-7-ил) O-(4-хлорфенил)тиокарбонат. Получали требуемый продукт в соответствии с методикой, описанной в примере 5, заменяя фенилтионохлорформиат на стадии Е 4-хлорфенилтионохлорформиатом. Точка плавления: 155-156 С. Элементный микроанализ: С НS Сl Теоретический % 48,18 3,79 7,02 16,08 8,89 Эмпирический % 48,64 3,93 6,91 16,08 8,98 Фармакологические исследования соединений по изобретению Исследования возбуждающих токов, вызванных AMPА, на ооцитах лягушки а - Способ. Получали мРНК из коры головного мозга самцов крыс Wistar при помощи способа с использованием тиоцианата гуанидина/фенола/хлороформа. Выделяли поли-(А+) мРНК путем хроматографии на олиго-dT целлюлозе и вводили в дозе 50 нг на ооцит. Ооциты инкубировали 2-3 дня при 18 С, чтобы позволить проявиться экспрессии рецепторов, и затем хранили при 8-10 С. Электрофизиологическую регистрацию осуществляли в камере Plexiglass при 20-24 С в среде OR2(J. Exp. Zool., 1973, 184, 321-334) при помощи 2-электродного "voltage-clamp" метода, третий электрод,помещенный в ванну, был контрольным, как описано в ссылке. Все соединения применяли при помощи инкубационной среды и электрический ток измеряли в конце периода введения. АМРА использовали в концентрации 10 мкМ. Для каждого исследуемого соединения определяли концентрацию, которая вызывает двукратное увеличение (ЕС 2 Х) или пятикратное увеличение (ЕС 5 Х) интенсивности тока, вызванного одним АМРА (5-50 нА). Соединения по изобретению в значительной степени усиливают возбуждающие действие АМРА, и их активность существенно выше по сравнению с активностью сравнительных соединений. Соединение из примера 2, в частности, обеспечивает ЕС 2 Х при концентрации 1,8 мкМ и ЕС 5 Х при концентрации 9,6 мкМ. Фармацевтическая композиция Состав для приготовления 1000 таблеток, каждая из которых содержит дозу 100 мг Соединение из примера 1 100 г Гидроксипропилцеллюлоза 2 г Пшеничный крахмал 10 г Лактоза 100 г Стеарат магния 3 г Тальк 3 г ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединения формулы (I) где R1 представляет собой арильную или гетероарильную группу,R2 представляет собой атом водорода, атом галогена или гидроксильную группу,X представляет собой атом кислорода или атом серы,Y представляет собой атом кислорода, атом серы или группу NR, где R представляет собой атом водорода или линейную или разветвленную C1-С 6-алкильную группу,А представляет собой NR4-группу,R3 представляет собой атом водорода, линейную или разветвленную C1-С 6-алкильную группу или-9 007492 С 3-С 7-циклоалкильную группу,R4 представляет собой атом водорода или линейную или разветвленную C1-С 6-алкильную группу,или А представляет собой атом азота и, вместе со смежной -CHR3-группой, образует кольцоm представляет собой 1, 2 или 3,R5 представляет собой атом водорода или атом галогена,их изомеры и их аддитивные соли с фармацевтически приемлемой кислотой или основанием,где подразумевается, что"арильная группа" обозначает ароматическую моноциклическую группу или бициклическую группу, в которой по крайней мере одно из колец является ароматическим, необязательно замещенную одной или более одинаковыми или разными группами: галогеном, линейным или разветвленным C1-С 6 алкилом, линейным или разветвленным C1-С 6-алкокси, линейным или разветвленным C1-С 6 пергалоалкилом, линейным или разветвленным C1-С 6-пергалоалкокси, гидрокси, циано, нитро, амино(необязательно замещенным одной или более линейной или разветвленной C1-С 6-алкильными группами),аминосульфонилом (необязательно замещенным одной или более линейной или разветвленной C1-С 6 алкильными группами), C1-С 6-алкилсульфониламино или фенилом (необязательно замещенным одной или более одинаковыми или разными группами: галогеном, линейным или разветвленным C1-С 6 алкилом, линейным или разветвленным C1-С 6-пергалоалкилом, гидрокси или линейным или разветвленным C1-С 6-алкокси),"гетероарильная группа" обозначает ароматическую моноциклическую группу или бициклическую группу, в которой по крайней мере одно из колец является ароматическим, содержащую один, два или три одинаковых или разных гетероатома, выбранных из азота, кислорода и серы, необязательно замещенную одной или более одинаковыми или разными группами: галогеном, линейным или разветвленным C1-С 6-алкилом, линейным или разветвленным C1-С 6-алкокси, линейным или разветвленным C1-С 6 пергалоалкилом, линейным или разветвленным C1-С 6-пергалоалкокси, гидрокси, циано, нитро, амино(необязательно замещенным одной или более линейной или разветвленной C1-С 6-алкильными группами),аминосульфонилом (необязательно замещенного одной или более линейной или разветвленной C1-С 6 алкильными группами) или C1-С 6-алкилсульфониламино. 2. Соединения формулы (I) по п.1, в которых R1 представляет собой арильную группу. 3. Соединения формулы (I) по п.1 или 2, в которых R2 представляет собой атом водорода. 4. Соединения формулы (I) по любому из пп.1-3, в которых А представляет собой группу NR4. 5. Соединения формулы (I) по любому из пп.1-3, в которых А, вместе со смежной группой -CHR3-,. образует кольцо 6. Соединения формулы (I) по п.5, в которых m представляет собой 1. 7. Способ получения соединений формулы (I), который характеризуется тем, что в качестве исходного вещества применяют соединение формулы (II) где R'1 представляет собой линейную или разветвленную C1-С 6-алкоксигруппу,R'2 представляет собой атом водорода, атом галогена или линейную или разветвленную C1-С 6 алкоксигруппу,которое подвергают реакции с хлорангидридом кислоты формулы (III) в присутствии основания в среде тетрагидрофурана или ацетонитрила Сl-СН 2-(СН 2)m-СН 2-СОСl(III),где m имеет значения, указанные для формулы (I),с получением соединения формулы (IV) где R'1, R'2 имеют значения, указанные выше,которое затем циклизуют в щелочной среде с получением соединения формулы (V) где R'1, R'2 и m имеют значения, указанные выше,которое восстанавливают в спиртовой среде или среде диметилформамида в присутствии борогидрида натрия, с получением соединения формулы (VI) где R'1, R'2 и m имеют значения, указанные выше,которое подвергают реакции с трибромидом бора, с получением соединения формулы (VII) где m имеет значения, указанные выше, и R2 имеет значения, указанные для формулы (I),которое подвергают реакции с соединением формулы (XIVa) где R1, X имеют значения, указанные для формулы (I), и Y' представляет собой атом кислорода,атом серы или группу NR', где R' представляет собой линейную или разветвленную C1-С 6-алкильную группу,или с соединением формулы (XIVb)(XIVb),где R1 и X имеют значения, указанные для формулы (I),с получением соединения формулы (I/a1) или (I/а 2), частного случая соединений формулы (I), где X, Y, R1, R2, R3 и R4 имеют значения, указанные для формулы (I), где X, Y, R1, R2 и m имеют значения, указанные для формулы (I),где соединения формулы (I/a1) или (I/а 2) при необходимости очищают в соответствии с обычными способами очистки, необязательно разделяют на изомеры в соответствии с обычными способами разделения и превращают, если это является желательным, в их аддитивные соли с фармацевтически приемлемой кислотой или основанием. 8. Фармацевтические композиции, которые содержат в качестве активного компонента соединение по любому из пп.1-6 в сочетании с одним или более фармацевтически приемлемыми, инертными, нетоксичными наполнителями или носителями. 9. Фармацевтические композиции по п.8, предназначенные для применения в качестве лекарственных средств, таких как АМРА модуляторы. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2/6
МПК / Метки
МПК: C07D 513/04, A61K 31/549, C07D 279/02, A61P 25/00, A61K 31/5415, C07D 209/00, C07D 285/00
Метки: бензотиазина, фармацевтические, композиции, получения, соединения, способ, которые, бензотиадиазина, содержат
Код ссылки
<a href="https://eas.patents.su/12-7492-soedineniya-benzotiazina-i-benzotiadiazina-sposob-ih-polucheniya-i-farmacevticheskie-kompozicii-kotorye-ih-soderzhat.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения бензотиазина и бензотиадиазина, способ их получения и фармацевтические композиции, которые их содержат</a>
Предыдущий патент: Производные нуклеозидов в качестве ингибиторов рнк-зависимой рнк вирусной полимеразы
Следующий патент: N-(2-арилэтил)бензиламины в качестве антагонистов 5-ht6- рецептора
Случайный патент: Моноклональные антитела к миостатину и их применения