19-норстероиды, галогенированные в положении 17, способы их получения и их применение, промежуточные продукты и фармацевтические композиции, их содержащие
Номер патента: 3325
Опубликовано: 24.04.2003
Авторы: Ван Де Вельд Патрик, Може Жак, Буали Йасмина, Ник Франсуа
Формула / Реферат
1. Соединения общей формулы (I)

в которой
R1 обозначает атом водорода, метил, этил, COCH3, COEt, COPh или CH2Ph,
R2 обозначает метил,
X обозначает атом галогена,
Y обозначает простую связь, O, NH, S, SO или SO2,
Z обозначает атом водорода или атом галогена,
n равно 2, 3, 4 или 5,
или R3 и R4, одинаковые или разные, обозначают атом водорода или алкил с 1-6 атомами углерода,
или R3 и R4 образуют вместе с атомом азота, с которым они связаны, один из следующих гетероциклов:
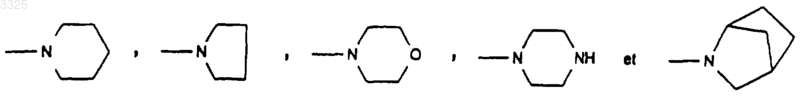
незамещенный или замещенный метилом,
пунктирные линии обозначают возможную вторую связь, а также их соли присоединения с основаниями или кислотами.
2. Соединения общей формулы (I) по п.1, а также их соли присоединения, в которой Х обозначает атом фтора в положении альфа и пунктирные линии не обозначают вторую связь.
3. Соединения общей формулы (I), по п.1 или п.2, а также их соли присоединения, в которой R1 обозначает атом водорода, R2 обозначает метил и Z обозначает либо атом водорода, либо атом хлора, Y обозначает атом кислорода и пунктирные линии не обозначают вторую связь.
4. Соединения общей формулы (I) по пп.1-3, а также их соли присоединения, в которой X обозначает атом фтора в положении альфа, R1 обозначает атом водорода, R2 обозначает метил, Y обозначает атом кислорода, Z обозначает атом водорода или атом хлора, n равно 2 или 3,
или R3 и R4, одинаковые или разные, обозначают алкильный радикал, содержащий от 1 до 6 атомов углерода,
или R3 и R4 образуют вместе с атомом азота, с которым они связаны, один из следующих насыщенных гетероциклов:
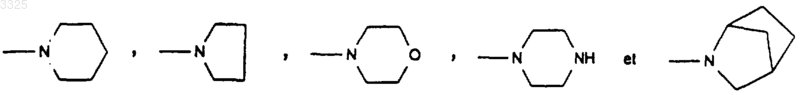
и пунктирные линии не обозначают вторую связь.
5. Соединения по любому из пп.1-4, названия которых следуют ниже:
17a -фтор-11b -[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ол,
хлоргидрат 17a -фтор-11b -[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)-триен-3-ола,
17a -фтор-11b -[4-[2-(1-диэтиламино)этокси]фенил]эстра-1,3,5,(10)триен-3-ол,
17a -фтор-11b -[4-[2-(1-пирролидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ол,
4-хлор-17a -фтор-11b -[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ол,
17-иод-11b -[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10),16-тетраен-3-ол,
17a -фтор-11b -[4-[2-(4-метил-1-пиперидинил)этокси]фенил)эстра-1,3,5,(10)триен-3-ол,
хлоргидрат 17a -фтор-11b -[4-(2-(4-метил-1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ола,
17a -фтор-3-метокси-11b -[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен,
17a -фтор-3-метокси-11b -[4-[2-(1-пирролидинил)этокси]фенил]эстра-1,3,5,(10)триен,
17a -фтор-3-метокси-11b -[4-[2-(1-диэтиламино)этокси]фенил]эстра-1,3,5,(10)триен,
(11b )-17 хлор-11-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10),16-тетраен-3-ол,
17a -хлор-11b -[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ол,
хлоргидрат 17-иод-11b -[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5, (10),16-тетраен-3-ола,
лактат 17a -фтор-11b -[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ола.
6. Способ получения соединений общей формулы (I), описанной в п.1, отличающийся тем, что соединение формулы (II)
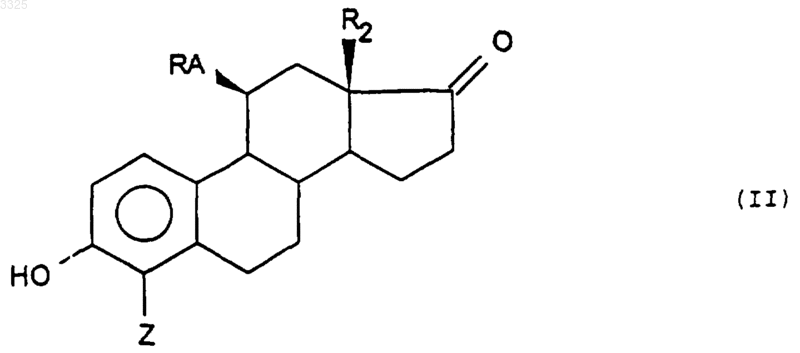
в которой
R2 и Z такие, как определено в п.1,
RA обозначает одну из следующих групп:

в которых Y, n, R3 и R4 такие, как определено в п.1, и Hal обозначает атом галогена,
подвергают после возможной защиты и/или активации гидроксильных групп, воздействию:
а) агента, восстанавливающего кетогруппу в положении 17, чтобы получить соединение формулы (IIIa)
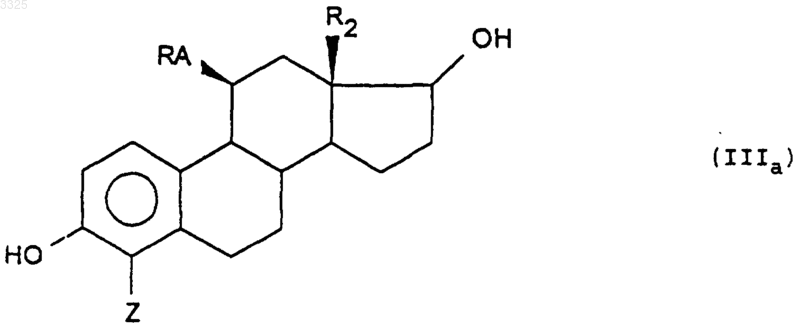
б) затем галогенирующего агента, в результате чего получают соединение формулы (I'a)
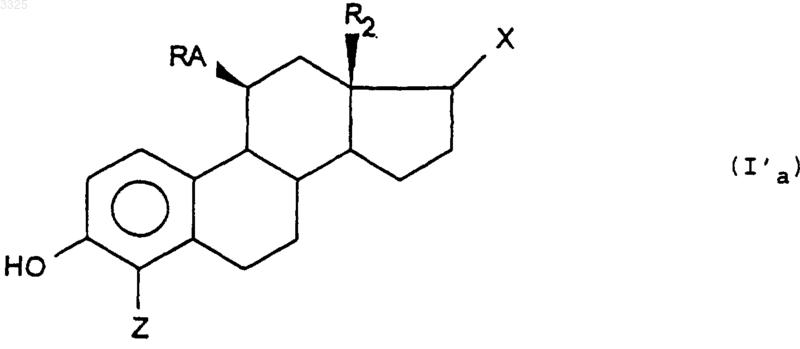
соответствующее некоторым соединениям формулы (I), когда RA обозначает -Ph-Y-(CH2)n-HR3R4,
при этом соединения формул (II), (IIIa) и (I'a) в защищенной или в незащищенной форме подвергают, если желают или если необходимо, одной или нескольким из следующих реакций:
снятию защиты с защищенной гидроксильной группы или защищенных гидроксильных групп,
ацилированию/алкилированию гидроксильной группы или гидроксильных групп,
воздействию HNR3R4 возможно в форме соли, если RA обозначает группу -Ph-Y-(CH2)n-Hal или активированную группу -Ph-Y-(CH2)n-OH,
солеобразованию.
7. Способ получения соединений общей формулы (I), описанной в п.1, отличающийся тем, что соединение формулы (II)
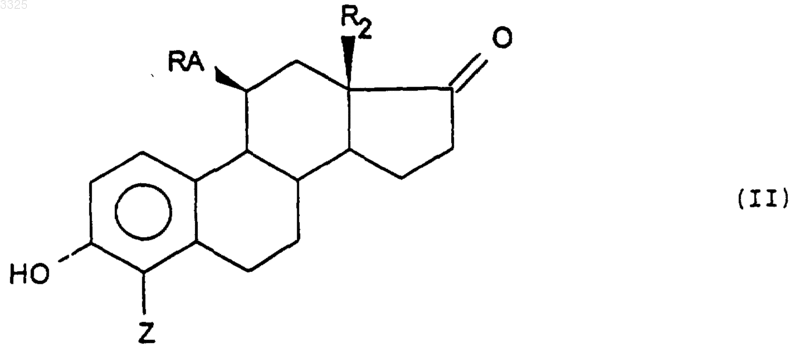
в которой
R2 и Z такие, как определено в п.1,
RA обозначает одну из следующих групп:
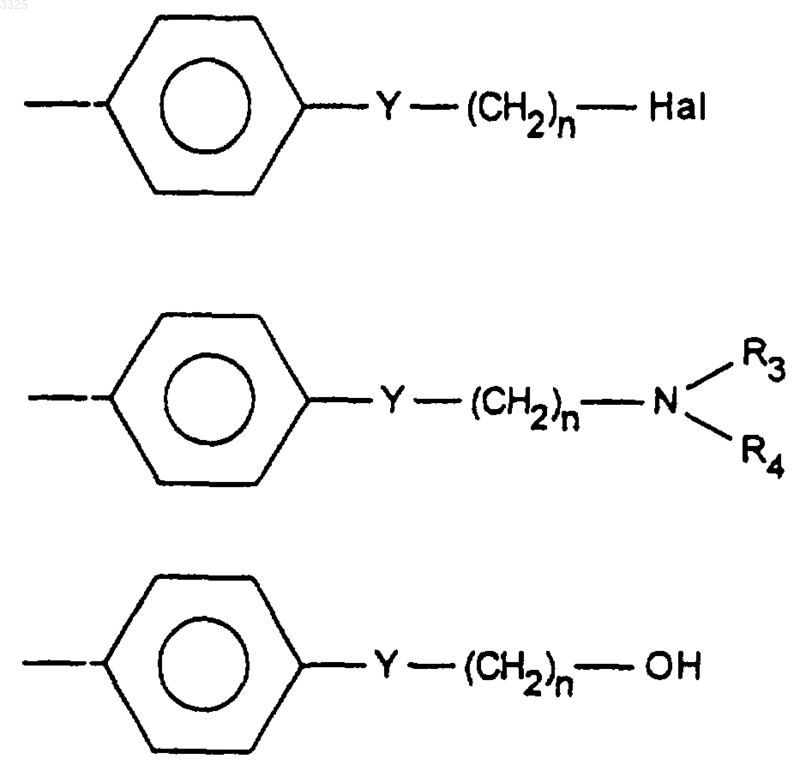
в которых Y, n, R3 и R4 такие, как определено в п.1, и Hal обозначает атом галогена,
подвергают после возможной защиты и/или активации гидроксильных групп, воздействию:
а) гидразина, чтобы получить соединение формулы (IIIb)
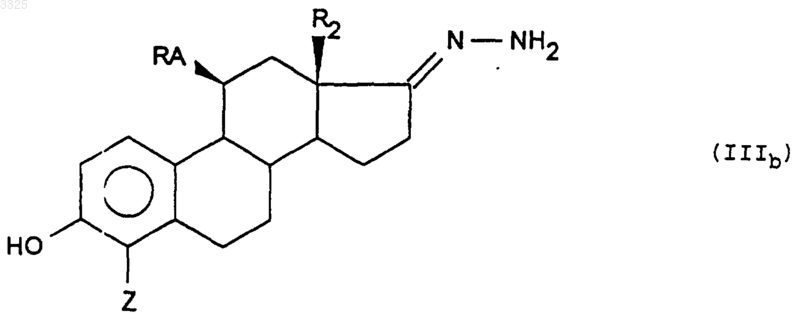
б) затем галогенирующего агента, в результате чего получают соединение формулы (I'b)
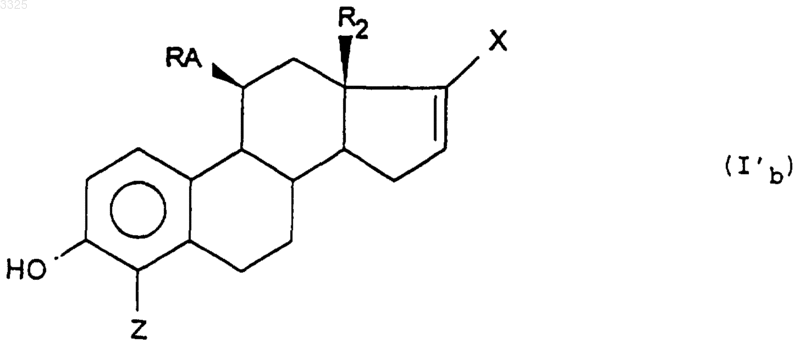
соответствующее некоторым соединениям формулы (I), когда RA обозначает -Ph-Y-(CH2)n-NR3R4,
при этом соединения формул (II), (IIIb) и (I'b) в защищенной или в незащищенной форме подвергают, если желают или если необходимо, одной или нескольким из следующих реакций:
снятию защиты с защищенной гидроксильной группы или защищенных гидроксильных групп,
ацилированию/алкилированию гидроксильной группы или гидроксильных групп,
воздействию HNR3R4 возможно в форме соли, если RA обозначает группу -Ph-Y-(CH2)n-Hal или активированную группу -Ph-Y-(CH2)n-OH,
солеобразованию.
8. Способ п.6 или 7 для получения соединений общей формулы (I), описанной в п.2, в которой X обозначает атом фтора в положении 17a и пунктирные линии не обозначают вторую связь, отличающийся тем, что галогенирующий агент представляет собой 1-перфторбутансульфонилфторид.
9. Применение соединений общей формулы (I) по п.1 или их фармацевтически приемлемых солей присоединения с кислотами или основаниями в качестве лекарственных средётт.
10. Применение соединений общей формулы (I) по любому из пп.2-4 или их фармацевтически приемлемых солей присоединения с кислотами в качестве лекарственных средств.
11. Применение соединений по п.5 или их фармацевтически приемлемых солей присоединения с кислотами в качестве лекарственных средств.
12. Фармацевтические композиции, содержащие одно или несколько соединений по любому из пп.1-5 или их фармацевтически приемлемых солей присоединения с кислотами или основаниями.
13. Соединения общей формулы (I'a) или (I'b), таких как определены в п.6 или 7, в качестве промежуточных продуктов.
14. Соединения общей формулы (IIIb), такой как определена в п.7, в качестве промежуточных продуктов.
15. Применение соединений формулы (I) по пп.1-5 для получения лекарственного средства, предназначенного для заместительной гормональной терапии менопаузы или перименопаузы, обладающего лишь незначительной эстрогенной активностью или не обладающего эстрогенной активностью на уровне матки.
16. Применение по п.15, отличающееся тем, что лекарственное средство предназначено для профилактики или лечения остеопороза.
17. Лекарственное средство, состоящее, по меньшей мере, из одного соединения по п.5, предназначенное для профилактики или лечения остеопороза.
18. Лекарственное средство, состоящее, по меньшей мере, из одного соединения по п.5, предназначенное для защиты сердечно-сосудистой системы.
Текст
1 Настоящее изобретение касается 19 норстероидов, галогенированных в положении 17, способа их получения и промежуточных продуктов, их применения в качестве лекарства и фармацевтических композиций, их содержащих. Остеопороз представляет собой патологию, характеризующуюся количественным уменьшением и снижением качества костной ткани, которые достаточны для того, чтобы повлечь за собой вертебральные или периферические переломы, произошедшие спонтанно или в результате минимального травматизма. Хотя эта патология имеет много факторов ее происхождения, у женщин преобладающим фактором потери костной ткани или остеопении является менопауза. Эта остеопения проявляется в разрежении и изменении формы губчатой кости, которая вследствие этого имеет повышенную скелетную хрупкость и подвержена опасности перелома. Потеря костной ткани сильно возрастает после менопаузы в результате ослабления деятельности яичника и достигает от 3 до 5% в год, чтобы замедлиться после 65 лет. В терапевтических целях, постменопаузная гормональная недостаточность может быть компенсирована при помощи заместительной гормонотерапии, в которой эстроген играет исключительно важную роль, сохраняя костную массу. Но продолжительная эстрогенотерапия сопровождается иногда нежелательным воздействием на половой аппарат (эндометриальная гиперплазия, опухоль молочной железы), что представляет собой исключительно важный недостаток и ограничивает ее применение. Таким образом, следует найти соединения,отличные от эстрадиола, обладающие пониженной эстрогенной активностью, а именно, эстрогенной активностью на костном уровне, при этом не обладающие или обладающие незначительной активностью как в отношении эндометриальной гиперплазии, так и в отношении пролиферации опухоли молочной железы. Итак, предметом изобретения являются соединения общей формулы (I)Z обозначает атом водорода или атом галогена,n равно 2, 3, 4 или 5,или R3 и R4, одинаковые или разные, обозначают атом водорода или алкил с 1-6 атомами углерода,или R3 и R4 образуют вместе с атомом азота, с которым они связаны, один из следующих гетероциклов незамещенный или замещенный метилом,пунктирные линии обозначают возможную вторую связь, а также их соли присоединения с основаниями или кислотами. Под галогеном подразумевают иод, бром,хлор или фтор. В положении 4 речь идет, предпочтительно, о хлоре или броме. В положении 17 речь идет, предпочтительно, о фторе. Соли соединений формулы (I) могут представлять собой соли, образованные минеральными или органическими кислотами с амином. В этом случае речь может идти о соляной, бромисто-водородной, азотной, серной, фосфорной,уксусной, муравьиной, пропионовой, бензойной, малеиновой, фумаровой, янтарной, винной,лимонной, щавелевой, глиоксалевой, аспартовой кислотах, алкансульфоновых кислотах, таких как метансульфоновая или этансульфоновая кислоты, арилсульфоновых кислотах, таких как бензолсульфоновая кислота или паратолуолсульфокислота, и арилкарбоновых кислотах. Когда соединения формулы (I) содержат кислотную функциональную группу, изобретение распространяется на соли щелочных металлов,щелочно-земельных металлов или аммония, в известных случаях, замещенные. Более конкретно, предметом изобретения являются соединения общей формулы (I), определенной выше, в которой Х обозначает атом фтора в положении альфа, и пунктирные линии не обозначают вторую связь (цикл D насыщенного стероида), а также их соли присоединения. Более конкретно, предметом изобретения являются также соединения общей формулы (I),в которой R1 обозначает атом водорода, R2 обозначает метил и Z обозначает либо атом водорода, либо атом хлора, Y обозначает атом кислорода, и пунктирные линии не обозначают вторую связь, а также их соли присоединения. Изобретение относится к соединениям общей формулы (I), такой, в которой: Х обозначает атом фтора в положении альфа, R1 обозначает атом водорода, R2 обозначает метил, Y обозначает атом кислорода, Z обозначает атом водорода или атом хлора, n равно 2 или 3,или R3 и R4, одинаковые или разные, обозначают алкильный радикал, содержащий от 1 до 6 атомов углерода, 3 или R3 и R4 образуют вместе с атомом азота, с которым они связаны, один из следующих насыщенных гетероциклов: и пунктирные штрихи не обозначают вторую связь, а также их соли присоединения. Наконец, изобретение относится к соединениям формулы (I), a также к их солям присоединения с кислотами, названия которых следуют ниже: 17 альфа-фтор-11 бета-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)-триен-3-ол,хлоргидрат 17 альфа-фтор-11 бета-[4-[2-(1 пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ола,17 альфа-фтор-11 бета-[4-[2-(1-диэтиламино)этокси]фенил]эстра-1,3,5,(10)-триен-3-ол,17 альфа-фтор-11 бета-[4-[2-(1-пирролидинил)этокси] фенил]эстра-1,3,5, (10)-триен-3-ол,4-хлор-17 альфа-фтор-11 бета-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)-триен 3-ол,17 иод-11 бета-[4-[2-(1-пиперидинил)этокси]фенил]-эстра-1,3,5, (10),16-тетраен-3-ол,17 альфа-фтор-11 бета-[4-[2-(4-метил-1 пиперидинил)этокси]фенил]-эстра-1,3,5,(10)триен-3-ол,хлоргидрат 17 альфа-фтор-11 бета-[4-[2-(4 метил-1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)-триен-3-ола,17 альфа-фтор-3-метокси-11 бета-[4-[2-(1 пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен,17 альфа-фтор-3-метокси-11 бета-[4-[2-(1 пирролидинил)этокси]фенил]эстра-1,3,5,(10)триен,17 альфа-фтор-3-метокси-11 бета-[4-[2-(1 диэтиламино)этокси]фенил]эстра-1,3,5,(10)триен,(11 бета)-17 хлор-11-[4-[2-(1-пиперидинил) этокси]фенил]эстра-1,3,5, (10),16-тетраен-3-ол,17 альфа-хлор-11 бета-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)-триен-3-ол,хлоргидрат 17 иод-11 бета-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10),16-тетраен-3-ола,лактат 17 альфа-фтор-11 бета-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)-триен-3 ола. Изобретение относится также к способу получения соединений формулы (I), в котором соединение формулы (II) в которых Y, n, R3 и R4 имеют указанные выше значения, и Hal обозначает атом галогена, подвергают после возможной защиты и/или активации гидроксильных групп воздействию,а) агента, восстанавливающего кетогруппу в положении 17, чтобы получить соединение формулы (IIIa) б) затем галогенирующего агента, в результате чего получают соединение формулы соответствующее некоторым соединениям формулы (I), когда RA обозначает -Ph-Y-(CH2)nNR3R4,при этом соединения формул (II), (IIIa), (I'a) в защищенной или в незащищенной форме,подвергают, если желают или если необходимо,одной или нескольким из следующих реакций: снятию защиты с защищенной гидроксильной группы или защищенных гидроксильных групп,ацилированию/алкилированию гидроксильной группы или гидроксильных групп,воздействию HNR3R4, возможно, в форме соли, если RA обозначает группу -Ph-Y-(СН 2)nНаl или активированную группу -Ph-Y-(CH2)nOH,солеобразованию. Изобретение относится также к способу получения соединений общей формулы (I), описанной выше, в котором соединение формулыR2 и Z такие, как определено в п.1,RA обозначает одну из следующих групп: в которой в которых Y, n, R3 и R4 такие, как определено выше, и Hal обозначает атом галогена, подвергают после возможной защиты и/или активации гидроксильных групп, воздействию: а) гидразина, чтобы получить соединение формулы (IIIb) б) затем галогенирующего агента, в результате чего получают соединение формулы соответствующее некоторым соединениям формулы (I), когда RA обозначает -Ph-Y-(СН 2)nNR3R4,при этом соединения формул (II), (IIIb) или(I'b), в защищенной или в незащищенной форме,подвергают, если желают или, если необходимо,одной или нескольким из следующих реакций: снятию защиты с защищенной гидроксильной группы или защищенных гидроксильных групп,ацилированию/алкилированию одной или нескольких гидроксильных групп,обработке соединением НNR3R4, возможно, в форме соли,если RA обозначает группу -Ph-Y-(CH2)nHal или активированную группу -Ph-Y-(CH2)nOH,солеобразованию. Реакцию галогенирования в положении 17 осуществляют, предпочтительно, с использованием таких реагентов, как XSO2C4F9, где X,предпочтительно, обозначает фтор, в присутствии стерически затрудненного основания, такого как ДБУ (диазабициклоундецен). Другие способы галогенирования, известные специалисту,также могут быть использованы. Когда гидроксильная группа исходного продукта находится в положении бета, при нуклеофильном замещении наблюдают обращение конфигурации и этим способом (галогенирующий агент : 1-перфторбутансульфонилфторид 6 пользованием Х 2 в щелочной среде, в частности,с использованием I2. Под активацией спирта подразумевают введение, в частности, мезилата, тозилата или трифторметансульфоната, которое способствует нуклеофильному замещению амином HNR3R4 соединений формул (II), (IIIa), (IIIb), (I'a), (I'b), в которых R3 обозначает группу -Ph-Y-(СН 2)n-ОН. Образование мезилата, тозилата или трифторметансульфоната, исходя из соответствующего спирта, осуществляют в присутствии основания, такого как триэтиламин. Можно также предварительно осуществить замещение спирта атомом галогена согласно обычным способам. Реакции защиты и снятия защиты представляют собой обычные способы, известные специалисту. Достаточно полный обзор находится в следующей работе: защитные группы в органических синтезах, T.W.Greene, John Wileysons (1981). Защитная группа Р (ОНОР) может представлять собой алкильный радикал, содержащий от 1 до 4 атомов углерода, бензильную группу, тетрагидропиранильную группу, группуRcRdReSi, в которой Rc, Rd и Re, одинаковые или разные, каждый независимо друг от друга,представляют собой алкильный радикал, содержащий от 1 до 4 атомов углерода, или фенил. Совсем конкретно, речь идет о группах-Si(Ме)2 СМе 3, или -Si(Ph)2 СМе 3, или -SiMe3. В качестве примера, реакции снятия защиты (ОРОН в положении 3), когда Р представляет собой трет-бутилдифенилсилильную группу, могут осуществляться путем воздействия раствором фторида тетрабутиламмония в тетрагидрофуране. Так же действуют, если Р представляет собой SO2C4F9, возникающую в результате реакции фторирования. Когда Р является тетрагидропиранильной группой, снятие защиты осуществляют в присутствии водной кислоты в спиртовом растворе,предпочтительно, под воздействием соляной кислоты в метаноле. Воздействие соединения формулы R3R4NH на соединения формул (II), (IIIa), (IIIb), (I'a) или(I'b), в которых R2 обозначает группу -Ph-Y(СН 2)n-ОН или -Ph-Y-(CH2)n-Hal, осуществляют в обычных условиях нуклеофильного замещения, в частности, в присутствии апротонного растворителя, такого как тетрагидрофуран. Когда ОН активирована, речь идет, в частности, о ОSO2 СН 3, OSO2-Ph-pMe или OSO2 СРh3. Реакции алкилирования или ацилирования группы ОН в положении 3, а также реакции солеобразования осуществляют согласно обычным способам, известным специалисту. Соединения общей формулы (I), а также их фармацевтически приемлемые соли присоединения с кислотами обладают, в частности, эстрогенной, антиэстрогенной и антипролиферирующей активностями.(I) могут быть использованы для лечения расстройств, связанных с гипофолликулинией, например, аминорей, дисменорей, повторящихся абортов, предменструальных расстройств, при лечении некоторых эстрогенозависимых патологий, таких как аденомы или карциномы предстательной железы, карциномы молочной железы и их метастазы, или при лечении доброкачественных опухолей молочной железы, в качестве антигистеротрофика, а также при заместительной терапии менопаузы или перименопаузы. Среди симптомов и последствий, связанных с менопаузой, более конкретно, имеют в виду приливы крови к лицу, потливость, атрофию и сухость влагалища, мочевые симптомы и в долгосрочной перспективе уменьшение костной массы и увеличение опасности переломов, а также потерю сердечно-сосудистой защиты,осуществляемой эстрогенами. В частности, соединения формулы (I), а также их фармацевтически приемлемые соли присоединения с кислотами или основаниями,могут таким образом быть использованы для профилактики или лечения остеопороза. Соединения формулы (I), а также их фармацевтически приемлемые соли присоединения с кислотами или основаниями, могут также быть использованы для профилактики или лечения остеопороза у мужчин. Равным образом, они могут быть использованы для профилактики или лечения вторичных остеопорозов (например, кортизоновых или связанных с иммобилизацией). Соединения формулы (I), а также их фармацевтически приемлемые соли присоединения с кислотами или основаниями, обладают, в частности, пониженной эстрогенной активностью. Под пониженной эстрогенной активностью подразумевают эстрогенную активность на костном уровне, при которой обнаруживается только минимальная активность матки, обеспечивающую таким образом отсутствие эндометриальной пролиферации (активность, гораздо меньшая, чем активность эстрадиола). Кроме того, соединения согласно изобретению обладают следующими преимуществами. Они обладают антиэстрогенной и/или антипролиферирующей активностью на уровне молочной железы. В противоположность эстрадиолу они не стимулируют рост опухолевых клеток молочных желез у человека и даже могут ингибировать их рост. Следовательно, соединения согласно изобретению особенно предпочтительны для лечения менопаузы у женщин с опасностью возникновения рака молочной железы (семейный анамнез), для которых таким образом исключена заместительная терапия эстрадиолом. 8 Равным образом, они могут быть использованы для лечения злокачественных опухолей молочных желез. Они приводят к снижению содержания сывороточного холестерина до уровня, по меньшей мере, эквивалентного уровню, индуцируемому эстрадиолом. Таким образом, они усиливают сердечно-сосудистую защиту. Наконец, соединения согласно изобретению не обладают никакой эстрогенной активностью в отношении матки, не нуждаются в их введении в сочетании с прогестомиметическим соединением. Итак, предметом изобретения являются соединения формулы (I), а также их фармацевтически приемлемые соли присоединения с кислотами или основаниями, в качестве лекарственного средства. Более конкретно, предметом изобретения являются соединения формулы (I), а также их фармацевтически приемлемые соли присоединения с кислотами или солями, в качестве лекарственного средства, предназначенного для профилактики или лечения остеопороза. Изобретение распространяется на фармацевтические композиции, содержащие в качестве действующего начала, по меньшей мере, одно из лекарственных средств, определенных выше. Соединения формулы (I) вводят через пищеварительный тракт, парентерально или локально, например, чрескожным путем. Они могут быть прописаны в форме простых таблеток или в форме драже, желатиновых капсул, гранул, свечей, вагинальных шариков, препаратов,пригодных для инъецирования, мазей, кремов,гелей, микросферических частиц, имплантантов,внутриматочных колец, лоскутов, которые получают согласно обычным способам. Действующее начало или действующие начала могут быть в них введены с эксципиентами, обычно используемыми в фармацевтических композициях, такими как тальк, гуммиарабик, лактоза, крахмал, стеарат магния, масло какао, водные или неводные наполнители, жировые вещества животного или растительного происхождения, парафиновые производные,гликоли, различные смачивающие агенты, диспергаторы или эмульгаторы, консерванты. Используемая доза изменяется в зависимости от излечиваемого расстройства и пути введения; для взрослых при пероральном приеме она может изменяться, например, от 1 до 1000 мгв день. Предметом изобретения является также применение соединений формулы (I) для получения лекарства, предназначенного для заместительной гормональной терапии менопаузы или перименопаузы, обладающего лишь незначительной эстрогенной активностью, или не обладающего эстрогенной активностью на 9 уровне матки, в частности, применение для профилактики или лечения остеопороза. Соединения формулы (II) или (IIIa) являются соединениями, известными или легко доступными. В частности, соединения формулы (II) с Z = Н, R2 = Me и RA = -Ph-Y-(CH2)n-Hal описаны в международной заявке на патент 93/13123 (соединения формулы (II; соединения формулы (II) с Z = Н, R2 = Me и RA = -Ph-Y-(CH2)n-ОН описаны в европейском патенте 0305242 В 1 (соединения формулы (III; соединения формулы (II) c Z=H, R2 = Me и RA =-Ph-Y-(CH2)n-NR3R4 описаны в европейском патенте 0097572, французском дополнительном патенте 2640977 или в европейском патенте 0305242. Соединения формулы (II), в которой Z обозначает атом галогена, описаны в международной заявке на патент 9845316 и получены,исходя из соединения формулы (IV) путем воздействия галогенирующего агента с целью получения соединения формулы (V) которое подвергают воздействию реагента, ароматизирующего цикл А, затем воздействию основания, чтобы получить соединение формулы(II), в которой Z обозначает атом водорода. Обработку галогенирующим реагентом,таким как N-бромсукцинимид или N-хлорсукцинимид, соединения формулы (IV) осуществляют, в частности, в присутствии полярного апротонного растворителя, такого как диметилформамид. Реакцию ароматизации с последующей реакцией омыления (обработка основанием) осуществляют согласно обычным способам, таким как описанные в европейском патенте 0097572. Предпочтительно, в качестве ароматизирующего агента используют смесь уксусного ангидрида и ацетилбромида, затем в качестве омыляющего агента используют основание, такое как раствор едкого натра в метаноле. Предметом изобретения являются также соединения формул (I'а), (IIIb) и (I'b) в качестве промежуточных продуктов. Примеры, следующие ниже, иллюстрируют изобретение, однако, никоим образом не ограничивают его. Растворители, описанные в примерах: 10 Пример 1. 17 Альфа-фтор-11 бета-[4-[2-(1 пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ол. Стадия А. Восстановление. 11 Бета-[4-(2-иодэтокси)фенил]эстра-1,3,5,(10)-триен-3,17 бета-диол. При 0 С к раствору 516 мг 3-гидрокси-11 бета-[4-(2-иодэтокси)фенил]эстра-1,3,5,(10)триен-17-она, полученного согласно методу,описанному в международном патенте 93/13123,в 5 мл МеОН и 5 мл ТГФ добавляют 76 мг боргидрида натрия и перемешивают 5 мин при этой температуре, а затем 1 ч 30 мин при комнатной температуре. Затем добавляют 20 мл 0,1 н. НСl и наблюдают кристаллизацию. Получают 460 мг целевого продукта.(1 Н, д, Н 4); 6,51(1 Н, дд, н 2); 4,11(2 Н, т, СН 2 О); 3,94 (1 Н, шир.т, Н 11); 3,72 (1 Н, шир.т, Н 17); 3,33 (2 Н, т, CH2I); 0,37(3 Н, с, 18-Ме). Стадия Б. Фторирование. Нонафторбутансульфонат 11-бета-[4-[2 иодэтокси]фенил]эстра-1,3,5,(10)-триен-3-ола. К суспензии 518 мг стероида, полученного на стадии А, в 5 мл толуола и 1 мл дихлорметана добавляют, при 0 С и в атмосфере азота, 0,45 мл ДБУ, затем 0,20 мл 1-перфторбутансульфонилфторида (FSO2C4F9) и выдерживают полученный раствор в течение 30 мин при комнатной температуре. Затем вливают реакционную среду в 20 мл воды, экстрагируют этилацетатом, промывают, сушат и выпаривают при пониженном давлении до получения 565 мг неочищенного продукта, который очищают при помощи хроматографии на Lichrosorb RP18,элюируя смесью ацетонитрил/вода 85/15. Получают 315 мг целевого продукта.(Whatman), Тпл = 110 С. ЯМР (СDСl3, 250 МГц) 7,00 (2 Н, м, H1 и Н 4); 6,93 и 6,63 (4 Н, 2 д, AA'BB', H ароматический в 11); 6,82 (1 Н, дд, Н 2); 4,44 (1 Н, дд,J1=55,5 Гц, J2=5 Гц, H17); 4,14 (2 Н, т, СН 2O); 4,03 (1 Н, м, Н 11); 3,35 (2 Н, т, CH2I); 0,23 (3 Н, д,J=2 Гц, СН 3). Стадия В. Введение амина и последующее снятие защиты. К раствору стероида, полученного на предыдущей стадии, в 3 мл ТГФ добавляют 0,4 мл пиперидина, все вместе кипятят в колбе с обратным холодильником в течение 2 ч, затем,после охлаждения, вливают в 10 мл воды, экстрагируют этилацетатом, промывают, сушат и выпаривают при пониженном давлении до получения 320 мг неочищенного желаемого продукта. После растворения в 30 мл ТГФ добавляют 2 мл тетрабутиламмонийфторида и нагревают 7 ч в колбе с обратным холодильником. После охлаждения, вливают в 20 мл воды, насыщенной бикарбонатом натрия, экстрагируют 11 этилацетатом, промывают, сушат и выпаривают при пониженном давлении. Получают 405 мг неочищенного продукта, очищают при помощи хроматографии на силикагеле, элюируя смесью этилацетат/ТЭА 95/5. Получают 160 мг чистого целевого продукта.+ CH2N и СН 2 впиперидина); 0,22 (3 Н, д, J=2 Гц, СН 3). ИК (СНСl3) ОН 3597 см-1 + ассоциированные ОН; ароматические группы 1608, 1582,1512, 1503 см-1. Пример 2. Хлоргидрат 17 альфа-фтор-11 бета-[4-[2-(1-пиперидинил)этокси]фенил]эстра 1,3,5,(10)-триен-3-ола. К раствору фторсодержащего соединения примера 1 в 10 мл этилацетата при температуре от 0 до +5 С добавляют 2 мл раствора 4 н. НСl в этилацетате и наблюдают кристаллизацию. Получают 1,6 г белых кристаллов.Rf (этилацетат/ТЭА 95/5) = 0,21 на SiO2F254 от Merck. Тпл = 216 С. ЯМР (CDCl3, 300 МГц) 6,95 и 6,43 (4 Н, 2 д,АА'ВВ', Н ароматические в 11); 6,79 (1H, д, H1); 6,66 (1H, д, Н 4); 6,59 (1H, дд, Н 2); 4,43 (1H, дд,J=56 Гц и 5 Гц, Н 17); 3,99 (1H, шир.т, Н 11); 4,26 и 3,87 (2 Н, 2 м, СН 2O); 3,48 (1H, подвижный,NH+); 2,8-3,25 (2 Н, м, CH2N+); 0,22 (3 Н, д, J=2 Гц, СН 3). ИК (СНСl3) ОН 3598 см+ + ассоциированные ОН; поглощение NH+, ароматические группы 1610, 1582, 1512 см-1. Пример 3. 17 альфа-Фтор-11 бета-[4-[2-(1 диэтиламино)этокси]фенил]эстра-1,3,5,(10)триен-3-ол. Действуют как в примере 1, но используя диэтиламин вместо пиперидина в ходе стадии В,получают 0,141 г целевого продукта.(дд, J=56 Гц и 5 Гц, Н 17); 6,32 (д, H1); 6,38 (дд,Н 2); 6,53 (д, Н 4); 6,57 и 6,96 (AA'BB', H ароматические в 11). Пример 4. 17 альфа-Фтор-11 бета-[4-[2-(1 пирролидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ол. Действуют как в примере 1, но используя пирролидин вместо пиперидина в ходе стадии В. Получают 0,049 г целевого продукта.(д, H1). Пример 5. 4-Хлор-17 альфа-фтор-11-бета[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)-триен-3-ол. Стадия А. Защита гидроксильной группы в положении 3. 4-Хлор-3-диметил(2,2-диметил)этил)силил]окси]-11-бета-[4-[2-(1-пиперидинил)этокси] фенил]-эстра-1,3,5,(10)-триен-3-он. К раствору 4-хлор-3-гидрокси-11 бета-[4[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)-триен-3-она, полученного действием NCS на соответствующее производное 4-5 9-10, 3 она с последующей реакцией ароматизации цикла А в 30 мл CH2Cl2, добавляют 1,3 г третбутилдиметилсилилхлорида, охлаждают до 0 С,затем по каплям добавляют 1,13 мл ТЭА. После 5 мин выдержки при 0 С реакционную смесь возвращают к комнатной температуре, выдерживают в течение 3 ч и затем вливают в 100 мл воды. После сушки органическую фазу упаривают при пониженном давлении до получения 4,55 г неочищенного продукта, который очищают при помощи хроматографии на силикагеле, элюируя смесью этилацетат/ТЭА 98/2. Получают 2,68 г чистого целевого продукта.SiO2F254 от Merck. ИК (СНСl3) С=O 1733 см-1; С-Н ароматическая 2936 - 2859 см-1. Стадия Б. Восстановление. 4-Хлор-3-диметил(2,2-диметилэтил)силил]окси]-11 бета-[4-[2-(1-пиперидинил)этокси] фенил]эстра-1,3,5,(10)-триен-17 бета-ол. К раствору стероида, полученного на предыдущей стадии, в 15 мл метанола, охлажденному при помощи ледяной бани, добавляют 189 мг NaBH4, перемешивают 5 мин при температуре от 0 до +5 С, затем 30 мин при комнатной температуре. Вливают в 100 мл воды, экстрагируют этилацетатом, промывают, сушат и выпаривают при пониженном давлении. Получают 1,5 г целевого продукта.SiO2F254 от Merck. Стадия В. Фторирование и последующее снятие защиты. Фторирование. К раствору 596 мг стероида, полученного на предыдущей стадии, в 5 мл толуола и 1 млCH2Cl2 при комнатной температуре в атмосфере азота добавляют 0,90 мл ДБУ, 0,04 мл перфторбутансульфонилфторида и перемешивают 2 ч. После вливания в 20 мл воды экстрагируют дихлорметаном, промывают, сушат и выпаривают при пониженном давлении. Получают 1,23 г неочищенного продукта, который очищают при 13 помощи хроматографии на силикагеле, элюируя смесью этилацетат/ТЭА 98/2. Выделяют 0,6 г фторсодержащего продукта, защищенного в положении 3. Снятие защиты. К раствору фторсодержащего продукта в 3 мл ТГФ добавляют 2 мл BLu4F, греют 4 ч в колбе с обратным холодильником, затем, после охлаждения, вливают в 20 мл воды. После экстрагирования дихлорметаном, промывки и сушки,выпаривают при пониженном давлении до получения сухого экстракта, который очищают при помощи хроматографии на Lichrosorb RP18,элюируя смесью МеОН/Н 2O/ТЭА 90/9/1. Получают 65 мг целевого продукта. 15 Пример 15. Лактат 17 альфа-фтор-11 бета[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)-триен-3-ола. Тпл = 138 С. ЯМР (СDСl3, 300 МГц) 0,22: (д, СН 3 в 18); 3,15: (CH2-N); 3,93: (м, СН 2-O); 3,98: (м,Н 11); 4,43: (дд, Н 17); 6,42: (дд, Н 2); 6,78: (д,H1); 6,48 - 6,97: (ароматические в 11), 1,36 (д) и 4,09 (м): лактат. Фармакологические исследования Влияние на пролиферацию клеток молочной железы Пролиферирующую активность молекул изучают в сравнении с пролиферирующей активностью эстрадиола на клетках молочной железы человека MCF-7 в культуре. Чтобы выявить действие эстрадиола и/или исследуемых молекул как агонистов, культурную среду, в которой содержатся клетки (богатую факторами роста и стероидами), заменяют обедненной средой, кроме того, лишенной стероидов (DMEM (модифицированная Дульбекко среда Игла) с добавкой 5% сыворотки, освобожденной от стероидов, и без фенолового красного). Клетки выдерживают в этих условиях в течение двух дней перед началом исследования. После 7 дней культивирования в присутствии исследуемых веществ клеточную пролиферацию оценивают, путем количественного определения ДНК. В каждом опыте влияние эстрадиола при концентрации 10-10 моль/л (рост клеток в присутствии эстрадиола минус рост клеток в присутствии растворителя) принимают за 100%-ую активность агониста. Активность молекул оценивают в сравнении с этим внутренним контрольным образцом. Молекулы, индуцирующие рост клеток, идентичный росту клеток, наблюдаемому с одним растворителем,классифицируют как "инертные", молекулы,индуцирующие рост клеток, меньший роста клеток, наблюдаемого с растворителем, классифицируют как "ингибитор". Активность Эстрадиол Агонист Пример 1 Инертное Пример 2 Инертное Исследование влияния вещества на костную ткань у самки крысы, подвергнутой овариэктомии в трехмесячном возрасте. Соединения испытывают с целью определения их влияния на костную массу и на активность образования и резорбции в модели крысы,подвергнутой овариэктомии в трехмесячном возрасте. Животных лечат профилактически. Животные: Вид Крыса ЛинияSprague-Dawley Пол Самка Масса от 250 до 280 г Число животных в группе 8 16 Вещества: 1- Исследуемое вещество: вещество примера 1 наполнитель(и): кукурузное масло, метилцеллюлоза 0,5%число введений: один раз/день; 5 дней/неделю в течение 4 недельпуть введения: перорально (п.о.) для веществаобъемы: 5 мл/кг (п.о.)период между последним введением и умерщвлением: 24 ччисло введений: 20. 2- Вещество сравнения: 17-эстрадиол, введенный подкожно при дозе 0,1 или 0,01 мг/кг/день в виде раствора в смеси масло из ростков кукурузы-бензиловый спирт (99 : 1, об./об.) в объеме 0,2 мл/кг. Протокол эксперимента Животные. Исследование проводят на самках, подвергнутых овариэктомии в трехмесячном возрасте. Животных содержат в комнате с кондиционированным воздухом (температура 20 С 2 С) в клетках, сгруппированными по 4 особи в клетке. Животные получают, по желанию, деминерализованную воду и прессованную пищу(пробки: AO4CR-10 UAR). Хирургия. Трехмесячных самок крыс, весящих около 250 г, подвергают овариэктомии при анестезии препаратом Imalgene 1000 при дозе 100 мг/кг интраперитональным путем (и.п.) в объеме 0,3 мл/кг. Они получают также Nembutal (3 мг/кг,и.п., в объеме 0,3 мл/кг). После бокового разреза кожный и мышечный слои рассекают. Удаление каждого яичника осуществляют после лигирования маточной трубы. Контрольных крыс "SHAM" подвергают анестезии в тех же самых условиях. После разреза кожного и мышечного слоев каждый яичник вынимают, затем возвращают на место insitu. Лечение. Влияние веществ определяют в ходе профилактического лечения. Их вводят немедленно после овариэктомии. Животные распределены по группам по 8 особей. Группа 1: контрольные крысы "SHAM",получающие наполнитель или наполнители. Группа 2: контрольные крысы "OVX", получающие наполнитель или наполнители. Группы X: крысы "OVX", получающие соответственно определенные дозы исследуемого вещества или исследуемых веществ. Взятие проб крови для анализа. По окончании четырех недель (продолжительность исследования) животных обезглавливают при помощи гильотины. Сыворотки, собранные после центрифугирования, консервируют при -20 С. Липидный баланс определяют, исходя из сывороточных доз общего холестерина, тригли 17 церидов и фосфолипидов, на аликвотном количестве сыворотки 500 мкл. Снижение содержания сывороточного холестерина выражают в % по отношению к содержанию, имеющемуся у животных, подвергнутых овариэктомии, получавших только растворитель. Изъятие органов. После умерщвления животных изымают следующие органы:- половой тракт. Матки изымают. Их взвешивают. Увеличение массы выражают в % по отношению к массе матки животных, подвергнутых овариэктомии, получавших только растворитель.density = плотность минеральных веществ костной ткани) измеряют методом двухфотонной рентгеновской абсорбциометрии при удвоенной энергии (DEXA). Измерения проводят на костях, вырезанных и очищенных от всех мягких тканей. BMD (плотность минеральных веществ кости) измеряют на целой кости, а также на метафизарной части на уровне, ближайшем к концу, для левой большеберцовой кости. Эта зона определена как область, наиболее богатая губчатыми костями, и, следовательно, является наиболее чувствительной к изменению объема костей и плотности минеральных веществ костной ткани. Результаты выражены в % согласно формуле: ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединения общей формулы (I)Y обозначает простую связь, О, NH, S, SO или SO2,Z обозначает атом водорода или атом галогена,n равно 2, 3, 4 или 5,или R3 и R4, одинаковые или разные, обозначают атом водорода или алкил с 1-6 атомами углерода,или R3 и R4 образуют вместе с атомом азота, с которым они связаны, один из следующих гетероциклов: незамещенный или замещенный метилом,пунктирные линии обозначают возможную вторую связь, а также их соли присоединения с основаниями или кислотами. 2. Соединения общей формулы (I) по п.1, а также их соли присоединения, в которой Х обозначает атом фтора в положении альфа, и пунктирные линии не обозначают вторую связь. 3. Соединения общей формулы (I) по п.1 или п.2, а также их соли присоединения, в которой R1 обозначает атом водорода, R2 обозначает метил и Z обозначает либо атом водорода, либо атом хлора, Y обозначает атом кислорода, и пунктирные линии не обозначают вторую связь. 4. Соединения общей формулы (I) по пп.13, а также их соли присоединения, в которой Х обозначает атом фтора в положении альфа, R1 обозначает атом водорода, R2 обозначает метил,Y обозначает атом кислорода, Z обозначает атом водорода или атом хлора, n равно 2 или 3,или R3 и R4, одинаковые или разные, обозначают алкильный радикал, содержащий от 1 до 6 атомов углерода,или R3 и R4 образуют вместе с атомом азота, с которым они связаны, один из следующих насыщенных гетероциклов: и пунктирные линии не обозначают вторую связь. 5. Соединения по любому из пп.1-4, названия которых следуют ниже: 17-фтор-11-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ол,хлоргидрат 17-фтор-11-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)-триен-3 ола,17-фтор-11-[4-[2-(1-диэтиламино)этокси]фенил]эстра-1,3,5,(10)триен-3-ол,17-фтор-11-[4-[2-(1-пирролидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ол,4-хлор-17-фтор-11-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ол,17-иод-11-[4-[2-(1-пиперидинил)этокси] фенил]эстра-1,3,5,(10),16-тетраен-3-ол,17-фтор-11-[4-[2-(4-метил-1-пиперидинил)этокси]фенил)эстра-1,3,5,(10)триен-3-ол, 19 хлоргидрат 17-фтор-11-[4-[2-(4-метил-1 пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ола,17-фтор-3-метокси-11-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен,17-фтор-3-метокси-11-[4-[2-(1-пирролидинил)этокси]фенил]эстра-1,3,5,(10)триен,17-фтор-3-метокси-11-[4-[2-(1-диэтиламино)этокси]фенил]эстра-1,3,5,(10)триен,(11)-17 хлор-11-[4-[2-(1-пиперидинил) этокси]фенил]эстра-1,3,5,(10),16-тетраен-3-ол,17-хлор-11-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ол,хлоргидрат 17-иод-11-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5, (10),16-тетраен-3 ола,лактат 17-фтор-11-[4-[2-(1-пиперидинил)этокси]фенил]эстра-1,3,5,(10)триен-3-ола. 6. Способ получения соединений общей формулы (I), описанной в п.1, отличающийся тем, что соединение формулы (II) 20 при этом соединения формул (II), (IIIa) и(I'а) в защищенной или в незащищенной форме подвергают, если желают или если необходимо,одной или нескольким из следующих реакций: снятию защиты с защищенной гидроксильной группы или защищенных гидроксильных групп,ацилированию/алкилированию гидроксильной группы или гидроксильных групп,воздействию HNR3R4 возможно в форме соли, если RA обозначает группу -Ph-Y-(СН 2)nНаl или активированную группу -Ph-Y-(СН 2)nОН,солеобразованию. 7. Способ получения соединений общей формулы (I), описанной в п.1, отличающийся тем, что соединение формулы (II)R2 и Z такие, как определено в п.1,RA обозначает одну из следующих групп: в которойR2 и Z такие, как определено в п.1,RA обозначает одну из следующих групп: в которых Y, n, R3 и R4 такие, как определено в п.1, и Hal обозначает атом галогена,подвергают после возможной защиты и/или активации гидроксильных групп, воздействию: а) агента, восстанавливающего кетогруппу в положении 17, чтобы получить соединение формулы (IIIa) в которых Y, n, R3 и R4 такие, как определено в п.1, и Hal обозначает атом галогена,подвергают после возможной защиты и/или активации гидроксильных групп, воздействию: а) гидразина, чтобы получить соединение формулы (IIIb) б) затем галогенирующего агента, в результате чего получают соединение формулы(I'b) б) затем галогенирующего агента, в результате чего получают соединение формулы соответствующее некоторым соединениям формулы (I), когда RA обозначает -Ph-Y-(СН 2)nNR3R4, соответствующее некоторым соединениям формулы (I), когда RA обозначает -Ph-Y-(CH2)nNR3R4,при этом соединения формул (II), (IIIb) и(I'b) в защищенной или в незащищенной форме подвергают, если желают или если необходимо,одной или нескольким из следующих реакций: снятию защиты с защищенной гидроксильной группы или защищенных гидроксильных групп,ацилированию/алкилированию гидроксильной группы или гидроксильных групп,воздействию HNR3R4 возможно в форме соли, если RA обозначает группу -Ph-Y-(CH2)nHal или активированную группу -Ph-Y-(CH2)nOH,солеобразованию. 8. Способ п.6 или 7 для получения соединений общей формулы (I), описанной в п.2, в которой Х обозначает атом фтора в положении 17 и пунктирные линии не обозначают вторую связь, отличающийся тем, что галогенирующий агент представляет собой 1-перфторбутансульфонилфторид. 9. Применение соединений общей формулы (I) по п.1 или их фармацевтически приемлемых солей присоединения с кислотами или основаниями в качестве лекарственных средств. 10. Применение соединений общей формулы (I) по любому из пп.2-4 или их фармацевтически приемлемых солей присоединения с кислотами в качестве лекарственных средств. 11. Применение соединений по п.5 или их фармацевтически приемлемых солей присоединения с кислотами в качестве лекарственных средств. 22 12. Фармацевтические композиции, содержащие одно или несколько соединений по любому из пп.1-5 или их фармацевтически приемлемых солей присоединения с кислотами или основаниями. 13. Соединения общей формулы (I'a) или(I'b), таких как определенные в п.6 или 7, в качестве промежуточных продуктов. 14. Соединения общей формулы (IIIb), такой как определенная в п.7, в качестве промежуточных продуктов. 15. Применение соединений формулы (I) по пп.1-5 для получения лекарственного средства, предназначенного для заместительной гормональной терапии менопаузы или перименопаузы, обладающего лишь незначительной эстрогенной активностью или не обладающего эстрогенной активностью, на уровне матки. 16. Применение по п.15, отличающееся тем, что лекарственное средство предназначено для профилактики или лечения остеопороза. 17. Лекарственное средство, состоящее, по меньшей мере, из одного соединения по п.5,предназначенное для профилактики или лечения остеопороза. 18. Лекарственное средство, состоящее, по меньшей мере, из одного соединения по п.5,предназначенное для защиты сердечно-сосудистой системы.
МПК / Метки
МПК: A61P 19/10, A61K 31/56, C07J 41/00
Метки: получения, фармацевтические, применение, способы, галогенированные, промежуточные, содержащие, 19-норстероиды, положении, продукты, композиции
Код ссылки
<a href="https://eas.patents.su/12-3325-19-norsteroidy-galogenirovannye-v-polozhenii-17-sposoby-ih-polucheniya-i-ih-primenenie-promezhutochnye-produkty-i-farmacevticheskie-kompozicii-ih-soderzhashhie.html" rel="bookmark" title="База патентов Евразийского Союза">19-норстероиды, галогенированные в положении 17, способы их получения и их применение, промежуточные продукты и фармацевтические композиции, их содержащие</a>
Предыдущий патент: Сфероиды, способ получения и фармацевтические композиции
Следующий патент: Способ лечения рака
Случайный патент: Системы и споcобы для автоматизированного быстрого обнаружения веществ с большим атомным номером
















