Композиции микросфер налтрексона для инъекций и их применение для уменьшения потребления героина и алкоголя
Номер патента: 4734
Опубликовано: 26.08.2004
Авторы: Феррелл Тереза М., Тайс Томас Р., Стаас Джей К.
Формула / Реферат
1. Композиция микросфер, содержащая свободное основание налтрексона в количестве в пределах от 15 до 50 мас.%, поли(D,L-лактид) в качестве матрицы и менее примерно 3 мас.% этилацетата, способная обеспечивать физиологически эффективный уровень налтрексона в течение 28 дней при внутримышечном введении млекопитающему, для уменьшения потребления героина и алкоголя, при этом по меньшей мере 90 мас.% указанной композиции составляют микросферы, имеющие диаметр в пределах от 20 до 100 мкм.
2. Композиция микросфер по п.1, в которой указанный налтрексон присутствует в количестве в пределах от 15 до 25 мас.% и указанный поли(D,L-лактид) имеет характеристическую вязкость в пределах от около 0,3 до 0,4 дл/г.
3. Композиция микросфер по п.1, в которой указанный налтрексон присутствует в количестве в пределах от 35 до 45 мас.% и указанный поли(D,L-лактид) имеет характеристическую вязкость в пределах от около 1,0 до 1,1 дл/г.
4. Композиция микросфер по п.1, в которой указанные микросферы покрыты маннитом.
5. Композиция микросфер по п.1, в которой указанный поли(D,L-лактид) является смесью поли(D,L-лактидов) различной характеристической вязкости.
6. Композиция микросфер по п.1, представляющая собой смесь микросфер, которые различаются, по меньшей мере, содержанием налтрексона и/или поли(D,L-лактида) различной характеристической вязкости.
7. Композиция микросфер по п.1, полученная введением раствора указанного налтрексона и поли(D,L-лактида) в этилацетате в водный раствор поли(винилового спирта), отделением полученных в результате микросфер путем экстрагирования этилацетата водой.
8. Композиция микросфер, содержащая от 35 до 45 мас.% налтрексона и матрицу поли(D,L-лактида), способная к высвобождению в организм человека в течение 4-недельного периода от около 10 до 40% в неделю от общего количества высвобождаемого налтрексона, обеспечивая в то же время терапевтическую дозировку по меньшей мере около 1 нг/мл в течение указанного 4-недельного периода.
9. Композиция микросфер по п.8, в которой только в течение одной недели из указанного 4-недельного периода высвобождается более чем около 20% от суммарного высвобожденного налтрексона.
10. Препарат для инъекции, содержащий композицию микросфер по п.1 или 8, карбоксиметилцеллюлозу и маннит.
11. Шприц, содержащий композицию по п.10.
12. Способ снижения потребления героина и алкоголя субъектом, имеющим зависимость по меньшей мере от одного из героина и алкоголя, включающий внутримышечное введение эффективной дозы композиции микросфер по п.1 в количестве, ингибирующем потребление героина и алкоголя.
13. Способ по п.12, в котором вводится от 2 до 4 мл носителя, содержащего микросферы.
14. Способ снижения потребления героина и алкоголя субъектом, имеющим зависимость по меньшей мере от одного из героина и алкоголя, включающий
введение эффективной дозы композиции микросфер по п.1, которая продолжает высвобождать налтрексон в течение более чем 28 дней при, по меньшей мере, эффективной дозе;
введение второй дозы указанной композиции налтрексона перед падением концентрации налтрексона ниже эффективной дозы, посредством чего сочетание указанной первоначальной эффективной дозы и указанной второй дозы обеспечивает эффективную дозу налтрексона в течение, по меньшей мере, дополнительно 28 дней, и
повторение указанного введения, чтобы налтрексон высвобождался и из первоначально введенной указанной композиции микросфер, и из позднее введенной композиции микросфер, чтобы поддерживать указанную эффективную дозу налтрексона.
15. Способ по п.14, в котором вводится от 2 до 4 мл носителя, содержащего микросферы.
16. Способ снижения потребления героина и алкоголя субъектом, имеющим зависимость по меньшей мере от одного из героина и алкоголя, включающий внутримышечное введение эффективной дозы композиции микросфер по п.8 в количестве, ингибирующем потребление героина и алкоголя.
Текст
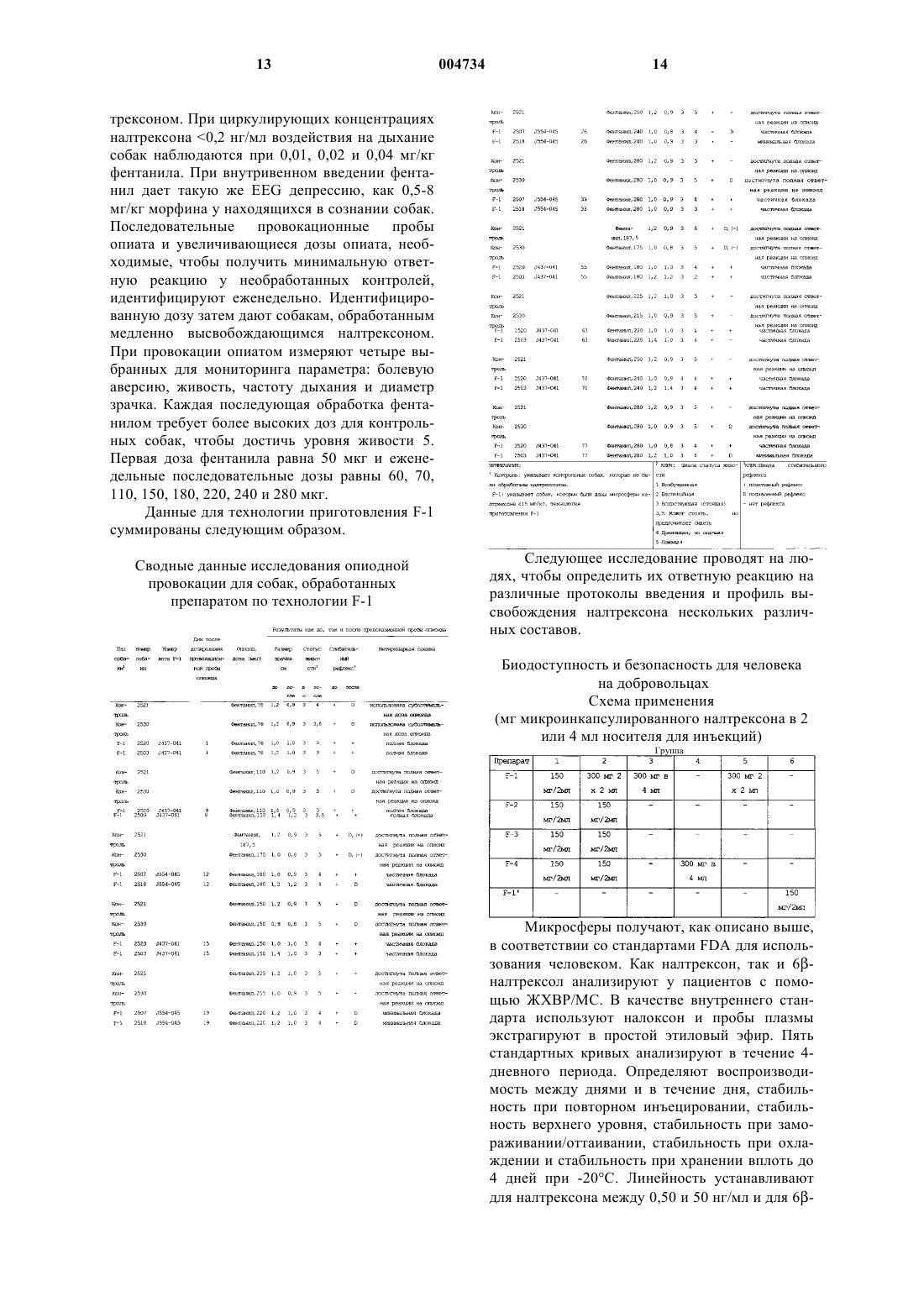
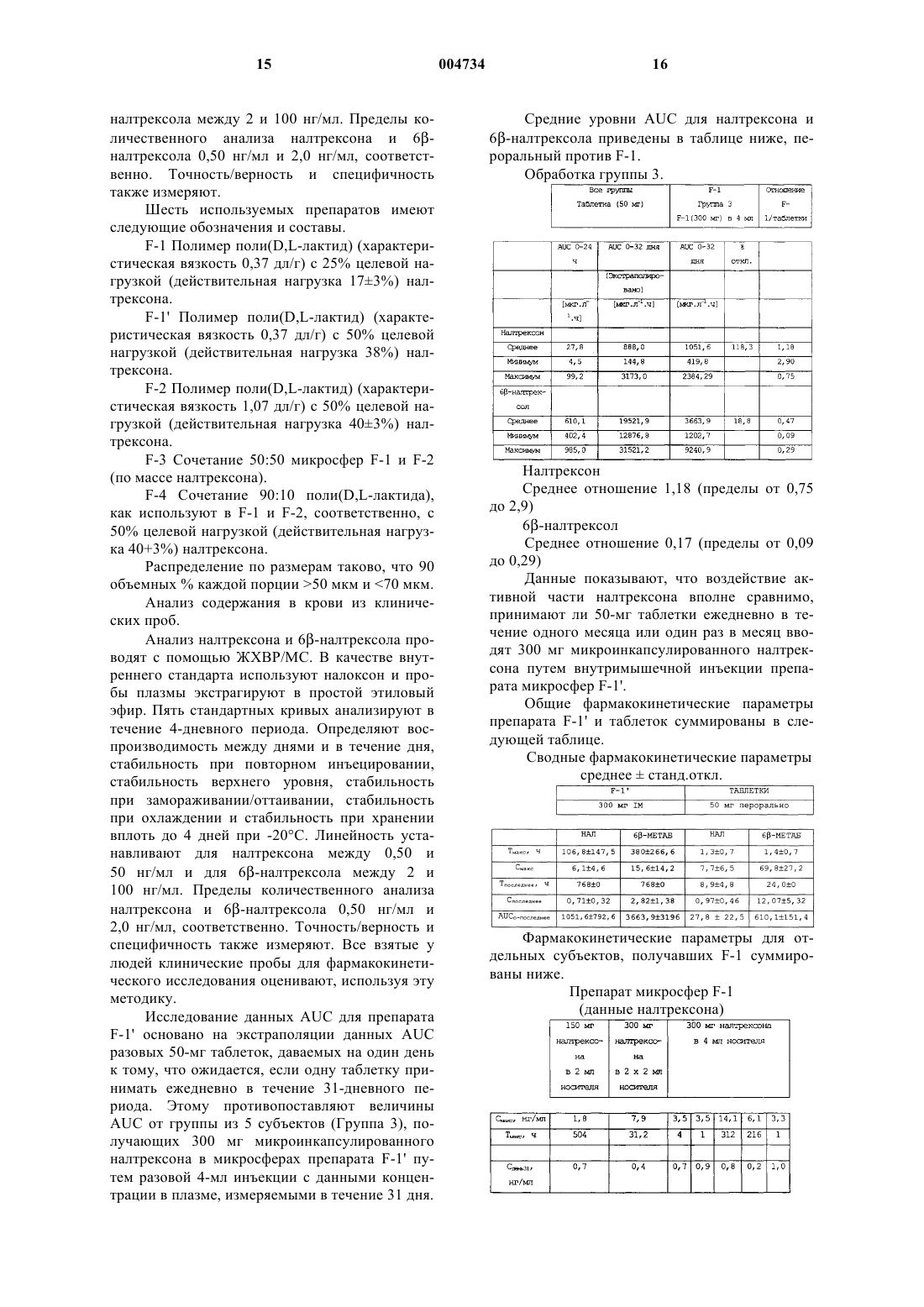
1 Предпосылки к созданию изобретения Злоупотребление веществ остается бедствием общества. Так как становится все более очевидным, что имеется генетическое предрасположение в приобретении зависимости, то скорее помощь страдающим от злоупотребления алкоголем и наркотиками, чтобы освободить их от зависимости или по меньшей мере достичь степени становления полноценным членом общества становится все более приемлемой политикой, чем лечение алкоголизма и наркомании. Различные программы были внедрены в общественных и частных секторах. В частных секторах существуют такие организации, как "Анонимные алкоголики" и "Анонимные наркоманы", которые играют важную роль в психосоциальной поддержке. Кроме того, существует много частных клиник, которые предоставляют и психологически социальную поддержку, и медицинскую поддержку, используя весьма ограниченный перечень лекарств, которые доступны. Имеются также обширные общественные программы привлечения внимания молодых людей и родителей к опасностям зависимости от веществ и чтобы отговаривать молодых людей прибегать к неправильному использованию лекарств. Также существуют метадоновые программы, которые, главным образом,находят общественную поддержку. Число зависимых от веществ в Соединенных Штатах совершенно ошеломляющее. По существующим оценкам около 15 миллионов человек страдают алкогольной зависимостью,около 1,3 миллиона страдают кокаиновой зависимостью в ее многочисленных проявлениях,около 0,8 миллиона зависят от амфетаминов и около 0,5-0,8 миллиона зависят от героина в дополнение к использованию других лекарств,таких как психотомиметические лекарства. Попытки снизить число потребителей перечисленных лекарств и алкоголя были постоянными и относительно тщетными. Те субъекты, которые вошли в программы, имели печальный рекорд рецидива, так что только малая часть людей,которые вошли в программы и удерживаются в программах, остаются чистыми долго после завершения программы. Одним значительным фактором в недостатке ретенции и рецидиве является соблюдение режима и схемы лечения. Повторный акт, такой как ежедневный прием пилюль, является непростым делом, даже когда субъект не испытывает позывов к рвоте при приеме пилюли. Для наркомана, который может испытывать физиологические и эмоциональные потребности в вызывающем зависимость веществе, выдерживание терапевтического режима является значительно более трудным. Терапевтические методики, которые требуют упорного и длительного воздействия на часть субъектов, снижают вероятность успеха лечения. Поэтому очень важно иметь возможность уменьшить степень вовлечения 2 субъекта, когда используются медицинские методы, особенно методы, которые предусматривают частое назначение, мониторинг соблюдения схемы лечения и выдерживание конкретного режима. Для того чтобы уменьшить трудности соблюдения режима лечения, были предприняты попытки использовать методики с замедленным высвобождением. Это методики с привлечением насосов, пластырей, депо и тому подобное. Когда высвобождающее приспособление доступно субъекту, всегда есть искушение удалить приспособление приступа. Эта возможность, которая может быть показателем силы желания, тем не менее подвергает риску субъект, который не выдерживает искушения. Введением лекарственного средства с длительным высвобождением удается избежать искушения, и лекарственное средство высвобождается в соответствии с предопределенным режимом в течение определенного периода времени. Это могут быть имплантируемые стержни, которые вводятся хирургически и должны быть удалены хирургически, или микросферы, которые вводят путем инъекции и которые предназначаются для высвобождения лекарственных средств в течение продолжительного периода времени регулируемым образом. Различные микросферы с длительным высвобождением (или микрочастицы) были разработаны для различных лекарственных средств,некоторые поступили в продажу. К удовлетворительному вводимому инъекцией препарату с длительным высвобождением предъявляется много требований: лекарство должно высвобождаться в течение продолжительного периода времени; во время лечения концентрация лекарственного средства, поддерживаемая в организме, должна быть эффективной концентрацией,не достигающей какого-либо опасного уровня; лекарственное средство должно высвобождаться медленно без катастрофического выброса лекарства; полимерная матрица, используемая для микросфер, должна быть биосовместимой и биоразлагаемой; какие-либо остаточные химические вещества должны быть ниже максимального приемлемого уровня; микросферы должны быть маленькими и пригодными для введения шприцем с иглой, которая приемлема для пациентов; результаты должны быть воспроизводимыми, такими как требуется для того, чтобы процесс мог быть точно регулируемым и не был чрезмерно чувствительным к незначительным изменениям условий; препарат для инъекций должен быть стерилизуем; метаболиты, которые образуются, должны быть в приемлемых количествах; также как другие характеристики, которые могут быть общепринятыми или специфическими для конкретного лекарственного средства. Свойства микросфер чувствительны к многим свойствам лекарственного средства и матрицы, а также к выбору способа и условий, в 3 которых получают и впоследствии перерабатывают микросферы. Краткое описание предшествующего уровня техникиRes 1998, 22:1074-1079 сообщает о лечении алкоголиков вводимым инъекцией препаратом частиц налтрексона с длительным высвобождением. Лабораторией Reuning были проведены многочисленные исследования, касающиеся налтрексона и его применения в форме с длительным высвобождением: Reuning и др., NIDAYamaguchi and Anderson, J. Control Release,1992, 19(1-3), стр. 299-314. Применение налтрексона в лечении алкоголизма описано в O=Маllеу и др., PsychiatricAnnals, ноябрь 1995, 11, стр. 681-688, а также в многочисленных других публикациях. К представляющим интерес патентам относятся патенты США 4568559, 4623588,4897267 и 5486362. Патент США 5407609 описывает способ, применимый к способу, используемому в данном изобретении. Применение полилактида для получения содержащих лекарственное средство микросфер описано в Benita и др., J. Pharm Sci, дек. 1984,73(12), стр. 1271-4; Speniehauer и др., там же,авг. 1986, 75(8), стр. 750-5, и Nihant и др.,окт.1994, 11(10), стр.1479-84. Краткое описание изобретения Предложены вводимые инъекцией препараты налтрексона с длительным высвобождением, содержащие терапевтически эффективное количество налтрексона, высвобождаемое в течение продолжительного периода времени, и матрицу, состоящую из полимера поли(D,Lлактида). Микросферы имеют диаметр менее 100 мкм и легко могут быть введены инъекцией внутримышечно. Различные профили высвобождения достигаются в зависимости от молекулярной массы полимера, гомогенности полимера по молекулярной массе, размера матрицы микросфер и процентной доли по массе нал 004734 4 трексона. Микросферы получают экстракцией растворителем эмульсии масла в воде, дисперсной масляной фазой является органический раствор налтрексона и полимера. Описание конкретных воплощений Предложены вводимые инъекцией препараты налтрексона с длительным высвобождением для применения при лечении алкоголиков и потребляющих героин наркоманов и других симптомов, для которых налтрексон найден эффективным. Предложены маленькие стерилизованные частицы, микросферы, которые могут проходить через иглу шприца и могут быть введены внутримышечно и оставаться на месте инъекции в течение продолжительного периода времени, при этом непрерывно высвобождая и поддерживая терапевтически эффективное количество налтрексона по меньшей мере около 28 дней. Обнаружено, что профиль высвобождения чувствителен к количеству налтрексона в микросферах, применению свободного основания по сравнению с солью и к характеристической вязкости и гомогенности (молекулярномассовый профиль) поли(D,L-лактида). Обнаружено, что профиль высвобождения менее чувствителен к условиям, в которых осуществляют процесс микроинкапсулирования, к распределению размеров микросфер, когда препарат по существу состоит из частиц в пределах от 20 до 100 мкм, и к количеству удержанного растворителя полимера до тех пор, пока количество растворителя полимера ниже примерно 3 маc.%. Микросферы, при наблюдении с помощью РЭМ, с лекарственным средством, диспергированным в матрице, по существу однородны. Микросферы имеют менее, чем около 3 мас.% этилацетата, органического растворителя, используемого при получении микросфер. Содержание налтрексона в микросферах от 5 до 50 мас.% может изменяться в пределах, зависящих от характеристической вязкости поли(D,Lлактида), образующего полимерную матрицу микросферы. Характеристическая вязкость полимера находится в пределах от около 0,3 до 1,2 дл/г (метод капиллярной вискозиметрии, хлороформ, концентрация полимера 0,5 г/дл, 30 С). Когда матрица имеет характеристическую вязкость в пределах около 0,3-0,4 дл/г, количество налтрексона бывает в пределах от около 5 до 45 мас.%, обычно от 10 до 40 мас.%, особенно от 10 до 30 мас.%. В то время как, когда характеристическая вязкость находится в пределах около 1,0-1,2 дл/г, обычно 1,0-1,1 дл/г, количество налтрексона бывает в пределах от около 35 до 50 мас.%, обычно от 35 до 45 мас.%. По большей части, полимеры, имеющие характеристическую вязкость в пределах от 0,45 до 0,95 дл/г,не будут использоваться. Смеси полимеров и/или микросфер могут быть использованы с тем, чтобы доставлять желательное количество налтрексона в течение желательного периода времени. Так, когда смешивают два полимера(перед микроинкапсулированием), имеющие различные характеристические вязкости, мас.% двух различных полимеров могут находиться в пределах от 1:99 до 99:1, более обычно от 10:90 до 90:10, где полимер с более низкой характеристической вязкостью (т.е. полимер с более низкой молекулярной массой будет в меньшем количестве, чем полимер с более высокой характеристической вязкостью (полимер с более высокой молекулярной массой). Подобно этому,микросферы налтрексона, полученные с полимером с низкой молекулярной массой, могут быть смешаны с микросферами, полученными с полимером более высокой молекулярной массой, где нагрузка лекарственного средства(мас.% налтрексона в препарате микросфер) может изменяться, когда две или больше микросфер смешивают вместе. С двумя различными рецептурами микросфер смесь имеет массовое отношение в пределах от 5:95 до 95:5, где микросферы, полученные с полимером с более низкой молекулярной массой, обычно присутствуют в количестве от около 10 до 65 мас.%. Более, чем около 90 мас.% микросфер имеют диаметр в пределах от около 20 до 100 мкм, и менее, чем около 5 мас.% имеют диаметр более, чем около 100 мкм. Чтобы уменьшить агломерацию, микросферы могут быть покрыты агентом против агломерации, таким как маннит, который используют в количестве менее, чем около 10 мас.%,обычно менее, чем около 5 мас.%, и может быть менее, чем около 2 мас.% от массы микросфер. Желательно, чтобы микросферы высвобождали налтрексон в течение периода по меньшей мере 4 недели, где площадь под кривой в мониторинге содержания налтрексона в плазме человека менее, чем около 40% в течение любого недельного периода и по меньшей мере около 10%, предпочтительно по меньшей мере около 12%. Как правило, относительная доля в течение по меньшей мере двух недель, предпочтительно 3 недель, не более, чем 25%, обычно не более, чем 20%. Желательно, когда по меньшей мере около 75%, предпочтительно по меньшей мере около 80% и не более, чем около 95% налтрексона, как определено по площади под кривой, высвобождается в течение первых 4 недель. Площадь под кривой определяют стандартной фармакокинетической компьютерной программой, озаглавленной WinNonlin Professional (версия 2.1, Pharsight, Inc., Mountain View, CA). Микросферы смешивают с подходящим носителем, чтобы обеспечить от около 150 до 350 мг налтрексона, обычно от 250 до 350 мг налтрексона, конкретно 30015 мг налтрексона,для введения. Носителем может быть стерильная вода, фосфатный буферный солевой раствор или другой приемлемый носитель для введения микросфер. Могут присутствовать добавки для уменьшения адгезии микросфер, уменьшения дискомфорта от инъекции, уменьшения отека, 004734 6 раздражения, опухолей или другого дискомфорта. Обычно маннит может присутствовать в количестве от около 2 до 10 мас.% от массы носителя, особенно от 4 до 7 мас.% от массы носителя. Другие физиологически приемлемые добавки могут включать неионные детергенты, например Tween, полисорбат и т.д., если они присутствуют, то составляют от около 0,05 до 0,2 мас.% носителя, повышающие вязкость агенты,например карбоксиметилцеллюлоза, в пределах от около 0,1 до 1 мас.% носителя и другие приемлемые добавки. Количество носителя, как правило, составляет в пределах от около 1,5 до 5 мл, обычно от 2 до 4 мл, особенно от 2 до 3 мл,где меньшие количества обычно влекут за собой многократные инъекции, напр. 2. Микросферы диспергируют в носителе непосредственно перед использованием. Обычно микросферы должны храниться после стерилизации в стерильной ампуле с перегородкой, где микросферы могут быть смешаны с носителем и затем забраны в шприц. Обычно игла не должна иметь внутренний диаметр больше, чем около 18. При введении несколькими инъекциями они могут быть на тех же самых, соседних или удаленных местах. Микросферы получают способом микроинкапсулирования, по существу, как описано в патенте США 5407609. Способ является процессом на основе эмульсии, который предусматривает приготовление эмульсии, содержащей непрерывную водную фазу (вода и поверхностно-активное вещество и/или загуститель) и гидрофобную дисперсную фазу (растворитель полимера, полимер и лекарственное средство). Вскоре после образования эмульсии растворитель полимера экстрагируют в водную экстракционную фазу. Затем экстрагируют достаточное количество растворителя полимера для отверждения микросфер, микросферы собирают на ситах и промывают, чтобы удалить поверхностно-активное вещество, остающееся на поверхности микросфер. Микросферы затем сушат на воздухе при комнатной температуре или сушат путем лиофилизации или другими обычными способами сушки. Для получения данных микросфер дисперсная фаза (органический раствор) содержит примерно от 1 до 10 мас.% налтрексона и примерно от 1 до 20 мас.% полимера, растворенного в этилацетате. Непрерывная фаза является водным раствором от около 1 до 10 мас. % поли(винилового спирта) и от 1 до 7 мас.% этилацетата. Экстракционной фазой является вода. Обычно количество используемого налтрексона будет в избытке от около 20 до 50 мас.% от конечного количества налтрексона в микрочастицах. Температуры могут быть температурами окружающей среды, обычно от около 15 до 30 С. После того, как микросферы собраны и высушены, они могут храниться при температу 7 рах окружающей среды, в частности в пределах от около 0 до 20 С в среде, не содержащей кислорода и воды, или могут быть разделены на аликвотные пробы в подходящие контейнеры и стерилизованы. Могут быть использованы различные способы стерилизации, обычно это гамма-облучение. Относительно простой аппарат может быть использован для изготовления микросфер. Используя накопительные контейнеры для удерживания различных жидкостей, трубопроводы,насосы, клапаны и гомогенизатор, систему легко собирают. Дополнительно могут быть включены различные контролирующие устройства,такие как расходомеры, устройства для контроля температуры, устройства для контроля размеров частиц и т.д. Органический раствор нагнетают насосом в первую трубу, которая вставлена в гомогенизатор. Подобным образом водный раствор (для непрерывной фазы) нагнетают насосом во вторую трубу, которая также вставлена в гомогенизатор. Регулируя скорость течения обоих потоков в трубах, присоединенных к гомогенизатору, можно контролировать отношение двух потоков, а также время пребывания в гомогенизаторе. Отходящий из гомогенизатора поток (эмульсия масла в воде) выходит через третий трубопровод, содержащий проточную воду. Вода экстрагирует растворитель полимера этилацетат из капелек эмульсии до образования микросфер. Снова отношение скоростей потоков регулирует количество эмульсии и воды, вводимой в третий трубопровод. Длина третьего трубопровода и скорость течения объединенных потоков регулируют время пребывания на стадии водной экстракции. Микросферы затем разделяют по размерам, пропуская их через два или более сит, которые отторгают микросферы, выходящие за пределы желательных размеров. Данные препараты применяют в основном как препараты для внутримышечных инъекций,хотя он может также использоваться для подкожных инъекций. Субъектом обычно будет человек с зависимостью от такого вещества, как алкоголь или героин, но данные препараты могут быть использованы и при других симптомах,таких как ожирение. Подходящее количество данного препарата вводят инъекцией непосредственно в обычное место, например ягодицы. После этого может быть произведен мониторинг концентрации налтрексона в плазме субъекта для гарантии того, что количество находится в терапевтических пределах по меньшей мере около 1 нг/мл, предпочтительно по меньшей мере около 2 нг/мл. Когда концентрация налтрексона в плазме падает ниже терапевтического предела, может быть сделана следующая инъекция, и этот процесс повторяется во время периода лечения. В случае героиновой зависимости субъекта обычно следует подвергнуть детоксикации од 004734 8 ним из различных возможных путей с использованием бупренорфина, клонидина, налтрексона и т.п. и проверке налоксоном. Реакция на налоксон показывает, что субъект неполностью детоксифицирован. Обнаружено также, что около 10% популяции, которая была подвергнута испытанию с пероральным введением налтрексона, имели побочные реакции, которые могут разрешиться сами по себе или исключением применения налтрексона. Кроме того, имеются некоторые сообщения о гепатотоксичности, являющейся результатом применения налтрексона в высоких дозах, с потенциалом таких высоких доз метаболита, 6-налтрексола, имеющего гепатотоксичность, так что субъекты, которые имеют подвергающуюся риску печень, например субъекты, инфицированные гепатитом С,могут быть исключены из лечения. В других отношениях, налтрексон был найден безопасным при вводимых количествах, превышающих количества, используемые с данными композициями. В случае алкоголиков, если однажды было определено, что субъект не реагирует неблагоприятно на налтрексон, данный препарат может вводиться инъекцией субъекту. Обнаружено, что налтрексон служит для улучшения контроля алкоголиков по количеству потребляемого алкоголя и числу выпивок. С помощью микросфер, которые имеют способность долгосрочного высвобождения, то есть более чем 28 дней, особенно более чем около 32 дней, можно наслаивать введение, так что путем периодических повторных инъекций достигается дополнительный эффект. Таким образом, после первой дозы могут вводиться более мелкие дозы, потому что продолжается высвобождение из микросфер, введенных первоначальной инъекцией, к которому добавляется высвобождение из введенных позднее микросфер, или можно использовать повышенные концентрации налтрексона без увеличения количества вводимых микросфер. Предусматривая это для микросфер, можно продолжать высвобождение при концентрациях в крови свыше 1 нг/мл, предпочтительно свыше 1,5 нг/мл в крови, более предпочтительно свыше 2 нг/мл в крови, более, чем около 28 дней после инъекции,часто по меньшей мере около 36 дней, еще чаще по меньшей мере около 42 дней. Таким образом,защита значительно улучшается, так как субъект постоянно защищен защитной концентрацией налтрексона, и можно обеспечить концентрации налтрексона, которые будут ингибировать реакцию на 50 мг провокационную дозу героина или эквивалентную дозу другого лекарственного средства, например фентанила. Следующие примеры предложены для пояснения, но не в качестве ограничения. Экспериментальная часть Способ микроинкапсулирования предусматривает микроинкапсулирование путем экстракции растворителем. Безводное основание 9 налтрексона, поли(D,L-лактид) и этилацетат объединяют и добавляют во встроенный гомогенизатор с водой и поверхностно-активным веществом. Получают эмульсию, добавляют дополнительную воду и начинают процесс экстракции. Продукт, микросферы налтрексона,сушат лиофилизацией в банках. Применяют гамма-стерилизацию при воздействии 2,5 Мрад и проводят мониторинг биозагрязнения, бактериостаза и фунгистаза. Подходящее количество сухих микросфер налтрексона развешивают в пустые склянки емкостью 5 см 3, закрывают резиновыми пробками, герметично закрывают алюминиевыми крышками и герметизируют в фольговых мешочках для транспортировки и стерилизации. Склянку, содержащую 2 мл разбавителя, содержащего 0,5% карбоксиметилцеллюлозы, 0,1% полисорбата 80 и 5% маннита, используют для повторного суспендирования микросфер. Суспензию набирают в шприц 3 см 3 с иглой 18 калибра. Внутримышечную инъекцию делают сразу же, чтобы предотвратить осаждение микросфер. Инъекция может состоять из одной или двух инъекций от 2 до 4 мл, обычно в сумме не более, чем 4 мл. Распределение по размерам контролируют так, что 90% по объему каждой партии составляют частицы 40 мкм и 90 мкм. Характеристики высвобождения in vitro определяют по % высвобожденного в течение первых 72 ч при 37 С. Описание микроинкапсулирования налтрексона содержится в следующих разделах. Стадия 1: 2,5 мас.% раствор полимера готовят смешиванием этилацетата с поли(D,Lлактидом) низкой молекулярной массы в 8 литровой колбе биореактора, оборудованной мешалкой с покрытым ПТФЭ перемешивающим стержнем. Минимум 4 ч требуется, чтобы полностью растворить полимер. Массу раствора полимера и его колбы измеряют и, если необходимо, добавляют дополнительный этил-ацетат,чтобы вернуть раствор снова к его желательной массе. Стадия 2: 2 мас.% раствор поли(винилового спирта) (ПВС) готовят перемешиванием ПВС в стерильной воде в 3-4 порциях и перемешивают при 90 С. Каждую порцию затем оставляют для охлаждения до комнатной температуры и затем снова добавляют воду,чтобы восполнить потери испарения. После успешного завершения префильтровального испытания монолитности на 200-литровой установке Millipak растворы фильтруют и заливают в 36-литровую колбу биоректора. Колбу и ее содержимое затем взвешивают, 2,5 мас.% этилацетата добавляют к раствору ПВС, и приводимая в действие мотором ПТФЭ мешалка перемешивает раствор минимум 30 мин. Стадия 3: Для каждых 15 г полученного лекарственного продукта минимум 8 л воды 10 подают в резервуар из нержавеющей стали емкостью 189,265 л (50 галлонов), закрывают и хранят. Стадия 4: Раствор дисперсной фазы налтрексона готовят добавлением налтрексона к раствору полимера при перемешивании. Раствор перемешивают минимум 1 ч, пока налтрексон не растворится. Стадия 5: Чтобы подготовить к работе оборудование для непрерывного микроинкапсулирования, проводят проверку дисперсной фазы, непрерывной фазы и экстракционной фазы и насосов, чтобы точно установить расход, например 25, 125 и 2000 г/мин, соответственно для получения препарата F-1. Иглу дисперсной фазы наполняют затем раствором дисперсной фазы и расход насоса дисперсной фазы поддерживают регулированием обходного пути. Затем запускают насос экстракционной фазы и линии экстракции заполняют и освобождают от пузырьков. Затем включают насос непрерывной фазы и позволяют ПВС течь в экстракционный трубопровод. Затем включают гомогенизатор и устанавливают на скорость перемешивания 65020 обор. в мин. Игольчатый клапан дисперсной фазы затем открывают и включают насос дисперсной фазы,чтобы позволить раствору дисперсной фазы течь в камеру гомогенизатора с раствором ПВС. Это является началом замеса. После гомогенизации эмульсия вытекает из встроенного гомогенизатора и течет в линию экстракции, содержащую проточную воду, которая экстрагирует этилацетат из микросфер. Водную суспензию микросфер затем собирают в накопительный резервуар из нержавеющей стали емкостью 189,265 л, оборудованный мешалкой с мотором. Микросферы перемешивают при 50050 обор. в мин при заполнении резервуара на 25-50%. Суспензию микросфер затем пропускают через вибрирующую ситовую деку RBF-12 Vorti-Sieve, содержащую последовательно расположенные 125-мкм и 20-мкм сита, используя центробежный насос. Если сита засоряются, их удаляют и заменяют новым набором чистых сит. 20-мкм сито смывают водой в резервуар промывочной ванны из нержавеющей стали емкостью 302,824 л и непрерывно перемешивают, пока остаток процесса не будет собран. После того, как последний раствор дисперсной фазы проходит в гомогенизатор, насос дисперсной фазы останавливают и игольчатый клапан дисперсной фазы закрывают. Это является концом периодического процесса. Окончательное количество раствора дисперсной фазы затем гомогенизируют, экстрагируют и фильтруют через сита. Затем через сита прокачивают насосом воду в течение 10 мин, чтобы промыть микросферы. Микросферы на 20-мкм сите затем смывают в резервуар промывочной ванны из нержавеющей стали емкостью 302,824 л и непрерывно 11 перемешивают 50050 обор. в мин минимум 3 ч. Микросферы затем пропускают через другие вибрирующие ситовые деки RBF-12 Vorti-Sieve,содержащие последовательно расположенные 125-мкм и 20-мкм сита, используя центробежный насос. Микросферы на 20-мкм сите переносят затем в накопительный резервуар путем смывания водой. Микросферы разбавляют водой, чтобы получить суспензию с 15% твердых веществ на основе оцененного выхода. Суспензию непрерывно перемешивают, в то время как содержимое разделяют в однолитровые колбы для лиофилизации, так что каждая колба содержит приблизительно определенные 20 г микросфер. После лиофилизации микросферы просеивают в сухом состоянии через 125-мкм сито. Микросферы затем взвешивают и распределяют в бутылки из янтарного стекла янтарного цвета. Бутылки закрывают крышками, герметизируют и упаковывают в пластиковые мешки с осушающим веществом силикагелем. Мешки хранят при 2-8 С. После того, как микросферы уже отвечают заранее определенным критериям по нагрузке ядра, распределению по размерам, теоретическому выходу и остаточному этилацетату, их упаковывают как разовые дозы в пузырьки из бесцветного стекла емкостью 5 см 3. Затем пузырьки закрывают покрытыми ПТФЭ резиновыми пробками, закрывают сверху алюминиевыми крышками, маркируют и герметизируют в отдельных мешочках из фольги. Руководство, описывающее подробное приготовление и компоненты наборов, представлено ниже. 1. Используя иглу 18 калибра, набирают 2,0 см 3 разбавителя в шприц 3 см 3 и выпускают в пузырек, содержащий микросферы. Выбрасывают эту иглу и шприц. 2. Энергично встряхивают ампулу в течение 30 с, чтобы суспендировать микросферы. 3. Помещают новую иглу 18 калибра на новый шприц на 3 см 3. 4. Набирают суспензию микросфер в шприц, перевернув пузырек. 5. Выпускают микросферы обратно в ампулу. 6. Повторяют стадии 4 и 5 дополнительно два раза. 7. Выбрасывают эту иглу и шприц. 8. Помещают новую иглу 18 калибра на новый шприц на 3 см 3. 9. Набирают суспензию микросфер в шприц, перевернув пузырек. Вынимают иглу из пузырька. 10. Удаляют воздушные пузырьки из суспензии и вводят дозу так быстро, насколько это возможно, чтобы предотвратить осаждение микросфер. Следующая таблица показывает специфические параметры приготовления микросфер и свойства и действие микросфер in vitro и in vivo. 12 В исследовании in vivo собакам внутримышечно инъецировали иглой 18 калибра около 2 мл раствора, содержащего микросферы в массе, указанной в таблице. Проводили мониторинг плазмы на налтрексон в указанное в таблице время. Для исследования in vitro микросферы поддерживали в 0,01 М фосфатном буфере, рН 7,4 при 37 С и остаточный налтрексон в микросферах определяли в указанное время. Анализ содержания в крови на собаках. Анализ налтрексона в плазме собаки проводят путем ЖХВР и электрохимического определения. Оценивают чистую плазму собаки, а также нарушенную (введением посторонних веществ) плазму. Нет никаких эндогенных соединений в плазме после экстракции пробы,которые влияли бы на определение налтрексона и внутренний стандарт. Метод характеризуется линейностью, правильностью, точностью и чувствительностью. Линейный диапазон метода простирается от 0,5 до 10 нг/мл налтрексона в плазме собаки. Точность является высокой с процентной разностью между теоретической и подтвержденной расчетами концентрацией стандартов менее, чем 15%. Нижний предел обнаружения 0,5 нг/мл. Все пробы фармакокинетического исследования на собаках оценивают с помощью этого метода. Собакам вводят фентанил, чтобы определить, будет ли ответная реакция на провокационную пробу фентанила притуплена нал 13 трексоном. При циркулирующих концентрациях налтрексона 0,2 нг/мл воздействия на дыхание собак наблюдаются при 0,01, 0,02 и 0,04 мг/кг фентанила. При внутривенном введении фентанил дает такую же EEG депрессию, как 0,5-8 мг/кг морфина у находящихся в сознании собак. Последовательные провокационные пробы опиата и увеличивающиеся дозы опиата, необходимые, чтобы получить минимальную ответную реакцию у необработанных контролей,идентифицируют еженедельно. Идентифицированную дозу затем дают собакам, обработанным медленно высвобождающимся налтрексоном. При провокации опиатом измеряют четыре выбранных для мониторинга параметра: болевую аверсию, живость, частоту дыхания и диаметр зрачка. Каждая последующая обработка фентанилом требует более высоких доз для контрольных собак, чтобы достичь уровня живости 5. Первая доза фентанила равна 50 мкг и еженедельные последовательные дозы равны 60, 70,110, 150, 180, 220, 240 и 280 мкг. Данные для технологии приготовления F-1 суммированы следующим образом. Сводные данные исследования опиодной провокации для собак, обработанных препаратом по технологии F-1 Следующее исследование проводят на людях, чтобы определить их ответную реакцию на различные протоколы введения и профиль высвобождения налтрексона нескольких различных составов. Биодоступность и безопасность для человека на добровольцах Схема применения(мг микроинкапсулированного налтрексона в 2 или 4 мл носителя для инъекций) Группа Микросферы получают, как описано выше,в соответствии со стандартами FDA для использования человеком. Как налтрексон, так и 6 налтрексол анализируют у пациентов с помощью ЖХВР/МС. В качестве внутреннего стандарта используют налоксон и пробы плазмы экстрагируют в простой этиловый эфир. Пять стандартных кривых анализируют в течение 4 дневного периода. Определяют воспроизводимость между днями и в течение дня, стабильность при повторном инъецировании, стабильность верхнего уровня, стабильность при замораживании/оттаивании, стабильность при охлаждении и стабильность при хранении вплоть до 4 дней при -20 С. Линейность устанавливают для налтрексона между 0,50 и 50 нг/мл и для 6 15 налтрексола между 2 и 100 нг/мл. Пределы количественного анализа налтрексона и 6 налтрексола 0,50 нг/мл и 2,0 нг/мл, соответственно. Точность/верность и специфичность также измеряют. Шесть используемых препаратов имеют следующие обозначения и составы.F-4 Сочетание 90:10 поли(D,L-лактида),как используют в F-1 и F-2, соответственно, с 50% целевой нагрузкой (действительная нагрузка 40+3%) налтрексона. Распределение по размерам таково, что 90 объемных % каждой порции 50 мкм и 70 мкм. Анализ содержания в крови из клинических проб. Анализ налтрексона и 6-налтрексола проводят с помощью ЖХВР/МС. В качестве внутреннего стандарта используют налоксон и пробы плазмы экстрагируют в простой этиловый эфир. Пять стандартных кривых анализируют в течение 4-дневного периода. Определяют воспроизводимость между днями и в течение дня,стабильность при повторном инъецировании,стабильность верхнего уровня, стабильность при замораживании/оттаивании, стабильность при охлаждении и стабильность при хранении вплоть до 4 дней при -20 С. Линейность устанавливают для налтрексона между 0,50 и 50 нг/мл и для 6-налтрексола между 2 и 100 нг/мл. Пределы количественного анализа налтрексона и 6-налтрексола 0,50 нг/мл и 2,0 нг/мл, соответственно. Точность/верность и специфичность также измеряют. Все взятые у людей клинические пробы для фармакокинетического исследования оценивают, используя эту методику. Исследование данных AUC для препаратаF-1' основано на экстраполяции данных AUC разовых 50-мг таблеток, даваемых на один день к тому, что ожидается, если одну таблетку принимать ежедневно в течение 31-дневного периода. Этому противопоставляют величиныAUC от группы из 5 субъектов (Группа 3), получающих 300 мг микроинкапсулированного налтрексона в микросферах препарата F-1' путем разовой 4-мл инъекции с данными концентрации в плазме, измеряемыми в течение 31 дня. Налтрексон Среднее отношение 1,18 (пределы от 0,75 до 2,9) 6-налтрексол Среднее отношение 0,17 (пределы от 0,09 до 0,29) Данные показывают, что воздействие активной части налтрексона вполне сравнимо,принимают ли 50-мг таблетки ежедневно в течение одного месяца или один раз в месяц вводят 300 мг микроинкапсулированного налтрексона путем внутримышечной инъекции препарата микросфер F-1'. Общие фармакокинетические параметры препарата F-1' и таблеток суммированы в следующей таблице. Сводные фармакокинетические параметры среднеестанд.откл. Фармакокинетические параметры для отдельных субъектов, получавших F-1 суммированы ниже. Препарат микросфер F-1 17 Общие концентрации в плазме F-1' обнаруживают первоначальный максимум между одним и четырьмя часами и второй максимум во время недели 2-3. Вероятно, что первоначальный пик отражает налтрексон на или вблизи поверхности микросфер, легко доступный при инъекции. Сразу после инъекции микросферы впитывают жидкости, которые образуют поры, через которые налтрексон растворяется, чтобы обеспечить непрерывную доставку лекарства. Вторые пики во время недель 2-3 являются отражением биодеградации микросфер и вероятности того, что первоначальная масса распадается, создавая увеличенную удельную поверхность открытого налтрексона на месте депо, с временным увеличением концентраций налтрексона в плазме. Непрерывное высвобождение налтрексона в течение одномесячного интервала с последующим введением доз обеспечивает движущую силу лекарства из места созданного инъекцией депо по кровотоку к опиоидному рецептору. Эта движущая сила будет обеспечивать блокаду рецептора в течение одномесячного интервала дозирования. Исследование данных площади под кривой(AUC) для препарата F-1' показывает непрерывное высвобождение лекарства в течение одного месяца и достаточно сравнимое воздействие налтрексона, вводят ли 300 мг инъекцией раз в месяц или дают перорально 50 мг ежедневно. Данные могут быть охарактеризованы следующим образом. AUC после разовой 50-мг таблетки экстраполируют на 32 дня, основываясь на предположении, что обычная доза при лечении зависимости от веществ составляет 50 мг/день. Дополнительно делают предположение, что нет разницы между фармакокинетическими профилями налтрексона и его метаболита после разовой и множественных доз, как продемонстрировано в предварительных клинических исследованиях. После инъекции F-1' АUС 0-32 день подобна таковой после 32 ежедневных 50-мг пероральных доз. Проявление метаболита после пероральных доз в 22 раза выше, чем проявление налтрексона. Отношение проявления метаболит/налтрексон равно 3,5 для F-1'. Тпоследнее после перорального введения равно в среднем 8,9 ч. С препаратами замедленного высвобождения обеспечивается постоянное присутствие налтрексона в плазме в пределах эффективной концентрации. Дополнительные данные представлены в следующей таблице и сопровождающем графическом материале. 18 Данная таблица показывает, что высвобождение налтрексона в течение 31-дневного периода составляет основную долю первоначально инъецированного общего количества налтрексона. Из указанных результатов очевидно, что длительная доставка налтрексона в физиологически активной концентрации может быть обеспечена in vivo. Таким образом можно избежать проблем с соблюдением режима приема лекарственного средства, связанных с требованием ежедневного приема пилюль. Наблюдение, чтобы определить, принимает ли субъект пилюли ежедневно, исключается. Субъект лучше способен справиться с проблемой зависимости от вещества, сознавая, что он лучше контролируется в случае алкоголизма и не достигнет желательной эйфории от героина. Рекомендации могут быть более эффективно претворены в жизнь,поскольку субъект не будет получать удовольствия от приема героина и в случае алкоголизма он лучше будет способен справиться с уменьшением приема алкоголя. Таким образом субъекты будут способны работать и выполнять свои обязанности по отношению к их семьям и обществу. Налтрексон медленного высвобождения снижает беспокойство в отношении гепатотоксичности, связанной с метаболитом 6 налтрексолом. Путем исключения интенсивного первоначального метаболизма, имеющего место при ежедневной дозе, и поддерживая постоянную доставку налтрексона в меньших количествах, снижают концентрации 6-налтрексола. Кроме того, избегают интенсивного высокого метаболизма, являющегося результатом первоначальной высокой концентрации налтрексона,когда таблетку принимают ежедневно. Меньшая потребность во введении налтрексона, снижает количество лекарства, требуемое для поддержания человека в течение одномесячного периода. Все публикации и патентные заявки, упомянутые в данном описании, включены в описание в качестве ссылок в той степени, насколько каждая отдельная публикация или патентная заявка заслуживают быть приобщенными к описанию. Исходя из полноты описанного изобретения, специалисту должно быть очевидно, что могут быть внесены различные изменения и модификации, не выходя за пределы сущности или объема прилагаемой формулы изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Композиция микросфер, содержащая свободное основание налтрексона в количестве в пределах от 15 до 50 мас.%, поли(D,L-лактид) в качестве матрицы и менее, примерно 3 мас.% этилацетата, способная обеспечивать физиологически эффективный уровень налтрексона в течение 28 дней при внутримышечном введении млекопитающему, для уменьшения потребления героина и алкоголя, при этом по меньшей мере 90 мас.% указанной композиции составляют микросферы, имеющие диаметр в пределах от 20 до 100 мкм. 2. Композиция микросфер по п.1, в которой указанный налтрексон присутствует в количестве в пределах от 15 до 25 мас.%, и указанный поли(D,L-лактид) имеет характеристическую вязкость в пределах от около 0,3 до 0,4 дл/г. 3. Композиция микросфер по п.1, в которой указанный налтрексон присутствует в количестве в пределах от 35 до 45 мас.%, и указанный поли(D,L-лактид) имеет характеристическую вязкость в пределах от около 1,0 до 1,1 дл/г. 4. Композиция микросфер по п.1, в которой указанные микросферы покрыты маннитом. 5. Композиция микросфер по п.1, в которой указанный поли(D, L-лактид) является смесью поли(D,L-лактидов) различной характеристической вязкости. 6. Композиция микросфер по п.1, представляющая собой смесь микросфер, которые различаются по меньшей мере содержанием налтрексона и/или поли(D,L-лактида) различной характеристической вязкости. 7. Композиция микросфер по п.1, полученная введением раствора указанного налтрексона и поли(D,L-лактида) в этилацетате в водный раствор поли(винилового спирта), отделением полученных в результате микросфер путем экстрагирования этилацетата водой. 8. Композиция микросфер, содержащая от 35 до 45 мас.% налтрексона и матрицу поли(D,L-лактида), способная к высвобождению в организм человека в течение 4-недельного периода от около 10 до 40% в неделю от общего количества высвобождаемого налтрексона,обеспечивая в то же время терапевтическую дозировку по меньшей мере около 1 нг/мл в течение указанного 4-недельного периода. 9. Композиция микросфер по п.8, в которой только в течение одной недели из указанного 4-недельного периода высвобождается более, 20 чем около 20% от суммарного высвобожденного налтрексона. 10. Препарат для инъекции, содержащий композицию микросфер по п.1 или 8, карбоксиметилцеллюлозу и маннит. 11. Шприц, содержащий композицию по п.10. 12. Способ снижения потребления героина и алкоголя субъектом, имеющим зависимость по меньшей мере от одного из героина и алкоголя, включающий внутримышечное введение эффективной дозы композиции микросфер по п.1 в количестве, ингибирующем потребление героина и алкоголя. 13. Способ по п.12, в котором вводится от 2 до 4 мл носителя, содержащего микросферы. 14. Способ снижения потребления героина и алкоголя субъектом, имеющим зависимость по меньшей мере от одного из героина и алкоголя, включающий введение эффективной дозы композиции микросфер по п.1, которая продолжает высвобождать налтрексон в течение более, чем 28 дней при по меньшей мере эффективной дозе; введение второй дозы указанной композиции налтрексона перед падением концентрации налтрексона ниже эффективной дозы, посредством чего, сочетание указанной первоначальной эффективной дозы и указанной второй дозы обеспечивает эффективную дозу налтрексона в течение по меньшей мере дополнительно 28 дней, и повторение указанного введения, чтобы налтрексон, высвобождался и из первоначально введенной указанной композиции микросфер, и из позднее введенной композиции микросфер,чтобы поддерживать указанную эффективную дозу налтрексона. 15. Способ по п.14, в котором вводится от 2 до 4 мл носителя, содержащего микросферы. 16. Способ снижения потребления героина и алкоголя субъектом, имеющим зависимость по меньшей мере от одного из героина и алкоголя, включающий внутримышечное введение эффективной дозы композиции микросфер по п.8 в количестве, ингибирующем потребление героина и алкоголя.
МПК / Метки
МПК: A61K 31/485
Метки: потребления, композиции, микросфер, героина, применение, алкоголя, инъекций, уменьшения, налтрексона
Код ссылки
<a href="https://eas.patents.su/11-4734-kompozicii-mikrosfer-naltreksona-dlya-inekcijj-i-ih-primenenie-dlya-umensheniya-potrebleniya-geroina-i-alkogolya.html" rel="bookmark" title="База патентов Евразийского Союза">Композиции микросфер налтрексона для инъекций и их применение для уменьшения потребления героина и алкоголя</a>
Предыдущий патент: Линейный индикатор для клапана
Следующий патент: Сульфонамиды и их производные, модулирующие активность эндотелина
Случайный патент: 4-аминотетрагидробензизоксазоловые или -изотиазоловые соединения, их применение и фармацевтическая композиция на их основе