Разветвленный ацилазидный пегилирующий агент, способ его получения и способ получения пегилированного интерферона
Номер патента: 23323
Опубликовано: 31.05.2016
Авторы: Гапонюк Петр Яковлевич, Маркова Инна Николаевна, Гапонюк Полина Петровна, Марков Илья Александрович, Маркова Елена Алексеевна
Формула / Реферат
1. Разветвленный ацилазидный пегилирующий агент (ПЭГ-агент) общей формулы (I)
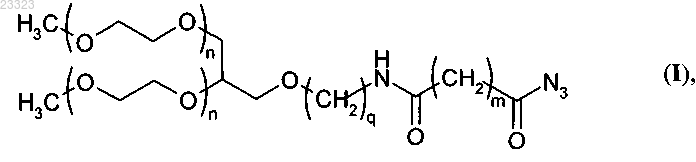
где n - целое число в интервале от 200 до 950;
q - целое число в интервале от 1 до 5;
m - целое число в интервале от 1 до 5.
2. Способ получения разветвленного ацилазидного пегилирующего агента (ПЭГ-агента) общей формулы (I)
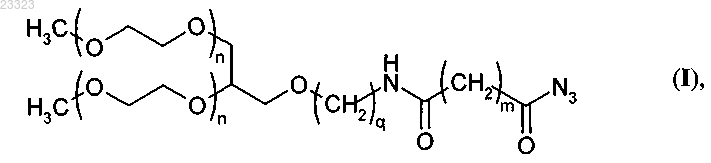
где n - целое число в интервале от 200 до 950;
q - целое число в интервале от 1 до 5;
m - целое число в интервале от 1 до 5,
характеризующийся тем, что активированный эфир (III)
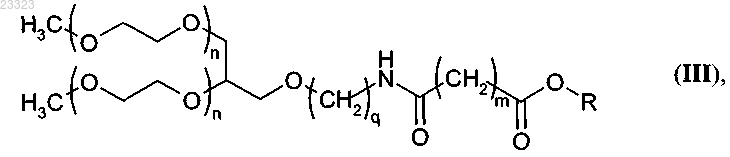
где O-R представляет собой остаток гидроксилсодержащего соединения, выбранный из N-гидроксисукцинимида, 4-нитрофенолята, 2,4-динитрофенолята, пентахлорфенолята или пентафторфенолята,
обрабатывают избытком гидразина или гидразингидрата в водной, водно-органической или органической среде в атмосфере инертного газа, которым является азот или аргон, при температуре от -10 до 30°С, где органическая среда выбрана из группы, состоящей из метанола, этанола, ацетонитрила, диоксана, тетрагидрофурана, диметилформамида, диметилсульфоксида, а водно-органической средой является смесь органической среды с водой в любых соотношениях, с получением гидразида (II)
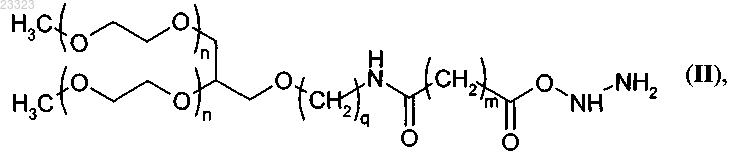
где n, q и m имеют указанные выше значения;
гидразид (II) выделяют экстракцией хлорированным растворителем, выбранным из группы, состоящей из дихлорметана, хлороформа, трихлорэтилена, тетрахлорида углерода, после чего осаждают диэтиловым эфиром и отфильтровывают;
гидразид (II) в среде хлористо-водородной кислоты при температуре 0-5°С обрабатывают водным раствором избытка нитрита щелочного или щелочно-земельного металла и после завершения реакции избыток азотистой кислоты удаляют прибавлением азида натрия.
3. Способ получения ПЭГ-агента по п.2, отличающийся тем, что активированный эфир (III) обрабатывают 1% водным раствором гидразингидрата при мольном соотношении гидразингидрата к эфиру (III), равном 6:1, пятикратно экстрагируют дихлорметаном, осаждают диэтиловым эфиром, отфильтровывают и дополнительно трижды переосаждают диэтиловым эфиром из раствора в изопропаноле; гидразид (II) в среде 0,5 М хлористо-водородной кислоты обрабатывают водным раствором нитрита натрия при мольном соотношении нитрита натрия к гидразиду (II), равном 10:1.
4. Способ получения пегилированного интерферона α-2b (IFN α-2b), характеризующийся тем, что активированный эфир (III)
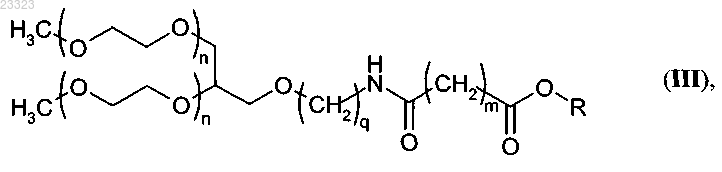
где O-R представляет собой остаток гидроксилсодержащего соединения, выбранный из N-гидроксисукцинимида, 4-нитрофенолята, 2,4-динитрофенолята, пентахлорфенолята или пентафторфенолята,
обрабатывают избытком гидразина или гидразингидрата в водной, водно-органической или органической среде в атмосфере инертного газа, которым является азот или аргон, при температуре от -10 до 30°С, где органическая среда выбрана из группы, состоящей из метанола, этанола, ацетонитрила, диоксана, тетрагидрофурана, диметилформамида, диметилсульфоксида, а водно-органической средой является смесь органической среды с водой в любых соотношениях, с получением гидразида (II)
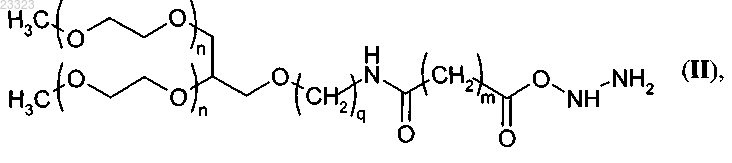
где n, q и m имеют указанные выше значения;
гидразид (II) выделяют экстракцией хлорированным растворителем, выбранным из группы, состоящей из дихлорметана, хлороформа, трихлорэтилена, тетрахлорида углерода, после чего осаждают диэтиловым эфиром и отфильтровывают;
гидразид (II) в среде хлористо-водородной кислоты при температуре 0-5°С обрабатывают водным раствором избытка нитрита щелочного или щелочно-земельного металла и после завершения реакции избыток азотистой кислоты удаляют прибавлением азида натрия с получением ПЭГ-агента общей формулы (I) по п.1;
к раствору IFN α-2b в фосфатном буфере с рН 8,0-8,7 при 0-5°С добавляют 4-5-кратный мольный избыток раствора ПЭГ-агента общей формулы (I);
по достижении степени превращения IFN α-2b 70-85% реакцию останавливают прибавлением избытка глицина;
реакционную смесь разбавляют в 5-15 раз, устанавливают значение рН 4,5-5,5, требуемое для хроматографического разделения продуктов на СМ-сефарозе, после чего проводят градиентное элюирование от 0,1 до 0,8 М NaCl;
отбирают фракции, которые анализируют обращенно-фазовой ВЭЖХ на содержание моно-ПЭГ-IFN α-2b, по результатам которого определяют целевые фракции, которые далее очищают до степени, достаточной для приготовления лекарственного препарата.
Текст
РАЗВЕТВЛЕННЫЙ АЦИЛАЗИДНЫЙ ПЕГИЛИРУЮЩИЙ АГЕНТ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ ПЕГИЛИРОВАННОГО ИНТЕРФЕРОНА Изобретение относится к фармацевтической промышленности, а именно к разветвлнному ацилазидному пегилирующему агенту, способному присоединяться к свободным аминогруппам белков с образованием амидной связи посредством реакции азидной конденсации, а также к способу его получения и способу пегилирования биологически активных белков, например,интерферонов. Изобретение обеспечивает способ получения разветвлнного ацилазидного пегилирующего агента и соответствующий способ пегилирования интерферонов (IFN), в частностиIFN -2b. Техническими результатами изобретения являются пегилирующий агент, способный присоединяться к свободным аминогруппам белков с образованием амидной связи посредством азидной конденсации, не вызывая рацемизации, окисления и/или агрегации субстрата, и способ его получения. Марков Илья Александрович,Маркова Елена Алексеевна, Гапонюк Полина Петровна, Маркова Инна Николаевна (RU), Гапонюк Петр Яковлевич (умер) Скибневский А.Ю. (RU) Область техники, к которой относится изобретение Изобретение относится к фармацевтической промышленности, а именно к пегилирующему агенту,способному присоединяться к свободным аминогруппам белков с образованием амидной связи посредством реакции азидной конденсации, а также к способу его получения и способу пегилирования биологически активных белков, например, интерферонов. Пегилированные интерфероны могут найти применение для приготовления противовирусных лекарственных средств. Предшествующий уровень техники Полиэтиленоксид (полиэтиленгликоль, ПЭГ) является широко распространенным полимером для ковалентной модификации (пегилирования) биологических макромолекул, например полипептидов, что имеет большое значение в современной медицине. Цель пегилирования - предотвращение деградации белков протеолитическими ферментами и защита от антигенных и иммуногенных эпитопов. Кроме того,пегилирование увеличивает размеры полипептидов, уменьшая почечную фильтрацию, а также изменяет объем биораспределения. Вс это способствует удлинению времени пребывания модифицированных физиологически активных белков в организме пациента, что повышает их ценность в качестве лекарственных средств. Молекула ПЭГ не способна непосредственно взаимодействовать с молекулами белков, поскольку не содержит реакционноспособных функциональных групп, которые могут реагировать с какими-либо функциональными группами протеинов. Поэтому в молекулу данного полимера требуется ввести такие реакционноспособные группы или их предшественники, которые переводят в активную форму незадолго до проведения реакции с белками. Наибольшее значение при пегилировании полипептидов имеет выбор пегилирующего агента и способа конъюгации, от которых зависит вид и структура конечного конъюгата, а следовательно, его биологическая активность, стабильность и время циркуляции в крови. Так, например, противовирусная активность пэгилированных интерферонов (ИНФ) в значительной степени зависит как от размера и геометрии молекулы ПЭГ, так и от места и способа присоединения полимера к молекуле белка, т.е. от функциональной группы ИНФ, с которой непосредственно взаимодействует соответствующий пэгилирующий агент (Roberts M.J. et al. "Chemistry for peptide and protein PEGylation". Adv. Drug Delivery Rev. Vol. 54. (2002), p. 459-476). Введение различных активных функциональных групп, способных взаимодействовать с функциональными группами протеинов в мягких условиях с получением соответствующих ковалентных конъюгатов, описано, в частности, Kozlowski A. et al. "Development of Pegylated Interferons for the Treatment ofChronic Hepatitis C". BioDrugs. No. 15(7) (2001). P. 419-429. Из химии пептидов (Гринштейн Дж., Виниц М. Химия аминокислот и пептидов. М.: Мир, 1965) известно, что при образовании амидной связи с оптически активными -аминокислотами, как правило, в той или иной мере наблюдается рацемизация субстрата, причем в наименьшей степени рацемизация наблюдается при использовании азидного метода, который заключается во взаимодействии ацилазида соответствующей защищенной аминокислоты или пептида со свободной аминогруппой соответствующего аминного субстрата. Основным недостатком ацилазидов является их низкая стабильность, ацилазиды получают из соответствующих стабильных гидразидов обработкой азотистой кислотой или ее эфирами непосредственно перед применением (Гершкович А., Кибирев В. Химический синтез пептидов. Киев:"Наукова Думка", 1992). В настоящее время известен достаточно широкий ассортимент линейных гидразидных производных ПЭГ, которые используются в качестве пегилирующих агентов непосредственно в гидразидной форме без переведения в ацилазид и применения азидной конденсации. Большинство подобных гидразидных производных ПЭГ вводят в реакцию с белками, имеющими карбоксильные фрагменты, активированные карбодиимидами. Недостатком такого способа конъюгации является побочная реакция взаимодействия активированных карбоксильных групп со свободными аминогруппами как между, так и внутри молекул протеинов, что приводит либо к слиянию белковых молекул в более крупные ковалентные агрегаты (межмолекулярное взаимодействие), либо к необратимому изменению конформации протеина (внутримолекулярное взаимодействие). Гидразидные производные разветвленного ПЭГ не находят значимого применения для модифицирования белков. В патенте ЕР 0605963 (опубл. 13.07.1994) раскрыты, в частности, гидразидные производные ПЭГ с молекулярной массой от 2 до 12 кДа, имеющие структуры: где Р представляет ПЭГ, а также способы их получения и применения. Указанными производными ПЭГ модифицируют, например, эритропоэтин, предварительно окисленный периодатом, с образованием гидразонной связи между полимерным и белковым доменами. В заявке US 20050118277 (опубл. 02.06.2005) описаны гидразидные соединения структурной формулы (I)R3-NH-NH-C(=O)-R2-P-R1,в которой Р представляет водорастворимый биоразлагаемый полимер с молекулярной массой от 250 до 50000 Да, R1 представляет водород, низший алкил, низший алкокси или -R2-C(=O)-NH-NH-R3, R3 представляет остаток естественной -L-аминокислоты или дипептида, обладающие ангиогенной активностью, которые получают взаимодействием дигидразида ПЭГ с соответствующими производными карбоновых кислот, активированных, например, 1-этил-3-(3-диметиламинопропил)карбодиимидом. Дигидразид ПЭГ получают обработкой полиэтиленгликоля (2 кДа) избытком фосгена, а затем Nгидроксисукцинимидом в присутствии триэтиламина. Полученный дисукцинимидилкарбонат ПЭГ переводят в дигидразид ПЭГ действием избытка гидразина. В заявке WO 1992/016555 (опубл. 01.10.1992) раскрыт ПЭГ-гидразид, который получают способом,включающим стадии (а) обработки монометоксиполиэтиленгликоля фосгеном с образованием ПЭГхлорформиата, (б) обработки полученного продукта избытком гидрохлорида этилового эфира -аланина в присутствии избытка триэтиламина с образованием этилового эфира ПЭГаланина и (в) обработки этилового эфира ПЭГаланина гидразином с образованием гидразида ПЭГаланина: или с углеводным фрагментом гликозилированного белка (Glycoprotein), окисленным периодатом, с последующим "закреплением" образовавшейся гидразонной связи восстановлением цианборогидридом натрия в соответствующий амин: Возможность применения указанного ПЭГ-агента в реакции азидной конденсации в известном изобретении не предполагается. Основными недостатками рассматриваемого пегилирующего агента является наличие относительно легко гидролизуемой карбаматной связи, и использование при получении ПЭГ-агента в качестве одного из промежуточных реагентов высокотоксичного фосгена. Кроме того, к недостаткам также можно отнести использование при конъюгации карбодиимида или периодата, которые вызывают ряд побочных реакций, например меж- и внутримолекулярное взаимодействие активированных карбоксильных групп с аминогруппами в белках, окисление и рацемизацию. К ПЭГ-агентам, взаимодействующим с протеином посредством азидной конденсации, относится,например, сшивающий ПЭГ-агент с молекулярной массой около 2,5 кДа, представляющий собой диацилазид полиэтиленгликоля, описанный в US 4101380 (опубл. 18.06.1978). Указанный агент получают непосредственно перед сшиванием белков из дигидразида ПЭГ, который, в свою очередь, получают обработкой дигликолята полиэтиленоксида тионилхлоридом с последующим гидразинолизом образовавшегося диацилхлорида. Данный сшивающий агент можно применять при получении белковых мембран, в частности, желатиновых и химотрипсиновых мембран. В патенте US 4179337 (опубл. 18.12.1979) описан ПЭГ-азид с молекулярной массой около 0,75 кДа,который получают из ПЭГ-гидразида обработкой нитритом натрия в солянокислом растворе при комнатной температуре непосредственно перед конъюгацией с уриказой. В свою очередь, ПЭГ-гидразид получают гидразинолизом метилового эфира ПЭГ-гликолевой кислоты, который образуется при взаимодействии полиэтиленгликоля с метиловым эфиром хлоруксусной кислоты в среде жидкого аммиака в присутствии металлического натрия. В заявке US 20060115450 (опубл. 01.06.2006) предложен ПЭГ-агент общей формулы (1) где R представляет углеводородную группу, имеющую от 1 до 24 углеродных атомов; ОА 1 и ОА 2 каждый представляет алкиленоксидную группу, имеющую от 2 до 4 углеродных атомов;m обозначает среднее число моль присоединнных алкиленоксидных групп и равно от 10 до 1000;Y обозначает линкер, представляющий собой простую эфирную, амидную, уретановую, сложноэфирную или карбонатную связь, вторичную аминогруппу или алкиленовую группу, включающую эти связи;X представляет функциональную группу, способную химически взаимодействовать с биологическими веществами, имеющую структуруZ представляет алкиленовую группу или алкиленовую группу, включающую простую эфирную или сложноэфирную связь, уретановую, амидную или карбонатную связь, вторичную аминогруппу. Гидразидные производные ПЭГ могут быть получены конденсацией карбоксильных производных ПЭГ с трет-бутоксикарбонилом гидразина (NH2-NH-Boc) в присутствии конденсирующих агентов, например дициклогексилкарбодиимида, 1-этил-3-(3-диметиламинопропил)карбодиимида или гексафторфосфата (бензотриазолилокси)-трис-(диметиламино)фосфония, с последующим удалением защитной группы. Данный ПЭГ-агент взаимодействует с альдегидной группой субстрата с образованием гидразонной связи: где Т обозначает остаточную группу биоактивного вещества. В качестве ближайшего аналога настоящего изобретения авторы рассматривают изобретение, раскрытое в заявке US 2006 0073113 (опубл. 06.04.2006), относящееся к разветвленным производным ПЭГ структурной формулы (1)m обозначает среднее число моль присоединнных алкиленоксидных групп и равно от 10 до 1000;X представляет функциональную группу, способную химически взаимодействовать с биологическими веществами, имеющую структуруZ представляет алкиленовую группу или алкиленовую группу, включающую простую эфирную или сложноэфирную связь, уретановую, амидную или карбонатную связь, вторичную аминогруппу. Гидразидные производные ПЭГ могут быть получены конденсацией карбоксильных производных ПЭГ с трет-бутоксикарбонилом гидразина (NH2-NH-Boc) в присутствии конденсирующих агентов, например дициклогексилкарбодиимида, 1-этил-3-(3-диметиламинопропил)карбодиимида или гексафторфосфата (бензотриазолилокси)-трис-(диметиламино)фосфония, с последующим удалением защитной группы. Имеется указание на возможность применения полученного ПЭГ-гидразида для образования гидразонной связи с белком, например, с интерфероном : где Т обозначает остаточную группу биоактивного вещества. Недостатком указанных выше аналогичных ПЭГ-агентов является невозможность их непосредственного конъюгирования с белками, такими как интерфероны, ввиду отсутствия в белках альдегидных групп. ПЭГ-агенты схожего строения могут образовывать белковые конъюгаты только после предварительного окисления гликозилированного домена, например периодатом, или целенаправленного введения формильной группы в полипептид, что ведет к непредсказуемому изменению активности субстрата и образованию побочных продуктов, например из-за меж- и внутримолекулярного образования дисульфидных связей в белках из тиолов цистеиновых фрагментов или меж- и внутримолекулярного взаимодействия формильных групп с тиолами или аминогруппами белка с образованием оснований Шиффа или тиоацеталей соответственно. Таким образом, техническими задачами настоящего изобретения являются разработка пегилирующих агентов, пригодных для получения стабильных производных белков, и расширение арсенала пегилирующих агентов и способов пегилирования биологически активных белков, например, интерферонов. Техническими результатами изобретения являются пегилирующий агент, способный присоединяться к свободным аминогруппам белков с образованием амидной связи посредством азидной конденсации,не вызывая рацемизации, окисления и/или агрегации субстрата, и способ его получения. Сущность изобретения В результате обширных исследований авторы установили, что выявленные недостатки известного уровня техники могут быть преодолены созданием и применением разветвлнного ацилазидного пегилирующего агента (ПЭГ-агента) общей формулы (I)m - целое число в интервале от 1 до 5. Изобретение также предоставляет способ получения разветвлнного ацилазидного пегилирующего агента (ПЭГ-агента) общей формулы (I)m - целое число в интервале от 1 до 5,характеризующийся тем, что активированный эфир (III) где O-R представляет собой остаток гидроксилсодержащего соединения, выбранный из Nгидроксисукцинимида, 4-нитрофенолята, 2,4-динитрофенолята, пентахлорфенолята или пентафторфенолята,обрабатывают избытком гидразина или гидразингидрата в водной, водно-органической или органической среде в атмосфере инертного газа, которым является азот или аргон, при температуре от -10 до 30 С, где органическая среда выбрана из группы, состоящей из метанола, этанола, ацетонитрила, диоксана, тетрагидрофурана, диметилформамида, диметилсульфоксида, а водно-органической средой является смесь органической среды с водой в любых соотношениях, с получением гидразида (II) где n, q и m имеют указанные выше значения; гидразид (II) выделяют экстракцией хлорированным растворителем, выбранным из группы, состоящей из дихлорметана, хлороформа, трихлорэтилена, тетрахлорида углерода, после чего осаждают диэтиловым эфиром и отфильтровывают; гидразид (II) в среде хлористо-водородной кислоты при температуре 0-5 С обрабатывают водным раствором избытка нитрита щелочного или щелочно-земельного металла и после завершения реакции избыток азотистой кислоты удаляют прибавлением азида натрия. В предпочтительном варианте осуществления способа получения ПЭГ-агента активированный эфир(III) обрабатывают 1% водным раствором гидразингидрата при мольном соотношении гидразингидрата к эфиру (III), равном 6:1, пятикратно экстрагируют дихлорметаном, осаждают диэтиловым эфиром, отфильтровывают и дополнительно трижды переосаждают диэтиловым эфиром из раствора в изопропаноле; гидразид (II) в среде 0,5 М хлористо-водородной кислоты обрабатывают водным раствором нитрита натрия при мольном соотношении нитрита натрия к гидразиду (II), равном 10:1. Далее изобретение обеспечивает способ получения пегилированного интерферона -2b (IFN -2b),характеризующийся тем, что активированный эфир (III) где O-R такой, как указано выше,обрабатывают избытком гидразина или гидразингидрата в водной, водно-органической или органической среде в атмосфере инертного газа, которым является азот или аргон, при температуре от -10 до 30 С, где органическая среда выбрана из группы, состоящей из метанола, этанола, ацетонитрила, диоксана, тетрагидрофурана, диметилформамида, диметилсульфоксида, а водно-органической средой является смесь органической среды с водой в любых соотношениях с получением гидразида (II) где n, q и m имеют указанные выше значения; гидразид (II) выделяют экстракцией хлорированным растворителем, выбранным из группы, состоящей из дихлорметана, хлороформа, трихлорэтилена, тетрахлорида углерода, после чего осаждают диэтиловым эфиром и отфильтровывают; гидразид (II) в среде хлористо-водородной кислоты при температуре 0-5 С обрабатывают водным раствором избытка нитрита щелочного или щелочно-земельного металла и после завершения реакции избыток азотистой кислоты удаляют прибавлением азида натрия; к раствору IFN -2b в фосфатном буфере с рН 8,0-8,7 при 0-5 С добавляют 4-5-кратный мольный избыток раствора ПЭГ-агента общей формулы (I); по достижении степени превращения IFN -2b 70-85% реакцию останавливают прибавлением избытка глицина; реакционную смесь разбавляют в 5-15 раз, устанавливают значение рН 4,5-5,5, требуемое для хроматографического разделения продуктов на СМ-сефарозе, после чего проводят градиентное элюирование от 0,1 до 0,8 М NaCl; отбирают фракции, которые анализируют обращено-фазовой ВЭЖХ на содержание моно-ПЭГ-IFN-2b, по результатам которого определяют целевые фракции, которые далее очищают до степени, достаточной для приготовления лекарственного препарата. Выражение "выбранный из группы, состоящей из" помимо индивидуальных альтернатив также включает возможные и рациональные комбинации двух или более таких альтернатив. Например, выражение "хлорированный растворитель, выбранный из группы, состоящей из дихлорметана, хлороформа,трихлорэтилена, тетрахлорида углерода" включает, в частности, смеси дихлорэтана и хлороформа, хлороформа и тетрахлорида углерода, ирихлорэтилена и тетрахлорида углерода. Пегилирующий агент (ПЭГ-агент) в соответствии с изобретением получают из соответствующего активированного эфира (II) в соответствии со схемой реакций где значения индексов n, q и m указаны выше;R-OH представляет гидроксилсодержащее соединение, выбранное из N-гидроксисукцинимида, 4 нитрофенола, 2,4-динитрофенола, пентахлорфенола или пентафторфенола. Активированные эфиры ПЭГ структуры (III) являются коммерчески доступными агентами. Получение соединения (II) включает обработку соответствующего активированного эфира (III) избытком гидразина или гидразингидрата в водной, водно-органической или органической среде. Реакцию ведут в атмосфере инертного газа, которым является азот или аргон, при температуре от -10 до 30 С. Органической средой является метанол, этанол, ацетонитрил, диоксан, тетрагидрофуран, диметилформамид, диметилсульфоксид или их смеси. Водно-органической средой является смесь органической среды с водой в любых соотношениях. Мольное соотношение гидразина или гидразингидрата к активированному эфиру (III) составляет от 5:1 до 30:1, предпочтительно оно составляет от 6:1 до 10:1. Гидразид (II) выделяют экстракцией хлорированным растворителем, которым может быть дихлорметан, хлороформ, трихлорэтилен, тетрахлорид углерода или их смеси, с последующим осаждением диэтиловым эфиром. Количество введенных гидразидных групп в (III) определяют спектрофотометрически в видимой области с реагентом 4-диметиламинобензальдегидом или нитритометрически. ПЭГ-агент (I) получают непосредственно перед конъюгацией с белком обработкой гидразида (II) избытком азотистой кислоты при пониженной температуре в интервале от -5 до 10 С. Источником азотистой кислоты является смесь нитрита щелочного или щелочно-земельного метала и кислоты, выбранной из серной, хлористо-водородной, бромисто-водородной, фосфорной, лимонной, уксусной или их смесей. Мольное соотношение азотистой кислоты к гидразиду (II) составляет от 10:1 до 50:1, предпочтительно оно составляет от 10:1 до 20:1. Количество азидных групп в полимере определяют, например, спектрофотометрически с реагентомFeCl3. По окончании реакции избыток азотистой кислоты удаляют добавлением азида щелочного металла,после чего, образовавшееся соединение (I) без выделения используют для конъюгации с белком. Конъюгацию осуществляют путем добавления раствора ПЭГ-азида (I) к раствору белка в нейтральном или слабощелочном буфере, выбранном из фосфатного, ацетатного, цитратного, боратного, карбонатного или их смесей. Далее изобретение проиллюстрировано предпочтительными примерами его осуществления, подтверждающими достижение технического результата. Сведения, подтверждающие возможность осуществления изобретения Пример 1. Получение ПЭГ-гидразида (II). В качестве гидроксисукцинимидного эфира (III) применяют диразветвлнные сукцимидилглутараты (в формуле (I) q=m=3, R=) с молярной массой 40 кДа (SUNBRIGHT GL2-400GS2) или 60 кДа (SUNBRIGHT GL2-600 GS2), выпускаемые фирмой NOF Corporation. В 30 мл охлажденного до 0 С 1% водного раствора гидразингидрата растворяют 100 мкмоль соответствующего гидроксисукцинимидного эфира (III). Смесь перемешивают 5 ч в атмосфере аргона при комнатной температуре, подкисляют 5% серной кислотой до рН 1-2 и 5-кратно экстрагируют дихлорметаном порциями по 30 мл. Органический слой промывают 10% сульфатом натрия до нейтральной реакции и высушивают над безводным сульфатом натрия в течение ночи. Высушенный дихлорметановый раствор ПЭГ-гидразида фильтруют, выпаривают при пониженном давлении, и продукт осаждают добавлением диэтилового эфира. Осадок отфильтровывают и трижды переосаждают диэтиловым эфиром из раствора в изопропаноле. Выход для обоих гидроксисукцинимидных эфиров (III) составляет 96-98%. Количество гидразидных групп в полимере по данным спектрофотометрического анализа составляет 98-101%. Пример 2. Получение ПЭГ-азида (I). К охлажденному до 0 С раствору 7 мкмоль гидразида ПЭГ-фенилаланина в 5 мл 0,5 М HCl приливают 70 мкмоль NaNO2 в 1 мл воды. Смесь перемешивают при охлаждении в течение 20 мин, далее избыток азотистой кислоты удаляют прибавлением 70 мкмоль NaN3 в 0,5 мл воды и сразу же используют для конъюгации с белком. Пример 3. Получение пегилированного интерферона -2b (IFN -2b). Раствор 7 мкмоль ПЭГ-азида (I), полученного в примере 2, приливают к охлажденному до 0-5 С раствору 1 мкмоль IFN -2b в фосфатном буфере с рН 8,5. Реакционную смесь при охлаждении перемешивают в течение 5 часов. Далее реакцию останавливают прибавлением избытка глицина. Реакционную смесь разбавляют в 10 раз, добавлением СН 3 СООН устанавливают рН 5,0 и наносят на СМ-сефарозу, предварительно уравновешенную 20 мМ ацетатным буфером с рН 5,0. После нанесения реакционной смеси сорбент промывают уравновешивающим буфером и далее градиентом от 0,1 до 0,8 МNaCl. Отобранные фракции анализируют обращено-фазовой ВЭЖХ на содержание моно-ПЭГ-IFN -2b. Целевые фракции объединяют и повторно анализируют, определяя чистоту и содержание монопэгилированного IFN -2b. Выход (в пересчете на IFN -2b) очищенного ПЭГ 40-IFN -2b составляет 42%, чистота составляет 98,1%; для очищенного ПЭГ 60-IFN -2b выход составляет 37%, чистота составляет 99,0%. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Разветвлнный ацилазидный пегилирующий агент (ПЭГ-агент) общей формулы (I)m - целое число в интервале от 1 до 5. 2. Способ получения разветвлнного ацилазидного пегилирующего агента (ПЭГ-агента) общей формулы (I)m - целое число в интервале от 1 до 5,характеризующийся тем, что активированный эфир (III) где O-R представляет собой остаток гидроксилсодержащего соединения, выбранный из Nгидроксисукцинимида, 4-нитрофенолята, 2,4-динитрофенолята, пентахлорфенолята или пентафторфенолята,обрабатывают избытком гидразина или гидразингидрата в водной, водно-органической или органической среде в атмосфере инертного газа, которым является азот или аргон, при температуре от -10 до 30 С, где органическая среда выбрана из группы, состоящей из метанола, этанола, ацетонитрила, диоксана, тетрагидрофурана, диметилформамида, диметилсульфоксида, а водно-органической средой является смесь органической среды с водой в любых соотношениях, с получением гидразида (II) где n, q и m имеют указанные выше значения; гидразид (II) выделяют экстракцией хлорированным растворителем, выбранным из группы, состоящей из дихлорметана, хлороформа, трихлорэтилена, тетрахлорида углерода, после чего осаждают диэтиловым эфиром и отфильтровывают; гидразид (II) в среде хлористо-водородной кислоты при температуре 0-5 С обрабатывают водным раствором избытка нитрита щелочного или щелочно-земельного металла и после завершения реакции избыток азотистой кислоты удаляют прибавлением азида натрия. 3. Способ получения ПЭГ-агента по п.2, отличающийся тем, что активированный эфир (III) обрабатывают 1% водным раствором гидразингидрата при мольном соотношении гидразингидрата к эфиру(III), равном 6:1, пятикратно экстрагируют дихлорметаном, осаждают диэтиловым эфиром, отфильтровывают и дополнительно трижды переосаждают диэтиловым эфиром из раствора в изопропаноле; гидразид (II) в среде 0,5 М хлористо-водородной кислоты обрабатывают водным раствором нитрита натрия при мольном соотношении нитрита натрия к гидразиду (II), равном 10:1. 4. Способ получения пегилированного интерферона -2b (IFN -2b), характеризующийся тем, что активированный эфир (III) где O-R представляет собой остаток гидроксилсодержащего соединения, выбранный из Nгидроксисукцинимида, 4-нитрофенолята, 2,4-динитрофенолята, пентахлорфенолята или пентафторфенолята,обрабатывают избытком гидразина или гидразингидрата в водной, водно-органической или органической среде в атмосфере инертного газа, которым является азот или аргон, при температуре от -10 до 30 С, где органическая среда выбрана из группы, состоящей из метанола, этанола, ацетонитрила, диоксана, тетрагидрофурана, диметилформамида, диметилсульфоксида, а водно-органической средой является смесь органической среды с водой в любых соотношениях, с получением гидразида (II) где n, q и m имеют указанные выше значения; гидразид (II) выделяют экстракцией хлорированным растворителем, выбранным из группы, состоящей из дихлорметана, хлороформа, трихлорэтилена, тетрахлорида углерода, после чего осаждают диэтиловым эфиром и отфильтровывают; гидразид (II) в среде хлористо-водородной кислоты при температуре 0-5 С обрабатывают водным раствором избытка нитрита щелочного или щелочно-земельного металла и после завершения реакции избыток азотистой кислоты удаляют прибавлением азида натрия с получением ПЭГ-агента общей формулы (I) по п.1; к раствору IFN -2b в фосфатном буфере с рН 8,0-8,7 при 0-5 С добавляют 4-5-кратный мольный избыток раствора ПЭГ-агента общей формулы (I); по достижении степени превращения IFN -2b 70-85% реакцию останавливают прибавлением избытка глицина; реакционную смесь разбавляют в 5-15 раз, устанавливают значение рН 4,5-5,5, требуемое для хроматографического разделения продуктов на СМ-сефарозе, после чего проводят градиентное элюирование от 0,1 до 0,8 М NaCl; отбирают фракции, которые анализируют обращенно-фазовой ВЭЖХ на содержание моно-ПЭГIFN -2b, по результатам которого определяют целевые фракции, которые далее очищают до степени,достаточной для приготовления лекарственного препарата.
МПК / Метки
МПК: C07K 14/715, A61K 47/48
Метки: способ, разветвленный, интерферона, ацилазидный, получения, агент, пегилирующий, пегилированного
Код ссылки
<a href="https://eas.patents.su/10-23323-razvetvlennyjj-acilazidnyjj-pegiliruyushhijj-agent-sposob-ego-polucheniya-i-sposob-polucheniya-pegilirovannogo-interferona.html" rel="bookmark" title="База патентов Евразийского Союза">Разветвленный ацилазидный пегилирующий агент, способ его получения и способ получения пегилированного интерферона</a>
Предыдущий патент: Производные гетероарилпиперидина и -пиперазина в качестве фунгицидов
Следующий патент: Мобильный комплекс для размещения радиоэлектронных средств
Случайный патент: Уплотнительный прокладочный материал (варианты)












