Способ прогнозирования резерва яичника в ответ на индукцию овуляции и набор для его осуществления
Формула / Реферат
1. Способ прогнозирования резерва яичника в ответ на индукцию овуляции у субъекта, который нуждается в индукции овуляции, включающий:
(a) определение уровня Мюллеровой ингибирующей субстанции (MIS) в сыворотке у субъекта;
(b) сравнение определенного сывороточного уровня MIS со стандартом, в котором коррелируют уровень MIS в сыворотке с числом ооцитов, полученных после индукции овуляции; и
(c) прогнозирование ожидаемого ответа яичника.
2. Способ по п.1, где резерв яичника определяют во время индукции овуляции.
3. Способ по п.1, где резерв яичника определяют до индукции овуляции.
4. Способ по п.1, который дополнительно включает оценку риска гиперстимуляции яичника из-за индукции овуляции.
5. Способ по п.1, где риск гиперстимуляции яичника оценивают во время индукции овуляции.
6. Способ по п.4, где риск гиперстимуляции яичника оценивают до индукции овуляции.
7. Набор для использования в способе по п.1, который содержит антитело для определения уровней MIS в сыворотке субъекта и обеспечивает корреляцию уровня MIS в сыворотке и числа зрелых ооцитов, обнаруженных после индукции овуляции.
Текст
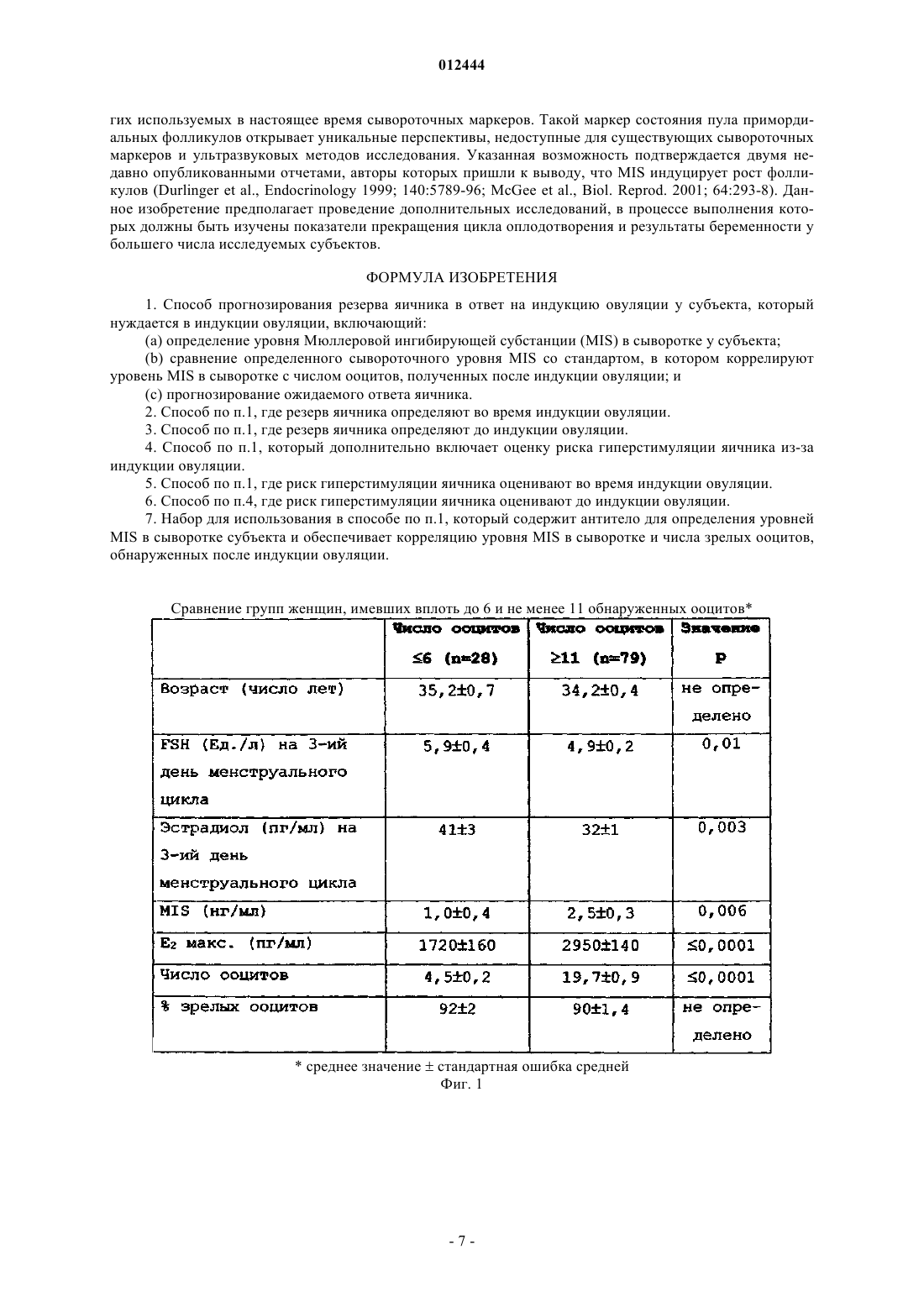
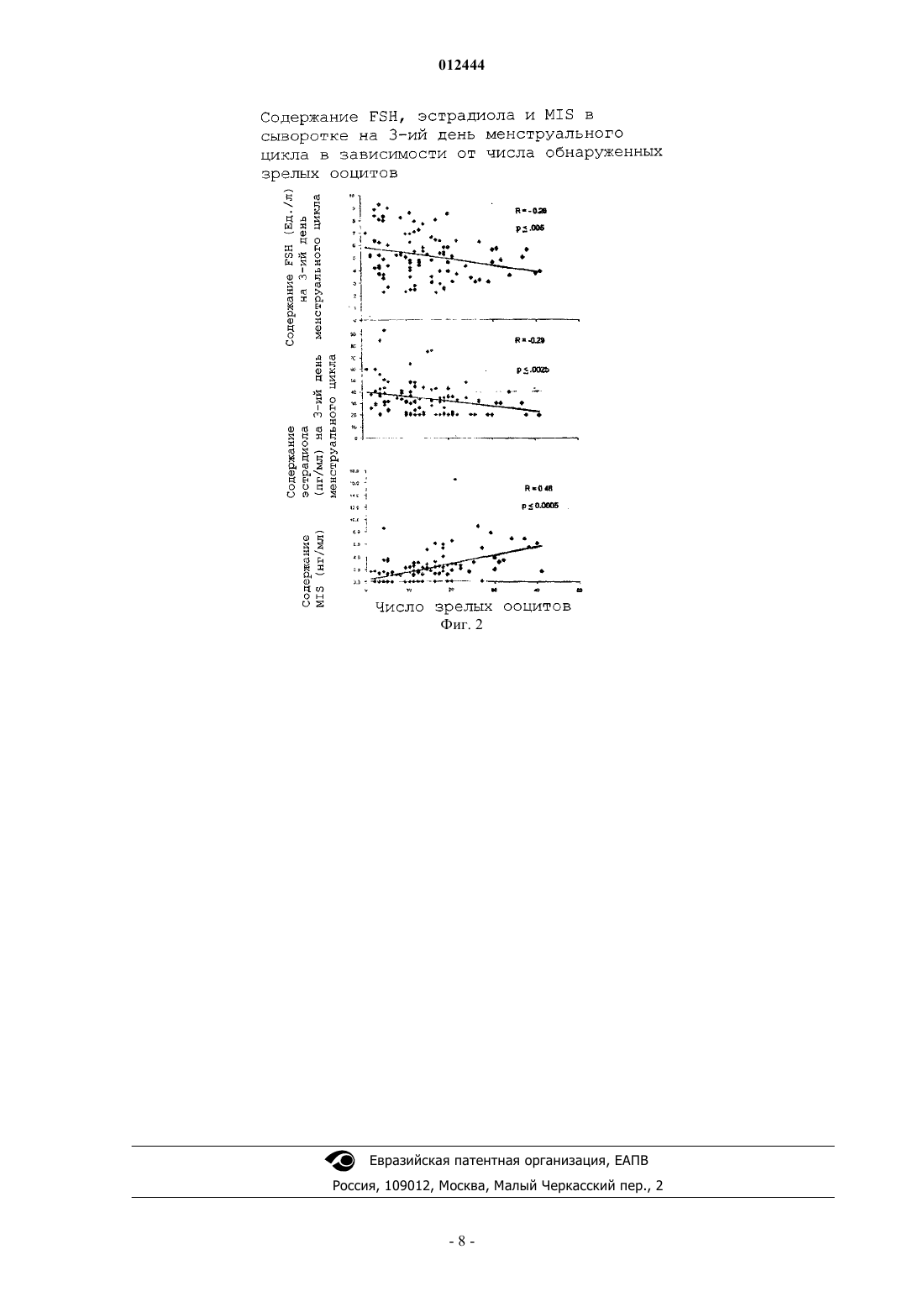
012444 Права правительства Настоящее изобретение сделано при частичной поддержке Национальных институтов здравоохранения на основании гранта под номером AG15425. Правительство имеет определенные права на данное изобретение. Перекрестные ссылки на родственные заявки Настоящая заявка на патент притязает на приоритет предварительной заявки на патент США 60/313545, поданной 20 августа 2001 г., которая полностью включена в данное описание изобретения в качестве ссылки. Область техники Настоящее изобретение относится к методам репродукции, биологии развития и молекулярной биологии, а также к оценке репродуктивного статуса женщин. В частности, данное изобретение относится к новым способам прогнозирования и контроля реакции женщины на лечение бесплодия, а также предотвращения у нее истощения резерва яичника. Предпосылки изобретения По тексту всей заявки и в конце описания изобретения приведены ссылки на различные публикации или патенты, в которых описан уровень техники в области, к которой относится данное изобретение. Все указанные публикации или патенты включены в данное описание изобретения в качестве ссылки. Бесплодие является заболеванием, в результате которого происходит нарушение функционирования репродуктивной системы человека. Указанное заболевание определяется как неспособность женщины забеременеть после одного года незащищенных половых сношений или неспособность сохранить беременность до рождения живого ребенка. По данным Центров по контролю за заболеваниями (СОС) 2,1 миллиона супружеских пар страдают бесплодием или имеют другие нарушения, которые делают их неспособными иметь детей, при этом в США бесплодными являются 6,1 миллиона женщин детородного возраста. Фертильность женщины начинает уменьшаться за много лет до наступления менопаузы несмотря на регулярные овариальные циклы. Хотя нет точного определения лучшего репродуктивного возраста у женщин, бесплодие чаще возникает после 35 лет. За последние тридцать лет средний возраст женщин,рожающих детей, существенно увеличился в связи с тем, что все больше женщин стремятся получить высшее образование и сделать карьеру, прежде чем завести семью, поэтому ко времени вступления в брак беспрецедентно большое число женщин достигает позднего репродуктивного возраста. Поэтому многие женщины нуждаются в лечении бесплодия, чтобы родить ребенка. Так как женщины готовы тратить тысячи долларов, желая осуществить свою мечту о полноценной семье, бесплодие стало прибыльной отраслью, ежегодно приносящей в США 2 миллиарда долларов. За исключением донорства ооцитов все применяемые в настоящее время методы лечения бесплодия у женщин, неспособных забеременеть естественным путем, зависят от резерва яичника женщины. Термин "резерв яичника" означает текущее наличие фолликулов в яичнике женщины и качество ооцитов и тесно связан с репродуктивным потенциалом. Как правило, чем больше число оставшихся яйцеклеток,тем выше вероятность оплодотворения. И наоборот, низкий резерв яичника существенно уменьшает шансы женщины на оплодотворение. С возрастом у женщины постепенно уменьшается количество яйцеклеток до полного их исчезновения ко времени наступления менопаузы. Еще до рождения количество яйцеклеток начинает уменьшаться. Большая часть ооцитов пропадает после пяти месяцев внутриутробной жизни, когда по научным данным максимальное число яйцеклеток составляет примерно семь миллионов. Во время рождения оба яичника содержат примерно один миллион примордиальных фолликулов. В начале репродуктивного периода при менархе насчитывается примерно 0,5 миллиона примордиальных фолликулов. Затем количество фолликулов уменьшается с постоянной скоростью, равной примерно 1000 фолликулов в месяц, причем указанный процесс ускоряется после 35 лет. Количество яйцеклеток продолжает уменьшаться по мере старения женщины, пока полностью не исчерпывается при наступлении менопаузы. Наиболее важным аспектом уменьшения резерва яичника и сопутствующего сокращения репродуктивного потенциала является то, что указанный процесс возникает у разных женщин в разное время. Функция яичника является весьма индивидуальной у каждой женщины как с точки зрения возраста максимальной репродуктивной активности, так и начала ослабления данной активности. Некоторые женщины с нормальными менструальными циклами не могут забеременеть уже в возрасте около тридцати лет. Из-за высокой индивидуальной изменчивости состояния яичника клиницистам жизненно важно оценить резерв яичника у бесплодной женщины. Оценка резерва яичника действительно является одним из наиболее важных факторов при определении причин бесплодия у женщин любого возраста. Женщины с пониженным резервом яичника хуже реагируют на индукцию овуляции, требуют больших доз гонадотропина, у них чаще наблюдается прекращение цикла оплодотворения in vitro (IVF) и реже наступает беременность в результате IVF. Применяемые в настоящее время методы оценки резерва яичника можно разделить на пассивные и на динамичные тесты. Целью обоих подходов является получение информации о качестве и количестве ооцитов, необходимой для назначения женщине определенного курса лечения от бесплодия. Стандарт-1 012444 ный пассивный тест резерва яичника включает измерение предельного количества фолликулостимулирующего гормона (FSH) и эстрадиола в сыворотке на 3-й день менструального цикла. На ранней стадии развития фолликула уровни FSH менее 10 м.Ед./мл и эстрадиола менее 80 пг/мл обычно считаются показателями нормального резерва яичника, хотя в научной литературе сообщалось о предельных значениях для FSH, равных 20-25 м.Ед./мл, вследствие использования при анализе FSH разных эталонов. Трудно установить абсолютные значения для уровней FSH из-за расхождений в лабораторных оценках и методах обработки. Кроме того, у женщин, имеющих предельно допустимые значения в нормальном диапазоне,могут быть низкие резервы яичника, и к тому времени, когда становится очевидным повышение уровняFSH, беременность уже может не наступить или лечение бесплодия может оказаться безуспешным. Некоторые женщины с нормальным уровнем FSH могут совершенно не знать о постоянном сокращении резерва яичника и пребывать в ложной уверенности относительно своих перспектив на создание полноценной семьи. Другие пассивные тесты резерва яичника находятся в процессе исследования и еще не были рекомендованы для клинического применения из-за ограниченного количества данных, подтверждающих их прогностическую ценность. В отличие от статических измерений резерва яичника тест на стимуляцию кломифенцитратом (СССТ) представляет динамичный подход. Данный анализ стимулирует продуцирование яичником яйцеклеток под действием кломифена, представляющего лекарственное средство от бесплодия. Хотя тест на стимуляцию кломифенцитратом считается более точным, чем тест на предельный уровень FSH в сыворотке, ни один из применяемых в настоящее время тестов не дает точного представления о резерве яичника. Таким образом, очевидно, что существует потребность в более точных и надежных способах прогнозирования и контроля реакции женщины на лечение бесплодия. Кроме того, в области методов репродукции весьма желателен новый способ, позволяющий предотвратить сокращение резерва яичника. Краткое описание чертежей На фиг. 1 показано сравнение двух групп женщин, у которых обнаружено до 6 и 11 и более ооцитов. Женщины в двух группах были одного возраста, при этом у них существенно не отличались значения FSH на 3-й день менструального цикла. Однако содержание мюллеровой ингибирующей субстанции(MIS) в сыворотке у женщин в группе с числом ооцитов 11 и более было в 2,5 раза выше, чем в группе женщин, у которых было обнаружено менее 6 ооцитов. Таким образом, уровни MIS в сыворотке имеют положительную корреляцию с числом продуцированных зрелых ооцитов и являются полезным показателем резерва яичника. На фиг. 2 показаны уровни FSH, эстрадиола и MIS на 3-й день менструального цикла в зависимости от числа выделенных зрелых ооцитов. Значения р подтверждают значимость указанных взаимосвязей и показывают, что наибольшая корреляция с числом ооцитов достигается при определении концентрацииMIS в сыворотке. Подробное описание изобретения В настоящее время существует большая потребность в сывороточных маркерах, позволяющих точно определить состояние резерва яичника женщины. Существующие сывороточные маркеры, используемые для определения резерва яичника, включают комбинированное исследование косвенно опосредующего гормона (FSH) и ряда прямо опосредующих гормонов, таких как эстрадиол (Е 2) или ингибин В(Sharara et al., Am J. Obstet. Gynecol. 1998; 179:804-812). На ранней стадии развития фолликула уровеньFSH в сыворотке отражает активность смеси гормонов яичника (Е 2, ингибины, активины, фоллистатины), которые образуют обратную связь с гипоталамусом и гипофизом. Эстрадиол секретируют в основном зернистые клетки в преантральных и антральных фолликулах. Ингибин В секретируется непосредственно зернистыми клетками в мелких антральных фолликулах. Ингибин А представляет продукт лютеинизированных зернистых клеток доминантного фолликула и желтого тела, который влияет на уровниFSH в сыворотке на ранней стадии развития фолликула благодаря его присутствию при переходе из желтого тела в фолликул. Таким образом, очевидно, что еще одним недостатком сывороточных маркеров,применяемых в настоящее время в клинической практике, является то, что они в основном отражают развитие FSH-зависимого фолликула от раннего антрального до преовуляторного состояния. Помимо трудностей, связанных с получением клинически обоснованных показателей и уменьшением расхождений результатов лабораторных анализов, существующие сывороточные маркеры, получаемые на основе развития FSH-зависимого доминантного фолликула, имеют ограниченное значение для оценки находящихся в состоянии покоя резервов яичниковых фолликулов. Более точная оценка резерва яичника обязательно включает определение числа находящихся в покое FSH-независимых примордиальных яичниковых фолликулов. Находящиеся в покое примордиальные яичниковые фолликулы постоянно пополняют пул растущих фолликулов в яичнике на протяжении всей жизни. Результаты исследований с использованием животных показывают, что число утраченных фолликулов обратно пропорционально числу примордиальных фолликулов, имеющихся в яичниках(Hirshfield A.N., Biol. Reprod. 1994; 50:421-428). После стимуляции роста фолликулов они могут достичь полной зрелости и овулировать или погибнуть в результате атрезии. Установлено, что развитие фолликула от первичной стадии до ранней антральной стадии происходит у человека в течение нескольких месяцев, и развитие фолликула от ранней антральной до преовуляторной стадии занимает примерно три-2 012444 месяца. Чтобы определить возможность женщины забеременеть в пределах обычного курса лечения от бесплодия (от нескольких месяцев до нескольких лет), гораздо важнее получить обоснованные данные о величине пула примордиальных фолликулов, чем оценивать небольшое число фолликулов, которые в данный момент быстро достигают зрелости и будут утрачены в ходе процессов, сопутствующих овуляции в текущем менструальном цикле. Мюллерова ингибирующая субстанция (MIS) является компонентом фолликулярной жидкости,продуцируемой зернистыми клетками (Vigier et al., Endocrinology, 1984; 114:1315-20; Takahashi et al.,Biol. Reprod., 1986; 35:447-53; Bezard et al., J. Reprod. Fertil., 1987; 80:509-16; Rajpert-De Metys et al., J.Clin. Endocrinol. Metab. 1999; 84:3836-44), и появляется в сыворотке человека в начале пубертатного возраста, сохраняется во взрослом состоянии и исчезает при наступлении менопаузы (Hudson et al., J. ClinEndocrinol Metab. 1990; 70:16-22; Josso et al., J. Clin Endocrinol Metab. 1990; 70:23-7; Lee et al., J. Clin. Endocrinol. Metab. 1996; 81:571-6). Как последовательности ДНК, так и белковые последовательности MIS хорошо известны в данной области (Lee and Donahoe, Endocrine Reviews 1993; 14(5):152-164; Cate et al.,Cell, 1986; 45:685-689). Уровни MIS незначительно изменяются во время менструального цикла (Cook etal., Fertil Steril 2000; 73:859-61), достигая максимума на поздней стадии образования фолликула. Уровни MIS в фолликулярной жидкости были измерены у женщин, проходивших обследование на возможность оплодотворения in vitro, в результате чего было обнаружено присутствие указанной субстанции в преовуляторных фолликулах женщин с высоким потенциалом овуляции (Seifer et al., J. Clin.Teixeira et al., Endocrinology 1996; 137: 160-5), причем MIS, по-видимому, действует подобно паракринной индукции, регулируя функцию зернистых клеток и ооцитов (Takahashi et al., Mol Cell Endocrinol 1986; 47:225-34; Kim et al., J. Clin. Endocrinol. Metab. 1992; 75:911-7; Seifer et al., J. Clin. Endocrinol. Metab. 1993; 76:711-4). Недавно выполненное исследование с использованием мышей, лишенных MIS, показало, что самки мышей, у которых отсутствует MIS, а также самки мышей, гетерозиготные в отношении мутации на отсутствие MIS, характеризуются относительно ранним истощением пула примордиальных фолликулов (Durlinger et al., Endocrinology 1999; 140: 5789-96). Полученные результаты подтверждают роль MIS в качестве регулятора рекрутинга примордиальных фолликулов и позволяют предположить,что секреция MIS отображает величину примордиального пула. Сывороточный маркер, являющийся показателем примордиального пула покоящихся FSH-независимых фолликулов до их инициации, должен быть очень полезен для прогнозирования возможной реакции яичника на лекарственные препараты, индуцирующие овуляцию, применяемые во время подготовки к циклу методов стимулируемой репродукции. Таким образом, настоящее изобретение относится к новому способу определения взаимосвязи (корреляции) уровней MIS в сыворотке и резерва яичника, а также к новым способам прогнозирования реакции яичника у женщин, подвергаемых индуцированной овуляции, в качестве составной части цикла методов стимулируемой репродукции (ART). Способы по данному изобретению позволяют клиницисту точно прогнозировать, какие женщины будут хорошо реагировать и какие женщины будут плохо реагировать на современные методы лечения бесплодия. Синдром гиперстимуляции яичника (OHSS) характеризуется рядом нарушений от незначительных до тяжелых и даже потенциально угрожающих жизни пациента. OHSS часто сопровождается такими симптомами, как сильные боли в области таза, вздутие живота, увеличение яичника, гемоконцентрированные асциты, экссудативный плеврит или перикардит либо то и другое вместе, почечная недостаточность, олигурия, гиперкальциемия и гиперкоагуляция. Указанный синдром часто возникает вследствие введения экзогенных гонадотропинов. Измеряя уровни MIS, клиницист может принять обоснованное решение о введении hCG во избежание риска гиперстимуляции яичника. Другим методом предотвращения синдрома гиперстимуляции яичника, известным как криоконсервация, является замораживание эмбрионов вместо переноса их в яичник женщины. При помощи способов по данному изобретению беременность можно отсрочить и сократить введение hCG до минимума до тех пор, пока не будет устранен риск гиперстимуляции яичника вследствие избытка hCG. Способы по настоящему изобретению можно применять для получения результатов, позволяющих прогнозировать хорошую, среднюю или плохую реакцию на лечение бесплодия. Таким образом, указанные способы весьма пригодны для применения в клинических условиях для определения оптимальной дозы лекарственных средств от бесплодия, назначаемых женщинам, проходящим курс лечения с целью оплодотворения in vitro (IVF). Клиники, занимающиеся оплодотворением in vitro, обычно полагаются на возраст пациента в качестве единственного показателя для определения назначаемой дозы лекарственных средств от бесплодия. Однако возраст является неспецифическим и ненадежным показателем реакции яичника, и настоящее изобретение представляет значительное усовершенствование по сравнению с применяемыми в настоящее время диагностическими средствами. Способы по настоящему изобретению можно применять для обследования всех пациентов до назначения лечения IVF с целью выявления женщин с плохой реакцией, что позволит сократить число неудачных попыток, а также для выявления женщин с повышенной реакцией, что позволит уменьшить риск гиперстимуляции. Таким образом, данное-3 012444 изобретение позволяет регулировать режим стимуляции яичника для компенсации недостаточного резерва яичника у женщин, у которых обнаружена средняя реакция. Одним объектом данного изобретения является способ определения взаимосвязи (корреляции) уровней MIS в сыворотке и резерва яичника. Для корреляции уровней MIS и резерва яичника определяют число ооцитов и уровни MIS в сыворотке у конкретного субъекта и выбирают графическое представление для полученных данных. В данной области хорошо известны методы выполнения эффективного анализа и представления данных. Такие методы включают использование статистических методов для анализа данных и оценки ошибок и применение компьютеров для выполнения указанных методов и других методов анализа. Кроме того, графическое представление данных и функций может включать использование таблиц, графиков и других диаграмм, а также компьютерных программ для выполнения вычислений и построения диаграмм, графиков и таблиц. Другим объектом настоящего изобретения является способ оценки резерва яичника у женщины, направляемой на лечение от бесплодия, путем определения уровня MIS в сыворотке и сравнения установленного уровня с данными, позволяющими коррелировать уровень MIS в сыворотке с числом обнаруженных зрелых ооцитов. Типичным примером представления данных корреляции уровней MIS в сыворотке и числа обнаруженных зрелых ооцитов является диаграмма, показанная на фиг. 2. Определяя уровень MIS в сыворотке и коррелированное значение обнаруженных ооцитов, можно достоверно оценить резерв яичника женщины и выбрать соответствующую схему лечения бесплодия. Родственным объектом данного изобретения является диагностический набор для определения резерва яичника у женщины путем измерения уровня MIS в сыворотке и корреляции полученного уровняMIS с эмпирическим значением обнаруженных зрелых ооцитов при помощи статистических данных,представленных на графике, показанном на фиг. 2. Уровень MIS в сыворотке можно измерить при помощи моноклональных или поликлональных антител, специфичных для MIS, и реагентов для меченияMIS-специфичных антител. Кроме того, для определения уровней MIS можно использовать рецепторMIS и выделенные из него пептиды. Указанный набор может дополнительно включать инструкции по его применению. Другим предпочтительным вариантом осуществления изобретения является способ прогнозирования реакции яичника женщины на индукцию овуляции путем определения уровня MIS в сыворотке данной женщины и сравнения установленного уровня со стандартным уровнем, благодаря чему можно прогнозировать реакцию яичника на индукцию овуляции. Родственный вариант осуществления настоящего изобретения относится к набору для прогнозирования реакции яичника на индукции овуляции. Указанный набор включает такие реагенты, как моноклональные и поликлональные антитела, специфичные дляMIS, и вещества для мечения, необходимые для определения уровня MIS в сыворотке, а также диаграмму для корреляции любого конкретного уровня MIS в сыворотке и возможного числа зрелых ооцитов. Указанный набор может далее включать инструкции по его применению и интерпретации полученных данных. Настоящее изобретение относится к набору для измерения уровней MIS в сыворотке у женщины в качестве прогностического индикатора реакции яичника на гиперстимуляцию и способу применения указанного набора. В данном наборе и способе его применения могут быть использованы моноклональные и/или поликлональные антитела к MIS в качестве диагностических реагентов для измерения физиологических уровней MIS, представляющих прогностический индикатор числа ооцитов и, что очень важно, качества ооцитов. Чем больше концентрация эндогенной MIS, продуцируемой в организме женщины,тем выше ее репродуктивный потенциал, если повышенные уровни MIS положительно коррелируют с репродуктивным потенциалом. См. фиг. 1 и 2. Определения терминов Термины, используемые в настоящем изобретении, имеют одинаковые значения как в описании изобретения, так и в формуле изобретения. В используемом здесь значении термин "MIS" означает мюллерову ингибирующую субстанцию,принадлежащую любому виду животных, включая мышей, крупный рогатый скот, овец, свиней, лошадей, птиц и предпочтительно человека, которая имеет нативную последовательность или созданную методами генетической инженерии и получена из любого источника, в частности, природного, синтетического или созданного методами рекомбинантных ДНК. Термин "парентеральный" означает введение полипептида внутривенным, внутриартериальным,внутрибрюшинным, внутримышечным, внутрижелудочковым, внутричерепным, подкожным, чрезвлагалищным, пероральным, назальным или ректальным способами. Термин "терапевтически эффективная доза" означает дозу, вызывающую эффект, для достижения которого вводят указанную дозу. Термин "паракринная индукция" означает форму передачи сигнала, когда клетка-мишень близко расположена от индуцирующей сигнал клетки. В используемом здесь значении термин "ооцит" означает гамету, образующуюся из фолликула самки животного. Термин "антитела" в используемом здесь значении означает поликлональные и моноклональные-4 012444 антитела, химерные, одноцепочечные и гуманизированные антитела, а также Fab-фрагменты, включая продукты библиотеки Fab-фрагментов и других экспрессируемых иммуноглобулинов. Термин "моноклональные антитела" означает, по существу, гомогенные популяции антител к определенному антигену. Моноклональные антитела могут быть получены любым методом, позволяющим продуцировать молекулы антител стабильными клеточными линиями в культуре. Моноклональные антитела могут быть получены методами, известными специалистам в данной области. См., например, Kohleret al., Nature 256:495-497, 1975, и патент США 4376110. Термин "поликлональные антитела" означает гетерогенные антитела, продуцированные разными лимфоцитами В в ответ на один и тот же антиген, причем разные антитела в данной группе узнают разные части антигена. Термин "гонадотропины" означают группу гликопротеиновых гормонов из передней доли гипофиза. Гонадотропины стимулируют рост гонад и секрецию половых гормонов. Примеры гонадотропинов включают наряду с прочими такие вещества, как фолликулостимулирующий гормон (FSH), лютеинизирующий гормон (LH), хорионический гонадотропин (hCG). Термины "стандарт" или "стандартный уровень" в используемом здесь значении означают концентрацию MIS, определенную в результате снятия нескольких показаний, предпочтительно статистически значимого числа показаний, как показано на фиг. 2. Стандарт может быть установлен произвольно в зависимости от степени точности определяемого показания выше или ниже стандарта. Примеры Нижеследующие примеры приведены для лучшей иллюстрации изобретения, описанного в формуле изобретения, и не должны ограничивать объем данного изобретения. Все конкретные вещества приведены только с целью иллюстрации и не ограничивают объем данного изобретения. Пример 1. Образцы сыворотки, полученные на 3-й день менструального цикла и хранившиеся при -80 С в период с марта 1999 по март 2001 г., оттаивали и анализировали в серии экспериментов на содержаниеMIS. Для анализа использовали по одному образцу сыворотки, полученной у 107 женщин, которых в течение 2 месяцев подвергали гипофизарной десенсибилизации лейпролидацетатом (Lupron; TAP Pharmaceuticals, North Chicago, IL) с последующей стимуляцией гонадотропином в составе препарата для оплодотворения in vitro (IVF). Метод стимуляции был аналогичен методам, описанным в предыдущей публикации (Seifer et al., J. Clin. Endocrinol. Metab. 1993; 76:711-4). Для стимуляции гонадотропином почти всегда использовали фолликулостимулирующий гормон. Введение лейпролидацетата иногда прекращали после начала введения гонадотропинов. В двух исследованных группах было получено 28 образцов у женщин, имевших 6 и менее ооцитов (диапазон 1-6 ооцитов), и 79 образцов у женщин, имевших 11 и более ооцитов (диапазон 11-44 ооцита). Критерии отбора, соответствующие 6 и менее и 11 и более ооцитам, были выбраны произвольно с тем, чтобы усилить потенциальные физиологические различия между группами женщин с разной реакцией яичника. Сыворотка женщин с повышенным уровнем FSH (более 10 Ед./л) была исключена из исследования, чтобы определить, взаимосвязана ли концентрация MIS в сыворотке на 3-й день менструального цикла с числом ооцитов, обнаруженных в "нормальном" диапазоне значений FSH в сыворотке на 3-й день менструального цикла. Фолликулы с диаметром не менее чем 18 мм отсасывали у пациентки,которой вводили седативный препарат, через 36 ч после инъекции hCG. Данное исследование не подлежало утверждению медицинским советом, так как образцы сыворотки хранили в качестве гарантии качества лабораторных исследований, и поэтому они считались клинически отработанным материалом. Пример 2. Анализ ELISA мюллеровой ингибирующей субстанции Анализ ELISA, используемый для измерения содержания MIS человека, хорошо описан в научной литературе (Hudson et al., J. Clin. Endocrinol. Metab. 1990; 70:16-22; Lee et al., J. Clin Endocrinol. Metab. 1996; 81:571-6). Образцы анализировали в двух копиях в виде шести серийных разведений; приведенные результаты представляют среднее значение для трех разведений, соответствующих линейной части стандартной кривой, построенной путем подбора логистической кривой по четырем параметрам при помощи программы DeltaSoft II (BioMetallics, Inc., Princeton, NJ). Чувствительность данного анализа равна 0,5 нг/мл; коэффициенты вариации внутри анализа и между анализами равны соответственно 9% и 15%. Анализ ELISA, служащий для определения MIS, не позволяет распознавать LH, FSH, активин, ингибин или TGF- и не вызывает перекрестной реакции с MIS крупного рогатого скота или грызунов (Hudson etal., J. Clin. Endocrinol. Metab. 1990; 70:16-22). Пример 3. Статистический анализ Показатели, полученные для сыворотки, во всех случаях выражены в виде среднего значениястандартная ошибка средней (SЕМ). Анализ на основании непарного t-критерия, выполненный при помощи программы StatView (Abacus Concepts, Inc., Berkeley, CA), был использован для выявления различий между сравниваемыми группами на статистически значимом уровне. Различия со значениями р 0,5 были признаны статистически значимыми. Корреляцию между данными содержания MIS и FSH, Е 2, числом обнаруженных ооцитов и числом обнаруженных зрелых ооцитов производили путем построения-5 012444 линейных кривых в соответствии с данными, приведенными на линейных осях. Наклоны полученных линий проверяли на наличие статистически значимых отличий от нуля, используя для этой цели значения р из таблиц критических значений для соответствующих коэффициентов корреляции. Результаты Результаты сравнения среднего возраста женщин, содержания FSH, Е 2, MIS, максимальных концентраций Е 2 цикла стимуляции и числа ооцитов у женщин, имевших 6 и менее ооцитов, и у женщин, имевших 11 и более обнаруженных ооцитов, суммированы в табл. 1. Средний возраст женщин в обеих группах был одинаковым. Хотя среднее значениестандартная ошибка средней для FSH (5,9 Ед./л 0,4 по сравнению с 4,9 Ед./л 0,2) и среднее значение Е 2 (41 пг/мл 3 по сравнению с 32 пг/мл 1) в сыворотке на 3-й день менструального цикла отличались на статистически значимом уровне (соответственно р=0,01 и р=0,003), соответствующие значения различий не были клинически значимыми. Максимально достигаемые уровни Е 2 были значительно выше в группе с большим числом ооцитов (2950 пг/мл 140 по сравнению с 1720 пг/мл 160; р 0,0001). Средние концентрации MIS составляли 1,0 нг/мл 0,4 по сравнению с 2,5 нг/мл 0,3, что указывает на более чем 2,5 кратную разницу концентрации MIS (р=0,006) в исследованных группах (табл. 1). Корреляция между содержанием MIS в сыворотке и другими измерениями функции яичника свидетельствует о статистически значимой обратной взаимосвязи между MIS, Е 2 (r=-0,169, р 0,05) и FSH (r=0,295, р 0,005) на 3-й день менструального цикла. Была отмечена статистически значимая положительная корреляция между MIS и числом обнаруженных ооцитов (r=0,522, р 0,001) и максимальной концентрацией Е 2 в сыворотке (r=0,328, р 0,001), полученной во время индукции овуляции. Кроме того, концентрация MIS в сыворотке на 3-й день менструального цикла в отличие от Е 2 илиFSH характеризовалась положительной корреляцией с числом обнаруженных зрелых ооцитов (фиг. 1). Хотя все корреляции были статистически значимыми, корреляция MIS (r=0,48, р 0,0005) была значительно точнее по сравнению с другими маркерами резерва яичника (то есть Е 2 или FSH). Выводы Мюллерова ингибирующая субстанция представляет димерный гликолротеин и является членом надсемейства трансформирующих -факторов роста. Указанная субстанция, продуцируемая зернистыми клетками яичника (Vigier et al., Endocrinology 1984; 114:1315-20; Takahashi et al., Biol. Reprod. 1986; 35:447-53; Bezard et al. J. Reprod. Fertil. 1987; 80:509-16; Rajpert-De Meyts et al., J. Clin. Endocrinol. Metab. 1999; 84:3836-44), появляется в сыворотке человека в начале пубертатного возраста, сохраняется во взрослом состоянии и исчезает при наступлении менопаузы (Hudson et al., J. Clin Endocrinol Metab. 1990; 70:16-22; Josso et al., J. Clin. Endocrinol Metab. 1990; 70: 23-7; McGee et al., Biol. Reprod. 2001; 64:293-8). У женщин, проходивших обследование на возможность оплодотворения in vitro, были измерены уровни мюллеровой ингибирующей субстанции в фолликулярной жидкости, в результате чего было обнаружено присутствие указанной субстанции в преовуляторных фолликулах женщин с высоким потенциалом овуляции (Seifer et al., J. Clin. Endocrinol. Metab. 1993; 76:711-4). Полученные данные впервые свидетельствуют о наличии взаимосвязи между содержанием MIS в сыворотке на ранней стадии развития фолликула и числом обнаруженных ооцитов несмотря на клинически одинаковые концентрации FSH и Е 2 в сыворотке на 3-й день менструального цикла. В частности,более высокие концентрации MIS в сыворотке ассоциируются с большим числом обнаруженных ооцитов. Кроме того, содержание MIS в сыворотке на 3-й день менструального цикла взаимосвязано с числом обнаруженных ооцитов и числом зрелых ооцитов несмотря на так называемый нормальный уровень FSH в сыворотке на 3-й день менструального цикла, составляющий вплоть до 10 Ед./л. Концентрация MIS в сыворотке может отражать величину пула примордиальных фолликулов и, как следствие этого, может служить маркером, ассоциированным с предполагаемым числом ооцитов после контролируемой стимуляции яичника с целью оплодотворения in vitro. Остается неясным, какое отношение пул примордиальных фолликулов, а также преантральные и ранние антральные фолликулы имеют к определению концентрации MIS в сыворотке на 3-й день менструального цикла. Так как экспрессия MIS начинается в последние три месяца беременности (Rajpert-De Metys et al., J. Clin. Endocrinol. Metab. 1999; 84:3836-44),фактически задолго до того, как она может быть обнаружена в сыворотке, вполне вероятно, что MIS играет важную роль на ранней стадии развития фолликула гораздо раньше, чем считалось до сих пор. Кроме того, экспрессия MIS, по-видимому, продолжается в большинстве, если не во всех фолликулах после рождения и до воздействия гонадотропинов. Однако после начала овариальных циклов уровни MIS в сыворотке слегка изменяются по сравнению с устойчивым базовым значением (Cook et al., Fertil. Steril. 2000; 73:859-61), главным образом, в результате стимуляции небольшого числа фолликулов и прекращения продуцирования MIS по мере образования желтого тела. Уровни MIS на ранней стадии развития фолликула определяются пулом фолликулов, которые начинают продуцировать MIS в матке независимо от системы гипоталамус-гипофиз, и поэтому могут отличаться от других гонадотропинзависимых индикаторов резерва яичника. Данное изобретение показывает, что содержание MIS в сыворотке на 3-й день менструального цикла может быть эффективным клиническим средством оценки резерва яичника помимо совокупности дру-6 012444 гих используемых в настоящее время сывороточных маркеров. Такой маркер состояния пула примордиальных фолликулов открывает уникальные перспективы, недоступные для существующих сывороточных маркеров и ультразвуковых методов исследования. Указанная возможность подтверждается двумя недавно опубликованными отчетами, авторы которых пришли к выводу, что MIS индуцирует рост фолликулов (Durlinger et al., Endocrinology 1999; 140:5789-96; McGee et al., Biol. Reprod. 2001; 64:293-8). Данное изобретение предполагает проведение дополнительных исследований, в процессе выполнения которых должны быть изучены показатели прекращения цикла оплодотворения и результаты беременности у большего числа исследуемых субъектов. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ прогнозирования резерва яичника в ответ на индукцию овуляции у субъекта, который нуждается в индукции овуляции, включающий:(a) определение уровня Мюллеровой ингибирующей субстанции (MIS) в сыворотке у субъекта;(b) сравнение определенного сывороточного уровня MIS со стандартом, в котором коррелируют уровень MIS в сыворотке с числом ооцитов, полученных после индукции овуляции; и(c) прогнозирование ожидаемого ответа яичника. 2. Способ по п.1, где резерв яичника определяют во время индукции овуляции. 3. Способ по п.1, где резерв яичника определяют до индукции овуляции. 4. Способ по п.1, который дополнительно включает оценку риска гиперстимуляции яичника из-за индукции овуляции. 5. Способ по п.1, где риск гиперстимуляции яичника оценивают во время индукции овуляции. 6. Способ по п.4, где риск гиперстимуляции яичника оценивают до индукции овуляции. 7. Набор для использования в способе по п.1, который содержит антитело для определения уровнейMIS в сыворотке субъекта и обеспечивает корреляцию уровня MIS в сыворотке и числа зрелых ооцитов,обнаруженных после индукции овуляции. Сравнение групп женщин, имевших вплоть до 6 и не менее 11 обнаруженных ооцитов среднее значениестандартная ошибка средней Фиг. 1
МПК / Метки
МПК: A61K 39/395, C12N 5/06, C07K 16/00
Метки: ответ, овуляции, индукцию, прогнозирования, яичника, резерва, набор, способ, осуществления
Код ссылки
<a href="https://eas.patents.su/9-12444-sposob-prognozirovaniya-rezerva-yaichnika-v-otvet-na-indukciyu-ovulyacii-i-nabor-dlya-ego-osushhestvleniya.html" rel="bookmark" title="База патентов Евразийского Союза">Способ прогнозирования резерва яичника в ответ на индукцию овуляции и набор для его осуществления</a>
Предыдущий патент: Фармацевтическая композиция, включающая 1-(3-хлорфенил)-3-алкилпиперазин, для лечения расстройств аппетита
Следующий патент: Синергетические гербицидные композиции и способы их применения
Случайный патент: Способы и композиции, содержащие жасмонаты или родственные соединения, для усиления биозащитной активности в растениях