Соединения имидазопиридина, способ их получения и фармацевтические композиции, которые их содержат
Номер патента: 8446
Опубликовано: 29.06.2007
Авторы: Кэньяр Даньель-Анри, Лансело Жан-Шарль, Бизо-Эспьяр Жан-Ги, Пфайффер Брюно, Ренар Пьер, Роль Сильвен, Копп Марина
Формула / Реферат
1. Соединения формулы (I)
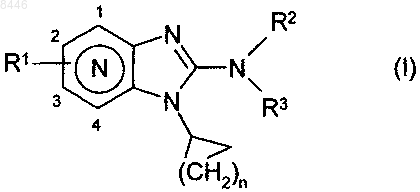
в которой R1 представляет собой атом водорода, атом галогена или алкильную, полигалоалкильную, циано, нитро, гидроксикарбонильную, алкоксикарбонильную, аминокарбонильную, алкиламинокарбонильную или диалкиламинокарбонильную группу,
R2 представляет собой атом водорода, алкильную группу, необязательно замещенную арильную группу, необязательно замещенную гетероарильную группу или группу R20-C(X)-, в которой
R20 представляет собой алкильную группу, алкоксигруппу, аминогруппу, алкиламиногруппу, диалкиламиногруппу, необязательно замещенную арильную группу или необязательно замещенную гетероарильную группу,
X представляет собой атом кислорода, атом серы или группу NR21, в которой R21 представляет собой атом водорода или алкильную группу,
R3 представляет собой атом водорода или алкильную группу,
n представляет собой целое число от 1 до 6 включительно,
изображение 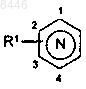 обозначает
обозначает 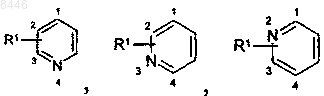 или
или 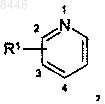
их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием,
и подразумевается, что
термин "алкил" обозначает линейную или разветвленную углеводородную цепь, содержащую от 1 до 6 атомов углерода,
термин "алкокси" обозначает алкилоксигруппу, в которой алкильная цепь, которая может быть линейной или разветвленной, содержит от 1 до 6 атомов углерода,
термин "арил" обозначает фенильную или бифенильную группу,
термин "полигалоалкил" обозначает линейную или разветвленную углеродную цепь, содержащую от 1 до 3 атомов углерода и от 1 до 7 атомов галогена,
термин "гетероарил" обозначает группу, содержащую от 5 до 11 кольцевых членов, которая является моноциклической или бициклической, в которой по крайней мере одно кольцо является ароматическим, и содержащую в моноциклической кольцевой системе или в бициклической кольцевой системе 1, 2 или 3 гетероатома, выбранных из азота, кислорода и серы, и
выражение "необязательно замещенный" в сочетании с выражениями "арил" и "гетероарил" обозначает, что данные группы необязательно замещены одним или двумя одинаковыми или разными заместителями, выбранными из атомов галогена и таких групп, как алкил, алкокси, полигалоалкил, гидрокси, циано, нитро, амино (необязательно замещенной одной или двумя алкильными группами) и -C(O)Rd, в которой Rd представляет собой группу, выбранную из гидрокси, алкокси и амино, и подразумевается, что гетероарильная группа также может быть замещена оксогруппой в неароматической части гетероарила.
2. Соединения формулы (I) в соответствии с п.1, где обозначение 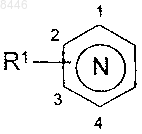 соответствует
соответствует  их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием.
их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием.
3. Соединения формулы (I) в соответствии с п.1 или 2, где R1 представляет собой атом водорода, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием.
4. Соединения формулы (I) в соответствии с любым из пп.1-3, где R2 представляет собой атом водорода, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием.
5. Соединения формулы (I) в соответствии с любым из пп.1-3, где R2 представляет собой группу R20-C(O)-, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием.
6. Соединения формулы (I) в соответствии с любым из пп.1-5, где R3 представляет собой атом водорода, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием.
7. Соединения формулы (I) в соответствии с любым из пп.1-3, 5 или 6, где R20 представляет собой алкоксигруппу, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием.
8. Соединения формулы (I) в соответствии с любым из пп.1-7, где n представляет собой целое число от 4 до 6 включительно, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием.
9. Соединения формулы (I) в соответствии с любым из пп.1-8, где 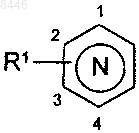 представляет собой
представляет собой 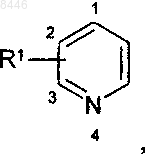 R1 представляет собой атом водорода, R2 представляет собой атом водорода или группу R20-C(O)-, в которой R20 представляет собой алкоксигруппу, и n представляет собой 4 или 5, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием.
R1 представляет собой атом водорода, R2 представляет собой атом водорода или группу R20-C(O)-, в которой R20 представляет собой алкоксигруппу, и n представляет собой 4 или 5, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием.
10. Соединение формулы (I) в соответствии с любым из пп.1-4, 6, 8 или 9, которое представляет собой 3-циклогептил-3H-имидазо[4,5-b]пиридин-2-амин.
11. Соединение формулы (I) в соответствии с любым из пп.1-4, 6 или 8, которое представляет собой 3-циклооктил-3H-имидазо[4,5-b]пиридин-2-амин.
12. Способ получения соединений формулы (I) в соответствии с п.1, который характеризуется тем, что в качестве исходного вещества применяют соединение формулы (II)
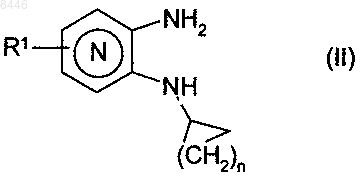
в которой R1 и n имеют значения, указанные для формулы (I), соединения формулы (II) конденсируют с изотиоцианатными соединениями (III)
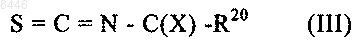
где X и R20 имеют значения, указанные для формулы (I), получая промежуточные продукты формулы (IV)
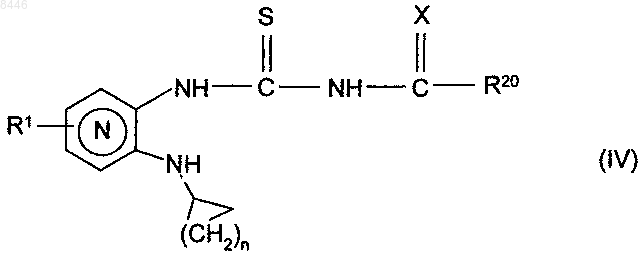
в которой R1, n, X и R20 имеют значения, указанные для формулы (I),
соединения формулы (IV) подвергают внутримолекулярной циклизации в щелочной среде и в присутствии подходящего катализатора, получая соединения (I/а)
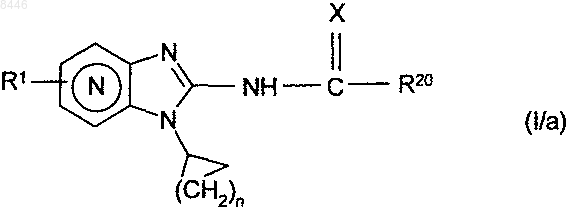
которые представляют собой частные случаи соединений формулы (I), в которой R1, n, X и R20 имеют значения, указанные для формулы (I),
соединения формулы (I/a) необязательно превращают в кислой среде в соединения формулы (I/b)
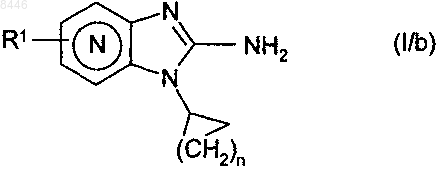
которые представляют собой частные случаи соединений формулы (I), в которой R1 и n имеют значения, указанные для формулы (I),
в соединениях формулы (I/b) функциональная аминогруппа может подвергаться функционализации в щелочной среде при помощи алкилгалогенида Alk-Z (где Alk представляет собой алкильную группу и Z представляет собой атом галогена), получая соединения формулы (I/с)
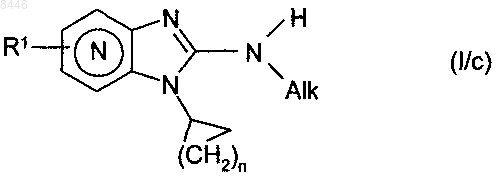
которые представляют собой частный случай соединений формулы (I), в которой R1 и n имеют значения, указанные для формулы (I), и Alk имеет значение, указанное выше,
соединения формул (I/b) и (I/с) можно в щелочной среде, необязательно в присутствии подходящих катализаторов, подвергать взаимодействию с R2-Z' (где R2 имеет значение, указанное для формулы (I), и Z' представляет собой нуклеофугальную группу, такую как атом галогена или тригалоалкильная группа), получая соединения формулы (I),
соединения формул (I/a), (I/b) и (I/с), которые представляют собой совокупность соединений формулы (I), и
могут, при необходимости, быть очищены в соответствии с обычными способами очистки,
разделены, при необходимости, на стереоизомеры в соответствии с обычными способами разделения,
превращены, если этю является желательным, в их соли присоединения с фармацевтически приемлемой кислотой или основанием,
и подразумевается, что
в любое время, если это является подходящим при осуществлении способа, описанного выше, для целей синтеза карбонильная, амино или алкиламиногруппа или группы исходных веществ (II) и (III) могут защищаться, а затем после конденсации защита снимается,
реагенты (II) и (III) получают в соответствии с обычными способами, описанными в литературе.
13. Фармацевтическая композиция, которая содержит в качестве активного компонента по крайней мере одно соединение в соответствии с любым из пп.1-11 отдельно или в сочетании с одним или несколькими инертными, нетоксичными, фармацевтически приемлемыми наполнителями или носителями.
14. Фармацевтическая композиция в соответствии с п.13, предназначенная для приготовления лекарственных средств, используемых в качестве активатора АМРК (протеинкиназы, активируемой аденозин монофосфатом).
15. Фармацевтическая композиция в соответствии с п.13, предназначенная для приготовления лекарственных средств для лечения инсулиннезависимого диабета II типа, ожирения, диабета I типа, гиперлипемии, гиперхолестеринемии и их сердечно-сосудистых осложнений.
16. Фармацевтическая композиция в соответствии с п.13, предназначенная для приготовления лекарственных средств для лечения диабета I и II типа и их сердечно-сосудистых осложнений.
17. Фармацевтическая композиция в соответствии с п.13, предназначенная для приготовления лекарственных средств для лечения диабета I и II типа.
Текст
008446 Изобретение относится к новым соединениям имидазопиридина, к способу их получения и к фармацевтическим композициям, которые их содержат. С точки зрения структуры многие соединения имидазопиридина известны из литературы, в особенности для терапевтического применения. Например, некоторые соединения применяются для лечения нарушений центральной нервной системы (WO 0153263), вирусных инфекций (WO 0100611), аллергий(ЕР 144101) или злокачественных новообразований (WO 0244156). Протеинкиназа, которая активируется AMP (AMPK), является протеинкиназой, вовлеченной в ответную реакции клеток на интенсивный стресс. Белок активируется путем повышения внутриклеточных концентраций AMP (аденозин монофосфата) с последующим снижением концентрации АТР (аденозин трифосфата), например, при физической нагрузке. АМРК фосфорилирует и модифицирует активность ключевых ферментов обмена углеводов и липидов. В действительности, АМРК играет важную роль в липогенезе, поскольку она ингибирует синтез жирных кислот и холестерина путем инактивации ацетил-СоА карбоксилазы и HMG коредуктазы. АМРК уменьшает экспрессию синтазы жирных кислот (FAS), которая контролирует синтез триглицеридов. Кроме того, АМРК также уменьшает экспрессию одного из ключевых ферментов неоглюкогенеза(РЕРСК), что само по себе приводит к значительному ингибированию образования глюкозы в печени. В конечном счете, АМРК повышает утилизацию глюкозы путем улучшения транспорта глюкозы в мышцах. Все эти свойства в целом обуславливают выбор АМРК в качестве ключевой мишени при лечении диабета и нарушений обмена веществ, связанных с ним, поэтому поиск фармакологических активаторов АМРК имеет решающее значения для лечения этих патологий [см. Winder W.W. и Hardie D.G.: АМРactivated protein kinase, a metabolic master switch: possible roles in type 2 diabetes; Am. J. Physiol., 40: E1E10, (1999) и процитированные ссылки]. Сейчас заявителем были обнаружены новые соединения имидазопиридина, которые обладают новой циклоалкилимидазопиридиновой структурой, обеспечивающей АМРК-активирующие свойства, и,более точно, антидиабетические и антигиперлипемические свойства. В частности, настоящее изобретение относится к соединениям формулы (I) в которой R1 представляет собой атом водорода, атом галогена или алкильную, полигалоалкильную,циано, нитро, гидроксикарбонильную, алкоксикарбонильную, аминокарбонильную, алкиламинокарбонильную или диалкиламинокарбонильную группу,R2 представляет собой атом водорода, алкильную группу, необязательно замещенную арильную группу, необязательно замещенную гетероарильную группу или группу R20-C(X)-, в которойR20 представляет собой алкильную группу, алкоксигруппу, аминогруппу, алкиламиногруппу, диалкиламиногруппу, необязательно замещенную арильную группу или необязательно замещенную гетероарильную группу,X представляет собой атом кислорода, атом серы или группу NR21, в которой R21 представляет собой атом водорода или алкильную группу,R3 представляет собой атом водорода или алкильную группу,n представляет собой целое число от 1 до 6 включительно,обозначает изображение к их энантиомерам, диастереоизомерам, а также к их солям присоединения с фармацевтически приемлемой кислотой или основанием,и подразумевается, что термин "алкил" обозначает линейную или разветвленную углеводородную цепь, содержащую от 1 до 6 атомов углерода,термин "алкокси" обозначает алкилоксигруппу, в которой алкильная цепь, которая может быть линейной или разветвленной, содержит от 1 до 6 атомов углерода,термин "арил" обозначает фенильную или бифенильную группу,термин "полигалоалкил" обозначает линейную или разветвленную углеродную цепь, содержащую от 1 до 3 атомов углерода и от 1 до 7 атомов галогена,термин "гетероарил" обозначает группу, содержащую от 5 до 11 кольцевых членов, которая является моноциклической или бициклической, в которой по крайней мере одно кольцо является ароматическим, и содержащую в моноциклической кольцевой системе или в бициклической кольцевой системе 1, 2-1 008446 или 3 гетероатома, выбранных из азота, кислорода и серы, и выражение "необязательно замещенный" в сочетании с выражениями "арил" и "гетероарил" обозначает, что данные группы необязательно замещены одним или двумя одинаковыми или разными заместителями, выбранными из атомов галогена и таких групп, как алкил, алкокси, полигалоалкил, гидрокси,циано, нитро, амино (необязательно замещенной одной или двумя алкильными группами) и -C(O)Rd, в которой Rd представляет собой группу, выбранную из гидрокси, алкокси и амино, и подразумевается, что гетероарильная группа также может быть замещена оксогруппой в неароматической части гетероарила. Среди фармацевтически приемлемых кислот можно отметить, но не ограничиваясь только ими, соляную кислоту, бромисто-водородную кислоту, серную кислоту, фосфоновую кислоту, уксусную кислоту, трифторуксусную кислоту, молочную кислоту, пировиноградную кислоту, малоновую кислоту, янтарную кислоту, глутаровую кислоту, фумаровую кислоту, винную кислоту, малеиновую кислоту, лимонную кислоту, аскорбиновую кислоту, метансульфоновую кислоту, камфорную кислоту и т.д. Среди фармацевтически приемлемых оснований можно отметить, но не ограничиваясь только ими,гидроокись натрия, гидроокись калия, триэтиламин и т.д. Предпочтительная группа, представленная представляет собой В предпочтительном варианте осуществления изобретение относится к соединениям, в которых R1 представляет собой атом водорода. Предпочтительными соединениями по изобретению являются те соединения, в которых R2 представляет собой атом водорода или группу R20-C(O)-. В другом предпочтительном варианте осуществления изобретение относится к соединениям, в которых R3 представляет собой атом водорода. Группа R20, что является предпочтительным в соответствии с изобретением, представляет собой алкоксигруппу и более предпочтительно этоксигруппу. В предпочтительных соединениях по изобретению n представляет собой целое число 4, 5 или 6 и более предпочтительно 5. В более предпочтительном варианте изобретение относится к соединениям формулы (I), в которойR1 представляет собой атом водорода, R2 представляет собой атом водорода или группу R20-C(O)-, в которой R20 представляет собой алкоксигруппу, и n представляет собой 4 или 5. Среди предпочтительных соединений по изобретению, которые можно отметить, более предпочтительными являются 3-циклогептил-3H-имидазо[4,5-b]пиридин-2-амин и 3-циклооктил-3H-имидазо[4,5b]пиридин-2-амин. Изобретение также относится к способу получения соединений формулы (I), который характеризуется тем, что в качестве исходного вещества применяют соединения формулы (II) в которой R1 и n имеют значения, указанные для формулы (I), соединения формулы (II) конденсируют с изотиоцианатными соединениями (III) где X и R20 имеют значения, указанные для формулы (I), получая промежуточные продукты формулы в которой R1, n, X и R20 имеют значения, указанные для формулы (I),соединения формулы (IV) подвергают внутримолекулярной циклизации в щелочной среде и в присутствии подходящего катализатора, получая соединения (I/а) которые представляют собой частные случаи соединений формулы (I), в которой R1, n, X и R20 имеют-2 008446 значения, указанные для формулы (I),соединения формулы (I/а) необязательно превращают в кислой среде в соединения формулы (I/b) которые представляют собой частные случаи соединений формулы (I), в которой R1 и n имеют значения,указанные для формулы (I),в соединениях формулы (I/b) функциональная аминогруппа может подвергаться функционализации в щелочной среде при помощи алкилгалогенида Alk-Z (где Alk представляет собой алкильную группу иZ представляет собой атом галогена), получая соединения формулы (I/с) которые представляют собой частный случай соединений формулы (I), в которой R1 и n имеют значения,указанные для формулы (I), и Alk имеет значение, указанное выше,соединения формул (I/b) и (I/с) можно в щелочной среде, необязательно в присутствии подходящих катализаторов, подвергать взаимодействию с R2-Z (где R2 имеет значение, указанное для формулы (I), иZ представляет собой нуклеофугальную группу, такую как атом галогена или тригалоалкильная группа),получая соединения формулы (I),соединения формул (I/a), (I/b) и (I/с), которые представляют собой совокупность соединений формулы (I), и могут, при необходимости, быть очищены в соответствии с обычными способами очистки,разделены, при необходимости, на стереоизомеры в соответствии с обычными способами разделения,превращены, если это является желательным, в их соли присоединения с фармацевтически приемлемой кислотой или основанием,и подразумевается, что в любое время, если это является подходящим при осуществлении способа, описанного выше, для целей синтеза карбонильная, амино или алкиламиногруппа или группы исходных веществ (II) и (III) могут защищаться, а затем после конденсации защита снимается,реагенты (II) и (III) получают в соответствии с обычными способами, описанными в литературе. Соединения обладают значительной активностью и в особенности снижают уровень триглицеридов и глюкозы в крови. Эти свойства обуславливают их терапевтическое применение для лечения и/или профилактики гипергликемии, дислипидемии и более предпочтительно для лечения инсулиннезависимого диабета II типа, ожирения, непереносимости глюкозы и осложнений диабета, в особенности сердечнососудистых осложнений. Действие этих соединений также предоставляет возможность их применения для лечения и/или профилактики других заболеваний, включая диабет I типа, гипертриглицеридемии, метаболический синдром, резистентность к инсулину, дислипемию при диабете, гиперлипемию и гиперхолестеринемию. Настоящее изобретение также относится к фармацевтическим композициям, которые содержат в качестве активного компонента по крайней мере одно соединение формулы (I) отдельно или в сочетании с одним или несколькими инертными, нетоксичными, фармацевтически приемлемыми наполнителями или носителями. Среди фармацевтических композиций согласно изобретению особенно можно отметить те, которые являются пригодными для перорального, парентерального и назального введения, таблетки или драже,подъязычные таблетки, желатиновые капсулы, лепешки, суппозитории, кремы, мази, кожные гели и др. Полезная дозировка изменяется в зависимости от возраста и веса пациента, природы и тяжести расстройства, пути введения, который может быть пероральным, назальным, ректальным или парентеральным. Как правило, стандартная доза находится в диапазоне от 0,1 до 500 мг в сутки на одно-три введения. Примеры, представленные ниже, приведены только с целью иллюстрации изобретения и никоим образом его не ограничивают. Структуру описанных соединений подтверждали при помощи обычных спектроскопических и спектрометрических методик. Используемые исходные материалы являются известными продуктами или продуктами, которые получают в соответствии с известными способами. Приготовление 1. N2-Циклогексил-2,3-пиридиндиамин. Стадия а. N-Циклогексил-3-нитро-2-пиридинамин. Смесь, содержащую 0,1 моль (15,85 г) 2-хлор-3-нитропиридина и 0,1 моль (11,50 мл) циклогекси-3 008446 ламина, нагревали при 120 С в течение 4 ч в 250 мл ДМФА в присутствии карбоната калия (13,81 г). Затем раствор экстрагировали 200 мл эфира и органическую фазу трижды промывали водой. После высушивания над сульфатом магния, эфир выпаривали. Стадия b. N2-Циклогексил-2,3-пиридиндиамин. 800 мл этанола, 0,05 моль (11,06 г) нитрованного соединения, полученного на предыдущей стадии,и 3,5 г палладия на угле вносили в автоклав. Смесь нагревали при 60 С в течение 30 мин под 50 кг водорода и затем горизонтально перемешивали при температуре окружающей среды в течение 3 ч для гомогенизации раствора. Затем раствор фильтровали через воронку Бюхнера и после этого дважды фильтровали для окончательного удаления остатков палладия на угле, и этанол выпаривали при пониженном давлении. Приготовление 2. N2-Циклогептил-2,3-пиридиндиамин. Экспериментальный протокол был аналогичный описанному для приготовления 1, исходя из циклогептиламина вместо циклогексиламина на стадии а. Приготовление 3. N2-Циклооктил-2,3-пиридиндиамин. Экспериментальный протокол был аналогичный описанному для приготовления 1, исходя из циклооктиламина вместо циклогексиламина на стадии а. Пример 1. Этил 3-циклогексил-3H-имидазо[4,5-b]пирид-2-илкарбамат. Стадия А. Этил [2-(циклогексиламино)-3-пиридил]имино(диэтиламино)метилкарбамат. Смесь 0,02 моль (3,82 г) 3-амино-2-циклогексиламинопиридина из приготовления 1 и 0,02 моль этоксикарбонилизотиоцианата перемешивали в 50 мл ДМФА при температуре окружающей среды в течение 3 ч. Затем раствор охлаждали до0 С и добавляли подряд 0,05 моль дипропиламина и затем 0,02 моль хлорида ртути. Через 15 мин ледяную баню удаляли и раствор перемешивали при температуре окружающей среды в течение 4 ч. После разбавления раствора 100 мл этилацетата, осуществляли фильтрацию через целит и растворители выпаривали при пониженном давлении. Затем полученный неочищенный продукт перекристаллизовывали из ацетонитрила. Стадия В. Этил 3-циклогексил-3H-имидазо[4,5-b]пирид-2-илкарбамат. 0,0048 моль соединения, полученного на предыдущей стадии, растворяли в 100 мл раствора метанола и 15% раствора гидроокиси натрия (50/50). После нагревания раствора в колбе с обратным холодильником в течение 3 ч, метанол выпаривали. Таким образом полученный осадок фильтровали с отсасыванием, промывали водой и перекристаллизовывали из ацетонитрила. Точка плавления: 264 С. Пример 2. Этил 3-циклогептил-3H-имидазо[4,5-b]пирид-2-илкарбамат. Экспериментальный протокол был аналогичный описанному в примере 1, исходя на стадии а из 3 амино-2-циклогептиламинопиридина из приготовления 2 вместо 3-амино-2-циклогексиламинопиридина. Точка плавления: 177 С. Пример 3. 3-Циклогексил-3H-имидазо[4,5-b]пиридин-2-амин. Соединение из примера 1 добавляли к 100 мл раствору диоксана, насыщенного газообразным НСl,и раствор нагревали в колбе с обратным холодильником в течение 12 ч. После охлаждения раствора осадок фильтровали с отсасыванием, промывали бикарбонатом натрия и затем перекристаллизовывали из ацетонитрила. Точка плавления: 210 С. Пример 4. 3-Циклогептил-3H-имидазо[4,5-b]пиридин-2-амин. Экспериментальный протокол был аналогичный описанному в примере 3, используя соединение из примера 2 в качестве исходного вещества. Точка плавления: 210 С. Пример 5. 3-Циклооктил-3H-имидазо[4,5-b]пиридин-2-амин. Экспериментальный протокол был аналогичный описанному в примере 1, исходя на стадии а из 3 амино-2-циклооктиламинопиридина из приготовления 3 вместо 3-амино-2-циклогексиламинопиридина. Точка плавления: 198 С. Фармакологическое исследование Пример А. Действие АМРК на модели клеток: гепатоциты, выделенные из крыс. Гепатоциты выделяли в соответствии с методикой Berry и Friend [J. Cell Biol., 43, 506-520 (1969)]. Активность АМРК измеряли в соответствии со способом, описанным Davies и др. [Eur. J. Biochem., 186,123-128 (1989)]. Последняя связана с фосфорилированием, исходя из [-32 Р]-АТР пептидного субстрата(SAMS), на основании последовательности, окружающей участок, фосфорилированный при помощи АМРК АСС. Реакцию для измерения активности АМРК прекращали путем внесения аликвоты реакционной среды на фосфофоцеллюлозную бумагу (Whatman P81), на которой пептид SAMS фиксировали и после промывания измеряли его радиоактивность. Например, соединение из примера 4 активирует АМРК, через 30 мин в концентрации 500 мкМ на 312% (по сравнению с исходной величиной), тогда как рибозид AICA в такой же концентрации, который использовался для сравнения, в тех же самых условиях активировал АМРК на 178%. Пример В. Гиполипемическое действие. Продукты по изобретению исследовали в условиях in vivo на страдающих ожирением мышах ob/ob,которые применялись в качестве модели ожирения, связанного с резистеностью к инсулину. Например,соединение из примера 4 существенно снижает концентрацию триглицеридов в дозе 125 мг/кг при перо-4 008446 ральном введении, тогда как метформин такое же снижение вызывает при пероральном введении в дозе 250 мг/кг. Таким образом, на этой модели показано, что соединения согласно изобретению являются эффективными гиполипемическими средствами. Пример С. Фармацевтическая композиция. Состав для приготовления 1000 таблеток, каждая из которых содержит 5 мг: Соединение из примера 4 5 г Гидроксипропилметилцеллюлоза 2 г Пшеничный крахмал 10 г Лактоза 100 г Стеарат магния 3 г ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединения формулы (I) в которой R1 представляет собой атом водорода, атом галогена или алкильную, полигалоалкильную,циано, нитро, гидроксикарбонильную, алкоксикарбонильную, аминокарбонильную, алкиламинокарбонильную или диалкиламинокарбонильную группу,R2 представляет собой атом водорода, алкильную группу, необязательно замещенную арильную группу, необязательно замещенную гетероарильную группу или группу R20-C(X)-, в которойR20 представляет собой алкильную группу, алкоксигруппу, аминогруппу, алкиламиногруппу, диалкиламиногруппу, необязательно замещенную арильную группу или необязательно замещенную гетероарильную группу,X представляет собой атом кислорода, атом серы или группу NR21, в которой R21 представляет собой атом водорода или алкильную группу,R3 представляет собой атом водорода или алкильную группу,n представляет собой целое число от 1 до 6 включительно, изображение обозначает или их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием,и подразумевается, что термин "алкил" обозначает линейную или разветвленную углеводородную цепь, содержащую от 1 до 6 атомов углерода,термин "алкокси" обозначает алкилоксигруппу, в которой алкильная цепь, которая может быть линейной или разветвленной, содержит от 1 до 6 атомов углерода,термин "арил" обозначает фенильную или бифенильную группу,термин "полигалоалкил" обозначает линейную или разветвленную углеродную цепь, содержащую от 1 до 3 атомов углерода и от 1 до 7 атомов галогена,термин "гетероарил" обозначает группу, содержащую от 5 до 11 кольцевых членов, которая является моноциклической или бициклической, в которой по крайней мере одно кольцо является ароматическим, и содержащую в моноциклической кольцевой системе или в бициклической кольцевой системе 1, 2 или 3 гетероатома, выбранных из азота, кислорода и серы, и выражение "необязательно замещенный" в сочетании с выражениями "арил" и "гетероарил" обозначает, что данные группы необязательно замещены одним или двумя одинаковыми или разными заместителями, выбранными из атомов галогена и таких групп, как алкил, алкокси, полигалоалкил, гидрокси,циано, нитро, амино (необязательно замещенной одной или двумя алкильными группами) и -C(O)Rd, в которой Rd представляет собой группу, выбранную из гидрокси, алкокси и амино, и подразумевается, что гетероарильная группа также может быть замещена оксогруппой в неароматической части гетероарила. 2. Соединения формулы (I) в соответствии с п.1, где обозначение соответствует их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием. 3. Соединения формулы (I) в соответствии с п.1 или 2, где R1 представляет собой атом водорода, их-5 008446 энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием. 4. Соединения формулы (I) в соответствии с любым из пп.1-3, где R2 представляет собой атом водорода, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием. 5. Соединения формулы (I) в соответствии с любым из пп.1-3, где R2 представляет собой группу 20R -C(O)-, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием. 6. Соединения формулы (I) в соответствии с любым из пп.1-5, где R3 представляет собой атом водорода, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием. 7. Соединения формулы (I) в соответствии с любым из пп.1-3, 5 или 6, где R20 представляет собой алкоксигруппу, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием. 8. Соединения формулы (I) в соответствии с любым из пп.1-7, где n представляет собой целое число от 4 до 6 включительно, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием. 9. Соединения формулы (I) в соответствии с любым из пп.1-8, где представляет собойR1 представляет собой атом водорода, R2 представляет собой атом водорода или группу R20-C(O)-, в которой R20 представляет собой алкоксигруппу, и n представляет собой 4 или 5, их энантиомеры, диастереоизомеры, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием. 10. Соединение формулы (I) в соответствии с любым из пп.1-4, 6, 8 или 9, которое представляет собой 3-циклогептил-3H-имидазо[4,5-b]пиридин-2-амин. 11. Соединение формулы (I) в соответствии с любым из пп.1-4, 6 или 8, которое представляет собой 3-циклооктил-3H-имидазо[4,5-b]пиридин-2-амин. 12. Способ получения соединений формулы (I) в соответствии с п.1, который характеризуется тем,что в качестве исходного вещества применяют соединение формулы (II) в которой R1 и n имеют значения, указанные для формулы (I), соединения формулы (II) конденсируют с изотиоцианатными соединениями (III) где X и R20 имеют значения, указанные для формулы (I), получая промежуточные продукты формулы в которой R1, n, X и R20 имеют значения, указанные для формулы (I),соединения формулы (IV) подвергают внутримолекулярной циклизации в щелочной среде и в присутствии подходящего катализатора, получая соединения (I/а) которые представляют собой частные случаи соединений формулы (I), в которой R1, n, X и R20 имеют значения, указанные для формулы (I),соединения формулы (I/a) необязательно превращают в кислой среде в соединения формулы (I/b)-6 008446 которые представляют собой частные случаи соединений формулы (I), в которой R1 и n имеют значения,указанные для формулы (I),в соединениях формулы (I/b) функциональная аминогруппа может подвергаться функционализации в щелочной среде при помощи алкилгалогенида Alk-Z (где Alk представляет собой алкильную группу иZ представляет собой атом галогена), получая соединения формулы (I/с) которые представляют собой частный случай соединений формулы (I), в которой R1 и n имеют значения,указанные для формулы (I), и Alk имеет значение, указанное выше,соединения формул (I/b) и (I/с) можно в щелочной среде, необязательно в присутствии подходящих катализаторов, подвергать взаимодействию с R2-Z' (где R2 имеет значение, указанное для формулы (I), иZ' представляет собой нуклеофугальную группу, такую как атом галогена или тригалоалкильная группа),получая соединения формулы (I),соединения формул (I/a), (I/b) и (I/с), которые представляют собой совокупность соединений формулы (I), и могут, при необходимости, быть очищены в соответствии с обычными способами очистки,разделены, при необходимости, на стереоизомеры в соответствии с обычными способами разделения,превращены, если это является желательным, в их соли присоединения с фармацевтически приемлемой кислотой или основанием,и подразумевается, что в любое время, если это является подходящим при осуществлении способа, описанного выше, для целей синтеза карбонильная, амино или алкиламиногруппа или группы исходных веществ (II) и (III) могут защищаться, а затем после конденсации защита снимается,реагенты (II) и (III) получают в соответствии с обычными способами, описанными в литературе. 13. Фармацевтическая композиция, которая содержит в качестве активного компонента по крайней мере одно соединение в соответствии с любым из пп.1-11 отдельно или в сочетании с одним или несколькими инертными, нетоксичными, фармацевтически приемлемыми наполнителями или носителями. 14. Фармацевтическая композиция в соответствии с п.13, предназначенная для приготовления лекарственных средств, используемых в качестве активатора АМРК (протеинкиназы, активируемой аденозин монофосфатом). 15. Фармацевтическая композиция в соответствии с п.13, предназначенная для приготовления лекарственных средств для лечения инсулиннезависимого диабета II типа, ожирения, диабета I типа, гиперлипемии, гиперхолестеринемии и их сердечно-сосудистых осложнений. 16. Фармацевтическая композиция в соответствии с п.13, предназначенная для приготовления лекарственных средств для лечения диабета I и II типа и их сердечно-сосудистых осложнений. 17. Фармацевтическая композиция в соответствии с п.13, предназначенная для приготовления лекарственных средств для лечения диабета I и II типа.
МПК / Метки
МПК: C07D 221/00, A61K 31/44, C07D 235/00, C07D 471/04
Метки: содержат, получения, имидазопиридина, соединения, фармацевтические, которые, способ, композиции
Код ссылки
<a href="https://eas.patents.su/8-8446-soedineniya-imidazopiridina-sposob-ih-polucheniya-i-farmacevticheskie-kompozicii-kotorye-ih-soderzhat.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения имидазопиридина, способ их получения и фармацевтические композиции, которые их содержат</a>
Предыдущий патент: 3-гетероарилзамещённые изоксазолины
Следующий патент: Полифункциональная пенная композиция для комплексной специальной обработки поверхностей, объемов и объектов от опасных агентов и веществ
Случайный патент: Защитное устройство для медицинской иглы (варианты) и устройство для сбора текучей среды












