Способ переработки руд на основе сульфида меди
Формула / Реферат
1. Способ переработки руд на основе сульфида меди, включающий их концентрирование, отличающийся тем, что при концентрировании (19) руду (4) разделяют на два сульфидных концентрата различного типа: первичный концентрат (7), в основном содержащий плохо растворимые компоненты, такие как халькопирит и содержащиеся в руде драгоценные металлы, и вторичный концентрат (8), в основном содержащий хорошо растворимые компоненты, такие как сульфид меди, прочие ценные сульфиды из руды и пирит; при этом вторичный концентрат (8) направляют на стадию (9) выщелачивания, а раствор (13), полученный на указанной стадии выщелачивания, и первичный концентрат подают по меньшей мере на одну стадию (11) химического превращения, где, по меньшей мере, медь, содержащуюся в растворе, превращают в сульфидную форму посредством сульфидной формы железа из первичного концентрата (7), при этом по меньшей мере часть раствора (12), полученного на стадии (11) химического превращения, возвращают на стадию (9) выщелачивания вторичного концентрата.
2. Способ по п.1, отличающийся тем, что он включает вторую стадию (16) химического превращения, следующую за первой стадией (11) химического превращения, где различные металлические компоненты превращают в сульфидную форму посредством железа (17) в сульфидной форме, подаваемого на указанную стадию химического превращения.
3. Способ по п.1 или 2, отличающийся тем, что выщелачивание (9) проводят при атмосферном давлении при температуре 50-105шС.
4. Способ по п.1 или 2, отличающийся тем, что выщелачивание (9) проводят в автоклаве.
5. Способ по любому из пп.1-4, отличающийся тем, что по меньшей мере одну стадию (11, 16) химического превращения проводят при температуре 90-200шС.
6. Способ по п.5, отличающийся тем, что по меньшей мере одну стадию (11, 16) химического превращения проводят при температуре 150-190шС.
7. Способ по любому из пп.1-6, отличающийся тем, что железо на первой стадии (11) химического превращения представляет собой халькопирит (CuFeS2).
8. Способ по любому из пп.1-7, отличающийся тем, что железо, добавляемое на второй стадии (16) химического превращения, представляет собой троилит (FeS).
9. Способ по любому из пп.1-6, отличающийся тем, что железо, добавляемое на второй стадии (16) химического превращения, представляет собой пирротит (Fe1-xS).
10. Способ по любому из пп.1-9, отличающийся тем, что концентрирование (19) руды осуществляют путем флотации, процесс которой контролируют посредством специфичных по отношению к минералам электрохимических измерений.
11. Способ по любому из пп.1-10, отличающийся тем, что стадию (9) выщелачивания, используемую при обработке концентрата, контролируют посредством специфичных по отношению к минералам электрохимических измерений.
12. Способ по любому из пп.1-11, отличающийся тем, что стадии (11, 16) химического превращения, используемые при обработке концентрата, контролируют посредством специфичных по отношению к минералам электрохимических измерений.
13. Способ по любому из пп.1-12, отличающийся тем, что на первой стадии (11) химического превращения извлекают драгоценные металлы, содержащиеся в концентратах.
Текст
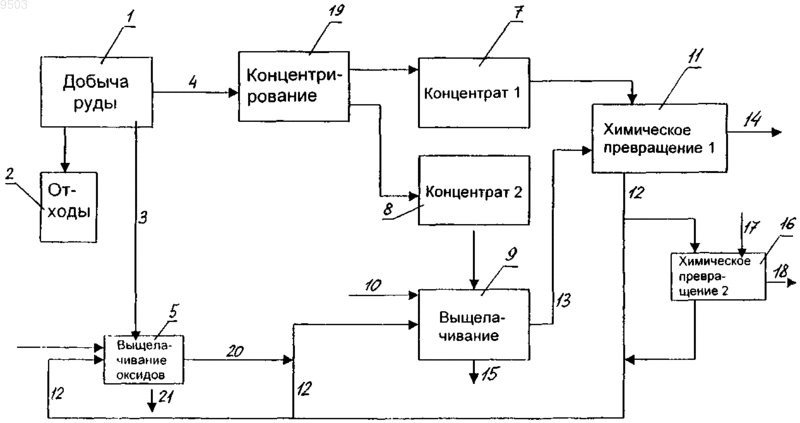
009503 Данное изобретение относится к способу переработки руд на основе сульфида меди, включающему концентрирование. Для первичной обработки содержащего медь сырья обычно существуют две основных схемы. Одна из них представляет собой схему концентрирование - сплавление - электролитическое рафинирование, а другая - схему выщелачивания (такое как кучное выщелачивание) - жидкостная экстракция электролитическое выделение. В отношении причин, связанных с качеством сырья, защитой окружающей среды, географией и экономикой, обе схемы переработки сталкиваются со все возрастающими трудностями. Начиная концентрировать сырье на основе меди, мы часто сталкиваемся с ситуацией, когда значительная доля минерального сырья окислена и возможно его трудно флотировать. Здесь особенно следует упомянуть месторождения медных руд, содержащие силикаты меди и оксиды железа. Также может быть почти невозможно провести флотацию в случае смешанных частиц с сульфидом меди и пиритом. Специфическую группу проблем представляют тонкоизмельченные, часто содержащие пирит медно-цинксвинцовые рудные отложения. Обработка указанных рудных отложений традиционными способами обычно дает весьма неудовлетворительный результат в отношении выхода и содержания концентратов. Если затраты на перевозку на медеплавильный завод часто являются слишком высокими с точки зрения конкуренции, даже в случае высококачественных концентратов, они еще выше в случае концентратов низкого качества. Что еще важнее, в таком случае увеличивается опасность для окружающей среды в двух различных пунктах, например, из-за мышьяка. Сам по себе процесс переплавки обычно включает много стадий, среди них плавление, например, в печи для взвешенной плавки, обработка в конвертере,обработка в печи с катодами Венельта и обрабатываемым металлом в качестве анода; получение серной кислоты для газов и процесс обработки в электрической печи или концентрирования для шлака. Часто причиной многостадийных процессов переплавки, которые являются экономически неэффективными,является плохое качество исходного материала, то есть концентрата. Что касается второго преимущественно применяемого способа - переработки, основанной на кучном выщелачивании - то он также переживает трудные времена. Если руда не содержит ни заметных количеств благородных металлов, ни заметных количеств меди в виде халькопирита, CuFeS2, или в виде другого соединения, которое трудно растворяется, то ситуация довольно благополучна. Однако, как правило, все возрастающая доля сырья даже в уже функционирующих рудниках состоит именно из плохо растворимых медных минералов. Это означает увеличение затрат. Другим недостатком способа, основанного на жидкостной экстракции, является ограниченное время существования почти всех рудников. Если цепочка процесса в целом, от рудника до катодной меди, основана только на одном месторождении,то завод обычно сталкивается с нездоровой ситуацией, поскольку объем рудного тела постепенно расходуется. В результате норма прибыли капиталовложений не является оптимальной. В геологии уже по меньшей мере сто лет назад было обнаружено, что сульфиды металлов имеют тенденцию превращаться, например, при осаждении из раствора, содержащего ионы другого элемента, в сульфиды. Эти наблюдения постоянно накапливались до действительного понимания причин этого явления, до тех пор, пока примерно 50 лет назад на этот предмет не был опубликован патент США 2568963. Согласно указанному патенту США концентрат меди разделяют на часть, которую будут выщелачивать,и на часть, используемую при осаждении сульфида меди (CuS). Полученный CuS выщелачивают сульфатом для получения меди. Твердые и растворимые побочные компоненты легко удаляются из процесса. Позднее, в 1956 г., те же самые авторы опубликовали новый патент США 2755172, где ионы металла из раствора, то есть медь, кобальт, никель и цинк, осаждают последовательно в виде сульфидов в порядкеCuS, CoS, NiS, ZnS путем использования сульфида металла типа MeS, который является более растворимым, чем элемент, который следует осадить. В процессе осаждения рН постепенно повышается, так что,например, при осаждении сульфида цинка (ZnS) рН сульфатного раствора находится в интервале 6,2-7. Поскольку исходной точкой способа по патенту США 2755172 является выщелачивание сырья, полученного при производстве серной кислоты, используемый интервал рН 6,2-7 означает, что имеется экономически обоснованная стадия нейтрализации. На этот факт обращается внимание и далее, где предполагаемыми реагентами для нейтрализации являются среди прочих аммиак, щелок или Са(ОН)2, или если предполагаемой промежуточной стадией процесса является реакция, где Fe3+ восстанавливают сероводородом (H2S) с получением серы, Fe2+ и H2SO4. Слабые стороны ноу-хау процессов, описанных в вышеупомянутых патентах США 2568963 и 2755172, а также нереалистичный подход как в химическом, так и в экономическом отношении, обнаруживаются теперь, почти 50 лет спустя, некоторыми характерными особенностями вышеупомянутых патентов США. Прежде всего, в действительности природные сульфидные минералы не представляют собой в основном лишь сульфиды типа MeS, но их соотношение металл/сера (соотношение Me/S) колеблется в широком диапазоне. Некоторые сульфиды металлов представляют собой смешанные сульфиды в том смысле, что металл (Me) частично замещен другими сульфидами, например, сера замещена мышьяком и сурьмой, не говоря об осаждении частиц и других структурных примесей, по сравнению с чистыми модельными минералами типа MeS. Как следствие вышеупомянутых фактов, способ согласно патенту США 2755172 просто не работает с реальным сырьем. Способ согласно патенту США 2568963 имеет-1 009503 лучшие шансы на работу, но он не предлагает, например, решения вопроса, как справиться с балансами по железу и балансами по кислоте. Кроме того, патент США 2568963 устанавливает, что для процесса выщелачивания необходим медный концентрат, поскольку другие концентраты являются слишком слабыми для выщелачивания. Более того, с помощью способа по патенту США 2568963 невозможно достичь продукта - металлической меди коммерческого качества. Одним из типов реакции получения обогащенных концентратов меди является Реакцию (1) часто считали медленной. Следовательно, решение искали в направлении условий восстановления. Используемыми восстановителями были, например, элементарные медь (Cu0), хром (Cr0),цинк (Zn0), кобальт (Со 0), никель (Ni0) или железо (Fe0), оксид серы (SO2) или органические восстановители. В лабораторных условиях полученное время реакции для реакции составляет один час, но понятно, что в реальности не так легко поддерживать контакт, например, между порошком Fe0 и частицей CuFeS2. Как таковой, сам основной принцип использования металлического порошка является из экономических соображений невозможным в коммерческих процессах. Что касается использования SO2, то это приводит к избытку кислоты H2SO4, которая возникает в этом процессе. Более того, было обнаружено, что для получения обогащенного по меди сульфида меди (CuxS) в принципе существует два пути, то есть основанный на превращении способ по реакции (1) и путь селективного выщелачивания с использованием кислого реагента. Последний путь можно проиллюстрировать, например, реакцией (3) Таким образом, типичный процесс, основанный на селективном выщелачивании, дает значительное количество серной кислоты и вносящий проблемы раствор FeSO4, без существенного увеличения полезного количества продукта - сульфида меди, поскольку он включает вредные ингредиенты, такие как FeS2 и силикаты. Согласно патентной заявке Германии 2207382 концентрат CuFeS2 обрабатывают в присутствии сульфата меди (CuSO4) путем превращения в интервале температур 90-180 С в CuxS и FeSO4. Полученный раствор FeSO4 гидролизуют в автоклаве в интервале температур 180-230 С до твердого соединенияFe3+ и раствора H2SO4. Твердый сульфид меди (CuxS) выщелачивают путем окисления H2SO4, до CuSO4,который после очистки цементацией, проводимой элементарной медью (Cu0), восстанавливают до меди водородом. Способ согласно патентной заявке Германии 2207382 осуществим с чистыми концентратами,которые содержат лишь небольшие количества, например, цинка, свинца и пирита. Подобные же проблемы имеются в способах, описанных в патентах СА 1069317 и США 3957602. В первом способе концентрат CuFeS2 превращается в CuxS и раствор FeCl2 путем хлоридного выщелачивания. CuxS выщелачивают и после очистки из CuCl восстанавливают металлическую медь. Примеси удаляют из раствораFeCl2 и посредством электролиза FeCl2 превращают в раствор FeCl3 и металлическое железо. Этот способ был бы вполне осуществимым, если бы не имели особого значения ни чистота продукта, ни экономические показатели. Способ согласно патенту США 3957602 является основной версией двух основных направлений, основанных на получении CuxS путем использования достаточно чистого медного концентрата. Здесь железо, содержащееся в CuFeS2, находится в связи с выщелачиванием CuxS, превращенного в ярозит. Однако способ согласно патенту США 3957602 не учитывает, например, выделение драгоценных металлов и MoS2, но его применение привносит дополнительные затраты в сравнении с существующими основными способами. Ближе к способу по данному изобретению лежат способы, описанные в приведенных в качестве ссылки публикациях Yuill W.A. et al., Copper Concentrate Enrichment Process (Способ обогащения медного концентрата), SME-AIME Annual Meeting, Los Angeles, California, 26 февраля - 1 марта 1984 г., и Bartlett R.W., A Process for Enriching Chalcopyrite Concentrates (Способ обогащения концентратов халькопирита), Новый Орлеан, 2-6 марта 1986, стр. 227-246. Что касается первой альтернативы, описанной в 1984 г. Yuill et al., то наиболее серьезные недостатки связаны с процессом выщелачивания, проводимом при температуре 200 С, и с окислением почти всей сульфидной серы, а также в значительной степени серы пирита, до сульфата, то есть до серной кислоты. Эту ситуацию попытались улучшить путем использования извести как в автоклаве для выщелачивания, так и в автоклаве для химической реакции, а также при удалении меди из растворов. Полученный продукт превращения в дальнейшем подвергают флотации,которая вызывает дополнительные затраты, и в действительности также потери меди и драгоценных металлов в этом процессе. В целом для полученного обогащенного по CuxS продукта не было обнаружено способа дальнейшей переработки, который был бы более предпочтительным в отношении использования, но концентрат CuxS должен конкурировать с традиционным медным концентратом. В способе, описанном Bartlett в 1987 г., стадии в автоклаве объединены в одну стадию выщелачивания CuFeS2 с химическим превращением, которую проводят при температуре 200 С. С точки зрения технологического оборудования, этот способ является упрощенным. Однако большей частью остаются те-2 009503 же проблемы, связанные с возникновением H2SO4, с удалением железа и с использованием извести. В качестве противовеса этому упрощению концентрат CuFeS2 является существенно более слабым, в продукте остаются смешанные гранулы FeS2 - сульфид меди, и выделение меди в конечном концентрате снижено, например, из-за возросших проблем селективной флотации этого конечного продукта. С точки зрения плавильной печи, полученный продукт все еще не является привлекательным в сравнении с традиционным концентратом. Целью данного изобретения является ликвидировать недостатки существующего положения и разработать способ для обработки сложного в химическом и структурном отношении медного сырья, который был бы более эффективным, чем существующий, с позиции затрат на технологию, технологии переработки и защиты окружающей среды. В существенной степени отличительные признаки данного изобретения перечислены в прилагаемой формуле изобретения. При применении способа по данному изобретению после добычи руды ее разделяют на три части: часть, которую следует сконцентрировать, часть, пригодную для кучного выщелачивания или для другого соответственного способа выщелачивания, и на часть, не представляющую промышленной ценности. Согласно данному изобретению, часть, которую следует сконцентрировать, обрабатывают способом,пригодным для данного сырья, например, способом флотации или способом, основанным на различии в удельных массах, или на магнитных свойствах, так, чтобы получить два сульфидных концентрата различных типов. Сульфидный концентрат первого типа, называемый первичным концентратом, представляет собой относительно плохо растворимый концентрат, в основном содержащий плохо растворимые компоненты, такие как халькопирит и содержащиеся в руде драгоценные металлы. Что касается сульфидного концентрата второго типа, или вторичного концентрата, то он представляет собой концентрат,задачей которого является максимально выделить ценные компоненты, выщелоченные каким-либо способом выщелачивания. Вторичный концентрат в основном содержит хорошо растворимые компоненты,такие как сульфид меди, прочие ценные сульфиды из руды и пирит. Если это желательно, то возникшие при получении концентратов отходы, то есть полученный при концентрировании песок, также можно подвергнуть концентрированию с помощью возможного окисного материала. Растворимый сульфидный концентрат второго типа, полученный при концентрировании, направляют на стадию выщелачивания, основанного на сульфате или хлориде, или же на стадию выщелачивания, осуществляемого сочетанием этих двух, и на эту же стадию выщелачивания можно также подать раствор, полученный при выщелачивании оксидных материалов, если это необходимо. Предпочтительно это выщелачивание проводят при атмосферном давлении в интервале температур 50-105 С. Это выщелачивание также можно проводить в автоклаве. Кроме того, по меньшей мере часть раствора со стадии химического превращения после стадии выщелачивания подают на стадию выщелачивания. Кислый раствор, полученный при выщелачивании концентрата второго типа, который может быть сконцентрирован путем рециркуляции, подают на стадию химического превращения, проводимую с концентратом первого типа в диапазоне температур 90-200 С, предпочтительно в интервале температур 150190 С. Теперь, в результате следующей принципиальной реакции (4) получают обогащенный по CuxS концентрат, преимущественно содержащий драгоценные металлы, который направляют на последующую обработку, например на производство черновой меди. В зависимости, например, от соотношения содержания сульфидов меди-цинка-свинца-железа в исходной руде и в скрапообразном материале, поступающем на выщелачивание, весь раствор после химического превращения идет сначала на циркуляцию, на выщелачивание, или затем часть его (в сбалансированной ситуации часть рециркулированного раствора) направляют по меньшей мере на еще одну вторую стадию химического превращения, следующую после первой стадии химического превращения, где, например,Zn2+ и/или Pb2+ из раствора осаждают в виде сульфида в присутствии сульфида железа или в соответствии с реакциями (5) и (6) с участием пирротита (Fe1-xS), или в соответствии с реакциями (7) и (8), где добавляемым компонентом является троилит (FeS) Получение сульфида свинца (PbS) здесь требует основы в виде раствора, например хлоридного раствора или смешанного сульфатно-хлоридного раствора, в котором растворим Pb2+. В этих случаях сульфид цинка (ZnS) и сульфид свинца (PbS) можно осадить или совместно, или раздельно, в зависимости, помимо прочего, от соотношения содержания цинка и свинца и от дальнейшей обработки сульфида цинка и сульфида свинца. Использование Fe1-xS требует или условий автоклава, или использования восстановителя для Fe3+. Использование (FeS) при осаждении ZnS и PbS является предпочтительным, поскольку указанные реакции протекают очень быстро уже при комнатной температуре. Поскольку перед осаждением ZnS и PbS подаваемый раствор легко можно очистить известными спосо-3 009503 бами от типичных примесей Pb и Zn, вышеописанная часть процесса является очень подходящей предварительной стадией для пирометаллургического получения как Pb, так и Zn, помимо прочих. Использование пирита (FeS2) в качестве реагента для получения Fe1-xS или FeS может быть оправдано, например, если пирит получают в тонко измельченном виде уже как побочный продукт при переработке руды, или если поблизости отсутствует пирротит (Fe1-xS), или если пирротит следует добывать отдельно. Более того, FeS2 часто содержит среди прочего золото, которое затем можно выделить в ходе осаждения сульфида цинка и/или сульфида свинца. Кроме кислоты основным компонентом рециркулируемого раствора, полученного на стадии химического превращения в способе по данному изобретению и возвращенного на стадию выщелачивания,является железо. Железо удаляют в основном в связи с выщелачиванием второго типа сульфидного концентрата в виде оксида, гидроксида или гидроксо-щелочного ярозита. Для получения более высокого содержания железа жизнеспособным является также регенерирующий кислоту термогидролиз, проводимый при повышенной температуре. Однако фактор, который обеспечивает оптимальную экономику и эффективную работу для всего процесса в целом в способе по данному изобретению, связан с контролем по конкретным минералам на каждой промежуточной стадии и с тем фактом, что процессы флотации, применяемые для создания концентратов первого и второго типов, предпочтительно контролировать электрохимическими измерениями, специфичными для минералов, описанными, например, в патентах США 5108495 и 4561970. Подобные процедуры реализуют также для других стадий процесса, например выщелачивания и химического превращения. Таким образом, путем измерения и регулирования особенно химии серы, содержания растворимых компонентов и скорости окисления различных минералов непосредственно в ходе процесса, каждую промежуточную стадию реализуют наилучшим возможным образом. Например, с позиции выщелачивания руд на основе халькопирита (CuFeS2), содержащих драгоценные металлы, двумя очень важными деталями являются выщелачивание CuFeS2 при атмосферных условиях, если это необходимо, и выщелачивание золота и серебра, а также их соединений, в растворах на основе сульфатов и хлоридов, до суспензий, содержащих сульфидные соединения. Обычно выщелачивание CuFeS2 проводят в интервале температур 50-105 С. В этом случае, согласно способу по данному изобретению, например, получают драгоценные металлы в растворе с хорошим выходом. Кроме того, важно поддерживать заданную величину потенциала для самого CuFeS2 и определенные соотношения HSO32-, S2O32-, S4O62-, S5O62- и т.д. в растворе и на поверхностях минералов. При флотации использование соответствующих методов обеспечивает результаты, которые позволяют приблизиться к пределам, определенным степенью измельчения. Хорошая область при выщелачивании CuFeS2 обычно расположена, в зависимости от материала сырья, помимо прочего, в пределах +450 - +650 мВ относительно AgCl/Ag. В то же время, однако, потенциал Cu1,98S должен быть явно ниже, и, например, потенциал серебряного (Ag0) электрода должен предпочтительно быть менее +200 мВ. Подобным образом, при контроле выщелачивания золота золото и серебро переходят в раствор в виде тиосульфатных комплексов, и они получаются в продукте CuxS при химическом превращении совместно с драгоценными металлами из сульфидного концентрата первого типа. Низкий уровень потенциала при выщелачивании может привести, например, к осаждению сульфида серебраAgSx, в то время как высокий уровень потенциала создает обогащенные по сере политионаты, которые удаляют, например, золото из раствора несколькими различными путями. По существу, естественно, что эффективный раствор для выщелачивания должен содержать, помимо прочего, пирит, определенное количество сульфита, или углерод. Кроме того, для регулирования промежуточных стадий процесса можно с успехом использовать каталитические агенты, такие как никель и кобальт, содержащиеся в рециркулируемых растворах. Ниже данное изобретение описано более подробно со ссылкой на приложенный чертеж; который представляет собой блок-схему, иллюстрирующую предпочтительное исполнение данного изобретения. Согласно этому чертежу содержащую медь руду добывают в шахте 1, и извлеченную из шахты руду подразделяют на различные части: часть 2, не представляющую промышленной ценности, содержащую оксиды фракцию 3 и фракцию 4, которую следует сконцентрировать. Содержащую оксид фракцию 3 направляют на выщелачивание 5 оксида, куда подается часть сульфатного раствора 12, рециркулируемого со стадии 11 химического превращения способа по данному изобретению, и, если это желательно,также содержащий медь скрап 6. Раствор 20, полученный при выщелачивании оксида, направляют на выщелачивание концентрата 6 второго типа, в то время как нерастворимая часть идет в отходы 21 выщелачивания оксида. При концентрировании, проводимом путем флотации 19, фракцию 4 подразделяют на два концентрата: концентрат 7 первого типа, содержащий главным образом плохо растворимые компоненты, такие как драгоценные металлы, и концентрат 8 второго типа, содержащий главным образом растворимые компоненты. Концентрат 8 второго типа направляют на выщелачивание 9, куда подают также серную кислоту 10 и раствор 20, полученный при выщелачивании 5 оксида. На стадию 9 выщелачивания подают также по меньшей мере часть сульфатного раствора 12, полученного на стадии 11 химического превращения.-4 009503 На стадии 9 выщелачивания вторичный концентрат 8 (концентрат второго типа) на основе сульфида меди выщелачивают и нейтрализуют, так что при выщелачивании 9 железо получают в отходах 15. Раствор 13, полученный при выщелачивании 9, направляют на стадию 11 химического превращения, на которую также подают концентрат 7 первого типа, т.е. первичный концентрат. На стадии 11 химического превращения медь возвращают в сульфидную форму, содержащую драгоценные металлы, посредством сульфида железа из концентрата 7 первого типа, который подают на стадию 11 химического превращения. Сульфид 14 меди, содержащий драгоценные металлы, удаляют со стадии 11 химического превращения и направляют на дальнейшую переработку. Часть сульфатного раствора 12 со стадии 11 химического превращения возвращают на стадию 9 выщелачивания концентрата 8 второго типа и на стадию 5 выщелачивания оксида, в то время как часть сульфатного раствора 12 преимущественно направляют, например, на вторую стадию 16 химического превращения, например, для того, чтобы превратить цинк и свинец, содержащиеся в растворе, в сульфидную форму посредством сульфида 17 железа, подаваемого на стадию 16 химического превращения, и для удаления 18 цинка и свинца для дальнейшей обработки. Раствор со второй стадии 16 химического превращения объединяют с сульфатным раствором 12 с первой стадии 11 химического превращения и, соответственно, возвращают на предыдущие стадии обработки. Пример Способ по данному изобретению был применен к руде сульфид меди-пирит с низким содержанием цинка; общее обработанное количество составило 447 кг, содержащее 1,6 мас.% меди и 0,47 мас.% цинка. В связи с концентрацией при обработке из концентрата был отделен концентрат сульфида цинка, который был направлен на дальнейшую переработку отдельным известным способом. Согласно данному изобретению концентрат, который подвергали обработке, был для дальнейшей обработки разделен на две части: первичный концентрат (8,7 кг) и вторичный концентрат (32,4 кг). Первичный концентрат содержал большое количество плохо растворимого халькопирита (CuFeS2), так что этот первичный концентрат содержал 2,1 кг меди, 3,5 кг железа, 4,1 кг серы, а также небольшое количество - 0,1 кг цинка. Кроме меди вторичный концентрат содержал большое количество пирита (FeS2), так что вторичный концентрат содержал 4,2 кг меди, 11,7 кг железа и 13,8 кг серы, а также 0,7 кг цинка. Вторичный концентрат сначала был направлен на выщелачивание серной кислотой, проводимое при температуре 100-105 С в окислительных условиях. Содержащий серную кислоту раствор, полученный при выщелачивании, содержащий 77 г/л меди, 59 г/л цинка и 30 г/л железа, был далее направлен на стадию химического превращения, проводимую при температуре 160-170 С, куда также подавали первичный концентрат. Согласно реакции (4), в принципе, медь, содержащуюся в растворе, превращали,посредством железа, содержащегося в первичном концентрате, в форму сульфида меди (CuxS); в то время как уже находящаяся в форме сульфида медь, содержащаяся в первичном концентрате, оставалась сульфидной. Полученное количество концентрата составило 10,7 кг, содержащее 5,9 кг меди. Раствор, полученный на стадии химического превращения, который согласно реакции (4), в принципе, содержал железо, переведенное в растворимую форму, а также цинк, был частично возвращен на стадию выщелачивания вторичного концентрата, где было удалено 40,1 кг железа в виде остатка после выщелачивания и в виде осадка ярозита. Часть раствора с этой первой стадии химического превращения была направлена на вторую стадию химического превращения, где цинк был осажден посредством троилита (FeS) в виде сульфида, принципиально в соответствии с реакцией (7). Полученное количество концентрата сульфида цинка составило 1,2 кг, и его объединили с концентратом сульфида цинка, полученным в связи со стадией концентрирования, и направили на дальнейшую переработку. Раствор сульфата железа, полученный на второй стадии химического превращения, был возвращен совместно с раствором,полученным на первой стадии химического превращения, на стадию выщелачивания вторичного концентрата. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ переработки руд на основе сульфида меди, включающий их концентрирование, отличающийся тем, что при концентрировании (19) руду (4) разделяют на два сульфидных концентрата различного типа: первичный концентрат (7), в основном содержащий плохо растворимые компоненты, такие как халькопирит и содержащиеся в руде драгоценные металлы, и вторичный концентрат (8), в основном содержащий хорошо растворимые компоненты, такие как сульфид меди, прочие ценные сульфиды из руды и пирит; при этом вторичный концентрат (8) направляют на стадию (9) выщелачивания, а раствор (13), полученный на указанной стадии выщелачивания, и первичный концентрат подают по меньшей мере на одну стадию (11) химического превращения, где, по меньшей мере, медь, содержащуюся в растворе, превращают в сульфидную форму посредством сульфидной формы железа из первичного концентрата (7), при этом по меньшей мере часть раствора (12), полученного на стадии (11) химического превращения, возвращают на стадию (9) выщелачивания вторичного концентрата. 2. Способ по п.1, отличающийся тем, что он включает вторую стадию (16) химического превращения, следующую за первой стадией (11) химического превращения, где различные металлические компоненты превращают в сульфидную форму посредством железа (17) в сульфидной форме, подаваемого на-5 009503 указанную стадию химического превращения. 3. Способ по п.1 или 2, отличающийся тем, что выщелачивание (9) проводят при атмосферном давлении при температуре 50-105 С. 4. Способ по п.1 или 2, отличающийся тем, что выщелачивание (9) проводят в автоклаве. 5. Способ по любому из пп.1-4, отличающийся тем, что по меньшей мере одну стадию (11, 16) химического превращения проводят при температуре 90-200 С. 6. Способ по п.5, отличающийся тем, что по меньшей мере одну стадию (11, 16) химического превращения проводят при температуре 150-190 С. 7. Способ по любому из пп.1-6, отличающийся тем, что железо на первой стадии (11) химического превращения представляет собой халькопирит (CuFeS2). 8. Способ по любому из пп.1-7, отличающийся тем, что железо, добавляемое на второй стадии (16) химического превращения, представляет собой троилит (FeS). 9. Способ по любому из пп.1-6, отличающийся тем, что железо, добавляемое на второй стадии (16) химического превращения, представляет собой пирротит (Fe1-xS). 10. Способ по любому из пп.1-9, отличающийся тем, что концентрирование (19) руды осуществляют путем флотации, процесс которой контролируют посредством специфичных по отношению к минералам электрохимических измерений. 11. Способ по любому из пп.1-10, отличающийся тем, что стадию (9) выщелачивания, используемую при обработке концентрата, контролируют посредством специфичных по отношению к минералам электрохимических измерений. 12. Способ по любому из пп.1-11, отличающийся тем, что стадии (11, 16) химического превращения, используемые при обработке концентрата, контролируют посредством специфичных по отношению к минералам электрохимических измерений. 13. Способ по любому из пп.1-12, отличающийся тем, что на первой стадии (11) химического превращения извлекают драгоценные металлы, содержащиеся в концентратах.
МПК / Метки
МПК: C22B 15/00, C22B 3/44
Метки: способ, руд, переработки, основе, меди, сульфида
Код ссылки
<a href="https://eas.patents.su/7-9503-sposob-pererabotki-rud-na-osnove-sulfida-medi.html" rel="bookmark" title="База патентов Евразийского Союза">Способ переработки руд на основе сульфида меди</a>
Предыдущий патент: Тонкая сигарета
Следующий патент: Способ прямого восстановления металлоносного сырьевого материала
Случайный патент: Способ получения циталопрама











