Способ получения сложного эфира n-замещенной карбаминовой кислоты, способ получения изоцианата с применением такого сложного эфира n-замещенной карбаминовой кислоты и композиция для транспортировки и хранения сложного эфира n-замещенной карбаминовой кислоты, содержащая сложный эфир n-замещенной карбаминовой кислоты и ароматическое гидроксисоединение
Формула / Реферат
1. Способ получения сложного эфира N-замещенной карбаминовой кислоты, получаемого из органического амина, производного угольной кислоты и гидроксикомпозиции, содержащей один или несколько видов гидроксисоединений,
в котором органический амин, производное угольной кислоты и гидроксикомпозиция реагируют с применением реакционного резервуара для получения уретана, снабженного конденсатором,
газ, содержащий гидроксикомпозицию, соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, и аммиак, образованный в качестве побочного продукта в ходе реакционного взаимодействия, вводится в конденсатор, предусмотренный в реакционном резервуаре для получения уретана, и гидроксикомпозиция и соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, конденсируются, и
в котором отношение гидроксисоединения, содержащегося в конденсированной гидроксикомпозиции к конденсированному соединению, имеющему карбонильную группу, полученному из производного угольной кислоты, составляет 1 или более, в расчете на стехиометрическое соотношение, и
соотношение числа карбонильных групп (-С(=O)-), содержащихся в соединении, имеющем карбонильную группу, которое образовано из производного угольной кислоты, и числа молекул аммиака, содержащихся в аммиаке, который извлечен в виде газа из конденсатора, составляет 1 или менее.
2. Способ получения по п.1, в котором гидроксисоединение является спиртом или ароматическим гидроксисоединением.
3. Способ получения по п.1, в котором гидроксикомпозиция и/или соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, которое сконденсировано конденсатором, используются повторно в реакционном взаимодействии.
4. Способ получения по п.1, в котором гидроксикомпозиция и соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, которое сконденсировано конденсатором, циркулируют внутри реакционного резервуара для получения уретана.
5. Способ получения по п.1, в котором производное угольной кислоты является карбамидом и/или сложным эфиром карбаминовой кислоты.
6. Способ получения по п.1, в котором сложный эфир N-замещенной карбаминовой кислоты получают посредством процесса, содержащего следующие стадии (а) и (b):
стадия (а): стадия получения реакционной смеси, содержащей соединение, имеющее уреидогруппу, посредством реакционного взаимодействия органического амина и производного угольной кислоты; и
стадия (b): стадия получения сложного эфира N-замещенной карбаминовой кислоты посредством реакционного взаимодействия соединения, имеющего уреидогруппу, которое получено на стадии (а), и гидроксикомпозиции при применении реакционного резервуара для получения уретана, снабженного конденсатором,
в котором газ, содержащий гидроксикомпозицию, соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, и аммиак, полученный в качестве побочного продукта в ходе реакционного взаимодействия, вводится в конденсатор, предусмотренный в реакционном резервуаре для получения уретана, и гидроксикомпозиция и соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, конденсируются.
7. Способ получения по п.6, в котором гидроксисоединение является спиртом или ароматическим гидроксисоединением.
8. Способ получения по п.6, в котором производное угольной кислоты на стадии (а) является карбамидом и/или сложным эфиром карбаминовой кислоты.
9. Способ получения по п.6, в котором реакционное взаимодействие на стадии (а) выполняется в присутствии соединения, выбранного из группы, состоящей из воды, спирта и ароматического гидроксисоединения.
10. Способ получения по п.6, в котором гидроксикомпозиция и/или соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, которое конденсировано конденсатором на стадии (b), используется повторно в реакционном взаимодействии на стадии (а).
11. Способ получения по п.5 или 8, в котором сложный эфир карбаминовой кислоты является сложным эфиром карбаминовой кислоты, полученным в соответствии со следующей стадией (с):
стадия (с): стадия получения сложного эфира карбаминовой кислоты посредством реакционного взаимодействия гидроксикомпозиции с (при этом гидроксикомпозиция с обозначает композицию, содержащую один или несколько видов гидроксисоединений) и карбамида.
12. Способ получения по п.11, в котором гидроксисоединение, которое образует гидроксикомпозицию с, является спиртом и/или ароматическим гидроксисоединением.
13. Способ получения по п.1 или 6, в котором конденсированная гидроксикомпозиция и/или соединение, имеющее карбонильную группу, полученное из сложного эфира карбаминовой кислоты, используется повторно на стадии (с).
14. Способ получения сложного эфира N-замещенной карбаминовой кислоты из органического амина, производного угольной кислоты и гидроксикомпозиции, содержащей один или несколько видов гидроксисоединений, данный способ содержит следующие стадии (а) и (b):
стадия (а): стадия получения реакционной смеси, содержащей соединение, имеющее уреидогруппу, посредством реакционного взаимодействия органического амина и производного угольной кислоты; и
стадия (b): стадия получения сложного эфира N-замещенной карбаминовой кислоты посредством реакционного взаимодействия соединения, имеющего уреидогруппу, которое получено на стадии (а), и гидроксикомпозиции при применении реакционного резервуара для получения уретана, снабженного конденсатором,
в котором газ, содержащий гидроксикомпозицию, соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, и аммиак, полученный в качестве побочного продукта в ходе реакционного взаимодействия, вводится в конденсатор, предусмотренный в реакционном резервуаре для получения уретана, и гидроксикомпозиция и соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, конденсируются.
15. Способ получения по п.14, в котором гидроксисоединение является спиртом и/или ароматическим гидроксисоединением.
16. Способ получения по п.14, в котором производное угольной кислоты на стадии (а) является карбамидом и/или сложным эфиром карбаминовой кислоты.
17. Способ получения по п.14, в котором реакционное взаимодействие на стадии (а) выполняется в присутствии соединения по меньшей мере одного вида, выбранного из группы, состоящей из воды, спирта и ароматического гидроксисоединения.
18. Способ получения по п.14, в котором гидроксикомпозиция и/или соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, которое конденсировано конденсатором на стадии (b), используется повторно на стадии (а).
19. Способ получения по п.16, в котором сложный эфир карбаминовой кислоты является сложным эфиром карбаминовой кислоты, полученным в соответствии со следующей стадией (с):
стадия (с): стадия получения сложного эфира карбаминовой кислоты посредством реакционного взаимодействия гидроксикомпозиции с и карбамида.
20. Способ получения по п.19, в котором гидроксисоединение, которое образует гидроксикомпозицию с, является спиртом и/или ароматическим гидроксисоединением.
21. Способ получения по п.19, в котором конденсированная гидроксикомпозиция и/или соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, используется повторно на стадии (с).
22. Способ получения по п.1 или 14, в котором реакционный резервуар для получения уретана является реакционным резервуаром в виде бака и/или в виде колонны, снабженным конденсатором.
23. Способ получения по п.1 или 14, в котором реакционный резервуар для получения уретана имеет газовую фазу, которая содержит гидроксикомпозицию, соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, и аммиак, образованный в качестве побочного продукта в ходе реакционного взаимодействия, и жидкую фазу, в которой выполняется реакционное взаимодействие, и объемное содержание жидкой фазы в реакционном резервуаре для получения уретана составляет 50% или менее.
24. Способ получения по любому из пп.2, 7 или 15, в котором гидроксисоединение является ароматическим гидроксисоединением, органический амин является соединением, представленным приведенной формулой (1), и полученный сложный эфир N-замещенной карбаминовой кислоты является О-Ar сложным эфиром N-замещенной карбаминовой кислоты, представленным приведенной формулой (2)
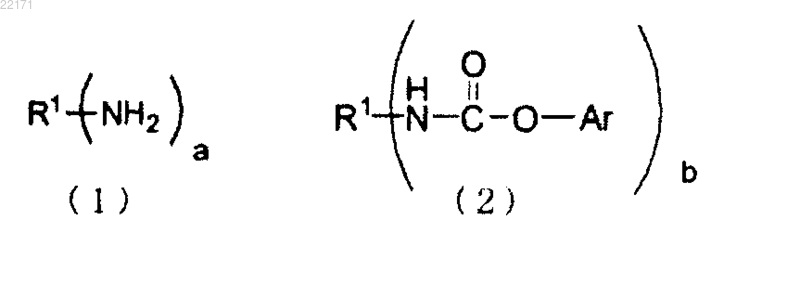
где R1 обозначает органическую группу, которая имеет от 1 до 85 атомов углерода и которая замещена а аминогруппами;
Ar обозначает группу, производную от ароматического гидроксисоединения, которая является остатком, в котором единственная гидроксильная группа, связанная с ароматическим кольцом ароматического гидроксисоединения, удалена;
а обозначает целое число от 1 до 10;
b обозначает целое число от 1 до 10.
25. Способ получения по любому из пп.2, 7 или 15, в котором гидроксисоединение является спиртом, органический амин является соединением, представленным приведенной формулой (3), и полученный сложный эфир N-замещенной карбаминовой кислоты является О-R2 сложным эфиром N-замещенной карбаминовой кислоты, представленным приведенной формулой (4)

где R1 обозначает органическую группу, которая имеет от 1 до 85 атомов углерода и которая замещена а аминогруппами;
R2 обозначает группу, производную от спирта, которая является остатком, в котором единственная гидроксильная группа, связанная с насыщенным атомом углерода спирта, удалена из спирта;
а обозначает целое число от 1 до 10;
с обозначает целое число от 1 до 10.
26. Способ получения по п.4, в котором О-Ar сложный эфир N-замещенной карбаминовой кислоты, представленный приведенной формулой (5) и имеющий группу сложного эфира, производную от ароматического гидроксисоединения, производится посредством реакционного взаимодействия О-R2 сложного эфира N-замещенной карбаминовой кислоты, представленного формулой (4) выше, и ароматического гидроксисоединения
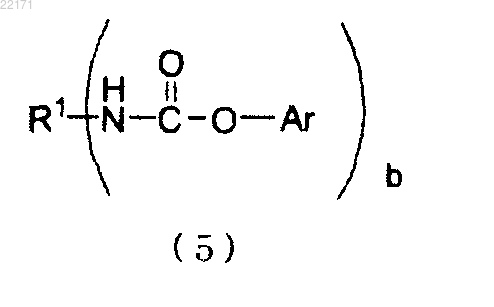
где R1 обозначает органическую группу, которая имеет от 1 до 85 атомов углерода и которая замещена а аминогруппами;
Ar обозначает группу, производную от ароматического гидроксисоединения, которая является остатком, в котором единственная гидроксильная группа, связанная с ароматическим кольцом ароматического гидроксисоединения, удалена из ароматического гидроксисоединения;
b обозначает целое число от 1 до 10.
27. Способ получения по п.24 или 26, в котором ароматическое гидроксисоединение является ароматическим гидроксисоединением с валентностью от единицы до трех (т.е. число гидроксильных групп, связанных с ароматическим кольцом, является целым числом от 1 до 3).
28. Способ получения по п.27, в котором ароматическое гидроксисоединение является ароматическим гидроксисоединением, представленным приведенной формулой (7)
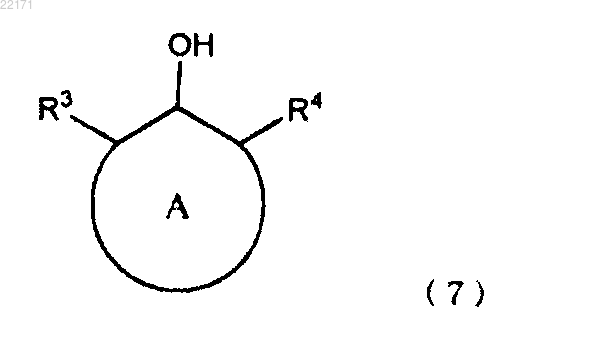
где кольцо А обозначает необязательно замещенный одноядерный или многоядерный ароматический углеводород;
R3 и R4 соответственно и независимым образом обозначают атом водорода или органическую группу;
число атомов углерода, которые образуют ароматическое гидроксисоединение, является целым числом от 6 до 50;
R3 и R4 могут образовывать кольцевую структуру посредством связывания с А.
29. Способ получения по п.28, в котором по меньшей мере одно из ароматических гидроксисоединений, которые образуют гидроксикомпозицию, является ароматическим гидроксисоединением, представленным приведенной формулой (8)
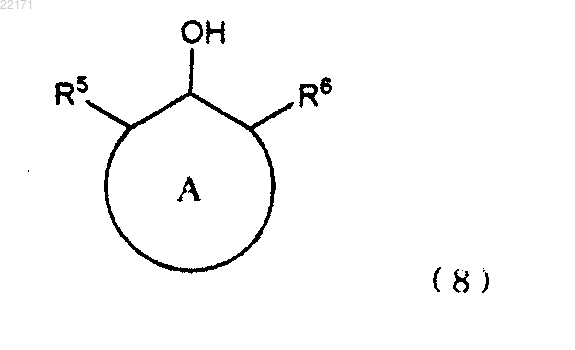
где кольцо А обозначает необязательно замещенный одноядерный или многоядерный ароматический углеводород;
R5 и R6 соответственно и независимым образом обозначают любую группу, определенную в пунктах (i)-(v) ниже;
число атомов углерода, которые образуют ароматическое гидроксисоединение, является целым числом от 6 до 50;
R5 и R6 могут образовывать кольцевую структуру посредством связывания с А:
(i) атом водорода,
(ii) атом галогена,
(iii) группа, в которой атом в α-положении является атомом азота и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода (за исключением водорода, связанного с атомом азота в α-положении), атом азота является вторичным атомом азота (т.е. атомом азота, который образует связь -NH-),
(iv) группа, в которой атом в α-положении является атомом углерода и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода, атом углерода является первичным или вторичным атомом углерода (т.е. углеродом метильной группы или углеродом, который образует связь -СН2-), при условии, что в случае, когда R5 и/или R6 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с ароматическим кольцом А, и конденсированное кольцо имеет 6 элементов или менее, атом углерода в α-положении может быть третичным или четвертичным атомом углерода, и также в случае, когда углерод в α-положении образует двойную или тройную связь с атомом в β-положении (атомом, который образует R5 и R6 и который также является смежным с атомом, связанным с ароматическим кольцом кольца А), атом углерода в α-положении может быть третичным или четвертичным атомом углерода, и
(v) группа, в которой атом в α-положении является атомом кислорода и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода.
30. Способ получения по п.29, в котором гидроксикомпозиция содержит ароматическое гидроксисоединение, представленное выше формулой (8), вместе с ароматическим гидроксисоединением, представленным приведенной формулой (9)
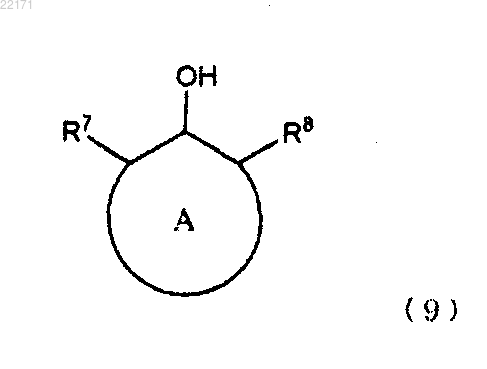
где кольцо А обозначает необязательно замещенный одноядерный или многоядерный ароматический углеводород;
R7 и R8 соответственно и независимым образом обозначают любую группу, определенную в пунктах (i)-(v) ниже;
число атомов углерода, которые образуют ароматическое гидроксисоединение, является целым числом от 6 до 50;
R7 и R8 могут образовывать кольцевую структуру посредством связывания с А:
(i) атом водорода,
(ii) атом галогена,
(iii) группа, в которой атом в α-положении является атомом азота и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода, атом азота является третичным атомом азота (т.е. атомом азота, который не имеет атома водорода),
(iv) группа, в которой атом в α-положении является атомом углерода и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода, атом углерода в α-положении является третичным или четвертичным атомом углерода (т.е. атомом углерода, который образует связь -СН-, или атомом углерода, не связанным с водородом); в случае, когда R7 и/или R8 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с ароматическим кольцом А, и конденсированное кольцо имеет 7 элементов или более, атом углерода в α-положении может быть первичным или вторичным атомом углерода (т.е. атомом углерода метильной группы или атомом углерода, который образует связь -СН2-); в случае, когда углерод в α-положении образует двойную связь с атомом в β-положении, углерод в α-положении является четвертичным углеродом; и группы, в которых углерод в α-положении образует тройную связь с атомом в β-положении, исключаются, и
(v) группа, в которой атом в α-положении является атомом кислорода и число атомов углерода составляет от 1 до 24 и которая не содержит активного водорода.
31. Способ получения по любому из пп.28, 29 или 30, в котором стандартная температура кипения ароматического гидроксисоединения, представленного формулами (7), (8) или (9), отличается на 10°С или более от стандартной температуры кипения изоцианата, в котором все аминогруппы органического амина замещены изоцианатными группами (группами -NCO).
32. Способ получения по п.24 или 26, в котором органический амин является органическим моноамином, представленным приведенной формулой (10), получают О-Ar сложный моноэфир N-замещенной карбаминовой кислоты, представленный приведенной формулой (11), и О-Ar сложный моноэфир N-замещенной карбаминовой кислоты применяют для получения О-Ar сложного полиэфира N-замещенной карбаминовой кислоты, представленного приведенной формулой (12), посредством выполнения следующей стадии (X):
стадия (X): О-Ar сложный моноэфир N-замещенной карбаминовой кислоты и метиленирующий агент реагируют с образованием поперечно сшитых связей ароматических групп, производных от органического моноамина, содержащегося в О-Ar сложном моноэфире N-замещенной карбаминовой кислоты, с метиленовыми группами (-СН2-) таким образом, чтобы получить O-Ar сложный полиэфир N-замещенной карбаминовой кислоты, представленный приведенной формулой (12)
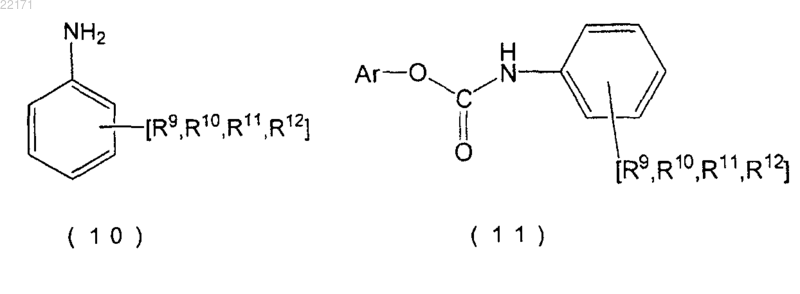
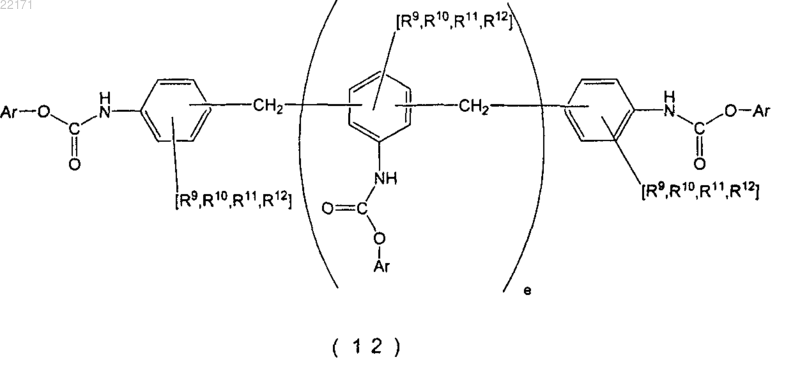
где Ar обозначает группу, производную от ароматического гидроксисоединения, которая является остатком, в котором единственная гидроксильная группа, связанная с ароматическим кольцом ароматического гидроксисоединения, удалена;
R9-R12 могут соответственно и независимым образом замещать ароматическое кольцо, R9-R12 могут взаимно соединяться, чтобы образовывать кольцо с ароматическим кольцом, и представляют атом водорода или группу, состоящую из групп, в которых алкильная группа, циклоалкильная группа, арильная группа или группа, выбранная из группы, состоящей из этих групп, связана насыщенными углеводородными связями и/или эфирными связями;
е обозначает 0 или положительное целое число;
общее число атомов углерода, которое содержит органический моноамин, представленный формулой (10), является целым числом от 6 до 50.
33. Способ получения по п.25, в котором органический амин является органическим моноамином, представленным приведенной формулой (13), получают О-R2 сложный моноэфир N-замещенной карбаминовой кислоты, представленный приведенной формулой (14), и О-R2 сложный моноэфир N-замещенной карбаминовой кислоты применяют для получения О-Ar сложного полиэфира N-замещенной карбаминовой кислоты, представленного приведенной формулой (16), посредством выполнения следующих стадий (X) и (Y):
стадия (X): О-R2 сложный моноэфир N-замещенной карбаминовой кислоты и метиленирующий агент реагируют с образованием поперечно сшитых связей ароматических групп, производных от органического моноамина, содержащегося в O-R2 сложном моноэфире N-замещенной карбаминовой кислоты, с метиленовыми группами (-СН2-) таким образом, чтобы получить O-R2 сложный полиэфир N-замещенной карбаминовой кислоты, представленный приведенной формулой (15); и
стадия (Y): O-R2 сложный полиэфир N-замещенной карбаминовой кислоты, полученный на стадии (X), реагирует с ароматическим гидроксисоединением, чтобы получить О-Ar сложный полиэфир N-замещенной карбаминовой кислоты, имеющий группы сложного эфира, производные от ароматического гидроксисоединения, представленный приведенной формулой (16)
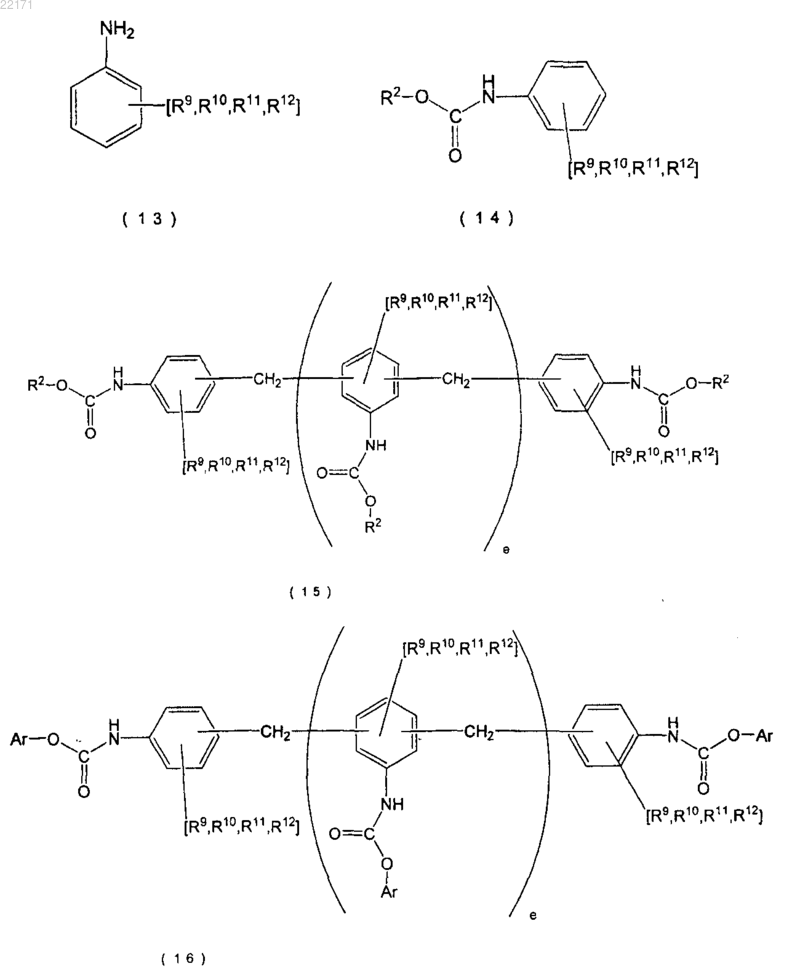
где R9-R12 могут соответственно и независимым образом замещать ароматическое кольцо, R9-R12 могут взаимно соединяться, чтобы образовывать кольцо с ароматическим кольцом, и представляют атомы водорода или группы, состоящие из групп, в которых алкильная группа, циклоалкильная группа, арильная группа или группа, выбранная из группы, состоящей из этих групп, связана насыщенными углеводородными связями и/или эфирными связями;
R2 обозначает группу, производную от спирта, которая является остатком, в котором единственная гидроксильная группа, связанная с насыщенным атомом углерода спирта, удалена из спирта;
Ar обозначает группу, производную от ароматического гидроксисоединения, которая является остатком, в котором единственная гидроксильная группа, связанная с ароматическим кольцом ароматического гидроксисоединения, удалена из ароматического гидроксисоединения;
е обозначает 0 или положительное целое число;
общее число атомов углерода, которое содержит органический моноамин, представленный формулой (13), является целым числом от 6 до 50.
34. Способ получения изоцианата, содержащий извлечение изоцианата и ароматического гидроксисоединения, которые образованы посредством выполнения реакции термического разложения для О-Ar сложного эфира N-замещенной карбаминовой кислоты по любому из пп.24, 26, 32 и 33.
35. Способ получения по п.34, в котором извлеченное ароматическое гидроксисоединение по п.34 используется повторно в качестве ароматического гидроксисоединения по п.2, и/или ароматического гидроксисоединения по п.7, и/или ароматического гидроксисоединения по п.9, и/или ароматического гидроксисоединения по п.12, и/или ароматического гидроксисоединения по п.15, и/или ароматического гидроксисоединения по п.17, и/или ароматического гидроксисоединения по п.20.
36. Способ получения по п.34, в котором остаточная жидкость, содержащая непрореагировавший О-Ar сложный эфир N-замещенной карбаминовой кислоты, извлеченный из нижней части реакционного резервуара для термического разложения, снова переносится в реакционный резервуар для термического разложения, и О-Ar сложный эфир N-замещенной карбаминовой кислоты подвергается реакции термического разложения.
37. Способ получения по п.34, в котором изоцианат, полученный в способе получения по п.34, содержит от 1 до 1000 млн-1 ароматического гидроксисоединения, которое образует ароматическую гидроксикомпозицию, в расчете на изоцианат.
38. Способ получения по любому из пп.1, 11, 14 или 19, в котором аммиак, извлеченный в виде газа, реагирует с диоксидом углерода, чтобы получить карбамид, и данный карбамид используется повторно.
Текст
СПОСОБ ПОЛУЧЕНИЯ СЛОЖНОГО ЭФИРА N-ЗАМЕЩЕННОЙ КАРБАМИНОВОЙ КИСЛОТЫ, СПОСОБ ПОЛУЧЕНИЯ ИЗОЦИАНАТА С ПРИМЕНЕНИЕМ ТАКОГО СЛОЖНОГО ЭФИРА N-ЗАМЕЩЕННОЙ КАРБАМИНОВОЙ КИСЛОТЫ И КОМПОЗИЦИЯ ДЛЯ ТРАНСПОРТИРОВКИ И ХРАНЕНИЯ СЛОЖНОГО ЭФИРАN-ЗАМЕЩЕННОЙ КАРБАМИНОВОЙ КИСЛОТЫ, СОДЕРЖАЩАЯ СЛОЖНЫЙ ЭФИР N-ЗАМЕЩЕННОЙ КАРБАМИНОВОЙ КИСЛОТЫ И АРОМАТИЧЕСКОЕ ГИДРОКСИСОЕДИНЕНИЕ Данное изобретение представляет собой способ получения сложного эфира N-замещенной карбаминовой кислоты, получаемого из органического амина, производного угольной кислоты и гидроксикомпозиции, содержащей один или несколько видов гидроксисоединений, в котором органический амин, производное угольной кислоты и гидроксикомпозиция реагируют с применением реакционного резервуара для получения уретана, снабженного конденсатором, газ,содержащий гидроксикомпозицию, соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, и аммиак, образованный в качестве побочного продукта в ходе реакционного взаимодействия, вводится в конденсатор, предусмотренный в реакционном резервуаре для получения уретана, и гидроксикомпозиция и соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, конденсируются, и в котором гидроксисоединение, содержащееся в сконденсированной гидроксикомпозиции, содержится,в расчете на стехиометрическое соотношение, в количестве 1 или более по отношению к сконденсированному соединению, имеющему карбонильную группу, образованному из производного угольной кислоты, и соотношение числа карбонильных групп (-С(=O)-),содержащихся в соединении, имеющем карбонильную группу, полученное из производного угольной кислоты, и числа молекул аммиака, содержащихся в аммиаке, извлеченном в виде газа из конденсатора, составляет 1 или менее.(71)(73) Заявитель и патентовладелец: АСАХИ КАСЕИ КЕМИКАЛЗ КОРПОРЕЙШН (JP) Область техники Данное изобретение относится к способу получения сложного эфира N-замещенной карбаминовой кислоты, способу получения изоцианата, в котором применяется этот сложный эфир N-замещенной карбаминовой кислоты, и композиции для транспортировки и хранения сложного эфира N-замещенной карбаминовой кислоты, содержащей сложный эфир N-замещенной карбаминовой кислоты и ароматическое гидроксисоединение. Уровень техники Изоцианаты широко применяются в качестве исходных веществ при производстве таких продуктов,как пенополиуретан, лакокрасочные материалы и адгезивы. Основной промышленный способ производства изоцианатов содержит реакционное взаимодействие амина с фосгеном (способ фосгенирования), и почти все количество изоцианатов, производимых в мире, производится способом фосгенирования. Однако способ фосгенирования имеет много недостатков. Во-первых, этот способ требует применения большого количества фосгена в качестве исходного вещества. Фосген чрезвычайно токсичен и требует особых мер предосторожности при обращении, чтобы предотвратить его воздействие на оператора, и также требует специального оборудования для утилизации отходов. Во-вторых, поскольку высококоррозионный хлористый водород образуется в больших количествах в качестве побочного продукта способа фосгенирования, то, в дополнение к необходимости в процессе для утилизации хлористого водорода, во многих случаях в произведенных изоцианатах содержится гидролитический хлор, который может оказывать отрицательное влияние на устойчивость к атмосферным воздействиям и теплостойкость полиуретановых продуктов в случае применения изоцианатов, произведенных способом фосгенирования. По указанным выше причинам предпринимаются попытки разработки способа получения изоцианатных соединений, в котором не используется фосген. Хотя примеры таких способов включают способ синтеза алифатического изоцианата из алифатического нитросоединения и монооксида углерода и способ преобразования алифатического амидного соединения в изоцианат разложением Хоффмана, оба эти способа имеют низкий выход и не подходят для промышленного применения. Давно известны способы получения изоцианата и гидроксисоединения термическим разложением сложного эфира N-замещенной карбаминовой кислоты, примеры которых могут включать способ, разработанный A.W. Hoffmann (см. непатентный документ 1). Этот способ делает возможным достижение высокого выхода более легким образом, чем способы, описанные выше, и основные реакции, используемые в этом способе, указаны ниже:R' обозначает одновалентный органический остаток;n обозначает целое число, равное 1 или более. Термическое разложение, представленное приведенными выше общими формулами, является обратимым, и хотя его равновесие смещено в сторону сложного эфира N-замещенной карбаминовой кислоты при низких температурах, направление к изоцианату и гидроксисоединению становится выгодным при высоких температурах. Таким образом, термическое разложение сложного эфира N-замещенной карбаминовой кислоты связано с жесткими условиями реакции, такими как то, что оно выполняется при высоких температурах,а также с сопутствующим протеканием различных необратимых побочных реакций. Как указано в публикации Schiff (см. непатентный документ 2) и исследовании Е. Dyer и G.C.Wright (см. непатентный документ 3), примеры таких побочных реакций могут включать такие реакции,которые приводят к образованию замещенных карбамидов, биуретов, уретодионов, карбодиимидов и изоциануратов. Эти побочные реакции не только вызывают уменьшение селективности и выхода целевого изоцианата, но также способствуют образованию полимеров, в особенности, во время производства полиизоцианата, и, в зависимости от обстоятельств, могут вызывать состояние, которое затрудняет долговременное функционирование, например вызывать засорение реактора вследствие осаждения твердого полимерного вещества. Большинство нежелательных побочных реакций происходит при повышенных температурах, при длительных временах реакции, и образованный изоцианат имеет тенденцию к дополнительному увеличению продолжительности соприкосновения с каждым из компонентов реакционной смеси. К настоящему времени предложены различные способы, относящиеся к достижению подходящего выхода изоцианата посредством сдерживания образования продуктов нежелательных побочных реакций во время термического разложения сложных эфиров N-замещенной карбаминовой кислоты. Во-первых, в отношении способов получения промежуточного продукта в виде сложного эфира N-1 022171 замещенной карбаминовой кислоты раскрыто несколько способов получения сложного эфира Nзамещенной карбаминовой кислоты, в которых не применяется фосген. Например, патентный документ 1 описывает способ окислительного уретанирования с применением первичного амина, монооксида углерода и алифатического спирта или ароматического гидроксисоединения в качестве исходных веществ и с применением катализатора на базе благородного металла. Однако поскольку этот способ использует высокотоксичный монооксид углерода и дорогой катализатор на базе благородного металла, то имели место такие проблемы, как необходимость в усложненном процессе и чрезмерные затраты для извлечения катализатора из продукта в виде сложного эфира N-замещенной карбаминовой кислоты. Кроме того, патентный документ 2 описывает способ получения О-арилового сложного эфира Nзамещенной карбаминовой кислоты реакционным взаимодействием N-алкил-N,N'-диалкилкарбамида,ароматического гидроксисоединения и газообразного хлористого водорода. Однако этот способ использует корродирующий газообразный хлористый водород, потребляет дорогостоящее и не являющееся обычным карбамидное соединение и имеет такие проблемы, как необходимость в усложненном процессе и чрезмерные затраты для извлечения O-арилового сложного эфира N-замещенной карбаминовой кислоты из гидрохлорида N,N'-диалкиламина, образованного в качестве побочного продукта. Были предложены способы с применением карбамида или производного угольной кислоты (такого как сложный эфир угольной кислоты или сложный эфир карбаминовой кислоты) в качестве способов получения сложного эфира N-замещенной карбаминовой кислоты, которые являются альтернативами способам с применением дорогостоящих исходных веществ или катализаторов и т.п., подобным способам, описанным выше. Патентный документ 3 описывает способ получения алифатического сложного эфира Nзамещенной карбаминовой кислоты, в котором не применяется фосген, в котором 1,3-дизамещенный карбамид производится из первичного амина и карбамид на первой стадии, и сложный эфир Nзамещенной карбаминовой кислоты производится на второй стадии посредством реакционного взаимодействия 1,3-дизамещенного карбамида с гидроксисоединением с последующим отделением и извлечением первичного амина, образованного в качестве побочного продукта, и возвратом его на первую стадию. Однако не только выход образованного сложного эфира N-замещенной карбаминовой кислоты является низким, но также требуется и дополнительное оборудование для повторного использования первичного амина, что чрезвычайно усложняет данный процесс и делает этот способ неудовлетворительным для промышленного применения. Пример способа получения O-алкилового сложного эфира N-замещенной карбаминовой кислоты с применением карбамида или производного угольной кислоты раскрыт в патентном документе 4, в котором диамин, спирт и карбамид реагируют с преобразованием в О-алкиловый сложный эфир Nзамещенной карбаминовой кислоты. Патентный документ 5 раскрывает способ получения О-алкилового сложного эфира N-замещенной карбаминовой кислоты после первоначального получения бис-карбамида из алифатического первичного полиамина, карбамида и спирта, в то время как патентный документ 6 раскрывает способ получения О-алкилового сложного эфира N-замещенной карбаминовой кислоты посредством парциального реакционного взаимодействия карбамида и спирта на первой стадии и последующей подачи диамина на следующей, второй, стадии. Однако поскольку О-алкиловые сложные эфиры N-замещенной карбаминовой кислоты, полученные этими способами, термически чрезвычайно стабильные, то реакция термического разложения, которая образует изоцианаты из этих О-алкиловых сложных эфиров N-замещенной карбаминовой кислоты,требует высокой температуры, которая вызывает образование полимеров вследствие нежелательных побочных реакций (например, реакций, представленных формулами (С)-(Е), приведенными ниже). Кроме того, хотя карбамид обычно добавляется в избытке, чтобы получить N-(алифатическая группа)замещенный-О-алкилуретан при высоком выходе, вследствие того, что остаточный избыток карбамида сам по себе подвергается реакции термического разложения при температурах 130 С или выше, образуются изоциановая кислота и газообразный аммиак (см., например, формулу (F), приведенную ниже), или изоциановая кислота образует биуреты, которые затем подвергаются термическому разложению при температурах 200 С или выше (см., например, формулы (G) и (Н), приведенные далее), что способствует образованию полимеров и т.п. (см., например, формулы (I)-(L), приведенные далее). Поскольку эти полимеры и т.п. имеют чрезвычайно низкую растворимость в растворителях и т.п., они часто прилипают к реакционному резервуару или затвердевают в нем, что делает эти способы не подходящими для промышленных масштабов. Кроме того, поскольку отсутствует описание в отношении извлечения карбамида или производного угольной кислоты, применяемого в избытке, то невозможно было избежать увеличенного количества применяемого карбамида или производного угольной кислоты.R' обозначает алифатическую группу; а обозначает целое число, равное 0 или более. Кроме того, хотя для упрощения пояснения приведенные выше формулы представляют реакции в случае, когда R обозначает двухвалентный органический остаток и R' обозначает одновалентный органический остаток, можно легко предположить, что подобные реакции протекают даже в случае, когда R и R' имеют валентность 2 или более. В отношении этого момента известно, что О-ариловые сложные эфиры N-замещенной карбаминовой кислоты легко разлагаются до их соответствующих изоцианатов и ароматических гидроксисоединений (см., например, непатентный документ 4), и раскрыто несколько способов получения О-ариловых сложных эфиров N-замещенной карбаминовой кислоты. Патентный документ 7 раскрывает способ получения алифатического О-арилового сложного эфираN-замещенной карбаминовой кислоты посредством одностадийной реакции карбамида, ароматического гидроксисоединения и алифатического первичного амина. Патентный документ 8 раскрывает способ получения О-арилового сложного эфира N-замещенной карбаминовой кислоты посредством реакционного взаимодействия карбамида и ароматического гидроксисоединения на первой стадии, за которым следует реакционное взаимодействие с первичным амином на второй стадии. В этих способах также необходимо применение избыточного количества карбамида или производного угольной кислоты по отношению к аминогруппе алифатического амина, чтобы улучшить выход из расчета на сравнительно дорогостоящий алифатический амин. Однако поскольку эти патентные документы также не описывают извлечение карбамида или производного угольной кислоты, применяемого в избытке, то невозможно было избежать увеличенного количества применяемого карбамида или производного угольной кислоты. Патентный документ 9 раскрывает способ получения алифатического О-арилового сложного эфираN-замещенной карбаминовой кислоты из алифатического первичного полиамина, ароматического гидро-3 022171 ксисоединения и карбамида и/или О-арилового соединения не-N-замещенной карбаминовой кислоты, в котором O-ариловое соединение не-N-замещенной карбаминовой кислоты извлекается из раствора, полученного реакцией уретанирования, и используется повторно в качестве исходного вещества для реакции уретанирования. В соответствии с этим способом сделана попытка сдерживания увеличения основных звеньев карбамида или O-арилового соединения не-N-замещенной карбаминовой кислоты. Этот способ содержит получение ароматического гидроксисоединения и изоциановой кислоты термическим разложением О-арилового соединения не-N-замещенной карбаминовой кислоты, содержащейся в растворе для реакции уретанирования, реабсорбцию изоциановой кислоты, образованной разложением с образованием ароматического гидроксисоединения, и последующее реакционное взаимодействие с ароматическим гидроксисоединением, чтобы извлечь О-ариловое соединение не-N-замещенной карбаминовой кислоты. Однако помимо того, что процесс усложнен, не могла быть достигнута достаточно удовлетворительная скорость извлечения О-арилового соединения не-N-замещенной карбаминовой кислоты. В случае всех способов, описанных выше, затруднено количественное получение О-арилового сложного эфира N-замещенной карбаминовой кислоты при применении карбамида и сложного эфира неN-замещенной карбаминовой кислоты в качестве исходных веществ, и не только формируются различные структуры полимеров (при этом во многих случаях содержатся полимеры, для которых их структуры не могут быть идентифицированы), но и эти полимеры прилипают к реакционному резервуару, или же,вследствие образования этих соединений, возникала проблема, связанная с количеством используемых соединений карбамида и амина. Кроме того, при получении изоцианатов посредством применения Оарилового сложного эфира N-замещенной карбаминовой кислоты для реакции термического разложения,эти полимеры дополнительно образуют другие полимеры вследствие реакционного взаимодействия с изоцианатами, образуемыми термическим разложением, что также может создавать проблемы, связанные с прилипанием к реакционному резервуару или затвердеванием в нем. Поэтому раскрыты способы, обеспечивающие возможность присутствия растворителя во время термического разложения O-ариловых сложных эфиров N-замещенной карбаминовой кислоты или Оалкиловых сложных эфиров N-замещенной карбаминовой кислоты, например, чтобы избежать проблемы с прилипанием полимеров к реакционному резервуару и их затвердеванием. Например, в соответствии с описанием патентного документа 10 термическое разложение алифатического, алициклического или ароматического поликарбамата выполняется при 150-350 С и 0,001-20 бар(0,1-200 кПа) в присутствии инертного растворителя и в присутствии или при отсутствии катализатора,вспомогательного агента в виде хлористого водорода, хлорида органической кислоты, алкилирующего агента или хлорида органического соединения олова. Образованные побочные продукты могут удаляться, например, непрерывным образом из реакционного резервуара вместе с реакционным раствором, и одновременно добавляется соответствующее количество свежего растворителя или извлеченного и повторно используемого растворителя. Однако недостатком этого способа является то, что, например, происходит снижение эффективности производства полиизоцианата вследствие применения возвращаемого растворителя, и, что еще важнее, требуется большое количество энергии, включая ту, что требуется, например, для извлечения растворителя. Более того, применяемый вспомогательный агент является летучим при условиях реакции, вследствие чего потенциально загрязняется продукт разложения. Кроме того,количество остатка является большим, в расчете на количество образованного полиизоцианата, что делает сомнительными экономическую эффективность и надежность данного способа при его применении в промышленных масштабах. Патентный документ 11 описывает один из способов непрерывного термического разложения карбамата,такого как алициклический диуретан в виде 5-(этоксикарбониламино)-1(этоксикарбониламинометил)-1,3,3-триметилциклогексана, подаваемого вдоль внутренней поверхности трубчатого реакционного резервуара в жидкой форме в присутствии высококипящего растворителя. Этот способ имеет недостатки, заключающиеся в низком выходе и низкой селективности при производстве(циклического) алифатического диизоцианата. Кроме того, отсутствует описание непрерывного способа сопутствующего извлечения повторно связанного или частично разложенного карбамата, и последующая обработка побочных продуктов и катализатора, содержащих растворитель, также не упоминается. С другой стороны, описание патентного документа 12, например, относится к циркуляционному способу получения (циклического) алифатического диизоцианата посредством преобразования соответствующего диамина в О-алкиловый сложный эфир N-замещенной карбаминовой кислоты с последующим термическим разложением этого О-алкилового сложного эфира N-замещенной карбаминовой кислоты в качестве примера способа выполнения термического разложения сложного эфира N-замещенной карбаминовой кислоты без применения растворителя. Этот способ минимизирует снижение выхода посредством повторного использования продукта от стадии разложения сложного эфира N-замещенной карбаминовой кислоты на стадии образования О-алкилового сложного эфира N-замещенной карбаминовой кислоты с последующим реакционным взаимодействием со спиртом. Побочные продукты, которые не могут быть повторно использованы, удаляются дистилляционным разделением реакционной смеси от стадии образования O-алкилового сложного эфира N-замещенной карбаминовой кислоты. В этом случае бесполезный остаток образуется в виде кубовых продуктов, в то время как все сравнительно низкокипя-4 022171 щие компоненты, включая О-алкиловый сложный эфир N-замещенной карбаминовой кислоты, удаляются из головной части колонны. Однако этот способ имеет недостаток, заключающийся в применении большого количества энергии. Это обусловлено тем, что требуется, чтобы весь О-алкиловый сложный эфир N-замещенной карбаминовой кислоты был выпарен в присутствии катализатора, и этот Оалкиловый сложный эфир N-замещенной карбаминовой кислоты должен также быть выпарен при уровне температуры в интервале температур разложения O-алкилового сложного эфира N-замещенной карбаминовой кислоты. Изоцианатные группы, образованные в применяемых продуктах, реагируют с группами остаточного сложного эфира карбаминовой кислоты, что часто приводит к образованию побочных продуктов со сравнительно высокой молекулярной массой, и это вызывает снижение выхода, при этом остается неразрешенной проблема с прилипанием полимеров к реакционному резервуару и их затвердеванием в нем. Кроме того, в соответствии с описанием патентного документа 13 раскрыт способ, посредством которого бесполезные побочные продукты частично удаляются перед выполнением термического разложения сложного эфира N-замещенной карбаминовой кислоты. Недостатком этого способа является то, что выход изоцианата уменьшается вследствие того, что сложный эфир N-замещенной карбаминовой кислоты содержится в частично удаляемых побочных продуктах. Кроме того, поскольку образуются полимерные соединения, которые прилипают к реакционному резервуару вследствие нагревания побочных продуктов, остающихся в реакционном резервуаре, которые не выпущены из реакционного резервуара, проблема с прилипанием полимеров к реакционному резервуару и затвердеванием их в нем остается нерешенной, и затруднено долговременное, непрерывное функционирование. Как описано выше, для разрешения этих проблем были разработаны способ термического разложения О-арилового сложного эфира не-N-замещенной карбаминовой кислоты, содержащегося в реакционном растворе от стадии образования сложного эфира N-замещенной карбаминовой кислоты, чтобы получить ароматическое гидроксисоединение и изоциановую кислоту, реабсорбции изоциановой кислоты,образованной разложением в ароматическое гидроксисоединение, и извлечения О-арилового соединения не-N-замещенной карбаминовой кислоты посредством реакционного взаимодействия с ароматическим гидроксисоединением (см. патентный документ 9) и способ очистки кристаллизацией (см. патентный документ 14). Однако в случае предшествующего способа затруднено адекватное уменьшение количества О-арилового соединения не-N-замещенной карбаминовой кислоты в реакционном растворе от стадии образования сложного эфира N-замещенной карбаминовой кислоты. Кроме того, в последующем способе с применением кристаллизации также затруднена селективная кристаллизация соединений, имеющих сходную структуру, при высоком выходе, наряду с тем, что создается проблема, связанная с потреблением энергии для разделения твердое тело-раствор и извлечения растворителя для кристаллизации. Кроме того, раскрыт способ удаления карбамида и производных угольной кислоты из реакционного раствора от стадии образования сложного эфира N-замещенной карбаминовой кислоты более простым образом, в котором аминовое соединение, карбамид и спирт реагируют, результирующий раствор О-алкилового сложного эфира N-замещенной карбаминовой кислоты вводится в дистилляционную колонну, и карбамид и сложный эфир угольной кислоты извлекают из дистилляционной колонны (см. патентный документ 15). Однако вследствие низкой температуры кипения применяемого спирта имеют место ограничения для заданной температуры и заданного давления дистилляционной колонны, вследствие чего уменьшается количество карбамида в растворе О-алкилового сложного эфира N-замещенной карбаминовой кислоты, наряду с тем, что эффект сдерживания образования побочных продуктов не обязательно отчетлив. Например, в патентном документе 16 описано, что, когда О-алкилуретан, полученный реакционным взаимодействием сложного эфира угольной кислоты и органического амина, подвергается термическому разложению в присутствии ароматического гидроксисоединения, незначительное количество производных угольной кислоты также присутствует. Здесь влияние производных угольной кислоты заключается в улучшении термической стабильности ароматического гидроксисоединения и не предназначено для оказания воздействия на О-алкиловый сложный эфир N-замещенной карбаминовой кислоты или изоцианат,образующийся во время термического разложения. Более того, отсутствует описание, относящееся к влиянию на О-ариловый сложный эфир N-замещенной карбаминовой кислоты. Кроме того, хотя патентный документ 15 описывает композицию для транспортировки и хранения О-арилового сложного эфираN-замещенной карбаминовой кислоты, которая поддерживает его стабильность посредством сдерживания реакции термической денатурации О-алкилового сложного эфира N-замещенной карбаминовой кислоты, а также процесс, в котором применяется эта композиция, в нем отсутствует упоминание об остаточном карбамиде соединений, производных от карбамида, как описано выше, в этой композиции и также отсутствует упоминание об О-ариловом сложном эфире N-замещенной карбаминовой кислоты. Патентный документ 1: патент США 4297501. Патентный документ 2: патент США 3873553. Патентный документ 3: патент США 2677698. Патентный документ 4: патент США 4713476. Патентный документ 5: заявка на европейский патент 0568782. Патентный документ 6: заявка на европейский патент 0657420. Патентный документ 7: патент США 4925971. Патентный документ 8: выложенная заявка на патент ЯпонииН 4-164060. Патентный документ 9: выложенная заявка на патент ЯпонииН 7-157463. Патентный документ 10: патент США 4388246. Патентный документ 11: патент США 4692550. Патентный документ 12: заявка на европейский патент 0355443. Патентный документ 13: патент Японии 3382289. Патентный документ 14: патент Японии 2804232. Патентный документ 15: WO 2008/120645. Патентный документ 16: WO 2008/084824. Непатентный документ 1: Berchte der Deutechen Chemischen Gesellschaft, Vol. 3, p. 653, 1870. Непатентный документ 2: Berchte der Deutechen Chemischen Gesellschaft, Vol. 3, p. 649, 1870. Непатентный документ 3: Journal of American Chemical Society, Vol. 81, p. 2138, 1959. Непатентный документ 4: О. Bayer, Das Diisocyanat-Polyaditions Verfahren, p. 12, 1963. Непатентный документ 5: Journal of Synthetic Organic Chemistry, Japan, Vol. 20, No. 11, p. 1003, 1962. Описание изобретения Задачи, подлежащие разрешению посредством данного изобретения. Таким образом, все еще требуется разрешение проблем, включающих образование полимеров посредством остаточного карбамида и соединений, производных от карбамида, и прилипание этих полимеров к реакционному резервуару, при производстве изоцианатов термическим разложением сложных эфиров N-замещенной карбаминовой кислоты и особенно О-ариловых соединений N-замещенной карбаминовой кислоты. Кроме того, карбамид и производные угольной кислоты, которые применяются в избытке при производстве сложного эфира N-замещенной карбаминовой кислоты, также были определены как вызывающие другие проблемы, помимо указанных. В способах получения О-алкиловых сложных эфиров N-замещенной карбаминовой кислоты или Оариловых сложных эфиров N-замещенной карбаминовой кислоты, в которых применяется карбамид и производные угольной кислоты, аммиак, образующийся в качестве побочного продукта, должен удаляться из системы для того, чтобы увеличить выход сложного эфира N-замещенной карбаминовой кислоты(см., например, патентный документ 7). Во многих случаях побочный аммиак удаляется из системы посредством предоставления трубопровода для выпуска аммиака в реакционном резервуаре для получения сложного эфира N-замещенной карбаминовой кислоты. Карбамид и производные угольной кислоты сами подвергаются реакции термического разложения, как описано ранее, и вовлекаются в образование полимеров вследствие образования изоциановой кислоты и образования биуретов изоциановой кислотой. Хотя большинство этих соединений, образованных из карбамида и производных угольной кислоты конденсируются и возвращаются в реакционную систему вместе со спиртом и ароматическим гидроксисоединением, часть их может быть выпущена в качестве газообразных компонентов вместе с побочным аммиаком. Когда функционирование выполняется в течение длительного периода времени, эти соединения прилипают и накапливаются на внутренних стенках трубопровода для выпуска аммиака, что обусловливает засорение трубопровода для выпуска аммиака. Однако, как описано выше, в предшествующем уровне техники отсутствуют примеры рассмотрения средств для разрешения проблемы засорения трубопровода для выпуска аммиака, и технологию, обеспечивающую возможность функционирования оборудования для производства сложного эфира Nзамещенной карбаминовой кислоты, еще предстоит создать. Таким образом, все еще существуют многочисленные проблемы, связанные с производством сложного эфира N-замещенной карбаминовой кислоты для применения в качестве предшественника изоцианата и производством изоцианатов, и поскольку способ, служащий альтернативой способу фосгенирования, еще предстоит создать, то имеет место настоятельная потребность в разрешении этих проблем. Как описано выше, были предложены различные способы получения О-алкиловых сложных эфировN-замещенной карбаминовой кислоты или О-ариловых сложных эфиров N-замещенной карбаминовой кислоты, в которых применяется карбамид или производные угольной кислоты. Имеется множество случаев, в которых карбамид или производные угольной кислоты, добавляемые в избытке, чтобы получить сложный эфир N-замещенной карбаминовой кислоты при высоком выходе в этих способах, вызывают образование полимеров и т.п., как описано выше, которые, в свою очередь, прилипают к реакционному резервуару и затвердевают в нем. Кроме того, во многих случаях имело место то, что полимеры, образованные вследствие побочных реакций и избытка карбамида или производных угольной кислоты, дополнительно образовывали разные виды полимеров вследствие протекания побочных реакций с изоцианатом, как описано ранее, во время получения изоцианата реакцией термического разложения О-алкилового сложного эфира N-замещенной карбаминовой кислоты или O-арилового сложного эфира N-замещенной карбаминовой кислоты, приводя к той проблеме, что эти полимеры также прилипают или затвердевают в реакционном резервуаре. Кроме того, имела место также проблема с увеличением количества применяемых карбамида, производных угольной кислоты и аминов вследствие образования этих полимеров. Однако отсутствуют описания способов эффективного извлечения и повторного использования избытка карбамида и производных угольной кислоты, и увеличения количества применяемых карбамида или производных угольной кислоты было невозможно избежать. Хотя аммиак образуется в качестве побочного продукта в случае получения О-алкилового сложного эфира N-замещенной карбаминовой кислоты или О-арилового сложного эфира N-замещенной карбаминовой кислоты с применением карбамида и производных угольной кислоты, также имеются проблемы с удалением этого аммиака. Хотя побочный аммиак часто выпускается посредством предоставления трубопровода для выпуска аммиака в реакционном резервуаре для получения сложного эфира Nзамещенной карбаминовой кислоты для того, чтобы увеличить выход О-алкилового сложного эфира Nзамещенной карбаминовой кислоты или О-арилового сложного эфира N-замещенной карбаминовой кислоты, во многих случаях имело место то, что твердые частицы прилипают и затвердевают на внутренних стенках трубопровода для выпуска аммиака, ухудшая таким образом функционирование. Целью данного изобретения является предоставление способа получения сложного эфира Nзамещенной карбаминовой кислоты, способа получения изоцианата термическим разложением сложного эфира N-замещенной карбаминовой кислоты и композиции для транспортировки и хранения сложного эфира N-замещенной карбаминовой кислоты, содержащей сложный эфир N-замещенной карбаминовой кислоты и ароматическое гидроксисоединение, которая подходит для транспортировки и хранения сложного эфира N-замещенной карбаминовой кислоты и особенно О-арилового сложного эфира Nзамещенной карбаминовой кислоты, а также подходит для производства изоцианата. Поэтому в результате проведения обширных исследований для разрешения вышеуказанных проблем авторы данного изобретения нашли, что данные проблемы могут быть решены посредством способа получения сложного эфира N-замещенной карбаминовой кислоты из органического амина, производного угольной кислоты и гидроксикомпозиции, в котором реакционное взаимодействие между органическим амином, производным угольной кислоты и гидроксикомпозицией выполняется с применением реакционного резервуара, снабженного конденсатором, число карбонильных групп, содержащихся в соединениях, имеющих карбонильные группы, которые образованы из производного угольной кислоты и содержатся в аммиаке, извлеченном в виде газа из конденсатора, соответствует заданному числу или менее, и извлеченное производное угольной кислоты используется повторно в получении сложного эфираN-замещенной карбаминовой кислоты; способа получения изоцианата посредством реакции термического разложения сложного эфира N-замещенной карбаминовой кислоты, полученной описанным выше способом; и специальной композиции, содержащей сложный эфир N-замещенной карбаминовой кислоты и ароматическую гидроксикомпозицию, что привело к завершению данного изобретения. А именно, в первой своей особенности данное изобретение предоставляет следующее.[1] Способ получения сложного эфира N-замещенной карбаминовой кислоты, получаемого из органического амина, производного угольной кислоты и гидроксикомпозиции, содержащей один или несколько видов гидроксисоединений,в котором органический амин, производное угольной кислоты и гидроксикомпозиция реагируют с применением реакционного резервуара для получения уретана, снабженного конденсатором,газ, содержащий гидроксикомпозицию, соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, и аммиак, образованный в качестве побочного продукта в ходе реакционного взаимодействия, вводится в конденсатор, предусмотренный в реакционном резервуаре для получения уретана, и гидроксикомпозиция и соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, конденсируются, и в котором отношение гидроксисоединения, содержащегося в конденсированной гидроксикомпозиции, к конденсированному соединению, имеющему карбонильную группу, полученному из производного угольной кислоты, составляет 1 или более, в расчете на стехиометрическое соотношение, и соотношение числа карбонильных групп (-С(=O)-), содержащихся в соединении, имеющем карбонильную группу, которое образовано из производного угольной кислоты, и числом молекул аммиака,содержащихся в аммиаке, который извлечен в виде газа из конденсатора, составляет 1 или менее.[2] Способ получения по пункту [1] выше, в котором гидроксисоединение является спиртом или ароматическим гидроксисоединением.[3] Способ получения по пункту [1] выше, в котором гидроксикомпозиция и/или соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, которое сконденсировано конденсатором, используется повторно в реакционном взаимодействии.[4] Способ получения по пункту [1] выше, в котором гидроксикомпозиция и соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, которое сконденсировано конденсатором, циркулируют внутри реакционного резервуара для получения уретана.[5] Способ получения по пункту [1] выше, в котором производное угольной кислоты является карбамидом и/или сложным эфиром карбаминовой кислоты.[6] Способ получения по пункту [1] выше, в котором сложный эфир N-замещенной карбаминовой кислоты получают посредством процесса, содержащего следующие стадии (а) и (b): стадия (а): стадия получения реакционной смеси, содержащей соединение, имеющее уреидогруппу,посредством реакционного взаимодействия органического амина и производного угольной кислоты; и стадия (b): стадия получения сложного эфира N-замещенной карбаминовой кислоты посредством реакционного взаимодействия соединения, имеющего уреидогруппу, которое получено на стадии (а), и гидроксикомпозиции при применении реакционного резервуара для получения уретана, снабженного конденсатором,в котором газ, содержащий гидроксикомпозицию, соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, и аммиак, образованный в качестве побочного продукта в ходе реакционного взаимодействия, вводится в конденсатор, предусмотренный в реакционном резервуаре для получения уретана, и гидроксикомпозиция и соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, конденсируются.[7] Способ получения по пункту [6] выше, в котором гидроксисоединение является спиртом или ароматическим гидроксисоединением.[8] Способ получения по пункту [6] выше, в котором производное угольной кислоты на стадии (а) является карбамидом и/или сложным эфиром карбаминовой кислоты.[9] Способ получения по пункту [6] выше, в котором реакционное взаимодействие на стадии (а) выполняется в присутствии соединения по меньшей мере одного вида, выбранного из группы, состоящей из воды, спирта и ароматического гидроксисоединения.[10] Способ получения по пункту [6] выше, в котором гидроксикомпозиция и/или соединение,имеющее карбонильную группу, полученное из производного угольной кислоты, которое сконденсировано конденсатором на стадии (b), используется повторно в реакционном взаимодействии на стадии (а).[11] Способ получения по пункту [5] или [8] выше, в котором сложный эфир карбаминовой кислоты является сложным эфиром карбаминовой кислоты, полученным в соответствии со следующей стадией(с): стадия (с): стадия получения сложного эфира карбаминовой кислоты посредством реакционного взаимодействия гидроксикомпозиции с (при этом гидроксикомпозиция с обозначает композицию, содержащую один или несколько видов гидроксисоединений) и карбамида.[12] Способ получения по пункту [11] выше, в котором гидроксисоединение, которое образует гидроксикомпозицию с, является спиртом и/или ароматическим гидроксисоединением.[13] Способ получения по пункту [1] или [6] выше, в котором конденсированная гидроксикомпозиция и/или соединение, имеющее карбонильную группу, полученное из сложного эфира карбаминовой кислоты, используется повторно на стадии (с). Во второй своей особенности данное изобретение также предоставляет следующее.[14] Способ получения сложного эфира N-замещенной карбаминовой кислоты из органического амина, производного угольной кислоты и гидроксикомпозиции, содержащей один или несколько видов гидроксисоединений, данный способ содержит следующие стадии (а) и (b): стадия (а): стадия получения реакционной смеси, содержащей соединение, имеющее уреидогруппу,посредством реакционного взаимодействия органического амина и производного угольной кислоты; и стадия (b): стадия получения сложного эфира N-замещенной карбаминовой кислоты посредством реакционного взаимодействия соединения, имеющего уреидогруппу, которое получено на стадии (а), и гидроксикомпозиции при применении реакционного резервуара для получения уретана, снабженного конденсатором,в котором газ, содержащий гидроксикомпозицию, соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, и аммиак, образованный в качестве побочного продукта в ходе реакционного взаимодействия, вводится в конденсатор, предусмотренный в реакционном резервуаре для получения уретана, и гидроксикомпозиция и соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, конденсируются.[15] Способ получения по пункту [14] выше, в котором гидроксисоединение является спиртом и/или ароматическим гидроксисоединением.[16] Способ получения по пункту [14] выше, в котором производное угольной кислоты на стадии(а) является карбамидом и/или сложным эфиром карбаминовой кислоты.[17] Способ получения по пункту [14] выше, в котором реакционное взаимодействие на стадии (а) выполняется в присутствии соединения по меньшей мере одного вида, выбранного из группы, состоящей из воды, спирта и ароматического гидроксисоединения.[18] Способ получения по пункту [14] выше, в котором гидроксикомпозиция и/или соединение,имеющее карбонильную группу, полученное из производного угольной кислоты, которое сконденсировано конденсатором на стадии (b), используется повторно на стадии (а).[19] Способ получения по пункту [16] выше, в котором сложный эфир карбаминовой кислоты является сложным эфиром карбаминовой кислоты, полученным в соответствии со следующей стадией (с): стадия (с): стадия получения сложного эфира карбаминовой кислоты посредством реакционного взаимодействия гидроксикомпозиции с и карбамида.[20] Способ получения по пункту [19] выше, в котором гидроксисоединение, которое образует гидроксикомпозицию с, является спиртом и/или ароматическим гидроксисоединением.[21] Способ получения по пункту [19] выше, в котором конденсированная гидроксикомпозиция и/или соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, используется повторно на стадии (с).[22] Способ получения по пункту [1] или [14] выше, в котором реакционный резервуар для получения уретана является реакционным резервуаром в виде бака и/или в виде колонны, снабженным конденсатором.[23] Способ получения по пункту [1] или [14] выше, в котором реакционный резервуар для получения уретана имеет газовую фазу, которая содержит гидроксикомпозицию, соединение, имеющее карбонильную группу, полученное из производного угольной кислоты, и аммиак, образованный в качестве побочного продукта в ходе реакционного взаимодействия, и жидкую фазу, в которой выполняется реакционное взаимодействие, и объемное содержание жидкой фазы в реакционном резервуаре для получения уретана составляет 50% или менее.[24] Способ получения по любому из пунктов [2], [7] или [15] выше, в котором гидроксисоединение является ароматическим гидроксисоединением, органический амин является соединением, представленным приведенной формулой (1), и полученный сложный эфир N-замещенной карбаминовой кислоты является О-Ar сложным эфиром N-замещенной карбаминовой кислоты, представленным приведенной формулой (2) где R1 обозначает органическую группу, которая имеет от 1 до 85 атомов углерода и которая замещена а аминогруппами;Ar обозначает группу, производную от ароматического гидроксисоединения, которая является остатком, в котором единственная гидроксильная группа, связанная с ароматическим кольцом ароматического гидроксисоединения, удалена; а обозначает целое число от 1 до 10;b обозначает целое число от 1 до а.[25] Способ получения по любому из пунктов [2], [7] или [15] выше, в котором гидроксисоединение является спиртом, органический амин является соединением, представленным приведенной формулой(3), и полученный сложный эфир N-замещенной карбаминовой кислоты является О-R2 сложным эфиромN-замещенной карбаминовой кислоты, представленным приведенной формулой (4) где R1 обозначает органическую группу, которая имеет от 1 до 85 атомов углерода и которая замещена а аминогруппами;R2 обозначает группу, производную от спирта, которая является остатком, в котором единственная гидроксильная группа, связанная с насыщенным атомом углерода спирта, удалена из спирта; а обозначает целое число от 1 до 10; с обозначает целое число от 1 до а.[26] Способ получения по пункту [25] выше, в котором О-Ar сложный эфир N-замещенной карбаминовой кислоты, представленный приведенной формулой (5) и имеющий группу сложного эфира, производную от ароматического гидроксисоединения, производится посредством реакционного взаимодействия О-R2 сложного эфира N-замещенной карбаминовой кислоты, представленного формулой (4) выше,и ароматического гидроксисоединения где R1 обозначает органическую группу, которая имеет от 1 до 85 атомов углерода и которая замещена а аминогруппами;Ar обозначает группу, производную от ароматического гидроксисоединения, которая является остатком, в котором единственная гидроксильная группа, связанная с ароматическим кольцом ароматического гидроксисоединения, удалена из ароматического гидроксисоединения;b обозначает целое число от 1 до а (где а является тем же самым обозначением, что и в формуле (3) выше, и обозначает целое число от 1 до 10). Кроме того, в третьей своей особенности данное изобретение предоставляет следующее.[27] Композицию для транспортировки и хранения О-Ar сложного эфира N-замещенной карбаминовой кислоты, содержащую O-Ar сложный эфир N-замещенной карбаминовой кислоты, представленный приведенной формулой (6), и ароматическую гидроксикомпозицию, содержащую один или несколько видов ароматических гидроксисоединений, в которой отношение числа молекул ароматического гидроксисоединения, которое образует ароматическую гидроксикомпозицию (В), к числу групп сложного эфира, которые образуют О-Ar сложный эфир N-замещенной карбаминовой кислоты (А), находится в интервале от 1 до 100 где R1 обозначает органическую группу, которая имеет от 1 до 85 атомов углерода и которая замещена а аминогруппами;Ar обозначает остаток, в котором единственная гидроксильная группа, связанная с ароматическим кольцом ароматического гидроксисоединения, удалена из ароматического гидроксисоединения (и ароматическое гидроксисоединение может быть таким же или отличающимся от ароматического гидроксисоединения, которое образует ароматическую гидроксикомпозицию);d обозначает целое число от 1 до 10.[28] Композицию для транспортировки и хранения по пункту [27] выше, в которой О-Ar сложный эфир N-замещенной карбаминовой кислоты является О-Ar сложным эфиром N-замещенной карбаминовой кислоты, произведенным из органического амина, производного угольной кислоты и ароматической гидроксикомпозиции, и композиция для транспортировки и хранения является композицией, содержащей по меньшей мере один вид соединения, которое является карбамидом и/или сложным эфиром карбаминовой кислоты и/или биуретом и/или соединением, которое имеет концевую биуретовую группу,(-NH-(C=O)-NH-(C=O)-NH2), производную от органического амина и образованную при реакционном взаимодействии органического амина, производного угольной кислоты и ароматической гидроксикомпозиции.[29] Композицию для транспортиртировки и хранения по пункту [27] выше, в которой композиция для транспортировки и хранения содержит сложный эфир угольной кислоты, производный от ароматической гидроксикомпозиции. В дополнение к этому, в своей предпочтительной особенности данное изобретение предоставляет следующее.[30] Способ получения по пункту [24] или [26] выше, в котором ароматическое гидроксисоединение является ароматическим гидроксисоединением с валентностью от единицы до трех (т.е. число гидроксильных групп, связанных с ароматическим кольцом, является целым числом от 1 до 3).[31] Способ получения по пункту [30] выше, в котором ароматическое гидроксисоединение является ароматическим гидроксисоединением, представленным приведенной формулой (7) где кольцо А обозначает необязательно замещенный одноядерный или многоядерный ароматический углеводород;R3 и R4 соответственно и независимым образом обозначают атом водорода или органическую группу; число атомов углерода, которые образуют ароматическое гидроксисоединение, является целым числом от 6 до 50;R3 и R4 могут образовывать кольцевую структуру посредством связывания с А.[32] Способ получения по пункту [31] выше, в котором по меньшей мере одно из ароматических гидроксисоединений, которые образуют гидроксикомпозицию, является ароматическим гидроксисоединением, представленным приведенной формулой (8) где кольцо А обозначает необязательно замещенный одноядерный или многоядерный ароматический углеводород;R5 и R6 соответственно и независимым образом обозначают любую группу, определенную в пунктах (i)-(v) ниже; число атомов углерода, которые образуют ароматическое гидроксисоединение, является целым числом от 6 до 50;R5 и R6 могут образовывать кольцевую структуру посредством связывания с А:(i) атом водорода,(ii) атом галогена,(iii) группа, в которой атом в -положении является атомом азота и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода (за исключением водорода, связанного с атомом азота в -положении), атом азота является вторичным атомом азота (т.е. атомом азота, который образует связь -NH-),(iv) группа, в которой атом в -положении является атомом углерода и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода, атом углерода является первичным или вторичным атомом углерода (т.е. углеродом метильной группы или углеродом, который образует связь-СН 2-), при условии, что в случае, когда R5 и/или R6 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с ароматическим кольцом А, и конденсированное кольцо имеет 6 элементов или менее, атом углерода в -положении может быть третичным или четвертичным атомом углерода, и также в случае, когда углерод в -положении образует двойную или тройную связь с атомом в -положении (атомом, который образует R5 и R6 и который также является смежным с атомом, связанным с ароматическим кольцом кольца А), атом углерода в -положении может быть третичным или четвертичным атомом углерода, и(v) группа, в которой атом в -положении является атомом кислорода и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода.[33] Способ получения по пункту [32] выше, в котором гидроксикомпозиция содержит ароматическое гидроксисоединение, представленное выше формулой (8), вместе с ароматическим гидроксисоединением, представленным приведенной формулой (9) где кольцо А обозначает необязательно замещенный одноядерный или многоядерный ароматический углеводород;R7 и R8 соответственно и независимым образом обозначают любую группу, определенную в пунктах (i)-(v) ниже; число атомов углерода, которые образуют ароматическое гидроксисоединение, является целым числом от 6 до 50;R7 и R8 могут образовывать кольцевую структуру посредством связывания с А:(i) атом водорода,(ii) атом галогена,(iii) группа, в которой атом в -положении является атомом азота и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода, атом азота является третичным атомом азота(т.е. атомом азота, который не имеет атома водорода),(iv) группа, в которой атом в -положении является атомом углерода и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода, атом углерода в -положении является третичным или четвертичным атомом углерода (т.е. атомом углерода, который образует связь -СН-, или атомом углерода, не связанным с водородом); в случае, когда R7 и/или R8 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с ароматическим кольцом А, и конденсированное кольцо имеет 7 элементов или более, атом углерода в -положении может быть первичным или вторичным атомом углерода (т.е. атомом углерода метильной группы или атомом углерода, который обра- 11022171 зует связь -СН 2-); в случае, когда углерод в -положении образует двойную связь с атомом в положении, углерод в -положении является четвертичным углеродом; и группы, в которых углерод в положении образует тройную связь с атомом в -положении, исключаются, и(v) группа, в которой атом в -положении является атомом кислорода и число атомов углерода составляет от 1 до 24 и которая не содержит активного водорода.[34] Способ получения по любому из пунктов [31], [32] или [33] выше, в котором стандартная температура кипения ароматического гидроксисоединения, представленного формулой (7), формулой (8) или формулой (9) отличается на 10 С или более от стандартной температуры кипения изоцианата, в котором все аминогруппы органического амина замещены изоцианатными группами (группами -NCO). Кроме того, в своей предпочтительной особенности данное изобретение предоставляет следующее.[35] Композицию по пункту [27] выше, в которой ароматическое гидроксисоединение, которое образует ароматическую гидроксикомпозицию, является ароматическим гидроксисоединением с валентностью от единицы до трех (т.е. число гидроксильных групп, связанных с ароматическим кольцом, является целым числом от 1 до 3).[36] Композицию по пункту [35] выше, в которой ароматическое гидроксисоединение, которое образует ароматическую гидроксикомпозицию, является ароматическим гидроксисоединением, представленным приведенной формулой (7) где кольцо А обозначает необязательно замещенный одноядерный или многоядерный ароматический углеводород;R3 и R4 соответственно и независимым образом обозначают атом водорода или органическую группу; число атомов углерода, которые образуют ароматическое гидроксисоединение, является целым числом от 6 до 50; иR3 и R4 могут образовывать кольцевую структуру посредством связывания с А.[37] Композицию по пункту [36] выше, в которой по меньшей мере одно из ароматических гидроксисоединений, которые образуют ароматическую гидроксикомпозицию, является ароматическим гидроксисоединением, представленным приведенной формулой (8) где кольцо А обозначает необязательно замещенный одноядерный или многоядерный ароматический углеводород,R5 и R6 соответственно и независимым образом обозначают любую группу, определенную в пунктах (i)-(v) ниже; число атомов углерода, которые образуют ароматическое гидроксисоединение, является целым числом от 6 до 50, иR5 и R6 могут образовывать кольцевую структуру посредством связывания с А:(i) атом водорода,(ii) атом галогена,(iii) группа, в которой атом в -положении является атомом азота и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода (за исключением водорода, связанного с атомом азота в -положении), атом азота является вторичным атомом азота (т.е. атомом азота, который образует связь -NH-),(iv) группа, в которой атом в -положении является атомом углерода и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода, атом углерода является первичным или вторичным атомом углерода (т.е. углеродом метильной группы или углеродом, который образует связь-СН 2-), при условии, что в случае, когда R5 и/или R6 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с ароматическим кольцом А, и конденсированное кольцо имеет 6 элементов или менее, атом углерода в -положении может быть третичным или четвертичным атомом углерода, и также в случае, когда углерод в -положении образует двойную или тройную связь с атомом в -положении (атомом, который образует R5 и R6 и который также является смежным с атомом, связан- 12022171 ным с ароматическим кольцом кольца А), атом углерода в -положении может быть третичным или четвертичным атомом углерода, и(v) группа, в которой атом в -положении является атомом кислорода и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода.[38] Композицию по пункту [37] выше, в которой ароматическая гидроксикомпозиция содержит ароматическое гидроксисоединение, представленное выше формулой (8), вместе с ароматическим гидроксисоединением, представленным приведенной формулой (9) где кольцо А обозначает необязательно замещенный одноядерный или многоядерный ароматический углеводород;R7 и R8 соответственно и независимым образом обозначают любую группу, определенную в пунктах (i)-(v) ниже; число атомов углерода, которые образуют ароматическое гидроксисоединение, является целым числом от 6 до 50;R7 и R8 могут образовывать кольцевую структуру посредством связывания с А:(i) атом водорода,(ii) атом галогена,(iii) группа, в которой атом в -положении является атомом азота и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода, атом азота является третичным атомом азота(т.е. атомом азота, который не имеет атома водорода),(iv) группа, в которой атом в -положении является атомом углерода и число атомов углерода составляет от 1 до 44 и которая не содержит активного водорода, атом углерода в -положении является третичным или четвертичным атомом углерода (т.е. атомом углерода, который образует связь -СН-, или атомом углерода, не связанным с водородом); в случае, когда R7 и/или R8 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с ароматическим кольцом А, и конденсированное кольцо имеет 7 элементов или более, атом углерода в -положении может быть первичным или вторичным атомом углерода (т.е. атомом углерода метильной группы или атомом углерода, который образует связь -СН 2-); в случае, когда углерод в -положении образует двойную связь с атомом в положении, углерод в -положении является четвертичным углеродом; и группы, в которых углерод в положении образует тройную связь с атомом в -положении, исключаются, и(v) группа, в которой атом в -положении является атомом кислорода и число атомов углерода составляет от 1 до 24 и которая не содержит активного водорода.[39] Композицию по любому из пунктов [36], [37] или [38] выше, в котором стандартная температура кипения ароматического гидроксисоединения, представленного формулой (7), формулой (8) или формулой (9), отличается на 10 С или более от стандартной температуры кипения изоцианата, в котором все аминогруппы органического амина замещены изоцианатными группами (группами -NCO). Более того, в своей предпочтительной особенности данное изобретение предоставляет следующее.[40] Способ получения по пункту [24] или [26] выше, в котором органический амин является органическим моноамином, представленным приведенной формулой (10), получают О-Ar сложный моноэфир N-замещенной карбаминовой кислоты, представленный приведенной формулой (11), и О-Ar сложный моноэфир N-замещенной карбаминовой кислоты применяют для получения О-Ar сложного полиэфира N-замещенной карбаминовой кислоты, представленного приведенной формулой (12), посредством выполнения следующей стадии (X): стадия (X): О-Ar сложный моноэфир N-замещенной карбаминовой кислоты и метиленирующий агент реагируют с образованием поперечно сшитых связей ароматических групп, производных от органического моноамина, содержащегося в О-Ar сложном моноэфире N-замещенной карбаминовой кислоты, с метиленовыми группами (-СН 2-) таким образом, чтобы получить O-Ar сложный полиэфир Nзамещенной карбаминовой кислоты, представленный приведенной формулой (12) где Ar обозначает группу, производную от ароматического гидроксисоединения, которая является остатком, в котором единственная гидроксильная группа, связанная с ароматическим кольцом ароматического гидроксисоединения, удалена;R9-R12 могут соответственно и независимым образом замещать ароматическое кольцо, R9-R12 могут взаимно соединяться, чтобы образовывать кольцо с ароматическим кольцом, и представляют атом водорода или группу, состоящую из групп, в которых алкильная группа, циклоалкильная группа, арильная группа или группа, выбранная из группы, состоящей из этих групп, связана насыщенными углеводородными связями и/или эфирными связями; е обозначает 0 или положительное целое число; общее число атомов углерода, которое содержит органический моноамин, представленный формулой (10), является целым числом от 6 до 50.[41] Способ получения по пункту [25] выше, в котором органический амин является органическим моноамином, представленным приведенной формулой (13), получают O-R2 сложный моноэфир Nзамещенной карбаминовой кислоты, представленный приведенной формулой (14), и О-R2 сложный моноэфир N-замещенной карбаминовой кислоты применяют для получения О-Ar сложного полиэфира Nзамещенной карбаминовой кислоты, представленного приведенной формулой (16), посредством выполнения следующих стадий (X) и (Y): стадия (X): О-R2 сложный моноэфир N-замещенной карбаминовой кислоты и метиленирующий агент реагируют с образованием поперечно сшитых связей ароматических групп, производных от органического моноамина, содержащегося в O-R2 сложном моноэфире N-замещенной карбаминовой кислоты, с метиленовыми группами (-СН 2-) таким образом, чтобы получить O-R2 сложный полиэфир Nзамещенной карбаминовой кислоты, представленный приведенной формулой (15); и стадия (Y): О-R2 сложный полиэфир N-замещенной карбаминовой кислоты, полученный на стадии(X), реагирует с ароматическим гидроксисоединением, чтобы получить О-Ar сложный полиэфир Nзамещенной карбаминовой кислоты, имеющий группы сложного эфира, производные от ароматического гидроксисоединения, представленный приведенной формулой (16) где R9-R12 могут соответственно и независимым образом замещать ароматическое кольцо, R9-R12 могут взаимно соединяться, чтобы образовывать кольцо с ароматическим кольцом, и представляют атомы водорода или группы, состоящие из групп, в которых алкильная группа, циклоалкильная группа,арильная группа или группа, выбранная из группы, состоящей из этих групп, связана насыщенными углеводородными связями и/или эфирными связями;R2 обозначает группу, производную от спирта, которая является остатком, в котором единственная гидроксильная группа, связанная с насыщенным атомом углерода спирта, удалена из спирта;Ar обозначает группу, производную от ароматического гидроксисоединения, которая является остатком, в котором единственная гидроксильная группа, связанная с ароматическим кольцом ароматического гидроксисоединения, удалена из ароматического гидроксисоединения; е обозначает 0 или положительное целое число; общее число атомов углерода, которое содержит органический моноамин, представленный формулой (13), является целым числом от 6 до 50. Кроме того, в четвертой своей особенности данное изобретение предоставляет следующее.[42] Способ получения изоцианата, содержащий извлечение изоцианата и ароматического гидроксисоединения, которые образованы посредством выполнения реакции термического разложения для ОAr сложного эфира N-замещенной карбаминовой кислоты по любому из пунктов [24], [26], [40] и [41] выше.[43] Способ получения изоцианата, содержащий извлечение изоцианата и ароматического гидроксисоединения, которые образованы переносом композиции для транспортировки и хранения О-Ar сложного эфира N-замещенной карбаминовой кислоты по любому из пунктов [27]-[29] выше в реакционный резервуар для термического разложения и выполнением реакции термического разложения сложного эфира N-замещенной карбаминовой кислоты.[44] Способ получения по пункту [42] или [43] выше, в котором извлеченное ароматическое гидроксисоединение по пункту [42] или [43] выше используется повторно в качестве ароматического гидроксисоединения по пункту [2] выше, и/или ароматического гидроксисоединения по пункту [7] выше,и/или ароматического гидроксисоединения по пункту [9] выше, и/или ароматического гидроксисоединения по пункту [12] выше, и/или ароматического гидроксисоединения по пункту [15] выше, и/или ароматического гидроксисоединения по пункту [17] выше, и/или ароматического гидроксисоединения по пункту [20] выше.[45] Способ получения по пункту [42] или [43] выше, в котором остаточная жидкость, содержащая непрореагировавший О-Ar сложный эфир N-замещенной карбаминовой кислоты, извлеченный из нижней части реакционного резервуара для термического разложения, снова переносится в реакционный резервуар для термического разложения, и О-Ar сложный эфир N-замещенной карбаминовой кислоты подвергается реакции термического разложения.[46] Способ получения по пункту [42] или [43] выше, в котором изоцианат, полученный в способе- 15022171 получения по пункту [42] или [43] выше, содержит от 1 до 1000 млн-1 (ppm) ароматического гидроксисоединения, которое образует ароматическую гидроксикомпозицию, в расчете на изоцианат.[47] Способ получения по любому из пунктов [1], [11], [14] или [19] выше, в котором аммиак, извлеченный в виде газа, реагирует с диоксидом углерода, чтобы получить карбамид, и данный карбамид используется повторно. Преимущества данного изобретения В соответствии с данным изобретением сложный эфир N-замещенной карбаминовой кислоты может быть получен выгодным образом в расчете на основные звенья карбамида. Кроме того, в качестве исходного вещества для производства изоцианата может быть предпочтительным образом использован сложный эфир N-замещенной карбаминовой кислоты. Также, в соответствии с данным изобретением производство сложного эфира N-замещенной карбаминовой кислоты может быть реализовано в течение длительного периода времени посредством обеспечения возможности предотвращения прилипания полимерных побочных продуктов к реакционному резервуару и их накапливания во время производства сложного эфира N-замещенной карбаминовой кислоты, а также засорения трубопровода для выпуска аммиака, образуемого в качестве побочного продукта во время производства сложного эфира N-замещенной карбаминовой кислоты. Описание фигур Фиг. 1 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме способа получения сложного эфира N-замещенной карбаминовой кислоты в соответствии со стадией (А). Фиг. 2 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме способа получения сложного эфира N-замещенной карбаминовой кислоты, содержащего стадию (а) и стадию (b). Фиг. 3 представляет собой принципиальное изображение, представляющее обработку газообразных компонентов, относящуюся к способу получения сложного эфира N-замещенной карбаминовой кислоты в данном варианте осуществления. Фиг. 4 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме повторного использования конденсированных компонентов. Фиг. 5 представляет собой принципиальное изображение, представляющее один из аспектов данного изобретения в форме способа получения сложного эфира N-замещенной карбаминовой кислоты, в котором применяется ароматическая гидроксикомпозиция, содержащая активное ароматическое гидроксисоединение и неактивное ароматическое гидроксисоединение. Фиг. 6 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме стадии (а). Фиг. 7 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме стадии (с). Фиг. 8 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме стадии (b) для получения сложного эфира Nзамещенной карбаминовой кислоты посредством реакционного взаимодействия соединения, имеющего уреидогруппы, которое получено на стадии (а), и гидроксикомпозиции. Фиг. 9 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме способа получения сложного эфира N-замещенной карбаминовой кислоты, в котором применяется ароматическая гидроксикомпозиция, содержащая активное ароматическое гидроксисоединение и неактивное ароматическое гидроксисоединение. Фиг. 10 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме стадии (Y) и повторного использования спирта, образованного на стадии (Y). Фиг. 11 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме стадии синтеза карбамида и повторного использования карбамида, полученного на стадии синтеза карбамида. Фиг. 12 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме стадии (F) и повторного использования ароматического гидроксисоединения, образованного на стадии (F). Фиг. 13 представляет собой принципиальное изображение, представляющее предпочтительную особенность (I) данного варианта осуществления изобретения. Фиг. 14 представляет собой принципиальное изображение, представляющее предпочтительную особенность (II) данного варианта осуществления изобретения. Фиг. 15 представляет собой принципиальное изображение, представляющее предпочтительную особенность (III) данного варианта осуществления изобретения. Фиг. 16 представляет собой принципиальное изображение, представляющее предпочтительную особенность (IV) данного варианта осуществления изобретения. Фиг. 17 представляет собой принципиальное изображение одного из аспектов данного варианта осуществления изобретения в форме стадии (X). Фиг. 18 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме способа получения полифункционального изоцианата из O-R2 сложного моноэфира N-замещенной карбаминовой кислоты, который объединяет стадию (X),стадию (Y) и стадию (F). Фиг. 19 представляет собой принципиальное изображение, представляющее один из аспектов данного варианта осуществления изобретения в форме другого способа получения полифункционального изоцианата из O-R2 сложного моноэфира N-замещенной карбаминовой кислоты, который объединяет стадию (X), стадию (Y) и стадию (F). Фиг. 20 представляет собой принципиальное изображение, представляющее предпочтительную особенность способа получения полифункционального изоцианата из О-Ar сложного моноэфира Nзамещенной карбаминовой кислоты данного варианта осуществления изобретения. Фиг. 21 представляет собой принципиальное изображение, представляющее устройство для получения сложного эфира N-замещенной карбаминовой кислоты, применяемое в примере данного варианта осуществления изобретения. Фиг. 22 представляет собой принципиальное изображение, представляющее устройство для получения сложного эфира N-замещенной карбаминовой кислоты, применяемое в примере данного варианта осуществления изобретения. Фиг. 23 представляет собой принципиальное изображение, представляющее устройство для получения сложного эфира N-замещенной карбаминовой кислоты, применяемое в примере данного варианта осуществления изобретения. Фиг. 24 представляет собой принципиальное изображение устройства для получения сложного эфира N-замещенной карбаминовой кислоты, применяемого в примере данного варианта осуществления изобретения. Фиг. 25 представляет собой принципиальное изображение устройства для получения сложного эфира N-замещенной карбаминовой кислоты, применяемого в примере данного варианта осуществления изобретения. Фиг. 26 представляет собой принципиальное изображение устройства для получения сложного эфира N-замещенной карбаминовой кислоты, применяемого в примере данного варианта осуществления изобретения. Фиг. 27 представляет собой принципиальное изображение устройства для получения изоцианата,применяемого в примере данного варианта осуществления изобретения. Фиг. 28 представляет собой принципиальное изображение устройства для получения изоцианата,применяемого в примере данного варианта осуществления изобретения. Фиг. 29 представляет собой принципиальное изображение устройства для получения изоцианата,применяемого в примере данного варианта осуществления изобретения. Фиг. 30 представляет собой принципиальное изображение устройства для проведения реакции конденсации для сложного моноэфира N-замещенной карбаминовой кислоты, применяемого в примере данного варианта осуществления изобретения. Фиг. 31 представляет собой принципиальное изображение устройства для проведения реакции переэтерификации, применяемого в примере данного варианта осуществления изобретения. Фиг. 32 представляет собой спектр 1 Н-ЯМР композиции для транспортировки и хранения сложного эфира N-замещенной карбаминовой кислоты примера 84 данного варианта осуществления изобретения. Фиг. 33 представляет собой спектр 1 Н-ЯМР композиции для транспортировки и хранения сложного эфира N-замещенной карбаминовой кислоты примера 104 данного варианта осуществления изобретения. Фиг. 34 представляет собой спектр 1 Н-ЯМР композиции для транспортировки и хранения сложного эфира N-замещенной карбаминовой кислоты примера 120 данного варианта осуществления изобретения. Вариант осуществления изобретения Представленное ниже описание предоставляет подробное пояснение варианта осуществления данного изобретения (ссылка на который дается как на "данный вариант осуществления"). Кроме того, данное изобретение не ограничивается данным вариантом осуществления, представленным ниже, и может быть модифицировано различным образом в пределах его сущности. Вначале дано описание соединений, применяемых в способе получения по данному варианту осуществления, и соединений, которые составляют композицию для транспортировки и хранения по данному варианту осуществления. Органический амин. В качестве органического амина в данном варианте осуществления предпочтительно применяется органический первичный амин. В данном документе органический первичный амин относится к "первичному амину" (первичным моноаминам и первичным полиаминам), как это определено нормой С-8 номенклатуры (IUPAC Nomenclature of Organic Chemistry), установленной Международным союзом теоретической и прикладной химии, ИЮПАК (IUPAC). Этот органический амин представлен приведенной формулой (29). Эта норма основана на Рекомендациях по органической и биохимической номенклатуре(Recommendations on OrganicBiochemical Nomenclature). Далее в данном изобретении, в случае ссылки на нормы ИЮПАК, а также на указываемые затем номенклатурные нормы, определенные ИЮПАК (за исключением случаев специально упоминаемых рекомендаций ИЮПАК других лет), делаются ссылки на такие нормативные документы, как "YukikagakuSeikagaku Meimeihou" (Organic Chemistry и Biochemistry Nomenclature) (2-я редакция, опубликована в Японии в 1992 г. компанией Nankodo Co., Ltd.), который основан на издании, содержащем все нормы для органической химии и биохимии, наряду с транслитерированными нормами для японского языка, опубликованными в качестве приложения к "ChemicalFields" в 1980 г. на основе Рекомендаций 1979 (Recommendations 1979), а также на всех последующих редакциях и рекомендациях. Термин "органический" относится в общем к группе соединений, рассматриваемых как объект номенклатуры, представленной в приведенных выше публикациях. Данные объекты могут быть объектами, описанными в рекомендациях, опубликованных в 1993 г. Однако "органические" соединения, покрываемые номенклатурой, описанной выше, включают металлоорганические соединения и металлические комплексы. В данном варианте осуществления, хотя приведенное ниже описание предоставляет разъяснения в отношении терминов "органический" и/или "органические группы" и/или "заместители" и т.п., а также соединений, применяемых в данном варианте осуществления, если не приведено специального пояснения, они состоят из атомов, которые не включают атомы металлов и/или полуметаллов. Более предпочтительно в данном варианте осуществления применяются "органические соединения", "органические группы" и "заместители", состоящие из атомов, выбранных из Н (атомов водорода), С (атомов углерода), N (атомов азота), О (атомов кислорода), S (атомов серы), Cl (атомов хлора), Br (атомов брома) и I (атомов йода). Кроме того, в представленных ниже пояснениях часто используются термины "алифатический" и"ароматический". В соответствии с вышеупомянутыми нормами ИЮПАК органические соединения описаны как разделенные на алифатические соединения и ароматические соединения. Алифатические соединения относятся к определениям групп в соответствии с алифатическими соединениями на основе рекомендаций 1995 ИЮПАК. Алифатические соединения определяются в этих рекомендациях как"ациклические или циклические насыщенные или ненасыщенные углеродные соединения, исключая ароматические соединения". Кроме того, алифатические соединения, применяемые в пояснении данного варианта осуществления, включают насыщенные и ненасыщенные, а также линейные и циклические алифатические соединения и относятся к "органическим соединениям", "органическим группам" и "заместителям", состоящим из атомов, выбранных из вышеуказанных Н (атомов водорода); С (атомов углерода); N (атомов азота); О (атомов кислорода); S (атомов серы); Si (атомов кремния); и атомов галогенов,выбранных из Cl (атомов хлора), Br (атомов брома) и I (атомов йода). Кроме того, в случае, когда ароматическая группа, такая как аралкильная группа, связана с алифатической группой, на такие группы часто указывают как на "алифатическую группу, замещенную ароматической группой" или "группу, состоящую из алифатической группы, связанной с ароматической группой". Это основано на реакционной способности в данном варианте осуществления, поскольку свойства,относящиеся к реакциям групп, таких как аралкильные группы, имеют тесное сходство в отношении реакционной способности с алифатическими группами, а не с ароматическими группами. Кроме того, на неароматические реакционные группы, включая такие группы, как аралкильные группы и алкильные группы, часто указывают как на "алифатические группы, необязательно замещенные ароматической группой", "алифатическую группу, замещенную ароматической группой" или "алифатическую группу,связанную с ароматической группой" и т.п. Кроме того, хотя определения в соответствии с номенклатурными нормами, установленными ИЮПАК, как описано выше, применяются при пояснении общих формул соединений, используемых в данном описании, обычные названия часто используются в качестве названий определенных групп или названий соединений, приводимых в качестве примеров. В дополнение к этому, хотя числа атомов, числа заместителей и числа соединений часто приводятся в данном описании, все они выражаются целыми где R1 обозначает органическую группу, которая имеет от 1 до 85 атомов углерода и замещена n аминогруппами; а обозначает целое число от 1 до 10. В формуле (29) выше R1 обозначает алифатическую группу, ароматическую группу или группу,связанную с алифатической группой и ароматической группой, и обозначает группу, состоящую из ациклической углеводородной группы или циклической углеводородной группы (такой как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, поперечно сшитая циклическая углеводородная группа, спироуглеводородная группа, углеводородная группа, образующая кольцо, циклическая углеводородная группа, имеющая боковую цепь, гетероциклическая группа, гетероциклическая спирогруппа, кольцевая группа, поперечно сшитая гетероатомом, или гетероциклическая группа), группу, связанную с одним или несколькими видами групп, выбранных из вышеуказанных ациклических углеводородных групп и циклических углеводородных групп, и группы, в которых вышеуказанные группы соединены ковалентной связью с определенным неметаллическим атомом (углеродом, кислородом, азотом, серой или кремнием). Кроме того, ковалентная связь с определенным неметаллическим атомом (углеродом, кислородом, азотом, серой или кремнием), как описано выше, находится в состоянии, в котором вышеуказанные группы соединены ковалентной связью, например, с группами, представленными следующими формулами (30)-(38): Среди этих групп R1 группы R1, которые предпочтительно могут быть использованы в данном варианте осуществления с учетом их меньшей подверженности к возникновению побочных реакций,включают группы, выбранные из группы, состоящей из ациклических углеводородных групп и циклических углеводородных групп, выбранных из алифатических групп, ароматических групп и групп, связанных с алифатическими группами и ароматическими группами (таких как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, поперечно сшитая циклическая углеводородная группа, спироуглеводородная группа, углеводородная группа, образующая кольцо, или циклическая углеводородная группа, имеющая боковую цепь), и группы, связанные по меньшей мере с одним видом групп, выбранных из этой группы, (взаимно замещенные группы), имеющие от 1 до 85 атомов углерода. С учетом текучести и т.п. число атомов углерода предпочтительно составляет от 1 до 70 и более предпочтительно от 1 до 13. Предпочтительные примеры органических аминов, образованных группой R1, могут включать: 1) необязательно алифатически и/или ароматически замещенные ароматические органические первичные моноамины, в которых группа R1 имеет от 6 до 85 атомов углерода и включает один или несколько видов ароматических колец, необязательно замещенных алифатической группой и/или ароматической группой, ароматическая группа в группе R1 замещена группой NH2, а равно 1; 2) ароматические органические первичные полиамины, в которых группа R1 имеет от 6 до 85 атомов углерода и включает один или несколько видов ароматических колец, необязательно замещенных алифатической группой и/или ароматической группой, ароматическая группа в группе R1 замещена группой NH2, а составляет 2 или более; 3) алифатические органические первичные полиамины, в которых группа R1 является алифатической группой, имеющей от 1 до 85 атомов углерода, необязательно замещенной ароматической группой,и а равно 2 или 3. В представленных выше описаниях атомы, связанные с группой NH2 (и предпочтительно атомы углерода), которые содержатся в ароматическом кольце, отличают как ароматические органические амины,в то время как случаи соединения с атомами не в ароматическом кольце (главным образом атомами угле- 19022171 рода) отличают как алифатические органические амины. Более предпочтительные алифатические группы являются линейными углеводородными группами, циклическими углеводородными группами и по меньшей мере одним видом группы, выбранной из линейных углеводородных групп и циклических углеводородных групп (относящихся, например, к циклическим углеводородным группам, замещенным линейной углеводородной группой, или линейным углеводородным группам, замещенным циклической углеводородной группой), имеющих от 6 до 70 атомов углерода. Ниже приведен перечень конкретных примеров предпочтительных органических первичных аминов. 1) Ароматические органические моноамины. Необязательно алифатически и/или ароматически замещенные ароматические органические первичные моноамины, в которых группа R1 является группой, имеющей от 6 до 85 атомов углерода и включает один или несколько видов ароматических колец, необязательно замещенных алифатической группой и/или ароматической группой, ароматическая группа в группе R1 замещена группой NH2, и а равно 1, предпочтительно ароматические органические моноамины, в которых группа R1 является группой, имеющей от 6 до 70 атомов углерода и а равно 1, и более предпочтительно, с учетом текучести и т.п., ароматические органические моноамины, в которых группа R1 имеет от 6 до 13 атомов углерода и включает один или несколько видов ароматических колец, "замещенных группой NH2", и а равно 1, которые являются ароматическими органическими моноаминами, представленными приведенной формулой (39) По меньшей мере одно положение из орто-положения и/или пара-положения группы NH2 ароматического органического первичного моноамина, представленного формулой (39), является незамещенной,R9-R12 соответственно обозначают замещающую группу в произвольном положении, которая сохраняет ароматические свойства кольца, R9-R12 могут соответственно и независимым образом являться заместителями ароматического кольца, R9-R12 могут взаимно соединяться, чтобы образовать кольцо с ароматическим кольцом, и представляют собой атомы водорода или группы, состоящие из групп, в которых алкильная группа, циклоалкильная группа, арильная группа или группа, выбранная из группы, состоящей из этих групп, связана насыщенными углеводородными связями и/или эфирными связями, число атомов углерода групп R9-R12 является целым числом в интервале от 0 до 7, и общее число атомов углерода, которые входят в состав ароматического органического первичного моноамина, представленного формулой (39), составляет от 6 до 13. Предпочтительные примеры ароматических органических первичных моноаминов, представленных формулой (39), могут включать те из них, в которых группы R9 по R12 являются атомами водорода или группами, выбранными из алкильных групп, таких как метильная группа или этильная группа, и примеры таких ароматических органических первичных моноаминов могут включать анилин, аминотолуол(включая изомеры), диметиланилин (включая изомеры), диэтиланилин (включая изомеры), дипропиланилин (включая изомеры), аминонафталин (включая изомеры), аминометилнафталин (включая изомеры),диметилнафтиламин (включая изомеры) и триметилнафтиламин (включая изомеры), при более предпочтительном применении анилина. 2) Ароматические органические первичные полиамины. Ароматические органические первичные полиамины, в которых группа R1 является группой, имеющей от 6 до 85 атомов углерода и содержащей одно или несколько ароматических колец, необязательно замещенных алифатической группой и/или ароматической группой, ароматическая группа в группе R1 замещена группой NH2, а равно 2 или более, предпочтительно ароматические органические полиамины,в которых группа R1 является группой, имеющей от 6 до 70 атомов углерода, и а равно 2 или более, более предпочтительно, с учетом текучести и т.п., ароматические органические полиамины, в которых группаR1 имеет от 6 до 13 атомов углерода и включает один или несколько видов ароматических колец, "замещенных группой NH2", ароматическое кольцо может также быть замещено алкильной группой, арильной группой или аралкильной группой, и а равно 2 или более. Примеры таких ароматических органических полиаминов могут включать диаминобензол (включая изомеры), диаминотолуол (включая изомеры),метилендианилин (включая изомеры), диаминомезитилен (включая изомеры), диаминобифенил (включая изомеры), диаминодибензил (включая изомеры), бис-(аминофенил)пропан (включая изомеры), бис(аминофенил)эфир (включая изомеры), бис-(аминофеноксиэтан) (включая изомеры), диаминоксилол(включая изомеры), диаминоанизол (включая изомеры), диаминофенетол (включая изомеры), диаминонафталин (включая изомеры), диаминометилбензол (включая изомеры), диаминометилпиридин (включая изомеры), диаминометилнафталин (включая изомеры) и полиметиленполифенилполиамины, представленные приведенной формулой (40) где f обозначает целое число от 0 до 6. 3) Алифатические органические полиамины. Алифатические органические полиамины, в которых группа R1 органического амина, представленного формулой (29), является алифатической группой, в которой число атомов углерода является целым числом в интервале от 1 до 85 и которая может быть замещена ароматической группой, n равно 2 или 3. Более предпочтительные органические амины являются алифатическими органическими первичными аминами, в которых алифатическая группа является линейной углеводородной группой, циклической углеводородной группой или группой, с которой связан по меньшей мере один вид группы, выбранной из линейных углеводородных групп и циклических углеводородных групп (такой как циклическая углеводородная группа, замещенная линейной углеводородной группой, или линейная углеводородная группа, замещенная циклической углеводородной группой). Более предпочтительно органический амин является алифатическим органическим полиамином, в котором группа R1 является алифатической группой,которая является ациклической углеводородной группой, циклической углеводородной группой или группой, с которой связан по меньшей мере один вид группы, выбранной из ациклических углеводородных групп и циклических углеводородных групп (такой как циклическая углеводородная группа, замещенная ациклической углеводородной группой, или ациклическая углеводородная группа, замещенная циклической углеводородной группой), имеющей от 1 до 70 атомов углерода, и а равно 2 или 3. С учетом текучести и т.п. при крупномасштабном промышленном производстве органический амин наиболее предпочтительно является алифатическим органическим первичным полиамином, в котором группа R1 является ациклической углеводородной группой, циклической углеводородной группой или группой, с которой связан по меньшей мере один вид группы, выбранной из ациклических углеводородных групп и циклических углеводородных групп (такой как циклическая углеводородная группа, замещенная ациклической углеводородной группой, или ациклическая углеводородная группа, замещенная циклической углеводородной группой), имеющей от 6 до 13 атомов углерода и состоящей из атомов углерода и атомов водорода. А именно, это относится к случаю, в котором группа R1 является линейной и/или разветвленной алкильной группой, циклоалкильной группой или группой, состоящей из алкильных групп и циклоалкильных групп. Примеры этих органических аминов могут включать алифатические первичные диамины, такие как этилендиамин, диаминопропан (включая изомеры), диаминобутан (включая изомеры), диаминопентан (включая изомеры), диаминогексан (включая изомеры) или диаминодекан (включая изомеры); алифатические триамины, такие как триаминогексан (включая изомеры), триаминононан(включая изомеры) или триаминодекан (включая изомеры); и замещенные циклические алифатические полиамины, такие как диаминоциклобутан (включая изомеры), диаминоциклогексан (включая изомеры),3-аминометил-3,5,5-триметилциклогексиламин (цис- и/или транс-формы) или метилен-бис(циклогексиламин) (включая изомеры). Производное угольной кислоты. Производное угольной кислоты в данном варианте осуществления относится к соединению, представленному приведенной формулой (41). Оно является компонентом, который используется в качестве исходного вещества для получения сложного эфира N-замещенной карбаминовой кислоты вместе с органическим амином и ароматической гидроксикомпозицией. Кроме того, оно является компонентом, который может содержаться в композиции для транспортировки и хранения сложного эфира N-замещенной карбаминовой кислоты.Y обозначает органическую группу, имеющую от 1 до 20 атомов углерода, или аминогруппу, имеющую от 0 до 20 атомов углерода. Примеры соединений, представленных формулой (41) выше, могут включать карбамидные соединения и сложные эфиры карбаминовой кислоты. Карбамидные соединения относятся к соединениям, имеющим по меньшей мере одну карбамидную связь в их молекуле, и предпочтительно являются соединениями, имеющими одну карбамидную связь,представленными приведенной формулой (42) где R13, R14, R15 и R16 соответственно и независимым образом обозначают алифатическую группу,имеющую от 1 до 20 атомов углерода, алифатическую группу, имеющую от 7 до 20 атомов углерода,замещенных группой ароматического соединения, ароматическую группу, имеющую от 6 до 20 атомов углерода, или атом водорода,общее число атомов углерода, которые входят в состав R13 и R14, является целым числом от 0 до 20,и общее число атомов углерода, которые входят в состав R15 и R16, является целым числом от 0 до 20. Примеры R13, R14, R15 и R16 могут включать атом водорода, алкильные группы, такие как метильная группа, этильная группа, пропильная группа (включая изомеры), бутильная группа (включая изомеры),пентильная группа (включая изомеры), гексильная группа (включая изомеры), гептильная группа (включая изомеры), октильная группа (включая изомеры), нонильная группа (включая изомеры), децильная группа (включая изомеры), ундецильная группа (включая изомеры), додецильная группа (включая изомеры), тридецильная группа (включая изомеры), тетрадецильная группа (включая изомеры), пентадецильная группа (включая изомеры), гексадецильная группа (включая изомеры), гептадецильная группа(включая изомеры), октадецильная группа (включая изомеры) или нонадецильная группа (включая изомеры); арильные группы, в которых число атомов углерода, составляющих группу, составляет от 6 до 20,такие как фенильная группа, метилфенильная группа (включая изомеры), этилфенильная группа (включая изомеры), пропилфенильная группа (включая изомеры), бутилфенильная группа (включая изомеры),пентилфенильная группа (включая изомеры), гексилфенильная группа (включая изомеры), гептилфенильная группа (включая изомеры), октилфенильная группа (включая изомеры), нонилфенильная группа(включая изомеры), децилфенильная группа (включая изомеры), бифенильная группа (включая изомеры), диметилфенильная группа (включая изомеры), диэтилфенильная группа (включая изомеры), дипропилфенильная группа (включая изомеры), дибутилфенильная группа (включая изомеры), дипентилфенильная группа (включая изомеры), дигексилфенильная группа (включая изомеры), дигептилфенильная группа (включая изомеры), терфенильная группа (включая изомеры), триметилфенильная группа (включая изомеры), триэтилфенильная группа (включая изомеры), трипропилфенильная группа (включая изомеры) или трибутилфенильная группа (включая изомеры); и аралкильные группы, в которых число атомов углерода, составляющих группу, составляет от 7 до 20, такие как фенилметильная группа, фенилэтильная группа (включая изомеры), фенилпропильная группа (включая изомеры), фенилбутильная группа (включая изомеры), фенилпентильная группа (включая изомеры), фенилгексильная группа (включая изомеры), фенилгептильная группа (включая изомеры), фенилоктильная группа (включая изомеры) или фенилнонильная группа (включая изомеры). Конкретные примеры могут включать карбамид, метилкарбамид, этилкарбамид, пропилкарбамид(включая изомеры),ди(фенилпропил)карбамид (включая изомеры), ди(фенилбутил)карбамид (включая изомеры),ди(фенилпентил)карбамид (включая изомеры), ди(фенилгексил)карбамид (включая изомеры),ди(фенилгептил)карбамид (включая изомеры), ди(фенилоктил)карбамид (включая изомеры) и ди(фенилнонил)карбамид (включая изомеры). Среди них предпочтительным является использование карбамида, в котором R13, R14, R15 и R16 в формуле (42) выше являются атомами водорода. Сложный эфир не-N-замещенной карбаминовой кислоты, представленный приведенной формулой(43), является предпочтительным для использования в качестве сложного эфира карбаминовой кислоты где R17 обозначает алифатическую группу, имеющую от 1 до 50 атомов углерода, аралкильную группу, имеющую от 7 до 50 атомов углерода, или ароматическую группу, имеющую от 6 до 50 атомов углерода. Примеры алифатических групп R17 могут включать группы, состоящие из специфических неметаллических атомов (атомов углерода, кислорода, азота, серы, кремния или галогена). Предпочтительные примеры этих алифатических групп могут включать группы, в которых алифатическая группа является линейной углеводородной группой, циклической углеводородной группой или группой, с которой связан по меньшей мере один вид группы, выбранной из линейных углеводородных групп и циклических углеводородных групп (такой как циклическая углеводородная группа, замещенная линейной углеводородной группой, или линейная углеводородная группа, замещенная циклической углеводородной группой). Кроме того, примеры в случае аралкильной группы относятся к группам, в которых линейная и/или разветвленная алкильная группа замещена ароматической группой, и представляют группы, в которых алкильная группа, имеющая от 1 до 44 атомов углерода, замещена ароматической группой, имеющей от 6 до 49 атомов углерода. Как было пояснено выше, ароматическая группа предпочтительно относится к группе, состоящей из специфических неметаллических атомов (атомов углерода, кислорода, азота, серы,кремния или галогена), примеры которой могут включать моноциклическую ароматическую группу,конденсированную полициклическую ароматическую группу, поперечно сшитую циклическую ароматическую группу, ароматическую группу, образующую кольцо, и гетероциклическую ароматическую группу, более предпочтительно является замещенной и/или незамещенной фенильной группой, замещенной и/или незамещенной нафтильной группой или замещенной и/или незамещенной антрильной группой. Примеры ароматических групп R17 могут включать группы, состоящие из специфических неметаллических атомов (атомов углерода, кислорода, азота, серы, кремния или галогена), примеры которых могут включать моноциклическую ароматическую группу, конденсированную полициклическую ароматическую группу, поперечно сшитую циклическую ароматическую группу, ароматическую группу, образующую кольцо, и гетероциклическую ароматическую группу, более предпочтительно является замещенной и/или незамещенной фенильной группой, замещенной и/или незамещенной нафтильной группой или замещенной и/или незамещенной антрильной группой. Заместителями могут являться атомы водорода, алифатические группы (линейные углеводородные группы, циклические углеводородные группы и группы, связанные по меньшей мере с одним видом группы, выбранным из линейных углеводородных групп и циклических углеводородных групп (такие как циклическая углеводородная группа, замещенная линейной углеводородной группой, или линейная углеводородная группа, замещенная циклической уг- 23022171 леводородной группой или вышеуказанные ароматические группы, и могут также являться группы,состоящие из вышеуказанных алифатических групп и ароматических групп. Примеры этой R17 могут включать алкильные группы, в которых число атомов углерода, входящих в состав группы, составляет от 1 до 50, такие как метильная группа, этильная группа, пропильная группа(включая изомеры), нонадецильная группа (включая изомеры) или эйкозильная группа (включая изомеры); арильные группы, в которых число атомов углерода, входящих в состав группы, составляет от 6 до 50, такие как фенильная группа, метилфенильная группа (включая изомеры), этилфенильная группа(включая изомеры) или трибутилфенильная группа (включая изомеры); и аралкильные группы, в которых число атомов углерода, входящих в состав группы, составляет от 7 до 50, такие как фенилметильная группа, фенилэтильная группа (включая изомеры), фенилпропильная группа (включая изомеры), фенилбутильная группа (включая изомеры), фенилпентильная группа (включая изомеры), фенилгексильная группа (включая изомеры), фенилгептильная группа (включая изомеры), фенилоктильная группа (включая изомеры) или фенилнонильная группа (включая изомеры). Конкретные примеры могут включать метилкарбамат, этилкарбамат, пропилкарбамат (включая изомеры), бутилкарбамат (включая изомеры), пентилкарбамат (включая изомеры), гексилкарбамат(включая изомеры). Сложный эфир N-замещенной карбаминовой кислоты, содержащийся в композиции для транспортировки и хранения по данному варианту осуществления, предпочтительно получен из органического амина, производного угольной кислоты и ароматической гидроксикомпозиции. При этом имеется множество случаев, в которых сложный эфир не-N-замещенной карбаминовой кислоты, содержащийся в композиции для транспортировки и хранения, является сложным эфиром не-N-замещенной карбаминовой кислоты, в котором эфирная группа сложного эфира не-N-замещенной карбаминовой кислоты является производной от ароматической гидроксикомпозиции. Сложный эфир угольной кислоты. Сложный эфир угольной кислоты является компонентом, предпочтительно содержащимся в заданном количестве в композиции для транспортировки и хранения по данному варианту осуществления. Сложный эфир угольной кислоты относится к соединению, в котором один или два из двух атомов водорода угольной кислоты СО(ОН)2 замещены алифатической группой или ароматической группой. В данном варианте осуществления предпочтительно использование соединения, представленного приведенной формулой (44) где R18 и R19 соответственно и независимым образом обозначают алифатическую группу, имеющую от 1 до 20 атомов углерода, аралкильную группу, имеющую от 7 до 50 атомов углерода, или ароматическую группу, имеющую от 6 до 50 атомов углерода. Примеры алифатических групп R18 и R19 могут включать группы, состоящие из специфических неметаллических атомов (атомов углерода, кислорода, азота, серы, кремния или галогена). Предпочтительные примеры этих алифатических групп могут включать группы, в которых алифатическая группа является линейной углеводородной группой, циклической углеводородной группы или группой, с которой связан по меньшей мере один вид группы, выбранной из линейных углеводородных групп и циклических углеводородных групп (такой как циклическая углеводородная группа, замещенная линейной углеводородной группой, или линейная углеводородная группа, замещенная циклической углеводородной группой). Кроме того, примеры в случае аралкильной группы относятся к группам, в которых линейная и/или разветвленная алкильная группа замещена ароматической группой, и представляют группы, в которых алкильная группа, имеющая от 1 до 44 атомов углерода, замещена ароматической группой, имеющей от 6 до 49 атомов углерода. Как было пояснено выше, ароматическая группа предпочтительно относится к группе, состоящей из специфических неметаллических атомов (атомов углерода, кислорода, азота, серы,кремния или галогена), примеры которой могут включать моноциклическую ароматическую группу,конденсированную полициклическую ароматическую группу, поперечно сшитую циклическую ароматическую группу, ароматическую группу, образующую кольцо, и гетероциклическую ароматическую группу, и более предпочтительно является замещенной и/или незамещенной фенильной группой, замещенной и/или незамещенной нафтильной группой или замещенной и/или незамещенной антрильной группой. Примеры ароматических групп R18 и R19 могут включать группы, состоящие из специфических неметаллических атомов (атомов углерода, кислорода, азота, серы, кремния или галогена), примеры которых могут включать моноциклическую ароматическую группу, конденсированную полициклическую ароматическую группу, поперечно сшитую циклическую ароматическую группу, ароматическую группу,образующую кольцо, и гетероциклическую ароматическую группу, более предпочтительно является замещенной и/или незамещенной фенильной группой, замещенной и/или незамещенной нафтильной группой или замещенной и/или незамещенной антрильной группой. Заместителями могут являться атомы водорода, алифатические группы (линейные углеводородные группы, циклические углеводородные группы и группы, связанные по меньшей мере с одним видом группы, выбранным из линейных углеводородных групп и циклических углеводородных групп (такие как циклическая углеводородная группа,замещенная линейной углеводородной группой, или линейная углеводородная группа, замещенная циклической углеводородной группой или вышеуказанные ароматические группы, и могут также являться группы, состоящие из вышеуказанных алифатических групп и ароматических групп. Примеры этих R18 и R19 могут включать алкильные группы, такие как метильная группа, этильная группа, пропильная группа (включая изомеры), бутильная группа (включая изомеры), пентильная группа(включая изомеры), гексадецильная группа (включая изомеры), гептадецильная группа (включая изомеры), октадецильная группа (включая изомеры), нонадецильная группа (включая изомеры) или эйкозильная группа (включая изомеры); арильные группы, такие как фенильная группа, метилфенильная группа(включая изомеры), триметилфенильная группа (включая изомеры), триэтилфенильная группа (включая изомеры), трипропилфенильная группа (включая изомеры) или трибутилфенильная группа (включая изомеры); и аралкильные группы, такие как фенилметильная группа, фенилэтильная группа (включая изомеры), фенилпропильная группа (включая изомеры), фенилбутильная группа (включая изомеры), фенилпентильная группа (включая изомеры), фенилгексильная группа (включая изомеры), фенилгептиль- 25022171(включая изомеры). Конкретные примеры могут включать диметилкарбонат, диэтилкарбонат, дипропилкарбонат
МПК / Метки
МПК: C07C 269/04, C07C 263/04, C07C 269/08, C07C 271/40, C07C 265/14
Метки: ароматическое, сложный, сложного, получения, карбаминовой, способ, такого, применением, гидроксисоединение, n-замещенной, композиция, транспортировки, содержащая, хранения, эфира, кислоты, изоцианата, эфир
Код ссылки
<a href="https://eas.patents.su/30-22171-sposob-polucheniya-slozhnogo-efira-n-zameshhennojj-karbaminovojj-kisloty-sposob-polucheniya-izocianata-s-primeneniem-takogo-slozhnogo-efira-n-zameshhennojj-karbaminovojj-kisloty-i.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения сложного эфира n-замещенной карбаминовой кислоты, способ получения изоцианата с применением такого сложного эфира n-замещенной карбаминовой кислоты и композиция для транспортировки и хранения сложного эфира n-замещенной карбаминовой кислоты, содержащая сложный эфир n-замещенной карбаминовой кислоты и ароматическое гидроксисоединение</a>
Предыдущий патент: Батарейное устройство для транспортного средства с разделяемыми соединениями
Следующий патент: Способ ослабления низкочастотных помех в данных морской сейсмической косы с двумя типами датчиков
Случайный патент: Способ обработки и строительства скважин












