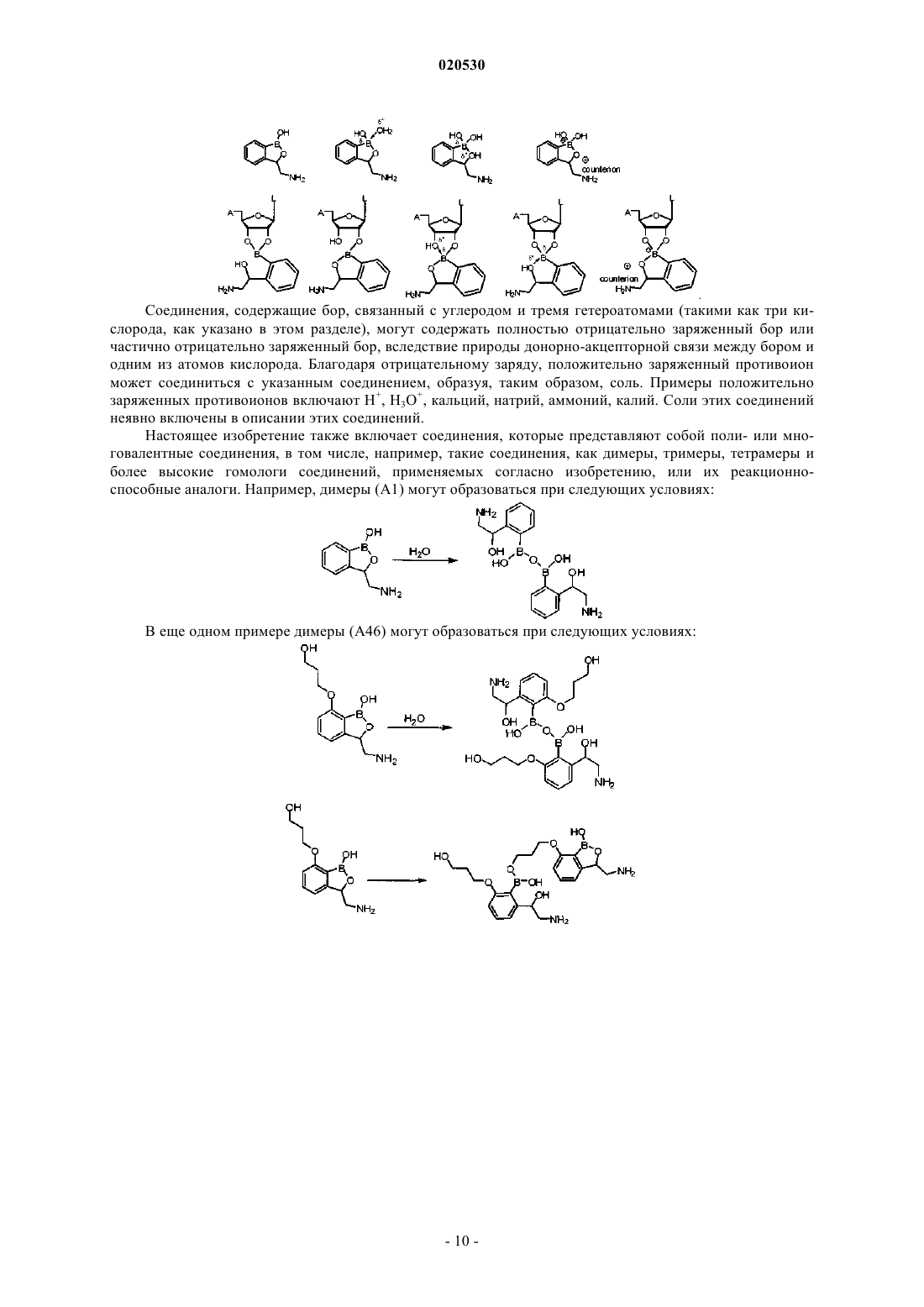
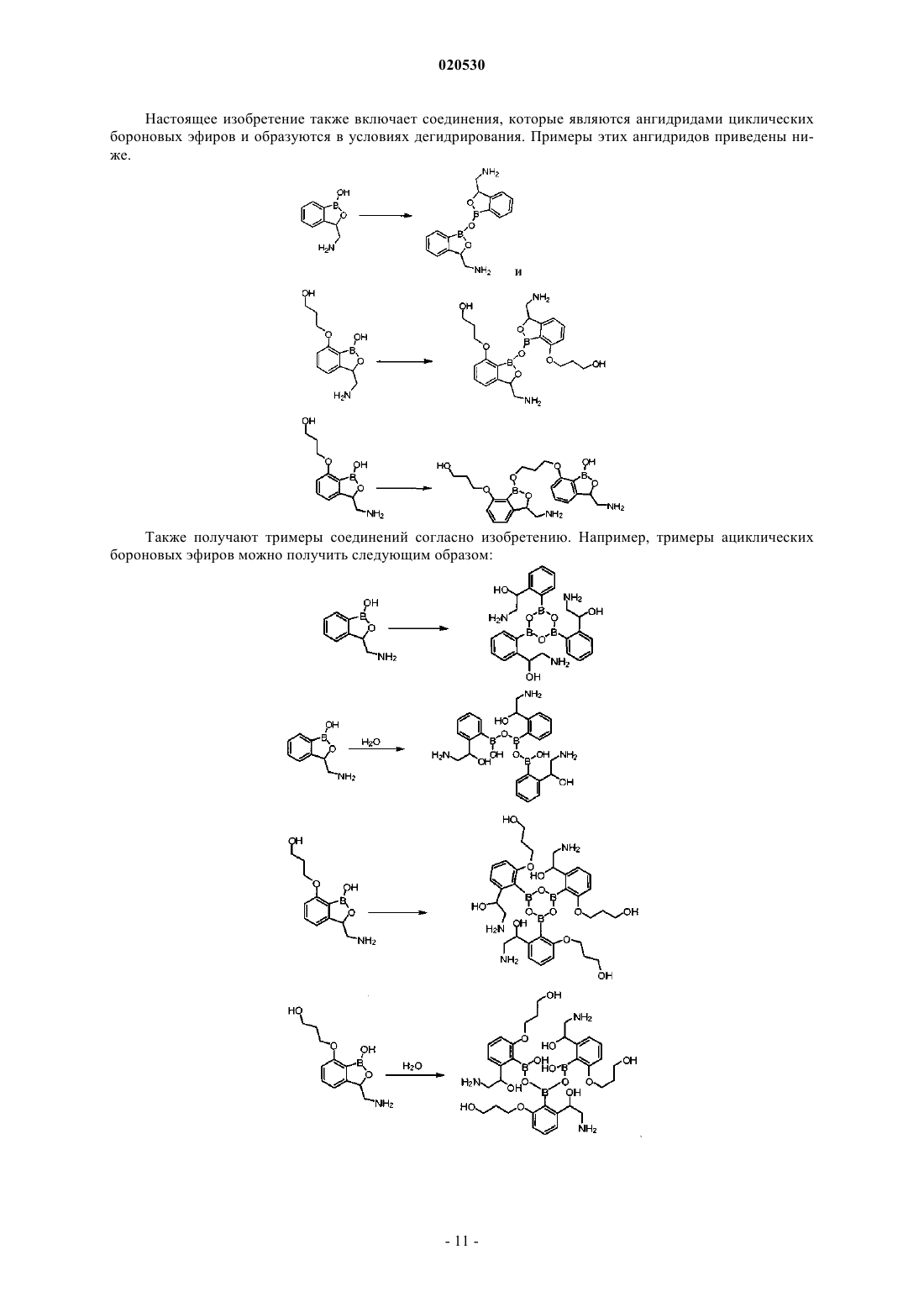
Борсодержащие молекулы небольшого размера
Номер патента: 20530
Опубликовано: 28.11.2014
Авторы: Ксиа Йи, Филлипс Джеймс Дж., Керамане Эль Мехди, Эрнандес Винсент С., Шарма Рашми, Лу Ксяозонг, Элли Майкл Ричард Кевин, Жоу Хучен, Ниман Джеймс А., Бейкер Стивен Дж., Ха Минх, Мохаммад Рахим, Акама Цутома, Жанг Йонг-Канг, Сингх Раджешвар, Платтнер Джейкоб Дж.
Формула / Реферат
1. Соединение формулы
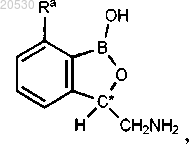
где С* является стереоцентром, имеющим конфигурацию, выбранную из (R) или (S);
Ra выбран из Н и -O(CR10R11)aR12; где
а представляет собой значение, выбранное из 1-10;
каждый из R10 и R11 выбран из Н, (С1-С10)алкила, который может быть разветвленным или циклическим, ОН, гидрокси(С1-С10)алкила и NH2;
R12 представляет собой R7, OR7, NH2, -C(O)R7, -C(O)OR7;
при этом R7 выбран из Н;
(С1-С10)алкила, который может быть разветвленным или циклическим и может быть замещен гидрокси;
при условии, что Ra и ОН совместно с атомами, к которым они присоединены, могут образовывать 6-10-членное гетероциклоалкильное кольцо, содержащее вплоть до двух атомов кислорода в качестве кольцевых атомов;
или его фармацевтически приемлемая соль, гидрат, сольват или ангидрид.
2. Соединение по п.1, где стереоцентр С* находится в (S)-конфигурации, или его соль.
3. Соединение по любому из пп.1-2, где а представляет собой значение, выбранное из 1-8, или его соль.
4. Соединение по п.3, где а представляет собой значение, выбранное из 2-4, или его соль.
5. Соединение по любому из пп.1-4, где каждый из R10 и R11 выбран из Н, (C1-С10)алкила, который может быть разветвленным или циклическим, ОН и NH2, или его соль.
6. Соединение по любому из пп.1-4, где каждый из R10 и R11 выбран из Н, гидрокси(С1-С10)алкила и NH2, или его соль.
7. Соединение по любому из пп.1-4, где по меньшей мере один из R10 или R11 выбран из гидрокси(С1-С10)алкила и NH2, или его соль.
8. Соединение по любому из пп.4-7, где
R12 выбран из Н и -OR7;
R7 выбран из Н, С1-С4алкила, которые могут быть замещены заместителями в количестве от 1 до 3, выбранными из (С1-С4)алкила и -ОСН3, или его соль.
9. Соединение по любому из пп.1-8, где R12 выбран из ОН, NH2, -СН3, -СН2СН3 и -С(О)ОН, или его соль.
10. Соединение по любому из пп.1-9, где R12 выбран из ОН, NH2, -СН3 и -СН2СН3, или его соль.
11. Соединение по любому из пп.1-10, где Ra выбран из -O(CH2)3NH2, -О(СН2)3OH, -ОСН2СН3,
-О(СН2)3ОСН3, -О(СН2)4ОН, -ОСН3, -О(СН2)3С(О)ОН, -O(CH2)4NH2, -O(CH2)2NH2,
-OCH2CH2CH(NH2)CH2OH, -ОСН2С(О)ОН и -ОСН2СН(СН2ОН)(СН2)ОН, или его соль.
12. Соединение по любому из пп.1-10, где Ra выбран из -О(СН2)3OH, -ОСН2СН3, -О(СН2)3ОСН3, -ОСН3,
-O(CH2)4NH2 и -O(CH2)3NH2, или его соль.
13. Соединение по любому из пп.1-10, где Ra выбран из Н, -О(СН2)3OH, -ОСН2СН3, -О(СН2)3ОСН3 и -ОСН3, или его соль.
14. Соединение по п.13, где Ra выбран из -О(СН2)3OH, -ОСН3 и -ОСН2СН3, или его соль.
15. Соединение по п.1, выбранное из
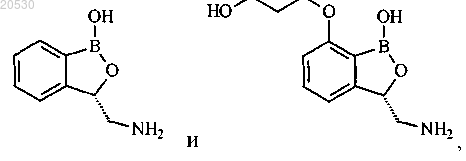
или его соль.
16. Соединение формулы
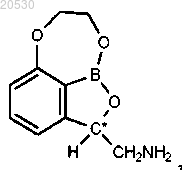
где С* представляет собой стереоцентр, или его фармацевтически приемлемая соль.
17. Соединение по п.16, где С* находится в (S)-конфигурации, или его соль.
18. Соединение по п.1, представляющее собой
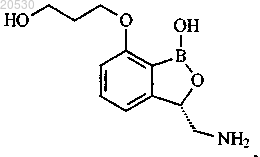
или его фармацевтически приемлемая соль, гидрат, сольват или ангидрид.
19. Соединение по п.18, представляющее собой
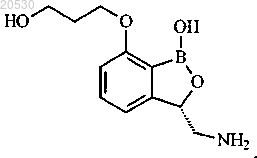
или его фармацевтически приемлемая соль.
20. Соединение по п.1, где каждый R10 и каждый R11 представляет собой Н, или его соль.
21. Соединение по п.20, где R12 представляет собой Н, и а представляет собой значение, выбранное из 2-4, или его соль.
22. Соединение по п.1, где Ra представляет собой Н, или его соль.
23. Соединение по п.1, где Ra представляет собой ОСН3, или его соль.
24. Соединение по п.1, где Ra представляет собой ОСН2СН3, или его соль.
25. Соединение по п.1, где Ra представляет собой О(СН2)3ОСН3, или его соль.
26. Соединение по п.1, где Ra представляет собой О(СН2)4ОН, или его соль.
27. Соединение по п.1, где Ra представляет собой О(СН2)СН[(СН2)ОН]2, или его соль.
28. Соединение по п.3 или 4, где R10 представляет собой Н; R11 представляет собой Н; и R12 представляет собой незамещенный циклоалкил, или его соль.
29. Соединение по п.1, где Ra представляет собой -О(СН2)3OH, или его соль.
30. Соединение по любому из пп.21-29, где С* находится в (S)-конфигурации.
31. Соединение по п.1, имеющее структуру
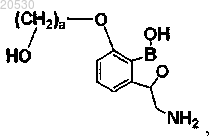
где а представляет собой значение, выбранное из 2-4, или его соль.
32. Соединение по п.31, имеющее структуру
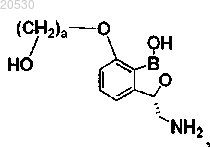
где а представляет собой значение, выбранное из 2-4, или его соль.
33. Фармацевтическая композиция для лечения заболевания, связанного с инфекцией, вызванной грамотрицательными бактериями, содержащая в качестве активного компонента
а) первый стереоизомер соединения по любому из пп.1-32, или его соль, гидрат или сольват,
б) второй стереоизомер указанного соединения,
при этом указанный первый стереоизомер присутствует в энантиомерном избытке, составляющем по меньшей мере 80% относительно указанного второго стереоизомера, и
в) фармацевтически приемлемый наполнитель.
34. Фармацевтическая композиция по п.33, где стереоцентр С* первого стереоизомера находится в (S)-конфигурации.
35. Фармацевтическая композиция для лечения заболевания, связанного с инфекцией, вызванной грамотрицательными бактериями, содержащая
а) соединение по любому из пп.1-32 или его соли, и
б) фармацевтически приемлемый наполнитель.
36. Способ ингибирования лейцил-тРНК-синтетазы, включающий приведение лейцил-тРНК-синтетазы в контакт с соединением по любому из пп.1-32 или его солью.
37. Способ предотвращения роста бактерии, включающий приведение указанного микроорганизма в контакт с эффективным количеством соединения по любому из пп.1-32 или его соли.
38. Способ уничтожения бактерии, включающий приведение указанного микроорганизма в контакт с эффективным количеством соединения по любому из пп.1-32 или его соли.
Текст
БОРСОДЕРЖАЩИЕ МОЛЕКУЛЫ НЕБОЛЬШОГО РАЗМЕРА В настоящем изобретении предложены новые соединения формулы Бейкер Стивен Дж., Эрнандес Винсент С. (US), Шарма Рашми, Ниман Джеймс А. (CA), Акама Цутома, Жанг Йонг-Канг, Платтнер Джейкоб Дж.,Элли Майкл Ричард Кевин (US),Сингх Раджешвар (CA), Ксиа Йи (US),Жоу Хучен (CN), Мохаммад Рахим,Керамане Эль Мехди, Лу Ксяозонг, Ха Минх (CA), Филлипс Джеймс Дж. (US) Поликарпов А.В., Борисова Е.Н. (RU) где С является стереоцентром, имеющим конфигурацию, выбранную из (R) или (S); и Ra выбран из Н и -O(CR10R11)aR12, где R10, R11, а и R12 имеют значения, определенные в описании изобретения; фармацевтические композиции для лечения заболевания, связанного с инфекцией,вызванной грамотрицательными бактериями, содержащие указанные соединения; а также способы ингибирования лейцил-тРНК-синтетазы, предотвращения роста бактерии и уничтожения бактерии с использованием указанных соединений. Перекрестные ссылки на родственные заявки Настоящая заявка испрашивает приоритет на основании предварительной заявки на патент США 60/945294, поданной 20 июня 2007 г., и предварительной заявки на патент США 61/041178, поданной 13 марта 2008 г., содержание каждой из которых в полном объеме включено в настоящее описание посредством ссылки для всех целей. Уровень техники Повсеместное увеличение устойчивости бактерий и других микроорганизмов к антибиотикам и противомикробным препаратам представляет собой, в целом, значительную угрозу. Поступление огромных количеств противомикробных препаратов в экосферу на протяжении последних 60 лет оказывало мощное селективное воздействие и привело к появлению и распространению патогенных микроорганизмов, устойчивых к противомикробным средствам. Соответственно, существует потребность в обнаружении новых противомикробных препаратов широкого спектра действия, таких как антибиотики, которые можно применять для борьбы с микроорганизмами, особенно теми, которые обладают множественной лекарственной устойчивостью. Борсодержащие молекулы, такие как оксаборолы, применяемые в качестве противомикробных препаратов, были ранее предложены, например, в публикациях патентов США US 20060234981 и 20070155699. В целом, оксаборол имеет следующую структуру и систему нумерации заместителей: Неожиданно было обнаружено, что некоторые классы оксаборолов, которые являются монозамещенными в 3-, 6- или 7-положении, или дизамещенными в 3-/6- или 3-/7-положениях, представляют собой эффективные противобактериальные средства. Это и другие применения таких оксаборолов предложены в настоящем изобретении. Краткое изложение сущности изобретения В настоящем изобретении предложено соединение формулыRa выбран из Н и -O(CR10R11)aR12; где а представляет собой значение, выбранное из 1-10; каждый из R10 и R11 выбран из Н, (С 1-С 10)алкила, который может быть разветвленным или циклическим, ОН, гидрокси(С 1-С 10)алкила и NH2;R12 представляет собой R7, OR7, NH2, -C(O)R7, -C(O)OR7; при этом R7 выбран из Н; (С 1-С 10)алкила, который может быть разветвленным или циклическим и может быть замещен гидрокси; при условии, что Ra и ОН совместно с атомами, к которым они присоединены, могут образовывать 6-10-членное гетероциклоалкильное кольцо, содержащее вплоть до двух атомов кислорода в качестве кольцевых атомов; или его фармацевтически приемлемая соль, гидрат, сольват или ангидрид. В одном воплощении соединений по изобретению стереоцентр С находится в (S)-конфигурации. В другом воплощении соединений по изобретению а представляет собой значение, выбранное из 18. В конкретном воплощении а представляет собой значение, выбранное из 2-4. В еще одном воплощении соединений по изобретению каждый из R10 и R11 выбран из Н, (С 1 С 10)алкила, который может быть разветвленным или циклическим, ОН и NH2. В еще одном воплощении соединений по изобретению каждый из R10 и R11 выбран из Н, гидрокси(С 1-С 10)алкила и NH2. В еще одном воплощении соединений по изобретению по меньшей мере один из R10 или R11 выбран из гидрокси(С 1-С 10)алкила и NH2. В еще одном воплощении соединений по изобретению R12 выбран из Н и -OR7; где R7 выбран из Н,С 1-С 4 алкила, которые могут быть замещены заместителями в количестве от 1 до 3, выбранными из (С 1 С 4)алкила и -ОСН 3. В еще одном воплощении соединений по изобретению R12 выбран из ОН, NH2, -СН 3, -СН 2 СН 3 и С(О)ОН. В конкретном воплощении R12 выбран из ОН, NH2, -СН 3 и -СН 2 СН 3.-1 020530 В еще одном воплощении соединений по изобретению Ra выбран из -О(СН 2)3NH2, -О(СН 2)3 ОН,ОСН 2 СН 3, -О(СН 2)3 ОСН 3, -О(СН 2)4 ОН, -ОСН 3, -О(СН 2)3 С(О)ОН, -O(CH2)4NH2, -O(CH2)2NH2,OCH2CH2CH(NH2)CH2OH, -ОСН 2 С(О)ОН и -ОСН 2 СН(СН 2 ОН)(СН 2)ОН. В конкретном воплощении соединений по изобретению Ra выбран из -О(СН 2)3 ОН, -ОСН 2 СН 3,О(СН 2)3 ОСН 3, -ОСН 3, -O(CH2)4NH2 и -O(CH2)3NH2. В еще одном воплощении соединений по изобретению Ra выбран из Н, -О(СН 2)3 ОН, -ОСН 2 СН 3,О(СН 2)3 ОСН 3 и -ОСН 3. В еще более конкретном воплощении Ra выбран из -О(СН 2)3 ОН, -ОСН 3 и -ОСН 2 СН 3. В другом воплощении соединение по изобретению выбрано из или их солей. Кроме того, в настоящем изобретении предложено соединение формулы где С представляет собой стереоцентр,или его фармацевтически приемлемая соль. В одном воплощении указанного соединения по изобретению С находится в (S)-конфигурации. В еще одном воплощении соединение по изобретению представляет собой или его фармацевтически приемлемую соль, гидрат, сольват или ангидрид. В конкретном воплощении соединение по изобретению представляет собой или его фармацевтически приемлемую соль. В еще одном воплощении соединений по изобретению каждый R10 и каждый R11 представляет собой Н. В еще одном воплощении соединений по изобретению R12 представляет собой Н, и а представляет собой значение, выбранное из 2-4. В еще одном воплощении соединений по изобретению Ra представляет собой Н. В еще одном воплощении соединений по изобретению Ra представляет собой ОСН 3. В еще одном воплощении соединений по изобретению Ra представляет собой OCH2CH3. В еще одном воплощении соединений по изобретению Ra представляет собой О(СН 2)3 ОСН 3. В еще одном воплощении соединений по изобретению Ra представляет собой О(СН 2)4 ОН. В еще одном воплощении соединений по изобретению Ra представляет собой О(СН 2)СН[(СН 2)ОН]2. В еще одном воплощении соединений по изобретению R10 представляет собой Н, R11 представляет собой Н, и R12 представляет собой незамещенный циклоалкил. В еще одном воплощении соединений по изобретению Ra представляет собой -О(СН 2)3 ОН. В конкретном воплощении соединений по изобретению С находится в (S)-конфигурации. В еще одном воплощении предложено соединение по изобретению, имеющее структуру где а представляет собой значение, выбранное из 2-4, или его соль. В еще одном воплощении предложено соединение по изобретению, имеющее структуру где а представляет собой значение, выбранное из 2-4, или его соль. В настоящем изобретении также предложена фармацевтическая композиция для лечения заболевания, связанного с инфекцией, вызванной грамотрицательными бактериями, содержащая в качестве активного компонента а) первый стереоизомер соединения по изобретению или его соль, гидрат или сольват; б) второй стереоизомер указанного соединения; при этом указанный первый стереоизомер присутствует в энантиомерном избытке, составляющем по меньшей мере 80% относительно указанного второго стереоизомера, и в) фармацевтически приемлемый наполнитель. В одном воплощении фармацевтической композиции стереоцентр С указанного первого стереоизомера находится в (S)-конфигурации. В настоящем изобретении также предложена фармацевтическая композиция для лечения заболевания, связанного с инфекцией, вызванной грамотрицательными бактериями, содержащая а) соединение по изобретению или его соли и б) фармацевтически приемлемый наполнитель. В настоящем изобретении также предложен способ ингибирования лейцил-тРНК-синтетазы, включающий приведение лейцил-тРНК-синтетазы в контакт с соединением по изобретению или его солью. Кроме того, в настоящем изобретении также предложен способ предотвращения роста бактерии,включающий приведение указанного микроорганизма в контакт с эффективным количеством соединения по изобретению или его соли. В настоящем изобретении также предложен способ уничтожения бактерии, включающий приведение указанного микроорганизма в контакт с эффективным количеством соединения по изобретению или его соли. Краткое описание графических материалов На фиг. 1 представлены данные минимальной ингибирующей концентрации (MIC) для репрезентативных соединений согласно изобретению. На фиг. 2 представлены данные концентрации, ингибирующей 50% активности (IC50), для репрезентативных соединений согласно изобретению. Подробное описание изобретения- тетрагидропиранил; Ас - ацетил; PTSA - пара-толуолсульфокислота; Pyr. - пиридин; Cbz - бензилоксикарбонил; МРМ - п-метоксибензил; DHP - дигидропиран; CSA - камфорсульфокислота; СТАВ - бромидцетилтриметиламмония; нас. - насыщенный; Су - циклогексил. В настоящем описании "соединение согласно изобретению" относится к соединениям, предложенным в настоящем изобретении, солям (например, фармацевтически приемлемым солям), пролекарствам,сольватам и гидратам этих соединений. МКИ, или минимальная концентрация ингибирования, представляет собой концентрацию, при которой соединение обеспечивает прекращение роста клеток более чем на 50%, предпочтительно более чем на 60%, предпочтительно более чем на 70%, предпочтительно более чем на 80%, предпочтительно более чем на 90%, относительно контрольной группы, не подвергаемой обработке. При обозначении заместителей с помощью соответствующих общепринятых химических формул,записанных слева направо, указанные заместители в равной степени включают химически идентичные заместители, полученные при написании структуры справа налево; например, подразумевают, что СН 2 О- также включает -ОСН 2-. В настоящем описании термин "поли" означает по меньшей мере 2. Например, поливалентный ион металла представляет собой ион металла, имеющий валентность по меньшей мере 2., применяемый в качестве связи или изображенный перпендикулярно к связи, указывает на место присоединения данной группы к остальной части молекулы. Термин "алкил", взятый в отдельности или как часть другого заместителя, означает, если не указано иное, прямую или разветвленную цепь, или циклический углеводородный радикал или их комбинацию,которая может быть полностью насыщенной, моно- или полиненасыщенной и может включать двух- и многовалентные радикалы, имеющие обозначенное количество углеродных атомов (т.е. C1-С 10 означает от одного до десяти атомов углерода). Согласно некоторым вариантам реализации термин "алкил" означает прямую или разветвленную цепь или их комбинации, которые могут быть полностью насыщенными, моно- или полиненасыщенными и могут включать двух- и многовалентные радикалы. Примеры насыщенных углеводородных радикалов включают, но не ограничиваются ими, такие группы как метил,этил, н-пропил, изопропил, н-бутил, т-бутил, изобутил, втор-бутил, циклогексил, (циклогексил)метил,циклопропилметил, гомологи и изомеры, например, н-пентила, н-гексила, н-гептила, н-октила и т. п. Ненасыщенная алкильная группа представляет собой группу, содержащую одну или более двойных связей или тройных связей. Примеры ненасыщенных алкильных групп включают, но не ограничиваются ими,винил, 2-пропенил, кротил, 2-изопентенил, 2-(бутадиенил), 2,4-пентадиенил, 3-(1,4-пентадиенил), этинил, 1- и 3-пропинил, 3-бутинил и последующие высшие гомологи и изомеры. Термин "алкилен", взятый в отдельности или как часть другого заместителя, означает двухвалентный радикал, образованный из алкана, например, помимо прочего, -СН 2 СН 2 СН 2 СН 2-, и также включает те группы, которые описаны ниже как "гетероалкилен". Обычно, алкильная (или алкиленовая) группа содержит от 1 до 24 углеродных атомов, при этом согласно настоящему изобретению группы с 10 или менее углеродными атомами являются предпочтительными. "Низший алкил" или " низший алкилен" представляет собой алкильную или алкиленовую группу с более короткой цепью, в общем случае содержащую восемь или менее углеродных атомов. Термины "алкокси", "алкиламино" и "алкилтио" (или тиоалкокси) применяются в их общепринятом смысле и относятся к тем алкильным группам, которые присоединены к оставшейся части молекулы через кислородный атом, аминогруппу или атом серы, соответственно. Термин "гетероалкил", взятый в отдельности или в комбинации с другим термином, означает, если не указано иное, стабильный углеводородный радикал с прямой или разветвленной цепью, или циклический углеводородный радикал, или их комбинации, содержащий указанное количество углеродных атомов и по меньшей мере один гетероатом. Согласно некоторым вариантам реализации изобретения термин "гетероалкил", взятый в отдельности или в комбинации с другим термином, означает стабильную прямую или разветвленную цепь, или их комбинации, состоящую из указанного количества углеродных атомов и по меньшей мере одного гетероатома. Согласно типичному варианту реализации изобретения гетероатомы можно выбрать из группы, включающей В, О, N и S, при этом атомы азота и серы могут быть окисленными, и гетероатом азота может быть четвертичным. Гетероатом (гетероатомы) В, О, N и S могут размещаться в любом положении внутри гетероалкильной группы или в положении, в котором алкильная группа присоединена к оставшейся части молекулы. Примеры включают, но не ограничиваются ими, -СН 2-СН 2-О-СН 3, -CH2-CH2-NH-CH3, -CH2-CH2-N(CH3)-CH3, -CH2-S-CH2-CH3, -CH2-CH2,-S(O)CH3, -CH2-CH2-S(O)2-CH3, -CH=CH-O-CH3, -CH2-CH=N-OCH3 и -CH=CH-N(CH3)-CH3. До двух гетероатомов могут следовать друг за другом, как, например, в -CH2-NH-OCH3. Аналогичным образом, термин"гетероалкилен", взятый в отдельности или как часть другого заместителя, означает двухвалентный радикал, образованный из гетероалкила, например, помимо прочего, -CH2-CH2-S-CH2-CH2- и -CH2-S-CH2CH2-NH-CH2-. Что касается гетероалкиленовых групп, гетероатомы также могут занимать одно или оба положения на концах цепи (например, алкиленокси, алкилендиокси, алкиленамино, алкилендиамино и т.п.). Кроме того, в отношении алкиленовых и гетероалкиленовых связывающих групп не принимают во внимание ориентацию связывающей группы по направлению, в котором записана формула связывающей группы. Например, формула -C(O)2R'- включает как -C(O)2R'-, так и -R'С(О)2-. Термины "циклоалкил" и "гетероциклоалкил", взятые в отдельности или в комбинации с другими терминами, представляют собой, если не указано иное, циклические модификации "алкила" и "гетероалкила", соответственно. Дополнительно, что касается гетероциклоалкила, гетероатом может занимать положение, по которому гетероцикл присоединен к оставшейся части молекулы. Примеры циклоалкила включают, но не ограничиваются ими, циклопентил, циклогексил, 1-циклогексенил, 3-циклогексенил,циклогептил и т.п. Примеры гетероциклоалкила включают, но не ограничиваются ими, 1-(1,2,5,6-4 020530 тетрагидропиридил), 1-пиперидинил, 2-пиперидинил, 3-пиперидинил, 4-морфолинил, 3-морфолинил, тетрагидрофуран-2-ил, тетрагидрофуран-3-ил, тетрагидротиен-2-ил, тетрагидротиен-3-ил, 1-пиперазинил, 2 пиперазинил и т.п. Термины "гало" или "галоген", сами по себе или как часть другого заместителя, означают, если не указано иное, атом фтора, хлора, брома или йода. Кроме того, предполагают, что такие термины, как "галоалкил", включают моногалоалкил и полигалоалкил. Например, предполагают, что термин "гало(С 1 С 4)алкил" включает, но не ограничивается ими, трифторметил, 2,2,2-трифторэтил, 4-хлорбутил, 3 бромпропил и т.п. Термин "арил" означает, если не указано иное, полиненасыщенный ароматический заместитель, который может представлять собой одно кольцо или несколько колец (предпочтительно от 1 до 3 колец),которые сконденсированы вместе или связаны ковалентной связью. Термин "гетероарил" относится к арильным группам (или кольцам), которые содержат от одного до четырех гетероатомов. Согласно типичному варианту реализации изобретения гетероатом выбирают из В, N, О и S, при этом атомы азота и серы возможно являются окисленными, и атом (атомы) азота возможно является четвертичным. Гетероарильная группа может быть присоединена к оставшейся части молекулы через гетероатом. Неограничивающие примеры арильных и гетероарильных групп включают фенил, 1-нафтил, 2-нафтил, 4-бифенил, 1 пирролил, 2-пирролил, 3-пирролил, 3-пиразолил, 2-имидазолил, 4-имидазолил, пиразинил, 2-оксазолил,4-оксазолил, 2-фенил-4-оксазолил, 5-оксазолил, 3-изоксазолил, 4-изоксазолил, 5-изоксазолил, 2 тиазолил, 4-тиазолил, 5-тиазолил, 2-фурил, 3-фурил, 2-тиенил 3-тиенил, 2-пиридил, 3-пиридил, 4 пиридил, 2-пиримидил, 4-пиримидил, 5-бензотиазолил, пуринил, 2-бензимидазолил, 5-индолил, 1 изохинолил, 5-изохинолил, 2-хиноксалинил, 5-хиноксалинил, 3-хинолил, 6-хинолил, диоксаборолан, диоксаборинан и диоксаборепан. Заместители в каждой из указанных арильных и гетероарильных кольцевых систем выбирают из группы приемлемых заместителей, описанных ниже. Для краткости, термин "арил" при использовании в комбинации с другими терминами (например,арилокси, арилтиокси, арилалкил) включает те радикалы, в которых арильная группа присоединена к остальной части молекулы через ближайшую группу. Таким образом, подразумевают, что термин "арилалкил" включает те радикалы, в которых арильная группа присоединена к алкильной группе (например,бензил, 1-(3-нитрофенил)этил и т.п.). Такой заместитель, как бензил или 1-(3-нитрофенил)этил, также может быть представлен как "замещенный алкил", при этом этиловый радикал содержит 3 нитрофенильную группу. Подразумевают, что термин "арилокси" включает те радикалы, в которых арильная группа присоединена к кислородному атому. Подразумевают, что термин "арилоксиалкил" включает те радикалы, в которых арильная группа присоединена к кислородному атому, который, в свою очередь, присоединен к алкильной группе (например, феноксиметил, 3-(1-нафтилокси)пропил и т.п.). Для краткости, термин "гетероарил" при использовании в комбинации с другими терминами (например, гетероарилокси, гетероарилтиокси, гетероарилалкил) включает те радикалы, в которых гетероарильная группа присоединена к остальной чти молекулы через ближайшую группу. Таким образом, подразумевают, что термин "гетероарилалкил" включает те радикалы, в которых гетероарильная группа присоединена к алкильной группе (например, пиридилметил и т.п.). Подразумевают, что термин "гетероарилокси" включает те радикалы, в которых гетероарильная группа присоединена к кислородному атому. Подразумевают, что термин "гетероарилоксиалкил" включает те радикалы, в которых арильная группа присоединена к кислородному атому, который затем присоединяется к алкильной группе (например, 2-пиридилоксиметил и т.п.). Подразумевают, что каждый из вышеуказанных терминов (например, "алкил", "гетероалкил","арил" и "гетероарил") включает как замещенные, так и незамещенные формы указанного радикала. Предпочтительные заместители для каждого вида радикалов приведены ниже. Заместители для алкильных и гетероалкильных радикалов (в том числе группы, упоминаемые как алкилен, алкенил, гетероалкилен, гетероалкенил, алкинил, циклоалкил, гетероциклоалкил, циклоалкенил и гетероциклоалкенил) в общем случае относятся к "заместителям алкильной группы", при этом они могут представлять собой одну или более из различных групп, выбранных из, помимо прочего: -R', -OR',=O, =NR', =N-OR', -NR'R", -SR', -галогена, -SiR'R"R'", -OC(O)R', -C(O)R', -CO2R', -CONR'R", OC(O)NR'R", -NR"C(O)R', -NR'-C(O)NR"R'", -NR"C(O)2R', -NR'-C(NR'R"R'")=NR, -NRC(NR'R")=NR'", -S(O)R', -S(O)2R', -S(O)2NR'R", -NR"SO2R', -CN, -NO2, -N3, -CH(Ph)2, фтор(С 1-С 4)алкокси и фтор(С 1-С 4)алкила, в количестве, варьирующемся от нуля до (2m'+1), где m' представляет собой суммарное количество углеродных атомов в таком радикале. Предпочтительно, если каждый R', R", R"', R и R"'" независимо относится к водороду, замещенному или незамещенному гетероалкилу, замещенному или незамещенному арилу, например, арилу, содержащему 1-3 галогена, замещенному или незамещенному алкилу, алкокси или тиоалкокси-группам, или арилалкильным группам. Если соединение согласно изобретению, например, содержит более чем одну R группу, каждую из R групп выбирают независимо,также как и каждые R', R", R"', R и R' группы, когда присутствует более чем одна из этих групп. ЕслиR' и R" присоединены к одному и тому же атому азота, они могут объединяться с атомом азота с образованием 5-, 6- или 7-членного кольца. Например, подразумевают, что -NR'R" включает, но не ограничиваются ими, 1-пирролидинил и 4-морфолинил. Из вышеуказанного описания заместителей для специали-5 020530 ста в данной области техники очевидно, что термин "алкил" включает группы, в том числе углеродные атомы, связанные с группами, отличными от водородных групп, таких как галоалкил (например, -CF3 и CH2CF3) и ацил (например, -С(О)СН 3, -C(O)CF3, -C(O)CH2OCH3 и т.п.). Подобно заместителям, описанным для алкильного радикала, заместители для арильных и гетероарильных групп, в общем случае, относятся к "заместителям арильной группы". Заместители выбирают,например, из -R', -OR', =O, =NR', =N-OR', -NR'R", -SR', -галогена, -SiR'R"R", -OC(O)R', -C(O)R', -CO2R', CONR'R", -OC(O)NR'R", -NR"C(O)R', -NR'-C(O)NR"R'", -NR"C(O)2R', -NR'-C(NR'R"R'")=NR, -NRC(NR'R")=NR'", -S(O)R', -S(O)2R', -S(O)2NR'R", -NR"SO2R', -CN, -NO2, -N3, -CH(Ph)2, фтор(С 1-С 4)алкокси и фтор(С 1-С 4)алкила, в количестве, варьирующемся от нуля до суммарного количества свободных валентностей в системе ароматических колец; и где R', R", R'", R и R' предпочтительно независимо выбирают из водорода, замещенного или незамещенного алкила, замещенного или незамещенного гетероалкила, замещенного или незамещенного арила и замещенного или незамещенного гетероарила. Если соединение согласно изобретению включает, например, более чем одну R группу, каждую из R групп выбирают независимо, также как и каждые R', R", R'", R и R' группы, когда присутствует более чем одна из этих групп. Два из заместителей у соседних атомов арильного или гетероарильного кольца могут быть заменены на заместитель формулы -T-C(O)-(CRR')q-U-, где Т и U независимо представляют собой -NR-, -O-, CRR'- или одинарную связь, и q представляет собой целое число от 0 до 3. Альтернативным образом, два из заместителей в соседних атомах арильного или гетероарильного кольца могут быть заменены на заместитель формулы -А-(СН 2)r-В-, где А и В независимо представляют собой -CRR'-, -O-, -NR-, -S-, -S(O), -S(O)2-, -S(O)2NR'- или одинарную связь, и r представляет собой целое число от 1 до 4. Одна из одинарных связей таким образом образованного нового кольца может быть заменена на двойную связь. Альтернативным образом, два заместителя в соседних атомах арильного или гетероарильного кольца могут быть заменены на заместитель формулы -(CRR')S-X-(CR"R'")d-, где s и d независимо представляют собой целые числа от 0 до 3, и X представляет собой -О-, -NR'-, -S-, -S(O)-, -S(O)2- или -S(O)2NR'-. Предпочтительно, если заместители R, R', R" и R'" независимо выбирают из водорода или замещенного или незамещенного (C1-С 6)алкила. В настоящем описании "кольцо" означает замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил. Кольцо включает конденсированные кольцевые группы. Количество атомов в кольце обычно определяется количеством членов в кольце. Например, "5-7-членное кольцо" означает,что кольцевая система содержит от 5 до 7 атомов. Если не указано специально, кольцо возможно включает гетероатом. Таким образом, термин "5-7-членное кольцо" включает, например фенил, пиридинил и пиперидинил. С другой стороны, термин "5-7-членное гетероциклоалкильное кольцо" скорее включает пиридинил и пиперидинил, но не фенил. Термин "кольцо" также включает кольцевую систему, содержащую более чем одно "кольцо", при этом каждое "кольцо" независимо определено, как указано выше. В настоящем описании термин "гетероатом" включает атомы, отличные от углерода (С) и водорода(Н). Примеры включают кислород (О), азот (N), серу (S), кремний (Si), германий (Ge), алюминий (Al) и бор (В). Термин "уходящая группа" означает функциональную группу или атом, который может быть заменен другой функциональной группой или атомом в ходе реакции замещения, такой как реакция нуклеофильного замещения. В качестве примера, типичные уходящие группы включают группы трифлат, хлор,бром и йод; группы сульфоэфиров, такие как мезилат, тозилат, брозилат, нозилат и т.п.; и ацилоксигруппы, такие как ацетокси, трифторацетокси и т.п. Термин "аминозащитная группа" обозначает защитную группу, подходящую для предотвращения нежелательных реакций азота аминогруппы. Типичные аминозащитные группы включают, но не ограничиваются ими, формил; ацильные группы, например алканоильные группы, такие как ацетил, трихлорацетил или трифторацетил; алкоксикарбонильные группы, такие как трет-бутоксикарбонил (Boc); арилметоксикарбонильные группы, такие как бензилоксикарбонил (Cbz) и 9-флуоренилметоксикарбонил(Fmoc); арилметильные группы, такие как бензил (Bn), тритил (Tr) и 1,1-2-(4'-метоксифенил)метил; силильные группы, такие как триметилсилил (TMS) и трет-бутилдиметилсилил (TBS) и т.п. Термин "гидроксизащитная группа" означает защитную группу, подходящую для предотвращения нежелательных реакций гидроксигруппы. Типичные гидроксизащитные группы включают, но не ограничиваются ими, алкильные группы, такие как метил, этил и трет-бутил; ацильные группы, например алканоильные группы, такие как ацетил; арилметильные группы, такие как бензил (Bn), п-метоксибензил(РМВ), 9-флуоренилметил (Fm) и дифенилметил (бензгидрил, DPM); силильные группы, такие как триметилсилил (TMS) и трет-бутилдиметилсилил (TBS) и т.п. Символ "R" является общепринятым сокращением, которое означает замещающую группу, которую выбирают из замещенных или незамещенных алкильных, замещенных или незамещенных гетероалкильных, замещенных или незамещенных арильных, замещенных или незамещенных гетероарильных,замещенных или незамещенных циклоалкильных и замещенных или незамещенных гетероциклоалкильных групп. Термин "образованный из" имеет общеупотребимое значение и также относится к молекуле, которая является на 99-80%, 75%, 70%, 65%, или 60% гомологичной относительно рассматриваемой молекулы. Молекулы, имеющие отношение к этому определению, включают цепи РНК или ДНК, олигонуклеотиды, полипептиды или белки любой длины и состава. Подразумевают, что термин "неродственный" охватывает как единственную, так и множественную формы слова, т.е. фраза "неродственная аминокислота" включает одну или более аминокислот. Под "эффективным" количеством лекарственного препарата, композиции или проникающего вещества подразумевают количество активного вещества, достаточное для обеспечения требуемого локального или системного эффекта. "Топически эффективное", "косметически эффективное", "фармацевтически эффективное" или "терапевтически эффективное" количество относится к количеству лекарственного препарата, необходимому для достижения требуемого терапевтического результата."Топически эффективный" относится к материалу, который при нанесении на кожу, ноготь, волосы,коготь или копыто обеспечивает требуемый фармакологический результат локально по месту нанесения или системно в результате трансдермального переноса активного ингредиента в материале."Косметически эффективный" относится к материалу, который при нанесении на кожу, ноготь, волосы, коготь или копыто приводит к требуемому косметическому результату локально по месту нанесения активного ингредиента в материале. Подразумевают, что термин "фармацевтически приемлемые соли" включает соли соединений согласно изобретению, которые получены с помощью относительно нетоксичных кислот или оснований, в зависимости от конкретных заместителей в соединениях, описанных в настоящем документе. Если соединения согласно настоящему изобретению содержат сравнительно кислотные функциональные группировки, соли присоединения основания можно получить путем приведения в контакт нейтральной формы таких соединений с достаточным количеством требуемого основания, неразбавленного или в подходящем инертном растворителе. Примеры фармацевтически приемлемых солей присоединения основания включают соль натрия, калия, кальция, аммония, органического амина или магния, или аналогичную соль. Если соединения согласно настоящему изобретению содержат сравнительно основные функциональные группы, соли присоединения кислоты можно получить путем приведения в контакт нейтральной формы таких соединений с достаточным количеством требуемой кислоты, неразбавленной или в подходящем инертном растворителе. Примеры фармацевтически приемлемых солей присоединения кислоты включают соли, образованные неорганическими кислотами подобно соляной, бромистоводородной, азотной, угольной кислотам, моногидрокарбонату, фосфорной кислоте, моногидрофосфату,дигидрофосфату, серной кислоте, моногидросульфату, йодисто-водородной или фосфористой кислотам и т.п., а также соли, образованные из относительно нетоксичных органических кислот, подобно уксусной,пропионовой, изомасляной, малеиновой, малоновой, бензойной, янтарной, пробковой, фумаровой, молочной, миндальной, фталевой, бензолсульфоновой, п-толилсульфоновой, лимонной, винной, метансульфоновой и т.п. В изобретение также включены соли аминокислот, такие как аргинат и т.п., и соли органических кислот подобно глюкуроновой или галактуроновой кислотам и т.п. (см., например, Berge etal., "Pharmaceutical Salts", Journal of Pharmaceutical Science 66: 1-19 (1977. Некоторые конкретные соединения согласно настоящему изобретению содержат как основные, так и кислотные функциональные группы, что позволяет превращать эти соединения в соли присоединения основания или кислоты. Нейтральные формы соединений предпочтительно восстанавливают путем приведения в контакт соли с основанием или кислотой и выделения исходных соединений обычным способом. Исходная форма соединения отличается от различных солевых форм некоторыми физическими свойствами, такими как растворимость в полярных растворителях. Помимо солевых форм в настоящем изобретении предлагают соединения, которые находятся в форме пролекарства. Пролекарства соединений или комплексов, описанных в настоящем документе, легко подвергаются химическим изменениям в физиологических условиях с образованием соединений согласно настоящему изобретению. Кроме того, пролекарства могут превращаться в соединения согласно настоящему изобретению посредством химических или биохимических способов в окружающей среде exvivo. Некоторые соединения согласно настоящему изобретению могут существовать в несольватированных формах, а также сольватированных формах, в том числе, гидратированных формах. В общем случае,сольватированные формы эквивалентны несольватированным формам и включены в настоящее изобретение. Некоторые соединения согласно настоящему изобретению могут существовать в разнообразных кристаллических или аморфных формах. В общем случае, все физические формы эквивалентны для применений согласно настоящему изобретению и, как подразумевают, находятся в рамках настоящего изобретения. Некоторые соединения согласно настоящему изобретению содержат асимметричные углеродные атомы (оптические центры) или двойные связи; рацематы, диастереоизомеры, геометрические изомеры и отдельные изомеры входят в объем настоящего изобретения. Графические изображения рацемических,амбискалемических и скалемических или энантиомерно чистых соединений согласно настоящему изобретению взяты из (Maehr, J. Chem. Ed. 1985, 62: 114-120). Сплошные и прерывистые клинья применяют для обозначения абсолютной конфигурации стереоцентра, если не указано иное. Если соединения, описанные в настоящем документе, содержат олефиновые двойные связи или другие центры геометрической асимметрии, и если не указано иное, подразумевают, что соединения включают как Е, так и Z геометрические изомеры. Подобным образом, включены все таутомерные формы. Соединения согласно изобретению могут существовать в виде конкретных геометрических или стереоизомерных форм. Изобретение включает все такие соединения, в том числе цис- и транс-изомеры, (-)и (+)-энантиомеры, (R)- и (S)-энантиомеры, диастереоизомеры, (D)-изомеры, (L)-изомеры, их рацемические смеси и другие их смеси, такие как энантиомерно или диастереоизомерно обогащенные смеси, которые находятся в рамках изобретения. В заместителе, таком как алкильная группа, могут присутствовать дополнительные асимметричные углеродные атомы. Подразумевают, что все указанные изомеры, а также их смеси включены в настоящее изобретение. Оптически активные (R)- и (S)-изомеры и d и l изомеры можно получить путем применения хиральных синтонов или хиральных реагентов, или разделить с применением общепринятых способов. Если, например, требуется конкретный энантиомер соединения согласно настоящему изобретению, его можно получить посредством асимметричного синтеза или путем получения производных с применением хирального вспомогательного вещества, при этом образовавшуюся диастереоизомерную смесь разделяют и вспомогательную группу расщепляют с получением чистых требуемых энантиомеров. Альтернативным образом, если молекула содержит основную функциональную группу, такую как аминогруппа,или кислотную функциональную группу, такую как карбоксильная группа, диастереоизомерные соли можно получить, применяя подходящую оптически активную кислоту или основание, с последующим повторным разделением полученных таким образом диастереоизомеров с помощью фракционной кристаллизации или хроматографических методов, известных в данной области техники, и последующим выделением чистых энантиомеров. Кроме того, разделение энантиомеров и диастереоизомеров, что осуществляют посредством хроматографии с применением хиральных неподвижных фаз, возможно в комбинации с химическим получением производных (например, получением карбаматов из аминов). Соединения согласно настоящему изобретению могут также содержать не встречающиеся в природе соотношения атомных изотопов по одному или более атомов, входящих в состав указанных соединений. Например, соединения могут быть мечены радиоактивными изотопами, такими как, например, тритий (3 Н), йод-125 (125I) или углерод-14 (14 С). Подразумевают, что все изотопные модификации соединений согласно настоящему изобретению, радиоактивные или нет, находятся в рамках настоящего изобретения. Термин "фармацевтически приемлемый носитель" или "фармацевтически приемлемая среда" относится к любому составу или носителю, который обеспечивает подходящее введение эффективного количества активного вещества, определенного в настоящем документе, не препятствует эффективной биологической активности активного вещества и является достаточно нетоксичным по отношению к хозяину или пациенту. Типичные носители включают воду, масла, как растительные, так и минеральные, основы для кремов, основы для лосьонов, основы для мазей и т.п. Эти основы включают суспендирующие вещества, загустители, усилители проникновения и т.п. Их состав хорошо известен специалистам в области косметических и топических фармацевтических препаратов. Дополнительную информацию относительно носителей можно найти в монографии (Remington: The Science и Practice of Pharmacy, 21st Ed., Lippincott, WilliamsWilkins (2005, содержание которой включено в настоящее описание посредством ссылки."Фармацевтически приемлемый топический носитель" и эквивалентные термины относятся к фармацевтически приемлемым носителям, описанным выше в настоящем документе, подходящим для топического применения. Неактивная жидкая или кремовая среда, способная суспендировать или растворять активное вещество (вещества) и имеющая свойства, которые делают ее нетоксичной и не вызывающей воспаление при нанесении на кожу, ноготь, волосы, коготь или копыто, является примером фармацевтически приемлемого топического носителя. Подразумевают, что этот термин, в частности, включает материалы для носителей, также одобренные для применения в топических косметических средствах. Термин "фармацевтически приемлемое вспомогательное вещество" относится к консервантам, антиоксидантам, ароматизаторам, эмульгаторам, красителям и наполнителям, известным или применяемым при получении лекарственных препаратов, которые чрезмерно не препятствуют эффективной биологической активности активного вещества и являются достаточно нетоксичными по отношению к хозяину или пациенту. Вспомогательные вещества для топических композиций хорошо известны в данной области техники и могут быть добавлены к топической композиции при условии, что они являются фармацевтически приемлемыми и не оказывают вредного воздействия на эпителиальные клетки или их функцию. Более того, они не должны вызывать ухудшения стабильности композиции. Например, инертные наполнители, вещества, снимающие раздражение, вещества для повышения клейкости, наполнители, ароматизаторы, замутнители, антиоксиданты, гелеобразующие вещества, стабилизаторы, поверхностно-активные вещества, смягчающие вещества, красящие вещества, консерванты, буферные вещества, другие усилители проникновения и другие обычные компоненты композиций для топического или трансдермального введения хорошо известны в данной области техники. Термины "усиление", "усиление проникновения" или "усиление всасывания" относятся к увеличению проницаемости кожи, ногтя, волос, когтя или копыта для лекарственного препарата с целью увеличения скорости, с которой лекарственный препарат проникает через кожу, ноготь, волосы, коготь или копыто. Усиление проникновения, возникающее благодаря применению таких усилителей, можно наблюдать, например, путем измерения скорости диффузии лекарственного препарата через кожу, ноготь,волосы, коготь или копыто животного с помощью диффузионного аппарата. Диффузор описан в статье"усилитель всасывания" или "усилитель проникновения" обозначает вещество или смесь веществ, которое, отдельно или в комбинации, увеличивает проницаемость кожи, ногтя, волос или копыта для лекарственного препарата. Как известно, термин "наполнители" условно означает носители, разбавители и/или среды, применяемые при получении лекарственных композиций, эффективных для заданного применения. Термин "топическое введение" относится к нанесению фармацевтического вещества на наружную поверхность кожи, ногтя, волос, когтя или копыта таким образом, что вещество проходит через наружную поверхность кожи, ногтя, волос, когтя или копыта и поступает в нижележащие ткани. Топическое введение включает нанесение композиции на неповрежденную кожу, ноготь, волосы, коготь или копыто,или на рваную, необработанную или открытую рану кожи, ногтя, волос, когтя или копыта. Топическое введение фармацевтического вещества может привести к ограниченному распределению вещества в кожу и окружающие ткани или, если вещество удаляется с места лечения кровотоком, может обеспечивать системное распределение вещества. Термин "трансдермальное введение" относится к диффузии вещества через барьер кожи, ногтя, волос, когтя или копыта, имеющей место в результате топического введения или другого применения композиции. Роговой слой действует как барьер, и немногие фармацевтические вещества способны проникать через неповрежденную кожу. Напротив, эпидермис и дерма являются проницаемыми для многих растворенных веществ и, следовательно, абсорбция лекарственных препаратов происходит более легко через кожу, ноготь, волосы, коготь или копыто, которые имеют царапины, или у которых иным образом поврежден роговой слой и обнажен эпидермис. Трансдермальное введение включает инъекцию или другое введение через любую чть кожи, ногтя, волос, когтя или копыта или слизистую оболочку и абсорбцию или проникновение через оставшуюся часть. Абсорбцию через нетронутую кожу, ноготь, волосы,коготь или копыто можно увеличить путем размещения активного вещества в подходящей фармацевтически приемлемой среде перед наложением на кожу, ноготь, волосы, коготь или копыто. Пассивное топическое введение может состоять из наложения активного вещества непосредственно на место лечения в комбинации со смягчающими веществами или усилителями проникновения. В настоящем описании подразумевают, что трансдермальное введение включает введение путем обеспечения проникновения через наружный покров, т.е. кожу, ноготь, волосы, коготь или копыто. Термин "микробная инфекция" или "инфекция, вызванная микроорганизмом" относится к любой инфекции ткани хозяина, вызванной возбудителем инфекции, в том числе, но не ограничиваясь ими, вирусами, бактериями, микобактериями, грибами и паразитами (см., например, публикации Harrison's Principles of Internal Medicine, pp. 93-98 (Wilson et al., eds., 12th ed. 1991); Williams et al., J. of Medicinal Chem. 42:1481-1485 (1999), содержание каждой из которых в полном объеме включено в настоящее описание посредством ссылки). В настоящем описании "биологическая среда" относится к биологическим средам in vitro и in vivo. Типичные "биологические среды" in vitro включают, но не ограничиваются ими, культуру клеток, культуру ткани, гомогенаты, плазму и кровь. Применение in vivo, в целом, осуществляют в организме млекопитающих, предпочтительно людей. В настоящем описании термины "ингибирование" и "блокирование" применяются взаимозаменяемо и относятся к частичной или полной блокаде фермента. Согласно типичному варианту реализации изобретения фермент представляет собой редактирующий домен синтетазы тРНК. В настоящем описании "элемент человеческого ногтя" может представлять собой ногтевую пластинку, ногтевое ложе, борозду ногтя, боковой ногтевой валик и их комбинации. Согласно настоящему изобретению бор при некоторых условиях способен образовывать донорноакцепторные связи с кислородом или азотом. Донорно-акцепторные связи обычно более слабые, чем ковалентные связи. В тех случаях, когда бор связан ковалентной связью по меньшей мере с одним кислородом или азотом и в то же самое время образует донорно-акцепторную связь с кислородом или азотом,соответственно, донорно-акцепторная связь и ковалентная связь между бором и двумя идентичными гетероатомами могут взаимопревращаться или находиться в форме резонансного гибрида. Существует потенциальная неопределенность, касающаяся точной природы и степени обобщения электронов в этих случаях. Подразумевают, что образуемые структуры не включают все или часть возможных механизмов связывания между бором и атомом, с которым он связан. Неограничивающие примеры этих связей приведены ниже. Соединения, содержащие бор, связанный с углеродом и тремя гетероатомами (такими как три кислорода, как указано в этом разделе), могут содержать полностью отрицательно заряженный бор или частично отрицательно заряженный бор, вследствие природы донорно-акцепторной связи между бором и одним из атомов кислорода. Благодаря отрицательному заряду, положительно заряженный противоион может соединиться с указанным соединением, образуя, таким образом, соль. Примеры положительно заряженных противоионов включают Н+, Н 3 О+, кальций, натрий, аммоний, калий. Соли этих соединений неявно включены в описании этих соединений. Настоящее изобретение также включает соединения, которые представляют собой поли- или многовалентные соединения, в том числе, например, такие соединения, как димеры, тримеры, тетрамеры и более высокие гомологи соединений, применяемых согласно изобретению, или их реакционноспособные аналоги. Например, димеры (А 1) могут образоваться при следующих условиях: В еще одном примере димеры (А 46) могут образоваться при следующих условиях: Настоящее изобретение также включает соединения, которые являются ангидридами циклических бороновых эфиров и образуются в условиях дегидрирования. Примеры этих ангидридов приведены ниже. Также получают тримеры соединений согласно изобретению. Например, тримеры ациклических бороновых эфиров можно получить следующим образом: Полимеры соединений согласно изобретению также получают путем удаления некоторых защитных групп в сильных кислотах. Например, тримеры ациклических бороновых эфиров можно получить следующим образом: В настоящем изобретении также применяют соединения, которые являются поли- или многовалентными, в том числе, например, такие соединения, как димеры, тримеры, тетрамеры и более высокие гомологи соединений, применяемых в изобретении, или их реакционно-способные аналоги. Поли- и многовалентные соединения можно получить из одного соединения или более чем одного соединения согласно изобретению. Например, димерная конструкция может быть "гомодимерной" или "гетеродимерной". Более того, в рамках объема настоящего изобретения находятся поли- и многовалентные конструкции, в которых соединение согласно изобретению или его реакционно-способный аналог присоединен к олигомерному или полимерному каркасу (например, полилизину, декстрану, гидроксиэтилкрахмалу и т.п.). Предпочтительно, если каркас является полифункциональным (т.е. содержит несколько реакционно-способных мест присоединения соединений, применяемых в изобретении). Более того, каркас может образовывать производные с одним соединением согласно изобретению или более чем одним соединением согласно изобретению. Кроме того, настоящее изобретение включает применение соединений в рамках основной структуры, представленной формулами, приведенными в настоящем описании, в которые введены функциональные группы с целью получения соединений с повышенной водорастворимостью относительно аналогичных соединений, которые не функционализированы подобным образом. Таким образом, любые из заместителей, перечисленных в настоящем описании, можно заменить аналогичными радикалами, которые увеличивают водорастворимость. Например, в рамках изобретения можно заменить гидроксильную группу диолом, или амин - четвертичным амином, гидроксиамином или похожей более водорастворимой группой. Согласно предпочтительному варианту реализации изобретения дополнительную водорастворимость придает замещение по положению, не существенному для активности по отношению к редактирующему домену соединений согласно настоящему изобретению, на группу, которая усиливает водорастворимость исходных соединений. Способы усиления водорастворимости органических соединений известны в данной области техники. Такие способы включают, но не ограничиваются ими, функционализирование органических центров с помощью группы с постоянным зарядом, например, четвертичного аммония, или с помощью группы, которая приобретает заряд при физиологически релевантном рН, например, карбоновой кислоты, амина. Другие способы включают прикрепление к органическому центру гидроксильных или аминосодержащих групп, например, спиртов, полиолов, полиэфиров и т.п. Типичные примеры включают, но не ограничиваются ими, полилизин, полиэтиленимин, поли(этиленгликоль) и поли(пропиленгликоль). Подходящий химизм и стратегии функционализации этих соединений известны в данной области техники (см., например, Dunn, R. L., et al., Eds. POLYMERIC DRUGS AND DRUG DELIVERY SYSTEMS, ACS Symposium Series. Vol. 469, American Chemical Society, Washington, D.C. 1991).II. Введение Согласно типичному варианту реализации в изобретении предлагают соединение, описанное в настоящем документе, или его соль, гидрат или сольват, или их комбинацию. Согласно типичному варианту реализации в изобретении предлагают соединение, описанное в настоящем документе, или соль, гидрат или сольват указанного соединения. Согласно типичному варианту реализации в изобретении предлагают соединение, описанное в настоящем документе, или его соль. Согласно типичному варианту реализации изобретения указанная соль представляет собой фармацевтически приемлемую соль. Согласно типичному варианту реализации в изобретении предлагают соединение, описанное в настоящем документе, или его гидрат. Согласно типичному варианту реализации в изобретении предлагают соединение,описанное в настоящем документе, или его сольват. Согласно типичному варианту реализации в изобретении предлагают соединение, описанное в настоящем документе, или его пролекарство. Согласно типичному варианту реализации в изобретении предлагают соль соединения, описанного в настоящем документе. Согласно типичному варианту реализации в изобретении предлагают фармацевтически приемлемую соль соединения, описанного в настоящем документе. Согласно типичному варианту реализации в изобретении предлагают гидрат соединения, описанного в настоящем документе. Согласно типичному варианту реализации в изобретении предлагают сольват соединения, описанного в настоящем документе. Согласно типичному варианту реализации в изобретении предлагают пролекарство соединения, описанного в настоящем документе. Согласно типичному варианту реализации в изобретении предлагают соединение, изображенное на фиг. 1 или 2. Согласно типичному варианту реализации изобретения алкил представляет собой группу, выбранную из линейного алкила и разветвленного алкила. Согласно еще одному типичному варианту реализации изобретения гетероалкил представляет собой группу, выбранную из линейного гетероалкила и разветвленного гетероалкила.III. b) Композиции, содержащие стереоизомеры В настоящем описании термин "хиральный", "энантиомерно обогащенный" или "диастереоизомерно обогащенный" относится к композиции, имеющей энантиомерный избыток (ее) или диастереоизомерный избыток (de) больше чем примерно 50%, предпочтительно больше чем примерно 70% и более предпочтительно больше чем примерно 90%. В общем случае, особенно предпочтительным является энантиомерный или диастереоизомерный избыток более примерно 90%, например, указанные композиции с больше чем примерно 95%, больше чем примерно 97% и больше чем примерно 99% ее или de. В настоящем описании термины "энантиомерный избыток" и "диастереоизомерный избыток" применяют взаимозаменяемо. Считают, что соединения с одним стереоцентром присутствуют в "энантиомерном избытке", соединения по меньшей мере с двумя стереоцентрами присутствуют в "диастереоизомерном избытке". Термин "энантиомерный избыток" хорошо известен в данной области и определяется как Термин "энантиомерный избыток" связан с более старым термином "оптическая чистота", при этом оба термина являются мерами одного и того же явления. Величина ее будет составлять число от 0 до 100,при этом ноль обозначает рацемически, а 100 - энантиомерно чистый. Композиции, которые в прошлом можно было назвать оптически чистыми на 98%, теперь более точно описываются величиной 96% ее. 90% ее свидетельствует о присутствии 95% одного энантиомера и 5% другого (других) энантиомеров в рассматриваемом веществе. Поэтому согласно одному варианту реализации в изобретении предлагают композицию, содержащую первый стереоизомер и по меньшей мере один дополнительный стереоизомер соединения согласно изобретению. Первый стереоизомер может присутствовать в диастереоизомерном или энантиомерном избытке, составляющем по меньшей мере примерно 80%, или по меньшей мере примерно 90%, или по меньшей мере примерно 92%, или по меньшей мере примерно 95%. Согласно еще одному типичному варианту реализации изобретения первый стереоизомер присутствует в диастереоизомерном или энантиомерном избытке, составляющем по меньшей мере примерно 96%, по меньшей мере примерно 97%, по меньшей мере примерно 98%, по меньшей мере примерно 99% или по меньшей мере примерно 99.5%. Согласно еще одному варианту реализации изобретения соединение, предлагаемое в изобретении, является энантиомерно или диастереоизомерно чистым (диастереоизомерный или энантиомерный избыток составляет примерно 100%). Энантиомерный или диастереоизомерный избыток может определяться относительно только одного другого стереоизомера, или может определяться относительно суммы по меньшей мере двух других стереоизомеров. Согласно типичному варианту реализации изобретения энантиомерный или диастереоизомерный избыток определяют относительно всех других поддающихся обнаружению стереоизомеров, которые присутствуют в смеси. Стереоизомеры поддаются обнаружению,если концентрацию указанного стереоизомера в анализируемой смеси можно определить с применением обычных аналитических способов, таких как хиральная ВЭЖХ. В настоящем описании, и если не указано иное, композиция, которая "по существу, не содержит" соединения, означает, что эта композиция содержит менее чем примерно 20 мас.%, или менее чем примерно 15 мас.%, или менее чем примерно 10 мас.%, или менее чем примерно 5 мас.%, или менее чем примерно 3 мас.%, или менее чем примерно 2 мас.%, или менее чем примерно 1 мас.% соединения. В настоящем описании термин "по существу, не содержит этот (или его) энантиомер" означает, что композиция, содержащая соединение согласно изобретению, содержит значительно большее количество одного энантиомера, чем его оптического антипода. Согласно одному варианту реализации изобретения термин "по существу, не содержит энантиомер" означает, что соединение состоит по меньшей мере из примерно 90 мас.% (S) энантиомера и примерно 10 мас.% или менее (R) стереоизомера. Согласно более предпочтительному варианту реализации изобретения термин "по существу, не содержит энантиомер" означает, что соединение состоит по меньшей мере из примерно 95 мас.% (S) энантиомера и примерно 5 мас.% или менее (R) стереоизомера. Согласно еще более предпочтительному варианту реализации изобретения термин "по существу, не содержит энантиомер" означает, что соединение состоит по меньшей мере из примерно 98 мас.% (S) энантиомера и примерно 2% или менее (R) стереоизомера. Согласно еще более предпочтительному варианту реализации изобретения термин "по существу, не содержит энантиомер" означает, что соединение состоит по меньшей мере из примерно 99 мас.% (S) энантиомера и примерно 1% или менее (R) стереоизомера. Согласно типичному варианту реализации в изобретении предлагают композицию, содержащую а) первый стереоизомер соединения, описанного в настоящем документе, при этом R3 не является Н; b) по меньшей мере один дополнительный стереоизомер первого стереоизомера, при этом первый стереоизомер присутствует в энантиомерном избытке, составляющем по меньшей мере 80% относительно вышеуказанного по меньшей мере одного дополнительного стереоизомера. Согласно типичному варианту реализации изобретения энантиомерный избыток составляет по меньшей мере 92%. Согласно типичному варианту реализации изобретения стереоцентр С первого стереоизомера находится в (S)-конфигурации. Согласно типичному варианту реализации изобретения стереоцентр С первого стереоизомера находится в (S)-конфигурации, и R3 представляет собой -CH2NH2. Согласно типичному варианту реализации в изобретении предлагают композицию, содержащую соединение согласно изобретению, при этом R3 не является Н и стереоцентр С находится в (S)конфигурации, а вышеуказанная композиция, по существу, не содержит энантиомера соединения. Согласно типичному варианту реализации изобретения композиция содержит А 2, А 49 или их комбинации,при этом композиция, по существу, не содержит энантиомер А 2 или А 49. Согласно типичному варианту реализации в изобретении предлагают композицию, содержащую соединение, описанное в настоящем документе, при этом R3 не является Н и стереоцентр С находится в (R) конфигурации.III.с) Комбинации, содержащие дополнительные терапевтические вещества Соединения согласно изобретению можно также применять в комбинации с дополнительными терапевтическими веществами. Таким образом, в дополнительном аспекте в изобретении предлагают комбинацию, содержащую соединение, описанное в настоящем документе, или его фармацевтически приемлемую соль вместе по меньшей мере с одним дополнительным терапевтическим веществом. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой соединение согласно изобретению. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество содержит атом бора. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество не содержит атом бора. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой соединение, описанное в разделе III.с). Если соединение согласно изобретению применяют в комбинации со вторым терапевтическим веществом, обладающим активностью против того же болезненного состояния, доза каждого соединения может отличаться от дозы, в которой соединение применяют по отдельности. Подходящие дозы легко могут быть определены специалистом в данной области техники. Очевидно, что количество соединения согласно изобретению, необходимое для лечения, будет варьироваться в зависимости от природы заболевания, подвергаемого лечению, возраста и состояния пациента и, в конечном счете, будет определено по усмотрению лечащего врача или ветеринара. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой антибиотик. Примеры классов антибиотиков, которые можно применять согласно изобретению, включают аминогликозид, ансамицин, карбацефен, карбапенем, цефалоспорин первого поколения, цефалоспорин второго поколения, цефалоспорин третьего поколения, цефалоспорин четвертого поколения, цефалоспорин пятого поколения, гликопептид,макролид, хинолон, сульфонамид и тетрациклин. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из амикацина, гентамицина, канамицина, неомицина, нетилмицина, стрептомицина, тобрамицина, паромомицина. Соглас- 14020530 но типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из гелданамицина и гербимицина. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой лоракарбеф. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из эртапенема, дорипенема, имипенема, силастатина и меропенема. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из цефадроксила, цефазолина, цефалотина и цефалексина. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из цефаклора, цефамандола, цефокситина, цефпрозила и цефуроксима. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный цефиксима, цефдинира, цефдиторена, цефоперазона, цефотаксима,цефподоксима, цефтазидима, цефтибутена, цефтизоксима и цефтриаксона. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой цефепим. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой цефтобипрол. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из теикопланина и ванкомицина. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из азитромицина, кларитромицина, диритромицина, эритромицина,рокситромицина, тролеандомицина, телитромицина и спектиномицина. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой азтреонам. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из амоксициллина, ампициллина, азлоциллина, карбенициллина,клоксациллина, диклоксациллина, флуклоксациллина, мезлоциллина, метициллина, нафциллина, оксациллина, пенициллина, пиперациллина и тикарциллина. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из бацитрацина, колистина и полимиксина В. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из ципрофлоксацина, эноксацина, гатифлоксацина, левофлоксацина, ломефлоксацина, моксифлоксацина, норфлоксацина, офлоксацина и тровафлоксацина. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из мафенида, пронтисила, сульфацетамида, сульфаметизола, сульфанилимида, сульфазалацина, сульфизоксазола, триметоприма и сульфаметоксазола. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из демеклоциклина, доксициклина, миноциклина, окситетрациклина и тетрациклина. Согласно типичному варианту реализации изобретения дополнительное терапевтическое вещество представляет собой препарат, выбранный из арсфенамина, хлорамфеникола,линкомицина, этамбутола, фосфомицина, фусидовой кислоты, фуразолидона, изониазида, линезолида,метронидазола, мупироцина, нитрофурантоина, платензимицина, пиразинамида, хинупристина, рифампина и тинидазола. Соединения согласно изобретению или их фармацевтические композиции можно также применять в комбинации с другими терапевтическими препаратами, например иммунными терапевтическими препаратами [например, интерфероном, таким как интерферон альфа-2 а (ROFERON-A; Hoffmann-LaRoche), интерферон альфа-2b (INTRON-A; Schering-Plough), интерферон альфакон-1 (INFERGEN; Intermune), пегинтерферон альфа-2b (PEGINTRON; Schering-Plough) или пегинтерферон альфа-2 а (PEGASYS; Hoffmann-La Roche)], терапевтическими вакцинами, противофиброзными препаратами, противовоспалительными препаратами [такими как кортикостероиды или нестероидные противовоспалительные препараты], бронхолитическими средствами [такими как бета-2 адренергические агонисты и ксантины (например, теофиллин)], муколитическими препаратами, противомускариновыми препаратами, антилейкотриеновыми препаратами, ингибиторами неспецифической адгезии клеток [например, антагонистами фактора межклеточной адгезии], антиоксидантами [например, N-ацетилцистеином], агонистами цитокина, антагонистами цитокина, легочными поверхностно-активными средствами и/или противомикробными препаратами. Композиции согласно изобретению можно также применять в комбинации с генной заместительной терапией. Отдельные компоненты таких комбинаций можно вводить одновременно или последовательно в дозированной лекарственной форме. Дозированная лекарственная форма может представлять собой единую дозированную форму или несколько дозированных лекарственных форм. Согласно типичному варианту реализации в изобретении предлагают комбинацию в виде единой дозированной формы. Примером единой дозированной лекарственной формы является капсула, где и соединение согласно изобретению, и дополнительное терапевтическое вещество содержатся в одной и той же капсуле. Согласно типичному варианту реализации в изобретении предлагают комбинацию в виде двух дозированных лекарственных форм. Примером двух дозированных лекарственных форм является первая капсула, которая содержит соединение согласно изобретению, и вторая капсула, которая содержит дополнительное терапевтическое вещество. Таким образом, термин единая "дозированная форма" или "две дозированных формы" или "несколько дозированных форм" относится к предмету, который проглатывает пациент, а не к находящимся внутри компонентам предмета. Специалист в данной области техники легко определит подходящие дозы известных терапевтических препаратов. Комбинации, упоминаемые в настоящем документе, легко можно приготовить для применения в форме фармацевтического композиции. Таким образом, типичный вариант реализации изобретения представляет собой фармацевтическую композицию, содержащую а) соединение согласно изобретению;b) дополнительный терапевтический препарат и с) фармацевтически приемлемый наполнитель. Согласно типичному варианту реализации изобретения фармацевтическая композиция представляет собой дозированную лекарственную форму. Согласно типичному варианту реализации изобретения фармацевтическая композиция представляет собой единую дозированную лекарственную форму. Согласно типичному варианту реализации изобретения фармацевтическая композиция представляет собой две дозированные лекарственные формы. Согласно типичному варианту реализации изобретения фармацевтическая композиция представляет собой две дозированные лекарственные формы, включающие первую дозированную лекарственную форму и вторую дозированную лекарственную форму, при этом в настоящем описании первая дозированная лекарственная форма содержит а) соединение согласно изобретению и b) первый фармацевтически приемлемый наполнитель; а вторая дозированная лекарственная форма содержит с) дополнительный терапевтический препарат и d) второй фармацевтически приемлемый наполнитель.III.е) Составы с кератином Если соединение согласно изобретению накладывают на компонент ногтя человека, соединение абсорбируется или проникает в ноготь. Человеческий ноготь в основном состоит из кератина (т.е. кератина волос или -кератина), а также следовых количеств липидных компонентов. Поэтому в процессе лечения заболевания ногтя или уничтожения или ингибирования роста микроорганизма образуется состав, содержащий элемент человеческого ногтя и соединение согласно изобретению. Согласно еще одному аспекту в изобретении предлагают состав, содержащий (а) соединение согласно изобретению; и (b) кератин-содержащий компонент животного. Согласно типичному варианту реализации изобретения соединение, предлагаемое в изобретении, представляет собой соединение, описанное в настоящем документе, или его фармацевтически приемлемую соль. Согласно типичному варианту реализации изобретения соединение, предлагаемое в изобретении, представляет собой соединение,описанное формулой, приведенной в настоящем документе. Согласно типичному варианту реализации изобретения соединение, предлагаемое в изобретении, представляет собой соединение, описанное в настоящем документе. Согласно типичному варианту реализации изобретения кератин-содержащий компонент животного представляет собой компонент, выбранный из элемента ногтя животного, кожи и волос. Согласно типичному варианту реализации изобретения соединение из части (а) вступает в контакт с компонентом из части (b). Согласно типичному варианту реализации изобретения животное является человеком. Согласно типичному варианту реализации изобретения кератин-содержащий компонент представляет собой ногтевую пластину элемента человеческого ногтя. Согласно типичному варианту реализации изобретения кератин-содержащий компонент представляет собой ногтевое ложе элемента человеческого ногтя. Согласно типичному варианту реализации изобретения кератин-содержащий компонент представляет собой борозду ногтя элемента человеческого ногтя. Согласно типичному варианту реализации изобретения кератин-содержащий компонент представляет собой боковой ногтевой валик элемента человеческого ногтя. Согласно еще одному типичному варианту реализации изобретения элемент человеческого ногтя включает компонент, выбранный из кератина и липида. Согласно еще одному типичному варианту реализации изобретения кератин представляет собой компонент, выбранный из кератина кожи и кератина ногтя/волос. Согласно еще одному типичному варианту реализации изобретения липид представляет собой компонент, выбранный из сульфата холестерина, цереброзида, керамида, свободного стерола, свободных жирных кислот, триглицеридов, стероловых эфиров, восковых эфиров и сквалена. Согласно типичному варианту реализации изобретения соединение присутствует в составе в концентрации, выбранной из примерно 0.001%, примерно 0.01%, примерно 0.05%, примерно 0.1%, примерно 0.5%, примерно 1%, примерно 1.5%, примерно 2%, примерно 2.5%, примерно 3%. Согласно еще одному типичному варианту реализации изобретения кератин присутствует в указанном составе в концентрации, выбранной из примерно 99.99%, примерно 99.95%, примерно 99.90%, примерно 99.5%, примерно 99.0%, примерно 98.5%, примерно 98.0%, примерно 97.5% и примерно 97%. Согласно еще одному типичному варианту реализации соединение согласно изобретению представляет собой соединение, описанное в настоящем документе, или его фармацевтически приемлемую соль. Согласно еще одному типичному варианту реализации изобретения соединение описано в настоящем документе. Согласно еще одному типичному варианту реализации изобретения соединение, которое представляет собой вещество,выбранное из присутствует в указанном составе в концентрации, выбранной из примерно 0.001%, примерно 0.01%, примерно 0.05%, примерно 0.1%, примерно 0.5%, примерно 1% и примерно 1.5%. Согласно еще одному аспекту в изобретении предлагают способ получения этого состава, при этом указанный способ включает нанесение указанного соединения на состав, содержащий кератин, и, тем самым, формирование указанного состава. Согласно типичному варианту реализации изобретения состав, содержащий кератин, представляет собой элемент человеческого ногтя. Согласно типичному варианту реализации изобретения состав, содержащий кератин, представляет собой элемент, выбранный из ногтевой пластины, ногтевого ложа, борозды ногтя, бокового ногтевого валика. Способы получения таких составов описаны в разделе примеров. Следует иметь в виду, что настоящее изобретение включает все комбинации аспектов и/или вариантов реализации изобретения, а также подходящие, пригодные и предпочтительные группы, описанные в настоящем документе.III.f) Получение борсодержащих ингибиторов редактирующего домена Соединения, применяемые в настоящем изобретении, можно получить, применяя коммерчески доступные исходные материалы, известные промежуточные вещества или с помощью синтетических способов, описанных и опубликованных в литературе, включенной в настоящий документ посредством ссылок, такой как публикации патентов США US 20060234981, US 20070155699 и US 20070293457. Нижеследующие общие методы применялись в соответствии с указаниями, приведенными при описании синтеза соединений-примеров, и могут быть применены на основе знаний специалистов в данной области техники при синтезе других подходящих соединений с целью получения дополнительных аналогов. Общий способ 1. Сульфонилирование амино-3 Н-бензо[с][1,2]оксаборол-1-олов Соединение 1 можно превратить в соединение 2 в условиях сульфонилирования. При применении этого общего метода незамещенный фенил или незамещенный пиридинилсульфонилхлорид (1-1.2 экв.) и основание (такое как NMM, K2CO3, или пиридин, 3-4 экв.) последовательно добавляли к раствору амина в MeCN (20 мл/г) при комнатной температуре. После завершения (обычная продолжительность в/н) летучие вещества удаляли в вакууме. К остатку добавляли Н 2 О и устанавливали рН смеси 6, применяя разбавленную HCl. Затем водную фазу экстрагировали органическим растворителем (таким как EtOAc) и объединенные органические фракции высушивали с применением осушителя,такого как Na2SO4 или MgSO4, фильтровали и концентрировали в вакууме. Продукт обычно очищали посредством перекристаллизации из Н 2 О, путем растирания в порошок с CH2Cl2 или EtOAc, или способом испарительной хроматографии. Общий способ 2. Удаление защитных групп бензил-защищенных спиртов или тиолов Соединение 3 можно превратить в соединение 4 в условиях удаления защитных групп. Смесь бензилированного спирта или тиола (1 экв.) и 20% Pd(OH)2 на углероде (50 вес.% во влажном состоянии, соотношение 1:2 по весу подложки к катализатору) в ледяном АсОН (10 мл/г) встряхивали в атмосфере Н 2 (40-50 psi) в аппарате для встряхивания Парра. После завершения реакции (ТСХ) смесь фильтровали через слой целита. Фильтрат концентрировали в вакууме и оставшийся АсОН удаляли посредством совместного испарения с толуолом (3) с получением спирта. Дальнейшую очистку выполняли способом испарительной хроматографии или препаративной ВЭЖХ, при необходимости. Общий способ 3. Алкилирование фенола или тиофенола в условиях реакции МицунобуDIAD (1 экв.) добавляли к раствору фенола или тиофенола (1 экв.) и PPh3 (1 экв.) в безводном ТГФ(200 мл/7 г фенола). Смесь перемешивали при комнатной температуре до завершения реакции (которое определяли способом ТСХ). Затем смесь концентрировали в вакууме. К остатку добавляли Et2O и после этого смесь концентрировали в вакууме. Опять добавляли Et2O и образовавшийся осадок удаляли посредством фильтрации. Фильтрат экстрагировали 2 N NaOH и Н 2 О. Органическую фазу высушивали(Na2SO4) и концентрировали в вакууме. Остаток дополнительно очищали способом испарительной хроматографии. Общий способ 4. Алкилирование фенола или тиофенола алкилбромидами и алкилмезилатами Раствор алкилгалогенида или мезилата (1-1.5 экв.), 2-бром-3-гидроксибензальдегида или 2-бром-3 меркаптобензальдегида (1 экв.) и основания, такого как K2CO3 (1-1.2 экв.) или Cs2CO3 (1.5-2 экв.), в апротонном растворителе, таком как ДМФ, перемешивали при 50-80 С (темп. бани) до завершения реакции(обычно всю ночь). Реакционную смесь охлаждали до комнатной температуры, разбавляли Н 2 О и экстрагировали растворителем, таким как EtOAc. Органические фракции промывали Н 2 О, затем соляным раствором, высушивали с применением осушителя, такого как MgSO4, и концентрировали в вакууме. Дальнейшую очистку осуществляли, при необходимости, способом испарительной хроматографии. Общий способ 5. Борилирование арилгалогенидов и трифлатов Соединение 7 можно превратить в соединение 8 в условиях борилирования. В раствор арилбромида или трифлата в безводном 1,4-диоксане (20 мл/1 г) добавляли B2pin2 (2 экв.) и KOAc (3 экв.) при комнатной температуре, затем дегазировали N2 в течение 10-40 мин. ДобавлялиPdCl2(dppf)CH2Cl2 (4-8 мол.%) и образовавшийся раствор перемешивали при 80-100 С до завершения реакции (2-16 ч). Раствор охлаждали до комнатной температуры и разбавляли EtOAc. Затем органическую фазу промывали Н 2 О, затем соляным раствором, высушивали (Na2SO4), фильтровали и концентрировали в вакууме. Как правило, продукт очищали способом испарительной хроматографии. Общий способ 6. Борилирование фенолов или тиофенолов с помощью их арилтрифлатов Трифторметансульфоновый ангидрид (1.2 экв.) добавляли по каплям к раствору пиридина (1.2 экв.) и фенола в CH2Cl2 (40 мл/8,6 г) при 0 С (темп. бани). Затем реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали до полного потребления исходного материала (которое определяли способом ТСХ). Затем добавляли Et2O и 2 N HCl. Органическую фазу отделяли и промывали насыщ. NaHCO3, затем соляным раствором. Органическую фазу высушивали (Na2SO4) и фильтровали через короткий силикагелевый тампон, промывая Et2O. Фильтрат концентрировали в вакууме и получали требуемый трифлат, который применяли непосредственно в общем методе 5. Общий способ 7. Замыкание кольца замещенных 2-(4,4,5,5-тетраметил[1,3,2]диоксаборолан-2-ил) бензальдегидовNaBH4 (1.5 экв.) добавляли порциями в холодный как лед раствор альдегида в спирте (обычно абсолютном EtOH или безводном МеОН (с=0.1 М). Реакцию оставляли нагреваться до комнатной температуры и контролировали способом ТСХ. Затем смесь подкисляли дорН 3, применяя 1 N NaHSO4 или 2 МHCl, и перемешивали всю ночь. Осадок собирали посредством фильтрации, многократно промывали Н 2 О и высушивали в вакууме. Дальнейшую очистку, при необходимости, выполняли способом испарительной хроматографии. Общий способ 8. Реакция Генри замещенных 2-(4,4,5,5-тетраметил[1,3,2]диоксаборолан-2-ил) бензальдегидовNaOH вод. (1.0 экв.) добавляли к альдегиду (в Н 2 О или ТГФ) при комнатной температуре и реакционную смесь перемешивали при комнатной температуре в течение 5 мин. Добавляли по каплям MeNO2(3 экв.) и смесь перемешивали при комнатной температуре в течение 16 ч. Реакционную смесь подкисляли 2 N HCl и экстрагировали EtOAc. Органическую фракцию промывали Н 2 О, затем соляным раствором,высушивали (MgSO4) и концентрировали в вакууме. Очистку обычно осуществляли способом испарительной хроматографии или осаждением из подкисленной реакционной смеси. Общий способ 9. Реакция Генри замещенных 2-(4,4,5,5-тетраметил[1,3,2]диоксаборолан-2-ил) бензальдегидов с применением катализатора фазового переноса СТАВ или CTACl (5 мол.%) добавляли к смеси MeNO2 и альдегида в вод. NaOH и ТГФ (1 мл/300 мг альдегида) при комнатной температуре. Реакцию контролировали способом ТСХ. После завершения(обычно 1-1.5 ч) рН смеси устанавливали 2-3 с помощью 2 N HCl или 1 М NaHSO4 и затем смесь перемешивали в течение 30 мин. Твердое вещество фильтровали и высушивали с получением требуемого нитросоединения, которое применяли непосредственно на следующей стадии. Если осаждение не происходило, органическое вещество экстрагировали из реакционной смеси посредством EtOAc. Затем органическую фракцию высушивали (MgSO4) и концентрировали в вакууме. Остаток очищали способом испарительной хроматографии. Общий способ 10. Восстановление алкилнитро- и/или алкилнитрильных соединений с получением Соединение 12 можно превратить в соединение 13 в условиях восстановления. Вос 2 О (2 экв.) и NiCl6 Н 2 О (1 экв.) добавляли при перемешивании к раствору алкилнитро- или алкилнитрил в безводном МеОН (3 мл/ммоль) при комнатной температурею Перемешивание продолжали до тех пор, пока большая часть NiCl2 не растворилась в МеОН (обычно 10 мин). Затем реакционную смесь охлаждали до 0 С (темп. бани) и порциями добавляли NaBH4 (6 экв.) в течение 10 мин. Реакция была экзотермической, шипучей и приводила к образованию высокодисперсного черного осадка. Реакционную смесь оставляли нагреваться до комнатной температуры и оставляли перемешиваться всю ночь. Затем смесь концентрировали в вакууме и остаток разбавляли EtOAc. Образовавшуюся суспензию фильтровали через слой целита и фильтрат концентрировали в вакууме. Затем остаток, при необходимости,дополнительно очищали способом испарительной хроматографии. Общий способ 11. Удаление защитных групп Вос-защищенных аминов Соединение 13 можно превратить в соединение 14 в условиях удаления защитных групп. Смесь N-Boc-защищенного амина и 1 М HCl в Et2O или 4 М HCl в диоксане (2 мл/ммоль) перемешивали при комнатной температуре. После полного потребления исходного материала (контролировали способом ТСХ, обычно 3-16 ч) смесь концентрировали в вакууме и неочищенный остаток растирали в порошок с Et2O и фильтровали. При необходимости, конечный продукт очищали способом препаративной ВЭЖХ. Общий способ 12. Восстановление алкилнитро и/или алкилнитрила с применением никеля Ренея(5 мл/1 г) и абсолютного EtOH (20 мл/1 г) встряхивали в атмосфере Н 2 (40-50 psi) в течение 3 ч при комнатной температуре. Образовавшуюся смесь фильтровали через прокладку целита и промывали EtOH. Фильтрат концентрировали в вакууме и получали свободный амин. Общий способ 13. Восстановление замещенных 3-нитрометил-3 Н-бензо[с][1,2]оксаборол-1-олов с применением катализатора Перлмана Соединение 11 можно превратить в соединение 16 в условиях восстановления. Смесь 3-нитрометил-3H-бензо[с][1,2]оксаборол-1-ола (1 экв.) и 20% Pd(OH)2 на углероде (50 вес.% во влажном состоянии, соотношение 1:2 по весу подложки к катализатору) в ледяном АсОН (10 мл/г) встряхивали в атмосфере Н 2 (45-50 psi) в аппарате для встряхивания Парра. После завершения реакции(ТСХ) смесь фильтровали через слой целита. Фильтрат концентрировали в вакууме и получали вязкий материал. Оставшийся АсОН удаляли путем совместного испарения с толуолом (3) и получали амин,обычно в виде рыхлого твердого вещества. Очистку осуществляли способом препаративной ВЭЖХ. Общий способ 14. Синтез замещенного (S)-3-(аминометил)-3-метилбензо[с][1,2]оксаборол-1(3 Н)олгидрохлорида (A7) К суспензии бромида метилтрифенилфосфония (1.2 экв.) в ТГФ при комнатной температуре добавляли порциями KOtBu (1.2 экв.). После перемешивания в течение 5 мин реакционную смесь обрабатывали подходящим образом замещенным 2'-бромацетофеноном (1 экв.). Реакционную смесь перемешивали в течение 3 ч при комнатной температуре, затем гасили насыщенным хлоридом аммония. После этого гашеную смесь экстрагировали 3Et2O и объединенные органические фазы промывали соляным раствором, высушивали над MgSO4 и испаряли под вакуумом. Затем фазы очищали способом силикагелевой хроматографии и получали замещенный 1-бром-2-(проп-1-ен-2-ил)бензол. Затем смесь растворяли в двухфазной смеси воды и tBuOH и охлаждали до 0 С. Добавляли замещенный 1-бром-2-(проп-1-ен-2-ил)бензол и перемешивали гетерогенную смесь при 0 С в течение 18 ч,гасили сульфатом натрия, нагревали до комнатной температуры и перемешивали в течение дополни- 20020530 тельного часа. Затем гашеную смесь экстрагировали 5DCM и объединенные органические фазы высушивали над MgSO4 и испаряли под вакуумом. Очищали способом силикагелевой хроматографии и получали замещенный (S)-2-(2-бромфенил)пропан-1,2-диол. Замещенный (S)-2-(2-бромфенил)пропан-1,2-диол растворяли в пиридине (1 экв.) и охлаждали до 0 С перед добавлением метансульфонилхлорида (1 экв.). Реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 2 ч. Пиридин удаляли под вакуумом и остаток распределяли между DCM и водным NaHCO3. Органическую фазу высушивали над MgSO4 и испаряли под вакуумом с получением неочищенного мезилата. Это вещество объединяли с NaN3 (4.5 экв.), растворяли в ДМФ и нагревали до 80 С в течение 18 ч. Добавляли воду и экстрагировали 3Et2O. Объединенные органические фазы промывали соляным раствором, высушивали над MgSO4 и испаряли под вакуумом. Потом смесь очищали способом силикагелевой хроматографии и получали замещенный (S)-1-азидо-2-(2 бромфенил)пропан-2-ол. Замещенный (S)-1-азидо-2-(2-бромфенил)пропан-2-ол (1 экв.) и триизопропил борат (1.2 экв.) растворяли в 20 эк. толуола. Реакционную смесь кипятили с применением аппарата Дина-Старка с целью удаления толуола и остаток растворяли в 17 эк. сухого ТГФ. Этот раствор охлаждали до -78 С и добавляли по каплям BuLi (25 М в гексане, 1.15 экв.) и перемешивали в течение 30 мин. Реакционную смесь нагревали до комнатной температуры и оставляли перемешиваться в течение 3 ч перед тем, как погасить ее с помощью 6 М HCl, и концентрировали под вакуумом. Смесь экстрагировали 3DCM. Объединенные органические фазы высушивали над MgSO4 и испаряли под вакуумом. Потом смесь очищали способом силикагелевой хроматографии и получали замещенный (S)-3-(азидометил)-3-метилбензо[с][1,2] оксаборол-1(3 Н)-ол. Замещенный (S)-3-(азидометил)-3-метилбензо[с][1,2]оксаборол-1(3 Н)-ол (1 экв.) и трифенил фосфин (2 экв.) растворяли в ацетонитриле. Через 5 мин добавляли концентрированную соляную кислоту (2 экв.) и реакционную смесь перемешивали в течение 24 ч при комнатной температуре перед концентрированием под вакуумом. Остаток помещали в DCM и промывали 32 М HCl. Объединенные водные фазы испаряли до сухости под вакуумом. Образовавшееся твердое вещество промывали EtOH и фильтровали с целью удаления побочных продуктов, концентрировали и кристаллизовали из ацетонитрила и получали гидрохлорид замещенного (S)-3-(аминометил)-3-метилбензо[с][1,2]оксаборол-1(3 Н)-ола в виде твердого белого вещества. Общий способ разделения энантиомеров методом хиральной ВЭЖХ Соединение 17 можно разделить на энантиомеры 18 и 19 с помощью хиральной ВЭЖХ в условиях разделения. Разделение двух энантиомеров осуществляли путем растворения вещества в подходящем растворителе и применения подходящей хиральной колонки и элюирующей системы. Затем собранные разделенные пробы энантиомеров концентрировали и применяли на следующей стадии без дальнейшей очистки. Применяя этот способ, можно достичь диапазона энантиомерных избытков разделенных энантиомеров. Общий способ хирального синтеза 3-аминометилбензоксаборолов Прямой стереоспецифический синтез 3-аминометилбензоксаборолов можно осуществить, исходя из 5- или 6-замещенного 2-бромацетофенона. Бром (1.0 экв.) медленно добавляют к подходящим образом замещенному 2'-бромацетофенону (1.0 экв.) в диэтиловом эфире при комнатной температуре и перемешивают в течение 2 ч. Добавляют воду и реакционную смесь перемешивают до исчезновения окраски. Фазы разделяют и водную фазу экстрагируют диэтиловым эфиром. Объединенные органические фазы промывают соляным раствором, высушивают над MgSO4, фильтруют и концентрируют при пониженном давлении с получением замещенного 2-бром-1-(2-бромфенил)этанона. (R)-(+)-2-Метил-CBSоксазаборолидин [для R-изомера] или (S)-(-)-2-метил-CBS-оксазаборолидин [для S-изомера] (0.11 экв.) добавляют при перемешивании к раствору замещенного 2-бром-1-(2-бромфенил)этанона (1.0 экв.) в ТГФ. Реакционную смесь охлаждают до -10 С, в смесь добавляют ВН 3 ТГФ (1.0 М в ТГФ, 1.20 экв.) в течение 4 ч. Реакционную смесь перемешивают в течение дополнительных 45 мин при -10 С перед добавлением метанола (130 мл). Реакционную смесь концентрируют при пониженном давлении. Образовавшийся остаток обрабатывают способом испарительной колоночной хроматографии с получением замещенного хирального 2-бром-1-(2-бромфенил)этанола. К раствору этого спирта (1.00 экв.) в ДМФ добавляют азид натрия при комнатной температуре. Затем реакционную смесь нагревают до 80 С в течение 24 ч. Добавляют воду (150 мл) и полученный раствор экстрагируют диэтиловым эфиром. Объединенные органические фазы промывают соляным раствором (50 мл), высушивают над MgSO4, фильтруют и концентрируют при пониженном давлении. Остаток обрабатывают способом испарительной колоночной хроматографии с получением замещенного 2-азидо-1-(2-бромфенил)этанола. К раствору этого вещества(1.00 экв.) в толуоле добавляют триизопропилборат (1.50 экв.). К реакционной колбе присоединяют холодильник Дина и Старка и орошают реакционную смесь с целью удаления приблизительно 3/4 объема растворителя. Темную реакционную смесь охлаждают до комнатной температуры, добавляют в нее ТГФ,затем охлаждают до -78 С. К реакционной смеси при -78 С добавляют по каплям н-бутиллитий (2.5 М в гексане, 1.15 экв.) и затем перемешивают в течение 30 мин при этой температуре. Затем реакционную смесь оставляют нагреваться до комнатной температуры, при которой ее перемешивают в течение 3 ч перед тем, как погасить посредством 6 М HCl (30 мл). Реакционную смесь концентрируют при пониженном давлении и образовавшийся остаток обрабатывают способом испарительной колоночной хроматографии с получением замещенного 3-(азидометил)бензо[с][1,2]оксаборол-1(3 Н)-ола. К раствору этого соединения (1.0 экв.) в метаноле добавляют трифенилфосфин (1.0 экв.) и смесь перемешивают в течение 3 ч при комнатной температуре. Добавляют концентрированный HCl и реакционную смесь перемешивают в течение дополнительных 2 ч перед концентрированием до сухости при пониженном давлении. Добавляют дихлорметан и экстрагируют 2 М HCl. Объединенные водные фазы промывают дихлорметаном перед уменьшением объема при пониженном давлении. Затем остаток перекристаллизовывают из горячей воды/ацетонитрила (3 мл воды/50-80 мл ацетонитрила на г соединения) и получают замещенный хиральный (R или S) 3-(аминометил)бензо[с][1,2]оксаборол-1(3 Н)-ол в виде гидрохлоридной соли. Соединения, описанные в настоящем документе, можно превращать в гидраты и сольваты способами, аналогичными описанным в настоящем документе.IV. Биологические исследования ингибиторов редактирующих доменов синтетазы тРНК Принятые в данной области методы генетики и молекулярной биологии применяют для идентификации соединений, которые связывают и/или ингибируют редактирующий домен тРНК-синтетазы. Более того, эти методы применяют, чтобы установить, связывает и/или ингибирует соединение синтетический домен, редактирующий домен или и редактирующий, и синтетический домены. При типовом биологическом исследовании была подтверждена активность репрезентативного соединения против редактирующего домена. Чтобы идентифицировать мишень нового борсодержащего противобактериального соединения (А 1), были выделены генетически модифицированные штаммыE.coli, демонстрирующие устойчивость к соединению (А 1). Исследование генетически модифицированных штаммов показало, что они характеризуются 32-256-кратным увеличением устойчивости к (А 1) по сравнению с диким типом. Кроме того, как было показано, генетически модифицированные штаммы являются чувствительными к различным противобактериальным препаратам с известными видами действия, что предполагает, что клеточная мишень (А 1) отличается от мишени других противобактериальных веществ. Ген leuS, полученный из генетически модифицированных штаммов, был клонирован в плазмиду, и их устойчивость была подтверждена МИК. Редактирующий домен, полученный из этих генетически модифицированных штаммов, образовывал последовательность, и все мутации были локализованы в редактирующем домене этого фермента. В настоящем изобретении также были проведены исследования с целью определения, связывает и/или ингибирует ли конкретное соединение редактирующий домен выбранной тРНК-синтетазы и насколько эффективно, при этом дополнительные исследования легко могут быть проведены специалистами в данной области техники. Коротко говоря, в типовом исследовании объединяют неправильно заряженную тРНК и тРНК-синтетазу, которая способна редактировать неправильно заряженную тРНК. Образовавшуюся смесь приводят в контакт с предполагаемым ингибитором и оценивают степень редакти- 22020530 рующего ингибирования. В еще одном анализе используют генетические методы, чтобы показать, что лекарственный препарат работает посредством редактирующего домена. В этом исследовании сначала исследуют активность соединения против штаммов клеток, избыточно экспрессирующих копии гена тРНК-синтетазы. Действие соединения на сверхэкспрессирующий штамм сравнивают с контрольным штаммом с целью определения, является ли соединение активным против синтетазы. Если минимальная концентрация ингибирования (МИК, MIC) в 2-раза выше в штамме с дополнительными копиями гена синтетазы, чем МИК ингибитора против клетки дикого типа, проводят дополнительный генетический скрининг для определения,обусловлена ли повышенная устойчивость мутациями в редактирующем домене. В этом втором скрининге контрольный штамм провоцируют высокой концентрацией ингибитора. Колонии, пережившие введение провокационной пробы, изолируют и выделяют ДНК из этих клеток. Редактирующий домен усиливают с помощью корректирующего фермента PCR и подходящих затравок. Продукт PCR можно очистить стандартными методами. Последовательную усиленную мутантную ДНК сравнивают с диким типом. Если мутантный ДНК содержит мутации в редактирующем домене, такие результаты означали бы, что соединение связывается с редактирующим доменом и воздействует на редактирующую функцию молекулы посредством этого домена. Исследования, описанные выше, можно применять, по существу, в любой микробной системе, например бактериальной, грибковой, паразитической, вирусной и т.п. В целом, в этих исследованиях тестируемые соединения применяют в диапазоне примерно от 1 пМ до примерно 100 мМ, предпочтительно примерно от 1 пМ до примерно 1 мкМ. Концентрации других соединений лежат в интервале примерно от 1 до примерно 100 нМ, предпочтительно примерно от 1 нМ до примерно 1 мкМ. Воздействие тестируемых соединений на функционирование ферментов можно также измерить на основе любого подходящего физиологического изменения. Когда функциональные последовательности определяют с применением интактных клеток или животных, можно также измерить различные эффекты, такие как выделение медиаторов, выделение гормонов, транскрипционные изменения относительно известных, так и неописанных генетических маркеров, изменения клеточного метаболизма, такие как рост клеток или изменения рН, и изменения внутриклеточных вторичных мессенджеров, таких как Са 2+,или циклических нуклеотидов. Высокопроизводительный скрининг (HTS) также применяют при идентификации перспективных соединений согласно изобретению. Применяя описанные в настоящем документе исследования и другие легкодоступные исследования в данной области, опытные специалисты без труда определят другие соединения и классы соединений,которые способны связывать и/или ингибировать редактирующий домен тРНК-синтетазы. Согласно еще одному аспекту в изобретении предлагают способ идентификации соединения, которое связывается с редактирующим доменом тРНК-синтетазы, включающий а) приведение указанного редактирующего домена в контакт с тестируемым соединением в условиях, подходящих для связывания; и b) обнаружение связывания указанного тестируемого соединения с указанным редактирующим доменом. Согласно типичному варианту реализации изобретения обнаружение связывания указанного соединения включает применение по меньшей мере одного поддающегося обнаружению элемента, изотопа или химической метки, присоединенной к вышеуказанному соединению. Согласно типичному варианту реализации изобретения элемент, изотоп или химическую метку обнаруживают с помощью флуоресцентных, люминесцентных, радиоактивных данных или путем измерения оптической плотности. Согласно типичному варианту реализации изобретения приведение указанного тестируемого соединения в контакт с указанным редактирующим доменом также включает дальнейшее приведение в контакт указанного тестируемого соединения и указанного редактирующего домена с группой, выбранной из АМФи молекулы с конечным аденозином. Согласно типичному варианту реализации изобретения указанную тРНК-синтетазу получают из соединения, выбранного из аланил-тРНК-синтетазы, изолейцил-тРНКсинтетазы, лейцил-тРНК-синтетазы, метионил-тРНК-синтетазы, лизил-тРНК-синтетазы, фенилаланилтРНК-синтетазы, пролил-тРНК-синтетазы, треонил-тРНК-синтетазы и валил-тРНК-синтетазы. Согласно типичному варианту реализации изобретения тРНК-синтетазу получают из лейцил-тРНК-синтетазы. Согласно типичному варианту реализации изобретения тРНК-синтетазы получают из генетически модифицированной синтетазы тРНК, при этом в настоящем документе указанная генетически модифицированная тРНК-синтетаза содержит аминокислотные мутации в редактирующем домене. Согласно еще одному типичному варианту реализации изобретения при этом в настоящем документе указанный редактирующий домен синтетазы тРНК содержит аминокислотную последовательность пептидной последовательности, описанную в настоящем документе. Согласно еще одному аспекту в изобретении предлагают способ идентификации соединения, которое связывается с редактирующим доменом тРНК-синтетазы, при этом указанное исследование включает а) приведение указанного редактирующего домена тРНК-синтетазы в контакт с указанным соединением в условиях, подходящих для связывания указанного соединения с указанным редактирующим доменом тРНК-синтетазы; b) сравнение биологической активности указанного редактирующего домена тРНК- 23020530 синтетазы, приведенного в контакт с указанным соединением, с указанной биологической активностью в случае отсутствия контакта с указанным соединением; и с) идентификацию указанного соединения как связанного с указанным редактирующим доменом тРНК-синтетазы, если указанная биологическая активность указанного редактирующего домена тРНК-синтетазы уменьшается при приведении в контакт с указанным соединением. Согласно типичному варианту реализации изобретения биологическая активность представляет собой гидролиз неродственной аминокислоты. Согласно еще одному типичному варианту реализации изобретения гидролиз указанной неродственной аминокислоты обнаруживают путем применения одной или более меток. Согласно еще одному типичному варианту реализации изобретения метки включают радиометку, флуоресцентный маркер, антитело или их комбинацию. Согласно еще одному типичному варианту реализации изобретения указанную метку можно обнаружить с помощью спектроскопии. Согласно еще одному типичному варианту реализации изобретения редактирующий домен тРНК-синтетазы получают из соединений, выбранных из аланил-тРНК-синтетазы, изолейцил-тРНКсинтетазы, лейцил-тРНК-синтетазы, метионил-тРНК-синтетазы, лизил-тРНК-синтетазы, фенилаланилтРНК-синтетазы, пролил-тРНК-синтетазы, треонил-тРНК-синтетазы и валил-тРНК-синтетазы. Согласно еще одному типичному варианту реализации изобретения указанный редактирующий домен тРНКсинтетазы получают из лейцил-тРНК-синтетазы. Согласно еще одному аспекту в изобретении предлагают способ получения тРНК молекул с помощью неродственных аминокислот, включающий а) создание или выделение мутированной тРНКсинтетазы посредством измененных аминокислотных редактирующих доменов, и b) приведение в контакт тРНК молекулы с указанной мутированной тРНК-синтетазой и неродственной аминокислотой. Согласно еще одному типичному варианту реализации изобретения генетически модифицированная тРНКсинтетаза содержит одну или более аминокислотных мутаций в редактирующем домене. Согласно еще одному типичному варианту реализации изобретения генетически модифицированная тРНК-синтетаза неспособна связаться с соединением согласно изобретению. Согласно еще одному типичному варианту реализации изобретения генетически модифицированная тРНК-синтетаза неспособна связаться с соединением, описанным в настоящем документе, или его фармацевтически приемлемой солью. Согласно еще одному типичному варианту реализации изобретения генетически модифицированная тРНК-синтетаза неспособна связаться с соединением согласно формуле, описанной в настоящем документе, или фармацевтически приемлемой солью указанного соединения. Согласно еще одному типичному варианту реализации соединение согласно изобретению представляет собой соединение, выбранное из Согласно типичному варианту реализации изобретения соединение представляет собой соединение,выбранное из Согласно еще одному типичному варианту реализации изобретения R представляет собой Н. Согласно еще одному аспекту в изобретении предлагают композицию, которая содержит одну или более молекул тРНК, присоединенных к неродственным аминокислотам, при этом в настоящем документе указанные молекулы тРНК синтезируют с применением одной или более мутированных тРНКсинтетаз, выделенных из микроорганизма или клеточной линии, полученной из микроорганизма. Согласно типичному варианту реализации изобретения микроорганизм представляет собой бактерии. Согласно типичному варианту реализации изобретения при этом указанные генетически модифицированные тРНК-синтетазы содержат аминокислотные мутации в редактирующих доменах.V. Аминокислотные и нуклеотидпые последовательности, применяемые в исследованиях тРНК последовательности, которые взаимодействуют с комплексом тРНК-синтетаза-соединение согласно изобретению-АМФ Транспортные РНК (тРНК) переносят мРНК в белок на рибосоме. Каждая транспортная РНК содержит антикодоновый участок, который создает гибрид с мРНК, и аминокислоту, которая может быть присоединена к растущему пептиду. Структурный ген тРНК имеет длину примерно от 72 до 90 нуклео- 24020530E.О. и Tocchini-Valentini, "Transcription by RNA polymerase III", Annu Rev. Biochem 57:873 914 (1988. Согласно одному варианту реализации изобретения соединение, описанное в настоящем документе,приводят в контакт с АМФ и тРНК-синтетазой, и тРНК-синтетазу, в свою очередь, приводят в контакт с молекулой тРНК. Согласно еще одному варианту реализации изобретения соединение, описанное в настоящем документе, приводят в контакт с АМФ из молекулы тРНК и тРНК-синтетазой. Нуклеотидную последовательность молекулы тРНК можно определить путем идентификации участвующей тРНКсинтетазы. Например, для лейцил-тРНК-синтетазы родственная связанная молекула тРНК будет представлять собой тРНК-лейцин (SEQ ID NO 1), а неродственная тРНК, такая как изолейцин, (SEQ ID NO 2) может быть связана при некоторых условиях. Согласно еще одному варианту реализации изобретения молекула тРНК представляет собой лейцил t-PHK. Согласно еще одному варианту реализации изобретения молекулу тРНК изображают как SEQ ID, описанную в настоящем документе. Согласно еще одному варианту реализации изобретения молекулу тРНК изображают как SEQ ID NO 14, SEQ ID NO 15, SEQ IDID NO 23 и SEQ ID NO 24. Согласно этому и другим вариантам реализации изобретения подразумевают,что термин "неродственный" включает как единственную, так и множественную форму слова, т.е. фраза"неродственная аминокислота" включает одну или более аминокислот. В нижеследующих последовательностях s4U=s4U; 4-тиоуридин; Gm=метилгуанин; Y=пиримидин; ms2i6A=ms2i6A; 2-метилтио-N-6 изопентенил аденозин и D=дигидроуридин. Полипептиды, применяемые при биологических исследованиях связывания и ингибирования В некоторых исследованиях связывания и ингибирования более эффективно применять часть молекулы тРНК-синтетазы, а не сам весь белок. В таких исследованиях в эксперименте применяют полипептиды, полученные из тРНК-синтетазы. Согласно одному предпочтительному варианту реализации в биологических исследованиях и экспериментах по изучению связывания применяют полипептидные фрагменты, соответствующие редактирующему домену молекулы тРНК-синтетазы. Такие фрагменты изображают как SEQ ID NO:3, SEQ IDNO:4, SEQ ID NO:5, SEQ ID NO:6 и SEQ ID NO:7. Согласно типичному варианту реализации изобретения фрагменты изображают как SEQ ID NO:5, SEQ ID NO:6 и SEQ ID NO:7. Согласно одному предпочтительному варианту реализации в биологических исследованиях и экспериментах по изучению связывания применяют полипептиды, соответствующие молекуле тРНКсинтетазы. Такие полипептиды изображают как SEQ ID NO:11, SEQ ID NO:12 и SEQ ID NO:13.VI. Способы ингибирования фермента Соединения согласно изобретению можно использовать для ингибирования фермента. Согласно типичному варианту реализации изобретения соединения согласно изобретению проявляют способность ингибировать редактирующий домен тРНК-синтетаз, таких как лейцил-тРНК-синтетаза, микроорганизмов, таких как бактерии, и, следовательно, имеют потенциал для применения в качестве ингибиторов редактирующего домена тРНК-синтетаз у микроорганизмов. Согласно еще одному аспекту изобретения предложен способ связывания и/или ингибирования редактирующего домена тРНК-синтетазы, который включает приведение в контакт тРНК-синтетазы с соединением согласно изобретению, ингибирующим редактирующий домен в условиях, при которых тРНК-синтетаза взаимодействует со своим субстратом с образованием промежуточного соединения аминоациладенилата и предпочтительно с образованием заряженной тРНК. Специалистам в данной области известны такие условия. Согласно типичному варианту реализации изобретения в настоящем документе описано соединение или его соль, гидрат или сольват или их комбинации. Согласно типичному варианту реализации в изобретении предлагают соединение, описанное в настоящем документе, или его соль, гидрат или сольват. Согласно типичному варианту реализации в изобретении предлагают соединение, описанное в настоящем документе, или соль указанного соединения. Согласно типичному варианту реализации в изобретении предлагают соединение, описанное в настоящем документе, или соль указанного соединения. тРНК-синтетазу приводят в контакт с соединением согласно изобретению в количестве, достаточном для достижения поддающегося обнаружению ингибирования тРНК-синтетазы. Этот способ можно осуществить на тРНК-синтетазе, которая содержится в организме или которая находится вне организма. Согласно типичному варианту реализации изобретения способ реализуют на тРНК-синтетазе, которая содержится в микроорганизме или микробной клетке, то есть в животном или на поверхности животного. Согласно типичному варианту реализации изобретения животное является человеком. Этот способ приводит к уменьшению количества заряженной тРНК, произведенной тРНК-синтетазой, которая содержит ингибированный редактирующий домен. Согласно типичному варианту реализации изобретения ингибирование происходит в клетке, такой как клетка микроба. Согласно еще одному типичному варианту реализации изобретения микробная клетка представляет собой бактерии, грибы, дрожжи или паразита. Согласно еще одному типичному варианту реализации изобретения тРНК-синтетаза представляет собой митохондральную тРНК-синтетазу или цитоплазматическую тРНК-синтетазу. Согласно еще одному типичному варианту реализации изобретения тРНК-синтетаза представляет собой группу, выбранную из аланил-тРНК-синтетазы, изолейцил-тРНК-синтетазы, лейцил-тРНК-синтетазы, метионилтРНК-синтетазы, лизил-тРНК-синтетазы, фенилаланил-тРНК-синтетазы, пролил-тРНК-синтетазы, треонил-тРНК-синтетазы и валил-тРНК-синтетазы. Согласно еще одному типичному варианту реализации изобретения тРНК-синтетаза представляет собой лейцил-тРНК-синтетазу. Согласно типичному варианту реализации в изобретении предлагают способ ингибирования кон- 29
МПК / Метки
МПК: A61K 31/69, A01N 55/08
Метки: небольшого, борсодержащие, молекулы, размера
Код ссылки
<a href="https://eas.patents.su/30-20530-borsoderzhashhie-molekuly-nebolshogo-razmera.html" rel="bookmark" title="База патентов Евразийского Союза">Борсодержащие молекулы небольшого размера</a>
Предыдущий патент: Пуриновые соединения
Следующий патент: Комбинированная терапия антикоагулирующего средства с соединением, которое действует как ингибитор фактора ха
Случайный патент: Рельсовое стыковое изолирующее соединение