Карбаматы, полученные из арилалкиламинов
Номер патента: 5520
Опубликовано: 28.04.2005
Авторы: Фернандес Серрат Анна, Микель Боно Игнасио-Хосе, Фернандес Гарсия Андрес, Бальса Лопес Долорс, Фарреронс Гальеми Карлес, Сальседо Рока Каролина, Бонилья Наварро Хосе Игнасио, Лагунас Арналь Кармен, Катена Руис Хуан Лоренсо
Формула / Реферат
1. Соединение формулы (I)
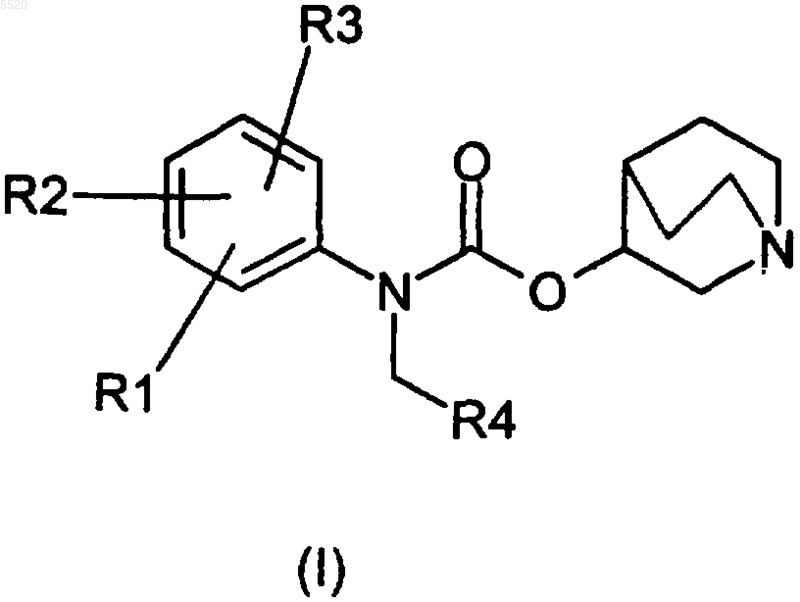
в которой
R1, R2 и R3 представляют собой одинаковые или различные радикалы, связанные с бензольным кольцом в любом из возможных для них положений, и выбраны из группы, включающей H, OH, SH, CN, F, Cl, Br, I, (C1-C4)-алкилтио, (C1-C4)-алкоксил, (C1-C4)-алкоксил, замещенный одним или несколькими F, карбамоиламином, (C1-C4)-алкилом и (C1-C4)-алкилом, замещенным одним или несколькими F или OH; альтернативно, любой из R1 и R2 или R2 и R3 может образовывать бирадикал, выбранный из группы, состоящей из -CH2-CH2-CH2- и -CH2-CH2-CH2-CH2-; и
R4 представляет собой радикал, выбранный из группы, включающей циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, норборненил, бицикло[2,2,1]гептанил, 2-,3-тиенил, 2-,3-фурил, 2-,3-,4-пиридил, 1-,2-нафтил, 1-,2-бензодиоксоланил, 1-,2-бензодиоксанил, фенил и фенил, замещенный одним или несколькими заместителями, выбранными из группы, состоящей из OH, SH, CN, F, Cl, Br, I, карбамоиламина, гидроксикарбонила, (C1-C4)-алкоксикарбонила, (C1-C4)-алкилтио, (C1-C4)-алкила, (C1-C4)-алкоксила, (C1-C4)-алкила, замещенного одним или несколькими F или OH, и (C1-C4)-алкоксила, замещенного одним или несколькими F;
и его фармацевтически приемлемые (C1-C4)-алкиламмониевые соли, образованные хинуклидильным атомом азота, и его N-оксиды, образованные хинуклидильным атомом азота; а также его стереоизомеры, смеси стереоизомеров, фармацевтически приемлемые соли и фармацевтически приемлемые сольваты.
2. Соединение по п.1, в котором R4 представляет собой фенил, или фенил, замещенный одним или несколькими заместителями, независимо выбранными из группы, состоящей из OH, SH, CN, F, Cl, Br, I, карбамоиламина, гидроксикарбонила, (C1-C4)-алкоксикарбонила, (C1-C4)-алкилтио, (C1-C4)-алкила, (C1-C4)-алкоксила, (C1-C4)-алкила, замещенного одним или несколькими F или OH, и (C1-C4)-алкоксила, замещенного одним или несколькими F.
3. Соединение по п.1, в котором R4 выбирают из группы, включающей циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, норборненил, бицикло[2,2,1]гептанил, 2-, 3-тиенил, 2-, 3-фурил, 2-, 3-, 4-пиридил, 1-, 2-нафтил, 1-, 2-бензодиоксоланил и 1-, 2-бензодиоксанил.
4. Соединение по любому из пп.1-3, в котором азот хинуклидинового кольца образует фармацевтически приемлемую (C1-C4)-алкиламмониевую соль.
5. Соединение по любому из пп.1-3, в котором азот хинуклидинового кольца образует N-оксид.
6. Соединение по любому из пп.1-5, в котором стереоцентр, соответствующий 3 положению хинуклидинового кольца, имеет (R)-конфигурацию, формулы

7. Применение соединения, определенного в любом из пп.1-6, для получения лекарственного средства для лечения непроизвольного мочеиспускания (недержания мочи).
8. Применение по п.7, где непроизвольное мочеиспускание вызвано нестабильным мочевым пузырем.
9. Применение соединения по любому из пп.1-6 для получения лекарственного средства для лечения синдрома раздраженного кишечника.
10. Применение соединения по любому из пп.1-6 для получения лекарственного средства для лечения респираторного заболевания.
11. Применение по п.10, где заболевание выбрано из группы, состоящей из хронического обструктивного легочного заболевания, хронического бронхита, астмы, эмфиземы и ринита.
12. Применение соединения, определенного по любому из пп.1-6, для получения лекарственного средства для офтальмологических вмешательств.
Текст
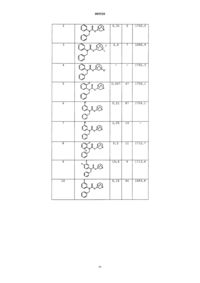
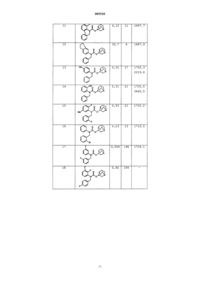
005520 Настоящее изобретение относится к новым соединениям типа хинуклидил N-фенил-Nалкилкарбамата, действующим как антагонисты мускаринового рецептора, к получению подобных соединений и к их применению для предупреждения и лечения заболеваний, связанных с дыхательным трактом, желудочно-кишечным трактом и мочевой системой. Предпосылки к созданию изобретения Известно, что соединения, обладающие антагонистическим эффектом в отношении мускариновых рецепторов, индуцируют бронходилатацию, ингибирование желудочно-кишечной моторики, снижение секреции желудочной кислоты, сухость рта, мидриазу, тахикардию, а также подавление сокращения мочевого пузыря. В период между 1983 и 1993 гг. в знаниях о фармакологии мускаринового рецептора производились постоянные достижения. В течение этого времени клонировали и экспрессировали в общей сумме пять генов человека, кодирующих подтипы мускариновых рецепторов (m1, m2, m3, m4 и m5), которые кодировали пять функциональных рецепторов (M1, М 2, М 3, М 4 и M5). Несмотря на то, что M5 охарактеризован не полностью, его уже считают функциональным рецептором в соответствии с NC-IUPHAR (М.Р. Caulfield et al.; Pharmacol. Rev. 1998, 50, 279-290). Рецептор M1 представляет собой постсинаптический нейронный рецептор, находящийся, главным образом, в мозге и периферических парасимпатических железах. В гладкой сердечной мышце находится основная популяция рецепторов M2. Рецептор М 3 преимущественно находится в тканях внешнесекреторных желез, таких как слюнные железы. Рецептор M4 находится, главным образом, в коре головного мозга, стриатуме и некоторых периферических участках в определенных частях. В гладкой мышце желудочно-кишечного тракта, мочевого пузыря и бронхах рецепторы М 2 и М 3 существуют совместно. Тем не менее, обычно принятая функциональная информация указывает на то, что рецептор М 3 отвечает за сократительный эффект эндогенного нейромедиатора в последних трех тканях. Таким образом, представляется интересным получить селективные антагонисты рецептора М 3 для того, чтобы избежать неблагоприятных эффектов вследствие блокирования других мускариновых рецепторов. В настоящее время среди прочих коммерчески доступными соединениями являются оксибутинин (Nippon Shinyaku) и толтеродин (Pharmacia), причем оба они проявляют пониженную селективность по отношению к рецепторам М 2 и М 3. Однако дарифенацин (Pfizer) и YM-905 (Yamanouchi), оба из которых находятся в стадии разработки, проявляют М 3 антагонистическую активность без какого-либо заметного сродства к рецептору М 2. Далее перечислены некоторые патентные заявки, в которых описаны соединения с карбаминовой структурой в качестве селективных антагонистов рецептора М 3: JP 04/95071-A, WO 95/06635-А, ЕР 747355-А и ЕР 801067-А. Все указанные заявки описывают карбаматы, отличающиеся от описанных в настоящем изобретении, а в последней заявке описаны структурно наиболее близкие к заявленным в настоящем изобретении. Таким образом, понятно, что существует большой интерес в получении новых терапевтических агентов, являющихся селективными антагонистами рецептора М 3. Краткое описание изобретения Один из аспектов настоящего изобретения относится к новым карбаматам общей формулы (I)-1 005520 и их стереоизомеров, смесей стереоизомеров, фармацевтически приемлемых солей и фармацевтически приемлемых сольватов, где R1, R2 и R3 представляют собой радикалы, независимо выбранные из группы, включающей Н, ОН, SH, CN, F, Cl, Вr, I, карбамоиламин, (C1-C4)-алкилтио, (C1-C4)-алкоксил, (C1-C4)алкоксил, замещенный одним или несколькими F, (C1-C4)-алкилом, и (C1-C4)-алкилом, замещенным одним или несколькими F или ОН; альтернативно, любой из R1 и R2, или R2 и R3 может образовывать бирадикал, выбранный из группы, состоящей из -СН 2-СН 2-СН 2- и -СН 2-СН 2-СН 2-СН 2-. В соединениях формулы (I) R4 представляет собой радикал, выбранный из группы, включающей циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, норборненил, бицикло[2,2,1]гептанил, 2-,3-тиенил, 2-,3-фурил, 2-,3-, 4-пиридил, 1-,2-нафтил, 1-,2-бензодиоксоланил, 1-,2 бензодиоксанил, фенил и фенил, замещенный одним или несколькими заместителями, выбранными из группы, состоящей из ОН, SH, CN, F, Cl, Вr, I, карбамоиламина, гидроксикарбонила, (C1-C4)алкоксикарбонила, (C1-C4)-алкилтио, (C1-C4)-алкила, (C1-C4)-алкоксила, (C1-C4)-алкила, замещенного одним или несколькими F или ОН, и (C1-C4)-алкоксила, замещенного одним или несколькими F. В конкретном способе воплощения R4 представляет собой фенил или фенил, замещенный одним или несколькими заместителями, выбранными из группы, включающей ОН, SH, CN, F, Cl, Вr, I, карбамоиламин, гидроксикарбонил, (C1-C4)-алкоксикарбонил, (C1-C4)-алкилтио, (C1-C4)-алкил, (C1-C4)алкоксил, (C1-C4)-алкил, замещенный одним или несколькими F или ОН, и (C1-C4)-алкоксил, замещенный одним или несколькими F. В другом конкретном способе воплощения R4 представляет собой радикал, выбранный из группы, включающей циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, норборненил, бицикло[2,2,1]гептанил, 2-,3-тиенил, 2-,3-фурил, 2-,3-,4-пиридил, 1-,2-нафтил, 1-,2-бензодиоксоланил, 1-,2-бензодиоксанил. Атом азота хинуклидинового кольца может находиться в окисленном состоянии (N-оксид) или в виде фармацевтически приемлемой четвертичной алкиламмониевой соли, и где алкильная цепь, включающая от 1 до 4 атомов углерода, может быть линейной или разветвленной. Особенно предпочтительными являются соединения формулы (I), в которых 3 атом углерода хинуклидинового кольца имеет (R) конфигурацию формулы В случаях, когда соединения формулы (I) имеют асимметрический атом углерода, их рацемические смеси можно разделить на энантиомеры обычными способами, такими как хроматографическое разделение с хиральной неподвижной фазой или путем фракционной кристаллизации их диастереомерных солей. Последние можно получить реакцией с энантиомерно чистыми кислотами. Хиральные соединения формулы (I) можно также получить энантиоселективным синтезом из хиральных предшественников. Настоящее изобретение относится также к физиологически приемлемым солям карбаматов общей структуры (I), в частности, к солям присоединения минеральных кислот, таких как хлористо-водородная,бромисто-водородная, азотная, серная и фосфорная кислоты, а также органических кислот, таких как щавелевая, янтарная, фумаровая, винная и малеиновая кислоты. Настоящее изобретение относится также к N-оксидам карбаматов общей структуры (I) и к четвертичным (C1-C4)-алкиламмониевым солям таких карбаматов с фармацевтически приемлемыми анионами. Соединения общей структуры (I) можно получить двумя общими способами (а именно, А и В),представленными на приведенной ниже схеме. Исходные арилалкиламины (II) коммерчески доступны или могут быть получены известными способами, такими как алкилирование анилинов, восстановительное аминирование или восстановление анилидов. По способу А сначала осуществляют ацилирование арилалкиламина (II) хлорформиатом (например,метилхлорформиатом, этилхлорформиатом, или 4-нитрофенилхлорформиатом) в инертном растворителе(например, диметилформамиде, СН 2 Сl2, 1,2-дихлорэтане, тетрагидрофуране или толуоле) при температуре, изменяющейся в интервале от 0 С до температуры кипения растворителя. В некоторых случаях целесообразно проводить реакцию при использовании соответствующего хлорформиата в качестве растворителя или с использованием такого основания, как третичный амин или карбонат калия. Затем вводят алкоксильную группу реакцией переэтерификации карбаматного промежуточного соединения (III) 3 хинуклидолом с использованием такого основания, как металлический натрий, гидрид натрия или метилат натрия. Данную реакцию можно проводить при температуре, изменяющейся в интервале от 20 С до температуры кипения используемого растворителя. По способу В 3-хинуклидол сначала вводят во взаимодействие с хлорформиатом (например, трихлорметилхлорформиатом) в инертном растворителе (например, диметилформамиде, СН 2 Сl2, 1,2 дихлорэтане) при температуре кипения растворителя для получения соответствующего гидрохлорида хинуклидолхлорформиата. Затем арилалкиламин (II) ацилируют хинуклидолхлорформиатом. Реакцию-2 005520 проводят в инертном растворителе (например, диметилформамиде, СН 2 Сl2, СНСl3, 1,2-дихлорэтане) при температуре, изменяющейся в интервале от 20 С до температуры кипения растворителя. Как показано в прилагаемых тестах на связывание мускаринового рецептора человека, соединения настоящего изобретения являются селективными антагонистами рецептора М 3 по сравнению с рецептором M2. По этой причине их можно использовать для лечения непроизвольного мочеиспускания (в частности, непроизвольного мочеиспускания, вызванного нестабильным мочевым пузырем), синдрома раздраженного кишечника и респираторных расстройств (в частности, хронического обструктивного легочного заболевания, хронического бронхита, астмы, эмфиземы и ринита), а также при офтальмологических вмешательствах. Таким образом, следующим аспектом настоящего изобретения является применение карбаматов формулы (I) для получения лекарственных средств для лечения следующих заболеваний: непроизвольного мочеиспускания, в частности, когда оно вызвано нестабильностью мочевого пузыря; синдрома раздраженного кишечника; респираторных расстройств, в особенности хронического обструктивного легочного заболевания, хронического бронхита, астмы, эмфиземы и ринита. Кроме того, часть данного изобретения составляет также их применение для получения лекарственного средства для офтальмологических вмешательств. Тест на связывание мускариновых рецепторов М 2 и М 3 В следующих тестах показана М 3 антагонистическая активность соединений формулы (I), а также их селективность по отношению к рецетору M2. Представлены результаты, полученные для клонированных мускариновых рецепторов М 2 и М 3 человека и описана использованная методика. Использовали мембраны клеток СНО-К 1, трансфектированных человеческими рецепторами М 2 или М 3 (Receptor Biology). Общая методика эксперимента для обоих рецепторов является следующей: мембраны (15-20 мкг) инкубировали с [3H]-NMS (0,3-0,5 нМ) в течение 60 мин при 25 С, в присутствии или в отсутствие антагонистов. Инкубацию проводили в 96-луночном планшете из полистирола при общем объеме инкубирования 0,2 мл PBS рН 7,4. Неспецифическое связывание определяли в параллельных пробах в присутствии атропина (5 мкМ). Образцы фильтровали через стекловолокно типа GF/C, предварительно инкубированное с PEI 0,3%. Фильтры промывали 3-4 раза 50 мМ Tris-HCl, 0,9% NaCl, pH 7,4 при 4 С и сушили при 50 С в течение 45 мин. Связанную на фильтре радиоактивность количественно определяли при помощи жидкостного сцинтилляционного счетчика. Для расчета константы ингибирования (Ki) кривые замещения анализировали методом нелинейной регрессии (GraphPad Prism). Константу диссоциации (КD) [3H]-NMS для каждого рецептора получали из-3 005520 кривых насыщения, полученных в тех же условиях, что и в опытах, проведенных с антагонистами. Полученные результаты, выраженные как средняя величина для двух независимых опытов, каждый из которых проводили дважды, приведены в таблице ниже. Соотношение М 2/М 3, превышающее 1, указывает на М 3 селективную антагонистическую активность. Изобретение иллюстрировано следующими неограничивающими примерами. Примеры Промежуточное соединение 1. Гидрохлорид (R)-3-хинуклидилхлорформиата. К раствору 8,7 мл (74,8 ммоль) трихлорметилхлорформиата в 240 мл дихлорметана прибавляли по каплям раствор 4,75 г (37,4 ммоль) (R)-3-хинуклидола в 240 мл дихлорметана при 0 С в атмосфере инертного газа и при непрерывном перемешивании. После этого смесь перемешивали при комнатной температуре в течение 24 ч и отгоняли растворитель при пониженном давлении, получая 8,46 г (37,4 ммоль) белого твердого вещества, соответствующего указанному в заголовке соединению, ИК (КВr, см-1): 3380, 2650-2500, 1776. Пример 1. Гидрохлорид 3-хинуклидил N-бензил-N-фенилкарбамата. Способ А. К раствору 5,1 г (20 ммоль) этил N-бензил-N-фенилкарбамата (Dannley, L. J. Org. Chem. 1957, 22,268) и 7,63 г (60 ммоль) 3-хинуклидола в 120 мл толуола прибавляли 800 мг (20 ммоль) гидрида натрия(60% дисперсии в масле) и кипятили смесь в течение 3 ч. В течение этого времени толуол должен был заместить отогнанный объем. Реакционную смесь оставляли охлаждаться и разбавляли толуолом (250 мл), промывали водой и сушили над безводным сульфатом натрия. Затем растворитель отгоняли при пониженном давлении. Полученное масло обрабатывали при комнатной температуре этанолом, насыщенным хлористым водородом, растворитель отгоняли, а полученное твердое вещество растирали в смеси этилацетат/диэтиловый эфир 1:1, получая 230 мг (0,6 ммоль) белого твердого вещества, соответствующего указанному в заголовке соединению (т.пл.: 54 С). Способ В. К суспензии 750 мг (2,58 ммоль) гидрохлорида 3-хинуклидилхлорформиата в 20 мл 1,2-дихлорэтана прибавляли по каплям раствор 395 мг (2,15 ммоль) N-фенилбензиламина в 5 мл 1,2-дихлорэтана. Сразу по окончании прибавления смесь кипятили с обратным холодильником в течение 3 ч. Реакционной смеси давали остыть и отгоняли растворитель при пониженном давлении. Остаток очищали колоночной хроматографией (элюент: хлороформ-метанол 10:1), получая 720 мг (1,95 ммоль) гигроскопичной пены, соответствующей указанному в заголовке соединению. ИК (КВr, см-1): 3400-3200, 2700-2300, 1700 см-1. ЯМР 1H (ТМС, СDСl3, м.д.): 12,30 (1 Н, с), 7,20-6,90 (10 Н, м), 5,10 (1 Н, м), 4,83 (2 Н, м), 3,52 (1 Н, м), 3,18 (4 Н,м), 2,80 (1 Н, м), 2,34 (1 Н, с), 1,92 (2 Н, м), 1,60 (2 Н, м). Пример 2. Гидрохлорид (R)-3-хинуклидил N-бензил-N-фенилкарбамата. Указанное в заголовке соединение получали способом, описанным в примере 1 (способ А), исходя из 390 мг (1,5 ммоль) этил N-бензил-N-фенилкарбамата, 587 мг (4,6 ммоль) (R)-3-хинуклидола и 61 мг(1,5 ммоль) гидрида натрия. Полученный остаток очищали на хроматографической колонке (элюент: хлороформ:метанол 5:1), выделенное масло обрабатывали при комнатной температуре этанолом, насыщенным хлористым водородом и отгоняли растворитель. Затем полученное твердое вещество растирали в диэтиловом эфире и сушили при пониженном давлении при 40 С, получая 310 мг (0,8 ммоль) белого твердого вещества, соответствующего указанному в заголовке гидрохлориду. Т.пл. 50 С. []25D: -26,5(с=1,0, H2O). ИК (КВr, см-1): 2700-2300, 1700. ЯМР 1H (ТМС, СDСl3, м.д.): 12,30 (1 Н, с), 7,20-6,90 (10 Н,м), 5,10 (1 Н, м), 4,83 (2 Н, м), 3,50 (1 Н, м), 3,18 (4 Н, м), 2,80 (1 Н, м), 2,35 (1 Н, с), 1,99 (2 Н, м), 1,61 (2 Н, м). Пример 3. Йодид (R)-3-(N-бензил-N-фенидкарбамоилокси)-1-метилхинуклидиния. Раствор 300 мг (0,89 ммоль) N-бензил-N-фенилкарбамата (R)-3-хинуклидила (пример 2) и 60 мкл йодистого метила (0,98 ммоль) в 9 мл ацетона кипятили с обратным холодильником в течение 2 ч. Реакционной смеси давали остыть до комнатной температуры и отгоняли растворитель при пониженном давлении. Полученное твердое вещество растирали в диэтиловом эфире и сушили в вакууме при 40 С, получая 480 мг (0,89 ммоль) гигроскопичного белого твердого вещества, соответствующего указанному в заголовке соединению. ИК (пленка, см-1): 1690. Пример 4. N-Oксид N-фенил-N-бензил-3-хинуклидилкарбамата. Суспензию 300 мг (0,9 ммоль) N-фенил-N-бензил-3-хинуклидилкарбамата в 20 мл дихлорметана и 95 мг(1,1 ммоль) гидрокарбоната натрия охлаждали до 0 С, а затем прибавляли 567 мг (1,1 ммоль) м-хлорпербензойной кислоты (70%). Оставляли реакционную смесь для взаимодействия при комнатной температуре при перемешивании в течение 1 ч. После этого органический слой промывали 5%-ным раствором тиосульфата натрия, сушили над безводным сульфатом натрия, фильтровали и отгоняли растворитель при пониженном давлении. Полученный остаток очищали на хроматографической колонке, используя смесь хлороформ:метанол 5:1 в качестве элюента. Получали 289 мг (0,82 ммоль) бесцветного масла, соответствующего указанному в заголовке соединению. ИК (пленка, см-1): 1702. В следующую таблицу включены другие примеры соединений, которые получены способами, аналогичными описанным в предшествующих примерах, что понятно любому специалисту в данной области. Значения антагонистической активности в отношении М 3 человека (выраженные в виде константы-4 005520 сродства к связыванию, K1 (нМ приведены в колонке М 3. Соотношение между сродством к рецепторам М 2 и М 3 приведено в колонке М 2/М 3, причем величина, превышающая 1, указывает на селективность в отношении к рецептору М 3.R1, R2 и R3 представляют собой одинаковые или различные радикалы, связанные с бензольным кольцом в любом из возможных для них положений, и выбраны из группы, включающей Н, ОН, SH, CN,F, Cl, Br, I, (C1-C4)-алкилтио, (C1-C4)-алкоксил, (C1-C4)-алкоксил, замещенный одним или несколькими F,карбамоиламином, (C1-C4)-алкилом и (C1-C4)-алкилом, замещенным одним или несколькими F или ОН; альтернативно, любой из R1 и R2 или R2 и R3 может образовывать бирадикал, выбранный из группы,состоящей из -СН 2-СН 2-СН 2- и -СН 2-СН 2-СН 2-СН 2-; иR4 представляет собой радикал, выбранный из группы, включающей циклопропил, циклобутил,циклопентил, циклогексил, циклогексенил, норборненил, бицикло[2,2,1]гептанил, 2-,3-тиенил, 2-,3 фурил, 2-,3-,4-пиридил, 1-,2-нафтил, 1-,2-бензодиоксоланил, 1-,2-бензодиоксанил, фенил и фенил, замещенный одним или несколькими заместителями, выбранными из группы, состоящей из ОН, SH, CN, F,Cl, Br, I, карбамоиламина, гидроксикарбонила, (C1-C4)-алкоксикарбонила, (C1-C4)-алкилтио, (C1-C4)алкила, (C1-C4)-алкоксила, (C1-C4)-алкила, замещенного одним или несколькими F или ОН, и (C1-C4)алкоксила, замещенного одним или несколькими F; и его фармацевтически приемлемые (C1-C4)-алкиламмониевые соли, образованные хинуклидильным атомом азота, и его N-оксиды, образованные хинуклидильным атомом азота; а также его стереоизомеры,смеси стереоизомеров, фармацевтически приемлемые соли и фармацевтически приемлемые сольваты.-13 005520 2. Соединение по п.1, в котором R4 представляет собой фенил, или фенил, замещенный одним или несколькими заместителями, независимо выбранными из группы, состоящей из ОН, SH, CN, F, Сl, Вr, I,карбамоиламина, гидроксикарбонила, (C1-C4)-алкоксикарбонила, (C1-C4)-алкилтио, (C1-C4)-алкила, (C1C4)-алкоксила, (C1-C4)-алкила, замещенного одним или несколькими F или ОН, и (C1-C4)-алкоксила, замещенного одним или несколькими F. 3. Соединение по п.1, в котором R4 выбирают из группы, включающей циклопропил, циклобутил,циклопентил, циклогексил, циклогексенил, норборненил, бицикло[2,2,1]гептанил, 2-, 3-тиенил, 2-, 3 фурил, 2-, 3-, 4-пиридил, 1-, 2-нафтил, 1-, 2-бензодиоксоланил и 1-, 2-бензодиоксанил. 4. Соединение по любому из пп.1-3, в котором азот хинуклидинового кольца образует фармацевтически приемлемую (C1-C4)-алкиламмониевую соль. 5. Соединение по любому из пп.1-3, в котором азот хинуклидинового кольца образует N-оксид. 6. Соединение по любому из пп.1-5, в котором стереоцентр, соответствующий 3 положению хинуклидинового кольца, имеет (R)-конфигурацию, формулы 7. Применение соединения, определенного в любом из пп.1-6, для получения лекарственного средства для лечения непроизвольного мочеиспускания (недержания мочи). 8. Применение по п.7, где непроизвольное мочеиспускание вызвано нестабильным мочевым пузырем. 9. Применение соединения по любому из пп.1-6 для получения лекарственного средства для лечения синдрома раздраженного кишечника. 10. Применение соединения по любому из пп.1-6 для получения лекарственного средства для лечения респираторного заболевания. 11. Применение по п.10, где заболевание выбрано из группы, состоящей из хронического обструктивного легочного заболевания, хронического бронхита, астмы, эмфиземы и ринита. 12. Применение соединения, определенного по любому из пп.1-6, для получения лекарственного средства для офтальмологических вмешательств.
МПК / Метки
МПК: C07D 453/02, A61K 31/439
Метки: карбаматы, полученные, арилалкиламинов
Код ссылки
<a href="https://eas.patents.su/15-5520-karbamaty-poluchennye-iz-arilalkilaminov.html" rel="bookmark" title="База патентов Евразийского Союза">Карбаматы, полученные из арилалкиламинов</a>
Предыдущий патент: Производные дифениловых эфиров, используемых в терапии
Следующий патент: Концентрированный, не образующий пены раствор четвертичных аммониевых соединений и способы его применения
Случайный патент: Носитель кристаллов ис