Способ получения титана
Формула / Реферат
1. Способ получения порошка металлического титана, содержащего поверхностный слой из AlF3, включающий стадию восстановления TiF3 алюминием с получением продукта восстановления, содержащего порошок металлического титана, покрытый AlF3.
2. Способ по п.1, отличающийся тем, что продукт восстановления нагревают до тех пор, пока содержание AlF3 на поверхности порошка металлического титана не станет равным величине между 0,005 и 40% от массы материала.
3. Способ по п.1, отличающийся тем, что содержание AlF3на поверхности порошка металлического титана равно величине между 0,05 и 10% от массы материала.
4. Способ по п.1, отличающийся тем, что содержание AlF3на поверхности порошка металлического титана составляет от 0,10 до 5% от массы материала.
5. Дезактивированный порошок титана, содержащий поверхностный слой AlF3, содержание которого составляет от 0,005 до 10% от массы материала.
6. Дезактивированный порошок титана по п.5, отличающийся тем, что содержание AlF3составляет от 0,05 до 10% от массы материала.
7. Дезактивированный порошок титана по п.5, отличающийся тем, что содержание AlF3составляет от 0,10 до 5% от массы материала.
8. Порошок титана, характеризующийся тем, что его рентгенограмма дифракционных полос сходна с рентгенограммой дифракционных полос AlTi3.
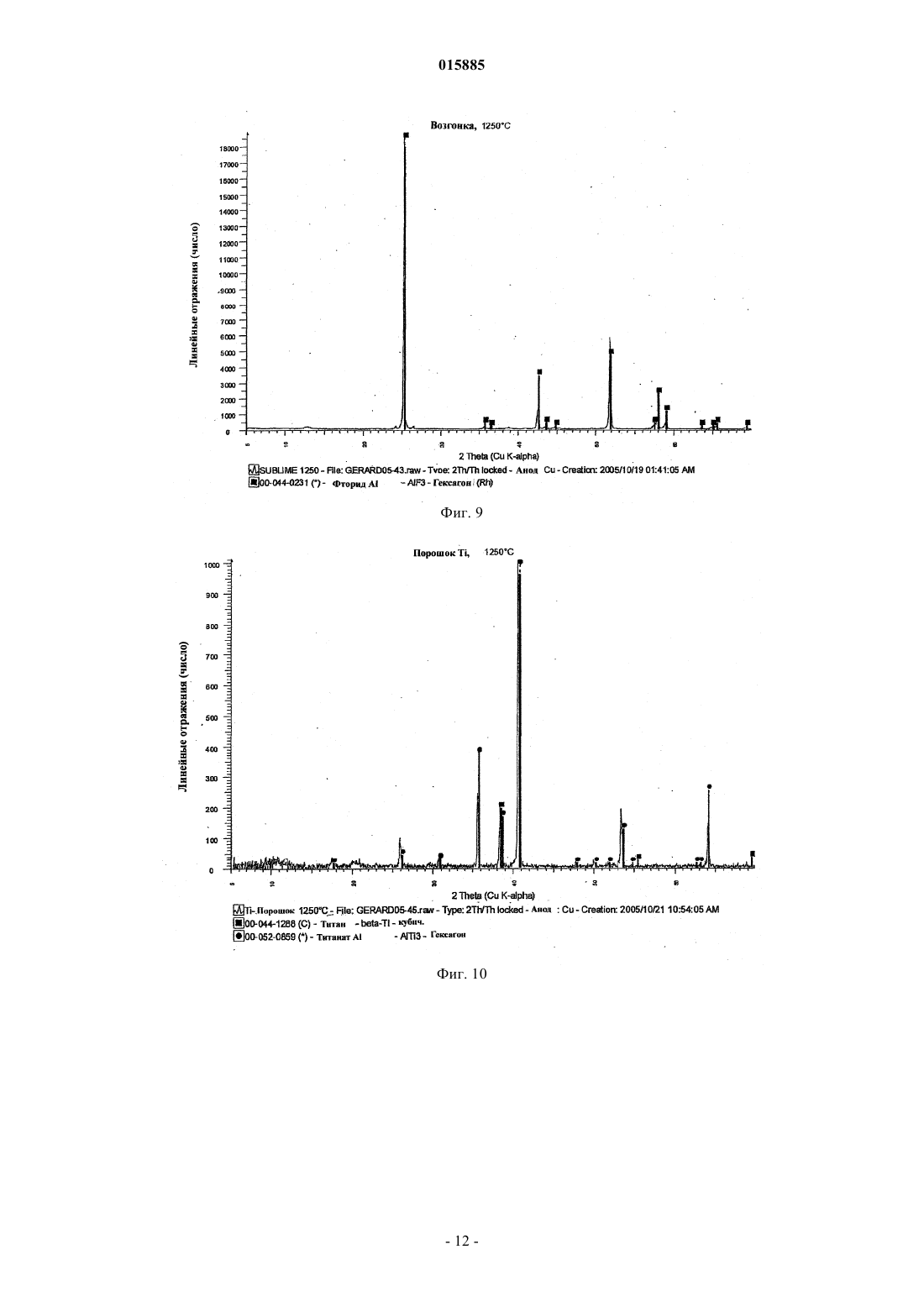
9. Порошок титана, характеризующийся тем, что его рентгенограмма дифракционных полос практически имеет вид, показанный на фиг. 10.
10. Способ получения порошка металлического титана, включающий стадии
восстановления TiF3 алюминием с получением продукта восстановления, содержащего порошок металлического титана и AlF3, и
нагрева этого продукта восстановления для возгонки AlF3для получения порошка титана, по существу, не содержащего алюминия в виде металла или сплава.
Текст
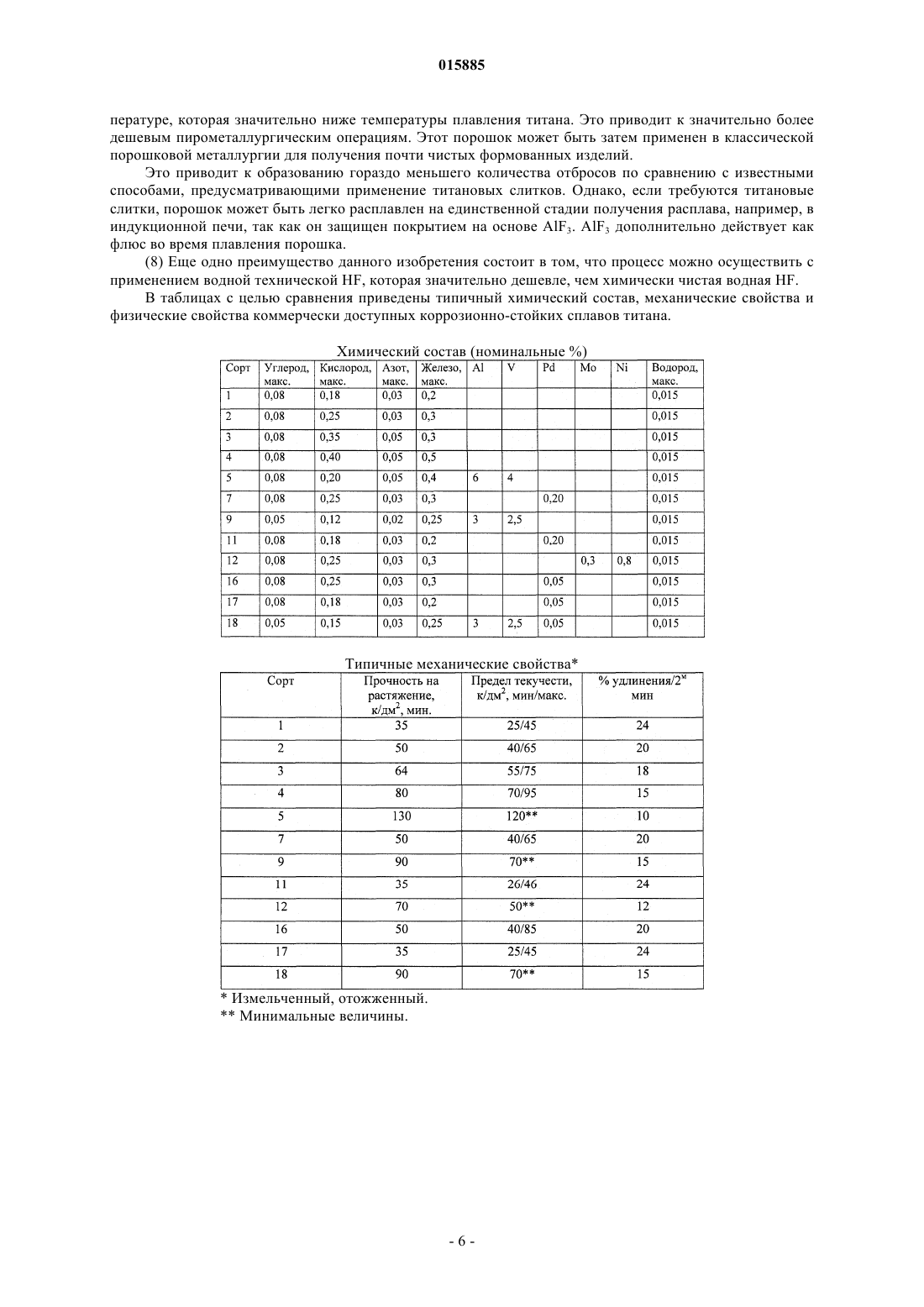
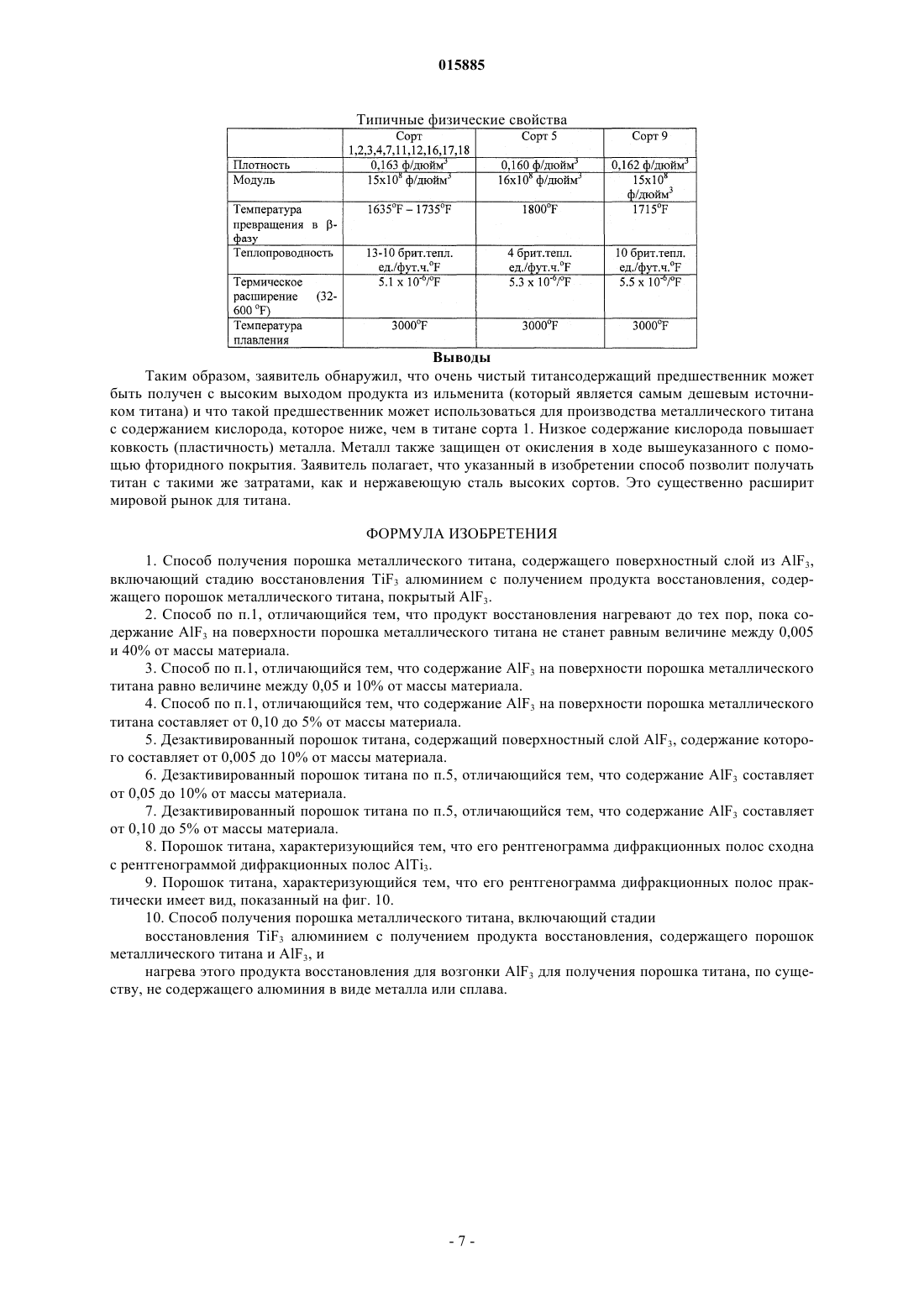
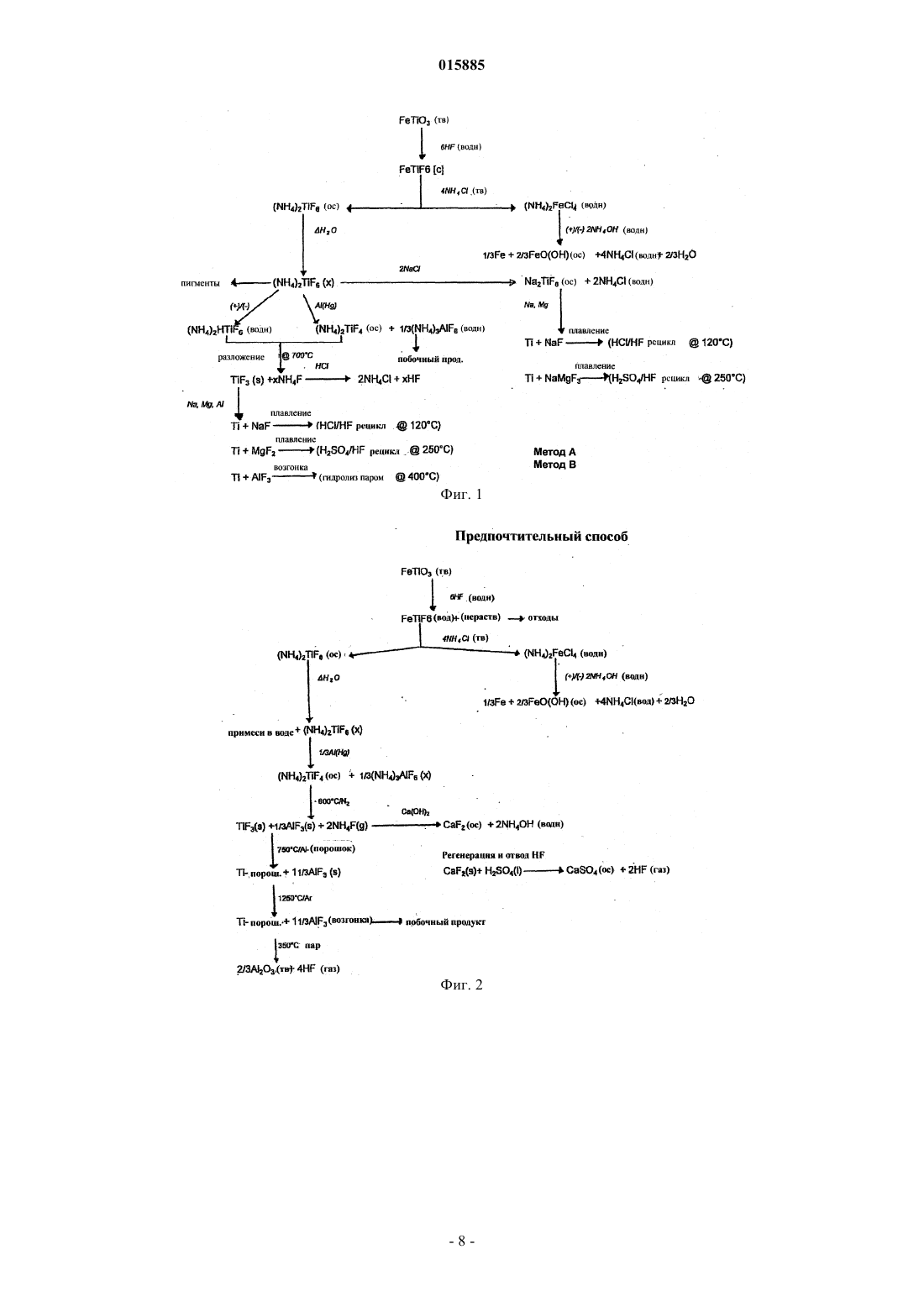
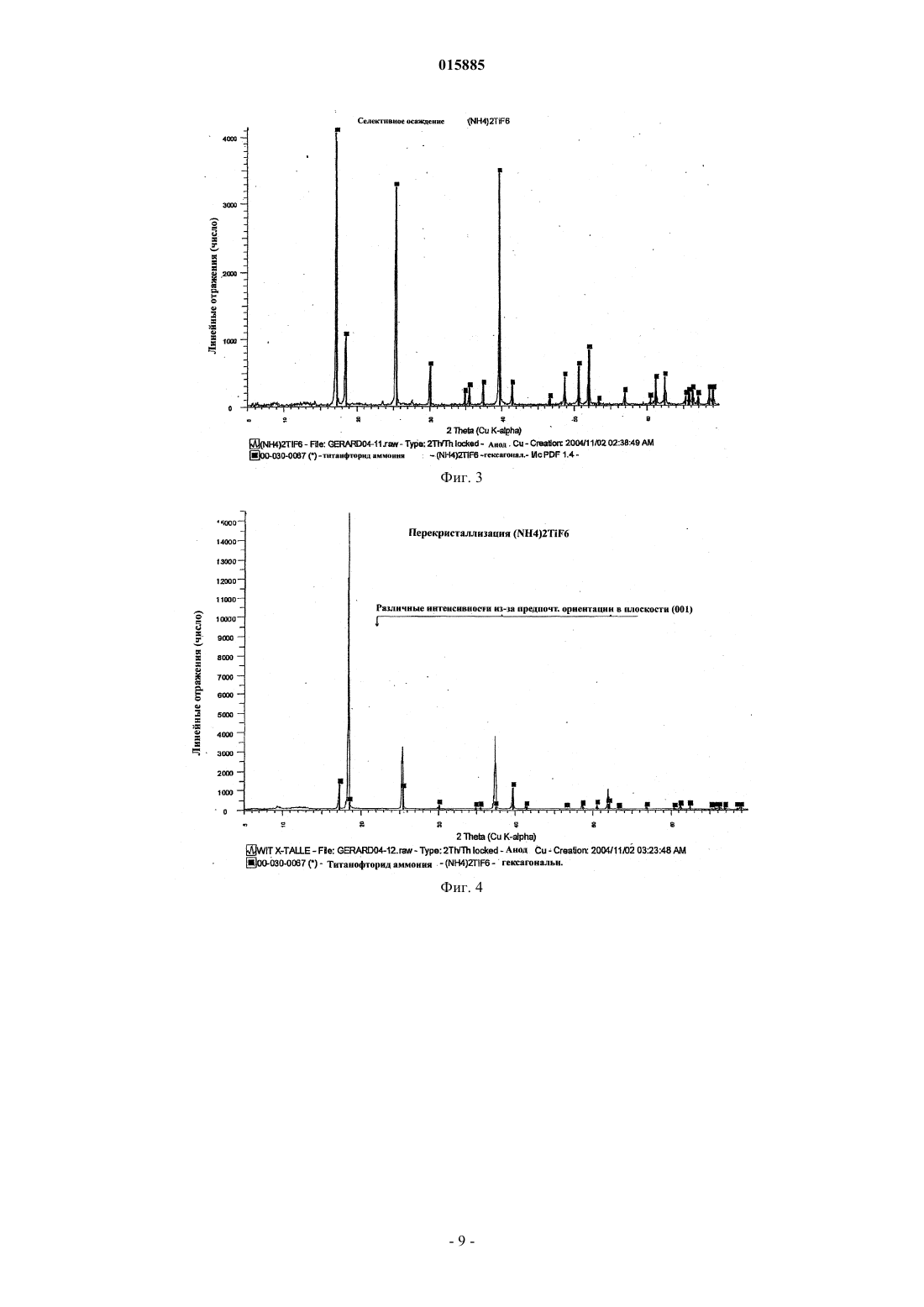
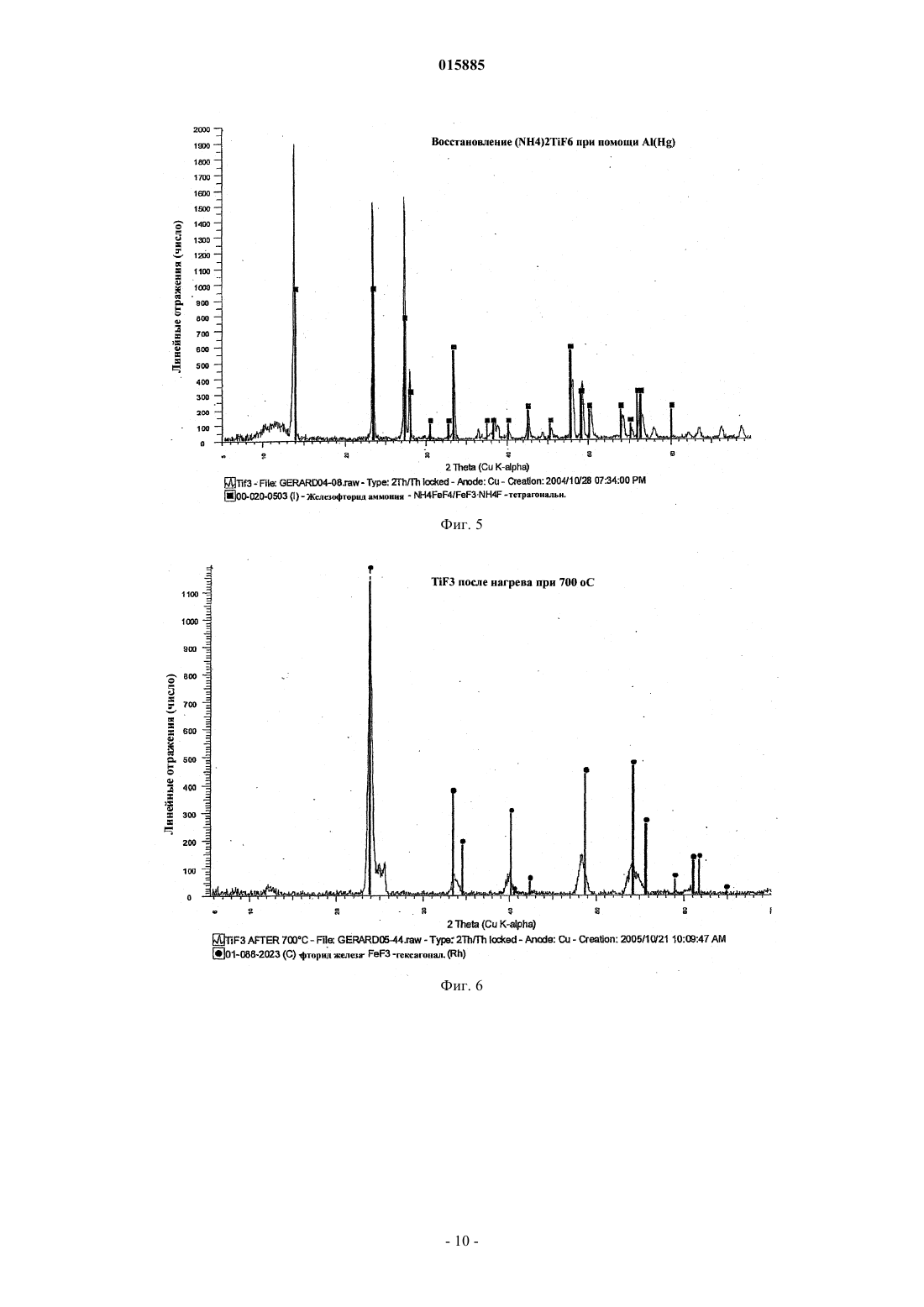
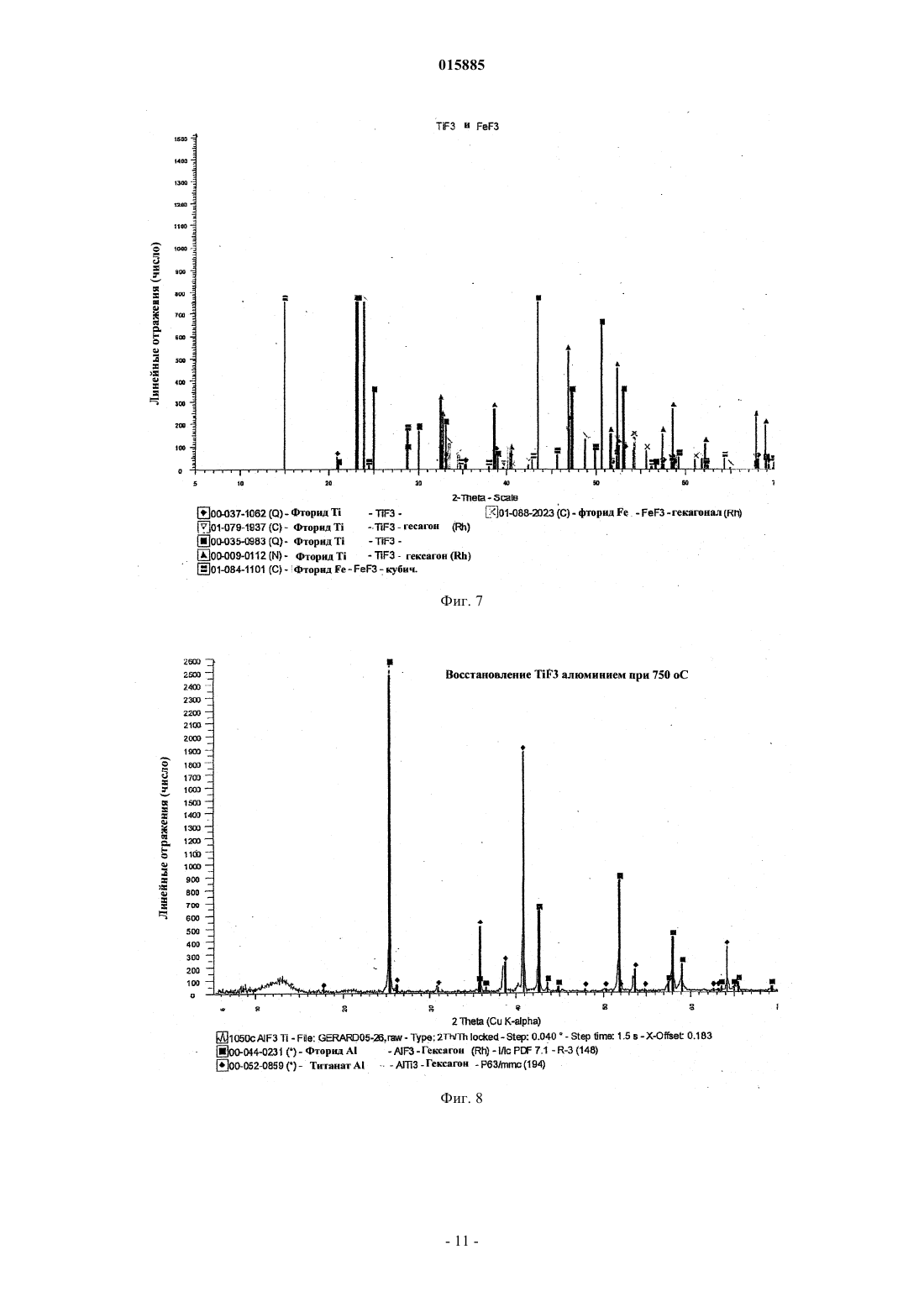
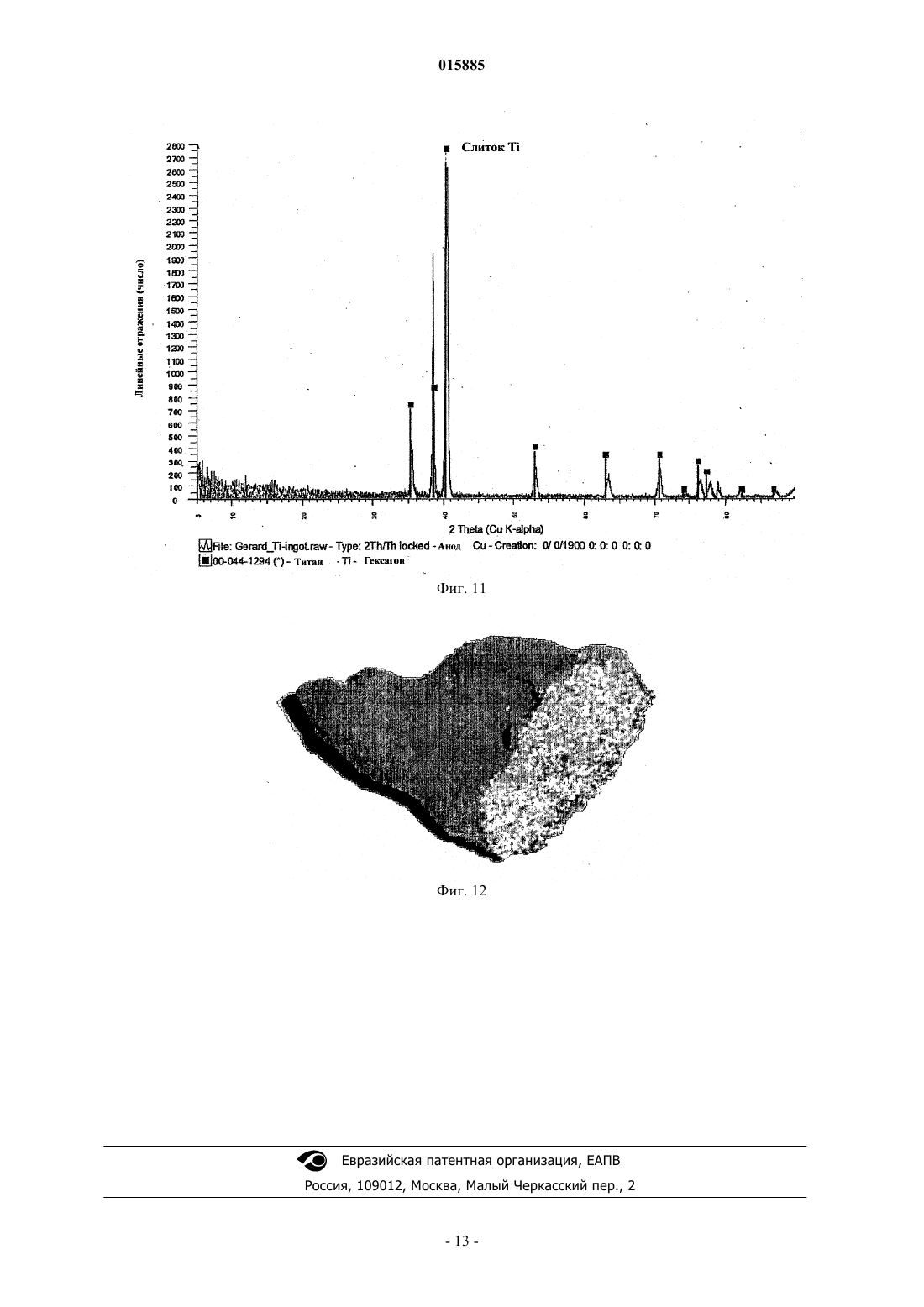
ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ЕВРАЗИЙСКОМУ ПАТЕНТУ Дата публикации и выдачи патента Изобретение относится к способу получения порошка металлического титана, включающему стадию восстановления TiF3 алюминием с получением продукта восстановления, содержащего порошок металлического титана и AlF3. Дезактивированный порошок титана содержит поверхностный слой AlF3, содержание AlF3 в котором составляет от 0,005 до 10% от массы материала. 015885 Данное изобретение относится к способам получения металлического титана, сплавов на основе титана и соединений титана. В промышленности титан обычно получают из тетрахлорида титана (TiCl4) по способам Хантера(Hunter) или Кроля (Kroll). Эти способы включают стадию восстановления натрия или магния. Титан получали также путем восстановления гексафтортитаната калия (K2TiF6) натрием, путем электролитического восстановления двуокиси титана (TiO2) и путем восстановления TiO2 магнием или кальцием. Титан также может быть получен из различных титансодержащих предшественников с применением различных восстанавливающих агентов. Плотность металлического титана составляет около 45% от плотности стали, однако титан является таким же прочным, как сталь, и имеет превосходную химическую стойкость. Титан является также девятым по распространенности в земной коре элементом, но, несмотря на его распространенность и превосходные свойства, продажа титана составляет только 1% от продажи алюминия и только 0,1% от продажи нержавеющей стали. Причиной этого является его стоимость. Только ограниченное число областей, таких как военная отрасль, аэрокосмическая отрасль и медицина, могут позволить себе применять титан. Основные причины такой высокой стоимости металлического титана состоят в том, что предшественники, применяемые в производстве титана, являются дорогими и во время плавления, литья и ковки благодаря окислению происходят большие потери. Данное изобретение предусматривает эффективный и недорогой способ получения титана.TiF3 может быть восстановлен с получением титана путем восстановления восстанавливающим агентом, выбранным из натрия, магния и алюминия. Согласно изобретению предусмотрен способ получения порошка металлического титана, причем этот способ включает стадию восстановления TiF3 алюминием с целью получения продукта восстановления, представляющего собой порошок металлического титана и AlF3. Этот способ может также включать стадию нагревания продукта восстановления до такой температуры и в течение такого промежутка времени, которые достаточны для сублимации большей части AlF3 и в то же время для удержания достаточного количества AlF3 на поверхности для снижения реакционноспособности порошка металлического титана. Этот способ может включать нагревание продукта восстановления до тех пор, пока количество AlF3 на поверхности порошка металлического титана не составит от примерно 0,005 до 40% от массы материала, предпочтительно от примерно 0,05 до 10% и более, более предпочтительно от примерно 0,1 до 5,0%. Остаточное количество AlF3 вызывает образование инертного слоя, который предпочтительно является монослоем достаточной толщины для того, чтобы образоваться на поверхности порошка титана. Это существенно повышает температуру, при которой спонтанное сгорание порошка титана происходит на воздухе, от величины, составляющей примерно 250 С до температуры выше 600 С. Соответственно этот порошок безопаснее применять и перевозить, чем известные порошки титана. Изобретение охватывает также дезактивированный порошок титана, содержащий поверхностный слой AlF3, при этом количество AlF3 составляет величину, находящуюся между примерно 0,05 и 10% от массы материала и предпочтительно между примерно 0,1 и 5% AlF3. Данное изобретение относится также к способу получения порошка металлического титана, при этом способ включает стадии восстановления TiF3 алюминием с получением продукта восстановления, содержащего порошок металлического титана и AlF3, и нагревания продукта восстановления для сублимации AlF3 с целью получения порошка металлического титана, практически не содержащего алюминия в виде металла или сплава. Обсуждение(Na, K)2TiF6, и происходит при температуре выше 700 С.NaF или MgF2 может быть выплавлен из титана, в то время как AlF3 возгоняется при температуре 1300 С. Далее изобретение описано в примере, показано на фигурах и в таблицах, при этом фиг. 1 представляет общую диаграмму способа по изобретению; фиг. 2 отражает диаграмму предпочтительного способа; на фиг. 3 представлена рентгенограмма дифракционных полос селективно осажденного (NH4)2TiF6; на фиг. 4 представлена рентгенограмма дифракционных полос (NH4)2TiF6, показанного на фиг. 3,после перекристаллизации; на фиг. 5 показана рентгенограмма дифракционных полос NH4TiF4, полученного восстановлением(NH4)2TiF6 при помощи Al(Hg); фиг. 6 отражает рентгенограмму дифракционных полос TiF3, полученного путем разложенияNH4TiF4, показанного на фиг. 5; на фиг. 7 показаны наложенные друг на друга рентгенограммы дифракционных полос стандартных-1 015885 образцов TiF3 и FeF3; на фиг. 8 представлена рентгенограмма дифракционных полос продукта восстановления TiF3 при помощи алюминия при 750 С; на фиг. 9 показана рентгенограмма дифракционных полос AlF3, сублимированного при температуре 1250 С; на фиг. 10 показана рентгенограмма дифракционных полос продукта, показанного на фиг. 8, после сублимации AlF3; фиг. 11 отражает рентгенограмму дифракционных полос металлического титана, полученного из порошка, показанного на фиг. 10; на фиг. 12 показан порошок титана по фиг. 10 после мягкого спекания при температуре 1250 С. В таблицах показаны химический состав, механические свойства и физические свойства различных сортов титана. Как показано на фиг. 1, способ по изобретению можно разделить на пять стадий. Эти стадии представляют собой выварку ильменита, селективное осаждение предшественника титана, полученного на стадии выварки, восстановление предшественника, плавление восстановленного титанового продукта с получением слитков и возвращение в цикл реагентов, использованных при проведении процесса. Пример. Получение титана из ильменита методом восстановления (NH4)2TiF6 при помощи Al(Hg). Стадия 1. Выварка ильменита в разбавленной HF. Исходное сырье. В качестве исходного сырья на стадии выварки применяли концентрат ильменита. Материал содержал примерно 89,5% ильменита, 6% гематита, 2,5% кварца и 2% окислов других металлов. Размер частиц был однородным и примерно 98% сырья характеризовались размером частиц между +45 мкм и-106 мкм. Исходный материал имел следующий химический состав: Стехиометрия. Количество HF, необходимое для 500 г ильменита. Используемый ильменит состоял из FeTiO3 (89,5%), Fe2O3 (6,0%), SiO2 (2,5%) и других компонентов (2%). Это соответствовало FeTiO3 (447,5 г; 2,95 моль), Fe2O3 (30 г; 0,19 моль) и SiO2 (12,5 г; 0,21 моль) в 500 г. FeTiO3, FeO3 и SiO2, каждая, требуют 6 моль HF на моль для конверсии соответственно в FeTiFe, FeF3 и H2SiF6. Следовательно, общее количество требующейся HF составляло(2,95+0,19+0,21)6=20,1 моль для 98%-ного исходного сырья. Однако для достижения полной выварки на этой стадии применяли 20%-ный избыток ильменита. После выварки около 94% от избытка ильменита могло быть регенерировано благодаря его высокой плотности и грубым частицам. Шихту готовили следующим образом. В полипропиленовый сосуд объемом 2 л добавляли ильменит(600 г) в водопроводной воде (500 мл, 20 С). При энергичном перемешивании добавляли HF (900 мл,40%) и сосуд закрывали незакрепленной тяжелой крышкой из пластика. Реакция была очень экзотермической и примерно через 10 мин суспензия достигала точки кипения и кипела в течение примерно 5 мин. Через 2 ч к раствору добавляли Fe (12 г, стальная вата) и смесь перемешивали в течение 1 ч для восстановления всего растворимого Fe(III) до Fe(II). Затем суспензию фильтровали и промывали водопроводной водой (250 мл). Получали на фильтре около 200 г влажного осадка. Этот материал вновь суспендировали для выделения большей части избытка ильменита и получали 1375 мл щелока, содержащего FeTiF6. Выход при экстракции. Концентрация Ti в щелоке составляла примерно 100 г/л, что соответствовало 137,5 г титана. Выход при экстракции определяли следующим образом: стехиометрия: 141,5 г Ti (загрузка 500 г)=97%; 20%-ный избыток: 169,8 г Ti (загрузка 600 г)=81%; 94%-ная регенерация избытка: 144 г Ti (загрузка 505 г)=95,5%. Стадия 2. Селективное осаждение (NH4)2TiF6. Щелок (1,375 л) содержал Ti (137,5 г, 2,865 моль). Для этого требовался NH4Cl (42,865=11,46 моль,613,11 г).NH4Cl (613 г) медленно добавляли к щелоку, содержащему FeTiF6 со стадии 1 (1,375 л), при энергичном перемешивании. Температура понижалась до величины ниже 10 С и ее повышали до 15 С на теплой бане. Затем суспензию перемешивали при 15 С в течение 1 ч. Полученный кристаллический (NH4)2TiF6 отфильтровывали при 15-20 С и прессовали в головке фильтра для удаления как можно большего избытка жидкости. Затем отключали вакуум и добавляли к продукту ледяную воду (184 мл, 5 С). Вакуум можно было включить только после того, как вода проникла в осадок на фильтре (примерно через 2 мин), кристаллический (NH4)2TiF6 имел вид сахарной глазури. Кристаллический продукт отсасывали и прессовали досуха, как только это было возможно. Затем кристаллический (NH4)2TiF6 подвергали сушке при 60 С. Выход был равен 522 г. Рентгено-2 015885 грамма дифракционных полос этого продукта показана на фиг. 3. Выход при осаждении. В расчете на (NH4)2TiF6 кристаллический продукт имеет степень чистоты, равную 100%(522 г=2,631 моль Ti), выход Ti равен 92%. Концентрация Fe в кристаллическом продукте обычно была равна примерно 0,50,4%. Содержались также другие примеси, такие как Si и Al. Однако эти примеси могут быть удалены предварительной обработкой сырья перед вываркой (например, путем выщелачивания каустической содой) или путем осаждения этих элементов после проведения выварки. Например, после восстановления Fe можно добавить NaCl для осаждения Na2SiF6 и(500 мл) в сосуде объемом 2 л. Было установлено, что безводный (NH4)2TiF6 обладает большей растворимостью, чем гидратированный или влажный (NH4)2TiF6 хН 2 О. К этой суспензии добавляли небольшой кусок полоски Al (примерно 100 мм 25 мм). Для предотвращения гидролиза и инициирования восстановления небольшого количества Ti(IV) алюминием при перемешивании добавляли HF (0,5 мл, 40%). Суспензию нагревали до температуры кипения (примерно 100 С). Пена, образующаяся на поверхности раствора, со временем уменьшалась и смешивалась с раствором. Цвет раствора становился бледно-фиолетовым, что указывало на наличие Ti(III). Это также свидетельствовало о том, что все содержащееся железо было в виде Fe(II). Когда раствор кипел, слой фиолетового TiF3 отравлял полоску Al и восстановление прекращалось. Образование небольшого количества(NH4)3AlF6 из-за добавления полоски алюминия не составляло никакой проблемы, так как этот продукт образуется как побочный на следующей стадии (стадия 3). После кипения раствора в течение примерно 1 мин его удаляли от источника нагрева и давали ему охладиться. Затем удаляли полоску Al и вновь использовали ее (без очистки) в следующем цикле. Сосуд охлаждали до температуры, равной около 40 С, холодной водой и затем лед и холодную воду применяли для охлаждения сосуда до 10 С при перемешивании образующегося кристаллического(NH4)2TiF6. Затем кристаллический продукт отфильтровывали и прессовали в головке фильтра для возможно полного удаления избытка жидкости. Затем отключали вакуум и к кристаллическому продукту добавляли ледяную воду (50 мл, 5 С). Вакуум можно было включить только после того, как вода проникла в осадок на фильтре (примерно через 2 мин), кристаллический (NH4)2TiF6 имел вид сахарной глазури. Кристаллический продукт отсасывали и прессовали досуха, как только это было возможно. Полученный кристаллический (NH4)2TiF6 сушили при 60 С. Обычно выход составлял 70% от исходного кристаллического продукта без испарения дополнительной воды. Рентгенограмма дифракционных полос этого продукта показана на фиг. 4. Недоработанный, но надежный метод определения степени чистоты высушенного кристаллического (NH4)2TiF6 заключался в добавлении этого продукта (примерно 5 г) к химически чистой HCl (примерно 25 мл, 32%) в стеклянном стакане объемом 50 мл. После выдержки в течение примерно 5 мин HCl становилась желтой или оранжевой, если содержалось какое-то количество железа. КонцентрированнаяHCl является очень чувствительной к железу, и интенсивность желтой или оранжевой окраски прямо пропорциональна концентрации железа при величинах концентрации между 1 и 0,01% Fe. Это определение проводили с применением исходного кристаллического продукта, перекристаллизованного продукта и эталонного (NH4)2TiF6. Стадия 3. Восстановление (NH4)2TiF6 при помощи Al(Hg). Активация Al ртутью. Алюминиевую крупку (диаметр около 10-15 мм, толщина 1-3 мм, 150 г) погружали в 1 N растворNaOH в стакане объемом 500 мл из пластика и добавляли ртуть (примерно 50 мл). Крупку перемешивали пластмассовой мешалкой и погружали в ртуть. Примерно через 5 мин крупка была полностью покрыта ртутью. Гидроокись натрия удаляли путем промывки крупки сильным потоком водопроводной воды в стакане в течение примерно 1 мин. Затем сливали избыток ртути с крупки, покрытой ртутью, через сито (500 мкм) и сразу же на крупку выливали ацетон. После выдержки в ацетоне в течение примерно 1-2 ч с крупки продолжала капать ртуть, после чего на крупке остался только микрослой ртути. Готовую к использованию крупку Al(Hg) просеивали через сито (500 мкм) из ацетона и свободнойHg и сразу же по крупицам добавляли в раствор (NH4)2TiF6, описанный выше. Восстановление. В сосуде объемом 2 л перекристаллизованный (NH4)2TiF6 со стадии 2 (500 г) растворяли в водопроводной воде (1,5 л). Температуру повышали до 30 С, образовывался прозрачный раствор. Крупку Al(Hg), полученную, как описано выше, добавляли к раствору (NH4)2TiF6 при перемешивании (без завихрений). Реакция была экзотермической и температура повышалась от 30 до 70 С в течение-3 015885 75 мин. Через 15 мин нагревания при 70 С суспензию охлаждали до температуры ниже 30 С и отфильтровывали. Крупка Al(Hg) промывалась водой и хранилась в ацетоне. Фиолетовый осадок отфильтровывали,отсасывали жидкость досуха и промывали водой (250 мл). Фиолетовый осадок высушивали при температуре 60 С (выход составил 475 г). Продукт, полученный при этом, состоял из NH4TiF4 и (NH4)3AlF6 в весовом отношении, равном примерно 75:25%. NH4TiF4 обладает низкой растворимостью в разбавленной HF и даже еще более низкой растворимостью в концентрированной HF. Таким образом, если необходимо, (NH4)3AlF6 (и другие примеси) может быть удален из продукта при промывке. Рентгенограмма дифракционных полос этого чистого продукта приведена на фиг. 5. Было также установлено, что, если вместо чистого (NH4)2TiF6 использовать сырой продукт, Fe(II),содержащийся в растворе, покрывал крупку Al(Hg) и отравлял ее. Однако это происходило только после того, как весь Ti(IV) восстанавливался до Ti(III). Заявитель считает, что этот метод может быть применен для удаления Fe до такой степени, когда перекристаллизация(NH4)2TiF6 перестанет быть необходимой. После восстановления отравленная крупка Al(Hg) может быть вновь активирована при помощи разбавленного щелока HCl с целью удаления железа. Стадия 4. Разложение NH4TiF4 и (NH4)3AlF6. Продукт восстановления, полученный на стадии 3, состоящий из смеси NH4TiF4 и (NH4)3AlF6, подвергали разложению при температуре 600 С в атмосфере азота или аргона в мягких условиях во вращающемся аппарате. Через 2-4 ч намачивания светло-коричневый продукт, состоящий из TiF3 и AlF3,совсем не содержал NH4F, который испарился. Испарившийся продукт конденсировали и собирали. Было найдено, что если оставались следы NH4F, то во время восстановления алюминием при 750 С образовывался TiN. В зависимости от отношения между NH4TiF4 и (NH4)3AlF6 выход продукта, полученного на стадии разложения, обычно был равен от 60 до 70% от исходного сырья. Рентгенограмма дифракционных полос чистого TiF3, полученного из чистого NH4TiF4, полученного как описано выше, показана на фиг. 6. До сих пор соль NH4TiF4 была неизвестной и соответственно нет данных, с которыми можно было бы сравнить рентгенограмму дифракционных полос NH4TiF4, показанную на фиг. 5. Наиболее подходящей для сравнения с рентгенограммой этой соли является рентгенограмма дифракционных полосNH4FeF4. Поэтому не является неожиданным тот факт, что продукт разложения NH4TiF4, представляющий собой TiF3, лучше сравнивать с FeF3 (их рентгенограммы). Рентгенограммы дифракционных полос стандартных образцов FeF3 и TiF3 показаны на фиг. 7. Стадия 5. Восстановление TiF3 алюминием и сублимация AlF3. После определения отношения между TiF3 и AlF3 в продукте, полученном на стадии (4), порошокAl (125 мкм) смешивали с этим продуктом. Использовали стехиометрическое количество Al к TiF3(1 моль:1 моль). Смесь помещали в стальной приемник в атмосферу аргона и нагревали до 750 С. Через 2 ч выдержки восстановление было полным без изменения массы. Рентгенограмма этого материала показана на фиг. 8. Было установлено, что для полного восстановления в статической установке самый грубый порошок Al, который можно было использовать, имел частицы размером 125 мкм. Ожидается, что во вращающемся аппарате жидкий Al может полностью смачиваться TiF3 и тем самым способствовать восстановлению. Или же Al может быть растворен в цинке для увеличения площади поверхности Al для того,чтобы восстановление было полным. После восстановления Zn может быть испарен при температуре 950 С, сконденсирован и снова применен в следующем цикле. После восстановления при температуре 750 С температуру повышали до 1250 С, сохраняя все еще атмосферу аргона. При этой температуре AlF3 возгонялся, затем конденсировался и собирался как чистый побочный продукт. Рентгенограмма дифракционных полос AlF3 показана на фиг 9. Когда образование белых паров прекратилось, возгонка была завершена. В зависимости от величины загрузки и площади поверхности намачивание при этой температуре длилось от 2 до 10 ч. После охлаждения полученный порошок Ti собирали. Рентгенограмма дифракционных полос этого порошка показана на фиг. 10. Заявитель установил, что полная возгонка AlF3 может быть нежелательной и что является предпочтительным оставлять следы (0,1-5%) для образования покрытия на порошке Ti. Было обнаружено, что это фторидное покрытие защищало порошок и повышало безопасность при манипулировании с порошком и его транспортировке. Известные ранее промышленные порошки Ti спонтанно возгорались при температуре около 250 С на воздухе. Однако эта температура повышается до 600 С, если имеется инертный слой AlF3. Когда порошок плавят или спекают (порошковая металлургия), слой AlF3 будет возгоняться и не будет загрязнять титан. Было также установлено, что металлическая корка образуется на поверхности порошка титана при температуре 1250 С (см. фиг. 15). Полагают, что эта крошка содержит примеси металлов, которые мигрировали с газообразным AlF3 на поверхность порошка и осадились на ней по мере сублимации AlF3-4 015885 аналогично зонному рафинированию. Стадия 6. Плавление порошка Ti. Порошок Ti, полученный на стадии (5), прессовали в металлоприемнике, изготовленном из глины и облицованном двуокисью циркония, и расплавляли в индукционной печи в атмосфере аргона. Он легко плавился с образованием небольшого слитка и следы AlF3 выделялись в виде паров. Рентгенограмма дифракционных полос металла показана на фиг. 11. Порошок Ti или металл, полученный этим способом,содержал очень низкие количества ( чем у Ti сорта 1) кислорода, азота, углерода и водорода благодаря защите фторидом, описанной выше. Как можно видеть по рентгенограмме дифракционных полос слитка Ti, способ по данному изобретению позволяет получать Ti путем восстановления алюминием без образования сплавов Al-Ti. Хотя рентгенограмма дифракционных полос порошка Ti после восстановления, показанная на фиг. 8 и после сублимации, как показано на фиг. 10, показывает наличие фазы AlTi3 (вместо фаз Ti только), заявитель полагает, что фаза AlTi3, которая ясно видна на рентгенограммах, является только фазой псевдо-AlTi3 и что в действительности алюминия нет. Причина того, что "Ti3" имеет кристаллическую структуру AlTi3,заключается в том, что она "родилась" из Al и при использованной низкой температуре (1300 С) для переориентации кристаллической структуры титана не хватает энергии. Перестройка кристаллической структуры титана происходит только тогда, когда Ti плавится или реагирует с чем-нибудь еще, например с азотом, с образованием TiN. На фиг. 12 показана рентгенограмма для случая, когда порошок Ti подвергался действию ограниченного количества N2 при температуре 1350 С. Как можно видеть на этой рентгенограмме, ни Al, ни сплав Al не были обнаружены. Это подтверждается также тем, что рентгенограмма дифракционных полос восстановленного алюминием порошка Ti (фиг. 8) показывает, что содержатся только фазы AlF3 и AlTi3. Так как было применено стехиометрическое отношение Al к TiF3, то, если Al в действительности образует сплав с Ti с образованием AlTi3, будет содержаться 25% непрореагировавшего TiF3, и это не видно из рентгенограммы. Основной причиной того, что Ti может быть восстановлен алюминием без образования сплавов, является тот факт, что в процессе восстановления Al реагирует с Ti(III), а не с Ti(IV). Первая реакция является умеренно экзотермической, в то время как вторая реакция является сильно экзотермической: Образование сплава происходит тогда, когда два металла находятся в контакте друг с другом и величина энергии является достаточной для образования сплава. Во время первой реакции энергия слишком мала, чтобы образование сплава стало возможным. Наличие AlTi3 также помогло поддержать температуру менее 1100 С, при которой AlTi3 начинает возгоняться, поглощая при этом энергию. Очевидно, что первое электронное восстановление Ti(IV) до Ti(III) является сильно экзотермическим. Согласно способу по данному изобретению энергия абсорбируется водой во время контролируемого восстановления (NH4)2TiF6 при помощи Al(Hg) в водной среде. Преимущества Способ согласно данному изобретению имеет несколько явных преимуществ по сравнению с известными из уровня техники способами.(1) Во-первых, в способе по изобретению применяются недорогие исходные материалы, такие как ильменит, который доступен в больших количествах.(2) Побочные продукты, получающиеся при осуществлении этого способа, все возвращаются в цикл и соответственно имеет место очень небольшое избыточное потребление реагентов.(3) Способ по изобретению позволяет также получать титан, который содержит защитное фторидное покрытие, как описано выше.(4) Дальнейшим преимуществом способа по изобретению является то, что вместо предшественника титана, такого как TiCl4, применяется промежуточный продукт (NH4)2TiF6, который не был ранее коммерчески доступен. Соль (NH4)2TiF6 стабильна на воздухе и в воде, она не вызывает коррозии и может быть легко получена в водной среде при комнатной температуре. С другой стороны, TiCl4 является очень токсичной жидкостью, которая быстро разлагается на воздухе и в воде и вызывает сильную коррозию. Ее трудно получить, так как нужны температуры порядка 1000 С и она находится в виде газа во время стадии восстановления. Титан, полученный из TiCl4, является дорогим и подвержен загрязнению О, N, Н иCl вследствие отсутствия фторидного покрытия, характерного для данного изобретения.(5) Дальнейшим важным преимуществом является тот факт, что титан, полученный способом согласно данному изобретению, имеет стоимость, сравнимую со стоимостью высококачественной нержавеющей стали.(6) Еще одно преимущество состоит в том, что алюминий, который существенно дешевле, чем натрий или магний (используемые в известных способах), применяется на стадии восстановления, и в конечном продукте не содержатся сплавы алюминия.(7) Далее, способ согласно данному изобретению приводит к получению порошка титана при тем-5 015885 пературе, которая значительно ниже температуры плавления титана. Это приводит к значительно более дешевым пирометаллургическим операциям. Этот порошок может быть затем применен в классической порошковой металлургии для получения почти чистых формованных изделий. Это приводит к образованию гораздо меньшего количества отбросов по сравнению с известными способами, предусматривающими применение титановых слитков. Однако, если требуются титановые слитки, порошок может быть легко расплавлен на единственной стадии получения расплава, например, в индукционной печи, так как он защищен покрытием на основе AlF3. AlF3 дополнительно действует как флюс во время плавления порошка.(8) Еще одно преимущество данного изобретения состоит в том, что процесс можно осуществить с применением водной технической HF, которая значительно дешевле, чем химически чистая водная HF. В таблицах с целью сравнения приведены типичный химический состав, механические свойства и физические свойства коммерчески доступных коррозионно-стойких сплавов титана. Химический состав (номинальные %) Выводы Таким образом, заявитель обнаружил, что очень чистый титансодержащий предшественник может быть получен с высоким выходом продукта из ильменита (который является самым дешевым источником титана) и что такой предшественник может использоваться для производства металлического титана с содержанием кислорода, которое ниже, чем в титане сорта 1. Низкое содержание кислорода повышает ковкость (пластичность) металла. Металл также защищен от окисления в ходе вышеуказанного с помощью фторидного покрытия. Заявитель полагает, что указанный в изобретении способ позволит получать титан с такими же затратами, как и нержавеющую сталь высоких сортов. Это существенно расширит мировой рынок для титана. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения порошка металлического титана, содержащего поверхностный слой из AlF3,включающий стадию восстановления TiF3 алюминием с получением продукта восстановления, содержащего порошок металлического титана, покрытый AlF3. 2. Способ по п.1, отличающийся тем, что продукт восстановления нагревают до тех пор, пока содержание AlF3 на поверхности порошка металлического титана не станет равным величине между 0,005 и 40% от массы материала. 3. Способ по п.1, отличающийся тем, что содержание AlF3 на поверхности порошка металлического титана равно величине между 0,05 и 10% от массы материала. 4. Способ по п.1, отличающийся тем, что содержание AlF3 на поверхности порошка металлического титана составляет от 0,10 до 5% от массы материала. 5. Дезактивированный порошок титана, содержащий поверхностный слой AlF3, содержание которого составляет от 0,005 до 10% от массы материала. 6. Дезактивированный порошок титана по п.5, отличающийся тем, что содержание AlF3 составляет от 0,05 до 10% от массы материала. 7. Дезактивированный порошок титана по п.5, отличающийся тем, что содержание AlF3 составляет от 0,10 до 5% от массы материала. 8. Порошок титана, характеризующийся тем, что его рентгенограмма дифракционных полос сходна с рентгенограммой дифракционных полос AlTi3. 9. Порошок титана, характеризующийся тем, что его рентгенограмма дифракционных полос практически имеет вид, показанный на фиг. 10. 10. Способ получения порошка металлического титана, включающий стадии восстановления TiF3 алюминием с получением продукта восстановления, содержащего порошок металлического титана и AlF3, и нагрева этого продукта восстановления для возгонки AlF3 для получения порошка титана, по существу, не содержащего алюминия в виде металла или сплава.
МПК / Метки
МПК: C22C 1/00, C22B 34/12, C01G 23/00
Метки: получения, титана, способ
Код ссылки
<a href="https://eas.patents.su/14-15885-sposob-polucheniya-titana.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения титана</a>
Предыдущий патент: Лопасть вентилятора градирни (варианты)
Следующий патент: Ингибиторы каспазы на основе пиридазинонового каркаса
Случайный патент: Устройство для грозозащиты с пружинными электродами и линия электропередачи, снабженная таким устройством