Фармацевтическая композиция управляемого высвобождения и способ ее получения
Номер патента: 8944
Опубликовано: 26.10.2007
Авторы: Джаянтхи Сурйакумар, Сен Химадри, Рагхаван Винеетх, Арра Ганга Сринивас
Формула / Реферат
1. Антиретровирусная фармацевтическая композиция, включающая селективную комбинацию
i. Состава управляемого высвобождения, включающего:
а) ламивудин или его фармацевтически приемлемое производное,
b) зидовудин или его фармацевтически приемлемое производное,
с) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, и
d) фармацевтически приемлемую соль кальция;
ii. Состава немедленного высвобождения, включающего по меньшей мере один селективный лекарственный препарат ненуклеозидных ингибиторов обратной транскриптазы (NNRTI) или его фармацевтически приемлемое производное вместе с фармацевтически приемлемыми наполнителями.
2. Антиретровирусная фармацевтическая композиция по п.1, где упомянутый лекарственный препарат NNRTI выбран из невирапина и эфавиренса.
3. Антиретровирусная фармацевтическая композиция по п.1, которая находится в форме двух отдельных слоев упомянутых состава управляемого высвобождения и состава немедленного высвобождения.
4. Антиретровирусная фармацевтическая композиция по п.1, которая находится в такой форме, что ядро представляет собой упомянутый состав управляемого высвобождения, а внешнее покрытие представляет собой состав немедленного высвобождения.
5. Антиретровирусная фармацевтическая композиция по п.1, включающая двухслойную селективную комбинацию
i. Первого слоя состава управляемого высвобождения, включающего:
а) ламивудин или его фармацевтически приемлемое производное,
b) зидовудин или его фармацевтически приемлемое производное,
с) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, и
d) фармацевтически приемлемую соль кальция;
ii. Второго слоя состава немедленного высвобождения, где упомянутый NNRTI является невирапином или его фармацевтически приемлемым производным вместе с фармацевтически приемлемыми наполнителями.
6. Антиретровирусная фармацевтическая композиция по п.1, включающая селективную комбинацию
i. Ядра, которое содержит состав управляемого высвобождения, включающий:
а) ламивудин или его фармацевтически приемлемое производное,
b) зидовудин или его фармацевтически приемлемое производное,
с) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, и
d) фармацевтически приемлемую соль кальция;
ii. Внешнего покрытия состава немедленного высвобождения, где упомянутый NNRTI является невирапином или его фармацевтически приемлемым производным вместе с фармацевтически приемлемыми наполнителями.
7. Антиретровирусная фармацевтическая композиция по п.1, включающая селективную двухслойную комбинацию
i. Первого слоя состава управляемого высвобождения, включающего:
а) ламивудин или его фармацевтически приемлемое производное,
b) зидовудин или его фармацевтически приемлемое производное,
с) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, и
d) фармацевтически приемлемую соль кальция;
ii. Второго слоя состава немедленного высвобождения, где упомянутый NNRTI является эфавиренсом или его фармацевтически приемлемым производным вместе с фармацевтически приемлемыми наполнителями.
8. Антиретровирусная фармацевтическая композиция по п.1, включающая селективную комбинацию
i. Ядра состава управляемого высвобождения, включающего:
а) ламивудин или его фармацевтически приемлемое производное,
b) зидовудин или его фармацевтически приемлемое производное,
с) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, и
d) фармацевтически приемлемую соль кальция;
ii. Внешнего покрытия состава немедленного высвобождения, где упомянутый NNRTI является эфавиренсом или его фармацевтически приемлемым производным вместе с фармацевтически приемлемыми наполнителями.
9. Композиция по любому из пп.1-8, где количество ламивудина или его фармацевтически приемлемого производного составляет от около 50 до около 500 мг.
10. Композиция по п.9, где количество ламивудина или его фармацевтически приемлемого производного составляет около 300 мг.
11. Композиция по любому из пп.1-8, где количество зидовудина или его фармацевтически приемлемого производного составляет от около 100 до около 1000 мг.
12. Композиция по п.11, где количество зидовудина или его фармацевтически приемлемого производного составляет 600 мг.
13. Композиция по любому из пп.1-12, где количество невирапина/эфавиренса или его фармацевтически приемлемого производного составляет от около 100 до около 1000 мг.
14. Композиция по п.13, где количество невирапина или его фармацевтически приемлемого производного составляет около 400 мг.
15. Композиция по п.13, где количество эфавиренса или его фармацевтически приемлемого производного составляет около 600 мг.
16. Композиция по любому из пп.1-15, где эфир целлюлозы выбран из гидроксипропилцеллюлозы, гидроксипропилметилцеллюлозы, карбоксиметилцеллюлозы, натрия карбоксиметилцеллюлозы, этилцеллюлозы, метилцеллюлозы, гидроксиэтилцеллюлозы.
17. Композиция по п.16, где эфир целлюлозы является гидроксипропилметилцеллюлозой и присутствует в количестве от около 2 до около 12 вес.% состава управляемого высвобождения.
18. Композиция по п.17, где эфир целлюлозы является гидроксипропилметилцеллюлозой и присутствует в количестве от около 3 до около 8 вес.% состава управляемого высвобождения.
19. Композиция по любому из пп.1-18, где полиуроновая кислота выбрана из альгиновой кислоты, альгината натрия, альгината кальция, альгината натрия-кальция, альгината калия, альгината аммония, альгината магния.
20. Композиция по п.19, где полиуроновая кислота является альгинатом натрия и присутствует в количестве от около 0,5 до около 10 вес.% состава управляемого высвобождения.
21. Композиция по п.20, где полиуроновая кислота является альгинатом натрия и присутствует в количестве от около 1 до около 6 вес.% состава управляемого высвобождения.
22. Композиция по любому из пп.1-21, где фармацевтически приемлемая смола выбрана из гуаровой смолы, ксантановой смолы, смолы карайя, трагакантовой смолы, акациевой смолы.
23. Композиция по п.22, где фармацевтически приемлемая смола является гуаровой смолой и присутствует в количестве от около 0,1 до около 10 вес.% состава управляемого высвобождения.
24. Композиция по п.23, где фармацевтически приемлемая смола является гуаровой смолой и присутствует в количестве от около 0,5 до около 6 вес.% состава управляемого высвобождения.
25. Композиция по любому из пп.1-24, где фармацевтически приемлемая соль кальция выбрана из группы, включающей сульфат кальция, фосфат кальция, карбонат кальция и хлорид кальция.
26. Композиция по п.25, где фармацевтически приемлемая соль кальция является сульфатом кальция и присутствует в количестве от около 0,1 до около 2,5 вес.% состава управляемого высвобождения.
27. Композиция по п.26, где фармацевтически приемлемая соль кальция является сульфатом кальция и присутствует в количестве от около 0,1 до около 2 вес.% состава управляемого высвобождения.
28. Композиция по любому из пп.1-27, где состав управляемого высвобождения дополнительно содержит по меньшей мере один разбавитель, способный диспергироваться в воде, или растворимый в воде разбавитель, выбранный из микрокристаллической целлюлозы, дикальциевую кислую соль фосфорной кислоты, карбоната кальция, лактозы, порошкообразной целлюлозы, крахмала, маннита.
29. Композиция по п.28, где разбавитель присутствует в количестве от около 1 до около 28 вес.% состртр управляемого высвобождения.
30. Композиция по п.29, где разбавитель является микрокристаллической целлюлозой.
31. Композиция по п.30, где количество микрокристаллической целлюлозы составляет от около 5 до около 20 вес.%.
32. Композиция по п.29, где разбавитель является дикальциевой кислой солью фосфорной кислоты.
33. Композиция по п.32, где количество дикальциевой кислой соли фосфорной кислоты составляет от около 1 до около 5 вес.%.
34. Композиция по любому из пп.1-33, где состав управляемого высвобождения дополнительно содержит по меньшей мере одну смазочную добавку, выбранную из стеарата магния, стеарата кальция, стеариновой кислоты, диоксида кремния, талька.
35. Композиция по п.34, где смазочная добавка присутствует в количестве от около 0,1 до 3 вес.%.
36. Композиция по любому из пп.1-35, где состав немедленного высвобождения включает от около 10 до около 95 вес.% невирапина или его фармацевтически приемлемого производного вместе с одним или несколькими фармацевтически приемлемыми наполнителями, выбранными из разбавителей, связывающих агентов, дезинтеграторов, смазочных добавок, красителей.
37. Композиция по п.36, где разбавитель выбран из микрокристаллической целлюлозы, дикальциевой кислой соли фосфорной кислоты, карбоната кальция, лактозы, порошкообразной целлюлозы, крахмала, маннита.
38. Композиция по п.37, где разбавитель является порошкообразной целлюлозой и присутствует в количестве от около 2 до около 15 вес.% состава немедленного высвобождения.
39. Композиция по п.36, где связывающий агент выбран из натрия карбоксиметилцеллюлозы, повидона, прежелатинизированного крахмала, желатина или их смесей.
40. Композиция по п.39, где связывающий агент присутствует в количестве от около 1 до около 10 вес.% состава немедленного высвобождения.
41. Композиция по п.36, где дезинтегратор выбран из кросповидона, натрия крахмалгликолята, прежелатинизированного крахмала, натрия карбоксиметилцеллюлозы, натрия кроскармелозы, крахмала и их смесей.
42. Композиция по п.41, где дезинтегратор присутствует в количестве от около 0,5 до около 15 вес.% состава немедленного высвобождения.
43. Композиция по п.36, где смазочная добавка выбрана из стеарата магния, стеарата кальция, стеариновой кислоты, диоксида кремния, талька.
44. Композиция по п.43, где смазочная добавка присутствует в количестве от около 0,1 до 3 вес.%.
45. Способ получения антиретровирусной фармацевтической композиции, который включает следующие этапы:
(i) получают состав управляемого высвобождения перемешиванием вместе активных ингредиентов, выбранных из ламивудина, зидовудина или их смесей, с гидрофильными полимерами, выбранными из эфиров целлюлозы, полиуроновых кислот, фармацевтически приемлемых смол или их смесей, и с фармацевтически приемлемой солью кальция, необязательно, с разбавителем и смазочной добавкой,
(ii) получают состав немедленного высвобождения, по меньшей мере, смешиванием NNRTI с фармацевтически приемлемыми наполнителями и
(iii) получают из них композицию прессованием образованных смесей в двухслойные таблетки.
46. Способ получения антиретровирусной фармацевтической композиции, который включает следующие этапы:
(i) получают ядро упомянутого состава управляемого высвобождения перемешиванием вместе активных ингредиентов, выбранных из ламивудина, зидовудина или их смесей, с гидрофильными полимерами, выбранными из эфиров целлюлозы, полиуроновых кислот, фармацевтически приемлемых смол или их смесей, с фармацевтически приемлемой солью кальция, необязательно, с разбавителем и смазочной добавкой,
(ii) получают внешнее покрытие состава немедленного высвобождения, по меньшей мере, из NNRTI, выбранного из невирапина и эфавиренса, смешанного с фармацевтически приемлемыми наполнителями, и
(iii) получают из них композицию путем нанесения упомянутого внешнего покрытия на упомянутое ядро прессованием покрытия.
47. Способ по п.45 или 46, в котором каждую смесь гранулируют сухим способом перед прессованием.
48. Способ по п.45 или 46, в котором каждую смесь гранулируют влажным способом перед прессованием.
49. Способ снижения лекарственной нагрузки на пациента, страдающего инфекцией ВИЧ и/или синдромом приобретенного иммунного дефицита, при котором вводят антиретровирусную фармацевтическую композицию из трех лекарственных препаратов, которая включает комбинацию ламивудина и зидовудина в качестве компонента управляемого высвобождения и невирапина или эфавиренса в качестве компонента немедленного высвобождения.
50. Способ снижения лекарственной нагрузки на пациента, страдающего инфекцией ВИЧ и/или синдромом приобретенного иммунного дефицита, при котором вводят антиретровирусную фармацевтическую композицию из трех лекарственных препаратов, которая включает ламивудин и зидовудин в качестве компонент управляемого высвобождения и невирапин или эфавиренс в качестве компонент немедленного высвобождения, причем композиция после введения упомянутому пациенту обеспечивает Сmaх от около 1,2 до 2,0 мкг/мл для ламивудина, от около 1,0 до 2,0 мкг/мл для зидовудина и от около 4,5 до 5,5 мкг/мл для невирапина.
51. Способ снижения лекарственной нагрузки на пациента, страдающего инфекцией ВИЧ и/или синдромом приобретенного иммунного дефицита, при котором вводят антиретровирусную фармацевтическую композицию из трех лекарственных препаратов, которая включает ламивудин и зидовудин в качестве компонента управляемого высвобождения и невирапин или эфавиренс в качестве компонента немедленноговысвобождения, причем композиция после введения упомянутому пациенту обеспечивает AUC0-t от около 8 до 14 мкг, ч/мл для ламивудина, от около 5 до 9 мкг, ч/мл для зидовудина и от около 32 до 40 мкг, ч/мл для невирапина.
52. Способ увеличения in vivo периода полувыведения ламивудина и зидовудина без влияния на период полувыведения невирапина и, следовательно, снижения лекарственной нагрузки на пациента, страдающего инфекцией ВИЧ и/или синдромом приобретенного иммунного дефицита, при котором вводят антиретровирусную композицию из трех лекарственных препаратов, которая включает ламивудин и зидовудин как компонент управляемого высвобождения и невирапин или эфавиренс как компонент немедленного высвобождения.
53. Способ по п.51, где композиция после введения упомянутому пациенту обеспечивает t1/2 около 5 ч для ламивудина, около 2 ч для зидовудина и около 29 ч для невирапина.
54. Способ снижения лекарственной нагрузки на пациента, страдающего инфекцией ВИЧ и/или синдромом приобретенного иммунного дефицита, при котором вводят антиретровирусную фармацевтическую композицию из трех лекарственных препаратов, которая включает ламивудин и зидовудин в качестве компонента управляемого высвобождения и невирапин или эфавиренс в качестве компонента немедленного высвобождения, где композиция после введения упомянутому пациенту обеспечивает Сmах упомянутых лекарственных препаратов в компоненте управляемого высвобождения, которая является в значительной степени подобной той, что обеспечивается композициями немедленного высвобождения упомянутых лекарственных препаратов, при введении совместно, последовательно или одновременно.
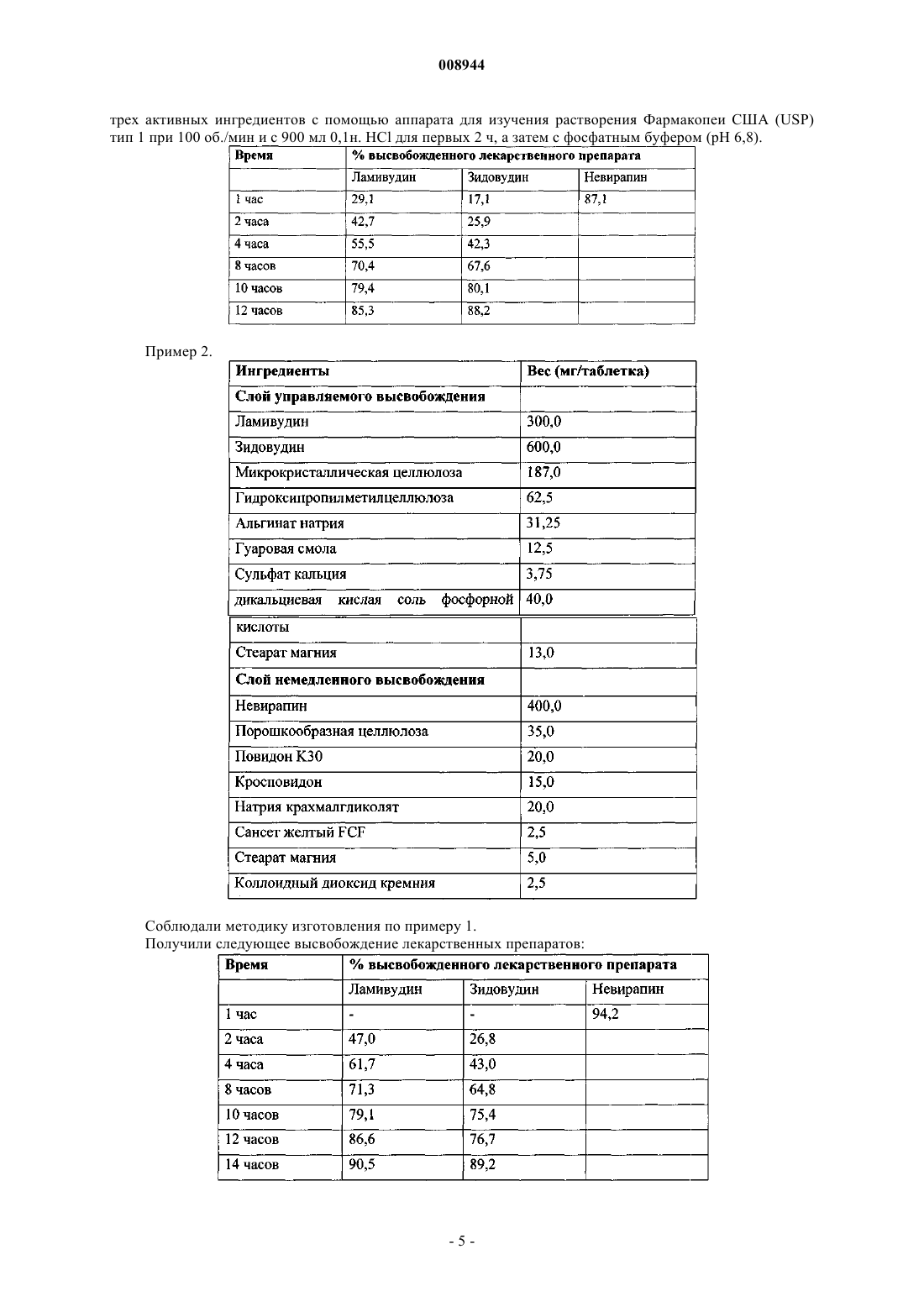
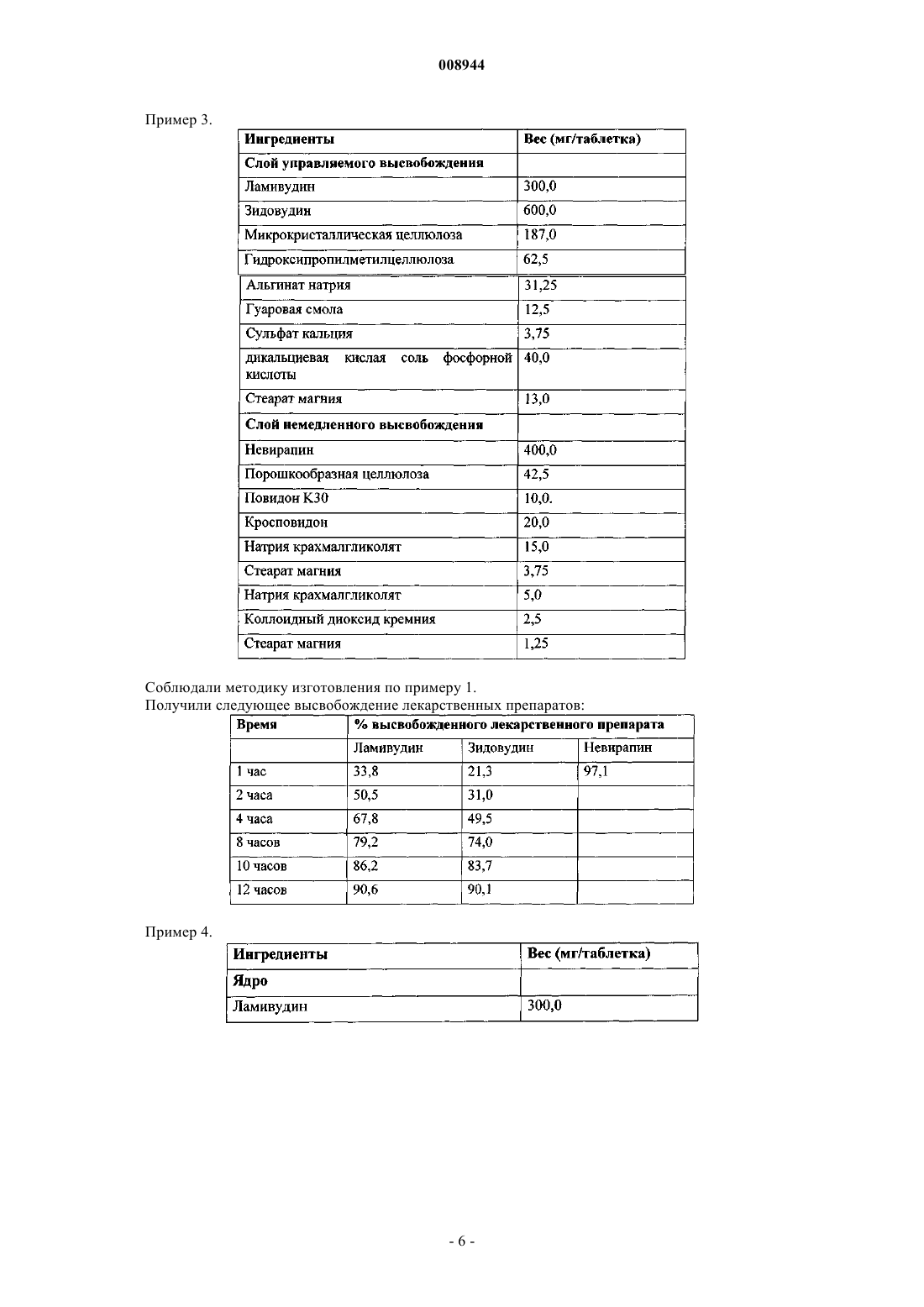
Текст
008944 Область данного изобретения Данное изобретение касается антиретровирусной фармацевтической композиции. Подробнее данное изобретение касается антиретровирусной фармацевтической композиции, содержащей селективную комбинацию активного состава управляемого высвобождения и активного состава немедленного высвобождения, для однократного суточного введения. Данное изобретение также касается способа получения такой однократной суточной антиретровирусной фармацевтической композиции. Предпосылки данного изобретения Синдром приобретенного иммунного дефицита (СПИД), который вызывается вирусом иммунодефицита человека (ВИЧ), одна из немногих болезней, для которых человечество упорно пытается найти способ лечения. В последние несколько лет открыто много антиретровирусных агентов, которые применяются для лечения СПИД. Лекарственные препараты, которые в настоящее время приняты в анти-ВИЧ терапии,разделены на три категории, а именно: 1. Нуклеозидные ингибиторы обратной транскриптазы (NRTI), которые включают ламивудин, зидовудин, диданозин, абакавир, ставудин и зальцитабин. 2. Ненуклеозидные ингибиторы обратной транскриптазы (NNRTI), которые включают невирапин,эфавиренс и делавирдин. 3. Ингибиторы протеазы (PI), которые включают индинавир, ритонавир, нелфинавир, саквинавир и ампренавир. Для успешного лечения какой-либо болезни, вызванной микроорганизмом, лекарственный препарат, используемый в терапии, должен устранять болезнетворный организм полностью, не позволяя микроорганизму мутировать. Мутация может привести к образованию устойчивых штаммов, которые могут затруднить лечение. Такое развитие устойчивых штаммов обычно наблюдается, если при лечении используется исключительно один агент или лекарственные препараты, принадлежащие одной категории. Выяснили, что большинство болезней, вызванных микроорганизмами, можно с большим успехом лечить комбинированием двух или нескольких лекарственных препаратов предпочтительно из различных классов. Лекарственные препараты высокоактивной антиретровирусной терапии первоначально назначались как свободная комбинация двух или трех лекарственных препаратов. Это было рационализировано применением комбинаций с фиксированными дозами, которые вводили дважды в день. В заявке на патентPCT/IN 02/00110, находящейся на стадии рассмотрения, описан состав, который способствует снижению лекарственной нагрузки до одного раза в день. Однако до настоящего времени нет сообщений о составе,принимаемом один раз в день, который включает комбинацию из трех лекарственных препаратов. Существует три известных альтернативных режима, например: 1) 3 NRTI,2) 2 NRTI + 1 NNRTI,3) 2 NRTI + 1 PI. Нуклеозидные ингибиторы обратной транскриптазы (NRTI) были первыми лекарственными препаратами, которые назначали как антиретровирусные агенты, и они остаются основой терапии против ВИЧ инфекции и синдрома приобретенного иммунного дефицита (СПИД). Хотя испытывали различные режимы лечения, указанные выше, сообщалось, что комбинация лекарственных препаратов, включающая три NRTI, не такая эффективная, как другие комбинации. Составляющая основу терапии комбинация двух NRTI, ламивудина и зидовудина с одним NNRTI, таким как невирапин или эфавиренс, является лучшей. Период полувыведения из сыворотки ламивудина составляет от около 3 до 6 ч, в то время как зидовудина - 1,1 ч. Невирапин имеет длинный период полувыведения более чем 25 ч и в настоящее время его назначают дозой по 200 мг дважды в день. Эфавиренс назначают дозой по 600 мг один раз в день. Предлагается применять 400 мг невирапина, который будет назначаться как комбинация с фиксированной дозой ламивудина и зидовудина один раз в день. В случае эфавиренса его количество или количество его фармацевтически приемлемого производного составляет предпочтительно 600-800 мг. Лечение несколькими лекарственными препаратами в случае антиретровирусов имеет преимущество, которое заключается в том, что лекарственные препараты имеют различные механизмы действия,действуют на различных стадиях жизненного цикла вируса и могут проявлять синергический эффект при таком использовании. Однако этот вид терапии приводит к тому, что пациент должен принимать множество таблеток несколько раз в день, а это, как известно, вызывает проблемы соблюдения режима лечения. Было проделано несколько попыток снизить лекарственную нагрузку для улучшения соблюдения режима пациентом. Ламивудин 150 мг и зидовудин 300 мг являются NRTI, которые назначаются дважды в день. Разработали комбинацию с фиксированной дозой ламивудина 150 мг и зидовудина 300 мг (комбивирин), которая снижает лекарственную нагрузку этой комбинации до двух. Аналогично, разработана комбинация из трех лекарственных препаратов с фиксированной дозой ламивудина 150 мг, зидовудина 300 мг и абакавира 300 мг (тризивир). Однако есть сообщения о токсичности, связанной с абакавиром. Кроме того,-1 008944 частота дозирования для комбинации из двух и из трех лекарственных препаратов все еще составляет два раза в день. В патенте США 6113920 раскрывается фармацевтическая композиция, включающая два активных фармацевтических ингредиента, а именно, ламивудин и зидовудин, и фармацевтически приемлемый ингредиент, обеспечивающий скольжение, выбранный из коллоидного диоксида кремния, микрокристаллической целлюлозы, стеаратов металлов, карбоната кальция и их комбинаций, в форме таблетки,покрытой пленкой. Композиция содержит ламивудин в количестве от 15 до 1500 мг на таблетку и зидовудин в количестве от 30 до 1000 мг на таблетку. Эта комбинация назначается дважды в день. В патенте США 4917900 раскрывается фармацевтический состав для орального введения, в котором дискретные элементы, включая зидовудин, осуществлены с покрытием управляемого высвобождения, включающим алкильные эфиры акриловой и метакриловой кислот и этилцеллюлозы с весовым соотношением 1:3-3:1. Эти сфероиды содержат по меньшей мере 80% зидовудина, микрокристаллической целлюлозы и маннита, как ядрообразующего агента. Как обсуждалось выше, несмотря на то, что продукт комбинации двух лекарственных препаратов может снизить лекарственную нагрузку на половину, его все еще нужно принимать дважды в день, а если соединить его с третьим лекарственным препаратом, лекарственная нагрузка существенно возрастет. Цели данного изобретения Основной целью данного изобретения является осуществление антиретровирусной фармацевтической композиции из трех лекарственных препаратов, которая снизила бы лекарственную нагрузку и частоту введения лекарственного препарата, таким образом, благоприятствуя соблюдению пациентом режима лечения и эффективности лечения. Другая цель заключается в осуществлении комбинации с фиксированной дозой ламивудина, зидовудина и по меньшей мере одного лекарственного препарата NNRTI, приемлемого для однократного суточного введения, которая снизила бы лекарственную нагрузку до единицы и частоту до одного раза в день. Следующая цель данного изобретения направлена на разработку комбинации из трех лекарственных препаратов с фиксированной дозой, включающей, по существу, антиретровирусные лекарственные препараты ламивудина, зидовудина и по меньшей мере одного лекарственного препарата NNRTI, предпочтительно выбранного из невирапина и эфавиренса, приемлемой для однократной суточной дозировки, причем ламивудин и зидовудин имели бы управляемое высвобождение, тогда как невирапин/эфавиренс - немедленное высвобождение. Еще одна цель данного изобретения касается способа увеличения in vivo периода полувыведения ламивудина и зидовудин, не затрагивая период полувыведения невирапина или эфавиренса, и, таким образом, снижения лекарственной нагрузки на пациента, страдающего ВИЧ-инфекцией и/или синдромом приобретенного иммунного дефицита, введением антиретровирусной композиции из трех лекарственных препаратов, которая включает ламивудин и зидовудин, как компонент управляемого высвобождения, и невирапин или эфавиренс, как компонент немедленного высвобождения. Следующая цель направлена на осуществление способа получения упомянутой антиретровирусной фармацевтической композиции, которая бы снизила лекарственную нагрузку и частоту введения лекарственного препарата, тем самым благоприятствуя соблюдению пациентом режима лечения и эффективности лечения. Краткое описание данного изобретение Таким образом, данное изобретение предусматривает антиретровирусную фармацевтическую композицию, включающую селективную комбинациюa) ламивудин или его фармацевтически приемлемое производное,b) зидовудин или его фармацевтически приемлемое производное,c) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, иd) фармацевтически приемлемую соль кальция;ii. Состава немедленного высвобождения, включающего по меньшей мере один селективный лекарственный препарат ненуклеозидных ингибиторов обратной транскриптазы (NNRTI) или его фармацевтически приемлемое производное вместе с фармацевтически приемлемыми наполнителями. Согласно следующим аспектам данное изобретение предусматривает способ получения фармацевтической композиции, включающий(i) смешивание активных ингредиентов, выбранных из ламивудина, зидовудина, или их фармацевтически приемлемых производных, или их смесей, с гидрофильными полимерами, выбранными из эфиров целлюлозы, полиуроновых кислот, фармацевтически приемлемых смол или их смесей, и с фармацевтически приемлемой солью кальция, в составе управляемого высвобождения необязательно предусмотрены разбавитель и смазочная добавка,(ii) получение состава немедленного высвобождения по меньшей мере из одного NNRTI или их фармацевтически приемлемых производных, смешанных с фармацевтически приемлемыми наполните-2 008944 лями, и(iii) получение композиции прессованием образованных смесей в двухслойные таблетки или нанесением упомянутого состава немедленного высвобождения как внешнего покрытия на ядро упомянутого состава управляемого высвобождения. Детальное описание данного изобретения Фармацевтическая композиция находится предпочтительно в форме двухслойной таблетки с управляемым высвобождением одного слоя и с немедленным высвобождением второго слоя. Альтернативно компонент управляемого высвобождения может быть в форме ядра, а второй слой немедленного высвобождения может покрывать ядро сверху. Слой управляемого высвобождения фармацевтической композиции включает ламивудин и зидовудин или их фармацевтически приемлемые производные вместе со смесью гидрофильных полимеров, выбранных из группы, включающей эфиры целлюлозы, полиуроновые кислоты, фармацевтически приемлемые смолы или их смеси. К тому же, этот слой также включает фармацевтически приемлемую соль кальция и, необязательно,один или несколько растворимых в воде или диспергируемых в воде фармацевтически приемлемых наполнителей. Эфир целлюлозы, применяемый по данному изобретению, выбран из широко известных в данной области, таких как гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза, натрия карбоксиметилцеллюлоза, этилцеллюлоза, метилцеллюлоза, гидроксиэтилцеллюлоза и т.п. Он присутствует в количестве от около 2 до около 12 вес.% слоя управляемого высвобождения и предпочтительно в количестве от около 3 до около 8 вес.% слоя управляемого высвобождения. Полиуроновая кислота, применяемая по данному изобретению, выбрана из альгиновой кислоты,альгината натрия, альгината кальция, альгината натрия кальция, альгината калия, альгината аммония,альгината магния и т.п. Она присутствует в количестве от около 0,5 до около 10 вес.% слоя управляемого высвобождения и предпочтительно в количестве от около 1 до около 6 вес.% слоя управляемого высвобождения. Фармацевтически приемлемая смола, применяемая по данному изобретению, выбрана из широко известных в данной области, таких как гуаровая смола, ксантановая смола, смола карайя, трагакантовая смола, акациевая смола и т.п. Она присутствует в количестве от около 0,1 до около 10 вес.% слоя управляемого высвобождения и предпочтительно в количестве от около 0,5 до около 6 вес.% слоя управляемого высвобождения. Соли кальция, применяемые вместе с определенными полимерами, особенно альгинаты, как известно, стабилизируют матрицу. В связи с этим, в предпочтительном варианте осуществления упомянутый слой управляемого высвобождения композиции также содержит фармацевтически приемлемую соль кальция. Соль кальция выбрана из группы, включающей сульфат кальция, фосфат кальция, карбонат кальция и хлорид кальция. Она присутствует в количестве от около 0,1 до около 2,5 вес.% слоя управляемого высвобождения, предпочтительно от около 0,1 до около 2 вес.% слоя управляемого высвобождения. Слой управляемого высвобождения композиции может дополнительно содержать один или несколько других фармацевтически приемлемых наполнителей, выбранных из растворимых в воде и/или диспергируемых в воде разбавителей и смазочных добавок. Диспергируемый в воде или растворимый в воде разбавитель выбран из микрокристаллической целлюлозы, дикальциевой кислой соли фосфорной кислоты, карбоната кальция, лактозы, порошкообразной целлюлозы, крахмала, маннита и т.п. Они присутствуют в количестве от около 1 до около 28 вес.% слоя управляемого высвобождения. Если разбавитель - микрокристаллическая целлюлоза, он присутствует в количестве от около 5 до около 20 вес.% слоя управляемого высвобождения. Если разбавитель - дикальциевая кислая соль фосфорной кислоты, он присутствует в количестве от около 1 до около 5 вес.% слоя управляемого высвобождения. Слой немедленного высвобождения включает по меньшей мере один NNRTI, выбранный из невирапина и эфавиренса или их фармацевтически приемлемых производных. Слой немедленного высвобождения может дополнительно включать фармацевтически приемлемые наполнители, выбранные из группы, включающей разбавители, связывающие вещества, дезинтеграторы,смазочные добавки, красители и т.п. Разбавитель выбран из микрокристаллической целлюлозы, дикальциевой кислой соли фосфорной кислоты, карбоната кальция, лактозы, порошкообразной целлюлозы, крахмала, маннита и т.п. Разбавитель присутствует в количестве от около 2 до около 15 вес.% слоя немедленного высвобождения. Связывающее вещество выбрано из натрия карбоксиметилцеллюлозы, повидона, прежелатинизированного крахмала, желатина и т.п. Связывающее вещество присутствует в количестве от около 1 до около 10 вес.% слоя немедленного высвобождения. Дезинтегратор выбран из кросповидона, натрия крахмалгликолята, прежелатинизированного крахмала, натрия карбоксиметилцеллюлозы, натрия кроскармелозы, крахмала и т.п. Он присутствует в коли-3 008944 честве от около 0,5 до около 15 вес.% слоя немедленного высвобождения. Каждый слой может также содержать смазочные добавки, выбранные из широко известных в данной области, таких как стеарат магния, стеарат кальция, стеариновая кислота, диоксид кремния, тальк и т.п. Добавка присутствует в количестве от около 0,1 до около 3 вес.% каждого слоя. Фармацевтические композиции по данному изобретению можно изготовить способами, широко известными специалистам в данной области. Согласно приемлемому способу получения гранулированной смеси для каждого слоя все активные ингредиенты смешали вместе с необходимыми наполнителями и затем уплотнили. Уплотненную массу затем измельчили для получения гранул. Альтернативно, гранулы можно также получить способом влажной грануляции с использованием приемлемого гранулирующего агента. Окончательную гранулированную смесь двух слоев либо прессуют в двухслойные таблетки на прессовальной машине, приемлемой для этой цели, либо слой управляемого высвобождения может являться ядром, а слой немедленного высвобождения является покрытием поверх ядра. Таблетки, полученные таким образом, могут быть дополнительно покрыты с применением растворимого в воде полимера. Вышеупомянутый способ дает фармацевтическую композицию, которая содержит три антиретровирусных агента в одной таблетке, приемлемой для однократного суточного введения. Эффективная терапевтическая доза, которую можно вводить, включает комбинацию 300 мг ламивудина, 600 мг зидовудина и 400 мг невирапина/ 600 мг эфавиренса. Композиция данного изобретения и ее преимущества подробно объясняются не ограничивающими примерами. Пример 1. Смесь слоя управляемого высвобождения: ламивудин, зидовудин, гидрофильные полимеры, сульфат кальция, дикальциевая кислая соль фосфорной кислоты и микрокристаллическую целлюлозу просеяли сквозь сито с 30 отверстиями на один дюйм и смешали со стеаратом магния. Смесь уплотнили, а полученные куски измельчили до образования гранул. Гранулы определенного размера смешали с тонкой фракцией и ввели смазочную добавку. Смесь слоя немедленного высвобождения: невирапин, целлюлозу, повидон и первую порцию натрия крахмалгликолята просеяли сквозь сито с 40 отверстиями на один дюйм и смешали со стеаратом магния. Смесь уплотнили и полученные куски измельчили до образования гранул. Гранулы смешали со второй порцией натрия крахмалгликолята, коллоидным диоксидом кремния и ввели смазочную добавку. Двухслойные таблетки: обе вышеупомянутые смеси прессовали в двухслойные таблетки с помощью прессовальной машины для двухслойных таблеток. Высвобождение лекарственного препарата: таблетки проанализировали на высвобождение всех-4 008944 трех активных ингредиентов с помощью аппарата для изучения растворения Фармакопеи США (USP) тип 1 при 100 об./мин и с 900 мл 0,1 н. НСl для первых 2 ч, а затем с фосфатным буфером (рН 6,8). Соблюдали методику изготовления по примеру 1. Получили следующее высвобождение лекарственных препаратов: Соблюдали методику изготовления по примеру 1. Получили следующее высвобождение лекарственных препаратов: Ядро: ламивудин, зидовудин, гидрофильные полимеры, сульфат кальция, дикальциевая кислая соль фосфорной кислоты и микрокристаллическую целлюлозу просеяли сквозь сито с 30 отверстиями на один дюйм и смешали со стеаратом магния. Смесь уплотнили, а полученные куски измельчили до образования гранул. Гранулы определенного размера смешали с тонкой фракцией, ввели смазочную добавку и прессовали в таблетки. Покрытие: невирапин, целлюлозу, повидон и первую порцию натрия крахмалгликолята просеяли сквозь сито с 40 отверстиями на один дюйм и смешали со стеаратом магния. Смесь уплотнили, а полученные куски измельчили до образования гранул. Гранулы смешали со второй порцией натрия крахмалгликолята, коллоидным диоксидом кремния, ввели смазочную добавку и нанесли прессованием на ядро таблетки. Получили следующее высвобождение лекарственных препаратов: Изучение применения одиночной дозы проводили с использованием таблеток по примеру 1 по сравнению с коммерчески доступной комбинацией немедленного высвобождения трех лекарственных препаратов. Результаты исследования помещены в следующей таблице.AUC - величина площади под кривой "концентрация-время",ER -длительное высвобождение,OD - один раз в день,IR - немедленное высвобождение,BD - два раза в день. Результаты показывают, что композиция по данному изобретению достигает Сmах ламивудина и зидовудина, которая эквивалентна полученной, если вводят лекарственные препараты в форме немедленного высвобождения. Однако данному изобретению также удается увеличить значение AUC0-t и периоды полувыведения всех лекарственных препаратов in vivo. Из приведенного выше очевидно, что фармацевтическая композиция по данному изобретению служит антиретровирусной комбинацией из трех лекарственных препаратов для однократной суточной дозировки комбинации лечения особенно NRTI и NNRTI. Однократная суточная дозированная форма по данному изобретению простая, экономически эффективная, служит снижению лекарственной нагрузки и частоты введения и способствует соблюдению пациентом необходимого режима приема лекарственного препарата для эффективного лечения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Антиретровирусная фармацевтическая композиция, включающая селективную комбинациюi. Состава управляемого высвобождения, включающего: а) ламивудин или его фармацевтически приемлемое производное,b) зидовудин или его фармацевтически приемлемое производное,с) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, иd) фармацевтически приемлемую соль кальция;ii. Состава немедленного высвобождения, включающего по меньшей мере один селективный лекарственный препарат ненуклеозидных ингибиторов обратной транскриптазы (NNRTI) или его фармацевтически приемлемое производное вместе с фармацевтически приемлемыми наполнителями. 2. Антиретровирусная фармацевтическая композиция по п.1, где упомянутый лекарственный препарат NNRTI выбран из невирапина и эфавиренса. 3. Антиретровирусная фармацевтическая композиция по п.1, которая находится в форме двух отдельных слоев упомянутых состава управляемого высвобождения и состава немедленного высвобождения. 4. Антиретровирусная фармацевтическая композиция по п.1, которая находится в такой форме, что ядро представляет собой упомянутый состав управляемого высвобождения, а внешнее покрытие представляет собой состав немедленного высвобождения. 5. Антиретровирусная фармацевтическая композиция по п.1, включающая двухслойную селективную комбинациюi. Первого слоя состава управляемого высвобождения, включающего: а) ламивудин или его фармацевтически приемлемое производное,b) зидовудин или его фармацевтически приемлемое производное,с) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, иd) фармацевтически приемлемую соль кальция;ii. Второго слоя состава немедленного высвобождения, где упомянутый NNRTI является невирапином или его фармацевтически приемлемым производным вместе с фармацевтически приемлемыми наполнителями. 6. Антиретровирусная фармацевтическая композиция по п.1, включающая селективную комбина-8 008944 циюi. Ядра, которое содержит состав управляемого высвобождения, включающий: а) ламивудин или его фармацевтически приемлемое производное,b) зидовудин или его фармацевтически приемлемое производное,с) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, иd) фармацевтически приемлемую соль кальция;ii. Внешнего покрытия состава немедленного высвобождения, где упомянутый NNRTI является невирапином или его фармацевтически приемлемым производным вместе с фармацевтически приемлемыми наполнителями. 7. Антиретровирусная фармацевтическая композиция по п.1, включающая селективную двухслойную комбинациюi. Первого слоя состава управляемого высвобождения, включающего: а) ламивудин или его фармацевтически приемлемое производное,b) зидовудин или его фармацевтически приемлемое производное,с) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, иd) фармацевтически приемлемую соль кальция;ii. Второго слоя состава немедленного высвобождения, где упомянутый NNRTI является эфавиренсом или его фармацевтически приемлемым производным вместе с фармацевтически приемлемыми наполнителями. 8. Антиретровирусная фармацевтическая композиция по п.1, включающая селективную комбинациюi. Ядра состава управляемого высвобождения, включающего: а) ламивудин или его фармацевтически приемлемое производное,b) зидовудин или его фармацевтически приемлемое производное,с) смесь гидрофильных полимеров, причем упомянутые полимеры выбраны из группы, включающей эфиры целлюлозы, полиуроновые кислоты и фармацевтически приемлемые смолы или их смеси, иd) фармацевтически приемлемую соль кальция;ii. Внешнего покрытия состава немедленного высвобождения, где упомянутый NNRTI является эфавиренсом или его фармацевтически приемлемым производным вместе с фармацевтически приемлемыми наполнителями. 9. Композиция по любому из пп.1-8, где количество ламивудина или его фармацевтически приемлемого производного составляет от около 50 до около 500 мг. 10. Композиция по п.9, где количество ламивудина или его фармацевтически приемлемого производного составляет около 300 мг. 11. Композиция по любому из пп.1-8, где количество зидовудина или его фармацевтически приемлемого производного составляет от около 100 до около 1000 мг. 12. Композиция по п.11, где количество зидовудина или его фармацевтически приемлемого производного составляет 600 мг. 13. Композиция по любому из пп.1-12, где количество невирапина/эфавиренса или его фармацевтически приемлемого производного составляет от около 100 до около 1000 мг. 14. Композиция по п.13, где количество невирапина или его фармацевтически приемлемого производного составляет около 400 мг. 15. Композиция по п.13, где количество эфавиренса или его фармацевтически приемлемого производного составляет около 600 мг. 16. Композиция по любому из пп.1-15, где эфир целлюлозы выбран из гидроксипропилцеллюлозы,гидроксипропилметилцеллюлозы, карбоксиметилцеллюлозы, натрия карбоксиметилцеллюлозы, этилцеллюлозы, метилцеллюлозы, гидроксиэтилцеллюлозы. 17. Композиция по п.16, где эфир целлюлозы является гидроксипропилметилцеллюлозой и присутствует в количестве от около 2 до около 12 вес.% состава управляемого высвобождения. 18. Композиция по п.17, где эфир целлюлозы является гидроксипропилметилцеллюлозой и присутствует в количестве от около 3 до около 8 вес.% состава управляемого высвобождения. 19. Композиция по любому из пп.1-18, где полиуроновая кислота выбрана из альгиновой кислоты,альгината натрия, альгината кальция, альгината натрия-кальция, альгината калия, альгината аммония,альгината магния. 20. Композиция по п.19, где полиуроновая кислота является альгинатом натрия и присутствует в количестве от около 0,5 до около 10 вес.% состава управляемого высвобождения. 21. Композиция по п.20, где полиуроновая кислота является альгинатом натрия и присутствует в количестве от около 1 до около 6 вес.% состава управляемого высвобождения. 22. Композиция по любому из пп.1-21, где фармацевтически приемлемая смола выбрана из гуаровой смолы, ксантановой смолы, смолы карайя, трагакантовой смолы, акациевой смолы.-9 008944 23. Композиция по п.22, где фармацевтически приемлемая смола является гуаровой смолой и присутствует в количестве от около 0,1 до около 10 вес.% состава управляемого высвобождения. 24. Композиция по п.23, где фармацевтически приемлемая смола является гуаровой смолой и присутствует в количестве от около 0,5 до около 6 вес.% состава управляемого высвобождения. 25. Композиция по любому из пп.1-24, где фармацевтически приемлемая соль кальция выбрана из группы, включающей сульфат кальция, фосфат кальция, карбонат кальция и хлорид кальция. 26. Композиция по п.25, где фармацевтически приемлемая соль кальция является сульфатом кальция и присутствует в количестве от около 0,1 до около 2,5 вес.% состава управляемого высвобождения. 27. Композиция по п.26, где фармацевтически приемлемая соль кальция является сульфатом кальция и присутствует в количестве от около 0,1 до около 2 вес.% состава управляемого высвобождения. 28. Композиция по любому из пп.1-27, где состав управляемого высвобождения дополнительно содержит по меньшей мере один разбавитель, способный диспергироваться в воде, или растворимый в воде разбавитель, выбранный из микрокристаллической целлюлозы, дикальциевую кислую соль фосфорной кислоты, карбоната кальция, лактозы, порошкообразной целлюлозы, крахмала, маннита. 29. Композиция по п.28, где разбавитель присутствует в количестве от около 1 до около 28 вес.% состава управляемого высвобождения. 30. Композиция по п.29, где разбавитель является микрокристаллической целлюлозой. 31. Композиция по п.30, где количество микрокристаллической целлюлозы составляет от около 5 до около 20 вес.%. 32. Композиция по п.29, где разбавитель является дикальциевой кислой солью фосфорной кислоты. 33. Композиция по п.32, где количество дикальциевой кислой соли фосфорной кислоты составляет от около 1 до около 5 вес.%. 34. Композиция по любому из пп.1-33, где состав управляемого высвобождения дополнительно содержит по меньшей мере одну смазочную добавку, выбранную из стеарата магния, стеарата кальция,стеариновой кислоты, диоксида кремния, талька. 35. Композиция по п.34, где смазочная добавка присутствует в количестве от около 0,1 до 3 вес.%. 36. Композиция по любому из пп.1-35, где состав немедленного высвобождения включает от около 10 до около 95 вес.% невирапина или его фармацевтически приемлемого производного вместе с одним или несколькими фармацевтически приемлемыми наполнителями, выбранными из разбавителей, связывающих агентов, дезинтеграторов, смазочных добавок, красителей. 37. Композиция по п.36, где разбавитель выбран из микрокристаллической целлюлозы, дикальциевой кислой соли фосфорной кислоты, карбоната кальция, лактозы, порошкообразной целлюлозы, крахмала, маннита. 38. Композиция по п.37, где разбавитель является порошкообразной целлюлозой и присутствует в количестве от около 2 до около 15 вес.% состава немедленного высвобождения. 39. Композиция по п.36, где связывающий агент выбран из натрия карбоксиметилцеллюлозы, повидона, прежелатинизированного крахмала, желатина или их смесей. 40. Композиция по п.39, где связывающий агент присутствует в количестве от около 1 до около 10 вес.% состава немедленного высвобождения. 41. Композиция по п.36, где дезинтегратор выбран из кросповидона, натрия крахмалгликолята,прежелатинизированного крахмала, натрия карбоксиметилцеллюлозы, натрия кроскармелозы, крахмала и их смесей. 42. Композиция по п.41, где дезинтегратор присутствует в количестве от около 0,5 до около 15 вес.% состава немедленного высвобождения. 43. Композиция по п.36, где смазочная добавка выбрана из стеарата магния, стеарата кальция, стеариновой кислоты, диоксида кремния, талька. 44. Композиция по п.43, где смазочная добавка присутствует в количестве от около 0,1 до 3 вес.%. 45. Способ получения антиретровирусной фармацевтической композиции, который включает следующие этапы:(i) получают состав управляемого высвобождения перемешиванием вместе активных ингредиентов,выбранных из ламивудина, зидовудина или их смесей, с гидрофильными полимерами, выбранными из эфиров целлюлозы, полиуроновых кислот, фармацевтически приемлемых смол или их смесей, и с фармацевтически приемлемой солью кальция, необязательно, с разбавителем и смазочной добавкой,(ii) получают состав немедленного высвобождения, по меньшей мере, смешиванием NNRTI с фармацевтически приемлемыми наполнителями и(iii) получают из них композицию прессованием образованных смесей в двухслойные таблетки. 46. Способ получения антиретровирусной фармацевтической композиции, который включает следующие этапы:(i) получают ядро упомянутого состава управляемого высвобождения перемешиванием вместе активных ингредиентов, выбранных из ламивудина, зидовудина или их смесей, с гидрофильными полимерами, выбранными из эфиров целлюлозы, полиуроновых кислот, фармацевтически приемлемых смол или их смесей, с фармацевтически приемлемой солью кальция, необязательно, с разбавителем и смазоч- 10008944 ной добавкой,(ii) получают внешнее покрытие состава немедленного высвобождения, по меньшей мере, изNNRTI, выбранного из невирапина и эфавиренса, смешанного с фармацевтически приемлемыми наполнителями, и(iii) получают из них композицию путем нанесения упомянутого внешнего покрытия на упомянутое ядро прессованием покрытия. 47. Способ по п.45 или 46, в котором каждую смесь гранулируют сухим способом перед прессованием. 48. Способ по п.45 или 46, в котором каждую смесь гранулируют влажным способом перед прессованием. 49. Способ снижения лекарственной нагрузки на пациента, страдающего инфекцией ВИЧ и/или синдромом приобретенного иммунного дефицита, при котором вводят антиретровирусную фармацевтическую композицию из трех лекарственных препаратов, которая включает комбинацию ламивудина и зидовудина в качестве компонента управляемого высвобождения и невирапина или эфавиренса в качестве компонента немедленного высвобождения. 50. Способ снижения лекарственной нагрузки на пациента, страдающего инфекцией ВИЧ и/или синдромом приобретенного иммунного дефицита, при котором вводят антиретровирусную фармацевтическую композицию из трех лекарственных препаратов, которая включает ламивудин и зидовудин в качестве компонент управляемого высвобождения и невирапин или эфавиренс в качестве компонент немедленного высвобождения, причем композиция после введения упомянутому пациенту обеспечивает Сmaх от около 1,2 до 2,0 мкг/мл для ламивудина, от около 1,0 до 2,0 мкг/мл для зидовудина и от около 4,5 до 5,5 мкг/мл для невирапина. 51. Способ снижения лекарственной нагрузки на пациента, страдающего инфекцией ВИЧ и/или синдромом приобретенного иммунного дефицита, при котором вводят антиретровирусную фармацевтическую композицию из трех лекарственных препаратов, которая включает ламивудин и зидовудин в качестве компонента управляемого высвобождения и невирапин или эфавиренс в качестве компонента немедленного высвобождения, причем композиция после введения упомянутому пациенту обеспечиваетAUC0-t от около 8 до 14 мкг, ч/мл для ламивудина, от около 5 до 9 мкг, ч/мл для зидовудина и от около 32 до 40 мкг, ч/мл для невирапина. 52. Способ увеличения in vivo периода полувыведения ламивудина и зидовудина без влияния на период полувыведения невирапина и, следовательно, снижения лекарственной нагрузки на пациента, страдающего инфекцией ВИЧ и/или синдромом приобретенного иммунного дефицита, при котором вводят антиретровирусную композицию из трех лекарственных препаратов, которая включает ламивудин и зидовудин как компонент управляемого высвобождения и невирапин или эфавиренс как компонент немедленного высвобождения. 53. Способ по п.51, где композиция после введения упомянутому пациенту обеспечивает t1/2 около 5 ч для ламивудина, около 2 ч для зидовудина и около 29 ч для невирапина. 54. Способ снижения лекарственной нагрузки на пациента, страдающего инфекцией ВИЧ и/или синдромом приобретенного иммунного дефицита, при котором вводят антиретровирусную фармацевтическую композицию из трех лекарственных препаратов, которая включает ламивудин и зидовудин в качестве компонента управляемого высвобождения и невирапин или эфавиренс в качестве компонента немедленного высвобождения, где композиция после введения упомянутому пациенту обеспечивает Сmах упомянутых лекарственных препаратов в компоненте управляемого высвобождения, которая является в значительной степени подобной той, что обеспечивается композициями немедленного высвобождения упомянутых лекарственных препаратов, при введении совместно, последовательно или одновременно.
МПК / Метки
МПК: A61K 9/20
Метки: получения, высвобождения, управляемого, способ, фармацевтическая, композиция
Код ссылки
<a href="https://eas.patents.su/12-8944-farmacevticheskaya-kompoziciya-upravlyaemogo-vysvobozhdeniya-i-sposob-ee-polucheniya.html" rel="bookmark" title="База патентов Евразийского Союза">Фармацевтическая композиция управляемого высвобождения и способ ее получения</a>
Предыдущий патент: Фунгицидные смеси для борьбы с фитопатогенными грибами, в частности с патогенами риса
Следующий патент: Пероральные композиции дезоксипеганина и их применение
Случайный патент: Калийная соль 5-[4-[2-(n-метил-n-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-диона и ее применение в качестве противодиабетического лекарственного средства