Способ обработки загрязнённой воды, основанный на использовании цеолитов
Номер патента: 10694
Опубликовано: 30.10.2008
Авторы: Виньола Родольфо, Систо Раффаэлло, Грилло Джованни, Бернарди Адриано
Формула / Реферат
1. Способ обработки воды, загрязненной винилхлоридом (ВХ), простым метил-третбутиловым эфиром (МТБЭ), нафталином, 2-метилнафталином, аценафтеном, фенантреном или их смесями, состоящий из обработки воды, загрязненной винилхлоридом (ВХ), простым метил-третбутиловым эфиром (МТБЭ), нафталином, 2-метилнафталином, аценафтеном, фенантреном или их смесями, одним или более аполярными цеолитами, характеризующимися соотношением оксид кремния/оксид алюминия >50 и наличием в структуре каналов, имеющих размеры, подобные размерам молекул загрязняющих соединений.
2. Способ по п.1, отличающийся тем, что обработку осуществляют по отношению к загрязненной подземной воде, при этом обработка состоит из пропускания воды через проницаемый реакционноспособный барьер (ПРБ), помещенный in situ перпендикулярно потоку подземной воды, причем реакционноспособная среда барьера состоит из указанных одного или более аполярных цеолитов.
3. Способ по п.1 или 2, где цеолит отличается наличием в структуре каналов, имеющих размеры в интервале от 4,5 до 7,5 Е.
4. Способ по п.3, где цеолит отличается наличием в структуре каналов, имеющих размеры в интервале от 5,0 до 7,0 Е.
5. Способ по п.1 или 2, где цеолит отличается соотношением оксид кремния/оксид алюминия > 200.
6. Способ по п.5, где цеолит состоит из силикалита или цеолита ZSM-5, или морденита.
7. Способ по п.1 или 2, где воду обрабатывают смесью цеолитов, указанных в п.1 и соответствующих типам загрязняющих веществ, присутствующих в самой воде.
Текст
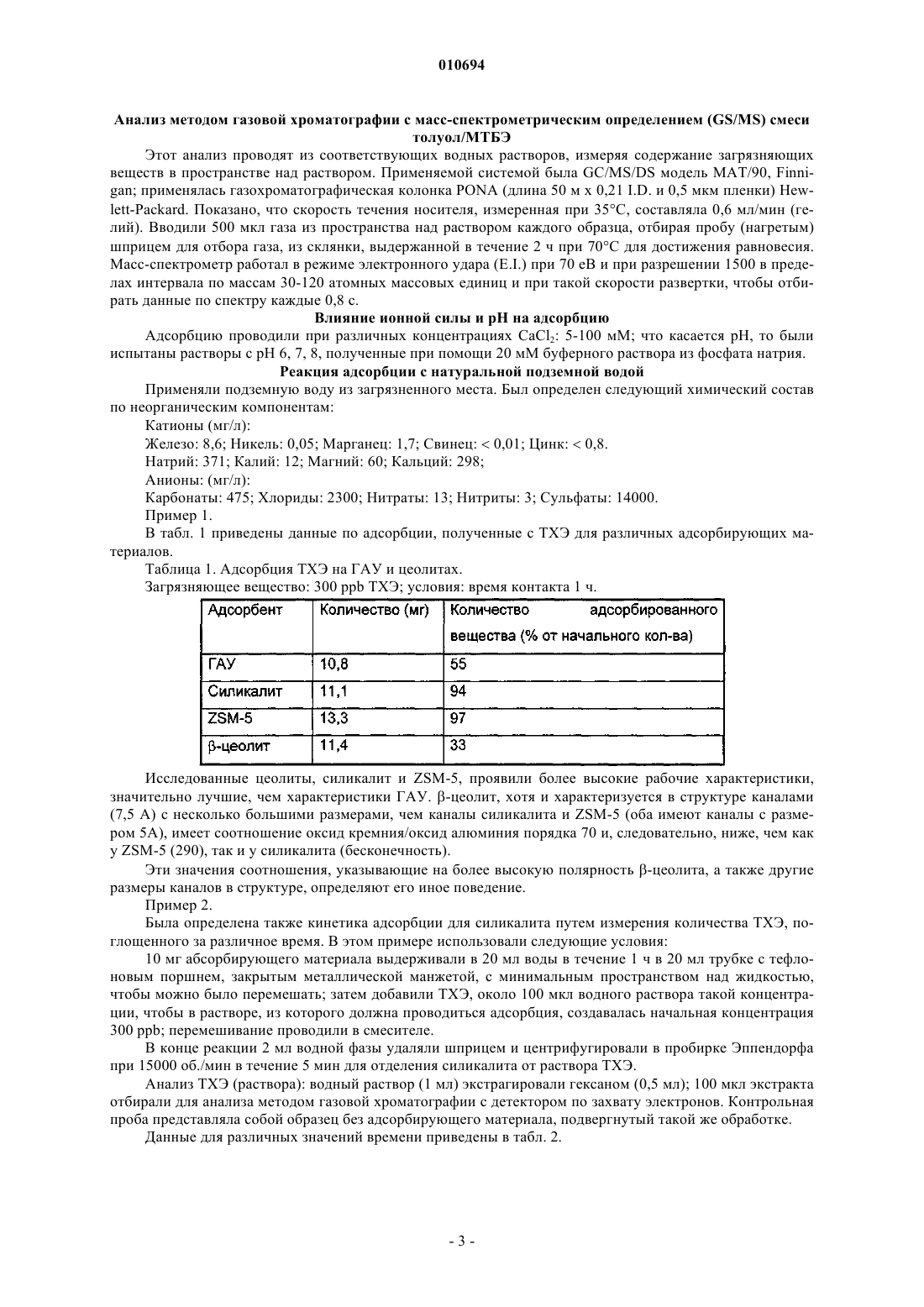
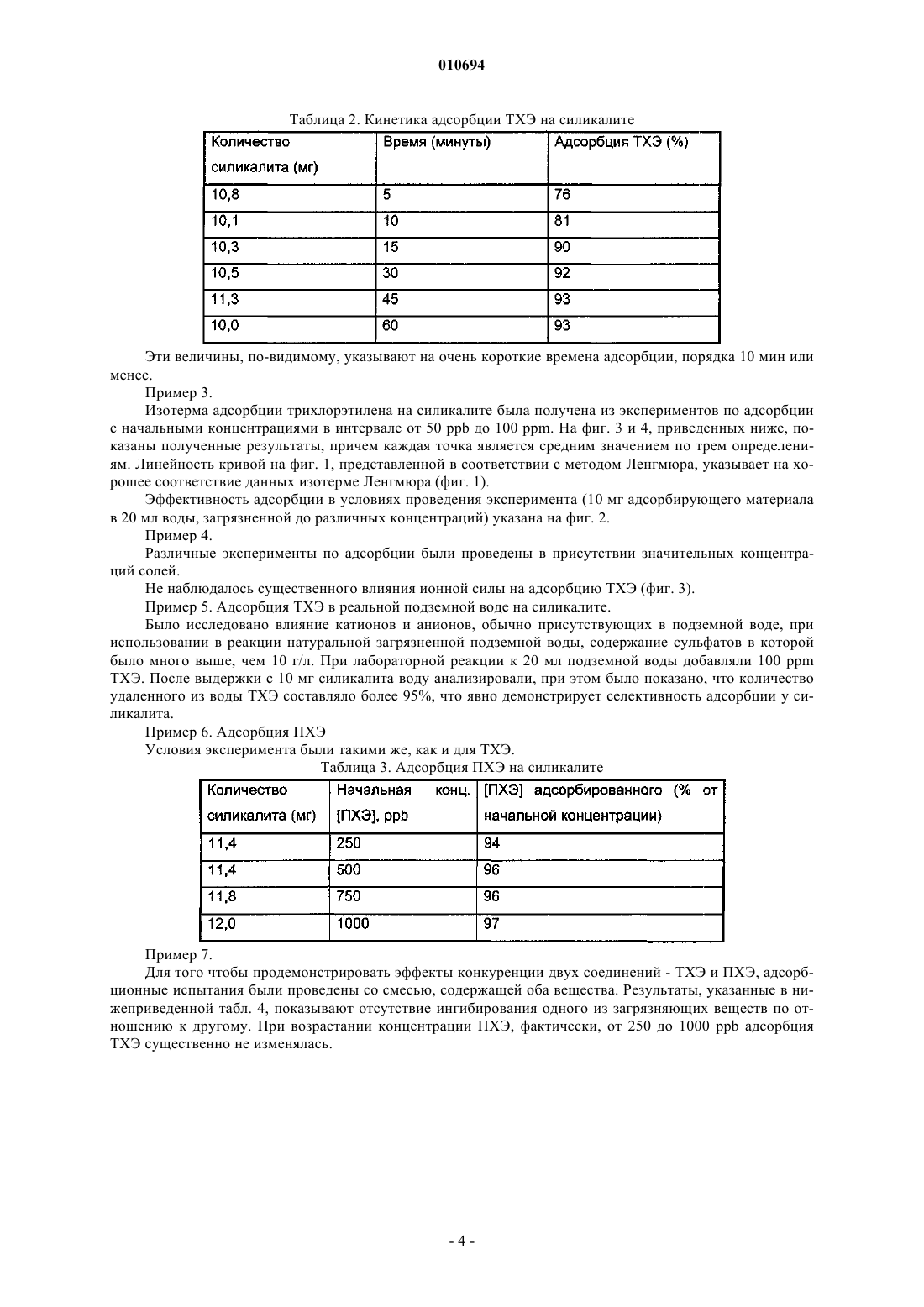
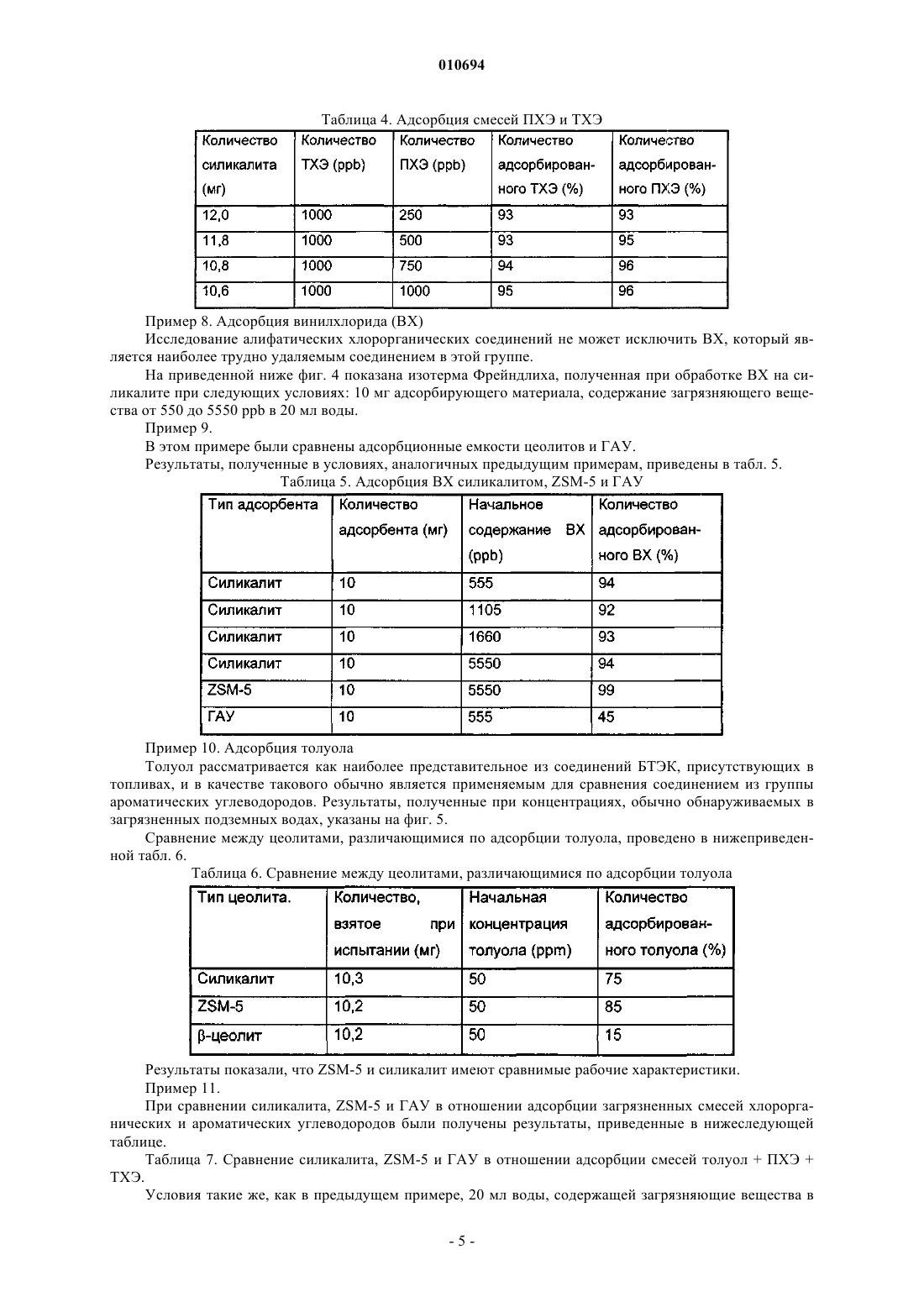
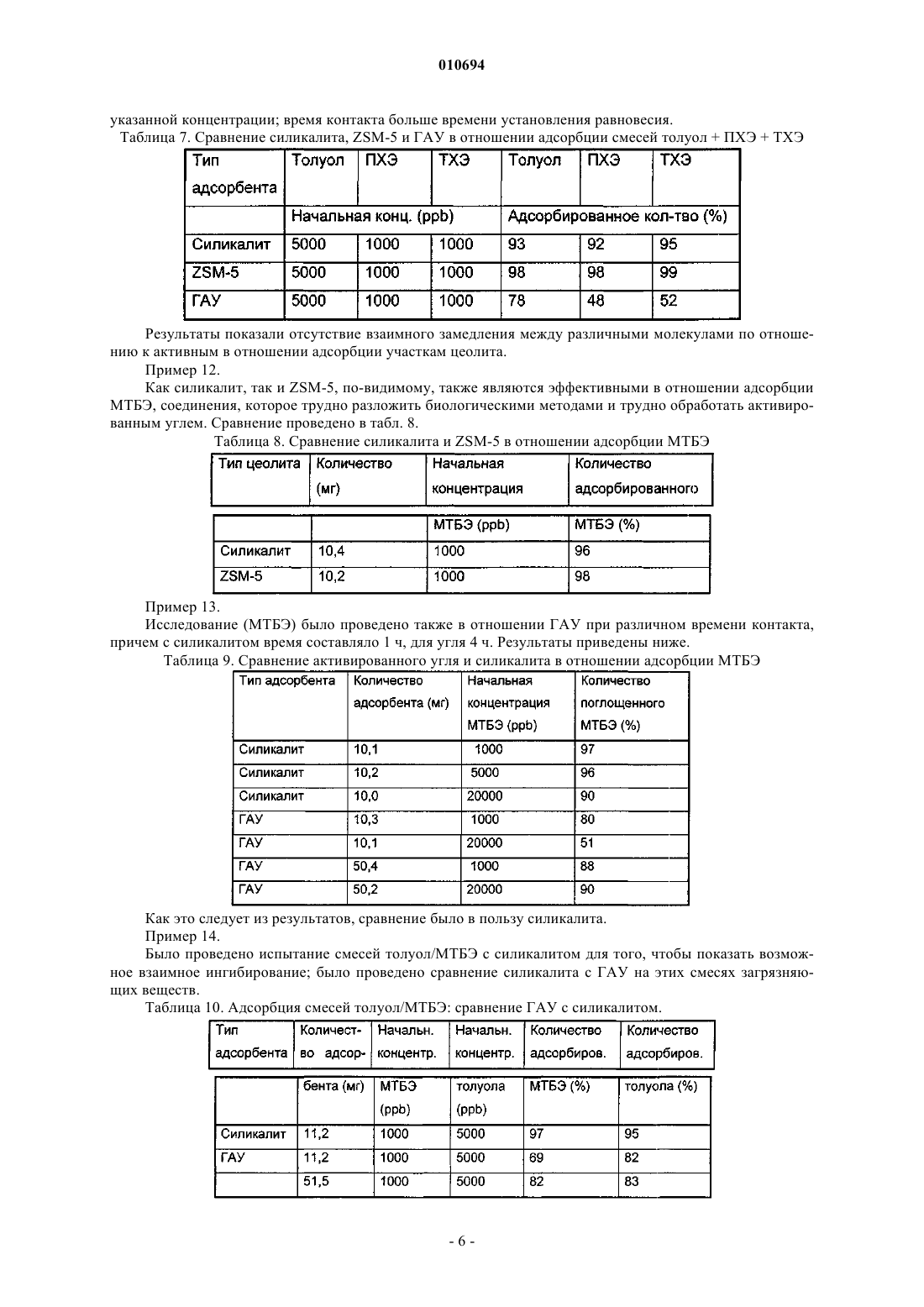
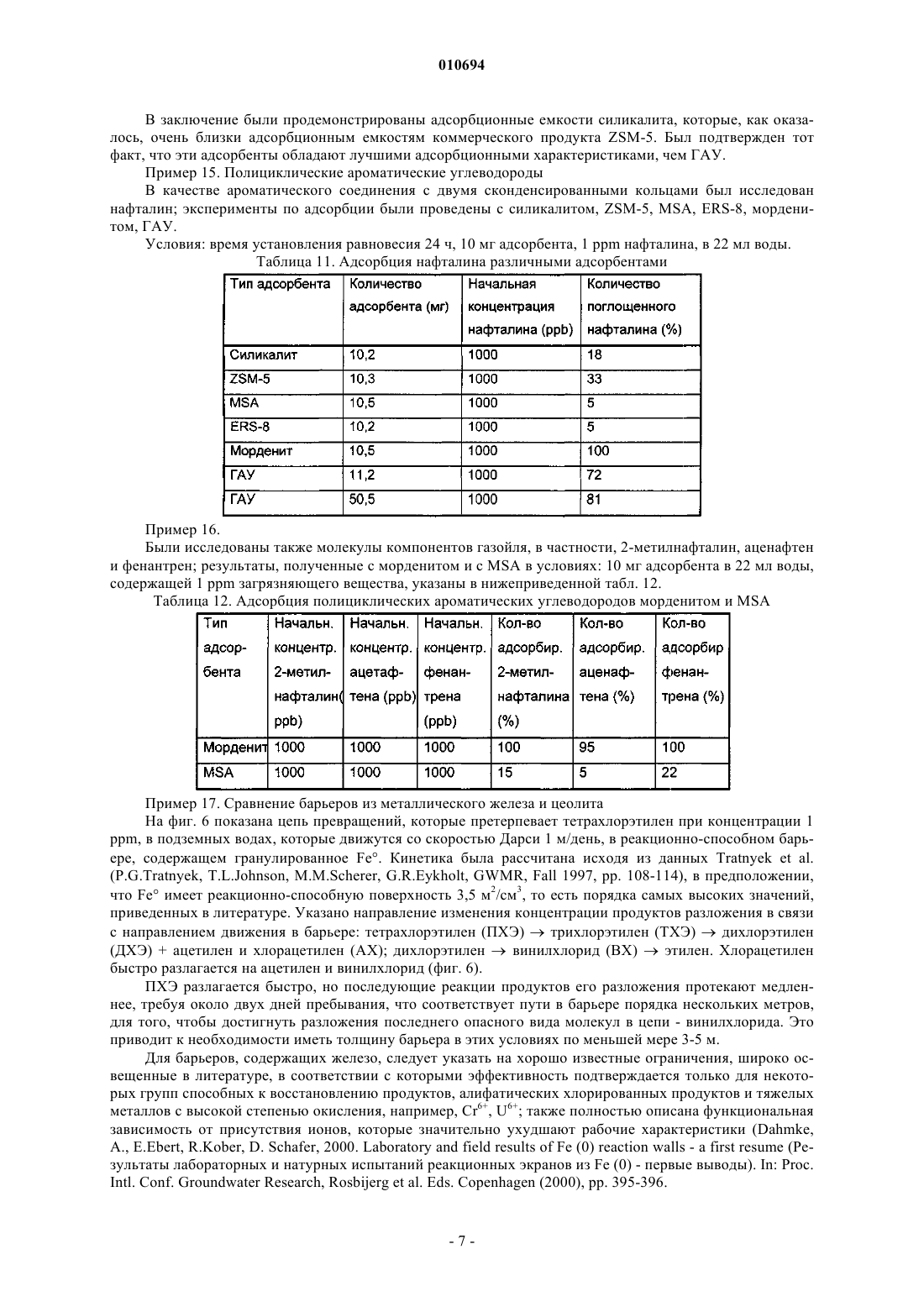
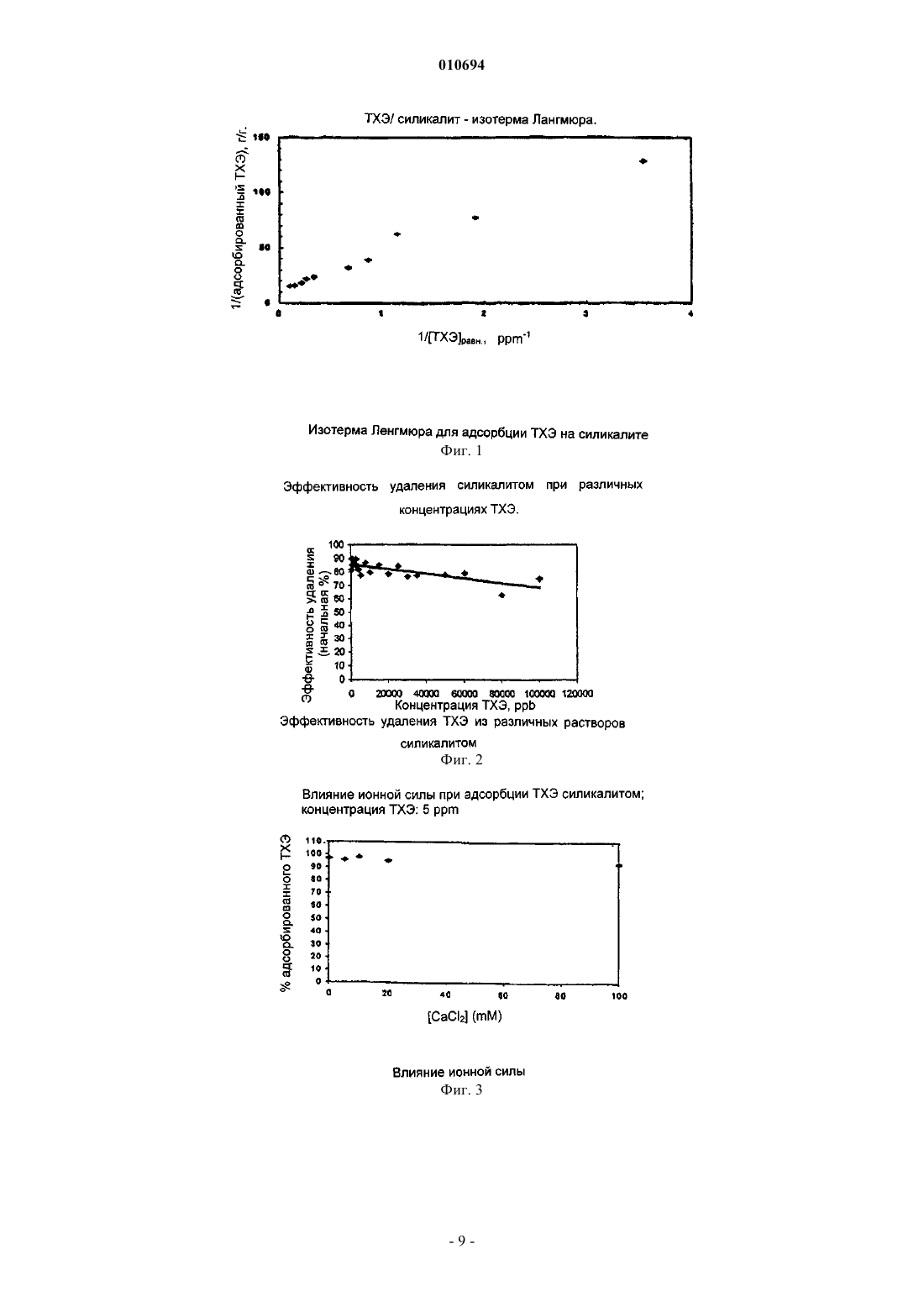
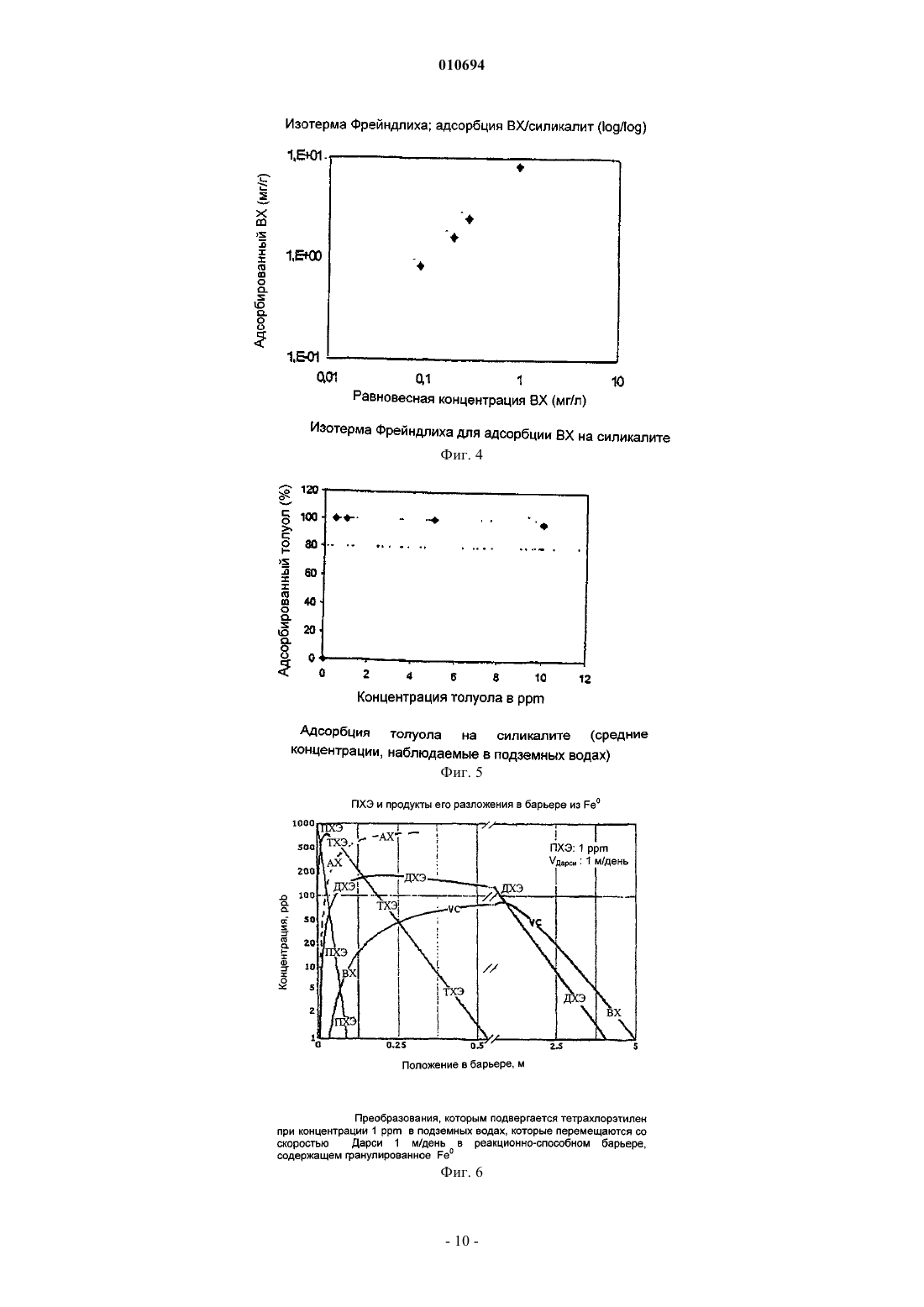
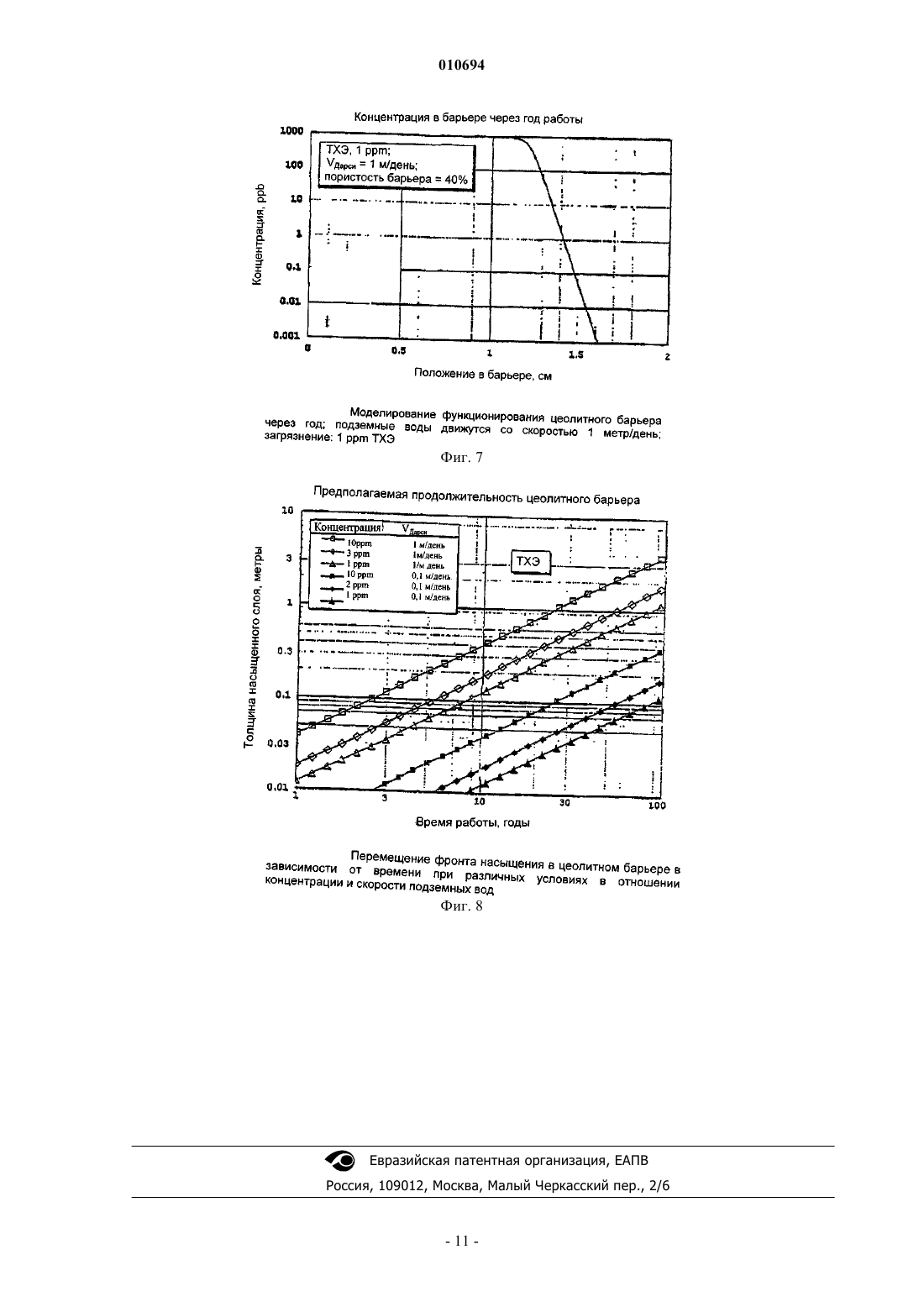
010694 Данное изобретение относится к способу обработки воды, загрязненной аполярными соединениями,основанному на использовании конкретных цеолитов. Более конкретно, данное изобретение относится к способу обработки воды, загрязненной аполярными соединениями, состоящими из галогенированных органических растворителей и ароматических углеводородов, который основан на использовании аполярных цеолитов, имеющих в структуре каналы с конкретными размерами. Способ по данному изобретению удобно применять для обработки загрязненных подземных вод при использовании проницаемого реакционно-способного барьера (ПРБ). Обычные ПРБ для очистки воды, загрязненной галогенированными растворителями, основаны на системах, применяющих металлическое железо и/или гранулированный активированный уголь (ГАУ). Первая система, работающая на основе восстановительной способности металла, активна только в отношении примесей, которые способны восстанавливаться, таких как хлорорганические продукты или металлы с высокой степенью окисления (US 5266213, WO 92/19556). Кроме того, при использовании железа с нулевой валентностью наблюдается снижение проницаемости барьера из-за образования налета или осадка минералов, которые образуются при реакциях между ионами окисленного металла и веществами, содержащимися в подземных водах. Вторая система представляет собой неспецифичный абсорбент, и как таковой он является не очень селективным по отношению к мешающим веществам, присутствующим в воде и, в частности, в подземных водах (ионы, гуминовые кислоты и т.д.). Если он применяется для производства проницаемых реакционно-способных барьеров, это, следовательно, вызывает истощение системы через короткий промежуток времени (Williamson, D. 2000. Construction of a funnel-and-gate treatment system for pesticide-contaminated groundwater. Chemical Oxidationand reactive barriers. (Конструкция системы обработки типа воронка-проход для подземных вод, загрязненных пестицидами. Химическое окисление и реакционно-способные барьеры.) Godage В. et al. Eds.In II Intl. Conf. on Remediation of chlorinated and recalcitrant compounds (Вторая Международная конференция по устранению хлорированных и трудно поддающихся обработке соединений). Monterey, ca,USA, Battelle press, Columbus (2000, p. 257-264.construction. In: Chemical Oxidation and reactive barriers (Система типа воронка-проход на давно построенном газовом заводе в Карлсруе, Германия: дизайн и конструкция. В: Химическое окисление и реакционно-способные барьеры). Godage В. et al. Eds., II Intl, Conf. on Remediation of chlorinated and recalcitrant compounds (Вторая Международная конференция по устранению хлорированных и трудно поддающихся обработке соединений). Monterey, CA, USA, Battelle Press, Columbus, (2000), 215-322. Однако было показано, что обе системы являются неэффективными при удалении всех основных загрязняющих веществ, которые часто одновременно присутствуют в загрязненных подземных водах под индустриальными зонами и которые часто представляют собой аполярные соединения, такие как галогенированные растворители и соединения, поступающие из нефтеперерабатывающей промышленности. Зачастую это продукты с высокой токсичностью, некоторые из которых имеют канцерогенную природу,концентрация которых в почвенных водах должна удовлетворять строгим ограничениям, установленным законом. Теперь найден способ обработки загрязненной воды, который позволяет удалять вышеупомянутые загрязняющие вещества эффективно и избирательно по отношению к минеральным солям, обычно растворенным в воде. Таким образом, предмет данного изобретения относится к способу обработки воды, загрязненной аполярными соединениями, который состоит в обработке такой воды одним или более аполярными цеолитами, которые характеризуются соотношением оксид кремния-оксид алюминия 50 и наличием в структуре каналов, размеры которых подобны размерам молекул загрязняющих соединений. Способ по данному изобретению является особенно эффективным при удалении загрязнений, состоящих из галогенированных растворителей, таких как четыреххлористый углерод, тетрахлорэтилен(ПХЭ), трихлорэтилен (ТХЭ), дихлорэтилен (ДХЭ), винилхлорид (ВХ) и алифатические и/или ароматические соединения, происходящие из нефтеперерабатывающей промышленности, например, простой метил-третбутиловый эфир (МТБЭ), БТЭК (бензол, толуол, этилбензол, ксилолы), нафталин, 2 метилнафталин, аценафтен, фенантрен. Способ по данному изобретению можно успешно применять для очистки подземных вод при использовании проницаемых реакционно-способных барьеров (ПРБ). В этом случае цеолит образует активную среду барьера, помещенного in situ перпендикулярно потоку подземной воды, который, при пересечении его столбом загрязненной воды, позволяет провести очистку путем иммобилизации загрязняющих частиц. Такие барьеры могут обработать подземные воды, загрязненные хлорированными растворителями,циклическими или полициклическими ароматическими углеводородами и соединениями, которые являются особенно устойчивыми как по отношению к биологическому разложению, так и к адсорбции, такими как, например, МТБЭ или винилхлорид (ВХ), с высокой селективностью по отношению к мешающим-1 010694 неорганическим продуктам. Винилхлорид рассматривается как загрязняющее вещество, которое трудно удалить. Действительно, он недостаточно задерживается активированным углем, и его разложение требует применения дополнительных структур, которые включают применение УФ-ламп. Присутствие МТБЭ в подземных водах также представляет собой проблему, которую трудно преодолеть и решение которой оправдывает применение относительно дорогих абсорбирующих материалов(Davis et al., J. Env. Eng., 126, p. 354, April 2000). Цеолиты, применяемые в способе по данному изобретению, характеризуются наличием в структуре каналов, имеющих размеры в интервале от 4,5 до 7,5 А. Предпочтительно применяют цеолиты, имеющие в структуре каналы с размерами в интервале от 5 до 7 А и соотношения оксид кремния/оксид алюминия 200, такие как,например, силикалит, цеолит ZSM-5, морденит. В результате их селективности, цеолиты имеют более высокие абсорбционную емкость и продолжительность работы, чем материалы, такие как активированный уголь, которые применяются в настоящее время в проницаемых реакционно-способных барьерах. Все это обусловлено свойствами такой реакционно-способной среды, которые основаны на размере каналов в структуре, соответственным образом откалиброванных для органических молекул, и на высокой аполярности, проистекающей из высоких соотношений оксид кремния/оксид алюминия, которая исключает любой тип взаимодействия с ионами или полярными соединениями. Таким образом, этот цеолит обладает селективным взаимодействием с молекулами аполярных загрязняющих веществ, в то время как он полностью исключает полярные ионы и молекулы, обычно присутствующие в почвенных водах совместно с гуминовыми веществами, имеющими более значительные размеры молекул, чем размеры каналов в его структуре. Кроме того, соответствующие смеси конкретных цеолитов позволяют одновременно удалять алифатические хлорорганические продукты, ароматические углеводороды, полиароматические углеводороды, характерные компоненты нефтепродуктов. Цеолит ZSM-5 и морденит с соотношением Si/Al200 являются материалами, известными как молекулярные сита или как носители для катализаторов, но их применение в качестве активных компонентов для производства ПРБ до сих пор не было описано в литературе. Цеолит ZSM-5 особенно пригоден для алифатических, галоген-алифатических и моноароматических молекул, таких как БТЭК и галогенированные производные бензола. С другой стороны, морденит применим для ароматических молекул с двумя или более ароматическими кольцами, замещенных галогеном или алкилом. Описание способов, применяемых для количественного определения свойств активных материалов Общая методика Материалы в количестве 10 мг, если не указано другое количество, выдерживают в 20 мл воды в трубке с тефлоновым поршнем, закрытым металлической манжетой, с минимальным пространством над раствором, чтобы обеспечить перемешивание; загрязняющее соединение (до 100 мкл водного раствора соответствующей концентрации) добавляют 100 мкл шприцем; осуществляют перемешивание в системе полного смешения (смеситель порошков). В конце реакции, через 24 ч, следовательно, через значительно большее время, чем время установления равновесия для каждого адсорбента, смесь центрифугируют в течение 15 мин при скорости вращения 700 об./мин для того, чтобы отделить адсорбирующийся материал, и определяют не адсорбировавшуюся примесь из ее остаточной концентрации в растворе. Каждое определение проводят, по меньшей мере, три раза. Для каждого определения в одинаковых условиях получают образец и контрольную пробу, состоящую из жидкости и загрязняющего вещества, без адсорбирующего материала. Этой процедуре следуют в случае всех исследуемых загрязняющих веществ. Определение времени достижения равновесия От 10 мг до 1 г адсорбирующего материала выдерживают с 20 мл воды, содержащей от 100 частей на миллиард (ppb) до 5 частей на миллион (ppm) загрязняющего вещества, при перемешивании при комнатной температуре в течение времени в интервале от 15 мин до 48 ч. Временем установления равновесия считается время, после достижения которого адсорбция не возрастает. При исследовании влияния условий на адсорбцию используется количество адсорбирующего материала, которое определяет адсорбцию, по меньшей мере, половины загрязняющего вещества, приведенного в контакт с ним. Анализ ТХЭ, ПХЭ, ВХ, толуола, МТБЭ, нафталина, 2-метилнафталина, аценафтена, фенантрена (раствор) Водный раствор экстрагируют гексаном в соотношении 5,666/1 (Н 2 О/гексан) в трубке, аналогичной реакционной трубке; миллилитр гексана отбирают для анализа методом газовой хроматографии с детектором по захвату электронов (GC-ECD) или методом газовой хроматографии с пламенно-ионизационным детектором (GC-FID). Контрольный образец представляет собой образец без адсорбирующего материала,который прошел такую же обработку.-2 010694 Анализ методом газовой хроматографии с масс-спектрометрическим определением (GS/MS) смеси толуол/МТБЭ Этот анализ проводят из соответствующих водных растворов, измеряя содержание загрязняющих веществ в пространстве над раствором. Применяемой системой была GC/MS/DS модель MAT/90, Finnigan; применялась газохроматографическая колонка PONA (длина 50 м х 0,21 I.D. и 0,5 мкм пленки) Hewlett-Packard. Показано, что скорость течения носителя, измеренная при 35 С, составляла 0,6 мл/мин (гелий). Вводили 500 мкл газа из пространства над раствором каждого образца, отбирая пробу (нагретым) шприцем для отбора газа, из склянки, выдержанной в течение 2 ч при 70 С для достижения равновесия. Масс-спектрометр работал в режиме электронного удара (E.I.) при 70 еВ и при разрешении 1500 в пределах интервала по массам 30-120 атомных массовых единиц и при такой скорости развертки, чтобы отбирать данные по спектру каждые 0,8 с. Влияние ионной силы и рН на адсорбцию Адсорбцию проводили при различных концентрациях CaCl2: 5-100 мМ; что касается рН, то были испытаны растворы с рН 6, 7, 8, полученные при помощи 20 мМ буферного раствора из фосфата натрия. Реакция адсорбции с натуральной подземной водой Применяли подземную воду из загрязненного места. Был определен следующий химический состав по неорганическим компонентам: Катионы (мг/л): Железо: 8,6; Никель: 0,05; Марганец: 1,7; Свинец:0,01; Цинк:0,8. Натрий: 371; Калий: 12; Магний: 60; Кальций: 298; Анионы: (мг/л): Карбонаты: 475; Хлориды: 2300; Нитраты: 13; Нитриты: 3; Сульфаты: 14000. Пример 1. В табл. 1 приведены данные по адсорбции, полученные с ТХЭ для различных адсорбирующих материалов. Таблица 1. Адсорбция ТХЭ на ГАУ и цеолитах. Загрязняющее вещество: 300 ppb ТХЭ; условия: время контакта 1 ч. Исследованные цеолиты, силикалит и ZSM-5, проявили более высокие рабочие характеристики,значительно лучшие, чем характеристики ГАУ. -цеолит, хотя и характеризуется в структуре каналами(7,5 А) с несколько большими размерами, чем каналы силикалита и ZSM-5 (оба имеют каналы с размером 5 А), имеет соотношение оксид кремния/оксид алюминия порядка 70 и, следовательно, ниже, чем как у ZSM-5 (290), так и у силикалита (бесконечность). Эти значения соотношения, указывающие на более высокую полярность -цеолита, а также другие размеры каналов в структуре, определяют его иное поведение. Пример 2. Была определена также кинетика адсорбции для силикалита путем измерения количества ТХЭ, поглощенного за различное время. В этом примере использовали следующие условия: 10 мг абсорбирующего материала выдерживали в 20 мл воды в течение 1 ч в 20 мл трубке с тефлоновым поршнем, закрытым металлической манжетой, с минимальным пространством над жидкостью,чтобы можно было перемешать; затем добавили ТХЭ, около 100 мкл водного раствора такой концентрации, чтобы в растворе, из которого должна проводиться адсорбция, создавалась начальная концентрация 300 ppb; перемешивание проводили в смесителе. В конце реакции 2 мл водной фазы удаляли шприцем и центрифугировали в пробирке Эппендорфа при 15000 об./мин в течение 5 мин для отделения силикалита от раствора ТХЭ. Анализ ТХЭ (раствора): водный раствор (1 мл) экстрагировали гексаном (0,5 мл); 100 мкл экстракта отбирали для анализа методом газовой хроматографии с детектором по захвату электронов. Контрольная проба представляла собой образец без адсорбирующего материала, подвергнутый такой же обработке. Данные для различных значений времени приведены в табл. 2.-3 010694 Таблица 2. Кинетика адсорбции ТХЭ на силикалите Эти величины, по-видимому, указывают на очень короткие времена адсорбции, порядка 10 мин или менее. Пример 3. Изотерма адсорбции трихлорэтилена на силикалите была получена из экспериментов по адсорбции с начальными концентрациями в интервале от 50 ppb до 100 ppm. На фиг. 3 и 4, приведенных ниже, показаны полученные результаты, причем каждая точка является средним значением по трем определениям. Линейность кривой на фиг. 1, представленной в соответствии с методом Ленгмюра, указывает на хорошее соответствие данных изотерме Ленгмюра (фиг. 1). Эффективность адсорбции в условиях проведения эксперимента (10 мг адсорбирующего материала в 20 мл воды, загрязненной до различных концентраций) указана на фиг. 2. Пример 4. Различные эксперименты по адсорбции были проведены в присутствии значительных концентраций солей. Не наблюдалось существенного влияния ионной силы на адсорбцию ТХЭ (фиг. 3). Пример 5. Адсорбция ТХЭ в реальной подземной воде на силикалите. Было исследовано влияние катионов и анионов, обычно присутствующих в подземной воде, при использовании в реакции натуральной загрязненной подземной воды, содержание сульфатов в которой было много выше, чем 10 г/л. При лабораторной реакции к 20 мл подземной воды добавляли 100 ppm ТХЭ. После выдержки с 10 мг силикалита воду анализировали, при этом было показано, что количество удаленного из воды ТХЭ составляло более 95%, что явно демонстрирует селективность адсорбции у силикалита. Пример 6. Адсорбция ПХЭ Условия эксперимента были такими же, как и для ТХЭ. Таблица 3. Адсорбция ПХЭ на силикалите Пример 7. Для того чтобы продемонстрировать эффекты конкуренции двух соединений - ТХЭ и ПХЭ, адсорбционные испытания были проведены со смесью, содержащей оба вещества. Результаты, указанные в нижеприведенной табл. 4, показывают отсутствие ингибирования одного из загрязняющих веществ по отношению к другому. При возрастании концентрации ПХЭ, фактически, от 250 до 1000 ppb адсорбция ТХЭ существенно не изменялась.-4 010694 Таблица 4. Адсорбция смесей ПХЭ и ТХЭ Пример 8. Адсорбция винилхлорида (ВХ) Исследование алифатических хлорорганических соединений не может исключить ВХ, который является наиболее трудно удаляемым соединением в этой группе. На приведенной ниже фиг. 4 показана изотерма Фрейндлиха, полученная при обработке ВХ на силикалите при следующих условиях: 10 мг адсорбирующего материала, содержание загрязняющего вещества от 550 до 5550 ppb в 20 мл воды. Пример 9. В этом примере были сравнены адсорбционные емкости цеолитов и ГАУ. Результаты, полученные в условиях, аналогичных предыдущим примерам, приведены в табл. 5. Таблица 5. Адсорбция ВХ силикалитом, ZSM-5 и ГАУ Пример 10. Адсорбция толуола Толуол рассматривается как наиболее представительное из соединений БТЭК, присутствующих в топливах, и в качестве такового обычно является применяемым для сравнения соединением из группы ароматических углеводородов. Результаты, полученные при концентрациях, обычно обнаруживаемых в загрязненных подземных водах, указаны на фиг. 5. Сравнение между цеолитами, различающимися по адсорбции толуола, проведено в нижеприведенной табл. 6. Таблица 6. Сравнение между цеолитами, различающимися по адсорбции толуола Результаты показали, что ZSM-5 и силикалит имеют сравнимые рабочие характеристики. Пример 11. При сравнении силикалита, ZSM-5 и ГАУ в отношении адсорбции загрязненных смесей хлорорганических и ароматических углеводородов были получены результаты, приведенные в нижеследующей таблице. Таблица 7. Сравнение силикалита, ZSM-5 и ГАУ в отношении адсорбции смесей толуол + ПХЭ + ТХЭ. Условия такие же, как в предыдущем примере, 20 мл воды, содержащей загрязняющие вещества в-5 010694 указанной концентрации; время контакта больше времени установления равновесия. Таблица 7. Сравнение силикалита, ZSM-5 и ГАУ в отношении адсорбции смесей толуол + ПХЭ + ТХЭ Результаты показали отсутствие взаимного замедления между различными молекулами по отношению к активным в отношении адсорбции участкам цеолита. Пример 12. Как силикалит, так и ZSM-5, по-видимому, также являются эффективными в отношении адсорбции МТБЭ, соединения, которое трудно разложить биологическими методами и трудно обработать активированным углем. Сравнение проведено в табл. 8. Таблица 8. Сравнение силикалита и ZSM-5 в отношении адсорбции МТБЭ Пример 13. Исследование (МТБЭ) было проведено также в отношении ГАУ при различном времени контакта,причем с силикалитом время составляло 1 ч, для угля 4 ч. Результаты приведены ниже. Таблица 9. Сравнение активированного угля и силикалита в отношении адсорбции МТБЭ Как это следует из результатов, сравнение было в пользу силикалита. Пример 14. Было проведено испытание смесей толуол/МТБЭ с силикалитом для того, чтобы показать возможное взаимное ингибирование; было проведено сравнение силикалита с ГАУ на этих смесях загрязняющих веществ. Таблица 10. Адсорбция смесей толуол/МТБЭ: сравнение ГАУ с силикалитом.-6 010694 В заключение были продемонстрированы адсорбционные емкости силикалита, которые, как оказалось, очень близки адсорбционным емкостям коммерческого продукта ZSM-5. Был подтвержден тот факт, что эти адсорбенты обладают лучшими адсорбционными характеристиками, чем ГАУ. Пример 15. Полициклические ароматические углеводороды В качестве ароматического соединения с двумя сконденсированными кольцами был исследован нафталин; эксперименты по адсорбции были проведены с силикалитом, ZSM-5, MSA, ERS-8, морденитом, ГАУ. Условия: время установления равновесия 24 ч, 10 мг адсорбента, 1 ppm нафталина, в 22 мл воды. Таблица 11. Адсорбция нафталина различными адсорбентами Пример 16. Были исследованы также молекулы компонентов газойля, в частности, 2-метилнафталин, аценафтен и фенантрен; результаты, полученные с морденитом и с MSA в условиях: 10 мг адсорбента в 22 мл воды,содержащей 1 ppm загрязняющего вещества, указаны в нижеприведенной табл. 12. Таблица 12. Адсорбция полициклических ароматических углеводородов морденитом и MSA Пример 17. Сравнение барьеров из металлического железа и цеолита На фиг. 6 показана цепь превращений, которые претерпевает тетрахлорэтилен при концентрации 1ppm, в подземных водах, которые движутся со скоростью Дарси 1 м/день, в реакционно-способном барьере, содержащем гранулированное Fe. Кинетика была рассчитана исходя из данных Tratnyek et al.(P.G.Tratnyek, T.L.Johnson, M.M.Scherer, G.R.Eykholt, GWMR, Fall 1997, pp. 108-114), в предположении,что Fe имеет реакционно-способную поверхность 3,5 м 2/см 3, то есть порядка самых высоких значений,приведенных в литературе. Указано направление изменения концентрации продуктов разложения в связи с направлением движения в барьере: тетрахлорэтилен (ПХЭ)трихлорэтилен (ТХЭ)дихлорэтилен(ДХЭ) + ацетилен и хлорацетилен (АХ); дихлорэтиленвинилхлорид (ВХ)этилен. Хлорацетилен быстро разлагается на ацетилен и винилхлорид (фиг. 6). ПХЭ разлагается быстро, но последующие реакции продуктов его разложения протекают медленнее, требуя около двух дней пребывания, что соответствует пути в барьере порядка нескольких метров,для того, чтобы достигнуть разложения последнего опасного вида молекул в цепи - винилхлорида. Это приводит к необходимости иметь толщину барьера в этих условиях по меньшей мере 3-5 м. Для барьеров, содержащих железо, следует указать на хорошо известные ограничения, широко освещенные в литературе, в соответствии с которыми эффективность подтверждается только для некоторых групп способных к восстановлению продуктов, алифатических хлорированных продуктов и тяжелых металлов с высокой степенью окисления, например, Cr6+, U6+; также полностью описана функциональная зависимость от присутствия ионов, которые значительно ухудшают рабочие характеристики (Dahmke,A., E.Ebert, R.Kober, D. Schafer, 2000. Laboratory and field results of Fe (0) reaction walls - a first resume (Результаты лабораторных и натурных испытаний реакционных экранов из Fe (0) - первые выводы). In: Proc.-7 010694 Пример 18. Функционирование барьера из цеолита Цеолиты, даже с относительно большими размерами частиц, благодаря их микропористой структуре, позволяют проводить адсорбцию значительно быстрее, в течение времени, которое может составлять порядка секунды и, следовательно, при протоке в части барьера толщиной порядка сантиметров. Следовательно, толщина цеолитного адсорбирующего барьера не зависит от кинетики, а зависит только от адсорбционной емкости самого цеолита по отношению к частицам, которые должны быть адсорбированы. На фиг. 7 показано моделирование на основе данных по изотерме адсорбции, полученных на материалах, применяемых в данном процессе, то есть на объекте данного изобретения, функционирования цеолитного барьера через год; при этом подземные воды, которые движутся со скоростью 1 м/день, имеют загрязненность 1 ppm по трихлорэтилену (ТХЭ). Через 1 год, таким образом, первые слои барьера,толщиной около 1 см, насыщаются, поглотив полное количество ТХЭ, соответствующее их емкости, рассчитанной по изотерме. Соответственно, ТХЭ проходит с неизменной концентрацией. Ниже по течению относительно этого слоя концентрация резко падает (фиг. 7). С другой стороны, на фиг. 8, также на основе расчетов по данным для материалов, используемых в процессе - объекте изобретения, показано перемещение фронта насыщения в цеолитном барьере за расчетное время при различных концентрациях и скорости подземных вод (фиг. 8). Этот график, таким образом, можно применять для оценки толщины, необходимой для поддержания барьера в эффективном состоянии в течение некоторого периода времени, исходя из предположения,что подземные воды содержат только ТХЭ. Если присутствуют другие органические молекулы, естественно, к толщине, полученной из фиг. 8, следует прибавить толщину, необходимую для адсорбции этих других молекул. Одной из сильных сторон цеолитов является то, что они не дают ингибирования адсорбции одной органической молекулы со стороны другой и, кроме того, то, что не существует конкуренции за активные адсорбционные места со стороны ионов вплоть до высоких концентраций. Это особенно важно, поскольку если данный материал также адсорбирует ионы, он может очень быстро исчерпать свои возможности, так как содержание ионов часто в сотни или тысячи раз превышает содержание органических молекул. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ обработки воды, загрязненной винилхлоридом (ВХ), простым метил-третбутиловым эфиром (МТБЭ), нафталином, 2-метилнафталином, аценафтеном, фенантреном или их смесями, состоящий из обработки воды, загрязненной винилхлоридом (ВХ), простым метил-третбутиловым эфиром (МТБЭ),нафталином, 2-метилнафталином, аценафтеном, фенантреном или их смесями, одним или более аполярными цеолитами, характеризующимися соотношением оксид кремния/оксид алюминия 50 и наличием в структуре каналов, имеющих размеры, подобные размерам молекул загрязняющих соединений. 2. Способ по п.1, отличающийся тем, что обработку осуществляют по отношению к загрязненной подземной воде, при этом обработка состоит из пропускания воды через проницаемый реакционноспособный барьер (ПРБ), помещенный in situ перпендикулярно потоку подземной воды, причем реакционноспособная среда барьера состоит из указанных одного или более аполярных цеолитов. 3. Способ по п.1 или 2, где цеолит отличается наличием в структуре каналов, имеющих размеры в интервале от 4,5 до 7,5 . 4. Способ по п.3, где цеолит отличается наличием в структуре каналов, имеющих размеры в интервале от 5,0 до 7,0 . 5. Способ по п.1 или 2, где цеолит отличается соотношением оксид кремния/оксид алюминия 200. 6. Способ по п.5, где цеолит состоит из силикалита или цеолита ZSM-5, или морденита. 7. Способ по п.1 или 2, где воду обрабатывают смесью цеолитов, указанных в п.1 и соответствующих типам загрязняющих веществ, присутствующих в самой воде.
МПК / Метки
МПК: C02F 1/28
Метки: воды, способ, использовании, обработки, основанный, цеолитов, загрязнённой
Код ссылки
<a href="https://eas.patents.su/12-10694-sposob-obrabotki-zagryaznyonnojj-vody-osnovannyjj-na-ispolzovanii-ceolitov.html" rel="bookmark" title="База патентов Евразийского Союза">Способ обработки загрязнённой воды, основанный на использовании цеолитов</a>
Предыдущий патент: 1,3-диметилбутилкарбоксанилиды для борьбы с нежелательными микроорганизмами
Следующий патент: Способ поверхностной обработки стекла металлическим алюминием
Случайный патент: Система для определения одной или нескольких мишеней в образце и способы ее применения