Новые производные бензоилгуанидина с эффективными своиствами, способ их получения и их применение при изготовлении лекарственных средств
Номер патента: 4687
Опубликовано: 24.06.2004
Авторы: Блех Штефан-Маттиас, Айккмайер Кристиан, Бюргер Эрих, Рос Отто
Формула / Реферат
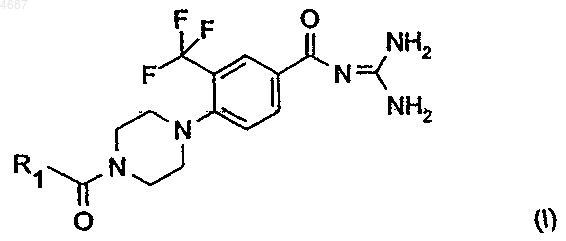
1. Производные бензоилгуанидина общей формулы I
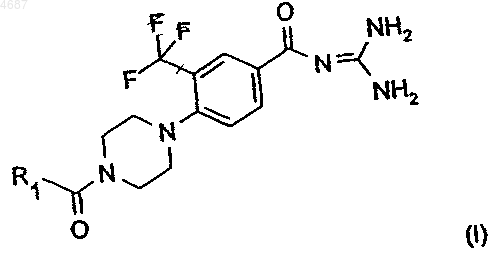
в которой R1 может обозначать гетероарил, представляющий собой 5-6-членное кольцо, содержащее в качестве гетероатома O или N, фенил или фенил, замещенный фтором или метильной, трифторметильной, метоксигруппой либо пирролильным остатком,
необязательно в форме отдельных таутомеров либо необязательно энантиомеров и их смесей, а также в виде свободных оснований либо соответствующих кислотно-аддитивных солей с фармакологически приемлемыми кислотами.
2. Соединения общей формулы I по п.1, отличающиеся тем, что R1 может обозначать незамещенное фенильное кольцо или фенильное кольцо, которое может быть замещено фтором или метильной, трифторметильной, метоксигруппой либо пирролильным остатком, или может представлять собой
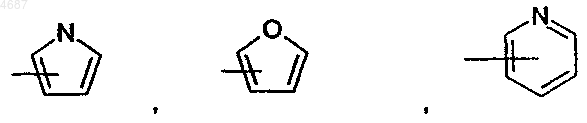
3. 4-(4-(2-Пирролилкарбонил)-1-пиперазинил)-3-трифторметилбензоилгуанидинметансульфонат
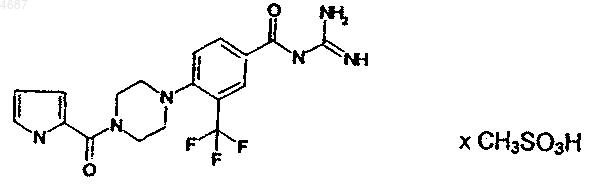
4. 4-(4-(4-Фторфенилкарбонил)-1-пиперазинил)-3-трифторметилбензоилгуанидинметансульфонат
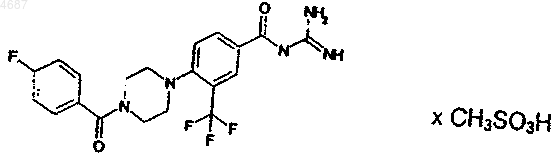
5. Способ получения соединений общей формулы I
отличающийся тем, что эфир 4-(1-пиперазинил)-3-трифторметилбензойной кислоты общей формулы II
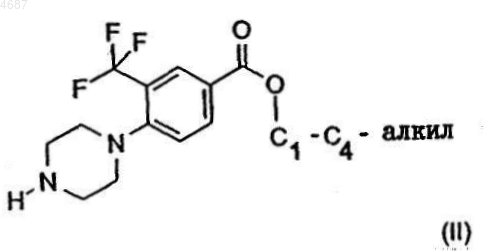
подвергают взаимодействию с соединением общей формулы III
R1C(O)Q (III),
в которой Q обозначает замещаемую азотом пиперазина уходящую группу, необязательно в присутствии вспомогательных веществ, предпочтительно карбонилдиимидазола, и полученное в результате производное бензойной кислоты общей формулы IV
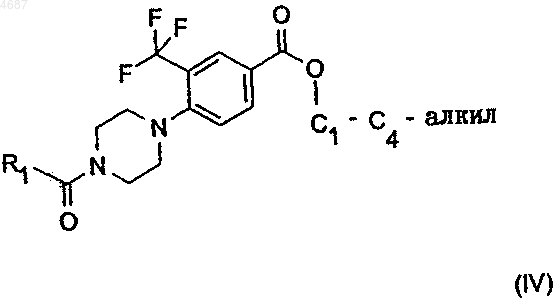
суспендируют в соответствующем, предпочтительно безводном, растворителе, предпочтительно в диметилформамиде, в смеси с раствором либо суспензией основания, предпочтительно гидрида натрия, в соответствующем безводном растворителе, предпочтительно в диметилформамиде, смешивают с солью гуанидина, предпочтительно гидрохлоридом гуанидина, и в завершение продукт реакции выделяют, а при необходимости с помощью фармакологически приемлемой кислоты получают требуемую кислотно-аддитивную соль.
6. Фармацевтическая композиция, отличающаяся тем, что она содержит в своем составе соединение по любому из пп.1-4 и его кислотно-аддитивные соли наряду с обычными вспомогательными веществами и носителями.
7. Применение соединений по любому из пп.1-4 в качестве лекарственных средств.
8. Применение по п.7 соединений в качестве лекарственных средств с ингибирующим действием по отношению к Na+ /H+-обмену.
9. Применение соединений общей формулы I, их кислотно-аддитивных солей при изготовлении соответствующего лекарственного средства для терапевтического лечения различных форм ишемии.
Текст
1 Настоящее изобретение относится к производным бензоилгуанидина нового типа общей формулы I, к способу их получения и к их применению при изготовлении лекарственных средств. В нижеприведенной общей формуле I в которой R1 может обозначать гетероарил,представляющий собой 5-6 членное кольцо, содержащее в качестве гетероатома О или N, фенил или фенил, замещенный фтором или метильной, трифторметильной, метоксигруппой либо пирролильным остатком,необязательно в форме отдельных таутомеров либо необязательно энантиомеров и их смесей, а также в виде свободных оснований либо соответствующих кислотно-аддитивных солей с фармакологически приемлемыми кислотами. В заявке также описаны производные бензоилгуанидина формулы I, в частности 2 разветвленной или неразветвленной С 1-С 4 алкоксигруппой, NH2-группой или первичной либо вторичной аминогруппой, трифторметильной группой, циано- либо нитрогруппой или галогеном,необязательно в форме отдельных таутомеров либо необязательно энантиомеров и их смесей, а также в виде свободных оснований либо соответствующих кислотно-аддитивных солей с фармакологически приемлемыми кислотами. Предпочтительными согласно настоящему изобретению являются соединения общей формулы I, в которой R1 может обозначать незамещенное фенильное кольцо либо фенильное кольцо, замещенное фтором или метильной,трифторметильной, метоксигруппой либо пирролильным остатком, или может обозначать Особенно предпочтительны следующие соединения: метансульфонат 4-(4-(2-пирролилкарбонил)-1-пиперазинил)-3-трифторметилбензоилгуанидина где R1 может обозначать С 1-С 8 алкил, гетероарил, незамещенный либо одно- или многозамещенный разветвленной или неразветвленной С 1-С 4 алкильной группой, циклоалкильной группой, разветвленной или неразветвленной C1 С 4 ал-коксигруппой, NH2-группой либо первичной или вторичной аминогруппой, трифторметильной группой, циано- либо нитрогруппой или галогеном,арил, незамещенный либо одно- или многозамещенный разветвленной или неразветвленной С 1-С 4 алкильной группой, разветвленной или неразветвленной С 1-С 4 алкоксигруппой,NH2-группой или первичной либо вторичной аминогруппой, трифторметильной группой,гидрокси-, циано- либо нитрогруппой или галогеном либо 5- или 6-членным гетероарильным остатком, который может содержать один, два,три, четыре или пять гетероатомов из группы,включающей азот, кислород или серу, причем эти гетероатомы могут быть идентичными либо разными, алкиларил, незамещенный либо одноили многозамещенный в арильной и/или алкильной части этой структуры разветвленной или неразветвленной С 1-С 4 алкильной группой, С 1-С 4 алкил, соответственно C1-C8 алкил представляет собой в основном разветвленный или неразветвленный углеводородный радикал с 1-4,соответственно 1-8 атомами углерода, который необязательно может быть замещен одним либо несколькими атомами галогена, предпочтительно фтором, причем атомы галогена могут быть идентичными или разными. В качестве примеров можно назвать следующие углеводородные радикалы: метил, этил, пропил, 1-метилэтил (изопропил), н-бутил, 1-метилпропил, 2-метилпропил,1,1-диметилэтил, пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 1,1-диметилпропил,1,2-диметилпропил, 2,2-диметилпропил, 1-этилпропил, гексил, 1-метил пентил, 2-метилпентил,3-метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,2 диметилбутил, 2,3-диметилбутил, 3,3-диметибутил, 1-этилбутил, 2-этилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этил-1 метилпропил и 1-этил-2-метилпропил. Предпочтительными, если не указано иное,являются (низш.) алкильные радикалы с 1-4 атомами углерода, такие как метил, этил, про 3 пил, изопропил, н-бутил, 1-метилпропил, 2 метилпропил или 1,1-диметилэтил. Алкокси представляет собой в основном связанную через атом кислорода прямоцепочечную либо разветвленную алкильную группу. Предпочтительной является (низш.)алкоксигруппа с 1-4 атомами углерода. Особенно предпочтительна метоксигруппа. Арил представляет собой в основном ароматический радикал с 6-10 атомами углерода, в том числе и в различных композициях (составах), при этом ароматическое соединение может быть замещено одной либо несколькими(низш.)алкильными группами, трифторметильными группами, цианогруппами, алкоксигруппами, нитрогруппами, аминогруппами и/или одним либо несколькими атомами галогена,идентичными или разными; предпочтительным арильным радикалом является необязательно замещенный фенильный радикал, при этом в качестве заместителей предпочтительны галоген, такой как фтор, хлор или бром, цианогруппа, а также гидроксил; в качестве галогена предпочтительным согласно изобретению является фтор. Арильный заместитель, предпочтительно фенил, может быть, кроме того, замещен 5- либо 6-членным гетероарильным радикалом,который может содержать один, два, три, четыре или пять гетероатомов, выбранных из группы, включающей азот, кислород и серу, при этом гетероатомы могут быть идентичными или разными. Аралкил представляет собой в основном связанный через алкиленовую цепь арильный радикал с 7-14 атомами углерода, при этом ароматическое соединение может быть замещено одной либо несколькими (низш.)алкильными группами, алкоксигруппами, нитрогруппами,аминогруппами и/или одним либо несколькими атомами галогена, идентичными или разными. Предпочтительными являются аралкильные радикалы с 1-6 атомами углерода в алифатическом фрагменте и 6 атомами углерода в ароматическом фрагменте. В качестве предпочтительных аралкильных радикалов можно назвать,если не указано иное, бензил, фенетил и фенилпропил. Галоген, если не указано иное, представляет собой фтор, хлор, бром, иод, предпочтительны из которых фтор, хлор или бром. Аминогруппа, если не указано иное, представляет собой функциональную NH2-группу,которая необязательно может быть замещена одним либо двумя С 1-С 8 алкильными, арильными или аралкильными радикалами, идентичными или разными. В соответствии с этим алкиламиногруппа представляет собой, например, метиламино, этиламино, пропиламино, 1-метиленэтиламино, бутиламино, 1-метилпропиламино,2-метилпропиламино или 1,1-диметилэтиламино. Диалкиламиногруппа в свою очередь представляет собой, например, диметиламино, ди 004687 4 этиламино, дипропиламино, дибутиламино,ди(1-метилэтил)амино, ди(1-метилпропил)амино, ди(2-метилпропил)амино, этилметиламино,метилпропиламино. Циклоалкил представляет собой в основном насыщенный или ненасыщенный циклический углеводородный радикал с 5-9 атомами углерода, который необязательно может быть замещен одним либо несколькими, идентичными или разными, атомами галогена, предпочтительно фтором. Предпочтительными являются циклические углеводородные радикалы с 3-6 атомами углерода. В качестве примеров можно назвать циклопропил, циклобутил, циклопентил, циклопентенил, циклогексил, циклогексенил, циклогептил, циклогептенил, циклогептадиенил, циклооктил, циклооктенил, циклооктадиенил и циклононинил. Гетероарил согласно указанному выше определению представляет собой в основном 5-6 членное кольцо, которое может содержать в качестве гетероатомов кислород, серу и/или азот и с которым может быть сконденсировано другое ароматическое кольцо. Предпочтительными являются 5- и 6-членные ароматические кольца, содержащие атом кислорода, атом серы и/или до двух атомов азота и необязательно сконденсированные с бензольным ядром. В качестве особых гетероциклических систем можно назвать, например, следующие: акридинил, акридонил, алкилпиридинил, антрахинонил, аскорбил, азаазуленил, азабензантраценил, азабензантренил, азахризенил, азациклазинил, азаиндолил, азанафтаценил, азанафталенил,азапренил, азатрифениленил, азепинил, азиноиндолил, азинопирролил, бензакридинил, бензазапинил, бензофурил, бензонафтиридинил, бензопиранонил, бензопиранил, бензопиронил, бензохинолинил, бензохинолизинил, бензотиепинил, бензотиофенил, бензилизохинолинил, бипиридинил, бутиролактонил, капролактамил,карбазолил, карболинил, катехинил, хроменопиронил, хромонопиранил, кумаринил, кумаронил,декагидрохинолинил,декагидрохинолонил, диазаантраценил, диазафенантренил,дибензазапинил, дибензофуранил, дибензотифенил, дихромиленил, дигидрофуранил, дигидроизокумаринил, дигидроизохинолинил, дигидропиранил, дигидропиридинил, дигидропиридонил, дигидропиронил, дигидротиопиранил,диприленил, диоксантиленил, энантолактамил,флаванил, флавонил, флуоранил, флуоресцеинил, фурандионил, фуранохроманил, фуранонил, фуранохинолинил, фуранил, фуропиранил,фуропиронил, гетероазуленил, гексагидропиразиноизохинолинил, гидрофуранил, гидрофуранонил, гидроиндолил, гидропиранил, гидропиридинил, гидропирролил, гидрохинолинил, гидротиохроменил, гидротиофенил, индолизидинил, индолизинил, индолонил, изатинил, изатогенил, изобензофурандионил, изобензфуранил,изохроманил, изофлавонил, изоиндолинил, изо 5 индолобензазапинил, изоиндолил, изохинолинил, изохинуклидинил, лактамил, лактонил, малеимидил, моноазабензонафтенил, нафталенил,нафтимидазопиридиндионил, нафтиндолизинедионил, нафтотодигидропиранил, нафтофуранил, нафтиридинил, оксепинил, оксиндолил,оксоленил, пергидроазолопиридинил, пергидроиндолил, фенантрахинонил, фталидеизохинолинил, фталимидил, фталонил, пиперидинил,пиперидонил, пролинил, пиразинил, пираноазинил, пираноазолил, пиранопирандионил, пиранопиридинил, пиранохинолинил, пиранопиразинил, пиранил, пиразолопиридинил, пиридинэтионил, пиридинонафталенил, пиридинопиридинил, пиридинил, пиридоколинил, пиридоиндолил, пиридопиридинил, пиридопиримидинил,пиридопирролил, пиридохинолинил, пиронил,пирроколинил, пирролидинил, пирролизидинил,пирролизинил, пирролодиоазинил, пирролонил,пирролопиримидинил, пирролохинолонил, пирролил, хинакридонил, хинолинил, хинолизидинил, хинолизинил, хинолонил, хинуклидинил,родаминил, спироцумаранил, сукцинимидил,сульфоланил, сульфоленил, тетрагидрофуранил,тетрагидроизохинолинил, тетрагидропиранил,тетрагидропиридинил, тетрагидротиапиранил,тетрагидротиофенил, тетрагидротиопиранонил,тетрагидротиопиранил, тетронил, тиафенил,тиахроманил, тиадекалинил, тианафтенил, тиапиранил, тиапиронил, тиазолопиридинил, тиенопиридинил, тиенопирролил, тиенотиофенил,тиепинил, тиохроменил, тиокумаринил, тиопиранил, триазаантраценил, триазиноиндолил,триазолопиридинил, тропанил, ксантенил, ксантонил, ксантидролил, аденинил, аллоксанил,аллоксазинил, антранилил, азабензантренил,азабензонафтенил, азанафтаценил, азафеноксазинил, азапуринил, азинил, азолоазинил, азолил,барбитуровая кислота, бензазинил, бензимидазолэтионил, бензимидазолонил, бензизотиазолил, бензизоксазолил, бензоциннолинил, бензодиазоцинил, бензодиоксоланил, бензодиоксолил, бензопиридазинил, бензотиазепинил, бензотиазинил, бензотиазолил, бензоксазинил, бензоксазолинонил, бензоксазолил, циннолинил,депсидинил, диазафенантренил, диазепинил,диазинил, дибензоксазепинил, дигидробензимидазолил, дигидробензотиазинил, дигидрооксазолил, дигидропиридазинил, дигидропиримидинил, дигидротиазинил, диоксанил, диоксенил,диоксепинил, диоксинонил, диоксоланил, диоксолонил, диоксопиперазинил, дипиримидопиразинил, дитиоланил, дитиоленил, дитиолил, флавинил, фуропиримидинил, глюкоциамидинил,гуанинил,гексагидропиразиноизохинолинил,гексагидропиридазинил, гидантоинил, гидроимидазолил, гидропаразинил, гидропиразолил,гидропиридазинил, гидропиримидинил, имидазолинил, имидазолил, имидазохиназолинил,имидазотиазолил, индазолебензопиразолил, индоксазенил, инозинил, изоаллоксазинил, изотиазолил, изоксазолидинил, изоксазолинонил, изо 004687 6 ксазолинил, изоксазолонил, изоксазолил, лумазинил, метилтиминил, метилурацилил, морфолинил, нафтимидазолил, оротицил, оксатианил,оксатиоланил, оксазинонил, оксазолидинонил,оксазолидинил, оксазолидонил, оксазолинонил,оксазолинил, оксазолонил, оксазолопиримидинил, оксазолил, пергидроциннолинил, пергидропирролоазинил, пергидропирролотиазинил,пергидротиазинонил, перимидинил, феназинил,фенотиазинил, феноксатиинил, феноксазинил,феноксазонил, фталазинил, пиперазиндионил,пиперазинодионил, полихиноксалинил, птеридинил, птеринил, пуринил, пиразинил, пиразолидинил, пиразолидонил, пиразолинонил, паразолинил, пиразолобензодиазепинил, пиразолонил, пиразолопиримидинил, пиразолотриазинил, пиразолил, пиридазинил, пиридазонил, пиридопиразинил, пиридопиримидинил, пиримидинэтионил, пиримидинил, пиримидионил, пиримидоазепинил, пиримидоптеридинил, пирролобензодиазепинил, пирролодиазинил, пирролопиримидинил, хиназолидинил, хиназолинонил, хиназолинил, хиноксалинил, сультамил,сультинил, сультонил, тетрагидрооксазолил,тетрагидропиразинил, тетрагидропиридазинил,тетрагидрохиноксалинил, тетрагидротиазолил,тиазепинил, тиазинил, тиазолидинонил, тиазолидинил, тиазолинонил, тиазолинил, тиазолобензимидазолил, тиазолил, тиенопиримидинил,тиазолидинонил, тиминил, триазолопиримидинил, урацилил, ксантинил, ксилитолил, азабензонафтенил, бензофуроксанил, бензотиадиазинил, бензотриазепинонил, бензотриазолил, бензоксадиазинил, диоксадиазинил, дитиадазолил,дитиазолил, фуразанил, фуроксанил, гидротриазолил, гидрокситризинил, оксадиазинил, оксадиазолил, оксатиазинонил, оксатриазолил, пентазинил, пентазолил, полиоксадиазолил, сидонил, тетраоксанил, тетразепинил, тетразинил,тетразолил, тиадиазинил, тиадиазолинил, тиадиазолил, тиадиоксазинил, тиатриазинил, тиатриазолил, триазепинил, триазиноиндолил, триазинил, триазолиндионил, триазолинил, триазолил, триоксанил, трифенодиоксазинил, трифенодитиазинил, тритиадиазепинил, тритианил или триоксоланил. Соединения этого типа уже известны из выложенной немецкой заявки 19601303.8. Подобные соединения благодаря их действию как ингибиторов Na+/Н+-обмена в клетках могут применяться в качестве биологически активных веществ в лекарственных средствах или их можно использовать в качестве промежуточных продуктов при получении таких активных веществ. Соединения по изобретению эффективны при аритмиях, возникающих, например, при гипоксии. Кроме того, они могут применяться при болезнях, обусловленных различными типами ишемии (примеры: сердечная,мозговая ишемия,ишемия желудочнокишечного тракта, такая как мензентериальная тромбоз/эмболия, легочная, почечная ишемия, 7 ишемия печени, ишемия скелетной мускулатуры). Примерами таких болезней являются ишемическая болезнь сердца, инфаркт миокарда,стенокардия, устойчивая стенокардия, желудочковые аритмии, поджелудочковые аритмии,сердечная недостаточность и др. Предлагаемые соединения в этих случаях могут применяться,кроме того, в качестве дополнительных средств при операциях по шунтированию (наложение байпаса), при операциях на открытом сердце,при операциях, требующих приостановки кровоснабжения сердца, при трансплантациях сердца. К болезням, обусловленным различными типами ишемии, относятся также эмболия в системе легочного кровообращения, острая или хроническая почечная недостаточность, инфаркт головного мозга, нарушения реперфузии при возобновленном кровоснабжении соответствующих участков головного мозга после устранения (лизиса) закупорок сосудов и острые и хронические нарушения кровотока в головном мозге. В этих случаях вышеназванные соединения эффективны также в сочетании с тромболитическими средствами, такими как трет-ПА,стрептокиназа и урокиназа. При реперфузии сосудов ишемического сердца (например после приступа стенокардии или инфаркта миокарда) могут иметь место необратимые повреждения кардиомиоцитов в пораженной области. В этом случае соединения по изобретению проявляют при определенных условиях кардиозащитное действие. Функциональное назначение предлагаемых соединений в случаях ишемии состоит также в их способности предотвращать повреждения пересаживаемых органов (например для защиты такого трансплатата, как, например,печень, почка, сердце или легкое, до, во время и после имплантации, а также при хранении трансплантатов), которые могут быть вызваны операцией при пересадке. Кроме того, соединения по изобретению проявляют в качестве лекарственных средств защитное действие при проведении ангиопластических операций на сердце и на сосудах периферической системы кровообращения. При эссенциальной гипертонии и диабетической нефропатии уровень обмена протонов натрия в клетках повышен, поэтому предлагаемые в изобретении соединения пригодны в качестве ингибиторов такого обмена для предупреждения названных заболеваний. Предлагаемые в изобретении соединения отличаются помимо этого исключительно эффективным ингибирующим действием по отношению к пролиферации клеток, поэтому они представляют интерес в качестве лекарственных средств для лечения заболеваний, при которых пролиферация клеток играет первичную или вторичную роль, и могут применяться в качестве средств против раковых заболеваний, доброкачественных опухолей или, например, при ги 004687 8 пертрофии предстательной железы, атеросклероза, гипертрофии и гиперплазии соответствующих органов, фиброзах и поздних диабетических осложнений. Известно далее, что соединения этого типа могут оказывать положительное влияние на уровень сывороточных липопротеинов в крови. Неожиданным образом было установлено,что соединения общей формулы I обладают по сравнению с уже известными из уровня техники производными бензоилгуанидина тем преимуществом, что наряду с неожиданно более высокой эффективностью их можно вводить при хорошей совместимости оральным путем. Активные вещества общей формулы I могут применяться в виде водных инъекционных растворов (например для внутривенного, внутримышечного или подкожного введения), в виде таблеток, суппозиториев, мазей, пластырей для чрескожного введения, аэрозолей для ингаляции через дыхательные пути или в качестве спрея для полости носа. Одна таблетка или один суппозиторий содержит активное вещество в количестве от 5 до 200 мг, предпочтительно от 10 до 50 мг. При ингаляции разовая доза содержит от 0,05 до 20 мг, предпочтительно от 0,2 до 5 мг. При парентеральной инъекции разовая доза содержит от 0,1 до 50 мг, предпочтительно от 0,5 до 20 мг. При необходимости указанные дозы могут назначаться соответственно для многоразового введения в течение суток. Ниже на примерах представлен состав некоторых фармацевтических препаратов, содержащих активное вещество. Таблетки, мг: Активное вещество общей формулы I 20,0 Стеарат магния 1,0 Кукурузный крахмал 62,0 Лактоза 83,0 Поливинилпирролидон 1,6 Раствор для инъекции, г: Активное вещество общей формулы I 0,3 Хлорид натрия 0,9 Вода для инъекций До 100 мл Этот раствор можно стерилизовать с помощью стандартных методов. Водный раствор для введения в полость носа или для ингаляции, г: Активное вещество общей формулы I 0,3 Хлорид натрия 0,9 Хлорид бензалкония 0,01 мг Вода очищенная До 100 мл Представленный раствор пригоден для введения в виде спрея в полость носа или для введения через дыхательные пути с использова 9 нием ингалятора, с помощью которого образуется аэрозоль с размером частиц от 2 до 6 мкм. Капсулы для ингаляции Из соединений общей формулы I в микронизированной форме (размер частиц преимущественно от 2 до 6 мкм) необязательно с добавками микронизированных субстанцийносителей, например лактозы, изготавливают капсулы с твердожелатиновой оболочкой. Для ингаляции используют обычные ингаляторы,предназначенные для порошковой ингаляции. В каждой капсуле содержится, например, от 0,2 до 20 мг активного вещества общей формулы I и 040 мг лактозы. Ингаляционный аэрозоль, части: Активное вещество общей формулы I 1 Соевый лецитин 0,2 Смесь пропеллентов До 100 Эту композицию предпочтительно помещают в аэрозольные баллончики с дозирующим клапаном, при этом рассчитано, что за одно нажатие выдается доза в 0,5 мг. При назначении других дозировок целесообразно использовать композиции с более высоким, соответственно с более низким содержанием активного вещества. Мазь (состав г/100 г мази): Активное вещество общей формулы I 2 Дымящая соляная кислота 0,011 Пиросульфит натрия 0,05 Смесь из равных частей цетилового спирта и стеарилового спирта 20 Белый вазелин 5 Синтетическое бергамотное масло 0,075 Дистиллированная вода До 100 мл Из указанных ингредиентов по обычной технологии изготавливают соответствующую мазь. Способы получения соединений по изобретению в принципе общеизвестны из уровня техники; так, например, предлагаемые соединения можно получать следующим путем. Эфиры 4-(1-пиперазинил)-3-трифторметилбензойной кислоты общей формулы II подвергают взаимодействию с соединением общей формулы III(III),в которой Q обозначает замещаемую пиперазиновым азотом уходящую группу, необязательно в присутствии вспомогательных веществ, предпочтительно карбонилдиимидазола, получая в результате производное бензойной кислоты общей формулы IV которое суспендируют в соответствующем,предпочтительно безводном, растворителе,предпочтительно в диметилформамиде, и смешивают со смесью из раствора либо суспензии основания, предпочтительно гидрида натрия, в соответствующем безводном растворителе,предпочтительно диметилформамиде, и соли гуанидина, предпочтительно гидрохлорида гуанидина, и в завершение выделяют требуемый продукт реакции. Ниже изобретение подробно поясняется на представленных примерах. Примеры. Метиловый эфир 4-фтор-3-трифторметилбензойной кислоты. К 35,4 г (170 ммолей) 4-фтор-3-(трифторметил)бензойной кислоты в 250 мл метанола при охлаждении льдом в течение 25 мин при 5 С примешивают 68 мл SOCl2. По завершении процесса добавления реакционную смесь в течение последующих 3 ч нагревают с обратным холодильником. Затем раствор охлаждают до комнатной температуры и упаривают под вакуумом. Маслянистый остаток растворяют в 200 мл диэтилового эфира и экстрагируют водой,NaHCO3-раствором и повторно водой. Объединенные органические фазы сушат над сульфатом магния и упаривают под вакуумом. Выход: 29,0 г (77%). Метиловый эфир 4-(4-бензил-1-пиперазинил)-3-трифторметилбензойной кислоты. 7 г (31,5 ммоля) метилового эфира 4-фтор 3-трифторметилбензойной кислоты растворяют в 60 мл сухого диметилсульфоксида (ДМСО) и смешивают с 5,55 г (31,5 ммоля) N-бензилпиперазина и 4,35 г (31,5 ммоля) карбоната калия. Эту смесь перемешивают в течение 12 ч при 90 С. После охлаждения смесь сливают в 200 мл воды и трижды экстрагируют этиловым эфиром уксусной кислоты (уксусным эфиром). Объединенные органические фазы промывают водой и насыщенным раствором хлорида натрия, сушат над сульфатом магния и отгоняют под вакуумом. Остаток хроматографируют на силикагеле с помощью смеси уксусного эфира и н-гептана. Выход: 3,93 г (33%). Метиловый эфир 4-(1-пиперазинил)-3-трифторметилбензойной кислоты. 20,2 г (53,3 ммоля) метилового эфира 4-(4 бензил-1-пиперазинил)-3-трифторметилбензойной кислоты растворяют в 200 мл метанола и смешивают с 2 г палладия на угле, после чего в течение 1,4 ч гидрируют при 70 С и давлении водорода 5 бар. Затем раствор отфильтровывают 11 вакуум-фильтрацией через целлит и отгоняют под вакуумом. Выход: 14,85 г (97%) Общие рекомендации по осуществлению реакции сочетания метилового эфира 4-(1-пиперазинил)-3-трифторметилбензойной кислоты с бензойными кислотами 5 ммолей соответствующей карбоновой кислоты растворяют в 30 мл абсолютного тетрагидрофурана (ТГФ) и в атмосфере защитного газа смешивают при 0 С с 810 мг (5 ммолей) карбонилдиимидазола, перемешивая в течение 2 ч при комнатной температуре (приблизительно 25 С). Затем к смеси добавляют 1,44 г (5 ммолей) метилового эфира 4-(1-пиперазинил)-3-трифторметилбензойной кислоты и продолжают перемешивание еще в течение примерно 12 ч. Далее раствор упаривают под вакуумом досуха и остаток растворяют с помощью уксусного эфира. После промывки насыщенным NaHCO3 pacтвором, насыщенным NaCl раствором и водой органические фазы сушат над MgSO4 и упаривают под вакуумом. После кристаллизации в соответствующем растворителе или после хроматографии на силикагеле с использованием соответствующего элюента получают следующие соединения: 1) метиловый эфир 4-(4-(3-метоксифенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты: хроматография на колонке: уксусный эфир/н-гептан (2:1) выход: 81%; 2) метиловый эфир 4-(4-(2-пирролилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты: кристаллизация из метанола выход: 75%, tпл 149 С; 3) метиловый эфир 4-(4-(4-фторфенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты: хроматография на колонке: уксусный эфир/н-гептан (2:1) выход: 77%; 4) метиловый эфир 4-(4-(2-метоксифенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты: хроматография на колонке: уксусный эфир/н-гептан (2:1) выход: 79%; 5) метиловый эфир 4-(4-(3-трифторметилфенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты: хроматография на колонке: уксусный эфир/н-гептан (2:1) выход: 83%; 6) метиловый эфир 4-(4-фенилкарбонил-1 пиперазинил)-3-трифторметилбензойной кислоты: хроматография на колонке: уксусный эфир/н-гептан (2:1) выход: 87%; 12 7) метиловый эфир 4-(4-(2-фурилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты: хроматография на колонке: уксусный эфир/н-гептан (2:1) выход: 75%; 8) метиловый эфир 4-(4-(3-метилфенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты: хроматография на колонке: уксусный эфир/н-гептан (2:1) выход: 79%; 9) метиловый эфир 4-(4-(4-(1-пиррил)фенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты: хроматография на колонке: уксусный эфир/н-гептан (2:1) выход: 87%; 10) метиловый эфир 4-(4-(2-пиридилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты хроматография на колонке: уксусный эфир/н-гептан (2:1) выход: 73%. Общие рекомендации по получению ацилгуанидинов из соответствующих метиловых эфиров карбоновых кислот 5,09 г (127,2 ммоля) 60%-ного НСl в белом(беленом) масле дважды промывают простым эфиром и декантируют. Затем добавляют 200 мл абсолютного ДМФ и при перемешивании и в атмосфере защитного газа добавляют небольшими порциями 12,15 г (127,2 ммоля) гидрохлорида гуанидина. После перемешивания в течение 1 ч добавляют 21,2 ммоля соответствующего метилового эфира и продолжают перемешивать еще в течение 2 ч при температуре порядка 120 С. Затем смесь охлаждают до комнатной температуры,фильтруют и фильтрат упаривают под вакуумом. После хроматографии на силикагеле с использованием соответствующего элюента и перевода с помощью соляной кислоты в простом эфире или других фармакологически приемлемых кислот в соответствующие соли получают представленные ниже соединения (в приведенных структурных формулах атомы водорода в целях большей наглядности не указаны, поскольку они связаны с атомом углерода либо с атомом азота и их отсутствие не затрудняет понимания сущности изобретения). Пример 1. Гидрохлорид 4-(4-(3-метоксифенилкарбонил)-1-пиперазинил)-3-трифторметилбензоилгуанидина Указанное в заголовке соединение получают из метилового эфира 4-(4-(3-метоксифенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты, хроматография на ко 13 Указанное в заголовке соединение получают из метилового эфира 4-(4-(2-пирролилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты, хроматография на колонке: уксусный эфир/метанол (5:1), выход: 66%, tпл 246 С, MC (M + H) + = 409 (свободное основание). Пример 3. 4-(4-(4-Фторфенилкарбонил)-1 пиперазинил)-3-трифторметилбензоилгуанидинметансульфонат Указанное в заголовке соединение получают из метилового эфира 4-(4-фенилкарбонил 1-пиперазинил)-3-трифторметилбензойной кислоты, хроматография на колонке: уксусный эфир/метанол (5:1), выход: 64%, tпл 214 С, МС Указанное в заголовке соединение получают из метилового эфира 4-(4-(4-фторфенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты, хроматография на колонке: уксусный эфир/метанол (5:1), выход: 40%, tпл 140 С, МС (М + Н)+=438 (свободное основание). Пример 4. Гидрохлорид 4-(4-(2-метоксифенилкарбонил)-1-пиперазинил)-3-трифторметилбензоилгуанидина Указанное в заголовке соединение получают из метилового эфира 4-(4-(2-метоксифенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты, хроматография на колонке: уксусный эфир/метанол (5:1), выход: 71%, tпл 219 С (разложение), МС (М + Н)+=450 (свободное основание). Пример 5. Гидрохлорид 4-(4-(3-трифторметилфенилкарбонил)-1-пиперазинил)-3-трифторметилбензоилгуанидина Указанное в заголовке соединение получают из метилового эфира 4-(4-(3-трифторметилфенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты, хроматография на колонке: уксусный эфир/метанол (5:1), выход: Указанное в заголовке соединение получают из метилового эфира 4-(4-(2-фурилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты, кристаллизация из простого эфира,выход: 19%, tпл 190 С (разложение), МС Указанное в заголовке соединение получают из метилового эфира 4-(4-(3-метилфенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты, кристаллизация из метанола/уксусного эфира, выход: 76%, tпл 199 С, МС Указанное в заголовке соединение получают из метилового эфира 4-(4-(4-(1-пиррил) фенилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты, кристаллизация из метанола, выход: 48%, tпл 150 С (разложение), МС Указанное в заголовке соединение получают из метилового эфира 4-(4-(2-пиридилкарбонил)-1-пиперазинил)-3-трифторметилбензойной кислоты, хроматография на колонке: уксусный эфир/метанол (5:1), выход: 34%, tпл 115 С(разложение), МС (М + Н)+=421 (свободное основание). Фармакологические характеристики Ингибирование Na+/H+-обмена в раковых клетках (НТ-29) кишечника человека Клетки НТ-29 инкубируют при 37 С, 5% СО 2 в питательной среде. По истечении 3-5 дней питательную среду удаляют, клетки промывают и затем в них вводят 7,5 мкМ BCECF-AM (чувствительный к изменению рН флуоресцентный краситель) при 37 С и без СО 2. По истечении 30 мин клетки промывают и подкисляют средой следующего состава: 70 мМ хлорид холина, 20 мМ NH4Cl, 1 мМ MgCl2, 1,8 мМ СаСl2, 5 мМ глюкоза и 15 мМ HEPES (N-2-гидроксиэтилпиперазин-N'-2-этансульфоновая кислота),рН 7,5. По истечении 6 мин инкубации при 37 С без СО 2 клетки промывают и в течение 5 мин инкубируют в среде для промывки следующего состава: 120 мМ хлорид холина, 5 мМ KСl, 1 мМ MgCl2, 1,8 мМ СаСl2, 5 мМ глюкоза и 15 мМMOPS, рН 7,0. Затем промывочную среду удаляют, после чего добавляют контрольную среду с тестируемым соединением, соответственно без него, следующего состава: 120 мМ NaCl, 5 мМKСl, 1 мМ MgCl2, 1,8 мМ СаСl2, 5 мМ глюкоза и 15 мМ MOPS, рН 7,0. Далее клетки в течение 4 мин инкубируют при 37 С в отсутствие СО 2 и исследуют методом флуориметрии (CytoFluor 2350). Флуоресценцию красителя BCECF измеряют при длине волны возбуждения 485 нм(чувствительный к изменению рН) и 440 нм (не чувствительный к изменению рН) и при длине волны испускания 530 нм. Цитоплазматический рН рассчитывают по соотношению флуоресценции при 485 и 440 нм. Это соотношение флуоресценции калибруют на основе измерения флуоресцентного сигнала после уравновешивания внешнего и внутреннего рН с помощью нигерицина. Пример 16 7 0,084 8 0,061 10 0,079 Соединения по изобретению неожиданно отличаются, кроме того, очень хорошей биосовместимостью и продолжительностью периода полураспада после орального введения, т.е. проявляют такие свойства, благодаря которым их можно в высшей степени эффективно применять для введения оральным путем. Фармакокинетические характеристики В экспериментальных исследованиях использовали мужских особей крыс (не натощак) весом приблизительно 200 г. Для внутривенного и орального введения субстанции растворяли в подкисленном водном растворе (рН 3). Отдельные болюсные инъекции (0,5 мг/кг внутривенно,2,5 мг/кг перорально) осуществляли путем введения в хвостовую вену (0,2 мл/200 г) или через канюлю в желудок (1 мл/200 г). Применяемые растворы анализировали с целью установить наличие вводимой дозы. Аликвоты крови объемом по 5 мл каждая отбирали из ретроорбитального сплетения вен при кратковременном наркозе галотаном с помощью гепаринизированных стеклянных капилляров согласно следующей схеме: после внутривенного введения: через 5, 15, 30 мин, 1, 2, 4, 6 и 8 ч; после орального введения: через 15 мин, 1, 2, 4, 6, 8, 24 и 32 ч. Отобранные образцы центрифугировали и плазму до начала проведения анализа помещали на хранение при -20 С. Подготовку образцов для анализа осуществляли жидкостножидкостной экстракцией с использованием внешнего стандарта. Экстракты плазмы анализировали посредством ЖХВР с обращенной фазой в сочетании с тандемным массспектрометром с ионизацией пучком электронов. Фармакологические характеристики определяли по соответствующим концентрациям плазмы неитеративным (бескомпартментным) анализом с помощью программы TopFit (HeinzelG., Woloszczak R., Thomann P., TopFit 2.0, Pharmacokinetic and pharmacodynamic data analysis,system for the PC, изд-во Gustav Fischer Verlag,Штутгарт, Йена, Нью-Йорк, 1993) При- F (биодос- t1/2 (внутри- t1/2 (перомер тупность) венно) рально) 2 63 1,3 5,0 3 71 3,1 5,4 5 58 5,4 7,5 Заявка DE 19843489, на основании которой испрашивается приоритет по настоящей заявке,в полном объеме включена в данное описание в качестве ссылки. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производные бензоилгуанидина общей формулы I 18 отличающийся тем, что эфир 4-(1-пиперазинил)3-трифторметилбензойной кислоты общей формулы II в которой R1 может обозначать гетероарил,представляющий собой 5-6-членное кольцо,содержащее в качестве гетероатома О или N,фенил или фенил, замещенный фтором или метильной, трифторметильной, метоксигруппой либо пирролильным остатком,необязательно в форме отдельных таутомеров либо необязательно энантиомеров и их смесей, а также в виде свободных оснований либо соответствующих кислотно-аддитивных солей с фармакологически приемлемыми кислотами. 2. Соединения общей формулы I по п.1, отличающиеся тем, что R1 может обозначать незамещенное фенильное кольцо или фенильное кольцо, которое может быть замещено фтором или метильной, трифторметильной, метоксигруппой либо пирролильным остатком, или может представлять собой 5. Способ получения соединений общей формулы I подвергают взаимодействию с соединением общей формулы III(III),в которой Q обозначает замещаемую азотом пиперазина уходящую группу, необязательно в присутствии вспомогательных веществ, предпочтительно карбонилдиимидазола, и полученное в результате производное бензойной кислоты общей формулы IV суспендируют в соответствующем, предпочтительно безводном, растворителе, предпочтительно в диметилформамиде, в смеси с раствором либо суспензией основания, предпочтительно гидрида натрия, в соответствующем безводном растворителе, предпочтительно в диметилформамиде, смешивают с солью гуанидина,предпочтительно гидрохлоридом гуанидина, и в завершение продукт реакции выделяют, а при необходимости с помощью фармакологически приемлемой кислоты получают требуемую кислотно-аддитивную соль. 6. Фармацевтическая композиция, отличающаяся тем, что она содержит в своем составе соединение по любому из пп.1-4 и его кислотно-аддитивные соли наряду с обычными вспомогательными веществами и носителями. 7. Применение соединений по любому из пп.1-4 в качестве лекарственных средств. 8. Применение по п.7 соединений в качестве лекарственных средств с ингибирующим действием по отношению к Na+ /H+-обмену. 9. Применение соединений общей формулы I, их кислотно-аддитивных солей при изготовлении соответствующего лекарственного средства для терапевтического лечения различных форм ишемии.
МПК / Метки
МПК: C07D 295/00
Метки: новые, бензоилгуанидина, своиствами, изготовлении, эффективными, применение, производные, лекарственных, средств, способ, получения
Код ссылки
<a href="https://eas.patents.su/10-4687-novye-proizvodnye-benzoilguanidina-s-effektivnymi-svoistvami-sposob-ih-polucheniya-i-ih-primenenie-pri-izgotovlenii-lekarstvennyh-sredstv.html" rel="bookmark" title="База патентов Евразийского Союза">Новые производные бензоилгуанидина с эффективными своиствами, способ их получения и их применение при изготовлении лекарственных средств</a>
Предыдущий патент: Лекарственный препарат для перорального применения
Следующий патент: Способ выделения применимой в фармацевтике динатриевой соли этидроната
Случайный патент: Способ прогнозирования предрасположенности к развитию аддиктивного заболевания или расстройства (варианты)














