Способ получения гибридного покрытия на металлических имплантатах
Номер патента: 22035
Опубликовано: 30.10.2015
Авторы: Больбасов Евгений Николаевич, Шестериков Евгений Викторович, Твердохлебов Сергей Иванович
Формула / Реферат
Способ получения гибридного покрытия на металлических имплантатах, включающий высокочастотное магнетронное напыление кальций-фосфатного покрытия путем распыления мишени из гидроксиапатита Ca10(PO4)6(OH)2 в атмосфере аргона, отличающийся тем, что предварительно имплантаты помещают в вакуумную печь, производят откачку ее рабочего объема до давления от 5 до 10 Па, проводят оксидирование имплантатов в атмосфере кислорода в течение от 30 до 60 мин при температуре от 500 до 600°С и давлении от 2700 до 3300 Па, отключают нагрев и прекращают подачу кислорода, откачивают рабочий объем до давления от 5 до 10 Па и охлаждают имплантаты до температуры от 20 до 40°С, затем проводят высокочастотное магнетронное напыление кальций-фосфатного покрытия в течение от 200 до 320 мин в атмосфере аргона и кислорода при суммарном парциальном давлении газовой смеси 0,3 Па с соотношением аргона и кислорода в смеси 1/1, при подаче удельной мощности на гидроксиапатитовую мишень 20 Вт/см2.
Текст
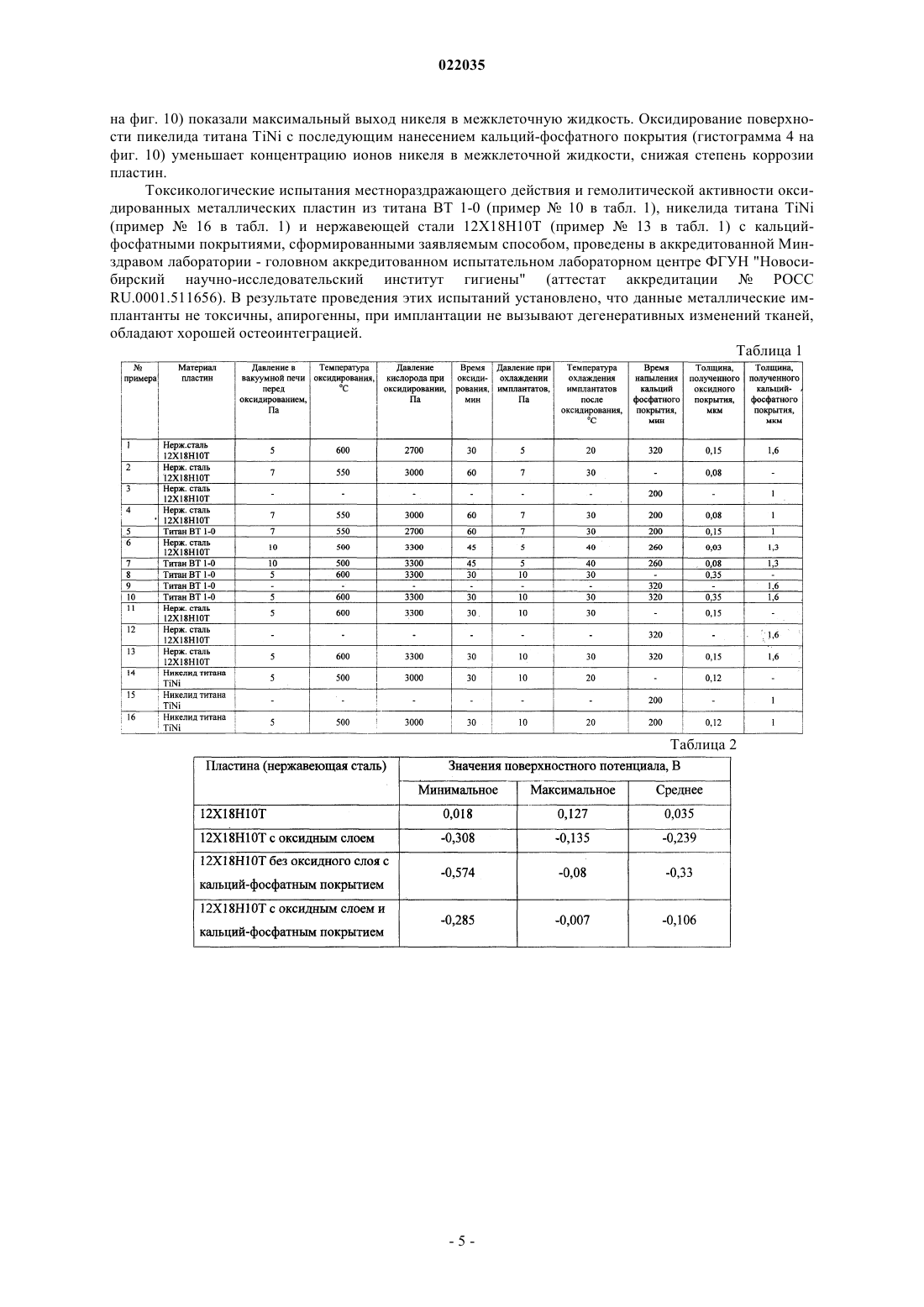
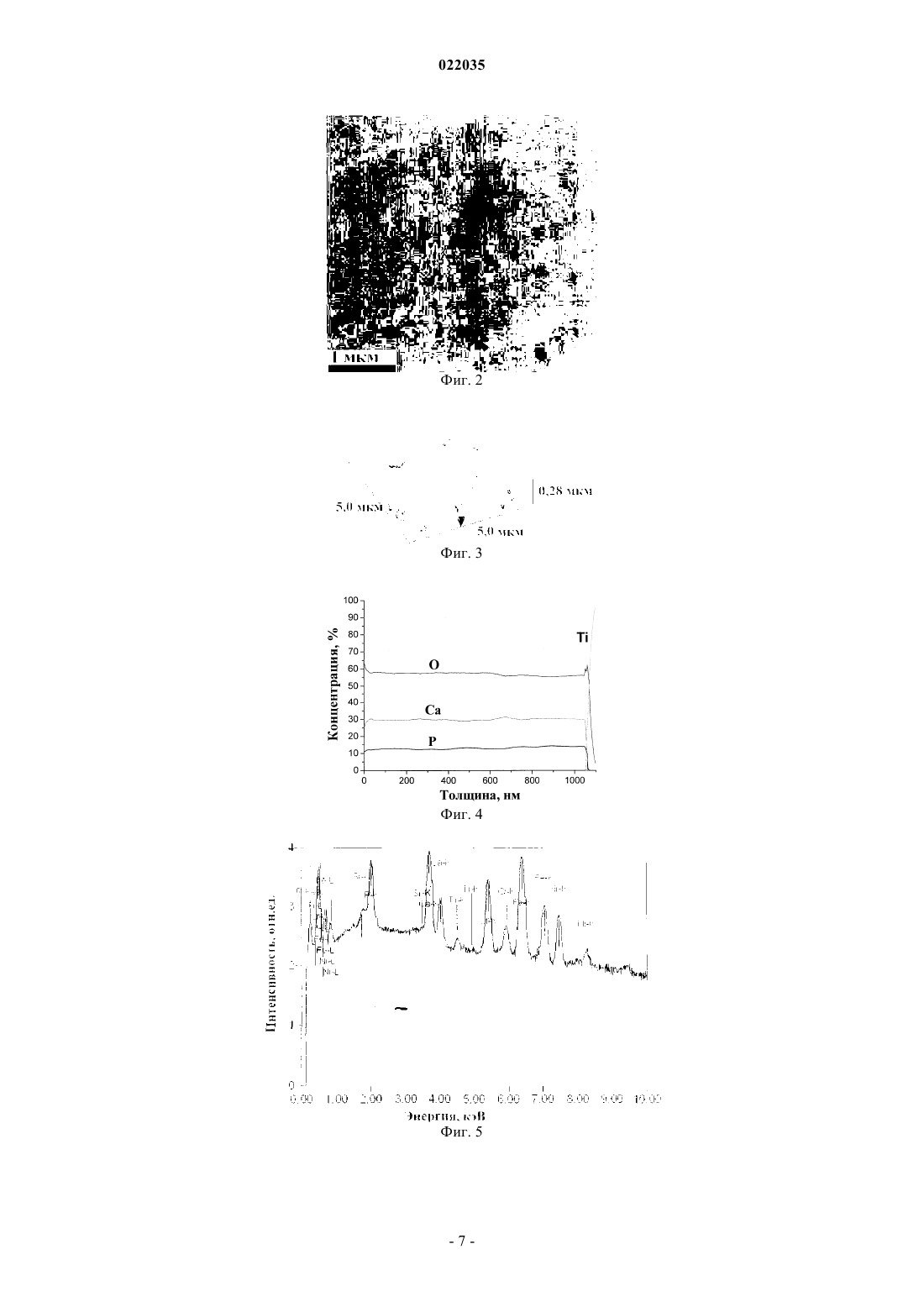
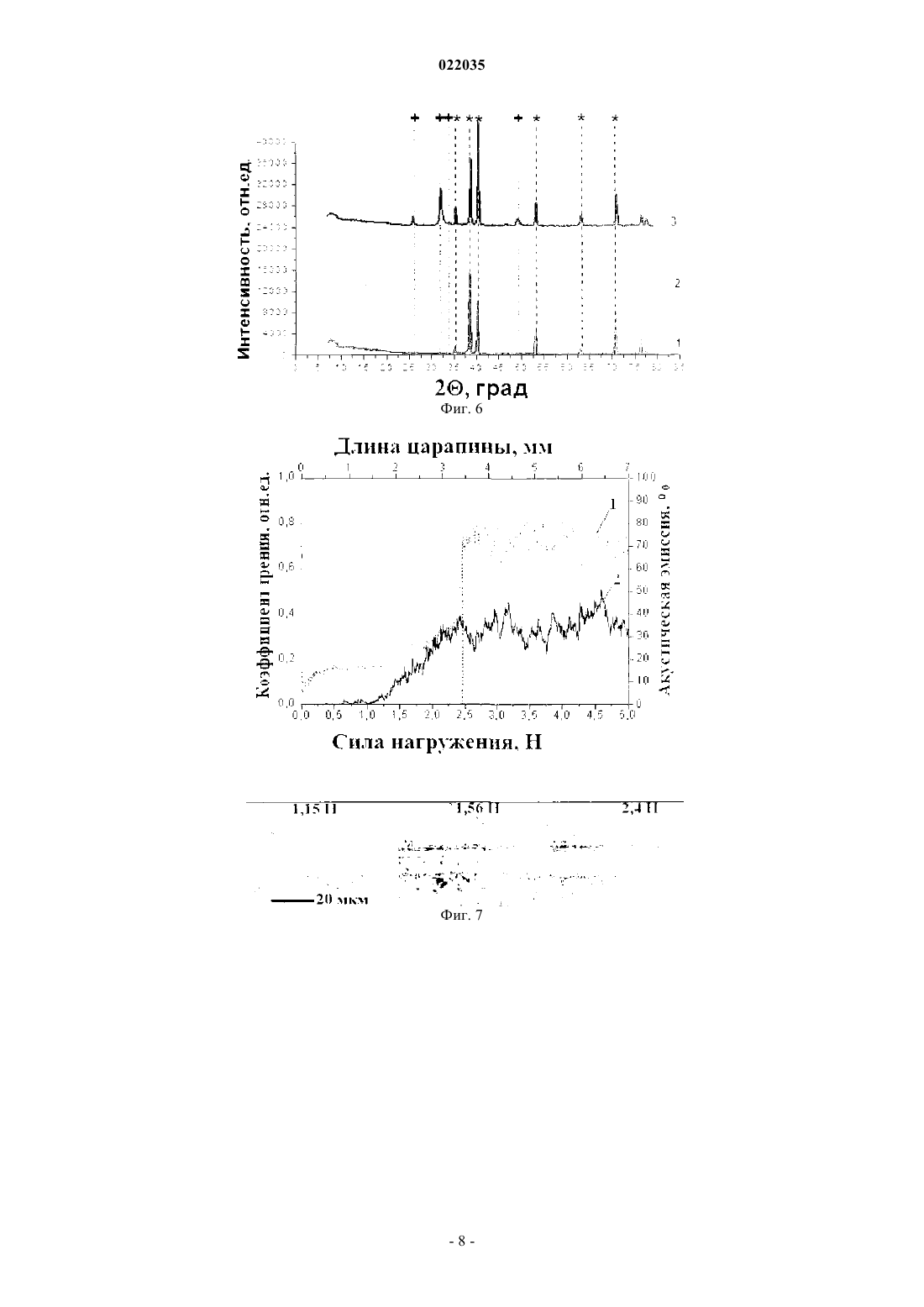
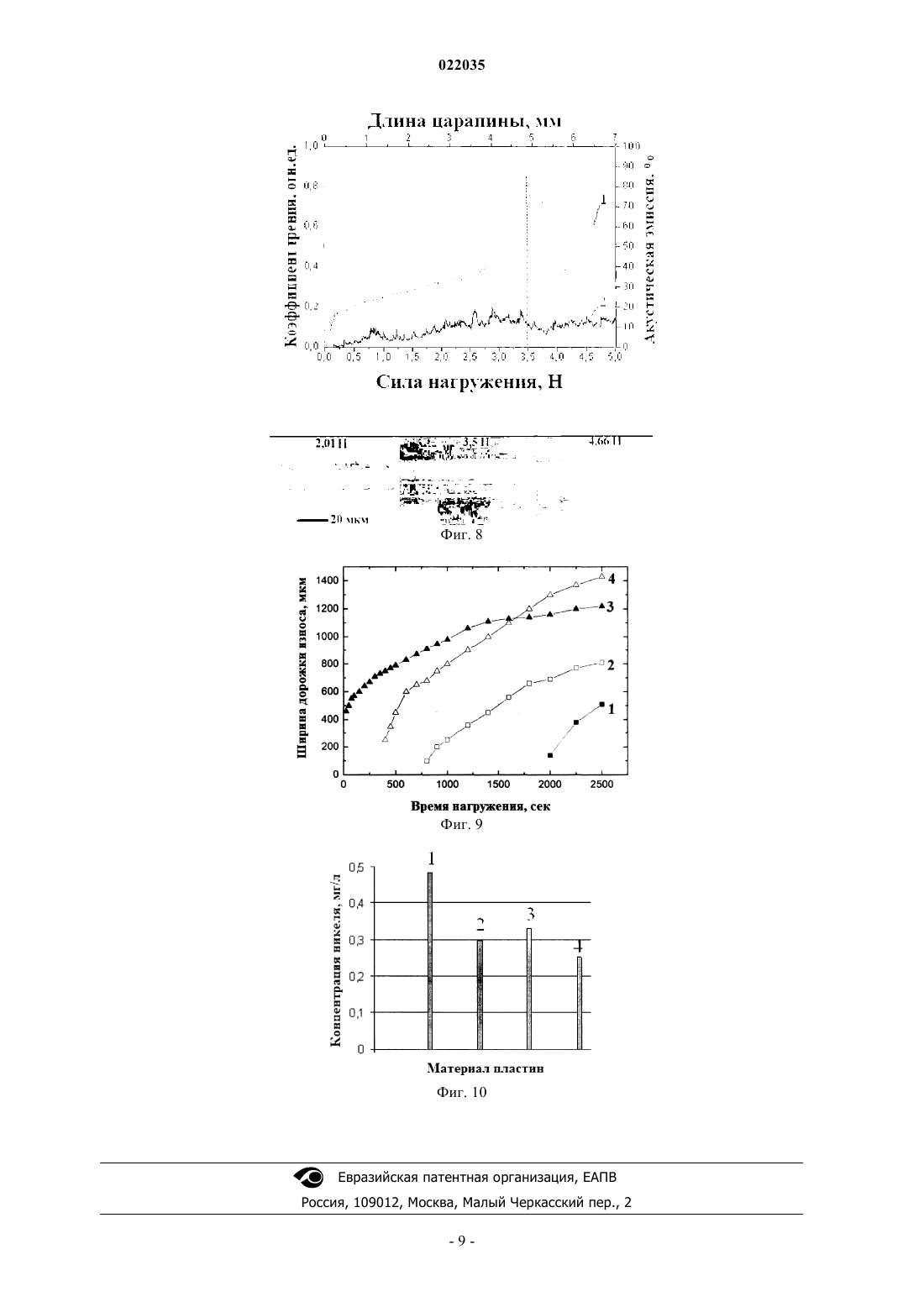
СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОГО ПОКРЫТИЯ НА МЕТАЛЛИЧЕСКИХ ИМПЛАНТАТАХWO-A1-2003003937 И.В. Родинов. Получение оксидных биосовместимых покрытий на чрескостных титановых имплантатах методом паротермического оксидирования. Перспективные материалы, 2009,5, с. 35-44 Изобретение относится к области медицины и может быть использовано для создания покрытия на имплантатах для остеосинтеза. Способ получения гибридного покрытия на металлических имплантатах заключается в том, что имплантаты помещают в вакуумную печь, производят откачку е рабочего объема до давления от 5 до 10 Па, проводят оксидирование имплантатов в атмосфере кислорода в течение от 30 до 60 мин при температуре от 500 до 600 С и давлении от 2700 до 3300 Па, отключают нагрев и прекращают подачу кислорода, откачивают рабочий объем до давления от 5 до 10 Па и охлаждают имплантаты до температуры от 20 до 40 С. Затем проводят высокочастотное магнетронное напыление кальций-фосфатного покрытия в течение от 200 до 320 мин в атмосфере аргона и кислорода при суммарном парциальном давлении газовой смеси 0,3 Па с соотношением аргона и кислорода в смеси 1/1, при подаче удельной мощности на гидроксиапатитовую мишень 20 Вт/см 2. Технический результат: получение гибридного покрытия, обладающего коррозионной стойкостью, высокими прочностными, износостойкими характеристиками и остеоинтеграционными свойствами.(71)(73) Заявитель и патентовладелец: ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ"НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ" (ФГБОУ ВПО НИ ТПУ) (RU) Изобретение относится к области медицины, а именно к покрытиям металлических имплантатов, и может быть использовано для создания гибридного биосовместимого покрытия на имплантатах для остеосинтеза. Известен способ получения тонких плотных кристаллических кальций-фосфатных покрытий[US 6419708 В 1, МПК 7 A61F 2/28, опубл. 16.07.2002 г.], включающий следующие стадии: размещение подложек над мишенью гидроксиапатита на расстоянии 50 мм, предварительную откачку рабочего объема до давления 1,3310-4 Па, напуск смеси рабочих газов (62,5% (об.) Ar + 12,5% (об.) Н 2 + 25,0% (об.)O2) в камеру до достижения давления 1,3310-1 Па, высокочастотное магнетронное распыление мишени при удельной мощности, приложенной к поверхности мишени, равной 2,2 Втсм-2, отжиг подложек с нанесенным покрытием в атмосфере Ar + H2O (1,3310-1 Па) в кварцевом реакторе при температуре 620 С продолжительностью 15 ч с целью кристаллизации аморфной фазы, обработку кальций-фосфатных покрытий в атмосфере O3 для очистки поверхности конденсата от углерода. Основными недостатками этого способа являются многостадийность процесса формирования кристаллических кальций-фосфатных покрытий; не сохранение фазового состава мишени, так как покрытие помимо гидроксиапатита содержит трикальций-фосфат; загрязнение кальций-фосфатных покрытий углеродом во время отжига; термическое воздействие на подложку при отжиге, приводящее в определенных случаях к ее разупрочнению. Известен способ получения кальций-фосфатного покрытия на образце [RU 2400423 С 1, МПК(2006.01) С 01 В 25/32, A61L 27/12, опубл. 27.09.2010 г.], который включает распыление мишени из стехиометрического гидроксиапатита - Ca10(PO4)6(OH)2 (Са/Р=1,67) в вакуумной камере в атмосфере аргона, где покрытие получают при плотности мощности высокочастотного разряда от 0,1 до 1 Вт/см 2, давлении аргона от 0,1 до 1 Па, отрицательном смещении на подложкодержателе от 0 до 100 В, расположении образцов как в области эрозии мишени, так и вне области эрозии мишени при времени формирования покрытия от 15 до 180 мин. Недостатками известного способа являются низкая скорость напыления кальций-фосфатного покрытия вследствие малой плотности мощности высокочастотного разряда, а также формирование кальций-фосфатного покрытия с преимущественной кристаллографической ориентацией [002], не характерной для гидроксиапатита. Известен способ получения на подложке кальций-фосфатного покрытия [RU 2372101 С 1, МПК(2006.01) A61L 27/32, С 30 В 23/02, С 30 В 29/10, В 82 В 3/00, опубл. 10.11.2009 г.], выбранный в качестве прототипа, в котором производят высокочастотное магнетронное распыление мишени из гидроксиапатита Ca10(PO4)6(OH)2 в течение 15-150 мин с использованием в качестве рабочего газа аргона при его давлении в рабочей камере 0,1 Па. Осаждение покрытия проводят на подложку, размещенную над кольцевой областью прикатодного пространства магнетрона, где силовыми линиями магнитного поля магнетрона локализована плазма высокочастотного разряда и воздействие заряженных частиц на подложку максимально, при удельной мощности высокочастотного разряда 50 Втсм-2. Основными недостатками этого технического решения являются большая неравномерность толщины и различный фазовый состав кальций-фосфатного покрытия по площади, формирование кальцийфосфатного покрытия с кристаллографической ориентацией [002], не характерной для стехиометрического гидроксиапатита. Кроме этого, не обеспечивается защита металлической основы имплантата от процессов электрохимической коррозии, возникающих после резорбции кальций-фосфатного покрытия. Задачей изобретения является получение гибридного покрытия на металлических имплантатах для остеосинтеза, обладающего коррозионной стойкостью, высокими прочностными, износостойкими характеристиками и остеоинтеграционными свойствами. Поставленная задача решена за счет того, что способ получения гибридного покрытия на металлических имплантатах, также как в прототипе, включает в себя высокочастотное магнетронное напыление кальций-фосфатного покрытия путем распыления мишени из гидроксиапатита Ca10(PO4)6(OH)2 в атмосфере аргона. Согласно изобретению предварительно имплантаты помещают в вакуумную печь, производят откачку е рабочего объема до давления от 5 до 10 Па, проводят оксидирование имплантатов в атмосфере кислорода в течение от 30 до 60 мин при температуре от 500 до 600 С и давлении от 2700 до 3300 Па. Отключают нагрев и прекращают подачу кислорода. Откачивают рабочий объем до давления от 5 до 10 Па и охлаждают имплантаты до температуры от 20 до 40 С. Затем проводят высокочастотное магнетронное напыление кальций-фосфатного покрытия в течение от 200 до 320 мин в атмосфере аргона и кислорода при суммарном парциальном давлении газовой смеси 0,3 Па с соотношением аргона и кислорода в смеси 1/1 и подаче удельной мощности на гидроксиапатитовую мишень 20 Вт/см 2. Известно, с позиции электрохимии и биомеханики, что толщина оксидной пленки на поверхности металлических имплантатов около 0,05 мкм является достаточной для их защиты от коррозии в организме (Биоматериалы и имплантаты для травматологии и ортопедии: монография. Т.С. Петровская, В.П. Шахов, В.И. Верещагин, В.П. Игнатов. - Томск: Изд-во Томского политехнического университета, 2011 г., с. 61). Экспериментально установлено, что в течение 30-60 мин в диапазоне температуры оксидирования 500-600 С формируется сплошное с высокой трещиноустойчивостью оксидное покрытие на всех типах металлических имплантатов без изменения их прочностных характеристик. Варьируя температурой в этом диапазоне, можно получать оксидное покрытие различной толщины. После 30 мин оксидирования при одной и той же температуре толщина оксидной пленки на поверхности металлических имплантатов в течение следующих 30 мин увеличивается на 5-8%. Поэтому время оксидирования в диапазоне 30-60 мин при фиксированной температуре является оптимальным. При оксидировании ниже 500 С формируется оксидная пленка на поверхности нержавеющей стали 12 Х 18 Н 10 Т менее 0,03 мкм, что недостаточно для образования барьерного слоя, препятствующего выходу легирующих компонентов материала в биологическую среду организма. При температуре в процессе оксидирования более 600 С нарушаются свойства металлических материалов: у титана ВТ 1-0 резко возрастает средний размер зерна с 1,4 мкм до 15 мкм [И.А. Курзина, Ю.П. Шаркеев, И.А. Ерошенко, Э.В. Козлов. Структурно-фазовое состояние титана с разным размером зерна, имплантированного ионами алюминия. Фазовые переходы, упорядоченные состояния и новые материалы,6, 2010 г.]; никелид титана TiNi охрупчивается [RU 2356966 С 1, МПК (2006.01) С 22 С 01/04, В 22F 3/24, А 61F 2/02, опубл. 27.05.2009 г.]; у нержавеющей стали 12 Х 18 Н 10 Т возрастает окисляемость титана из-за усиленного поглощения O2, а также уменьшается термодинамическая устойчивость интерметаллида FeNi и оксидаFe2O3, что сопровождается сильным снижением уровня механической прочности металлооксида [Родионов И.В. Воздушно-термические оксидные покрытия на ортопедических имплантатах: структура, свойства и функциональные особенности: Предварительное вакуумирование рабочего объема вакуумной печи, используемой для оксидирования металлических имплантатов, до давления 5-10 Па позволяет проводить их оксидирование в сверхчистом кислороде при давлении ниже атмосферного в диапазоне 2700-3300 Па. Это многократно снижает расход кислорода в процессе оксидирования и исключает его утечку в помещение. После оксидирования требуется охлаждение в камере вакуумной печи металлических имплантатов до температуры ниже 40 С. Это исключает любые изменения свойств оксидированной поверхности имплантатов при напуске в рабочий объем воздушной атмосферы. При этом остаточное давление в камере 5-10 Па в процессе охлаждения исключает попадание в камеру посторонних газов и позволяет сократить расход кислорода. При удельной высокочастотной мощности на мишени менее 20 Вт/см 2 существенно снижается скорость напыления кальций-фосфатных покрытий, а увеличение высокочастотной удельной мощности более 20 Вт/см 2 приводит к разогреву стенок вакуумной камеры и постепенному выходу из строя е резиновых уплотнений. В атмосфере рабочего газа аргона и кислорода при суммарном парциальном давлении газовой смеси 0,3 Па с соотношением аргона и кислорода в смеси 1/1 формируются кальций-фосфатные покрытия,по молекулярному соотношению элементов, химическим связям и структуре близкие к гидроксиапатиту. В течение 320 мин напыления формируются кальций-фосфатные покрытия толщиной 1,6 мкм. Как показали исследования, разрушение кальций-фосфатных покрытий толщиной менее 1,6 мкм происходит только после проникновения наноиндентора до границы раздела покрытие-подложка, тогда как покрытия с большей толщиной разрушаются в результате отслоения и появления сколов вдоль направления царапания при небольших значениях силы нагружения [The preparation of calcium phosphate coatings onS.I., Prymak O., Epple M. Surface and Coatings Technology. 2008. T. 202.16. С. 3913-3920]. В течение 200 мин напыления формируются кальций-фосфатные покрытия толщиной 1 мкм, которые не позволяют полностью прокрывать боковые стенки отверстий и прорезей в имплантатах, что приводит к ухудшению их остеоинтеграционных свойств. Таким образом, предложенный способ позволяет получать гибридные покрытия на металлических имплантатах для остеосинтеза, обладающие коррозионной стойкостью, высокими прочностными, износостойкими характеристиками и остеоинтеграционными свойствами. В табл. 1 приведены режимы формирования покрытий и их толщины на различных металлических имплантатах. В табл. 2 приведены величины поверхностного потенциала образцов из нержавеющей стали 12 Х 18 Н 10 Т. В табл. 3 приведены модуль упругости, нанотвердость и упругое восстановление различных пластин при нагрузке 1-5 мН. На фиг. 1 представлена фотография, в нижней части которой изображен внешний вид кальцийфосфатного покрытия, а в верхней части - поверхность пластины оксидированной нержавеющей стали 12 Х 18 Н 10 Т, с которой снято кальций-фосфатное покрытие. На фиг. 2 представлена фотография внешнего вида кальций-фосфатного покрытия, представленно-2 022035 го на фиг. 1, в увеличенном масштабе. На фиг. 3 приведена морфология кальций-фосфатного покрытия, сформированного на оксидированной нержавеющей стали 12X18H10 Т. На фиг. 4 приведен профиль концентрации по толщине основных элементов кальций-фосфатного покрытия на оксидированной пластине из титана ВТ 1-0. На фиг. 5 приведен энергодисперсионный спектр кальций-фосфатного покрытия на оксидированной пластине из нержавеющей стали 12 Х 18 Н 10 Т. На фиг. 6 приведены рентгеновские дифрактограммы: 1 - оксидированной титановой пластины ВТ 1-0; 2 - гидроксиапатитовой мишени; 3 - кальций-фосфатного покрытия, нанесенного на оксидированную титановую пластину ВТ 1-0; гдеобозначены пики титана, + обозначены пики гидроксиапатита. На фиг. 7 приведены зависимости коэффициента трения (кривая 1), сигнала акустической эмиссии(кривая 2) от силы нагружения индентора и фотографии следов разрушения кальций-фосфатных покрытий на пластине из нержавеющей стали 12X18H10 Т без оксида. На фиг. 8 приведены зависимости коэффициента трения (кривая 1), сигнала акустической эмиссии(кривая 2) от силы нагружения индентора и фотографии следов разрушения кальций-фосфатных покрытий на пластине из нержавеющей стали 12 Х 18 Н 10 Т с оксидом. На фиг. 9 приведены зависимости величины износа кальций-фосфатных покрытий от времени нагружения, где кривая: 1 - для пластины из нержавеющей стали 12 Х 18 Н 10 Т с оксидом, 2 - для пластины из нержавеющей стали 12 Х 18 Н 10 Т без оксида, 3 - для пластины из титана ВТ 1-0 без оксида, 4 - для пластины из титана ВТ 1-0 с оксидом. На фиг. 10 приведены гистограммы средних концентраций никеля в межклеточной жидкости при контакте никелид титановых TiNi пластин с различным типом покрытия с миелокариоцитами "in vitro" в течение 1 ч при 37 С, где 1 - для пластины чистого никелид титана TiNi; 2 - для пластины никелид титана TiNi с кальций-фосфатным покрытием; 3 - для пластины оксидированного никелид титана TiNi; 4 для пластины оксидированного никелид титана TiNi с кальций-фосфатным покрытием. Способ получения гибридного покрытия на металлических имплантатах реализован следующим образом. Металлические имплантаты, изготовленные в виде пластин размером 10101 мм из нержавеющей стали 12 Х 18 Н 10 Т, титана ВТ 1-0, никелида гитана TiNi, помещали в вакуумную печь "ОКБ-8092", вакуумировали е рабочий объем до давления 5-10 Па. Затем осуществляли оксидирование металлических имплантатов в атмосфере кислорода в течение 30-60 мин при температуре 500-600 С и давлении 27003300 Па. Отключали нагрев и прекращали подачу кислорода, откачивали рабочий объем вакуумной печи до давления от 5 до 10 Па, охлаждали имплантаты до температуры 20-40 С и вынимали из печи. Затем на оксидированные имплантанты производили высокочастотное магнетронное напыление кальцийфосфатного покрытия на установке "КАТОД-1 М" путем распыления гидроксиапатитовой мишениCa10(PO4)6(OH)2 в течение 200-320 мин в атмосфере аргона и кислорода при суммарном парциальном давлении газовой смеси 0,3 Па с соотношением аргона и кислорода в смеси 1/1 при подаче удельной мощности на мишень 20 Вт/см 2. Режимы формирования гибридного покрытия на металлических имплантатах приведены в табл. 1. Указанные в табл. 1 толщины оксидных покрытий измеряли методом калотеста на установке "CALOTEST". Толщины кальций-фосфатных покрытий измеряли методом профилометрии на установке"AMBIOS technology XP-2". Исследование внешнего вида и морфологии покрытий проводили на электронном микроскопе"RAITH 150-TWO" и на атомно-силовом микроскопе Solver-HV. Сравнительный анализ поверхности кальций-фосфатного покрытия, сформированного на пластине из оксидированной нержавеющей стали 12X181110 Т (пример 1 в табл. 1) с исходной поверхностью оксидированной пластины 12 Х 18 Н 10 Т (фиг. 1-3), показывает, что кальций-фосфатное покрытие увеличивает параметры шероховатости оксидированной нержавеющей пластины 12 Х 18 Н 10 Т с Ra=0,026 мкм,Rz=0,143 мкм до Ra=0,045 мкм, Rz=0,213 мкм, где Ra - среднее арифметическое отклонение профиля,Rz - высота неровностей профиля по десяти точкам. Структура кальций-фосфатного покрытия, сформированного на оксидированной нержавеющей стали 12 Х 18 Н 10 Т, плотная, однородная и не содержит видимых дефектов. В процессе оксидирования и напыления кальций-фосфатного покрытия изменялась величина поверхностного потенциала металлических имплантатов. Значения поверхностных потенциалов пластин из нержавеющей стали 12 Х 18 Н 10 Т (примеры 2-4 в табл. 1) были измерены на атомно-силовом микроскопе Solver-HV и представлены в табл. 2. Так, заряженная положительно исходная поверхность пластины из нержавеющей стали 12X18H10 Т после оксидирования и формирования кальций-фосфатного покрытия приобрела отрицательный заряд. Следовательно, поверхность пластины притягивает положительно заряженные ионы Са 2+, находящиеся в организме, что способствует сначала образованию промежуточных кальцийсодержащих фаз, а затем устойчивого в средах организма слоя гидроксиапатита. Элементный состав кальций-фосфатных покрытий, полученных на оксидированных пластинах, оп-3 022035 ределяли на оже-спектрофотометре "Шхуна-2" и на сканирующем электронном микроскопе JSM-7500F со встроенной приставкой для энергодисперсионного анализа "Quanta 200 ESEM FEG". По результатам оже-спектроскопии концентрация элементов (фиг. 4), входящих в состав кальцийфосфатного покрытия, сформированного на оксидированной титановой пластине ВТ 1-0 (пример 5 в табл. 1), практически постоянна по всей его толщине, при этом молекулярное отношение Са/Р=1,720,09. Результаты энергодисперсионного анализа (фиг. 5) кальций-фосфатного покрытия, сформированного на оксидированной пластине из нержавеющей стали 12 Х 18 Н 10 Т (пример 6 в табл. 1), дают отношение Са/Р=1,63, близкое к гидроксиапатитовой мишени, для которой Са/Р=1,67. Фазовый состав кальций-фосфатных покрытий оценивали методом рентгеновской дифракционной спектроскопии с помощью дифрактометра "ДРОН 3 М". Кальций-фосфатное покрытие, сформированное на оксидированной титановой пластине ВТ 1-0(пример 7 в табл. 1) имеет на дифрактограмме (фиг. 6) рефлексы при 25,89 (002), 31,77 (211), 34,05(202), 49,47 (213), соответствующие гидроксиапатиту, и рефлексы при 35,09; 38,42; 40,17; 53,00; 62,95; 70,66, соответствующие титановой пластине ВТ 1-0. Пиков других соединений кальцийфосфатов, таких как -трикальций-фосфат (TCP-Ca3(PO4)2), тетракальций-фосфат (ТТСР-Ca4P2O9), СаО в кальций-фосфатном покрытии нет. Преимущественная ориентация кристаллических граней в кальцийфосфатном покрытии в плоскости [211] такая же, как у гидроксиапатитовой мишени. Таким образом, молекулярное соотношение элементов и структура кальций-фосфатного покрытия свидетельствует о его близком соответствии с гидроксиапатитом. Величины нанотвердости Н, модуля упругости E и упругого восстановления R металлических пластин и сформированных на них покрытий определяли с помощью нанотвердомера "NanoTest 600" при нагрузке на индентор 1-5 мН. Как видно из табл. 3, низкий модуль упругости и высокая нанотвердость кальций-фосфатного покрытия на металлических пластинах из титана ВТ 1-0 и нержавеющей стали 12 Х 18 Н 10 Т (примеры 813 в табл. 1) увеличивают их прочностные характеристики, что благоприятно с точки зрения переноса костью функциональных нагрузок и стимулирования нарастания костной ткани. Комбинация высокой твердости и упругого восстановления характеризует кальций-фосфатное покрытие, как твердый и в то же время упругий материал, что является важнейшим фактором для имплантатов, работающих под нагрузкой. Оценку величины адгезии кальций-фосфатных покрытий, нанесенных на пластины из нержавеющей стали 12 Х 18 Н 10 Т без оксидного слоя и с оксидным слоем, проводили методом склерометрии с использованием алмазного индентора типа "Роквелла" с радиусом скругления наконечника 20 мкм на установке "Micro Scratch Tester". Предварительное оксидирование пластин из нержавеющей стали 12 Х 18 Н 10 Т (примеры 12, 13 в табл. 1) значительно увеличивает прочность сцепления кальций-фосфатных покрытий с поверхностью пластины за счет образования прочных химических связей между покрытием и диэлектрическим оксидным слоем в процессе магнетронного напыления. Разрушение кальций-фосфатного покрытия на пластине из нержавеющей 12X18H10T без оксида наступает при нагрузке на индентор 2,4 Н (фиг. 7), тогда как на оксидированной пластине из нержавеющей стали 12X18H10 Т - при нагрузке 3,5 Н (фиг. 8). Наблюдаемый характер разрушений кальций-фосфатного покрытия указывает на незначительные уровни внутренних остаточных напряжений, особенно на предварительно оксидированных пластинах. Это говорит о высоких прочностных свойствах кальций-фосфатных покрытий, получаемых заявляемым способом. Износостойкость кальций-фосфатных покрытий на различных пластинах исследовали методом трибологических испытаний по схеме "палец-диск" в условиях сухого трения на установке "УМТ-1". В качестве контртела при испытаниях на износ использованы шарики диаметром 3 мм, изготовленные из закаленной стали ШХ 15. Интенсивность износа кальций-фосфатных покрытий (примеры 9, 10, 12, 13 в табл. 1) на стадии приработки от 0 до 1000 с, сформированных в различных режимах на пластине из титана ВТ 1-0 с окислом и без (кривая 3 и 4 на фиг. 9), в разы больше, чем па пластине из нержавеющей стали 12 Х 18 Н 10 Т с окислом и без (кривая 1 и 2 на фиг. 9). Минимальную кривую износа имеет оксидированная пластина из нержавеющей стали 12 Х 18 Н 10 Т с кальций-фосфатным покрытием (кривая 1 на фиг. 9), причем на стадии приработки износа не наблюдали. Во всех случаях после износа отсутствовали трещины и сколы по краям дорожки трения, что подтверждает высокие износостойкие свойства и трещиноустойчивость кальцийфосфатных покрытий. Изучение коррозионной стойкости проводили путем растворения никелид титановых TiNi пластин с кальций-фосфатными покрытиями с учетом требований ISO 10993-5 в условиях их одночасового культивирования при температуре 37 С в среде RPMI-1640, объемом 2 мл, содержащей костный мозг мышейCBA/CaLac. Межклеточную жидкость отделяли от клеток посредством центрифугирования при ускорении 500 g в течение 10 мин, затем методом инверсионной вольтамперометрии определяли концентрацию никеля. Контакт никелид титановых TiNi пластин (примеры 14-16 в табл. 1) с межклеточной жидкостью (фиг. 10) не сопровождался существенным выходом никеля из пластин в жидкость и увеличением гибели клеток костного мозга мышей. Никелид титановые TiNi пластины без покрытия (гистограмма 1 на фиг. 10) показали максимальный выход никеля в межклеточную жидкость. Оксидирование поверхности пикелида титана TiNi с последующим нанесением кальций-фосфатного покрытия (гистограмма 4 на фиг. 10) уменьшает концентрацию ионов никеля в межклеточной жидкости, снижая степень коррозии пластин. Токсикологические испытания местнораздражающего действия и гемолитической активности оксидированных металлических пластин из титана ВТ 1-0 (пример 10 в табл. 1), никелида титана TiNi(пример 16 в табл. 1) и нержавеющей стали 12 Х 18 Н 10 Т (пример 13 в табл. 1) с кальцийфосфатными покрытиями, сформированными заявляемым способом, проведены в аккредитованной Минздравом лаборатории - головном аккредитованном испытательном лабораторном центре ФГУН "Новосибирский научно-исследовательский институт гигиены" (аттестат аккредитацииРОССRU.0001.511656). В результате проведения этих испытаний установлено, что данные металлические имплантанты не токсичны, апирогенны, при имплантации не вызывают дегенеративных изменений тканей,обладают хорошей остеоинтеграцией. Таблица 1 ФОРМУЛА ИЗОБРЕТЕНИЯ Способ получения гибридного покрытия на металлических имплантатах, включающий высокочастотное магнетронное напыление кальций-фосфатного покрытия путем распыления мишени из гидроксиапатита Ca10(PO4)6(OH)2 в атмосфере аргона, отличающийся тем, что предварительно имплантаты помещают в вакуумную печь, производят откачку е рабочего объема до давления от 5 до 10 Па, проводят оксидирование имплантатов в атмосфере кислорода в течение от 30 до 60 мин при температуре от 500 до 600 С и давлении от 2700 до 3300 Па, отключают нагрев и прекращают подачу кислорода, откачивают рабочий объем до давления от 5 до 10 Па и охлаждают имплантаты до температуры от 20 до 40 С, затем проводят высокочастотное магнетронное напыление кальций-фосфатного покрытия в течение от 200 до 320 мин в атмосфере аргона и кислорода при суммарном парциальном давлении газовой смеси 0,3 Па с соотношением аргона и кислорода в смеси 1/1, при подаче удельной мощности на гидроксиапатитовую мишень 20 Вт/см 2.
МПК / Метки
МПК: A61L 27/40, C23C 28/00, C23C 8/10, A61L 27/32
Метки: металлических, имплантатах, гибридного, покрытия, способ, получения
Код ссылки
<a href="https://eas.patents.su/10-22035-sposob-polucheniya-gibridnogo-pokrytiya-na-metallicheskih-implantatah.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения гибридного покрытия на металлических имплантатах</a>
Следующий патент: Огнеупорный, керамический ударопоглощающий стакан
Случайный патент: Пара для тихоходного трения