Способ получения липидных комплексов или липосом водонерастворимого диаминоциклогександикарбоксилата платины
Формула / Реферат
1. Способ получения липидных комплексов или липосом водонерастворимого диаминоциклогександикарбоксилата платины путем добавления к водному раствору диаминоциклогексаннитрата платины раствора фосфолипида в неводном растворителе и дикарбоновой кислоты с последующим удалением указанного неводного растворителя.
2. Способ по п.1, где указанный водонерастворимый диаминоциклогександикарбоксилат платины представляет собой соединение общей формулы
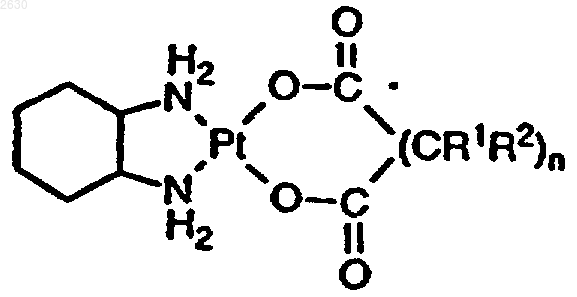
где R1 и R2 являются одинаковыми или различными и представляют собой атом водорода, C1-С10 алкил, С6-С10 арил, C7-C18 алкарил, С7-С10 аралкил, или R1 и R2 входят в состав замещенного или незамещенного, насыщенного или ненасыщенного 4, 5, или 6 членного кольца, или R1 и R2 могут объединяться с заместителями R1 и R2 при соседнем атоме углерода с образованием замещенного или незамещенного, насыщенного или ненасыщенного 4, 5, или 6-членного кольца и n равно 0-10.
3. Способ по п.2, где указанный дикарбоксилат Pt выбирают из группы, состоящей из диаминоциклогексаноксалата-Pt, диаминоциклогексанмалоната-Pt, диаминоциклогексансукцината-Pt, диаминоциклогексанглутурата-Pt, диаминоциклогексанадипата-Pt, диаминоциклогексанпимелата-Pt, диаминоциклогексанмалеата-Pt, диаминоциклогексанфумарата-Pt, диаминоциклогексанфталата-Pt и диаминоциклогексантартрата-Pt.
4. Способ по п.1, где указанную карбоновую кислоту выбирают из группы, состоящей из янтарной кислоты, глутаровой кислоты, адипиновой кислоты, пимелиновой кислоты, малеиновой кислоты, фумаровой кислоты, азелаиновой кислоты, пробковой кислоты, себациновой кислоты, винной кислоты и фталевой кислоты.
5. Способ по п.3, где указанный диаминоциклогександикарбоксилат-Pt представляет собой диаминоциклогексанмалонат-Pt.
6. Способ по п.1, где указанный фосфолипид выбирают из группы, состоящей из димиристоилфосфатидилхолина, димиристоилфосфатидилглицерина, дистеароилфосфатидилхолина, дистеароилфосфатидилглицерина и их любого сочетания.
7. Способ по п.6, где указанный фосфолипид представляет собой смесь димиристоилфосфатидилхолина и димиристоилфосфатидилглицерина.
8. Способ по п.7, где указанный димиристоилфосфатидилхолин присутствует в весовом отношении к указанному димиристоилфосфатидилглицерину, равном приблизительно 7:3.
9. Способ по п.1, где указанный комплекс указанного фосфолипида и указанного водонерастворимого дикарбоксилата-Pt образует коллоидную дисперсию при воспроизведении в фармацевтически приемлемом водном растворителе.
10. Способ по п.1, где указанный комплекс указанного фосфолипида и указанный водонерастворимый комплекс дикарбоксилата-Pt находится в лиофилизованном состоянии.
11. Способ по п.10, где к комплексу добавлен фармацевтически приемлемый эксципиент.
12. Способ по п.11, где указанный эксципиент представляет собой маннит.
13. Способ по п.10, где к комплексу добавлен холестерин или его полусукцинатные производные.
14. Способ по п.10, где указанный липидный комплекс образует коллоидную дисперсию при воспроизведении в физиологически приемлемом водном растворителе.
Текст
1 Настоящее изобретение относится к липидным комплексам или липосомам совершенно нерастворимых комплексов платины и, более конкретно, к фосфолипидному комплексу дикарбоксилата платины, который может быть повторно составлен с фармацевтически приемлемым носителем, с лиофилизацией или без нее,и назначен пациенту при лечении рака и других заболеваний. Несколько комплексов платины продемонстрировали отличную активность против рака. Клиническое использование таких комплексов было в некоторой степени ограничено из-за нерастворимости комплекса в фармацевтически приемлемых носителях. Например было показано, что диаминоциклогексановые (ДАЦ) комплексы с платиновыми соединениями являются активными против нескольких типов рака. Однако диаминоциклогексановые комплексы платины совершенно нерастворимы в водных носителях и многих органических растворителях. Нерастворимость диаминоциклогексан-платины в органических растворителях препятствует их инкапсулированию в липосомах или их использованию в липидных комплексах известными способами. Соответственно, существует потребность в солюбилизированной, фармацевтически стабильной форме существенно нерастворимых частиц, таких как комплексы ДАЦ-платина. Сущность изобретения Целью настоящего изобретения является разработка растворимой, фармацевтически приемлемой формы дозировки для нерастворимых в воде комплексов платины. Другой целью этого изобретения является разработка фосфолипидных комплексов или липосом для диаминоциклогексановых комплексов платины. Еще одной целью изобретения является разработка лиофилизированной фармацевтически приемлемой формы дозировки диаминоциклогексан-платина-фосфолипидных комплексов или липосом. Хотя это изобретение в последующем будет описано в отношении получения липидных комплексов или липосом диаминоциклогексанмалонат платины и продуктов лиофилизации липидных комплексов диаминоциклогексанмалонат платины, квалифицированные специалисты в этой области техники могут признать,что рекомендованные здесь способы также применимы для получения липидных комплексов или липосом и продуктов лиофилизации других комплексов платины, которые считаются нерастворимыми в воде и не могут быть введены посредством инъекции или инфузии. В соответствии с конкретным воплощением настоящего изобретения предоставляются фосфолипидные комплексы или липосомы диаминоциклогександикарбоксилата платины, которые могут быть повторно воссозданы в фар 002630 2 мацевтически приемлемом водном разбавителе,таком как вода для инъекции. Растворимый фосфолипидный комплекс диаминоциклогександикарбоксилат платины получают in situ по способу, который включает взаимодействие диаминоциклогексана с тетрахлорплатинатом калия и йодистым калием, чтобы образовался диаминоциклогексаниодид платины с последующим взаимодействием диаминоциклогексаниодид платины с нитратом серебра, с образованием диаминоциклогексаннитрат платины. Затем ДАЦ-нитрат платины одновременно взаимодействует с фосфолипидом в растворе хлороформ/этанол и с карбоновой кислотой с образованием продукта - липидного комплекса диаминоциклогександикарбоксилат платины. Было установлено, что карбоксилирование комплекса платины значительно уменьшает его растворимость в воде. В соответствии с изобретением, посредством откладывания карбоксилирования, до тех пор пока не образуется липидный комплекс или липосома, растворимость платиновых частиц поддерживается на таком уровне, что для образования липидных комплексов или липосом имеется раствор этого комплекса. Диаминоциклогександикарбоксилаты платины настоящего изобретения также можно получить в виде липосом. Липосомы подробно описаны в литературе, а их структура хорошо известна. В настоящем изобретении липосомы получают путем образования пленки активного компонента, в данном случае диаминоциклогексаннитрат платины и фосфолипида, добавляя карбоновую кислоту и выпаривая растворитель фосфолипида, например хлороформ/этанол,чтобы образовалась пленка, добавляют воду для инъекции и окончательно гомогенизируют полученную липосому. Сведения, подтверждающие возможность осуществления изобретения Термин "липидный комплекс" является признанным термином уровня техники при приготовлении фармацевтических композиций. Липидные комплексы характеризуются нековалентным связыванием между липидом и фармацевтическим соединением, которое наблюдается как фазовое изменение в дифференциальной сканирующей калориметрии. Используемый здесь термин "фармацевтически приемлемый водный разбавитель" относится к воде для инъекций, физиологическому раствору и другим известным водным носителям. Термин "вспомогательное средство лиофилизации" относится к веществу, которое добавляют в раствор до лиофилизации, чтобы усилить такие характеристики как цвет, текстуру,прочность и объем комка. Примеры вспомогательных средств лиофилизации приведены ниже. 3 В соответствии с одним воплощением настоящего изобретения, липидные комплексы диаминоциклогексан-платиновых комплексов получают согласно следующей схеме реакции: Как показано выше, на первой стадии диаминоциклогексан (1), тетрахлорплатинат калия(2) и иодид калия (3) в стехиометрических количествах взаимодействуют в воде с образованием диаминоциклогексаниодид платины (4),которая только слабо растворима в воде. Добавляют раствор нитрата серебра (5) к диаминоциклогексаниодид платине (4), чтобы образовался диаминоциклогексаннитрат платины (6). Этот диаминоциклогексаннитрат платины (6) растворим в воде, но не используется в качестве неопластического агента, из-за его нефротоксичных свойств. Подходящий фосфолипид (7),предпочтительно смесь димиристоилфосфатидилхолина (DMPC) и димиристоилфосфатидилглицерина (DMPG), в растворе хлороформ/этанол, добавляют к диаминоциклогексаннитрат платине (6) одновременно с избытком дикарбоновой кислоты (8), такой как малоновая кислота (показана на схеме). При удалении растворителя хлороформ/этанол посредством продувки азотом образуется диаминоциклогександикарбоксилат платина (9), которая в то же самое время образует комплекс с фосфолипидом. Затем продукт - комплекс диаминоциклогександикарбоксилат платины - центрифугируют и повторно суспендируют в воде для инъекции. Хотя указанная выше методика посвящена получению комплексов диаминоциклогексана,специалист в этой области техники может признать, что можно использовать другие лиганды или хелатные агенты, чтобы обеспечить образование других комплексов. Карбоновые кислоты, используемые в настоящем изобретении для получения диаминоциклогександикарбоксилатов платины, включают щавелевую кислоту, малоновую кислоту,янтарную кислоту, глутаровую кислоту, адипиновую кислоту, пимелиновую кислоту, малеиновую кислоту, фумаровую кислоту, азелаиновую кислоту, пробковую кислоту, себациновую кислоту, винную кислоту, фталевую кислоту и т.п. Эта кислота может быть замещенной или незамещенной. В предпочтительном варианте этого изобретения выбранной кислотой является малоновая. Диаминоциклогександикарбоксилаты платины, используемые в настоящем изобретении,имеют следующую структуру: где R1 и R2 являются одинаковыми или различными и представляют собой атом водорода, C1-С 10 алкил,С 6-С 10 арил, C7-C18 алкарил, C7-C18 аралкил или R1 иR2 могут образовать замещенное или незамещенное, насыщенное или ненасыщенное, 4-, 5- или 6 членное кольцо, или R1 и R2 могут объединиться с заместителями R1 и R2 при соседнем атоме углерода с образованием замещенного или незамещенного, насыщенного или ненасыщенного, 4-, 5- или 6 членного кольца; и n равно 0-10. Обычно диаминоциклогексанкарбоксилатом платины является диаминоциклогексаноксалат платины; диаминоциклогексанмалонат платины, диаминоциклогексансукцинат платины, диаминоциклогексанглутарат платины,диаминоциклогексанадипинат платины, диаминоциклогексанпимелат платины, диаминоциклогексанмалеат платины, диаминоциклогексанфумарат платины, диаминоциклогексанфталат платины и диаминоциклогексантартрат. Предпочтительным диаминоциклогександикарбоксилатом платины является диаминоциклогексанмалонат платины или диаминоциклогексанмалонат платины, в котором малонат замещен,например алкильной группой или подобной группой, такой как бутильная группа. Органический растворитель, используемый для получения раствора фосфолипидов,должен быть совместимым с фосфолипидами и не вызывать их дестабилизацию, или комплекса диаминоциклогексаннитрат платины. Кроме того, липиды должны обладать достаточной растворимостью в растворителе, с тем чтобы ввести достаточное количество липида для образования комплекса, и еще минимизировать количество растворителя, который позднее должен быть удален. Наиболее предпочтительным является летучий или малолетучий растворитель, который можно легко удалить из дисперсии липидного комплекса. Наиболее типичным растворителем, применяемым для получения этого раствора, является хлороформ, этанол,или хлористый метилен, или их смеси. В настоящем изобретении хорошие результаты обеспечивает смесь хлороформа и этанола. Фосфолипиды являются амфипатическими по своей природе, то есть эти молекулы имеют гидрофобный хвост, такой как длинная углеводородная цепочка, и гидрофильную голову. В водной среде, такой как вода или физиологический раствор, эти хвосты выстраиваются относительно друг друга, вдали от водных молекул,в то время как головные части обращаются наружу в водную фазу. Именно такая природа фосфолипидов делает их весьма эффективными для составления рецептур весьма нерастворимых медикаментов, таких как медикаменты настоящего изобретения. 5 Фосфолипиды, применяемые в этом изобретении, выбирают таким образом, чтобы температура их фазового перехода была приблизительно равной или ниже температуры тела, или около 37 С. Представительные примеры полезных фосфолипидов включают синтетические фосфолипиды - димиристоилфосфатидилхолин (DMPC),димиристоилфосфатидилглицерин (DMPG), дипальмитоилфосфатидилхолин (DPPC), дипальмитоилфосфатидилглицерин (DPPG), дистеароилфосфатидилхолин (DSPC) или дистеароилфосфатидилглицерин (DSPG), или их сочетание. Другие примеры фосфолипидов можно найти в справочнике М.А. Марша "CRC Handbook of Lipid Bilayers",CRCDMPG около 7:3, они имитируют клеточную мембрану. Раствор липида добавляют в раствор диаминоциклогексаннитрат платины таким образом, чтобы весовое отношение диаминоциклогексаннитрата платины к липиду составляло приблизительно от 1:80 до 1:5, предпочтительно приблизительно от 1:80 до 1:10, более предпочтительно приблизительно от 1:45 до 1:25. В некоторых областях применения было найдено желательным добавлять холестерин,или его полусукцинатные производные, к липидному комплексу. Полагают, что холестерин обеспечивает более плотную упаковку двойных слоев и тем самым замедляется выделение медикамента. Этот подход может быть особенно желательным для подкожных рецептур, которые могут вызвать сильный некроз, если медикамент подается слишком быстро. Холестерин добавляют в раствор фосфолипида. Холестерин можно использовать в количестве приблизительно от 0,5 до 15 частей на 100 частей фосфолипида. Для удаления растворителя из комплекса диаминоциклогександикарбоксилат платины можно использовать любую методику из множества известных из уровня техники. Например,такой растворитель, как рассмотренная выше смесь хлороформа и этанола, можно удобно удалять путем продувки инертным газом, таким как азот. Фосфолипидные комплексы диаминоциклогександикарбоксилат платины можно суспендировать в фармацевтически приемлемом носителе, таком как вода для инъекций, или комплекс может быть лиофилизирован с фармацевтически приемлемым вспомогательным средством лиофилизации. В качестве такого вспомогательного средства обычно используют маннит,однако можно использовать и другие вспомогательные средства, которые не взаимодействуют с медикаментом или липидным комплексом. Обычными примерами вспомогательного средства являются фосфаты натрия или калия, лимонная кислота, винная кислота, желатин и углеводы, такие как лактоза, декстран, декстроза, 002630 6 эта-крахмал и другие, которые также считаются эффективными в этом изобретении. Вспомогательные средства могут использоваться индивидуально или в сочетании, чтобы обеспечить комок хорошего качества, который легко диспергируется в воде при повторном составлении рецептуры. Обычно вспомогательное средство добавляют в дисперсию в виде водного раствора. И здесь желательно использовать концентрированные растворы, чтобы минимизировать количество воды, удаляемой посредством лиофилизации. Количество вспомогательного средства регулируется таким образом, как хорошо известно из уровня техники, чтобы обеспечить комок, который не растрескивается или сморщивается, и является пористым, так чтобы он легко растворялся и обладал хорошим внешним видом. Было найдено, что маннит является эффективным. Маннит добавляют в дисперсию в виде раствора, имеющего концентрацию приблизительно от 5 до 150 г/мл. Маннит добавляют в количестве приблизительно от 1 до 100 весовых частей на 1 часть комплекса фосфолипиддиаминоциклогександикарбоксилат платины. После удаления растворителей и добавления вспомогательного средства дисперсию пропускают через гомогенизатор (например, роторно-статарный гомогенизатор Текмар, модель Т 25, или струйный гомогенизатор с погружной микроструйной техникой, модель М 110 У). Как общее правило, чем меньше размер частиц дисперсии, тем быстрее можно высушить рецептуру в течение цикла лиофилизации. Было установлено, что дисперсия, имеющая распределение частиц по размеру в интервале приблизительно от 10 до 500 нм и в среднем около 250 нм, является удовлетворительной для лиофилизации. Оптимальный размер частиц может изменяться в зависимости от способа назначения. Ниже предоставлен типичный цикл лиофилизации, применяемый в соответствии с настоящим изобретением. Этот цикл может изменяться в зависимости от имеющегося оборудования и инженерного обеспечения, таким образом, как хорошо известно из уровня техники. Гомогенизированный состав можно разлить в ампулы, имеющие номинальный объем от 5 до 50 мл. Эти ампулы помещают в камеру лиофилизации при температуре около 5 С. Обычно размер ампул подбирают таким образом, чтобы каждая ампула содержала разовую дозу комплекса фосфолипиддиаминоциклогександикарбоксилат платины. Температура этой камеры понижается до -30 С в течение 1 ч, после чего эту температуру поддерживают приблизительно в течение 4 ч. Затем снижают давление в камере лиофилизации до 200-250 микрон давления для остальной части цикла. После снижения давления в камере температуру поднимают до +25 С в течение периода 15 ч, и про 7 дукт выдерживают при 25 С в течение 5 ч. Затем температуру резкоповышают до +40 С в течение периода 20 мин, и продукт выдерживают при 40 С в течение 2 ч. Предпочтительно,лиофилизированный продукт имеет окончательное содержание влаги меньше, чем приблизительно 5% и обычно приблизительно от 1 до 2%. Для внутривенного или подкожного введения комплекс может быть повторно воссоздан с использованием таких носителей как вода, физиологический раствор или другой электролит. Лиофилизированный продукт при добавлении воды обеспечивает образование коллоидной дисперсии липидного комплекса в водном растворе вспомогательного средства. Ни комплекс,ни липиды не растворимы в воде. Коллоидная дисперсия состоит, по меньшей мере, из двух отдельных фаз. Первая фаза является диспергированной или внутренней фазой. Вторая фаза является непрерывной или внешней фазой. Системы в коллоидном состоянии содержат одно или несколько веществ, которые имеют, по меньшей мере, один размер в интервале от 10100 Ангстрем до нескольких микрон (см. стр. 272-274 в главе 19 "Дисперсные системы", справочника Remington's Pharmaceutical Sciences, 18 е издание, 1990, Mack Publ. Co., Easton, PA 18042). В коллоидных дисперсиях настоящего изобретения диспергированная или внутренняя фаза содержит частицы фосфолипидного комплекса диаминоциклогексан-дикарбоксилат платины, которые имеют размер частиц в интервале приблизительно от 10 до 1000 нм. При выборе водного носителя рекомендуется использовать такой, который имеет удельный вес почти равный с липидным комплексом (приблизительно 1,08 г/см 3), чтобы минимизировать тенденцию дисперсии к разделению. Продукт лиофилизации липидных комплексов может быть повторно воссоздан в рецептуру с водой, физиологическим раствором,или другим фармацевтически приемлемым водным разбавителем, для внутривенного назначения. При таком повторном составлении получают дисперсию, которая пригодна для инъекции. Продукт лиофилизации также можно вводить перорально в виде водной дисперсии или как пасту. Для перорального введения продукт лиофилизации можно составить, чтобы получить оральную дисперсию или рецептуру пасты. Альтернативно продуктом лиофилизации можно заполнять мягкие желатиновые капсулы для перорального введения. Комплексы фосфолипиддиаминоциклогександикарбоксилат платины вводят в терапевтически эффективном количестве. Дозировки для комплекса описаны в литературе. Лекарство предпочтительно вводят в виде непрерывной инфузии в течение 3-21 суток, используя программируемый амбулаторный насос для непре 002630 8 рывной инфузии. Рекомендуется, чтобы лекарство вводилось с фактором, стимулирующим колонию гранулоцитов (GCSF). Хотя комплексы фосфолипиддиаминоциклогександикарбоксилат платины можно лиофилизировать, эти комплексы фосфолипиддиаминоциклогександикарбоксилат платины являются фармакологически активными и обычно их составляют в дозировочную рецептуру для перорального, внутривенного или подкожного введения без лиофилизации. Для увеличения стабильности комплекса можно использовать рецептурные вспомогательные средства, такие как противомикробные или антиокислительные агенты. Липосомы комплексов фосфолипиддиаминоциклогександикарбоксилат платины получают путем добавления раствора диаминоциклогексаннитрата платины к подходящему фосфолипиду, с добавлением дикарбоновой кислоты,выпариванием растворителя, использованного с фосфолипидом, для того чтобы получить пленку,добавления воды для инъекции и гомогенизации полученной липосомы. Теперь это изобретение будет описано более подробно со ссылкой на следующие не ограничивающие примеры. Пример 1. Растворяют в 600 мл воды 20,0 г тетрахлорплатината калия, K2PtCl4, 54,2 г иодида калия, KI, и 5,0 г диаминоциклогексана, и реакционной смеси дают прореагировать в течение 1 ч. Продукт диаминоциклогексан-РtI2 осаждается из воды. Растворяют в 170 мл воды 10,8 г нитрата серебра, АgNО 3. В этот раствор при перемешивании добавляют 17,9 г диаминоциклогексанРtI2. Реакционной смеси дают прореагировать в течение ночи, чтобы получить диаминоциклогексан-РtNО 3. К раствору диаминоциклогексан-PtNO3(3,1 мл), имеющему концентрацию 65 мг/мл,добавляют 0,1-молярный раствор гидроксида натрия до установления рН между 5,5 и 5,7. Растворяют в 8,5 мл абсолютного спирта 4200 мг димиристоилфосфатидилхолина(DMPC). В этот раствор добавляют 1800 мг димиристоилфосфатидилглицерина (DMPG), растворенного в 5 мл хлороформа. Готовят раствор малоновой кислоты (13 вес./об. %). Значение рН раствора доводят до 5,5-5,7 гидроксидом натрия. Раствор липида нагревают до 40-50 С в сосуде, закрытом крышкой, и добавляют к нему раствор диаминоциклогексан-PtNO3. Содержимое перемешивают в течение 20 мин. Затем удаляют крышку из сосуда и дают испариться растворителям. В эту смесь добавляют 25 мл 0,9%-го раствора хлорида натрия. Остатки растворителей удаляют продуванием азотом. Суспензию липидного комплекса доводят до объе 9 ма 50 мл. Частицы измельчают, используя гомогенизатор Текмара. Пример 2. Повторяют методику примера 1, за исключением того, что применяемой дикарбоновой кислотой является бутилмалоновая кислота. В таблице проиллюстрирована противоопухолевая активность фосфолипидных комплексов диаминоциклогексанмалоната платины и диаминоциклогексанбутилмалоната платины, 002630 10 которые сопоставлены с цис-платиной и плацебо (контрольное лекарство). После подробного описания этого изобретения со ссылкой на предпочтительные варианты его осуществления, очевидно, что возможны его видоизменения и варианты, без отклонения от объема изобретения, определяемого в прилагаемой формуле изобретения. Таблица. Противоопухолевая активность соединений диаминоциклогексан-платины относительно стойкой к платине клеточной линии Р 388 Рецептура Доза, Средняя продолжитель- Увеличение продолжитель- Изменение тяжести %Т/С мг/кг ность жизни, сутки ности жизни, % опухоли (log10) Диаминоциклогсксан 60,0 23,5+1,7 103,8 Контроль (плацебо); 13,0 исходная тяжесть опухоли = 1,0 х 106 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения липидных комплексов или липосом водонерастворимого диаминоциклогександикарбоксилата платины путем добавления к водному раствору диаминоциклогексаннитрата платины раствора фосфолипида в неводном растворителе и дикарбоновой кислоты с последующим удалением указанного неводного растворителя. 2. Способ по п.1, где указанный водонерастворимый диаминоциклогександикарбоксилат платины представляет собой соединение общей формулы где R1 и R2 являются одинаковыми или различными и представляют собой атом водорода, C1-С 10 алкил,С 6-С 10 арил, C7-C18 алкарил, С 7-С 10 аралкил, или R1 и R2 входят в состав замещенного или незамещенного, насыщенного или ненасыщенного 4, 5, или 6 членного кольца, или R1 и R2 могут объединяться с заместителями R1 и R2 при соседнем атоме углерода с образованием замещенного или незамещенного, насыщенного или ненасыщенного 4, 5, или 6 членного кольца и n равно 0-10. 3. Способ по п.2, где указанный дикарбоксилатPt выбирают из группы, состоящей из диаминоциклогексаноксалата-Pt, диаминоциклогексанмалоната-Pt, диаминоциклогексансукцината-Pt,диаминоциклогексанглутурата-Pt, диаминоциклогексанадипата-Pt, диаминоциклогексанпимелата-Pt, диаминоциклогексанмалеата-Pt, диами ноциклогексанфумарата-Pt, диаминоциклогексанфталата-Pt и диаминоциклогексантартратаPt. 4. Способ по п.1, где указанную карбоновую кислоту выбирают из группы, состоящей из янтарной кислоты, глутаровой кислоты, адипиновой кислоты, пимелиновой кислоты, малеиновой кислоты, фумаровой кислоты, азелаиновой кислоты, пробковой кислоты, себациновой кислоты, винной кислоты и фталевой кислоты. 5. Способ по п.3, где указанный диаминоциклогександикарбоксилат-Pt представляет собой диаминоциклогексанмалонат-Pt. 6. Способ по п.1, где указанный фосфолипид выбирают из группы, состоящей из димиристоилфосфатидилхолина, димиристоилфосфатидилглицерина, дистеароилфосфатидилхолина,дистеароилфосфатидилглицерина и их любого сочетания. 7. Способ по п.6, где указанный фосфолипид представляет собой смесь димиристоилфосфатидилхолина и димиристоилфосфатидилглицерина. 8. Способ по п.7, где указанный димиристоилфосфатидилхолин присутствует в весовом отношении к указанному димиристоилфосфатидилглицерину, равном приблизительно 7:3. 9. Способ по п.1, где указанный комплекс указанного фосфолипида и указанного водонерастворимого дикарбоксилата-Pt образует коллоидную дисперсию при воспроизведении в фармацевтически приемлемом водном растворителе. 10. Способ по п.1, где указанный комплекс указанного фосфолипида и указанный водоне 11 растворимый комплекс дикарбоксилата-Pt находится в лиофилизованном состоянии. 11. Способ по п.10, где к комплексу добавлен фармацевтически приемлемый эксципиент. 12. Способ по п.11, где указанный эксципиент представляет собой маннит. 12 13. Способ по п.10, где к комплексу добавлен холестерин или его полусукцинатные производные. 14. Способ по п.10, где указанный липидный комплекс образует коллоидную дисперсию при воспроизведении в физиологически приемлемом водном растворителе.
МПК / Метки
МПК: A61K 9/127
Метки: платины, комплексов, получения, водонерастворимого, способ, липидных, липосом, диаминоциклогександикарбоксилата
Код ссылки
<a href="https://eas.patents.su/7-2630-sposob-polucheniya-lipidnyh-kompleksov-ili-liposom-vodonerastvorimogo-diaminociklogeksandikarboksilata-platiny.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения липидных комплексов или липосом водонерастворимого диаминоциклогександикарбоксилата платины</a>
Предыдущий патент: Акустическое устройство панельного типа с использованием мод колебаний изгибных волн
Следующий патент: Производные 4-циано-4-деформилсордарина
Случайный патент: Устройство и способ вырабатывания тепла с магнитокалорическим материалом











