Пиразолопиримидины
Номер патента: 9517
Опубликовано: 28.02.2008
Авторы: Гайер Херберт, Херрманн Штефан, Кук Карл-Хайнц, Гебауэр Олаф, Эльбе Ханс-Людвиг, Хиллебранд Штефан, Эбберт Рональд, Дамен Петер, Гут Оливер, Хайнеман Ульрих, Гройль Йорг Нико, Вахендорф-Нойман Ульрике
Формула / Реферат
1. Пиразолопиримидины формулы (I)
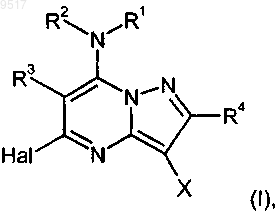
где R1 означает алкил, содержащий 1-6 атомов углерода, который может быть замещен от однократно до пятикратно, одинаково или различно галоидом, циано-, гидрокси-, алкоксигруппой, содержащей 1-4 атома углерода, и/или циклоалкилом, содержащим 3-6 атомов углерода, или
R1 означает алкенил, содержащий 2-6 атомов углерода, который может быть замещен от однократно до трехкратно, одинаково или различно галоидом, циано-, гидрокси-, алкоксигруппой, содержащей 1-4 атома углерода, и/или циклоалкилом, содержащим 3-6 атомов углерода, или
R1 означает циклоалкил, содержащий 3-6 атомов углерода, который может быть замещен от однократно до трехкратно, одинаково или различно галоидом и/или алкилом, содержащим 1-4 атома углерода,
R2 означает водород или алкил, содержащий 1-4 атома углерода, или
R1 и R2 вместе с атомом азота, к которому они присоединены, означают насыщенное или ненасыщенное гетероциклическое кольцо, содержащее 3-6 атомов в кольце, причем гетероцикл может содержать дополнительно атом азота, кислорода или серы в качестве атома кольца и может быть замещен до трехкратно фтором, хлором, бромом, алкилом, содержащим 1-4 атома углерода, и/или галоидалкилом, содержащим 1-4 атома углерода и 1-9 атомов фтора и/или хлора,
R3 означает насыщенный или ненасыщенный гетероциклил, содержащий 5 или 6 атомов в кольце и 1-4 гетероатома, таких как азот и/или сера, причем гетероциклил может быть замещен от однократно до четырехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, алкилом, алкоксигруппой, гидроксиминоалкилом или алкоксиминоалкилом с 1-3 атомами углерода в каждой алкильной части,
галоидалкилом или галоидалкоксигруппой, содержащими 1-3 атома углерода и 1-7 атомов галоида,
R4 означает водород,
Hal означает фтор, хлор или бром и
X означает цианогруппу, фтор, хлор, бром, йод, формил, алкенил, содержащий 2-6 атомов углерода, алкенил, содержащий 2-5 атомов углерода в алкенильной части и замещенный карбоксигруппой, метоксикарбонилом или этоксикарбонилом, алкоксикарбонил, содержащий 1-4 атома в алкоксильной части.
2. Пиразолопиримидины формулы (I) по п.1, в которых R1 означает радикал формулы
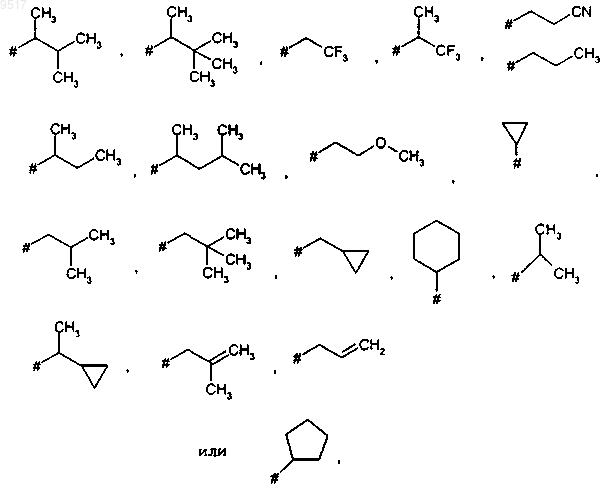
причем # означает место присоединения,
R2 означает водород, метил, этил или пропил или
R1 и R2 вместе с атомом азота, к которому они присоединены, означают пирролидинил, пиперидинил, морфолинил, тиоморфолинил, пиперазинил, 3,6-дигидро-1(2Н)-пиперидинил или тетрагидро-1(2Н)-пиридазинил, причем эти радикалы могут быть замещены 1-3 атомами фтора, 1-3 метильными группами и/или трифторметилом, или
R1 и R2 вместе с атомом азота, к которому они присоединены, означают радикал формулы
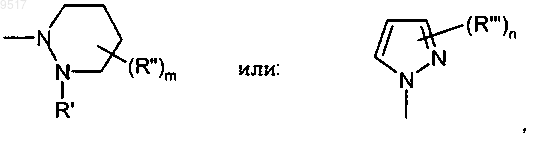
где R' означает водород или метил,
R" означает метил, этил, фтор, хлор или трифторметил,
m означает числа 0, 1, 2 или 3, причем R" означает одинаковые или различные радикалы, если m означает 2 или 3,
R'" означает метил, этил, фтор, хлор или трифторметил и
n означает числа 0, 1, 2 или 3, причем R'" означает одинаковые или различные радикалы, если n означает 2 или 3,
R3 означает пиридил, который присоединен во 2 или 4 положении и может быть замещен от однократно до четырехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, метилом, этилом, метокси-, метилтиогруппой, гидроксиминометилом, гидроксиминоэтилом, метокси-минометилом, метоксиминоэтилом и/или трифторметилом, или
R3 означает пиримидил, который присоединен во 2 или 4 положении и может быть замещен от однократно до трехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, метилом, этилом, метокси-, метилтиогруппой, гидроксиминометилом, гидроксиминоэтилом, метоксиминометилом, метоксиминоэтилом и/или трифторметилом, или
R3 означает тиенил, который присоединен во 2 или 3 положении и может быть замещен от однократно до трехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, метилом, этилом, метокси-, метилтиогруппой, гидроксиминометилом, гидроксиминоэтилом, метоксиминоме-тилом, метоксиминоэтилом и/или трифторметилом, или
R4 означает водород,
Hal означает фтор или хлор, и
X означает цианогруппу, фтор, хлор, бром, йод, формил или метоксикарбонил, или
X означает радикал формулы
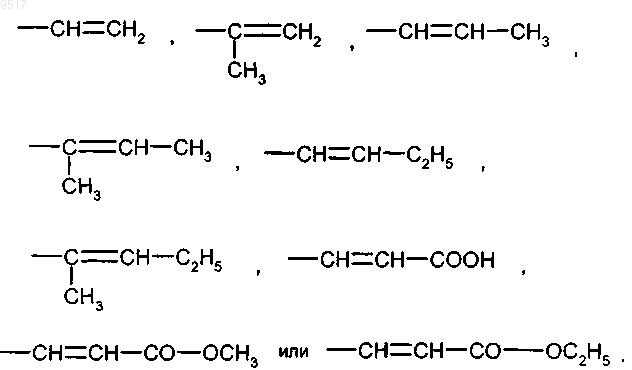
3. Способ получения пиразолопиримидинов формулы (I) по п.1, отличающийся тем, что галоид-пиразолопиримидины формулы
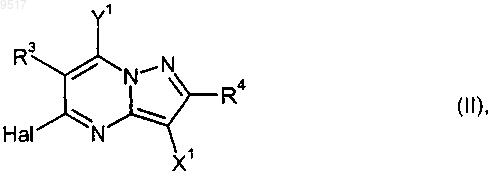
где
R4 и Hal имеют значения, приведенные в п.1,
R3 означает пиридил, который присоединен во 2 или 4 положении и может быть замещен от однократно до четырехкратно трифторметилом, или
R3 означает пиримидил, который присоединен во 2 или 4 положении и может быть замещен от однократно до трехкратно, одинаково или различно фтором и/или хлором,
R3 означает тиенил, который присоединен во 2 или 3 положении и может быть замещен от однократно до трехкратно хлором или метилом,
X1 означает цианогруппу или формил, и
Y1 означает галоид,
подвергают взаимодействию с аминами формулы
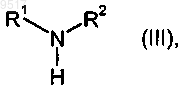
где
R1 и R2 имеют значения, приведенные в п.1,
при необходимости в присутствии разбавителя, при необходимости в присутствии акцептора кислоты и при необходимости в присутствии катализатора.
4. Средство для борьбы с нежелательными микроорганизмами, отличающееся тем, что содержит как минимум один пиразолопиримидин формулы (I) по п.1 или 2, наряду с наполнителями и/или поверхностно-активными веществами.
5. Применение пиразолопиримидинов формулы (I) по п.1 или 2 для борьбы с нежелательными микроорганизмами.
6. Способ борьбы с нежелательными микроорганизмами, отличающийся тем, что наносят на нежелательные микроорганизмы и/или на их жизненную среду пиразолопиримидины формулы (I) по п.1 или 2.
7. Способ получения средств для борьбы с нежелательными микроорганизмами, отличающийся тем, что смешивают наполнители и/или поверхностно-активные вещества с пиразолопиримидинами формулы (I) по п.1 или 2.
8. Галоидпиразолопиримидины формулы
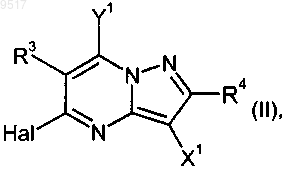
где R3 означает пиридил, который присоединен во 2- или 4-положении и может быть замещен от однократно до четырехкратно трифторметилом, или
R3 означает пиримидил, который присоединен во 2- или 4-положении и может быть замещен от однократно до трехкратно, одинаково или различно фтором и/или хлором, или
R3 означает тиенил, который присоединен во 2- или 3-положении и может быть замещен от однократно до трехкратно хлором или метилом,
R4 означает водород, Hal означает галоид,
X1 означает цианогруппу, формил или алкоксикарбонил, содержащий 1-4 атома углерода в алкоксильной части, и
Y1 означает галоид.
9. Способ получения галоидпиразолопиримидинов формулы (II) по п.8, отличающийся тем, что гидроксипиразолопиримидины формулы

где R3 и R4 имеют значения, приведенные в п.8, и
R означает цианогруппу или алкоксикарбонил, содержащий 1-4 атома углерода в алкоксильной части,
подвергают взаимодействию с галоидирующими средствами при необходимости в присутствии разбавителя.
10. Способ получения галоидпиразолопиримидинов формуыы (II) по п.8, у которых X1 означает формил, отличающийся тем, что гидроксипиразолопиримидины формулы
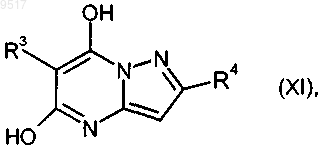
где
R3 и R4 имеют значения, приведенные в п.8,
подвергают взаимодействию с фосфороксихлоридом в присутствии диметилформамида и при необходимости при добавлении пентахлорида фосфора.
11. Гидроксипиразолопиримидины формулы
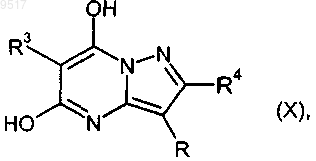
где R3 имеет указанное в п.8 значение,
R4 означает водород, и
R означает цианогруппу или алкоксикарбонил, содержащий 1-4 атома углерода в алкильной части.
12. Способ получения гидроксипиразолопиримидинов формулы (X) по п.11, отличающийся тем, что гетероциклилмалоновый эфир формулы

где R3 имеет значения, приведенные в п.11, и
R12 означает алкил, содержащий 1-4 атома углерода,
подвергают взаимодействию с аминопиразолами формулы
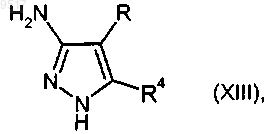
где R4 и R имеют значения, приведенные в п.11,
при необходимости в присутствии разбавителя и при необходимости в присутствии средства, связывающего кислоту.
13. Пиридилмалоновый эфир формулы
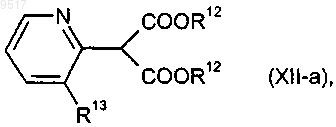
где
R12 означает алкил, содержащий 1-4 атома углерода,
R13 означает галоидалкил, содержащий 1-4 атома углерода.
14. Способ получения пиридилмалоновых эфиров формулы (XII-a) по п.13, отличающийся тем, что галоидпиридины формулы
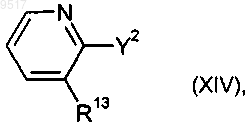
где
R13 имеет значения, приведенные в п.13, и
Y2 означает галоид,
подвергают взаимодействию с малоновыми эфирами формулы
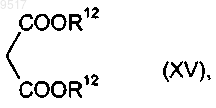
где R12 имеет значения, приведенные в п.13,
при необходимости в присутствии разбавителя, при необходимости в присутствии соли меди и при необходимости в присутствии акцептора кислоты.
15. Пиримидилмалоновый эфир формулы
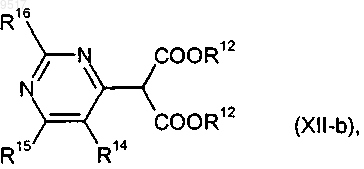
где R12 означает алкил, содержащий 1-4 атома углерода,
R14 означает галоид и
R15 и R16 каждый означает водород.
16. Способ получения пиримидилмалоновых эфиров формулы (ХII-b) по п.15, отличающийся тем, что галоидпиримидины формулы
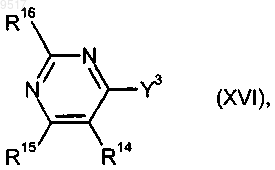
где R14, R15 и R16 имеют значения, приведенные в п.15, и
Y3 означает галоид,
подвергают взаимодействию с малоновыми эфирами формулы
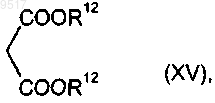
где R12 имеет значения, приведенные в п.15,
при необходимости в присутствии разбавителя, при необходимости в присутствии соли меди и при необходимости в присутствии акцептора кислоты.
Текст
009517 Данное изобретение относится к азотсодержащим гетероциклическим соединениям с биологической активностью, более конкретно к новым пиразолопиримидинам, к способу их получения, их применению для борьбы с нежелательными микроорганизмами, новым промежуточным соединениям и способам их получения. Известно, что определенные пиразолопиримидины обладают фунгицидными свойствами (см. DE-A 3130633 или FR-A 2794745). Эффективность этих веществ хорошая, однако при малых применяемых количествах в некоторых случаях недостаточна. Задачей изобретения является разработка новых пиразолопиримидинов, которые с успехом можно применять для борьбы с нежелательными микроорганизмами. Поставленная задача решается предлагаемыми пиразолопиримидинами формулы (I) где R1 означает алкил, содержащий 1-6 атомов углерода, который может быть замещен от однократно до пятикратно, одинаково или различно галоидом, циано-, гидрокси-, алкоксигруппой, содержащей 1-4 атома углерода, и/или циклоалкилом, содержащим 3-6 атомов углерода, илиR1 означает алкенил, содержащий 2-6 атомов углерода, который может быть замещен от однократно до трехкратно, одинаково или различно галоидом, циано-, гидрокси-, алкоксигруппой, содержащей 14 атома углерода, и/или циклоалкилом, содержащим 3-6 атомов углерода, илиR1 означает циклоалкил, содержащий 3-6 атомов углерода, который может быть замещен от однократно до трехкратно, одинаково или различно галоидом и/или алкилом, содержащим 1-4 атома углерода,R2 означает водород или алкил, содержащий 1-4 атома углерода, илиR1 и R2 вместе с атомом азота, к которому они присоединены, означают насыщенное или ненасыщенное гетероциклическое кольцо, содержащее 3-6 атомов в кольце, причем гетероцикл может содержать дополнительно атом азота, кислорода или серы в качестве атома кольца и может быть замещен до трехкратно фтором, хлором, бромом, алкилом, содержащим 1-4 атома углерода, и/или галоидалкилом,содержащим 1-4 атома углерода и 1-9 атомов фтора и/или хлора,R3 означает насыщенный или ненасыщенный гетероциклил, содержащий 5 или 6 атомов в кольце и 1-4 гетероатома, таких как азот и/или сера, причем гетероциклил может быть замещен от однократно до четырехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, алкилом, алкоксигруппой, гидроксиминоалкилом или алкоксиминоалкилом с 1-3 атомами углерода в каждой алкильной части, галоидалкилом или галоидалкоксигруппой, содержащими 1-3 атома углерода и 1-7 атомов галоида,R4 означает водород,Hal означает фтор, хлор или бром иX означает цианогруппу, фтор, хлор, бром, йод, формил, алкенил, содержащий 2-6 атомов углерода,алкенил, содержащий 2-5 атомов углерода в алкенильной части и замещенный карбоксигруппой, метоксикарбонилом или этоксикарбонилом, алкоксикарбонил, содержащий 1-4 атома в алкоксильной части. Предпочтительными пиразолопиримидинами формулы (I) являются соединения, у которыхR2 означает водород, метил, этил или пропил илиR1 и R2 вместе с атомом азота, к которому они присоединены, означают пирролидинил, пиперидинил, морфолинил, тиоморфолинил, пиперазинил, 3,6-дигидро-1(2 Н)-пиперидинил или тетрагидро-1(2 Н)пиридазинил, причем эти радикалы могут быть замещены 1-3 атомами фтора, 1-3 метильными группами и/или трифторметилом, или где R' означает водород или метил,R" означает метил, этил, фтор, хлор или трифторметил,m означает числа 0, 1, 2 или 3, причем R" означает одинаковые или различные радикалы, если m означает 2 или 3,R'" означает метил, этил, фтор, хлор или трифторметил иn означает числа 0, 1, 2 или 3, причем R'" означает одинаковые или различные радикалы, если n означает 2 или 3,R3 означает пиридил, который присоединен во 2- или 4-положении и может быть замещен от однократно до четырехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, метилом, этилом, метокси-, метилтиогруппой, гидроксиминометилом, гидроксиминоэтилом, метоксиминометилом, метоксиминоэтилом и/или трифторметилом, илиR3 означает пиримидил, который присоединен во 2- или 4-положении и может быть замещен от однократно до трехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, метилом, этилом, метокси-, метилтиогруппой, гидроксиминометилом, гидроксиминоэтилом, метоксиминометилом, метоксиминоэтилом и/или трифторметилом, илиR3 означает тиенил, который присоединен во 2- или 3-положении и может быть замещен от однократно до трехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, метилом, этилом, метокси-, метилтио-группой, гидроксиминометилом, гидроксиминоэтилом, метоксиминометилом, метоксиминоэтилом и/или трифторметилом, илиR4 означает водород,Hal означает фтор или хлор и Соединения согласно данному изобретению могут быть представлены в зависимости от положения заместителей при необходимости в виде смесей различных возможных изомерных форм, в частности стереоизомеров, таких как Е- и Z-, трео- и эритро-, а также оптических изомеров, при необходимости также в форме таутомеров. Если R3 на обоих атомах, соседних с местом присоединения, неодинаково замещен, то соответствующие соединения могут быть представлены в особом виде стереоизомеров, и,причем, атропоизомеров. Пиразолопиримидины вышеприведенной формулы (I) получают за счет того, что галоидпиразолопиримидины формулы где R4 и Hal имеют вышеприведенные значения,R3 означает пиридил, который присоединен во 2- или 4-положении и может быть замещен от однократно до четырехкратно трифторметилом, илиR3 означает пиримидил, который присоединен во 2- или 4-положении и может быть замещен от однократно до трехкратно, одинаково или различно фтором и/или хлором,R3 означает тиенил, который присоединен во 2- или 3-положении и может быть замещен от однократно до трехкратно хлором или метилом,X1 означает цианогруппу или формил, и где R1 и R2 имеют вышеприведнные значения,при необходимости в присутствии разбавителя, при необходимости в присутствии акцептора кислоты и при необходимости в присутствии катализатора. Данный способ, который ниже обозначается как способ а), является объектом изобретения. Пиразолопиримидины вышеприведенной формулы (I) можно также получать за счет того, что) с диизобутилалюминийгидридом в присутствии водного раствора хлорида аммония, а также в присутствии органического разбавителя, или) с соединениями Гриньяра формулы где R5 означает алкил иX2 означает хлор или бром,в присутствии разбавителя и при необходимости в присутствии катализатора, или с) пиразолопиримидины формулыR6 означает водород или алкил,подвергают взаимодействию или) с аминосоединениями формулы где R7 означает водород или алкил,в присутствии разбавителя и при необходимости в присутствии катализатора, причем аминосоединения формулы (V) можно использовать и в виде их солей присоединения с кислотой, или) с трифенилфосфониевыми солями формулы где Ph означает фенил иR8 означает водород или не замещенный или замещенный алкил, в присутствии основания, а также в присутствии разбавителя, или) с диизобутилалюминийгидридом в присутствии водного раствора хлорида аммония, а также в присутствии органического разбавителя, или с боргидридом натрия в присутствии разбавителя,и при необходимости образующиеся при этом пиразолопиримидины формулыX3 означает хлор, бром, йод или радикал R9O-SO2-O-, при необходимости в присутствии основания и в присутствии разбавителя, или где R1, R2, R3, R4 и Hal имеют значения, приведенные выше,R10 означает водород или не замещенный или замещенный алкил,подвергают взаимодействию с сильными основаниями в присутствии разбавителя,или е) пиразолопиримидины формулы где R1, R2, R3, R4 и Hal имеют значения, приведенные выше, подвергают взаимодействию с ацилпроизводными формулы где R11 означает алкил иX4 означает хлор или радикал формулы в присутствии катализатора и в присутствии разбавителя. Пиразолопиримидины формулы (I) очень хорошо пригодны для борьбы с нежелательными микроорганизмами. Они проявляют прежде всего сильную фунгицидную эффективность и могут быть применены как при защите растений, так и при защите материалов. Неожиданно оказалось, что пиразолопиримидины формулы (I) обладают существенно лучшей микробицидной эффективностью по сравнению с похожими по строению ранее известными веществами того же направления действия. Соединения формулы (I) согласно данному изобретению при необходимости могут быть представлены в виде смесей различных изомерных форм, в частности стереоизомеров, таких как Е- и Z-, трео- и эритро-, а также оптических изомеров, таких как R-и S-изомеры или атропоизомеров, при необходимости также и в виде таутомеров. Как чистые стереоизомеры, так и любые смеси этих изомеров являются предметом данного изобретения, даже если вообще здесь речь идет только о соединениях формулы (I). В зависимости от типа указанных выше заместителей соединения формулы (I) проявляют кислые или основные свойства и могут образовывать соли. Если соединения формулы (I) содержат гидрокси-,карбокси- или другие группы, вызывающие кислотные свойства, то эти соединения могут быть с помощью оснований превращены в соли. Подходящими основаниями являются, например, гидроксиды, карбонаты, гидрокарбонаты щелочных и щелочноземельных металлов, в частности, натрия, калия, магния и кальция, кроме того, аммиака, первичных, вторичных и третичных аминов с (C1-C4)-алкильными радикалами, а также моно-, ди- и триалканоламины (С 1-С 4)-алканолов. Если соединения формулы (I) содержат амино-, алкиламино- или другие группы, вызывающие основные свойства, то эти соединения могут быть с помощью кислот превращены в соли. Подходящими кислотами являются, например, минеральные кислоты, такие как соляная, серная и фосфорная кислота, органические кислоты, такие как уксусная или щавелевая кислота, и кислые соли, такие как NaHSO4 и KHSO4. Полученные таким образом соли также проявляют фунгицидные и микробицидные свойства. В объем изобретения также входят солеобразные производные, которые получают из соединений формулы (I) при взаимодействии с основными, соответственно, с кислыми соединениями, а также Nоксиды, получаемые обычными способами оксигенирования. Если в качестве исходных веществ используют 3-циано-5,7-дихлор-6-(3-трифторметилпиридин-2 ил)пиразоло[1,5-а]пиримидин и 2,2,2-трифторизопропиламин, то осуществление способа (а) согласно данному изобретению можно наглядно представить в виде следующей схемы. Если в качестве исходного вещества используют 3-циано-5-хлор-6-(3-трифторметилпиридин-2-ил)7-(2,2,2-трифторизопропиламино)пиразоло[1,5-а]пиримидин и в качестве реакционного компонента используют диизобутилалюминийгидрид, то осуществление способа (b) (вариант ) можно наглядно описать в виде следующей схемы. Если в качестве исходного вещества используют 3-циано-5-хлор-6-(3-трифторметилпиридин-2-ил)7-(2,2,2-трифторизопропиламино)пиразоло[1,5-а]пиримидин и в качестве реакционного компонента используют метилмагнийбромид, то осуществление способа (b) (вариант ) можно наглядно представить в виде следующей схемы. Если в качестве исходных веществ используют 3-формил-5-хлор-4-(3-трифторметилпиридин-2-ил)7-(2,2,2-трифторизопропиламино)пиразоло[1,5 а]пиримидин и гидрохлорид метоксиамина, то осуществление способа (с) (вариант ) можно наглядно представить в виде следующей схемы. Если в качестве исходного вещества используют 3-метилкарбонил-5-хлор-6-(3-трифторметилпиридин-2-ил)-7-(2,2,2-трифторизопропиламино)пиразоло[1,5 а]пиримидин и в качестве реакционного компонента используют трифенилметилфосфонийбромид, то осуществление способа (с) (вариант ) можно наглядно представить в виде следующей схемы. Если в качестве исходного вещества используют 3-метилкарбонил-5-хлор-6-(3-трифторметилпиридин-2-ил)-7-(2,2,2-трифторизопропиламино)пиразоло[1,5 а]пиримидин и в качестве реакционных компонентов используют диизобутилалюминийгидрид на первой стадии и метилйодид на второй стадии,то осуществление способа (с) (вариант ) можно наглядно представить в виде следующей схемы. Если в качестве исходного вещества используют 3-(1,2-дибромпропил)-5-хлор-6-(5 хлорпиримидин-4-ил)-7-(4-метилпиперидино)пиразоло[1,5 а]пиримидин и в качестве реакционного компонента используют трет-бутилат калия, то осуществление способа (d) можно наглядно представить в виде следующей схемы. Если в качестве исходного вещества используют 5-хлор-6-(5-хлорпиримидин-4-ил)-7-(4 метилпиперидино)пиразоло[1,5 а]пиримидин, в качестве реакционного компонента используют ацетилхлорид и в качестве катализатора используют трихлорид алюминия, то осуществление способа (е) можно наглядно представить в виде следующей схемы. Галоидпиразолопиримидины формулы (II) являются новыми соединениями. Эти вещества также пригодны для борьбы с нежелательными микроорганизмами. Галоидпиразолопиримидины формулы (II) можно получить, если f) гидроксипиразолопиримидины формулыR означает цианогруппу или алкоксикарбонил, содержащий 1-4 атома углерода в алкоксильной части,подвергают взаимодействию с галоидирующими средствами, при необходимости в присутствии где R3 и R4 имеют значения, приведенные выше,подвергают взаимодействию с фосфороксихлоридом в присутствии диметилформамида и при необходимости при добавлении пятихлористого фосфора продолжить взаимодействие. Если в качестве исходного вещества используют 3-циано-6-(3-трифторметилпиридин-2-ил)пиразоло[1,5-а]пиримидин-5,7-диол и в качестве галоидирующего средства используют фосфороксихлорид в смеси с пятихлористым фосфором, то осуществление способа (f) можно наглядно представить в виде следующей схемы. Гидроксипиразолопиримидины формулы (X) также до настоящего времени не были известны. Их можно получить, если где R4 и R имеют значения, приведенные выше,при необходимости в присутствии разбавителя и при необходимости в присутствии средства, связывающего кислоту. Если в качестве исходных веществ используют диметиловый эфир 2-(3-трифторметилпиридин-2 ил)-малоновой кислоты и 3-амино-4-цианопиразол, то осуществление способа (h) можно наглядно представить в виде следующей схемы. Гетероциклилмалоновые эфиры формулы (XII) частично известны (см. DE 3820538-А, WO 0111965 и WO 99-32464). Новыми являются пиридилмалоновые эфиры формулыR13 означает галоидалкил, содержащий 1-4 атома углерода. Новыми являются пиримидилмалоновые эфиры формулыR15 и R16 каждый означает водород. Пиридилмалоновые эфиры формулы (ХII-а) можно получить, если (i) галоидпиридины формулы где R12 имеет значение, приведенное выше, при необходимости в присутствии разбавителя, при необходимости в присутствии соли меди и при необходимости в присутствии акцептора кислоты. Если в качестве исходных веществ используют 2-хлор-3-трифторметилпиридин и диметиловый эфир малоновой кислоты, то осуществление способа (i) согласно данному изобретению можно наглядно представить в виде следующей схемы. Галоидпиридины формулы (XIV) являются известными химическими реактивами для синтеза. Малоновые эфиры формулы (XV), также используемые при осуществлении способа (i) согласно данному изобретению, также являются известными химическими реактивами для синтеза. Пиримидилмалоновые эфиры формулы (XII-b) можно получить, если (j) галоидпиримидины формулы где R12 имеет значение, приведенное выше,при необходимости в присутствии разбавителя, при необходимости в присутствии соли меди и при необходимости в присутствии акцептора кислоты. Если в качестве исходных веществ используют 4,5-дихлорпиримидин и диметиловый эфир малоновой кислоты, то осуществление способа (j) согласно данному изобретению можно наглядно представить в виде следующей схемы. Галоидпиримидины, используемые в качестве исходных веществ при осуществлении способа (j) согласно данному изобретению, описываются в общем виде формулой (XVI). В этой формуле радикал R14 предпочтительно означает фтор, хлор, Y3 предпочтительно означает хлор или бром. Галоидпиримидины формулы (XVI) являются известными соединениями и могут быть получены-8 009517 известными способами (см. J. Chem. Soc. 1955, 3478, 3481). Аминопиразолы, используемые в качестве реакционных компонентов при осуществлении способа(h) согласно данному изобретению, описываются в общем виде формулой (XIII). В этой формуле радикалR4 имеет предпочтительно такие значения, которые в связи с описанием веществ формулы (I) согласно данному изобретению указаны в качестве предпочтительных значений для этого радикала. Радикал R имеет предпочтительно такие значения, которые в связи с описанием гидроксипиразолопиримидинов формулы (X) были указаны в качестве предпочтительных значений для этого радикала. Аминопиразолы формулы (XIII) известны или могут быть получены известными способами. В качестве галоидирующих средств при осуществлении способа (f) подходят все обычные компоненты для замещения гидроксильных групп галоидами. Предпочтительно можно использовать трихлорид фосфора, трибромид фосфора, пентахлорид фосфора, фосфороксихлорид, тионилхлорид, тионилбромид или их смеси. Соответствующие фторсодержащие соединения формулы (II) можно получить из хлор- или бромсодержащих соединений при взаимодействии с фторидом калия. Названные галоидирующие средства известны. Способ (g) пригоден для получения галоидпиразолопиримидинов формулы где R3 и R4 имеют значения, приведенные выше. Гидроксипиразолопиримидины, используемые в качестве исходных веществ при осуществлении способа (g), описываются в общем виде формулой (XI). В этой формуле радикалы R3 и R4 имеют предпочтительно такие значения, которые в связи с описанием соединений формулы (I) согласно данному изобретению указаны в качестве предпочтительных значений для этих радикалов. Гидроксипиразолопиримидины формулы (XI) получают способом (h), в котором используют аминопиразолы формулы (XIII), у которых радикал R означает водород. Способ (g) осуществляют при условиях Вилсмайеровского формилирования с помощью фосфороксихлорида в присутствии диметилформамида. При этом можно также добавлять пятихлористый фосфор в качестве хлорирующего средства. Температуры реакций при осуществлении способа (g) могут варьироваться в широких интервалах. Вообще работают при температурах от -10 до +150 С, более предпочтительно от 0 до 120 С. При осуществлении способа (g) берут на 1 моль гидроксипиразолопиримидинов формулы (XI) вообще от 2 до 5 молей диметилформамида, от 5 до 15 молей фосфороксихлорида и при необходимости от 0 до 2 молей пятихлористого фосфора. Переработку осуществляют обычными способами. Амины, также используемые при осуществлении способа (а) согласно данному изобретению, описываются в общем виде формулой (III). В этой формуле радикалы R1 и R2 имеют предпочтительно такие значения, которые в связи с описанием соединений формулы (I) согласно данному изобретению указаны в качестве предпочтительных значений для радикалов R1 и R2. Амины формулы (III) известны или могут быть получены известными способами. В качестве разбавителей при осуществлении способа (а) согласно данному изобретению пригодны все обычные инертные органические растворители. Предпочтительно используют галоидированные углеводороды, такие как, например, хлорбензол, дихлорбензол, дихлорметан, хлороформ, тетрахлорметан,дихлорэтан или трихлорэтан; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, метил-трет-бутиловый эфир, метил-трет-амиловый эфир, диоксан, тетрагидрофуран, 1,2-диметоксиэтан,1,2-диэтоксиэтан или анизол; нитрилы, такие как ацетонитрил, пропионитрил, н- или изобутиронитрил или бензонитрил; амиды, такие как N,N-диметиформамид, N,N-диметилацетамид, N-метилформанилид,N-метилпирролидон или триамид гексаметилфосфорной кислоты; сложные эфиры, такие как метиловый или этиловый эфир уксусной кислоты; сульфоксиды, такие как диметилсульфоксид; сульфоны, такие как сульфолан. В качестве акцептора кислоты при осуществлении способа (а) согласно данному изобретению подходят все обычные для такого рода взаимодействий неорганические или органические основания. Предпочтительно используют гидриды, гидроксиды, амиды, алкоголяты, ацетаты, карбонаты или гидрокарбонаты щелочно-земельных или щелочных металлов, например гидрид натрия, амид натрия, диизопропиламид лития, метилат натрия, этилат натрия, трет-бутилат калия, гидроксид натрия, гидроксид калия,ацетат натрия, ацетат калия, ацетат кальция, карбонат натрия, карбонат калия, гидрокарбонат калия и гидрокарбонат натрия, и, кроме того, соединения аммония, такие как гидроксид аммония, ацетат аммония и карбонат аммония, а также третичные амины, такие как триметиламин, триэтиламин, трибутиламин, N,N-диметиланилин, N,N-диметилбензиламин, пиридин, N-метилпиперидин, N-метилморфолин,N,N-диметиламинопиридин, диазабициклооктан (DABCO), диазабициклононен (DBN) или диазабициклоундецен (DBU). В качестве катализаторов при осуществлении способа (а) согласно данному изобретению подходят-9 009517 все обычные для такого рода взаимодействий ускорители реакций. Предпочтительно используют фториды, такие как фторид натрия, фторид калия или фторид аммония. Температуры реакций при осуществлении способа (а) согласно данному изобретению могут варьироваться в широком интервале. Вообще работают при температурах от 0 до 150 С, более предпочтительно при температурах от 0 до 80 С. При осуществлении способа (а) согласно данному изобретению берут на 1 моль галоидпиразолопиримидина формулы (II) вообще от 0,5 до 10 молей, предпочтительно от 0,8 до 2 молей амина формулы(III). Переработку осуществляют обычными способами. Пиразолопиримидины, используемые в качестве исходных веществ при осуществлении способа (b),описываются в общем виде формулой (Ia). В этой формуле радикалы R1, R2, R3, R4 и Hal имеют предпочтительно такие значения, которые в связи с описанием соединений формулы (I) согласно данному изобретению указаны в качестве предпочтительных значений для этих радикалов. В случае пиразолопиримидинов формулы (Ia) имеются в виду вещества согласно данному изобретнию, которые могут быть получены по способу (а) согласно данному изобретению. В качестве разбавителей при осуществлении способа (b) (вариант ) пригодны все обычные инертные, органические растворители. Предпочтительно используют алифатические или ароматические при необходимости галоидированные углеводороды, такие как толуол, дихлорметан, хлороформ или четыреххлористый углерод. Температуры реакций при осуществлении способа (b) (вариант ) могут варьироваться в определенном интервале. Вообще работают при температурах от -80 до +20 С, более предпочтительно от -60 до+10 С. При осуществлении способа (b) (вариант ) берут на 1 моль пиразолопиримидина формулы (Ia) вообще эквивалентное количество или также избыток, предпочтительно от 1,1 до 1,2 моля диизобутилалюминийгидрида и в заключение добавляют избыток водного раствора хлорида аммония. Переработку осуществляют обычными способами. Как правило, поступают таким образом, что подкисляют реакционную смесь, отделяют органическую фазу, водную фазу экстрагируют органическим растворителем, слабо смешивающимся с водой, объединенные органические фазы промывают, сушат и отгоняют растворитель при пониженном давлении. Соединения Гриньяра, используемые в качестве реакционных компонентов при осуществлении способа (b) (вариант ), описываются в общем виде формулой (IV). В этой формуле радикал R5 предпочтительно означает алкил, содержащий 1-4 атома углерода, более предпочтительно означает метил или этил. X2 предпочтительно означает бром. В качестве катализатора при осуществлении способа (b) (вариант Р) пригодны все ускорители реакций, пригодные для такого рода реакций Гриньяра. В качестве примера можно назвать йодид калия и йод. В качестве разбавителя при осуществлении способа (b) (вариант ) подходят все обычные для такого рода взаимодействий инертные органические растворители. Предпочтительно используют простые эфиры, такие как диэтиловый эфир, диоксан или тетрагидрофуран, наряду с этим, используют ароматические углеводороды, такие как толуол, а также смеси простых эфиров и ароматических углеводородов,такие как толуол/тетрагидрофуран. Температуры реакций при осуществлении способа (b) (вариант ) могут варьироваться в определенном интервале. Вообще работают при температурах от -20 до +100 С, более предпочтительно от 0 до 80 С. При осуществлении способа (b) (вариант ) берут на 1 моль пиразолопиримидина формулы (Ia) как правило 2-3 моля соединения Гриньяра формулы (IV). В заключение проводят водную переработку обычными способами. Пиразолопиримидины, используемые в качестве исходных веществ при осуществлении способа (с),описываются в общем виде формулой (Ib). В этой формуле радикалы R1, R2, R3, R4 и Hal имеют предпочтительно такие значения, которые в связи с описанием веществ формулы (I) согласно данному изобретению указаны в качестве предпочтительных значений для этих радикалов. Радикал R6 предпочтительно означает водород или алкил, содержащий 1-4 атома углерода, более предпочтительно означает водород,метил или этил. В случае пиразолопиримидинов формулы (Ib) имеются в виду вещества согласно данному изобретению, которые можно получить способом (b) согласно данному изобретению. Аминосоединения, используемые в качестве реакционных компонентов при осуществлении способа (с) (вариант ), описываются в общем виде формулой (V). В этой формуле радикал R7 предпочтительно означает водород или алкил, содержащий 1-4 атома углерода, более предпочтительно означает водород, метил или этил. В качестве реакционных компонентов имеются в виду также соли присоединения с кислотой, предпочтительно соли присоединения с хлороводородом аминосоединений формулы (V). Как аминосоединения формулы (V) , так и их соли присоединения с кислотой известны или могут- 10009517 быть получены известными способами. В качестве разбавителей при осуществлении способа (с) (вариант ) пригодны все обычные инертные органические растворители. Предпочтительно используют спирты, такие как метанол, этанол, нпропанол или изопропанол. В качестве катализаторов при осуществлении способа (с) (вариант ) пригодны все ускорители реакций обычные для такого рода взаимодействий. Предпочтительно используют кислые или основные катализаторы, такие как, например, основный ионообменник, находящийся в продаже под названием амберлист А-21. Температуры реакций при осуществлении способа (с) (вариант ) могут варьироваться в определенном интервале. Вообще работают при температурах от 0 до 80 С, более предпочтительно от 10 до 60 С. При осуществлении способа (с) (вариант ) берут на 1 моль пиразолопиримидина формулы (Ib) вообще эквивалентное количество или избыток, предпочтительно от 1,1 до 1,5 молей аминосоединения формулы (V) или его соли присоединения с кислотой. Переработку осуществляют обычными способами. Вообще поступают таким образом, что реакционную смесь при необходимости фильтруют, после этого отгоняют растворитель и чистят. Трифенилфосфониевые соли, используемые в качестве реакционной компоненты при осуществлении способа (с) (вариант (3), описываются в общем виде формулой (VI). В этой формуле Ph означает фенил. Радикал R8 предпочтительно означает водород или алкил, содержащий 1-4 атома углерода, причем,алкильные радикалы могут быть замещены карбоксилом, метоксикарбонилом или этоксикарбонилом. Особенно предпочтительно радикал R8 означает водород, метил или этил, причем два последних радикала могут быть замещены карбоксилом, метоксикарбонилом или этоксикарбонилом. Трифенилфосфониевые соли формулы (VI) известны или могут быть получены известными способами. В качестве оснований для осуществления способа (с) (вариант ) согласно данному изобретению пригодны все обычные для такого рода реакций Виттига депротонирующие средства. Предпочтительно используют бутиллитий. В качестве разбавителей при осуществлении способа (с) (вариант ) пригодны все обычные для таких реакций Виттига органические растворители. Предпочтительно используют простые эфиры, такие как диоксан и тетрагидрофуран. Температуры реакций при осуществлении способа (с) (вариант ) можно варьировать в определенном интервале. Вообще работают при температурах от -78 до +30 С. При осуществлении способа (с) (вариант ) берут на 1 моль пиразолопиримидина формулы (Ib) эквивалентное количество или избыток трифенилфосфониевой соли формулы (VI), а также эквивалентное количество или избыток основания. Переработку осуществляют обычными способами. Алкилирующие средства, используемые в качестве реакционных компонентов при осуществлении способа (с) (вариант ), описываются общей формулой (VII). В этой формуле радикал R9 предпочтительно означает алкил, содержащий 1-4 атома углерода, более предпочтительно означает метил или этил. X3 предпочтительно означает хлор, бром, йод или радикал R9-O-SO2-O-, где R9 имеет значения, приведенные выше. Алкилирующие средства формулы (VII) известны или могут быть получены известными способами. Если при осуществлении способа (с) (вариант ) на первой стадии используют диизобутилалюминийгидрид в качестве восстановительного средства, то целесообразно работать при таких условиях, которые уже упомянуты в связи с описанием способа (b, вариант ) согласно данному изобретению. Если при осуществлении способа (с) (вариант ) на первой стадии используют боргидрид натрия в качестве восстановительного средства, то в качестве разбавителей используют, как правило, спирты,предпочтительно метанол, этанол или изопропанол. При восстановлении боргидридом натрия темературы реакции могут варьироваться в определенном интервале. Вообще работают при температурах от 0 до 70 С, предпочтительно от 0 до 50 С. При осуществлении восстановления боргидридом натрия берут на 1 моль пиразолопиримидина формулы (Ib) эквивалентное количество или избыток боргидрида натрия. Переработку осуществляют обычными способами. При осуществлении второй стадии способа (с) (вариант ) согласно данному изобретению в качестве оснований подходят все обычные средства, связывающие кислоту. Предпочтительно используют гидриды, алкоголяты и карбонаты щелочных металлов, такие как гидрид натрия, метилат натрия, третбутилат калия, карбонат натрия, карбонат калия или карбонат лития. В качестве разбавителей при осуществлении второй стадии способа (с) (вариант ) согласно данному изобретению подходят все обычныеинертные органические растворители. Предпочтительно используют простые эфиры, такие как диоксан или тетрагидрофуран, и, кроме того, нитрилы, такие как ацетонитрил.- 11009517 Температуры при осуществлении второй стадии способа (с) (вариант ) могут варьироваться в широком интервале. Вообще работают при температурах от 0 до 100 С, более предпочтительно от 20 до 80 С. При осуществлении второй стадии способа (с) (вариант ) берут на 1 моль пиразолопиримидина формулы (Ic) вообще 1-2 моля, более предпочтительно 1-1,5 моля алкилирующего средства. Переработку осуществляют обычными способами. Пиразолопиримидины, используемые в качестве исходных веществ при осуществлении способа (d),описываются в общем виде формулой (Id). В этой формуле радикалы R1, R2, R3, R4 и Hal имеют предпочтительно такие значения, которые в связи с описанием веществ формулы (I) согласно данному изобретению указаны в качестве предпочтительных значений для этих радикалов. R10 предпочтительно означает водород или алкил, содержащий 1-4 атома углерода, более предпочтительно означает водород, метил,этил или пропил, причем каждый из трех последних радикалов может быть замещен карбоксилом, метоксикарбонилом или этоксикарбонилом. В случае пиразолопиримидинов формулы (Id) имеются в виду вещества согласно изобретению, которые могут быть получены способом (а). По особому варианту способа можно получить пиразолопиримидины, если где R1, R2, R3, R4, R10 и Hal имеют значения, приведенные выше,подвергают взаимодействию с бромом в присутствии инертного органического разбавителя, такого как дихлорметан, трихлорметан или тетрахлорметан, при температурах от -20 до +20 С. Реакционные компоненты при этом вводят предпочтительно в приблизительно эквивалентных количествах. Переработку осуществляют обычными способами. В качестве сильных оснований при осуществлении способа (d) предпочтительно используют алкоголяты щелочных металлов, причем, в качестве примера можно назвать метилат натрия и трет-бутилат калия. В качестве разбавителей при осуществлении способа (d) подходят все обычные для такого рода взаимодействий инертные органические растворители. Предпочтительно используют спирты, такие как метанол или этанол, а также нитрилы, такие как ацетонитрил. Температуры при осуществлении способа (d) могут варьироваться в определенных интервалах. Вообще работают при температурах от -10 до +80 С, более предпочтительно от 0 до 60 С. При осуществлении способа (d) берут на 1 моль пиразолопиримидина формулы (Id) вообще 2-3 эквивалента или более высокий избыток сильного основания. Переработку осуществляют обычными способами. Пиразолопиримидины, используемые в качестве исходных веществ при осуществлении способа (е),описываются общей формулой (VIII). В этой формуле радикалы R1, R2, R3, R4 и Hal имеют предпочтительно такие значения, которые в связи с описанием веществ формулы (I) согласно данному изобретению указаны в качестве предпочтительных значений для этих радикалов. Пиразолопиримидины формулы (VIII) известны или могут быть получены известными способами(см. РСТ/ЕР 03/05 159). Ацил-производные, используемые в качестве реакционных компонентов при осуществлении способа (е), описываются общей формулой (IX). В этой формуле радикал R11 предпочтительно означает алкил,содержащий 1-4 атома углерода, более предпочтительно означает метил, этил или н-пропил. X4 предпочтительно означает хлор или радикал формулы где R11 имеет значения, приведенные выше. Ацилпроизводные формулы (IX) известны или могут быть получены известными способами. В качестве катализаторов при осуществлении способа (е) подходят все ускорители реакций, обычные для такого рода реакций Фриедель-Крафтса. Предпочтительно используют хлориды металлов, такие как трихлорид алюминия или хлорид железа (III). В качестве разбавителей при осуществлении способа (е) подходят все обычные для такого рода взаимодействий инертные органические растворители. Предпочтительно используют простые эфиры,такие как диэтиловый эфир, диоксан или тетрагидрофуран. Температуры при осуществлении способа (е) могут варьироваться в определенном интервале. Вообще работают при температурах от -20 до +20 С, более предпочтительно от -10 до +10 С. При осуществлении способа (е) берут на 1 моль пиразолопиримидина формулы (VIII) вообще 2-5- 12009517 молей ацилпроизводного формулы (IX), а также соответствующее количество катализатора. Переработку осуществляют обычными способами. В качестве разбавителей при осуществлении способа (f) подходят все растворители пригодные для такого рода реакций галоидирования. Предпочтительно используют галоидированные алифатические или ароматические углеводороды, такие как хлорбензол. В качестве разбавителя может также использоваться само галоидирующее средство, например фосфороксихлорид или смесь галоидирующих средств. Температуры при осуществлении способа (f) могут варьироваться в широком интервале. Вообще работают при температурах от 0 до 150 С, более предпочтительно от 10 до 120 С. При осуществлении способа (f) берут гидроксипиразолопиримидин общей формулы (X), как правило, с избытком галоидирующего средства. Переработку осуществляют обычными способами. В качестве разбавителей при осуществлении способа (h) пригодны все обычные для такого рода взаимодействий инертные органические растворители. Предпочтительно используют спирты, такие как метанол, этанол, н-пропанол, изопропанол, н-бутанол и трет-бутанол. В качестве средства, связывающего кислоту, при осуществлении способа (h) пригодны все обычные для такого рода взаимодействий неорганические и органические основания. Предпочтительно используют третичные амины, такие как трибутиламин, или пиридин. Амин, используемый в избытке, может также являться разбавителем. Температуры при осуществлении способа (h) могут варьироваться в широком интервале. Вообще работают при температурах от 20 до 200 С, более предпочтительно от 50 до 180 С. При осуществлении способа (h) берут гетероциклилмалоновый эфир формулы (XII) и аминопиразол формулы (XIII), как правило, в эквивалентных количествах. Однако также возможно использовать один или другой компонент в избытке. Переработку осуществляют обычными способами. В качестве разбавителей при осуществлении способов (i) и (j) используют все обычные инертные органические растворители. Предпочтительно используют галоидированные углеводороды, такие как,например, хлорбензол, дихлорбензол, дихлорметан, хлороформ, тетрахлорметан, дихлорэтан или трихлорэтан; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, метил-трет-бутиловый эфир, метил-трет-амиловый эфир, диоксан, тетрагидрофуран, 1,2-диметоксиэтан, 1,2-диэтоксиэтан или анизол; нитрилы, такие как ацетонитрил, пропионитрил, н- или изобутиронитрил или бензонитрил; амиды, такие как N,N-диметилформамид, N,N-диметилацетамид, N-метилформанилид, N-метилпирролидон или триамид гексаметилфосфорной кислоты; сульфоксиды, такие как диметилсульфоксид; сульфоны,такие как сульфолан; спирты, такие как метанол, этанол, н- или изопропанол, н-, изо-, втор- или третбутанол, этандиол, пропан-1,2-диол, этоксиэтанол, метоксиэтанол, монометиловый эфир диэтиленгликоля, моноэтиловый эфир диэтиленгликоля, их смеси с водой или чистую воду. В качестве солей меди при осуществлении способов (i) и (j) подходят все обычные соли меди. Предпочтительно используют хлорид меди(I) или бромид меди(I). В качестве акцепторов кислоты при осуществлении способов (i) и (j) подходят все обычные неорганические или органические основания. Предпочтительно используют гидриды, гидроксиды, амиды, алкоголяты, ацетаты, карбонаты или гидрокарбонаты щелочноземельных или щелочных металлов, например, гидрид натрия, амид натрия, диизопропиламид лития, метилат натрия, этилат натрия, трет-бутилат калия, гидроксид натрия, гидроксид калия, ацетат натрия, ацетат калия, ацетат кальция, карбонат натрия,карбонат калия, гидрокарбонат калия и гидрокарбонат натрия, и, кроме того, соединения аммония, такие как гидроксид аммония, ацетат аммония и карбонат аммония, а также третичные амины, такие как триметиламин, триэтиламин, трибутиламин, N,N-диметиланилин, N,N-диметилбензиламин, пиридин, Nметилпиперидин, N-метилморфолин, N,N-диметиламинопиридин, диазабициклооктан (DABCO), диазабициклононен (DBN) или диазабициклоундецен (DBU). Температуры реакций при осуществлении способов (i) и (j) могут варьироваться в широком интервале. Вообще работают при температурах от 0 до 150 С, более предпочтительно при температурах от 0 до 80 С. При осуществлении способа (i) берут на 1 моль галоидпиридина формулы (XIV), как правило, от 1 до 15 молей, более предпочтительно от 1,3 до 8 молей малонового эфира формулы (XV). Переработку осуществляют обычными способами. При осуществлении способа (j) берут на 1 моль галоидпиримидина формулы (XVI), как правило, от 1 до 15 молей, более предпочтительно от 1,3 до 8 молей малонового эфира формулы (XV). Переработку осуществляют обычными способами. Все вышеупомянутые способы осуществляют в основном при атмосферном давлении. Однако возможна также работа при повышенном давлении. Соединения обнаруживают сильное микробицидное действие и могут быть использованы для борьбы с нежелательными микроорганизмами, такими как грибы и бактерии при защите растений и при защите материалов. Фунгициды применяют при защите растений для борьбы с Plasmodiophoromycetes, Oomycetes, Chytridiomycetes, Zygomycetes, Ascomycetes, Basidiomycetes и Deuteromycetes. Бактерициды используют при защите растений для борьбы с Pseudomonadaceae, Rhizobiaceae, En- 13009517terobacteriaceae, Corynebacteriaceae и Streptomycetaceae. В качестве примера, но не ограничиваясь этим, можно назвать некоторых возбудителей грибковых и бактериальных заболеваний, которые подпадают под перечисленные выше родовые понятия: виды рода ксантомонас (Xanthomonas), такие как, например, Xanthomonas campestris pv.oryzae; виды рода псевдомонас (Pseudomonas), такие как, например, Pseudomonas syringae pv.lachrymans; виды рода эрвиниа (Erwinia), такие как, например, Erwinia amylovora; виды рода питиум (Pythium), такие как, например, Pythium ultimum; виды рода фитофтора (Phytophthora), такие как, например, Phytophthora infestans; виды рода псевдопероноспора (Pseudoperonospоra), такие как, например, Pseudoperonospora humuli или Pseudoperonospora cubensis; виды рода плазмопара (Plasmopara), такие как, например, Plasmopara viticola; виды рода бремиа (Bremia), такие как, например, Bremia lactucae; виды рода пероноспора (Peronospora), такие как, например, Peronospora pisi или P. brassicae; виды рода эризифе (Erysiphe), такие как, например, Erysiphe graminis; виды рода сферотека (Sphaerotheca), такие как, например, Sphaerotheca fuliginea; виды рода подосфера (Podosphaera), такие как, например, Podosphaera leucotricha; виды рода вентурия (Venturia), такие как, например, Venturia inaequalis; виды рода пиренофора (Pyrenophora), такие как, например, Pyrenophora teres или P. graminea (конидиевая форма: дрекслера, син: гельминтоспориум); виды рода кохлиоболюс (Cochliobolus), такие как, например, Cochliobolus sativus (конидиевая форма: дрекслера, син: гельминтоспориум); виды рода уромицес (Uromyces), такие как, например, Uromyces appendiculatus; виды рода пукциния (Puccinia), такие как, например, Puccinia recondita; виды рода склеротиния (Sclerotinia), такие как, например, Sclerotinia sclerotiorum; виды рода тиллеция (Tilletia), такие как, например, Tilletia caries; виды рода устиляго (Ustilago), такие как, например, Ustilago nuda или Ustilago avenae; виды рода пелликулария (Pellicularia), такие как, например, Pellicularia sasakii; виды рода пирикулария (Pyricularia), такие как, например, Pyricularia oryzae; виды рода фузарий (Fusarium), такие как, например, Fusarium. culmorum; виды рода ботритис (Botrytis), такие как, например, Botrytis cinerea; виды рода септория (Septoria), такие как, например, Septoria nodorum; виды рода лептосферия (Leptosphaeria), такие как, например, Leptosphaeria nodorum; виды рода церкоспора (Cercospora), такие как, например, Cercospora canescens; виды рода альтернария (Alternaria), такие как, например, Aiternaria brassicae; виды рода псевдоспорелла (Pseudocercosporella), такие как, например, Pseudocercosporella herpotrichoides. Биологически активные вещества согласно данному изобретению проявляют также сильно укрепляющее воздействие на растения. Поэтому они пригодны для активации собственных защитных сил растений по отношению к нападению нежелательных микроорганизмов. Под веществами, укрепляющими растения (индуцирующими устойчивость), следует понимать в данном контексте такие вещества, которые способны таким образом стимулировать защитную систему растений, что обработанные растения при последующей инокуляции нежелательными микроорганизмами проявляют длительную устойчивость по отношению к этим микроорганизмам. Под нежелательными микроорганизмами в данном случае следует понимать фитопатогенные грибы, бактерии и вирусы. Вещества согласно данному изобретению могут быть таким образом использованы для того, чтобы защитить растения в течение определенного промежутка времени после обработки от нападения указанных вредных возбудителей. Временной интервал, в течение которого вырабатывается защита, составляет в общем от 1 до 10 дней, предпочтительно от 1 до 7 дней после обработки растений биологически активными веществами. Хорошая переносимость растениями этих биологически активных веществ в концентрациях, необходимых для борьбы с болезнями растений, позволяет вести обработку частей растений, находящихся над поверхностью почвы, обработку посадочного и семенного материала и почвы. При этом биологически активные вещества согласно данному изобретению могут с особенно хорошим успехом использовать для борьбы с болезнями зерновых культур, например, против Erysiphe-видов и с болезнями в виноградарстве, садоводстве и овощеводстве, например, против Botrytis-, VenturiaSphaerotheca- и Podosphaera-видов. Биологически активные вещества согласно данному изобретению пригодны также для повышения урожая. Кроме того, они обладают низкой токсичностью и обнаруживают хорошую переносимость растениями. Биологически активные вещества согласно данному изобретению могут при необходимости в определенных концентрациях и расходных количествах использоваться как гербициды для воздействия на рост растений, а также для борьбы с животными вредителями. Их можно использовать, при необходимо- 14009517 сти, в качестве промежуточных и исходных продуктов для синтеза других биологически активных веществ. Согласно данному изобретению можно обрабатывать все растения и части растений. При этом под растениями понимают все растения и популяции растений, такие как желательные и нежелательные дикие растения или культурные растения (включая естественно встречающиеся культурные растения). К культурным относят также растения, которые могут быть получены обычными селекционными или оптимизирующими методами, или биотехнологическими и гентехнологическими методами или комбинацией этих методов, включая трансгенные растения и включая сорта растений, защищаемые или не защищаемые правами защиты сорта. Под частями растений понимают все надземные и подземные части и органы растений, такие как ростки, листья, соцветья и корни, причем в качестве примера можно привести листья, хвою, стебли, стволы, соцветья, плоды, фрукты и семена, а также корни, клубни и корневища. К частям растений относятся урожай, а также вегетативный и генеративный материал для размножения,например саженцы, клубни, корневища, отводки и семена. Обработку растений и частей растений согласно данному изобретению биологически активными веществами проводят напрямую или воздействием на окружающую среду, среду обитания и помещение для хранения обычными способами обработки, например, окунанием, опрыскиванием, образованием пара, образованием тумана, рассыпанием, намазыванием, инъекцией, а в случае материала для размножения, в особенности, семян также однослойным или многослойным обволакиванием. В случае защиты материалов вещества согласно данному изобретению применяют для защиты технических материалов от нападения и разрушения нежелательными микроорганизмами. Под техническими материалами в этом контексте понимают неживые материалы, которые приготовлены для применения в технике. Например, к техническим материалам, которые могут быть защищены биологически активными веществами согласно данному изобретению от изменений и разрушений,вызываемых микробами, относятся клеящие средства, глины, бумага и картон, текстильные материалы,кожа, древесина, красящие вещества и пластмассовые изделия, охлаждающие смазки и другие материалы, которые могут подвергнуться нападению микроорганизмов или быть разрушены ими. К материалам,подлежащим защите, относятся также части промышленных установок, например, трубопроводы циркуляции охлаждающей воды, которые могут пострадать от размножения микроорганизмов. В рамках данного изобретения в качестве технических материалов предпочтительно следует назвать клеящие средства, глины, бумагу и картон, кожу, древесину, красящие вещества, охлаждающие смазки и теплопереносящие жидкости, особенно предпочтительно древесину. В качестве микроорганизмов, которые могут вызвать разрушение или изменение технических материалов, можно, например, назвать бактерии, грибы, дрожжи, водоросли и слизневые организмы. Биологически активные вещества согласно данному изобретению предпочтительно действуют на грибы, в особенности на плесневые грибы, на грибы, окрашивающие древесину и разрушающие древесину (Basidiomyceten), а также на слизневые грибы и на водоросли. В качестве примера следует назвать микроорганизмы следующих родов: альтернария (Alternaria),такие виды как Alternaria tenuis, аспергиллус (Aspergillus), такие виды как Aspergillus niger, хетомиум(Chaetomium), такие виды как Chaetomium globosum, кониофора (Coniophora), такие виды как Coniophorapuetana, лентинус (Lentinus), такие виды как Lentinus tigrinus, пенициллиум (Penicillium), такие виды какPenicillium glaucum, полипорус (Polyporus), такие виды как Polyporus versicolоr, ауреобазидиум (Aureobasidium), такие виды как Aureobasidium pullulans, склерофома (Sclerophoma), такие виды как Sderophomapityophila, триходерма (Trichoderma), такие виды как Trichoderma viride, эшерихия (Escherichia), такие виды как Escherichia coli, псевдомонас (Pseudomonas), такие виды как Pseudomonas aeruginosa, стафиллококкус (Staphylococcus), такие виды как Staphylococcus aureus. Биологически активные вещества в зависимости от присущих им физических и/или химических свойств можно перевести в обычные готовые формы, такие как растворы, эмульсии, суспензии, порошки,пены, пасты, грануляты, аэрозоли, в очень маленькие капсулы в полимерных веществах и в покровные массы для семенного материала, а также в готовые формы с ультрамалым объемом для образования холодного и горячего тумана. Эти готовые формы препаратов получают известным образом, например, перемешиванием активных веществ с наполнителями, то есть с растворителями, с сжиженными газами, находящимися под давлением, и/или с твердыми носителями, при необходимости с использованием поверхностно-активных веществ, то есть эмульгирующих средств и/или диспергирующих средств, и/или вспенивающих средств. В случае использования воды в качестве разбавителя, например, можно использовать и органические растворители в качестве вспомогательных средств для растворения. В качестве жидких растворителей в существенной мере имеют в виду ароматические соединения, такие как ксилол, толуол или алкилнафталины, хлорированные ароматические или хлорированные алифатические углеводороды, такие как хлорбензолы, хлорэтилены или метиленхлорид, алифатические углеводороды, такие как циклогексан или парафины, например, фракции нефтей, спирты, такие как бутанол или гликоль, а также их эфиры и сложные эфиры, кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон или циклогексанон, сильно полярные растворители, такие как диметилформамид и диметилсульфоксид, а также воду. Под сжижен- 15009517 ными газообразными разбавителями или носителями понимают такие жидкости, которые при нормальной температуре и нормальном давлении газообразны, например вспенивающие газы аэрозолей, такие как галоидуглеводороды, а также бутан, пропан, азот и двуокись углерода. В качестве твердых носителей имеют в виду например, помолы природных горных пород, таких как каолин, глиноземы, тальк, мел,кварц, аттапульгит, монтмориллонит или диатомовая земля, и помолы синтетических камней, таких как высокодисперсная кремниевая кислота, окись алюминия и силикаты. В качестве твердых носителей для гранулятов имеют в виду измельченные и фракционированные природные каменные породы, такие как кальцит, мрамор, пемза, сепиолит, доломит, а также синтетические грануляты из неорганической и органической муки, а также грануляты из органического материала, такого как древесные опилки, скорлупа кокосовых орехов, кукурузные кочерыжки и стебли табака. В качестве эмульгирующих и/или пенообразующих средств имеют в виду например, неионогенные и анионные эмульгаторы, такие как зфиры полиоксиэтилен-жирных кислот, эфиры полиоксиэтилен-жирных спиртов, например алкиларилполигликолевый эфир, алкилсульфонаты, алкилсульфаты, арилсульфонаты, а также гидролизаты яичного белка. В качестве диспергирующих средств имеют в виду, например, лигнин-сульфитовые щелоки и метилцеллюлозу. В готовых формах препаратов могут быть использованы адгезионные средства, такие как карбоксиметилцеллюлоза, природные и синтетические порошкообразные, зернистые или в латексной форме полимеры, такие как гуммиарабик, поливиниловый спирт, поливинилацетат, а также природные фосфолипиды, такие как кефалины и лецитины, и синтетические фосфолипиды. Другими добавками могут быть минеральные и растительные масла. Могут использоваться красители, такие как неорганические пигменты, например окись железа,окись титана, ферроциан синий и органические красители, такие как ализариновые, азо- и металлфталоцианиновые красители и следовые количества питательных веществ, таких как соли железа, марганца,бора, меди, кобальта, молибдена и цинка. Готовые формы препаратов содержат, как правило, от 0,1 до 95 вес.% биологически активного вещества, предпочтительно от 0,5 до 90 вес.%. Биологически активные вещества согласно данному изобретению могут сами по себе или в их готовых формах препаратов применяться и в смеси с известными фунгицидами, бактерицидами, акарицидами, нематицидами или инсектицидами, например, для того чтобы расширить спектр действия или чтобы предупредить развитие устойчивости к ним. Во многих случаях при этом возникают синергические эффекты, то есть эффективность смеси оказывается выше суммы эффективностей компонентов при отдельном применении. В качестве примешиваемого компонента можно использовать, например, следующие соединения. Фунгициды 2-фенилфенол; сульфат 8-гидроксихинолина; ацибензольный-S-метил; алдиморф; амидофлумет; ампропилфос; ампропилфоскалий; андоприм; анилазины; азаконазолы; азоксистробин; беналаксил; беноданил; беномил; бентиаваликарбизопропил; бензамакрил/бензамакрилизобутил; биланафос; биналакрил; бифенил; битертанол; бластицидин-S; бромуконазолы; бупириматы; бутиобаты; бутиламин; полисульфиды кальция; капсимицин; каптафол; каптан; карбендазим; карбоксин; карпропамид; карвоны; хинометионат; хлобентиазоны; хлорфеназолы; хлоронеб; хлороталонил; хлозолинаты; клозилакон; циазофамид; цифлуфенамид; цимоксанил; ципроконазолы; ципродинил; ципрофурам; даггер G; дебакарб; дихлофлуанид; дихлоны; дихлорофен; диклоцимет; дикломезины; диклоран; диэтофенкарб; дифеноконазолы; дифлуметорим; диметиримол; диметоморф; димоксистробин; диниконазолы; диниконазолы-M; динокап; дифениламины; дипиритионы; диталимфос; дитианон; додины; дразоксолон; эдифенфос; эпоксиконазолы; этабоксам; этиримол; этридиазолы; фамоксадоны; фенамидоны; фенапанил; фенаримол; бенбуконазолы; фенфурам; фенгексамид; фенитропан; феноксанил; фенпиклонил; фенпропидин; фенпропиморф; фербам; флуазинам; флубензимины; флудиоксонил; флуметовер; флуморф; флуоромиды; флуоксастробин; флуквинконазолы; флурпримидол; флусилазолы; флусульфамиды; флутоланил; флутриафол; фолпет; фозетил-А 1; фозетилнатрий; фуберидазолы; фуралаксил; фураметпир; фуркарбанил; фурмециклокс; гуазатины; гексахлоробензены; гексаконазолы; гимексазол; имазалил; имибенконазолы; иминоктадина триацетаты; иминоктадина трис(албесил); иодокарб; ипконазолы; ипробенфос; ипродионы; ипроваликарб; ирумамицин; изопротиоланы; изоваледионы; касугамицин; крезоксимметил; манкозеб; манеб; меферимзоны; мепанипирим; мепронил; металаксил; металаксил-M; метконазолы; метасульфокарб; метфуроксам; метирам; метоминостробин; метсульфовакс; милдиомицин; миклобутанил; миклозолин; натамицин; никобифен; нитротализопропил; новифлумурон; нуаримол; офурацы; оризастробин; оксадиксил; оксолиниковая кислота; окспоконазолы; оксикарбоксин; оксифентиин; паклобутразол; пефуразоаты; пенконазолы; пенцикурон; фосдифен; фталиды; пикоксистробин; пипералин; полиоксины; полиоксорим; пробеназолы; прохлораз; процимидоны; пропамокарб; пропанозиненатрий; пропиконазолы; пропинеб; проквиназид; протиоконазолы; пираклостробин; пиразофос; пирифенокс; пириметанил; пироквилон; пироксифур; пирролнитрины; квинконазолы; квиноксифен; квинтозены; симеконазолы; спироксамины; сера; тебуконазолы; теклофталам; текназены; тетциклацис; тетраконазолы; тиабендазолы; тициофен; тифлузамиды; тиофанатеметил; тирам; тиоксимид; толклофосметил; толилфлуанид; триадимефон; триа- 16009517 дименол; триазбутил; триазоксиды; трицикламиды; трициклазолы; тридеморф; трифлоксистробин; трифлумизолы; трифорины; тритиконазолы; униконазолы; валидамицин А; винклозолин; зинеб; зирам; зоксамиды;(2S)-N-[2-[4-3-(4-хлорфенил)-2-пропинил]окси]-3-метоксифенил]этил]-3-метил-2[(метилсульфонил)амино]бутанамид; 1-(1-нафталенил)-1 Н-пиррол-2,5-дион; 2,3,5,6-тетрахлор-4(метилсульфонил)пиридин; 2-амино-4-метил-N-фенил-5-тиазолкарбоксамид; 2-хлор-N-(2,3-дигидро 1,1,3-триметил-1 Н-инден-4-ил)-3-пиридинкарбоксамид; 3,4,5-трихлор-2,6-пиридиндикарбонитрил; актиноваты; цис-1-(4-хлорфенил)-2-(1 Н-1,2,4-триазол-1-ил)-циклогептанол; метил-1-(2,3-дигидро-2,2 диметил-1 Н-инден-1-ил)-1 Н-имидазол-5-карбоксилат; гидрокарбонат калия; N-(6-метокси-3-пиридинил)циклопропанкарбоксамил; натрийтетратиокарбонат; а также соли меди и медные препараты, такие как бордосская смесь; гидроксид меди; нафтенат меди; оксихлорид меди; сульфат меди; куфранеб; оксид меди; манкоппер; оксинекоппер. Бактерициды Бронопол, дихлорофен, нитрапирин, никельдиметилдитиокарбамат, касугамицин, октилинон, фуранкарбоновая кислота, окситетрациклин, пробеназол, стрептомицин, теклофталам, сульфат меди и другие медные препараты. Инсектициды / акарициды / нематициды Абамектин, ABG-9008, ацефаты, ацеквиноцил, ацетамиприд, ацетопролы, акринатрин, AKD-1022,AKD-3059, AKD-3088, аланикарб, алдикарб, алдоксикарб, аллетрин, аллетрин 1R-изомеры, альфациперметрин (альфаметрин), амидофлумет, аминокарб, амитраз, авермектин, AZ-60541, азадирахтин,азаметифос, азинфосметил, азинфосэтил, азоциклотин, Bacillus popilliae, Bacillus sphaericus, Bacillus subtilis, Bacillus thuringiensis, Bacillus thuringiensis линия EG-2348, Bacillus thuringiensis линия GC-91, Bacillus thuringiensis линия NCTC-11821, бакуловирусы, Beauveria bassiana, Beauveria tenella, бендиокарб, бенфуракарб, бенсултап, бензоксиматы, бета-цифлутрин, бета-циперметрин, бифеназаты, бифентрин, бинапакрил, биоаллетрин, биоаллетрин-S-циклопентилизомер, биоэтанометрин, биоперметрин, биоресметрин, бистрифлурон, ВРМС, брофенпрокс, бромофосэтил, бромопропилаты, бромфенвинфос (-метил),BTG-504, BTG-505, буфенкарб, бупрофезин, бутатиофос, бутокарбоксим, бутоксикарбоксим, бутилпиридабен, кадусафос, камфехлор, карбарил, карбофуран, карбофенотион, карбосульфан, картап, CGA-50439,хинометионат, хлорданы, хлордимеформ, хлоэтокарб, хлорэтоксифос, хлорфенапир, хлорфенвинфос,хлорфлуазурон, хлормефос, хлоробензилаты, хлоропикрин, хлорпроксифен, хлорпирифос-метил, хлорпирифос (-этил), хловапортрин, хромафенозиды, цис-циперметрин, цис-ресметрин, цис-перметрин, клоцитрин, клоэтокарб, клофентезины, клотианидин, клотиазобен, кодлемоны, коумафос, цианофенфос,цианофос, циклопрены, циклопротрин, Cydia pomonella, цифлутрин, цигалотрин, цигексатин, циперметрин, цифенотрин (1R-транс-изомер), циромазины, DDT, дельтаметрин, деметон-S-метил, деметон-Sметилсульфон, диафентиурон, диалифос, диазинон, дихлофентион, дихлорвос, дикофол, дикротофос,дицикланил, дифлубензурон, диметоаты, диметилвинфос, динобутон, динокап, динотефуран, диофенолан, дисульфотон, докузатнатрий, дофенапин, DOWCO-439, эфлусиланаты, эмамектин, эмамектинбензоаты, эмпентрин (1R-изомер), эндосульфан, Entomopthora spp., EPN, эсфенвалераты, этиофенкарб,этипролы, этион, этопрофос, этофенпрокс, этоксазолы, этримфос, фамфур, фенамифос, феназаквин, фенбутатин оксиды, фенфлутрин, фенитротион, фенобукарб, фенотиокарб, феноксакрим, феноксикарб, фенпропатрин, фенпирад, фенпиритрин, фенпироксиматы, фенсульфотион, фентион, фентрифанил, фенвалераты, фипронил, флоникамид, флуакрипирим, флуазурон, флубензимины, флуброцитринаты, флуциклоксурон, флуцитринаты, флуфенерим, флуфеноксурон, флуфенпрокс, флуметрин, флупиразофос, флутензин (флуфензины), флувалинаты, фонофос, форметанаты, формотион, фосметилан, фостиазаты, фубфенпрокс (флупроксифен), фуратиокарб, гамма-НСН, госсиплуры, грандлуры, грануловирусы, галфенпрокс, галофенозиды, НСН, HCN-801, гептенофос, гексафлумурон, гекситиазокс, гидраметилноны, гидропрены, IKA-2002, имидаклоприд, имипротрин, индоксакарб, иодофенфос, ипробенфос, изазофос, изофенфос, изопрокарб, изоксатион, ивермектин, японилуры, кадетрин, вирусы с полиэдровым ядром, кинопрены, лямбда-цигалотрин, линданы, луфенурон, малатион, мекарбам, месульфенфос, метальдегид,метам-натрий, метакрифос, метамидофос, Metharhizium anisopliae, Metharhizium flavoviride, метидатион,метиокарб, метомил, метопрекы, метоксихлор, метоксифенозиды, метолкарб, метоксадиазоны, мевинфос, милбемектин, милбемицин, MKI-245, MON-45700, монокротофос, моксидектин, MTI-800, налед,NC-104, NC-170, NC-184, NC-194, NC-196, никлосамиды, никотины, нитенпирам, нитиазины, NNI-0001,NNI-0101, NNI-0250, NNI-9768, новалурон, новифлумурон, OK-5101, OK-5201, OK-9601, OK-9602, OK9701, OK-9802, ометоаты, оксамил, оксидеметонметил, Paecilomyces fumosoroseus, паратионметил, паратион(-этил), перметрин (цис-, транс-), петролеум, РН-6045, фенотрин (1R-транс-изомер), фентоаты, фораты, фозалоны, фосмет, фосфамидон, фосфокарб, фоксим, пиперонил бутоксиды, пиримикарб, пиримифосметил, пиримифосэтил, праллетрин, профенофос, промекарб, пропафос, пропаргиты, пропетамфос,пропоксур, протиофос, протоаты, протрифенбуты, пиметрозины, пираклофос, пиресметрин, пиретрум,пиридабен, пиридалил, пиридафентион, пиридатион, пиримидифен, пирипроксифен, квиналфос, ресметрин, RH-5849, рибавирин, RU-12457, RU-15525, S-421, S-1833, салитион, себуфос, SI-0009, силафлуофен,спиносад, спиродиклофен, спиромезифен, сульфлурамид, сульфотеп, сулпрофос, SZI-121, тауфлувалинаты, тебуфенозиды, тебуфенпирад, тебупиримфос, тефлубензурон, тефлутрин, темефос, теми- 17009517 винфос, тербам, тербуфос, тетрахлорвинфос, тетрадифон, тетраметрин, тетраметрин (1R-изомер), тетрасул, тета-циперметрин, тиаклоприд, тиаметоксам, тиапронил, тиатрифос, тиоциклам гидрооксалаты, тиодикарб, тиофанокс, тиометон, тиосултапнатрий, турингиенсин, толфенпирад, тралоцитрин, тралометрин,трансфлутрин, триаратены, триазаматы, триазофос, триазурон, трихлофенидины, трихлорфон, трифлумурон, триметакарб, вамидотион, ванилипролы, вербутин, Verticillium lecanii, WL-108477, WL-40027, YI5201, YI-5301, YI-5302, XMC, ксилилкарб, ZA-3274, зета-циперметрин, золапрофос, ZXI-8901, соединение 3-метилфенилпропилкарбамат (тсумациде Z), соединение 3-(5-хлор-3-пиридинил)-8-(2,2,2 трифторэтил)-8-азабицикло[3.2.1]октан-3-карбонитрил (CAS-Reg.-Nr. 185982-80-3) и соответствующие 3-эндо-изомеры (CAS-Reg.-Nr. 185984-60-5) (см. WO 96/37494, WO 98/25923), а также препараты, которые содержат инсектицидно действующие экстракты растений, нематоды, грибы или вирусы. Возможны также смеси с другими известными биологически активными веществами, такими как гербициды, или с удобрениями и регуляторами роста растений, защитными веществами, соответственно,семиохимикатами. Кроме того, соединения формулы (I) согласно данному изобретению обнаруживают очень хорошее антимикотическое (противогрибковое) действие. Они обладают очень широким антимикотическим спектром действия, в особенности, по отношению к дерматофитам и отростковым грибам, плесени и дифазным грибам (например, по отношению к Candida-видам, таким как Candida albicans, Candida glabrata), a также Epidermophyton floccosum, Aspergillus-видам, таким как Aspergillus niger и Aspergillus fumigatus,Trichophyton-видам, таким как Trichophyton mentagrophytes, Microsporon-видам, таким как Microsporoncanis и audouinii. Перечисление этих грибов ни в коем случае не ограничивает охватываемый микотический спектр, а только носит пояснительный характер. Наряду с этим соединения формулы (I) согласно данному изобретению пригодны для подавления роста опухолевых клеток у человека и млекопитающих животных. Это свойство базируется на взаимодействии соединений согласно данному изобретению с канальцами и микроканальцами и содействии полимеризации микроканальцев. Для этой цели следует принимать эффективное количество одного или нескольких соединений формулы (I) или их фармацевтически приемлемых солей. Биологически активные вещества могут применяться сами по себе, в виде готовых форм их препаратов или в виде приготовленных из них форм, готовых для применения, таких как готовые для применения растворы, суспензии, порошки для опрыскивания, пасты, растворимые порошки, средства для распыления и грануляты. Применение осуществляют обычными способами, например, поливанием, разбрызгиванием, опрыскиванием, рассыпанием, распылением, вспениванием, смазыванием и т.п. Далее можно наносить биологически активные вещества способом ультрамалых объемов или инъецировать препарат активного вещества или само активное вещество в почву. Можно также обработать семенной материал растений. При применении биологически активных веществ согласно данному изобретению в качестве фунгицидов применяемые количества в зависимости от способа применения могут варьироваться в широких пределах. При обработке частей растений применяемые количества биологически активного вещества составляют, как правило, от 0,1 до 10000 г/га, предпочтительно от 10 до 1000 г/га. При обработке семенного материала применяемые количества биологически активного вещества составляют, как правило, от 0,001 до 50 г на килограмм семенного материала, предпочтительно от 0,01 до 10 г на килограмм семенного материала. При обработке почвы применяемые количества биологически активного вещества составляют, как правило, от 0,1 до 10000 г/га, предпочтительно от 1 до 5000 г/га. Как уже упомянуто выше, можно согласно данному изобретению обрабатывать все растения и их части. В одном из предпочтительных вариантов воплощения обрабатывают растения, встречающиеся с диком виде или полученные обычными биологическими методами селекции, такими как скрещивание,фузия протоплазмы: виды растений и сорта растений, а также их части. В другом предпочтительном варианте воплощения данного изобретения обрабатывают трансгенные растения и сорта растений, которые получены гентехнологическими методами, при необходимости, в комбинации с обычными методами(генетически модифицированные организмы) и части растений. Понятие "части", соответственно, "части растений " пояснено выше. Особенно предпочтительно согласно данному изобретению обрабатывают растения, обычно находящихся в продаже или применяемых сортов растений. Под сортами растений понимают растения с новыми свойствами ("треитс"), которые выведены обычной селекцией, с помощью мутагенеза или с помощью рекомбинантной ДНК-техники. Это могут быть сорта, расы, био- и генотипы. В зависимости от видов растений, соответственно, сортов растений, их местонахождения и условий роста (почва, климат, вегетационный период, питание) при обработке согласно данному изобретению могут наблюдаться сверхаддитивные ("синергические") эффекты. Так, например, возможны уменьшенные применяемые количества и/или расширение спектра действия, и/или усиление действия веществ и средств, примененных согласно изобретению, улучшенный рост растений, повышенная толерантность по отношению к высоким или низким температурам, повышенная толерантность к сухости или по отношению к содержанию соли в воде или в почве, повышенная эффективность цветения, облегченный сбор- 18009517 урожая, ускорение созревания, повышение урожайности, более высокое качество и/или высокая питательность продуктов урожая, лучшая сохраняемость и/или лучшая перерабатываемость продуктов урожая, которые выходят за границы ожидаемых эффектов. К предпочтительным трансгенным (полученным с помощью генных технологий) растениям, соответственно, сортам растений, которые можно обработать согласно данному изобретению, относятся все растения, которые получили генетический материал в результате гентехнологической модификации,придавшей этим растениям особые предпочтительные ценные свойства ("треитс"). Примерами таких свойств являются лучший рост растений, повышенная толерантность по отношению к высоким или низким температурам, повышенная толерантность к сухости или по отношению к содержанию соли в воде или в почве, повышенная эффективность цветения, облегченный сбор урожая, ускорение созревания,повышение урожайности, более высокое качество и/или высокая питательность продуктов урожая, лучшая сохраняемость и/или лучшая перерабатываемость продуктов урожая. Другими и особенно предпочтительными примерами таких свойств является повышенная защита растений по отношению к животным и микробным вредителям, таким как инсекты, клещи, грибы, патогенные для растений, бактерии и/или вирусы, а также повышенная толерантность растений по отношению к определенным гербицидно активным веществам. В качестве примера трансгенных растений следует упомянуть важные культурные растения, такие как зерновые культуры (пшеница, рис), кукуруза, соя, картофель, хлопок, табак, рапс, а также фруктовые растения (с такими фруктами, как яблоки, груши, цитрусовые фрукты и виноград), причем кукуруза, соя, картофель, хлопок, табак и рапс особенно предпочтительны. В качестве свойств ("треитс") особенно предпочтительна повышенная защита растений по отношению к инсектам, паукообразным животным, нематодам и улиткам, вызванная образующимися в растениях токсинами, в особенности такими,которые создаются в растениях с помощью генетического материала из Bacillus thuringiensis (например, с помощью генов CryIA(a), CryIA(b), CryIA(c), CryIIA, CryIIIA, CryIIIB2, Cry9c Cry2Ab, Cry3Bb и CryIF, а также их комбинаций) (в дальнейшем "Bt растения"). В качестве свойств ("треитс") также особенно предпочтительна повышенная защита растений по отношению к грибам, бактериям и вирусам с помощью системной благоприобретенной резистентности (устойчивости) (СВР), системина, фитоалексина,элициторов, а также резистентных генов и соответствующим образом экспримированных протеинов и токсинов. В качестве свойств ("треитс") далее особенно предпочтительна повышенная толерантность растений по отношению к определенным гербицидно активным веществам, например к имидазолинонам,сульфонилмочевинам, глифозатам или фосфинотрицину (например, "РАТ"-ген). Гены, которые придают в каждом случае желательные свойства ("треитс") могут встречаться в трансгенных растениях и в комбинациях друг с другом. В качестве примера "Bt растений" можно привести сорта кукурузы, сорта хлопчатника, сорта сои и сорта картофеля, которые поставляются под торговыми марками YIELD GARD(например, кукуруза, хлопок, соя), KnockOut (например, кукуруза), StarLink (например, кукуруза),Bollgard (хлопок), Nucoton (хлопок) и NewLeaf (картофель). В качестве примера растений, толерантных к гербицидам, следует назвать сорта кукурузы, сорта хлопчатника и сорта сои, которые поставляются под торговыми марками Roundup Ready (толерантность к глифозатам, например, кукуруза, хлопок, соя), Liberty Link (толерантность к фосфинотрицину, например, рапс), IMI (толерантность к имидазолинонам) и STS (толерантность к сульфонилмочевинам, например, кукуруза). В качестве устойчивых к гербицидам (специально на толерантность к гербицидам выведенных) растений следует назвать и сорта, поставляемые под торговой маркой Clearfield (например, кукуруза). Само собой разумеется что эти высказывания справедливы и для сортов растений, которые будут созданы в будущем, соответственно, будут предложены на рынке с этими свойствами или со вновь созданными генетическими свойствами ("треитс"). Приведенные растения могут быть особенно предпочтительно обработаны согласно данному изобретению соединениями общей формулы (I), соответственно, смесями биологически активных веществ согласно изобретению. Предпочтительные области, приведенные выше для биологически активных веществ, соответственно, смесей, подходят и для обработки этих растений. Особенно предпочтительно обработка растений специально приведенными ранее в тексте соединениями, соответственно смесями. Получение и применение биологически активных веществ согласно данному изобретению, видно из приведенных ниже примеров. Примеры получения соединений пример 1(Способ а) К раствору 0,2 г (0,56 ммоля) 3-циано-5,7-дихлор-6-(3-трифторметилпиридин-2-ил)пиразоло[1,5-а] пиримидина в 10 мл ацетонитрила добавляют 0,065 г (1,12 ммоля) фторида калия, перемешивают в тече- 19009517 нии 2 ч при температуре 80 С и в заключение охлаждают до 0 С. К этому раствору добавляют 0,13 г(1,17 ммоля) (S)-2,2,2-трифтор-изопропиламина и перемешивают в течении 18 ч при температуре 80 С. После этого реакционную смесь охлаждают до комнатной температуры и примешивают 30 мл разбавленной соляной кислоты. Экстрагируют дихлорметаном, органическую фазу промывают два раза водой,сушат над сульфатом натрия и отгоняют растворитель при пониженном давлении. Остаток смешивают со смесью петролейный эфир/метил-трет-бутиловый эфир = 15:1 и фильтрируют через короткую силикагелевую колонку. Таким образом получают 0,15 г (58,5% от теор.) 3-циано-5-хлор-6-(3-трифторметилпиридин-2-ил)пиразоло[1,5-а]-пиримидин-N-[(1,S)-2,2,2-трифтор-1-метилэтил]амина. ЖХВД (жидкостная хроматография высокого давления): logP = 3,14. Приведенными выше способами получают также приведенные в таблице 1 пиразолопиримидины формулы Получение исходных продуктов формулы (II) пример 65 Способ (f) В смесь, состоящую из 5,8 г (18,1 ммоля) 3-циано-6-(3-трифторметилпиридин-2-ил)пиразоло[1,5-а] пиримидин-5,7-диола и 22,15 г (144,5 ммоля) фосфороксихлорида, добавляют при комнатной температуре при перемешивании 3,0 г (14,5 ммоля) пентахлорида фосфора пятью порциями. Рекционную смесь нагревают в течение 4 ч с дефлегмацией, после этого охлаждают до комнатной температуры и при пониженном давлении отгоняют растворитель. К полученному остатку добавляют 100 мл воды и после этого- 23009517 экстрагируют трижды по 100 мл дихлорметана. Объединенные органические фазы промывают дважды по 50 мл воды, сушат над сульфатом натрия и при пониженном давлении отгоняют растворитель. Полученный остаток хроматографируют с гексан/этиловым эфиром уксусной кислоты = 3:1 на силикагеле. Получают 0,88 г (14,8% от теор.) 3-циано-5,7-дихлор-6-(3-трифторметилпиридин-2-ил)-пиразоло[1,5-а] пиримидина. ЖХВД: logP = 2,68. Пример 66 К смеси, состоящей из 2,0 г (10,74 ммоля) 2-тиенилмалоновой кислоты и 1,16 г (10,74 ммоля) 3 амино-4-цианопиразола добавляют при комнатной температуре при перемешивании в течении 2 мин 41,13 г (268 ммолей) фосфороксихлорида. После этого нагревают в течении 18 ч при температуре 90 С и после этого охлаждают до комнатной температуры. В реакционную смесь добавляют 250 мл ледяной воды и полученную при этом суспензию перемешивают в течении 1 ч. Отсасывают и промывают 50 мл воды. Для дальнейшей очистки продукт суспендируют в 50 мл циклогексан/этиловый эфир уксусной кислоты = 1:1 и кипятят недолгое время, после этого охлаждают, отсасывают через короткую силикагелевую колонку и промывают 8 раз по 50 мл циклогексан/этиловым эфиром уксусной кислоты = 1:1. Фильтрат сушат над сульфатом натрия и после этого заново фильтруют. Остаток после фильтрования промывают мальм количеством циклогексан/этилового эфира уксусной кислоты = 1:1. Из объединенного фильтрата отгоняют растворитель при пониженном давлении. Получают 1,48 г (30,34% от теор.) 5,7 дихлор-3-циано-6-(тиен-3-ил)пиразоло[1,5-а]пиримидина в виде твердого вещества. Пример 67 Через раствор 7,5 г (25,41 ммоля) 5,7-дихлор-3-циано-6-(тиен-3-ил)пиразоло[1,5-а]пиримидина в 80 мл дихлорметана пропускают при температурах от -5 С до 0 С в течении двух часов лоток газообразного хлора. После этого реакционную смесь нагревают до комнатной температуры и отгоняют растворитель при пониженном давлении. К полученному остатку добавляют дихлорметан и отсасывают. При этом получают 2,0 г требуемого продукта. Ранее собранный фильтрат после отгонки растворителя хроматографируют с циклогексан/этиловым эфиром уксусной кислоты = 1:1 на силикагеле. После отгонки растворителя из элюата выделяют еще 3,5 г требуемого продукта. Таким путем получают всего 5,5 г (54,13% от теор.) 5,7-дихлор-3-циано-(2,5-дихлор-тиен-3-ил)пиразоло[1,5-а]пиримидина. Получение исходного продукта формулы (X). Пример 68 Способ (h) Смесь, состоящую из 4,1 г (14,8 моля) диметилового эфира 2-(3-трифторметилпиридин-2-ил) малоновой кислоты, 1,6 г (14,8 ммоля) 3-амино-4-цианопиразола и 3,02 г (16,3 ммолей) три-н-бутиламина в течении 2 ч перемешивают при нагревании на 180 С. При этом образующийся при взаимодействии метанол постоянно отгоняют. В заключение реакционную смесь охлаждают до комнатной температуры. Отделяющийся три-н-бутиламин декантируют и остающуюся смесь дистиллируют при пониженном давлении. Получают 5,8 г продукта который согласно ЖХВД на 60% состоит из 3-циано-6-(3-трифторметилпиридин-2-ил)пиразоло[1,5-а]-пиримидин-5,7-диола. Рассчитанный отсюда выход составляет 73,25% от теор. Продукт используют без дополнительной очистки для дальнейшего синтеза. ЖХВД: logP = 0,29. Получение исходного продукта формулы (XII-а) Пример 69- 24009517 9 г (207 ммолей) 60 процентной суспензии гидрида натрия суспендируют в 300 мл диоксана. К ней добавляют по каплям при температуре 55-60 С 27,29 г (206,6 ммоля) диметилового эфира малоновой кислоты и продолжают перемешивать в течении 30 мин при той же температуре. После добавления 8,18 г (82,63 ммоля) хлорида меди(I) нагревают до 80 С и добавляют по каплям 15 г (82,63 ммоля) 2-хлор-3 трифторметилпиперидина. Реакционную смесь перемешивают еще в течении 14 ч при 100 С. После заключительного охлаждения до температуры 15-20 С медленно добавляют по каплям концентрированную соляную кислоту до тех пор пока смесь не станет давать кислую реакцию. Теперь добавляют 600 мл воды и 300 мл дихлорметана и отфильтровывают нерастворимые компоненты. От фильтрата отделяют органическую фазу, сушат ее над сульфатом натрия и отгоняют растворитель при пониженном давлении. Остаток хроматографируют с гексан/эфиром уксусной кислоты (4:1) на силикагеле. Получают 10,1 г(40% от теор.) диметилового эфира 2-[(3-трифторметил)пиримидин-2-ил]малоновой кислоты. ЖХВД: logP = 2,05. Получение исходного продукта формулы (XII-b). Пример 70 Способ (j) 2,6 г (65,4 ммоля) 60 процентной суспензии гидрида натрия суспендируют в 100 мл тетрагидрофурана. К суспензии при температуре около 0 С добавляют 6,9 г (52,4 ммсля) диметилового эфира малоновой кислоты и перемешивают в течении 0,5 часа при той же температуре. В заключение добавляют по каплям раствор 6,5 г (43,63 ммоля) 4,5-дихлорпиримидина в 50 мл тетрагидрофурана и перемешивают еще 3 часа при комнатной температуре. После этого добавляют медленно по каплям 150 мл 1 Н соляной кислоты и экстрагируют после этого 100 мл дихлорметана. Отделяют органическую фазу, сушат над сульфатом натрия и отгоняют растворитель при пониженном давлении. Остаток хроматографируют с метил-трет-бутиловый эфир/петролейным эфиром (1:9) на силикагеле. Получают 7 г (65,6% от теор.) диметилового эфира 2-(5-хлорпиримидин-4-ил)-малоновой кислоты. ЖХВД: logP = 1,33. Пример 71. Получение 4,5-дихлорпиримидина К раствору 112,5 г (673,7 ммоля) хлорида 5-хлор-6-оксо-1,6-дигидропиримидин-1-ия в 630 мл фосфороксихлорида добавляют 1,6 мл диметиламина и нагревают в течении 3 ч при обратной перегонке. После этого отгоняют избыточный фосфороксихлорид при пониженном давлении. После охлаждения остаток выливают в 1,5 л ледяной воды, экстрагируют 500 мл дихлорметана, органическую фазу сушат над сульфатом натрия и отгоняют растворитель при пониженном давлении. Получают 72,3 г (66,3% от теор.) 4,4-дихлорпиримидина. ЖХВД: logP = 1,35. Пример 72. Получение хлорида 5-хлор-6-оксо-1,6-дигидропиримидин-1-ия К раствору 77 г (0,8 моля) 4(3 Н)-пиримидинона в 770 мл ледяного уксуса добавляют 6,5 г (40 ммоль) хлорида железа (III) и подают в раствор в течении 2 ч при температуре 40-45 С 113,6 г (1,6 моля) хлора. Реакционную смесь охлаждают до 15 С, полученный твердый продукт отсасывают и промывают эфиром. Получают 112,5 г (84% от теор.) хлорида 5-хлор-6-оксо-1,6-дигидропиримидин-1-ия. Пример 73. Получение 4(3 Н)-пиримидинона Смесь 103 г (0,804 моля) 6-меркапто-4(1H)-пиримидинона (JP 50053381, Chem. Abstr. CAN 84: 17404) и 141,5 г (1,2 моля) никеля Рэнея в 1,2 л этанола в течении 8 ч нагревают с обратной перегонкой. Раствор фильтруют в горячем состоянии, остаток промывают этанолом и из фильтрата отгоняют растворитель при пониженном давлении. Получают 67,2 г (87% от теор.) 4(3 Н)-пиримидинона.) Определение значений logP проводят согласно инструкции EEC-Directive 79/831 Annex V. А 8 с помощью ЖХВД (способ градиентов, ацетонитрил/0,1% водная фосфорная кислота). Смесь, состоящую из 5 ммолей 5,7-дихлор-6-(5-хлорпиримидин-4-ил)-3-формилпиразоло[1,5-а] пиримидина, 5 ммолей 4-метилпиперидина и 5 ммолей карбоната калия в 30 мл ацетонитрила, перемешивают в течении 15 ч при комнатной температуре. После этого реакционную смесь помещают в 120 мл воды. Три раза экстрагируют этиловым эфиром уксусной кислоты, объединенные органические фазы сушат над сульфатом натрия и отгоняют растворитель при пониженном давлении. Полученный остаток хроматографируют с циклогексан/этиловым эфиром уксусной кислоты = 3:1 на силикагеле. Таким образом получают 1,15 ммоля 5-хлор-6-(5-хлорпиримидин-4-ил)-3-формил-7-(4-метилпиперидин-1-ил)пиразоло[1,5-а]пиримидина. ЖХВД: log P = 3,04. Пример 75 В раствор 1,4 ммоля бромида метилтрифенил-фосфония и 1,4 ммоля н-бутиллития в 58 мл тетрагидрофурана добавляют при температуре -70 С и при перемешивании 1,3 ммоля 5-хлор-6-(5-хлорпиримидин-4-ил)-3-формил-7-(4-метилпиперидин-1-ил)пиразоло[1,5-а]-пиримидина. Перемешивают в течении 15 ч при комнатной температуре, отгоняют растворитель при пониженном давлении и к остатку добавляют воду. Полученную смесь три раза экстрагируют этиловым эфиром уксусной кислоты. Объединенные органические фазы сушат над сульфатом натрия и затем отгоняют растворитель при пониженном давлении. Остаток хроматографируют с циклогексан/этиловым эфиром уксусной кислоты = 7:3 на силикагеле. Таким образом получают 0,2 ммоля 5-хлор-6-(5-хлорпиримидин-4-ил)-3-этенил-7-(4-метилпиперидин-4 ил)пиразоло[1,5-а]пиримидина. ЖХВД: log P = 4,70. Пример 76 100 ммолей 3-аминопиразола и 100 ммолей диметилового эфира 2-(5-хлорпиримидин-4 ил)малоновой кислоты добавляют при перемешивании при комнатной температуре в 27 мл три-нбутиламина. После окончания добавления реакционную смесь в течении 3 ч перемешивают с нагревом до 185 С. При этом метанол, образующийся при взаимодействии, постоянно отгоняется. Затем охлаждают до комнатной температуры, декантируют три-н-бутиламин, остаток перемешивают со смесью изопропанола и метилтретбутилового эфира и в заключение повторно декантируют. При пониженном давлении отгоняют еще содержащиеся остатки растворителя. Полученный таким образом 5,7-дигидрокси-6(5-хлор-пиримидин-4-ил)-пиразоло[1,5-а]пиримидин используют без дополнительной очистки для дальнейших взаимодействий. Пример 77 Смесь, состоящую из 56 ммолей 5,7-дигидрокси-6-(5-хлорпиримидин-4-ил)пиразоло[1,5-а] пиримидина и 560 ммолей фосфороксихлорида, перемешивают 30 мин при 30 С, затем охлаждают до 0 С и после этого добавляют по каплям при перемешивании 85 ммолей диметилформамида. После окончания- 26009517 добавления реакционную смесь продолжают перемешивать еще 12 ч при комнатной температуре и затем в течении 6 часов нагревают с обратной перегонкой. В заключение к реакционной смеси добавляют 56 ммолей пентахлорида фосфора и продолжают нагревать еще 12 ч при обратной перегонке. После охлаждения до комнатной температуры из реакционной смеси отгоняют при пониженном давлении растворитель и затем подают ее в ледяную воду. Образовавшуюся смесь экстрагируют три раза этиловым эфиром уксусной кислоты. Объединенные органические фазы сушат над сульфатом натрия и затем отгоняют растворитель при пониженном давлении. Полученный 3-формил-5,7-дихлор-8-(5-хлорпиримидин-4-ил)пиразоло[1,5-а]пиримидин используют без дополнительной очистки для дальнейших синтезов. Пример А. Тест на Venturia (яблони) / защитный. Растворитель: 24,5 вес. ч. ацетона,24,5 вес. ч. диметилацетамида. Эмульгатор: 1 вес. ч. алкиларилполигликолевого эфира. Для получения целесообразной рецептуры биологически активного вещества смешивают 1 вес. ч. биологически активного вещества с указанными количествами растворителя и эмульгатора и разбавляют концентрат водой до нужной концентрации. Для испытания защитной эффективности молодые растения опрыскивают рецептурой биологически активного вещества указанными расходными количествами. После высыхания налета после опрыскивания растения инокулируют водной суспензией конидий возбудителя парши яблонь Venturia inaequalis и оставляют в инкубационной кабине на один день при температуре около 20 С и относительной влажности воздуха 100%. Растения помещают в теплицу при температуре около 21 С и относительной влажности воздуха около 90%. Спустя 10 дней после инокуляции происходит оценка. При этом 0% означает эффективность, которая соответствует эффективности контроля, в то время как эффективность 100% означает, что не наблюдается никакого поражения. В этом тесте соединения согласно данному изобретению, приведенные в примерах 1, 2, 3, 4 и 5, показывают эффективность свыше 90% при расходных количествах 100 г/га. Пример В. Тест на Botrytis (фасоль) / защитный. Растворитель: 24,5 вес. ч. ацетона,24,5 вес. ч. диметилацетамида. Эмульгатор: 1 вес. ч. алкиларилполигликолевого эфира. Для получения целесообразной рецептуры биологически активного вещества смешивают 1 вес. ч. биологически активного вещества с указанными количествами растворителя и эмульгатора и разбавляют концентрат водой до нужной концентрации. Для испытания защитной активности молодые растения опрыскивают рецептурой биологически активного вещества указанными расходными количествами. После высыхания налета после опрыскивания на каждый листик помещают два маленьких кусочка агара, обросшие Botrytis cinerea. Инокулированные растения помещают в затемненную камеру при температуре около 20 С и относительной влажности воздуха 100%. Спустя 2 дня после инокуляции оценивают величину пятен на листьях, соответствующих нападению. При этом 0% означает эффективность, которая соответствует эффективности контроля, в то время как эффективность 100% означает, что не наблюдается никакого поражения. В этом тесте соединения согласно данному изобретению, приведенные в примерах 2, 3 и 5, показывают эффективность свыше 85% при расходных количествах 500 г/га. Пример С. Тест на Puccinia (пшеница) / защитный. Растворитель: 50 вес. ч. N,N-диметилацетамида. Эмульгатор: 1 вес. ч. алкиларилполигликолевого эфира. Для получения целесообразной рецептуры биологически активного вещества смешивают 1 вес. ч. биологически активного вещества с указанными количествами растворителя и эмульгатора и разбавляют концентрат водой до нужной концентрации. Для испытания защитной активности молодые растения опрыскивают рецептурой биологически активного вещества указанными расходными количествами. После высыхания налета после опрыскивания растения опрыскивают водной суспензией конидий Puccinia recondita. Растения оставляют в инкубационной кабине на 48 часов при температуре 20 С и относительной влажности воздуха 100%. Растения помещают после этого в теплицу при температуре около 20 С и относительной влажности воздуха около 80%, для того чтобы создать благоприятные условия для развития пустул ржавчины. Спустя 10 дней после инокуляции происходит оценка. При этом 0% означает эффективность, которая соответствует эффективности контроля, в то время как эффективность 100% означает, что не наблюдается никакого поражения. В этом тесте соединения согласно данному изобретению, приведенные в примерах 2 и 39, показывают эффективность свыше 85% при расходных количествах 500 г/га. Пример D. Тест на Podosphaera (яблони) / защитный. 24,5 вес. ч. ацетона,24,5 вес. ч. диметилацетамида. Эмульгатор: 1 вес. ч. алкиларилполигликолевого эфира. Для получения целесообразной рецептуры биологически активного вещества смешивают 1 вес. ч. биологически активного вещества с указанными количествами растворителя и эмульгатора и разбавляют концентрат водой до нужной концентрации. Для испытаний защитной активности молодые растения опрыскивают рецептурой биологически активного вещества с указанными расходными количествами. После высыхания налета после опрыскивания растения инокулируют водной суспензией спор возбудителя мучнистой росы на яблонях Podosphaeraleucotricha. Затем растения помещают в теплицу при температуре около 23 С и относительной влажности воздуха около 70%. Спустя 10 дней после инокуляции происходит оценка. При этом 0% означает эффективность, которая соответствует эффективности контроля, в то время как эффективность 100% означает, что не наблюдается никакого поражения. В этом тесте соединения согласно данному изобретению, приведенные в примерах 3 и 5, показывают эффективность свыше 90% при расходных количествах 100 г/га. Пример Е. Тест in vitro для определения ED50 микроорганизмов. Растворитель: метанол. Эмульгатор: алкиларилполигликолевый эфир. Смешивают 2 мг биологически активного вещества с 100 мкл метанола и затем разбавляют концентрат, полученный таким образом, смесью 1000 мл метанола и 6 г приведенного выше эмульгатора до любой необходимой концентрации. В кавитации (углубления) микротитровальных пластин помещают пипетками по 10 мкл приготовленного препарата. После испарения растворителя в каждое углубление помешают 200 мкл картофельнодекстрозной среды, к которой перед этим была добавлена необходимая концентрация спор, соответственно, мицел испытуемого микроорганизма. Результирующие концентрации биологически активного вещества в кавитациях составляют: 0,1 млн. долей,1 млн. долей,10 млн. долей,100 млн. долей, соответственно. Результирующая концентрация эмульгатора составляет в каждом случае 300 млн. долей. Для инкубации микротитровальные пластины затем помещают на 3-5 дней во встряхивающее устройство при температуре 22 С и встряхивают до тех пор, пока на необработанном контроле не будет обнаружен необходимый рост соответствующих микроорганизмов. Оценку осуществляют фотометрически при длине волны 620 нм. Из результатов измерений для различных концентраций определяют дозу биологически активного вещества, которая ведет к 50 процентному торможению роста грибов (ED50) по сравнению с необработанным контролем. Согласно этому тесту значение ED50 для соединения согласно данному изобретению, приведенного в примере 1, по отношению к Botrytis cinerea достигается при дозе биологически активного вещества,которая составляет меньше, чем 10 млн. долей. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Пиразолопиримидины формулы (I) где R1 означает алкил, содержащий 1-6 атомов углерода, который может быть замещен от однократно до пятикратно, одинаково или различно галоидом, циано-, гидрокси-, алкоксигруппой, содержащей 1-4 атома углерода, и/или циклоалкилом, содержащим 3-6 атомов углерода, илиR1 означает алкенил, содержащий 2-6 атомов углерода, который может быть замещен от однократно до трехкратно, одинаково или различно галоидом, циано-, гидрокси-, алкоксигруппой, содержащей 14 атома углерода, и/или циклоалкилом, содержащим 3-6 атомов углерода, илиR1 означает циклоалкил, содержащий 3-6 атомов углерода, который может быть замещен от однократно до трехкратно, одинаково или различно галоидом и/или алкилом, содержащим 1-4 атома углерода,R2 означает водород или алкил, содержащий 1-4 атома углерода, илиR1 и R2 вместе с атомом азота, к которому они присоединены, означают насыщенное или ненасы- 28009517 щенное гетероциклическое кольцо, содержащее 3-6 атомов в кольце, причем гетероцикл может содержать дополнительно атом азота, кислорода или серы в качестве атома кольца и может быть замещен до трехкратно фтором, хлором, бромом, алкилом, содержащим 1-4 атома углерода, и/или галоидалкилом,содержащим 1-4 атома углерода и 1-9 атомов фтора и/или хлора,R3 означает насыщенный или ненасыщенный гетероциклил, содержащий 5 или 6 атомов в кольце и 1-4 гетероатома, таких как азот и/или сера, причем гетероциклил может быть замещен от однократно до четырехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, алкилом, алкоксигруппой, гидроксиминоалкилом или алкоксиминоалкилом с 1-3 атомами углерода в каждой алкильной части,галоидалкилом или галоидалкоксигруппой, содержащими 1-3 атома углерода и 1-7 атомов галоида,R4 означает водород,Hal означает фтор, хлор или бром и причемозначает место присоединения,R2 означает водород, метил, этил или пропил илиR1 и R2 вместе с атомом азота, к которому они присоединены, означают пирролидинил, пиперидинил, морфолинил, тиоморфолинил, пиперазинил, 3,6-дигидро-1(2 Н)-пиперидинил или тетрагидро-1(2 Н)пиридазинил, причем эти радикалы могут быть замещены 1-3 атомами фтора, 1-3 метильными группами и/или трифторметилом, или где R' означает водород или метил,R" означает метил, этил, фтор, хлор или трифторметил,m означает числа 0, 1, 2 или 3, причем R" означает одинаковые или различные радикалы, если m означает 2 или 3,R'" означает метил, этил, фтор, хлор или трифторметил иn означает числа 0, 1, 2 или 3, причем R'" означает одинаковые или различные радикалы, если n означает 2 или 3,R3 означает пиридил, который присоединен во 2 или 4 положении и может быть замещен от однократно до четырехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, метилом, этилом, метокси-, метилтиогруппой, гидроксиминометилом, гидроксиминоэтилом, метоксиминометилом, метоксиминоэтилом и/или трифторметилом, илиR3 означает пиримидил, который присоединен во 2 или 4 положении и может быть замещен от однократно до трехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, метилом, этилом, метокси-, метилтиогруппой, гидроксиминометилом, гидроксиминоэтилом, метоксиминометилом, метоксиминоэтилом и/или трифторметилом, илиR3 означает тиенил, который присоединен во 2 или 3 положении и может быть замещен от одно- 29009517 кратно до трехкратно, одинаково или различно фтором, хлором, бромом, циано-, нитрогруппой, метилом, этилом, метокси-, метилтиогруппой, гидроксиминометилом, гидроксиминоэтилом, метоксиминометилом, метоксиминоэтилом и/или трифторметилом, илиR4 означает водород,Hal означает фтор или хлор, и 3. Способ получения пиразолопиримидинов формулы (I) по п.1, отличающийся тем, что галоидпиразолопиримидины формулыR4 и Hal имеют значения, приведенные в п.1,R3 означает пиридил, который присоединен во 2 или 4 положении и может быть замещен от однократно до четырехкратно трифторметилом, илиR3 означает пиримидил, который присоединен во 2 или 4 положении и может быть замещен от однократно до трехкратно, одинаково или различно фтором и/или хлором,R3 означает тиенил, который присоединен во 2 или 3 положении и может быть замещен от однократно до трехкратно хлором или метилом,X1 означает цианогруппу или формил, иR1 и R2 имеют значения, приведенные в п.1,при необходимости в присутствии разбавителя, при необходимости в присутствии акцептора кислоты и при необходимости в присутствии катализатора. 4. Средство для борьбы с нежелательными микроорганизмами, отличающееся тем, что содержит как минимум один пиразолопиримидин формулы (I) по п.1 или 2, наряду с наполнителями и/или поверхностно-активными веществами. 5. Применение пиразолопиримидинов формулы (I) по п.1 или 2 для борьбы с нежелательными микроорганизмами. 6. Способ борьбы с нежелательными микроорганизмами, отличающийся тем, что наносят на нежелательные микроорганизмы и/или на их жизненную среду пиразолопиримидины формулы (I) по п.1 или 2. 7. Способ получения средств для борьбы с нежелательными микроорганизмами, отличающийся тем, что смешивают наполнители и/или поверхностно-активные вещества с пиразолопиримидинами формулы (I) по п.1 или 2. 8. Галоидпиразолопиримидины формулы где R3 означает пиридил, который присоединен во 2- или 4-положении и может быть замещен от
МПК / Метки
МПК: C07D 213/55, C07D 487/04, C07D 213/61, A01N 43/90
Метки: пиразолопиримидины
Код ссылки
<a href="https://eas.patents.su/30-9517-pirazolopirimidiny.html" rel="bookmark" title="База патентов Евразийского Союза">Пиразолопиримидины</a>
Предыдущий патент: Композиция для уменьшения токсических, алиментарных и/или метаболических нарушений, связанных с раком, и/или химиотерапией рака, и способы её применения
Следующий патент: Соединения, модулирующие активность ppar, и способы их получения
Случайный патент: Бульдозер-погрузчик с трансформирующимся рабочим органом







