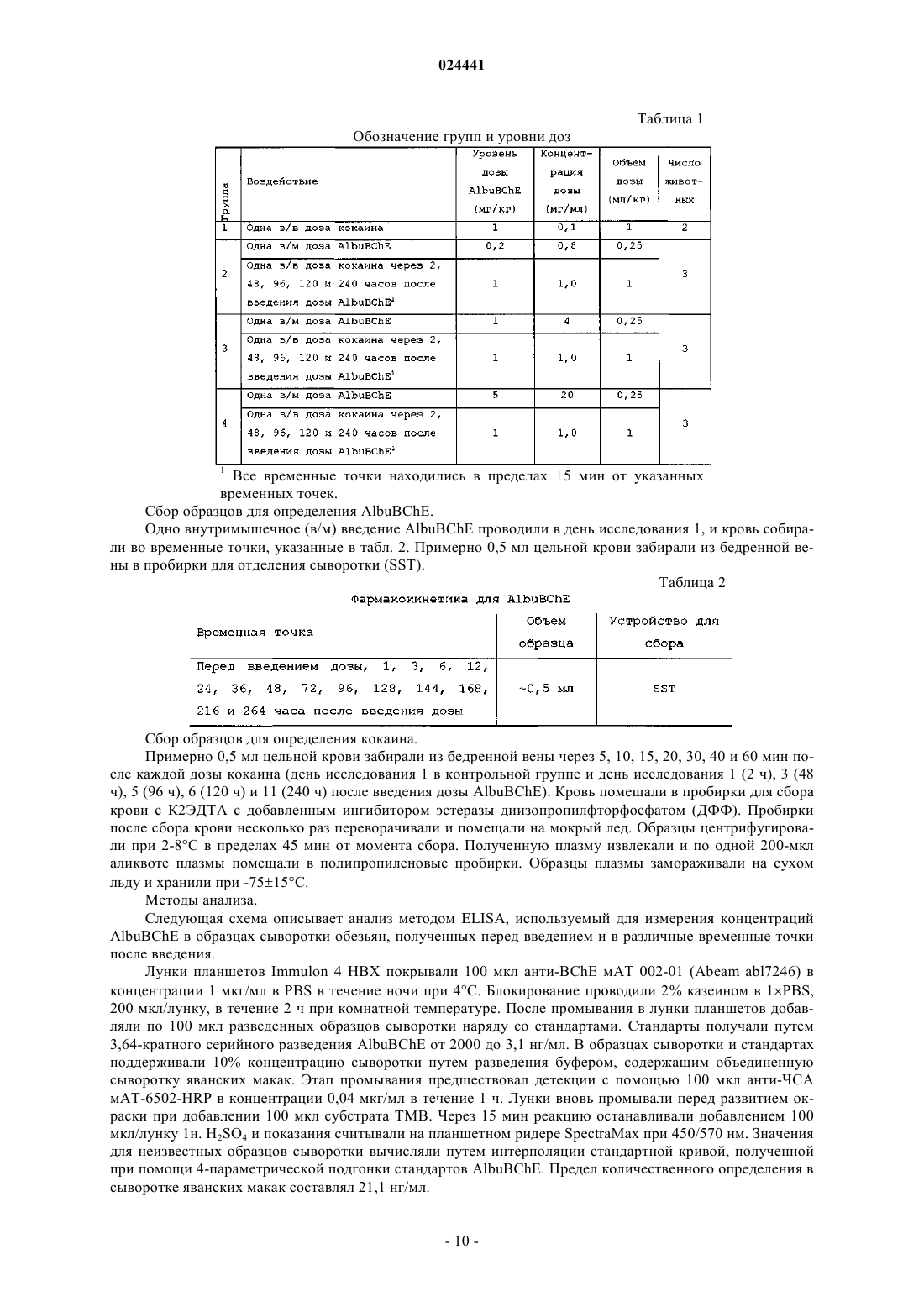
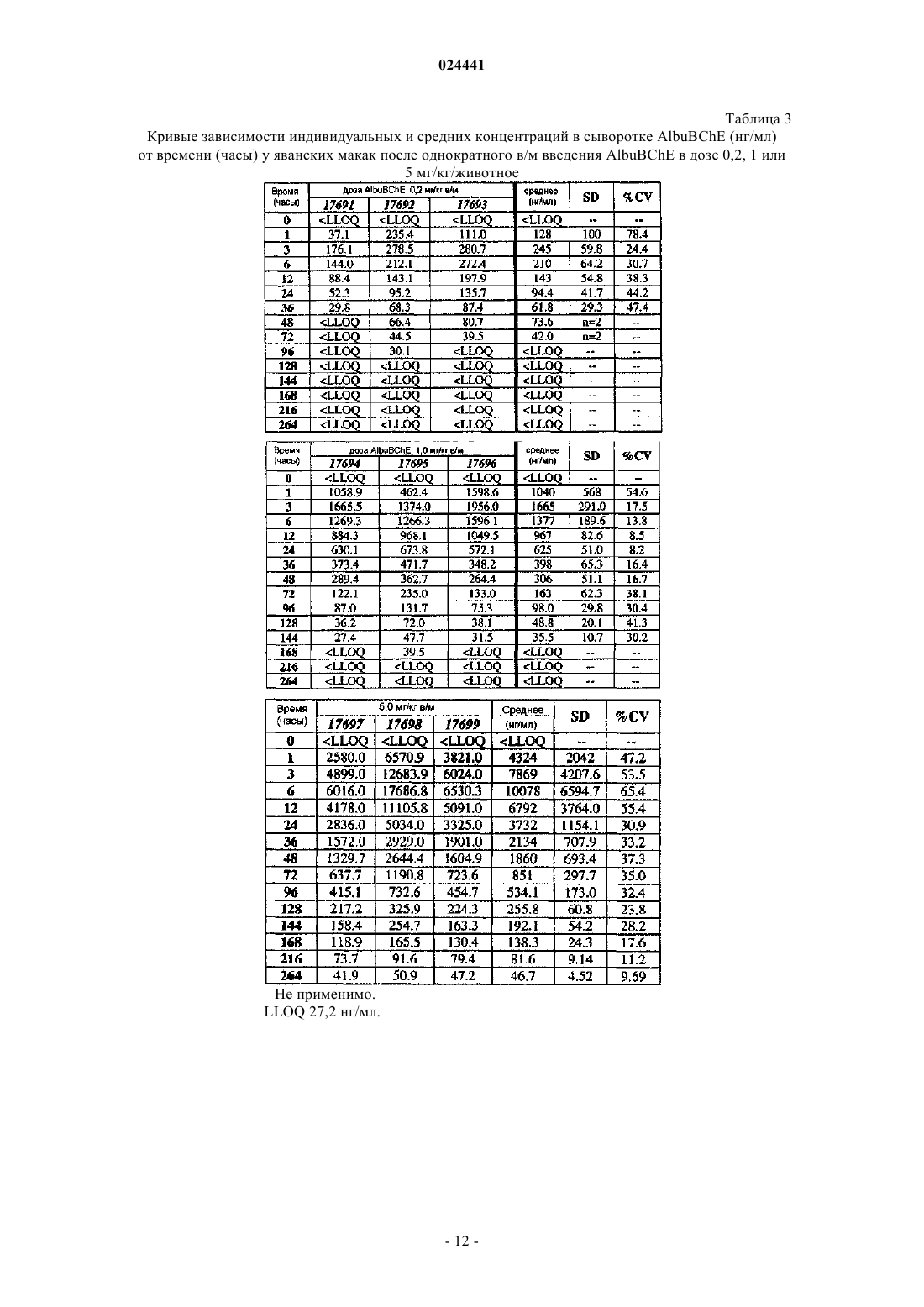
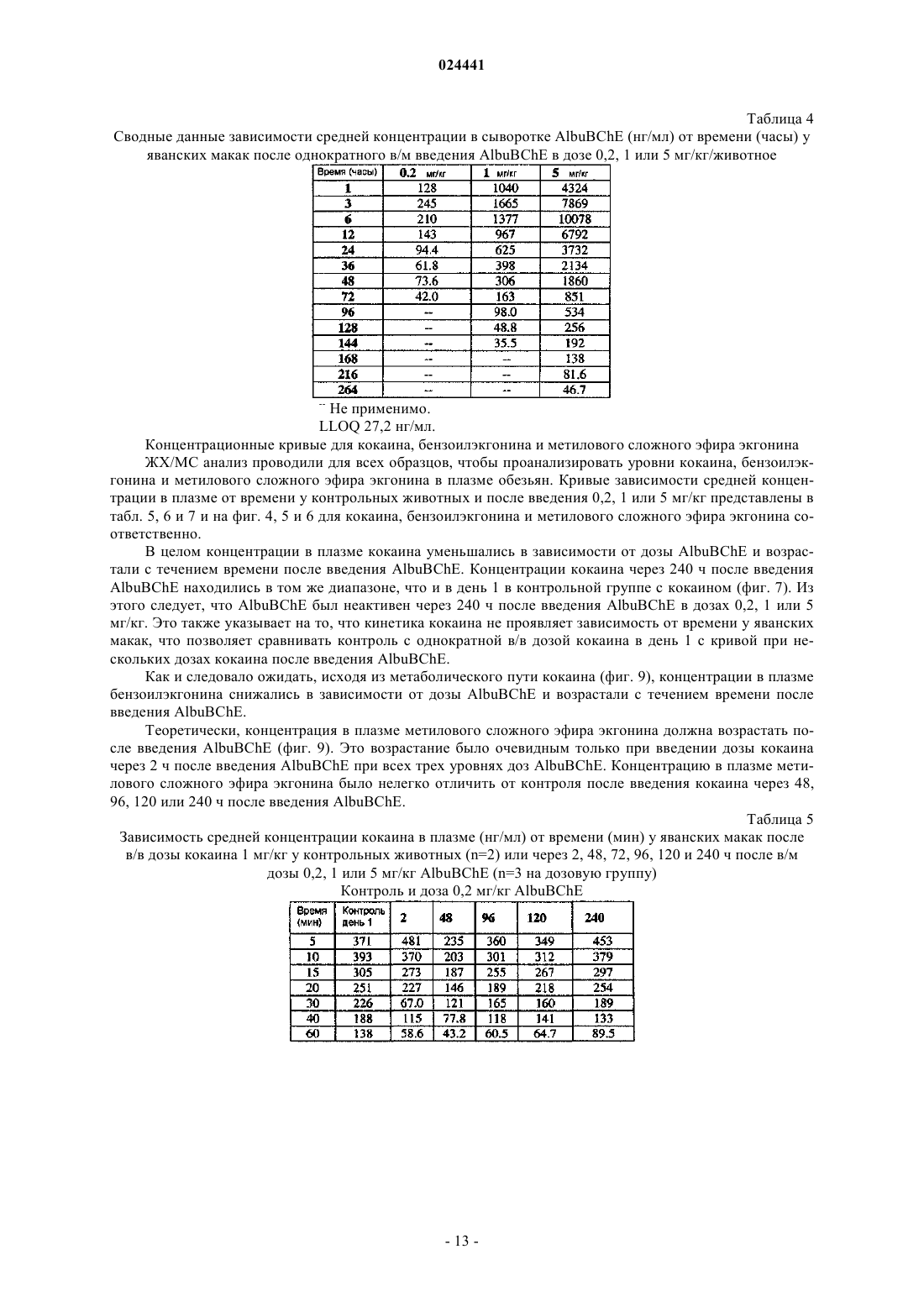
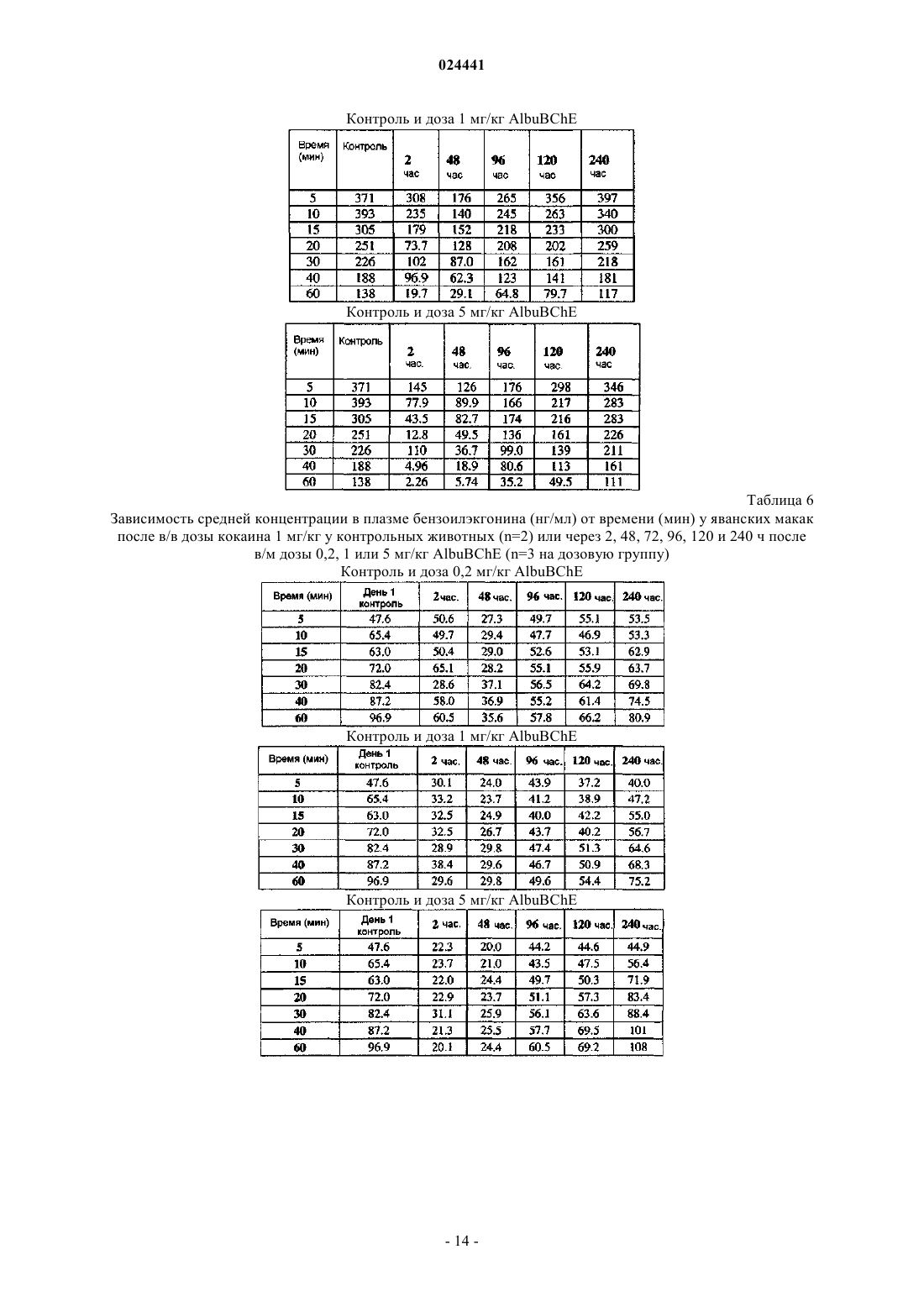
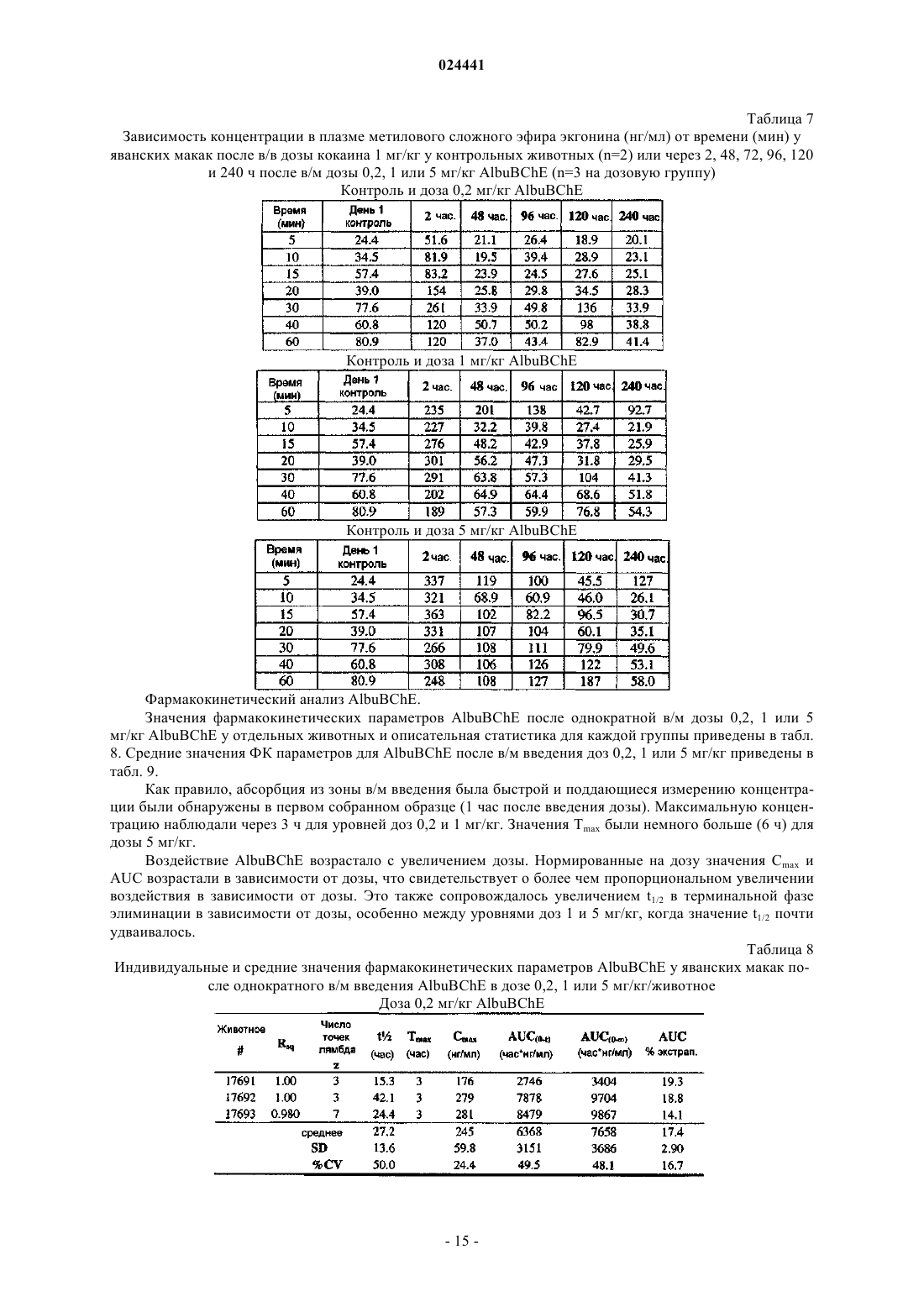
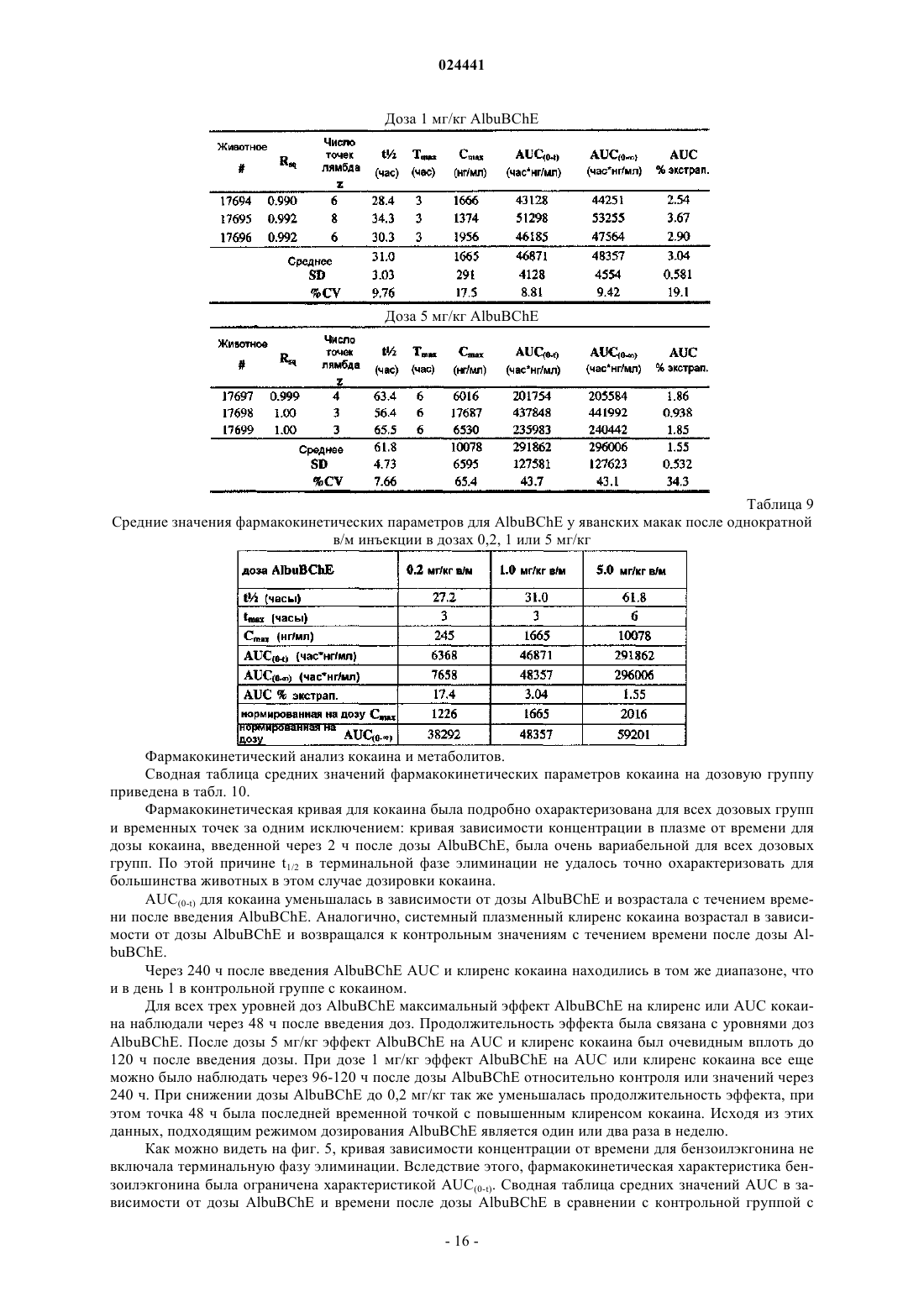
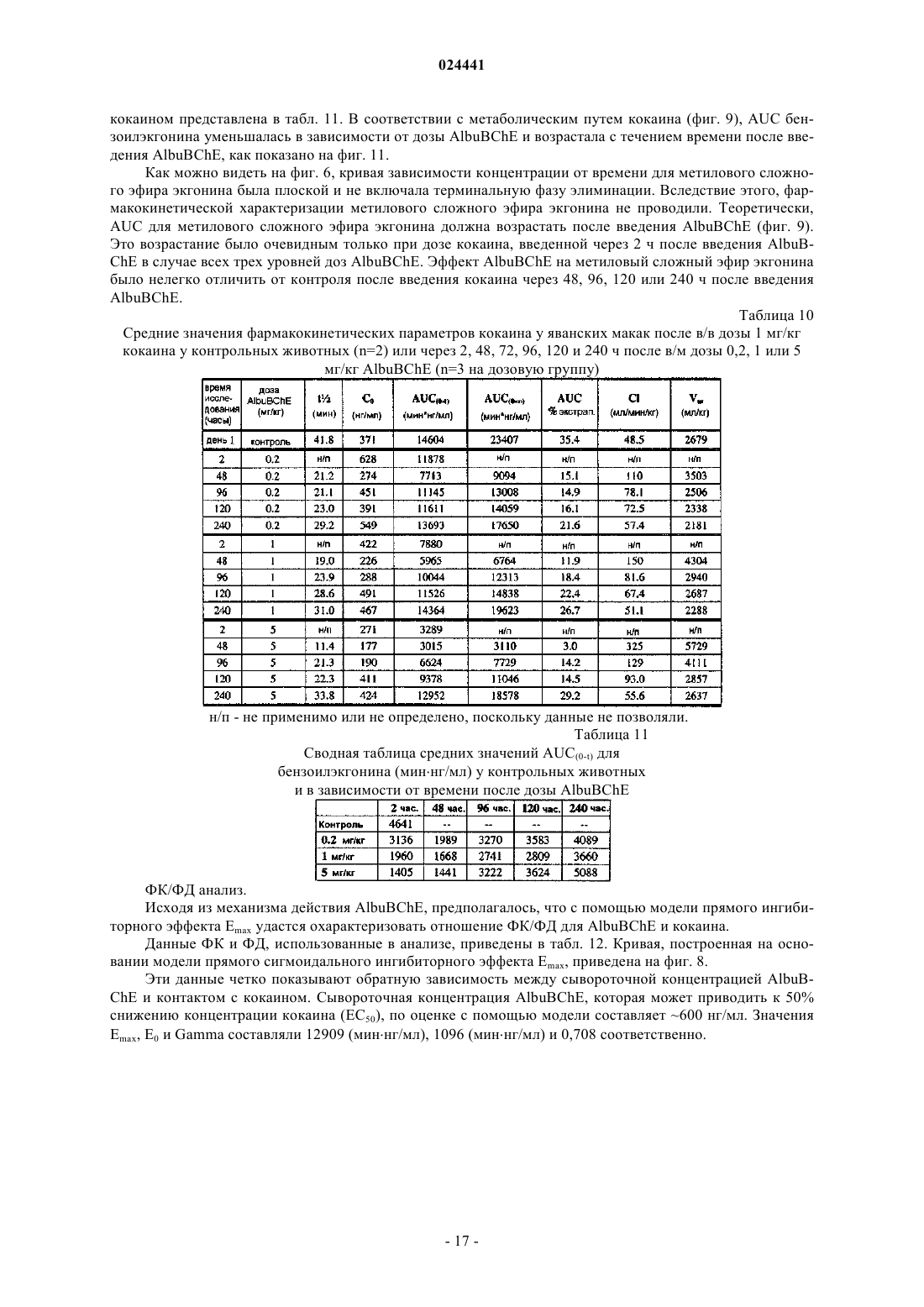
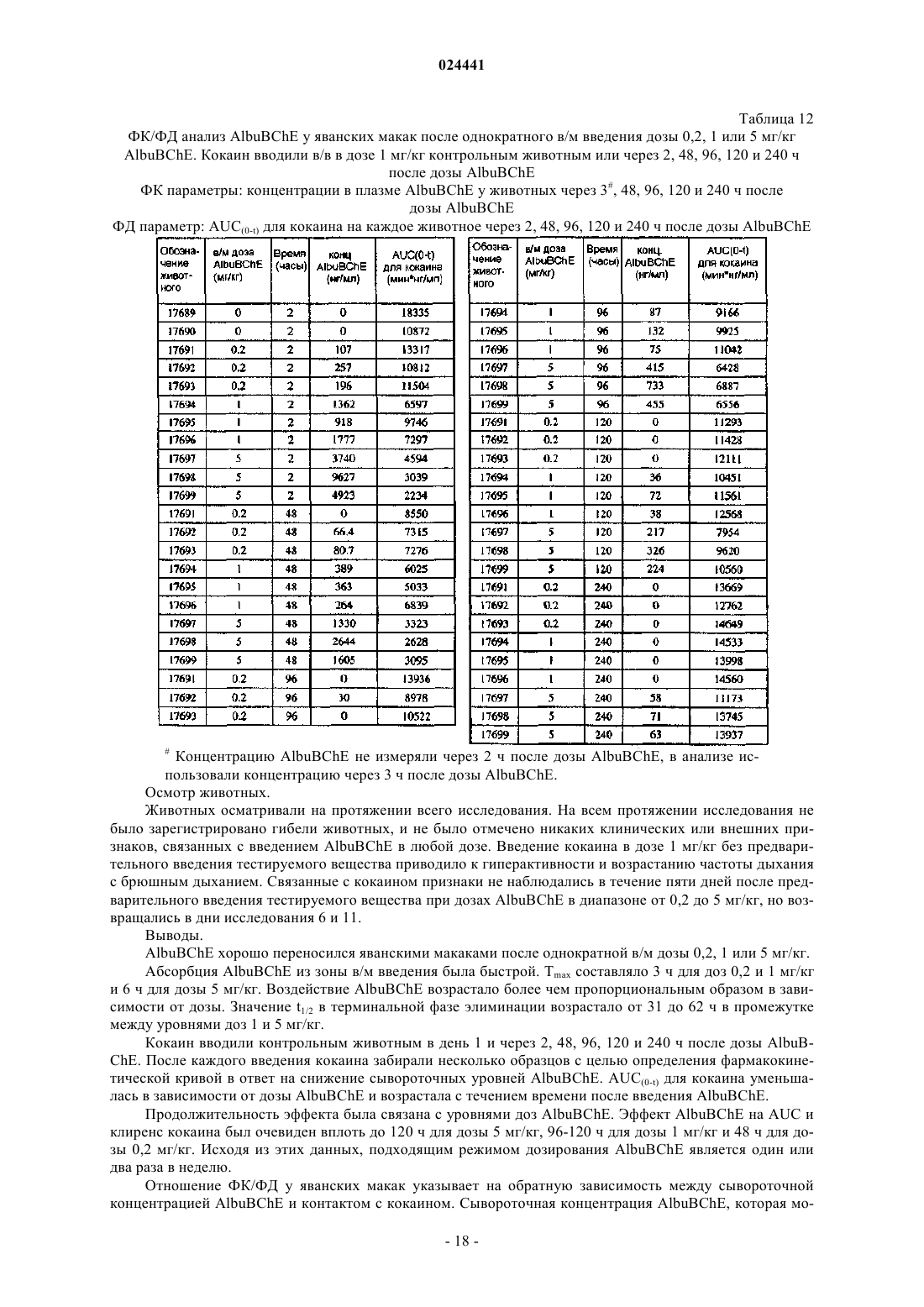
Слитый белок bche-альбумин для лечения злоупотребления кокаином
Номер патента: 24441
Опубликовано: 30.09.2016
Авторы: Шемеш-Дарвиш Лирон, Лафлер Дэвид, Пирятинский Виктор, Розеншток Моти, Рошке Виктор, Халлак Хуссейн, Склэр-Таврон Лиора
Формула / Реферат
1. Способ ослабления биологического эффекта контакта с кокаином у примата, включающий введение эффективного количества слитого белка, содержащего:
(а) мутантный полипептид бутирилхолинэстеразы (BChE), содержащий последовательность

(b) полипептид человеческого сывороточного альбумина (ЧСА), содержащий последовательность

где количество слитого белка является эффективным для ослабления биологического эффекта контакта с кокаином у примата.
2. Способ по п.1, в котором слитый белок содержит последовательность


3. Способ по п.1 или 2, в котором слитый белок вводят до контакта примата с кокаином.
4. Способ по п.1 или 2, в котором слитый белок вводят после контакта примата с кокаином.
5. Способ по п.1 или 2, в котором слитый белок вводят вплоть до 1 дня до или вплоть до 1 ч после контакта примата с кокаином.
6. Способ по любому из пп.1-5, в котором контакт с кокаином является однократным или повторяющимся.
7. Способ по любому из пп.1-6, в котором биологический эффект представляет собой увеличение артериального давления, увеличение частоты сердечных сокращений или температуры тела или поведение примата, направленное на поиск кокаина.
8. Способ по п.7, в котором биологический эффект представляет собой поведение примата, направленное на поиск кокаина.
9. Способ по п.8, в котором поведение, направленное на поиск кокаина, имеет место в период воздержания от кокаина после контакта с кокаином или следует за рецидивом.
10. Способ по любому из пп.7-9, в котором ослабление поведения, направленного на поиск кокаина, приводит к:
(i) периоду воздержания от кокаина, составляющему от 2 до 3 недель;
(ii) большему относительному числу дней, когда примат не подвергается воздействию кокаина, чем в ситуации без введения;
(iii) большему числу дней подряд, в которые примат не подвергается воздействию кокаина, чем в ситуации без введения; или
(iv) любому сочетанию вышеперечисленных (i)-(iii).
11. Способ по любому из пп.1-10, в котором:
(i) введение слитого белка приводит к понижению общего контакта с кокаином у примата, чем в ситуации без введения;
(ii) эффективное количество слитого белка представляет собой количество, которое снижает уровень кокаина в сыворотке примата до примерно 0 нг/мл в течение примерно 30 мин при внутривенной дозе кокаина 1 мг/кг;
(iii) слитый белок вводят один раз в неделю или два раза в неделю;
(iv) слитый белок вводят внутримышечной инфекцией или подкожной инъекцией;
(v) слитый белок находится в буфере для препарата, содержащем 10 мМ фосфата натрия, 200 мМ маннитола, 60 мМ трегалозы и 0,01% (w/v) полисорбат 80, рН 7,2; или
(vi) имеет место любое сочетание вышеперечисленных (i)-(v).
12. Способ по любому из пп.1-11, в котором примат представляет собой человека.
13. Способ по п.12, в котором:
(i) эффективное количество слитого белка представляет собой количество, которое снижает уровень кокаина в сыворотке человека до примерно 0 нг/мл в течение примерно 30 мин при внутривенном введении дозы кокаина 40 мг;
(ii) эффективное количество сбитого белка составляет от 0,06 до 5 мг/кг или
(iii) эффективное количество слитого белка составляет от 50 до 300 мг.
14. Способ по любому из пп.1-13, в котором слитый белок вводят внутримышечным путем.
15. Способ по любому из пп.1-13, в котором эффективное количество слитого белка составляет от 150 до 300 мг.
16. Слитый белок, содержащий:
(a) сигнальный пептид, содержащий последовательность
MRPTWAWWLFLVLLLALWAPARG (SEQ ID NO: 3);
(b) мутантный полипептид бутирилхолинэстеразы (BChE), содержащий последовательность

(с) полипептид человеческого сывороточного альбумина (ЧСА), содержащий последовательность

пригодный для применения в ослаблении биологического эффекта от контакта с кокаином у примата.
17. Слитый белок по п.16, содержащий последовательность

Текст
СЛИТЫЙ БЕЛОК BChE-АЛЬБУМИН ДЛЯ ЛЕЧЕНИЯ ЗЛОУПОТРЕБЛЕНИЯ КОКАИНОМ Способ ослабления биологического эффекта контакта с кокаином у примата. Такой способ включает введение примату некоторого количества слитого белка BChE-альбумин, содержащего аминокислотные замены A227S, S315G, A356W и Y360G, при этом количество слитого белка является эффективным для ослабления биологического эффекта контакта с кокаином у примата.(71)(73) Заявитель и патентовладелец: ТЕВА ФАРМАСЬЮТИКАЛ ИНДАСТРИЗ ЛТД. (IL) По заявке на данный патент испрашивается приоритет предварительных патентных заявок США 61/412205, поданной 10 ноября 2010 г., и 61/283791, поданной 8 декабря 2009 г., полное содержание которых включено в данный документ посредством ссылок. На всем протяжении данного изобретения приведены ссылки на различные публикации, опубликованные патентные заявки и патенты. Полное содержание этих документов включено в данный патент посредством ссылок в целях более полного описания состояния области техники, к которой относится данное изобретение. Уровень техники Злоупотребление кокаином и зависимость от него имеют катастрофические медицинские и социальные последствия, которые делают разработку эффективного лечения высокоприоритетной (Pan, Y.,Gao, D., Yang, W., Cho, H., Yahg, G., Tai, H., Zhan, C., "Computational redesign of human butyrylcholinesterase for anticocaine medication", PNAS, 102(46): 16656-61, 2005). Однако, как заявлено в статье Brimijoin et al., "нет надежного средства для лечения передозировки кокаина или снижения вероятности рецидива у употребляющих его людей, которые добились отказа от наркотика. Бутирилхолинэстераза (BChE) из человеческой плазмы принимает участие в нормальном метаболизме кокаина и предполагается для использования в лечении кокаиновой токсичности" (Brimijoin, S., Gao, Y., Anker, J., Gliddon, L., LaFleur,D., Shah, R., Zhao, Q., Singh, M., Carroll, M., "A Cocaine Hydrolase Engineered from Human Butyrylcholinesterase Selectively Blocks Cocaine Toxicity and Reinstatement of Drug Seeking in Rats", Neuropsychopharmacology, 33: 2715-25, 2008).BChE дикого типа, будучи важной для метаболизма кокаина в организме, имеет низкую каталитическую эффективность в отношении кокаина. Из-за низкой гидролазной активности в отношении кокаина BChE дикого типа потребовалось бы использование чрезмерно больших количеств очищенного фермента для лечения кокаиновой зависимости или передозировки. Мутагенез, примененный к человеческойBChE с целью усиления гидролазной активности в отношении кокаина, привел к созданию двойного мутанта A328W/Y332A (остатки 356 и 360 относительно полноразмерной BChE), который имеет kcat в 40 раз выше, чем BChE дикого типа, лишь с ненамного увеличенной KM (Sun H., Shen M., Pang Y., Lockridge О., Brimijoin S., "Cocaine Metabolism Accelerated by a Re-Engineered Human Butyrylcholinesterase",Journal of Pharmacology and Experimental Therapeutics, 302(2): 710-716, 2002). Дальнейшие эксперименты с использованием молекулярной динамики для моделирования переходного состояния для первой стадии химической реакции катализируемого BChE гидролиза кокаина привели к созданию мутанта BChE A227S/S315G/A356W/Y360G, имеющего каталитическую активность,в 500 раз превышающую активность BChE дикого типа и превышающую активность других ранее созданных мутантов BChE (Pan, Y., Gao, D., Yang, W., Cho, H., Yang, G., Tai, H., Zhan, C., "Computationalredesign of human butyrylcholinesterase for anticocaine medication", PNAS, 102(46): 16656-61, 2005). Для получения формы мутанта A227S/S315G/A356W/Y360G BChE, подходящей для терапевтического применения, мутант BChE, разработанный Pan et al., был слит по его С-концу с человеческим сывороточным альбумином (ЧСА) (HSA), поскольку было замечено, что продукты подобного слияния обладают благоприятными фармакокинетическими свойствами с высокой стабильностью и более продолжительными периодами полувыведения из плазмы. Было отмечено, что слитый белок BChE-альбумин,содержащий вышеуказанные мутации, сохраняет высокую каталитическую эффективность в отношении кокаина и характеризуется периодом полувыведения из плазмы, равным 8 ч, после в/в инъекции крысам.Rats", Neuropsycopharmacology, 33: 2715-25, 2008). До настоящего времени не разработан эффективный способ лечения злоупотребления кокаином или его передозировки у приматов, в котором бы использовался слитый белок BChE-альбумин, содержащий мутации A227S, S315G, A356W и Y360G. Сущность изобретения Изобретение относится к способу ослабления биологического эффекта от контакта с кокаином у примата, включающему введение примату некоторого количества слитого белка, содержащего:(а) мутантный полипептид бутирилхолинэстеразы (BChE), содержащий последовательностьb) полипептид человеческого сывороточного альбумина (ЧСА), содержащий последовательностьMRPTWAWWLFLVLLLALWAPARG (SEQ ID NO: 3),при этом количество слитого белка является эффективным для ослабления биологического эффекта от контакта с кокаином у примата. Описание фигур На фиг. 1 (SEQ ID NO:4) представлена аминокислотная последовательность AlbuBChE, слитого белка BChE-альбумин, содержащего мутации A227S, S315G, A356W и Y360G. На фиг. 2 представлен график зависимости концентрации в сыворотке AlbuBChE от времени у отдельных яванских макак после однократного в/м введения AlbuBChE в дозе 0,2, 1 или 5 мг/кг (верхняя панель - линейная шкала, нижняя панель полулогарифмическая шкала). На фиг. 3 представлен график зависимости средней концентрации в сыворотке AlbuBChE от времени у яванских макак после однократного в/м введения AlbuBChE в дозе 0,2, 1 или 5 мг/кг (верхняя панель - линейная шкала, нижняя панель полулогарифмическая шкала). На фиг. 4 представлен график зависимости средней концентрации кокаина от времени у контрольных животных (n=2) и график зависимости от времени после введения дозы AlbuBChE (n=3). На фиг. 5 представлен график зависимости средней концентрации бензоилэкгонина от времени у контрольных животных (n=2) и график зависимости от времени после введения дозы AlbuBChE (n=3). На фиг. 6 представлен график зависимости средней концентрации метилового сложного эфира экгонина от времени у контрольных животных (n=2) и график зависимости от времени после введения дозы AlbuBChE (n=3). На фиг. 7 приведено сравнение графика зависимости средней концентрации кокаина от времени для дня 1 в контрольной группе с кокаином с графиком для дня 11 (240 ч) после введения AlbuBChE в дозе 0,2, 1 или 5 мг/кг. На фиг. 8 представлен ФК/ФД (PK/PD) анализ для AlbuBChE у яванских макак после однократного в/м введения AlbuBChE в дозе 0,2, 1 или 5 мг/кг. Кокаин вводили в/в в дозе 1 мг/кг контрольным животным или через 2, 48, 96, 120 и 240 ч после введения дозы AlbuBChE. На фиг. 9 представлены метаболические пути кокаина. На фиг. 10 представлена средняя AUC(0-t) для кокаина после в/в дозы кокаина 1 мг/кг у контрольных животных (n=2) и график зависимости от времени после введения дозы AlbuBChE (n=3). На фиг. 11 представлена средняя AUC(0-t) для бензоилэкгонина после в/в дозы кокаина 1 мг/кг у контрольных животных (n=2) и график зависимости от времени после введения дозы AlbuBChE (n=3). На фиг. 12 представлен график зависимости концентрации в сыворотке AlbuBChE от времени у отдельных беличьих обезьян после однократного в/м введения AlbuBChE в дозе 5 мг/кг (полулогарифми-2 024441 ческая шкала). На фиг. 13 представлен график зависимости средней концентрации кокаина от времени у контрольных животных (n=2) и график зависимости от времени после введения дозы AlbuBChE (n=3). На фиг. 14 представлена средняя концентрация метилового сложного эфира экгонина через 5 мин после в/в дозы кокаина 1 мг/кг у контрольных животных (n=2) и график зависимости от времени после введения дозы AlbuBChE (n=3). На фиг. 15 представлена средняя концентрация бензоилэкгонина через 5 мин после в/в дозы кокаина 1 мг/кг у контрольных животных (n=2) и график зависимости от времени после введения дозы AlbuBChE (n=3). На фиг. 16 представлены сводные данные об уровнях кокаина и метаболитов кокаина метилового сложного эфира экгонина (ЕМЕ) и бензоилэкгонина (BZ) в крови беличьих обезьян через 5 мин (верхняя панель) и 30 мин (нижняя панель) после инъекции кокаина. На фиг. 17 представлен ФК/ФД анализ для AlbuBChE у беличьих обезьян после однократного в/м введения AlbuBChE в дозе 5 мг/кг. Кокаин вводили в/в в дозе 1 мг/кг контрольным животным (n=2) и через 2, 72 и 96 ч после дозы AlbuBChE (n=3). На фиг. 18 представлен график зависимости средней частоты сердечных сокращений от времени у яванских макак до и после однократного в/м введения AlbuBChE в дозе 15 мг/кг или буфера для препарата. На фиг. 19 представлен график зависимости среднего значения произведения значения систолического давления на значение частоты сердечных сокращений (rate pressure product) от времени у яванских макак до и после однократного в/м введения AlbuBChE в дозе 15 мг/кг или буфера для препарата. На фиг. 20 представлен график зависимости среднего артериального давления от времени у яванских макак до и после однократного в/м введения AlbuBChE в дозе 15 мг/кг или буфера для препарата. На фиг. 21 представлен график зависимости среднего диастолического давления от времени у яванских макак до и после однократного в/м введения AlbuBChE в дозе 15 мг/кг или буфера для препарата. На фиг. 22 представлен график зависимости среднего систолического давления от времени у яванских макак до и после однократного в/м введения AlbuBChE в дозе 15 мг/кг или буфера для препарата. На фиг. 23 представлен график зависимости средней температуры тела от времени у яванских макак до и после однократного в/м введения AlbuBChE в дозе 15 мг/кг или буфера для препарата. На фиг. 24 А представлен график зависимости средней частоты дыхания от времени у яванских макак до и после однократного в/м введения AlbuBChE в дозе 15 мг/кг или буфера для препарата. Данные для самцов яванских макак приведены на фиг. 24 В, верхняя панель, а данные для самок яванских макак приведены на фиг. 24 В, нижняя панель. На фиг. 25 А представлен график зависимости средних уровней SPO2 от времени у яванских макак до и после однократного в/м введения AlbuBChE в дозе 15 мг/кг или буфера для препарата. Данные для самцов яванских макак приведены на фиг. 25 В, верхняя панель, а данные для самок яванских макак приведены на фиг. 25 В, нижняя панель. На фиг. 26 представлен график зависимости средних уровней ЕТСО 2 от времени у яванских макак до и после однократного в/м введения AlbuBChE в дозе 15 мг/кг или буфера для препарата. Данные для самцов яванских макак приведены на фиг. 26 В, верхняя панель, а данные для самок яванских макак приведены на фиг. 26 В, нижняя панель. На фиг. 27 представлен график зависимости среднего артериального давления от времени у яванских макак после дозы 1 мг/кг кокаина, введенной в/в через 3 ч после дозы 15 мг/кг AlbuBChE. Дозу кокаина вводили во временной точке t=0. На фиг. 28 представлен график зависимости среднего диастолического давления от времени у яванских макак после дозы 1 мг/кг кокаина, введенной в/в через 3 ч после дозы 15 мг/кг AlbuBChE. Дозу кокаина вводили во временной точке t=0. На фиг. 29 представлен график зависимости среднего систолического давления от времени у яванских макак после дозы 1 мг/кг кокаина, введенной в/в через 3 ч после дозы 15 мг/кг AlbuBChE. Дозу кокаина вводили во временной точке t=0. На фиг. 30 представлен график зависимости средней частоты сердечных сокращений от времени у яванских макак после дозы 1 мг/кг кокаина, введенной в/в через 3 ч после дозы 15 мг/кг AlbuBChE. Дозу кокаина вводили во временной точке t=0. На фиг. 31 представлен график зависимости среднего значения произведения значения систолического давления на значение частоты сердечных сокращений от времени у яванских макак после дозы 1 мг/кг кокаина, введенной в/в через 3 ч после дозы 15 мг/кг AlbuBChE. Дозу кокаина вводили во временной точке t=0. На фиг. 32 представлен график зависимости средней температуры тела от времени у яванских макак после дозы 1 мг/кг кокаина, введенной в/в через 3 ч после дозы 15 мг/кг AlbuBChE. Дозу кокаина вводили во временной точке t=0. На фиг. 33 представлены показатели частоты реагирования яванских макак (верхние панели) и число инъекций (нижние панели) во время сессий самовведения в течение последовательных дней, когда либо кокаин, либо физиологический раствор были доступны для самовведения. Реагирование регистрировали в течение пяти дней после введения растворителя или AlbuBChE (5 мг/кг). На фиг. 34 представлены уровни восстановления самовведения кокаина после введения AlbuBChE или растворителя для AlbuBChE. AlbuBChE или растворитель вводили в/м. Через 2, 48 и 96 ч в/в дозу 0,3 мг/кг кокаина (левые панели) или в/в дозу 0,1 мг/кг кокаина (правые панели) вводили за 5 мин до сессии замены на физиологический раствор. На фиг. 35 показано модулирование эффектов различительного стимула кокаина у приученных к метамфетамину подопытных животных при помощи AlbuBChE. На фиг. 36 представлены эффекты различительного стимула метамфетамина у приученных к метамфетамину подопытных животных после введения AlbuBChE. На фиг. 37 представлена относительная концентрация в сыворотке слитого с альбумином белка по сравнению с не слитым пептидом в условиях, когда слитый с альбумином белок вводят один раз в неделю, а не слитый пептид вводят ежедневно. На фиг. 38 представлен SDS-ПААГ AlbuBChE, очищенного из клеток СНО. Дорожка 1 представляет собой маркер молекулярной массы, а дорожки 2 и 4 соответствуют очищенному AlbuBChE в восстанавливающих и не восстанавливающих условиях соответственно. На фиг. 39 представлен график зависимости числа пересечений лучей от времени у крыс, получавших BChE дикого типа или Albu-СосН перед дозой кокаина, крыс, получавших только дозу кокаина, и крыс, не получавших ни кокаин, ни BChE. Локомоторную активность оценивали, регистрируя пересечение инфракрасных лучей, как описано в статье Brimijoin et al. На фиг. 40 представлен график зависимости концентрации AlbuBChE от времени у мышей после дозы AlbuBChE, а также представлен график зависимости гидролиза кокаина (представленного как процент кокаина, преобразованного в бензойную кислоту (% БК) в течение 60 мин после введения кокаина) от времени после дозы AlbuBChE. На фиг. 41 показано содержание кокаина в головном мозге исердцах, собранных от крыс (n=6), получавших дозу AlbuBChE (3 мг/кг) или физиологический раствор через хвостовую вену, с последующим введением через 10 мин 30 мкКи 3 Н-кокаина (3,5 мг/кг), также через хвостовую вену. Мозг и сердца собирали через 10 мин после дозы 3 Н-кокаина. Слева направо, контрольным данным соответствуют столбцы 1 и 3, а данным по AlbuBChE соответствуют столбцы 2 и 4. На фиг. 42 представлены уровни кокаина (левый график) и бензоата (правый график) в головном мозге, сердце и плазме, собранных от крыс, получавших дозу 3 мг/кг AlbuBChE или физиологический раствор за 10 мин до дозы 30 мкКи 3 Н-кокаина (3,5 мг/кг). Мозг, сердца и плазму собирали через 10 мин после дозы кокаина. На фиг. 43 представлен экспериментальный дизайн исследования по изучению способности AlbuBChE защищать от смертельной передозировки. На фиг. 44 приведено количество в процентах крыс, у которых наблюдали гиперактивность, судороги и смерть в ответ на дозу 100 мг/кг кокаина, введенную через 10 мин после дозы 0, 1, 3 или 10 мг/кгAlbuBChE. На фиг. 45 представлен график зависимости концентрации кокаина от времени у крыс Sprague Dawley, получавших в/в дозу 0, 2 и 10 мг/кг AlbuBChE с дальнейшим введением через 5 мин в/б дозы 60 или 100 мг/кг кокаина. На фиг. 46 представлена поведенческая модель зависимости и рецидива. "S" и "D" обозначают физиологический раствор и наркотик кокаин соответственно. Животных приучают нажимать на рычаг, чтобы получить инфузию кокаина. После стабилизации (поддерживания навыка) кокаин заменяют на физиологический раствор и дожидаются прекращения такого поведения. В следующей фазе восстановления делают примирующую инъекцию кокаина попеременно с физиологическим раствором. На фиг. 47 представлена избирательная блокада примированного кокаином восстановления поведения, направленного на поиск наркотика, возникающая в результате лечения AlbuBChE. Крыс, которые прежде самостоятельно вводили себе кокаин и прекращали это делать, когда кокаин заменяли на физиологический раствор, примировали в/в инъекцией физиологического раствора (S), кокаина (С, 10 мг/кг) или амфетамина (А, 2 мг/кг). AlbuBChE вводили в/в (Е, 2 мг/кг) за 2 ч до поведенческой сессии. На фиг. 48 показано число нажатий на рычаг во время каждой сессии у крыс после инъекции физиологического раствора, инъекции кокаина (10 мг/кг, в/в) или AlbuBChE (2 мг/кг, в/в) с последующим введением кокаина (10 мг/кг, в/в) после фазы зависимости и вынужденного воздержания. На фиг. 49 представлены данные по биодоступности, периоду полувыведения и времени для достижения максимальной концентрации, Tmax, AlbuBChE у яванских макак после однократной внутривенной (в/в), подкожной (п/к) или внутримышечной (в/м) инъекции. Абсолютную биодоступность AlbuBChE при в/м и п/к маршрутах введения рассчитывали относительно уровня дозы 3 мг/кг при в/в введении. Подробное описание изобретения Изобретение относится к способу ослабления биологического эффекта от контакта с кокаином у примата, включающему введение примату некоторого количества слитого белка, содержащего:(а) мутантный полипептид бутирилхолинэстеразы (BChE), содержащий последовательностьb) полипептид человеческого сывороточного альбумина (ЧСА), содержащий последовательностьMRPTWAWWLFLVLLLALWAPARG (SEQ ID NO: 3),при этом количество слитого белка является эффективным для ослабления биологического эффекта от контакта с кокаином у примата. В одном из вариантов осуществления способа слитый белок содержит последовательность В другом варианте осуществления способа слитый белок вводят до контакта с кокаином. В другом варианте осуществления слитый белок вводят вплоть до одного дня до контакта с кокаи-5 024441 ном. В другом варианте осуществления слитый белок вводят вплоть до 216 ч до контакта с кокаином. Слитый белок можно вводить за 1, 2, 3, 4, 5, 6, 7, 8 или 9 дней до контакта с кокаином. В другом варианте осуществления способа слитый белок вводят после контакта с кокаином. В следующем варианте осуществления слитый белок вводят вплоть до 6 ч после контакта с кокаином. В другом варианте осуществления слитый белок вводят вплоть до 1 ч после контакта с кокаином. В другом варианте осуществления способа контакта с кокаином является однократным контактом с кокаином. В другом варианте осуществления способа контакта с кокаином является повторяющимся контактом с кокаином. В другом варианте осуществления способа повторяющийся контакт с кокаином является злоупотреблением кокаином или кокаиновой зависимостью. В другом варианте осуществления способа повторяющийся контакт с кокаином включает по меньшей мере шесть однократных воздействий кокаина за период двенадцать месяцев. В другом варианте осуществления способа повторяющийся контакт с кокаином включает по меньшей мере двадцать однократных воздействий кокаина на протяжении всей жизни примата. В другом варианте осуществления способа биологический эффект вызван передозировкой кокаина у примата и ослабление представляет собой лечение или предотвращение биологического эффекта. В другом варианте осуществления способа биологический эффект представляет собой увеличение артериального давления. В другом варианте осуществления способа продолжительность увеличения артериального давления сокращается на 60-90%. В другом варианте осуществления способа продолжительность увеличения артериального давления сокращается примерно на 78%. В другом варианте осуществления способа биологический эффект представляет собой увеличение частоты сердечных сокращений или температуры тела. В другом варианте осуществления способа степень ослабления этих эффектов составляет 45-70%. В другом варианте осуществления способа степень ослабления этих эффектов составляет 57%. В другом варианте осуществления способа биологический эффект представляет собой поведение примата, направленное на поиск кокаина. В другом варианте осуществления способа поведение, направленное на поиск кокаина, имеет место в период воздержания от кокаина после контакта с кокаином. В другом варианте осуществления способа поведение, направленное на поиск кокаина, следует за рецидивом. В другом варианте осуществления способа введение слитого белка за 2 ч до рецидива ослабляет поведение примата, направленное на поиск кокаина, сразу после рецидива. В другом варианте осуществления способа введение слитого белка за 2 ч до контакта с кокаином приводит к 50-100% ослаблению направленного на поиск кокаина поведения примата. В другом варианте осуществления способа ослабление поведения, направленного на поиск кокаина,наблюдается вплоть до четырех дней после введения слитого белка. В другом варианте осуществления способа введение слитого белка приводит к уменьшению общего контакта с кокаином у примата, по сравнению с ситуацией без введения. В другом варианте осуществления способа ослабление поведения, направленного на поиск кокаина,приводит к периоду воздержания от кокаина у примата. В другом варианте осуществления способа период воздержания составляет от 2 до 3 недель. В другом варианте осуществления способа ослабление поведения, направленного на поиск кокаина,приводит к большему относительному числу дней, в которые примат не подвергается воздействию кокаина, чем в ситуации без введения. В другом варианте осуществления способа ослабление поведения, направленного на поиск кокаина,приводит к большему числу дней подряд, в которые примат не подвергается воздействию кокаина, чем в ситуации без введения. В другом варианте осуществления способа ослабление поведения, направленного на поиск кокаина,приводит к уменьшению степени зависимости от кокаина или злоупотребления кокаином, что оценивают при помощи оценки степени тяжести избирательной зависимости от кокаина (CSSA) или диагностического и статистического руководства по психическим расстройствам IV (Diagnostic and Statistical Manualof Mental Disorders IV) (DSM-IV). В другом варианте осуществления способа эффективное количество слитого белка представляет собой количество, которое снижает уровень кокаина в сыворотке примата до примерно 0 нг/мл в течение примерно 30 мин при внутривенной дозе кокаина 1 мг/кг. В другом варианте осуществления способа введение слитого белка снижает уровень кокаина в сыворотке примата до менее чем 12% от уровня кокаина в сыворотке в ситуации без введения в течение примерно 5 мин при внутривенной дозе кокаина 1 мг/кг. В другом варианте осуществления способа введение слитого белка снижает уровень кокаина в сы-6 024441 воротке примата до 7% от уровня кокаина в сыворотке в ситуации без введения в течение примерно 5 мин при внутривенной дозе кокаина 1 мг/кг. В другом варианте осуществления способа слитый белок вводят только один раз, ежедневно, два раза в неделю, один раз в неделю, один раз в две недели или один раз в месяц. В другом варианте осуществления слитый белок вводят один раз в неделю или два раза в неделю. В другом варианте осуществления слитый белок вводят в виде одной дозы после контакта с кокаином. В другом варианте осуществления слитый белок вводят в виде одной дозы после передозировки кокаина. В другом варианте осуществления способа слитый белок вводят внутримышечной инъекцией или подкожной инъекцией. В другом варианте осуществления способа слитый белок находится в буфере для препарата, содержащем 10 мМ фосфат натрия, 200 мМ маннитол, 60 мМ трегалозу и 0,01% (w/v) полисорбат 80, рН 7,2. В другом варианте осуществления способа слитый белок присутствует в препарате в концентрации по меньшей мере 30 мг/мл. В другом варианте осуществления способа ослабление биологического эффекта наблюдается вплоть до 72 ч после введения слитого белка. В другом варианте осуществления способа примат является человеком. В другом варианте осуществления способа контакт с кокаином является однократным контактом с кокаином в количестве от 10 мг до 60 мг или повторяющимся контактом с кокаином, когда количество кокаина при каждом однократном воздействии из повторяющихся воздействий кокаина составляет от 10 до 60 мг. В другом варианте осуществления способа эффективное количество слитого белка представляет собой количество, которое снижает уровень кокаина в сыворотке человека до примерно 0 нг/мл в течение примерно 30 мин при внутривенном введении дозы кокаина 40 мг. В другом варианте осуществления способа эффективное количество слитого белка составляет от 0,06 до 5 мг/кг. В другом варианте осуществления способа эффективное количество слитого белка составляет 0,06, 0,3, 1,6 или 4,8 мг/кг. В другом варианте осуществления способа эффективное количество слитого белка составляет от 50 до 300 мг. В другом варианте осуществления способа эффективное количество слитого белка составляет 50, 100, 150 или 300 мг. Вариант осуществления слитого белка BChE-альбумин, содержащего аминокислотные заменыA227S, S315G, A356W и Y360G представлен на фиг. 1 (SEQ ID NO: 4). Аминокислотная последовательность, представленная на фиг. 1, содержит гетерологичный сигнальный пептид, выделенный подчеркиванием, домен BChE, содержащий аминокислоты E29-V529 BChE человека, и человеческий сывороточный альбумин (ЧСА), выделенный курсивом. Аминокислотные замены A227S, S315G, A356W и Y360G на фиг. 1 выделены жирным шрифтом и подчеркнуты. Замены пронумерованы относительно полноразмерной BChE. Белок, кодируемый аминокислотной последовательностью на фиг. 1, называется "AlbuBChE" на протяжении всего данного изобретения. Понятно, что все комбинации описанных выше вариантов осуществления изобретения находятся в пределах объема изобретения. Используемый в данном документе термин "примат" относится к любому представителю отряда млекопитающих, которые характеризуются, в частности, хорошо развитым бинокулярным зрением, приспособленностью конечностей для захвата и увеличением больших полушарий головного мозга, и куда относятся люди, человекообразные обезьяны, обезьяны и родственные виды. Используемый в данном документе термин "степень ослабления" означает снижение биологического эффекта от контакта с кокаином, которое наблюдается после введения слитого белка BChE-альбумин,по сравнению с биологическим эффектом от контакта с кокаином, наблюдаемым в отсутствие слитого белка BChE-альбумин. Степень ослабления рассчитывают по следующей формуле: Например, если контакт с кокаином повышает исходную температуру с 38 до 38,7 С в отсутствие слитого белка BChE-альбумин и контакт с кокаином повышает исходную температуру с 38 до 38,3 С в присутствии слитого белка BChE-альбумин, то степень ослабления составляет 57,1% 0,7 С-0,3 С)/0,7 С). Используемый в данном документе термин "однократный контакт с кокаином" означает один контакт с кокаином, выделенный из любых других случаев контакта с кокаином. "Повторяющийся контакт с кокаином" означает более чем один однократный контакт с кокаином. Повторяющийся контакт с кокаином может представлять собой регулярную или нерегулярную схему однократных контактов с кокаином,начиная со второго или последующих однократных контактов с кокаином у субъекта. Индивидуум, периодически подвергающийся воздействию кокаина, может соответствовать крите-7 024441 риям для кокаиновой зависимости или злоупотребления кокаином согласно диагностическому и статистическому руководству по психическим расстройствам IV (DSM-IV). Используемый в данном документе термин "общий контакт с кокаином" означает суммарные контакты с кокаином в течение определенного временного интервала. Общий контакт с кокаином можно измерять во время или после периода лечения, призванного ослаблять поведение, направленное на поиск наркотика, или другие биологические эффекты от контакта с кокаином. Используемый в данном документе термин "период воздержания от кокаина" означает период времени после контакта с кокаином, когда примат не подвергается воздействию кокаина вновь. Используемый в данном документе термин "рецидив" означает контакт с кокаином после периода воздержания от кокаина. Понятно, что при указании диапазона параметра, все десятичные значения целых чисел в пределах данного диапазона охвачены рамками изобретения. Например, "от 0,2 до 15 мг/кг" включает 0,2, 0,3, 0,4,0,5 мг/кг и т.д., вплоть до 15,0 мг/кг включительно. Доза для животных может быть переведена в эквивалентную дозу для человека (HED) с помощью таблицы пересчета, приведенной в публикации "Guidance for Industry: Estimating the Maximum Safe Starting Dose in Initial Clinical Trials for Therapeutics in Adult Healthy Volunteers", Департамент здравоохранения и социальных служб США, Центр оценки и исследования лекарств (CDER) Управления по контролю качества продовольствия и медикаментов США, июль 2005 г. Дозы для яванских макак в мг/кг можно переводить в HED в мг/кг путем деления дозы для яванских макак на 3,1. Дозы для беличьих обезьян в мг/кг можно переводить в HED в мг/кг путем деления дозы для беличьих обезьян на 5,3. Список сокращенийAUC(0-t) - площадь под кривой зависимости концентрации в плазме от времени с момента времени ноль вплоть до последнего момента с поддающейся обнаружению концентрацией (tz);AUC(0-) - площадь под кривой зависимости концентрации в плазме от времени с момента времени ноль до бесконечности;% AUCex - часть AUC в процентах, полученная в результате экстраполяции от tz до бесконечности;BQL - ниже предела количественного определения;LLOQ - нижний предел количественного определения; мин - минута(ы);NCA - анализ без учета компартментов;% RSD - относительное стандартное отклонение в процентах;VZ - объем распределения в терминальной фазе. Слитый белок BChE-альбумин, приведенный на фиг. 1 (AlbuBChE), использовали в испытаниях,как описано ниже в примерах. Пример 1. Фармакокинетические и фармакодинамические исследования на яванских макаках после однократного внутримышечного введения AlbuBChE и нескольких внутривенных доз кокаина. Цели. Целью данного исследования было определение фармакокинетической (ФК) кривой для AlbuBChE у самцов яванских макак после однократного внутримышечного введения AlbuBChE при уровнях доз 0,2, 1 или 5 мг/кг и определение активности AlbuBChE в зависимости от времени путем внутривенного введения дозы 1 мг/кг кокаина через 2, 48, 96, 120 и 240 ч после введения дозы AlbuBChE.AlbuBChE представляет собой слитый белок из человеческого сывороточного альбумина (ЧСА) и генетически модифицированной формы человеческой бутирилхолинэстеразы (BChE), который проявляет высокую каталитическую эффективность гидролиза кокаина до бензойной кислоты. AlbuBChE находится в стадии разработки в качестве потенциального средства для предотвращения рецидива поведения,направленного на поиск наркотика. Показано, что слияние белка с альбумином улучшает фармакокинетические свойства белка путем уменьшения клиренса и увеличения периода полувыведения. Следствием более продолжительного периода полувыведения, как ожидается, станет более длинный промежуток между введением доз и более строгое соблюдение пациентом режима лечения. Обоснование выбора вида животных. Яванские макаки (macaca mulatta) были выбраны для данного исследования на основании их анатомического, физиологического и биохимического сходства с людьми, что может облегчить экстраполяцию наблюдаемых фармакокинетических и фармакодинамических свойств на людей. Известно, что у обезьян экспрессируется бутирилхолинэстераза, которая является компонентом данного лекарственного средства. Обезьяны также физиологически реагируют на кокаин. Обоснование выбора уровня доз и способа введения. В предыдущем исследовании была оценена фармакокинетическая кривая для AlbuBChE у яванских макак. В том исследовании тестируемое вещество вводили п/к (7,8, 2,4 и 0,78 мг/кг), в/м (2,4 мг/кг) и в/в(2,4 мг/кг). Фармакокинетические свойства AlbuBChE имели линейный характер при всех вводимых п/к тестируемых дозах. Выбор в/м введения для данного исследования был основан на большей биодоступности при в/м по сравнению с п/к введением (79% и 35-39% соответственно), наблюдаемой в предыдущем исследовании. Кроме того, были выбраны для в/м введения уровни доз AlbuBChE 0,2, 1 и 5 мг/кг,чтобы определить фармакодинамический диапазон для AlbuBChE у яванских макак. Дозу кокаина 1 мг/кг для в/в введения выбрали в качестве дозы, достаточно высокой для получения соответствующего физиологического эффекта и достижения поддающейся измерению концентрации кокаина в крови, и в то же время не слишком стимулирующей животных. Число животных в каждой группе представляет собой минимальное количество животных в группе,необходимое для оценки межиндивидуальной вариабельности у животных. Поскольку данное исследование являлось пилотным, были исследованы животные только одного пола (самцы). Тестируемые растворы. Тестируемое вещество, AlbuBChE, хранили в маточном растворе в виде замороженного жидкого препарата, содержащего 29,9 мг/мл при -7015 С. Перед введением доз препарат тестируемого вещества оставляли оттаивать до комнатной температуры. Когда препарат тестируемого вещества полностью оттаивал, содержимое контейнера перемешивали осторожным переворачиванием и разбавляли соответствующим объемом разбавителя для тестируемого вещества до достижения концентрации 20 мг/мл. Этот препарат серийно разводили разбавителем для тестируемого вещества для достижения концентраций 4 и 0,8 мг/мл. Кокаина гидрохлорид, тестируемое вещество для фармакодинамики, приобретали у Sigma. Уровни доз выражали в виде гидрохлоридной соли. Дизайн эксперимента. В исследовании принимали участие в общей сложности 11 ранее не используемых в экспериментах взрослых самцов яванских макак, которые были разделены на четыре дозовые группы: контрольная группа из двух яванских макак, которые получали только одну в/в дозу кокаина; три дозовые группы, получавшие одну в/м дозу AlbuBChE, составляющую 0,2, 1 или 5 мг/кг. Каждая дозовая группа включала трех ранее не используемых в экспериментах взрослых самцов яванских макак. После введения AlbuBChE дозу кокаина 1 мг/кг вводили в/в через 2, 48, 96, 120 и 240 ч после введения дозы AlbuBChE. Сводные данные о назначении доз и уровнях доз представлены в табл. 1. Индивидуальные дозы рассчитывали, исходя из массы тела, зарегистрированной в день введения доз. Животные не голодали до введения доз. Все временные точки находились в пределах 5 мин от указанных временных точек. Сбор образцов для определения AlbuBChE. Одно внутримышечное (в/м) введение AlbuBChE проводили в день исследования 1, и кровь собирали во временные точки, указанные в табл. 2. Примерно 0,5 мл цельной крови забирали из бедренной вены в пробирки для отделения сыворотки (SST). Таблица 2 Сбор образцов для определения кокаина. Примерно 0,5 мл цельной крови забирали из бедренной вены через 5, 10, 15, 20, 30, 40 и 60 мин после каждой дозы кокаина (день исследования 1 в контрольной группе и день исследования 1 (2 ч), 3 (48 ч), 5 (96 ч), 6 (120 ч) и 11 (240 ч) после введения дозы AlbuBChE). Кровь помещали в пробирки для сбора крови с К 2 ЭДТА с добавленным ингибитором эстеразы диизопропилфторфосфатом (ДФФ). Пробирки после сбора крови несколько раз переворачивали и помещали на мокрый лед. Образцы центрифугировали при 2-8 С в пределах 45 мин от момента сбора. Полученную плазму извлекали и по одной 200-мкл аликвоте плазмы помещали в полипропиленовые пробирки. Образцы плазмы замораживали на сухом льду и хранили при -7515 С. Методы анализа. Следующая схема описывает анализ методом ELISA, используемый для измерения концентрацийAlbuBChE в образцах сыворотки обезьян, полученных перед введением и в различные временные точки после введения. Лунки планшетов Immulon 4 НВХ покрывали 100 мкл анти-BChE мАТ 002-01 (Abeam abl7246) в концентрации 1 мкг/мл в PBS в течение ночи при 4 С. Блокирование проводили 2% казеином в 1PBS,200 мкл/лунку, в течение 2 ч при комнатной температуре. После промывания в лунки планшетов добавляли по 100 мкл разведенных образцов сыворотки наряду со стандартами. Стандарты получали путем 3,64-кратного серийного разведения AlbuBChE от 2000 до 3,1 нг/мл. В образцах сыворотки и стандартах поддерживали 10% концентрацию сыворотки путем разведения буфером, содержащим объединенную сыворотку яванских макак. Этап промывания предшествовал детекции с помощью 100 мкл анти-ЧСА мАТ-6502-HRP в концентрации 0,04 мкг/мл в течение 1 ч. Лунки вновь промывали перед развитием окраски при добавлении 100 мкл субстрата ТМВ. Через 15 мин реакцию останавливали добавлением 100 мкл/лунку 1 н. H2SO4 и показания считывали на планшетном ридере SpectraMax при 450/570 нм. Значения для неизвестных образцов сыворотки вычисляли путем интерполяции стандартной кривой, полученной при помощи 4-параметрической подгонки стандартов AlbuBChE. Предел количественного определения в сыворотке яванских макак составлял 21,1 нг/мл. Количественное определение кокаина в сыворотке методом ЖХ/МС. Следующая схема описывает анализ методом ЖХ/МС, используемый для измерения количества кокаина в образцах плазмы. Перед МС-анализом образцы плазмы, калибровочные стандарты и контроли экстрагировали методом жидкостной экстракции в нанесенном слое (SLE-ISOLUTE, Biotage). В 25 мкл образцов добавляли 150 мкл 5% гидроксида аммония и 25 мкл раствора внутреннего стандарта (кокаинd3). После смешивания и переноса на пластину для SLE образцы элюировали метиленхлоридом и выпаривали досуха. После ресуспендирования в 50 мкл восстанавливающего раствора - 5% ACN в 10 мМ ацетате аммония в воде, 10 мкл наносили инжектором на колонку Thermo Hypercarb при скорости 0,5 мл/мин. Подвижная фаза была двухфазной. Масс-спектрофотометрическую детекцию проводили при помощи Api 4000, APCI положительного интерфейса и мониторинга множественных реакций (MRM). С помощью этого метода определяли концентрации в плазме кокаина, бензоилэкгонина и метилового сложного эфира экгонина. ФК анализ AlbuBChE. Значения фармакокинетических параметров AlbuBChE определяли при помощи кривых зависимости концентрации в сыворотке от времени для отдельных животных. Использовали компьютерную программу WinNonlin Professional (версия 4.0.1 Pharsight Corporation, США). Конкретно использовали модель для анализа без учета компартментов с внесосудистым входом. Если в терминальной фазе сывороточной концентрационной кривой было менее чем 3 точки данных, период полувыведения в терминальной фазе и ФК параметры, полученные из периода полувыведения, не были рассчитаны для данной кривой. Анализируемые параметры включали рассчитанные tmax, Cmax, t1/2, AUC(0-t) и AUC(0-). ФК анализ кокаина. Если данные позволяли, значения фармакокинетических параметров для кокаина и его метаболитов определяли при помощи кривых зависимости концентрации в плазме от времени для отдельных животных во все дни исследования, когда вводили кокаин. Использовали компьютерную программу WinNonlinProfessional (версия 4.0.1 Pharsight Corporation, США). Конкретно использовали модель для анализа без учета компартментов с в/в болюсным входом для кокаина и внесосудистым входом для метаболитов. Если в терминальной фазе плазменной концентрационной кривой было менее чем 3 точки данных, период полувыведения в терминальной фазе и ФК параметры, полученные из периода полувыведения, не были рассчитаны для данной кривой. ФК/ФД анализ. Отношение ФК/ФД для AlbuBChE определяли при помощи компьютерной программы WinNonlinProfessional (версия 4.0.1 Pharsight Corporation, США). Конкретно использовали модель прямого сигмоидального ингибиторного эффекта Emax, в которой максимальный эффект (Emax), измеряемый при помощиAUC для кокаина, предполагался при концентрации AlbuBChE, равной нулю. Модельное уравнение можно записать следующим образом: Сигмоидальный ингибиторный эффект Emax, С=0 при Emax, С=бесконечность при Е 0 Сигмоидальная модель была выбрана в связи с более высокой активностью, наблюдаемой во временной точке 48 ч, по сравнению с временной точкой 2 ч. ФД параметр, используемый в анализе, представлял собой AUC для кокаина. ФК параметрами, используемыми в модели, являлись концентрации в плазме AlbuBChE через 2, 48, 96, 120 и 240 ч после дозы AlbuBChE. В связи с тем, что концентрацию AlbuBChE не измеряли через 2 ч после дозыAlbuBChE, в анализе использовали концентрацию через 3 ч после дозы, предполагая, что концентрацияAlbuBChE через 3 ч после дозы AlbuBChE может отражать концентрацию AlbuBChE через 2 ч после дозы AlbuBChE. Статистические методы. Общие статистические расчеты концентрационных кривых и значений ПК параметров по экспериментальной группе проводили при помощи функции описательной статистики в WinNonlin. Представленными статистическими параметрами являются N, среднее, SD и коэффициент вариаций в процентах(% CV). Результаты. Концентрационная кривая для AlbuBChE. Данные о зависимости концентрации AlbuBChE от времени и сводные статистические данные приведены в табл. 3 и 4. Кривые зависимости концентрации в сыворотке AlbuBChE от времени для отдельных животных после однократной в/м инъекции AlbuBChE в дозах 0,2, 1 или 5 мг/кг приведены на фиг. 2. Кривые зависимости средней концентрации в сыворотке от времени для трех дозовых групп AlbuBChE приведены на фиг. 3. После в/м инъекции у всех животных были поддающиеся измерению концентрации AlbuBChE. Межиндивидуальная вариабельность у животных в дозовой группе была в пределах разумного, на что указывают значения % CV, находящиеся в диапазоне от 8,2 до 78,4 для всех временных точек. Концентрация в сыворотке AlbuBChE возрастала с увеличением дозы. Таблица 3 Кривые зависимости индивидуальных и средних концентраций в сыворотке AlbuBChE (нг/мл) от времени (часы) у яванских макак после однократного в/м введения AlbuBChE в дозе 0,2, 1 или 5 мг/кг/животное Таблица 4 Сводные данные зависимости средней концентрации в сыворотке AlbuBChE (нг/мл) от времени (часы) у яванских макак после однократного в/м введения AlbuBChE в дозе 0,2, 1 или 5 мг/кг/животноеLLOQ 27,2 нг/мл. Концентрационные кривые для кокаина, бензоилэкгонина и метилового сложного эфира экгонина ЖХ/МС анализ проводили для всех образцов, чтобы проанализировать уровни кокаина, бензоилэкгонина и метилового сложного эфира экгонина в плазме обезьян. Кривые зависимости средней концентрации в плазме от времени у контрольных животных и после введения 0,2, 1 или 5 мг/кг представлены в табл. 5, 6 и 7 и на фиг. 4, 5 и 6 для кокаина, бензоилэкгонина и метилового сложного эфира экгонина соответственно. В целом концентрации в плазме кокаина уменьшались в зависимости от дозы AlbuBChE и возрастали с течением времени после введения AlbuBChE. Концентрации кокаина через 240 ч после введенияAlbuBChE находились в том же диапазоне, что и в день 1 в контрольной группе с кокаином (фиг. 7). Из этого следует, что AlbuBChE был неактивен через 240 ч после введения AlbuBChE в дозах 0,2, 1 или 5 мг/кг. Это также указывает на то, что кинетика кокаина не проявляет зависимость от времени у яванских макак, что позволяет сравнивать контроль с однократной в/в дозой кокаина в день 1 с кривой при нескольких дозах кокаина после введения AlbuBChE. Как и следовало ожидать, исходя из метаболического пути кокаина (фиг. 9), концентрации в плазме бензоилэкгонина снижались в зависимости от дозы AlbuBChE и возрастали с течением времени после введения AlbuBChE. Теоретически, концентрация в плазме метилового сложного эфира экгонина должна возрастать после введения AlbuBChE (фиг. 9). Это возрастание было очевидным только при введении дозы кокаина через 2 ч после введения AlbuBChE при всех трех уровнях доз AlbuBChE. Концентрацию в плазме метилового сложного эфира экгонина было нелегко отличить от контроля после введения кокаина через 48,96, 120 или 240 ч после введения AlbuBChE. Таблица 5 Зависимость средней концентрации кокаина в плазме (нг/мл) от времени (мин) у яванских макак после в/в дозы кокаина 1 мг/кг у контрольных животных (n=2) или через 2, 48, 72, 96, 120 и 240 ч после в/м дозы 0,2, 1 или 5 мг/кг AlbuBChE (n=3 на дозовую группу) Контроль и доза 0,2 мг/кг AlbuBChE Таблица 6 Зависимость средней концентрации в плазме бензоилэкгонина (нг/мл) от времени (мин) у яванских макак после в/в дозы кокаина 1 мг/кг у контрольных животных (n=2) или через 2, 48, 72, 96, 120 и 240 ч после в/м дозы 0,2, 1 или 5 мг/кг AlbuBChE (n=3 на дозовую группу) Контроль и доза 0,2 мг/кг AlbuBChE Таблица 7 Зависимость концентрации в плазме метилового сложного эфира экгонина (нг/мл) от времени (мин) у яванских макак после в/в дозы кокаина 1 мг/кг у контрольных животных (n=2) или через 2, 48, 72, 96, 120 и 240 ч после в/м дозы 0,2, 1 или 5 мг/кг AlbuBChE (n=3 на дозовую группу) Контроль и доза 0,2 мг/кг AlbuBChE Фармакокинетический анализ AlbuBChE. Значения фармакокинетических параметров AlbuBChE после однократной в/м дозы 0,2, 1 или 5 мг/кг AlbuBChE у отдельных животных и описательная статистика для каждой группы приведены в табл. 8. Средние значения ФК параметров для AlbuBChE после в/м введения доз 0,2, 1 или 5 мг/кг приведены в табл. 9. Как правило, абсорбция из зоны в/м введения была быстрой и поддающиеся измерению концентрации были обнаружены в первом собранном образце (1 час после введения дозы). Максимальную концентрацию наблюдали через 3 ч для уровней доз 0,2 и 1 мг/кг. Значения Tmax были немного больше (6 ч) для дозы 5 мг/кг. Воздействие AlbuBChE возрастало с увеличением дозы. Нормированные на дозу значения Cmax иAUC возрастали в зависимости от дозы, что свидетельствует о более чем пропорциональном увеличении воздействия в зависимости от дозы. Это также сопровождалось увеличением t1/2 в терминальной фазе элиминации в зависимости от дозы, особенно между уровнями доз 1 и 5 мг/кг, когда значение t1/2 почти удваивалось. Таблица 8 Индивидуальные и средние значения фармакокинетических параметров AlbuBChE у яванских макак после однократного в/м введения AlbuBChE в дозе 0,2, 1 или 5 мг/кг/животное Доза 0,2 мг/кг AlbuBChE Таблица 9 Средние значения фармакокинетических параметров для AlbuBChE у яванских макак после однократной в/м инъекции в дозах 0,2, 1 или 5 мг/кг Фармакокинетический анализ кокаина и метаболитов. Сводная таблица средних значений фармакокинетических параметров кокаина на дозовую группу приведена в табл. 10. Фармакокинетическая кривая для кокаина была подробно охарактеризована для всех дозовых групп и временных точек за одним исключением: кривая зависимости концентрации в плазме от времени для дозы кокаина, введенной через 2 ч после дозы AlbuBChE, была очень вариабельной для всех дозовых групп. По этой причине t1/2 в терминальной фазе элиминации не удалось точно охарактеризовать для большинства животных в этом случае дозировки кокаина.AUC(0-t) для кокаина уменьшалась в зависимости от дозы AlbuBChE и возрастала с течением времени после введения AlbuBChE. Аналогично, системный плазменный клиренс кокаина возрастал в зависимости от дозы AlbuBChE и возвращался к контрольным значениям с течением времени после дозы AlbuBChE. Через 240 ч после введения AlbuBChE AUC и клиренс кокаина находились в том же диапазоне, что и в день 1 в контрольной группе с кокаином. Для всех трех уровней доз AlbuBChE максимальный эффект AlbuBChE на клиренс или AUC кокаина наблюдали через 48 ч после введения доз. Продолжительность эффекта была связана с уровнями дозAlbuBChE. После дозы 5 мг/кг эффект AlbuBChE на AUC и клиренс кокаина был очевидным вплоть до 120 ч после введения дозы. При дозе 1 мг/кг эффект AlbuBChE на AUC или клиренс кокаина все еще можно было наблюдать через 96-120 ч после дозы AlbuBChE относительно контроля или значений через 240 ч. При снижении дозы AlbuBChE до 0,2 мг/кг так же уменьшалась продолжительность эффекта, при этом точка 48 ч была последней временной точкой с повышенным клиренсом кокаина. Исходя из этих данных, подходящим режимом дозирования AlbuBChE является один или два раза в неделю. Как можно видеть на фиг. 5, кривая зависимости концентрации от времени для бензоилэкгонина не включала терминальную фазу элиминации. Вследствие этого, фармакокинетическая характеристика бензоилэкгонина была ограничена характеристикой AUC(0-t). Сводная таблица средних значений AUC в зависимости от дозы AlbuBChE и времени после дозы AlbuBChE в сравнении с контрольной группой с кокаином представлена в табл. 11. В соответствии с метаболическим путем кокаина (фиг. 9), AUC бензоилэкгонина уменьшалась в зависимости от дозы AlbuBChE и возрастала с течением времени после введения AlbuBChE, как показано на фиг. 11. Как можно видеть на фиг. 6, кривая зависимости концентрации от времени для метилового сложного эфира экгонина была плоской и не включала терминальную фазу элиминации. Вследствие этого, фармакокинетической характеризации метилового сложного эфира экгонина не проводили. Теоретически,AUC для метилового сложного эфира экгонина должна возрастать после введения AlbuBChE (фиг. 9). Это возрастание было очевидным только при дозе кокаина, введенной через 2 ч после введения AlbuBChE в случае всех трех уровней доз AlbuBChE. Эффект AlbuBChE на метиловый сложный эфир экгонина было нелегко отличить от контроля после введения кокаина через 48, 96, 120 или 240 ч после введенияAlbuBChE. Таблица 10 Средние значения фармакокинетических параметров кокаина у яванских макак после в/в дозы 1 мг/кг кокаина у контрольных животных (n=2) или через 2, 48, 72, 96, 120 и 240 ч после в/м дозы 0,2, 1 или 5 мг/кг AlbuBChE (n=3 на дозовую группу) н/п - не применимо или не определено, поскольку данные не позволяли. Таблица 11 Сводная таблица средних значений AUC(0-t) для бензоилэкгонина (миннг/мл) у контрольных животных и в зависимости от времени после дозы AlbuBChE ФК/ФД анализ. Исходя из механизма действия AlbuBChE, предполагалось, что с помощью модели прямого ингибиторного эффекта Emax удастся охарактеризовать отношение ФК/ФД для AlbuBChE и кокаина. Данные ФК и ФД, использованные в анализе, приведены в табл. 12. Кривая, построенная на основании модели прямого сигмоидального ингибиторного эффекта Emax, приведена на фиг. 8. Эти данные четко показывают обратную зависимость между сывороточной концентрацией AlbuBChE и контактом с кокаином. Сывороточная концентрация AlbuBChE, которая может приводить к 50% снижению концентрации кокаина (EC50), по оценке с помощью модели составляет 600 нг/мл. Значения Таблица 12 ФК/ФД анализ AlbuBChE у яванских макак после однократного в/м введения дозы 0,2, 1 или 5 мг/кгAlbuBChE. Кокаин вводили в/в в дозе 1 мг/кг контрольным животным или через 2, 48, 96, 120 и 240 ч после дозы AlbuBChE ФК параметры: концентрации в плазме AlbuBChE у животных через 3, 48, 96, 120 и 240 ч после дозы AlbuBChE ФД параметр: AUC(0-t) для кокаина на каждое животное через 2, 48, 96, 120 и 240 ч после дозы AlbuBChE Концентрацию AlbuBChE не измеряли через 2 ч после дозы AlbuBChE, в анализе использовали концентрацию через 3 ч после дозы AlbuBChE. Осмотр животных. Животных осматривали на протяжении всего исследования. На всем протяжении исследования не было зарегистрировано гибели животных, и не было отмечено никаких клинических или внешних признаков, связанных с введением AlbuBChE в любой дозе. Введение кокаина в дозе 1 мг/кг без предварительного введения тестируемого вещества приводило к гиперактивности и возрастанию частоты дыхания с брюшным дыханием. Связанные с кокаином признаки не наблюдались в течение пяти дней после предварительного введения тестируемого вещества при дозах AlbuBChE в диапазоне от 0,2 до 5 мг/кг, но возвращались в дни исследования 6 и 11. Выводы.AlbuBChE хорошо переносился яванскими макаками после однократной в/м дозы 0,2, 1 или 5 мг/кг. Абсорбция AlbuBChE из зоны в/м введения была быстрой. Tmax составляло 3 ч для доз 0,2 и 1 мг/кг и 6 ч для дозы 5 мг/кг. Воздействие AlbuBChE возрастало более чем пропорциональным образом в зависимости от дозы. Значение t1/2 в терминальной фазе элиминации возрастало от 31 до 62 ч в промежутке между уровнями доз 1 и 5 мг/кг. Кокаин вводили контрольным животным в день 1 и через 2, 48, 96, 120 и 240 ч после дозы AlbuBChE. После каждого введения кокаина забирали несколько образцов с целью определения фармакокинетической кривой в ответ на снижение сывороточных уровней AlbuBChE. AUC(0-t) для кокаина уменьшалась в зависимости от дозы AlbuBChE и возрастала с течением времени после введения AlbuBChE. Продолжительность эффекта была связана с уровнями доз AlbuBChE. Эффект AlbuBChE на AUC и клиренс кокаина был очевиден вплоть до 120 ч для дозы 5 мг/кг, 96-120 ч для дозы 1 мг/кг и 48 ч для дозы 0,2 мг/кг. Исходя из этих данных, подходящим режимом дозирования AlbuBChE является один или два раза в неделю. Отношение ФК/ФД у яванских макак указывает на обратную зависимость между сывороточной концентрацией AlbuBChE и контактом с кокаином. Сывороточная концентрация AlbuBChE, которая мо- 18024441 жет приводить к 50% снижению концентрации кокаина (ЕС 50), по оценке с помощью модели прямого сигмоидального ингибиторного эффекта Emax составляет 600 нг/мл. Пример 2. Фармакокинетические и фармакодинамические (ФК/ФД) исследования AlbuBChE на беличьих обезьянах. Цель. Оценить фармакокинетику и фармакодинамику AlbuBChE после однократной внутримышечной инъекции 5 мг/кг AlbuBChE беличьим обезьянам. Фармакодинамический эффект AlbuBChE определяли после в/в введение кокаина в дозе 1 мг/кг контрольным животным или через 2, 72 и 96 ч после дозы AlbuBChE. Дизайн исследования. Уровень дозы. Уровень дозы AlbuBChE, равный 5 мг/кг, был выбран, исходя из предыдущих исследований на яванских макаках, у которых, как установлено, этот уровень дозы эффективен для уменьшения контакта с кокаином. В/в доза кокаина 1 мг/кг основана на литературных данных, свидетельствующих о том, что такой дозы достаточно для вызывания эффекта у обезьян без стимулирования избыточной гиперактивности. В/м способ введения для AlbuBChE был выбран, поскольку это предполагаемый способ введения людям. Таблица 13 Тест-система и чистые материалы Образцы для фармакокинетики AlbuBChE. Образцы крови (0,4 мл) собирали из бедренной вены и помещали в пробирки для отделения сыворотки (SST) перед введением дозы, через 24, 72, 96 и 336 ч после введения дозы (образцы, собранные через 336 ч (14 дней) после введения дозы, предназначались для оценки иммуногенности). Образцы также анализировали на концентрацию AlbuBChE. Пробирки выдерживали при комнатной температуре в течение по меньшей мере 1 ч, но не более 4 ч, до центрифугирования. Образцы центрифугировали, и по меньшей мере 200 мкл сыворотки собирали и хранили на сухом льду до последующего хранения при примерно -70 С. Образцы для фармакокинетики кокаина. Примерно 0,4 мл цельной крови забирали из бедренной вены после каждой дозы кокаина через 5 и 30 мин после введения дозы. Кровь помещали в пробирки для сбора крови с К 2 ЭДТА с добавленным ингибитором эстеразы диизопропилфторфосфатом (ДФФ). Пробирки после сбора крови несколько раз переворачивали и помещали на мокрый лед. Образцы центрифугировали при 2-8 С в пределах 45 мин от момента сбора. Полученную плазму извлекали, и по одной 200-мкл аликвоте плазмы помещали в полипропиленовые пробирки. Образцы плазмы замораживали на сухом льду и хранили при примерно -70 С. Анализ образцов AlbuBChE. В следующем параграфе кратко описан анализ методом ELISA, используемый для измерения концентраций AlbuBChE в образцах сыворотки. Лунки планшетов Immulon 4 НВХ покрывали 100 мкл мАТ 002-01 против BChE человека (Abeamabl7246) в концентрации 1 мкг/мл в PBS в течение ночи при 4 С. Блокирование проводили 2% казеином в фосфатно-солевом буферном растворе (PBS), 200 мкл/лунку, в течение 2 ч при комнатной температуре. После промывания в планшеты добавляли по 100 мкл разведенных образцов сыворотки наряду со стандартами. Стандарты получали путем 2,6-кратного серийного разведения AlbuBChE от 420 до 5,2 нг/мл. В образцах сыворотки и стандартах поддерживали 10% концентрацию сыворотки путем разведения буфером, содержащим объединенную сыворотку яванских макак. Этап промывания предшествовал детекции с помощью 100 мкл анти-ЧСА мАТ-6502-HRP в концентрации 0,04 мкг/мл в течение 1 ч. Лунки вновь промывали перед развитием окраски при добавлении 100 мкл субстрата тетраметилбензидина. Через 15 мин реакцию останавливали добавлением 100 мкл/лунку 1 н. H2SO4 и показания считывали на планшетном ридере SpectraMax при 450/570 нм. Значения для неизвестных образцов сыворотки вычисляли путем интерполяции стандартной кривой, полученной при помощи 5-параметрической подгонки стандартовAlbuBChE. Образцы сыворотки, собранные перед введением дозы и в день 14 после введения дозы также анализировали на иммуногенность. Фармакокинетический и ФК/ФД анализ AlbuBChE. Значения фармакокинетических параметров AlbuBChE определяли при помощи кривых зависимости концентрации в сыворотке от времени для отдельных животных. Использовали компьютерную программу WinNonlin Professional (версия 4.0.1 Pharsight Corporation, США). Конкретно использовали модель для анализа без учета компартментов с внесосудистым входом. Несмотря на ограниченное количество данных, была сделана попытка охарактеризовать отношение ФК/ФД. Использовали компьютерную программу WinNonlin Professional (версия 4.0.1 Pharsight Corporation, США). Конкретно использовали модель прямого ингибиторного эффекта Emax, в которой Emax предположительно был при концентрации AlbuBChE, равной нулю. Модельное уравнение можно записать следующим образом:E=Emax(1-(С/(С+ЕС 50 ФД параметр, используемый в анализе, представлял собой концентрацию в плазме кокаина через 5 мин после дозы кокаина. ФК параметрами, используемыми в модели, являлись концентрации в плазмеAlbuBChE через 2, 72 и 96 ч после дозы AlbuBChE. В связи с тем, что концентрацию AlbuBChE не измеряли через 2 ч после дозы AlbuBChE, в анализе использовали образец, собранный в 1-ю временную точку(через 24 ч после дозы AlbuBChE), предположив, что концентрация AlbuBChE через 24 ч после дозы AlbuBChE может отражать концентрацию AlbuBChE через 2 ч после дозы AlbuBChE. Из-за ограниченности данных и допущений, использованных в данном анализе, значения параметров из данного ФК/ФД анализа нужно рассматривать как приблизительные оценки. Результаты.AlbuBChE. В табл. 15 и на фиг. 12 представлены кривые зависимости сывороточной концентрации AlbuBChE от времени у трех самцов беличьих обезьян после однократного внутримышечного введения дозы 5 мг/кгAlbuBChE. В табл. 16 приведены значения фармакокинетических параметров для AlbuBChE у беличьих обезьян. Наклон кривой для AlbuBChE в терминальной фазе элиминации был хорошо охарактеризован, о чем свидетельствовали значения Rsq выше, чем 0,9. Площадь под кривой также была хорошо охарактеризована, о чем свидетельствовало экстраполированное значение % AUC менее чем 20%. Начальная фаза абсорбции на кривой зависимости концентрации AlbuBChE от времени не была охарактеризована, поскольку первый образец был собран через 24 ч после введения дозы. По этой причине приведенные Tmax и Cmax являются предполагаемыми, поскольку действительные значения, как ожидается, имеют место между 3 и 6 ч. Воздействие AlbuBChE было единообразным у трех животных, разница в уровнях была очевидна только через 2 недели. Например, значения AUC для трех животных находились в узком диапазоне с % CV, составляющим 7%. По оценке, значение t1/2 для AlbuBChE в терминальной фазе элиминации находилось в диапазоне от 45,5 до 65,5 ч (средний период полувыведения 56,6 ч). Таблица 15 Кривая зависимости концентрации в сыворотке AlbuBChE (нг/мл) от времени (часы) у отдельных беличьих обезьян после однократного в/м введения AlbuBChE в дозе 5 мг/кг/животное Таблица 16 Значения фармакокинетических параметров AlbuBChE у отдельных беличьих обезьян после однократного в/м введения AlbuBChE в дозе 5 мг/кг/животноеAlbuBChE (n=3). Биоаналитическим методом измеряли концентрации в плазме кокаина и двух его метаболитов: метилового сложного эфира экгонина и бензоилэкгонина. Метаболический путь кокаина приведен на фиг. 9, метаболит метиловый сложный эфир экгонина образуется непосредственно из кокаина при помощи фермента бутирилхолинэстеразы. В силу этого, можно предположить, что количество данного метаболита будет возрастать после введения AlbuBChE. Данные о зависимости индивидуальных и средних концентраций в плазме кокаина (нг/мл) от времени (часы) у контрольных и получавших AlbuBChE беличьих обезьян приведены в табл. 17. Сводные данные о зависимости средних концентраций кокаина от времени приведены на фиг. 13. Наивысшие концентрации кокаина наблюдали у контрольных животных. Наименьшие уровни кокаина наблюдали через 2 ч после введения AlbuBChE, которые достигали значений, составляющих примерно 7% от контроля. Концентрации кокаина возрастали с течением времени после введения AlbuBChE, но даже через 96 ч после введения AlbuBChE концентрации кокаина все еще составляли 60% от уровня у контрольных животных. Данные о зависимости индивидуальных и средних концентраций в плазме метилового сложного эфира экгонина (нг/мл) от времени (часы) у контрольных и получавших AlbuBChE беличьих обезьян приведены в табл. 18. Сводные данные о средних концентрациях метилового сложного эфира экгонина приведены на фиг. 14. Как и ожидалось, концентрация метилового сложного эфира экгонина через 5 мин после введения кокаина была низкой у контрольных животных. Значения были в 40 раз выше у животных, получавших AlbuBChE, при этом наивысшие концентрации наблюдались через 2 ч после дозы AlbuBChE. Концентрации метилового сложного эфира экгонина снижались с течением времени после введения AlbuBChE, но даже через 96 ч после введения AlbuBChE концентрации метилового сложного эфира экгонина были все еще выше, чем у контрольных животных. Данные о зависимости индивидуальных и средних концентраций в плазме бензоилэкгонина (нг/мл) от времени (часы) у контрольных и получавших AlbuBChE беличьих обезьян приведены в табл. 19. Сводные данные о средних концентрациях бензоилэкгонина приведены на фиг. 15. Как показано на фигуре, эффект AlbuBChE на метаболит кокаина бензоилэкгонин был менее выраженным. На фиг. 16 приведены сводные данные об уровнях в крови кокаина и метаболитов кокаина метилового сложного эфира экгонина (ЕМЕ) и бензоилэкгонина (BZ) через 5 и 30 мин после инъекции кокаина. По сравнению с инъекцией кокаина в контроле после введения растворителя, в ситуации через 2 ч после введения AlbuBChE уровни в крови кокаина были значительно снижены как во временной точке 5 мину,так и 30 мин (F3,7=7,34, p0,05 и F3,7=14,4, p0,005 соответственно). Через 72 ч после дозы AlbuBChE уровни кокаина были все еще значительно ниже контрольных уровней через 30 мин после введения кокаина. Эффекты AlbuBChE не были значительными ни во временной точке 5 мин, ни в точке 30 мин через 96 ч после введения. Эффекты AlbuBChE на уровни ЕМЕ были аналогичными, но противоположно направленными в сравнении с кокаином. Уровни в крови ЕМЕ были повышены как во временной точке 5 мин, так и 30 мин через 2 ч после введения AlbuBChE (F3,7=5,6, р 0,05 и F3,7=33,3, p0,001). Уровни в крови ЕМЕ оставались значительно повышенными через 72 ч после дозы AlbuBChE для временной точки 30 мин. В то время как уровни в крови BZ были немного снижены через 2 ч после дозы AlbuBChE, эти эффекты не были значительными. Таблица 17 Зависимость концентрации в плазме кокаина (нг/мл) от времени (часы) у отдельных беличьих обезьян после однократного в/м введения дозы 5 мг/кг AlbuBChE. Кокаин вводили в/в в дозе 1 мг/кг контрольным животным (n=2) или через 2, 72 и 96 ч после дозы AlbuBChE (n=3) Концентрация кокаина через 5 мин после дозы кокаина через 2, 72 и 96 ч после дозы AlbuBChELLOQ (1 нг/мл) Концентрация кокаина через 30 мин после дозы кокаина через 2, 72 и 96 ч после дозы AlbuBChELLOQ (1 нг/мл) Концентрация кокаина через 5 и 30 мин после дозы кокаина у контрольных животныхLLOQ (1 нг/мл) Сводная таблица зависимости средней концентрации кокаина от времени у контрольных животных и в зависимости от времени после дозы AlbuBChE Таблица 18 Зависимость концентрации в плазме метилового сложного эфира экгонина (нг/мл) от времени (часы) у отдельных беличьих обезьян после однократного в/м введения дозы 5 мг/кг AlbuBChE. Кокаин вводили в/в в дозе 1 мг/кг контрольным животным (n=2) или через 2, 72 и 96 ч после дозы AlbuBChE (n=3) Концентрация метилового сложного эфира экгонина через 5 мин после дозы кокаина через 2, 72 и 96 ч после дозы AlbuBChELLOQ (1 нг/мл) Концентрация метилового сложного эфира экгонина через 30 мин после дозы кокаина через 2, 72 и 96 ч после дозы AlbuBChELLOQ (1 нг/мл) Концентрация метилового сложного эфира экгонина через 5 и 30 мин после дозы кокаина у контрольных животныхLLOQ (1 нг/мл) Сводная таблица зависимости средней концентрации метилового сложного эфира экгонина от времени у контрольных животных и в зависимости от времени после дозы AlbuBChE Таблица 19 Зависимость концентрации в плазме бензоилэкгонина (нг/мл) от времени (часы) у отдельных беличьих обезьян после однократного в/м введения дозы 5 мг/кг AlbuBChE. Кокаин вводили в/в в дозе 1 мг/кг контрольным животным (n=2) или через 2, 72 и 96 ч после дозы AlbuBChE (n=3) Концентрация бензоилэкгонина через 5 мин после дозы кокаина через 2, 72 и 96 ч после дозы AlbuBChELLOQ (1 нг/ил) Концентрация бензоилэкгонина через 30 мин после дозы кокаина через 2, 72 и 96 ч после дозы AlbuBChELLOQ (1 нг/мл) Концентрация бензоилэкгонина через 5 и 30 мин после дозы кокаина у контрольных животных Сводная таблица зависимости средней концентрации бензоилэкгонина от времени у контрольных животных и в зависимости от времени после дозы AlbuBChE Отношение ФК/ФД для AlbuBChE. Несмотря на ограниченное число временных точек и животных, была сделана попытка охарактеризовать отношение ФК/ФД для AlbuBChE у самцов беличьих обезьян. ФК и ФД данные, использованные в анализе, приведены в табл. 20. Индивидуальные данные и кривая, построенная на основании модели прямого ингибиторного эффекта Emax, приведены на фиг. 17. Эти данные четко показывают обратную зависимость между сывороточной концентрацией AlbuBChE и уровнями кокаина. Сывороточная концентрация AlbuBChE, способная приводить к 50% уменьшению концентрации кокаина (EC50), по оценке,основанной на модели, составляла 400 нг/мл. Emax составлял 213 нг/мл. Из-за ограниченности данных и допущений, использованных в данном анализе, значения параметров из данного ФК/ФД анализа нужно рассматривать как приблизительные оценки. Таблица 20 ФК/ФД анализ AlbuBChE у беличьих обезьян после однократного в/м введения дозы 5 мг/кг AlbuBChE. Кокаин вводили в/в в дозе 1 мг/кг контрольным животным (n=2) или через 2, 72 и 96 ч после дозы AlbuBChE (n=3) ФК параметры: концентрации в плазме AlbuBChE через 24, 72 и 96 ч после дозы AlbuBChE ФД параметр: концентрация в плазме кокаина через 5 мин после дозы кокаина В связи с тем, что концентрацию AlbuBChE не измеряли через 2 ч после дозы AlbuBChE,в анализе использовали образец, собранный в 1-ю временную точку (через 24 ч после дозыAlbuBChE через 24 ч после дозы AlbuBChE может отражать концентрацию AlbuBChE через 2 ч после дозы AlbuBChE. Выводы. Фармакокинетическую кривую AlbuBChE характеризовали у трех самцов беличьих обезьян после однократной в/м дозы 5 мг/кг AlbuBChE. Степень вариабельности воздействия была минимальной (7%). По оценке, значение t1/2 для AlbuBChE в терминальной фазе элиминации находилось в диапазоне от 45,5 до 65,5 ч. Кокаин вводили в/в в дозе 1 мг/кг контрольным животным (n=2) или через 2, 72 и 96 ч после дозыAlbuBChE вызывал уменьшение контакта с кокаином. Этот эффект был наиболее выражен через 2 ч после дозы AlbuBChE (7% от контроля). Контакт с кокаином составлял 60% от контроля через 96 ч после дозы AlbuBChE. В соответствии с механизмом действия AlbuBChE, воздействие метаболита кокаина метилового сложного эфира экгонина возрастало в 40 раз через 2 ч после введения AlbuBChE и снижалось с течением времени после введения дозы AlbuBChE. Эффект AlbuBChE на метаболит кокаина бензоилэкгонин был менее выражен. Отношение ФК/ФД у беличьих обезьян указывает на обратную зависимость между сывороточной концентрацией AlbuBChE и уровнями кокаина. Сывороточная концентрация AlbuBChE, способная при- 24024441 водить к 50% уменьшению концентрации кокаина (ЕС 50), по оценке, основанной на модели прямого ингибиторного эффекта Emax, составляла 400 нг/мл. Из-за ограниченности данных и допущений, использованных в данном анализе, значения параметров из данного ФК/ФД анализа нужно рассматривать как приблизительные оценки. Пример 3. AlbuBChE: фармакологические исследования безопасности для сердечно-сосудистой системы на яванских макаках с введением или без введения кокаина. Цель. Оценить безопасность для сердечно-сосудистой и дыхательной систем AlbuBChE, введенного внутримышечно (в/м) 3 самцам и 3 самкам яванских макак. Кроме того, влияние кокаина (введенного внутривенно (в/в, AlbuBChE и их сочетания на безопасность для сердечно-сосудистой системы оценивали в другой группе из 3 самцов и 3 самок яванских макак. Дизайн исследования. До начала исследования обезьянам были хирургически вживлены телеметрические передатчики и порты сосудистого доступа. Контролировали следующие СС параметры: систолическое давление, диастолическое давление, среднее артериальное давление, среднюю частоту сердечных сокращений и среднее значение произведения значения систолического давления на значение частоты сердечных сокращений (rate pressure product). Также контролировали изменения температуры тела. Группа исследования 1 (3 самца и 3 самки) служила в качестве контрольной группы для тестирования эффекта одного AlbuBChE в сравнении с его растворителем. Обезьянам вводили (в/м) контрольное вещество - буфер для препарата AlbuBChE в дни исследования (ДИ) (SD) 1 и 4. Через 3 ч после введения буфера для препарата регистрировали дыхательные и сердечно-сосудистые (СС) параметры соответственно. Одну в/м дозу тестируемого вещества (AlbuBChE в концентрации 15 мг/кг) вводили в ДИ 8 и 11. Через 3 ч после введения дозы AlbuBChE (что соответствует Tmax для AlbuBChE) контролировали СС и дыхательные параметры соответственно. Эффект предварительного воздействия AlbuBChE до введения дозы кокаина на СС параметры тестировали во второй группе (группа 2) животных (3 самца и 3 самки). Первые исходные СС параметры регистрировали в ДИ 15 после в/м введения буфера для препарата AlbuBChE с последующим однократным в/в введением физиологического раствора (растворитель для кокаина) через 3 ч. Эффект кокаина на СС параметры измеряли в ДИ 18, когда животные получали одну в/м инъекцию буфера для препаратаAlbuBChE с последующей однократной в/в дозой кокаина (1 мг/кг, в/в) через 3 ч. Эффект предварительного введения AlbuBChE на вызванные кокаином изменения СС параметров проверяли в ДИ 22. СС параметры регистрировали после однократной в/м дозы AlbuBChE (15 мг/кг) с последующей однократной в/в дозой кокаина (1 мг/кг) через 3 ч (см. табл. 21). Всех животных осматривали по меньшей мере дважды в день на предмет заболеваемости, смертности, травм, а также возможности доступа к корму и воде. Контролировали физиологическую реакцию на введение тестируемого вещества, включая артериальное давление, частоту сердечных сокращений, температуру тела, а также электрокардиограмму (ЭКГ). Таблица 21 Обозначение групп и уровни доз Результаты. Все животные дожили до окончания исследования. Группа исследования 1.AlbuBChE в дозе 15 мг/кг (в/м не вызывал каких-либо значительных изменений ни в регистрируемых СС параметрах, ни в температуре тела по сравнению с исходными значениями, определенными с использованием буфера для препарата AlbuBChE, как показано на фиг. 18-26. Группа исследования 2. В течение 2 мин после введения кокаина (1,0 мг/кг, в/в) среднее артериальное давление (САД)(MAP) возрастало на примерно 35 мм рт. ст. над исходным значением, равным 105 мм рт. ст Предварительное введение 15 мг/кг AlbuBChE до дозы кокаина показало, что не только максимальное артериальное давление было снижено благодаря AlbuBChE, но и время до устранения эффекта было также сокращено в 4,5 раза (17 мин при предварительном воздействии AlbuBChE до дозы кокаина, по сравнению с 77 минутами при введении одного кокаина), как показано на фиг. 27. Введение кокаина (1,0 мг/кг, в/в) вызывало резкое увеличение частоты сердечных сокращений от исходного уровня 140 ударов/мин, достигая пикового значения 240 ударов/мин (70% увеличение) в течение примерно 3 мин. Это вызванное кокаином увеличение частоты сердечных сокращений сохранялось в течение примерно 15 мин, постепенно снижаясь и возвращаясь к исходному уровню через 2 ч после введения кокаина. Предварительное введение AlbuBChE ослабляло вызванное кокаином увеличение частоты сердечных сокращений, о чем свидетельствовало быстрое, но умеренное возрастание на 30% до пикового значения 182 ударов/мин в течение примерно 3 мин. Это умеренное увеличение частоты сердечных сокращений было полностью обращено вспять с восстановлением исходного уровня уже через 30 мин после дозы кокаина, как показано на фиг. 30. Введение кокаина (1,0 мг/кг, в/в) вызывало умеренное скачкообразное повышение температуры тела с пиковым значением 38,7 С через 45 мин после дозы по сравнению с исходной температурой 38 С. Предварительное введение AlbuBChE (15 мг/кг, в/м) до дозы кокаина вызывало только легкое повышение температуры тела до значения 38,3 С, как показано на фиг. 32. Пример 4. AlbuBChE: исследование самовведения кокаина и восстановления самовведения кокаина у беличьих обезьян. Методы. Подопытные животные. В качестве подопытных животных использовали взрослых самцов беличьих обезьян (Saimiri sciureus) весом от 0,8 до 1,2 кг. Все обезьяны были размещены индивидуально в помещении с контролируемыми условиями влажности и температуры и имели свободный доступ к воде. Обезьян кормили после любой экспериментальной процедуры количеством пищи (Lab Diet 5045, PMI NutritionInternational, Richmond, IN; Banana Softies, Bio-Serv, Frenchtown, NJ), предназначенным для поддержания постоянного веса. Ежедневно им также предоставлялись свежие фрукты, овощи и обогащение среды обитания. Помещения для содержания животных имели полную аккредитацию AAALAC и все эксперименты были одобрены комиссией по контролю за содержанием и использованием лабораторных животных внутренней программы исследований NIDA. Самовведение кокаина. Три обезьяны были обучены самостоятельно вводить себе в/в кокаин в дозе 30 мкг/кг/инъекцию. Подробности метода обучения самовведению препарата можно найти в другом литературном источнике(Justinova et al., 2003). Вкратце, обезьян помещали в сидячем положении в кресло для иммобилизации из плексигласа. Кресло было заключено в большей акустической камере. На передней стенке кресла для иммобилизации находился рычаг реагирования и сигнальные лампы. Зеленый свет служил сигналом к началу сессии. Обезьяны были приучены реагировать, делая 10 нажатий (фиксированное количество, FR,10), для получения в/в инъекции кокаина. Инъекция кокаина сопровождалась выключением зеленого света и включением на 2 секунды желтой сигнальной лампы. После каждой инъекции кокаина также был 60-секундный перерыв. По окончании перерыва включался зеленый свет. Сессии продолжались в течение 1 ч. Иногда кокаин был заменен на физиологический раствор. После развития стабильного навыка самовведения кокаина и надежного исчезновения реагирования после замены его на физиологический раствор AlbuBChE (5 мг/кг, в/м) или его растворитель (в/м) вводили за 2 ч до сессии самовведения. Затем измеряли реагирование для самовведения в течение 5 последовательных дней. После каждого теста с наркотиком или используемым вместо него физиологическим раствором, реагирование для получения 30 мкг/кг/инъекцию кокаина было восстановлено в течение по меньшей мере 5 дней. После проверки восстановления навыка (см. ниже) дозу кокаина, доступную для самовведения, снижали до 10 мкг/кг/инъекцию и вновь определяли эффект AlbuBChE (5 мг/кг, в/м). Восстановление навыка самовведения кокаина. Кокаин заменяли на физиологический раствор для обезьян, которые устойчиво вводили себе в/в кокаин в дозе 30 мкг/кг/инъекцию. Реагирование быстро снижалось и оставалось на этом низком уровне в течение ряда дней. Затем вводили растворитель для AlbuBChE за 2 ч до введения кокаина (0,3 мг/кг, в/в),который вводили за 5 мин до сессии, в которой для самовведения был доступен физиологический рас- 26024441 твор, для определения того, сможет ли кокаин восстановить реагирование для самовведения. Такую же дозу кокаина также вводили до сессий самовведения физиологического раствора через 48 и 96 ч. Впоследствии, AlbuBChE (5 мг/кг, в/м) вводили за 2 ч до второй последовательности из 3 тестов по восстановлению навыка с 0,3 мг/кг в/в кокаина. После этих тестов обезьян возвращали к исходной ситуации,когда 30 мкг/кг/инъекцию кокаина было доступно для самовведения. Впоследствии, кокаин опять заменяли на физиологический раствор и проводили вторую серию тестов на восстановление навыка аналогичным образом за исключением того, что вводили в/в кокаин в дозе 0,1 мг/кг до сессий по восстановлению навыка. Лекарственные средства.AlbuBChE поставлялся компанией TEVA Pharmaceutical (Netanya, Israel) в замороженном растворе с концентрацией 30 мг/мл. После оттаивания раствор разводили до 15 мг/мл растворителем, а затем вводили обезьянам в объеме 0,33 мл/кг. Раствор кокаина (NIDA, Baltimore, MD) готовили в стерильном физиологическом растворе и предоставляли в объеме 0,2 мл для самовведения. При использовании для предварительного введения в исследованиях по восстановлению навыка, кокаин предоставляли в объеме 0,3 мл/кг. Анализ данных. Данные по содержанию в крови анализировали отдельно для каждого метаболита и временной точки (5 или 30 мин). Проводили однофакторный дисперсионный анализ (ANOVA) с последующими тестами Даннета, используя результаты, полученные от обезьян, получавших растворитель в качестве контроля. Данные по самовведению анализировали отдельно на частоту реагирования или инъекции после либо введения растворителя, либо введения AlbuBChE. Контрольные данные включали в анализ, беря среднее из последних 3 дней для непосредственно предшествующего исходного состояния. Затем проводили внутригрупповой анализ ANOVA с последующими тестами, сопоставляя дни после введения растворителя или AlbuBChE с контролем. Для тестов по восстановлению навыка проводили двухфакторныйANOVA, как для частоты реагирования, так и для инъекций, при этом время после введения растворителя или AlbuBChE являлось внутригрупповым фактором, а предварительное введение (растворителя илиAlbuBChE) межгрупповым фактором. При последующем сопоставлении сравнивали растворитель и AlbuBChE в каждой временной точке. Результаты. У обезьян, самостоятельно вводящих себе кокаин в дозе 30 мкг/кг/инъекцию, AlbuBChE уменьшал самовведение. На панелях фиг. 33 показана частота реагирования (верхняя панель) и инъекции (нижняя панель) на протяжении последовательных дней. Первые пять дней показывают исходное реагирование. Затем кокаин заменяли на физиологический раствор, и как частота (F5,10=37,0, р 0,001), так и инъекции(F5,10=188,7, р 0,001) значительно снижались в течение 5 дней замены по сравнению со средними значениями последних 3 дней предшествующего исходного периода. После 5 дней возврата к исходной ситуации обезьянам вводили растворитель и отводили 5 дней на тренировку самовведения. При сравнении со средними значениями последних 3 дней предшествующего исходного периода, введение растворителя не оказывало влияния на инъекции (F5,10=2,6, p=0,10). Общий эффект от дней наблюдали для частоты реагирования (F5,10=4,6, p0,05), однако при последующих сопоставлениях не удалось выявить никаких существенных изменений в реагировании относительно контроля ни в одном из 5 дней после введения растворителя. После введения растворителя обезьяны получали 5 мг/кг AlbuBChE, и самовведение кокаина отслеживали в течение 5 дней. Значительные изменения относительно среднего значения из последних 3 дней предшествующего исходного периода наблюдали как для частоты реагирования (F5,10=4,6, p0,05),так и для инъекций (F5,10=14,1, р 0,001). При последующих сопоставлениях было выявлено, что частота реагирования отличалась от контроля в дни 1-4 после введения и инъекции существенно отличались от контроля в день 1 и 4 после введения. После тестирования на восстановление навыка (см. ниже) обезьян возвращали в условия самовведения при более низкой дозе кокаина (10 мкг/кг/инъекцию). Снижение поддерживающей дозы уменьшало частоту реагирования и число инъекций (фиг. 33, правые панели). После стабилизации исходного уровня обезьянам делали инъекцию растворителя, и самовведение продолжалось в течение 5 дней. Ни частота реагирования, ни инъекции существенно не изменялись после инъекции растворителя по сравнению со средним значением из последних 3 дней исходного периода. Затем вводили AlbuBChE(5 мг/кг), и самовведение кокаина продолжалось в течение еще 5 дней. Как частота реагирования, так и инъекции уменьшались через 2 ч после инъекции AlbuBChE, однако эти эффекты не достигали уровня статистической значимости. У обезьян, которые реагировали на кокаин в дозе 30 мкг/кг/инъекцию, замена кокаина на физиологический раствор приводила к быстрому уменьшению реагирования. Затем вводили в/м растворитель дляAlbuBChE. Через 2, 48 и 96 ч кокаин в дозе 0,3 мг/кг вводили в/в за 5 мин до сессии с заменой на физиологический раствор. Введение кокаина приводило к восстановлению реагирования для самовведения кокаина, как показано черными столбцами на левых панелях фигуры 34. Когда 5 мг/кг AlbuBChE вводили в/м и через 2, 48 и 96 ч кокаин в дозе 0,3 мг/кг вводили в/в непосредственно перед сессией с заменой на физиологический раствор, восстановление реагирования было в значительной степени заблокировано во временной точке 2 ч, как для частоты реагирования (F1,4=16,9, р 0,05), так и для инъекций (F1,4=34,9,p0,001). Впоследствии обезьян тестировали идентичным образом с использованием 0,1 мг/кг кокаина в качестве дозы для восстановления. Несмотря на то что восстановление до более низкой дозы кокаина отличалось большей вариабельностью, сходную картину результатов наблюдали с эффектом 5 мг/кг AlbuBChE, опять-таки статистически значимым в точке 2 ч, как для частоты реагирования (F1,4=15,2,р 0,05), так и для инъекций (F1,4=129,7, p0,001). У 4 обезьян, которые были натренированы отличать 0,6 мг/кг метамфетамина от физиологического раствора, метамфетамин полностью заменяли кокаином в дозе 0,3 мг/кг (фиг. 35, верхняя панель). Когда 5 мг/кг AlbuBChE вводили за 2 ч до определения зависимости эффекта кокаина от дозы, не происходило генерализации кокаина в дозе 0,3 мг/кг до метамфетаминового стимула. Частичную замену (примерно 70%) наблюдали при более высокой дозе кокаина (1,0 мг/кг). Через 24 ч после AlbuBChE кокаин в дозе 0,3 мг/кг все еще полностью не генерализовался до метамфетаминового стимула (примерно 70%), однако теперь кокаин в дозе 1,0 мг/кг полностью генерализовался до метамфетамина. Через 48 ч после AlbuBChE кокаин в дозе 0,3 мг/кг полностью генерализовался до метамфетаминового стимула. Предварительное введение AlbuBChE за 2 ч до определения зависимости эффекта метамфетамина от дозы не влияло на генерализацию метамфетамина до метамфетаминового стимула (фиг. 36, верхняя панель). Предварительное введение AlbuBChE не влияло на частоту реагирования при любых условиях воздействия (фиг. 35 и 36, нижние панели). Обезьяны, приученные к самовведению кокаина и также протестированные на процедуру восстановления навыка, получали в общей сложности 4 инъекции AlbuBChE. Кровь забирали для определения антител к AlbuBChE после первой, второй и четвертой инъекций AlbuBChE. После первых 2 инъекций уровни антител были ниже уровня обнаружения (уровень титра 20). Однако после четвертой инъекции уровни антител оказались повышенными. У 2 обезьян титр антител был слегка повышенным над пределом обнаружения (21 и 43). У третьей обезьяны уровни антител были явно повышены (643). Концентрация AlbuBChE в крови этой третьей обезьяны через неделю после инъекции AlbuBChE также была снижена (27 нг/мл против 55 и 53 нг/мл у 2 других обезьян). Обсуждение. Результаты этих исследований четко показывают, что предварительное введение модифицированной формы BChE эффективно для противодействия поведенческим эффектам кокаина у приматов, отличных от человека. Данная работа является продолжением предыдущего исследования данного соединения на грызунах, в котором было показано, что AlbuBChE может противодействовать токсическим эффектам кокаина у крыс и, кроме того, блокирует вызванное кокаином восстановление навыка самовведения кокаина (Brimijoin et al., 2008). В настоящей работе предварительное введение 5 мг/кг AlbuBChE уменьшало как частоту реагирования, так и инъекции у обезьян, самостоятельно вводящих себе кокаин в дозе 30 мкг/кг/инъекцию. У тех же самых обезьян, протестированных на восстановление навыка самовведения кокаина после прекращения самовведения, доза 5 мг/кг AlbuBChE была способна блокировать восстановление реагирования при помощи дозы либо 0,3 мг/кг, либо 0,1 мг/кг кокаина. Когда дозу, доступную для самовведения, снижали до 10 мкг/кг/инъекцию, AlbuBChE опять-таки снижал частоту реагирования и число получаемых инъекций, хотя эти эффекты с дозой кокаина 10 мкг/кг/инъекцию были более вариабельными и не достигали уровня статистической значимости. И наконец, доза 5 мг/кг AlbuBChE также была способна противодействовать генерализации кокаина до метамфетаминового различительного стимула, однако данный эффект был специфичен для кокаина, поскольку AlbuBChE не обладал способностью противодействовать эффектам различительного стимула метамфетамина. При тестировании в случае самовведения кокаина в дозе 30 мкг/кг/инъекцию эффекты AlbuBChE были по-прежнему очевидны через 3 дня, хотя и с меньшей эффективностью. Однако эффекты AlbuBChE на восстановление навыка и различение стимулов не были очевидны через 48 ч после введения. Как показано,период полувыведения AlbuBChE составляет примерно 56 ч и эффекты на метаболизм кокаина были все еще очевидны через 72 после введения AlbuBChE, так что можно было бы ожидать, что некоторый эффект на эти процедуры будет заметен через 72 ч. Различные факторы могут служить причиной того, что невозможно увидеть уменьшение восстановления навыка или генерализации кокаина через 72 ч. В процессе самовведения небольшие дозы кокаина вводятся на протяжении продолжительного периода времени. В других процедурах относительно большую дозу кокаина вводили болюсной инъекцией. Возможно, AlbuBChE с большей легкостью метаболизирует кокаин до того, как он достигнет головного мозга в условиях самовведения, чем при других условиях. Когда AlbuBChE метаболизирует кокаин в условиях самовведения, его эффект заключается в том, чтобы создать условия для прекращения процесса. Восстановление поведения в результате прекращения также может продлевать эффекты от воздействия AlbuBChE на самовведение. В исследовании по восстановлению навыка результатом реагирования являлся физиологический раствор и стимул, прежде связанный с подкреплением. Когда обезьяны возобновляли реагирование после инъекции кокаина, обезьяны по-прежнему получали физиологический раствор при реагировании, но также получали стимул, прежде связанный с кокаином. Демонстрация этого стимула, возможно, также способствовала продолжительному реагированию в условиях восстановления навыка (Spealman et al., 1999), маскируя некоторые из эффектов AlbuBChE. Эффекты AlbuBChE почти наверняка были связаны с его эффектами на метаболизм кокаина. Введение AlbuBChE снижало количество кокаина в крови на по меньшей мере 72 ч. Тот факт, что уровни ЕМЕ также были увеличены в течение по меньшей мере 72 ч после AlbuBChE, предполагает, что AlbuBChE метаболизировал кокаин подобно природной BChE (Jones, 1984). Эта динамика метаболизма кокаина аналогична той, которая наблюдалась в эксперименте по самовведению, когда для подкрепления у обезьян использовали кокаин в дозе 30 мкг/кг/инъекцию. Кроме того, AlbuBChE не оказывал влияния на частоту реагирования в исследовании по различению стимулов, что указывает на то, что он не производит неспецифический эффект на специфическое реагирование, независимо от наличия кокаина в крови. Наблюдаемое наличие относительно высоких уровней антител к AlbuBChE у одной обезьяны после его четвертой инъекции указывает на то, что AlbuBChE может потерять часть своей эффективности при нескольких инъекциях. Несмотря на то что результаты для этой одной конкретной обезьяны, судя по всему, не отличались от результатов двух других протестированных обезьян, обнаружение антител предполагает, что некоторая часть AlbuBChE будет связана антителами, что может снизить его способность метаболизировать кокаин. Потребуется дальнейшая работа для выяснения того, насколько распространена выработка антител у приматов и являются ли наблюдаемые уровни антител достаточными для снижения способности AlbuBChE метаболизировать кокаин. Согласно исследованиям DAWN, кокаин продолжает фигурировать в сводках пунктов неотложной помощи и в отчетах судебно-медицинской экспертизы. Вследствие этого, лекарственное средство, способное противодействовать токсическим эффектам кокаина, может быть полезным дополнением к мерам неотложной помощи для пациентов, злоупотребляющих кокаином. Преимущество использования лекарственного средства, которое метаболизирует кокаин, заключается в том, что оно будет специфичным для кокаина и будет иметь минимальные побочные эффекты. Однако будет необходимо подтверждение того,что пациент употребляет кокаин, поскольку AlbuBChE не будет эффективен против токсичности других наркотиков, таких как амфетамины, которые могут вызывать аналогичный спектр токсических эффектов. В дополнение к лечению токсических эффектов кокаина AlbuBChE может также быть полезным в качестве дополнения к другим методам лечения злоупотребления кокаином. Можно ожидать, что человек с достаточным уровнем в крови AlbuBChE, принимающий кокаин, будет испытывать пониженный субъективный эффект кокаина. В контексте настоящего исследования результатом этого станет меньшее введение себе кокаина, в меньшей степени восстановление привычки вводить себе кокаин и неспособность кокаина генерализоваться до метамфетаминового различительного стимула. Поскольку рецидив злоупотребления кокаином остается проблемой в лечении, ожидается, что уменьшение субъективных эффектов кокаина будет сокращать рецидивы. У проходящего курс лечения человека, у которого случается рецидивупотребления наркотика, благодаря присутствию в крови AlbuBChE большинство кокаина будет метаболизироваться и это будет потенциально снижать вероятность дальнейшего употребления кокаина. Для этого потребуется, чтобы индивидуум продолжал принимать AlbuBChE на протяжении периода времени, в течение которого ожидается рецидив. Вследствие этого, крайне важно определить,насколько распространена выработка антител к AlbuBChE и как это может влиять на его способность метаболизировать кокаин. В заключение, благодаря предварительному введению беличьим обезьянам AlbuBChE у них удалось снизить количество кокаина в крови после болюсного приема кокаина. Благодаря предварительному введению AlbuBChE также удалось уменьшить самовведение кокаина обезьянами, приученными к самовведению кокаина в дозах 10 и 30 мкг/кг/инъекцию. AlbuBChE оказался способен блокировать вызванное кокаином восстановление навыка самовведения кокаина при 2 различных дозах кокаина. И наконец, AlbuBChE был также способен противодействовать различительным эффектам кокаина у беличьих обезьян. Тот факт, что AlbuBChE был способен противодействовать поведенческим эффектам кокаина в 3 различных моделях поведенческих эффектов кокаина, предполагает, что он будет эффективен в качестве потенциальной терапии злоупотребления кокаином. Пример 5. Двойное слепое плацебо-контролируемое исследование действия однократных нарастающих доз AlbuBChE с последующим применением нескольких доз кокаина для оценки фармакокинетических и фармакодинамических параметров кокаина после введения AlbuBChE на добровольцах, принимающих кокаин для развлечения. Цель. Определение уровней в крови кокаина после нескольких доз, принятых вслед за введением AlbuBChE, и определение поведенческих, физиологических эффектов и безопасности кокаина после приема нескольких доз вслед за введением AlbuBChE. Оценка фармакокинетики, безопасности и переносимостиAlbuBChE. Дизайн исследования. Исследование проводилось на 5 группах добровольцев, и было двойным слепым рандомизированным активным и плацебо-контролируемым исследованием в параллельных группах для сравнения лечения AlbuBChE с плацебо в качестве отрицательного контроля. Сорок (40) не нуждающихся в лечении здоровых взрослых людей, которые употребляли кокаин,были произвольно разделены на пять (5) лечебных групп. В каждой группе было по восемь участников.
МПК / Метки
МПК: A61K 38/16, C12P 21/04
Метки: bche-альбумин, белок, злоупотребления, лечения, кокаином, слитый
Код ссылки
<a href="https://eas.patents.su/30-24441-slityjj-belok-bche-albumin-dlya-lecheniya-zloupotrebleniya-kokainom.html" rel="bookmark" title="База патентов Евразийского Союза">Слитый белок bche-альбумин для лечения злоупотребления кокаином</a>
Предыдущий патент: Криогенная система для удаления кислотных газов из потока газообразных углеводородов
Следующий патент: Лист стекла с противомикробными свойствами
Случайный патент: Способ получения полимерно-битумных вяжущих